Изобретение относится к атомной энергетике, в частности к технологии кондиционирования и переработки радиоактивных отходов и может быть использовано для дезактивации отработанных ионообменных смол.
Образование частиц оксидов/гидроксидов железа в конденсационной воде контура АЭС происходит вследствие частичной коррозии стальных элементов. Данный процесс может усиливаться вследствие радиолиза воды в поле излучения реактора, который приводит к образованию O2 и H2O2. Процесс растворения стальных элементов включает в себя гидролиз иона Fe3+, образование аморфных оксо- и гидроксосоединений с последующим их старением с образованием кристаллических фаз гематита, гетита и лепидокроцита. Такие частицы имеют общее название - круд, их химический состав представлен главным образом оксидами и гидроксидами железа.
Присутствующий в контурной воде круд способен к адсорбции и накоплению радионуклидов коррозионной группы, его удаление проводится механической фильтрацией на ионообменных смолах с последующей обратной отмывкой, что приводит к повышенным дозовым нагрузкам обслуживающего персонала. Тем не менее, с увеличением количества отфильтрованного круда ионообменная ёмкость смол снижается, что негативно сказывается на их способности удалять калий и натрий из контурной воды. С ростом времени эксплуатации ионообменных смол эффективность механического удаления частиц оксида железа из контурной воды возрастает вследствие эффекта «старения», проявляющегося в виде постепенного снижения степени сшивки ионитов, а также увеличения удельной поверхности зерна смолы. Негативным эффектом данного процесса является тот факт, что происходит необратимое загрязнение ионитов вследствие облегчённой диффузии частиц круда в поровое пространство ионитов в процессе их старения, а также адсорбции Fe2+ и Fe3+ на функциональных группах смолы, с формированием частиц оксо- и гидроксосоединений непосредственно в объеме зерна смолы. Такие частицы уже не могут быть извлечены обратной промывкой, а эффективность их удаления с использованием химической регенерации не превышает 50%.
В связи с этим проблема переработки отработанных ионообменных смол (ОИОС), загрязнённых частицами оксида железа, является актуальной.
Радиоактивность частиц круда обусловлена адсорбцией вследствие изоморфного замещения короткоживущих радионуклидов коррозионной группы, из которых наибольшим периодом полураспада обладает Co-60. В связи с чем, остаточная активность выдержанных ОИОС, загрязненных оксидами железа, будет определяться гамма-активностью Co-60.
Методы утилизации ОИОС основаны на их переводе в безопасную форму, что минимизирует потенциальную опасность для окружающей среды и здоровья человека, а также поддерживает устойчивое развитие ядерной энергетики. Одним из активно используемых способов является иммобилизация ОИОС в цементной матрице. Недостатком такого метода является увеличение конечного объёма радиоактивных отходов, снижение со временем прочности цементного компаунда и увеличение скорости выщелачивания радионуклидов, что создает опасность с экологической точки зрения.
В пат. US №10593437 (опубл. 17.03.2020) предложен способ уменьшения объёмов ОИОС за счёт пиролиза радиоактивных серосодержащих и/или галогенсодержащих отходов. Заявленный способ осуществляют следующим образом. Содержащий фильтр реактор нагревают до 250-1050 °C, добавляют ОИОС и один или несколько реагентов для образования слоя в нижней части реактора. Затем смесь перемешивают, проводят частичное псевдоожижение или распыление слоя при 250–1050 °C для образования остатка пиролизованных радиоактивных отходов и отходящих газов. Отработанные газы подают в термоокислитель для сжигания, а остатки из реактора удаляют для последующего захоронения.
Недостатком предложенного способа является высокое энергопотребление и образование углекислого газа, приводящего к парниковому эффекту в атмосфере.
Указанные недостатки минимизированы в пат. US №10157691 (опубл. 18.12.2018), где предложен способ обработки ОИОС, содержащих радионуклиды, путём ступенчатой термической обработки и устройство для его реализации. Способ включает следующие стадии: сушка содержащих радионуклиды ОИОС при 150 °C в течение 2,5 часов (этап 1); нагрев до 350 °C в реакторе со шнековым конвейером для разделения ионообменной смолы и радионуклидов (стадия 2); преобразование при температуре около 550 °C в течение 30 минут летучих соединений радионуклидов в нелетучие оксиды серы, содержащие радионуклиды (стадия 3); преобразование в процессе термообработки при 700 °C в течение 2 часов с последующей выгрузкой из реактора оксидов серы с радионуклидами в хлориды, содержащие радионуклиды (стадия 4); отделение и сбор радионуклидов из хлоридов, содержащих радионуклиды путём помещения в реактор неорганического хлорирования с последующей термообработкой в присутствии газообразного хлора 100 ppm, газообразного кислорода 100 ppm и газообразного азота 1 атм. при 800 °C на 90 минут для испарения и конденсации (этап 5). Реагенты, полученные на этапе 5, подвергают термообработке при 1400 °C в условиях вакуума для отделения испарившегося радионуклида, который затем конденсируют во влажном газоочистителе.
Поэтапная термическая обработка уменьшает образование CO2, выхлопных газов с высоким содержанием SO2 и SO3 и имеет хорошую степень уменьшения объёма радиоактивных загрязнений для окружающей среды, что является несомненным достоинством настоящего изобретения. Тем не менее, как любой термический процесс, дезактивация ОИОС предложенным способом энергетически затратна, что увеличивает себестоимость процесса.
Известен способ переработки ОИОС, основанный на отмывке, интенсифицированной ультразвуковыми колебаниями, распространяемыми в среде водных растворов специально очищенных реагентов [Балашевская Ю.В. и др. «Утилизация отработавших ионообменных смол, загрязнённых радионуклидами» // Сотрудничество для решения проблемы отходов: 9-я Международная конференция, Харьков, 28-29 марта 2012 (http://ecovestnik.ru/index.php/obrashchenie-s-otkhodami/1473)]. ОИОС, содержащие 2,7 – 7,0 ⋅105 Cs134 и Cs137 очищали порциями по 5 г в три этапа по 15 мин с заменой растворов на свежие. Эффективность дезактивации составила от 74 до 97%.
Недостатком предложенного способа является, прежде всего, низкая степень дезактивации, что требует дальнейшей очистки от радионуклидов.
Невысокая эффективность дезактивации связана с наличием железооксидных отложений на ОИОС. Этой проблеме уделено внимание в подходах, основанных на процессах химической дезактивации ОИОС. При этом эффективность удаления железа из ОИОС будет определяться полнотой растворения гематита, образование которого может происходить при окислении магнетита растворенным кислородом или вследствие трансформации гетита. При этом скорость образования гематита увеличивается с ростом температуры, например, в охлаждающей воде реактора. Гематит с трудом поддается растворению в минеральных кислотах по сравнению с магнетитом и поэтому практически не удаляется с ОИОС при обработке ультразвуком. Восстановительное растворение гематита может быть проведено с использованием органических соединений - аскорбиновой или щавелевой кислоты, а также с добавлением солей Cu(I) и Sn(II). На скорость растворения гематита влияет размер частиц, а также температура процесса. Восстановленный Fe2+ поступает в раствор, где в свою очередь способствует дальнейшему растворению гематита вследствие перераспределения электронной плотности между Fe2+ в водной фазе и Fe3+ кристаллической фазы оксида. Лимитирующей стадией такого процесса растворения будет являться переход Fe2+ в водную фазу. Однако, присутствие в системе растворенного кислорода будет приводить к значительному ингибированию растворения вследствие окисления Fe2+.
Жидкофазное окисление ОИОС на основе реакции окисления по Фентону позволяет относительно эффективно разрушать матрицу ионитов с железооксидными отложениями при относительно низких температурах с выделением нетоксичных продуктов в виде CO2. К серьезным недостаткам данного метода, ограничивающего его использование, можно отнести значительный расход пероксида водорода, при котором, однако, не достигается 100% растворения ОИОС. Улучшение качества дезактивации предложено в процессе жидкофазного окисления с применением реакции окисления по Фентону в сочетании с электрохимическим восстановлением железа Fe3+ до Fe2+ на катоде, подключенном к источнику постоянного тока [Cheng T.-H., еt al. «Kinetic study and optimization of electro-Fenton process for dissolution and mineralization of ion exchange resins»//Chem.Eng.J., 2017, V/308, pp. 954-962]. В процессе реакции Фентона пероксид водорода, катализируемый ионами железа, разрушает органические вещества. В указанном способе смешанную смолу (гранулы полистирола сульфированного и четвертичного аммония с массовым соотношением 40:60%) загружали в металлический титан сетчатого типа, покрытый IrO2/ RuO2 (Ti-DSA), который использовали в качестве анода, а сетку из нержавеющей стали использовали в качестве катода. Использование электрохимического окисления увеличивает эффективность разрушения ОИОС. Превращение ОИОС в растворимые фрагменты и удаление общего органического углерода достигло 92% и 99,4%, соответственно, в условиях твердой нагрузки 40 г/л, pH=2, приложенного тока 2 А, скорости потока H2O2 = 1,2 мл/мин, FeSO4 = 20 мМ при 85 °С. Кинетическая модель псевдопервого порядка последовательных реакций указала, что эффективность окисления по реакции Фентона с электрохимическим процессом сильно зависит от медленно генерируемого стирола в водной фазе под действием H2O2 и сильной кислоты, который быстро минерализуется гидроксильными радикалами.
К недостаткам предложенного способа относится использование агрессивного раствора пероксида водорода концентрацией 50% в большом количестве, необходимость его транспортировки, хранения на производстве и утилизации, а также образование в ходе процесса токсичного стирола, что накладывает повышенные требования к безопасности труда. Также способ имеет недостаток, связанный с неполным окислением и дезактивацией ОИОС.
Наиболее оптимальный подход к переработке ОИОС основан на использовании химических методов, не приводящих к разрушению матрицы ионита, что позволяет значительно сокращать объём радиоактивных отходов за счёт повторного использования дезактивирующих растворов. Дезактивированные ОИОС в последствии могут быть захоронены на полигоне бытовых отходов.
Прототипом заявляемого изобретения является электрохимический метод, предложенный в [Semmler J. and Chi L. «Treatment of liquid waste and regeneration of spent ion exchange resin using electrochemical techniques» // Waste Management, Decommissioning and Environmental Restoration for Canada’s Nuclear Activities; 2011 September 11 to 14; Marriot Toronto Downtown Eaton Centre, CW-127140-CONF-0032011 September 11 to 14] для уменьшения объёма ОИОС за счёт удаления металлов из отработанной смолы под действием электрического поля. Данный метод использует электрохимическую обработку ОИОС в растворе ЭДТА, лимонной и аскорбиновой кислот. В результате сопутствующей электрохимической обработки происходит восстановление железа с переходом в растворённую форму с образованием комплексных соединений, а также постепенное восстановление на катоде ионов Fe2+ до металлического железа. Для осуществления способа была разработана и изготовлена электрохимическая ячейка из поликарбоната, разделённая мембранами на три части. Центральное отделение содержало жидкие отходы или ОИОС, а анодное и катодное отделения содержали электролиты. В качестве анода использовали платиновую фольгу, а катод изготавливали из нержавеющей стали 304 (304SS). Электрод сравнения - Ag/AgCl (4 М KCl). Испытания осаждения железа проводили при постоянном потенциале. Тестовый раствор, имитирующий состав реальных ЖРО содержал 600 мг/л ЭДТА в лимонной кислоте, 200 мг/л ионов трехвалентного железа (в виде цитрата железа) и 880 мг/л аскорбиновой кислоты, используемой в качестве восстанавливающего агента. При температуре 60 °С, значении рН в диапазоне 3–4, силе потенциала 15–35 В из раствора было удалено от 10 до 52,5% железа. В ходе процесса ионы железа из ОИОС через мембрану мигрировали в катодный отсек, где восстанавливались до металла и осаждались на катоде.
Недостатками предложенного способа являются низкие значения растворения железооксидных отложений, что снижает эффективность дезактивации ОИОС таким методом. Данный факт связан с тем, что в присутствии хелатирующих агентов, таких как ЭДТА растворимость гематита ниже, по сравнению с магнетитом, что связано с более стабильной кристаллической решеткой. Помимо этого, использование электролита, содержащего ЭДТА затрудняет процесс растворения отложений на ОИОС за счёт формирования комплексов ЭДТА с железом и кобальтом, что в дальнейшем также затруднит очистку полученного раствора после обработки ОИОС. Помимо этого, осаждение железа в металлическом виде уменьшает работоспособность катода.
Несомненно, восстановительное растворение гематита является достаточно эффективным методом очистки ОИОС от железооксидных отложений, однако, внесение органических комплексообразователей может создавать ряд трудностей при очистке образующихся вторичных радиоактивных отходов. Это связано с тем, что комплексы Co(II)-ЭДТА чрезвычайно устойчивы, поэтому задача последующего извлечения или концентрирования радионуклида Co-60 из вторичных жидких радиоактивных отходов не может быть решена с использованием распространённых осадительных или сорбционных методов.
В связи с этим, задачей предлагаемого изобретения является разработка способа дезактивации ОИОС, удобного в технологическом оснащении, с возможностью дальнейшего концентрирования радионуклидов и иммобилизации в цементные матрицы.
Технический результат изобретения заключается в глубокой дезактивации катионообменных ОИОС, загрязнённых Со-57 и в присутствии железооксидных отложений, в процессе электрохимической обработки в прикатодном пространстве в растворах минеральных кислот, при этом восстановителем является водород, выделяющийся на катоде в результате электролиза молекулы кислоты.
Растворение гематита в прикатодном восстановительном пространстве происходит по следующей схеме:
• 2H+ + 2ē → 2H2↑ (катод)
• 2H2O - 4ē → O2↑ + 4H+ (анод)
• Fe2O3 + 6H+ + 2ē → 2Fe2+(раств.) + 3H2O.
Заявляемый способ позволяет быстро и эффективно обеспечивать растворение частиц гематита в сравнении с обычной кислотной обработкой. Достоинства подхода заключаются в отсутствии необходимости добавления дополнительных восстановителей таких как щавелевая или аскорбиновые кислоты, а также использования ЭДТА. Конечная стадия доочистки ОИОС от радионуклида в динамических условиях с использованием солей натрия позволяет предотвратить вторичную адсорбцию Co-57 на функциональных группах ионита, что способствует 100% удалению радионуклида из ОИОС.
Технический результат достигается способом дезактивации отработанных ионообменных смол, содержащих кобальт-57 и оксиды железа, электрохимической обработкой в растворах минеральных кислот, в котором ячейку с ОИОС располагают в прикатодном пространстве и используют минеральные кислоты в отсутствии восстановителей и комплексообразователей. После электрохимической обработки с целью предотвращения вторичной адсорбции радионуклида смолу промывают в динамических условиях раствором состава NaNO3 - 2 моль/л, HNO3 - 1 моль/л. Для уменьшения объёмов вторичных отходов проводят осаждение радионуклида из кислотных растворов подщелачиванием NaOH с образованием осадка Fe(OH)3.
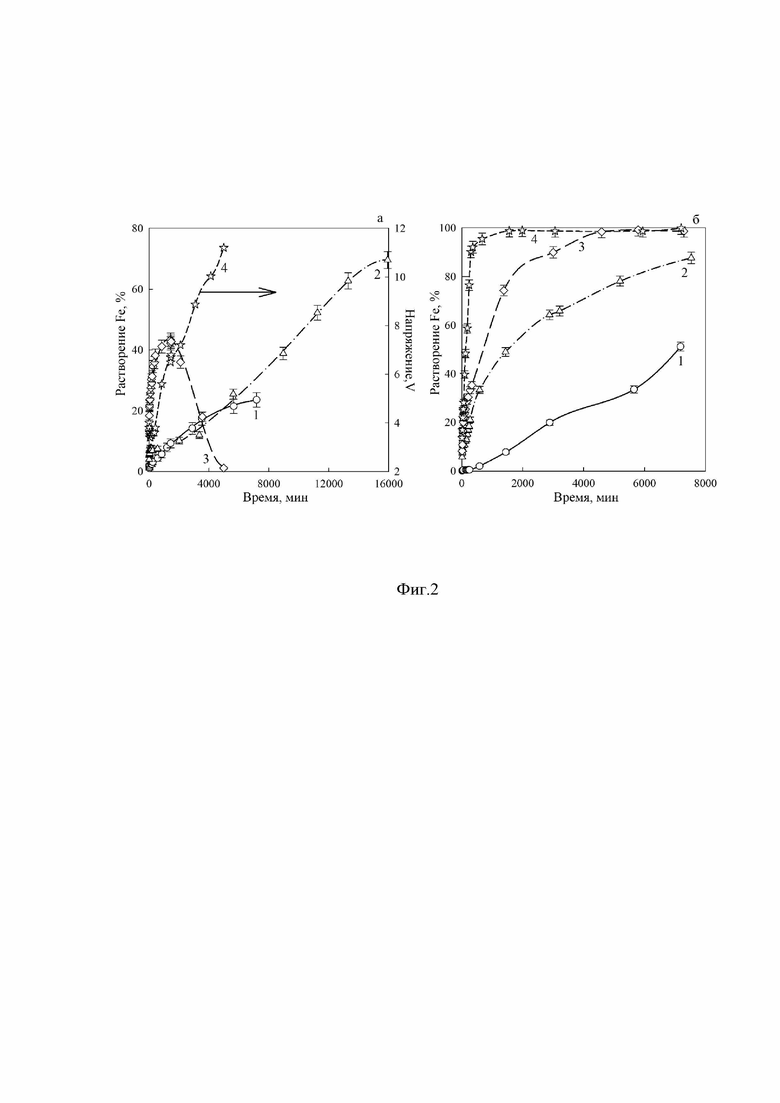
Дезактивацию модельных ОИОС с активностью 2 500 Бк/мл проводили в статических условиях с использованием электрохимической ячейки, конструкция которой приведена на Фиг.1, где 1 - цилиндрическая ёмкость, выполненная из боросиликатного стекла, 2 - крышка из тефлона, 3 - отверстия в крышке для отвода газообразных продуктов, 4 - корзина из кислотостойкой полимерной сетки, 5 - платиновый катод, чистота 99,99%, выполненный в виде в виде спирали, 6 - анод в виде квадратной пластинки из платины чистотой 99,99%. Процесс проводили с использованием источника постоянного тока в режиме стабилизации силы тока.
Для оценки эффективности и скорости растворения железооксидных отложений ОИОС, в процессе электрохимической обработки через определенные интервалы времени отбирали фиксированный объём раствора, в котором определяли концентрацию железа. Отобранную часть рабочего раствора восполняли свежим раствором кислоты, что в дальнейшем учитывали при расчётах. Каждые 6-12 часов, в зависимости от режима электрохимической обработки, восполняли затраченный на электролиз объём раствора свежей порцией дистиллированной воды. Для эффективности дезактивации ОИОС через определённые временные интервалы отбирали раствор, объемом 10 мл и измеряли удельную активность. После измерения раствор возвращали в электрохимическую ячейку.
Эффективность заявляемого способа оценивали при сравнении результатов степени растворения железооксидных отложений на модельных ОИОС в растворах HNО3 и Н2SO4 в статических условиях без дополнительной обработки постоянным током. Для этого к воздушно-сухой навеске модельной ОИОС добавляли аликвоту раствора кислоты известного объёма и заданной концентрации с последующим непрерывным перемешиванием. Через 7 дней смолу отделяли декантацией от раствора, в котором определяли концентрацию железа. Эффективную в отношении растворения железооксидных отложений соляную кислоту HCl не использовали, так как в реальных условиях её применение ограничено или вовсе запрещено на объектах ядерно-топливного цикла, в виду быстрой коррозии стальных конструкций в присутствии хлорид-ионов, удаление которых из технологических растворов на радиохимических производствах является сложной технологической задачей.
Полноту растворения железооксидных отложений на ОИОС, а также полноту дезактивации рассчитывали по уравнению:
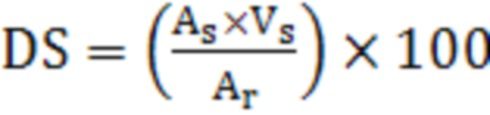 ,
,
где, As - активность раствора кислоты (Бк/мл) или концентрация железа (мг/мл), Vs - объем раствора кислоты (мл), Ar - исходная активность навески смолы (Бк) или исходное удельное содержание железа (мг).
Для контроля остаточного содержания железа в модельных ОИОС, иониты отделяли от раствора, промывали на фильтре дистиллированной водой и сушили при 80 °С в течение 6 часов. Высушенные иониты измельчали и заливали фиксированным объёмом раствора HCl концентрацией 10 моль/л и выдерживали в течение суток при нагревании и периодическом перемешивании. После чего, раствор соляной кислоты разбавляли дистиллированной водой фиксированного объёма и определяли концентрацию железа.
Содержание железа в рабочем растворе оценивали с использованием атомно-абсорбционной пламенной спектроскопии. Удельную активность Со-57 (энергия фотопика: 122 кэВ) определяли прямым радиометрическим методом на гамма-спектрометре с детектором, выполненным из NaI(Tl) размером 63×63 мм. Рентгенофазовый анализ выполняли на дифрактометре D8 ADVANCE.
Режимы обработки, подтверждающие примеры осуществления изобретения, приведены в Таблице 1 (№ 2, 4, 5, 7, 9, 10, 12). Параллельно проводили оценку эффективности растворения железоокисдных отложений без электрохимической обработки, примеры № 1, 3, 6, 8, 11.
Таблица 1. Режимы обработки и эффективность растворения железооксидных отложений на ОИОС
В соответствии с данными остаточного содержания железа в модельных ОИОС в зависимости от способа обработки (Табл. 1), режимы обработки по примерам 1–9 малоэффективны для растворения гематитовых отложений. Использование электрохимической обработки позволяет заметно повысить эффективность растворения гематита по сравнению с обычной отмывкой растворами минеральных кислот. Так, с ростом концентрации раствора H2SO4, а также силы постоянного тока, скорость и полнота растворения гематитовых отложений и, соответственно эффективность дезактивации, возрастают. Полнота растворения составляет 99,3 и 99,7% для режимов по примерам 10 и 12, соответственно. Стоит отметить, при контакте ионита с раствором H2SO4 2 моль/л, степень растворения гематита составляет 98,4%. Однако, использование режима электрохимической обработки по примеру 10 является более предпочтительным, так как при использовании менее концентрированного раствора H2SO4 достигается большая полнота растворения гематитовых отложении (99,3%), что снижает затраты на реактивы и снижает коррозию оборудования.
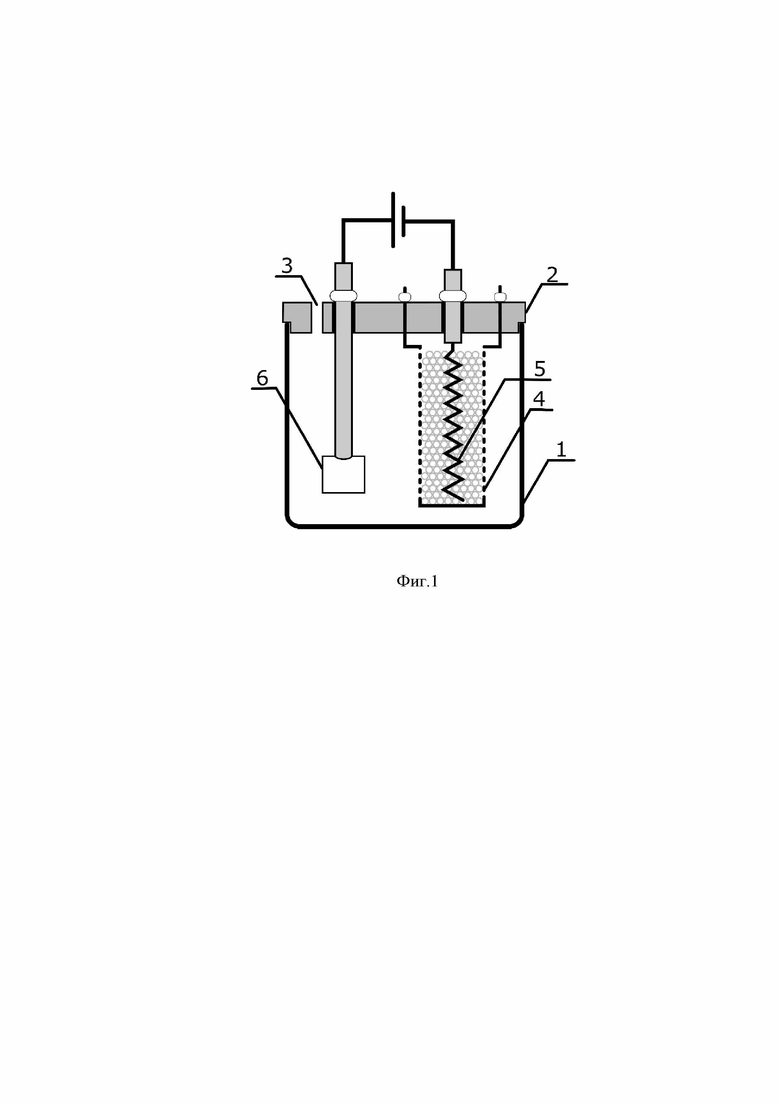
Эффективность растворения железооксидных отложений с поверхности ОИОС, загрязнённой гематитом от времени электрохимической обработки и от режимов обработки приведена на Фиг. 2. Электрохимическое растворение проводят: (а) в растворе HNO3, где кривая 1 соответствует режиму по примеру 2, кривая 2 - по примеру 4, кривая 3 - по примеру 5, кривая 4 - изменение напряжения в процессе обработки; (б) в растворе H2SO4, где кривая 1 соответствует режиму по примеру 7, кривая 2 - по примеру 9, кривая 3 - по примеру 10, кривая 4 - по примеру 12.
При использовании азотной кислоты заметный эффект на растворение гематита обнаруживается при концентрации 3 моль/л, при этом увеличение силы тока с 0,5A до 2,0А (пример 3) сопровождается постепенным ростом напряжения в результате чего происходит значительный разогрев раствора с последующим выпадением осадка гидроксида железа. Причиной выпадения осадка является смещение рН раствора в слабощелочную область до 8,53±0,1. На момент окончания эксперимента анод был покрыт слоем тёмного налёта что, предположительно, привело к росту сопротивления и как следствие напряжению. Из рентгенофазового анализа установлено, что налёт, образующийся в процессе электрохимической обработки смолы, представлен слабокристаллизованными фазами соединений FePt3 и FePt.
С ростом концентрации раствора H2SO4 и силы тока закономерно увеличивается как скорость, так степень растворения. Для режимов электрохимической обработки по примерам 10 и 12 степень растворения превышает 99%, поэтому использование серной кислоты является более предпочтительным. При использовании серной кислоты образования налёта на аноде или изменения напряжения не происходило. Применение неконцентрированных растворов H2SO4 позволяет увеличить полноту растворения гематитовых отложений, эффективность дезактивации при использовании 1М раствора достигает 80%.
Тем не менее, в качестве электролита и дезактивирующего раствора предпочтительно использование растворов H2SO4 с концентрацией до 1 моль/л (примеры 7, 9, 10). Это связано с тем, что концентрированные растворы приводят к образованию малорастворимых сложных солей, снижающих эффективность дезактивации, а также по причине коррозии оборудования. Использование растворов HNO3 является малоэффективным и может приводить к загрязнению анода.
Экспериментально установлено, что при использовании ионообменных смол типа КУ 2-8, свойства которых не изменяются в процессе гидротермальной обработки, происходит как фиксация радионуклида Co-57 железооксидными отложениями (фиксированная часть), так и его сорбция в процессе ионного обмена на функциональных группах смолы (обменная часть). По этой причине дезактивация ОИОС проходит через максимум, что свидетельствует о процессе вторичной адсорбции радионуклида Co-57, поступившего в раствор H2SO4 вследствие растворения гематита, на сорбционных центрах ионита. Для удаления адсорбированного радионуклида ОИОС, после электрохимической обработки, были дополнительно промыты раствором состава: NaNO3 - 2 моль/л, HNO3 - 1 моль/л объемом 30 мл в динамических условиях при скорости фильтрации 5 колоночных объёмов в час. В результате такой обработки фотопики Co-57 обнаружены не были, что свидетельствует о полной дезактивации модельной ОИОС.
Для уменьшения объёма вторичных отходов, растворы после дезактивации модельных ионитов подщелачивали с использованием NaOH. Изменение рН раствора приводит к выпадению осадка Fe(OH)3 с одновременным соосаждением радионуклида Co-57. После центрифугирования фотопики Co-57 в растворах не были зафиксированы, что говорит о полном соосаждении радионуклида на осадке Fe(OH)3 масса которого во влажном состоянии составила 0,2 г, что составляет менее 20% от исходного веса и объёма ОИОС. Кроме того, гидроксиды железа в отличие от ОИОС успешно поддаются цементированию без нарушения характеристик цементного компаунда, что позволяет решать проблему безопасной окончательной утилизации радиоактивных отходов.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ дезактивации отработанных ионообменных смол ядерно-топливного цикла, загрязненных гематитом | 2022 |
|
RU2788675C1 |
| СПОСОБ ДЕЗАКТИВАЦИИ ОТРАБОТАННЫХ ИОНООБМЕННЫХ СМОЛ, ЗАГРЯЗНЁННЫХ РАДИОНУКЛИДАМИ ЦЕЗИЯ И КОБАЛЬТА | 2019 |
|
RU2713232C1 |
| Способ переработки отработанных резорцинформальдегидных ионообменных смол, применяемых для очистки ЖРО от радионуклидов цезия | 2021 |
|
RU2755362C1 |
| СПОСОБ ДЕЗАКТИВАЦИИ ОТРАБОТАННЫХ ИОНООБМЕННЫХ СМОЛ, ЗАГРЯЗНЕННЫХ РАДИОНУКЛИДАМИ | 2014 |
|
RU2573826C1 |
| СПОСОБ УДАЛЕНИЯ ПЕРЕХОДНЫХ МЕТАЛЛОВ И РАДИОНУКЛИДОВ ИЗ РАСТВОРОВ, СОДЕРЖАЩИХ КОМПЛЕКСООБРАЗУЮЩИЙ АГЕНТ | 2012 |
|
RU2458418C1 |
| СПОСОБ ПОДДЕРЖАНИЯ ВОДНО-ХИМИЧЕСКОГО РЕЖИМА ЯДЕРНОЙ ЭНЕРГЕТИЧЕСКОЙ УСТАНОВКИ | 2011 |
|
RU2450376C1 |
| СПОСОБ ДЕЗАКТИВАЦИИ РАДИОАКТИВНЫХ ИОНООБМЕННЫХ СМОЛ | 2016 |
|
RU2631942C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ОПТИМАЛЬНЫХ ПАРАМЕТРОВ РАСТВОРЕНИЯ ОКСИДОВ ПЕРЕХОДНЫХ МЕТАЛЛОВ В РАСТВОРАХ, СОДЕРЖАЩИХ КОМПЛЕКСООБРАЗУЮЩИЙ АГЕНТ | 2012 |
|
RU2516274C2 |
| НЕОРГАНИЧЕСКИЙ СФЕРОГРАНУЛИРОВАННЫЙ КОМПОЗИЦИОННЫЙ СОРБЕНТ НА ОСНОВЕ ГИДРОКСИДА ЦИРКОНИЯ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1996 |
|
RU2113024C1 |
| СПОСОБ ОЧИСТКИ ЖИДКИХ РАДИОАКТИВНЫХ ОТХОДОВ, ЗАГРЯЗНЁННЫХ НЕФТЕПРОДУКТАМИ, ПРОДУКТАМИ КОРРОЗИИ И ШЛАМАМИ | 2019 |
|
RU2724925C1 |
Изобретение относится к атомной энергетике, в частности к технологии кондиционирования и переработки радиоактивных отходов, и может быть использовано для утилизации отработанных ионообменных смол и их перевода в безопасную форму. Способ дезактивации содержащих кобальт-57 и оксиды железа катионообменных смол проводят электрохимической обработкой в растворах минеральных кислот. Ячейку для размещения отработанных ионообменных смол крепят в прикатодном пространстве и используют минеральные кислоты в отсутствие восстановителей и комплексообразователей. Изобретение позволяет проводить глубокую дезактивацию катионообменных ОИОС. 3 з.п. ф-лы, 2 ил.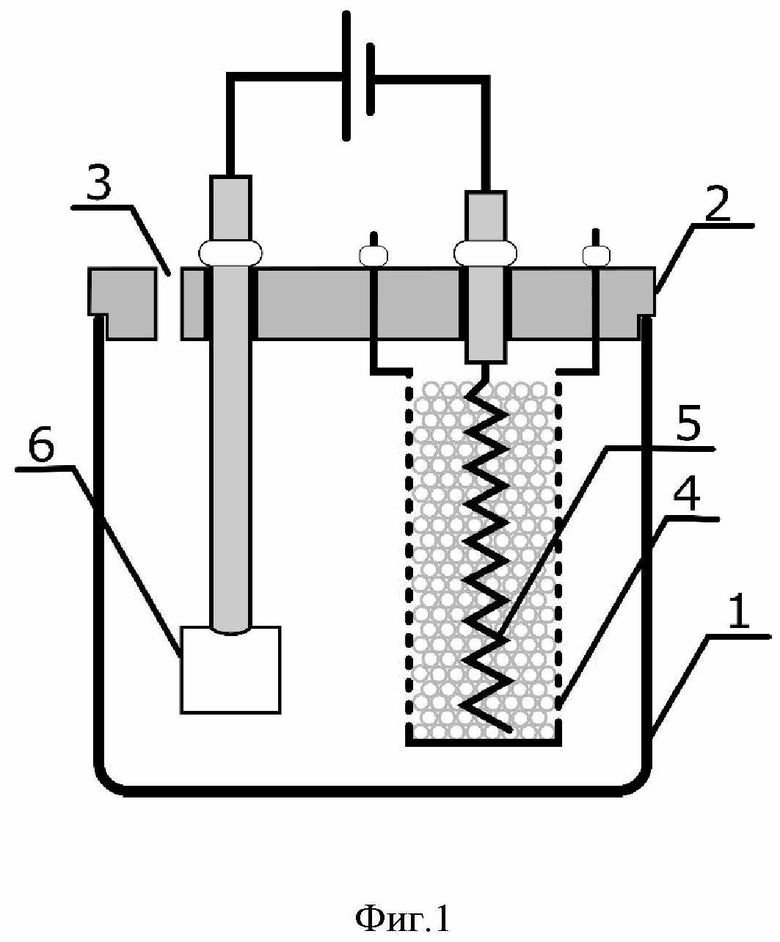
1. Способ дезактивации отработанных катионообменных смол, содержащих кобальт-57 и оксиды железа, электрохимической обработкой в растворах кислот, отличающийся тем, что ячейку для размещения отработанных ионообменных смол располагают в прикатодном пространстве и используют минеральные кислоты в отсутствие восстановителей и комплексообразователей.
2. Способ по п. 1, характеризующийся тем, что предпочтительно используют раствор H2SO4 в концентрации до 2 моль/л.
3. Способ по п. 1, характеризующийся тем, что с целью предотвращения вторичной адсорбции смолу после электрохимической обработки промывают в динамических условиях раствором состава NaNO3 2 моль/л, HNO3 1 моль/л.
4. Способ по п. 1, характеризующийся тем, что для уменьшения объёмов вторичных отходов проводят осаждение радионуклида из кислотных растворов подщелачиванием NaOH.
| СПОСОБ ДЕЗАКТИВАЦИИ ОТРАБОТАННЫХ ИОНООБМЕННЫХ СМОЛ, ЗАГРЯЗНЁННЫХ РАДИОНУКЛИДАМИ ЦЕЗИЯ И КОБАЛЬТА | 2019 |
|
RU2713232C1 |
| СПОСОБ ДЕЗАКТИВАЦИИ ОТРАБОТАННОЙ ИОНООБМЕННОЙ СМОЛЫ ИЗ ЕМКОСТИ ХРАНИЛИЩА РАДИОАКТИВНЫХ ОТХОДОВ АТОМНОЙ ЭЛЕКТРОСТАНЦИИ | 2001 |
|
RU2224310C2 |
| СПОСОБ ДЕЗАКТИВАЦИИ ОТРАБОТАННОГО КАТИОНИТА УСТАНОВОК ОБРАБОТКИ РАДИОАКТИВНЫХ СРЕД АТОМНОЙ ЭЛЕКТРОСТАНЦИИ | 2000 |
|
RU2183871C1 |
| Автомат Калашникова | 2020 |
|
RU2750123C1 |
| US 9208915 B2, 08.12.2015. | |||
Авторы
Даты
2021-05-19—Публикация
2020-11-28—Подача