Область техники, к которой относится изобретение
Настоящее изобретение относится к диазабицикло-соединению для лечения и/или профилактики заболевания или расстройства, связанного с вирусом гепатита, способу применения этого соединения для лечения и/или профилактики заболевания или расстройства, связанного с вирусом гепатита, и применению этого соединения для получения лекарственного средства для лечения и/или профилактики заболевания или расстройства, связанного с вирусом гепатита, или для устранения и/или облегчения заболевания или расстройства, связанного с вирусом гепатита.
Предпосылки создания изобретения
Гепатит или заболевание печени обычно вызывается вирусом гепатита. Вирусы гепатита как правило, подразделяют на следующие типы: A, B, C, D, E и G, при этом вирус гепатита B вызывает хронические заболевания, которые в настоящее время распространены по всему миру, и у значительной части гепатит B может перейти в рак печени на более поздней стадии развития заболевания, если его не контролировать ненадлежащим образом. В настоящее время в мире насчитывается около 280000000 пациентов с гепатитом В (или носителями вируса гепатита В (HBV)).
В соответствии с Руководством по профилактике и лечению хронического гепатита B (CHB) версии 2015 года в Китае, лечение хронического гепатита B имеет целью максимизировать долговременное ингибирование репликации HBV, уменьшить воспалительный некроз клеток печени и фиброз печени и отсрочить и уменьшить печеночную недостаточность и декомпенсацию цирроза печени, HCC и других осложнений, улучшая, таким образом, качество жизни и продлевая время выживания. В процессе лечения, для некоторых подходящих пациентов, необходимо в максимально возможной степени придерживаться курса на клиническое излечение хронического гепатита В, то есть после окончания лечения должен быть постоянный вирусологический ответ, отрицательная конверсия HBsAg или сопровождаемая положительной конверсией анти-HBs, нормальный уровень ALT, незначительное или вообще отсутствие поражений тканей печени. Полное излечение означает, что, за исключением антител, ДНК HBV, различные антигены и кзкДНК в организме отсутствуют.
В настоящее время во многих международных руководствах по профилактике и лечению хронического гепатита В отрицательная конверсия поверхностного антигена (HBsAg) (также известная как функциональное излечение) считается идеальной целью для противовирусной терапии CHB. Однако, хотя существующие противовирусные препараты, такие как интерфероны (интерферон альфа, IFN-б) и нуклеозидные(нуклеотидные) аналоги [NUC] могут ингибировать репликацию вируса, клиренс или сероконверсия HBsAg вряд ли могут происходить в течение ограниченного или длительного курса лечения. В настоящее время существует 7 противовирусных лекарственных средств, одобренных FDA, для лечения инфекции хронического гепатита B, включая обычные и пегилированные интерфероны и 5 пероральных нуклеозидных(нуклеотидных) аналогов (т.е. ламивудин, адефовир дипивоксил, энтекавир, телбивудин и тенофовир дисопроксил фумарат (TDF)), из которых энтекавир (ETV) и тенофовир дисопроксил фумарат рекомендованы в качестве терапевтических лекарственных средств первой линии (Liaw, Leung et al. 2008; Lok и McMahon 2009; Liu, Yang et al. 2014; Gish, Given et al. 2015). Однако после клинического применения существующих NUC лекарственных средств в течение 5 лет отрицательная конверсия HBsAg составляла менее 5%; и для субъектов, демонстрирующих ответ после лечения пегилированным интерфероном (PEG-IFN), отрицательная конверсия HBsAg составляла менее 10% в течение длительного периода последующего наблюдения (Sundaram and Kowdley 2015). Для пациентов с CHB препараты NUC могут только ингибировать синтез вирусных положительных и отрицательных цепей в нуклеокапсидах; во время противовирусной терапии главным образом исчезает репликация ДНК, и нет никакого непосредственного эффекта на кзкДНК в ядре клеток печени и транскрибируемые и экспрессируемые при этом вирусные антигены (Wong, Seto et al. 2013). Другой класс лекарственных средств, IFNб, обладает как иммунорегуляторными, так и прямыми противовирусными эффектами и может индуцировать экспрессию APOBEC3A в HBV-инфицированных клетках печени, стимулировать деградацию кзкДНК посредством редактирования оснований и оказывать непосредственное противовирусное действие (Lucifora, Xia et al. 2014). Однако было подтверждено, что HBV может антагонизировать сигнальный путь IFNб, что приводит к плохому терапевтическому эффекту IFNб препаратов (Bertoletti and Ferrari 2012). Поэтому, учитывая ограничения современных противовирусных лекарственных средств, другие терапевтические стратегии, такие как стимуляция и/или восстановление противовирусного иммунитета, в настоящее время являются наиболее актуальными в исследованиях по устранению хронической HBV инфекции (Lucifora and Trepo 2015).
Специфический для хозяина иммунный ответ важен для клиренса HBV. HBV-специфический ответ Т-лимфоцитов представляет собой наиболее важные эффекторные клетки для устранения HBV инфекции в клетках печени. После того, как HBV инфицирует и проникает в клетки печени через натриевый ион/таурохолат котранспортирующий полипептидный рецептор, вирусный геном может быть восстановлен ДНК-полимеразой хозяина с образованием стабильной ковалентно замкнутой кольцевой ДНК (кзкДНК) и паразитировать в ядре клеток печени. Важной причиной сложности терапии при клиническом противовирусном лечении является трудность удаления кзкДНК микрохромосом как исходной матрицы для репликации вируса и экспрессии генов в печени (Nassal 2015). HBV эффекторные Т-клетки могут непосредственно убивать инфицированные клетки печени, индуцировать апоптоз клеток-мишеней и устранять кзкДНК и другие вирусные продукты через киллинг-эффекты гранзимов, перфорина или цитотоксический путь апоптоза гепатоцитов, индуцированный FasL (Hoh, Heeg et al. 2015). Кроме того, цитокины, такие как IFNг и TNFб, секретируемые эффекторными Т-клетками, могут также воздействовать на инфицированные клетки печени и индуцировать внутриклеточную экспрессию антивирусных генов через нецитолитический путь для ингибирования вирусной репликации и синтеза кзкДНК (Guidotti, Rochford et al. 1999). Последние исследования показывают, что эффекторные Т-клетки могут прикрепляться к печеночным синусоидам через тромбоциты и непосредственно контактировать с инфицированными клетками печени, презентирующими вирусные антигены через эндотелиальные клеточные щели, а затем секретировать цитокины, такие как IFNг и TNFб, для непосредственной индукции апоптоза инфицированных клеток печени, чтобы устранить HBV (Guidotti, Inverso et al. 2015). Кроме того, B-клетки также играют очень важную роль в контроле HBV-инфекции. При острой HBV-инфекции антитело к поверхностному антигену вируса гепатита B (HBsAb), продуцируемое B-клетками, может нейтрализовать и блокировать HBV-инфекцию клеток печени.
Белки IAP являются ключевым классом регуляторов апоптоза и характеризуются присутствием одного или нескольких BIR (бакуловирусный IAP повтор) доменов. Среди IAP клеточные IAP1 (cIAP1) и cIAP2 играют ключевую роль в регуляции апоптоза, опосредованного рецептором смерти, в то время как X-сцепленный IAP (XIAP) ингибирует опосредованный рецептором смерти и митохондриально-опосредованный апоптоз путем связывания и ингибирования каспазы-3/7 и каспазы-9 (три цистеиновые протеазы, которые имеют критическое значение для осуществления апоптоза). Эти IAP белки сверхэкспрессируются на высоком уровне как в раковых клеточных линиях, так и в опухолевых тканях человека, и имеют низкую экспрессию в нормальных клетках и тканях. Широкие исследования показали, что сверхэкспрессия IAP белков делает раковые клетки резистентными к апоптозу, индуцируемому различными противораковыми лекарственными средствами. Подробное обсуждение белков IAP и их влияния на рак, а также апоптоз описано в патенте США № 7960372.
Одной из категорий центрального отрицательного регулятора апоптоза является ингибитор белка апоптоза (IAP). Эта категория включает белки, такие как XIAP, cIAP1, cIAP2, мл-IAP, HIAP, KIAP, TSIAP, NAIP, сурвивин, ливин, ILP-2, аполлон и BRUCE.
Также известны низкомолекулярные ингибиторы IAP белков. Например, публикация патента США № 2005/0197403 и патент США № 7960372 раскрывают димерные миметические соединения Smac. Среди них бисдиазабицикло-соединения представляют собой класс соединений, которые ингибируют IAP.
Исследования показали, что пептидные ингибиторы являются полезными инструментами для выяснения антиапоптотической функции IAP и роли IAP в ответе раковых клеток на химиотерапевтические средства. Предшествующий уровень техники не содержит никакого раскрытия или предположения, что бисдиазабицикло-соединения эффективны для ингибирования или элиминации вирусов гепатита, особенно вирусов HBV.
Сущность изобретения
В ходе исследования авторы настоящей заявки неожиданно обнаружили, что бисдиазабицикло-соединения чрезвычайно эффективны для ингибирования и/или элиминации вирусов гепатита, в особенности вируса HBV.
Соответственно, первый аспект настоящего изобретения относится к бисдиазабицикло-соединению для лечения и/или профилактики заболевания или расстройства, связанного с вирусом гепатита, где соединение представляет собой бисдиазабицикло-соединение. Кроме того, бисдиазабицикло-соединение представляет собой соединение, имеющее следующую структуру, или его фармацевтически приемлемую соль:
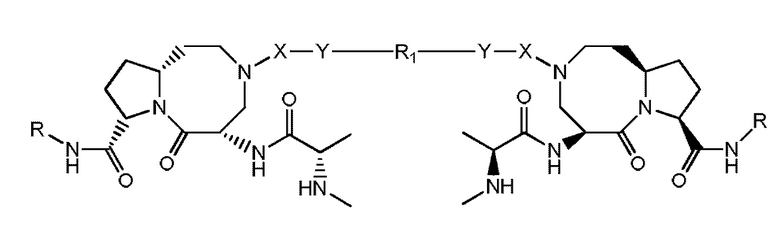 (I)
(I)
где X выбран из:  и -SO2-;
и -SO2-;
Y выбран из -NH-, -O-, -S- и отсутствует;
R выбран из 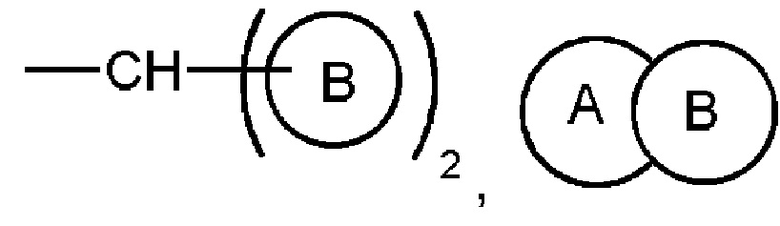 (где кольцо A представляет собой C4-8 алифатическое кольцо), -C3-6 циклоалкилен
(где кольцо A представляет собой C4-8 алифатическое кольцо), -C3-6 циклоалкилен 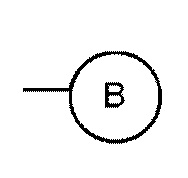 и
и 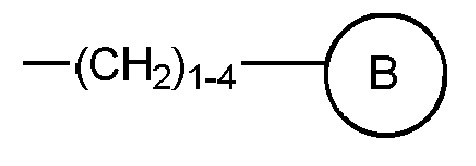 (где кольцо B представляет собой фенил, нафтил, пиридил, пиридазинил, пиразинил или пиримидинил, и кольцо B является необязательно замещенным);
(где кольцо B представляет собой фенил, нафтил, пиридил, пиридазинил, пиразинил или пиримидинил, и кольцо B является необязательно замещенным);
R1 выбран из 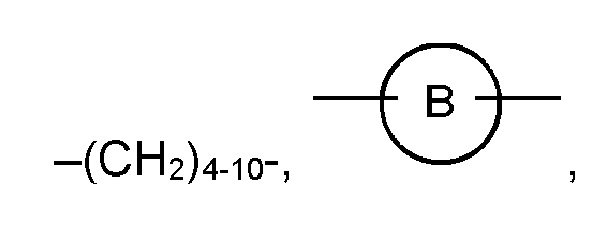
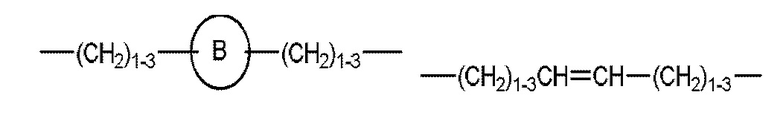 ,
,
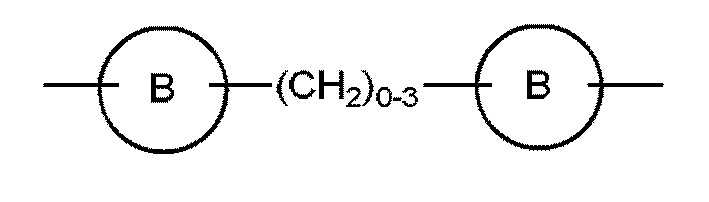 и
и 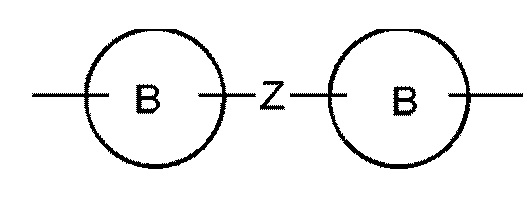 , где Z представляет собой O, S, NH или
, где Z представляет собой O, S, NH или
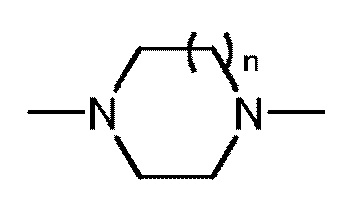 , где n имеет значение 0, 1 или 2, и где кольцо B представляет собой фенил, нафтил, пиридил, пиридазинил, пиразинил или пиримидинил, и кольцо B является необязательно замещенным.
, где n имеет значение 0, 1 или 2, и где кольцо B представляет собой фенил, нафтил, пиридил, пиридазинил, пиразинил или пиримидинил, и кольцо B является необязательно замещенным.
Предпочтительно, в соединении R представляет собой
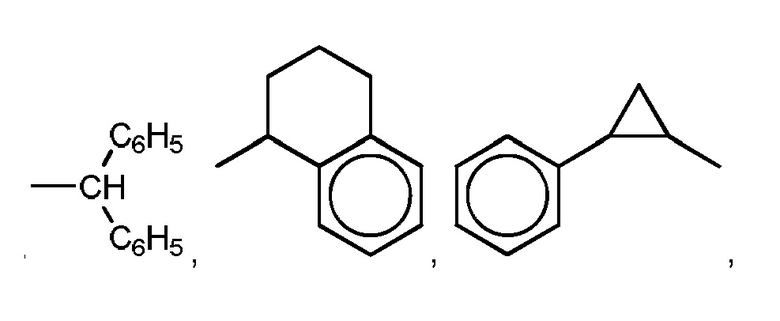
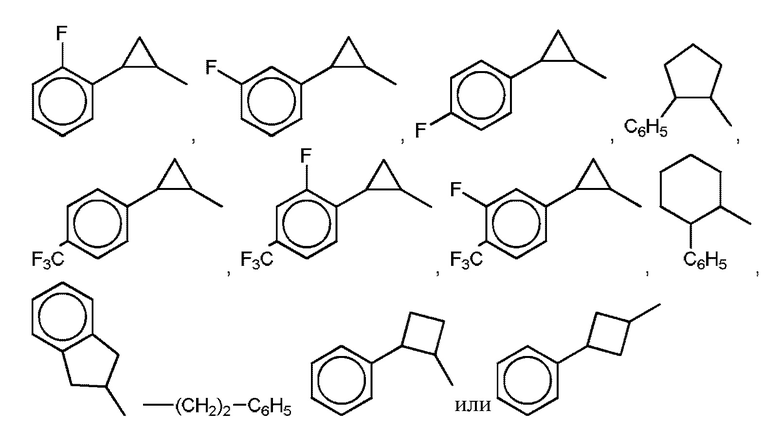
Предпочтительно, в соединении R1 представляет собой
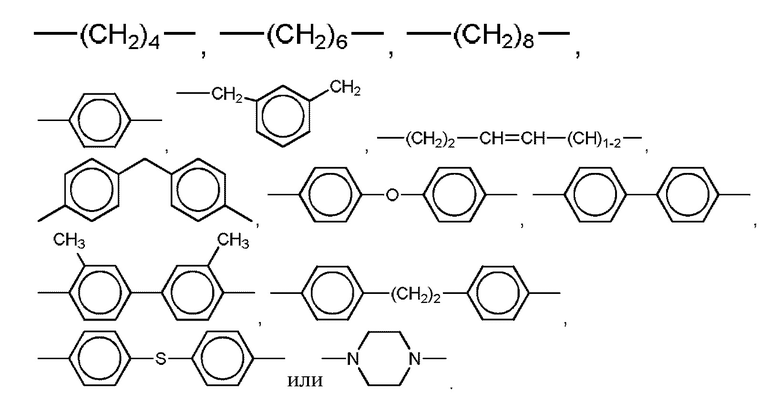
Предпочтительно, в соединении X представляет собой SO2, и Y отсутствует.
Предпочтительно, соединение представляет собой
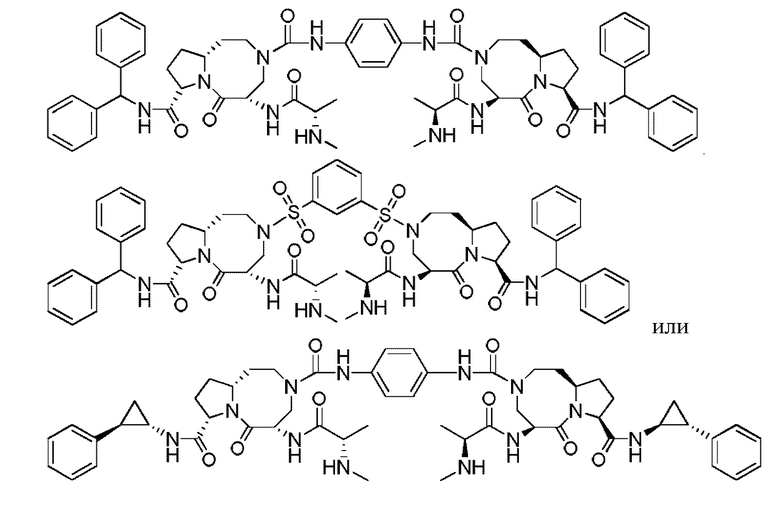 .
.
Предпочтительно, соединение выбрано из:
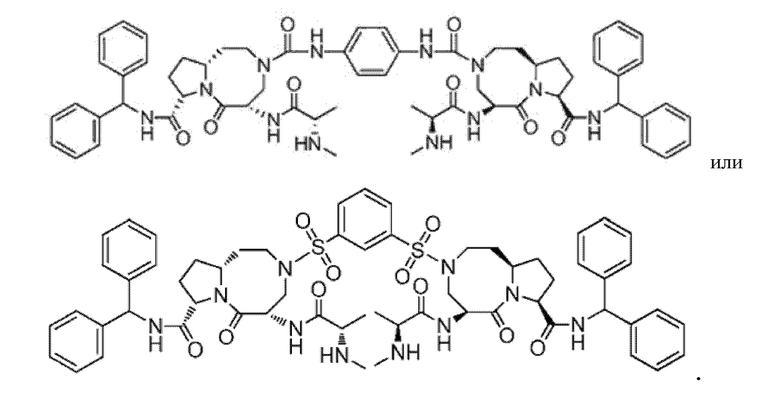
Также, заболевание или расстройство, связанное с вирусом гепатита, представляет собой заболевание или расстройство, связанное с поздней стадией вирусной инфекции гепатита. Предпочтительно, заболевание или расстройство, связанное с вирусом гепатита, представляет собой заболевание или расстройство, связанное с вирусом гепатита А, вирусом гепатита В или вирусом гепатита С. Более предпочтительно, заболевание или расстройство, связанное с вирусом гепатита, включает, но не ограничивается этим: гепатит A, гепатит B, гепатит C и цирроз печени. Кроме того, соединение лечит и/или предотвращает заболевание или расстройство, связанное с вирусом гепатита, путем модулирования иммунного ответа.
Второй аспект настоящего изобретения относится к применению соединения, определенного выше, для получения лекарственного средства для лечения и/или профилактики заболевания или расстройства, связанного с вирусом гепатита.
Третий аспект настоящего изобретения относится к способу лечения и/или профилактики заболевания или расстройства, связанного с вирусом гепатита, включающему введение терапевтически и/или профилактически эффективного количества соединения пациенту, страдающему от заболевания или расстройства, связанного с вирусом гепатита, и при этом соединение представляет собой бисдиазабицикло-соединение.
Четвертый аспект настоящего изобретения относится к фармацевтической композиции, включающей соединение, определенное выше, где фармацевтическая композиция является полезной для лечения и/или профилактики заболевания или расстройства, связанного с вирусом гепатита.
Описание чертежей
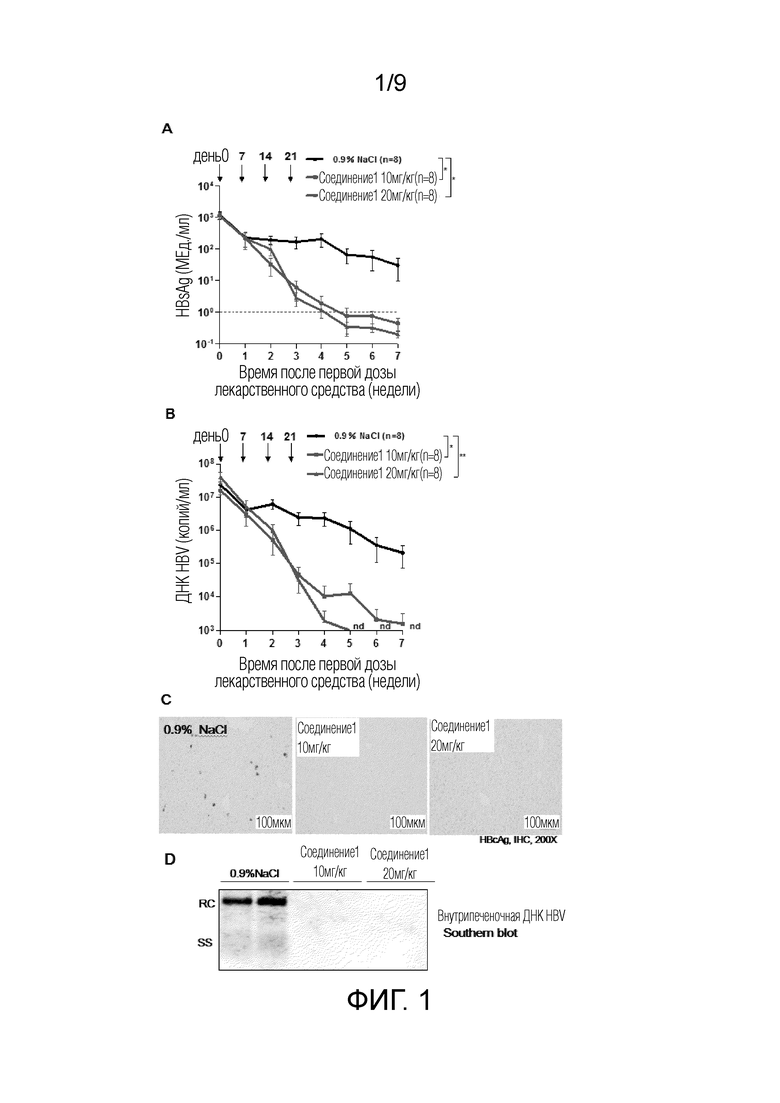
Фиг. 1 показывает эффект инъекции одной дозы Соединения 1 на HBV в мышиной модели C57BL/6J, установленной путем инъекции плазмиды pAAV-HBV1.2 в хвостовую вену под высоким давлением. A: динамические изменения HBsAg в сыворотке для каждой группы; B: динамические изменения ДНК HBV в сыворотке для каждой группы; C: экспрессия HBcAg в ткани печени для каждой группы, определенная через 7 недель иммуногистохимическим окрашиванием; D: средний уровень репликации HBV в печени для каждой группы, определенный через 7 недель саузерн-блот методом.
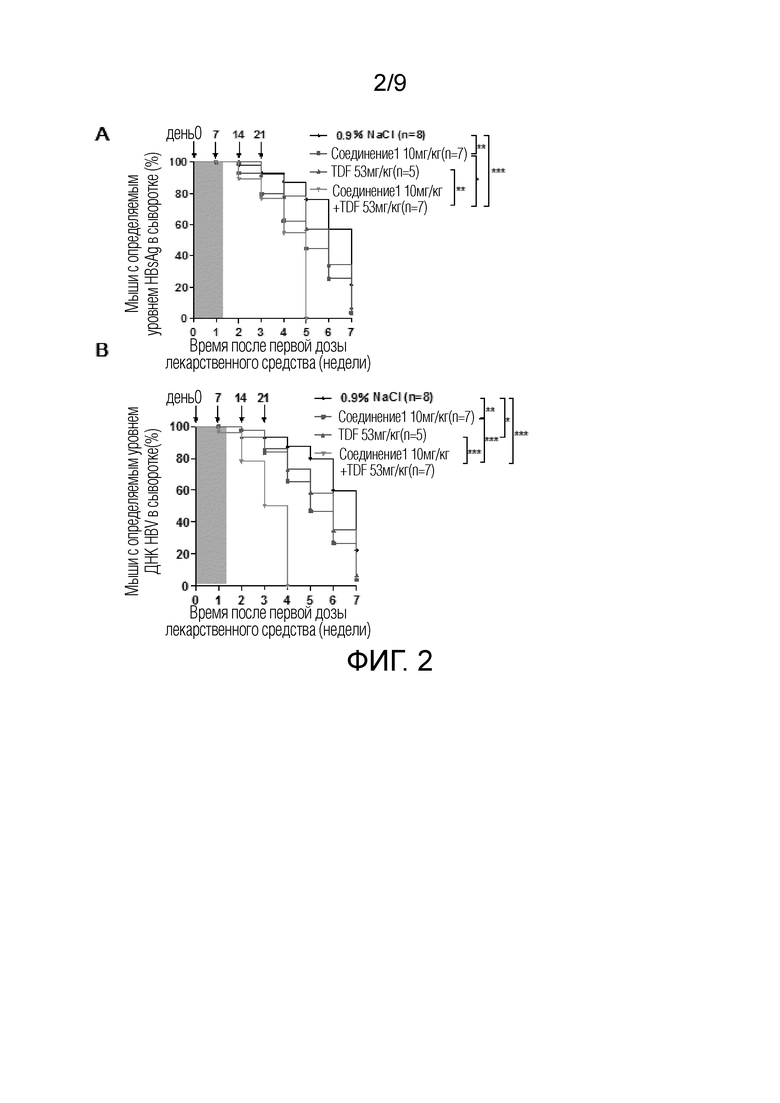
Фиг. 2 показывает эффект введения Соединения 1 в комбинации с тенофовир дисопроксил фумаратом (TDF) на HBV в мышиной модели C57BL/6J, установленный путем инъекции плазмиды pAAV-HBV1.2 в хвостовую вену под высоким давлением. A: сравнение скоростей клиренса HBsAg из сыворотки для разных групп в разные моменты времени; B: сравнение скоростей клиренса ДНК HBV в сыворотке для разных групп в разные моменты времени.
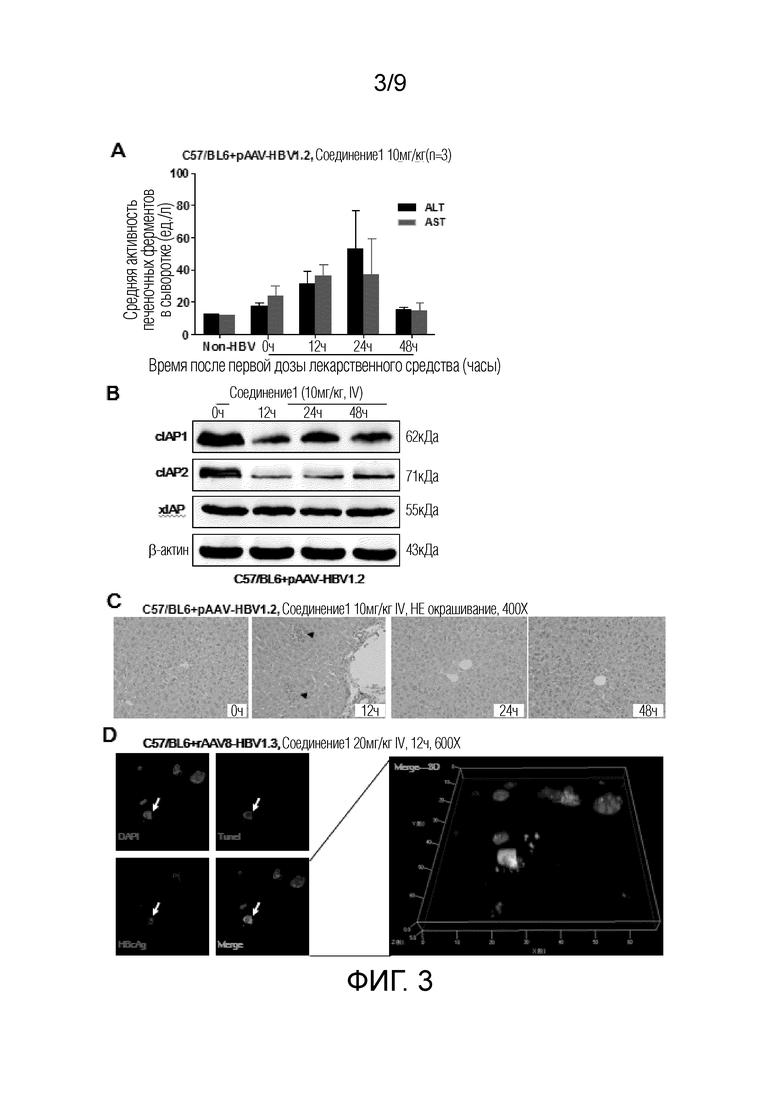
Фиг. 3 показывает эффект Соединения 1 на апоптоз гепатоцитов у HBV-инфицированных мышей. A: динамические изменения ALT и AST в сыворотке в разные моменты времени после инъекции Соединения 1 мышам C57BL/6J, которым вводили под высоким давлением инъекцию плазмиды pAAV-HBV1.2 в хвостовую вену; B: изменения экспрессии cIAPs в ткани печени в разные моменты времени после инъекции Соединения 1: C: HE окрашивание срезов ткани печени мышей в разные моменты времени после инъекции Соединения 1; D: апоптоз HBV-инфицированных клеток печени, определенный методом HBcAg иммунофлуоресценции и двойного окрашивания Tunnel.
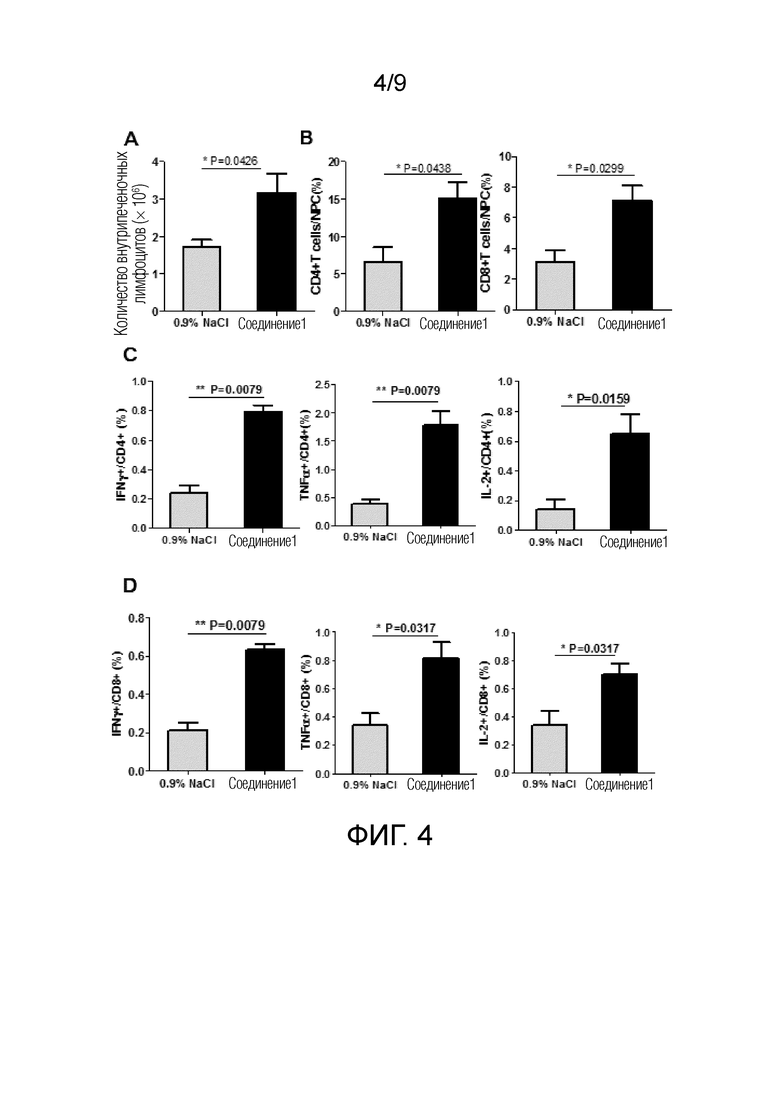
Фиг. 4 показывает эффект влияния лечения Соединением 1 на иммунный ответ на HBV у мышей. A: изменения общего количества лимфоцитов в печени после элиминации вирусов из печени мышей в группе обработки Соединением 1; B: изменение количества инфильтрированных CD4+ T-клеток и CD8+ T-клеток в печени; C: функция HBV-специфических CD4+ T-клеток в отношении секреции IFNг, TNFб, IL-2; D: функция HBV-специфических CD8+ T-клеток в отношении секреции IFNг, TNFб, IL-2.
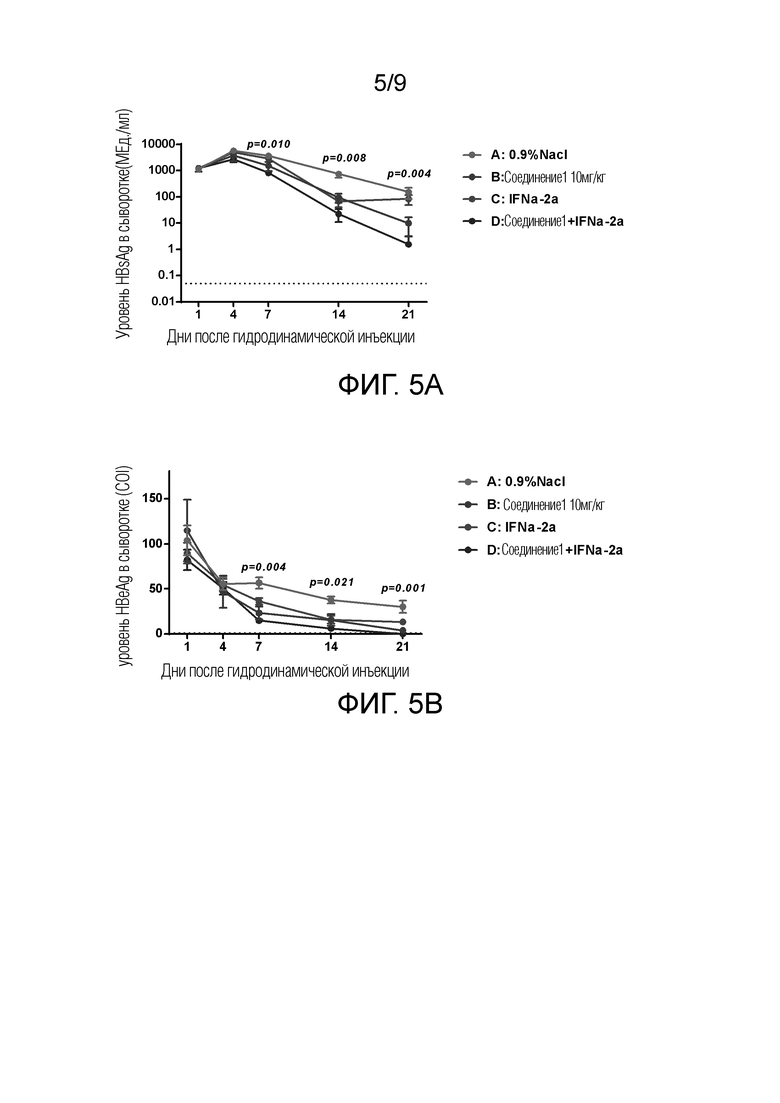
Фиг. 5 показывает анти-HBV эффект введения Соединения 1 в комбинации с IFNб2a в C57BL/6J мышиной модели хронической HBV-инфекции. Фиг. 5A: изменения индивидуальных уровней HBsAg в сыворотке в разные моменты времени в течение 21 дня после первого введения для каждой группы (Группа А (группа, получавшая инъекцию 0,9% физиологического раствора): pAAV-HBV1.2+pKCMvint+0,9%NaCl; Группа В (группа, получавшая внутривенную инъекцию 10 мг/кг Соединения 1): pAAV-HBV1.2+pKCMvint+Соединение 1 10 мг/кг; Группа С (группа IFNб-2a): pAAV-HBV1.2+pKCMvint IFNб-2a+0,9%NaCl; Группа D (группа введения Соединения 1 в комбинации с IFNб-2a): pAAV-HBV1.2+pKCMvint IFNб-2a+APG 10 мг/кг). Фиг. 5B: изменения индивидуальных уровней HBeAg в сыворотке в разные моменты времени в течение 21 дня после первого введения для каждой группы (Группа А (группа, получавшая инъекцию 0,9% физиологического раствора): pAAV-HBV1.2+pKCMvint+0,9%NaCl; Группа В (группа, получавшая внутривенную инъекцию 10 мг/кг Соединения 1): pAAV-HBV1.2+pKCMvint+Соединение 1 10 мг/кг; Группа С (группа IFNб-2a): pAAV-HBV1.2+pKCMvint IFNб-2a+0,9%NaCl; Группа D (группу введения Соединения 1 в комбинации с IFNб-2a): pAAV-HBV1.2+pKCMvint IFNб-2a+APG 10 мг/кг).
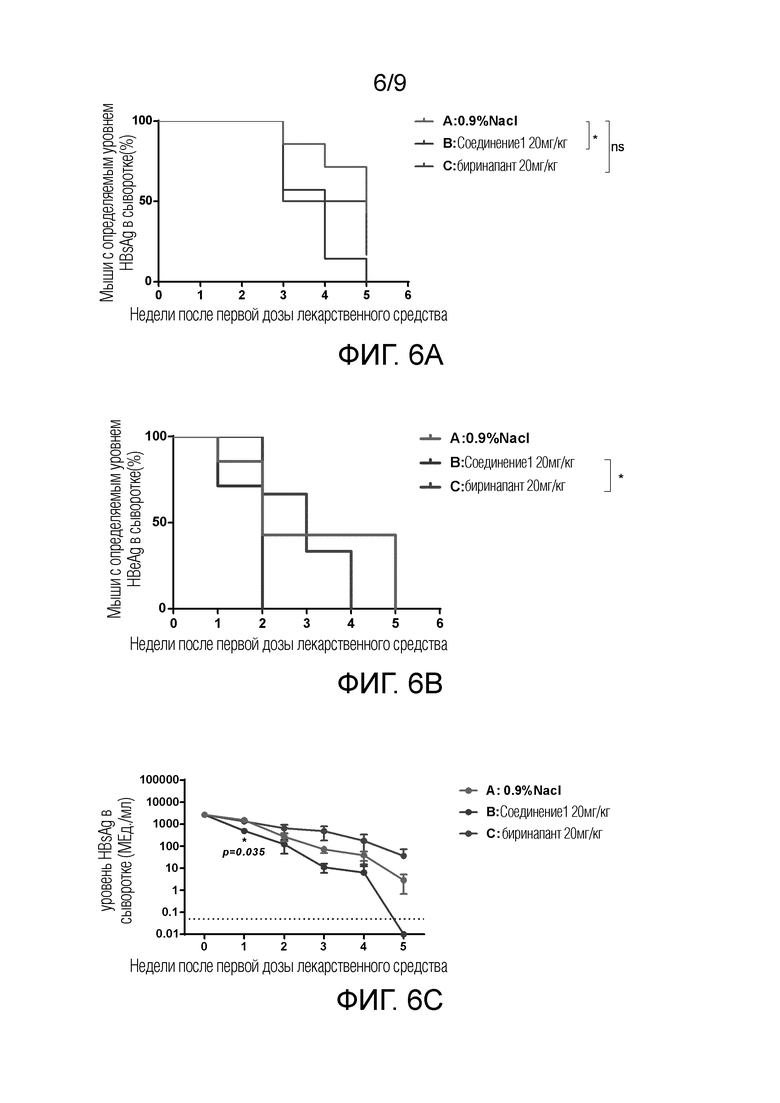
Фиг. 6 показывает сравнение анти-HBV эффектов Соединения 1 и Биринапанта в C57BL/6J мышиной модели с хронической HBV-инфекцией, установленной путем инъекции плазмиды pAAV-HBV1.2 в хвостовую вену под высоким давлением. Фиг. 6A: изменения общего уровня HBsAg в сыворотке в разные моменты времени в течение пяти недель после первого введения для каждой группы (Группа А: группа, получавшая инъекцию физиологического раствора 0,9% NaCl; Группа В: группа, получавшая внутривенную инъекцию 20 мг/кг Соединения 1; Группа С: группа, получавшая внутривенную инъекцию 20 мг/кг Биринапанта); Фиг. 6B: изменения общего уровня HBeAg в сыворотке в разные моменты времени в течение пяти недель после первого введения для каждой группы (Группа А: группа, получавшая инъекцию физиологического раствора 0,9% NaCl; Группа В: группа, получавшая внутривенную инъекцию 20 мг/кг Соединения 1; Группа С: группа, получавшая внутривенную инъекцию 20 мг/кг Биринапанта); Фиг. 6C: изменения индивидуальных уровней HBsAg в сыворотке в разные моменты времени в течение пяти недель после первого введения для каждой группы (Группа А: группа, получавшая инъекцию физиологического раствора 0,9% NaCl; Группа В: группа, получавшая внутривенную инъекцию 20 мг/кг Соединения 1; Группа С: группа, получавшая внутривенную инъекцию 20 мг/кг Биринапанта); Фиг. 6D: изменения индивидуальных уровней HBeAg в сыворотке в разные моменты времени в течение четырех недель после первого введения для каждой группы (Группа А: группа, получавшая инъекцию физиологического раствора 0,9% NaCl; Группа В: группа, получавшая внутривенную инъекцию 20 мг/кг Соединения 1; Группа С: группа, получавшая внутривенную инъекцию 20 мг/кг Биринапанта).
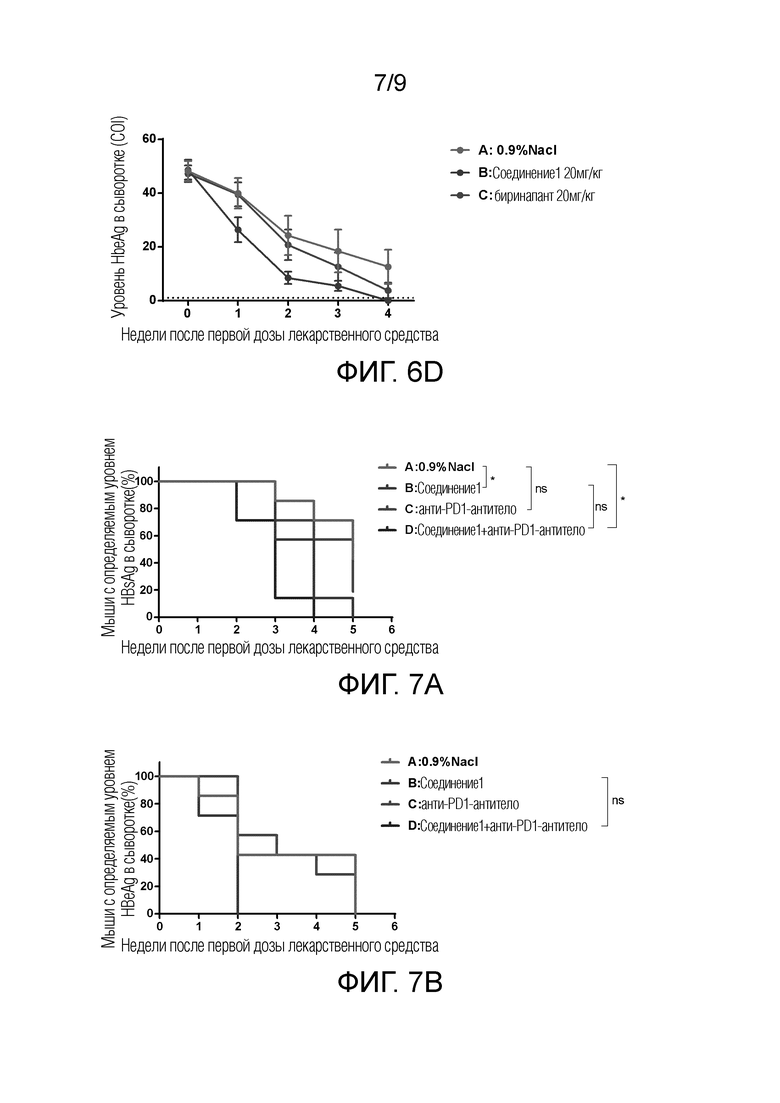
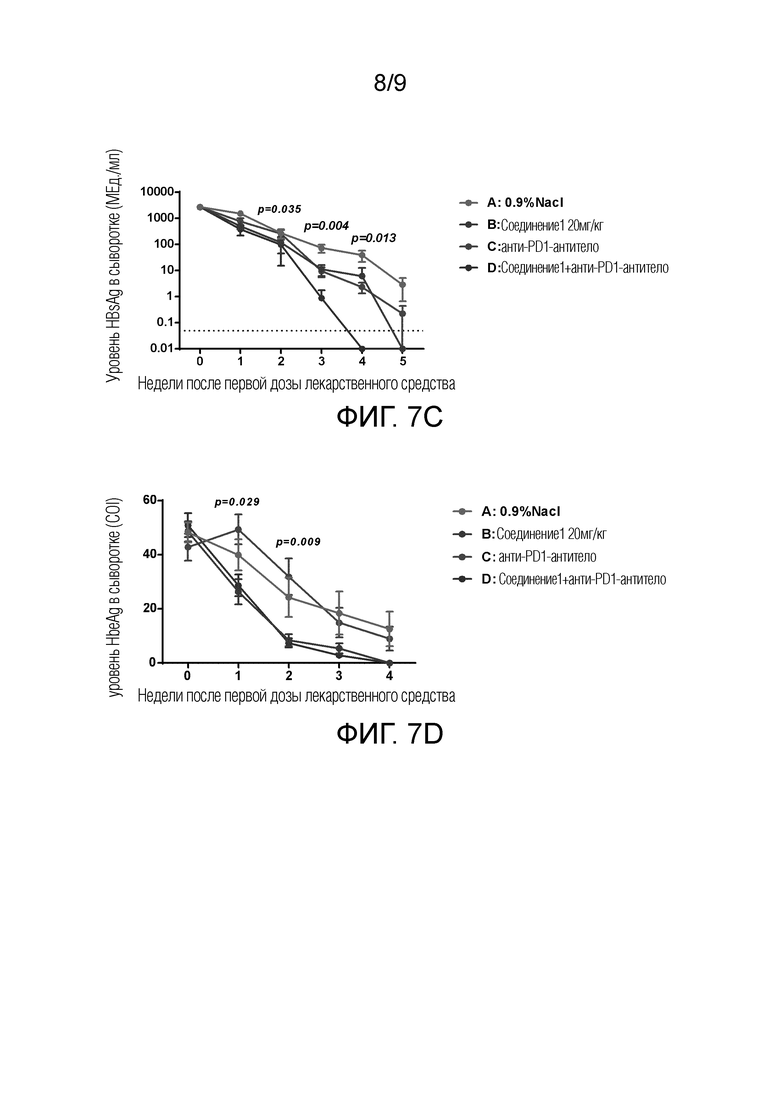
Фиг. 7 показывает анти-HBV эффект введения Соединения 1 в комбинации с анти-PD1 антителом в C57BL/6J мышиной модели хронической HBV-инфекции, установленной путем инъекции плазмиды pAAV-HBV1.2 в хвостовую вену под высоким давлением. Фиг. 7A: изменения общего уровня HBsAg в сыворотке в разные моменты времени в течение пяти недель после первого введения для каждой группы (Группа А: группа, получавшая инъекцию физиологического раствора 0,9% NaCl; Группа В: группа, получавшая внутривенную инъекцию 20 мг/кг Соединения 1; Группа С: группа, получавшая внутрибрюшинную инъекцию анти-PD1 антитела; Группа D: группа введения Соединения 1 в комбинации с анти-PD1 антителом); Фиг. 7B: изменения общего уровня HBeAg в сыворотке в разные моменты времени в течение пяти недель после первого введения для каждой группы (Группа А: группа, получавшая инъекцию физиологического раствора 0,9% NaCl; Группа В: группа, получавшая внутривенную инъекцию 20 мг/кг Соединения 1; Группа С: группа, получавшая внутрибрюшинную инъекцию анти-PD1 антитела; Группа D: группа введения Соединения 1 в комбинации с анти-PD1 антителом); Фиг. 7C: изменения индивидуальных уровней HBsAg в сыворотке в разные моменты времени в течение пяти недель после первого введения для каждой группы (Группа А: группа, получавшая инъекцию физиологического раствора 0,9% NaCl; Группа В: группа, получавшая внутривенную инъекцию 20 мг/кг Соединения 1; Группа С: группа, получавшая внутрибрюшинную инъекцию анти-PD1 антитела; Группа D: группа введения Соединения 1 в комбинации с анти-PD1 антителом); Фиг. 7D: изменения индивидуальных уровней HBeAg в сыворотке в разные моменты времени в течение четырех недель после первого введения для каждой группы (Группа А: группа, получавшая инъекцию физиологического раствора 0,9% NaCl; Группа В: группа, получавшая внутривенную инъекцию 20 мг/кг Соединения 1; Группа С: группа, получавшая внутрибрюшинную инъекцию анти-PD1 антитела; Группа D: группа введения Соединения 1 в комбинации с анти-PD1 антителом).
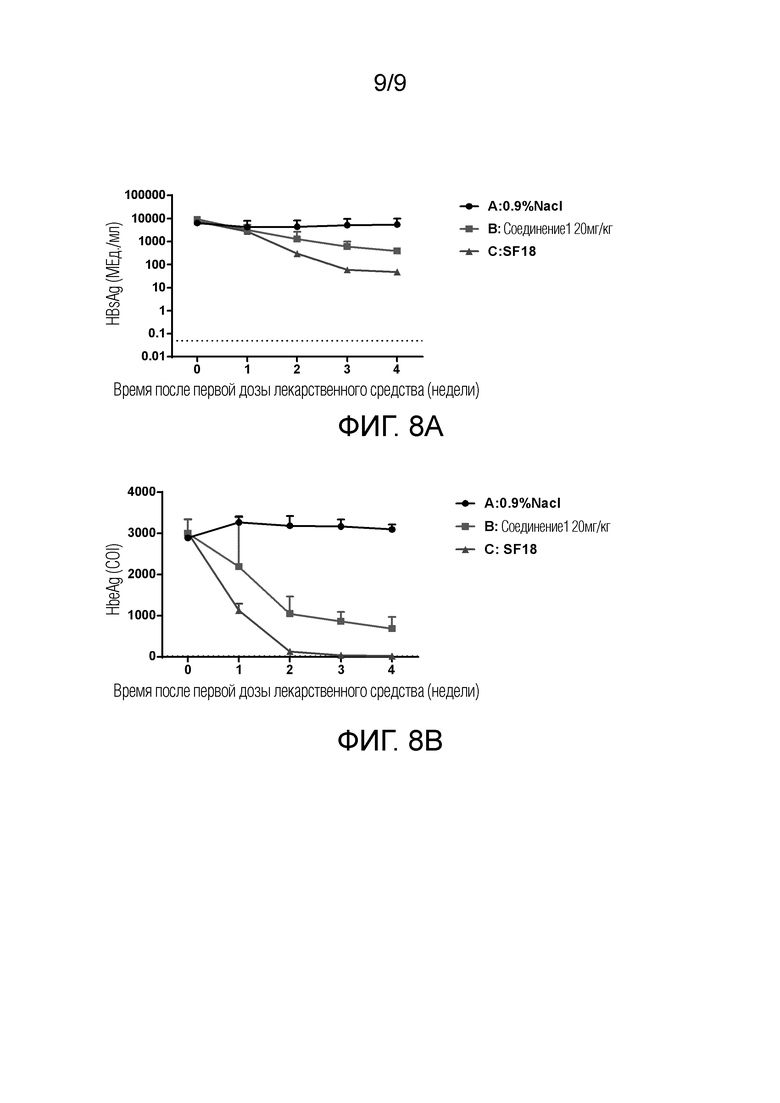
Фиг. 8 показывает анти-HBV эффекты Соединения 1 и SF18 в C57BL/6J мышиной модели, установленной путем инъекции вируса rAAV8-HBV1.3 (ayw) в хвостовую вену. Фиг. 8A: изменения индивидуальных уровней HBsAg в разные моменты времени в течение четырех недель после первого введения для каждой группы (Группа А: группа, получавшая инъекцию физиологического раствора 0,9% NaCl; Группа В: группа, получавшая внутривенную инъекцию 20 мг/кг Соединения 1; Группа С: группа, получавшая внутривенную инъекцию SF18 20 мг/кг); Фиг. 8B: изменения индивидуальных уровней HBeAg в разные моменты времени в течение четырех недель после первого введения для каждой группы (Группа А: группа, получавшая инъекцию физиологического раствора 0,9% NaCl; Группа В: группа, получавшая внутривенную инъекцию 20 мг/кг Соединения 1; Группа С: группа, получавшая внутривенную инъекцию SF18 20 мг/кг).
Подробное описание изобретения
Определения
Термин "C4-8 алифатическое кольцо" в контексте настоящей заявки относится к циклобутилу, циклопентилу, циклогексилу, циклогептилу или циклооктилу, незамещенному или замещенному 1-3 группами (например, C1-4 алкилом, галогеном, трифторметилом, трифторметокси, гидрокси, алкокси, нитро, циано, алкиламино или амино).
Термин "алкил" в контексте настоящей заявки относится к насыщенной C1-10 углеводородной группе с прямой или разветвленной цепью, и ее неограничивающие примеры включают метил, этил и пропил, бутил, пентил, гексил, гептил, октил, нонил и децил с прямой или разветвленной цепью.
Термин "C3-6 циклоалкилен" относится к дизамещенному циклоалкану, содержащему 3-6 атомов углерода, например, 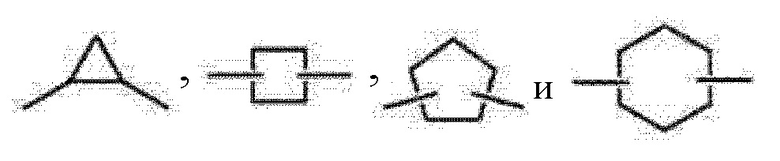 . "C3-6 циклоалкилен" может быть незамещенным или замещен 1-3 группами, такими как C1-4 алкил, галоген, трифторметил, трифторметокси, гидрокси, алкокси, нитро, циано, алкиламино или амино.
. "C3-6 циклоалкилен" может быть незамещенным или замещен 1-3 группами, такими как C1-4 алкил, галоген, трифторметил, трифторметокси, гидрокси, алкокси, нитро, циано, алкиламино или амино.
Термин "галоген" в контексте настоящей заявки определен как фтор, хлор, бром или йод.
Термин "гидрокси" в контексте настоящей заявки определен как -OH.
Термин "алкокси" в контексте настоящей заявки определен как -OR, где R представляет собой алкил.
Термин "амино" в контексте настоящей заявки определен как -NH2, и термин "алкиламино" определен как -NR2, где по меньшей мере один R представляет собой алкильную группу, а второй R представляет собой алкильную группу или водород.
Термин "нитро" в контексте настоящей заявки определен как -NO2.
Термин "циано" в контексте настоящей заявки определен как -CN.
Термин "трифторметил" в контексте настоящей заявки определен как -CF3.
Термин "трифторметокси" в контексте настоящей заявки определен как -OCF3.
Термин "необязательно замещенный" в контексте настоящей заявки означает замещенный одной или несколькими, в частности, одной-четырьмя группами, независимо выбранными из, например, галогена, алкила, алкенила, -OCF3, -NO2, -CN, -NC, -OH, алкокси, амино, алкиламино, -CO2H, -CO2алкила, алкинила, циклоалкила, нитро, меркапто, имино, амидо, фосфоната, фосфината, силила, алкилтио, сульфонила, сульфонамидо, альдегида, гетероциклоалкила, трифторметила, арила и гетероарила.
Термин "арил" в контексте настоящей заявки относится к моноциклической или полициклической ароматической группе, предпочтительно моноциклической или бициклической ароматической группе, такой как фенил или нафтил.
Термин "гетероарил" в контексте настоящей заявки относится к моноциклической или бициклической кольцевой системе, содержащей одно или два ароматических кольца и содержащей по меньшей мере от одного и до четырех атомов азота в одном из ароматических колец.
Термин "заболевание" или "расстройство" означает нарушенное и/или аномальное состояние, которое обычно рассматривается как патологическое состояние или функция, и которое может проявляться как специфические признаки, расстройства и/или дисфункции.
Термин "лечение" заболевания или расстройства означает элиминацию, ингибирование, ослабление или облегчение заболевания или расстройства, и термин "профилактика" означает недопущение и избежание заболевания или расстройства, или предотвращение возникновения или появления заболевания или расстройства.
Первый аспект настоящего изобретения относится к бисдиазабицикло-соединению, которое используют для лечения и/или профилактики или устранения и/или облегчения заболевания или расстройства, связанного с вирусом гепатита, где соединение представляет собой бисдиазабицикло-соединение.
Бисдиазабицикло-соединение представляет собой соединение, имеющее следующую структуру, или его фармацевтически приемлемую соль:
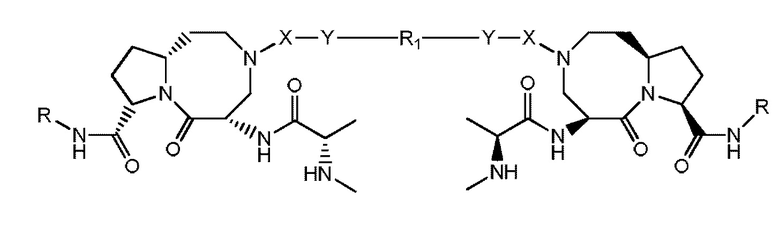 (I)
(I)
где X выбран из: 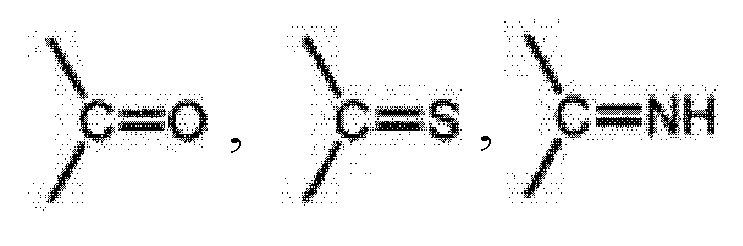 и -SO2-;
и -SO2-;
Y выбран из -NH-, -O-, -S- и отсутствует;
R выбран из 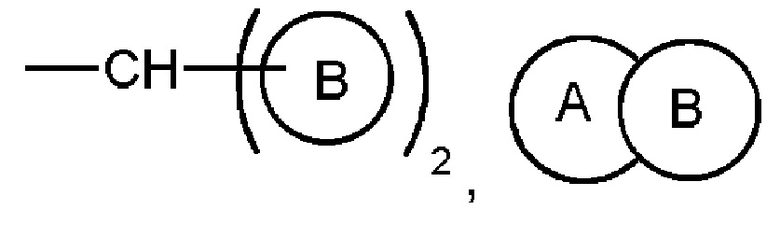 (где кольцо A представляет собой C4-8 алифатическое кольцо), -C3-6 циклоалкилен
(где кольцо A представляет собой C4-8 алифатическое кольцо), -C3-6 циклоалкилен 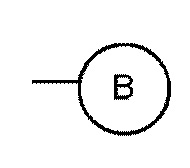 и
и 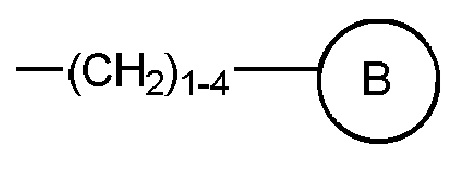 (где кольцо B представляет собой фенил, нафтил, пиридил, пиридазинил, пиразинил или пиримидинил, и кольцо B является необязательно замещенным);
(где кольцо B представляет собой фенил, нафтил, пиридил, пиридазинил, пиразинил или пиримидинил, и кольцо B является необязательно замещенным);
R1 выбран из 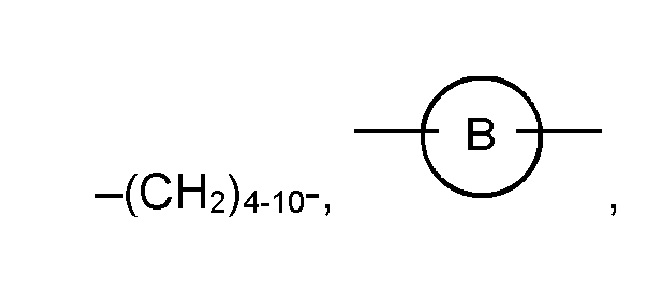
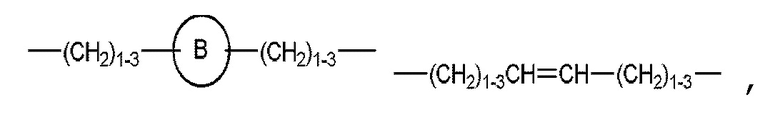
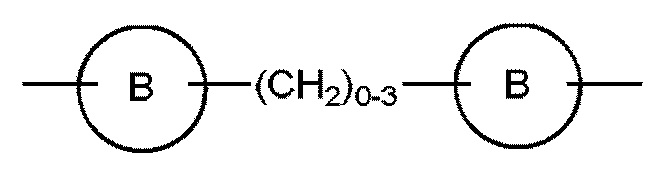 и
и 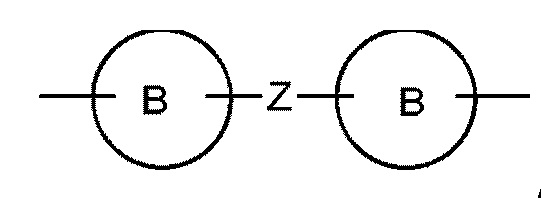 , где Z представляет собой O, S, NH или
, где Z представляет собой O, S, NH или
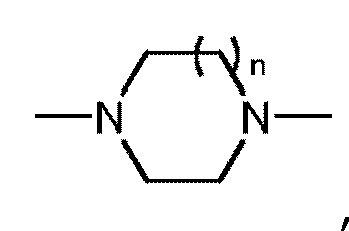 где n имеет значение 0, 1 или 2, и где кольцо B представляет собой фенил, нафтил, пиридил, пиридазинил, пиразинил или пиримидинил, и кольцо B является необязательно замещенным.
где n имеет значение 0, 1 или 2, и где кольцо B представляет собой фенил, нафтил, пиридил, пиридазинил, пиразинил или пиримидинил, и кольцо B является необязательно замещенным.
Предпочтительно, в соединении R представляет собой
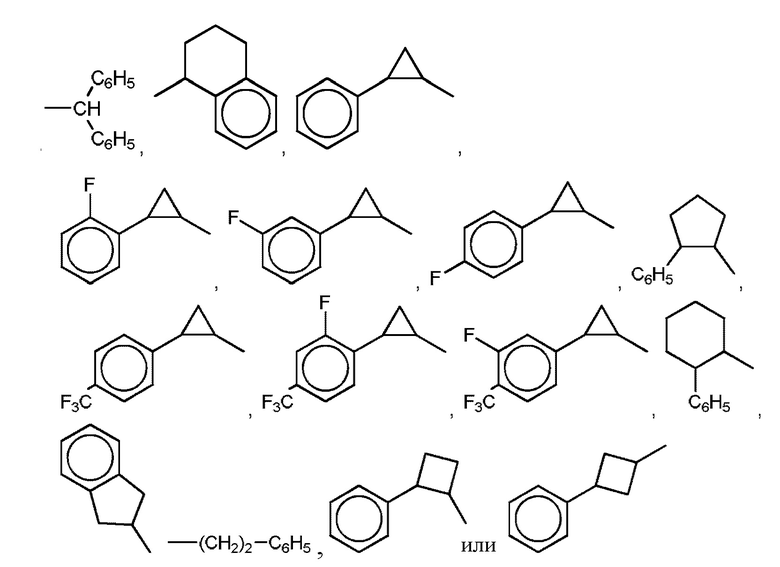
Предпочтительно, в соединении R1 представляет собой
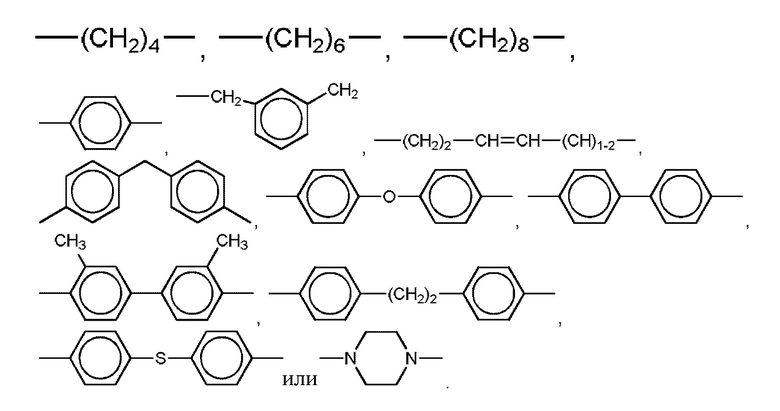
Предпочтительно, в соединении X представляет собой SO2, и Y отсутствует.
Предпочтительно, соединение представляет собой
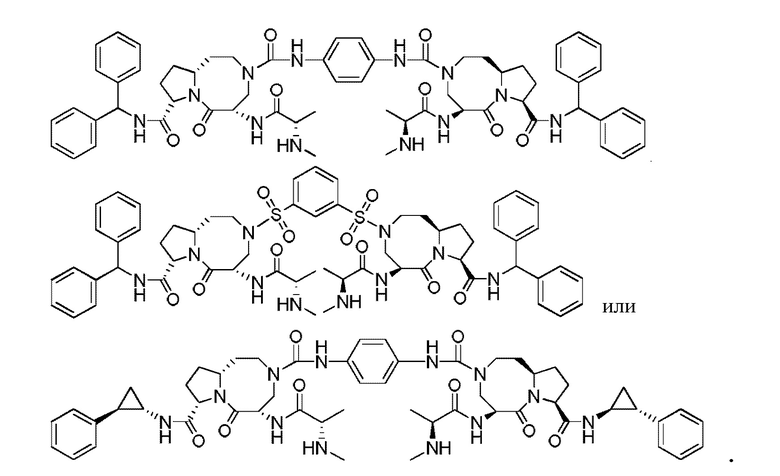
Также, бисдиазабицикло-соединение представляет собой соединение, имеющее следующую структуру, или его фармацевтически приемлемую соль:
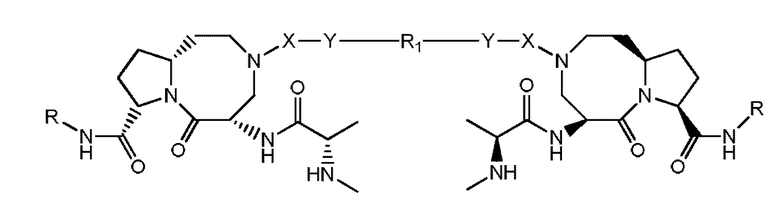 (I)
(I)
где X выбран из: 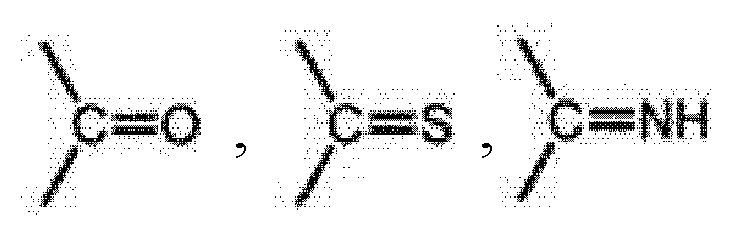 и -SO2-;
и -SO2-;
Y выбран из -NH-, -O-, -S- и отсутствует, когда X представляет собой -SO2-;
R выбран из 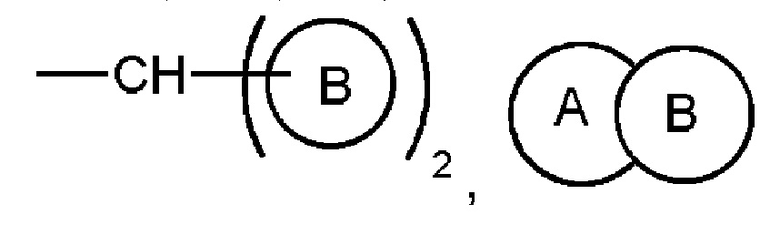 и -C3-6 циклоалкилена
и -C3-6 циклоалкилена 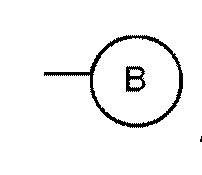 ; и
; и
R1 выбран из 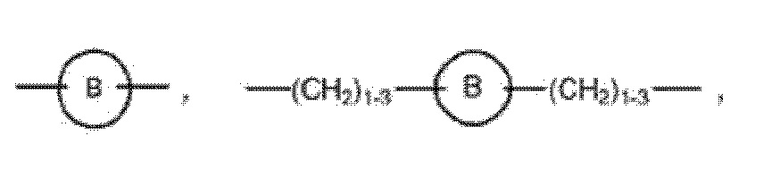
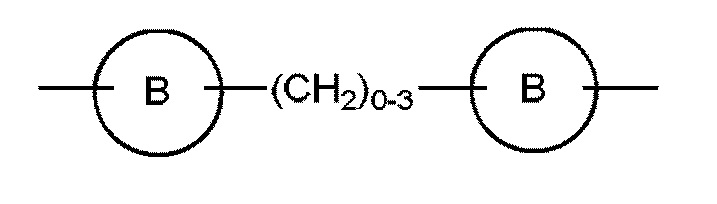 и
и 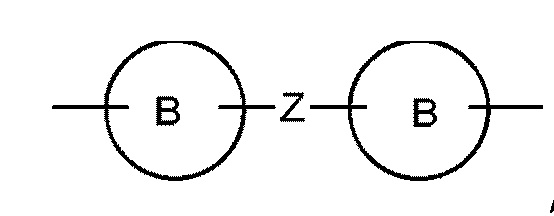 , где Z представляет собой O, S или NH;
, где Z представляет собой O, S или NH;
где кольцо A представляет собой C4-8 алифатическое кольцо; и B представляет собой фенил, нафтил, пиридил, пиридазинил, пиразинил или пиримидинил, и необязательно замещен 1-4 группами, независимо выбранными из галогена, -OCF3, -NO2, -CN, -NC, -OH, амино, C1-10 алкила, C1-10 алкилокси и C1-10 алкиламино.
Предпочтительно, в соединении R представляет собой 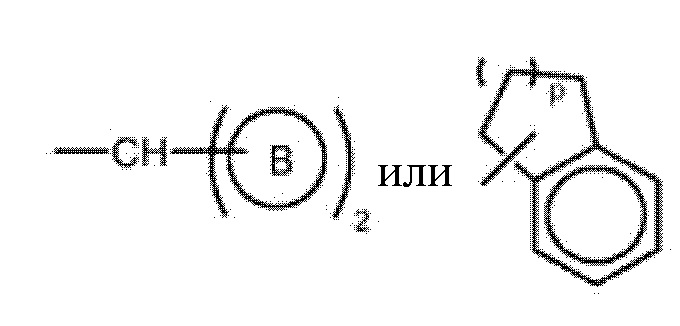 , где p имеет значение от 0 до 4.
, где p имеет значение от 0 до 4.
Предпочтительно, в соединении R представляет собой 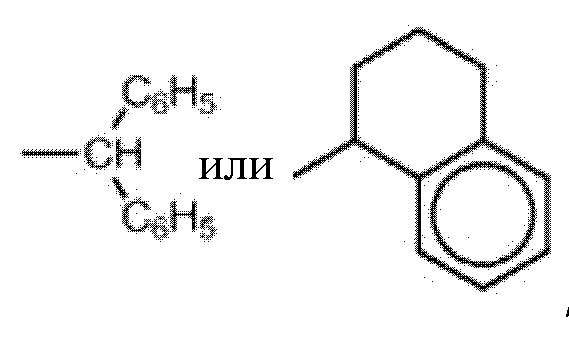 , где фенил необязательно замещен 1-4 группами, независимо выбранными из галогена, -OCF3, -NO2, -CN, -NC, -OH, амино, C1-10 алкила, C1-10 алкилокси и C1-10 алкиламино.
, где фенил необязательно замещен 1-4 группами, независимо выбранными из галогена, -OCF3, -NO2, -CN, -NC, -OH, амино, C1-10 алкила, C1-10 алкилокси и C1-10 алкиламино.
Предпочтительно, в соединении R представляет собой 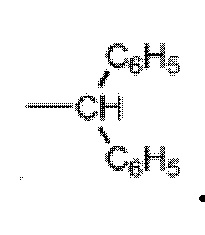 .
.
Предпочтительно, в соединении R1 представляет собой, 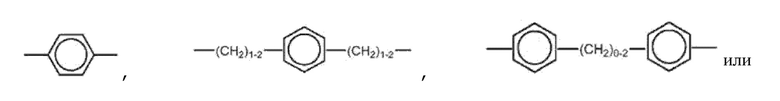
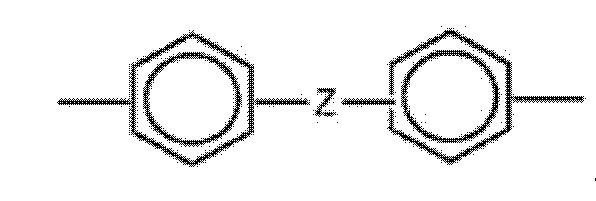 , где фенил необязательно замещен 1-4 группами, независимо выбранными из галогена, -OCF3, -NO2, -CN, -NC, -OH, амино, C1-10 алкила, C1-10 алкилокси и C1-10 алкиламино.
, где фенил необязательно замещен 1-4 группами, независимо выбранными из галогена, -OCF3, -NO2, -CN, -NC, -OH, амино, C1-10 алкила, C1-10 алкилокси и C1-10 алкиламино.
Предпочтительно, в соединении R1 представляет собой 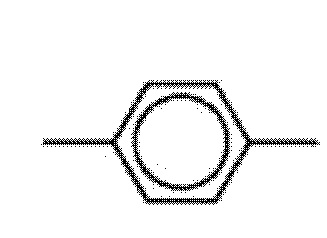 или
или 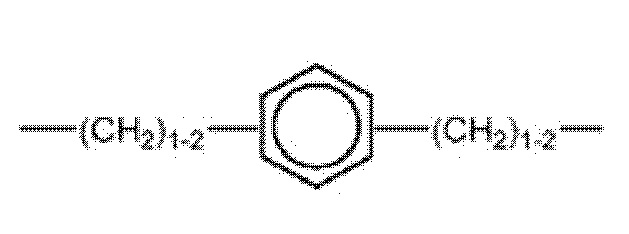 , где фенил необязательно замещен 1-4 группами, независимо выбранными из галогена, -OCF3, -NO2, -CN, -NC, -OH, амино, C1-10 алкила, C1-10 алкилокси и C1-10 алкиламино.
, где фенил необязательно замещен 1-4 группами, независимо выбранными из галогена, -OCF3, -NO2, -CN, -NC, -OH, амино, C1-10 алкила, C1-10 алкилокси и C1-10 алкиламино.
Предпочтительно, в соединении X представляет собой 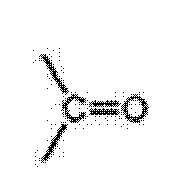 , и Y представляет собой -NH-.
, и Y представляет собой -NH-.
Предпочтительно, в соединении X представляет собой  , и Y представляет собой -NH-.
, и Y представляет собой -NH-.
Предпочтительно, в соединении X представляет собой 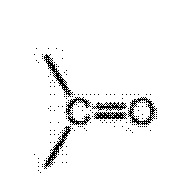 , и Y представляет собой O.
, и Y представляет собой O.
Предпочтительно, соединение выбрано из
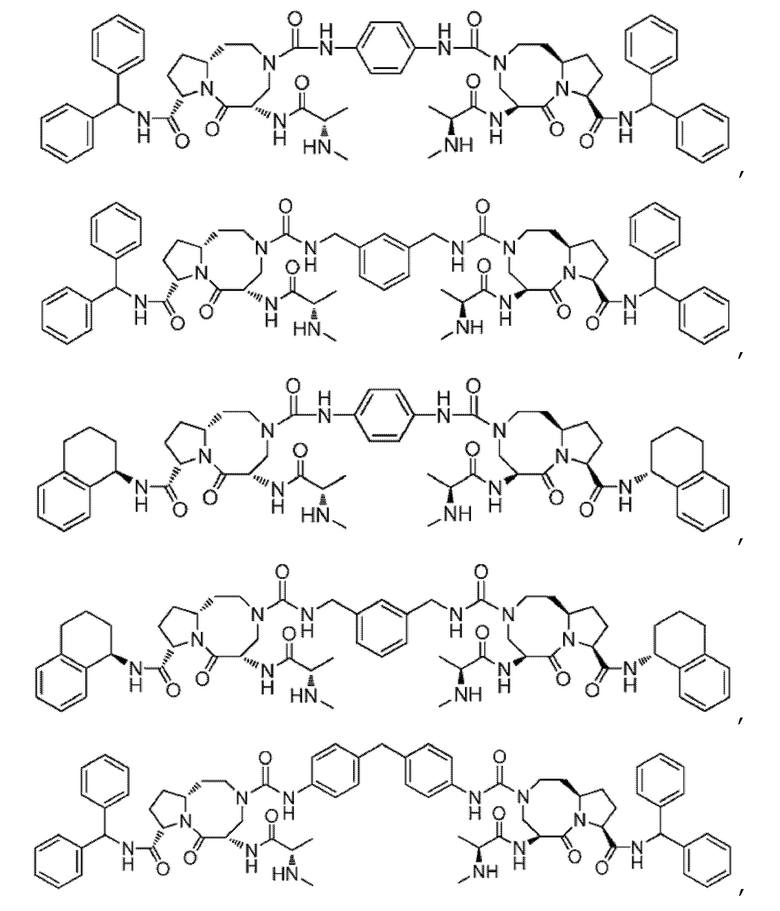
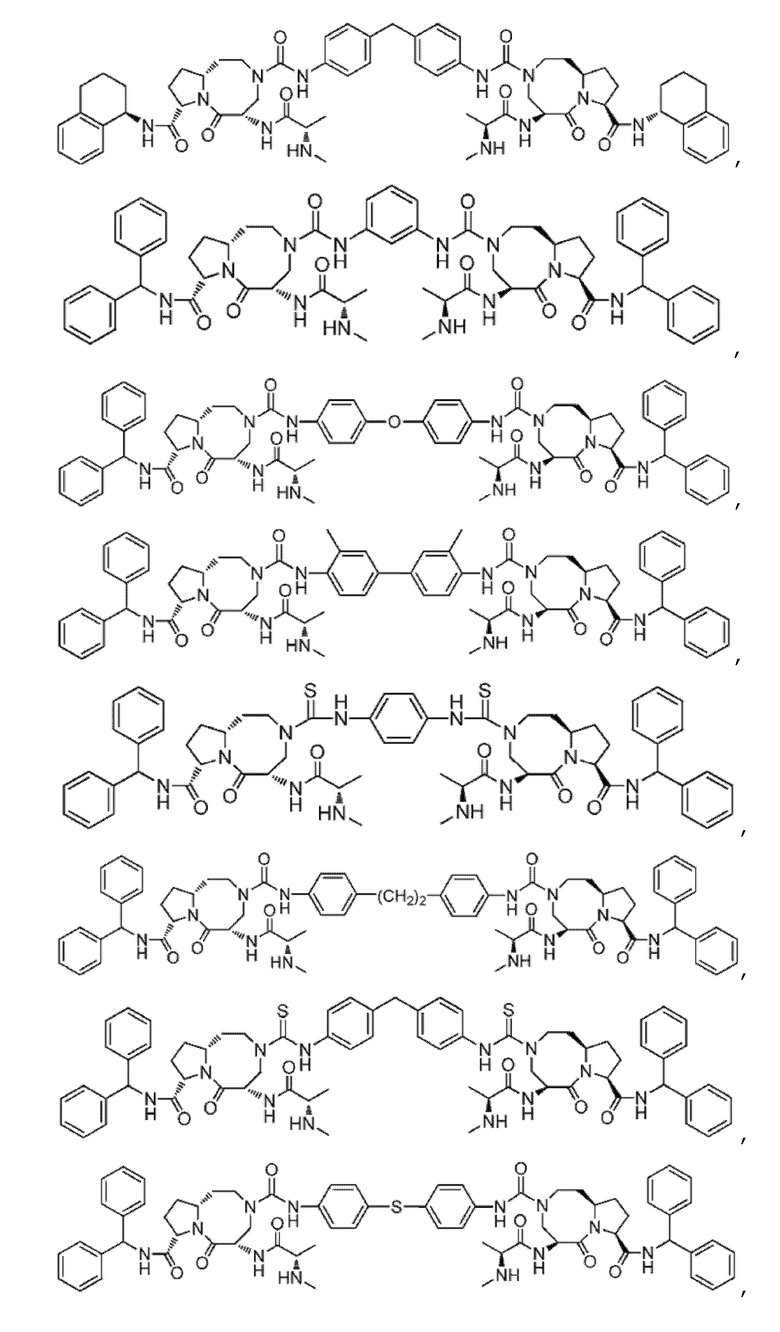
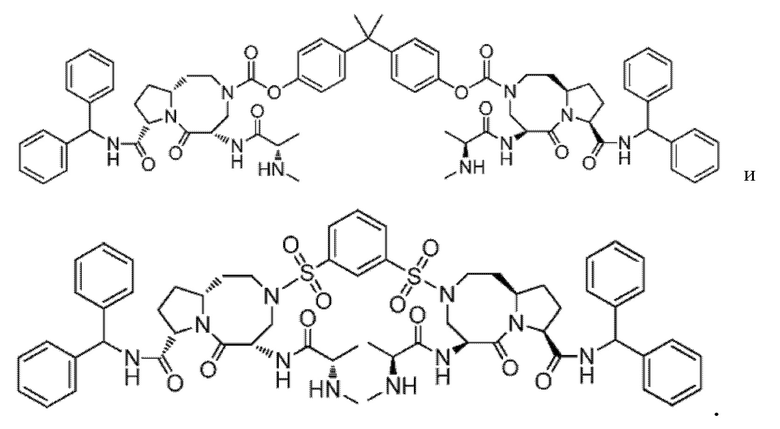 .
.
Предпочтительно, соединение представляет собой
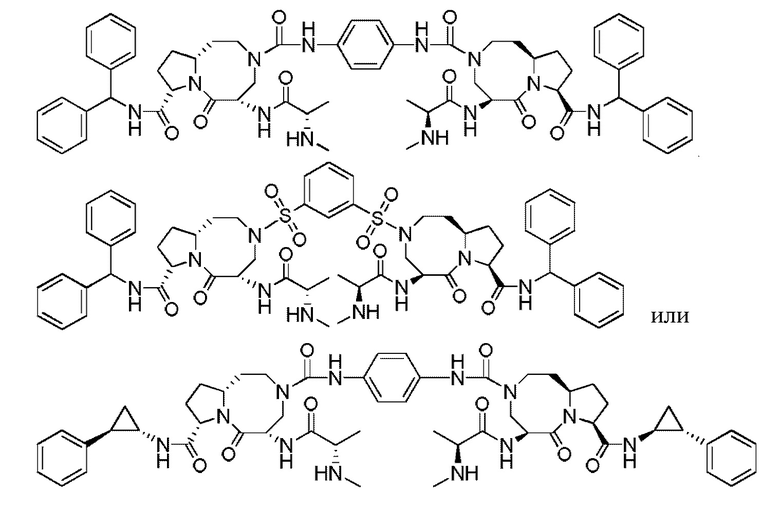 .
.
Предпочтительно, соединение выбрано из
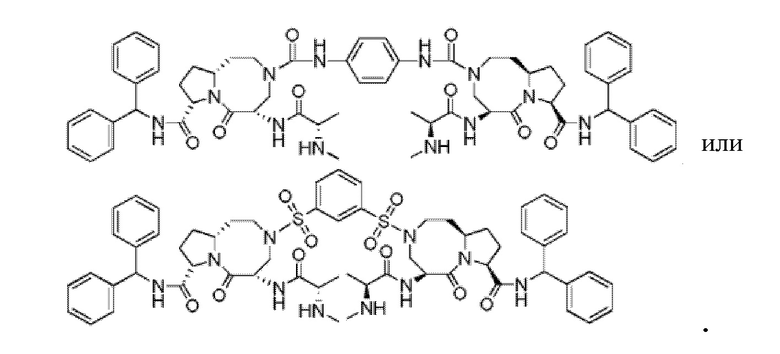
Предпочтительно, соединение представляет собой SF18, который имеет следующую структуру:
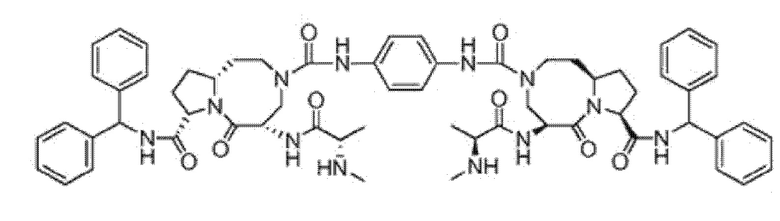 .
.
Предпочтительно, соединение представляет собой Соединение 1, т.е. 1,3-бензол-ди[7-(3S,5S,9aR)-5-((S)-2-метиламино-пропионамидо)-3-дифенилметиламинокарбонил-4-оксо-3a,7-диаза-декагидро-циклопентаноциклооктен)]-сульфонамид, имеющий следующую структуру:
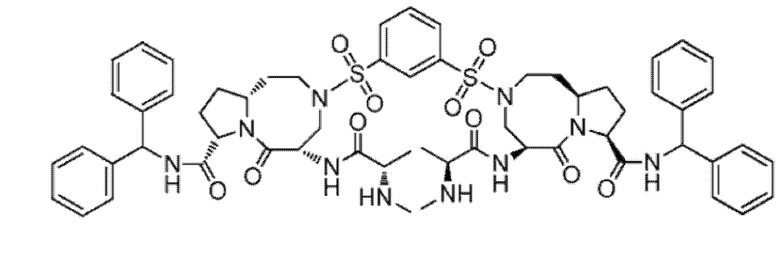 .
.
В соответствии с настоящим изобретением, соединение получают в соответствии со способом получения, раскрытым в PCT/US2013/055384 (WO2014/031487), полное содержание которой включено в настоящую заявку посредством ссылки.
В соответствии с настоящим изобретением, соединение по настоящему изобретению можно использовать в форме мономера или композиции. Также, соединение по настоящему изобретению можно вводить пациенту, нуждающемуся в лечении, интестинальным, парентеральным или местным путем. Интестинальный путь обычно включает пероральное введение, и форма соединения по настоящему изобретению для интестинального пути введения включает пероральные растворы, таблетки, капсулы, гранулы и суспензии. Парентеральный путь обычно включает подкожный, внутримышечный, внутрибрюшинный, внутривенный пути и т.д., и форма соединения по настоящему изобретению для парентерального пути введения включает инъекции и лиофилизированные препараты. Форма соединения по настоящему изобретению для местного применения включает пластыри, пасты, мази и т.д.
Также, заболевание или расстройство, связанное с вирусом гепатита, представляет собой заболевание или расстройство, связанное с поздней стадией вирусной инфекции гепатита; заболевание или расстройство, связанное с вирусом гепатита, представляет собой заболевание или расстройство, связанное с вирусом гепатита А, вирусом гепатита В или вирусом гепатита С; предпочтительно, заболевание или расстройство, связанное с вирусом гепатита, включает, но не ограничивается этим: гепатит A, гепатит B, гепатит C и/или цирроз печени.
Кроме того, соединение лечит и/или предотвращает заболевание или расстройство, связанное с вирусом гепатита, путем модуляции иммунного ответа. Предпочтительно, иммунный ответ вовлечен в специфический Т-клеточный ответе на вирус гепатита (включая, но не ограничиваясь этим, вирус гепатита А, вирус гепатита В и вирус гепатита С, в частности вирус гепатита В). Более предпочтительно, иммунный ответ вовлечен в секрецию IFNг, TNFб, IL-2 в CD4+ T клетках и CD8+ T клетках.
Второй аспект настоящего изобретения относится к использованию бисдиазабицикло-соединения для получения лекарственного средства для лечения и/или профилактики или устранения и/или облегчения заболевания или расстройства, связанного с вирусом гепатита.
Также, соединение представляет собой соединение, определенное выше. Кроме того, лекарственное средство включает известное лекарственное средство для лечения вируса гепатита, особенно HBV, котороа включает, но не ограничивается этим: IFNб-2a, Биринапант, анти-PD1 антитело, пегилированный интерферон б2b, пегилированный интерферон б2a, ламивудин, адефовир, энтекавир и/или тенофовир (в частности, тенофовир дисопроксил фумарат).
Также, заболевание или расстройство, связанное с вирусом гепатита, представляет собой заболевание или расстройство, связанное с поздней стадией вирусной инфекции гепатита; заболевание или расстройство, связанное с вирусом гепатита, представляет собой заболевание или расстройство, связанное с вирусом гепатита А, вирусом гепатита В или вирусом гепатита С; предпочтительно заболевание или расстройство, связанное с вирусом гепатита, включает, но не ограничивается этим: гепатит A, гепатит B, гепатит C и/или цирроз печени.
Также, лекарственное средство лечит и/или предотвращает заболевание или расстройство, связанное с вирусом гепатита, путем модуляции иммунного ответа. Предпочтительно иммунный ответ вовлечен в специфический Т-клеточный ответ на вирус гепатита (включая, но не ограничиваясь этим, вирус гепатита А, вирус гепатита В и вирус гепатита С, в частности вирус гепатита В). Более предпочтительно, иммунный ответ участвует в секреции IFNг, TNFб, IL-2 в CD4+ T клетках и CD8+ T клетках.
Третий аспект настоящего изобретения относится к способу лечения и/или профилактики или устранения и/или облегчения заболевания или расстройства, связанного с вирусом гепатита, при этом способ включает введение терапевтически и/или профилактически эффективного количества соединения пациенту, страдающему от заболевания или расстройства, связанного с вирусом гепатита.
Также, соединение представляет собой соединение, определенное выше. Кроме того, соединение также можно использовать в комбинации с известным лекарственным средством для лечения вируса гепатита, особенно HBV, при этом известное лекарственное средство для лечения вируса гепатита, особенно HBV, включает, но не ограничивается этим: пегилированный интерферон б2b, пегилированный интерферон б2a, ламивудин, адефовир (в частности, адефовир дипивоксил), энтекавир и/или тенофовир (в частности, тенофовир дисопроксил фумарат).
Также, когда соединение используют в комбинации с лекарственным средством, известным для лечения вируса гепатита, особенно HBV, соединение и лекарственное средство, известное для лечения вируса гепатита, особенно HBV, можно вводить вместе, раздельно и последовательно.
Также, заболевание или расстройство, связанное с вирусом гепатита, представляет собой заболевание или расстройство, связанное с поздней стадией вирусной инфекции гепатита; заболевание или расстройство, связанное с вирусом гепатита, представляет собой заболевание или расстройство, связанное с вирусом гепатита А, вирусом гепатита В или вирусом гепатита С; предпочтительно, заболевание или расстройство, связанное с вирусом гепатита, включает, но не ограничивается этим: гепатит A, гепатит B, гепатит C и/или цирроз печени.
Также, соединение лечит и/или предотвращает заболевание или расстройство, связанное с вирусом гепатита, путем модуляции иммунного ответа. Предпочтительно, иммунный ответ вовлечен в специфический Т-клеточный ответ на вирус гепатита (включая, но не ограничиваясь этим, вирус гепатита А, вирус гепатита В и вирус гепатита С, в частности вирус гепатита В). Более предпочтительно, иммунный ответ участвует в секреции IFNг, TNFб, IL-2 в CD4+ T клетках и CD8+ T клетках.
Четвертый аспект настоящего изобретения относится к фармацевтической композиции, включающей бисдиазабицикло-соединение, при этом фармацевтическую композицию используют для лечения и/или профилактики или устранения и/или облегчения заболевания или расстройства, связанного с вирусом гепатита.
Также, бисдиазабицикло-соединение представляет собой соединение, определенное выше. Кроме того, фармацевтическая композиция может дополнительно включать известное лекарственное средство для лечения вируса гепатита, особенно HBV, при этом известное лекарственное средство включает, но не ограничивается этим: интерферон б2b, интерферон б2a, ламивудин, адефовир (в частности, адефовир дипивоксил), энтекавир и/или тенофовир (в частности, тенофовир дисопроксил фумарат).
Также, заболевание или расстройство, связанное с вирусом гепатита, представляет собой заболевание или расстройство, связанное с поздней стадией вирусной инфекции гепатита; заболевание или расстройство, связанное с вирусом гепатита, представляет собой заболевание или расстройство, связанное с вирусом гепатита А, вирусом гепатита В или вирусом гепатита С; предпочтительно, заболевание или расстройство, связанное с вирусом гепатита, включает, но не ограничивается этим: гепатит A, гепатит B, гепатит C и/или цирроз печени.
Также, соединение лечит и/или предотвращает заболевание или расстройство, связанное с вирусом гепатита, путем модуляции иммунного ответа. Предпочтительно, иммунный ответ вовлечен в специфический Т-клеточный ответ на вирус гепатита (включая, но не ограничиваясь этим, вирус гепатита А, вирус гепатита В и вирус гепатита С, в частности вирус гепатита В). Более предпочтительно, иммунный ответ участвует в секреции IFNг, TNFб, IL-2 в CD4+ T клетках и CD8+ T клетках.
Конкретные модели для осуществления настоящего изобретения
Следующие примеры используются для дальнейшего описания настоящего изобретения, но не предназначены для ограничения настоящего изобретения каким-либо образом.
Пример 1. Эффект однократной инъекции соединения 1 на HBV в C57BL/6J мышиной модели, установленной путем инъекции плазмиды pAAV-HBV1.2 в хвостовую вену под высоким давлением
1.1 Экспериментальные методы
Мышиную модель с хронической HBV инфекцией устанавливали с использованием мышей C57BL/6J путем инъекции плазмиды pAAV-HBV1.2 в хвостовую вену под высоким давлением для имитации пациентов с хроническим гепатитом B, которые могли бы спонтанно достигать иммунного контроля. Самцов мышей C57/B6 (возраст 6-8 недель, масса тела 20±2г) отбирали для установления мышиной модели для введения инъекции в хвостовую вену под высоким давлением, в которой хвосты мышей протирали 75% спиртом и затем облучали с использованием физиотерапевтического устройства дальнего инфракрасного диапазона в течение 2-3 минут, чтобы хвостовая вена мышей была набухшей и отчетливо видна. Иглу вставляли параллельно вдоль хвостовой вены до ощущения пустоты или появления возврата крови, указывающих на то, что игла вошла в вену, и затем инъекцию завершали в течение 10 секунд путем осторожного нажатия. Каждой мыши инъецировали 10 мкг плазмиды pAAV/HBV1.2, и количество инъецируемой жидкости (PBS) составляло 10% от массы тела (2 мл/20 г). На 14-й день после инъекции собирали кровь для определения HBsAg, и мышей, у которых моделирование прошло успешно, с HBsAg>500 МЕ/мл отбирали для дальнейших экспериментов (Huang, Wu et al. 2006; Chou, Chien et al. 2015). После того, как моделирование прошло успешно, C57BL/6J мышей разделяли на 4 группы: группу введения инъекции физиологического раствора 0,9% NaCl (Группа 1 на Фиг. 1A и 1B, черные линии), группу введения внутривенной инъекции 10 мг/кг Соединения 1 (Группа 2 на Фиг. 1A и 1B, красные линии), группу введения внутривенной инъекции 20 мг/кг Соединения 1 (Группа 3 на Фиг. 1A и 1B, синие линии). В каждой группе было по 6-8 мышей, введение которым осуществляли один раз в неделю 4 раза подряд и наблюдали в течение 7 недель.
После 20-кратного разведения мышиной сыворотки при помощи PBS титры HBsAg и HBeAg в сыворотке определяли с использованием автоматического детектора хемилюминесценции микрочастиц Abbott i2000SR. Содержащуюся в сыворотке ДНК HBV экстрагировали с использованием набора QIAamp DNA Mini Kit (Qiagen), уровень ДНК HBV в сыворотке определяли количественно при помощи ПЦР-анализа в режиме реального времени (LightCycler 480, Roche) (LightCycler 480, Roche) с использованием набора для ДНК-амплификации SYBR Green Kit (Roche), и продукты HBV плазмиды PSM2 с серией градиентов концентрации использовали в качестве стандартов. HBV праймеры, используемые в этом эксперименте, были синтезированы Invitrogen (Shanghai) Trading Co., Ltd., и последовательности праймеров были следующими: HBV Hope-F (от 5' к 3' TACTAGGAGGCTGTAGGCATA) и HBV Hope-R (от 5' к 3' GGAGACTCTAAGGCTTCCC). Ткани печени мышей подвергали обычной фиксации формалином и заливке в парафин, полученные 4 мкм срезы подвергали термообработке при 65°С в течение 2 часов, дегидратировали с использованием обычных градиентов этанола, пропитывали перекисью водорода при комнатной температуре в течение 30 минут, промывали при помощи PBS 5 минут/раз, всего 3 раза, и блокировали при комнатной температуре в течение 1 часа. Затем добавляли кроличье-античеловеческое HBcAg (B0586, DAKO) и инкубировали во влажной камере при комнатной температуре в течение 1 часа, набор GTvision III для иммуногистохимической детекции анти-кроличьего анти-мышиного общего типа (GK50075, Shanghai Gene Technology Co., Ltd.) использовали для инкубации вторичных антител и развития цвета, и снимки при 200х увеличении получали при помощи обычного оптического микроскопа. Отвешивали 60 мг гомогената ткани печени, добавляли 900 мкл лизата (50 ммоль/л Tris-HCl PH 7,5+1 ммоль/л EDTA), помещали на лед и после обработки всех образцов добавляли 5 мкл NP-10 и лизис осуществляли на льду и затем ДНК HBV в ткани печени экстрагировали фенолом/хлороформом, растворяли путем добавления 15 мкл не содержащей РНКазы воды, наносили на 1% агарозный гель, переносили на мембрану; затем добавляли полноразмерный HBV зонд, меченный дигоксином, выдерживали в течение ночи при 46°C, промывали промывочным буфером DIG один раз в течение 5 минут, добавляли анти-дигоксигенин-Ap Fab фрагмент (11093274910, Roche) и использовали Image Quant LAS 4000mini для экспозиции и детекции.
Graphpad Prism 5.0 использовали для картирования и соответствующего статистического анализа, Н-критерий Краскела-Уоллиса и критерий множественных сравнений Данна использовали для множественных сравнений между группами в один и тот же момент времени, лог-ранговый критерий Мантеля-Кокса использовали для сравнения скорости клиренса HBsAg и ДНК HBV в сыворотке, * означает P <0,05, ** означает p <0,01 и *** означает p <0,001, где P <0,05 означает статистически значимую разницу.
1.2 Экспериментальные результаты
Как показано на Фиг. 1, в сравнении с контрольной группой введения физиологического раствора, группы ведения инъекции соединения 1 показали быстрое снижение HBsAg в сыворотке (Фиг. 1A) и ДНК HBV в сыворотке (Фиг. 1B) после введения и уровни как HbsAg, так и ДНК HBV в сыворотке были ниже предела обнаружения вплоть до 7-й недели, при этом группа, получавшая инъекцию 20 мг/кг соединения 1 показала, что сывороточные HBsAg и ДНК HBV были полностью элиминированы на 5-й неделе, что было быстрее, чем в группе введения дозы 10 мг/кг соединения 1. Результаты иммуногистохимического окрашивания HBcAg в ткани печени показали, что экспрессия HBcAg не наблюдалась в печени мышей групп введения соединения 1 после 7 недель введения, но экспрессия HBcAg в печени некоторых мышей в контрольной группе введения физиологического раствора все еще могла быть обнаружена (Фиг. 1C). Результаты саузерн-блот анализа ДНК HBV в ткани печени через 7 недель после введения показали, что промежуточный уровень репликации HBV не обнаружен в ткани печени группы введения соединения 1 по сравнению с группой введения физиологического раствора (Фиг. 1D).
Вышеуказанные результаты подтвердили, что четыре последовательных инъекции Соединения 1 в дозе 20 мг/кг могли полностью элиминировать HBsAg и ДНК HBV в периферической крови на мышиной модели с хронической HBV-инфекцией и полностью элиминировать промежуточные продукты экспрессии HBcAg и репликации HBV в печени на 5-ой неделе. Эти результаты показали, что Соединение 1 может полностью элиминировать вирусные антигены и нуклеиновокислотные продукты у субъекта с хронической HBV-инфекцией. (*, p <0,05; **, p <0,01).
Пример 2. Эффект соединения 1 в комбинации с тенофовир дисопроксил фумаратом (TDF) на HBV в C57BL/6J мышиной модели, установленной путем инъекции плазмиды pAAV-HBV1.2 в хвостовую вену под высоким давлением
2.1 Экспериментальные методы
Мышиную модель C57BL/6J устанавливали путем введения в хвостовую вену под высоким давлением инъекции плазмиды pAAV-HBV1.2. После того, как моделирование прошло успешно, мышей C57BL/6J (6-8 недель, масса тела 20±2г) разделяли на 4 группы, т.е. группу внутривенной инъекции 0,9% NaCl (Группа 1 на Фиг. 2A и 2B, черные линии), группу внутривенной инъекции 10 мг/кг Соединения 1 (Группа 2 на Фиг. 2A и 2B, красные линии), группу введения TDF 53 мг/кг через желудочный зонд (Группа 3 на Фиг. 2A и 2B, синие линии), группу введения Соединения 1 10 мг/кг в комбинации с TDF 53 мг/кг (Группа 4 на Фиг. 2A и 2B, фиолетовые линии). В каждой группе было по 6-8 мышей, Соединение 1 вводили один раз в неделю 4 раза подряд, TDF вводили через желудочный зонд каждый день в течение 10 дней, и мышей наблюдали в течение 7 недель. Серологические методы определения HBsAg и ДНК HBV были такими же, как описано выше.
2.2 Экспериментальные результаты
Как показано на Фиг. 2, что касается скорости клиренса сывороточного HBsAg (Фиг. 2A), группа введения только соединения 1 и группа введения соединения 1 в комбинации TDF показали статистически значимую разницу скорости клиренса HBsAg из сыворотки по сравнению с контрольной группой, и в группе введения соединения 1 в комбинации с TDF HBsAg мог быстрее выводиться из сыворотки, и эта группа показала статистически значимую разницу по сравнению с группой введения только соединения 1 или группой введения только TDF. Вышеуказанные результаты показали, что Соединение 1 в комбинации с TDF могут действовать синергически для выведения HBsAg из сывороткы. Что касается скорости клиренса ДНК HBV из сыворотки (Фиг. 2B), группа введения соединения 1, группа введения TDF и группа введения соединения 1 в комбинации с TDF показали статистически значимую разницу по сравнению с контрольной группой, и в группе введения соединения 1 в комбинации с TDF ДНК HBV могла быстрее выводиться из сыворотки, чем в группе введения только TDF или в группе введения только соединения 1.
Вышеуказанные результаты показали, что Соединение 1 в комбинации с TDF может ускорять элиминацию ДНК HBV из сыворотки, обеспечивая, таким образом, синергетический эффект против вируса. (*, p <0,05; **, p <0,01; ***, p <0,001).
Пример 3. Эффект соединения 1 на апоптоз клеток печени у мышей, инфицированных HBV
3.1 Экспериментальный метод
Мышиные модели с хронической HBV-инфекцией устанавливали путем введения в хвостовую вену под высоким давлением инъекции плазмиды pAAV-HBV1.2 или инъекции рекомбинантного вируса rAAV8-1.3HBV мышам C57BL/6J (возраст 6-8 недель, масса 20±2 г). После того, как моделирование прошло успешно у мышей C57BL/6J путем инъекции плазмиды pAAV-HBV1.2 в хвостовую вену под высоким давлением, мышам внутривенно вводили соединение 1 в дозе 10 мг/кг и собрали сыворотку и ткань печени мышей через 12, 24 и 48 часов после инъекции. Для определения уровней ALT и AST в сыворотке использовали набор, содержащий глутаминовую-щавелевоуксусную трансаминазу (AST/GOT) (Nanjing Jiancheng, C010-2), и набор, содержащий глютаминовую-пирувиновую трансаминазу (ALT/GPT) (Nanjing Jiancheng, C009-2). Вестерн-блот использовали для детекции экспрессии молекул cIAP в тканях печени, а в-актин использовали в качестве контроля. Внутрипеченочное воспаление и некроз гепатоцитов определяли путем HE окрашивания срезов ткани печени. Мышей C57BL/6J подвергали обычной инъекции вируса rAAV8-1.3HBV (ayw) в хвостовую вену в количестве 5Ч105 v.g./мышь (Yang, Liu et al. 2014) для для установления мышиной модели C57BL/6J с инъекцией вируса rAAV8-HBV1.3; мышей умерщвляли через 12 часов после внутривенной инъекции соединения 1 при 20 мг/кг и апоптоз инфицированных HBV гепатоцитов определяли методом иммунофлуоресценции HBcAg с двойным окрашиванием и методом Tunnel.
3.2 Экспериментальные результаты
Как показано на Фиг. 3, после инъекции соединения 1 сывороточные трансаминазы ALT и AST, которые отражали повреждение клеток печени, показали кратковременное увеличение, то есть их уровень достигал самых высоких значений через 12 часов, затем медленно снижался и возвращался к нормальному уровню примерно через 48 часов (Фиг. 3A). Обнаружение молекул IAP в печени методом вестерн-блота показало, что Соединение 1 имело сильный ингибирующий эффект на cIAP2 в тканях печени, который достигал наибольшего значения через 12 часов; оно также оказывало ингибирующий эффект на cIAP1, но он был значительно слабее, чем на cIAP2; при этом не наблюдали никакого значительного ингибирующего эффекта на XIAP (Фиг. 3B). HE окрашивание ткани печени также показало, что через 12 часов после инъекции вблизи портальных зон в ткани печени появились рассеянные некротические поражения, сопровождаемые инфильтрацией лимфоцитов (Фиг. 3C). Эксперимент с двойным окрашиванием в методе Tunnel и флуоресценцию HBcAg использовали для наблюдения апоптоза HBV-инфицированных клеток печени, и в комбинации с анализом 3D изображения с двойным окрашиванием было обнаружено, что через 12 часов после инъекции соединения 1 может быть индуцирован апоптоз HBcAg-положительных клеток печени (Фиг. 3D).
Вышеуказанные результаты позволяют предположить, что Соединение 1 может специфически индуцировать апоптоз HBV-инфицированных клеток печени и способствовать клиренсу вируса; кроме того, оно только индуцировало временное внутрипеченочное воспаление и не вызывало фульминантный гепатит, уменьшая, таким образом, побочные реакции, которые могут быть вызваны лечением.
Пример 4. Эффект соединения 1 на иммунный ответ на HBV у мышей
4.1 Экспериментальные методы
Мышей C57BL/6J (возраст 6-8 недель, масса тела 20±2г) подвергали инъекции плазмиды pAAV-HBV1.2 в хвостовую вену под высоким давлением для установления мышиной модели с хронической HBV инфекцией. После того, как моделирование прошло успешно, мышей разделяли на две группы: Группу А: группа, получавшая инъекцию физиологического раствора 0,9% NaCl; Группу В: группа, получавшая инъекцию 20 мг/кг соединения 1. В каждой группе было по 5-6 мышей, введение которым осуществляли один раз в неделю четыре раза подряд, и их умерщвляли на 7-й неделе, лимфоциты печени мышей выделяли и использовали подсчет клеток и проточную цитометрию для детекции экспрессии молекул CD4 и CD8 в лимфоцитах печени. Детекцию HBV-специфического Т-клеточного ответа осуществляли с использованием корового монопептида HBV (Core93-100) для стимуляции лимфоцитов, и количество CD4+ и CD8+ T-клеток, которые секретировали IFNг, TNFб и IL-2, определяли методом проточной цитометрии с внутриклеточным окрашиванием цитокинов.
4.2 Экспериментальные результаты
Как показано на Фиг. 4, после элиминации вируса из печени мышей в группе обработки Соединением 1, общее количество лимфоцитов в печени было значительно выше, чем в контрольной группе введения физиологического раствора (Фиг. 4A). Дальнейший анализ показал, что по сравнению с контролем количество инфильтрированных CD4+ T-клеток и CD8+ T-клеток в печени было значительно увеличено (Фиг. 4B). После стимуляции коровым монопептидом HBV (Core93-100) количество CD4+ T-клеток, которые секретировали IFNг, TNFб и IL-2, значительно возросло (Фиг. 4C), и значительно возросло количество CD8+ T-клеток, которые секретировали IFNг, TNFб и IL-2 (Фиг. 4D).
Вышеуказанные результаты показали, что после лечения Соединением 1 и клиренса вируса функция специфического Т-клеточного ответа против HBV в печени значительно усиливалась, что способствовало клиренсу вируса. Кроме того, Соединение 1 может специфически индуцировать апоптоз HBV-инфицированных гепатоцитов путем положительной регуляции HBV-специфических Т-клеточных ответов, обеспечивая таким образом элиминацию вирусных антигенов и других вирусных продуктов.
Пример 5. Анти-HBV эффект введения соединения 1 в комбинации с IFNб2a в C57BL/6J мышиной модели хронической HBV-инфекции
5.1 Экспериментальные методы
Мышиную модель с хронической HBV инфекцией устанавливали с использованием мышей C57BL/6J (6-8 недель, масса тела 20±2г), которых подвергали введению в хвостовую вену под высоким давлением инъекции смеси pAAV-HBV1.2 плазмиды и pKCMvint IFNб-2a плазмиды или контрольной плазмиды pKCMvint (6 мкг/мышь) и экспрессированного IFNб2a. Через один день после моделирования мышей разделяли на 4 группы. Группа А (группа, получавшая инъекцию 0,9% физиологического раствора): pAAV-HBV1.2+pKCMvint+0,9%NaCl; Группа В (группа, получавшая внутривенную инъекцию 10 мг/кг Соединения 1): pAAV-HBV1.2+pKCMvint+Соединение 1 10 мг/кг; Группа С (Группа введения IFNб-2a): pAAV-HBV1.2+pKCMvint IFNб-2a+0,9%NaCl; Группа D (группа введения Соединения 1 в комбинации с IFNб-2a): pAAV-HBV1.2+pKCMvint IFNб-2a+APG 10 мг/кг. В каждой группе было по 5 мышей (кроме Группы D, которая включала 7 мышей), введение осуществляли последовательно 3 раза, то есть в день 1 после моделирования и в дни 7 и 14 после моделирования; кровь собирали один раз в месте края орбиты за один день до введения, и уровни HBsAg/HBeAg в сыворотке определяли с использованием прибора Roche 601.
5.2 Экспериментальные результаты
Как показано на Фиг. 5A и 5B, уровни HBsAg и HBeAg в сыворотке были статистически разными в разных группах лечения на 7, 14 и 21 день после моделирования. Как показано на Фиг. 5A, при сравнении Группы В, Группы С и Группы D с Группой А, первые 3 группы показали статистически значимую разницу содержания HBsAg в сыворотке на 7, 14 и 21 день, то есть Р значение составляло 0,010 на 7ой день, Р значение составляло 0,008 на 14ый день, и Р значение составляло 0,004 на 21ый день, при этом статистическую разницу между группами определяли, когда P значение было менее 0,05, и снижение HBsAg в сыворотке в группе D комбинированного лечения оказалось наиболее значимым. На 21ый день, по сравнению с Группой С, уровни в сыворотке в группе B и группе D значительно снизились, и их P значения составляли 0,008, то есть P значение группы C по сравнению с группой B составляло 0,008, и P значение Группы C по сравнению с группой D составило 0,008 (P значения отдельных сравнений для обоих не показаны на Фиг.). Как показано на Фиг. 5B, при сравнении Группы В, Группы С и Группы D с Группой А, первые 3 группы показали статистически значимую разницу уровня HBeAg в сыворотке на 7, 14 и 21 день, т.е., Р значение составляло 0,004 на 7ой день, Р значение составляло 0,021 на 7ой день, и Р значение составляло 0,001 на 21ый день, при этом статистическую разницу между группами определяли, когда P значение было менее 0,05, и снижение уровня HBeAg в Группе D комбинированного лечения было наиболее значимым. На 21ый день, по сравнению с Группой С и Группой В, уровень в сыворотке в Группе D был значительно снижен, и оба P значения составляли 0,008, т.е., P значение для Группы D по сравнению с Группой В составляло 0,008, и P значение для Группы D по сравнению с Группой С составляло 0,008 (P значения отдельных сравнений для обоих не показаны на Фиг.).
Вышеуказанные результаты показали, что группа введения соединения 1 в комбинации с IFNб2a имела наиболее значимый эффект снижения HBsAg/HBeAg. Следовательно, группа введения соединения 1 в комбинации с IFNб2a имела анти-HBV эффект в мышиной модели хронической HBV-инфекции, установленной у мышей C57BL/6J путем введения в хвостовую вену под высоким давлением инъекции смеси pAAV-HBV1.2 плазмиды и pKCMvint IFNб-2a плазмиды или контрольной pKCMvint плазмиды.
Пример 6. Сравнение анти-HBV эффекта соединения 1 и Биринапанта в C57BL/6J мышиной модели хронической HBV-инфекции, установленной путем инъекции pAAV-HBV1.2 плазмиды в хвостовую вену под высоким давлением
6.1 Экспериментальный метод
Мышей C57BL/6J (возраст 6-8 недель, масса тела 20±2г) подвергали инъекции плазмиды pAAV-HBV1.2 в хвостовую вену под высоким давлением для установления мышиной модели с хронической HBV-инфекцией. После того, как моделирование прошло успешно, мышей разделяли на 3 группы: Группа А: группа, получавшая инъекцию физиологического раствора 0,9% NaCl; Группа В: группа, получавшая внутривенную инъекцию 20 мг/кг Соединения 1, и Группа С: группа, получавшая внутривенную инъекцию 20 мг/кг Биринапанта. В Группе А и Группе В было по 7 мышей, и в Группе С было 6 мышей. Соединение 1 и Биринапант вводили один раз в неделю в течение пяти последовательных недель. Кровь собирали у края орбиты каждую неделю перед введением и уровни HBsAg/HBeAg в супернатанте определяли с использованием прибора Roche 601.
6.2 Экспериментальные результаты
Как можно видеть по изменениям общих уровней HBsAg и HBeAg в плазме, как показано на Фиг. 6A, что касается такого эффекта, как клиренс HBsAg, была статистически значимая разница между группой введения внутривенной инъекции соединения 1 и группой введения физиологического раствора. Как показано на Фиг. 6B, что касается такого эффекта, как клиренс HBeAg, была статистически значимая разница между группой внутривенного введения соединения 1 и группой введения Биринапанта (*, p <0,05).
Как можно видеть по изменениям индивидуальных уровней HBsAg и HBeAg в плазме, как показано на Фиг. 6C, после одной недели лечения лекарственными средствами, уровни HBsAg в сыворотке в группах лечения обоими лекарственными средствами значительно снизились, и уровень HBsAg в сыворотке в группе введения соединения 1 был значительно ниже, чем в группе введения Биринапанта (p=0,035).
После 4 недель введения 86% мышей в группе введения соединения 1 имели уровни HBsAg в сыворотке ниже нижнего предела обнаружения, в то время как соответствующая доля мышей в группе введения Биринапанта составляла 57%, и это значение проиллюстрировано на Фиг. 6A (данные не показаны).
Вышеуказанные результаты показали, что Соединение 1 превосходило Биринапант, что касается такого эффекта, как клиренс HBsAg и HBeAg. Следовательно, при той же дозировке и режиме введения, противовирусный эффект соединения 1 был выше, чем у Биринапанта.
Пример 7. Анти-HBV эффект введения соединения 1 в комбинации с анти-PD1 антителом в C57BL/6J мышиной модели хронической HBV-инфекции, установленный путем инъекции плазмиды pAAV-HBV1.2 в хвостовую вену под высоким давлением
7.1 Экспериментальные методы
Мышей C57BL/6J (возраст 6-8 недель, масса тела 20 ± 2г) подвергали инъекции плазмиды pAAV-HBV1.2 в хвостовую вену под высоким давлением для установления мышиной модели с хронической HBV-инфекцией. После того, как моделирование прошло успешно, мышей разделяли на 4 группы: Группу А: группа, получавшая инъекцию физиологического раствора 0,9% NaCl; Группу В: группа, получавшая внутривенную инъекцию 20 мг/кг Соединения 1; Группу С: группа введения перитонеальной инъекции анти-PD1 антитела 200 мкг/мышь/раз; Группу D: группа введения соединения 1 в комбинации с анти-PD1 антителом. В каждой группе было по 7 мышей. Соединение 1 вводили внутривенно один раз в неделю, а анти-PD1 антитело вводили внутрибрюшинно два раза в неделю. Кровь собирали у края орбиты перед введением соединения 1 каждую неделю и уровни HBsAg/HBeAg в супернатанте определяли с использованием прибора Roche 601.
7.2 Экспериментальные результаты
Как можно видеть по изменениям общих уровней HBsAg и HBeAg в плазме, как показано на Фиг. 7A и 7B, группа введения только соединения 1 и группа введения соединения 1 в комбинации с анти-PD1 антителом могли продемонстрировать значительное снижение уровней HBsAg/HBeAg в сыворотке. Группа введения только анти-PD1 антитела не показала никакого значительного снижения HBsAg/HBeAg эффекта.
Как можно видеть по изменениям индивидуальных уровней HBsAg и HBeAg в плазме, как показано на Фиг. 7C, при сравнении Группы В, Группы С и Группы D с Группой А, 3 группы введения разных лекарственных средств показали статистически значимую разницу уровней HBsAg в сыворотке на 2ой, 3ей и 4ой неделе, т.е., значение Р составляло 0,035 на 2ой неделе, т.е. Р значение составляло 0,005 на 3ей неделе, и Р составляло значение 0,013 на 4ой неделе, при этом статистическую разницу между группами определяли, когда P значение было менее 0,05, и снижение HBsAg в сыворотке в группе D комбинированного лечения оказалась наиболее значимым. По сравнению с Группой С, уровень HBsAg в сыворотке в группе D снижался более существенно на 2ой и 3ей неделе после введения, и P значения составляли 0,015 и 0,037, соответственно (P значения отдельных сравнений для обоих на 2 и 3 неделе не показано на чертежах). Как показано на Фиг. 7D, при сравнении Группы В, Группы С и Группы D с Группой А, 3 группы введения разных лекарственных средств показали статистически значимую разницу уровней HBeAg в сыворотке на 1ой и 2ой неделе, т.е. Р значение составляло 0,029 на 1ой неделе, Р значение составляло 0,009 на 2ой неделе, и статистическую разницу между группами определяли, когда P значение было менее 0,05. По сравнению с Группой С, уровни HBeAg в сыворотке в Группе В и в Группе D снижались более значительно на 1ой и 2ой неделе после введения, P значения на 1ой неделе составляли 0,016 и 0,007, соответственно, и P значения на 2ой неделе составляли 0,007 и 0,002, соответственно (P значения отдельных сравнений для обоих на 1ой и 2ой неделе не показаны на чертежах), но статистически значимой разницы между Группой В и Группой D не было.
Вышеуказанные результаты показали, что Соединение 1 и Соединение 1 в комбинации с анти-PD1 антителом обладали анти-HBV эффектом в C57BL/6J мышиной модели хронической HBV-инфекции, установленной путем инъекции плазмиды pAAV-HBV1.2 в хвостовую вену под высоким давлением.
Пример 8. Анти-HBV эффект соединения 1 и SF18 в C57BL/6J мышиной модели, установленной путем инъекции в хвостовую вену вируса rAAV8-HBV1.3 (ayw)
8.1 Экспериментальные методы
Мышей C57BL/6J подвергали обычной инъекции в хвостовую вену вируса rAAV8-HBV1.3 (ayw), объем инъекции вируса составлял 5Ч105 vg/мышь (Yang, Liu et al. 2014) и таким образом устанавливали мышиную модель C57BL/6J с инъекцией вируса rAAV8-HBV1.3. После того, как моделирование прошло успешно, мышей разделяли на три группы: Группу А: группа, получавшая инъекцию физиологического раствора 0,9% NaCl; Группу В: группа, получавшая внутривенную инъекцию 20 мг/кг Соединения 1, и Группу С: группа, получавшая внутривенную инъекцию SF18 20 мг/кг. В каждой группе было по 3 мыши. Введения осуществляли в течение четырех недель подряд, кровь собирали у края орбиты один раз в неделю и уровни HBsAg/HBeAg в супернатанте определяли при помощи прибора Roche 601.
8.2 Экспериментальные результаты
Как показано на Фиг. 8A и 8B, скорости снижения HBsAg/HBeAg в сыворотке у мышей группы SF18 были значительно быстрее, чем в группе введения соединения 1, но были случаи смерти одной мыши на 2ой и 4ой неделях в группе введения SF18, соответственно.
Вышеуказанные результаты показали, что как Соединение 1, так и SF18 обладали анти-HBV эффектом, и анти-HBV эффект SF18 был сильнее, чем у Соединения 1.
Литература:
Bertoletti, A. and C. Ferrari (2012). "Innate and adaptive immune responses in chronic hepatitis B virus infections: towards restoration of immune control of viral infection." Gut 61 (12): 1754-1764.
Chou, HH, WH Chien, LL Wu, CH Cheng, CH Chung, JH Horng, YH Ni, HT Tseng, D. Wu, X. Lu, HY Wang, PJ Chen and DS Chen (2015). "Age-related immune clearance of hepatitis B virus infection requires the establishment of gut microbiota." Proc Natl Acad Sci USA 112 (7): 2175-2180.
European Association For The Study Of The, L. (2012). "EASL clinical practice guidelines: Management of chronic hepatitis B virus infection." J Hepatol 57 (1): 167-185.
Gish, RG, BD Given, C.-L. Lai, SA Locarnini, JYN Lau, DL Lewis and T. Schluep (2015). "Chronic hepatitis B: Virology, natural history, current management and a glimpse at future opportunities." Antiviral Research 121: 47-58.
Guidotti, LG, D. Inverso, L. Sironi, P. Di Lucia, J. Fioravanti, L. Ganzer, A. Fiocchi, M. Vacca, R. Aiolfi, S. Sammicheli, M. Mainetti, T. Cataudella, A. Raimondi, G. Gonzalez-Aseguinolaza, U. Protzer, ZM Ruggeri, FV Chisari, M. Isogawa, G. Sitia and M. Iannacone (2015). "Immunosurveillance of the liver by intravascular effector CD8 (+) T cells." Cell 161 (3): 486-500.
Guidotti, L. G., R. Rochford, J. Chung, M. Shapiro, R. Purcell and F. V. Chisari (1999). "Viral clearance without destruction of infected cells during acute HBV infection." Science 284 (5415): 825-829.
Hoh, A., M. Heeg, Y. Ni, A. Schuch, B. Binder, N. Hennecke, HE Blum, M. Nassal, U. Protzer, M. Hofmann, S. Urban and R. Thimme (2015) "Hepatitis B Virus-Infected HepG2hNTCP Cells Serve as a Novel Immunological Tool To Analyze the Antiviral Efficacy of CD8+T Cells In Vitro." J Virol 89 (14): 7433-7438.
Huang, L. R., H. L. Wu, P. J. Chen and D. S. Chen (2006). "An immunocompetent mouse model for the tolerance of human chronic hepatitis B virus infection." Proc Natl Acad Sci U S A 103 (47): 17862-17867.
Liaw, YF, N. Leung, JH Kao, T. Piratvisuth, E. Gane, KH Han, R. Guan, GK Lau, S. Locarnini and BGWP ot A.-PA ft S. ot L. Chronic Hepatitis (2008) "Asian-Pacific consensus statement on the management of chronic hepatitis B: a 2008 update." Hepatol Int 2 (3): 263-283.
Liu, J., HI Yang, MH Lee, SN Lu, CL Jen, R. Batrla-Utermann, LY Wang, SL You, CK Hsiao, PJ Chen, CJ Chen and REVEALHS Group (2014). "Spontaneous seroclearance of hepatitis B seromarkers and subsequent risk of hepatocellular carcinoma." Gut 63 (10): 1648-1657.
Lok, A. S. and B. J. McMahon (2009). "Chronic hepatitis B: update 2009." Hepatology 50 (3): 661-662.
Lucifora, J. and C. Trepo (2015). "Hepatitis: After HCV cure, HBV cure?" Nat Rev Gastroenterol Hepatol 12 (7): 376-378.
Lucifora, J., Y. Xia, F. Reisinger, K. Zhang, D. Stadler, X. Cheng, MF Sprinzl, H. Koppensteiner, Z. Makowska, T. Volz, C. Remouchamps, WM Chou, WE Thasler, N. Huser, D. Durantel, TJ Liang, C. Munk, MH Heim, JL Browning, E. Dejardin, M. Dandri, M. Schindler, M. Heikenwalder and U. Protzer (2014). "Specific and nonhepatotoxic degradation of nuclear hepatitis B virus cccDNA." Science 343 (6176): 1221-1228.
Nassal, M. (2015). "HBV cccDNA: viral persistence reservoir and key obstacle for a cure of chronic hepatitis B." Gut 64 (12): 1972-1984.
Sundaram, V. and K. Kowdley (2015). "Management of chronic hepatitis B infection." BMJ 351: h4263.
Wong, D. K., W. K. Seto, J. Fung, P. Ip, F. Y. Huang, C. L. Lai and M. F. Yuen (2013). "Reduction of hepatitis B surface antigen and covalently closed circular DNA by nucleos(t)ide analogues of different potency." Clin Gastroenterol Hepatol 11(8): 1004-1010 e1001.
Yang, D., L. Liu, D. Zhu, H. Peng, L. Su, Y. X. Fu and L. Zhang (2014). "A mouse model for HBV immunotolerance and immunotherapy." Cell Mol Immunol 11(1): 71-78.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБЫ ЛЕЧЕНИЯ ИНФЕКЦИИ ГЕПАТИТА В | 2018 |
|
RU2780021C2 |
| ИНГИБИТОР СБОРКИ КАПСИДНОГО БЕЛКА, СОДЕРЖАЩИЙ N-ГЕТЕРОЦИКЛИЧЕСКОЕ ПЯТИЧЛЕННОЕ КОЛЬЦО, ЕГО ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И ПРИМЕНЕНИЕ | 2019 |
|
RU2802259C2 |
| ПЕГИЛИРОВАННЫЙ КОНЪЮГАТ ВАРИАНТА РЕКОМБИНАНТНОГО КОНСЕНСУСНОГО ИНТЕРФЕРОНА И СПОСОБ ЕГО ПОЛУЧЕНИЯ, И ПРИМЕНЕНИЕ | 2011 |
|
RU2575796C9 |
| СПОСОБ ЛЕЧЕНИЯ ОСТРОГО ВИРУСНОГО ГЕПАТИТА B | 2001 |
|
RU2207135C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ЭФФЕКТИВНОСТИ ИНТЕРФЕРОНОТЕРАПИИ ПРИ ХРОНИЧЕСКОМ ГЕПАТИТЕ B | 2005 |
|
RU2287826C1 |
| СПОСОБ ЛЕЧЕНИЯ ВИРУСНОГО ГЕПАТИТА B У ДЕТЕЙ | 1998 |
|
RU2154478C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ХРОНИЧЕСКОГО ТЕЧЕНИЯ ВИРУСНОГО ГЕПАТИТА В У ДЕТЕЙ С ПИЩЕВОЙ АЛЛЕРГИЕЙ | 2013 |
|
RU2531938C1 |
| Иммуностимулирующие олигонуклеотиды | 2012 |
|
RU2610690C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ЭФФЕКТИВНОСТИ ПРОТИВОВИРУСНОЙ ТЕРАПИИ (ПВТ) ХРОНИЧЕСКОГО ГЕПАТИТА В (ХГВ) | 2011 |
|
RU2454666C1 |
| СРЕДСТВА И СПОСОБЫ ПРЕДСКАЗАНИЯ ОТВЕТА НА ЛЕЧЕНИЕ ГЕПАТИТА B | 2013 |
|
RU2640256C2 |
Изобретение относится к применению указанных ниже соединений или их фармацевтически приемлемых солей для получения фармацевтической композиции для лечения и/или профилактики заболевания или расстройства, связанного с вирусом гепатита, где заболевание или расстройство, связанное с вирусом гепатита, выбрано из гепатита A, гепатита B, гепатита C и цирроза печени. Изобретение относится также к применению фармацевтической композиции для лечения и/или профилактики заболевания или расстройства, связанного с вирусом гепатита, где заболевание или расстройство, связанное с вирусом гепатита, выбрано из гепатита A, гепатита B, гепатита C и цирроза печени, содержащей соединение, выбранное из указанных ниже, и лекарственное средство, известное для лечения HBV, выбранное из тенофовир дисопроксил фумарата, IFNα-2a, Биринапанта и анти-PD1 антитела. 2 н. и 4 з.п. ф-лы, 8 ил., 8 пр.
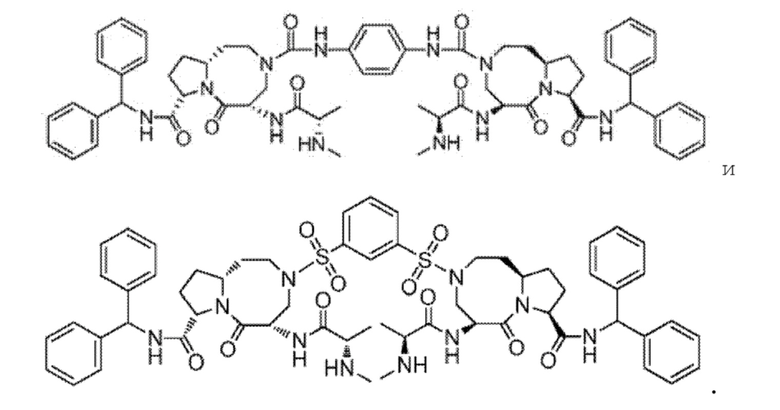
1. Применение соединения или его фармацевтически приемлемой соли для получения фармацевтической композиции для лечения и/или профилактики заболевания или расстройства, связанного с вирусом гепатита, где заболевание или расстройство, связанное с вирусом гепатита, выбрано из гепатита A, гепатита B, гепатита C и цирроза печени, где соединение имеет следующую структуру:
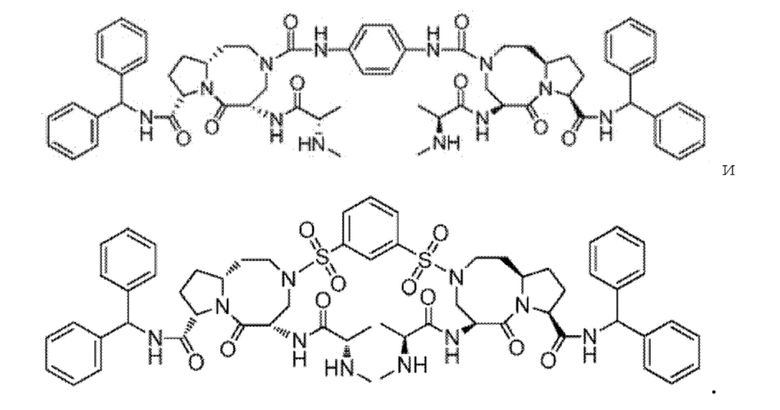
2. Применение по п.1, где соединение имеет следующую структуру:
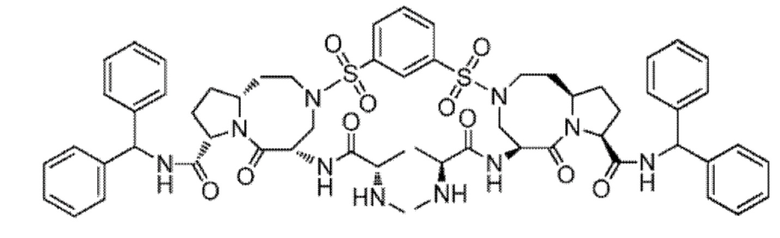 ;
;
или его фармацевтически приемлемая соль.
3. Применение по любому из пп.1 или 2, где соединение лечит и/или предотвращает заболевание или расстройство, связанное с вирусом гепатита, путем модуляции иммунного ответа.
4. Применение по п.1, где фармацевтическая композиция лечит и/или предотвращает заболевание или расстройство, связанное с вирусом гепатита, путем модуляции иммунного ответа.
5. Применение фармацевтической композиции для лечения и/или профилактики заболевания или расстройства, связанного с вирусом гепатита, где заболевание или расстройство, связанное с вирусом гепатита, выбрано из гепатита A, гепатита B, гепатита C и цирроза печени, содержащей соединение, выбранное из следующих структур:

 ,
,
где фармацевтическая композиция дополнительно содержит лекарственное средство, известное для лечения HBV, выбранное из тенофовир дисопроксил фумарата, IFNα-2a, Биринапанта и анти-PD1 антитела.
6. Применение по п.5, где указанное лекарственное средство, известное для лечения HBV, представляет собой тенофовир дисопроксил фумарат.
| Способ защиты переносных электрических установок от опасностей, связанных с заземлением одной из фаз | 1924 |
|
SU2014A1 |
| R.SHENG et al | |||
| КИНЕМАТОГРАФИЧЕСКИЙ АППАРАТ ДЛЯ ПОЛУЧЕНИЯ И ПРОЕКТИРОВАНИЯ СНИМКОВ В НАТУРАЛЬНЫХ ЦВЕТАХ | 1922 |
|
SU1200A1 |
| Колосоуборка | 1923 |
|
SU2009A1 |
| N.LI et al | |||
| Приспособление для перемещения и просушивания склеенных картонных коробок | 1924 |
|
SU1387A1 |
Авторы
Даты
2021-06-16—Публикация
2018-11-20—Подача