Способ относится к медицине, а именно к миниинвазивной хирургии печени, и может быть использован для лечения гемангиом печени.
Гемангиома – доброкачественная опухоль гемопоэтической ткани, которая состоит из каверн синусоидного и венозного типов и составляет 84,6% среди всех доброкачественных опухолей печени. Отсутствие хирургического лечения таких опухолей может быть чревато развитием тяжелых осложнений, таких как: разрыв опухоли и, как следствие, массивное внутреннее кровотечение. Также, в зависимости от расположения, могут наблюдаться портальная гипертензия, механическая желтуха и другие осложнения.
Длительное время открытые резекционные вмешательства являлись золотым стандартом в лечении гемангиом печени, вследствие чего перед хирургами часто вставал вопрос: что весомее – риск разрыва опухоли или риск развития послеоперационных осложнений. Было разработано и применяется несколько различных миниинвазивных методов лечения гемангиом печени (криодеструкция, этанолдеструкция, эндоваскулярная окклюзия питающей артерии и ветви воротной вены, радиочастотная и СВЧ – термоабляция и т.д.).
Наиболее современными из методов минимально инвазивной локальной деструкции являются радиочастотная термоабляция (РЧТА) и микроволновая абляция (СВЧ).
В настоящее время эти методы в лечении больных с гемангиомами печени имеют ограниченное применение, так как в связи с обильной васкуляризацией опухоли и быстрым теплоотведением за счет интенсивного кровотока, а также неоднородного строения опухоль прогревается неравномерно, что значительно снижает эффективность данных методик.
Нужно отметить, что РЧТА, в отличие от СВЧ, позволяет регулировать мощность излучения электрода в зависимости от изменения импеданса тканей, в том числе в автоматическом режиме, позволяя, таким образом, достичь более равномерного и глубокого прогрева, чем при СВЧ. Для гемангиом это особенно актуально, учитывая тот факт, что плотность и электропроводимость, а соответственно, и импеданс тканей гемангиомы, распределение тепла из-за наличия как фиброзного, так и сосудисто-кавернозного компонента меняется неравномерно при удалении от центра опухоли (электрода).
Известно о результатах выполнения эндоваскулярной окклюзии сосудов, питающих гемангиомы (Гемангиомы печени – «ниша» эндоваскулярной хирургии. Дурлештер В.М., Бухтояров А.Ю., Никитин С.П., Мадаминов И.Я., Виттек М.М. Научный вестник здравоохранения Кубани. 2015. № 1 (37). С. 1-8). В указанной работе тактику лечения определяли в соответствии с клинической картиной, по данным УЗИ и КТ с использованием ультразвуковых аппаратов, компьютерных томографов и ангиографа. По наблюдениям авторов после эмболизации приводящих сосудов к опухоли в сроки от одного месяца до одного года роста опухолей не отмечено. По мнению авторов, эндоваскулярные технологии необходимо шире применять в лечении больных с гемангиомой печени, так как они позволяют избежать возможных осложнений основного заболевания и оперативного вмешательства. Оперативное лечение показано больным с гемангиомой печени больших размеров (более 7 см) при подкапсульной локализации и наличии выраженной клинической симптоматики заболевания. Авторы выполняют всем пациентам с гемангиомами печени ангиографию, которая является инвазивным методом диагностики и не совсем целесообразна как изолированный диагностический метод.
Другие авторы (Аксенов И. В., Федорченко А. Н. Тактика лечения гемангиом печени. Хирургия. Журнал им. Н.И. Пирогова. 2010;(6):40-42) применяли эндоваскулярную эмболизацию только при размерах опухоли от 4 до 7 см, что, по нашему мнению, является более рациональным решением, так как эндоваскулярная окклюзия при больших размерах опухоли имеет весьма сомнительную эффективность и ведет к частым рецидивам.
Точные и объективные параметры, по которым можно выбрать тактику ведения пациентов с гемангиомами печени на этапе хирургического лечения при показаниях к эмболизации приносящего сосуда, отсутствуют.
Задачей изобретения является разработка способа выбора тактики ведения пациентов с гемангиомами правой доли печени на этапе хирургического лечения при показаниях к эмболизации приносящего сосуда.
Технический результат – повышение эффективности лечения пациентов с гемангиомами печени, уменьшение частоты проведения открытых резекционных вмешательств, что в свою очередь приводит к уменьшению развития серьёзных послеоперационных осложнений, снижению длительности пребывания в стационаре и летальности у данной категории больных.
Технический результат достигается тем, что в способе выбора тактики ведения пациентов с гемангиомами печени на этапе хирургического лечения при показаниях к эмболизации приносящего сосуда, включающем ультразвуковое исследование с определением размеров гемангиомы, если диаметр гемангиомы правой доли печени от 5 до 10 см, то пациенту проводят УЗИ с контрастированием, определяют время накопления контраста в ткани опухоли в артериальную фазу, время выведения контраста из ткани опухоли в венозную и отсроченные фазы, проводят селективную эндоваскулярную эмболизацию, на следующий день после эмболизации проводят повторно УЗИ с контрастированием и определяют стагнацию артериального кровотока по сравнению с исходным, при стагнации 70% и более хирургический этап лечения считают завершенным, при стагнации от 30% до 70% и выполнении эмболизации спиральными эмболами выполняют радиочастотную термоабляцию, а в остальных случаях выполняют открытое резекционное вмешательство.
Способ выбора тактики ведения пациентов с гемангиомами печени на этапе хирургического лечения при показаниях к эмболизации приносящего сосуда осуществляют следующим образом. При поступлении в стационар пациента с гемангиомой печени пациенту проводят ультразвуковое исследование, которое позволяет верифицировать диагноз и определить размер опухоли. При размерах опухоли менее 3 см хирургическое лечение (методы локальной деструкции) проводят в случае клинических проявлений, таких как дискомфорт в правом подреберье, диспепсические расстройства. При размерах опухоли от 3 до 5 см с тенденцией к росту или клиническими проявлениями выполняют РЧТА. В случае, если диаметр гемангиомы левой доли печени более 5 см или диаметр гемангиомы правой доли печени более 10 см, используют резекционные методы лечения. Если диаметр гемангиомы правой доли печени от 5 до 10 см, то пациенту проводят УЗИ с контрастированием и определяют время накопления в ткани и выведения контраста из ткани опухоли. Планируют селективную эндоваскулярную эмболизацию. Предварительная эндоваскулярная окклюзия питающей опухоль артерии в большинстве случаев приводит к стагнации артериального кровотока в опухоли, как следствие, уменьшению теплоотведения. Выполняют ангиографию и селективную эндоваскулярную эмболизацию питающей опухоль артерии. На следующий день после эмболизации повторно проводят УЗИ с контрастированием и определяют время накопления и выведения контраста из ткани опухоли. Сравнивают полученные значения с предоперационными для определения степени стагнации кровотока в опухоли. Для оценки стагнации рассчитывают отношение разницы между значениями, полученными после эмболизации и до эмболизации к значению до эмболизации в каждую из фаз. Из полученных значений выбирают минимальное. Если стагнация кровотока в опухоли после эмболизации по сравнению с кровотоком в ней до эмболизации составляет 70% и более, то эмболизацию считают успешной, хирургический этап лечения считают завершенным, пациента оставляют под наблюдением и проводят контроль УЗИ. Если определяют, что стагнация кровотока в опухоли находится в диапазоне от 30% до 70% и эмболизация была проведена спиральными эмболами, то проводят последующую РЧТА опухоли. При проведении эмболизации эмбосферами (в связи с риском их расплавления при РЧТА), а также при стагнации кровотока менее 30% выполняют открытое резекционное вмешательство.
Способ позволяет повысить эффективность лечения пациентов с гемангиомами печени, прежде всего за счет применения при недостаточной стагнации кровотока по данным УЗИ исследования с контрастированием выполненного на следующий день после артериоваскулярной эмболизации по сравнению с исходными значениями одного из современных миниинвазивных методов локальной деструкции, снизить, таким образом, необходимость открытых резекционных вмешательств, а соответственно, уменьшить количество послеоперационных осложнений, койко-дней в стационаре, летальность у данной категории больных.
Приводим примеры использования способа.
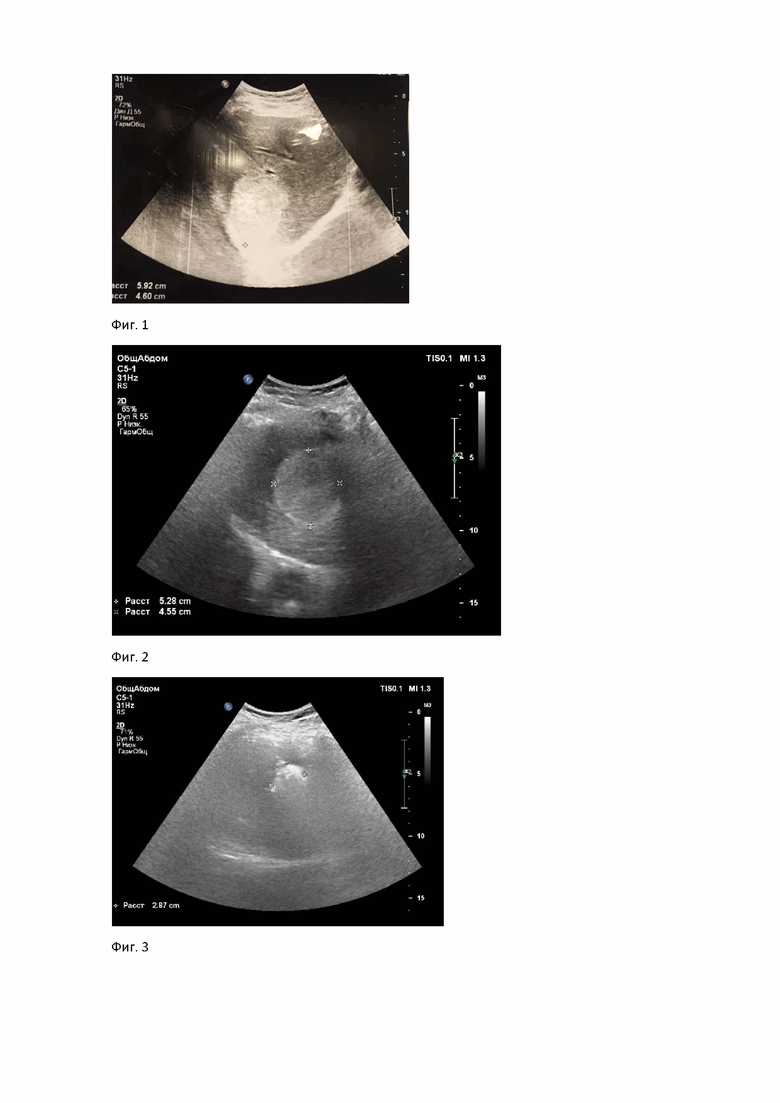
Пример 1. Пациентка С., 39 лет. Поступила 28.03.2018. Основное заболевание: «Гемангиома правой доли печени». Сопутствующее заболевание: анемия легкой степени. Миома матки. АИТ. При поступлении больная предъявляла жалобы на дискомфорт в правом подреберье. УЗИ и МРТ: гемангиома 7 сегмента печени диаметром 5,2 см (фиг. 1).
Целиакография: при контрастировании печеночных артерий визуализировалась патологическая сосудистая сеть, усиленное накопление контрастного вещества в артериальную, венозную и паренхиматозную фазу в 7 сегменте правой доли печени.
Поведено УЗИ исследованием с контрастированием для оценки накопления и выведения контраста опухолью (артериальная фаза – 16,7 сек, венозная фаза – 39,5 сек, отсроченная фаза – 127 сек).
30.03.2017 больной была выполнена селективная эндоваскулярная эмболизация питающей опухоль артерии: была достигнута стагнация артериального кровотока в опухоли 7 сегмента печени. Эмболизация выполнялась спиральными эмболами.
31.03.2017 выполнено контрастное ультразвуковое исследование (артериальная фаза – 28,4 сек, венозная фаза – 68,3 сек, отсроченная фаза – 224,8 сек). Оценена длительность артериальной, венозной и отсроченной фаз после выполнения эндоваскулярной окклюзии.
Таким образом, в артериальную фазу длительность времени накопления и выведения контраста изменилась по сравнению с исходной следующим образом: артериальная фаза – (28,4-16,7)/16,7=0,7 (70%), венозная фаза – (68,3-39,5)/39,5=0,73 (73%), отсроченная фаза – (224,8-127)/127=0,77 (77%). Стагнация составляет 70%, что соответствует критерию «70% и более». Этап эмболизации приносящего сосуда оставлен окончательным методом лечения. Больная была выписана 05.04.2017 под наблюдение хирурга по месту жительства.
Пример 2.
Пациентка Л., 42 года, находилась в хирургическом отделении с 15.03.2018 по 30.03.2018. Основное заболевание: «Гемангиома правой доли печени». Сопутствующее заболевание: эрозивный гастрит. При поступлении больная предъявляла жалобы на боли и тяжесть в правом подреберье. УЗИ и МРТ: гемангиома 7 сегмента печени диаметром 5,3 см (фиг. 2).
Целиакография: при контрастировании печеночных артерий визуализировалась патологическая сосудистая сеть, усиленное накопление контрастного вещества в артериальную, венозную и паренхиматозную фазу в 7 сегменте правой доли.
С помощью контрастного ультразвукового исследования оценивали длительность артериальной, венозной и отсроченной фаз накопления и выведения контраста опухолью до выполнения селективной эндоваскулярной окклюзии питающей опухоль артерии (артериальная фаза – 17,5 сек, венозная фаза – 37,5 сек, отсроченная фаза – 120 сек).
23.03.2018 больной была выполнена селективная эндоваскулярная эмболизация (спиральными эмболами) питающей опухоль артерии: была достигнута стагнация артериального кровотока в опухоли 7 сегмента печени.
24.03.2018 было выполнено повторно контрастное ультразвуковое исследование. Оценена длительность артериальной, венозной и отсроченной фаз после выполнения эндоваскулярной окклюзии (артериальная фаза – 22,92 сек, венозная фаза – 48,75 сек, отсроченная фаза – 159,6 сек).
Таким образом, в артериальную фазу длительность времени накопления и выведения контраста изменилась по сравнению с исходной следующим образом: артериальная фаза – (22,92-17,5)/17,5=0,31 (31%), венозная фаза – (48,75-37,5)/37,5=0,30 (30%), отсроченная фаза – (159,6-120)/120=0,33 (33%). Стагнация кровотока 30%, что соответствует диапазону «от 30% до 70%». Так как эмболизация выполнялась спиральными эмболами, 26.03.18 была выполнена чрескожная мультифокальная радиочастотная термоабляция гемангиомы правой доли печени.
Послеоперационный период протекал без осложнений. УЗИ: контроль 29.03.18: гемангиома правой доли печени диаметром 28 мм с признаками очагового фиброза порядка 80% объема (фиг. 3). Получен хороший результат лечения.
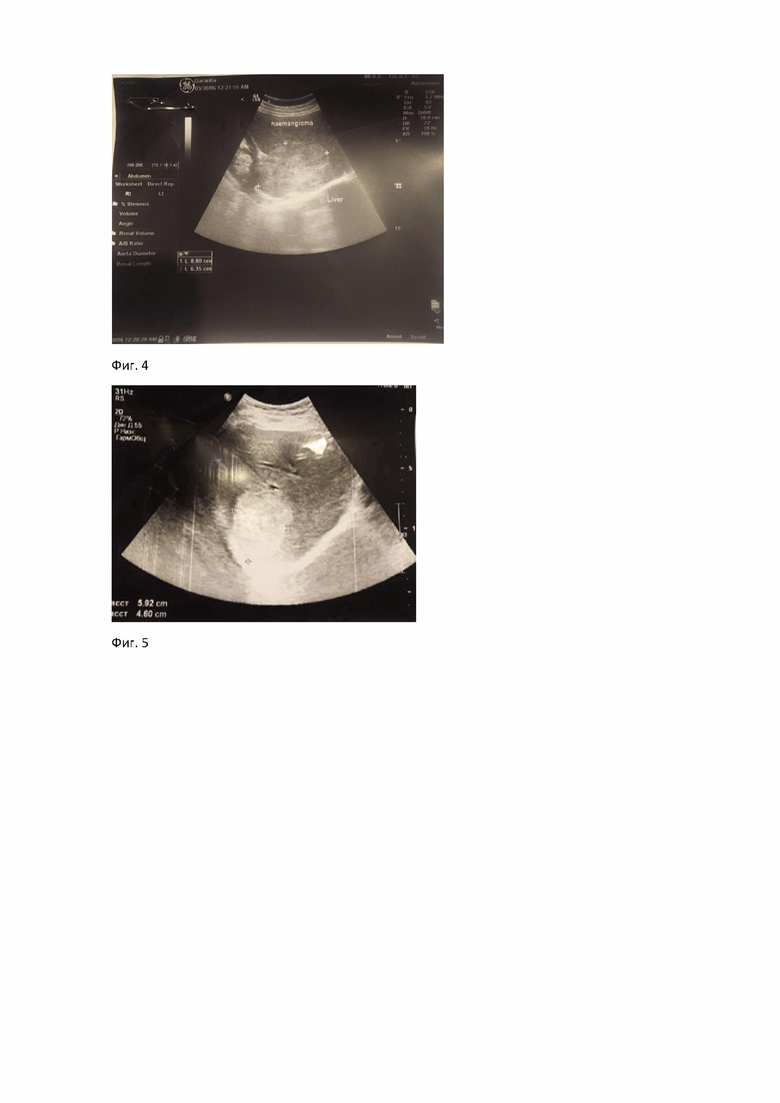
Пример 3. Пациентка П., 56 лет, находилась в хирургическом отделении с 08.06.2017 по 20.06.2017. Основное заболевание: «Гемангиома правой доли печени». Сопутствующее заболевание: эрозивный гастрит. При поступлении больная предъявляла жалобы на боли и тяжесть в правом подреберье. УЗИ и МРТ: гемангиома 7 сегмента печени размером 8,8×6,35 см (фиг. 4).
Целиакография: при контрастировании печеночных артерий визуализировалась патологическая сосудистая сеть, усиленное накопление контрастного вещества в артериальную, венозную и паренхиматозную фазу в 7 сегменте правой доли.
С помощью контрастного ультразвукового исследования оценивали длительность артериальной, венозной и отсроченной фаз накопления и выведения контраста опухолью до выполнения селективной эндоваскулярной окклюзии питающей опухоль артерии (артериальная фаза – 16,9 сек, венозная фаза – 35,8 сек, отсроченная фаза – 112 сек).
13.06.2017 больной была выполнена селективная эндоваскулярная эмболизация (спиральными эмболами) питающей опухоль артерии: была достигнута стагнация артериального кровотока в опухоли 7 сегмента печени.
14.06.2017 было выполнено повторно контрастное ультразвуковое исследование. Оценена длительность артериальной, венозной и отсроченной фаз после выполнения эндоваскулярной окклюзии (артериальная фаза – 10,0 сек, венозная фаза – 21,2 сек, отсроченная фаза – 66,4 сек).
Таким образом, в артериальную фазу длительность времени накопления и выведения контраста изменилась по сравнению с исходной следующим образом: артериальная фаза – (16,9-10)/10,0=0,69 (69%), венозная фаза – (35,8-21,2)/21,2=0,689 (69%), отсроченная фаза – (112-66,4)/66,4=0,687 (69%). Стагнация кровотока 69%, что соответствует диапазону «от 30% до 70%». Так как эмболизация выполнялась спиральными эмболами, а в опухоли сохранялись васкуляризированные участки, 15.06.17 была выполнена чрескожная мультифокальная радиочастотная термоабляция гемангиомы правой доли печени.
Послеоперационный период протекал без осложнений. УЗИ: контроль 19.06.17: очаговый фиброз гемангиомы (фиг. 5). Таким образом, получен хороший результат лечения.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ оценки эффективности рентгенэндоваскулярной эмболизации при гемангиомах печени | 2024 |
|
RU2838459C1 |
| Способ рентгенэндоваскулярной эмболизации висцеральных ветвей через артерии верхних конечностей при помощи катетера Headhunter при различных патологиях желудочно-кишечного тракта | 2016 |
|
RU2652743C1 |
| СПОСОБ ЭНДОВАСКУЛЯРНОГО ЛЕЧЕНИЯ МЕСТНОРАСПРОСТРАНЕННОГО РАКА ПРЯМОЙ КИШКИ, ОСЛОЖНЕННОГО ТОЛСТОКИШЕЧНОЙ НЕПРОХОДИМОСТЬЮ | 2011 |
|
RU2469658C2 |
| Способ бескровной резекции селезенки | 2018 |
|
RU2675355C1 |
| СПОСОБ ОПТИМИЗАЦИИ ПРОЦЕССА ЭМБОЛИЗАЦИИ ВЕТВЕЙ ПЕЧЕНОЧНОЙ АРТЕРИИ ПРИ ГЕМАНГИОМЕ | 2003 |
|
RU2255665C2 |
| СПОСОБ ЭНДОВАСКУЛЯРНОГО ЛЕЧЕНИЯ ХРОНИЧЕСКОГО ГЕМОРРОЯ | 2004 |
|
RU2268754C1 |
| СПОСОБ ЛЕЧЕНИЯ ГЕМАНГИОМ | 1996 |
|
RU2102014C1 |
| СПОСОБ ЛЕЧЕНИЯ ДИФФУЗНОГО ТОКСИЧЕСКОГО ЗОБА | 1992 |
|
RU2028103C1 |
| СПОСОБ ЭНДОВАСКУЛЯРНОЙ ХИМИОЭМБОЛИЗАЦИИ ПЕЧЕНОЧНЫХ АРТЕРИЙ | 2017 |
|
RU2655191C1 |
| Способ радикального лечения больных с метастатическими опухолями печени | 2022 |
|
RU2804994C2 |
Изобретение относится к медицине, а именно к миниинвазивной хирургии печени. Проводят ультразвуковое исследование и определяют размеры гемангиомы. Если диаметр гемангиомы правой доли печени от 5 до 10 см, то пациенту проводят УЗИ с контрастированием и определяют время накопления контраста в ткани опухоли в артериальную фазу, время выведения из ткани опухоли в венозную и отсроченные фазы. Проводят артериоваскулярную эмболизацию. На следующий день после эмболизации проводят повторно УЗИ с контрастированием и определяют стагнацию артериального кровотока по сравнению с исходным. При стагнации 70% и более хирургический этап лечения считают завершенным. При стагнации от 30 до 70% и выполнении эмболизации спиральными эмболами выполняют радиочастотную термоабляцию, а в остальных случаях выполняют открытое резекционное вмешательство. Способ позволяет повысить эффективность лечения пациентов с гемангиомами печени, уменьшить частоту проведения открытых резекционных вмешательств и развитие серьёзных послеоперационных осложнений, снизить длительность пребывания в стационаре и летальность у данной категории больных. Способ позволяет повысить эффективность лечения пациентов с гемангиомами печени, прежде всего за счет применения при недостаточной стагнации кровотока по данным УЗИ исследования с контрастированием, выполненного на следующий день после артериоваскулярной эмболизации по сравнению с исходными значениями одного из современных миниинвазивных методов локальной деструкции, снизить, таким образом, необходимость открытых резекционных вмешательств, а соответственно, уменьшить количество послеоперационных осложнений, койко-дней в стационаре, летальность у данной категории больных. 3 пр., 5 ил.
Способ выбора тактики ведения пациентов с гемангиомами печени на этапе хирургического лечения при показаниях к эмболизации приносящего сосуда, включающий ультразвуковое исследование с определением размеров гемангиомы, отличающийся тем, что если диаметр гемангиомы правой доли печени от 5 до 10 см, то пациенту проводят УЗИ с контрастированием, определяют время накопления контраста в ткани опухоли в артериальную фазу, время выведения из ткани опухоли в венозную и отсроченные фазы, проводят селективную эндоваскулярную эмболизацию, на следующий день после эмболизации проводят повторно УЗИ с контрастированием и определяют стагнацию артериального кровотока по сравнению с исходным, при стагнации 70% и более хирургический этап лечения считают завершенным, при стагнации от 30 до 70% и выполнении эмболизации спиральными эмболами выполняют радиочастотную термоабляцию, а в остальных случаях выполняют открытое резекционное вмешательство.
| БАЗАЕВ А.В | |||
| и др | |||
| Критерии выбора оптимального метода лечения гемангиом печени | |||
| Современные технологии в медицине | |||
| Способ восстановления спиралей из вольфрамовой проволоки для электрических ламп накаливания, наполненных газом | 1924 |
|
SU2020A1 |
| Способ гальванического снятия позолоты с серебряных изделий без заметного изменения их формы | 1923 |
|
SU12A1 |
| Кипятильник для воды | 1921 |
|
SU5A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ВАСКУЛЯРИЗАЦИИ ОЧАГОВЫХ ПОРАЖЕНИЙ ПЕЧЕНИ | 1999 |
|
RU2156112C1 |
| СПОСОБ ОПТИМИЗАЦИИ ПРОЦЕССА ЭМБОЛИЗАЦИИ ВЕТВЕЙ ПЕЧЕНОЧНОЙ АРТЕРИИ ПРИ ГЕМАНГИОМЕ | 2003 |
|
RU2255665C2 |
| UA 60065 А, 15.09.2003 | |||
| ХАЦКО В.В | |||
| и др | |||
| Диагностика и лечение гемангиом печени (Научный обзор) | |||
| Украинский журнал хирургии | |||
| Способ защиты переносных электрических установок от опасностей, связанных с заземлением одной из фаз | 1924 |
|
SU2014A1 |
| Способ получения продукта конденсации бетанафтола с формальдегидом | 1923 |
|
SU131A1 |
Авторы
Даты
2021-07-14—Публикация
2020-12-29—Подача