Область техники, к которой относится изобретение
Настоящее изобретение в целом относится к системам и способам, подходящим для производства высокоэффективного белка. В настоящем изобретении представлена система, содержащая две отдельные молекулы РНК, которые функционально связаны: одна молекула РНК, репликазная конструкция, содержит конструкцию РНК для экспрессии альфавирусной репликазы, а вторая молекула РНК, транс-репликон, содержит последовательность РНК, которая может реплицироваться репликазой in trans. Транс-репликон может содержать представляющий интерес ген, например, ген, кодирующий вакцину, для экспрессии. Конструкция РНК для экспрессии альфавирусной репликазы содержит 5’-кэп. Было обнаружено, что 5’-кэп играет важнейшую роль в высокоэффективной экспрессии представляющего интерес гена in trans. Настоящее изобретение не требует размножения вирусных частиц и применимо для эффективного и безопасного получения представляющего интерес белка, например, терапевтического белка или антигенного белка, такого как вакцина, в целевом организме, например, у животного.
Предшествующий уровень техники изобретения
Внедрение чужой генетической информации, кодирующей один или несколько полипептидов для профилактических и терапевтических целей, представляло собой цель биомедицинских исследований на протяжении многих лет. Подходы предшествующего уровня техники характеризуются доставкой молекулы нуклеиновой кислоты в целевую клетку или организм, но различаются по типу молекулы нуклеиновой кислоты и/или системы доставки: под влиянием опасений за безопасность, связанных с применением молекул дезоксирибонуклеиновой кислоты (ДНК), молекулы рибонуклеиновой кислоты (РНК) в последние годы получили повышенное внимание. Были предложены различные подходы, включающие в себя введение одноцепочечной или двухцепочечной РНК в форме голой РНК или в связанной в комплекс или упакованной форме, например, в невирусных или вирусных средствах доставки. В вирусах и в вирусных средствах доставки генетическая информация, как правило, инкапсулируется белками и/или липидами (вирусная частица). Например, в качестве средства доставки для обработки растений (публикация международной заявки WO 2000/053780 A2) или для вакцинации млекопитающих были предложены сконструированные частицы РНК-вирусов, полученные из РНК-вирусов (Tubulekas et al., 1997, Gene, vol. 190, pp. 191-195).
В общем, РНК-вирусы представляют собой разнообразную группу инфекционных частиц с геномом РНК. РНК-вирусы могут быть сгруппированы в вирусы с одноцепочечной РНК (оцРНК) и двухцепочечной РНК (дцРНК), а вирусы с оцРНК могут быть дополнительно разделены на вирусы с положительной нитью ((+)-нить) и/или отрицательной нитью [(-)-нить]. РНК-вирусы с положительной нитью являются, на первый взгляд, привлекательными в качестве системы доставки в биомедицине, потому что их РНК может служить непосредственно в качестве матрицы для трансляции в клетке-хозяине.
Альфавирусы являются типичными представителями вирусов с положительной нитью РНК. Альфавирусы реплицируются в цитоплазме инфицированных клеток (для обзора жизненного цикла альфавируса смотрите публикацию José et al., Future Microbiol., 2009, vol. 4, pp. 837–856). Общая длина генома многих альфавирусов, как правило, составляет от 11000 до 12000 нуклеотидов, и геном, как правило, содержит 5’-кэп и 3’-поли(А)-хвост. Геном альфавирусов кодирует неструктурные белки (вовлеченные в транскрипцию, модификацию и репликацию вирусной РНК и в модификацию белка) и структурные белки (образующие вирусную частицу). В геноме, как правило, имеются две открытые рамки считывания (ORF). Четыре неструктурных белка (nsP1-nsP4), как правило, кодируются вместе первой ORF, начинающейся возле 5′-конца генома, тогда как структурные белки альфавирусов вместе кодируются второй ORF, которая находится ниже по ходу транскрипции от первой ORF и продолжается вблизи 3′-конца генома. Как правило, первая ORF больше, чем вторая ORF, причем отношение составляет приблизительно 2:1.
В инфицированных альфавирусом клетках из геномной РНК транслируются только неструктурные белки, тогда как структурные белки представляют собой транслируемые из субгеномного транскрипта, который представляет собой молекулу РНК, характеризующуюся сходством с эукариотической матричной РНК (мРНК, Gould et al., 2010, Antiviral Res., vol. 87, pp. 111–124). После инфицирования, то есть на ранних стадиях жизненного цикла вируса, (+)-нитевая геномная РНК непосредственно действует в качестве матричной РНК для трансляции неструктурного полипротеина (nsP1234). В некоторых альфавирусах существует опал стоп-кодон между кодирующими последовательностями nsP3 и nsP4: полипротеин P123, содержащий nsP1, nsP2 и nsP3, производится тогда, когда трансляция заканчивается в опал стоп-кодоне, а полипротеин P1234, содержащий дополнительно nsP4, производится при считывания через этот опал-кодон (Strauss & Strauss, Microbiol. Rev., 1994, vol. 58, pp. 491-562; Rupp et al., 2015, J. Gen. Virology, vol. 96, pp. 2483–2500). nsP1234 аутопротеолитически расщепляется на фрагменты nsP123 и nsP4. Полипептиды nsP123 и nsP4 соединяются с образованием репликазного комплекса с (-)-нитью, который транскрибирует (-)-нитевую РНК, используя (+)-нитевую геномную РНК в качестве матрицы. Как правило, на более поздних стадиях фрагмент nsP123 полностью расщепляется на отдельные белки nsP1, nsP2, nsP3 и nsP4 (Shirako & Strauss, 1994, J. Virol. Vol. 68, pp. 1874-1885); эти белки собираются с образованием (+)-нитевого репликазного комплекса, который синтезирует новые (+)-нитевые геномы с использованием (-)-нитевого комплемента геномной РНК в качестве матрицы (Kim et al., 2004, Virology, vol. 323, pp. 153-163, Vasiljeva et al., 2003, J. Biol. Chem. Vol. 278, pp. 41636-41645).
Альфавирусные структурные белки (белок C сердцевины нуклеокапсида, белок P62 оболочки и белок E1 оболочки, все составляющие вирусной частицы), как правило, кодируются одной единственной открытой рамкой считывания под контролем субгеномного промотора (Strauss & Strauss, Microbiol. Rev., 1994, vol. 58, p. 491-562). Субгеномный промотор распознается альфавирусными неструктурными белками, действующими in cis. В частности, альфавирусная репликаза синтезирует (+)-нитевый субгеномный транскрипт с использованием (-)-нитевого комплемента геномной РНК в качестве матрицы. (+)-нитевый субгеномный транскрипт кодирует структурные белки альфавируса (Kim et al., 2004, Virology, vol. 323, pp. 153-163, Vasiljeva et al., 2003, J. Biol. Chem. Vol. 278, pp. 41636-41645). Субгеномный транскрипт РНК служит в качестве матрицы для трансляции открытой рамки считывания, кодирующей структурные белки, в виде одного полипротеина, а полипротеин расщепляется с образованием структурных белков. На поздней стадии альфавирусной инфекции в клетке-хозяине сигнал упаковки, который находится в кодирующей последовательности nsP2, обеспечивает селективную упаковку геномной РНК в почкующиеся вирионы, упакованные посредством структурных белков (White et al., 1998, J. Virol., vol. 72, pp. 4320-4326).
В инфицированных клетках субгеномная РНК, а также новая геномная РНК обеспечивается 5’-кэпом посредством nsP1 (Pettersson et al. 1980, Eur. J. Biochem. 105, 435-443; Rozanov et al., 1992, J. Gen. Virology, vol. 73, pp. 2129-2134) и обеспечивается полиаденилатным (поли(А)) хвостом посредством nsP4 (Rubach et al., Virology, 2009, vol. 384, pp. 201-208). Таким образом, как субгеномная РНК, так и геномная РНК являются похожими на матричную РНК (мРНК).
Геном альфавируса содержит четыре консервативных элемента последовательностей (CSE), которые, как понимают, важны для репликации вирусной РНК в клетке-хозяине (Strauss & Strauss, Microbiol. Rev., 1994, vol. 58, pp. 491-562). Считается, что CSE 1, обнаруженный на 5’-конце вирусного генома или около него, функционирует в качестве промотора для синтеза (+)-нитей из матриц (-)-нитей. Считается, что CSE 2, расположенный ниже по ходу транскрипции от CSE1, но все еще близко к 5’-концу генома в кодирующей последовательности для nsP1, выступает в качестве промотора для инициирования синтеза (-)-нитей из матрицы геномной РНК (следует обратить внимание, что транскрипт субгеномной РНК, который не содержит CSE 2, не функционирует в качестве матрицы для синтеза (-)-цепей). CSE 3 находится в области соединения между кодирующей последовательностью для неструктурных и структурных белков и действует как основной промотор для эффективной транскрипции субгеномного транскрипта. Наконец, подразумевается, что CSE 4, который расположен только выше против хода транскрипции от поли(А)-последовательности в 3′-нетранслируемой области генома альфавируса, представляет собой основной промотор для инициирования синтеза (-)-нитей (José et al., Future Microbiol., 2009, vol. 4, pp. 837–856). Подразумевается, что CSE 4 и поли(A)-хвост альфавируса функционируют совместно для эффективного синтеза (-)-нитей (Hardy & Rice, J. Virol., 2005, vol. 79, pp. 4630-4639). В дополнение к альфавирусным белкам, также факторы клетки-хозяина, предположительно белки, могут связываться с консервативными элементами последовательности (Strauss & Strauss, Microbiol. Rev., 1994, vol. 58, pp. 491-562).
Некоторые особенности генома типичного альфавируса, вируса леса Семлики (SFV), проиллюстрированы на фиг. 1А.
Хозяева альфавирусов включают в себя широкий круг животных, включая в себя насекомых, рыб и млекопитающих, таких как домашние животные и люди; поэтому полученные из альфавирусов векторы были рассмотрены в качестве потенциального вектора для доставки чужой генетической информации в широкий круг целевых организмов. Некоторые подходы предшествующего уровня техники к применению альфавируса в качестве векторов для доставки генетической информации рассматриваются публикации Strauss & Strauss, Microbiol. Rev., 1994, vol. 58, pp. 491-562 и совсем недавно - в публикации Ljungberg and Liljeström, 2015, Expert Rev. Vaccines, vol. 14, pp. 177-94. Уже Strauss & Strauss считали векторы на основе альфавируса особенно выгодными для доставки генетической информации; эти авторы описывают векторы, которые кодируют представляющий интерес белок ниже по ходу транскрипции от субгеномного промотора. Соответствующая молекула нуклеиновой кислоты (репликон) схематически изображена на фиг. 1B. Предполагается, что когда репликон, схематически изображенный на фиг. 1B, вводится в клетку-хозяина, синтезируется закодированная репликаза, образуя комплексы репликации, связанные с инвагинациями мембран, что может способствовать цис-репликации. Для вируса краснухи была продемонстрирована цис-предпочтительная репликация (Liang and Gillam, 2001, Virology 282, 307-319), представителя семейства тогавирусов с аналогичной организацией генома как у альфавирусов.
Однако репликация не происходит исключительно по цис-схеме, была описана транс-репликация, основанная на альфавирусных элементах на двух отдельных молекулах нуклеиновой кислоты. Полученные из альфавируса системы транс-репликации содержат две молекулы нуклеиновой кислоты, причем одна молекула нуклеиновой кислоты кодирует вирусную репликазу, а другая молекула нуклеиновой кислоты способна реплицироваться указанной репликазой in trans (системе транс-репликации). Такие системы транс-репликации требуют для транс-репликации наличия обеих молекул нуклеиновой кислоты в одной клетке-хозяине.
Вирусные РНК-векторы часто считались невыгодными из-за их способности размножаться у подвергнутого лечению человека путем образования для размножения компетентных вирусных частиц. Это может быть связано с рисками для здоровья не только для подвергающегося лечению человека, но и для популяции в целом: например, некоторые альфавирусы являются патогенными для человека (например, вирус Чикунгунья, вирус венесуэльского лошадиного энцефалита (VEEV), роль альфавирусов в заболевании человека и животных рассмотрена в публикации Strauss & Strauss, Microbiol. Rev., 1994, vol. 58, pp. 491-562).
В альтернативных подходах было предложено вводить невирусную систему транс-репликации в клетки-хозяева (Sanz et al., Cellular Microbiol., 2015, vol. 17, pp. 520-541; Spuul et al., J. Virol., 2011, vol. 85, pp. 4739-4751). Системы транс-репликации в соответствии с этими ссылками основаны на введении векторов ДНК в клетки-хозяева, причем векторы содержат промотор бактериофага T7 и причем клетки-хозяева представляют собой специализированные сконструированные клетки, экспрессирующие полимеразу Т7 (Buchholz et al., J. Virol., 1999, vol. 73, pp. 251-259). Конструкции ДНК, используемые Spuul с соавт., кодируют элемент участка внутреннего посадки рибосомы (IRES) ниже по ходу транскрипции от промотора T7; согласно этой статье, элемент IRES участвует в усилении экспрессии предположительно некэпированных транскриптов РНК, синтезированных полимеразой Т7 в клетках. Sanz с соавт. дополнительно описывают прямое использование репликазной РНК-конструкции (кодирующей nsP1-4) ниже по ходу транскрипции от IRES; конструкцию РНК получают in vitro в отсутствие кэпирующей структуры m7G(5’)ppp(5’)G. Таким образом, эти два исследования показывают, что системы транс-репликации являются функциональными либо в виде непрямых ДНК-векторов с бактериофаговым промотором для синтеза РНК в сконструированных клетках-хозяевах, которые экспрессируют бактериофаговую РНК-полимеразу, либо в форме прямых РНК-систем, которые содержат IRES для управления трансляцией репликазы.
Принимая во внимание соображения безопасности, медицинское и ветеринарное сообщество неохотно вводит в организм человека или животных ДНК-векторы или самовоспроизводящиеся вирусные нуклеиновые кислоты. В дополнение к этому, многие подходы предшествующего уровня техники к доставке нуклеиновых кислот, особенно РНК, связаны с неудовлетворительными уровнями трансгенной экспрессии.
Таким образом, существует потребность в безопасных и эффективных способах доставки нуклеиновой кислоты, кодирующей белок с терапевтической ценностью, такой как вакцина. Как описано в настоящем документе, аспекты и варианты осуществления настоящего изобретения направлены на эту потребность.
Краткое раскрытие настоящего изобретения
Иммунотерапевтические стратегии представляют собой перспективные варианты профилактики и лечения, например, инфекционных заболеваний и онкологических заболеваний. Идентификация растущего числа связанных с патогенами и опухолями антигенов привела к широкому набору подходящих мишеней для иммунотерапии. Настоящее изобретение, как правило, охватывает средства и способы, подходящие для эффективного иммунотерапевтического лечения для профилактики и лечения заболеваний.
Согласно первому аспекту в настоящем изобретении предусмотрена система, содержащая:
конструкцию РНК для экспрессии альфавирусной репликазы,
РНК-репликон, который может быть реплицирован репликазой в ходе трансрепликации,
причем конструкция РНК для экспрессии альфавирусной репликазы содержит 5’-кэп для управления трансляцией репликазы.
Согласно одному варианту осуществления 5’-кэп представляет собой природный 5’-кэп или аналог 5’-кэп.
Согласно одному варианту осуществления конструкция РНК для экспрессии альфавирусной репликазы не содержит элемент участка внутренней посадки рибосомы (IRES). Таким образом, трансляция репликазы не управляется элементом IRES.
Согласно одному варианту осуществления конструкция РНК для экспрессии альфавирусной репликазы содержит открытую рамку считывания (ORF), кодирующую репликазу. Кроме того, может присутствовать 5’-UTR и/или 3’-UTR. Согласно предпочтительному варианту осуществления конструкция РНК для экспрессии альфавирусной репликазы содержит
(1) 5' UTR,
(2) открытую рамку считывания, кодирующую репликазу, и
(3) 3' UTR.
Предпочтительно 5' UTR и/или 3' UTR являются гетерологичными или ненативными для альфавируса, из которого получена репликаза.
Предпочтительно открытая рамка считывания, кодирующая альфавирусную репликазу, содержит кодирующую область(-и) для неструктурных белков, необходимых для репликации РНК.
Согласно одному варианту осуществления конструкция РНК для экспрессии альфавирусной репликазы содержит 3' поли(А)-последовательность.
Согласно одному варианту осуществления конструкция РНК для экспрессии альфавирусной репликазы не может быть реплицирована репликазой.
Согласно одному варианту осуществления репликон РНК содержит:
(1) 5' репликационную последовательность распознавания альфавируса и
(2) 3' репликационную последовательность распознавания альфавируса.
Согласно одному варианту осуществления 5' репликационная последовательность распознавания альфавируса и 3' репликационная последовательность распознавания альфавируса способны направлять репликацию РНК-репликона в присутствии репликазы. Таким образом, когда конструкция РНК для экспрессии альфавирусной репликазы и РНК-репликон присутствуют вместе, эти репликационные последовательности распознавания направляют репликацию РНК.
Согласно одному варианту осуществления 5' репликационная последовательность распознавания альфавируса и 3' репликационная последовательность распознавания альфавируса являются нативными для альфавируса, из которого получена репликаза.
Согласно одному варианту осуществления РНК-репликон содержит гетерологичную нуклеиновую кислоту.
Согласно одному варианту осуществления РНК-репликон содержит открытую рамку считывания, кодирующую представляющий интерес белок.
Предпочтительно открытая рамка считывания, кодирующая представляющий интерес белок, является ненативной по отношению к альфавирусу, из которого получена репликаза. Предпочтительно открытая рамка считывания, кодирующая представляющий интерес белок, не кодирует структурные белки альфавируса.
Согласно одному варианту осуществления РНК-репликон содержит субгеномный промотор.
Предпочтительно ген, кодирующий представляющий интерес белок (то есть представляющий интерес ген), находится под контролем субгеномного промотора. Это допускает возможность того, что экспрессия открытой рамки считывания, кодирующей представляющей интерес белок, находится под контролем субгеномного промотора.
Предпочтительно субгеномный промотор является нативным для альфавируса, из которого получена репликаза.
Предпочтительно субгеномный промотор представляет собой промотор структурного белка альфавируса. Это означает, что субгеномный промотор представляет собой промотор, который является нативным для альфавируса и который контролирует транскрипцию гена одного или нескольких структурных белков в указанном альфавирусе.
Согласно одному варианту осуществления РНК-репликон содержит 3' поли(А)-последовательность.
Согласно одному альтернативному или дополнительному варианту осуществления РНК-репликон содержит 5’-кэп.
Согласно одному варианту осуществления конструкция РНК для экспрессии альфавирусной репликазы и/или РНК-репликон не содержит открытую рамку считывания, кодирующую интактный структурный белок альфавируса.
Согласно одному варианту осуществления альфавирус представляет собой вирус леса Семлики.
Согласно второму аспекту в настоящем изобретении предусмотрена конструкция РНК для экспрессии альфавирусной репликазы, содержащей 5’-кэп для управления трансляцией репликазы.
Согласно третьему аспекту в настоящем изобретении предусмотрена ДНК, содержащая последовательность нуклеиновой кислоты, кодирующая конструкцию РНК для экспрессии альфавирусной репликазы в соответствии с первым аспектом настоящего изобретения, РНК-репликон в соответствии с первым аспектом настоящего изобретения или и то, и другое. Предпочтительно ДНК кодирует систему в соответствии с первым аспектом настоящего изобретения.
Согласно четвертому аспекту в настоящем изобретении предусмотрен способ получения белка в клетке, предусматривающий следующие стадии:
(а) получение конструкции РНК для экспрессии альфавирусной репликазы,
(b) получение РНК-репликона, который может быть реплицирован репликазой в ходе трансрепликации и содержит открытую рамку считывания, кодирующую белок, и
(c) инокуляция смеси конструкции РНК и РНК-репликона в клетку для экспрессии альфавирусной репликазы,
причем конструкция РНК для экспрессии альфавирусной репликазы содержит 5’-кэп для управления трансляцией репликазы.
Согласно различным вариантам осуществления способа конструкция РНК для экспрессии альфавирусной репликазы и/или РНК-репликон являются такими, как определено выше для системы по настоящему изобретению.
Согласно пятому аспекту в настоящем изобретении предусмотрена клетка, содержащая систему по первому аспекту. Согласно одному варианту осуществления клетку подвергают инокуляции в соответствии со способом согласно четвертому аспекту. Согласно одному варианту осуществления клетка может быть получена способом четвертого аспекта настоящего изобретения. Согласно одному варианту осуществления клетка представляет собой часть организма.
Согласно шестому аспекту в настоящем изобретении предусмотрен способ получения белка у субъекта, предусматривающий следующие стадии:
(а) получение конструкции РНК для экспрессии альфавирусной репликазы,
(b) получение РНК-репликона, который может быть реплицирован репликазой в хоте трансрепликации и содержит открытую рамку считывания, кодирующую белок, и
(c) введение конструкции РНК для экспрессии альфавирусной репликазы и РНК-репликона субъекту,
причем конструкция РНК для экспрессии альфавирусной репликазы содержит 5’-кэп для трансляции репликазы.
Согласно различным вариантам осуществления способа конструкция РНК для экспрессии альфавирусной репликазы и/или РНК-репликон являются такими, как определено выше для системы по настоящему изобретению.
Краткое описание графических материалов
Фиг. 1: Организация генома альфавируса и сконструированные конструкции нуклеиновых кислот, содержащие элементы, полученные из генома альфавируса:
Символы и аббревиатуры: An: поли(A)-хвост; C: кэп; SGP: субгеномный промотор (включая в себя CSE3); SFV: вирус леса Семлики; CSE: консервативный элемент последовательности.
Фиг. 1A: Геном альфавирусов представляет собой положительно-полярную одноцепочечную РНК (оцРНК(+)), которая кодирует две открытые рамки считывания (ORF) для больших полипротеинов. ORF на 5’-конце генома кодирует неструктурные белки от nsP1 до nsP4 (nsP1-4), которые транслируются и процессируют в РНК-зависимую РНК-полимеразу (репликазу); ORF на 3’-конце кодирует структурные белки - капсид и гликопротеины. ORF на 3’-конце находится под транскрипционным контролем субгеномного промотора (SGP). Геном альфавируса можно назвать системой цис-репликации.
Фиг. 1B: цис-репликон: посредством генной инженерии структурные белки ниже по ходу транскрипции от субгеномного промотора (SGP) могут быть заменены представляющим интерес геном. Соответствующая конструкция, которая может быть реплицирована альфавирусной репликазой, называется цис-репликоном. Цис-репликон отличается от транс-репликона по настоящему изобретению (смотрите подробное описание).
Фиг. 1С: схематическое представление аспектов системы транс-репликации по настоящему изобретению. В системе транс-репликации РНК, кодирующая альфавирусную репликазу (репликазную конструкцию), и РНК-репликон («трансрепликон»), представляет собой две отдельные молекулы РНК. РНК-репликон предпочтительно кодирует представляющий интерес ген. Предпочтительно, репликазная конструкция похожа на клеточную мРНК с одним или несколькими, предпочтительно со всеми, из следующего: 5’-кэп, 5’-UTR, 3’-UTR и поли(A)-хвост (кодирующая репликазу мРНК). В репликазной конструкции, как правило, отсутствуют элементы последовательности, необходимые для репликации с помощью альфавирусной репликазы. Элементы последовательности, необходимые для репликации с помощью альфавирусной репликазы, однако, находятся на РНК-репликоне. Согласно некоторым вариантам осуществления РНК-репликон содержит CSE 1, 2 и 4 и SGP.
Фиг. 2. Структуры динуклеотидов кэпа.
Вверху: природный динуклеотид кэпа, m7GpppG.
Внизу: фосфоротиоатный аналог кэпа динуклеотид бета-S-ARCA. Существует два диастереомера бета-S-ARCA из-за стереогенного P-центра, которые обозначены D1 и D2 в соответствии с их характеристиками элюирования в ВЭЖХ с обращенной фазой.
Фиг. 3: Эффективность экспрессии трансгена, кодируемого репликоном, зависит от молекулярного окружения ORF, кодирующей репликазу. Интенсивность флуоресценции eGFP, измеренная посредством FACS, после совместной доставки РНК цис-репликона и РНК транс-репликона (слева), или совместной доставки кодирующей репликазу мРНК и РНК транс-репликона (справа) в клетки BHK21 (пример 1). Показан процент eGFP-положительных клеток (столбики) и средняя интенсивность флуоресценции (MFI) eGFP-положительных клеток (ромбы). мРНК = репликазная конструкция в соответствии с настоящим изобретением.
Фиг. 4: Экспрессия генов в первичных клетках подтверждает эффективность системы транс-репликации. Интенсивность флуоресценции eGFP, измеренная после доставки системы цис-репликации (РНК eGFP-репликона) или совместной доставки системы транс-репликации (содержащей РНК репликазы и РНК транс-репликона) в фибробласты крайней плоти человека. РНК, кодирующую ингибитор E3 протеинкиназы R (PKR) вируса осповакцины, совместно доставляли для подавления активации PKR и тем самым увеличивали трансляцию РНК (пример 2). Показан процент eGFP-положительных клеток (столбики) и средняя интенсивность флуоресценции (MFI) eGFP-положительных клеток (ромбы).
Фиг. 5: Влияние количества РНК репликазы и использования кодонов репликазы.
Фиг. 5A: Относительные световые единицы [RLU] (секретируемая NanoLuc), измеренные после липофекции первичных фибробластов крайней плоти человека с различными количествами кодирующей репликазу мРНК (пример 3).
Фиг. 5B: интенсивность флуоресценции eGFP, измеренная посредством FACS после совместной доставки РНК репликазы и РНК транс-репликона в клетки BHK21 (пример 4). Показан процент eGFP-положительных клеток (столбики) и средняя интенсивность флуоресценции (MFI) eGFP-положительных клеток (ромбы). Как описано в примере 4, модификация использования кодонов является невыгодной для экспрессии трансгена и для продуктивной репликации транс-репликона (подробности смотрите в примере 4). Использование кодонов hs: адаптированное к Homo sapiens использование кодонов; использования кодонов wt: использование кодонов альфавируса дикого типа.
Нижняя часть: Вестерн-блоттинг, указывающий на уровни myc-nsP3 и актина.
Фиг. 6: Эффективная экспрессия in vivo трансгена, кодируемого транс-репликоном. Биолюминесцентная визуализация (BLI) мышей после внутримышечной (i.m.) и внутрикожной (i.d.) совместной инъекции системы транс-репликации в соответствии с настоящим изобретением, содержащей кодирующую люциферазу РНК транс-репликона и репликазную конструкцию в форме мРНК (пример 5 ). Люминесценция выражается в виде фотонов в секунду [p/s].
Фиг. 7: Транс-репликоны, кодирующие грипп HA в качестве представляющего интерес белка, обеспечивают защиту от летальных вирусных инфекций. Как описано в примере 6, мышей Balb/C вакцинировали внутрикожно дважды (примирование) в течение 3 недель либо цис-репликоном, кодирующим грипп HA (R-HA), в дозе 5 мкг, либо транс-репликоном (TR-HA) в дозе 1 мкг. Там, где это указано, от 4 мкг до 14 мкг мРНК, кодирующей репликазу, вводили совместно с транс-репликоном. Там, где это указано, для улучшения трансляции вводили совместно различные количества мРНК, кодирующей E3 вируса осповакцины.
Положительный контроль: инактивированный вирус (IAV). Отрицательный контроль: растворитель (буфер PBS).
Фиг. 7A: Определение титра нейтрализации вируса (VNT) за день до заражения инфекцией летальными дозами вируса гриппа.
Фиг. 7B: анализ ингибирования гемагглютинина (HAI) сывороток мыши.
Фиг. 7C: Кривые Каплана-Мейера, показывающие выживаемость мышей после заражения инфекциями. Мыши, получавшие буфер PBS, умерли в течение 5 дней.
Фиг. 8: Влияние кэпа. Клетки BHK21 подвергали электропорации с РНК транс-репликона, кодирующей eGFP и secNLuc (секретируемую люциферазу), разделенные саморасщепляющимся пептидом P2A (свиным тесковирусом-1 2A) вместе либо с кэпированной бета-S-ARCA (D2) репликазной мРНК, либо некэпированной мРНК с IRES (EMCV) (участок внутренней посадки рибосомы от вируса энцефаломиокардита) выше против хода транскрипции от ORF репликазы. Через 24 часа после электропорации клетки анализировали с помощью FACS на экспрессию eGFP (A), супернатанты анализировали на уровни секреции secNLuc с помощью системы анализа люциферазы Nano-Glo® (Promega) (B) и экспрессию репликазы анализировали с помощью Вестерн-блоттинга (C).
Подробное описание настоящего изобретения
Хотя настоящее изобретение подробно описано ниже, следует понимать, что настоящее изобретение не ограничено конкретными способами, протоколами и реагентами, описанными в настоящем документе, поскольку они могут различаться. Следует также понимать, что используемая в настоящем документе терминология предназначена только для описания конкретных вариантов осуществления и не предназначена для ограничения объема настоящего изобретения, который будет ограничен только прилагаемой формулой настоящего изобретения. Если не указано иное, все технические и научные термины, используемые в настоящем документе, имеют те же значения, которые, как правило, понимаются специалистом в настоящей области техники.
Предпочтительно используемые в настоящем документе термины определяются, как описано в «Многоязычном словаре биотехнологических терминов: (Рекомендации IUPAC)», H.G.W. Leuenberger, B. Nagel и H. Kölbl, Eds., Helvetica Chimica Acta, CH-4010 Basel, Switzerland, (1995).
В практике настоящего изобретения будут использованы, если не указано иное, традиционные способы химии, биохимии, клеточной биологии, иммунологии и рекомбинантной ДНК, которые объясняются в литературе в этой области (смотрите, например, Molecular Cloning: A Laboratory Manual, 2nd Edition, J. Sambrook et al. eds., Cold Spring Harbor Laboratory Press, Cold Spring Harbor 1989).
Ниже будут описаны элементы настоящего изобретения. Эти элементы перечислены в конкретных вариантах осуществления, однако следует понимать, что они могут быть объединены любым способом и в любом числе для создания дополнительных вариантов осуществления. Различные описанные примеры и предпочтительные варианты осуществления не должны толковаться как ограничивающие настоящее изобретение только явно описанными вариантами осуществления. Это описание следует понимать как раскрытие и объединение в себе вариантов осуществления, которые объединяют явно описанные варианты осуществления с любым количеством раскрытых и/или предпочтительных элементов. Кроме того, любые перестановки и комбинации всех описанных элементов в этом приложении следует рассматривать как раскрытые этим описанием, если контекст не указывает иное.
Термин «приблизительно» означает около или примерно, и в контексте численного значения или диапазона, изложенного в настоящем документе, предпочтительно означает +/- 10% от указанного или заявленного численного значения или диапазона.
Неопределенные и определенные артикли и аналогичные ссылки, используемые в контексте описания настоящего изобретения (особенно в контексте формулы изобретения), должны толковаться как охватывающие как единственное, так и множественное число, если иное не указано в настоящем документе или явно не противоречит контексту. Перечисление диапазонов значений в настоящем документе просто предназначено для использования в качестве сокращенного способа индивидуальной ссылки на каждое отдельное значение, входящее в диапазон. Если не указано иное, каждое индивидуальное значение включается в спецификацию, как если бы оно было отдельно представлено в настоящем документе. Все описанные в настоящем документе способы могут быть выполнены в любом подходящем порядке, если иное не указано в настоящем документе или иначе явно не противоречит контексту. Использование любых и всех примеров или иллюстративного языка (например, «такой как»), приведенного в настоящем документе, предназначено просто для лучшей иллюстрации настоящего изобретения и не представляет собой ограничение объема настоящего изобретения, заявленного иным образом. Никакой язык в спецификации не следует истолковывать как указание на какой-либо незаявленный элемент, необходимый для практики настоящего изобретения.
Если прямо не указано иное, термин «содержащий» используется в контексте настоящего документа, чтобы указать на то, что дополнительные представители могут необязательно присутствовать в дополнение к представителям перечня, представленного посредством термина «содержащий». Однако в качестве конкретного варианта осуществления настоящего изобретения предполагается, что термин «содержащий» охватывает возможность отсутствия каких-либо дополнительных представителей, то есть для целей этого варианта осуществления «содержащий» следует понимать как имеющий значение «состоящий из».
Указания относительных количеств компонента, характеризуемого общим термином, означают общее количество всех конкретных вариантов или представителей, охватываемых указанным общим термином. Если определенный компонент, определяемый общим термином, указывается как присутствующий в определенном относительном количестве, и если этот компонент дополнительно характеризуется как специфический вариант или представитель, охватываемый общим термином, подразумевается, что никакие другие варианты или представители, охватываемые общим термином, дополнительно не присутствуют таким образом, что общее относительное количество компонентов, охватываемых общим термином, превышает указанную относительную величину; более предпочтительно нет других вариантов или представителей, охватываемых общим термином.
В тексте данного описания настоящего изобретения приводится несколько документов. Каждый из приведенных в настоящем документе документов (включая все патенты, заявки на патент, научные публикации, описания производителя, инструкции и т.д.), независимо от того, представлены ли они выше или ниже, полностью включены в настоящий документ посредством ссылки. Ничто в настоящем документе не должно толковаться как признание того, что настоящее изобретение не имеет права датировать более ранним числом такое раскрытие.
Используемые в настоящем документе такие термины, как «уменьшить» или «ингибировать», означают способность вызывать общее снижение, предпочтительно на 5% или более, 10% или более, 20% или более, более предпочтительно 50% или более и наиболее предпочтительно 75% или более. Термин «ингибировать» или подобные фразы включают в себя полное или практически полное ингибирование, то есть снижение до нуля или по существу до нуля.
Такие термины, как «увеличение» или «повышение» предпочтительно относятся к увеличению или повышению приблизительно на 10%, предпочтительно по меньшей мере на 20%, предпочтительно по меньшей мере на 30%, более предпочтительно по меньшей мере на 40%, более предпочтительно по меньшей мере на 50%, еще более предпочтительно по меньшей мере на 80% и наиболее предпочтительно по меньшей мере на 100%.
Термин «суммарный заряд» относится к заряду на целом объекте, таком как соединение или частица.
Ион, имеющий общий суммарный положительный заряд, представляет собой катион, тогда как ион, имеющий общий суммарный отрицательный заряд, представляет собой анион. Таким образом, согласно настоящему изобретению анион представляет собой ион с большим количеством электронов, чем протоны, что дает ему суммарный отрицательный заряд; а катион представляет собой ион с меньшим количеством электронов, чем протоны, что дает ему суммарный положительный заряд.
Такие термины как «заряженные», «суммарный заряд», «отрицательно заряженные» или «положительно заряженные» применительно к данному соединению или частице относятся к электрическому суммарному заряду данного соединения или частицы при растворении или суспендировании в воде при рН 7,0.
Термин «нуклеиновая кислота» согласно настоящему изобретению также предусматривает химическое получение производных нуклеиновой кислоты на нуклеотидном основании, на сахаре или на фосфате, и нуклеиновые кислоты, содержащие неприродные нуклеотиды и нуклеотидные аналоги. Согласно некоторым вариантам осуществления нуклеиновая кислота представляет собой дезоксирибонуклеиновую кислоту (ДНК) или рибонуклеиновую кислоту (РНК).
В соответствии с настоящим изобретением термин «РНК» или «молекула РНК» относится к молекуле, которая содержит рибонуклеотидные остатки и которая предпочтительно полностью или по существу состоит из рибонуклеотидных остатков. Термин «рибонуклеотид» относится к нуклеотиду с гидроксильной группой в 2’-положении β-D-рибофуранозильной группы. Термин «РНК» включает в себя двухцепочечную РНК, одноцепочечную РНК, выделенную РНК, такую как частично или полностью очищенная РНК, по существу чистую РНК, синтетическую РНК и рекомбинантно произведенную РНК, такую как модифицированная РНК, которая отличается от природной РНК добавлением, делецией, заменой и/или изменением одного или нескольких нуклеотидов. Такие изменения могут включать в себя добавление ненуклеотидного материала, например, на конце (концах) РНК или внутри, например, к одному или нескольким нуклеотидам РНК. Нуклеотиды в молекулах РНК могут также содержать нестандартные нуклеотиды, такие как не встречающиеся в природе нуклеотиды или химически синтезированные нуклеотиды или дезоксинуклеотиды. Эти измененные РНК можно назвать аналогами, особенно аналогами встречающихся в природе РНК.
Согласно настоящему изобретению РНК может быть одноцепочечной или двухцепочечной. Согласно некоторым вариантам осуществления настоящего изобретения одноцепочечная РНК является предпочтительной. Термин «одноцепочечная РНК», как правило, относится к вариантам осуществления, при которых ни одна комплементарная цепь нуклеиновой кислоты (как правило, без комплементарной цепи РНК, то есть без комплементарной молекулы РНК) не связана с молекулой РНК. Одноцепочечная РНК может существовать как минус-нить [(-)-нить] или как плюс-нить [(+)-нить]. (+)-нить представляет собой нить, которая содержит или кодирует генетическую информацию. Генетическая информация может представлять собой, например, полинуклеотидную последовательность, кодирующую белок. Когда (+)-нитевая РНК кодирует белок, (+)-нить может служить непосредственно в качестве матрицы для трансляции (синтеза белка). (-)-нить является комплементарной к (+)-нити. В случае двухцепочечной РНК (+)-нить и (-)-нить представляют собой две отдельные молекулы РНК, и обе эти молекулы РНК связываются друг с другом с образованием двухцепочечной РНК («дуплексная РНК»).
Термин «стабильность» РНК относится к «периоду полужизни» РНК. «Период полужизни» относится к периоду времени, который необходим для устранения половины активности, количества или числа молекул. В контексте настоящего изобретения период полужизни РНК является показателем стабильности указанной РНК. Период полужизни РНК может влиять на «продолжительность экспрессии» РНК. Можно ожидать, что РНК, характеризующаяся длительным периодом полужизни, будет экспрессироваться в течение длительного периода времени.
«Фрагмент» или «фрагмент последовательности нуклеиновой кислоты» относится к части последовательности нуклеиновой кислоты, то есть последовательности, которая представляет собой последовательность нуклеиновой кислоты, укороченную на 5'- и/или 3'-конце(-ах). Предпочтительно фрагмент последовательности нуклеиновой кислоты содержит по меньшей мере 80%, предпочтительно по меньшей мере 90%, 95%, 96%, 97%, 98% или 99% нуклеотидных остатков от указанной последовательности нуклеиновой кислоты. В настоящем изобретении предпочтительными являются те фрагменты молекул РНК, которые сохраняют стабильность РНК и/или эффективность трансляции.
Термин «вариант» в отношении, например, последовательностей нуклеиновых кислот и аминокислот согласно настоящему изобретению включает в себя любые варианты, в частности мутанты, вирусные штаммы, варианты сращивания, конформации, изоформы, аллельные варианты, видовые варианты и видовые гомологи, в частности те, которые присутствуют в природе. Аллельный вариант относится к изменению нормальной последовательности гена, значение которого часто неясно. Полное секвенирование генов часто идентифицирует многочисленные аллельные варианты для данного гена. Что касается молекул нуклеиновой кислоты, термин «вариант» включает в себя вырожденные последовательности нуклеиновой кислоты, причем вырожденная нуклеиновая кислота согласно настоящему изобретению представляет собой нуклеиновую кислоту, которая отличается от эталонной нуклеиновой кислоты в последовательности кодонов из-за вырожденности генетического кода. Видовой гомолог представляет собой нуклеиновую кислоту или аминокислотную последовательность, происходящую от другого вида, чем данная последовательность нуклеиновой кислоты или аминокислотная последовательность. Гомолог вируса представляет собой нуклеиновую кислоту или аминокислотную последовательность, происходящую от другого вируса, чем данная последовательность нуклеиновой кислоты или аминокислотная последовательность.
В соответствии с настоящим изобретением варианты нуклеиновой кислоты включают в себя одиночные или множественные нуклеотидные делеции, добавления, мутации и/или вставки по сравнению с эталонной нуклеиновой кислотой. Делеции включают в себя удаление одного или нескольких нуклеотидов из эталонной нуклеиновой кислоты. Варианты добавлений предусматривают 5'- и/или 3'-концевые слияния одного или нескольких нуклеотидов, например, 1, 2, 3, 5, 10, 20, 30, 50 или более нуклеотидов. Мутации могут включать в себя, без ограничения, замены, причем по меньшей мере один нуклеотид в последовательности удаляется, и вместо него вставляется другой нуклеотид (например, трансверсии и транзиции), участки с удаленными азотистыми основаниями, сшитые сайты и химически измененные или модифицированные основания. Вставки включают в себя добавление по меньшей мере одного нуклеотида в эталонную нуклеиновую кислоту.
Варианты конкретных последовательностей нуклеиновых кислот предпочтительно характеризуются по меньшей мере одним функциональным свойством указанных конкретных последовательностей и предпочтительно являются функционально эквивалентными указанным конкретным последовательностям, например, последовательностям нуклеиновых кислот, обладающим свойствами, идентичными или сходными таковым конкретных последовательностей нуклеиновых кислот.
Предпочтительно степень идентичности между данной последовательностью нуклеиновой кислоты и последовательностью нуклеиновой кислоты, которая представляет собой вариант указанной данной последовательности нуклеиновой кислоты, будет составлять по меньшей мере 70%, предпочтительно по меньшей мере 75%, предпочтительно по меньшей мере 80%, более предпочтительно по меньшей мере 85%, еще более предпочтительно по меньшей мере 90% или наиболее предпочтительно по меньшей мере 95%, 96%, 97%, 98% или 99%. Степень идентичности предпочтительно определяется для области, составляющей по меньшей мере приблизительно 30, по меньшей мере приблизительно 50, по меньшей мере приблизительно 70, по меньшей мере приблизительно 90, по меньшей мере приблизительно 100, по меньшей мере приблизительно 150, по меньшей мере приблизительно 200, по меньшей мере приблизительно 250, по меньшей мере приблизительно 300 или по меньшей мере приблизительно 400 нуклеотидов. Согласно предпочтительным вариантам осуществления степень идентичности определяется для всей длины эталонной последовательности нуклеиновой кислоты.
«Сходство последовательностей» указывает на процент аминокислот, которые либо идентичны, либо представляют собой консервативные аминокислотные замены. «Идентичность последовательностей» между двумя последовательностями полипептида или нуклеиновой кислоты показывает процент аминокислот или нуклеотидов, которые идентичны между последовательностями.
Термин «% идентичности» предназначен, в частности, для обозначения процента нуклеотидов, которые идентичны при оптимальном выравнивании между двумя подлежащими сравнению последовательностями, причем указанный процент является чисто статистическим, а различия между этими двумя последовательностями могут быть случайно распределены по всей длине последовательности, и подлежащая сравнению последовательность может содержать добавления или удаления по сравнению с эталонной последовательностью, чтобы получить оптимальное выравнивание между двумя последовательностями. Сравнение двух последовательностей, как правило, выполняется путем сравнения указанных последовательностей после оптимального выравнивания относительно сегмента или «окна сравнения» для идентификации локальных областей соответствующих последовательностей. Оптимальное выравнивание для сравнения может быть выполнено вручную или с помощью алгоритма поиска локальной гомологии от Smith and Waterman, 1981, Ads App. Math. 2, 482, с помощью алгоритма поиска локальной гомологии от Needleman and Wunsch, 1970, J. Mol. Biol. 48, 443 и с помощью алгоритма поиска подобия от Pearson and Lipman, 1988, Proc. Natl Acad. Sci. USA 85, 2444 или с помощью компьютерных программ с использованием указанных алгоритмов (GAP, BESTFIT, FASTA, BLAST P, BLAST N и TFASTA в пакете программного обеспечения Wisconsin Genetics, Genetics Computer Group, 575 Science Drive, Madison, Wis.).
Процент идентичности получают путем определения количества идентичных положений, в которых соответствуют подлежащие сравнению последовательности, деля их на количество сравниваемых положений и умножая этот результат на 100.
Например, может быть использована программа BLAST «последовательности BLAST 2», которая доступна на веб-сайте http://www.ncbi.nlm.nih.gov/blast/bl2seq/wblast2.cgi.
Нуклеиновая кислота «способна гибридизоваться» или «гибридизуется» с другой нуклеиновой кислотой, если две последовательности являются комплементарными друг другу. Нуклеиновая кислота является «комплементарной» по отношению к другой нуклеиновой кислоте, если две последовательности способны образовывать стабильный дуплекс друг с другом. Согласно настоящему изобретению гибридизацию предпочтительно проводят в условиях, которые позволяют специфическую гибридизацию между полинуклеотидами (строгие условия). Строгие условия описаны, например, в публикации Molecular Cloning: A Laboratory Manual, J. Sambrook et al., Editors, 2nd Edition, Cold Spring Harbor Laboratory press, Cold Spring Harbor, New York, 1989 или Current Protocols in Molecular Biology, F.M. Ausubel et al., Editors, John Wiley & Sons, Inc., New York и, например, относятся к гибридизации при температуре 65°C в буфере для гибридизации (3,5 × SSC, фиколл в концентрации 0,02%, поливинилпирролидон в концентрации 0,02%, бычий сывороточный альбумин в концентрации 0,02%, NaH2PO4 в концентрации 2,5 мМ (pH 7), ДСН в концентрации 0,5%, ЭДТА в концентрации 2 мМ). SSC представляет сбой 0,15 М хлорида натрия/0,15 М цитрата натрия, рН 7. После гибридизации мембрану, на которую переносили ДНК, промывают, например, в 2 × SSC при комнатной температуре, а затем в 0,1-0,5 × SSC/0,1 × SDS при температурах до 68°C.
Процент комплементарности указывает на процент смежных остатков в молекуле нуклеиновой кислоты, которая может образовывать водородные связи (например, спаривание оснований Уотсона-Крика) со второй последовательностью нуклеиновой кислоты (например, 5, 6, 7, 8, 9, 10 из 10 комплементарны на 50%, 60%, 70%, 80%, 90% и 100%). «Совершенно комплементарный» или «полностью комплементарный» означает, что все смежные остатки последовательности нуклеиновой кислоты будут связаны посредством водородной связи с таким же количеством смежных остатков во второй последовательности нуклеиновой кислоты. Предпочтительно, степень комплементарности согласно настоящему изобретению составляет по меньшей мере 70%, предпочтительно по меньшей мере 75%, предпочтительно по меньшей мере 80%, более предпочтительно по меньшей мере 85%, еще более предпочтительно по меньшей мере 90% или наиболее предпочтительно по меньшей мере 95% 96%, 97%, 98% или 99%. Наиболее предпочтительно, степень комплементарности согласно настоящему изобретению составляет 100%.
Термин «производное» включает в себя любое получение нуклеиновой кислоты химическим способом на нуклеотидном основании, на сахаре или на фосфате. Термин «производное» также включает в себя нуклеиновые кислоты, которые содержат нуклеотиды и нуклеотидные аналоги, не встречающиеся в природе. Предпочтительно, получение нуклеиновой кислоты химическим способом повышает ее стабильность.
В соответствии с настоящим изобретением «последовательность нуклеиновой кислоты, которая получена из последовательности нуклеиновой кислоты» относится к нуклеиновой кислоте, которая представляет собой вариант нуклеиновой кислоты, из которой она получена. Предпочтительно последовательность, которая представляет собой вариант по отношению к определенной последовательности, когда она заменяет конкретную последовательность в молекуле РНК, сохраняет стабильность РНК и/или эффективность трансляции.
Термины «транскрипция» и «транскрибирование» относятся к процессу, в ходе которого молекула нуклеиновой кислоты с определенной последовательностью нуклеиновой кислоты («матрица нуклеиновой кислоты») считывается РНК-полимеразой, так что РНК-полимераза производит одноцепочечную молекулу РНК. Во время транскрипции генетическая информация в матрице нуклеиновой кислоты транскрибируется. Матрица нуклеиновой кислоты может представлять собой ДНК; однако, например, в случае транскрипции из матрицы альфавирусной нуклеиновой кислоты матрица, как правило, представляет собой РНК. Впоследствии транскрибируемая РНК может быть транслирована в белок. В соответствии с настоящим изобретением термин «транскрипция» включает в себя «транскрипцию in vitro», причем термин «транскрипция in vitro» относится к процессу, при котором РНК, в частности мРНК, синтезируется in vitro в бесклеточной системе. Предпочтительно векторы клонирования применяются для производства транскриптов. Эти векторы клонирования, как правило, обозначаются как векторы транскрипции и согласно настоящему изобретению охватываются термином «вектор». В соответствии с настоящим изобретением РНК предпочтительно представляет собой транскрибированную in vitro РНК (IVT-РНК) и может быть получена посредством транскрипции in vitro соответствующей матрицы ДНК. Промотором для контроля транскрипции может быть любой промотор для любой РНК-полимеразы. Матрица ДНК для транскрипции in vitro может быть получена путем клонирования нуклеиновой кислоты, в частности кДНК, и введения ее в соответствующий вектор для транскрипции in vitro. кДНК может быть получена путем обратной транскрипции РНК.
Одноцепочечная молекула нуклеиновой кислоты, полученная во время транскрипции, как правило, содержит последовательность нуклеиновой кислоты, которая представляет собой комплементарную последовательность по отношению к матрице.
В соответствии с настоящим изобретению термины «матрица» или «матрица нуклеиновой кислоты» или «матричная нуклеиновая кислота», как правило, относятся к последовательности нуклеиновой кислоты, которая может быть реплицирована или транскрибирована.
Термин «последовательность нуклеиновой кислоты, транскрибируемая из последовательности нуклеиновой кислоты» относится к последовательности нуклеиновой кислоты, где это применимо, в виде части полной молекулы РНК, которая представляет собой продукт транскрипции последовательности-матрицы нуклеиновой кислоты. Как правило, транскрибированная последовательность нуклеиновой кислоты представляет собой одноцепочечную молекулу РНК.
«3'-конец нуклеиновой кислоты» относится в соответствии с настоящим изобретением к тому концу, который содержит свободную гидроксигруппу. В схематическом представлении двухцепочечных нуклеиновых кислот, в частности ДНК, 3'-конец всегда находится с правой стороны. «5'-конец нуклеиновой кислоты» относится в соответствии с настоящим изобретением к тому концу, который содержит свободную фосфатную группу. В схематическом представлении двухцепочечных нуклеиновых кислот, в частности ДНК, 5'-конец всегда находится с левой стороны.
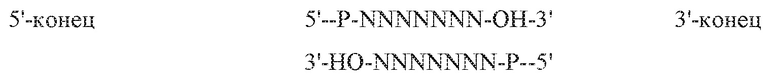
«Выше против хода транскрипции» описывает относительное позиционирование первого элемента молекулы нуклеиновой кислоты по отношению ко второму элементу этой молекулы нуклеиновой кислоты, причем оба элемента содержатся в одной и той же молекуле нуклеиновой кислоты, причем первый элемент расположен ближе к 5'-концу молекулы нуклеиновой кислоты, чем второй элемент этой молекулы нуклеиновой кислоты. Второй элемент потому называется как находящийся «ниже по ходу транскрипции» от первого элемента этой молекулы нуклеиновой кислоты. Элемент, который расположен «выше против хода транскрипции» от второго элемента, может быть синонимично обозначен как расположенный «5’» от этого второго элемента. Для двухцепочечной молекулы нуклеиновой кислоты указания относительно «выше против хода транскрипции» и «ниже по ходу транскрипции» даются относительно (+)-нити.
В соответствии с настоящим изобретением «функциональная связь» или «функционально связанный» относится к соединению в рамках функциональной связи. Нуклеиновая кислота «функционально связана», если между ней и другой последовательностью нуклеиновой кислоты установлена функциональная связь. Например, промотор функционально связан с кодирующей последовательностью, если он влияет на транскрипцию указанной кодирующей последовательности. Функционально связанные нуклеиновые кислоты, как правило, примыкают друг к другу, где соответствующие нуклеиновые кислоты отделены друг от друга дополнительными последовательностями нуклеиновых кислот и, согласно конкретным вариантам осуществления, транскрибируются РНК-полимеразой с получением одной молекулы РНК (общий транскрипт).
Согласно конкретным вариантам осуществления нуклеиновая кислота функционально связана в соответствии с настоящим изобретением с последовательностями контроля экспрессии, которые могут быть гомологичными или гетерологичными по отношению к нуклеиновой кислоте.
Термин «последовательность контроля экспрессии» включает в себя согласно настоящему изобретению промоторы, связывающие рибосомы последовательности и другие контрольные элементы, которые контролируют транскрипцию гена или трансляцию полученной РНК. Согласно конкретным вариантам осуществления настоящего изобретения последовательности контроля экспрессии можно регулировать. Точная структура последовательностей контроля экспрессии может варьировать в зависимости от вида или типа клеток, но, как правило, включает в себя 5'-нетранскрибируемые и 5'- и 3'-нетранслируемые последовательности, участвующие в инициации транскрипции и трансляции, соответственно. Более конкретно, 5'-нетранскрибируемые последовательности контроля экспрессии включают в себя промоторную область, которая охватывает последовательность промотора для контроля транскрипции функционально связанного гена. Последовательности контроля экспрессии могут также включать в себя энхансерные последовательности или последовательности активаторов выше против хода транскрипции. Последовательность контроля экспрессии молекулы ДНК, как правило, включает в себя 5'-нетранскрибируемые и 5'- и 3'-нетранслируемые последовательности, такие как TATA-бокс, кэпирующую последовательность, последовательность CAAT и тому подобное. Последовательность контроля экспрессии альфавирусной РНК может включать в себя субгеномный промотор и/или один или несколько элементов консервативной последовательности. Конкретная последовательность контроля экспрессии в соответствии с настоящим изобретением представляет собой субгеномный промотор альфавируса, как описано в настоящем документе.
Указанные в настоящем документе последовательности нуклеиновой кислоты, в частности транскрибируемые и кодирующие последовательности нуклеиновой кислоты, могут быть объединены с любыми последовательностями контроля экспрессии, в частности промоторами, которые могут быть гомологичными или гетерологичными по отношению к указанным последовательностям нуклеиновых кислот, причем термин «гомологичный» относится к факту того, что последовательность нуклеиновой кислоты также функционально связана природным образом с последовательностью контроля экспрессии, а термин «гетерологичный» относится к тому факту, что последовательность нуклеиновой кислоты функционально не связана природным образом с последовательностью контроля экспрессии.
Транскрибируемая последовательность нуклеиновой кислоты, в частности последовательность нуклеиновой кислоты, кодирующая пептид или белок, и последовательность контроля экспрессии «функционально» связаны друг с другом, если они ковалентно связаны друг с другом таким образом, что транскрипция или экспрессия транскрибируемой и, в частности, кодирующей последовательности нуклеиновой кислоты находится под контролем или под влиянием последовательности контроля экспрессии. Если последовательность нуклеиновой кислоты подлежит трансляции в функциональный пептид или белок, индукция последовательности контроля экспрессии, функционально связанной с кодирующей последовательностью, приводит к транскрипции указанной кодирующей последовательности, не вызывая сдвига рамки в кодирующей последовательности, или кодирующая последовательность не может быть транслирована в желаемый пептид или белок.
Термин «промотор» или «область промотора» относится к последовательности нуклеиновой кислоты, которая контролирует синтез транскрипта, например, транскрипта, содержащего кодирующую последовательность, путем предоставления сайта распознавания и связывания для РНК-полимеразы. Область промотора может включать в себя дополнительные сайты распознавания или связывания для дополнительных факторов, связанных с регуляцией транскрипции указанного гена. Промотор может контролировать транскрипцию прокариотического или эукариотического гена. Промотор может быть «индуцируемым» и инициировать транскрипцию в ответ на индуктор или быть «конститутивным», если транскрипция не контролируется индуктором. Индуцируемый промотор экспрессируется только в очень малой степени или вообще не экспрессируется, если индуктор отсутствует. В присутствии индуктора ген «включен» или уровень транскрипции увеличивается. Это, как правило, опосредуется связыванием специфического фактора транскрипции. Специфический промотор в соответствии с настоящим изобретением представляет собой субгеномный промотор альфавируса, как описано в настоящем документе. Другими специфическими промоторами являются геномные плюс-нитевые или минус-нитевые промоторы альфавируса.
Термин «основной промотор» относится к последовательности нуклеиновой кислоты, которая состоит из промотора. Основной промотор, как правило, представляет собой минимальную часть промотора, необходимую для правильной инициации транскрипции. Основной промотор, как правило, включает в себя сайт начала транскрипции и сайт связывания для РНК-полимеразы.
«Полимераза», как правило, относится к молекулярному объекту, способному катализировать синтез полимерной молекулы из мономерных структурных блоков. «РНК-полимераза» представляет собой молекулярный объект, способный катализировать синтез молекулы РНК из рибонуклеотидных структурных блоков. «ДНК-полимераза» представляет собой молекулярный объект, способный катализировать синтез молекулы ДНК из дезоксирибонуклеотидных структурных блоков. В случае ДНК-полимераз и РНК-полимераз молекулярный объект, как правило, представляет собой белок или сборку или комплекс из нескольких белков. Как правило, ДНК-полимераза синтезирует молекулу ДНК на основе матричной нуклеиновой кислоты, которая, как правило, представляет собой молекулу ДНК. Как правило, РНК-полимераза синтезирует молекулу РНК на основе матричной нуклеиновой кислоты, которая представляет собой либо молекулу ДНК (в этом случае РНК-полимераза представляет собой ДНК-зависимую РНК-полимеразу, DdRP), либо представляет собой молекулу РНК (в этом случае РНК полимераза представляет собой РНК-зависимую РНК-полимеразу, RdRP).
«РНК-зависимая РНК-полимераза» или «RdRP» представляет собой фермент, который катализирует транскрипцию РНК из матрицы РНК. В случае альфавирусной РНК-зависимой РНК-полимеразы последовательный синтез (-)-нитевого комплемента геномной РНК и (+)-нитевой геномной РНК приводит к репликации РНК. Таким образом, альфавирусная РНК-зависимая РНК-полимераза синонимично называется «РНК-репликазой». В природе РНК-зависимые РНК-полимеразы, как правило, кодируются всеми РНК-вирусами, кроме ретровирусов. Типичными представителями вирусов, кодирующих РНК-зависимую РНК-полимеразу, являются альфавирусы.
В соответствии с настоящим изобретением «репликация РНК», как правило, относится к молекуле РНК, синтезированной на основе нуклеотидной последовательности данной молекулы РНК (молекула-матрица РНК). Молекула РНК, которая синтезируется, может быть, например, идентичной или комплементарной молекуле-матрице РНК. В общем случае репликация РНК может происходить посредством синтеза промежуточного соединения ДНК или может происходить непосредственно с помощью РНК-зависимой репликации РНК, опосредованной РНК-зависимой РНК-полимеразой (RdRP). В случае альфавирусов репликация РНК не происходит через промежуточное звено ДНК, но опосредуется РНК-зависимой РНК-полимеразой (RdRP): матричная цепь РНК (первая цепь РНК) служит в качестве матрицы для синтеза второй цепи РНК, которая является комплементарным первой цепи РНК или ее части. Вторая цепь РНК может, в свою очередь, необязательно служить в качестве матрицы для синтеза третьей цепи РНК, которая комплементарна второй цепи РНК или ее части. Таким образом, третья цепь РНК идентична первой цепи РНК или ее части. Таким образом, РНК-зависимая РНК-полимераза способна непосредственно синтезировать комплементарную цепь РНК-матрицы и косвенно синтезировать идентичную цепь РНК (через комплементарную промежуточную цепь).
Согласно настоящему изобретению термин «ген» относится к определенной последовательности нуклеиновой кислоты, которая отвечает за производство одного или нескольких клеточных продуктов и/или за достижение одной или нескольких межклеточных или внутриклеточных функций. Более конкретно, указанный термин относится к сектору нуклеиновой кислоты (как правило, ДНК, но РНК в случае РНК-вирусов), который содержит нуклеиновую кислоту, кодирующую специфический белок или функциональную или структурную молекулу РНК.
Используемая в настоящем документе «выделенная молекула» предназначена для обозначения молекулы, которая по существу не содержит других молекул, таких как другой клеточный материал. Термин «выделенная нуклеиновая кислота» означает в соответствии с настоящим изобретением, что нуклеиновая кислота была (i) амплифицирована in vitro, например, посредством полимеразной цепной реакции (ПЦР), (ii) рекомбинантно произведена клонированием, (iii) очищена, например путем расщепления и гель-электрофоретического фракционирования, или (iv) синтезирована, например, путем химического синтеза. Выделенная нуклеиновая кислота представляет собой нуклеиновую кислоту, доступную для манипуляции рекомбинантными способами.
Термин «вектор» используется в настоящем документе в его самом общем значении и включает в себя любые промежуточные носители для нуклеиновой кислоты, которые, например, позволяют вводить указанную нуклеиновую кислоту в прокариотические и/или эукариотические клетки-хозяева и, при необходимости, интегрироваться в геном. Такие векторы предпочтительно реплицируются и/или экспрессируются в клетке. Векторы содержат плазмиды, фагемиды, вирусные геномы и их фракции.
Термин «рекомбинантный» в контексте настоящего изобретения означает «сделанный с помощью генной инженерии». Предпочтительно, «рекомбинантный объект», такой как рекомбинантная клетка в контексте настоящего изобретения, является неприродным.
Используемый в настоящем документе термин «природный» относится к тому факту, что объект может быть обнаружен в природе. Например, пептид или нуклеиновая кислота, которая присутствует в организме (включая в себя вирусы) и может быть выделена из источника в природе и которая не была намеренно модифицирована человеком в лаборатории является природной.
В соответствии с настоящим изобретением термин «экспрессия» используется в его наиболее общем значении и включает в себя получение РНК или РНК и белка. Он также включает в себя частичную экспрессию нуклеиновых кислот. Кроме того, экспрессия может быть временной или стабильной. Что касается РНК, термин «экспрессия» или «трансляция» относится к процессу в рибосомах клетки, с помощью которой нить матричной информационной РНК направляет сборку последовательности аминокислот для получения пептида или белка.
В соответствии с настоящим изобретением термин «мРНК» означает «матричную РНК» и относится к транскрипту, который, как правило, производится с использованием ДНК-матрицы и кодирует пептид или белок. Как правило, мРНК содержит 5’-UTR, область кодирования белка, 3’-UTR и поли(А)-последовательность. мРНК может быть получена путем транскрипции in vitro из ДНК-матрицы. Специалисту в настоящей области техники известен способ транскрипции in vitro. Например, существует множество коммерчески доступных наборов транскрипции in vitro. В соответствии с настоящим изобретением мРНК может быть модифицирована путем стабилизации модификаций и кэпирования.
В соответствии с настоящим изобретением термины «поли(А)-последовательность» или «поли(А)-хвост» относятся к непрерывной или прерывающейся последовательности остатков аденилата, которая, как правило, расположена на 3'-конце молекулы РНК. Непрерывная последовательность характеризуется последовательными остатками аденилата. В природе характерна непрерывная поли(А)-последовательность. Хотя поли(А)-последовательность, как правило, не кодируется в эукариотической ДНК, но прикрепляется при транскрипции эукариот в ядре клетки к свободному 3'-концу РНК с помощью независимой от матрицы РНК-полимеразы после транскрипции, настоящее изобретение охватывает поли(А)-последовательности, кодируемые ДНК.
В соответствии с настоящим изобретением такая нуклеиновая кислота, как РНК, например, мРНК, может кодировать пептид или белок. Соответственно, транскрибируемая последовательность нуклеиновой кислоты или ее транскрипт может содержать открытую рамку считывания (ORF), кодирующую пептид или белок.
В соответствии с настоящим изобретением термин «нуклеиновая кислота, кодирующая пептид или белок», означает, что нуклеиновая кислота, если она присутствует в подходящей окружающей среде, предпочтительно внутри клетки, может направлять сборку аминокислот для получения пептида или белка во время процесса трансляции. Предпочтительно, РНК согласно настоящему изобретению способна взаимодействовать с механизмом трансляции клеток, обеспечивая трансляцию пептида или белка.
В соответствии с настоящим изобретением термин «пептид» включает в себя олиго- и полипептиды и относится к веществам, которые содержат два или более, предпочтительно 3 или более, предпочтительно 4 или более, предпочтительно 6 или более, предпочтительно 8 или более, предпочтительно 10 или более, предпочтительно 13 или более, предпочтительно 16 или более, предпочтительно 20 или более и предпочтительно до 50, предпочтительно до 100 или предпочтительно до 150 последовательных аминокислот, связанных друг с другом посредством пептидных связей. Термин «белок» относится к большим пептидам, предпочтительно пептидам, содержащим по меньшей мере 151 аминокислоту, но термины «пептид» и «белок», как правило, используются в настоящем документе как синонимы.
Термины «пептид» и «белок» включают в себя в соответствии с настоящим изобретением вещества, которые содержат не только аминокислотные компоненты, но и неаминокислотные компоненты, такие как сахара и фосфатные структуры, а также содержат вещества, содержащие связи, такие как сложноэфирная, тиоэфирная или дисульфидная связи.
В соответствии с настоящим изобретением термин «альфавирус» следует понимать в широком смысле, и он включает в себя любую вирусную частицу, которая обладает характеристиками альфавирусов. Характеристики альфавируса включают в себя наличие (+)-нитевой РНК, которая кодирует генетическую информацию, подходящую для репликации в клетке-хозяине, включая в себя активность РНК-полимеразы. Дополнительные характеристики многих альфавирусов описаны, например, в публикациях Strauss & Strauss, Microbiol. Rev., 1994, vol. 58, pp. 491-562; Gould et al., 2010, Antiviral Res., vol. 87, pp. 111–124; Rupp et al., 2015, J. Gen. Virology, vol. 96, pp. 2483–2500. Термин «альфавирус» включает в себя альфавирус, обнаруженный в природе, а также любой его вариант или производное. Согласно некоторым вариантам осуществления вариант или производное не обнаружены в природе.
Согласно одному варианту осуществления альфавирус представляет собой альфавирус, обнаруженный в природе. Как правило, обнаруженный в природе альфавирус является инфекционным для любого одного или нескольких эукариотических организмов, таких как животное (включая в себя позвоночных, таких как человек, и членистоногих, таких как насекомое). Согласно типичным вариантам осуществления обнаруженный в природе альфавирус является инфекционным для животного. Многие обнаруженные в природе альфавирусы являются инфекционными для позвоночных и/или членистоногих (Strauss & Strauss, Microbiol. Rev., 1994, vol. 58, pp. 491-562).
Альфавирус, обнаруженный в природе, предпочтительно выбирают из группы, состоящей из следующих вирусов: комплекс вирусов леса Барма (содержащий вирус леса Барма); комплекс восточного лошадиного энцефалита (содержащий семь антигенных типов вируса восточного лошадиного энцефалита); комплекс вирусов Мидделбурга (содержащий вирус Мидделбурга); комплекс вирусов Ндуму (содержащий вирус Ндуму); комплекс вирусов леса Семлики (содержащий вирус Бебару, вирус Чикунгунья, вирус Майаро и его подтип вирус Уна, вирус O'Нйонг Нйонг и его подтип вирус Игбо-Ора, вирус Росс-ривер и его подтипы вирус Бебару, вирус Гета, вирус Сагияма, вирус леса Семлики и его подтип вирус Me Tri); комплекс венесуэльского лошадиного энцефалита (содержащий вирус Кабассоу, вирус Эверглейдс, вирус Mosso das Pedras, вирус Мукамбо, вирус Paramana, вирус Пиксуна, вирус Рио-Негро, вирус Трокара и его подтип вирус Бижу-Бридж, вирус венесуэльского лошадиного энцефалита); комплекс западного лошадиного энцефалита (содержащий вирус Аура, вирус Бабанки, вирус Кызылагач, вирус Синдбис, вирус Окелбо, вирус Ватароа, вирус Багги-Крик, вирус Форт-Морган, вирус Хайлендс Джи, вирус западного лошадиного энцефалита); и некоторые неклассифицированные вирусы, включающие в себя вирус панкреатической болезни лосося; вирус нарколептической болезни; вирус южного морского слона; вирус Tonate. Более предпочтительно, чтобы альфавирус был выбран из группы, состоящей из комплекса вирусов леса Семлики (содержащего указанные выше типы вирусов, включая в себя вирус леса Семлики), комплекса западного лошадиного энцефалита (содержащего указанные выше типы вирусов, включая в себя вирус Синдбис), комплекса восточного лошадиного энцефалита (содержащего указанные выше типы вирусов), комплекса венесуэльского лошадиного энцефалита (содержащего указанные выше типы вирусов, включая вирус венесуэльского лошадиного энцефалита).
Согласно дополнительному предпочтительному варианту осуществления альфавирус представляет собой вирус леса Семлики. Согласно альтернативному дополнительному предпочтительному варианту осуществления альфавирус представляет собой вирус Синдбис. Согласно альтернативному дополнительному предпочтительному варианту осуществления альфавирус представляет собой вирус венесуэльского лошадиного энцефалита.
Согласно некоторым вариантам осуществления настоящего изобретения альфавирус представляет собой не обнаруженный в природе альфавирус. Как правило, не обнаруженный в природе альфавирус представляет собой вариант или производное обнаруженного в природе альфавируса, который отличается от обнаруженного в природе альфавируса по меньшей мере одной мутацией в нуклеотидной последовательности, то есть геномной РНК. Мутация в нуклеотидной последовательности может быть выбрана из вставки, замены или делеции одного или нескольких нуклеотидов по сравнению с обнаруженным в природе альфавирусом. Мутация в нуклеотидной последовательности может быть связана или не связана с мутацией в полипептиде или белке, кодируемом нуклеотидной последовательностью. Например, не обнаруженный в природе альфавирус может представлять собой аттенуированный альфавирус. Не обнаруженный в природе аттенуированный альфавирус представляет собой альфавирус, который, как правило, содержит по меньшей мере одну мутацию в своей нуклеотидной последовательности, благодаря которой он отличается от обнаруженного в природе альфавируса, и который либо не является инфекционным вообще, либо является инфекционным, но характеризуется более низкой болезнетворной способностью или вообще не характеризуется болезнетворной способностью. В качестве иллюстративного примера TC83 представляет собой аттенуированный альфавирус, который отличается от обнаруженного в природе вируса венесуэльского лошадиного энцефалита (VEEV) (MyKinney et al., 1963, Am. J. Trop. Med. Hyg., 1963, vol. 12; pp. 597-603).
Термин «обнаруженный в природе» означает «присутствующий в природе» и включает в себя известные объекты, а также объекты, которые еще не были обнаружены в природе и/или выделены из природного источника, но которые могут быть обнаружены и/или выделены в будущем из природного источника.
Представители рода альфавирусов также могут быть классифицированы на основе их относительных клинических особенностей у людей: альфавирусы, связанные прежде всего с энцефалитом, и альфавирусы, связанные прежде всего с лихорадкой, сыпью и полиартритом.
Термин «альфавирусный» означает обнаруженный в альфавирусе или происходящий от альфавируса, или полученный из альфавируса, например, посредством генной инженерии.
В соответствии с настоящим изобретением «SFV» означает вирус леса Семлики. В соответствии с настоящим изобретением «SIN» или «SINV» означает вирус Синдбис. В соответствии с настоящим изобретением «VEE» или «VEEV» означает вирус венесуэльского лошадиного энцефалита.
Термин «консервативный элемент последовательности» или «CSE» относится к нуклеотидной последовательности, обнаруженной в альфавирусной РНК. Эти элементы последовательности называются «консервативными», поскольку ортологи присутствуют в геноме разных альфавирусов, а ортологические CSE разных альфавирусов предпочтительно характеризуются высоким процентом идентичности последовательности и/или аналогичной вторичной или третичной структурой. Термин CSE включает в себя CSE 1, CSE 2, CSE 3 и CSE 4 (подробнее смотрите José et al., Future Microbiol., 2009, vol. 4, pp. 837–856).
В соответствии с настоящим изобретением термин «субгеномный промотор» или «SGP» относится к последовательности нуклеиновой кислоты выше против хода транскрипции (5') от последовательности нуклеиновой кислоты (например, кодирующей последовательности), которая контролирует транскрипцию указанной последовательности нуклеиновой кислоты путем обеспечения сайта распознавания и связывания для РНК-полимеразы, как правило, РНК-зависимой РНК-полимеразы. SGP может включать в себя дополнительные сайты распознавания или связывания для дополнительных факторов. Субгеномный промотор, как правило, представляет собой генетический элемент вируса РНК с положительной нитью, такого как альфавирус. Субгеномный промотор альфавируса представляет собой последовательность нуклеиновой кислоты, содержащуюся в вирусной геномной РНК. Субгеномный промотор, как правило, характеризуется тем, что он позволяет инициировать транскрипцию (синтез РНК) в присутствии РНК-зависимой РНК-полимеразы, например, альфавирусной репликазы. (-)-нить РНК, то есть комплемент альфавирусной геномной РНК, служит в качестве матрицы для синтеза (+)-нити субгеномной РНК-молекулы, а синтез субгеномной (+)-нити, как правило, инициируется в субгеномном промоторе или вблизи него. Для иллюстративных и неограничивающих целей типичная локализация SGP, содержащаяся в примере альфавирусного генома, проиллюстрирована на фиг. 1А. Однако используемый в настоящем документе термин «субгеномный промотор» не ограничивается какой-либо конкретной локализацией в нуклеиновой кислоте, содержащей такой субгеномный промотор. Согласно некоторым вариантам осуществления SGP идентичен CSE 3 или перекрывается с CSE 3 или содержит CSE 3.
Термин «аутологичный» используется для описания всего, что получают от одного и того же субъекта. Например, «аутологичная клетка» относится к клетке, полученной от одного и того же субъекта. Введение аутологичных клеток в субъект выгодно, поскольку эти клетки преодолевают иммунологический барьер, который в противном случае приводит к отторжению.
Термин «аллогенный» используется для описания всего, что получают от разных особей одного и того же вида. Два или более индивидуумов считаются аллогенными друг по отношению к другу, когда гены в одном или нескольких локусах не идентичны.
Термин «сингенный» используется для описания всего, что получают от индивидуумов или из тканей, имеющих идентичные генотипы, то есть идентичных близнецов или животных одного и того же инбредного штамма, или их тканей или клеток.
Термин «гетерологичный» используется для описания того, что состоит из нескольких разных элементов. В качестве примера, введение клетки одного индивидуума другим индивидуумам представляет собой гетерологичную трансплантацию. Гетерологичный ген представляет собой ген, полученный из источника, отличного от субъекта.
Ниже приводятся конкретные и/или предпочтительные варианты отдельных особенностей настоящего изобретения. Настоящее изобретение также рассматривает в качестве особенно предпочтительных вариантов осуществления те варианты осуществления, которые получают путем объединения двух или более конкретных и/или предпочтительных вариантов осуществления, описанных для двух или более особенностей настоящего изобретения.
Система по настоящему изобретению
Согласно первому аспекту в настоящем изобретении предусмотрена система, содержащая:
конструкцию РНК для экспрессии альфавирусной репликазы,
РНК-репликон, который может быть реплицирован репликазой in trans,
причем конструкция РНК для экспрессии альфавирусной репликазы содержит 5’-кэп. 5’-кэп служит для управления трансляцией репликазы.
Таким образом, в настоящем изобретении предусмотрена система, содержащая две молекулы нуклеиновой кислоты: первую молекулу РНК для экспрессии репликазы (то есть кодирующую репликазу); и вторую молекулу РНК (репликон). Конструкция РНК для экспрессии репликазы синонимично упоминается в настоящем документе как «репликазная конструкция».
В системе настоящего изобретения роль репликазы заключается в амплификации репликона in trans. Поэтому репликон можно назвать транс-репликоном. Если репликон кодирует представляющий интерес ген для экспрессии, уровни экспрессии представляющего интерес гена и/или продолжительность экспрессии могут регулироваться in trans, изменяя уровни репликазы.
В общем, РНК представляет собой привлекательную альтернативу ДНК, чтобы обойти потенциальные риски безопасности, связанные с использованием ДНК в терапии людей и животных. Преимущества терапевтического применения РНК включают в себя временную экспрессию и нетрансформирующий характер, и РНК не требуется вводить в ядро для ее экспрессии, тем самым минимизируя риск онкогенеза.
Несмотря на эти преимущества, использование РНК для клинических применений было ограничено, особенно из-за нестабильности РНК и связанного с этим короткого периода полужизни РНК. В настоящем изобретении короткий период полужизни РНК может быть скомпенсирован системой, которая управляет репликацией РНК в клетке-хозяине или в организме. В дополнение к этому, в настоящем изобретении предусмотрены конкретные модификации РНК, составы, носители и способы доставки, которые являются предпочтительными для стабильности РНК. Они будут описаны ниже. Действительно, когда РНК системы по настоящему изобретению вводится в клетку или животное, достигается эффективная экспрессия генетической информации.
Преимущество настоящего изобретения по сравнению с известными подходами заключается в том, что без транскрипции ДНК-матрицы и переноса транскрипта из ядра в цитозоль можно обойтись. Это устраняет зависимость от правильного функционирования ДНК-зависимой РНК-полимеразы и транспорта мРНК. Вместо этого репликазная конструкция по настоящему изобретению немедленно доступна для трасляции.
Как описано в настоящем документе, система по настоящему изобретению подходит для эффективного получения желаемого полипептида (например, трансгена) в клетке-хозяине или организме-хозяине. Одним из преимуществ настоящего изобретения является то, что может быть достигнута более высокая экспрессия трансгена, чем в случае полноразмерных репликонов, подходящих для репликации in cis. Еще одним преимуществом системы по настоящему изобретению является то, что высокоэффективную экспрессию представляющего интерес гена можно получить в первичных клетках дикого типа (смотрите пример 2) и у живых животных, то есть in vivo (примеры 5 и 6). Это является значительным преимуществом по сравнению с известными в настоящей области техники системами, которые зависят от сконструированных клеточных линий, экспрессирующих ДНК-зависимую РНК-полимеразу бактериофагового происхождения, РНК-полимеразу Т7 (Spuul et al., J. Virol., 2011, vol. 85, pp. 4739-4751; Sanz et al., Cellular Microbiol., 2015, vol. 17, pp. 520-541). Клетки млекопитающих, как правило, не экспрессируют РНК-полимеразу Т7, если они специально не сконструированы (Buchholz et al., J. Virol., 1999, vol. 73, pp. 251-259). Таким образом, система на основе РНК по настоящему изобретению выгодна по сравнению с традиционными подходами к генной доставке или генной терапии.
Система по настоящему изобретению может быть легко получена. Например, молекулы РНК могут быть транскрибированы in vitro из матрицы ДНК. Согласно одному варианту осуществления РНК по настоящему изобретению представляет собой транскрибированную in vitro РНК (IVT-РНК). Таким образом, согласно одному варианту осуществления система по настоящему изобретению содержит IVT-РНК. Предпочтительно, все молекулы РНК системы по настоящему изобретению представляют собой IVT-РНК. Транскрибированная in vitro РНК (IVT-РНК) представляет особый интерес для терапевтических подходов.
Система по настоящему изобретению содержит по меньшей мере две молекулы нуклеиновой кислоты. Таким образом, она может содержать две или более, три или более, четыре или более, пять или более, шесть или более, семь или более, восемь или более, девять или более или десять или более молекул нуклеиновой кислоты. Согласно предпочтительному варианту осуществления она содержит ровно две молекулы нуклеиновой кислоты, предпочтительно молекулы РНК, репликон и репликазную конструкцию. Согласно альтернативным предпочтительным вариантам осуществления система содержит в дополнение к репликазной конструкции более чем один репликон, каждый из которых предпочтительно кодирует по меньшей мере один представляющий интерес белок. Согласно этим вариантам осуществления репликаза, закодированная репликазной конструкцией, может действовать на каждый репликон для управления репликацией и производством субгеномных транскриптов, соответственно. Например, каждый репликон может кодировать фармацевтически активный пептид или белок. Это выгодно, например, если требуется вакцинация субъекта против нескольких разных антигенов.
Предпочтительно, система по настоящему изобретению не способна образовывать вирусные частицы, в частности вирусные частицы следующего поколения. Предпочтительно, репликазная конструкция по настоящему изобретению не способна к саморепликации в целевой клетке или в целевом организме.
Хотя аспекты и преимущества РНК описаны в настоящем документе, согласно некоторым вариантам осуществления альтернативно возможно, что система по настоящему изобретению содержит одну или несколько молекул ДНК. Любая одна или несколько молекул нуклеиновой кислоты системы по настоящему изобретению, согласно некоторых вариантам осуществления, могут представлять собой молекулу ДНК. Возможно, что репликазная конструкция и/или репликон представляют собой молекулу ДНК. В случае молекулы ДНК предпочтительно присутствует промотор ДНК-зависимой РНК-полимеразы, что позволяет транскрибировать инфицированную или вакцинированную клетку-хозяина или организм-хозяина.
Дополнительные варианты осуществления и преимущества системы по настоящему изобретению описаны ниже.
Характеристика репликазной конструкции
Предпочтительно, конструкция РНК для экспрессии альфавирусной репликазы (репликазная конструкция) содержит открытую рамку считывания (ORF), кодирующую альфавирусную репликазу.
В соответствии с настоящим изобретением «репликаза» относится к РНК-зависимой РНК-полимеразе (RdRP). RdRP характеризуется ферментной функцией. Репликаза, как правило, относится к полипептиду или комплексу или объединению более чем одного идентичных и/или неидентичных белков, которые способны катализировать синтез (-)-нитевой РНК на основе (+)-нитевой РНК-матрицы и/или которые способны катализировать синтез (+)-нитевой РНК на основе (-)-нитевой РНК-матрицы. Репликаза может дополнительно характеризоваться одной или несколькими дополнительными функциями, такими как, например, функции протеиназы (для ауторасщепления), геликазы, концевой аденилаттрансферазы (для добавления поли(А)-хвоста), метилтрансферазы и гуанилтрансферазы (для получения нуклеиновой кислоты с 5’-кэпом), сайтов ядерной локализации, трифосфатазы (Gould et al., 2010, Antiviral Res., vol. 87, pp. 111–124; Rupp et al., 2015, J. Gen. Virol., vol. 96, pp. 2483-500).
В соответствии с настоящим изобретением «альфавирусная репликаза» относится к РНК-репликазе из альфавируса, включая в себя РНК-репликазу из встречающегося в природе альфавируса и РНК-репликазу из варианта или производного альфавируса, например, из аттенуированного альфавируса. В контексте настоящего изобретения термины «репликаза» и «альфавирусная репликаза» используются взаимозаменяемо, если только контекст не указывает, что какая-либо конкретная репликаза не представляет собой альфавирусную репликазу. Термин «репликаза» предусматривает все варианты, в частности посттрансляционно модифицированные варианты, конформации, изоформы и гомологи альфавирусной репликазы, которые экспрессируются инфицированными альфавирусами клетками или которые экспрессируются клетками, которые были трансфицированы нуклеиновой кислотой, которая кодирует репликазу. Более того, термин «репликаза» включает в себя все формы репликазы, которые были получены и могут быть получены рекомбинантными способами. Например, репликаза, содержащая метку, которая облегчает обнаружение и/или очистку репликазы в лаборатории, например, myc-метку, HA-метку или олигогистидиновую метку (His-метку), может быть получена рекомбинантными способами.
Необязательно, репликаза дополнительно функционально определяется способностью связываться с любым одним или несколькими из следующего: консервативный элемент последовательности 1 альфавируса (CSE1) или его комплементарная последовательность, консервативный элемент последовательности 2 альфавируса (CSE2) или его комплементарная последовательность, консервативный элемент последовательности 3 альфавируса (CSE3) или его комплементарная последовательность, консервативный элемент последовательности 4 альфавируса (CSE 4) или его комплементарная последовательность. Предпочтительно репликаза способна связываться с CSE 2 [т.е. с (+)-нитью] и/или с CSE 4 [т.е. с (+)-нитью] или связываться с комплементом CSE 1 [т.е. с (-)-нитью] и/или с комплементом CSE 3 [т.е. с (-)-нитью].
Происхождение репликазы не ограничивается каким-либо конкретным альфавирусом. Согласно предпочтительному варианту осуществления альфавирусную репликазу получают из вируса леса Семлики, включая в себя встречающийся в природе вируса леса Семлики и вариант или производное вируса леса Семлики, например, аттенуированный вирус леса Семлики. Согласно альтернативному предпочтительному варианту осуществления репликазу получают из вируса Синдбис, включая в себя природный вирус Синдбис и вариант или производное вируса Синдбис, такое как аттенуированный вирус Синдбис. Согласно альтернативному предпочтительному варианту осуществления репликазу получают из вируса венесуэльского лошадиного энцефалита (VEEV), включая в себя природный VEEV и вариант или производное VEEV, такое как аттенуированный VEEV.
Альфавирусная репликаза, как правило, содержит или состоит из альфавирусных неструктурных белков (nsP). В этом контексте «неструктурные белки» относятся к любому одному или нескольким отдельным неструктурным белкам, происходящим от альфавируса (nsP1, nsP2, nsP3, nsP4), или к полипептиду, содержащему полипептидную последовательность более чем одного неструктурного происходящего от альфавируса белка, например, nsP1234. Согласно некоторым вариантам осуществления «неструктурный белок» относится к nsP123. Согласно другим вариантам осуществления «неструктурный белок» относится к nsP1234. Согласно другим вариантам осуществления «неструктурный белок» относится к комплексу или объединению nsP123 (синонимично P123) и nsP4. Согласно некоторым вариантам осуществления «неструктурный белок» относится к комплексу или объединению nsP1, nsP2 и nsP3. Согласно некоторым вариантам осуществления «неструктурный белок» относится к комплексу или объединению nsP1, nsP2, nsP3 и nsP4. Согласно некоторым вариантам осуществления «неструктурный белок» относится к комплексу или объединению любого из одного или нескольких белков, выбранных из группы, состоящей из nsP1, nsP2, nsP3 и nsP4.
Предпочтительно «комплекс или объединение» представляет собой функциональный ансамбль множества элементов. В контексте альфавирусной репликазы термин «комплекс или объединение» описывает множество по меньшей мере из двух молекул белка, из которых по меньшей мере один представляет собой неструктурный белок альфавируса, причем комплекс или объединение содержит РНК-зависимую РНК-полимеразу (RdRP). Комплекс или объединение может состоять из нескольких различных белков (гетеромультимер) и/или нескольких копий одного конкретного белка (гомомультимер). В контексте мультимера или множества «мульти» означает более одного, например, два, три, четыре, пять, шесть, семь, восемь, девять, десять или более десяти.
Комплекс или объединение также может содержать белки более чем из одного другого альфавируса. Например, в комплексе или объединении согласно настоящему изобретению, который содержит различные неструктурные белки альфавируса, не требуется, чтобы все неструктурные белки происходили из одного и того же альфавируса. Гетерологические комплексы или объединения в равной степени включены в настоящее изобретение. Для иллюстративных целей гетерологичный комплекс или объединение может содержать один или несколько неструктурных белков (например, nsP1, nsP2) из первого альфавируса (например, вируса Синдбис) и один или несколько неструктурных белков (nsP3, nsP4) из второго альфавируса (например, вируса леса Семлики).
Термины «комплекс» или «объединение» относятся к двум или более одинаковым или различным молекулам белка, которые находятся в пространственной близости. Белки комплекса предпочтительно находятся в прямом или косвенном физическом или физико-химическом контакте друг с другом. Комплекс или объединение может состоять из нескольких различных белков (гетеромультимер) и/или нескольких копий одного конкретного белка (гомомультимер).
Термин «репликаза» включает в себя каждую и все котрансляционно или посттрансляционно модифицированные формы, включая в себя модифицированные углеводами (например, гликозилированные) и модифицированные липидом формы альфавирусных неструктурных белков.
Термин «репликаза» включает в себя каждый и все функциональные фрагменты альфавирусной репликазы. Фрагмент является функциональным, когда он функционирует как РНК-зависимая РНК-полимераза (RdRP).
Согласно некоторым вариантам осуществления репликаза способна образовывать мембранные комплексы репликации и/или вакуоли в клетках, в которых экспрессируется репликаза.
Предпочтительно репликазная конструкция содержит кодирующую область (области) для репликации, как определено выше. Кодирующая область (области) может состоять из одной или нескольких открытых рамок считывания.
Согласно одному варианту осуществления репликазная конструкция кодирует все nsP1, nsP2, nsP3 и nsP4 альфавируса. Согласно одному варианту осуществления репликазная конструкция кодирует nsP1, nsP2, nsP3 и nsP4 альфавируса в виде одного единственного, необязательно расщепляемого полипротеина: nsP1234, кодируемого одной единственной открытой рамкой считывания. Согласно одному варианту осуществления репликазная конструкция кодирует nsP1, nsP2 и nsP3 альфавируса в виде одного единственного, необязательно расщепляемого полипротеина: nsP123, кодируемого одной единственной открытой рамкой считывания. Согласно этому варианту осуществления nsP4 может кодироваться отдельно.
Предпочтительно, репликазная конструкция по настоящему изобретению не содержит субгеномный промотор альфавируса.
Предпочтительно, репликазная конструкция представляет собой молекулу мРНК. Молекула мРНК предпочтительно не содержит ни CSE 1, ни CSE 4. Без ограничения теорией предполагается, что такая мРНК не будет конкурировать с репликоном за связывание репликазы, так что репликон может быть реплицирован очень эффективно с помощью репликазы.
РНК репликазной конструкции предпочтительно не является двухцепочечной, предпочтительно она представляет собой одноцепочечную, более предпочтительно (+)-нитевую РНК. Репликаза кодируется открытой рамкой считывания на репликазной конструкции.
Согласно одному варианту осуществления репликазная конструкция по настоящему изобретению представляет собой не содержащую интрон РНК, предпочтительно не содержащую интрон мРНК. Предпочтительно, репликазная конструкция представляет собой природную не содержащую интрон РНК (мРНК). Например, не содержащая интрон РНК (мРНК) может быть получена путем синтеза in vitro, например, транскрипцией in vitro. Согласно одному варианту осуществления репликазная конструкция содержит открытую рамку считывания, кодирующую nsP1234, которая не содержит интрон. Согласно одному варианту осуществления репликазная конструкция содержит открытую рамку считывания, кодирующую nsP123, которая не содержит интрон. Предпочтительно, репликазная конструкция не содержит интрон, полученный из гена бета-глобина кролика (как описано в публикации международной заявки WO 2008/119827 A1).
Используемый в настоящем документе «интрон» определяется как некодирующий участок мРНК-предшественника (пре-мРНК), который удаляется, т.е. сплайсируется из РНК, до трансляции кодирующей последовательности РНК в полипептид. Как только интроны были сплайсированы из пре-мРНК, полученная последовательность мРНК готова к трансляции в полипептид. Другими словами, нуклеотидная последовательность интрона, как правило, не транслируется в белок. Не содержащая интрон мРНК представляет собой мРНК, содержащую в последовательном порядке кодоны (триплеты оснований) для трансляции в полипептид. Не содержащая интрон мРНК может быть либо природной не содержащей интрон (т.е. первоначально синтезироваться как не содержащая интрон мРНК, например, в клетке или транскрипции in vitro), либо может созревать в не содержащую интрон мРНК путем сплайсинга содержащей интрон пре-мРНК. В настоящем изобретении предпочтительна природная не содержащая интрон транскрибированная in vitro РНК.
Репликазная конструкция по настоящему изобретению отличается от альфавирусной геномной РНК по меньшей мере тем, что она не способна к саморепликации и/или что она не содержит открытую рамку считывания под контролем субгеномного промотора. Когда она не может самореплицироваться, репликазная конструкция может также называться «суицидная конструкция».
Предпочтительно, репликазная конструкция по настоящему изобретению не связана со структурными белками альфавируса. Предпочтительно, репликазная конструкция не упакована альфавирусными структурными белками. Более предпочтительно, репликазная конструкция не упакована в вирусную частицу. Предпочтительно, репликазная конструкция не связана с вирусными белками (не содержащая вирусные белки система). Не содержащая вирусные белки система обеспечивает преимущество по сравнению с системой на основе вируса-помощника, известной в настоящем уровне техники, например, в публикации Bredenbeek с соавт., смотрите выше.
Предпочтительно, репликазная конструкция не содержит по меньшей мере один консервативный элемент последовательности (CSE), который необходим для синтеза (-)-нити на основе матрицы (+)-нити и/или для синтеза (+)-нити на основе матрицы (-)-нити. Более предпочтительно, репликазная конструкция не содержит каких-либо консервативных элементов последовательности (CSE), полученных из альфавируса. В частности, среди четырех CSE альфавируса (Strauss & Strauss, Microbiol. Rev., 1994, vol. 58, pp. 491-562; José et al., Future Microbiol., 2009, vol. 4, pp. 837–856), любой один или несколько из следующих CSE предпочтительно не присутствуют в репликазной конструкции.
- CSE 1, который, как полагают, функционирует в качестве промотора для синтеза (+)-нити на матрице (-)-нити в альфавирусе, обнаруженном в природе;
- CSE 2, который, как полагают, функционирует как промотор для синтеза (-)-нити на (+)-нити геномной РНК альфавируса, обнаруженного в природе;
- CSE 3, который, как полагают, способствует эффективной транскрипции субгеномной (+)-нитевой РНК в альфавирусе, обнаруженном в природе;
- CSE 4, который, как полагают, функционирует в качестве основного промотора для инициирования синтеза (-)-нити на основе (+)-нити геномной РНК в альфавирусе, обнаруженном в природе.
Согласно одному варианту осуществления CSE 1, CSE 3 и CSE 4 отсутствуют, а CSE 2 может присутствовать или отсутствовать.
В частности, в отсутствие какого-либо одного или нескольких альфавирусных CSE репликазная конструкция по настоящему изобретению напоминает типичную эукариотическую мРНК намного больше, чем она напоминает альфавирусную геномную РНК.
Согласно одному варианту осуществления репликазная конструкция по настоящему изобретению представляет собой выделенную молекулу нуклеиновой кислоты.
Кэп
Конструкция РНК для экспрессии альфавирусной репликазы (репликазная конструкция) содержит 5’-кэп. Термины «5’-кэп», «кэп», «структура 5’-кэп», «структура кэп» используются синонимично для обозначения динуклеотида, который находится на 5’-конце некоторых первичных транскриптов эукариот, таких как предшественник матричной РНК. 5’-кэп представляет собой структуру, в которой (необязательно модифицированный) гуанозин связан с первым нуклеотидом молекулы мРНК через 5'-5'-трифосфатную связь (или модифицированную трифосфатную связь в случае некоторых аналогов кэпа). Термины могут относиться к обычному кэпу или к аналогу кэпа. Для иллюстрации некоторые конкретные динуклеотиды кэпа (включая в себя аналоги динуклеотидов кэпа) показаны на фиг. 2.
Термин «РНК, которая содержит 5’-кэп» или «РНК, которая предусмотрена с 5’-кэпом», или «РНК, которая модифицирована 5’-кэпом», или «кэпированная РНК», относится к РНК, которая содержит 5’-кэп. Например, обеспечение РНК 5'-кэпом может быть достигнуто путем транскрипции in vitro матрицы ДНК в присутствии указанного 5'-кэпа, причем указанный 5'-кэп котранскрипционно встраивается в произведенную цепь РНК или РНК может быть получена, например, путем транскрипции in vitro, и 5'-кэп может быть присоединен к РНК после транскрипции с использованием кэпирующих ферментов, например, кэпирующих ферментов вируса осповакцины. В кэпированной РНК 3’-положение первого основания (кэпированной) молекулы РНК связано с 5’-положением последующего основания молекулы РНК («второе основание») через фосфодиэфирную связь. Для иллюстрации на фиг. 1 положение кэпа в молекулах нуклеиновых кислот согласно настоящему изобретению символизируется буквой С.
Термин «обычный 5’-кэп» относится к встречающемуся в природе 5’-кэпу, предпочтительно к 7-метилгуанозиновому кэпу. В 7-метилгуанозиновом кэпе гуанозин кэпа представляет собой модифицированный гуанозин, в котором модификация состоит из метилирования в 7-положении (вверху на фиг. 2).
В контексте настоящего изобретения термин «аналог 5’-кэпа» относится к молекулярной структуре, которая напоминает обычный 5’-кэп, но модифицирована, чтобы обладать способностью стабилизировать РНК, если она присоединена к ней, предпочтительно in vivo и/или в клетке. Аналог кэпа не представляет собой обычный 5’-кэп.
Настоящее изобретение отличается от систем транс-репликации предшествующего уровня техники тем, что трансляция репликазы управляется 5’-кэпом на репликазной конструкции. Авторы настоящего изобретения обнаружили, что конкретно 5’-кэп на репликазной конструкции оказывает очень положительное влияние не только на экспрессию репликазы, но и на производительность системы в целом: может быть достигнуто очень эффективное производство представляющего интерес гена, закодированного in trans (смотрите примеры). Согласно одному варианту осуществления репликазная конструкция по настоящему изобретению не содержит элемент участка внутренней посадки рибосомы (IRES).
В общем, участок внутренней посадки рибосомы, сокращенно IRES, представляет собой нуклеотидную последовательность, которая позволяет инициировать трансляцию из матричной РНК (мРНК) от положения, отличного от 5’-конца последовательности мРНК, такое как, например, положение в середине последовательности мРНК. Термины IRES и элемент IRES используются в настоящем документе взаимозаменяемо. Элементы IRES обнаруживаются у эукариот, а также у вирусов, способных инфицировать эукариотов. Однако механизм вирусной функции IRES на сегодняшний день лучше охарактеризован, чем механизм эукариотической функции IRES (López-Lastra et al., 2005, Biol. Res., vol. 38, pp. 121–146). Было предложено использовать IRES для управления экспрессией альфавирусной репликазы в эукариотических клетках (например, Sanz et al., Cellular Microbiol., 2015, vol. 17, pp. 520-541). Авторы настоящего изобретения показывают, что согласно различным вариантам осуществления эффективная генная экспрессия гена, кодируемого на транс-репликоне, может быть достигнута, когда репликазная конструкция не содержит IRES (смотрите примеры с 1 по 6). Таким образом, согласно одному варианту осуществления конструкция РНК для экспрессии альфавирусной репликазы (репликазная конструкция) не содержит элемент участка внутренней посадки рибосомы (IRES). Предпочтительно, трансляция репликазы не управляется элементом IRES. Известно, что уровни транслируемого белка, кодируемого в открытой рамке считывания ниже по ходу транскрипции от IRES, широко варьируют и зависят от типа и последовательности конкретных IRES и от деталей экспериментальной установки (представлено в Balvay et al., 2009, Biochim. Biophys. Acta, vol. 1789, pp. 542-557). В случае экспрессии гена из содержащей IRES РНК в предшествующем уровне техники было обнаружено, что экспрессия генов менее эффективна из больших транс-репликонов по сравнению с коротким транс-репликоном (Spuul et al., J. Virol., 2011, vol. 85, pp. 4739-4751) и что размер мембранных комплексов репликации, характерных для альфавирусной репликазы, зависит от длины транс-репликона (Kallio Kallio et al., 2013, J. Virol., vol. 87, pp. 9125-9134). Содержащие IRES РНК также транскрибировали in vitro и трансфицировали в клетки вместе с транс-репликонами (Sanz et al., Cellular Microbiol., 2015, vol. 17, pp. 520-541). Это исследование показало, что использование транскрибируемой in vitro содержащей IRES мРНК функционально для экспрессии репликазы в клетке и для опосредования репликации репликона in trans.
Подход настоящего изобретения значительно отличается от предшествующего уровня техники: Spuul с соавт., смотрите выше, предположили, что их РНК (полученная in situ в трансфицированных клетках) является некэпированной. Spuul с соавт. не предусматривали включения кэпа в некэпированную РНК: они выбрали альтернативный подход и включили элемент участка внутренней посадки рибосомы (IRES) ниже по ходу транскрипции от промотора T7; согласно этой ссылке, элемент IRES участвует в усилении экспрессии предположительно некэпированной РНК. Репликазная конструкция по настоящему изобретению также отличается от содержащейся IRES некэпированной транскрибируемой in vitro РНК, кодирующей nsP1-4, описанной Sanz с соавт., смотрите выше.
Замена IRES (как используется Sanz с соавт., выше, и Spuul с соавт., выше) 5’-кэпом в настоящем изобретении представляет собой конкретную модификацию молекулы РНК, которая не влияет на последовательность полипептида, который кодируется молекулой РНК (модификация, изменяющая неполипептид-кодирующие последовательности).
В принципе, любая кодирующая РНК поддается модификации, изменяющей неполипептид-кодирующие последовательности. В современной молекулярной биологии возможные эффекты модификаций, изменяющих неполипептид-кодирующие последовательности, например, на эффективность экспрессии генов, изучались в нескольких системах. Однако не было установлено общеприменимых правил относительно того, какой тип модификации, изменяющей неполипептид-кодирующие последовательности, следует выбирать для достижения эффективной экспрессии гена, например, улучшенной экспрессии гена по сравнению с немодифицированной последовательностью. Следовательно, выбор подходящей модификации, изменяющей неполипептид-кодирующие последовательности, для любой конкретной кодирующей нуклеиновой кислоты и/или любой конкретной системы экспрессии является сложной задачей. В настоящей области техники было описано множество различных модификаций, изменяющих неполипептид-кодирующие последовательности. Например, для эукариотических матричных РНК модификации, изменяющие неполипептид-кодирующие последовательности, которые были изучены, включают в себя выбор конкретных нетранслируемых областей (UTR, как описано, например, в публикации международной заявки WO 2013/143699 A1, WO 2013/143698 A1, Holtkamp et al., Blood, 2006, vol. 108, pp. 4009-4017), введение интрона, например, последовательности интрона II бета-глобина кролика (например, Li et al., J. Exp. Med., 1998, vol. 188, pp. 681-688) или молчащая модификация кодирующей последовательности, например, путем адаптации к преимущественному использованию кодонов клетки-хозяина или организма-хозяина без изменения кодированной последовательности полипептида (молчащая модификация, как правило, описываемая, например, в публикации международной заявки WO 2003/085114 A1). Насколько известно исследователям в настоящее время нет доступных систематических сравнительных исследований влияния различных модификаций, изменяющих неполипептид-кодирующие последовательности, в системах экспрессии на основе альфавируса.
В исследовании, проведенном для достижения настоящего изобретения, различные подходы, включающие в себя, например, модификации, изменяющие неполипептид-кодирующие последовательности, были тщательно исследованы, и в результате неожиданно было обнаружено, что, в частности, замена IRES на 5’-кэп на репликазной конструкции оказывает благотворное влияние in trans, то есть положительный эффект на уровне репликона in trans: производство представляющего интерес белка, закодированного репликоном в соответствии с настоящим изобретением, эффективно, когда кэп присутствует на репликазной конструкции. Это замечательно, особенно потому, что альтернативная модификация, изменяющая неполипептид-кодирующие последовательности, то есть адаптация модификации кодирующей последовательности, не улучшила работу системы по настоящему изобретению: напротив, эффективность производства представляющего интерес белка, закодированного репликоном, была даже уменьшена. Это проиллюстрировано в примере 4. Таким образом, для случая системы транс-репликации, основанной на альфавирусных РНК-элементах, включение 5’-кэпа в репликазную конструкцию представляет собой особенно предпочтительную модификацию, изменяющую неполипептид-кодирующую последовательность. Выводы настоящего изобретения также являются неожиданными с точки зрения публикации международной заявки WO 2008/119827 A1, в которой описано, что адаптированная по кодону репликаза вируса леса Семлики экспрессируется в трансфицированных клетках-хозяевах BHK-21, и в которой сделано заключение, что оптимизированная по кодону репликаза SFV является высокоактивной и способна усилить экспрессию репортерного гена in trans. Таким образом, направление публикации международной заявки WO 2008/119827 A1 отличается от настоящего изобретения, предполагая что альтернативная модификация, изменяющая неполипептид-кодирующую последовательность, то есть введение интрона в кодирующую последовательность репликазы, полезна для эффективной экспрессии репликазы.
Считается, что в эукариотической мРНК присутствие 5’-кэпа играет роль, в частности, в регулировании ядерного экспорта мРНК и в процессинге, в частности, в содействии иссечению 5'-проксимального интрона (Konarskaet al., 2014, Cell, vol. 38, pp. 731–736). Репликазную конструкцию по настоящему изобретению, как правило, не нужно ни экспортировать из ядра, ни подвергать процессингу. Тем не менее было неожиданно установлено, что наличие 5’-кэпа на репликазной конструкции является преимуществом.
В случае эукариотической мРНК 5’-кэп также, как правило, был описан как включенный в эффективную трансляцию мРНК: в целом у эукариот трансляция инициируется только на 5'-конце молекулы матричной РНК (мРНК), если IRES отсутствует. Эукариотические клетки способны обеспечить РНК 5’-кэпом во время транскрипции в ядре: вновь синтезированные мРНК, как правило, модифицируют с помощью структуры 5’-кэпа, например, когда транскрипт достигает длины от 20 до 30 нуклеотидов. Сначала 5'-концевой нуклеотид pppN (ppp, представляющий собой трифосфат, N, представляющий собой любой нуклеозид), превращается в клетке в 5' GpppN с помощью кэпирующего фермента, характеризующегося 5'-трифосфатазной и гуанилилтрансферазной активностью РНК. Затем GpppN может быть метилирован в клетке вторым ферментом с (гуанин-7)-метилтрансферазной активностью с образованием монометилированного кэпа m7GpppN. Согласно одному варианту осуществления 5’-кэп, используемый в настоящем изобретении, представляет собой природный 5’-кэп.
В настоящем изобретении природный 5’-кэп-динуклеотид, как правило, выбирают из группы, состоящей из неметилированного кэпа-динуклеотида (G(5')ppp(5')N, также называемого GpppN) и метилированного кэпа-динуклеотида ((m7G(5')ppp(5')N, также называемого m7GpppN). m7GpppN (где N представляет собой G) представлен следующей формулой:
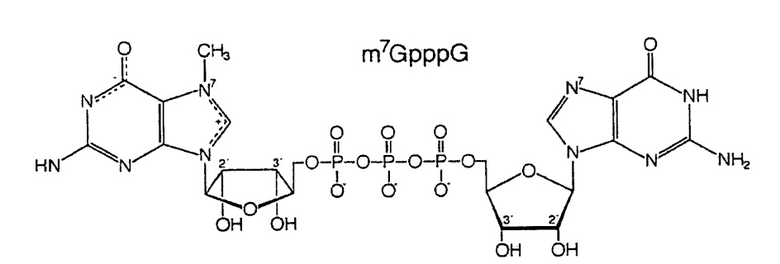
Репликазная конструкция по настоящему изобретению не зависит от кэпирующего инструмента в клетке-хозяине. Предполагается, что при трансфекции в клетку-хозяина репликазная конструкция по настоящему изобретению, как правило, не локализуется в ядре клетки, то есть на участке, где могло бы происходить кэпирование в типичных эукариотических клетках.
Не желая связывать себя теорией и по аналогии с IRES на конструкциях предшествующего уровня техники, можно предположить, что 5’-кэп на репликазной конструкции применим для запуска инициирования трансляции репликазы. Можно предположить, что эукариотический фактор инициации трансляции elF4E участвует в связывании кэпированной мРНК согласно настоящему изобретению с рибосомой. Авторы настоящего изобретения неожиданно обнаружили, что наличие 5’-кэпа значительно увеличивает производительность. Таким образом, репликазная конструкция по настоящему изобретению содержит 5’-кэп.
Наличие 5’-кэпа также обеспечивает неожиданные синергетические эффекты в системе транс-репликации по настоящему изобретению: как показано в примерах, кэпированные репликазные конструкции более эффективно запускают производство представляющего интерес белка, когда предусмотрена кэпированная репликазная конструкция in trans по отношению к РНК-репликону (смотрите, например, пример 1). Таким образом, в настоящем документе продемонстрирован синергический эффект 5’-кэпа и репликации in trans, то есть превосходящий репликацию in cis.
Кэпированная РНК по настоящему изобретению может быть получена in vitro и, следовательно, не зависит от инструмента кэпирования в клетке-хозяине. Наиболее часто используемый способ получения кэпированных РНК in vitro состоит в том, чтобы транскрибировать ДНК-матрицу либо с помощью бактериальной, либо с помощью бактериофаговой РНК-полимеразы в присутствии всех четырех рибонуклеозидтрифосфатов и кэпа-динуклеотида, такого как m7G(5')ppp(5')G (также называемого m7GpppG). РНК-полимераза инициирует транскрипцию с нуклеофильной атакой 3'-OH гуанозинового фрагмента m7GpppG на α-фосфате следующего матричного нуклеозидтрифосфата (pppN), в результате чего получают промежуточное m7GpppGpN (где N является вторым основанием молекулы РНК). Образование конкурирующего инициированного GTP продукта pppGpN подавляется путем установления молярного отношения кэпа к GTP от 5 до 10 при транскрипции in vitro.
Согласно предпочтительным вариантам осуществления настоящего изобретения 5’-кэп представляет собой аналог 5’-кэпа. Эти варианты осуществления особенно подходят, если РНК получена путем транскрипции in vitro, например, представляет собой транскрибированную in vitro РНК (IVT-РНК). Аналоги кэпа изначально описаны для облегчения синтеза высокоэффективных транскриптов РНК посредством транскрипции in vitro.
В отличие от ранее описанных сконструированных систем репликации альфавирусов (например, публикация международной заявки WO 2008/119827 A1, WO 2012/006376 A2), репликазная конструкция по настоящему изобретению предпочтительно содержит аналог кэпа. Таким образом, трансляция репликазы системы по настоящему изобретению предпочтительно управляется посредством аналога кэпа. В идеале выбирают аналог кэпа, который связан с более высокой эффективностью трансляции и/или повышенной устойчивостью к деградации in vivo и/или повышенной устойчивостью к деградации in vitro. Таким образом, в настоящем изобретении предусмотрен подход, который заметно отличается от известного уровня техники (публикация международной заявки WO 2012/006376 A2), который описывает конструкции экспрессии альфавирусов, которые предпочтительно не содержат каких-либо модифицированных нуклеотидов и которые содержат природный кэп (m7G(5')ppp(5')G, также называемый m7GpppG, который необязательно добавляют посредством коммерчески доступной системы кэпирования ScriptCap m7G (Epicenter Biotechnologies).
Для матричной РНК некоторые известные аналоги кэпа (синтетические структуры кэп), как правило, описаны на сегодняшний день, и все они могут использоваться в контексте настоящего изобретения. Предпочтительно используют аналог кэпа, который может быть включен только в цепь РНК в одной ориентации. В публикации Pasquinelli et al. (1995, RNA J., vol., 1, pp. 957-967) показано, что во время транскрипции in vitro бактериофаговые РНК-полимеразы используют блок 7-метилгуанозина для инициирования транскрипции, при этом приблизительно 40-50% транскриптов с кэпом обладают кэпом-динуклеотидом в обратной ориентации (т.е. исходный продукт реакции представляет собой Gpppm7GpN). По сравнению с РНК с правильным кэпом, РНК с обратным кэпом не являются функциональными по отношению к трансляции кодированных белков. Таким образом, желательно включить кэп в правильной ориентации, то есть в результате получить РНК со структурой, по существу соответствующей m7GpppGpN и т.д. Было показано, что обратное интегрирование кэпа-динуклеотида ингибируется заменой либо 2'-, либо 3'-OH группы метилированного гуанозина (Stepinski et al., 2001; RNA J., vol. 7, pp. 1486-1495; Peng et al., 2002; Org. Lett., vol. 24, pp. 161-164). РНК, которые синтезируются в присутствии таких «аналогов кэп-структур с правильной ориентацией», транслируются более эффективно, чем РНК, которые транскрибируются in vitro в присутствии обычного 5’-кэпа m7GpppG. С этой целью один аналог кэпа, в котором группа 3’-OH метилированного гуанозина замещена OCH3, описан в публикации Holtkamp et al., 2006, Blood, vol. 108, pp. 4009-4017 (7-метил(3’-O-метил) GpppG, аналог кэп-структуры с правильной ориентацией (ARCA)). ARCA является подходящим кэпом-динуклеотидом в соответствии с настоящим изобретением.
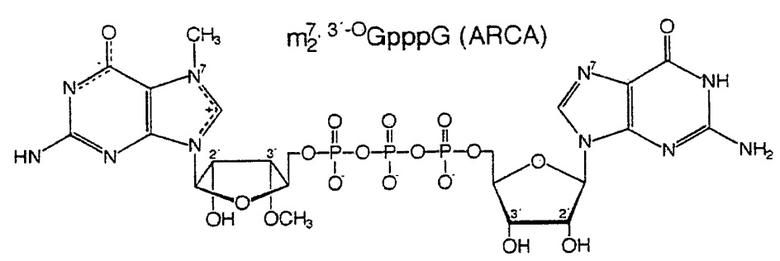
Согласно предпочтительному варианту осуществления настоящего изобретения РНК по настоящему изобретению по существу не подвержена декэпированию. Это важно, потому что в целом количество белка, полученного из синтетических мРНК, вводимых в культивируемые клетки млекопитающих, ограничено естественной деградацией мРНК. Один из путей in vivo для деградации мРНК начинается с удаления кэпа мРНК. Это удаление катализируется гетеродимерной пирофосфатазой, которая содержит регуляторную субъединицу (Dcp1) и каталитическую субъединицу (Dcp2). Каталитическая субъединица расщепляется между α- и β-фосфатными группами трифосфатного мостика. В настоящем изобретении может быть выбран или может присутствовать аналог кэпа, который не восприимчив или менее восприимчив к этому типу расщепления. Соответствующий аналог кэпа для этой цели может быть выбран из кэпа-динуклеотида согласно формуле (I):
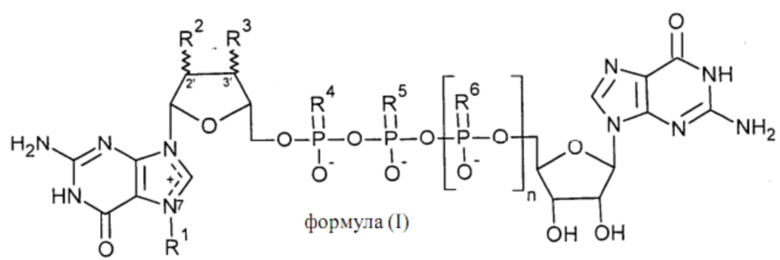
где R1 выбран из группы, содержащей необязательно замещенный алкил, необязательно замещенный алкенил, необязательно замещенный алкинил, необязательно замещенный циклоалкил, необязательно замещенный гетероциклил, необязательно замещенный арил и необязательно замещенный гетероарил,
R2 и R3 независимо выбраны из группы, состоящей из H, галогена, ОН и необязательно замещенного алкокси, или R2 и R3 вместе образуют O-X-O, где X выбран из группы, состоящей из необязательно замещенных CH2, CH2CH2, CH2CH2CH2, CH2CH(CH3) и C(CH3)2, или R2 объединяют с атомом водорода в положении 4' кольца, к которому присоединен R2, с образованием -O-CH2- или -CH2-O-,
R5 выбран из группы, состоящей из S, Se и BH3,
R4 и R6 независимо выбраны из группы, состоящей из O, S, Se и BH3,
а также
n равно 1, 2 или 3.
Предпочтительные варианты осуществления для R1, R2, R3, R4, R5, R6 раскрыты в публикации международной заявки WO 2011/015347 A1 и могут быть соответственно выбраны в настоящем изобретении. Согласно одному варианту осуществления настоящего изобретения R1 представляет собой метил и R2 и R3 независимо представляют собой гидрокси или метокси.
Например, согласно предпочтительному варианту осуществления настоящего изобретения РНК по настоящему изобретению содержит фосфоротиоатный аналог кэпа. Фосфоротиоатные аналоги кэпа представляют собой специфические аналоги кэпа, в которых один из трех немостиковых атомов O в трифосфатной цепи замещен атомом S, то есть один из R4, R5 или R6 в формуле (I) представляет собой S. Фосфоротиоатные аналоги кэпа были описаны в публикации J. Kowalska et al., 2008, RNA, vol. 14, pp. 1119-1131, в качестве решения нежелательного процесса декэпирования и, таким образом, для повышения стабильности РНК in vivo. В частности, замена атома кислорода атомом серы в бета-фосфатной группе 5'-кэпа приводит к стабилизации против Dcp2. Согласно этому варианту осуществления, который является предпочтительным в настоящем изобретении, R5 в формуле (I) представляет собой S, а R4 и R6 представляют собой O.
Согласно еще одному предпочтительному варианту осуществления настоящего изобретения РНК по настоящему изобретению содержит фосфоротиоатный аналог кэпа, в котором фосфоротиоатная модификация 5'-кэпа РНК сочетается с модификацией в виде «аналога кэп-структуры с правильной ориентацией» (ARCA). Соответствующие фосфоротиоатные аналоги ARCA-кэпа описаны в публикации международной заявки WO 2008/157688 A2, и все они могут быть использованы в РНК по настоящему изобретению. Согласно этому варианту осуществления по меньшей мере один из R2 или R3 в формуле (I) не представляет собой OH, предпочтительно один из R2 и R3 представляет собой метокси (OCH3), а другой из R2 и R3 предпочтительно представляет собой ОН. Согласно предпочтительному варианту осуществления атом кислорода заменен атомом серы в бета-фосфатной группе (так что R5 в формуле (I) представляет собой S, а R4 и R6 представляют собой O). Считается, что фосфоротиоатная модификация ARCA гарантирует, что α, β и γ фосфатные и фосфоротиоатные группы точно расположены в активных сайтах связывающих кэп белков в обоих трансляционных и декэпирующих инструментах. По меньшей мере некоторые из этих аналогов по существу устойчивы к пирофосфатазе Dcp1/Dcp2. Было описано, что модифицированные фосфоротиоатом ARCA имеют гораздо более высокое сродство к eIF4E, чем соответствующие ARCA, лишенные фосфоротиоатной группы.
Соответствующий аналог кэпа, который является особенно предпочтительным в настоящем изобретении, т.е. m2’7,2’-OGppspG, называется бета-S-ARCA (публикация международной заявки WO 2008/157688 A2; Kuhn et al., Gene Ther., 2010, vol. 17, pp. 961-971). Таким образом, согласно одному варианту осуществления настоящего изобретения репликазная конструкция по настоящему изобретению модифицирована бета-S-ARCA. Бета-S-ARCA представлен следующей структурой:
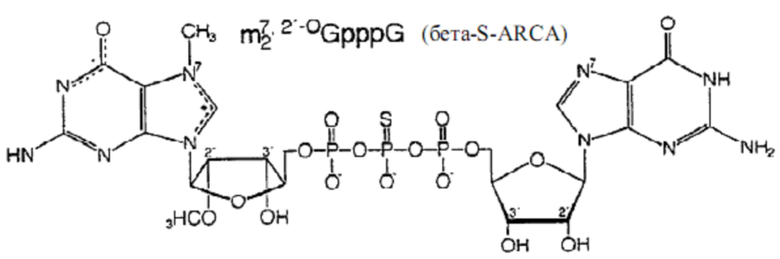
В общем случае замещение атома кислорода атомом серы в мостиковом фосфате приводит к образованию фосфоротиоатных диастереомеров, обозначенных D1 и D2, в соответствии с их профилем элюирования в ВЭЖХ. Вкратце, диастереомер D1 «бета-S-ARCA» или «бета-S-ARCA(D1)» представляет собой диастереомер бета-S-ARCA, который элюирует первым на колонке ВЭЖХ по сравнению с диастереомером D2 бета-S-ARCA (бета-S-ARCA(D2)) и, таким образом, проявляет более короткое время удерживания. Определение стереохимической конфигурации с помощью ВЭЖХ описано в публикации международной заявки WO 2011/015347 A1.
Согласно первому особенно предпочтительному варианту осуществления настоящего изобретения репликазная конструкция по настоящему изобретению модифицирована диастереомером бета-S-ARCA(D2). Два диастереомера бета-S-ARCA отличаются чувствительностью к нуклеазам. Было показано, что РНК, несущая диастереомер D2 бета-S-ARCA, практически полностью устойчива к расщеплению Dcp2 (всего лишь 6% расщепления по сравнению с РНК, которая была синтезирована в присутствии немодифицированного 5'-кэпа ARCA), тогда как РНК с 5'-кэпом бета-S-ARCA(D1) обладает промежуточной чувствительностью к расщеплению Dcp2 (расщепление 71%). Дополнительно было показано, что повышенная устойчивость к расщеплению Dcp2 коррелирует с повышенной экспрессией белка в клетках млекопитающих. В частности, было показано, что РНК, несущие кэп бета-S-ARCA(D2), более эффективно транслируются в клетках, чем РНК, несущие кэп бета-S-ARCA(D1). Поэтому согласно одному варианту осуществления настоящего изобретения репликазная конструкция по настоящему изобретению модифицирована с помощью аналога кэпа согласно формуле (I), характеризующегося стереохимической конфигурацией на атоме Р, содержащего заместитель R5 в формуле (I), который соответствует таковому у атома Pβ диастереомера D2 бета-S-ARCA. Согласно этому варианту осуществления R5 в формуле (I) представляет собой S, а и R4 и R6 представляют собой O. Кроме того, по меньшей мере один из R2 или R3 в формуле (I) предпочтительно не является OH, предпочтительно один из R2 и R3 представляет собой метокси (OCH3), а другой из R2 и R3 предпочтительно представляет собой ОН.
Согласно второму особенно предпочтительному варианту осуществления репликазная конструкция по настоящему изобретению модифицирована диастереомером бета-S-ARCA(D1). Этот вариант осуществления особенно подходит для переноса кэпированной РНК в незрелые антигенпрезентирующие клетки, например, в целях вакцинации. Было продемонстрировано, что диастереомер бета-S-ARCA(D1) при переносе соответственно кэпированной РНК в незрелые антигенпрезентирующие клетки особенно подходит для повышения стабильности РНК, повышения эффективности трансляции РНК, продления трансляции РНК, повышения общей белковой экспрессии РНК и/или повышения иммунного ответа против антигена или антигенного пептида, кодируемого указанной РНК (Kuhn et al., 2010, Gene Ther., Vol. 17, pp. 961-971). Следовательно, согласно альтернативному варианту осуществления настоящего изобретения репликазная конструкция по настоящему изобретению модифицирована с помощью аналога кэпа согласно формуле (I), характеризующегося стереохимической конфигурацией у атома Р, содержащего заместитель R5 в формуле (I), который соответствует таковому у атома Pβ диастереомера D1 бета-S-ARCA. Соответствующие аналоги и варианты их осуществления описаны в публикации международной заявки WO 2011/015347 A1 и в публикации Kuhn et al., 2010, Gene Ther., vol. 17, pp. 961-971. Любой аналог кэпа, описанный в публикации международной заявки WO 2011/015347 A1, в котором стереохимическая конфигурация у атома P, включающая заместитель R5, соответствует таковому у атома Pβ диастереомера D1 бета-S-ARCA, может быть использован в настоящем изобретении. Предпочтительно R5 в формуле (I) представляет собой S, а R4 и R6 представляют собой O. Кроме того, по меньшей мере один из R2 или R3 в формуле (I) предпочтительно не представляет собой OH, предпочтительно один из R2 и R3 представляет собой метокси (OCH3), а другой из R2 и R3 предпочтительно представляет собой ОН.
Согласно одному варианту осуществления репликазная конструкция по настоящему изобретению модифицирована структурой 5'-кэп в соответствии с формулой (I), причем любая фосфатная группа замещена боранофосфатной группой или фосфороселеноатной группой. Такие структуры кэп повышают стабильность как in vitro, так и in vivo. Необязательно, соответствующее соединение содержит 2'-O- или 3'-O-алкильную группу (где алкил предпочтительно представляет собой метил); соответствующие аналоги структуры кэп называются BH3-ARCA или Se-ARCA. Соединения, которые особенно подходят для кэпирования мРНК, включают в себя β-BH3-ARCA и β-Se-ARCA, как описано в публикации международной заявки WO 2009/149253 A2. Для этих соединений предпочтительной является стереохимическая конфигурация у атома Р, содержащая заместитель R5 в формуле (I), который соответствует таковому у атома Pβ диастереомера D1 бета-S-ARCA.
UTR
Термин «нетранслируемая область» или «UTR» относится к области, которая транскрибируется, но не транслируется в аминокислотную последовательность, или к соответствующей области в молекуле РНК, такой как молекула мРНК. 3’-UTR, если она присутствует, расположена на 3'-конце гена ниже по ходу транскрипции от кодона терминации кодирующей белок области, но термин «3’-UTR» предпочтительно не включает в себя поли(А)-хвост. Таким образом, 3’-UTR находится выше против хода транскрипции от поли(А)-хвоста (если он присутствует), например, непосредственно примыкая к поли(А)-хвосту.
5’-UTR, если присутствует, расположена на 5'-конце гена, выше против хода транскрипции от стартового кодона кодирующей белок области. 5’-UTR находится ниже по ходу транскрипции от 5’-кэпа (если он присутствует), например, непосредственно примыкая к 5’-кэпу.
5'- и/или 3'-нетранслируемые области могут, в соответствии с настоящим изобретением, быть функционально связаны с открытой рамкой считывания для того, чтобы эти области были связаны с открытой рамкой считывания таким образом, чтобы увеличивать стабильность и/или эффективность трансляции РНК, содержащей указанную открытую рамку считывания.
Нетранслируемая область (UTR) может присутствовать 5’ (выше против хода транскрипции) от открытой рамки считывания, кодирующей репликазу (5’-UTR), и/или 3’ (ниже по ходу транскрипции) от открытой рамки считывания, кодирующей репликазу (3’-UTR). Согласно предпочтительному варианту осуществления конструкция РНК для экспрессии альфавирусной репликазы (репликазная конструкция) содержит
(1) 5' UTR,
(2) открытую рамку считывания, кодирующую репликазу, и
(3) 3' UTR.
В частности, согласно варианту осуществления репликазной конструкции по настоящему изобретению термин «3'-UTR» относится к области, которая расположена 3' от кодирующей области для репликазы, а термин «5'-UTR» относится к области которая расположена 5' от кодирующей области для репликазы.
UTR участвуют в стабильности и эффективности трансляции РНК, что является предпосылкой эффективного иммунного ответа с использованием вакцин на основе РНК. И то и то может быть улучшено, помимо структурных модификаций, касающихся 5’-кэпа и/или 3’ поли(А)-хвоста, как описано в настоящем документе, путем выбора специфических 5’ и/или 3’ нетранслируемых областей (UTR). Как правило, элементы последовательности в UTR влияют на эффективность трансляции (в основном, 5’-UTR) и стабильность РНК (в основном 3’-UTR). Предпочтительно, чтобы присутствовала 5’-UTR, которая активна для повышения эффективности трансляции и/или стабильности последовательности нуклеиновой кислоты. Независимо или дополнительно предпочтительно, чтобы присутствовала 3’-UTR, которая активна для повышения эффективности трансляции и/или стабильности последовательности нуклеиновой кислоты.
Термин «последовательность нуклеиновой кислоты, которая активна для повышения эффективности трансляции и/или стабильности последовательности нуклеиновой кислоты» применительно к первой последовательности нуклеиновой кислоты (например, UTR), означает, что первая последовательность нуклеиновой кислоты способна к модификации в общем транскрипте со второй последовательностью нуклеиновой кислоты, влияя на эффективность трансляции и/или стабильность указанной второй последовательности нуклеиновой кислоты таким образом, что эффективность трансляции и/или стабильность трансляции увеличивается по сравнению с эффективностью трансляции и/или стабильностью указанной второй последовательности нуклеиновой кислоты в отсутствие указанной первой последовательности нуклеиновой кислоты. В этом контексте термин «эффективность трансляции» относится к количеству продукта трансляции, предоставленному молекулой РНК в течение определенного периода времени, а термин «стабильность» относится к периоду полужизни молекулы РНК.
Предпочтительно, репликазная конструкция содержит 5'-UTR и/или 3'-UTR, которая является гетерологичной или ненативной для альфавируса, из которого получена репликаза. Это позволяет создавать нетранслируемые области в соответствии с требуемой эффективностью трансляции и стабильностью РНК. Таким образом, гетерологичные или ненативные UTR обеспечивают высокую степень гибкости, и эта гибкость является предпочтительной по сравнению с нативными альфавирусными UTR. В частности, хотя известно, что альфавирусная (нативная) РНК также содержит 5' UTR и/или 3' UTR, альфавирусные UTR выполняют двойную функцию, то есть (i) для управления репликацией РНК, а также (ii) для управления трансляцией. В то время как сообщалось, что альфавирусные UTR были неэффективны для трансляции (Berben-Bloemheuvel et al., 1992, Eur. J. Biochem., vol. 208, pp. 581-587), они не могут быть легко заменены более эффективными UTR из-за их двойной функции. Однако в настоящем изобретении 5’-UTR и/или 3’-UTR репликазной конструкции могут быть выбраны независимо от их потенциального влияния на репликацию РНК.
Предпочтительно, репликазная конструкция содержит 5’-UTR и/или 3’-UTR, которая происходит не от вирусов; в особенности не от альфавирусов. Согласно одному варианту осуществления РНК содержит 5’-UTR, полученную из эукариотической 5’-UTR, и/или 3’-UTR, полученную из эукариотической 3’-UTR.
5’-UTR в соответствии с настоящим изобретением может содержать любую комбинацию из более чем одной последовательности нуклеиновой кислоты, необязательно разделенной линкером. 3’-UTR в соответствии с настоящим изобретением может содержать любую комбинацию из более чем одной последовательности нуклеиновой кислоты, необязательно разделенной линкером.
Термин «линкер» в соответствии с настоящим изобретением относится к последовательности нуклеиновой кислоты, добавляемой между двумя последовательностями нуклеиновой кислоты для соединения указанных двух последовательностей нуклеиновой кислоты. Нет никаких особых ограничений относительно последовательности линкера.
3’-UTR, как правило, составляет в длину от 200 до 2000 нуклеотидов, например, от 500 до 1500 нуклеотидов. 3'-нетранслируемые области мРНК иммуноглобулина относительно короткие (менее 300 нуклеотидов), тогда как 3'-нетранслируемые области других генов относительно длинные. Например, 3'-нетранслируемая область tPA составляет в длину приблизительно 800 нуклеотидов, а фактор VIII составляет в длину приблизительно 1800 нуклеотидов, а длина эритропоэтина составляет приблизительно 560 нуклеотидов.
3'-нетранслируемые области мРНК млекопитающих, как правило, содержат область гомологии, известную как гексануклеотидная последовательность AAUAAA. Эта последовательность, по-видимому, представляет собой сигнал присоединения поли(A) и часто находится на расстоянии от 10 до 30 оснований выше против хода транскрипции от сайта связывания поли(A).
3'-нетранслируемые области могут содержать один или несколько инвертированных повторов, которые могут складываться, чтобы создавать структуры «петля-на-стебле», которые действуют как барьеры для экзорибонуклеаз или взаимодействуют с белками, известными, как повышающие стабильность РНК (например, РНК-связывающими белками).
3'-UTR бета-глобина человека, особенно две последовательные идентичные копии 3'-UTR бета-глобина человека, способствует высокой стабильности транскрипции и эффективности трансляции (Holtkamp et al., 2006, Blood, vol. 108, pp. 4009-4017). Таким образом, согласно варианту осуществления репликазная конструкция по настоящему изобретению содержит две последовательные идентичные копии 3'-UTR бета-глобина человека. Таким образом, она содержит в направлении 5'→3': (а) необязательно 5’-UTR; (b) открытую рамку считывания, кодирующую репликазу; (c) 3’-UTR; указанная 3'-UTR содержит две последовательные идентичные копии 3’-UTR бета-глобина человека, ее фрагмент или вариант 3’-UTR бета-глобина человека или ее фрагмент.
Согласно одному варианту осуществления репликазная конструкция по настоящему изобретению содержит 3’-UTR, которая активна для повышения эффективности трансляции и/или стабильности репликазной конструкции, но которая не представляет собой 3’-UTR бета-глобина человека, ее фрагмент или вариант 3’-UTR бета-глобина человека или ее фрагмента.
Согласно одному варианту осуществления репликазная конструкция по настоящему изобретению содержит 5’-UTR, которая активна для повышения эффективности трансляции и/или стабильности репликазной конструкции.
UTR-содержащую РНК согласно настоящему изобретению можно получить, например, посредством транскрипции in vitro. Это может быть достигнуто путем генетической модификации экспрессии молекул нуклеиновых кислот по настоящему изобретению (например, ДНК) таким образом, что они позволяют транскрипцию РНК с 5’-UTR и/или 3’-UTR.
Поли(A)-последовательность
Согласно одному варианту осуществления конструкция РНК для экспрессии альфавирусной репликазы (репликазная конструкция) содержит 3' поли(А)-последовательность.
В альфавирусах считается, что 3' поли(А)-последовательность по меньшей мере из 11 последовательных аденилатных остатков или по меньшей мере из 25 последовательных аденилатных остатков важна для эффективного синтеза минусовой нити. В частности, понятно, что в альфавирусах 3' поли(А)-последовательность по меньшей мере из 25 последовательных аденилатных остатков функционирует вместе с консервативным элементом последовательности 4 (CSE 4) для содействия синтезу (-)-нити (Hardy & Rice, J. Virol., 2005, vol. 79, pp. 4630-4639). В настоящем изобретении, однако, синтез (-)-нити репликазной конструкции, как правило, не желателен, и поли(А)-последовательность в основном выполняет функции влияния на стабильность РНК и трансляцию белка в трансфицированных эукариотических клетках. Действительно, было продемонстрировано, что 3' поли(А)-последовательность приблизительно из 120 нуклеотидов А оказывает благотворное влияние на уровни РНК в трансфицированных эукариотических клетках, а также на уровни белка, который транслируется из открытой рамки считывания (5’) 3' поли(А)-последовательности (Holtkamp et al., 2006, Blood, vol. 108, pp. 4009-4017). В соответствии с настоящим изобретением согласно одному варианту осуществления поли(А)-последовательность содержит или по существу состоит, или состоит по меньшей мере из 20, предпочтительно по меньшей мере из 26, предпочтительно по меньшей мере из 40, предпочтительно по меньшей мере из 80, предпочтительно по меньшей мере из 100 и содержит предпочтительно до 500, предпочтительно до 400, предпочтительно до 300, предпочтительно до 200 и, в частности, до 150, нуклеотидов А и, в частности, приблизительно 120 нуклеотидов А. В этом контексте «по существу состоит из» означает, что большинство нуклеотидов в поли(А)-последовательности, как правило, по меньшей мере на 50% и предпочтительно по меньшей мере на 75% по количеству нуклеотидов в «поли(А)-последовательности» представляют собой нуклеотиды А, но позволено, чтобы оставшиеся нуклеотиды были нуклеотидами, отличными от нуклеотидов А, такими как нуклеотиды U (уридилат), нуклеотиды G (гуанилат), нуклеотиды C (цитидилат). В этом контексте «состоит из» означает, что все нуклеотиды в поли(А)-последовательности, то есть 100% по количеству нуклеотидов в поли(А)-последовательности, являются нуклеотидами А. Термин «нуклеотид А» или «А» относится к аденилату.
В настоящем изобретении предусмотрена 3’ поли(А)-последовательность, которая должна быть присоединена во время транскрипции РНК, то есть во время получения транскрибируемой РНК in vitro на основе ДНК-матрицы, содержащей повторяющиеся нуклеотиды dT (дезокситимидилат) в цепи, комплементарной кодирующей цепи. Последовательность ДНК, кодирующая поли(А)-последовательность (кодирующая цепь), называется поли(А)-кассетой.
Согласно предпочтительному варианту осуществления настоящего изобретения 3' поли(А)-кассета, присутствующая в кодирующей цепи ДНК, по существу состоит из нуклеотидов dA, но прерывается случайной последовательностью, имеющей равное распределение четырех нуклеотидов (dA, dC, dG, dT). Такая случайная последовательность может составлять от 5 до 50, предпочтительно от 10 до 30, более предпочтительно от 10 до 20 нуклеотидов. Такая кассета раскрыта в публикации международной заявки WO 2016/005004 A1. В настоящем изобретении может быть использована любая поли(А)-кассета, раскрытая в публикации международной заявки WO 2016/005004 A1. Поли(А)-кассета, которая по существу состоит из нуклеотидов dA, но прерывается случайной последовательностью, характеризующейся равным распределением четырех нуклеотидов (dA, dC, dG, dT) и составляющая в длину, например, от 5 до 50 нуклеотидов на уровне ДНК, показывает, на уровне ДНК, постоянное воспроизведение плазмидной ДНК в E.coli и по-прежнему связана, на уровне РНК, с полезными свойствами в отношении поддержания стабильности РНК и эффективности трансляции.
Следовательно, согласно предпочтительному варианту осуществления настоящего изобретения 3' поли(А)-последовательность, содержащаяся в молекуле РНК, описанной в настоящем документе, по существу состоит из нуклеотидов А, но прерывается случайной последовательностью, характеризующейся равным распределением четырех нуклеотидов (А, C, G, U). Такая случайная последовательность может составлять от 5 до 50, предпочтительно от 10 до 30, более предпочтительно от 10 до 20 нуклеотидов.
Использование кодонов
В общем, вырожденность генетического кода сделает возможным замену некоторых кодонов (триплеты оснований), которые присутствуют в последовательности РНК другими кодонами (триплетами оснований), сохраняя при этом ту же самую способность кодирования. Согласно некоторым вариантам осуществления настоящего изобретения по меньшей мере один кодон открытой рамки считывания, состоящий из молекулы РНК, отличается от соответствующего кодона в соответствующей открытой рамке считывания у видов, из которых происходит открытая рамка считывания. Согласно этому варианту осуществления кодирующая последовательность открытой рамки считывания называется «адаптированной».
Например, когда кодирующая последовательность открытой рамки считывания адаптирована, могут быть выбраны часто используемые кодоны: в публикации международной заявки WO 2009/024567 A1 описана адаптация кодирующей последовательности молекулы нуклеиновой кислоты с заменой редких кодонов более часто используемыми кодонами. Поскольку частота использования кодонов зависит от клетки-хозяина или организма-хозяина, этот тип адаптации подходит для подгонки последовательности нуклеиновой кислоты для экспрессии в конкретной клетке-хозяине или организме-хозяине. В общем случае, чаще используемые кодоны, как правило, более эффективно транслируются в клетке-хозяине или в организме-хозяине, хотя адаптация всех кодонов открытой рамки считывания не всегда требуется.
Например, когда кодирующая последовательность открытой рамки считывания адаптирована, содержание остатков G (гуанилата) и остатков C (цитидилата) может быть изменено путем выбора кодонов с наибольшим богатым на GC содержанием для каждой аминокислоты. Сообщалось, что молекулы РНК с богатыми на GC открытыми рамками считывания характеризуются потенциалом для снижения иммунной активации и улучшения трансляции и полужизни РНК (Thess et al., 2015, Mol. Ther., 23, 1457-1465).
Открытая рамка считывания, кодирующая репликазу в соответствии с настоящим изобретением, может быть адаптирована соответственно.
Характеристика репликона
Система по настоящему изобретению содержит репликон. Конструкция нуклеиновой кислоты, которая может быть реплицирована репликазой, предпочтительно альфавирусной репликазой, называется репликоном. Как правило, репликон в соответствии с настоящим изобретением представляет собой молекулу РНК.
Согласно настоящему изобретению термин «репликон» определяет молекулу РНК, которая может быть реплицирована РНК-зависимой РНК-полимеразой, получая, без промежуточной ДНК, одну или несколько идентичных или по существу идентичных копий репликона РНК. «Без промежуточной ДНК» означает, что в процессе образования копий РНК-репликона не образуется копия или комплемент дезоксирибонуклеиновой кислоты (ДНК) репликона и/или что молекула дезоксирибонуклеиновой кислоты (ДНК) не используется в качестве матрицы в процессе образования копий РНК-репликона или их комплемента.
Согласно настоящему изобретению термин «может быть реплицирована», как правило, описывает, что можно получить одну или несколько идентичных или по существу идентичных копий нуклеиновой кислоты. При использовании вместе с термином «репликаза», например, «может быть реплицирована репликазой», термин «может быть реплицирована» описывает функциональные характеристики репликона по отношению к репликазе. Эти функциональные характеристики предусматривают по меньшей мере одно из следующего: (i) репликаза способна распознавать репликон и (ii) репликаза способна действовать как РНК-зависимая РНК-полимераза (RdRP). Предпочтительно, репликаза способна как (i) распознавать репликон, так и (ii) действовать как РНК-зависимая РНК-полимераза. РНК-зависимая РНК-полимераза может использовать репликон, его комплемент или часть любого из них в качестве матрицы.
Выражение «способна распознавать» описывает, что репликаза способна физически связываться с репликоном, и предпочтительно, что репликаза способна связываться с репликоном, как правило, нековалентно. Термин «связывание» может означать, что репликаза обладает способностью связываться с любым одним или несколькими из следующего: консервативный элемент последовательности 1 (CSE 1) или его комплементарная последовательность (если составлена репликоном), консервативный элемент последовательности 2 (CSE 2) или его комплементарная последовательность (если составлена репликоном), консервативный элемент последовательности 3 (CSE 3) или его комплементарная последовательность (если составлена репликоном), консервативный элемент последовательности 4 (CSE 4) или его комплементарная последовательность (если составлена репликоном). Предпочтительно репликаза способна связываться с CSE 2 [т.е. с (+)-нитью] и/или с CSE 4 [т.е. с (+)-нитью] или связываться с комплементом CSE 1 [т.е. с (-)-нитью] и/или с комплементом CSE 3 [т.е. с (-)-нитью].
Выражение «способна действовать как RdRP» включает в себя то значение, что репликаза способна катализировать синтез (-)-нитевого комплемента альфавирусной геномной (+)-нити РНК, причем (+)-нить РНК характеризуется функцией матрицы, и/или что репликаза способна катализировать синтез (+)-нити альфавирусной геномной РНК, причем (-)-нить РНК характеризуется функцией матрицы. В общем, выражение «способна действовать как RdRP» также может включать в себя то, что репликаза способна катализировать синтез субгеномного транскрипта (+)-нити, причем (-)-нить РНК характеризуется функцией матрицы и причем синтез субгеномного транскрипта (+)-нити, как правило, инициируют в субгеномном промоторе альфавируса.
Выражения «способны связываться» и «способны действовать как RdRP» относятся к способности в нормальных физиологических условиях. В частности, выражения относятся к условиям внутри клетки, которая экспрессирует альфавирусную репликазу или которая трансфицирована нуклеиновой кислотой, которая кодирует альфавирусную репликазу. Клетка предпочтительно представляет собой эукариотическую клетку. Способность связываться и/или способность действовать как RdRP может быть экспериментально испытана, например, в бесклеточной системе in vitro или в эукариотической клетке. Необязательно указанная эукариотическая клетка представляет собой клетку от вида, к которому конкретный альфавирус, от которого происходит репликаза, характеризуется инфекционностью. Например, когда используется альфавирусная репликаза из конкретного альфавируса, который является инфекционным для человека, нормальные физиологические условия представляют собой условия в клетке человека. Более предпочтительно, эукариотическая клетка (в одном примере человеческая клетка) происходит из той же ткани или органа, к которой конкретный альфавирус, от которого происходит репликаза, характеризуется инфекционностью.
Ввиду этих функциональных характеристик репликон по настоящему изобретению и репликазная конструкция по настоящему изобретению образуют функциональную пару. Альфавирусная репликаза может представлять собой любую альфавирусную репликазу в соответствии с настоящим изобретением, и нуклеотидная последовательность РНК-репликона особо не ограничена, если репликон может быть реплицирован альфавирусной репликазой in trans.
Когда система по настоящему изобретению вводится в клетку, предпочтительно эукариотическую клетку, репликаза, закодированная в репликазной конструкции, может быть транслирована, тем самым производя фермент репликазу. После трансляции репликаза способна реплицировать репликон РНК in trans. Таким образом, в настоящем изобретении предусмотрена система для репликации РНК in trans. Следовательно, система по настоящему изобретению представляет собой систему транс-репликации. Таким образом, репликон в соответствии с настоящим изобретением представляет собой транс-репликон.
В настоящем документе транс (например, в контексте транс-действующего, транс-регуляторного), в общем, означает «действие из другой молекулы» (то есть межмолекулярное). Это противоположно цис (например, в контексте цис-действующего, цис-регуляторного), что, в общем, означает «действующий из той же молекулы» (то есть внутримолекулярный). В контексте синтеза РНК (включая в себя транскрипцию и репликацию РНК) транс-действующий элемент включает в себя последовательность нуклеиновой кислоты, которая содержит ген, кодирующий фермент, способный синтезировать РНК (репликаза). Репликаза функционирует в синтезе второй молекулы нуклеиновой кислоты, то есть другой молекулы. Говорят, что как транс-действующая РНК, так и белок, которые она кодирует, «действуют in trans» на целевой ген. В контексте настоящего изобретения транс-действующая РНК кодирует альфавирусную РНК-полимеразу. Альфавирусная РНК-полимераза способна реплицировать РНК и поэтому называется репликазой. Репликаза действует in trans на вторую молекулу РНК (репликон). Репликон, который может быть реплицирован репликазой in trans в соответствии с настоящим изобретением, синонимично упоминается в настоящем документе как «транс-репликон» или «репликон в соответствии с настоящим изобретением».
Тот факт, что альфавирусная репликаза, как правило, способна распознавать и реплицировать РНК-матрицу in trans, была первоначально обнаружена в 1980-х годах, но потенциал транс-репликации для биомедицинских применений не был признан, в частности, поскольку транс-реплицированная РНК считалась ингибирующей эффективную репликацию: она была обнаружена в случае дефектной интерферирующей (DI) РНК, которая совместно реплицирует альфавирусные геномы в инфицированных клетках (Barrett et al., 1984, J. Gen. Virol., vol. 65 ( Pt 8), pp. 1273-1283; Lehtovaara et al., 1981, Proc. Natl. Acad. Sci. U. S. A, vol. 78, pp. 5353-5357; Pettersson, 1981, Proc. Natl. Acad. Sci. U. S. A, vol. 78, pp. 115-119). DI РНК представляют собой транс-репликоны, которые могут происходить квази-естественным образом во время инфекций клеточных линий с высокой вирусной нагрузкой. DI-элементы кореплицируются настолько эффективно, что они уменьшают вирулентность родительского вируса и, таким образом, действуют как ингибирующая паразитная РНК (Barrett et al., 1984, J. Gen. Virol., Vol. 65 (Pt 11), pp. 1909- 1920). Хотя потенциал для биомедицинских применений не был распознан, феномен транс-репликации использовался в нескольких базовых исследованиях, направленных на выяснение механизмов репликации без необходимости экспрессировать репликазу из той же молекулы in cis; кроме того, разделение репликазы и репликона также позволяет проводить функциональные исследования с участием мутантов вирусных белков, даже если соответствующие мутанты представляют собой мутанты с потерями функциональности (Lemm et al., 1994, EMBO J., vol. 13, pp. 2925-2934). Эти исследования потери функции и DI РНК не предполагали, что системы транс-активации, основанные на альфавирусных элементах, могут в конечном итоге стать доступными для терапевтических целей. Более поздний подход для доставки РНК in vivo позвоночному животному предполагает систему цис-репликации, содержащую самовосстанавливающуюся молекулу РНК (публикация международной заявки WO 2012/006376 A2).
В противоположность предложениям предшествующего уровня техники система транс-репликации по настоящему изобретению очень подходит для экспрессии генов: она связана с высокими уровнями экспрессии, высоким титром антигена и достаточная степень выживаемости вакцинированных животных может быть достигнута даже тогда, когда уровень антиген-кодирующей РНК является относительно низким. В частности, введение 1 мкг транс-репликона РНК системы по настоящему изобретению может приводить к титру нейтрализации вируса и титру HA, сравнимому с введением 5 мкг цис-репликона (смотрите пример 6 и фиг. 7). Это представляет собой значительный вклад в настоящую область техники, особенно в продвижении области вакцинации животных, поскольку общее количество кодирующей вакцину нуклеиновой кислоты может быть снижено. Это экономит затраты и время на производство и важно по меньшей мере по следующим причинам.
Прежде всего, универсальность системы по настоящему изобретению, содержащей две отдельные молекулы РНК, позволяет разрабатывать и/или получать репликон и репликазную конструкцию в разное время и/или на разных участках. Согласно одному варианту осуществления репликазную конструкцию получают в первый момент времени, а репликон получают в более поздний момент времени. Например, после его получения репликазная конструкция может быть сохранена для использования в более поздний момент времени. В настоящем изобретении предусмотрена повышенная гибкость по сравнению с цис-репликонами: при появлении нового патогена система по настоящему изобретению может быть разработана для вакцинации путем клонирования в репликон нуклеиновой кислоты, кодирующей полипептид, который вызывает иммунный ответ против нового патогена. Предварительно полученную репликазную конструкцию можно восстановить из хранилища. Таким образом, не требуется, чтобы во время разработки и получения репликазной конструкции была известна природа конкретного патогена или антигена(ов) конкретного патогена. Следовательно, не требуется, чтобы во время разработки и получения репликазной конструкции, был доступен репликон, кодирующий полипептид, который вызывает иммунный ответ против конкретного нового патогена. Другими словами, репликазная конструкция может быть разработана и получена независимо от любого конкретного репликона. Это позволяет быстро реагировать на появление новых патогенов или на патогены, характеризующиеся экспрессией по меньшей мере одного нового антигена, поскольку получение репликона, лишенного репликазы, требует меньше усилий и ресурсов, чем получение цис-репликонов. История говорит, что необходима система, позволяющая быстро реагировать на патогены: это иллюстрируется, например, появлением в последние годы патогенов, вызывающих тяжелый острый респираторный синдром (SARS), Эбола и различные подтипы вируса гриппа.
Во-вторых, в случае вакцинации животных стоимость вакцины является ключом к ее успеху в ветеринарии и фермерском сообществе. Поскольку репликон по настоящему изобретению может быть реплицирован в присутствии неструктурного белка функционального альфавирусного, например, в клетке вакцинированного животного, могут быть достигнуты высокие уровни экспрессии представляющего интерес гена, даже если вводятся относительно небольшие количества РНК-репликона. Низкие количества РНК-репликона положительно влияют на стоимость вакцины на одного субъекта.
В-третьих, транс-репликон в соответствии с настоящим изобретением, как правило, представляет собой более короткую молекулу нуклеиновой кислоты, чем типичный цис-репликон. Это обеспечивает более быстрое клонирование репликона, кодирующего представляющий интерес белок, например, иммуногенный полипептид, и обеспечивает более высокие выходы представляющего интерес белка (смотрите, например, пример 1).
Согласно предпочтительному варианту осуществления репликон может быть реплицирован альфавирусной репликазой из вируса леса Семлики, включая в себя встречающийся в природе вирус леса Семлики, а также вариант или производное вируса леса Семлики, например, аттенуированный вирус леса Семлики. Согласно альтернативному предпочтительному варианту осуществления репликон может быть реплицирован альфавирусной репликазой из вируса Синдбис, включая в себя встречающийся в природе вирус Синдбис и вариант или производное вируса Синдбис, такое как аттенуированный вирус Синдбис. Согласно альтернативному предпочтительному варианту осуществления репликон может быть реплицирован альфавирусной репликазой из вируса венесуэльского лошадиного энцефалита (VEEV), включая в себя встречающийся в природе VEEV и вариант или производное VEEV, например, аттенуированный VEEV.
РНК-репликон в соответствии с настоящим изобретением предпочтительно представляет собой одноцепочечную молекулу РНК. В общем, одноцепочечные кодирующие молекулы нуклеиновой кислоты содержат в два раза больше генетической информации на единицу массы (например, мкг) материала нуклеиновой кислоты. Таким образом, одноцепочечный характер представляет собой дополнительное преимущество по сравнению с двухцепочечными векторами ДНК предшествующего уровня техники, используемыми, например, Spuul с соавт., смотрите выше. Репликон в соответствии с настоящим изобретением, как правило, представляет собой (+)-нитевую молекулу РНК.
Согласно одному варианту осуществления репликон РНК представляет собой выделенную молекулу нуклеиновой кислоты.
Система транс-репликации по настоящему изобретению пригодна для инокуляции клетки-хозяина и для экспрессии представляющего интерес гена в клетке-хозяине (смотрите, например, примеры 1-3). В некоторых экспериментальных примерах настоящего изобретения РНК транс-репликона содержит в качестве представляющего интерес гена ген, кодирующий репортерный белок (например, флуоресцентный белок, такой как GFP или eGFP), который позволяет легко определить эффективность экспрессии соответствующего представляющего интерес гена. Как показано в примере 2, система транс-репликации, содержащая две РНК, связана со значительно лучшей эффективностью экспрессии представляющего интерес гена по сравнению с цис-репликацией (РНК-репликон с eGFP).
Система транс-репликации по настоящему изобретению подходит для эффективной экспрессии представляющего интерес гена у человека или животного, например, для высокоэффективной экспрессии. В частности, в примере 5 показано, что может быть эффективно произведен репортерный белок, а в примере 6 показано, что терапевтический эффект, защищающий от патогенной инфекции, может быть достигнут у животных, подвергнутых воздействию системой по настоящему изобретению.
Без ограничения какой-либо конкретной теории можно предположить, что, например, приблизительно 7400 нуклеотидов, которые кодируют репликазу в типичных обнаруженных в природе альфавирусах, навязывают нагрузку на клетку, так как потребуется амплификация полноразмерного репликона. Понятно, что основная часть этой нагрузки устраняется, когда не репликативная репликазная конструкция, например, в форме мРНК, используется для экспрессии репликазы. Это позволяет использовать транс-репликон для амплификации РНК и трансгенной экспрессии. Если репликазная конструкция не реплицируется в клетке (т.е. единственная чужеродная конструкция, которая реплицируется, представляет собой транс-репликон по настоящему изобретению), избегают отходов клеточной энергии и ресурсов (нуклеотидов и т.д.), что может объяснять более высокие уровни экспрессии. Более того, более короткий РНК-репликон, вероятно, требует меньше времени для синтеза РНК. Поэтому вполне возможно, что сохранение времени, клеточной энергии и/или ресурсов способствует высокоэффективной репликации.
Консервативные элементы последовательности
Согласно одному варианту осуществления репликон представляет собой или содержит альфавирусную геномную РНК или получен из альфавирусной геномной РНК. Согласно одному варианту осуществления репликон в соответствии с настоящим изобретением содержит один или несколько консервативных элементов последовательности (CSE) (Strauss & Strauss, Microbiol. Rev., 1994, vol. 58, pp. 491-562). В частности, репликон может содержать один или несколько консервативных элементов последовательности (CSE) обнаруженного в природе альфавируса или его варианта или производного:
- CSE 1, который, как полагают, функционирует как промотор для синтеза (+)-нитей из (-)-нитевых матриц. Если присутствует, то CSE 1, как правило, находится на 5’-конце РНК-репликона или возле него.
- CSE 2, который, как полагают, выступает в качестве промотора или энхансера для синтеза (-)-нитей из геномной (+)-нитевой РНК-матрицы. Если присутствует, CSE 2, как правило, располагается ниже по ходу транскрипции от CSE 1, но выше против хода транскрипции от CSE 3.
- CSE 3, который, как полагают, способствует эффективной транскрипции субгеномной РНК; если присутствует, CSE 3, как правило, располагается выше против хода транскрипции от кодирующей последовательности для представляющего интерес гена (если есть), но ниже по ходу транскрипции от CSE 2.
- CSE 4, который, как полагают, выступает в качестве основного промотора для инициации синтеза (-)-нитей. Если присутствует, то CSE 4, как правило, располагается ниже по ходу транскрипции от кодирующей последовательности для представляющего интерес гена (если есть). Во всяком случае, CSE 4, как правило, присутствует ниже по ходу транскрипции от CSE 3. Подробная информация о последовательности CSE 4 (также называемой 3’ CSE) в различных альфавирусах была описана в публикации Hardy & Rice, J. Virol., 2005, vol. 79, pp. 4630-4639, а в настоящем изобретении последовательность CSE 4 может быть выбрана, например, в соответствии с идеей этого документа.
Согласно одному варианту осуществления РНК-репликон в соответствии с настоящим изобретением содержит:
(1) 5' репликационную последовательность распознавания альфавируса и
(2) 3' репликационную последовательность распознавания альфавируса.
Согласно одному варианту осуществления 5' репликационная последовательность распознавания альфавируса содержит CSE 1 и/или CSE 2 альфавируса. В альфавирусе, встречающемся в природе, CSE 1 и/или CSE 2, как правило, содержатся в 5' репликационной последовательности распознавания.
Согласно одному варианту осуществления 3' репликационная последовательность распознавания альфавируса содержит CSE 4 альфавируса. В альфавирусе, встречающемся в природе, CSE 4, как правило, содержится в 3' репликационной последовательности распознавания.
Согласно одному варианту осуществления 5' репликационная последовательность распознавания альфавируса и 3' репликационная последовательность распознавания альфавируса способны направлять репликацию РНК-репликона в соответствии с настоящим изобретением в присутствии репликазы. Таким образом, когда они присутствуют отдельно или предпочтительно вместе, эти последовательности распознавания направляют репликацию РНК-репликона в присутствии репликазы. Без ограничения какой-либо конкретной теорией понятно, что консервативные элементы последовательности альфавируса (CSE) 1, 2 и 4 представляют собой (входят в состав) последовательности распознавания, которые направляют репликацию РНК-репликона в присутствии репликазы. Таким образом, согласно этому варианту осуществления репликон будет, как правило, содержать CSE 1, 2 и 4.
Предпочтительно, чтобы репликаза, которая кодируется репликазной конструкцией, представляла собой альфавирусную репликазу, которая способна распознавать как 5' репликационную последовательность распознавания альфавируса, так и 3' репликационную последовательность распознавания альфавируса.
Согласно одному варианту осуществления это достигается, когда 5' репликационная последовательность распознавания альфавируса и 3' репликационная последовательность распознавания альфавируса являются нативными для альфавируса, из которого получена репликаза. Нативный означает, что природное происхождение этих последовательностей представляет собой один и тот же альфавирус. Согласно одному варианту осуществления CSE 1, CSE 2 и CSE 4 являются нативными по отношению к альфавирусу, из которого получена репликаза.
Согласно альтернативному варианту осуществления 5' репликационная последовательность распознавания (и/или CSE 1 и/или CSE 2) и/или 3' репликационная последовательность распознавания (и/или CSE 4) не являются нативными для альфавируса, из которого получена репликаза, при условии, что альфавирусная репликаза способна распознавать как 5' репликационную последовательность распознавания (и/или CSE 1, и/или CSE 2), так и 3' репликационную последовательность распознавания (и/или CSE 4) репликона. Другими словами, репликаза совместима с 5' репликационной последовательностью распознавания (и/или CSE 1, и/или CSE 2) и 3' репликационной последовательностью распознавания (и/или CSE 4). Когда ненативная альфавирусная репликаза способна распознавать соответствующую последовательность или элемент последовательности, репликаза считается совместимой (межвирусная совместимость). Примеры межвирусной совместимости относительно (3’/5’) репликационных последовательностей распознавания и CSE, соответственно, с ненативными репликазами из разных альфавирусов известны в настоящей области техники (например, Strauss & Strauss, Microbiol. Rev., 1994, vol. 58, pp. 491-562). Любая комбинация (3’/5’) репликационных последовательностей распознавания и CSE, соответственно, с альфавирусной репликазой возможна до тех пор, пока существует межвирусная совместимость. Межвирусная совместимость может быть легко исследована квалифицированным специалистом, работающим над настоящим изобретением, путем инкубирования исследуемой репликазы вместе с РНК, где РНК содержит 3’ и 5’ репликационные последовательности распознавания, подлежащие исследованию, в условиях, подходящих для репликации РНК, например, в подходящей клетке-хозяине. Если происходит репликация, (3’/5’) репликационные последовательности распознавания и репликаза определяются как совместимые.
Субгеномный промотор
Согласно конкретным вариантам осуществления репликон РНК в соответствии с настоящим изобретением содержит последовательность контроля экспрессии. Типичная последовательность контроля экспрессии представляет собой или содержит промотор. Согласно одному варианту осуществления РНК-репликон в соответствии с настоящим изобретением содержит субгеномный промотор. Предпочтительно, субгеномный промотор представляет собой субгеномный промотор альфавируса. Нуклеотидная последовательность субгеномного промотора высококонсервативна среди альфавирусов (Strauss & Strauss, Microbiol. Rev., 1994, vol. 58, pp. 491-562).
Предпочтительно, субгеномный промотор представляет собой промотор структурного белка альфавируса. Это означает, что субгеномный промотор представляет собой промотор, который является нативным для альфавируса и который контролирует транскрипцию гена одного или нескольких структурных белков в указанном альфавирусе.
Предпочтительно, чтобы субгеномный промотор был совместим с репликазой репликазной конструкции. Совместимость в этом контексте означает, что альфавирусная репликаза способна распознавать субгеномный промотор. Таким образом, предпочтительно, чтобы репликаза, которая кодируется репликазной конструкцией, представляла собой альфавирусную репликазу, которая способна распознавать субгеномный промотор репликона.
Согласно одному варианту осуществления это достигается, когда субгеномный промотор является нативным для альфавируса, из которого получена репликаза. Нативный означает, что природное происхождение субгеномного промотора и репликазы представляет собой один и тот же альфавирус.
Согласно альтернативному варианту осуществления субгеномный промотор не является нативным для альфавируса, из которого получена репликаза, при условии, что альфавирусная репликаза способна распознавать субгеномный промотор репликона. Другими словами, репликаза совместима с субгеномным промотором (межвирусная совместимость). Любая комбинация субгеномного промотора и репликазы возможна, если существует межвирусная совместимость. Межвирусная совместимость может быть легко исследована специалистом, работающим по настоящему изобретению, путем инкубирования исследуемой репликазы вместе с РНК, причем РНК содержит подлежащий исследованию субгеномный промотор, в условиях, подходящих для синтеза РНК из субгеномного промотора. Если получают субгеномный транскрипт, субгеномный промотор и репликаза определяются как совместимые. Известны различные примеры межвирусной совместимости: в некоторых случаях ненативный субгеномный промотор приводит даже к более эффективной транскрипции, чем нативный субгеномный промотор (обзор в публикации Strauss & Strauss, Microbiol. Rev., 1994, vol. 58, pp. 491-562).
Предпочтительно, чтобы репликон в соответствии с настоящим изобретением содержал консервативный элемент последовательности 3 (CSE 3) из альфавируса. Считается, что CSE 3 способствует эффективной транскрипции субгеномной РНК. Известно, что транскрипция субгеномной РНК происходит очень эффективно, когда присутствует CSE 3. Как правило, CSE 3 представляет собой полинуклеотид длиной приблизительно 24 нуклеотида. В альфавирусных геномах CSE 3 находится в области соединения между кодирующей последовательностью неструктурных и структурных белков. В транс-репликоне по настоящему изобретению CSE 3, как правило, присутствует выше против хода транскрипции (5’) от открытой рамки считывания (ORF) под контролем субгеномного промотора. В случае, если репликон в соответствии с настоящим изобретением содержит одну ORF под контролем субгеномного промотора, CSE 3 находится 5’ от этой одной ORF. В случае, если репликон в соответствии с настоящим изобретением содержит более одной ORF под контролем субгеномного промотора, CSE 3 может быть расположен 5’ от каждой такой ORF. Согласно одному варианту осуществления CSE 3 является нативным для альфавируса, из которого получена репликаза. Согласно альтернативному варианту осуществления CSE 3 является не нативным для альфавируса, из которого получена репликаза, при условии, что альфавирусная репликаза способна распознавать CSE 3 репликона.
Дополнительные особенности репликона
Согласно одному варианту осуществления репликон РНК в соответствии с настоящим изобретением содержит 3' поли(А)-последовательность. Было описано, что поли(А)-последовательность альфавирусной РНК играет роль в эффективности трансляции вирусных неструктурных белков и стабильности РНК, аналогично ее роли в клеточной мРНК (Hardy & Rice, J. Virol., 2005, vol. 79, pp. 4630-4639). В настоящем изобретении предполагается, что поли(А)-последовательность играет роль в эффективности трансляции представляющего интерес гена и стабильности репликона.
Варианты осуществления и предпочтительные варианты осуществления 3' поли(А)-последовательности репликона в соответствии с настоящим изобретением могут быть выбраны среди тех, которые раскрыты в настоящем документе для 3' поли(А)-последовательности репликазной конструкции. В дополнение к этому согласно одному варианту осуществления поли(А)-последовательности (если она присутствует на репликоне в соответствии с настоящим изобретением) предшествует элемент консервативной последовательности 4 альфавируса (CSE 4). Предпочтительно она непосредственно примыкает к CSE 4, так что самый 3’ нуклеотид CSE 4 непосредственно примыкает к самому 5’ нуклеотиду A поли(А)-хвоста.
Согласно одному варианту осуществления репликон РНК в соответствии с настоящим изобретением содержит 5’-кэп (включая аналог кэпа). Для иллюстрации на фиг. 1 кэп (или аналог кэпа) обозначен буквой С. Аспекты кэпа (или аналога) репликона в соответствии с настоящим изобретением идентичны аспектам, описанным в настоящем документе для кэпа (или аналога) репликазной конструкции, за исключением того, что наличие кэпа не является обязательным для случая РНК-репликона. Таким образом, согласно альтернативному варианту осуществления РНК-репликон в соответствии с настоящим изобретением не содержит кэп. Согласно этому варианту осуществления он может содержать свободный 5’-ОН-конец или любую подходящую 5’-модификацию. Этот вариант осуществления в равной степени охватывается настоящим изобретением, независимо от того, что на фиг. 1 схематически изображен альтернативный вариант осуществления, при котором репликон содержит кэп, иллюстрируемый буквой С.
Согласно одному варианту осуществления кодирующая последовательность открытой рамки (рамок) считывания, присутствующей на репликоне в соответствии с настоящим изобретением (если есть), адаптирована. Варианты осуществления и предпочтительные варианты осуществления адаптации кодона репликона в соответствии с настоящим изобретением могут быть выбраны среди тех, которые раскрыты в настоящем документе для случая адаптации кодонов репликазной конструкции. Кодоны открытой рамки (рамок) считывания могут быть адаптированы для экспрессии в клетке-хозяине или в организме-хозяине.
Гетерологичная последовательность нуклеиновой кислоты
Согласно одному варианту осуществления репликон дополнительно содержит по меньшей мере одну последовательность нуклеиновой кислоты, которая не происходит от вируса, в частности, от альфавируса. Согласно предпочтительным вариантам осуществления репликон РНК в соответствии с настоящим изобретением содержит гетерологичную последовательность нуклеиновой кислоты. В соответствии с настоящим изобретением термин «гетерологичный» относится к ситуации, когда последовательность нуклеиновой кислоты функционально не связана в природе с последовательностью нуклеиновой кислоты альфавируса, такой как последовательность контроля экспрессии альфавируса, особенно субгеномный промотор альфавируса. Гетерологичная последовательность нуклеиновой кислоты состоит из последовательности нуклеиновой кислоты репликона.
Предпочтительно, гетерологичная последовательность нуклеиновой кислоты находится под контролем субгеномного промотора, предпочтительно субгеномного промотора альфавируса. Более предпочтительно, гетерологичная последовательность нуклеиновой кислоты локализуется ниже по ходу транскрипции от субгеномного промотора. Субгеномный промотор альфавируса очень эффективен и поэтому подходит для высокоэффективной гетерологичной экспрессии генов (José et al., Future Microbiol., 2009, vol. 4, pp. 837–856). Предпочтительно, субгеномный промотор контролирует производство субгеномной РНК, содержащей транскрипт гетерологичной последовательности нуклеиновой кислоты или ее части.
Предпочтительно, чтобы субгеномный промотор представлял собой промотор структурного белка альфавируса. Это означает, что субгеномный промотор представляет собой промотор, природный для альфавируса, и который контролирует транскрипцию кодирующей последовательности одного или нескольких структурных белков в указанном альфавирусе. В соответствии с настоящим изобретением гетерологичная последовательность нуклеиновой кислоты может частично или полностью замещать последовательность вирусной нуклеиновой кислоты, такую как последовательность нуклеиновой кислоты, кодирующую структурные белки альфавируса. Предпочтительно, чтобы гетерологичная последовательность нуклеиновой кислоты не происходила от альфавируса; в частности, предпочтительно, чтобы гетерологичная последовательность нуклеиновой кислоты не была получена из того же альфавируса, из которого получен субгеномный промотор. Согласно одному варианту осуществления репликон содержит CSE 3, а гетерологичная последовательность нуклеиновой кислоты является гетерологичной для CSE 3.
Представляющий интерес белок
Согласно одному варианту осуществления РНК-репликон в соответствии с настоящим изобретением содержит открытую рамку считывания, кодирующую представляющий интерес пептид или представляющий интерес белок. Предпочтительно, чтобы представляющий интерес белок кодировался гетерологичной нуклеиновой кислотой. Предпочтительно, чтобы ген, кодирующий представляющий интерес белок (то есть представляющий интерес ген), присутствовал вместе с последовательностью контроля экспрессии. Предпочтительно, чтобы представляющий интерес ген был под контролем промотора, предпочтительно, под контролем субгеномного промотора, как описано в настоящем документе. Более предпочтительно, чтобы представляющий интерес ген был расположен ниже по ходу транскрипции от субгеномного промотора.
Ген, кодирующий представляющий интерес белок, синонимично называется «представляющий интерес ген» или «трансген». Трансген присутствует в репликоне в соответствии с настоящим изобретением, предпочтительно под контролем субгеномного промотора, и его локализация, таким образом, напоминает локализацию структурных генов в альфавирусе. Предпочтительно, местоположение ниже по ходу транскрипции от субгеномного промотора таково, что субгеномный транскрипт будет содержать транскрипт представляющего интерес гена. Предпочтительно, представляющий интерес ген содержит открытую рамку считывания, содержащую стартовый кодон (триплет оснований), как правило, AUG (в молекуле РНК) или ATG (в соответствующей молекуле ДНК).
Предпочтительно, если РНК-репликон в соответствии с настоящим изобретением содержит по меньшей мере одну открытую рамку считывания (область кодирования белка), репликон представляет собой молекулу мРНК.
Репликон в соответствии с настоящим изобретением может кодировать единственный полипептид или несколько полипептидов. Несколько полипептидов можно кодировать как единственный полипептид (слитый полипептид) или в виде отдельных полипептидов. Если полипептиды кодируются как отдельные полипептиды, то один или несколько из них могут быть снабжены IRES выше против хода транскрипции или дополнительным элементом вирусного промотора. Альтернативно, репликон в соответствии с настоящим изобретением может содержать более одной открытой рамки считывания, каждая из которых находится под контролем субгеномного промотора. Когда такой репликон с несколькими ORF помещается в эукариотические клетки, будут получены множественные субгеномные транскрипты, каждый из которых инициируется собственным субгеномным промотором (Strauss & Strauss, Microbiol. Rev., 1994, vol. 58, pp. 491-562). Альтернативно полипептид или слитый полипептид содержит отдельные полипептиды, разделенные аутокаталитической протеазой (например, белок 2А вируса ящура) или интеином.
Предпочтительно, открытая рамка считывания, кодирующая представляющий интерес белок, является ненативной по отношению к альфавирусу, из которого получена репликаза. Предпочтительно, открытая рамка считывания под контролем субгеномного промотора не кодирует какой-либо альфавирусный белок. Согласно предпочтительным вариантам осуществления открытая рамка считывания под контролем субгеномного промотора не кодирует какой-либо полноразмерный альфавирусный неструктурный белок (nsP) или его фрагмент и/или не кодирует какой-либо полноразмерный структурный белок альфавируса (sP) или его фрагмент. Предпочтительно, открытая рамка считывания, кодирующая представляющий интерес белок под контролем субгеномного промотора, не кодирует никакого структурного белка альфавируса. Согласно одному варианту осуществления система по настоящему изобретению не содержит последовательность нуклеиновой кислоты, кодирующую один или несколько структурных белков альфавируса. Согласно одному варианту осуществления система не содержит последовательность нуклеиновой кислоты, кодирующую любой белок C нуклеокапсида сердцевины, белок P62 оболочки и/или белок E1 оболочки.
Преимуществом системы по настоящему изобретению является то, что она не требует наличия или введения вируса-помощника, кодирующего структурные белки альфавируса. Это является преимуществом по сравнению с предшествующим уровнем техники (например, в публикации Bredenbeek et al., J. Virol, 1993, vol. 67, pp. 6439-6446 описана система транс-репликации, способная упаковывать репликонные векторы, которые не содержат ORF структурного белка, в вирусные частицы, причем структурные белки должны экспрессироваться in trans из РНК-помощника. Репликация этих РНК-помощников, кодирующих структурные белки альфавируса, как правило, зависит от репликазы, экспрессированной из РНК-репликона, которая кодирует антиген. У самой РНК-помощника отсутствует функциональная репликаза и она содержит только консервативные элементы последовательности РНК, необходимые для репликации (Smerdou & Liljeström, 1999, J. Virol., vol. 73, pp. 1092-1098; Ehrengruber & Lundstrom, 1999, Proc. Natl. Acad. Sci. U. S. A, vol. 96, pp. 7041-7046). Однако такая РНК-помощник, кодирующая структурные белки альфавируса, не требуется для достижения успеха настоящего изобретения. Таким образом, предпочтительно, чтобы молекула нуклеиновой кислоты по настоящему изобретению не кодировала альфавирусные структурные белки.
Согласно одному варианту осуществления открытая рамка считывания кодирует репортерный белок. Согласно этому варианту осуществления открытая рамка считывания содержит репортерный ген. Определенные гены могут быть выбраны в качестве репортеров, потому что характеристики, которые они придают клеткам или организмам, экспрессирующим их, могут быть легко идентифицированы и измерены, или потому что они являются селектируемыми метками. Репортерные гены часто используются в качестве индикатора того, был ли поглощен определенный ген или экспрессирован в популяции клеток или организмов. Предпочтительно, продукт экспрессии репортерного гена визуально обнаруживается. Обычные визуально обнаруживаемые репортерные белки, как правило, содержат флуоресцентные или люминесцирующие белки. Примеры конкретных репортерных генов включают в себя ген, который кодирует зеленый флуоресцентный белок медузы (GFP), который заставляет клетки, которые его экспрессируют, светить зеленым под синим светом, фермент люциферазу, который катализирует реакцию с люциферином для получения света, и красный флуоресцентный белок (RFP). Возможны варианты любого из этих специфических репортерных генов, если варианты обладают визуально обнаруживаемыми свойствами. Например, eGFP представляет собой вариант GFP с точечной мутацией. Вариант осуществления репортерного белка особенно подходит для исследования экспрессии, опосредованной системой транс-репликации по настоящему изобретению in vitro и in vivo, смотрите, например, примеры 2 и 4. Например, в обоих случаях (система цис-репликации и система транс-репликации, соответственно) присутствие репортерного белка предполагает, что получают субгеномный транскрипт, содержащий последовательность нуклеиновой кислоты, кодирующую репортерный белок. В свою очередь, производство субгеномного транскрипта в клетке предполагает, что в этой клетке присутствует репликазная конструкция и что ген репликазы экспрессируется.
Согласно альтернативному варианту осуществления открытая рамка считывания не кодирует репортерный белок. Например, когда система по настоящему изобретению разработана для введения фармацевтически активного пептида или белка человеку или животному, как показано, например, в примере 6, возможно, что флуоресцентный репортерный белок не кодируется. Например, фармацевтически активный белок может быть единственным белком, кодируемым открытой рамкой считывания под контролем субгеномного промотора.
В соответствии с настоящим изобретением согласно одному варианту осуществления РНК репликона содержит или состоит из фармацевтически активной РНК. «Фармацевтически активная РНК» может представлять собой РНК, которая кодирует фармацевтически активный пептид или белок. Предпочтительно, чтобы РНК-репликон в соответствии с настоящим изобретением кодировал фармацевтически активный пептид или белок. Предпочтительно, чтобы открытая рамка считывания кодировала фармацевтически активный пептид или белок. Предпочтительно, чтобы РНК-репликон содержал открытую рамку считывания, которая кодирует фармацевтически активный пептид или белок, предпочтительно, под контролем субгеномного промотора.
«Фармацевтически активный пептид или белок» оказывает положительное или благоприятное действие на состояние или заболевание субъекта при введении субъекту в терапевтически эффективном количестве. Предпочтительно, фармацевтически активный пептид или белок обладает лечебными или паллиативными свойствами и может вводиться для улучшения, ослабления, облегчения, обращения, задержки начала или уменьшения тяжести одного или нескольких симптомов заболевания или нарушения. Фармацевтически активный пептид или белок может характеризоваться профилактическими свойствами и может быть использован для замедления начала заболевания или уменьшения тяжести такого заболевания или патологического состояния. Термин «фармацевтически активный пептид или белок» включает в себя целые белки или полипептиды и также может относиться к их фармацевтически активным фрагментам. Он также может включать в себя фармацевтически активные аналоги пептида или белка. Термин «фармацевтически активный пептид или белок» включает в себя пептиды и белки, которые представляют собой антигены, то есть пептид или белок вызывает иммунный ответ у субъекта, который может быть терапевтическим или частично или полностью защитным. Фармацевтически активный пептид или белок можно также назвать терапевтическим пептидом или белком.
Согласно одному варианту осуществления фармацевтически активный пептид или белок представляет собой или содержит иммунологически активное соединение или антиген или эпитоп.
Согласно настоящему изобретению термин «иммунологически активное соединение» относится к любому соединению, изменяющему иммунный ответ, предпочтительно путем индуцирования и/или подавления созревания иммунных клеток, индуцирования и/или подавления биосинтеза цитокинов и/или изменения гуморального иммунитета с помощью стимулирования производства антител В-клетками. Согласно одному варианту осуществления иммунный ответ включает в себя стимуляцию ответа антитела (как правило, включающего в себя иммуноглобулин G (IgG)). Иммунологически активные соединения обладают мощной иммуностимулирующей активностью, включая в себя, без ограничения, противовирусную и противоопухолевую активность, а также могут понижающе регулировать другие аспекты иммунного ответа, например, сдвигать иммунный ответ от иммунного ответа TH2, что применимо для лечения широкого спектра заболеваний, опосредованных TH2.
Согласно настоящему изобретению термин «антиген» или «иммуноген» охватывает любое вещество, которое будет вызывать иммунный ответ. В частности, «антиген» относится к любому веществу, которое специфически реагирует с антителами или Т-лимфоцитами (Т-клетками). В соответствии с настоящим изобретением термин «антиген» включает в себя любую молекулу, которая содержит по меньшей мере один эпитоп. Предпочтительно, антиген в контексте настоящего изобретения представляет собой молекулу, которая, необязательно после процессинга, индуцирует иммунную реакцию, которая предпочтительно является специфической для антигена. В соответствии с настоящим изобретением может быть использован любой подходящий антиген, который является кандидатом для иммунной реакции, причем иммунная реакция может представлять собой как гуморальную, так и клеточную иммунную реакцию. В контексте вариантов осуществления настоящего изобретения антиген предпочтительно представлен клеткой, предпочтительно антигенпрезентирующей клеткой, в контексте молекул МНС, что приводит к иммунной реакции против антигена. Антиген предпочтительно представляет собой продукт, который соответствует природному антигену или происходит от него. Такие встречающиеся в природе антигены могут включать в себя или могут происходить из аллергенов, вирусов, бактерий, грибов, паразитов и других инфекционных агентов и патогенов или антиген также может представлять собой опухолевый антиген. В соответствии с настоящим изобретением антиген может соответствовать встречающемуся в природе продукту, например, вирусному белку или его части. Согласно предпочтительным вариантам осуществления антиген представляет собой поверхностный полипептид, то есть полипептид, естественно отображаемый на поверхности клетки, патоген, бактерию, вирус, гриб, паразит, аллерген или опухоль. Антиген может вызывать иммунный ответ против клетки, патогена, бактерии, вируса, гриба, паразита, аллергена или опухоли.
Термин «патоген» относится к патогенному биологическому материалу, способному вызывать заболевание в организме, предпочтительно в организме позвоночных. Патогены включают в себя микроорганизмы, такие как бактерии, одноклеточные эукариотические организмы (простейшие), грибы, а также вирусы.
Термины «эпитоп», «антигенный пептид», «антигенный эпитоп», «иммуногенный пептид» и «связывающий МНС пептид» используются в настоящем документе взаимозаменяемо и относятся к антигенной детерминанте в молекуле, такой как антиген, то есть к части или фрагменту иммунологически активного соединения, которое распознается иммунной системой, например, которое распознается Т-клеткой, в частности, когда оно представлено в контексте молекул МНС. Эпитоп белка предпочтительно содержит непрерывную или прерывистую часть указанного белка и предпочтительно составляет от 5 до 100, предпочтительно от 5 до 50, более предпочтительно от 8 до 30, наиболее предпочтительно от 10 до 25 аминокислот в длину, например, эпитоп может составлять предпочтительно 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24 или 25 аминокислот в длину. В соответствии с настоящим изобретением эпитоп может связываться с молекулами MHC, такими как молекулы MHC на поверхности клетки и, таким образом, может представлять собой «связывающий MHC пептид» или «антигенный пептид». Термин «основной комплекс гистосовместимости» и сокращение «MHC» включает в себя молекулы MHC класса I и MHC класса II и относится к комплексу генов, который присутствует у всех позвоночных. Белки или молекулы MHC важны для передачи сигналов между лимфоцитами и антигенпрезентирующими клетками или пораженными клетками в иммунных реакциях, причем белки или молекулы MHC связывают пептиды и презентируют их для распознавания Т-клеточными рецепторами. Белки, кодируемые MHC, экспрессируются на поверхности клеток и отображают как аутоантигены (пептидные фрагменты из самой клетки), так и неаутоантигены (например, фрагменты вторгающихся микроорганизмов) для Т-клетки. Предпочтительные такие иммуногенные части связываются с молекулой МНС класса I или класса II. Как используется в настоящем документе, иммуногенная часть называется частью, которая «связывается с» молекулой МНС класса I или класса II, если такое связывание обнаруживается с использованием любого анализа, известного в настоящей области техники. Термин «связывающий MHC пептид» относится к пептиду, который связывается с молекулой MHC класса I и/или MHC класса II. В случае комплексов MHC класса I с пептидом связывающие пептиды, как правило, составляют 8-10 аминокислот в длину, хотя могут быть эффективными и более длинные или более короткие пептиды. В случае комплексов MHC класса II с пептидом связывающие пептиды, как правило, составляют в длину 10-25 аминокислот и, в частности, составляют 13-18 аминокислот, тогда как могут быть эффективными и более длинные и более короткие пептиды.
Согласно одному варианту осуществления представляющий интерес белок в соответствии с настоящим изобретением содержит эпитоп, подходящий для вакцинации целевого организма. Специалисту в настоящей области техники известно, что один из принципов иммунобиологии и вакцинации основан на том факте, что иммунозащитная реакция на заболевание вырабатывается путем иммунизации организма антигеном, который является иммунологически релевантным по отношению к подлежащему лечению заболеванию. В соответствии с настоящим изобретением антиген выбирают из группы, содержащей аутоантиген и неаутоантиген. Неаутоантиген предпочтительно представляет собой бактериальный антиген, вирусный антиген, грибковый антиген, аллерген или паразитный антиген. Предпочтительно, чтобы антиген содержал эпитоп, который способен вызывать иммунный ответ в целевом организме. Например, эпитоп может вызывать иммунный ответ против бактерии, вируса, гриба, паразита, аллергена или опухоли.
Согласно некоторым вариантам осуществления неаутоантиген представляет собой бактериальный антиген. Согласно некоторым вариантам осуществления антиген вызывает иммунный ответ против бактерии, которая заражает животных, включая в себя птиц, рыб и млекопитающих, включая в себя домашних животных. Предпочтительно, бактерия, против которой вызывается иммунный ответ, представляет собой патогенную бактерию.
Согласно некоторым вариантам осуществления неаутоантиген представляет собой вирусный антиген. Вирусный антиген может представлять собой, например, пептид из поверхностного белка вируса, например, капсидный полипептид или полипептид шипа. Согласно некоторым вариантам осуществления антиген вызывает иммунный ответ против вируса, который заражает животных, включая в себя птиц, рыб и млекопитающих, включая в себя домашних животных. Предпочтительно, вирус, против которого вызывается иммунный ответ, представляет собой патогенный вирус.
Согласно некоторым вариантам осуществления неаутоантиген представляет собой полипептид или белок из гриба. Согласно некоторым вариантам осуществления антиген вызывает иммунный ответ против гриба, который заражает животных, включая в себя птиц, рыб и млекопитающих, включая в себя домашних животных. Предпочтительно, гриб, против которого вызывается иммунный ответ, представляет собой патогенный гриб.
Согласно некоторым вариантам осуществления неаутоантиген представляет собой полипептид или белок из одноклеточного эукариотического паразита. Согласно некоторым вариантам осуществления антиген вызывает иммунный ответ против одноклеточного эукариотического паразита, предпочтительно патогенного одноклеточного эукариотического паразита. Патогенные одноклеточные эукариотические паразиты могут быть, например, из рода Plasmodium, например, P. falciparum, P. vivax, P. malariae или P. ovale, из рода Leishmania или из рода Trypanosoma, например, T. cruzi или T. brucei.
Согласно некоторым вариантам осуществления неаутоантиген представляет собой аллергенный полипептид или аллергенный белок. Аллергенный белок или аллергенный полипептид подходит для иммунотерапии аллергеном, также известной как гипосенсибилизация.
Согласно некоторым вариантам осуществления антиген представляет собой аутоантиген, в частности опухолевый антиген. Опухолевые антигены и их определение известны специалисту в настоящей области техники.
В контексте настоящего изобретения термин «опухолевый антиген» или «опухолеассоциированный антиген» относится к белкам, которые в нормальных условиях специфически экспрессируются в ограниченном числе тканей и/или органов или на конкретных стадиях развития, например, опухолевый антиген может в нормальных условиях специфически экспрессироваться в ткани желудка, предпочтительно в слизистой оболочке желудка, в репродуктивных органах, например, в яичках, в трофобластической ткани, например, в плаценте или в клетках зародышевой линии, и экспрессируются или аберрантно экспрессируются в одной или нескольких опухолевых или злокачественных тканях. В этом контексте «ограниченное число» предпочтительно означает не более 3, более предпочтительно не более 2. Опухолевые антигены в контексте настоящего изобретения включают в себя, например, антигены дифференцировки, предпочтительно специфические к клеточному типу антигены дифференцировки, т.е. белки, которые в нормальных условиях специфически экспрессируются в определенном типе клеток на определенной стадии дифференциации, антигены злокачественной опухоли/яичка, то есть белки, которые в нормальных условиях специфически экспрессируются в яичках, а иногда и в плаценте, и специфические к зародышевой линии антигены. В контексте настоящего изобретения опухолевый антиген предпочтительно ассоциирован с клеточной поверхностью злокачественной клетки и предпочтительно не экспрессируется или только редко экспрессируется в нормальных тканях. Предпочтительно, опухолевый антиген или аберрантная экспрессия опухолевого антигена идентифицирует злокачественные клетки. В контексте настоящего изобретения опухолевый антиген, который экспрессируется злокачественной клеткой у субъекта, например, страдающего от злокачественного заболевания пациента, предпочтительно представляет собой собственный белок у указанного субъекта. Согласно предпочтительным вариантам осуществления опухолевый антиген в контексте настоящего изобретения экспрессируется в нормальных условиях, особенно в ткани или органе, который является несущественным, т.е. ткани или органы, которые при повреждении иммунной системой не приводят к гибели субъекта, или в органах или структурах организма, которые недоступны или едва ли доступны иммунной системе. Предпочтительно, аминокислотная последовательность опухолевого антигена идентична между опухолевым антигеном, который экспрессируется в нормальных тканях, и опухолевым антигеном, который экспрессируется в злокачественных тканях.
Примерами опухолевых антигенов, которые могут быть использованы в настоящем изобретении, являются p53, ART-4, BAGE, β-катенин/m, Bcr-abL CAMEL, CAP-1, CASP-8, CDC27/m, CDK4/m, CEA, белки клеточной поверхности семейства клаудин, такие как CLAUDIN-6, CLAUDIN-18.2 и CLAUDIN-12, c-MYC, CT, Cyp-B, DAM, ELF2M, ETV6-AML1, G250, GAGE, GnT-V, Gap100 , HAGE, HER-2/neu, HPV-E7, HPV-E6, HAST-2, hTERT (или hTRT), LAGE, LDLR/FUT, MAGE-A, предпочтительно, MAGE-A1, MAGE-A2, MAGE-A3, MAGE-A, MAGE-A5, MAGE-A6, MAGE-A7, MAGE-A8, MAGE-A9, MAGE-A10, MAGE-A11 или MAGE-A12, MAGE-B, MAGE-C, MART-1/мелан-A, MC1R, миозин/m, MUC1, MUM-1, -2, -3, NA88-A, NF1, NY-ESO-1, NY-BR-1, p190 минорный BCR-abL, Pm1/RARa, PRAME , протеиназа 3, PSA, PSM, RAGE, RU1 или RU2, SAGE, SART-1 или SART-3, SCGB3A2, SCP1, SCP2, SCP3, SSX, SURVIVIN, TEL/AML1, TPI/m, TRP-1, TRP- 2, TRP-2/INT2, TPTE и WT. Особенно предпочтительные опухолевые антигены включают в себя CLAUDIN-18.2 (CLDN18.2) и CLAUDIN-6 (CLDN6).
Согласно некоторым вариантам осуществления не требуется, чтобы фармацевтически активный пептид или белок был антигеном, который вызывает иммунный ответ. Подходящие фармацевтически активные пептиды или белки могут быть выбраны из группы, состоящей из цитокинов и белков иммунной системы, таких как иммунологически активные соединения (например, интерлейкины, колониестимулирующий фактор (CSF), гранулоцитарный колониестимулирующий фактор (G-CSF), гранулоцитарно-макрофагальный колониестимулирующий фактор (GM-CSF), эритропоэтин, фактор некроза опухоли (TNF), интерфероны, интегрины, адрессины, селектины, «хоминг»-рецепторы, Т-клеточные рецепторы, иммуноглобулины), гормоны (инсулин, гормон щитовидной железы, катехоламины, гонадотрофины, трофические гормоны, пролактин, окситоцин, дофамин, бычий соматотропин, лептины и тому подобное), гормоны роста (например, гормон роста человека), факторы роста (например, эпидермальный фактор роста, фактор роста нервов, инсулиноподобный фактор роста и тому подобное), рецепторы фактора роста , ферменты (тканевый активатор плазминогена, стрептокиназа, биосинтеза или деградации холестерина, стероидогенные ферменты, киназы, фосфодиэстеразы, метилазы, деметилазы, дегидразы, целлюлазы, протеазы, липазы, фосфолипазы, ароматазы, цитохромы, аденилат- или гуанилатциклазы, нейрамидазы и тому подобное), рецепторы (рецепторы стероидных гормонов, пептидные рецепторы), связывающие белки (связывающие гормон роста или связывающие фактор роста белки и т.п.), факторы транскрипции и трансляции, подавляющие опухолевый рост белки (например, белки, которые ингибируют ангиогенез), структурные белки (такие как коллаген, фибрин, фибриноген, эластин, тубулин, актин и миозин), белки крови (тромбин, сывороточный альбумин, фактор VII, фактор VIII, инсулин, фактор IX, фактор X, активатор тканевого плазминогена, белок C, фактор фон Виллебранда, антитромбин III, глюкоцереброзидаза, эритропоэтин, гранулоцитарный колониестимулирующий фактор (GCSF) или модифицированный фактор VIII, антикоагулянты и т.п. Согласно одному варианту осуществления фармацевтически активный белок согласно настоящему изобретению представляет собой цитокин, который участвует в регуляции лимфоидного гомеостаза, предпочтительно, цитокин, который участвует и предпочтительно индуцирует или усиливает развитие, праймирование, размножение, дифференцировку и/или выживание Т-клеток. Согласно одному варианту осуществления цитокин представляет собой интерлейкин, т.е. IL-2, IL-7, IL-12, IL-15 или IL-21.
Универсальность системы по настоящему изобретению
Преимущества системы по настоящему изобретению включают в себя независимость от ядерной транскрипции и наличия ключевой генетической информации о двух отдельных молекулах РНК, что обеспечивает беспрецедентную свободу дизайна. Ввиду своих универсальных элементов, которые сочетаются друг с другом, настоящее изобретение позволяет оптимизировать экспрессию репликазы для желаемого уровня амплификации РНК, для желаемого целевого организма, для желаемого уровня производства представляющего интерес белка и т.д. Репликон, который может быть реплицирован репликазой in trans, может быть разработан независимо.
Например, следующие элементы могут быть индивидуально выбраны, разработаны и/или адаптированы на основе настоящего раскрытия в настоящем документе: кэпирование репликазной конструкции (в частности, выбор специфического кэпа); 5’-UTR репликазной конструкции; кодирующая последовательность ORF, кодирующая репликазу (оптимизация кодонов); 3’-UTR репликазной конструкции; поли(A)-хвост репликазной конструкции; 5’-UTR репликона (до тех пор, пока репликон содержит 5’ репликационную последовательность распознавания для альфавирусной репликазы); субгеномная промоторная последовательность; 5’-UTR субгеномного транскрипта, полученного из репликона; кодирующая последовательность ORF, кодирующая представляющий интерес ген (оптимизация кодонов); 3’-UTR репликона и/или субгеномного транскрипта, полученного из репликона (до тех пор, пока репликон содержит 3’ репликационную последовательность распознавания для альфавирусной репликазы); поли(A)-хвост репликона и/или субгеномного транскрипта, полученного из репликона.
В дополнение к этому настоящее изобретение позволяет совместно трансфицировать оптимальные количества репликона и репликазной конструкции для любого данного типа клеток - покоящегося или циклирующего, in vitro или in vivo.
Особенности безопасности вариантов осуществления настоящего изобретения
Следующие особенности предпочтительны в настоящем изобретении отдельно или в любой подходящей комбинации:
Предпочтительно, система по настоящему изобретению не содержит какого-либо структурного белка альфавируса, такого как белок C нуклеокапсида сердцевины, белок P62 оболочки и/или белок E1 оболочки.
Предпочтительно система по настоящему изобретению не представляет собой систему образования частиц. Это означает, что после инокуляции клетки-хозяина системой по настоящему изобретению клетка-хозяин не производит вирусные частицы, такие как вирусные частицы следующего поколения. Согласно одному варианту осуществления система полностью не содержит генетической информации, кодирующей любой структурный белок альфавируса, такой как белок C нуклеокапсида сердцевины, белок оболочки P62 и/или белок оболочки E1. Этот аспект настоящего изобретения обеспечивает дополнительную ценность с точки зрения безопасности по сравнению с известными системами, в которых структурные белки кодируются транс-реплицирующей РНК-помощником (например, Bredenbeek et al., J. Virol, 1993, vol. 67, pp. 6439- 6446).
Предпочтительно, ни репликон, ни репликазная конструкция не способны управлять своей собственной репликацией, то есть цис-репликацией. Согласно одному варианту осуществления репликон не кодирует функциональную альфавирусную репликазу. Согласно одному варианту осуществления репликазная конструкция не содержит по меньшей мере один элемент последовательности (предпочтительно, по меньшей мере один CSE), который требуется для синтеза (-)-нити на основе (+)-нитевой матрицы и/или для синтеза (+)-нити на основе (-)-нитевой матрицы. Согласно одному варианту осуществления репликазная конструкция не содержит CSE 1 и/или CSE 4.
Предпочтительно, чтобы ни репликон в соответствии с настоящим изобретением, ни репликазная конструкция в соответствии с настоящим изобретением не содержали сигнал упаковки альфавируса. Например, сигнал упаковки альфавируса, содержащийся в кодирующей области nsP2 в SFV (White et al., 1998, J. Virol., Vol. 72, pp. 4320-4326), может быть удален, например, путем удаления или мутации. Подходящий способ удаления сигнала упаковки альфавируса предусматривает адаптацию использования кодонов в кодирующей области nsP2. Вырожденность генетического кода может позволить удалить функцию сигнала упаковки, не затрагивая аминокислотную последовательность закодированного nsP2.
Согласно одному варианту осуществления система по настоящему изобретению представляет собой выделенную систему. Согласно этому варианту осуществления система отсутствует внутри клетки, например, внутри клетки млекопитающего, или отсутствует внутри капсида вируса, например, внутри слоя, содержащего структурные белки альфавируса. Согласно одному варианту осуществления система по настоящему изобретению присутствует in vitro.
Ингибирование передачи сигналов интерферона (IFN)
Сообщалось, что жизнеспособность клеток, в которые была введена РНК для экспрессии, снижается, в частности, если клетки многократно трансфицируются с РНК. В качестве решения было обнаружено, что совместная трансфекция с ингибирующими IFN средствами повышает жизнеспособность клеток, в которых РНК должна быть экспрессирована (публикация международной заявки WO 2014/071963 A1). Любой ингибитор внутриклеточной передачи сигналов IFN или внеклеточной передачи сигналов IFN, как описано в публикации международной заявки WO 2014/071963 A1, является подходящим в настоящем изобретении. Предпочтительно ингибитор представляет собой ингибитор передачи сигналов IFN типа I.
Согласно одному варианту осуществления настоящего изобретения система по настоящему изобретению может быть разработана для улучшения трансляции, в частности для подавления негативного влияния на трансляцию. Это может предусматривать ингибирование внутриклеточного интерферона (IFN) в клетках и предотвращение вовлечения рецептора IFN с помощью внеклеточного IFN. Предотвращение вовлечения рецептора IFN с помощью внеклеточного IFN и ингибирование внутриклеточной передачи сигналов IFN в клетках делает возможной стабильную экспрессию РНК в клетках. Альтернативно или дополнительно, предотвращение вовлечения рецептора IFN с помощью внеклеточного IFN и ингибирование внутриклеточной передачи сигналов IFN повышает выживаемость клеток, в частности, если клетки повторно трансфицируют с РНК. Без ограничения теорией предполагается, что внутриклеточная передача сигналов IFN может привести к ингибированию трансляции и/или деградации РНК. Это может быть устранено путем ингибирования одного или нескольких индуцируемых IFN обладающих антивирусной активностью эффекторных белков. Индуцируемый IFN обладающий антивирусной активностью эффекторный белок может быть выбран из группы, состоящей из РНК-зависимой протеинкиназы (PKR), 2',5'-олигоаденилатсинтетазы (OAS) и RNaseL. Ингибирование внутриклеточной передачи сигналов IFN может предусматривать ингибирование PKR-зависимого пути и/или OAS-зависимого пути. Ингибирование PKR-зависимого пути может предусматривать ингибирование фосфорилирования eIF2-alpha. Ингибирование PKR может предусматривать обработку клетки по меньшей мере одним ингибитором PKR. Ингибитор PKR может представлять собой вирусный ингибитор PKR. Предпочтительный вирусный ингибитор PKR представляет собой вирус осповакцины E3. Если пептид или белок (например, E3, K3) предназначен для ингибирования внутриклеточной передачи сигналов IFN, предпочтительна внутриклеточная экспрессия пептида или белка.
Вирус осповакцины E3 представляет собой дцРНК-связывающий белок размером 25 кДа (кодируемый геном E3L), который связывается и отделяет дцРНК, чтобы предотвратить активацию PKR и OAS. E3 может связываться непосредственно с PKR и ингибировать его активность, что приводит к снижению фосфорилирования eIF2-альфа. Другими подходящими ингибиторами передачи сигналов IFN являются вирус ICP34.5 простого герпеса, вирус NSS тосканской лихорадки, вирус ядерного полиэдроза PK2 Bombyx mori и HCV NS34A.
Ингибитор внутриклеточной передачи сигналов IFN может быть предоставлен клетке в виде последовательности нуклеиновой кислоты (например, РНК), кодирующей ингибитор внутриклеточной передачи сигналов IFN.
Согласно одному варианту осуществления ингибитор внутриклеточной или внеклеточной передачи сигналов IFN кодируется молекулой мРНК. Эта молекула мРНК может содержать модифицирующую неполипептидной последовательностью модификацию, как описано в настоящем документе, например, кэп, 5’-UTR, 3’-UTR, поли(A)-последовательность, адаптацию использования кодонов.
Согласно альтернативному варианту осуществления ингибитор внутриклеточной или внеклеточной передачи сигналов IFN кодируется репликоном, предпочтительно транс-репликоном. Репликон содержит элементы последовательности нуклеиновой кислоты, которые позволяют реплицировать альфавирусную репликазу, как правило, CSE 1, CSE 2 и CSE 4; и предпочтительно также элементы последовательности нуклеиновой кислоты, которые позволяют производить субгеномный транскрипт, то есть субгеномный промотор, как правило, содержащий CSE 3. Репликон может дополнительно содержать одну или несколько модификаций, изменяющих неполипептид-кодирующие последовательности, как описано в настоящем документе, например, кэп, поли(A)-последовательность, адаптация использования кодонов.
Конструкция РНК для экспрессии альфавирусной репликазы
Согласно второму аспекту в настоящем изобретении предусмотрена конструкция РНК для экспрессии альфавирусной репликазы (репликазная конструкция), содержащая 5’-кэп для управления трансляцией репликазы. Согласно второму аспекту, возможно, нет репликона альфавируса в соответствии с настоящим изобретением. Другими словами, согласно второму аспекту настоящего изобретения описанная в настоящем документе репликазная конструкция по настоящему изобретению может быть предусмотрена независимо от репликона по настоящему изобретению. Согласно второму аспекту репликазная конструкция может быть независимо охарактеризована любым одним или несколькими особенностями репликазной конструкции согласно первому аспекту настоящего изобретения. Согласно одному варианту осуществления конструкция РНК для экспрессии альфавирусной репликазы представляет собой выделенную молекулу нуклеиновой кислоты. Это предусматривает вариант осуществления, когда она выделена, то есть практически свободна, от других молекул нуклеиновой кислоты.
Конструкция РНК согласно второму аспекту подходит, например, для комбинации с подходящим репликоном в виде системы или набора.
ДНК в соответствии с настоящим изобретением
Согласно третьему аспекту в настоящем изобретении предусмотрена ДНК, содержащая последовательность нуклеиновой кислоты, кодирующую конструкцию РНК для экспрессии альфавирусной репликазы (репликазную конструкцию) в соответствии с первым аспектом настоящего изобретения, РНК-репликон в соответствии с первым аспектом настоящего изобретения или и то и другое.
Согласно одному варианту осуществления молекула ДНК в соответствии с настоящим изобретением кодирует репликон и репликазную конструкцию системы в соответствии с первым аспектом настоящего изобретения. Согласно альтернативному варианту осуществления первая молекула ДНК кодирует один элемент РНК (репликон или репликазную конструкцию) системы в соответствии с первым аспектом настоящего изобретения, а вторая молекула ДНК кодирует соответствующий другой РНК-элемент системы в соответствии с настоящим изобретением.
Предпочтительно, ДНК является двухцепочечной.
Согласно предпочтительному варианту осуществления ДНК в соответствии с третьим аспектом настоящего изобретения представляет собой плазмиду. Используемый в настоящем документе термин «плазмида», как правило, относится к конструкции внехромосомного генетического материала, как правило, к кольцевому дуплексу ДНК, который может реплицироваться независимо от хромосомной ДНК.
ДНК по настоящему изобретению может содержать промотор, который может быть распознан ДНК-зависимой РНК-полимеразой. Это позволяет транскрибировать закодированную РНК in vivo или in vitro, например, РНК по настоящему изобретению. IVT-векторы могут использоваться стандартным образом в качестве матрицы для транскрипции in vitro. Примерами промоторов, предпочтительных в соответствии с настоящим изобретением, являются промоторы для полимеразы SP6, T3 или T7.
Согласно одному варианту осуществления ДНК по настоящему изобретению представляет собой выделенную молекулу нуклеиновой кислоты.
Способы получения РНК
Любая молекула РНК в соответствии с настоящим изобретением, будь она частью системы по настоящему изобретению или нет, может быть получена путем транскрипции in vitro. Транскрибируемая in vitro РНК (IVT-РНК) представляет особый интерес в настоящем изобретении. IVT-РНК получают путем транскрипции из молекулы нуклеиновой кислоты (в частности, молекулы ДНК). Молекулы ДНК согласно третьему аспекту настоящего изобретения пригодны для таких целей, особенно если они содержат промотор, который может быть распознан ДНК-зависимой РНК-полимеразой.
РНК в соответствии с настоящим изобретением может быть синтезирована in vitro. Это позволяет добавлять аналоги кэпа в реакцию транскрипции in vitro. Как правило, поли(A)-хвост кодируется поли(dT)-последовательностью на матрице ДНК. Альтернативно, кэпирование и добавление поли(А)-хвоста могут быть достигнуты ферментативно после транскрипции.
Специалисту в настоящей области техники известен способ транскрипции in vitro. Например, как упоминалось в публикации международной заявки WO 2011/015347 A1, множество наборов транскрипции in vitro являются коммерчески доступными.
Набор
В настоящем изобретении также предусмотрен набор, содержащий систему в соответствии с первым аспектом настоящего изобретения или конструкцию РНК для экспрессии альфавирусной репликазы в соответствии со вторым аспектом настоящего изобретения.
Согласно одному варианту осуществления составляющие набора присутствуют в виде отдельных объектов. Например, одна молекула нуклеиновой кислоты набора может присутствовать в одном объекте, а другая нуклеиновая кислота набора может присутствовать в отдельном объекте. Например, открытый или закрытый контейнер является подходящим объектом. Предпочтительным является закрытый контейнер. Используемый контейнер предпочтительно должен быть без РНКазы или по существу без РНКазы.
Согласно одному варианту осуществления набор по настоящему изобретению содержит РНК для инокуляции клетки и/или для введения человеку или животному.
Набор в соответствии с настоящим изобретением необязательно содержит этикетку или другую форму информационного элемента, например, электронный носитель данных. Этикетка или информационный элемент предпочтительно содержит инструкции, например, напечатанные инструкции или инструкции в электронной форме, которые могут быть распечатаны. Инструкции могут касаться по меньшей мере одного подходящего возможного применения набора.
Фармацевтическая композиция
Описанная в настоящем документе конструкция для экспрессии альфавирусной репликазы и/или репликона может присутствовать в форме фармацевтической композиции. Фармацевтическая композиция в соответствии с настоящим изобретением может содержать по меньшей мере одну молекулу нуклеиновой кислоты, предпочтительно РНК, в соответствии с настоящим изобретением. Фармацевтическая композиция в соответствии с настоящим изобретением содержит фармацевтически приемлемый разбавитель и/или фармацевтически приемлемое вспомогательное вещество, и/или фармацевтически приемлемый носитель, и/или фармацевтически приемлемый наполнитель. Выбор фармацевтически приемлемого носителя, наполнителя, вспомогательного вещества или разбавителя конкретно не ограничен. Можно использовать любой подходящий фармацевтически приемлемый носитель, наполнитель, вспомогательное вещество или разбавитель, известный в настоящей области техники.
Согласно одному варианту осуществления настоящего изобретения фармацевтическая композиция может дополнительно содержать такой растворитель, как водный растворитель или любой растворитель, который позволяет сохранить целостность РНК. Согласно предпочтительному варианту осуществления фармацевтическая композиция представляет собой водный раствор, содержащий РНК. Водный раствор может необязательно содержать растворенные вещества, например, соли.
Согласно одному варианту осуществления настоящего изобретения фармацевтическая композиция находится в форме лиофилизированной композиции. Лиофилизированную композицию можно получить путем лиофилизации соответствующей водной композиции.
Согласно одному варианту осуществления фармацевтическая композиция содержит по меньшей мере один катионный объект. Как правило, катионные липиды, катионные полимеры и другие вещества с положительными зарядами могут образовывать комплексы с отрицательно заряженными нуклеиновыми кислотами. Можно стабилизировать РНК в соответствии с настоящим изобретением путем комплексообразования с катионными соединениями, предпочтительно поликатионными соединениями, такими как, например, катионный или поликатионный пептид или белок. Согласно одному варианту осуществления фармацевтическая композиция в соответствии с настоящим изобретением содержит по меньшей мере одну катионную молекулу, выбранную из группы, содержащей протамин, полиэтиленимин, поли-L-лизин, поли-L-аргинин, гистон или катионный липид.
В соответствии с настоящим изобретением катионный липид представляет собой катионную амфифильную молекулу, например, молекулу, которая содержит по меньшей мере один гидрофильный и липофильный фрагменты. Катионный липид может быть монокатионным или поликатионным. Катионные липиды, как правило, содержат липофильный фрагмент, такой как стерол, ацильную или диацильную цепь, и характеризуются общим положительным зарядом. Головная группа липида, как правило, несет положительный заряд. Катионный липид предпочтительно имеет положительный заряд от 1 до 10 валентностей, более предпочтительно положительный заряд составляет от 1 до 3 валентностей и более предпочтительно положительный заряд составляет 1 валентность. Примеры катионных липидов включают в себя, без ограничения, 1,2-ди-O-октадеценил-3-триметиламмонийпропан (DOTMA); диметилдиоктадециламмоний (DDAB); 1,2-диолеил-3-триметиламмонийпропан (DOTAP); 1,2-диолеил-3-диметиламмонийпропан (DODAP); 1,2-диацилокси-3-диметиламмонийпропаны; 1,2-диалкилокси-3-диметиламмонийпропаны; хлорид диоктадецилдиметиламмония (DODAC), 1,2-димиристоилоксипропил-1,3-диметилгидроксиэтиламмоний (DMRIE) и трифторацетат 2,3-диолеилокси-N-[2(сперминкарбоксамид)этил]-N,N-диметил-1-пропанамида (DOSPA). Катионные липиды также включают в себя липиды с третичной аминогруппой, включая в себя 1,2-дилинолилокси-N,N-диметил-3-аминопропан (DLinDMA). Катионные липиды подходят для получения составов РНК в липидных составах, как описано в настоящем документе, таких как липосомы, эмульсии и липоплексы. Как правило, положительные заряды вносятся по меньшей мере одним катионным липидом, а отрицательные заряды вносят РНК. Согласно одному варианту осуществления фармацевтическая композиция содержит по меньшей мере один вспомогательный липид, в дополнение к катионному липиду. Вспомогательный липид может быть нейтральным или анионным липидом. Вспомогательный липид может представлять собой природный липид, такой как фосфолипид, или аналог природного липида, или полностью синтетический липид, или липидоподобную молекулу, не имеющую сходства с природными липидами. В случае, когда фармацевтическая композиция содержит как катионный липид, так и вспомогательный липид, молярное отношение катионного липида к нейтральному липиду может быть соответствующим образом определено с учетом стабильности состава и тому подобного.
Согласно одному варианту осуществления фармацевтическая композиция в соответствии с настоящим изобретением содержит протамин. В соответствии с настоящим изобретением протамин применим в качестве катионного средства-носителя. Термин «протамин» относится к любому из различных сильноосновных белков с относительно низкой молекулярной массой, которые богаты аргинином и встречаются, в частности, с ДНК вместо соматических гистонов в клетках спермы животных, таких как рыба. В частности, термин «протамин» относится к белкам, обнаруженным в сперме рыб, которые являются сильноосновными, растворимы в воде, не коагулируют при нагревании и содержат несколько мономеров аргинина. В соответствии с настоящим изобретением используемый в настоящем документе термин «протамин» подразумевает, что он содержит любую аминокислотную последовательность протаминов, полученную или происходящую из природных или биологических источников, включая в себя их фрагменты и мультимерные формы указанной аминокислотной последовательности или ее фрагмента. Кроме того, этот термин охватывает (синтезированные) полипептиды, которые являются искусственными и специально разработаны для конкретных целей и не могут быть выделены из природных или биологических источников.
Согласно некоторым вариантам осуществления композиции по настоящему изобретению могут содержать один или несколько адъювантов. Адъюванты могут быть добавлены к вакцинам для стимуляции ответа иммунной системы; адъюванты, как правило, не обеспечивают иммунитет сами. Иллюстративные адъюванты включают в себя, без ограничения, следующие: неорганические соединения (например, квасцы, гидроксид алюминия, фосфат алюминия, гидроксид фосфата кальция); минеральное масло (например, парафиновое масло), цитокины (например, IL-1, IL-2, IL-12); иммуностимулирующий полинуклеотид (такой как РНК или ДНК, например, CpG-содержащие олигонуклеотиды); сапонины (например, сапонины растений из килайи, сои, Polygala senega); масляные эмульсии или липосомы; полиоксиэтиленовый эфир и полиоксиэтиленовые сложные эфиры; полифосфазен (PCPP); мурамиловые пептиды; соединения имидазохинолинов; тиосемикарбазоновые соединения; лиганд Flt3 (публикация международной заявки WO 2010/066418 A1) или любой другой адъювант, который известен специалисту в настоящей области техники. Предпочтительным адъювантом для введения РНК в соответствии с настоящим изобретением является лиганд Flt3 (публикация международной заявки WO 2010/066418 A1). Когда лиганд Flt3 вводят вместе с РНК, которая кодирует антиген, может наблюдаться сильное увеличение антигенспецифических CD8+ Т-клеток.
Фармацевтической композиции согласно изобретению можно придать буферные свойства (например, ацетатным буфером, цитратным буфером, сукцинатным буфером, трис-буфером, фосфатным буфером).
РНК-содержащие частицы
Согласно некоторым вариантам осуществления из-за неустойчивости незащищенной РНК предпочтительно предоставлять молекулы РНК по настоящему изобретению в виде комплексов или в инкапсулированной форме. Соответствующие фармацевтические композиции предусмотрены в настоящем изобретении. В частности, согласно некоторым вариантам осуществления фармацевтическая композиция по настоящему изобретению содержит содержащие нуклеиновую кислоту частицы, предпочтительно содержащие РНК частицы. Соответствующие фармацевтические композиции называются состоящими из частиц составами. В состоящих из частиц составах в соответствии с настоящим изобретением частица содержит нуклеиновую кислоту в соответствии с настоящим изобретением и фармацевтически приемлемый носитель или фармацевтически приемлемый наполнитель, который подходит для доставки нуклеиновой кислоты. Содержащие нуклеиновую кислоту частицы могут быть, например, в форме белковых частиц или в виде липидсодержащих частиц. Подходящие белки или липиды называются образующими частицы средствами. Белковые частицы и липидсодержащие частицы были описаны ранее, как пригодные для доставки альфавирусной РНК в форме частиц (например, публикация Strauss & Strauss, Microbiol. Rev., 1994, vol. 58, pp. 491-562). В частности, структурные белки альфавируса (предоставленные, например, вирусом-помощником) являются подходящим носителем для доставки РНК в форме белковых частиц.
Когда система в соответствии с настоящим изобретением составлена в виде состоящего из частиц состава, возможно, что каждый вид РНК (например, репликон, репликазная конструкция и необязательные дополнительные виды РНК, такие как РНК, кодирующая белок, подходящий для ингибирования IFN), отдельно составляется в виде отдельного состоящего из частиц состава. В этом случае каждый отдельный состоящий из частиц состав будет содержать один вид РНК. Отдельные состоящие из частиц составы могут присутствовать в виде отдельных объектов, например, в отдельных контейнерах. Такие составы можно получить, предоставляя каждый вид РНК отдельно (обычно каждый в форме РНК-содержащего раствора) вместе с образующим частицы средством, тем самым позволяя образовывать частицы. Соответствующие частицы будут содержать исключительно специфические виды РНК, которые предоставляются, когда образуются частицы (отдельные состоящие из частиц составы).
Согласно одному варианту осуществления фармацевтическая композиция в соответствии с настоящим изобретением содержит более одного отдельного состоящего из частиц состава. Соответствующие фармацевтические композиции называются смешанными состоящими из частиц составами. Смешанные состоящие из частиц составы согласно настоящему изобретению можно получить, образуя, раздельно, отдельные состоящие из частиц составы, как описано выше, с последующей стадией смешивания отдельных состоящих из частиц составов. На стадии смешивания можно получить один состав, содержащий смешанную популяцию РНК-содержащих частиц (для иллюстрации: например, первая популяция частиц может содержать репликон в соответствии с настоящим изобретением, а второй состав частиц может содержать репликазную конструкцию в соответствии с настоящим изобретением). Отдельные состоящие из частиц популяции могут быть вместе в одном контейнере, состоящем из смешанной популяции отдельных состоящих из частиц составов.
Альтернативно, возможно, что все виды РНК фармацевтической композиции (например, репликон, репликазная конструкция и необязательные дополнительные виды, такие как РНК, кодирующая белок, подходящий для ингибирования IFN), составляют вместе в виде комбинированного состоящего из частиц состава. Такие составы можно получить путем обеспечения комбинированного состава (как правило, комбинированного раствора) всех видов РНК вместе с образующим частицы средством, тем самым позволяя образовывать частицы. В отличие от смешанного состоящего из частиц состава комбинированный состоящий из частиц состав, как правило, содержит частицы, которые содержат более одного вида РНК. В комбинированном состоящем из частиц составе различные виды РНК, как правило, присутствуют вместе в одной частице.
Согласно одному варианту осуществления состоящий из частиц состав по настоящему изобретению представляет собой состоящий из наночастиц состав. Согласно этому варианту осуществления композиция в соответствии с настоящим изобретением содержит нуклеиновую кислоту в соответствии с настоящим изобретением в форме наночастиц. Состоящие из наночастиц составы могут быть получены посредством различных протоколов и с различными комплексообразующими соединениями. Липиды, полимеры, олигомеры или амфифилы являются типичными составляющими состоящих из наночастиц составов.
Используемый в настоящем документе термин «наночастица» относится к любой частице, имеющей диаметр, который делает частицу подходящей для системного, в частности парентерального, введения, в частности нуклеиновые кислоты, как правило, диаметром 1000 нанометров (нм) или менее. Согласно одному варианту осуществления наночастицы характеризуются средним диаметром в диапазоне от приблизительно 50 нм до приблизительно 1000 нм, предпочтительно от приблизительно 50 нм до приблизительно 400 нм, предпочтительно от приблизительно 100 нм до приблизительно 300 нм, например, от приблизительно 150 нм до приблизительно 200 нм. Согласно одному варианту осуществления наночастицы характеризуются диаметром в диапазоне от приблизительно 200 до приблизительно 700 нм, от приблизительно 200 до приблизительно 600 нм, предпочтительно от приблизительно 250 до приблизительно 550 нм, в частности от приблизительно 300 до приблизительно 500 нм или от приблизительно 200 до приблизительно 400 нм.
Согласно одному варианту осуществления показатель полидисперсности (PI) описанных в настоящем документе наночастиц, измеренный динамическим рассеянием света, составляет 0,5 или менее, предпочтительно 0,4 или менее или даже более предпочтительно 0,3 или менее. «Индекс полидисперсности» (PI) представляет собой измерение однородного или гетерогенного распределения по размеру отдельных частиц (таких как липосомы) в смеси частиц и указывает ширину распределения частиц в смеси. PI можно определить, например, как описано в публикации международной заявки WO 2013/143555 A1.
Используемый в настоящем документе термин «состоящий из наночастиц состав» или аналогичные термины относятся к любому состоящему из частиц составу, содержащему по меньшей мере одну наночастицу. Согласно некоторым вариантам осуществления состоящая из наночастиц композиция представляет собой однородный набор наночастиц. Согласно некоторым вариантам осуществления состоящая из наночастиц композиция представляет собой липидсодержащий фармацевтический состав, такой как липосомный состав или эмульсия.
Липидсодержащие фармацевтические композиции
Согласно одному варианту осуществления фармацевтическая композиция по настоящему изобретению содержит по меньшей мере один липид. Предпочтительно, по меньшей мере один липид представляет собой катионный липид. Указанная липидсодержащая фармацевтическая композиция содержит нуклеиновую кислоту в соответствии с настоящим изобретением. Согласно одному варианту осуществления фармацевтическая композиция в соответствии с настоящим изобретением содержит РНК, инкапсулированную в везикуле, например, в липосоме. Согласно одному варианту осуществления фармацевтическая композиция в соответствии с настоящим изобретением содержит РНК в форме эмульсии. Согласно одному варианту осуществления фармацевтическая композиция в соответствии с настоящим изобретением содержит РНК в комплексе с катионным соединением, образуя, например, так называемые липоплексы или полиплексы. Инкапсуляция РНК в везикулах, таких как липосомы, отличается, например, от комплексов липид/РНК. Комплексы липид/РНК могут быть получены, например, когда РНК, например, смешивают с предварительно образованными липосомами.
Согласно одному варианту осуществления фармацевтическая композиция в соответствии с настоящим изобретением содержит РНК, инкапсулированную в везикулу. Такой состав представляет собой конкретный состоящий из частиц состав в соответствии с настоящим изобретением. Везикула представляет собой липидный бислой, свернутый в сферическую оболочку, вмещающий небольшое пространство и отделяющий это пространство от пространства вне везикулы. Как правило, пространство внутри везикулы представляет собой водное пространство, т.е. содержит воду. Как правило, пространство вне везикулы представляет собой водное пространство, т.е. содержит воду. Липидный бислой образован одним или несколькими липидами (образующими везикулы липидами). Мембрана, вмещающая везикулу, представляет собой ламеллярную фазу, аналогичную таковой плазматической мембраны. Везикула в соответствии с настоящим изобретением может представлять собой многослойную везикулу, однослойную везикулу или их смесь. При инкапсулировании в везикулу РНК, как правило, отделена от любой внешней среды. Таким образом, она присутствует в защищенной форме, функционально эквивалентной защищенной форме в природном альфавирусе. Подходящими везикулами являются частицы, особенно наночастицы, как описано в настоящем документе.
Например, РНК может быть инкапсулирована в липосому. Согласно этому варианту осуществления фармацевтическая композиция представляет собой или содержит липосомный состав. Инкапсуляция внутри липосомы, как правило, будет защищать РНК от расщепления РНКазой. Возможно, что липосомы включают в себя некоторую внешнюю РНК (например, на своей поверхности), но по меньшей мере половина РНК (а в идеале вся она) инкапсулируется в сердцевине липосомы.
Липосомы представляют собой микроскопические липидные везикулы, часто содержащие один или несколько бислоев образующего везикулы липида, такого как фосфолипид, и способны инкапсулировать лекарственное средство, например, РНК. В контексте настоящего изобретения могут быть использованы различные типы липосом, включая в себя, без ограничения, многослойные везикулы (MLV), небольшие однослойные везикулы (SUV), большие однослойные везикулы (LUV), стерически стабилизированные липосомы (SSL), мультивезикулярные везикулы (MV) и большие мультивезикулярные везикулы (LMV), а также другие двуслойные формы, известные в настоящей области техники. Размер и слойность липосомы будут зависеть от способа получения. Существует несколько других форм супрамолекулярной организации, в которых липиды могут присутствовать в водной среде, включая в себя ламеллярные фазы, гексагональную и обратную гексагональные фазы, кубические фазы, мицеллы, обратные мицеллы, состоящие из монослоев. Эти фазы также могут быть получены в комбинации с ДНК или РНК, а взаимодействие с РНК и ДНК может существенно влиять на фазовое состояние. Такие фазы могут присутствовать в состоящих из наночастиц РНК составах по настоящему изобретению.
Липосомы могут быть образованы с использованием стандартных способов, известных специалисту в настоящей области техники. Соответствующие способы предусматривают способ обратного испарения, способ инъекции этанола, способ регидратации дегидратации, ультразвук или другие подходящие способы. После образования липосом липосомы могут быть отсортированы по размеру для получения популяции липосом, характеризующихся по существу однородным диапазоном размеров.
Согласно предпочтительному варианту осуществления настоящего изобретения РНК присутствует в липосоме, которая содержит по меньшей мере один катионный липид. Соответствующие липосомы могут быть образованы из одного липида или из смеси липидов при условии использования по меньшей мере одного катионного липида. Предпочтительные катионные липиды содержат атом азота, который способен к протонированию; предпочтительно такие катионные липиды представляют собой липиды с третичной аминогруппой. Особенно подходящим липидом с третичной аминогруппой является 1,2-дилинолеилокси-N,N-диметил-3-аминопропан (DLinDMA). Согласно одному варианту осуществления РНК в соответствии с настоящим изобретением присутствует в составе липосом, как описано в публикации международной заявки WO 2012/006378 A1: липосома, содержащая липидный бислой, инкапсулирующий водную сердцевину, содержащую РНК, причем липидный бислой содержит липид с pKa в диапазоне от 5,0 до 7,6, который предпочтительно содержит третичную аминогруппу. Предпочтительные катионные липиды с третичной аминогруппой содержат DLinDMA (pKa 5.8) и, как правило, описаны в публикации международной заявки WO 2012/031046 A2. Согласно публикации международной заявки WO 2012/031046 A2 липосомы, содержащие соответствующее соединение, особенно подходят для инкапсуляции РНК и, следовательно, для липосомной доставки РНК. Согласно одному варианту осуществления РНК в соответствии с настоящим изобретением присутствует в составе липосом, причем липосома содержит по меньшей мере один катионный липид, головная группа которого содержит по меньшей мере один атом азота (N), который способен к протонированию, причем липосома и РНК имеет отношение N:P от 1:1 до 20:1. В соответствии с настоящим изобретением «отношение N:P» относится к молярному соотношению атомов азота (N) в катионном липиде к атомам фосфата (Р) в РНК, содержащейся в липидсодержащей частице (например, липосоме), как описано в публикации международной заявки WO 2013/006825 A1. Отношение N:P от 1:1 до 20:1 связано с суммарным зарядом липосомы и эффективностью доставки РНК в клетку позвоночных.
Согласно одному варианту осуществления РНК в соответствии с настоящим изобретением присутствует в липосомном составе, который содержит по меньшей мере один липид, который включает в себя фрагмент полиэтиленгликоля (ПЭГ), причем РНК инкапсулируется в пегилированную липосому, так что фрагмент ПЭГ присутствует на внешней стороне липосомы, как описано в публикациях международных заявок WO 2012/031043 A1 и WO 2013/033563 A1.
Согласно одному варианту осуществления РНК в соответствии с настоящим изобретением присутствует в составе липосом, причем липосома характеризуется диаметром в диапазоне 60-180 нм, как описано в публикации международной заявки WO 2012/030901 A1.
Согласно одному варианту осуществления РНК в соответствии с настоящим изобретением присутствует в составе липосом, причем РНК-содержащие липосомы характеризуются суммарным зарядом, близким к нулю или отрицательным, как описано в публикации международной заявки WO 2013/143555 A1.
Согласно другим вариантам осуществления РНК в соответствии с настоящим изобретением присутствует в форме эмульсии. Ранее были описаны эмульсии для доставки молекул нуклеиновых кислот, таких как молекулы РНК, в клетки. Предпочтительными в настоящем документе являются эмульсии масло-в-воде. Соответствующие частицы эмульсии содержат сердцевину-масло и катионный липид. Более предпочтительными являются катионные эмульсии масло-в-воде, в которых РНК в соответствии с настоящим изобретением образует комплексы с частицами эмульсии. Частицы эмульсии содержат сердцевину-масло и катионный липид. Катионный липид может взаимодействовать с отрицательно заряженной РНК, тем самым привязывая РНК к частицам эмульсии. В эмульсии масло-в-воде частицы эмульсии диспергируют в водной дисперсионной фазе. Например, средний диаметр частиц эмульсии, как правило, может составлять от приблизительно 80 до 180 нм. Согласно одному варианту осуществления фармацевтическая композиция по настоящему изобретению представляет собой катионную эмульсию масло-в-воде, причем частицы эмульсии содержат сердцевину-масло и катионный липид, как описано в публикации международной заявки WO 2012/006380 A2. РНК в соответствии с настоящим изобретением может присутствовать в форме эмульсии, содержащей катионный липид, причем отношение N:P эмульсии составляет по меньшей мере 4:1, как описано в публикации международной заявки WO 2013/006834 A1. РНК в соответствии с настоящим изобретением может присутствовать в форме катионной липидной эмульсии, как описано в публикации международной заявки WO 2013/006837 A1. В частности, композиция может содержать РНК, образовавшую комплекс с частицей катионной эмульсии масло-в-воде, причем отношение масло/липид составляет по меньшей мере приблизительно 8:1 (моль:моль).
Согласно другим вариантам осуществления фармацевтическая композиция в соответствии с настоящим изобретением содержит РНК в формате липоплекса. Термин «липоплекс» или «РНК-липоплекс» относится к комплексу липидов и нуклеиновых кислот, таких как РНК. Липоплексы могут образовываться из катионных (положительно заряженных) липосом и анионной (отрицательно заряженной) нуклеиновой кислоты. Катионные липосомы могут также содержать нейтральный липид-«помощник». В простейшем случае липоплексы образуются спонтанно путем смешивания нуклеиновой кислоты с липосомами с определенным протоколом смешивания, однако могут применяться различные другие протоколы. Понятно, что электростатические взаимодействия между положительно заряженными липосомами и отрицательно заряженной нуклеиновой кислотой являются движущей силой образования липоплекса (публикация международной заявки WO 2013/143555 A1). Согласно одному варианту осуществления настоящего изобретения суммарный заряд частиц липоплекса РНК близок к нулю или отрицателен. Известно, что электро-нейтральные или отрицательно заряженные липоплексы РНК и липосом приводят к значительной экспрессии РНК в дендритных клетках селезенки (DC) после системного введения и не связаны с повышенной токсичностью, о которой сообщалось для положительно заряженных липосом и липоплексов (смотрите публикацию международной заявки WO 2013/143555 A1). Поэтому согласно одному варианту осуществления настоящего изобретения фармацевтическая композиция в соответствии с настоящим изобретением содержит РНК в формате наночастиц, предпочтительно наночастиц-липоплексов, в которых (i) число положительных зарядов в наночастицах не превышает число отрицательных зарядов в наночастицах и/или (ii) наночастицы характеризуются нейтральным или суммарным отрицательным зарядом, и/или (iii) отношение зарядов положительных зарядов к отрицательным зарядам в наночастицах составляет 1,4:1 или менее, и/или (iv) зета-потенциал наночастиц составляет 0 или менее. Как описано в публикации международной заявки WO 2013/143555 A1, зета-потенциал представляет собой научный термин для электрокинетического потенциала в коллоидных системах. В настоящем изобретении (а) зета-потенциал и (b) отношение заряда катионного липида к РНК в наночастицах может быть рассчитано как описано в публикации международной заявки WO 2013/143555 A1. Таким образом, фармацевтические композиции, представляющие собой состоящие из наночастиц-липоплексов составы с определенным размером частиц, в которых суммарный заряд частиц близок к нулю или отрицателен, как описано в публикации международной заявки WO 2013/143555 A1, представляют собой предпочтительные фармацевтические композиции в контексте настоящего изобретения.
Способы получения белка
Согласно четвертому аспекту в настоящем изобретении предусмотрен способ получения белка в клетке, предусматривающий следующие стадии:
(а) получение конструкции РНК для экспрессии альфавирусной репликазы,
(b) получение РНК-репликона, который может быть реплицирован репликазой in trans и содержит открытую рамку считывания, кодирующую белок, и
(c) инокуляция смеси конструкции РНК для экспрессии альфавирусной репликазы и РНК-репликона в клетку,
причем конструкция РНК для экспрессии альфавирусной репликазы содержит 5’-кэп для трансляции репликазы.
Конструкция РНК для экспрессии альфавирусной репликазы согласно (а) может быть охарактеризована посредством любой одной или нескольких особенностей репликазной конструкции, содержащейся в системе в соответствии с первым аспектом настоящего изобретения.
РНК-репликон в соответствии с (b) может быть охарактеризован посредством любой одной или нескольких особенностей репликона, содержащегося в системе в соответствии с первым аспектом настоящего изобретения.
Согласно одному варианту осуществления конструкция РНК для экспрессии альфавирусной репликазы согласно (а) и РНК-репликон согласно (b), используемые в способе получения белка в клетке, представляют собой составляющие системы в соответствии с настоящим изобретением.
Клетка, в которую можно инокулировать одну или несколько молекул нуклеиновой кислоты, можно назвать «клеткой-хозяином». В соответствии с настоящим изобретением термин «клетка-хозяин» относится к любой клетке, которая может быть трансформирована или трансфицирована экзогенной молекулой нуклеиновой кислоты. Термин «клетка» предпочтительно представляет собой интактную клетку, т.е. клетку с неповрежденной мембраной, которая не высвобождает свои нормальные внутриклеточные компоненты, такие как ферменты, органеллы или генетический материал. Интактная клетка предпочтительно представляет собой жизнеспособную клетку, т.е. живую клетку, способную выполнять свои нормальные метаболические функции. Термин «клетка-хозяин» включает в себя, в соответствии с настоящим изобретением, прокариотические (например, E.coli) или эукариотические клетки (например, клетки человека и животных и клетки насекомых). Особое предпочтение отдается клеткам млекопитающих, таким как клетки людей, мышей, хомяков, свиней, домашних животных, включая в себя лошадей, коров, овец и коз, а также приматов. Клетки могут быть получены из множества типов тканей и содержать первичные клетки и клеточные линии. Конкретные примеры включают в себя кератиноциты, лейкоциты периферической крови, стволовые клетки костного мозга и эмбриональные стволовые клетки. Согласно другим вариантам осуществления клетка-хозяин представляет собой антигенпрезентирующую клетку, в частности дендритную клетку, моноцит или макрофаг. Нуклеиновая кислота может присутствовать в клетке-хозяине в одной или нескольких копиях и согласно одному варианту осуществления экспрессируется в клетке-хозяине.
Клетка может представлять собой прокариотическую клетку или эукариотическую клетку. Прокариотические клетки пригодны в настоящем документе, например, для увеличения количества ДНК в соответствии с настоящим изобретением, а эукариотические клетки пригодны в настоящем документе, например, для экспрессии открытой рамки считывания репликона.
В способе по настоящему изобретению можно использовать любое из системы в соответствии с настоящим изобретением или набора в соответствии с настоящим изобретением, или фармацевтической композиции в соответствии с настоящим изобретением. РНК может быть использована в форме фармацевтической композиции или в виде голой РНК, например, для электропорации. Ранее была описана инокуляция содержащих РНК композиций в клетки, а также электропорация голой РНК в клетки (смотрите ссылки, приведенные в настоящем документе в разделе, посвященном фармацевтическим композициям в соответствии с настоящим изобретением).
Согласно способу настоящего изобретения может быть достигнута эффективная экспрессия представляющего интерес гена в клетке-хозяине (смотрите, например, примеры 1 и 2).
В способе получения белка в клетке в соответствии с настоящим изобретением различные молекулы РНК в соответствии с первым аспектом (репликон и репликазная конструкция) могут быть либо инокулированы в один и тот же момент времени, либо их можно альтернативно инокулировать в разные моменты времени. Во втором случае репликазную конструкцию, как правило, инокулируют в первый момент времени, а репликон, как правило, инокулируют во второй, более поздний, момент времени. В этом случае предполагается, что репликон будет немедленно реплицирован, поскольку репликаза уже будет транслирована в клетке. Второй момент времени, как правило, происходит вскоре после первого момента времени, например, через от 1 минуты до 24 часов после первого момента времени.
Согласно одному варианту осуществления дополнительная молекула РНК, предпочтительно молекула мРНК, может быть введена в клетку. Необязательно, дополнительная молекула РНК кодирует белок, подходящий для ингибирования IFN, такой как E3, как описано в настоящем документе. Необязательно, дополнительная молекула РНК может быть введена до введения репликона или репликазной конструкции или системы согласно настоящему изобретению.
В способе получения белка в клетке в соответствии с настоящим изобретением клетка может представлять собой антигенпрезентирующую клетку, и этот способ может быть использован для экспрессии РНК, кодирующей антиген. С этой целью настоящее изобретение может предусматривать введение антигена, кодирующего РНК, в антигенпрезентирующие клетки, такие как дендритные клетки. Для трансфекции антигенпрезентирующих клеток, таких как дендритные клетки, может быть использована фармацевтическая композиция, содержащая кодирующую антиген РНК.
Согласно одному варианту осуществления способ получения белка в клетке представляет собой способ in vitro. Согласно одному варианту осуществления способ получения белка в клетке не предусматривает удаление клетки из субъекта-человека или субъекта-животного хирургическим путем или терапией.
Согласно этому варианту осуществления клетка, инокулированная в соответствии с четвертым аспектом настоящего изобретения, может вводиться субъекту, чтобы производить белок у субъекта и обеспечивать субъекта белком. Клетка может быть аутологичной, сингенной, аллогенной или гетерологичной по отношению к субъекту.
Согласно другому варианту осуществления клетка в способе получения белка в клетке может присутствовать у субъекта, такого как пациент. Согласно этому варианту осуществления способ получения белка в клетке представляет собой способ in vivo, который предусматривает введение молекулы РНК субъекту.
В этом отношении в настоящем изобретении также предусмотрен способ получения белка у субъекта, предусматривающий следующие стадии:
(а) получение конструкции РНК для экспрессии альфавирусной репликазы,
(b) получение РНК-репликона, который может быть реплицирован репликазой in trans, и содержит открытую рамку считывания, кодирующую белок, и
(c) введение конструкции РНК для экспрессии альфавирусной репликазы и репликона РНК субъекту,
причем конструкция РНК для экспрессии альфавирусной репликазы содержит 5’-кэп для управления трансляцией репликазы.
Конструкция РНК для экспрессии альфавирусной репликазы согласно (а) может быть охарактеризована любой одной или несколькими особенностями репликазной конструкции, содержащейся в системе в соответствии с первым аспектом настоящего изобретения. Конструкцию РНК согласно (а) можно получить, например, как описано в настоящем документе.
РНК-репликон в соответствии с (b) может быть охарактеризован любым одним или несколькими особенностями репликона, содержащегося в системе в соответствии с первым аспектом настоящего изобретения. Предпочтительно репликон в соответствии с (b) кодирует фармацевтически активный пептид или белок в качестве представляющего интерес белка. Согласно одному варианту осуществления фармацевтически активный пептид или белок представляет собой иммунологически активное соединение или антиген. РНК-репликон в соответствии с (b) может быть получен, например, как описано в настоящем документе. Способ получения белка у субъекта в соответствии с настоящим изобретением особенно подходит для профилактических и терапевтических применений. Предпочтительно, в способе получения белка у субъекта РНК-репликон кодирует в качестве представляющего интерес гена фармацевтически активный белок или полипептид.
В способе получения белка у субъекта репликазную конструкцию РНК в соответствии с (а) и репликон в соответствии с (b) можно вводить либо в один и тот же момент времени, либо альтернативно вводить в разные моменты времени. Во втором случае репликазную конструкцию согласно (а), как правило, вводят в первый момент времени, а репликон согласно (b), как правило, вводят во второй, более поздний, момент времени. В этом случае предполагается, что репликон будет немедленно реплицирован, поскольку репликаза уже будет транслирована в клетке. Второй момент времени, как правило, происходит вскоре после первого момента времени, например, через от 1 минуты до 24 часов после первого момента времени. Предпочтительно введение репликона проводят в одном и том же месте и посредством одного и того же пути введения, что и введение репликазной конструкции, с тем чтобы увеличить перспективы того, что репликон и репликазная конструкция достигают одной и той же целевой ткани или клетки. «Место» относится к части тела субъекта. Подходящими местами являются, например, левая рука, правая рука и т.д.
Согласно одному варианту осуществления субъекту может быть введена дополнительная молекула РНК, предпочтительно молекула мРНК. Необязательно, дополнительная молекула РНК кодирует белок, подходящий для ингибирования IFN, такой как E3, как описано в настоящем документе. Необязательно, дополнительную молекулу РНК можно вводить перед введением репликона или репликазной конструкции или системы согласно настоящему изобретению.
Любое из системы в соответствии с настоящим изобретением или набора в соответствии с настоящим изобретением, или фармацевтической композиции в соответствии с настоящим изобретением может быть использовано в способе получения белка у субъекта в соответствии с настоящим изобретением. Например, в способе по настоящему изобретению РНК может быть использована в форме фармацевтической композиции, например, как описано в настоящем документе, или в виде голой РНК. Введение фармацевтических композиций, содержащих РНК, было описано ранее, смотрите, например, ссылки, приведенные в настоящем документе в разделе, описывающем фармацевтические композиции в соответствии с настоящим изобретением.
Принимая во внимание потенциальную возможность, подлежащую введению субъекту, каждая система в соответствии с настоящим изобретением или набор в соответствии с настоящим изобретением, или фармацевтическая композиция в соответствии с настоящим изобретением могут упоминаться как «лекарственное средство» или тому подобное. Настоящее изобретение предусматривает, что система, набор и/или фармацевтическая композиция по настоящему изобретению предназначены для применения в качестве лекарственного средства. Лекарственное средство можно использовать для лечения субъекта. Под «лечением» подразумевается введение соединения или композиции или другого объекта, как описано в настоящем документе, субъекту. Термин включает в себя способы лечения организма человека или животного путем терапии.
Вышеописанное лекарственное средство, как правило, не содержит ДНК и, таким образом, связано с дополнительными особенностями безопасности по сравнению с ДНК-вакцинами, описанными в предшествующем уровне техники (например, в публикации международной заявки WO 2008/119827 A1).
Альтернативное медицинское применение в соответствии с настоящим изобретением предусматривает способ получения белка в клетке в соответствии с четвертым аспектом настоящего изобретения, причем клетка может представлять собой антигенпрезентирующую клетку, такую как дендритная клетка, с последующим введением указанной клетки субъекту. Например, система, содержащая репликон, кодирующий фармацевтически активный белок, такой как антиген, может быть введена (трансфицирована) в антигенпрезентирующие клетки ex vivo, например, антигенпрезентирующие клетки, взятые у субъекта, и антигенпрезентирующие клетки, необязательно клонированно размноженные ex vivo, могут быть повторно введены одному и тому же или другому субъекту. Трансфицированные клетки могут быть повторно введены субъекту с использованием любых средств, известных в настоящей области техники.
Лекарственное средство в соответствии с настоящим изобретением может вводиться нуждающемуся в этом субъекту. Лекарственное средство по настоящему изобретению может быть использовано как в профилактических, так и в терапевтических способах лечения субъекта.
Лекарственное средство в соответствии с настоящим изобретением вводят в эффективном количестве. «Эффективное количество» относится к количеству, которого достаточно, отдельно или вместе с другими дозами, чтобы вызвать реакцию или желаемый эффект. В случае лечения определенного заболевания или определенного состояния у субъекта желаемым эффектом является ингибирование прогрессирования заболевания. Это включает в себя замедление прогрессирования заболевания, в частности прерывание прогрессирования заболевания. Желаемый эффект при лечении заболевания или состояния может также представлять собой задержку вспышки заболевания или ингибирование вспышки заболевания.
Эффективное количество будет зависеть от подвергаемого лечению состояния, тяжести заболевания, индивидуальных параметров пациента, включающих в себя возраст, физиологическое состояние, размер и массу, продолжительности лечения, типа сопровождающей терапии (если таковая имеется), конкретного способа введения и других факторов.
Вакцинация
Термин «иммунизация» или «вакцинация», как правило, относится к процессу лечения субъекта по терапевтическим или профилактическим причинам. Лечение, в частности профилактическое лечение, представляет собой или предусматривает, предпочтительно, лечение, направленное на индуцирование или усиление иммунного ответа субъекта, например, против одного или нескольких антигенов. Если в соответствии с настоящим изобретением желательно индуцировать или усиливать иммунный ответ с использованием РНК, как описано в настоящем документе, иммунный ответ может быть вызван или усилен посредством РНК. Согласно одному варианту осуществления в настоящем изобретении предусмотрено профилактическое лечение, которое представляет собой или предусматривает предпочтительно вакцинацию субъекта. Вариант осуществления настоящего изобретения, при котором репликон кодирует в качестве представляющего интерес белка фармацевтически активный пептид или белок, который является иммунологически активным соединением или антигеном, особенно применим для вакцинации.
Ранее была описана РНК для вакцинации против чужеродных патогенов, включающих в себя патогены или злокачественную опухоль (недавно рассмотренная в публикации Ulmer et al., 2012, Vaccine, vol. 30, pp. 4414-4418). В отличие от общих подходов в предшествующем уровне техники репликон в соответствии с настоящим изобретением является особенно подходящим элементом для эффективной вакцинации из-за способности реплицироваться in trans с помощью репликазы, кодируемой репликазной конструкцией по настоящему изобретению. Вакцинация в соответствии с настоящим изобретением может быть использована, например, для индукции иммунного ответа на слабо иммуногенные белки. В случае РНК-вакцин согласно настоящему изобретению белковый антиген никогда не подвергается воздействию сывороточных антител, а производится самими трансфицированными клетками после трансляции РНК. Поэтому анафилаксия не должна быть проблемой. Таким образом, настоящее изобретение позволяет повторную иммунизацию пациента без риска аллергических реакций.
Пример 5 настоящего изобретения делает правдоподобным то, что трансгенсодержащий репликон достигает большого числа копий у вакцинированных животных, что видно из очень сильной экспрессии рекомбинантного белка. В примере 6 показано, что вакцинация в соответствии с настоящим изобретением, при которой репликон кодирует терапевтический белок, является очень эффективной. Таким образом, настоящее изобретение обеспечивает эффективную вакцинацию с помощью системы транс-репликации РНК на основе альфавируса.
В способах, предусматривающих вакцинацию в соответствии с настоящим изобретением, лекарственное средство по настоящему изобретению вводится субъекту, в частности, если желательно лечить субъекта, имеющего заболевание с участием антигена или подверженного риску заболевания с участием антигена.
В способах, предусматривающих вакцинацию в соответствии с настоящим изобретением, представляющий интерес белок, кодируемый репликоном в соответствии с настоящим изобретением, кодирует, например, бактериальный антиген, против которого должен быть направлен иммунный ответ, или вирусный антиген, против которого должен быть направлен иммунный ответ, или антиген злокачественной опухоли, против которой должен быть направлен иммунный ответ, или антиген одноклеточного организма, против которого должен быть направлен иммунный ответ. Эффективность вакцинации может быть оценена известными стандартными способами, такими как измерение антигенспецифических IgG-антител из организма. В способах, предусматривающих аллергенспецифическую иммунотерапию в соответствии с настоящим изобретением, представляющий интерес белок, кодируемый репликоном в соответствии с настоящим изобретением, кодирует антиген, имеющий отношение к аллергии. Аллергенспецифическая иммунотерапия (также известная как гипосенсибилизация) определяется как введение предпочтительно увеличенной дозы аллергенной вакцины в организм с одной или несколькими аллергиями для достижения состояния, при котором симптомы, связанные с последующим воздействием возбудительного аллергена облегчаются. Эффективность аллергенспецифической иммунотерапии может быть оценена известными стандартными способами, такими как измерение аллергенспецифических антител IgG и IgE в организме.
Лекарственное средство по настоящему изобретению может вводиться субъекту, например, для лечения субъекта, включая вакцинацию субъекта.
Термин «субъект» относится к позвоночным, особенно млекопитающим. Например, млекопитающими в контексте настоящего изобретения являются люди, отличные от человека приматы, одомашненные млекопитающие, такие как собаки, кошки, овцы, крупный рогатый скот, козы, свиньи, лошади и т.д., лабораторные животные, такие как мыши, крысы, кролики, морские свинки и т. д., а также животные в неволе, такие как животные зоопарков. Термин «субъект» также относится к немлекопитающим позвоночным, таким как птицы (особенно одомашненные птицы, такие как куры, утки, гуси, индюки), и к рыбе (особенно выращиваемая рыба, например, лосось или сом). Используемый в настоящем документе термин «животное» также включает в себя людей.
Введение одомашненным животным, таким как собаки, кошки, кролики, морские свинки, хомяки, овцы, крупный рогатый скот, козы, свиньи, лошади, верблюды, куры, утки, гуси, индюки, или диким животным, например, лисицам, оленям, косулям, кабанам, предпочтительнее согласно некоторым вариантам осуществления. Например, профилактическая вакцинация в соответствии с настоящим изобретением может быть пригодна для вакцинации популяции животных, например, в сельском хозяйстве или в популяции диких животных. Могут быть вакцинированы другие популяции животных в неволе, такие как домашние животные или животные зоопарков.
При введении субъекту репликон и/или репликазная конструкция, используемые в качестве лекарственного средства, предпочтительно не содержат последовательностей из типа альфавируса, который является инфекционным для вида или рода, к которому относится подвергаемый лечению субъект. Предпочтительно, в этом случае репликон и/или репликазная конструкция не содержат никакой нуклеотидной последовательности из альфавируса, который может инфицировать соответствующие виды или род. Этот вариант осуществления имеет то преимущество, что рекомбинация с инфекционным (например, полностью функциональным или диким) альфавирусом невозможна, даже если субъект, которому вводится РНК, (например, случайно) поражен инфекционным альфавирусом. В качестве иллюстративного примера, для лечения свиней, используемый репликон и/или репликазная конструкция не содержит никакой нуклеотидной последовательности из альфавируса, который может инфицировать свиней.
Способ введения
Лекарственное средство в соответствии с настоящим изобретением может быть применено к субъекту посредством любого подходящего пути введения.
Например, лекарственное средство можно вводить системно, например, внутривенно (i.v.), подкожно (s.c.), внутрикожно (i.d.) или путем ингаляции.
Согласно одному варианту осуществления лекарственное средство в соответствии с настоящим изобретением вводят в мышечную ткань, такую как скелетная мышца или кожа, например, подкожно. Как правило, понимается, что перенос РНК в кожу или мышцы приводит к высокой и устойчивой локальной экспрессии, параллельно с сильной индукцией гуморальных и клеточных иммунных реакций (Johansson et al., 2012, PLoS. One., 7, e29732; Geall et al., 2012, Proc. Natl. Acad. Sci. US A, vol. 109, pp. 14604-14609).
Альтернативы введению в мышечную ткань или кожу включают в себя, без ограничения: внутрикожное, интраназальное, внутриглазное, внутрибрюшинное, внутривенное, интерстициальное, трансбуккальное, трансдермальное или подъязычное введение. Внутрикожное и внутримышечное введение представляют собой два предпочтительных пути.
Введение может быть достигнуто различными способами. Согласно одному варианту осуществления лекарственное средство в соответствии с настоящим изобретением вводят путем инъекции. Согласно предпочтительному варианту осуществления инъекцию осуществляют через иглу. В качестве альтернативы можно использовать инъекцию без иглы.
Настоящее изобретение описано подробно и иллюстрируется графическими материалами и примерами, которые используются только для иллюстративных целей и не предназначены для ограничения. Благодаря описанию и примерам, дополнительные варианты осуществления, которые также включены в настоящее изобретение, доступны для квалифицированного работника.
Примеры
Материал и способы:
Следующие материалы и способы были использованы в примерах, которые описаны ниже.
ДНК, кодирующая репликон, репликазную конструкцию и E3L, и транскрипция in vitro
(1) ДНК, кодирующую используемый в примерах цис-репликон, получали следующим образом: получали ДНК-плазмиду, подходящую для транскрипции in vitro РНК-репликона, который способен реплицироваться репликазой вируса леса Семлики (SFV): плазмиду репликона эталонного вируса леса Семлики в (pSFV-ген-GFP) любезно предоставил K. Lundstrom (Lundstrom et al., 2001, Histochem. Cell Biol., Vol. 115, pp. 83-91; Ehrengruber & Lundstrom, 1999, Proc. Natl. Acad. Sci. US A, vol. 96, pp. 7041-7046). Кодированную pSFV-ген-GFP поли(A)-кассету удлиняли от 62 аденилатных остатков в исходном векторе до 120 аденилатных остатков, а сайт рестрикции SapI помещали непосредственно ниже по ходу транскрипции от поли(А)-кассеты. Было описано, что этот поли(А)-дизайн усиливает экспрессию синтетической мРНК (Holtkamp et al., 2006, Blood, vol. 108, pp. 4009-4017). Наконец, фаго-полимеразный промотор изменяли с SP6 на Т7.
(2) Кодирующую транс-репликоны ДНК конструировали из вышеописанных цис-репликонов путем удаления основных частей открытой рамки считывания, кодирующей альфавирусную репликазу (нуклеотиды 222-6321 ORF репликазы), сохраняя основную цепь вектора.
(1a, 2a) Авторы настоящего изобретения самостоятельно клонировали репортерные гены люциферазы светлячков, секретируемой NanoLuc (оба были коммерциализированы Promega, Madison, WI, USA), гемагглютинин вируса гриппа A/Puerto Rico/08/1934 (HA) и усиленный зеленый флуоресцентный белок (eGFP, на фигурах «GFP» или «eGFP») 3’ по отношению к субгеномному промотору цис- и транс-репликонов.
(3) Чтобы создать репликазную конструкцию, открытую рамку считывания, кодирующую репликазу SFV, клонировали в плазмиду pST1, характеризующуюся тандемной копией 3’UTR, поли(А120)-хвоста и сайта рестрикции SapI ниже по ходу транскрипции от поли(А)-хвоста бета-глобина человека (Holtkamp et al., 2006, Blood, vol. 108, pp. 4009-4017).
(4) Открытую рамку считывания, кодирующую вирус осповакцины E3L, клонировали в плазмиду pST1, характеризующуюся тандемной копией 3’UTR, поли(А120)-хвоста и сайта рестрикции SapI ниже по ходу транскрипции от поли(А)-хвоста бета-глобина человека (Holtkamp et al., 2006, Blood, vol. 108, pp. 4009-4017).
Выполняли транскрипцию in vitro из полученных из pST1 и pSFV-ген-GFP плазмид [(1a), (2a), (3) и (4)] и очистку РНК, как описано выше, за исключением того, что аналог кэпа бета-S-ARCA(D2) использовали вместо ARCA (Holtkamp et al., смотрите выше, Kuhn et al., 2010, Gene Ther., Vol. 17, pp. 961-971). Качество очищенной РНК оценивали с помощью спектрофотометрии и анализа на BioAnalyzer 2100 (Agilent, Santa Clara, USA). Используемая в примерах РНК представляет собой очищенную IVT-РНК.
Перенос РНК в клетки:
Для электропорации РНК электропорировали в клетки при комнатной температуре с использованием устройства для электропорации с квадратной волной (BTX ECM 830, Harvard Apparatus, Holliston, MA, USA), используя следующие настройки: 750 В/см, 1 импульс 16 миллисекунд (мс)). Для электропорации РНК ресуспендировали в конечном объеме 62,5 мкл/мм зазора формующей щели кюветы.
Липофекции РНК проводили с использованием RNAiMAX липофектамина в соответствии с инструкциями производителя (Life Technologies, Darmstadt, Germany). Клетки высевали в количестве приблизительно 20000 клеток/см2 площади роста и трансфицировали общим количеством 260 нг/см2 РНК и 1 мкл/см2 RNAiMAX. РНК смешивали в пробирках Эппендорфа без РНКазы и выдерживали на льду до применения для трансфекции.
Клеточная культура: все среды для роста, телячья фетальная сыворотка (FCS), антибиотики и другие добавки были предоставлены Life Technologies/Gibco, за исключением случаев, когда указано иное. Фибробласты крайней плоти человека, полученные из System Bioscience (HFF, неонатальные) или ATCC (CCD-1079Sk), культивировали в минимальных поддерживающих средах (MEM), содержащих FCS в концентрации 15%, 1 ед./мл пенициллина, 1 мкг/мл стрептомицина, незаменимые аминокислоты в концентрации 1%, пируват натрия в концентрации 1 мМ при температуре 37°С. Клетки выращивали при температуре 37°С в увлажненной атмосфере, уравновешенной до 5% СО2. Клетки BHK21 (ATCC; CCL10) выращивали в минимальной поддерживающей среде Игла, дополненной 10% FCS.
Проточная цитометрия: Если не указано иное, трансфицированные клетки собирали через 16 ч после трансфекции для измерения эффективности продуктивных трансфекций и экспрессии трансгена (eGFP) с помощью проточной цитометрии (FACS). Измерение проводили с помощью проточной цитометрии с использованием проточного цитометра FACS Canto II (BD Bioscience, Heidelberg, Germany), а полученные данные анализировали с помощью соответствующего программного обеспечения Diva или программного обеспечения FlowJo (Tree Star Inc., Ashland, OR, USA).
Анализ люциферазы. Для оценки экспрессии люциферазы в трансфицированных клетках трансфицированные клетки высевали в 96-луночные белые микропланшеты (Nunc, Langenselbold, Germany). Обнаружение люциферазы светлячков проводили с помощью системы анализа люциферазы Bright-Glo; NanoLuc обнаруживали с использованием набора NanoGlo (оба Promega, Madison, WI, USA) в соответствии с инструкциями производителя. Биолюминесценцию измеряли с использованием микропланшетного ридера люминесценции Infinite M200 (Tecan Group, Männedorf, Switzerland). Данные представлены в относительных люциферазных единицах [RLU], отрицательные по люциферазе клетки использовали для вычитания фонового сигнала.
Животные: мышей Balb/c, в возрасте 6-8 недель, приобретали у Janvier LABS (Saint Berthevin Cedex, France) и размещали в нормальных лабораторных условиях с циркадными циклами света/темноты и свободным доступом к стандартной для мышей еде и водопроводной воде. Все эксперименты были одобрены Комитетом по этике Регионального совета по экспериментам на животных (Koblenz/ Rhineland-Palatinate, Germany, G 13-8-063).
Получение вируса гриппа и определение титра. Для инфицирования клетки Мадин-Дарби почек собак II (MDCK-II) культивировали в MEM, содержащем бычий сывороточный альбумин в концентрации 0,2% (30% БСА без IgG, Sigma) вместо FCS (инфекционная среда). Адаптированный для мышей вирус гриппа A/Puerto Rico/08/1934 размножали в клетках MDCK-II в инфицирующей среде, содержащей 1 мкг/мл тозилсульфонилфенилаланилхлорметилкетона (TPCK)- трипсина (Sigma). Супернатанты клеток очищали низкоскоростным центрифугированием и хранили при температуре -80°С. Вирусные титры (бляшкообразующие единицы (PFU) на мл) определяли с помощью анализа бляшек с использованием монослоев клеток MDCK-II с конфлюэнтностью 70-80% (12-луночный планшет). Клетки инокулировали посредством 200 мкл вирусных препаратов с серийным 10-кратным разведением (от 10-2 до 10-8). Вирусу позволяли адсорбировать в течение 1 часа при температуре 37°С, прежде чем клетки были покрыты низковязкой средой Avicel для снижения вирусной диффузии и образования бляшек. Раствор Avicel в концентрации 2,4% разбавляли 2×MEM/TPCK-трипсином в концентрации 1 мкг/мл для достижения конечной концентрации Avicel 1,2%. Спустя три дня покрытия удаляли и клетки окрашивали с использованием водного 1%-ного раствора кристаллического фиолетового, содержащего 10% формальдегид (10 мин при комнатной температуре). Окрашенные клетки промывали водой, подсчитывали количество бляшек на лунку и рассчитывали PFU/мл.
Титр гемагглютинации (титр HA): единицы гемагглютинации (HAU) определяли с использованием куриных эритроцитов (RBC, Fitzgerald, USA) в соответствии с рекомендациями, опубликованными ВОЗ в 2011 году в «Руководстве по лабораторной диагностике и вирусологическому надзору за гриппом». Вкратце, серийное разведение вирусных препаратов (2-кратное) проводили в V-образных 96-луночных планшетах, а затем инкубировали с 50 мкл куриных эритроцитов в концентрации 0,5% («стандартизованные эритроциты») в течение 30 мин при температуре 25°C. Гемагглютинация считалась полной, когда эритроциты все еще находились в суспензии после инкубации с препаратом вируса, тогда как неагглютинированные эритроциты осаждались на дне лунок. Титр HA регистрировали как инверсию наименьшего разведения, которая показала полную агглютинацию, и определяли как одну единицу гемагглютинации (HAU) на 50 мкл, количество вируса, которое необходимо для агглютинации равного объема стандартизованного эритроцита.
Анализ ингибирования гемагглютинации (HAI). Для определения сывороточного содержания антител к НА, которые ингибируют гемагглютинацию у иммунизированных мышей, сыворотки собирали и обрабатывали в течение ночи с помощью разрушающего рецептор фермента II «Seiken» в соотношении 1:5 (RDE (II), Denka Seiken Co.Ltd., Japan), а затем инактивировали нагреванием в течение 30 мин при температуре 56°С. Сыворотки использовали в дубликатах, а серийные разведения (1:2) выполняли перед добавлением 25 мкл разведения вируса PR8 (4 HAU/50 мкл). После 15-минутной инкубации при комнатной температуре добавляли 50 мкл эритроцитов в концентрации 0,5% и инкубировали смесь в течение 30 минут перед оценкой агглютинации. Титр HAI регистрировали как инверсию наименьшего разведения, при котором ингибировалась агглютинация (HAI/50 мкл).
Определение титра нейтрализации вирусов (VNT): Чтобы определить титр нейтрализующих вирус антител в сыворотке вакцинированных мышей, авторы настоящего изобретения анализировали способность антител сыворотки предотвращать заражение и, следовательно, высвобождение вируса de novo из клеток Мадин-Дарби почки собаки (MDCK). С этой целью серийные 1:2 разведения инактивированных нагреванием сывороток (при температуре 56°C в течение 30 минут) от вакцинированных и контрольных мышей инкубировали с фиксированной концентрацией инфекционного вируса гриппа (2 TCID50/мкл) (инфекционная доза тканевой культуры (50)). Контроль включает в себя отсутствие сыворотки и никакого контроля над вирусами на каждом микротитровальном планшете, а также обратное титрование препарата вируса в отсутствие сыворотки для подтверждения титра вирусного препарата. Все препараты (смеси сывороточных вирусов и контрольные образцы) инкубировали в течение 2 ч при температуре 37°С в присутствии тозилсульфонилфенилаланилхлорметилкетона (TPCK)- трипсина в концентрации 1 мкг/мл перед тем, как подвергнуть клетки MDCK действию препарата в течение 3 дней при температуре 37°С. Через 3 дня супернатанты клеточной культуры собирали из клеток MDCK и подвергали определению титра HA, как описано выше.
Интрадермальные иммунизации, вирусное заражение и оценка животных: Самок мышей BALB/c в возрасте 8-10 недель использовали для экспериментов по иммунизации. Мышей анестезировали изофлурановой ингаляцией, дорзальную область выбривали, а РНК HA-репликона в комбинации с мРНК репликазы и E3, растворенную в 20 мкл PBS без РНКазы, инъецировали внутрикожно в день 0 и 21. Кровь брали под изофлурановой анестезией посредством кровотечения из орбитального венозного сплетения в дни 20, 35 и 55 после первой иммунизации. Продукты клеточного распада осаждали из крови центрифугированием, а образцы сыворотки непосредственно использовали для анализа гемагглютинина (HAI). Для оценки защиты от заражения вирусом гриппа иммунизированным мышам вводили интраназально 10-кратную LD50 адаптированного к мыши вируса гриппа A/Puerto Rico/08/1934 (PR8) при анестезии с помощью кетамина/ксилазина. Мышей ежедневно взвешивали и умерщвляли через 14 дней после заражения или когда был достигнут критерий прекращения (25% потеря веса).
Пример 1. Эффективность экспрессии трансгена зависит от типа молекулы РНК, которая кодирует репликазу.
РНК цис-репликона, кодирующую репликазу и кодирующую люциферазу ниже по ходу транскрипции от SGP («РНК цис-репликона»), или синтетическую мРНК, кодирующую репликазу («мРНК»), каждую вместе с РНК транс-репликона, кодирующей eGFP ниже по ходу транскрипции от SGP, вводили путем электропорации в BHK21 (фиг. 3). Экспрессию транс-репликона определяли путем измерения флуоресценции eGFP с помощью FACS, экспрессия люциферазы из цис-репликона не представляла интереса. В частности, успех эксперимента определяли количественно путем определения скорости трансфекции, которая отражается на проценте eGFP-положительных клеток (столбики на фиг. 3); и путем определения уровня экспрессии eGFP, который отражается средней интенсивностью флуоресценции (MFI) eGFP-положительных клеток (ромбы на фиг. 3). Как показано на фиг. 3, система транс-репликации (в которой репликаза предусмотрена in trans в форме мРНК) дает как более высокий процент eGFP-положительных клеток, так и более высокую среднюю интенсивность флуоресценции eGFP-положительных клеток по сравнению с репликазой, экспрессированной из репликона, способного к цис-репликации («РНК цис-репликона»). Таким образом, репликаза, экспрессированная из репликона, способного к цис-репликации, менее эффективна для амплификации субгеномного транскрипта транс-репликона, что приводит к более низкому уровню экспрессии трансгена. Кроме того, система, содержащая репликазную мРНК и РНК транс-репликона, совместно поставляемые в клетки BHK21, более вероятно, будет продуктивно реплицировать транс-репликон, как это определено из процента eGFP-положительных клеток (столбики на фиг. 3).
Таким образом, было сделано заключение, что экспрессия представляющего интерес гена в системе транс-репликации более эффективна при использовании мРНК для доставки репликазы.
Пример 2. Система транс-репликации, состоящая из репликазы, кодируемой мРНК, и транс-репликона, кодирующего трансген, обеспечивает высокий уровень экспрессии трансгена также в первичных клетках и приводит к более высокой экспрессии по сравнению с цис-репликоном, кодирующим трансген.
РНК-репликон, способный к цис-репликации («РНК eGFP-репликона»); или мРНК, кодирующую репликазу («репликазную мРНК») вместе с РНК-транс-репликоном («РНК eGFP-трансрепликона») трансфицировали в первичные фибробласты крайней плоти человека (фиг. 4). Чтобы снизить активность протеинкиназы R, к каждому образцу РНК добавляли мРНК, кодирующую белок E3 вируса осповакцины. Трансфекцию проводили путем объединения РНК или смесей РНК с реагентом трансфекции RNAiMAX и добавления этой композиции в среду клеток (таким образом возможна совместная доставка РНК в тех же липосомах).
Экспрессию представляющего интерес гена определяли путем измерения флуоресценции eGFP, то есть путем определения процента eGFP-положительных клеток (столбики на фиг. 4); и путем определения средней интенсивности флуоресценции (MFI) eGFP-положительных клеток (ромбы на фиг. 4). Система транс-репликации («РНК eGFP-трансрепликона» вместе с «репликазной мРНК») давала как более высокий процент eGFP-положительных клеток, так и более высокую среднюю интенсивность флуоресценции eGFP-положительных клеток, чем система цис-репликации («РНК eGFP-репликона»). Таким образом, в случае системы транс-репликации вероятность того, что произойдет продуктивная репликация кодирующей трансген РНК, выше. В обеих системах вероятность создания продуктивной репликации зависит от дозы, но 50 нг РНК транс-репликона приблизительно так же эффективно, как 625 нг эталонного репликона (цис-репликона), а 10 нг транс-репликона столь же эффективно, как и 500 нг репликона. Кроме того, система транс-репликации дает более высокие уровни экспрессии трансгена на клетку (отражаемую MFI), чем контрольный репликон (ромбы на фиг .4).
Пример 3: Получение представляющего интерес белка зависит от дозы репликазы.
РНК, кодирующую репликазу («репликазная мРНК»), вместе с РНК-транс-репликоном («трансрепликон») и мРНК Е3 подвергали липофекции в первичные фибробласты крайней плоти человека, как показано на фиг. 5А. РНК-транс-репликон кодирует секретируемый репортерный белок NanoLuc люциферазы в качестве представляющего интерес гена. Эффективность производства белка может быть модулирована количеством репликазной РНК дозозависимым образом, о чем свидетельствует измерение секретируемого NanoLuc (фиг. 5A).
Пример 4. Модификация использования кодонов в репликазной конструкции представляет собой невыгодную модификацию, изменяющую неполипептид-кодирующие последовательности.
В этом примере использовали систему транс-репликации, в которой репликазная конструкция кодирует myс-меченный nsP3. Myc-метку встраивали в вариабельную область nsP3, чтобы обеспечить обнаружение уровней nsP3 (отражающих суммарные количества репликазы) посредством Вестерн-блоттинга антителами к myc. Вставки в вариабельную область nsP3 не влияют на активность полипротеина репликазы (Spuul et al., 2010, J. Virol, vol. 85, pp. 7543-7557). Использование кодонов myc-меченной репликазы («использование кодонов репликазы wt») необязательно адаптировали к использованию кодонов Homo sapiens (для получения «использования кодонов репликазы hs»). Транс-репликон, кодирующий eGFP в качестве представляющего интерес гена, подвергали совместной липофекции в клетки BHK21 вместе с различными количествами репликазной РНК, как указано (фиг. 5B).
Экспрессию представляющего интерес гена определяли путем измерения флуоресценции eGFP, то есть путем определения процента eGFP-положительных клеток (столбиков на фиг. 5B) и путем определения средней интенсивности флуоресценции (MFI) eGFP-положительных клеток (ромбы на фиг. 5B).
Модификация использования кодонов приводит к увеличению содержания репликазы (содержание myc-меченных nsP3), но это не выгодно для экспрессии представляющего интерес гена из кодирующего eGFP транс-репликона: гораздо более высокая экспрессия репликазы из оптимизированной кодоном РНК по сравнению с неоптимизированной кодоном репликазной РНК не отражается более высокой экспрессией eGFP (ромбы на фиг. 5B), и вероятность создания продуктивной репликации транс-репликона снижается, как показано в процентах от eGFP-положительных клеток (столбики на фиг. 5B).
Пример 5. Эффективная экспрессия трансгена, кодируемого репликоном в соответствии с настоящим изобретением, может быть достигнута in vivo.
IVT-РНК, кодирующую репликазу вместе с РНК-транс-репликоном и с мРНК, кодирующей белок E3 вируса осповакцины, ресуспендировали в забуференном фосфатом физиологическом растворе (PBS) и вводили совместно мышам, внутрикожно или в переднюю большеберцовую мышцу (внутримышечно). Открытая рамка считывания транс-репликона кодирует люциферазу репортерного белка в качестве представляющего интерес белка.
Использовали две группы с 3 животными на группу. Каждое животное инъецировали в двух местах. Экспрессию люциферазы in vivo измеряли, как описано (Kuhn et al., 2010, Gene Ther., Vol. 17, pp. 961-971). Экспрессия длится по меньшей мере 9 дней, как показано с помощью биолюминесцентной визуализации (BLI) мышей после внутримышечной (i.m.) и внутрикожной (i.d.), соответственно, совместной инъекции РНК. Результаты показаны на фиг. 6.
Пример 6: Вакцинация системой транс-репликации, содержащей репликон в соответствии с настоящим изобретением, кодирующий грипп HA в качестве представляющего интерес белка, обеспечивает защиту от летальных вирусных инфекций.
Мышей Balb/C вакцинировали внутрикожно дважды (примирование) в течение 3 недель с использованием РНК-репликона, кодирующего гемагглютинин (НА), в качестве представляющего интерес гена (на фиг. 7: «R-HA»); или РНК, кодирующей репликазу (на фиг. 7: «репликаза»), и РНК транс-репликона, кодирующей гемагглютинин (НА), в качестве представляющего интерес гена (на фиг. 7: «TR-HA»), как показано на фиг. 7. Чтобы улучшить трансляцию, кодирующую E3 осповакцины мРНК котрансфицировали, где указано. Контрольные животные либо были вакцинированы инактивированным вирусом (IAV), либо получили растворитель (PBS).
За день до заражения смертельными дозами вируса гриппа сыворотки всех животных собирали и использовали для определения титра нейтрализации вируса (VNT). В группе эталонного репликона все животные показывают близкие титры VNT животных, обработанных IAV. В группе транс-репликона VNT увеличивался с увеличением количества репликазной мРНК, которая была совместно перенесена. С 14-кратным избытком репликазной мРНК относительно транс-репликона был достигнут такой же высокий VNT, как и в контроле репликона, что означает, что только 20% антиген-кодирующей РНК (1 мкг TR-HA против 5 мкг R-HA) приводило к сопоставимым титрам VNT (фиг. 7A).
Сыворотки мышей также подвергали анализу ингибирования гемагглютинина (HAI). Все вакцинированные РНК животные показали сопоставимые титры HAI (фиг. 7В).
Мониторили выживаемость мышей после заражения инфекцией. Мыши, обработанные буфером, умерли в течение 5 дней. Все вакцинированные мыши выжили, за одним исключением в группе, вакцинированной TR-HA и 15 мкг E3 (фиг. 7C).
Таким образом, было сделано заключение, что вакцинация транс-репликоном, кодирующим НА, обеспечивает защиту от летальной вирусной инфекции и позволяет уменьшить количество антиген-кодирующей РНК.
Пример 7: Влияние кэпа.
Клетки BHK21 электропорировали с РНК транкрепликона, кодирующей eGFP и secNLuc (секретируемая люцифераза), разделенные саморасщепляющимся пептидом P2A (тесковирус-1 2A свиней) вместе либо с кэпированной бета-S-ARCA(D2) репликазной мРНК, либо некэпированной мРНК с IRES(EMCV) (участок внутренней посадки рибосомы из вируса энцефаломиокардита) выше против хода транскрипции от ORF репликазы. Через 24 часа после электропорации клетки анализировали с помощью FACS на экспрессию eGFP (фиг. 8А), супернатанты анализировали на уровни секреции secNLuc с помощью системы анализа люциферазы Nano-Glo® (Promega) (фиг. 8В) и экспрессию репликазы анализировали с помощью Вестерн-блоттинга (фиг. 8С).
Как показано на фиг. 8А, кэпированная репликазная мРНК приводит к большей вероятности обеспечить репликацию трансрепликона, что измерено посредством процентного соотношения eGFP-положительных клеток (столбики), и к более высоким уровням экспрессии eGFP в положительных клетках (ромбы).
Для количественной оценки разницы измеряли активность секретируемой люциферазы и выяснили, что обе репликазные мРНК являются функциональными (фоном анализа является ~ 10 RLU), но описанная трансреплицирующая система в 37 раз более эффективна, когда используется кэпированная мРНК, как показано на фиг. 8B.
Как показано на фиг. 8C, причиной вышеуказанного наблюдения является более высокая концентрация белка репликазы, когда экспрессия управляется кэпом (левая половина) по сравнению с IRES (правая половина), как показано путем зондирования образцов антителом к myc (верхнее пятно). Зондирование образцов антителом к eGFP (среднее пятно) подтвердило более высокую экспрессию eGFP, как уже показано на фиг. 8А. Равная загрузка геля подтверждается обнаружением клеточного белка α-тубулина с соответствующим антителом (нижнее пятно).
| название | год | авторы | номер документа |
|---|---|---|---|
| РНК-РЕПЛИКОН ДЛЯ УНИВЕРСАЛЬНОЙ И ЭФФЕКТИВНОЙ ГЕННОЙ ЭКСПРЕССИИ | 2017 |
|
RU2748892C2 |
| РЕЦЕПТУРА ДЛЯ ВВЕДЕНИЯ РНК | 2019 |
|
RU2797147C2 |
| СОСТАВ ДЛЯ ВВЕДЕНИЯ РНК | 2017 |
|
RU2746118C2 |
| СПОСОБ ПОВЫШЕНИЯ ЭКСПРЕССИИ РНК В КЛЕТКЕ | 2018 |
|
RU2784654C2 |
| ПЛАТФОРМЫ ДОСТАВКИ АНТИГЕНОВ | 2011 |
|
RU2597974C2 |
| ПОСЛЕДОВАТЕЛЬНОСТИ 3'-UTR ДЛЯ СТАБИЛИЗАЦИИ РНК | 2016 |
|
RU2720934C2 |
| ПОСЛЕДОВАТЕЛЬНОСТИ 3'-UTR ДЛЯ СТАБИЛИЗАЦИИ РНК | 2016 |
|
RU2783165C1 |
| ЭМУЛЬСИИ ТИПА "МАСЛО В ВОДЕ", КОТОРЫЕ СОДЕРЖАТ НУКЛЕИНОВЫЕ КИСЛОТЫ | 2012 |
|
RU2606846C2 |
| МИКРОЧАСТИЦЫ ДЛЯ ДОСТАВКИ ГЕТЕРОЛОГИЧНЫХ НУКЛЕИНОВЫХ КИСЛОТ | 2001 |
|
RU2295954C2 |
| АДЕНОВИРУСНЫЙ/АЛЬФА-ВИРУСНЫЙ ГИБРИДНЫЙ ВЕКТОР ДЛЯ ЭФФЕКТИВНОГО ВВЕДЕНИЯ И ЭКСПРЕССИИ ТЕРАПЕВТИЧЕСКИХ ГЕНОВ В ОПУХОЛЕВЫЕ КЛЕТКИ | 2005 |
|
RU2394104C2 |
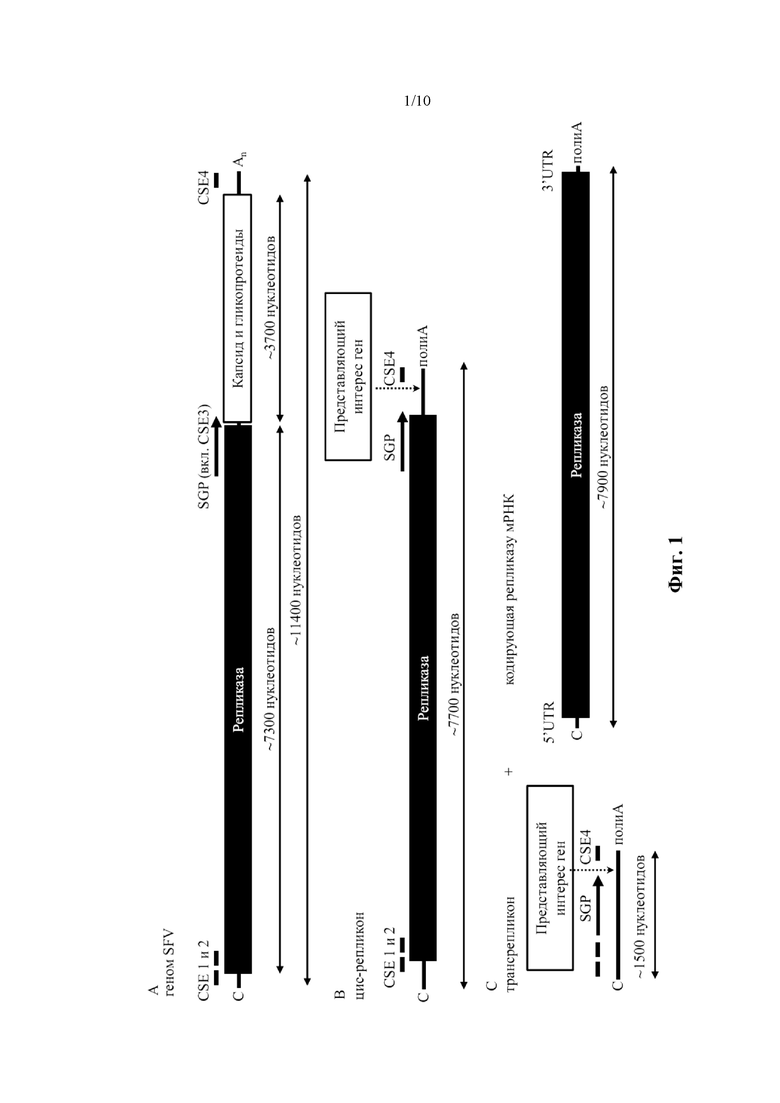
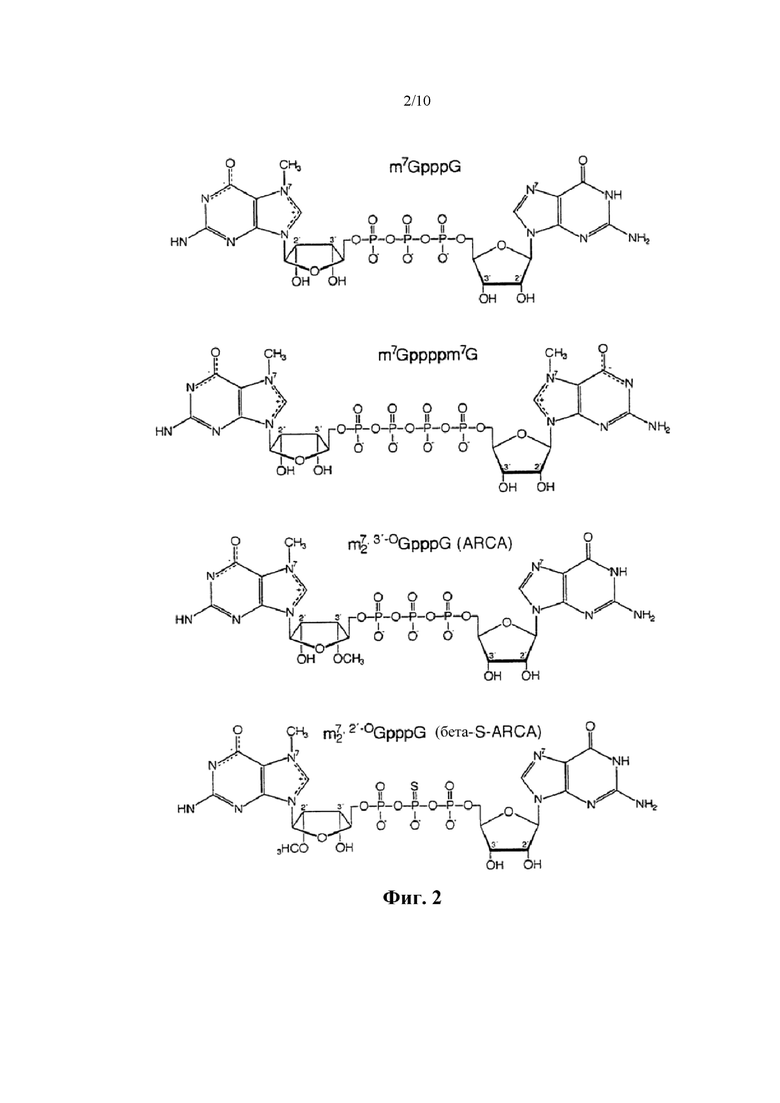
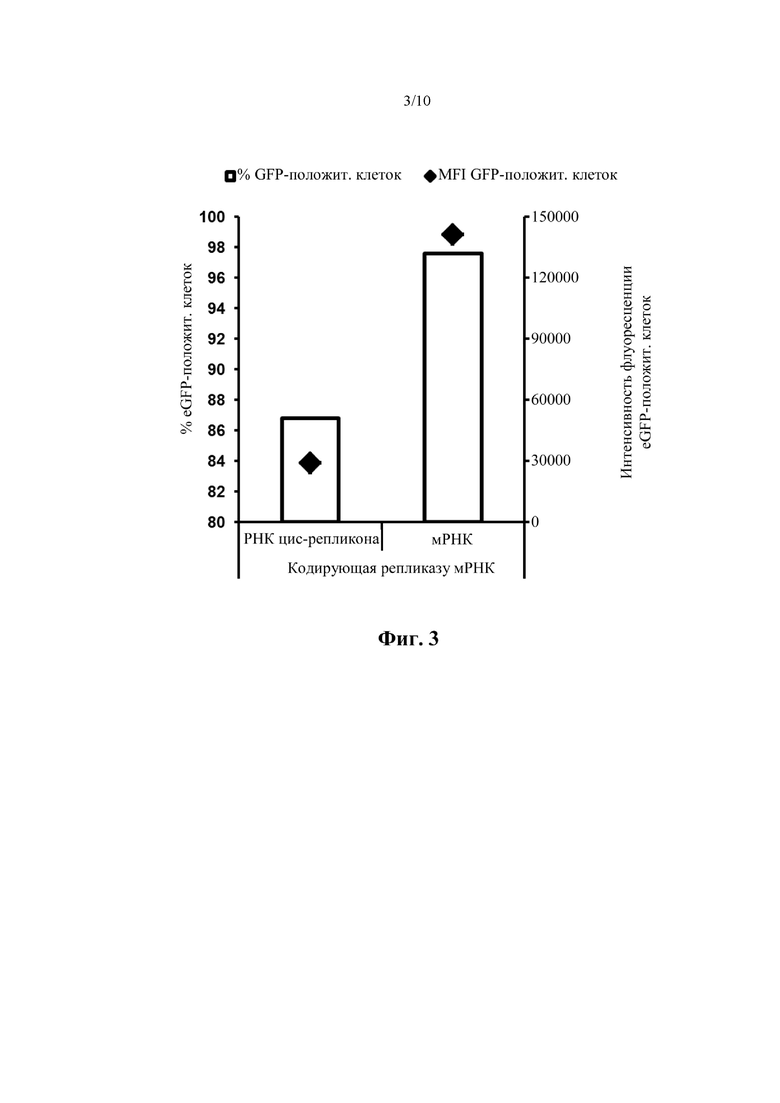
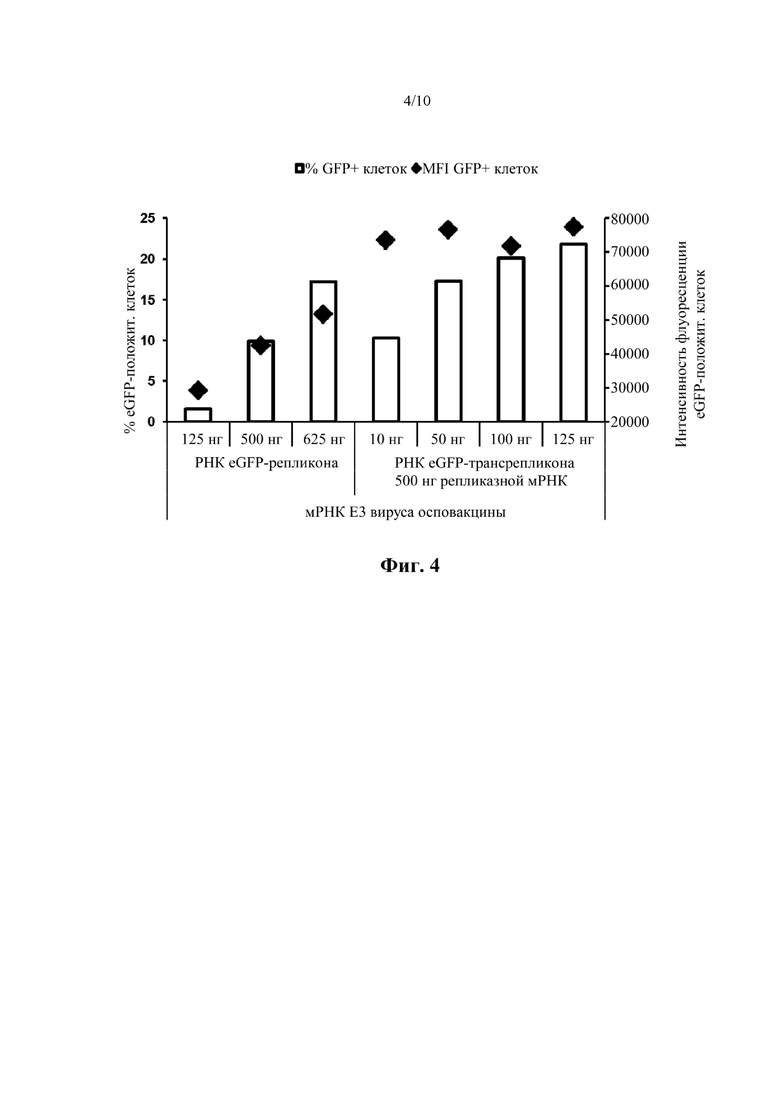
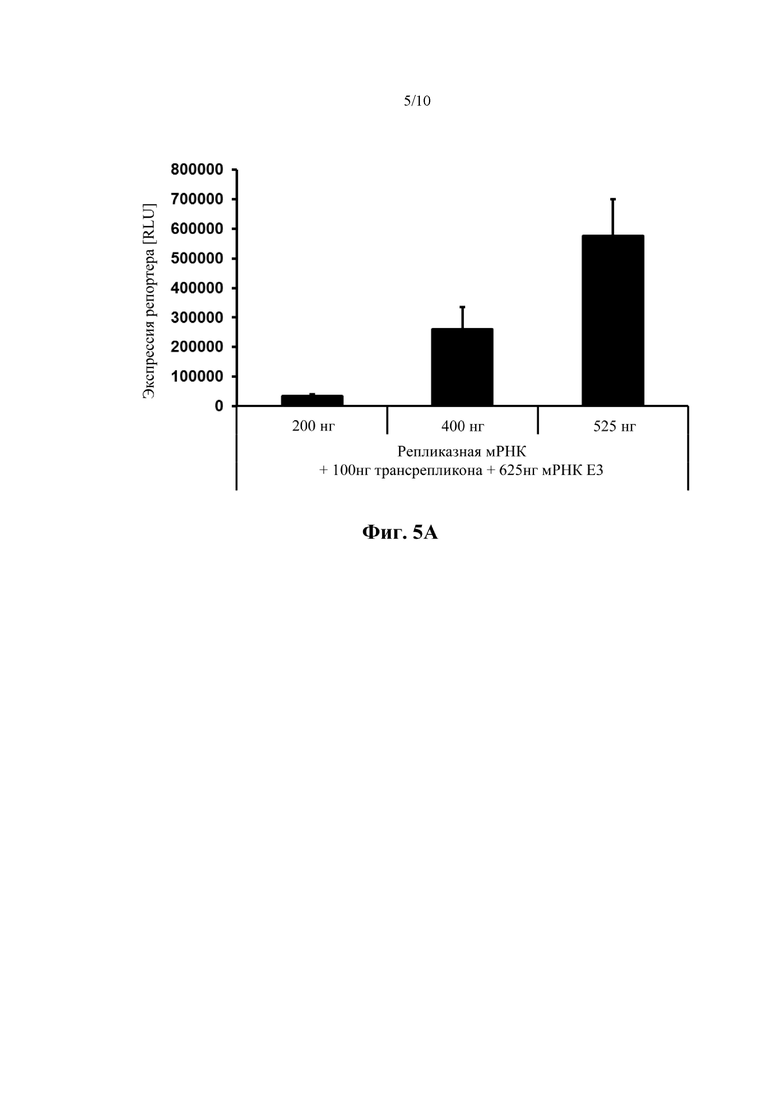
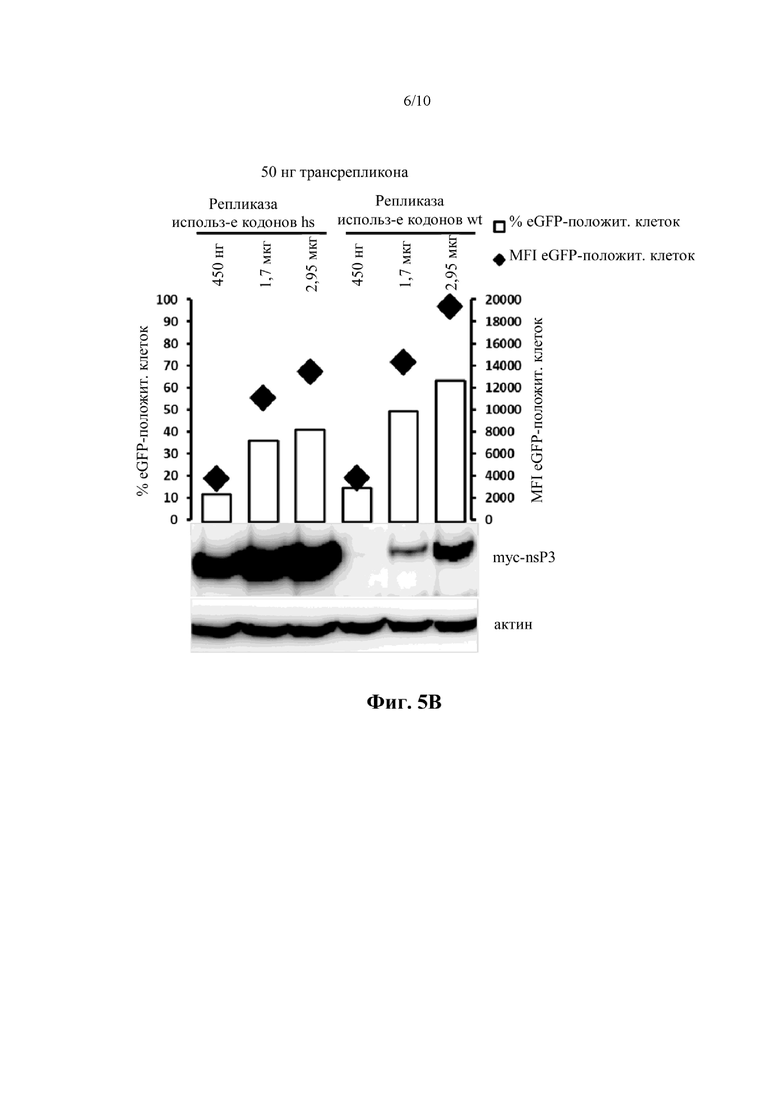
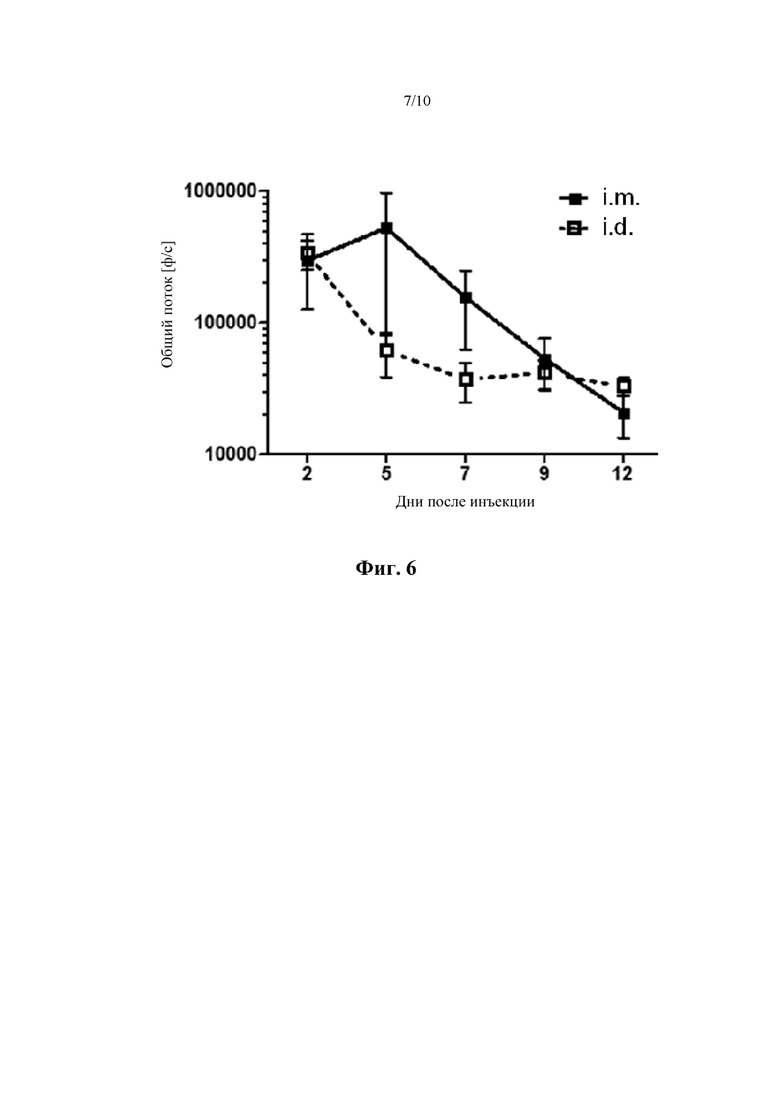
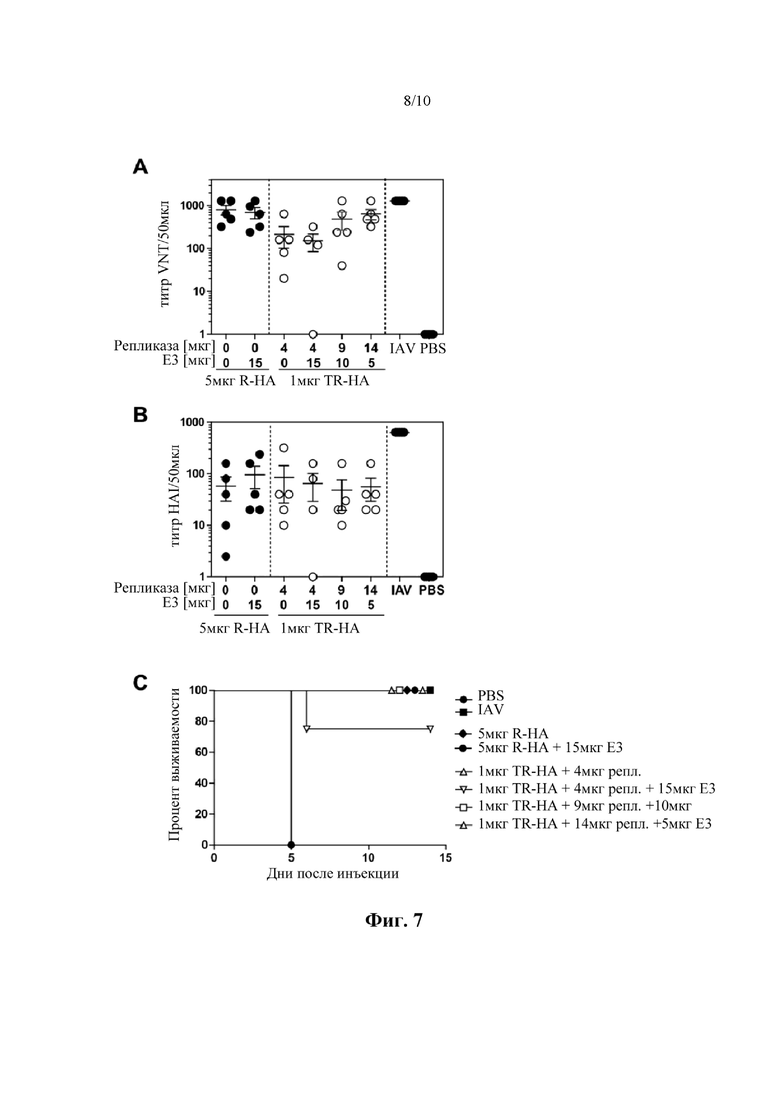

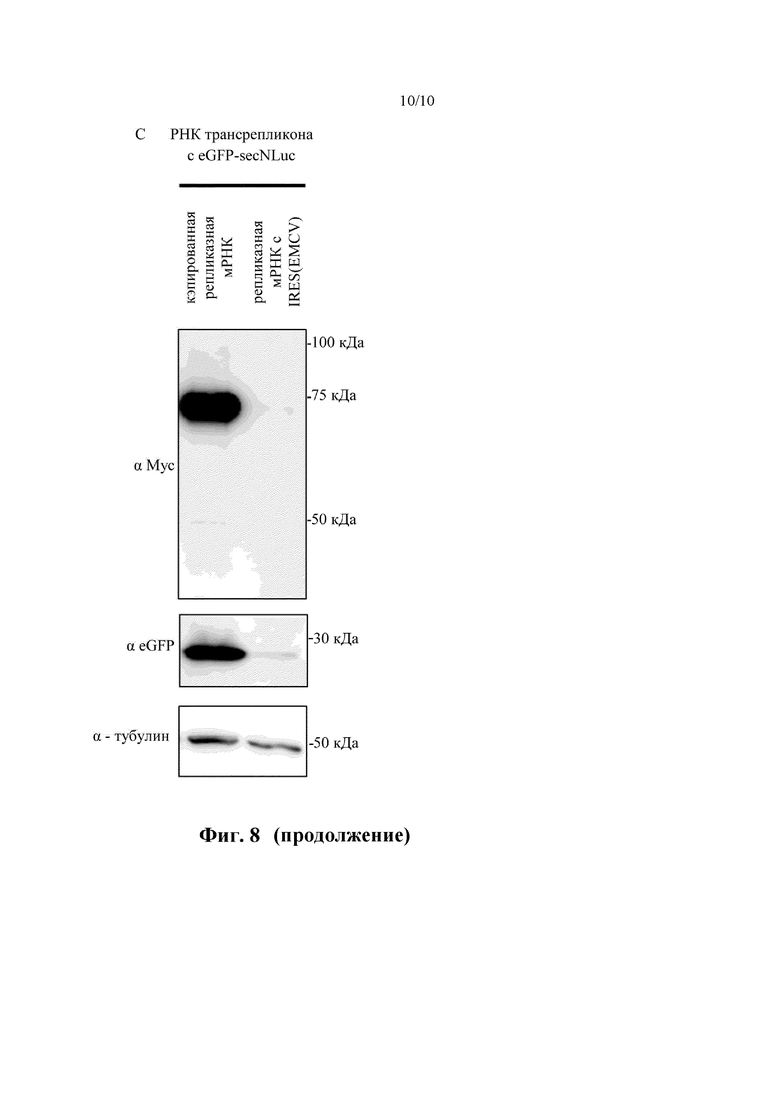
Изобретение относится к области биотехнологии. Описана группа изобретений, включающая систему для получения белка, фармацевтическую композицию для экспрессии альфавирусной репликазы и/или репликона, способ получения белка в клетке, эукариотическую клетку-хозяин для получения белка и способ получения белка у субъекта. В одном из вариантов реализации система содержит конструкцию РНК для экспрессии альфавирусной репликазы и РНК-репликон, который может быть реплицирован репликазой in trans, причем конструкция РНК содержит 5' UTR, открытую рамку считывания, кодирующую репликазу, и 3' UTR, где конструкция РНК содержит 5’-кэп для трансляции репликазы, и РНК-репликон содержит 5' репликационную последовательность распознавания альфавируса, открытую рамку считывания, кодирующую представляющий интерес белок, и 3' репликационную последовательность распознавания альфавируса. 5 н. и 10 з.п. ф-лы, 8 ил., 7 пр.
1. Система для получения белка, содержащая:
(a) конструкцию РНК для экспрессии альфавирусной репликазы и
(b) РНК-репликон, который может быть реплицирован репликазой in trans,
причем конструкция РНК (a) содержит 5' UTR, открытую рамку считывания, кодирующую репликазу, и 3' UTR, где конструкция РНК содержит 5’-кэп для трансляции репликазы, и
причем РНК-репликон (b) содержит:
(i) 5' репликационную последовательность распознавания альфавируса;
(ii) открытую рамку считывания, кодирующую представляющий интерес белок; и
(iii) 3' репликационную последовательность распознавания альфавируса;
причем 5' репликационная последовательность распознавания альфавируса и 3' репликационная последовательность распознавания альфавируса направляют репликацию РНК-репликона в присутствии репликазы.
2. Система по п. 1, в которой 5’-кэп представляет собой природный 5’-кэп или аналог 5’-кэпа.
3. Система по п. 1 или 2, в которой конструкция РНК для экспрессии альфавирусной репликазы не содержит элемент участка внутренней посадки рибосомы (IRES) для трансляции репликазы.
4. Система по пп. 1-3, в которой 5' UTR и/или 3' UTR являются ненативными для альфавируса, из которого получена репликаза.
5. Система по любому из пп. 1-4, в которой открытая рамка считывания, кодирующая альфавирусную репликазу, содержит кодирующую область(-и) для неструктурных белков, необходимых для репликации РНК.
6. Система по любому из пп. 1-5, в которой конструкция РНК для экспрессии альфавирусной репликазы содержит 3' поли(А)-последовательность.
7. Система по любому из пп. 1-6, в которой РНК-репликон содержит гетерологичную нуклеиновую кислоту.
8. Система по любому из пп. 1-7, в которой экспрессия открытой рамки считывания, кодирующей представляющий интерес белок, находится под контролем субгеномного промотора.
9. Система по п. 8, в которой субгеномный промотор представляет собой промотор структурного белка альфавируса.
10. Система по любому из пп. 1-9, в которой конструкция РНК для экспрессии альфавирусной репликазы и/или РНК-репликон не содержит открытую рамку считывания, кодирующую интактный структурный белок альфавируса.
11. Система по любому из пп. 1-10, в которой альфавирус представляет собой вирус леса Семлики, или вирус венесуэльского лошадиного энцефалита, или вирус Синдбис, или вирус Чикунгунья.
12. Фармацевтическая композиция для экспрессии альфавирусной репликазы и/или репликона, содержащая (а) конструкцию РНК для экспрессии альфавирусной репликазы, содержащая 5’-кэп для трансляции репликазы и (б) РНК-репликон, который может быть реплицирован репликазой in trans,
причем конструкция (а) содержит 5' UTR, открытую рамку считывания, кодирующую репликазу, и 3' UTR и
причем РНК-репликон (б) содержит:
(i) 5' репликационную последовательность распознавания альфавируса;
(ii) открытую рамку считывания, кодирующую представляющий интерес белок; и
(iii) 3' репликационную последовательность распознавания альфавируса;
причем 5' репликационная последовательность распознавания альфавируса и 3' репликационная последовательность распознавания альфавируса направляют репликацию РНК-репликона в присутствии репликазы.
13. Способ получения белка в клетке, предусматривающий следующие стадии:
(а) получение конструкции РНК для экспрессии альфавирусной репликазы,
(b) получение РНК-репликона, который может быть реплицирован репликазой in trans и содержит открытую рамку считывания, кодирующую белок, и
(c) инокуляция клетки смесью конструкции РНК для экспрессии альфавирусной репликазы и РНК-репликона,
причем конструкция РНК для экспрессии альфавирусной репликазы содержит 5' UTR, открытую рамку считывания, кодирующую репликазу, и 3' UTR, где конструкция РНК содержит 5’-кэп для трансляции репликазы,
причем РНК-репликон (б) содержит:
(i) 5' репликационную последовательность распознавания альфавируса;
(ii) открытую рамку считывания, кодирующую представляющий интерес белок; и
(iii) 3' репликационную последовательность распознавания альфавируса;
причем 5' репликационная последовательность распознавания альфавируса и 3' репликационная последовательность распознавания альфавируса направляют репликацию РНК-репликона в присутствии репликазы.
14. Эукариотическая клетка-хозяин для получения белка, инокулированная по способу по п. 13, содержащая:
(а) конструкцию РНК для экспрессии альфавирусной репликазы и
(б) РНК-репликон, который может быть реплицирован репликазой in trans,
причем конструкция РНК (а) для экспрессии альфавирусной репликазы содержит 5' UTR, открытую рамку считывания, кодирующую репликазу, и 3' UTR, где конструкция РНК содержит 5’-кэп для трансляции репликазы, и
причем РНК-репликон (б) содержит:
(i) 5' репликационную последовательность распознавания альфавируса;
(ii) открытую рамку считывания, кодирующую представляющий интерес белок; и
(iii) 3' репликационную последовательность распознавания альфавируса;
причем 5' репликационная последовательность распознавания альфавируса и 3' репликационная последовательность распознавания альфавируса направляют репликацию РНК-репликона в присутствии репликазы.
15. Способ получения белка у субъекта, предусматривающий следующие стадии:
(а) получение конструкции РНК для экспрессии альфавирусной репликазы,
(b) получение РНК-репликона, который может быть реплицирован репликазой in trans, и
(c) введение конструкции РНК для экспрессии альфавирусной репликазы и РНК-репликона субъекту,
причем конструкция РНК содержит 5' UTR, открытую рамку считывания, кодирующую репликазу, и 3' UTR, где конструкция РНК содержит 5’-кэп для трансляции репликазы,
причем РНК-репликон (б) содержит:
(i) 5' репликационную последовательность распознавания альфавируса;
(ii) открытую рамку считывания, кодирующую представляющий интерес белок; и
(iii) 3' репликационную последовательность распознавания альфавируса;
причем 5' репликационная последовательность распознавания альфавируса и 3' репликационная последовательность распознавания альфавируса направляют репликацию РНК-репликона в присутствии репликазы.
| Gregory J | |||
| Atkins, Marina N | |||
| Fleeton and Brian J | |||
| Sheahan | |||
| "Therapeutic and prophylactic applications of alphavirus vectors", Expert reviews in molecular medicine, 2008, 10, e33, DOI 10.1017/S1462399408000859 | |||
| WO 2008156829 A2, 24.12.2008 | |||
| Духовой шкаф | 1991 |
|
SU1791678A1 |
| ПЛАТФОРМЫ ДОСТАВКИ АНТИГЕНОВ | 2011 |
|
RU2597974C2 |
| US 7425337 B2, 16.09.2008. | |||
Авторы
Даты
2021-07-29—Публикация
2017-03-13—Подача