Изобретение относится к области медицины и фармацевтики, а именно к гуминовым препаратам, и может использоваться в качестве антибактериального средства.
Гуминовые кислоты, фульвокислоты оказывают на любой живой организм мощное воздействие благодаря богатому составу. В них содержится полный набор аминокислот, макро- и микроэлементов, минералов, а также полисахариды природного происхождения, витамины, пептиды, жирные кислоты, полифенолы, кетоны, катехины и т.д. Всего около 70 полезных компонентов. Такой насыщенный состав объясняет положительные биологические эффекты гуминовой кислоты (см.https://fb.ru/article/288472/guminovvie-kislotvi-chto-eto-takoe-i-kak-oni-vlivavut-na-organizm).
Известно, что гуминовые кислоты способны стимулировать некоторые функции нейтрофилов человека. Для препаратов на основе гуминовых и гуминовоподобных веществ выявлена антивирусная активность, например, для симплексного вируса герпеса -HSV. Гуминовые соединения могут быть использованы в качестве микробиоцидов, профилактических средств против распространения ВИЧ/СПИД. Были исследованы цитотоксические и антивирусные свойства гуминовых кислот и фульвокислот, выделенных из угля и торфа. Исследования показали, что все изученные соединения были малотоксичными и обладали достаточно высоким ингибирующим эффектом в отношении ВИЧ-инфекции (А.И. Попов, В.Н. Зеленков, Т.В. Теплякова Биологическая активность и биохимия гуминовых веществ. Часть 2. Медико-биологический аспект (обзор литературы). Вестник Российской Академии Наук, 2016/5, с. 9-15). Было показано, что Оксигумат повышает активность Th-1 клеток и уменьшает продукцию цитокинов Th-2 клетками [Mariette et al., 2002]. Наблюдаемая стимуляция пролиферации лимфоцитов человека была связана с повышением продукции ИЛ-2 и экспрессией ИЛ-2 рецепторов вместе с уменьшением количества ИЛ-10 под действием Оксигумата [Joone et al., 2003]. In vivo показано, что пероральный прием гуминовых веществ улучшает параметры врожденного иммунитета у экспериментальных животных: происходит усиление антибактериальной активности сыворотки крови, фагоцитарной активности, активности лизозима и бактериальной агглютинации [Sanmiguel et al., 2016]. Это делает гуминовые вещества потенциальными продуктами для разработки многомишеневых иммуноактивных микробицидов.
Гуминовые кислоты оказывают на патогенную микрофлору действие в форме прямого воздействия на бактериальные клетки и их обмен веществ (подавление синтеза фолиевой кислоты). Это приводит к прямому ускоренному разрушению клеток бактерий или вирусов. Второй антибактериальный эффект гуминовых кислот основан на внутреннем связывании высокомолекулярных белковых фракций - бактериальных токсинов, вследствие чего их токсический эффект на физиологические процессы может быть значительно ослаблен или полностью нейтрализован. Гуминовые кислоты оказывают установленное антибактериальное действие на следующие патогенные микроорганизмы: С. Albicans, Prot. Vulgaris, Ps. Aeruginosa, S. Typhimurium, St. aureus, St. epidermidis, St. pyogenes. Они существенно ускоряют метаболизм бактерий, что приводит к усиленному разрушению микробных клеток. В кишечнике гуминовые кислоты нейтрализуют патогенную микрофлору. Связанные бактерии и токсины выводятся естественным путем.
По данным экспериментальных исследований, гуминовые кислоты и их соли, фульвокислоты и их соли проявляют антибактериальные (Бокучава и Микая, 2004; Исматова и др., 2006; Anesio et al., 2004; Kodama et al., 2008) и фунгицидные свойства (Федько, 2005). Наиболее вероятным механизмом данных видов активности является нарушение метаболизма белков и карбоангидратов по каталитическому механизму, а также способность образовывать межионные связи с высокомолекулярными субстратами микроорганизмов (Бузлама и Черных, 2010). В одном исследовании говорится о воздействии фульвокислоты на 8 патогенных или условно патогенных организмов: Streptococcus faecalis, Staphylococcus aureus, Pseudomonas aeruginosa, Escherichia coli, Streptococcus pyogenes, Klebsiella pneumoniae, Proteus mirabilis, Candida albicans. Большая часть микроорганизмов оказалась чувствительна к фульвокислоте при ее концентрации 15 мг/мл, a Enterococcus faecalis и Klebsiella pneumoniae при концентрации 5 мг/мл (van Rensburg et al., 2000). В другом исследовании показано, что гумат натрия задерживает рост Trichophyton rubrum, Trichophyton mentagrophytes и Microsporum canis в концентрациях 15,6-31,2 мкг/мл, а также проявляет ингибирующее действие в отношении Aspergillus niger при концентрации 1 мг/мл (Исматова и др., 2007).
Из уровня техники известен препарат Биостим-К - природное вещество, выделенное из торфяников Кировской области, является продуктом взаимодействия торфа с водными растворами гидроксида и карбоната натрия и представляет собой прозрачную жидкость темно-коричневого цвета со слабым специфическим запахом. Массовая доля влаги в этом препарате составляет 95,7%, гуматов натрия (в пересчете на сухое вещество) - не более 3%, рН препарата - не более 9. Указанные препарат Биостим-К обладает выраженными бактериоцидными и бактериостатическими свойствами (О.Г. Малых, В.Е. Романов Антибактериальная активность препарата Биостим-К. Вестник ветеринарии, №64, (1/2013), с. 80-82).
Недостатком известного препарата является то, что он содержит только узкую фракцию гуминовых веществ (гумат натрия) в малой концентрации и не содержит других активных компонентов гуминовых веществ.
Задачей настоящего изобретения является получение гуминового средства, содержащего широкий спектр гуминовых веществ и обладающего антибактериальной активностью, без использования химических реагентов.
Техническим результатом заявленного изобретения является получение антибактериального гуминового средства, содержащего широкий спектр гуминовых веществ и не имеющего химических примесей, которое может быть использовано в области медицины и фармацевтики.
Указанный технический результат достигается за счет того, что заявленное гуминовое средство, обладающее антибактериальной активностью, содержит воду и гуминовые вещества, полученные из гуминосодержащего сырья, выбранного группы, включающей леонардит, лигнин, уголь, торф и/или сапропель, методом ультразвукового диспергирования при температуре 30-80°С и давлении 0,05-0,8 МПа, при этом масса гуминовых веществ составляет от 1 до 20 мас. %, а гуминовые вещества включают гуминовые и фульво-кислоты и их соли, а также гидрохинон в количестве не превышающем 3 мас. % от массы гуминовых веществ.
Также предлагается применение полученного гуминового средства в качестве антибактериального препарата.
Для получения заявленного средства использовали предварительно измельченное сырье (леонардит, лигнин, уголь, торф, сапропель) в смеси с водой, которое помещали в ультразвуковую установку. Помещенную в ультразвуковую установку смесь гуминосодержащего сырья с водой нагревали до 30-80°С, и при достижении требуемой температуры производили обработку ультразвуком при давлении 0,05-0,8 МПа. После ультразвуковой обработки раствор охлаждали до комнатной температуры. Полученное средство разбавляли водой до содержания гуминовых веществ, составляющего от 1 до 20 мас. %.
Исследование состава полученного средства проводили методом ГХ-МС на анализаторе «Хроматэк», состоящем из газового хроматографа «Хроматэк-Кристал 5000» и жидкостного дозатора ДАЖ-2М. Для идентификации дериватов использовали автоматическую базу поиска и идентификации данных хромато-масс-спектрометрии NIST17 MS Library.
Условия исследования:

Результаты исследования приведены в табл. 1

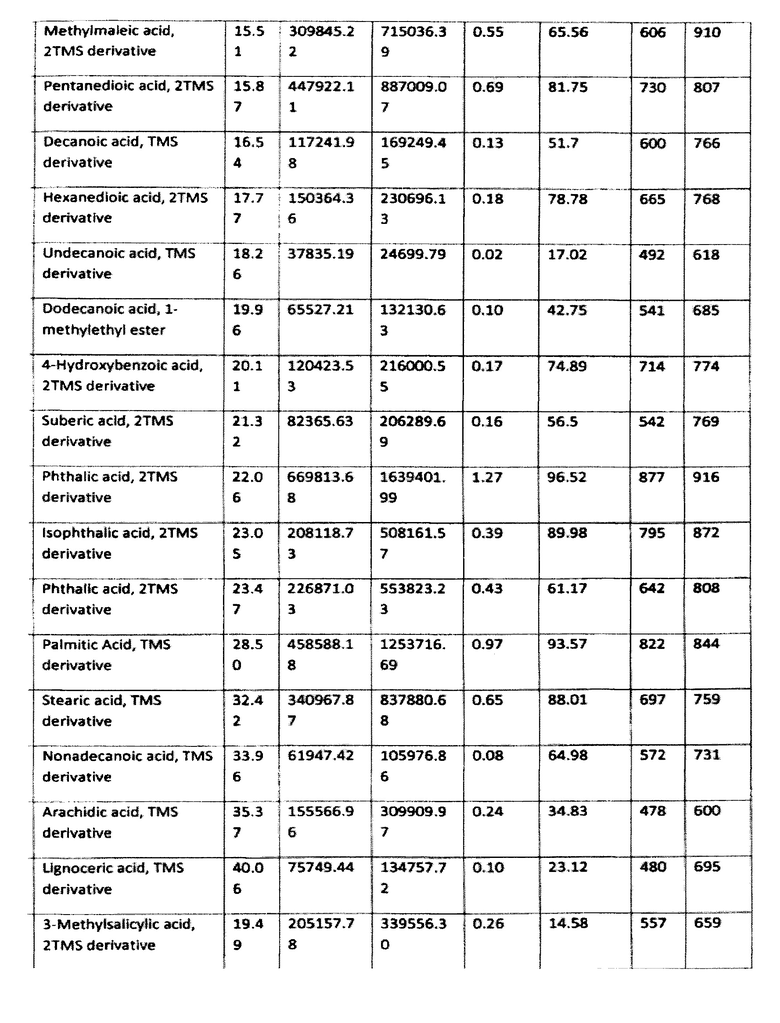
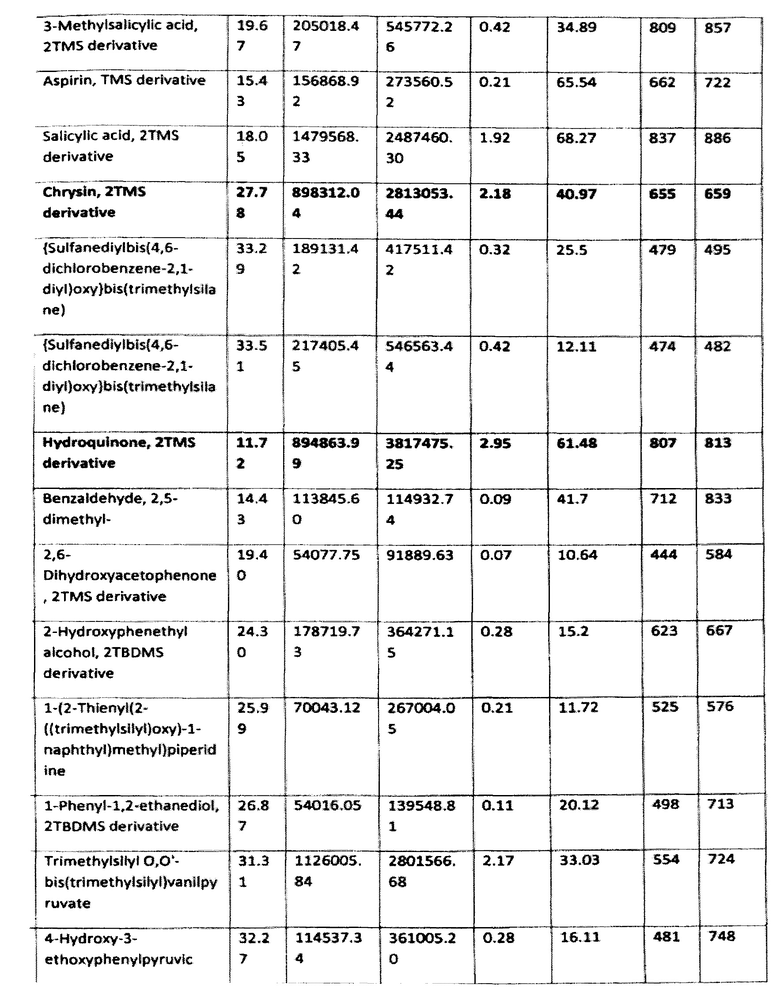
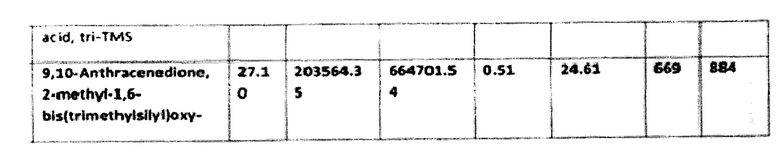
Согласно приведенным данным в состав заявленного средства, помимо гуминовых и фульвокислот, входят также фенольные производные, в частности гидрохинон, флаваноиды (хризин) и другие активные вещества. Следовательно, заявленное средство характеризуется широким спектром активных веществ.
Исследование на токсичность.
Определение показателей острой токсичности включало эксперименты на мышах. Животные распределялись по группам случайным образом методом рандомизации. В качестве критериев приемлемости рандомизации считали отсутствие внешних признаков заболеваний и гомогенность групп по массе тела (±10%). Введение препарата осуществляли внутрижелудочно в возрастающих дозах по Литчфилду-Уилкоксону. Наивысшая доза была лимитирована максимально возможным объемом введения препарата. Для исследования каждой дозы препарата использовались группы по 10 животных разного пола. Период наблюдения составлял 14 суток. При введении препарата в дозах 4000-8000 мг/кг (по гуминовой кислоте) у животных выявлено изменение реакции на взятие в руки, изменение дыхания, двигательной активности, и тонуса мускулатуры, у некоторых животных наблюдалось изменение консистенции кала. При введении препарата в дозе до 4000 мг/кг (по гуминовой кислоте) все животные выжили, при введении препарата в концентрации 6000 мг/кг (по гуминовой кислоте) погибло 5 животных из 10, а при введении препарата в дозе 8000 мг/кг (по гуминовой кислоте) погибло 8 животных из 10. Выжившие животные удовлетворительно перенесли интоксикацию и по окончании действия препарата на протяжении 14 дней наблюдения, признаков отсроченного влияния не отмечено. Признаков пролонгированной клинической интоксикации отмечено не было. Динамика массы тела опытных животных не отличалась от контроля. По окончании периода наблюдения - на 14 день, был произведен забой выживших животных с целью определения возможных патологических изменений после однократного приема препарата. Осмотр опытной и контрольных групп показал, что все животные в них были нормально упитаны, имели правильное телосложение, гладкий и блестящий волосяной покров, блестящие, обычной окраски слизистые оболочки, чистые и опрятные естественные отверстия. При макроскопическом исследовании внутренних органов каких-либо особенностей не было выявлено. Анализ величин массовых коэффициентов не выявил каких-либо достоверных отличий между группами животных, получавшими разные дозы препарата. Таким образом, полученные результаты позволяют предположить, что полученные препарат можно отнести к V классу, т.е. практически нетоксичных лекарственных веществ.
Исследование антибактериальной активности заявленного средства.
Пример 1. Антибактериальная активность гуминового средства изобретения (ГС) в отношении бактерий, резистентных к множеству лекарственных средств.
Оценку эффективности проводили in vitro, определяя антибактериальную активность ГС в отношении энтеробактерий (Enterobactenaceae), резистентных к множеству лекарственных средств.
а) Штаммы
Тесты на восприимчивость к лекарственным средствам проводили с использованием ряда штаммов энтеробактерий, резистентных к множеству лекарственных средств. Подробная информация об использованных штаммах приводится в таблице 2.
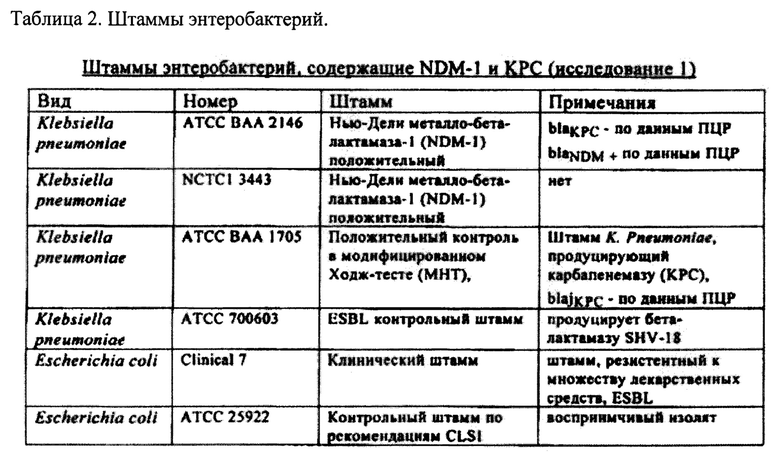
б) Размораживание и рост штаммов микроорганизмов и получение инокулята.
Все штаммы после длительного хранения при -80°С размораживали и культивировали в планшетах на агаре цистин-лактоза-электролит-недостаточный. Затем планшеты инкубировали на воздухе при 35-37°С в течение 24 ч. Если после визуальной оценки колонии соответствовали требованиям чистоты и характеристикам колоний данного штамма микроорганизма, то изоляты признавались пригодными для использования.
Инокулят (посевную культуру) каждого штамма получали следующим образом: собирали клетки из 5-10 индивидуальных колоний, сформировавшихся в культуральных планшетах, а затем клетки суспендировали в 3 мл стерильного физиологического раствора. Инокулят ресуспендировали за счет интенсивного перемешивания в смесителе Vortex в течение 15 с. Затем мутность препаратов доводили до стандартного значения №0,5 по тесту McFarland (1-5×106 КОЕ/мл). Затем инокулят разбавляли бульоном Мюллера-Хинтона, который используют для определения минимальной ингибирующей концентрации (МИК), при этом в каждой лунке планшета конечная концентрация инокулята составляла 2-8×105 КОЕ/мл.
МИК определяли в бульоне Мюллера-Хинтона, как описано в соответствующих рекомендациях Института клинических и лабораторных стандартов (CLSI).
в) Добавление исследуемого препарата ГС.
В качестве исходного раствора использовали 4% раствор. Затем указанный раствор разбавляли средой бульоном Мюллера-Хинтона, при этом получали 2% раствор, т.е. раствор с максимальной начальной концентрацией, используемой в испытаниях. Для сравнения результатов теста использовали контроль для каждого штамма. Диапазон конечных концентраций для контроля (ципрофлоксацин) составлял 0,03-16 мг/мл. В каждую лунку столбцов 2-12 вносили по 100 мкл бульона Мюллера-Хинтона. В каждую лунку столбца 1 вносили по 200 мкл раствора ГС (4%).
Из лунок столбца 1 многоканальным дозатором (коэффициент вариации ±2%) переносили по 100 мкл раствора в лунки столбца 2, таким образом разбавляя раствор в 2 раза. Затем раствор из лунок столбца 2 переносили дозатором по 100 мкл в лунки столбца 3 и т.д. вплоть до столбца 10, из которого последние 100 мкл отбрасывали. Ряд 11 использовали в качестве положительного контроля (лекарственное средство или ГС не добавляли, но добавляли бактериальные штаммы), ряд 12 использовали в качестве отрицательного контроля (лекарственное средство или ГС не добавляли, а также микроорганизмы не добавляли).
В соответствующие лунки вносили по 100 мкл суспензии соответствующего инокулята, разведенного в бульоне Мюллера-Хинтона. В результате конечный объем в лунке составлял 200 мкл (100 мкл разбавленного соединения или разбавителей +100 мкл инокулята или только бульона).
Все планшеты инкубировали в темноте на воздухе при 35-37°С в течение 18-24 ч.
Визуальный анализ и спектрофотометрический анализ (450 нм) планшетов осуществляли через 20 ч или 72 ч после внесения инокулята. В качестве конечных параметров определяли степень ингибирования в %: 50%>, 80%>и 100%> (или конечные параметры оценивали после визуального анализа согласно рекомендациям CLSI).
г) Результаты
Только ГС изобретения проявляло эффективность в отношении штаммов К. Pneumoniae, положительных в отношении NDM-1-, КРС- и ESBL, а также Е. coli, резистентных к множеству лекарственных средств, при этом, как следует из данных, представленных в таблице 3, МИК для ГС, при которой наблюдается 100% ингибирование, составляет только 0,06-0,12%.
ГС изобретения проявляет эффективность по сравнению с ципрофлоксацином, который не эффективен ни в отношении NDM-1-, ни в отношении КРС-положительных штаммов К. Pneumoniae, и МИК которого составляет более 16 мкг/мл. ГС проявляло эффективность в отношении ESBL-положительных штаммов К. Pneumoniae и Е. Coli на уровне ципрофлоксацина.
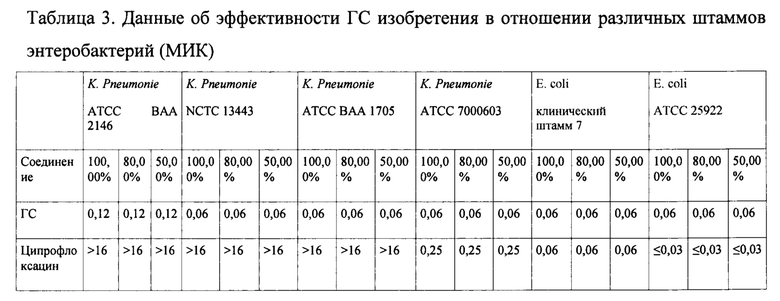
ГС изобретения характеризуется высокой эффективностью в отношении грамотрицательных бактерий, резистентных к множеству лекарственных средств, включая NDM-1 положительные штаммы, при этом 100% ингибирование всех микроорганизмов наблюдается при концентрации ГС ≤0,12%.
Пример 2. Эффективность ГС изобретения в модели инфицирования бедра мыши бактериями К. Pneumoniae
В данном исследовании использовали мышей, не инфицированных специфической патогенной микрофлорой. В работе использовали линию мышей CD1, которая представляет собой хорошо охарактеризованную линию беспородных мышей., при этом мыши имели массу тела 16-18 г и проходили акклиматизацию в течение 7 сут при поступлении (требуемая масса тела животных перед началом экспериментов должна составлять 22-25 г).
Мышей содержали в стерильных индивидуальных вентилируемых клетках для мышей, при этом все время воздух подвергали стерилизации с использованием фильтров НЕРА. Мыши имели свободный доступ к воде и корму (стерильные), дно клетки было покрыто стерильной осиновой стружкой (замену осуществляли через каждые 3-4 сут или по мере необходимости). В помещении поддерживали температуру 22°С±1°С, относительная влажность воздуха составляла 50-60%, максимальный уровень фонового шума составлял 56 дБ. Мышей содержали в 12-часовом циклическом режиме (12 ч свет/12 ч темнота с фазами «рассвет»/«закат»).
Во всех экспериментах использовали штамм Klebsiella pneumoniae АТСС ВАА2146 NDM-1+(blandm).
В указанных исследованиях каждая экспериментальная лечебная группа включала 6 мышей.
У мышей вызывали временную нейтропению за счет подавления иммунного ответа после введения циклофосфамина в дозе 150 мг/кг за 4 сут до инфицирования и 100 мг/кг за 1 сут до инфицирования в виде внутрибрюшинной инъекции. Указанный режим подавления иммунного ответа приводит к развитию нейтропении через 24 ч после введения указанного соединения, которая наблюдается в течение всего эксперимента.
Через 24 ч после введения второй инъекции соединения для подавления иммунного ответа мышей инфицировали, вводя внутримышечно в обе боковые мышцы бедра суспензию К. pneumoniae (2,5×10 КОЕ/бедро мыши).
Антибактериальную терапию начинали через 2 ч после инфицирования и вводили ГС два раза в сутки (интервал между введениями составлял ровно 12 ч). Значение рН аликвоты 4%-ного исходного раствора ГС доводили до 5, используя 10М раствор гидроксида натрия, затем ее разбавляли 0,9% раствором хлорида натрия в соотношении 1:2 или 1:8, при этом соответственно получали 2% (20 мг/кг) и 0,5% (5 мг/кг) раствор ГС, предназначенный для введения. ГС вводили через желудочный зонд.
Через 24 ч после инфицирования оценивали клиническое состояние всех животных, а затем их умерщвляли гуманным способом. Массу тела животного определяли до отделения обоих бедер, которые затем взвешивали каждое в отдельности. Образцы индивидуальных тканей бедра гомогенизировали в охлажденном на ледяной бане стерильном фосфатно-солевом буферном растворе. Затем гомогенизаты тканей бедра культивировали на агаре Cled и инкубировали при 37°С в течение 24 ч, а затем ежедневно подсчитывали число колоний.
В контрольной группе (тяжелая форма инфекции, животным вводили носитель и мышей инфицировали бактериями в количестве ~11 log 10 КОЕ/г) через 24 ч успешно формировалась модель тяжелой формы инфекции бедра бактериями К. pneumoniae. У мышей, которым вводили носитель, наблюдалось инфицирование средней тяжести. Лечение с использованием ГС характеризовалось хорошей переносимостью в ходе испытаний, при этом отрицательные эффекты не наблюдались.
Данные количественной оценки тяжести поражения тканей бедра указывают на то, что наблюдается статистически значимое снижение тяжести поражения тканей бедра по сравнению с мышами, которым вводили только носитель (снижение 1,28 log10, P<0,0001). При этом,
1. ГС (2%), п/о 2, раза в сут (снижение 2,51 log10, P<0,0001),
2. ГС (0,5%), п/о, 2 раза в сут (снижение 2,58 log10, P<0,0001),
Следует отметить, что при лечении ГС при введении 2% и 0,5% растворов (20 и 5 мг/кг) наблюдалась равная эффективность снижения тяжести поражения.
Таким образом заявленное гуминовое средство (ГС) имеет высокую биологическую активность, которая проявляется в антибактериальной эффективности в отношении многих штаммов бактерий, в том числе в отношении Klebsiella pneumoniae, резистентной к множеству лекарственных средств, в модели локального инфекционного поражения бедра. Следовательно, заявленное средство может использоваться в качестве антибактериального средства, что подтверждает достижение заявленного технического результата.
Группа изобретений относится к фармацевтике, а именно к антибактериальному гуминовому средству и его применению в качестве антибактериального препарата. Антибактериальное гуминовое средство содержит воду и гуминовые вещества, полученные из гуминосодержащего сырья, выбранного из группы, включающей леонардит, лигнин, уголь, торф и/или сапропель, методом ультразвукового диспергирования предварительно измельченного сырья в смеси с водой при температуре 30-80°С и давлении 0,05-0,8 МПа, после которого раствор охлаждают до комнатной температуры и разбавляют водой до содержания гуминовых веществ от 1 до 20 мас. %, при этом гуминовые вещества включают гуминовые и фульвокислоты и их соли, а также гидрохинон в количестве, не превышающем 3 мас. % от массы гуминовых веществ. Вышеописанное изобретение позволяет получить и использовать гуминовое средство, содержащее широкий спектр гуминовых веществ и не имеющее химических примесей, обладающее антибактериальным действием. 2 н.п. ф-лы, 4 табл., 2 пр.
1. Антибактериальное гуминовое средство, содержащее воду и гуминовые вещества, полученные из гуминосодержащего сырья, выбранного из группы, включающей леонардит, лигнин, уголь, торф и/или сапропель, методом ультразвукового диспергирования предварительно измельченного сырья в смеси с водой при температуре 30-80°С и давлении 0,05-0,8 МПа, после которого раствор охлаждают до комнатной температуры и разбавляют водой до содержания гуминовых веществ, составляющего от 1 до 20 мас.%, при этом гуминовые вещества включают гуминовые и фульвокислоты и их соли, а также гидрохинон в количестве, не превышающем 3 мас. % от массы гуминовых веществ.
2. Применение гуминового средства по п. 1 в качестве антибактериального препарата.
| C | |||
| E | |||
| J | |||
| Van RENSBURGA et al | |||
| An in vitro investigation of the antimicrobial activity of oxifulvic acid//Article in Journal of Antimicrobial Chemotheraу | |||
| ЩИТОВОЙ ДЛЯ ВОДОЕМОВ ЗАТВОР | 1922 |
|
SU2000A1 |
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
| Гуминовый препарат и способ его получения | 2019 |
|
RU2717659C1 |
| US 2019183760 A1, 20.06.2019 | |||
| СПОСОБ ПОЛУЧЕНИЯ СОЛЕЙ ГУМИНОВЫХ КИСЛОТ | 2001 |
|
RU2205166C1 |
| ЛИТУСОВ Н.В | |||
| Морфология и структура бактерий | |||
| Иллюстрированное учебное | |||
Авторы
Даты
2021-08-18—Публикация
2020-10-16—Подача