Уровень техники изобретения
[0001] 1. Область техники, к которой относится изобретение
[0002] Настоящее изобретение относится к новым фармацевтическим конструкциям, в частности, к фармацевтическим конструкциям, модифицированным двумя или более молекулами жирных кислот или дикарбоновых жирных кислот, что повышает их аффинность связывания с альбумином и увеличивает продолжительность их присутствия в сыворотке крови.
[0003] 2. Описание предшествующего уровня техники
[0004] Разработка фармацевтических препаратов с множественными функциями стала вызывающей очень большой интерес областью исследований. Например, разветвленные линкерные единицы, раскрытые в публикации Международной патентной заявки No. WO 2016112870 (A1) и родственных с ней заявок, представляют собой основные химические соединения для конструирования молекул с двумя или более функциональными частями. Однако в публикации WO 2016112870 для реакции клик-химии используются аминокислоты со встроенными функциональными группами, такими как тетразин, циклооктен и циклооктин; еще эти аминокислоты недоступны для включения в пептидную основу во время твердофазного пептидного синтеза. Кроме того, в соответствии с публикацией WO 2016112870 связывание фрагмента с тетразиновой, циклооктеновой или циклооктиновой группой осуществляется путем встраивания посредством реакции между тиольной группой остатка цистеина и малеимидной группой гетеробифункционального линкера, который содержит малеимидную группу на одном конце и тетразиновую, циклооктеновую или циклооктиновую группу на другом конце. Известно, что продукт реакции тиола и малеимида нестабилен, подвержен обратной реакции или реакции обмена с соседними молекулами, содержащими тиоловую группу, что может повлиять на стабильность конъюгированных линкеров при хранении. Кроме того, когда пептидная основа содержит остаток цистеина, как указано в публикации WO 2016112870, не представляется возможным проводить непрерывный твердофазный синтез (разветвление пептида) связывающих фрагментов с функциональной группой, которая может реагировать с тиольной группой на пептидной основе. Кроме того, альфа-аминогруппа на N-конце пептидной основы требует дополнительного этапа блокирования, тем самым снижая выход и чистоту пептидной основы или линкерной единицы.
[0005] Кроме того, является желательным увеличить время полужизни лекарственных средств в определенных клинических условиях, чтобы требовалось менее частое введение лекарственного средства и происходило меньше колебаний концентраций лекарственного средства в крови, что может привести к снижению затрат и повышению приверженности лечению.
[0006] Для увеличения времени полужизни лекарственных средств применяется несколько методологий. Это может быть достигнуто структурным изменением, таким как мутации аминокислотных остатков пептидных или белковых молекул лекарственного средства, без обращения к специальной композиции или конъюгации с другими химическими фрагментами. Например, внесение аминокислотных замен для снижения чувствительности к протеазам, изменения изоэлектрических точек и увеличения растворимости в липидах может увеличить время полужизни некоторых лекарственных средств. Генетически измененный тканевой активатор плазминогена, тенектеплаза, имеет несколько сайт-специфичных мутаций и устойчив к ингибитору активатора плазминогена и, следовательно, имеет более продолжительное время полужизни, чем активаза дикого типа. Присутствующая на рынке версия инсулина человека (инсулин гларгин), которая содержит остаток аспарагина, заменяющий глицин, и снижает растворимость при нейтральном значении рН, агрегирует при подкожной инъекции пациенту. Агрегированный инсулин затем медленно растворяется и диффундирует в систему кровообращения и, следовательно, достигает более продолжительного времени полужизни, чем у обычного (дикого типа) инсулина.
[0007] Некоторые лекарственные средства смешивают с образующими матрицу веществами, такими как поли-лактид-со-гликолид, или упаковывают в липосомы или другие типы микросфер/наночастиц. Когда такие лекарственные препараты вводят пациенту, они обеспечивают кинетику замедленного высвобождения. Некоторые химиотерапевтические препараты, такие как таксол и доксорубицин, и гормоны, такие как аналог соматостатина, (ацетат октреотида) и аналог гонадотропин-рилизинг-гормона (лейпрорелин), изготавливают с микросферами в качестве депо для длительного медленного высвобождения.
[0008] Многие белковые лекарственные средства, такие как интерферон-α, интерферон-β, эритропоэтин, гормон роста человека, гранулоцитарный колониестимулирующий фактор, аденозиндеаминаза и аспарагиназа, модифицированы полиэтиленгликолем (ПЭГ) для улучшения фармакокинетической активности и стабильности, и уменьшения иммуногенности. Недостатком использования ПЭГ для модификации является неоднородность конъюгированных продуктов. Длинноцепочечный ПЭГ может также оборачиваться вокруг молекулы белка и, таким образом, ингибировать активность белкового лекарственного средства. Длинноцепочечный ПЭГ также устойчив к деградации и накапливается у пациентов.
[0009] Другая методология для улучшения фармакокинетических свойств белкового лекарственного средства заключается в слиянии белка с доменами CH2-CH3 Fc части IgG. Белковое лекарственное средство и сегмент CH2-CH3 экспрессируются в виде непрерывного рекомбинантного пептида, и два из таких пептидов образуют димерную конфигурацию. Fc-слитые белки рецепторов некоторых цитокинов и белков клеточной поверхности, такие как белатацепт для белка 4 цитотоксических Т-лимфоцитов (CTLA-4), этанерцепт для фактора некроза опухоли-α (ФНО-α), афлиберцепт для фактора роста эндотелия сосудов (VEGF) и рилонацепт для интерлейкина 1 (IL-1), были разработаны и широко используются в клинической практике. Многие из цитокинов и рецепторов цитокинов имеют время полужизни в сыворотке менее 1 дня. Конъюгация с Fc IgG может удлинить время их полужизни до более чем 1 недели.
[0010] Слияние с альбумином представляет собой еще один способ продлить время полужизни пептидного или белкового лекарственного препарата. Альбумин имеет время полужизни в кровотоке равное 19 дням. Поскольку альбумин представляет собой белок, состоящий из одного полипептида, слитый белок альбумина с пептидом или белком может быть получен в виде рекомбинантного пептида. Например, альбиглютид является слитым белком альбумина с димером дипептидилпепдидаза-4-устойчивого глюкагоноподобного пептида 1 (GLP-1), и он был одобрен для лечения диабета 2 типа. Альбиглютид имеет время полужизни в сыворотке 4-7 дней, по сравнению с 1-2 часами обычного GLP-1. Идельвион представляет собой слитый белок альбумина с фактором коагуляции IX. Он позволяет проводить лечение один раз каждые 14 дней для контроля и предотвращения кровотечений у детей и взрослых, страдающих гемофилией B.
[0011] Тем не менее обычные средства для увеличения времени полужизни в сыворотке терапевтических лекарственных препаратов не являются достаточно гибкими. То есть часто они не могут быть адаптированы к лекарственным средствам, для которых требуются разные фармакокинетические профили. Следовательно, поиск лекарственных средств с улучшенными или регулируемыми фармакокинетическими характеристиками остается важным направлением исследований и разработок.
Сущность изобретения
[0012] В первом аспекте настоящее изобретение относится к платформенной технологии, связанной с линкерными единицами, для увеличения времени полужизни в сыворотке терапевтического лекарственного средства. В частности, линкерная единица содержит два или более производных жирных кислот или производных дикарбоновых жирных кислот, которые могут быть конъюгированы с терапевтическим лекарственным средством (одного или нескольких лекарственных средств) при помощи реакции клик-химии. Таким образом, цепи жирных кислот линкерной единицы могут встраиваться в разные гидрофобные полости одного сывороточного альбумина человека (HSA) или в гидрофобные полости разных HAS, увеличивая тем самым силу связывания линкерной единицы (и, следовательно, конъюгата линкерной единицы и лекарственного средства в целом), с HSA. Кроме того, при помощи настоящей платформенной технологии можно легко регулировать число цепей жирных кислот и расстояние между двумя цепями жирных кислот. Таким образом, можно изменять фармакокинетический профиль терапевтического лекарственного средства по мере необходимости или по желанию, варьируя длину и количество цепей жирных кислот, и расстояние между двумя цепями жирных кислот.
[0013] В соответствии с некоторыми вариантам осуществления настоящего изобретения, линкерная единица содержит центральную основу и от 2 до 5 первых элементов. В соответствии с вариантами осуществления настоящего изобретения центральная основа содержит,
(1) от 2 до 5 остатков лизина (K);
(2) необязательно, один или несколько наполнителей, где любые два из остатков K непосредственно следуют друг за другом или разделены наполнителем;
(3) необязательно, концевой спейсер, где концевые спейсеры представляют собой N-концевой спейсер, связанный с N-концом первого остатка K, или C-концевой спейсер, связанный с C-концом последнего остатка K; и
(4) конъюгирующий фрагмент, связанный с концевым остатком K, или, в случае присутствия концевого спейсера, концевым аминокислотным остатком концевого спейсера путем образования с ним амидной связи, где конъюгирующий фрагмент имеет конъюгирующую группу, выбранную из группы, состоящей из азидной, алкиновой, тетразиновой, циклооктеновой и циклооктиновой группы.
[0014] Как правило, основа содержит 2, 3, 4 или 5 остатков K. В разных вариантах осуществления изобретения любые два из остатков K непосредственно следуют друг за другом (то есть между ними нет наполнителя) или разделены наполнителем. Когда имеется несколько наполнителей, состав каждого наполнителя может отличаться друг от друга.
[0015] По своей структуре каждый из множества наполнителей и концевого спейсера независимо содержит (i) от 1 до 12 аминокислотных остатков, которые независимо выбраны из аминокислотных остатков, отличных от остатка K, или (ii) пегилированную аминокислоту, имеющую от 1 до 12 мономерных единиц этиленгликоля (EG). В соответствии с некоторыми иллюстративными вариантами осуществления изобретения наполнитель или концевой спейсер может содержать один или несколько остатков глицина (G) и/или серина (S). В некоторых примерах наполнитель или концевой спейсер состоит из 2-10 аминокислотных остатков; предпочтительно от 2 до 5 аминокислотных остатков. В некоторых вариантах осуществления изобретения наполнитель или концевой спейсер содержит от 2 до 5 повторов EG.
[0016] В соответствии с некоторыми вариантами осуществления настоящего изобретения основа содержит N-концевой спейсер, который связан с N-концом первого связывающего аминокислотного остатка, начиная с N-конца. Дополнительно или альтернативно, основа содержит C-концевой спейсер, который связан с C-концом последнего связывающего аминокислотного остатка, начиная с N-конца.
[0017] В соответствии с некоторыми необязательными вариантами осуществления настоящего изобретения линкерная единица содержит два конъюгирующих фрагмента (например, первый конъюгирующий фрагмент и второй конъюгирующий фрагмент).
[0018] В некотором необязательном варианте осуществления изобретения конъюгирующий фрагмент может иметь функциональную группу, которая способна образовывать ковалентную связь с α-аминогруппой (-NH2) концевого аминокислотного остатка (то есть первого связывающего аминокислотного остатка или N-концевого аминокислотного остатка N-концевого спейсера) или карбоксильной группой (-COOH) концевого аминокислотного остатка (то есть последнего связывающего аминокислотного остатка или С-концевого аминокислотного остатка С- концевого спейсера), так что конъюгирующий фрагмент становится связанным с ними. В конкретном варианте осуществления изобретения основа может иметь только один из N- и C-концевых спейсеров и имеет как первый, так и второй конъюгирующие фрагменты, которые соответственно связаны с двумя концевыми аминокислотными остатками (которые могут быть концевым связывающим аминокислотным остатком или концевым аминокислотным остатком концевого спейсера). Также существуют варианты осуществления, в которых основа содержит оба N- и C-концевых спейсера, и два конъюгирующих фрагмента соответственно связаны с концевыми аминокислотными остатками двух концевых спейсеров. В предпочтительных вариантах осуществления изобретения ковалентная связь, образованная между конъюгирующим фрагментом и концевым аминокислотным остатком, представляет собой амидную связь. Понятно, что для обеспечения однородности полученной линкерной единицы важно, чтобы один конъюгирующий фрагмент имел только одну функциональную группу, способную реагировать либо с α-аминогруппой, либо с карбоксильной группой.
[0019] При выборе двух конъюгирующих групп желательно, чтобы эти две конъюгирующие группы не могли вступить в реакцию клик-химии. В соответствии с одним вариантом осуществления изобретения, когда первая конъюгирующая группа представляет собой азидную, алкиновую или циклооктиновую группу, вторая конъюгирующая группа не может быть любой из азидной, алкиновой или циклооктиновой группы, чтобы избежать реакции между двумя конъюгирующими группами; предпочтительно связывающая группа может быть тетразиновой или циклооктеновой группой. В некоторых других вариантах осуществления изобретения, когда первая конъюгирующая группа представляет собой тетразиновую или циклооктеновую группу, вторая конъюгирующая группа не может быть тетразиновой или циклооктеновой группой; вместо этого вторая конъюгирующая группа может быть азидной, алкиновой или циклооктиновой группой. Понятно, что в ситуации, когда два конъюгирующих фрагмента предназначены для конъюгирования с одним видом функционального элемента, конъюгирующие группы двух конъюгирующих фрагментов могут быть одинаковыми или могут подвергаться одной и той же реакции клик-химии.
[0020] Каждый из первых элементов независимо представляет собой производное C8-28 жирной кислоты или производное C8-28 дикарбоновой жирной кислоты и связано с одним из остатков K через ε-аминокислотную группу остатка K. В соответствии с различными вариантами осуществления настоящего изобретения первый элемент представляет собой производное жирной кислоты, которое получают из октановой кислоты, пеларгоновой кислоты, декановой кислоты, ундекановой кислоты, лауриновой кислоты, тридекановой кислоты, миристиновой кислоты, пентадекановой кислоты, пальмитиновой кислоты, маргариновой кислоты, стеариновой кислоты, нонадекановой кислоты, арахидиновой кислоты, геникозановой кислоты, бегеновой кислоты, трикозановой кислоты, лигноцериновой кислоты, пальмитолеиновой кислоты, олеиновой кислоты, линолевой кислоты, рицинолевой кислоты или вакценовой кислоты, эйкозапентаеновой кислоты (ЭПК) докозагексановой кислоты (ДГК). В соответствии с некоторыми вариантами осуществления настоящего изобретения первый элемент представляет собой производное дикарбоновой жирной кислоты, которое получают из субериновой кислоты, азелаиновой кислоты, себациновой кислоты, ундекандиовой кислоты, додекандиовой кислоты, брассиловой кислоты, тетрадекандиовой кислоты, пентадекандиовой кислоты, тапсиевой кислоты, гептадекандиовой кислоты или октадекандиовой кислоты. В некоторых вариантах осуществления настоящий первый элемент получают из миристиновой кислоты или пальмитиновой кислоты. В других вариантах осуществления настоящий первый элемент получают из тетрадекандиовой кислоты или тапсиевой кислоты.
[0021] В некоторых вариантах осуществления изобретения производное жирной кислоты (или дикарбоновой жирной кислоты) представляет собой химически модифицированную молекулу жирной кислоты (или дикарбоновой жирной кислоты). Например, карбоксильная группа молекулы жирной кислоты (или одна из карбоксильной группы молекулы дикарбоновой жирной кислоты) реагирует с химической молекулой с двумя функциональными группами, в которых одна функциональная группа является карбоксил-реактивной (образуя, таким образом, ковалентную связь с молекулой (дикарбоновой) жирной кислоты), тогда как другая функциональная группа является группой, реагирующей с аминогруппой боковой цепи остатка лизина. В соответствии с необязательными вариантами осуществления настоящего изобретения химическая молекула, модифицирующая молекулу (дикарбоновой) жирной кислоты, представляет собой глутаматный остаток, аспартатный остаток, амино-ЭГ2-кислоту, гамма-аминомасляную кислоту или тому подобное; однако настоящее изобретение не ограничивается этими молекулами.
[0022] В соответствии с вариантами осуществления настоящего изобретения два или более первых элементов, связанных с основой, могут быть одинаковыми или разными. Понятно, что во время твердофазного синтеза пептидной основы вместо присоединения первых элементов к основе после того, как основа была синтезирована, также возможно включение в пептидную цепь остатка аминокислоты K, модифицированного конкретным первым элементом. Таким образом, в соответствии с различными вариантами осуществления настоящего изобретения, остатки K, модифицированные различными первыми элементами, могут быть добавлены последовательно во время твердофазного синтеза, чтобы получить группу однородных линкерных единиц, где каждая линкерная единица может иметь два или более связанных с ней различных первых элементов.
[0023] В соответствии с некоторыми вариантами осуществления настоящего изобретения, настоящая линкерная единица дополнительно содержит второй элемент, который связан с конъюгирующей группой при помощи катализируемой медью реакции азид-алкинового циклоприсоединения (CuAAC), реакции клик-химии активированных азида и алкина (SPAAC) или реакции Дильса-Алдера с обращенными электронными требованиями (iEDDA). Вторым элементом может быть любая молекула, которая обеспечивает терапевтическую пользу при лечении заболевания или патологического состояния. Предпочтительно, вторым элементом является лекарственное средство на основе пептида, например, инсулин, инсулиноподобный фактор роста, агонист глюкагоноподобного пептида-1, соматостатин и аналоги соматостатина, кальцитонин, гормон роста, эритропоэтин, гонадотропин-рилизинг-фактор, гранулоцитарный колониестимулирующий фактор, аденозиндеаминаза, аспарагиназа, интерферон-α, интерферон-β, рецептор ФНО-α, рецептор IL-1, рецептор EGF, агалсидаза β, агалсидаза α, ларонидаза, идурсульфаза, альглюкозидаза α и галсульфаза, или их производное или вариант.
[0024] Понятно, что вторая молекула может быть модифицирована так, чтобы иметь реакционноспособную группу, соответствующую конъюгирующей группе, так чтобы второй элемент был связан с конъюгирующей группой основы. В некоторых вариантах осуществления изобретения лекарственное средство на основе пептида может иметь только один остаток лизина или один неспаренный остаток цистеина, и такой остаток лизина или цистеина не является важным для биологической активности или терапевтической функциональности лекарственного средства на основе пептида; в этих случаях остаток лизина или неспаренного цистеина модифицируют реакционноспособной группой. Например, химическая молекула, имеющая реакционноспособную группу, реагирует ε-аминогруппой остатка лизина или SH-группой остатка цистеина. В некоторых вариантах осуществления изобретения химическая молекула, имеющая реакционноспособную группу, может представлять собой бифункциональный сшивающий агент, в котором функциональная группа на одном конце является реакционноспособной по отношению к ε-аминогруппе или группе SH, а другой конец имеет реакционноспособную группу. Кроме того, для лекарственного средства на основе пептида без остатка лизина или остатка цистеина, доступный для растворителя остаток на поверхности белковой молекулы, который не требуется для биологической активности белка, может быть мутирован в остаток лизина или цистеина. В некоторых вариантах осуществления изобретения лекарственное средство на основе пептида может иметь остаток лизина или цистеина, который важен для биологической активности лекарственного средства, или лекарственное средство на основе пептида может иметь более одного остатка лизина или несколько парных остатков цистеина. В этих случаях доступный для растворителя остаток на поверхности белковой молекулы, который не требуется для биологической активности белка, может быть мутирован в остаток цистеина. В качестве другого примера, альфа-аминогруппа N-концевого аминокислотного остатка лекарственного средства на основе пептида может быть модифицирована реакционноспособной группой; такой Пример особенно подходит для пептидов, полученных с использованием твердофазного синтеза. Понятно, что вышеупомянутые стратегии являются только иллюстративными примерами модификации лекарственного средства на основе пептида таким образом, чтобы оно имело реакционноспособную группу, которая может подвергаться реакции клик-химии с конъюгирующей группой основы, и что настоящее изобретение не ограничивается этими примерами.
[0025] В некоторых необязательных вариантах осуществления изобретения второй элемент может присутствовать в форме группы лекарственных средств, которая содержит более одного второго элемента. Например, группа лекарственных средств может иметь структуру, описанную в публикациях Международных патентных заявок Nos. WO 2016/112870, WO 2016/184426, WO 2017/036255 и WO 2017/036407; полное содержание этих публикаций приведено здесь путем ссылки. Альтернативно, группа лекарственных средств может содержать структуру, которая аналогична структуре линкерной единицы настоящего изобретения, за исключением того, что первый элемент (то есть производное жирной кислоты или дикарбоновой жирной кислоты) заменяется вторым элементом, описанным выше. В кратком изложении, группа лекарственных средств содержит вторую основу, второй конъюгирующий фрагмент, множество необязательных вторых связывающих фрагментов, один или несколько необязательных наполнителей и один или два необязательных концевых спейсера, и второй элемент связан с основой через аминогруппу боковой цепи остатков лизина во второй основе или во втором связывающем фрагменте.
[0026] Предпочтительно, когда линкерная единица содержит две конъюгирующие группы (то есть первую и вторую конъюгирующие группы), одна из конъюгирующих групп представляет собой азидную, пиколилазидную, алкиновую или циклооктиновую группу, а другая из конъюгирующих групп представляет собой тетразиновую или циклооктеновую группу.
[0027] При необходимости, линкерная единица может дополнительно содержать второй и третий элементы, соответственно связанные с конъюгирующими группами (то есть с первой и второй конъюгирующими группами), в которых второй элемент связан с первой конъюгирующей группой при помощи реакции CuAAC, реакции SPAAC или реакции iEDDA; и третий элемент связан со второй конъюгирующей группой при помощи реакции CuAAC, реакции SPAAC или реакции iEDDA, которая отличается от реакции между вторым элементом и первой конъюгирующей группой.
[0028] Как правило, циклооктеновая группа представляет собой норборнен или транс-циклооктен (TCO); и циклооктиновая группа представляет собой дибензоциклооктин (DBCO или DIBO), дифторированный циклооктин (DIFO), бициклононин (BCN) или дибензоазациклооктин (DIBAC). Тетразиновая группа представляет собой 1,2,3,4-тетразин, 1,2,3,5-тетразин или 1,2,4,5-тетразин или их производные. Азидная группа может быть пиколилазидной или -N3 группой.
Краткое описание чертежей
[0029] Настоящее описание будет лучше понято из следующего подробного описания в свете прилагаемых чертежей, кратко обсуждаемых ниже.
[0030] Фиг. 1A-1H представляют собой схематические диаграммы, иллюстрирующие центральные основы в соответствии с некоторыми вариантами осуществления настоящего изобретения.
[0031] Фиг. 2A-2C представляют собой схематические диаграммы, иллюстрирующие линкерные единицы в соответствии с некоторыми вариантами осуществления настоящего изобретения.
[0032] Фиг. 3A-3C представляют собой схематические диаграммы, иллюстрирующие линкерные единицы T-E в соответствии с некоторыми вариантами осуществления настоящего изобретения.
[0033] На фиг. 4А и 4В показаны соответственно профиль аналитической ВЭЖХ с обращенной фазой и результат MALDI-TOF азидсодержащего агониста GLP-1 в соответствии с одним примером настоящего изобретения.
[0034] На фиг. 5 показан результат MALDI-TOF алкинсодержащей линкерной единицы, имеющей две пальмитоильные цепи, в соответствии с одним примером настоящего изобретения.
[0035] На фиг. 6А и 6В соответственно показаны аналитической профиль ВЭЖХ с обращенной фазой и результат MALDI-TOF для DBCO-содержащей разветвленной линкерной единицы, конъюгированной с тремя аналогами соматостатина, в соответствии с одним примером настоящего изобретения.
[0036] На фиг. 7 показан анализ MALDI-TOF алкинсодержащей линкерной единицы с двумя пальмитильными цепями в соответствии с одним примером настоящего изобретения.
[0037] На фиг. 8А и фиг. 8В показаны соответственно профиль аналитической ВЭЖХ с обращенной фазой и результат MALDI-TOF агониста GLP-1-Ala8-EG4-2FA-C16 в соответствии с одним примером настоящего изобретения.
[0038] На фиг. 9A и фиг. 9B соответственно показаны профиль аналитической ВЭЖХ с обращенной фазой и результат MALDI-TOF GLP-1-Ala8-EG4-2E-2FA-C16 в соответствии с одним примером настоящего изобретения.
[0039] На фиг. 10A и фиг. 10B соответственно показаны профиль аналитической ВЭЖХ с обращенной фазой и MALDI-TOF агониста GLP-1-Aib8-EG4-2E-2FA-C16 в соответствии с одним примером настоящего изобретения.
[0040] На фиг. 11А и фиг. 11В соответственно показаны профиль аналитической ВЭЖХ с обращенной фазой и MALDI-TOF агониста кислоты GLP-1-Aib8-EG4-2E-2FA-C16 в соответствии с одним примером настоящего изобретения.
[0041] На фиг. 12A и фиг. 12B соответственно показаны профиль аналитической ВЭЖХ с обращенной фазой и MALDI-TOF агониста кислоты GLP-1-Aib8-EG2-2E-2FA-C16 в соответствии с одним примером настоящего изобретения.
[0042] На фиг. 13А и фиг. 13В соответственно показаны профиль аналитической ВЭЖХ с обращенной фазой и MALDI-TOF агониста кислоты GLP-1-Aib8-EG2-2E-2FA-C18 в соответствии с одним примером настоящего изобретения.
[0043] Фиг. 14 представляет собой результат ИФА анализа, который показывает аффинность связывания агониста 2FA-GLP-1 с рецептором GLP-1, где слитый белок GLP-1R-IgG.Fc нанесен на планшет для микротитрования с последующим добавлением азидсодержащего агониста GLP-1 (GLP-1-азид), агониста 2FA-GLP-1 (2FA-GLP-1), лираглутида и контрольного пептида (пептид P1-P2, GLAGGSAQSQRAPDRVLCHSGQQQGLPRAAGGSVPHPR, SEQ ID NO: 3) конечная концентрация 1 или 10 мкг/мл, в соответствии с одним примером настоящего изобретения.
[0044] Фиг. 15 представляет собой результат ИФА анализа, который показывает аффинность связывания агониста 2FA-GLP-1 с человеческим сывороточным альбумином (HSA), в котором HSA наносят на планшет для микротитрования с последующим добавлением азидсодержащего агониста GLP-1 (GLP-1-азид), лираглутида, 2FA- агониста GLP-1 (2FA-GLP-1) и алкинсодержащего 2FA (Алкин-2FA), в соответствии с одним примером настоящего изобретения.
[0045] На фиг. 16А и 16В соответственно показана аффинность связывания агониста 2FA-GLP-1 с HSA с использованием анализа диализного равновесия и процентного содержания агониста 2FA-GLP-1 и лираглутида, связанного с HSA.
[0046] На фиг. 17 показано измерение цАМФ клеток INS-1, инкубированных с синтезированными аналогами GLP-1, в соответствии с одним примером настоящего изобретения.
[0047] На фиг. 18А и 18В показаны результат анализа ингибирования экспрессии активированной каспазы-3 в клетках INS-1 синтезированными аналогами GLP-1 в соответствии с одним примером настоящего изобретения.
[0048] На фиг. 19 показаны результаты анализа пролиферации клеток INS-1, инкубированных с синтезированными аналогами GLP-1, в соответствии с одним примером настоящего изобретения.
[0049] В соответствии с общепринятой практикой различные описанные признаки/элементы изображены не в масштабе, а вместо этого нарисованы для лучшей иллюстрации конкретных признаков/элементов настоящего изобретения. Кроме того, одинаковые ссылочные позиции и обозначения на различных чертежах используются для обозначения одинаковых элементов/частей там, где это возможно.
Описание
[0050] Подробное описание, приведенное ниже вместе с прилагаемыми чертежами, предлагается в качестве описания настоящих примеров и не предназначено для представления единственных форм, в которых настоящий Пример может быть воспроизведен или использован. В описании изложены функции примера и последовательность этапов для осуществления и применения примера. Однако одинаковые или эквивалентные функции и последовательности могут быть выполнены с помощью различных примеров.
[0051] Для удобства некоторые термины, используемые в описании, примерах и прилагаемой формуле изобретения, собраны здесь ниже. Если иное не определено в данном документе, научные и технические термины, используемые в настоящем изобретение, должны иметь те значения, которые обычно понимаются и используются специалистом в данной области техники.
[0052] Если контекст не требует иного, следует понимать, что термины в единственном числе включают в себя множественные формы одного и того же термина, а термины во множественном числе должны включать в себя единственное число. В частности, используемые в описании и в формуле изобретения формы единственного числа включают в себя ссылку на множественное число, если из контекста явно не следует иное. Также используемые в описании и в формуле изобретения термины «по меньшей мере, один» и «один или более» имеют одинаковое значение и включают в себя один, два, три или более. Кроме того, предполагается, что используемые в данном описании и прилагаемой формуле изобретения термины «по меньшей мере, один из A, B и C», «по меньшей мере, один из A, B или C» и «по меньшей мере, один из A, B и/или C» включают в себя только A, только B, только C, A и B вместе, B и C вместе, A и C вместе, а также A, B и C вместе.
[0053] Несмотря на то что числовые диапазоны и параметры, определяющие широкий объём изобретения, являются приблизительными, числовые значения, приведенные в конкретных примерах, сообщаются с максимально возможной точностью. Однако любое числовое значение по своей природе содержит определенные ошибки, неизбежно возникающие из-за стандартного отклонения, обнаруженного в соответствующих тестовых измерениях. Кроме того, используемый здесь термин «примерно» обычно означает «в пределах 10%, 5%, 1% или 0,5% от заданного значения или диапазона». Альтернативно, термин «примерно» означает «в пределах допустимой стандартной ошибки среднего значения», как это понимает специалист в данной области техники. За исключением операционных/рабочих примеров, или если иное прямо не указано, все числовые диапазоны, количества, значения и проценты, такие как приводимые в данном документе для количеств материалов, продолжительности времени, температуры, рабочих условий, соотношений количеств и тому подобного, следует понимать как измененные во всех случаях термином «примерно». Соответственно, если не указано иное, то числовые параметры, изложенные в настоящем описании и прилагаемой формуле изобретения, являются приблизительными значениями, которые могут изменяться по желанию. По крайней мере, каждый числовой параметр должен быть, по меньшей мере, истолкован с учетом числа сообщаемых значащих цифр и с использованием обычных методов округления. Диапазоны могут быть выражены здесь как от одной конечной точки к другой конечной точке или указаны как интервал между двумя конечными точками. Все раскрытые в здесь диапазоны включают в себя конечные точки, если не указано иное.
[0054] Настоящее изобретение в целом относится к линкерным единицам, где каждая линкерная единица содержит от двух до пяти гидрофобных цепей (группа жирных кислот), которые могут увеличивать или изменять время полужизни терапевтического лекарственного средства в сыворотке крови. Линкерная единица также содержит эффекторный элемент или связку лекарственного средства, содержащую множество эффекторных элементов. Эффекторный элемент или группу лекарственных средств, связанных с группой жирных кислот при помощи реакции клик-химии. Линкерная единица также может содержать нацеливающий элемент, способный направлять линкерную единицу к месту заболевания у субъекта или рядом с ним.
[0055] Используемый здесь термин «нацеливающий элемент» относится к части линкерной единицы, которая прямо или опосредованно связывается с представляющей интерес мишенью (например, рецептором на поверхности клетки или белком в ткани), облегчая тем самым транспортировку настоящей линкерной единицы к представляющей интерес мишени. В некоторых примерах нацеливающий элемент может направлять линкерную единицу к месту рядом с клеткой-мишенью. В других случаях нацеливающий элемент специфично связывается с молекулой, присутствующей на поверхности клетки-мишени, или со второй молекулой, которая специфично связывается с молекулой, присутствующей на поверхности клетки. В некоторых случаях нацеливающий элемент может быть интернализован вместе с настоящей линкерной единицей, как только она связывается с представляющей интерес мишенью, следовательно, перемещается в цитозоль клетки-мишени. Направляющий элемент может представлять собой антитело или лиганд для рецептора клеточной поверхности, или он может быть молекулой, которая связывает такое антитело или лиганд, тем самым опосредовано нацеливая настоящую линкерную единицу на сайт-мишень (например, на поверхность выбранной клетки). Локализация эффектора (терапевтического агента) в пораженном участке будет усиливаться или улучшаться с помощью настоящих линкерных единиц по сравнению с терапевтическим средством без целевой функции. Локализация определяется как степень или относительная пропорция; оно не является абсолютной или полной локализации эффектора в пораженном участке.
[0056] В соответствии с настоящим изобретением термин «эффекторный элемент» относится к части линкерной единицы, которая вызывает биологическую активность (например, индукцию или подавление иммунной активности, проявление цитотоксических эффектов, ингибирование ферментов и тому подобное) или другую функциональную активность (например, рекрутирование иммуноцитов или других меченых гаптенами терапевтических молекул) после того, как линкерная единица направлена на свой сайт-мишень. «Эффект» может быть терапевтическим или диагностическим. Эффекторные элементы включают в себя те, которые связываются с клетками и/или внеклеточными иммунорегуляторными факторами. Эффекторный элемент включает в себя такие агенты, как белки, нуклеиновые кислоты, липиды, углеводы, гликопептиды, лекарственные вещества (как низкомолекулярные лекарственные средства, так и биологические препараты), соединения, элементы и изотопы, а также их фрагменты.
[0057] Хотя термины «первый, второй, третий и т.д.» могут использоваться здесь для описания различных элементов, компонентов, областей и/или разделов, эти элементы (а также компоненты, области и/или разделы) не ограничиваются этими терминами. Кроме того, использование таких порядковых чисел не подразумевает последовательность или порядок, если это явно не следует из контекста. Как правило, эти термины просто используются, чтобы отличить один элемент от другого. Таким образом, первый элемент, обсуждаемый ниже, может быть назван вторым элементом, не отступая от идей приведенных в качестве примеров вариантов осуществления изобретения.
[0058] Термины «связь», «пара» и «конъюгаты» используются здесь взаимозаменяемо для обозначения любых средств соединения двух компонентов либо через прямую связь, либо через опосредованную связь между двумя компонентами.
[0059] Используемый здесь термин «полипептид» относится к полимеру, имеющему, по меньшей мере, два аминокислотных остатка. Как правило, полипептид содержит аминокислотные остатки в количестве от 2 до около 200 остатков; предпочтительно от 2 до 50 остатков. Когда в настоящем изобретении упоминается аминокислотная последовательность, то также имеются в виду варианты последовательности с L-, D- или бета-аминокислотами. Полипептиды также включают в себя аминокислотные полимеры, в которых один или несколько аминокислотных остатков являются искусственным химическим аналогом соответствующей встречающейся в природе аминокислоты, а также встречающихся в природе аминокислотных полимеров. Кроме того, этот термин применяется к аминокислотам, соединенным пептидной связью или другими «модифицированными связями», например, когда пептидная связь заменена α-эфиром, β-эфиром, тиоамидом, фосфорамидом, карбоксатом, гидроксилатом, и тому подобным. В настоящем изобретении термин «терапевтические препараты на основе пептидов» или «лекарственные препараты на основе пептидов» используется в широком смысле для обозначения любых молекул с терапевтическим эффектом, содержащих в основном аминокислотные остатки, такие как иммуноглобулины, антитела, фрагменты антител, ферменты, факторы роста, рецепторы, цитокины и так далее.
[0060] В некоторых вариантах осуществления изобретения предусматриваются консервативные замены аминокислот, содержащихся в любой из последовательностей, описанных в настоящем изобретении. В различных вариантах осуществления изобретения один, два, три, четыре или пять различных остатков являются замещенными. Термин «консервативная замена» используется для отражения аминокислотных замен, которые существенно не изменяют активность (например, биологическую или функциональную активность и/или специфичность) молекулы. Как правило, консервативные аминокислотные замены включают в себя замену одной аминокислоты другой аминокислотой со сходными химическими свойствами (например, заряд или гидрофобность). Некоторые консервативные замены включают в себя «замены аналогом», где стандартную аминокислоту заменяют нестандартной (например, редкой, синтетической и т.д.) аминокислотой, минимально отличающейся от исходного остатка. Аминокислотные аналоги являются полученными синтетическим путем из стандартных аминокислот без достаточного изменения структуры исходной аминокислоты, являются изомерами или предшественниками метаболитов. В настоящей заявке аминокислотные остатки (1) лизин, который содержит группу NH2 в своей боковой цепи, (2) цистеин, который содержит группу SH в своей боковой цепи, (3) серин и треонин, которые содержат OH группу в своих боковых цепях, и (4) аспарагиновая кислота и глутаминовая кислота, которые содержат группу CO2H в своих боковых цепях, считаются четырьмя отдельными группами аминокислот. Эти четыре группы аминокислот содержат в своих боковых цепях уникальную функциональную группу, которую можно использовать для конъюгирования с различными химическими компонентами. Неприродные аминокислоты, которые содержат одинаковые функциональные группы в боковых цепях, могут быть заместителями для аналогичных целей. Важно отметить, что группа CO2H остатка аспарагиновой кислоты или глутаминовой кислоты может подвергаться реакции образования амидной связи с группой NH2 элемента. Такая химическая реакция подобна образованию амидной связи между группой NH2 остатка лизина и элементом, который имеет группу CO2H. Таким образом, остаток аспарагиновой кислоты или глутаминовой кислоты может быть использован вместо остатка лизина в центральной основе, и для конъюгации первых элементов могут использоваться одинаковые химические реакции для образования амидной связи.
[0061] В некоторых вариантах осуществления настоящее изобретение также относится к полипептидам, имеющим, по меньшей мере, 80%, предпочтительно, по меньшей мере, 85% или 90% и более предпочтительно, по меньшей мере, 95% или 98% идентичности по последовательностей с любой из описанных здесь последовательностей.
[0062] «Процент (%) идентичности аминокислотной последовательности» по отношению к указанным здесь полипептидным последовательностям определяется как процент полипептидных остатков в последовательности-кандидате, которые идентичны аминокислотным остаткам в конкретной полипептидной последовательности после выравнивания последовательности и введения пропусков, если это необходимо, для достижения максимальной процентной идентичности последовательности, не рассматривая любые консервативные замены как часть идентичности последовательности. Выравнивание для определения процента идентичности последовательности может проводить различными способами, которые известны специалисту в данной области техники, например, с использованием общедоступного программного обеспечения, такого как программное обеспечение BLAST, BLAST-2, ALIGN или Megalign (DNASTAR). Специалисты в данной области техники могут определить подходящие параметры для оценки выравнивания, включая любые алгоритмы, необходимые для достижения максимального выравнивания по всей длине сравниваемых последовательностей. Для целей настоящего изобретения сравнение последовательностей в случае двух полипептидных последовательностей осуществляли с помощью компьютерной программы Blastp (белок-белок BLAST), предоставленной в режиме онлайн Национальным центром биотехнологической информации (NCBI). Процент идентичности аминокислотной последовательности данной полипептидной последовательности A с данной полипептидной последовательностью B (что можно альтернативно сформулировать как данная полипептидная последовательность A, которая имеет определенный % идентичности аминокислотной последовательности с данной полипептидной последовательностью B) рассчитывают по следующей формуле:
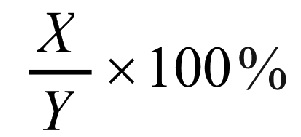
где X - количество аминокислотных остатков, оцененных программой выравнивания последовательностей BLAST как идентичные совпадения в этой программе выравнивания A и B, и где Y - общее количество аминокислотных остатков в A или B, в зависимости от того, какая из этих последовательностей короче.
[0063] Используемый здесь термин «пегилированная аминокислота» относится к цепи полиэтиленгликоля (ПЭГ) с одной аминогруппой и одной карбоксильной группой. Как правило, пегилированная аминокислота имеет формулу NH2-(CH2CH2O)n-CO2H. В настоящем изобретении значение n составляет от 1 до 20; предпочтительно в пределах от 2 до 12.
[0064] Используемый здесь термин «конец» в отношении полипептида относится к аминокислотному остатку на N- или C-конце полипептида. В случае полимера, термин «конец» относится к структурной единице полимера (например, полиэтиленгликоль по настоящему изобретению), которая расположена на конце основной цепи полимера. В настоящем описании и формуле изобретения термин «свободный конец» используется для обозначения концевого аминокислотного остатка или составной структурной единицы, которые химически не связаны с какой-либо другой молекулой.
[0065] Используемый здесь термин «лечение» включает превентивное (например, профилактическое), лечебное или паллиативное лечение; и используемый здесь термин «лечить», также включает в себя превентивное (например, профилактическое), лечебное или паллиативное лечение. В частности, используемый здесь термин термин «лечить» относится к применению или введению настоящей линкерной единицы или содержащей ее фармацевтической композиции субъекту, у которого есть медицинское состояние, симптом, связанный с этим медицинским состоянием, заболевание или расстройство, вторичные по отношению к этому медицинскому состоянию, или предрасположенностью к этому медицинскому состоянию, с целью частичного или полного ослабления, улучшения, облегчения, задержки начала, замедления прогрессирования, уменьшения тяжести и/или уменьшения частоты возникновения одного или нескольких симптомов или признаки указанного конкретного заболевания, расстройства и/или состояния. Лечение может быть назначено субъекту, у которого нет признаков заболевания, расстройства и/или состояния, и/или субъекту, у которого проявляются только ранние признаки заболевания, расстройства и/или состояния, с целью уменьшения риск развития патологии, связанной с заболеванием, расстройством и/или состоянием.
[0066] Используемый здесь термин «эффективное количество» относится к количеству настоящей линкерной единицы, достаточному для получения желаемого терапевтического ответа. Эффективное количество агента не требуется для лечения заболевания или состояния, но оно обеспечивает лечение заболевания или состояния, при котором начало заболевания или состояния задерживается, затрудняется или предотвращается, или облегчаются симптомы заболевания или состояния. Эффективное количество может быть разделено на одну, две или более доз в подходящей форме для введения один, два или более раз в течение обозначенного периода времени. Конкретное эффективное или достаточное количество будет варьироваться в зависимости от таких факторов, как конкретное состояние, подлежащее лечению, физическое состояние пациента (например, масса тела, возраст или пол), тип получающего лечение субъекта, продолжительность лечения, характер параллельной терапии (если таковая имеется), а также конкретные применяемые препараты и структура соединений или их производных. Эффективное количество может быть выражено, например, как общая масса активного компонента (например, в граммах, миллиграммах или микрограммах) или как отношение массы активного компонента к массе тела, например, в миллиграммах на килограмм (мг/кг).
[0067] Термины «применение» и «введение» используются здесь взаимозаменяемо для обозначения применения линкерной единицы или фармацевтической композиции настоящего изобретения у субъекта, нуждающегося в лечении ими.
[0068] Используемый здесь термин «последовательный», используемый в связи с остатком K настоящего изобретения, относится к двум остаткам K полипептида, которые непосредствено следуют друг за другом (т.е. без каких-либо других аминокислотных остатков, расположенных между ними). В некоторых примерах настоящего изобретения два последовательных остатка K в центральной основе разделены, по меньшей мере, одним наполнителем настоящего изобретения, например, два последовательных остатка K в центральной основе могут быть разделены GS, GGS или GSG.
[0069] Термины «субъект» и «пациент» используются здесь взаимозаменяемо и предназначены для обозначения животного, включая человека, которое подлежит лечению при помощи линкерной единицы, фармацевтической композиции и/или способа настоящего изобретения. Термин «субъект» или «пациент» предназначен для обозначения как мужского, так и женского пола, если только один пол специально не указан. Соответственно, термин «субъект» или «пациент» включает в себя любое млекопитающее, которому способ лечения настоящего изобретения может принести пользу. Примеры «субъекта» или «пациента» включают в себя без ограничений человека, крысу, мышь, морскую свинку, обезьяну, свинью, козу, корову, лошадь, собаку, кошку, птицу и домашнюю птицу. В приводимом в качестве примера варианте осуществления изобретения пациент является человеком. Термин «млекопитающее» относится ко всем членам класса млекопитающих, включая людей, приматов, домашних и сельскохозяйственных животных, таких как кролик, свинья, овца и крупный рогатый скот; а также животных зоопарков, спортивных животных или животных компаньенов; и грызунов, таких как мышь и крыса. Термин «не являющееся человеком млекопитающее» относится ко всем членам класса млекопитающих, кроме человека.
[0070] Альбумин является основным белком в сыворотке крови, и содержится там в количестве 35-50 г/л. Альбумин может служить транспортером и депо для многих веществ, включая некоторые жирные кислоты, метаболиты, молекулы лекарственных средств и т.д. Каждая молекула альбумина содержит, по меньшей мере, семь карманов (или гидрофобных полостей) и цепь жирной кислоты может плотно прилегать к такому карману. Следовательно, связь с альбумином может изменить фармакокинетические свойства фармацевтического препарата. Некоторые фармацевтические препараты модифицированы жирной кислотой с длинной цепью и, таким образом, обладают способностью связываться с альбумином нековалентным образом и имеют значительно увеличенное время полужизни.
[0071] Коммерческий вариант инсулина (инсулин детемир) содержит жирную кислоту, миристиновую кислоту, конъюгированную с аминогруппой остатка лизина (29-й аминокислотный остаток в B-цепи). Вариант агониста GLP-1 (лираглутид) имеет жирную кислоту (пальмитоильную группу), конъюгированную с остатком глутаминовой кислоты, которая затем конъюгируется с аминогруппой остатка лизина (25-й аминокислотный остаток); другой остаток лизина в 33-й позиции мутирован в аргинин. Модифицированный агонист инсулина и рецептора GLP-1 может связываться с альбумином и, следовательно, обладать фармакокинетикой длительного действия.
[0072] Концепция использования альбумина в качестве депо для фармацевтических препаратов может применяться более разнообразно и широко для многих других фармацевтических препаратов. Для многих существующих лекарственных средств и новых лекарственных средств, находящихся в стадии разработки, возможно создание новых форм для различных клинических показаний, если методы модификации фармацевтических препаратов с аффинностью связывания с альбумином будут улучшены.
[0073] Фермент-заместительная терапия применяется для ряда редких генетических заболеваний. Терапевтические ферменты обычно производятся в виде рекомбинантных белков. Например, агалзидаза β и агалзидаза α для болезни Фабри; ларонидаза для синдрома Херлера-Шейе (также известного как мукополисахаридоз типа 1, MPS-I); идурсульфаза для болезни Хантера (также известной как MPS-II); алглюкозидаза α для болезни Помпе; галсульфаза для синдрома Марото-Лами. Эти ферменты не явлются подготовленными для длительного действия, и их дозы должны вводиться часто. Поскольку пациенты, принимающие эти ферменты, страдают от тяжелых клинических состояний, менее частое введение лекарственного препарата должно помочь этим пациентам и сократить расходы на использование этих ферментов. Таким образом, существуют веские причины для получения новых вариантов этих ферментов с более длительным временем полужизни.
[0074] Настоящее изобретение основано на новой платформе, которая предоставляет гибкие и простые средства для конструирования групп жирных кислот, которые могут быть конъюгированы с терапевтическим лекарственным средством (то есть эффектором), чтобы изменить или, предпочтительно, улучшить фармакокинетические характеристики (например, время полужизни в сыворотке) эффекторного элемента. Настоящая платформа имеет то преимущество, что количество цепей жирной кислоты (и дикарбоновой кислоты; если не указано иное, термин «жирная кислота» также включает в себя дикарбоновую жирную кислоту) можно регулировать, изменяя количество остатков K в основе. Кроме того, расстояние между двумя остатками K можно варьировать, изменяя длину наполнителя между остатками K основы. Понятно, что чем больше цепей жирных кислот переносится данной линкерной единицей, тем выше вероятность того, что линкерная единица может нековалентно ассоциироваться с большим количеством карманов одного HSA или с карманом различных HSA. Кроме того, расстояние между двумя цепями жирных кислот может влиять на кинетику ассоциации между цепью жирных кислот и одинаковыми или разными HSA.
[0075] Часть I Разветвленные линкеры для лечения определенных заболеваний
[0076] I-(i) Пептидная основа для применения в разветвленном линкере
[0077] Белки, которые имеют в крови самые высокие концентрации, включают в себя альбумин (35-50 г/л), иммуноглобулин (Ig)G (7-18 г/л), IgA (0,8-6 г/л), IgM (0,4-4 г/л) и фибриноген (2-4,5 г/л) у взрослых людей. Известно, что эти белки имеют более долгое время полужизни по сравнению с другими белками. Например, время полужизни альбумина составляет 19 дней, а время полужизни IgG (IgG1, IgG2 и IgG4) - более 20 дней. Основываясь на фармакокинетических свойствах, эти белки могут служить гаванью для временного, неустойчивого связывания фармацевтических молекул, тем самым продлевая время их полужизни в сыворотке крови.
[0078] Соответственно, в первом аспекте настоящее изобретение относится к линкерной единице, которая включает в себя, (1) центральную основу, которая содержит 2-5 остатков лизина (K), и (2) 2-5 первых элементов, соответственно связанных с остатками K центральной основы. Настоящая центральная основа характеризуется наличием одной или двух конъюгирующих групп, связанных с ее N- или/и C-концом. В соответствии с вариантами осуществления настоящего изобретения конъюгирующая группа используется для эффективного соединения функционального элемента (например, эффекторного элемента) с центральной основой, тогда как каждый из первых элементов представляет собой жирную кислоту (или дикарбоновую кислоту), обладающую аффинностью связывания с альбумином, или одноцепочечный вариабельный фрагмента (scFv) специфичного по отношению к альбумину IgG, IgA или IgM. Настоящая линкерная единица обеспечивает средство для увеличения времени полужизни функционального элемента и, таким образом, улучшения его терапевтического эффекта.
[0079] В соответствии с некоторыми вариантами осуществления настоящего изобретения каждый из 2-5 первых элементов представляет собой жирную кислоту или дикарбоновую кислоту или их производное. При получении настоящей линкерной единицы первый элемент связан с боковой цепью остатка K посредством образования амидной связи между группой CO2H жирной кислоты (или дикарбоновой кислоты) и аминогруппой остатка K. В некоторых вариантах осуществления изобретения жирная кислота или дикарбоновая кислота модифицирована с помощью химического элемента, и такое производное жирной кислоты или дикарбоновой кислоты связано с аминогруппой боковой цепи остатка К через функциональную группу химического элемента. Например, в соответствии с одним вариантом осуществления настоящего изобретения жирная кислота или дикарбоновая кислота модифицируется глутаматом.
[0080] В соответствии с различными вариантами осуществления настоящего изобретения первый элемент представляет собой производное жирной кислоты, которое получают из октановой кислоты, пеларгоновой кислоты, декановой кислоты, ундекановой кислоты, лауриновой кислоты, тридекановой кислоты, миристиновой кислоты, пентадекановой кислоты, пальмитиновой кислоты, маргариновой кислоты, стеариновой кислоты, нонадекановой кислоты, арахидиновой кислоты, геникозановой кислоты, бегеновой кислоты, трикозановой кислоты, лигноцериновой кислоты, пальмитолеиновой кислоты, олеиновой кислоты, линолевой кислоты, рицинолевой кислоты или вакценовой кислоты, эйкозапентаеновой кислоты (ЭПК) докозагексановой кислоты (ДГК). В соответствии с некоторыми вариантами осуществления настоящего изобретения первый элемент представляет собой производное дикарбоновой жирной кислоты, которое получают из субериновой кислоты, азелаиновой кислоты, себациновой кислоты, ундекандиовой кислоты, додекандиовой кислоты, брассиловой кислоты, тетрадекандиовой кислоты, пентадекандиовой кислоты, тапсиевой кислоты, гептадекандиовой кислоты или октадекандиовой кислоты. В некоторых вариантах осуществления настоящий первый элемент получают из миристиновой кислоты или пальмитиновой кислоты. В других вариантах осуществления настоящий первый элемент получают из тетрадекандиовой кислоты или тапиновой кислоты.
[0081] В соответствии с вариантами осуществления настоящего изобретения центральная основа представляет собой полипептид, который имеет 5-120 аминокислотных остатков в длину и содержит от 2 до 5 остатков K, где каждый остаток K и его следующий остаток K (т.е. два последовательных остатка К) непосредственно следуют друг за другом или разделены наполнителем.
[0082] Понятно, что количество первых элементов, связанных с центральной основой, в основном определяется количеством остатков К, содержащихся в центральной основе. Поскольку в настоящей центральной основе содержится, по меньшей мере, два остатка K, настоящая линкерная единица может содержать несколько первых элементов.
[0083] В зависимости от остатков К, содержащихся в центральной основе, аминокислотные остатки наполнителя соответственно выбраны из группы, состоящей из остатков глицина (G), серина (S), аргинина (R), гистидина (H), треонина (T), аспарагина (N), глутамина (Q), пролина (P), аланина (A), валина (V), изолейцина (I), лейцина (L), метионина (M), фенилаланина (F), тирозина (Y) и триптофана (W).
[0084] В соответствии с некоторыми вариантами осуществления настоящего изобретения аминокислотные остатки наполнителей независимо выбраны из группы, состоящей из остатков G, S, R и H. В альтернативном примере аминокислотные остатки наполнителя представляют собой соответственно остатки R или H.
[0085] Наполнитель, помещенный между остатками K, может представлять собой вариации указанных аминокислотных остатков в произвольных последовательностях и/или длинах. Более длинные наполнители могут быть использованы для полипептида с меньшим количеством остатков K, и более короткие наполнители для полипептида с большим количеством остатков K. Гидрофильные аминокислотные остатки, такие как N, Q, R и H, могут быть вставлены в наполнители вместе с G и S. В качестве альтернатив для наполнителей, состоящих из остатков G и S, наполнители также могут быть получены из гибких растворимых петель в общих сывороточных белках человека, таких как альбумин и иммуноглобулины.
[0086] Альтернативно, наполнитель может представлять собой пегилированную аминокислоту, имеющую от 2 до 12 повторов мономерных единиц этиленгликоля (EG).
[0087] Обычно наполнители в центральной основе могут быть одинаковыми или разными. В частности, каждый из наполнителей может содержать одинаковые или различные аминокислотные остатки/единицы EG. Альтернативно, некоторые из наполнителей центральной основы могут представлять собой пегилированную аминокислоту, имеющую 3 повтора единиц EG, тогда как другие наполнители центральной основы могут представлять собой пегилированную аминокислоту, имеющую 5-7 повторов единиц EG.
[0088] Кроме наполнителей, настоящая центральная основа дополнительно содержит один или два необязательных концевых спейсера, имеющих связанную с ними конъюгирующую группу. Концевой спейсер включает в себя (i) два или более аминокислотных остатка, которые независимо выбраны из аминокислотных остатков, отличных от остатка К, или (ii) пегилированную аминокислоту, имеющую от 2 до 12 повторов единицы EG. В соответствии с вариантами осуществления настоящего изобретения конъюгирующая группа связана с альфа-NH2-группой концевого спейсера (то есть альфа-NH2-группой аминокислотного остатка/пегилированной аминокислоты, расположенной на N-конце концевого спейсера) или связана с группой CO2H концевого спейсера (то есть группой CO2H аминокислотного остатка/пегилированной аминокислоты, расположенной на С-конце концевого спейсера).
[0089] В соответствии с одним вариантом осуществления настоящего изобретения центральная основа содержит один концевой спейсер, который расположена перед N-концевым остатком K; в этом варианте осуществления изобретения конъюгирующая группа связана с альфа-NH2-группой концевого спейсера. В соответствии с другим вариантом осуществления настоящего изобретения центральная основа содержит один концевой спейсер, который расположен после C-концевого остатка K; в этом варианте осуществления изобретения конъюгирующая группа связана с группой СО2Н концевого спейсера. В соответствии с еще одним вариантом осуществления настоящего изобретения центральная основа содержит два концевых спейсера, в которых один из концевых спейсеров расположен перед N-концевым остатком K и имеет первую конъюгирующую группу, связанную с его альфа-NH2-группой; а другой из концевых спейсеров расположен после C-концевого остатка K и имеет вторую конъюгирующую группу, связанную с его группой СО2Н.
[0090] Конъюгирующая группа выбрана из группы, состоящей из азидной, пиколилазидной, алкиновой, тетразиновой, циклооктеновой, циклооктиновой, малеимидной, винилсульфоновой, моносульфононовой, метилсульфонилбензотиазольной, йодо и йодацетамидной группы. В соответствии с предпочтительным примером настоящего изобретения, конъюгирующая группа представляет собой азидную, пиколилазидную, алкиновую, тетразиновую, циклооктеновую или циклооктиновую группу. Понятно, что когда центральная основа имеет две связанные с ней конъюгирующие группы, эти две конъюгирующие группы могут быть одинаковыми или разными. Предпочтительно две конъюгирующие группы являются разными; например, одна из конъюгирующих групп может быть азидной, алкиновой или циклооктиновой группой, а другая из конъюгирующих групп может быть тетразиновой или циклооктеновой группой.
[0091] Как правило, циклооктеновая группа может представлять собой норборнен или группу TCO; а циклооктиновая группа может представлять собой группу DBCO/DIBO, DIFO, BCN или DIBAC. Что касается тетразиновой группы, то она может представлять собой 1,2,3,4-тетразин, 1,2,3,5-тетразин или 1,2,4,5-тетразин или их производные. В соответствии с одним вариантом осуществления настоящего изобретения тетразиновая группа представляет собой 6-метил-тетразин.
[0092] На Фиг. 1А-1Е, каждая изображенная на них центральная основа 10а, 10b, 10с, 10d и 10е имеет связанную с ней конъюгирующую группу,. На Фиг. 1A-1D тетразиновая группа, TCO-группа, азидная группа и алкиновая группа соответственно связаны с альфа-NH2-группами концевых спейсеров центральных основ 10a, 10b, 10c и 10d. На Фиг. 1Е представлен альтернативный пример, в котором ацетильная группа, служащая в качестве защитной группы, связана с альфа-NH2-группой N-концевого спейсера пептидной основы 10е, тогда как группа DBCO, служащая в качестве конъюгирующей группы, связана с группой CO2H С-концевого аминокислотного остатка центральной основы 10е.
[0093] В некоторых вариантах осуществления настоящего изобретения центральная основа содержит две конъюгирующие группы. Фиг. 1F иллюстрирует такой пример, где тетразиновая группа и группа DBCO соответственно связаны с альфа-NH2-группой N-концевого спейсера и группой CO2H C-концевого спейсера пептидной основы 10f. На Фиг. 1G показан другой пример, в котором группа TCO и группа DBCO соответственно связаны с альфа-NH2-группой N-концевого спейсера и группой CO2H C-концевого спейсера пептидной основы 10g. В альтернативном примере альфа-NH2-группа N-концевого спейсера и группа CO2H C-концевого спейсера пептидной основы 10h соответственно связаны с алкиновой группой и группой DBCO (Фиг. 1H).
[0094] На схемах 1-3 приведены примеры получения центральной основы, имеющей одну или две указанные конъюгирующие группы, связанные с ней.
[0095] Синтез полипептида с использованием пегилированных аминокислот включает меньше этапов, чем синтез с обычными аминокислотами, такими как остатки G и S. Кроме того, могут быть использованы пегилированные аминокислоты с различной длиной (то есть числом повторяющихся звеньев этиленгликоля), обеспечивающие гибкость в отношении растворимости и расстояния между соседними аминогруппами остатков K. В дополнение к пегилированным аминокислотам центральные основы также могут быть сконструированы так, чтобы они содержали искусственные аминокислоты, такие как аминокислоты в D-форме, гомоаминокислоты, N-метиламинокислоты и т.д. Предпочтительно, пегилированные аминокислоты с различной длиной полиэтиленгликоля (ПЭГ) используются для создания центральной основы, поскольку фрагменты ПЭГ, содержащиеся в молекулах аминокислот, обеспечивают конформационную гибкость и достаточное расстояние между конъюгирующими группами, повышают растворимость в воде и, как правило, обладают низкой иммуногенностью. Синтез центральной основы, содержащей пегилированные аминокислоты, аналогичен процедурам синтеза обычных полипептидов.
«Схема 1 Получение центральной основы, имеющей тетразиновую или TCO-группу, связанную с её N-концом»
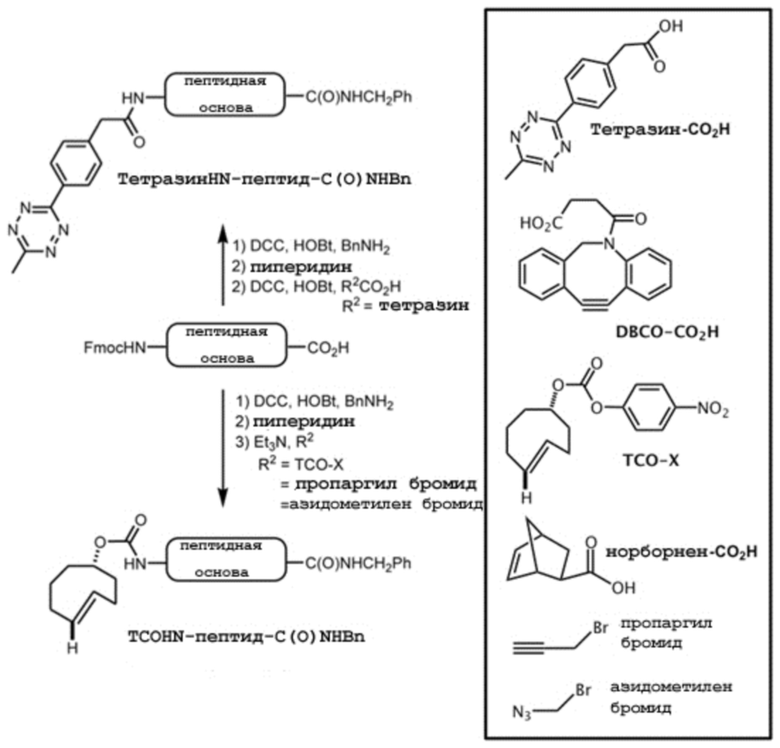
«Схема 2 Получение центральной основы, имеющей группу DBCO, связанную с её С-концом»
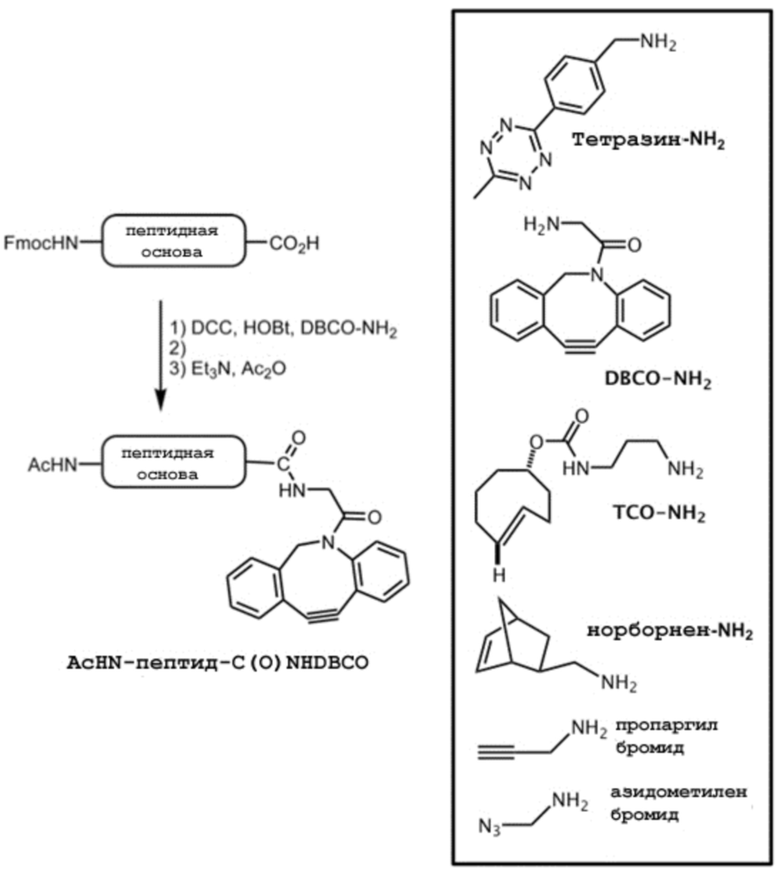
[0096] В целях стабильности, в случае, когда N-конец центральной основы не связан с конъюгирующей группой, он предпочтительно связан с ацетильной группой.
[0097] В настоящем изобретении реакция между альфа-NH2-группой центральной основы и конъюгирующей группой или между группой CO2H центральной основы и конъюгирующей группой на всех чертежах обозначена символом «×».
«Схема 3 Получение центральной основы, имеющей две конъюгирующие группы, соответственно связанные с ее N- и C-концами»
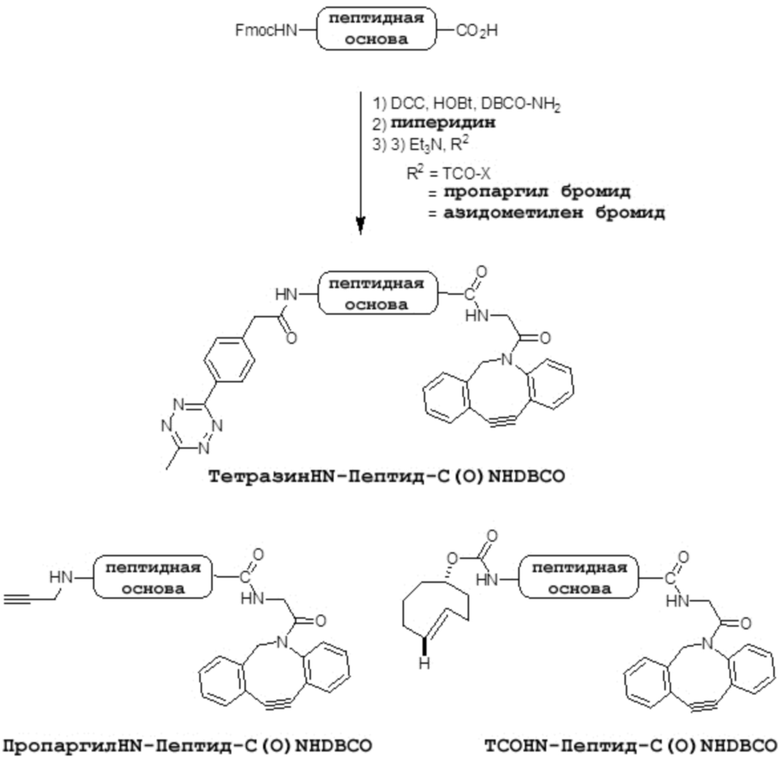
[0098] На фиг. 2А линкерная единица 20А включает в себя центральную основу 20а, содержащую три остатка K, соответственно разделенных наполнителями (обозначены точками на всех чертежах). Концевой спейсер (обозначенный символом «~» на всех чертежах) расположен перед первым остатком K и имеет тетразиновую группу 25, связанную с его альфа-NH2-группой. В этом примере три первых элемента 21a-21c соответственно связаны с остатками K.
[0099] На фиг. 2В показана линкерная единица, содержащая две конъюгирующие группы, в соответствии с другим вариантом осуществления настоящего изобретения. Центральная основа 20b содержит четыре остатка K. Первый и второй концевые спейсеры соответственно расположены на N-конце и С-конце центральной основы, в которой группа 28 DBCO связана с альфа-NH2-группой первого концевого спейсера, и группа 26 TCO связана с группой CO2H второго концевого спейсера. В этом примере остатки K соответственно связаны с первыми элементами 21a-21d.
[0100] Альтернативно, первый элемент может представлять собой scFv специфичных по отношению к альбумину IgG, IgA или IgM. В этом случае первый элемент связан с центральной основой через связывающий фрагмент. В частности, цепь ПЭГ, имеющая NH2-реактивную группу (например, N-гидроксисукцинимидильную (NHS) группу) на одном конце и функциональную группу на другом конце, может быть связана с любым остатком K центральной основы путем образования амидной связи между NH2-реактивной группой цепи ПЭГ и аминогруппой остатка K. В настоящем изобретении цепь ПЭГ, связанная с остатком K, называется связывающим фрагментом, который имеет функциональную группу на своем свободном конце. Обычно функциональная группа выбрана из группы, состоящей из гидроксила, трет-бутилдиметилсилила (TBDMS), NHS, малеимида, винилсульфонона, моносульфонона, метилсульфонилбензотиазола, йода, йодацетамида, азида, пиколилазида, алкина, циклооктина, тетразина и циклооктена. В зависимости от желаемых целей малеимидная группа может представлять собой замещенный малеимид, например, арилмалеимид, 3-броммалеимид и 3,4-диброммалеимид. Предпочтительно, когда конъюгирующая группа представляет собой азидную, пиколилазидную, алкиновую или циклооктиновую группу, функциональная группа не является какой-либо из азидной, пиколилазидной, алкиновой или циклооктиновой группы. Альтернативно, когда конъюгирующая группа центрального ядра представляет собой тетразиновую или циклооктеновую группу, тогда функциональная группа не является ни тетразиновой группой, ни циклооктеновой группой.
[0101] Соответственно, первый элемент, имеющий соответствующую функциональную группу, может быть связан со свободным концом связывающего фрагмента посредством любой из следующих химических реакций,
(1) образование амидной связи между ними: в этом случае связывающий фрагмент имеет группу NHS на свободном конце, а первый элемент имеет аминогруппу;
(2) образование сложноэфирной связи между ними: в этом случае связывающий фрагмент имеет гидроксильную или TBDMS-группу на свободном конце, а первый элемент имеет гидроксил-реактивную группу (например, тозил-O-группу);
(3) реакция тиол-малеимид (или винилсульфон): в этом случае связывающий фрагмент имеет малеимидную, винилсульфоновую, моносульфоновую или метилсульфонилбензотиазольную группу на свободном конце, а первый элемент имеет тиоловую группу;
(4) реакция SN2: в этом случае связывающий фрагмент имеет йодную или йодоацетамидную группу на свободном конце, а первый элемент имеет тиольную группу;
(5) катализируемая медью (I) реакция алкил-азидного циклоприсоединения (реакция CuAAC или кратко реакция клик-химии): один из свободных концов связывающего фрагмента и первый элемент имеют азидную или пиколилазидную группу в то время как другой имеет алкиновую группу; реакция CuAAC показана на Схемах 4 и 5;
(6) реакция Дильса-Алдера с обращенными электронными требованиями (iEDDA): один из свободных концов связывающего фрагмента и первый элемент имеют тетразиновую группу, а другой имеет TCO или норборненовую группу; реакция iEDDA показана на Схемах 6 и 7; или
(7) реакция клик-химии активированных азида и алкина (SPAAC): один из свободных концов связывающего фрагмента и первый элемент имеют азидную группу, тогда как другой имеет циклооктиновую группу; реакция SPAAC показана на Схеме 8.
«Схема 4 Реакция CuAAC между азидной и алкиновой группами»
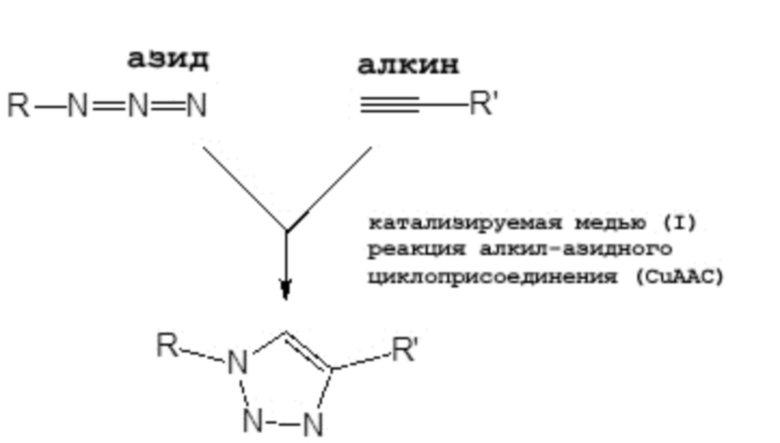
«Схема 5 Реакция CuAAC между пиколилазидной и алкинильной группами»
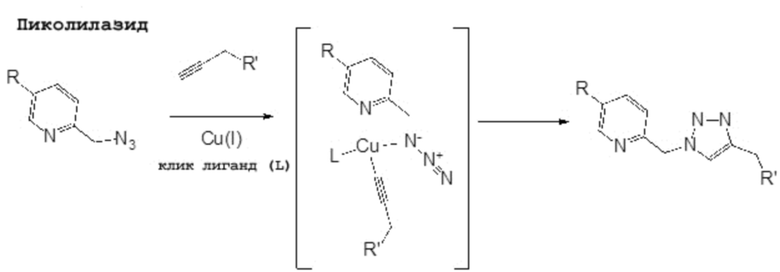
«Схема 6 Реакция iEDDA между TCO и тетразиновыми группами»
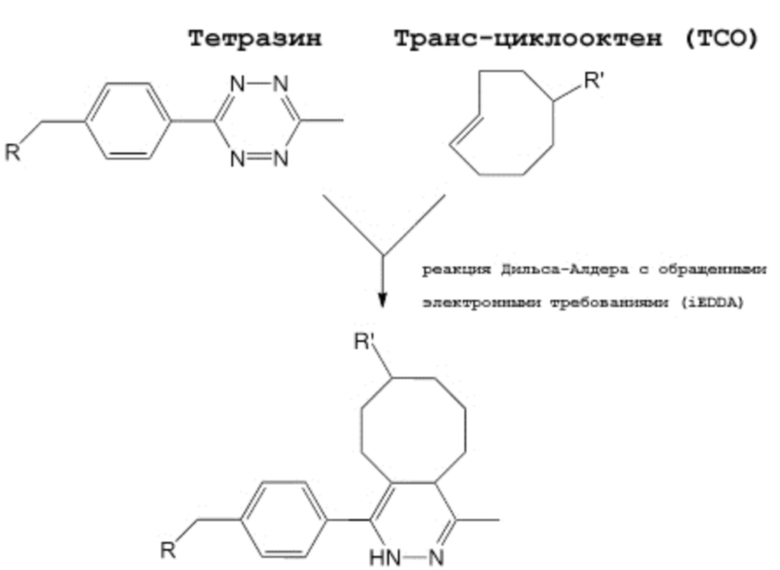
«Схема 7 Реакция iEDDA между норборненовой и тетразиновой группами»

«Схема 8 Реакция SPAAC между азидом и группой DBCO»
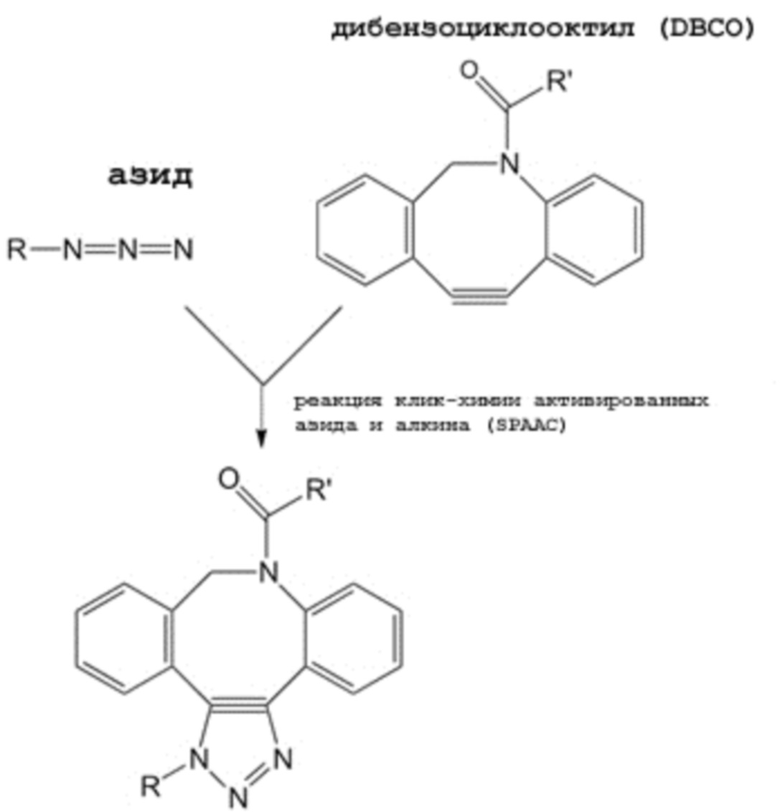
[0102] На Фиг. 2С линкерная единица 20С имеет аналогичную структуру с линкерной единицей 20А, за исключением того, что три первых элемента (23а, 23b и 23с) соответственно связаны с остатками K через связь из трех связывающих фрагментов (22а, 22b и 22с).
[0103] В соответствии с некоторыми вариантами осуществления настоящего изобретения центральная основа содержит две конъюгирующие группы, соответственно связанные с альфа-NH2-группой N-концевого спейсера и группой CO2H C-концевого спейсера центральной основы. В этих вариантах осуществления изобретения одна из конъюгирующих групп представляет собой азидную, пиколилазидную, алкиновую или циклооктиновую группу, а другая из конъюгирующих групп представляет собой тетразиновую или циклооктеновую группу; предпочтительно функциональной группой связывающего фрагмента является гидроксильная, TBDMS, NHS, малеимидная, винилсульфоновая, моносульфоновая, метилсульфонилбензотиазольная, йодо или йодоацетамидная группа.
[0104] Связывающий фрагмент предпочтительно представляет собой цепь ПЭГ, имеющую 2-20 повторов единиц EG. Альтернативно, связывающий фрагмент может представлять собой цепь ПЭГ, имеющую 2-20 повторов единиц EG с дисульфидной связью на конце, которая не связана со связывающим фрагментом. Понятно, что применимые связывающие фрагменты не ограничиваются цепями ПЭГ. могут быть использованы Пептиды, содержащие гидрофильные остатки глицина, серина и других аминокислот, а также полисахариды и другие биосовместимые линейные полимеры, которые модифицированы, чтобы содержать функциональные группы (например, NHS, малеимидную, азидную, алкиновую, тетразиновую или напряженную алкиновую группу), также могут быть использованы.
[0105] Понятно, что определенные признаки, обсужденные выше в отношении линкерных единиц 20А-20С или любых других следующих линкерных единиц, являются общими для других линкерных единиц, раскрытых в данном заявке, и, следовательно, некоторые или все из этих признаков также применимы в следующих примерах, если это не противоречит контексту конкретного варианта осуществления изобретения. Однако, для краткости, эти общие признаки не могут быть явно повторены ниже.
[0106] Настоящая линкерная единица может дополнительно содержать один или два функциональных элемента, связанных с конъюгирующей группой (например, азидной, пиколилазидной, алкиновой, тетразиновой, циклооктеновой или циклооктиновой группой) центральной основы. В частности, функциональный элемент может необязательно быть конъюгирован с короткой цепью ПЭГ (предпочтительно имеющей 2-12 повторов единиц EG) и затем связан с конъюгирующей группой.
[0107] В соответствии с некоторыми вариантами осуществления настоящего изобретения центральная основа содержит одну конъюгирующую группу (то есть азидную, пиколилазидную, алкиновую, тетразиновую, циклооктеновую или циклооктиновую группу); и, соответственно, функциональный элемент (то есть второй элемент), имеющий азид-реактивную группу (например, алкин или группу DBCO), алкин-реактивную группу (например, азид или пиколилазидную группу), тетразин-реактивную группу (например, TCO или норборненовую группа), циклооктен-реактивную группу (например, азидную группу) или циклооктин-реактивную группу (например, тетразиновую группу), может быть связан с конъюгирующей группой центральной основы при помощи реакции CuAAC, реакции iEDDA или реакции SPAAC.
[0108] На Фиг. 3А линкерная единица 30А имеет аналогичную структуру с линкерной единицей 20А, за исключением того, что второй элемент 33 связан с тетразиновой группой, связанной с концевым спейсером. Закрашенный кружок 27 на Фиг. 3А, представляет химическую связь, возникшую в результате реакции iEDDA, происходящей между тетразиновой группой и вторым элементом.
[0109] В соответствии с другими вариантами осуществления настоящего изобретения центральная основа содержит две конъюгирующие группы. Как упомянуто выше, когда первая конъюгирующая группа представляет собой азидную, пиколилазидную, алкиновую или циклооктиновую группу, тогда вторая конъюгирующая группа предпочтительно представляет собой тетразиновую или циклооктеновую группу. Соответственно, два функциональных элемента (то есть второй и третий элементы) могут быть соответственно связаны с центральной основой при помощи реакций SPAAC и iEDDA или при помощи реакций CuAAC и iEDDA. Например, второй элемент, имеющий циклооктин-реактивную группу (например, азидную группу), может быть связан с первой конъюгирующей группой при помощи реакции SPAAC; в то время как третий элемент, имеющий алкино-реактивную группу (например, азидную или пиколилазидную группу), тетразин-реактивную группу (например, TCO или норборненовую группу) или циклооктен-реактивную группу (например, тетразиновую группу), может быть связан со второй конъюгирующей группой при помощи реакции CuAAC или реакции iEDDA. Альтернативно, второй элемент, имеющий тетразин-реактивную группу (например, TCO или норборненовую группу) или циклооктен-реактивную группу (например, тетразиновую группу), может быть связан с первой конъюгирующей группой при помощи реакции iEDDA; и третий элемент, имеющий азид-реактивную группу (например, алкин или группу DBCO), алкин-реактивную (например, азидную или пиколилазидную группу) или циклооктин-реактивную группу (например, азидную группу) может быть связаны со второй конъюгирующей группой при помощи реакции CuAAC или SPAAC.
[0110] На Фиг. 3В представлен Пример линкерной единицы 30В, содержащей две конъюгирующие группы, соответственно связанные со вторым и третьим элементами. Линкерная единица 30B имеет аналогичную структуру с линкерной единицей 20B, за исключением того, что второй элемент 33 связан с группой DBCO, а третий элемент 35 связан с группой TCO. Закрашенный треугольник 29 на Фиг. 3В, обозначает химическую связь, возникшую в результате реакции SPAAC, произошедшей между группой DBCO и вторым элементом; а закрашенный кружок 27 на Фиг. 3В, обозначает химическую связь, возникшую в результате реакции iEDDA, происходящей между группой TCO и третьим элементом.
[0111] На Фиг. 3С представлен альтернативный Пример настоящего линкерной единицы. Линкерная единица 30С содержит два функциональных элемента (то есть второй и третий элемент), где второй элемент 33 связан с тетразиновой группой, связанной с N-концевым спейсером центральной основы 20а, а третий элемент 35 связан с азидной группой, связанной с С-концевым спейсером центральной основы 20а. Закрашенный кружок 27 на Фиг. 3C, обозначает химическую связь, возникшую в результате реакции iEDDA, происходящей между тетразиновой группой и вторым элементом; а ромб 30 на Фиг. 3С обозначает химическую связь, возникшую в результате реакции CuAAC, произошедшей между азидной группой и третьим элементом.
[0112] В зависимости от желаемых целей, функциональный элемент, связанный с конъюгирующей группой центральной основы, может представлять собой любую молекулу, которая обеспечивает терапевтическое преимущество при лечении заболевания или состояния. Типичные функциональные элементы включают в себя без ограничений инсулин, инсулиноподобный фактор роста, агонист глюкагоноподобного пептида-1, соматостатина и аналоги соматостатина, кальцитонин, гормон роста, эритропоэтин, гонадотропин-рилизинг-фактор, гранулоцитарный колониестимулирующий фактор, аденозиндеаминазу, аспарагиназу, интерферон-α, интерферон-β, рецептор ФНО-α, рецептор IL-1, рецептор EGF, агалсидазу β, агалсидазу α, ларонидазу, идурсульфазу, альглюкозидазу α и галсульфазу, или их производное или вариант.
[0113] I-(ii) Применение разветвленного линкера
[0114] Настоящее изобретение также относится к способу лечения различных заболеваний с применением подходящей линкерной единица. Как правило, способ включает в себя этап введения субъекту, нуждающемуся в таком лечении, эффективного количества линкерной единицы в соответствии с вариантами осуществления настоящего изобретения.
[0115] По сравнению с ранее известными терапевтическими конструкциями, настоящая линкерная единица, описанная в части I, имеет преимущества в трех аспектах:
(1) Количество первых элементов (то есть жирной кислоты или scFv специфичного по отношению к альбумину IgG, IgA или IgM) можно регулировать в соответствии с потребностями и/или вариантами применений. Настоящая линкерная единица может содержать один функциональный элемент (то есть второй элемент) или два функциональных элемента (то есть второй и третий элементы) в соответствии с требованиями применения (например, заболевание, которое лечат, способ введения настоящей линкерной единицы и авидность и/или аффинность связывания антитела, переносимого настоящей линкерной единицей). Например, когда настоящая линкерная единица непосредственно доставляется в ткань/орган (например, для лечения глаз), второго элемента, действующего в качестве эффекторного элемента, может быть достаточно, что устраняет необходимость в третьем элементе, действующем в качестве нацеливающего элемент. Однако когда настоящая линкерная единица доставляется периферически (например, перорально, энтерально, назально, местно, трансмукозально, путем внутримышечной, внутривенной или внутрибрюшинной инъекции), может потребоваться, чтобы настоящая линкерная единица одновременно содержала нацеливающий элемент, который специфично направляет настоящую линкерную единицу к области поражения, и эффекторный элемент, который оказывает терапевтическое воздействие на область поражения. В целях повышения эффективности нацеливания или лечения или повышения стабильности настоящей линкерной единицы в настоящую линкерную единицу может быть дополнительно включен третий элемент (например, второй нацеливающий элемент, второй эффекторный элемент или цепь ПЭГ).
(2) Первый элемент представлен в виде группы. Как описано выше, количество первых элементов (то есть жирных кислот) может варьироваться в зависимости от количества остатков K, содержащихся в центральной основе. Если число остатков K в центральной основе находится в диапазоне от 2 до 5, то, в каждой линкерной единице могут содержаться, по меньшей мере, два первых элемента, что эффективно увеличивает время полужизни и терапевтический эффект функциональных элементов (то есть второго и/или третьего элемента).
(3) Линкерная единица может быть эффективно связана с функциональным элементом или другой молекулярной конструкцией (см. Часть II ниже) через связанную с ней конъюгирующую группу. Настоящее центральная основа может быть коммерчески синтезирована. В другом случае, как показано на Схемах 4-8, настоящая центральная основа может быть легко получена из синтетического полипептида, в котором N-концевой 9-флуоренилметоксикарбонил (Fmoc), служащий в качестве защитной группы для защиты α-аминогруппы, замещен конъюгирующей группой (т.е. азидной, пиколилазидной, алкиновой, тетразиновой, циклооктеновой или циклооктиновой группой). Дополнительно или альтернативно, конъюгирующая группа может быть связана с полипептидом посредством взаимодействия с группой CO2H полипептида. Полученная таким образом центральная основа содержит одну или две конъюгирующие группы, которые служат в качестве соединителя для соединения функциональных элементов (например, настоящего второго и/или третьего элемента) и центральной основы без необходимости дополнительных этапов обработки.
[0116] Часть II. Соединенные линкером молекулярные конструкции для лечения конкретных заболеваний
[0117] В другом аспекте настоящее изобретение относится к молекулярной конструкции, содержащей, по меньшей мере, две линкерные единицы, где одна линкерная единица несет несколько жирных кислот (например, группу жирных кислот), тогда как другая линкерная единица несет несколько эффекторных элементов (например, группу лекарственных средств). В настоящем изобретении молекулярные конструкции, содержащие две или более линкерные единицы, упоминаются как соединенные линкером молекулярные конструкции. В соответствии с различными вариантами осуществления настоящего изобретения соединенная линкером молекулярная конструкция содержит две линкерные единицы, как описано в Части I.
[0118] II-(i) Структура соединенной линкером молекулярной конструкции
[0119] В соответствии с некоторыми вариантами осуществления настоящего изобретения молекулярная конструкция содержит две линкерные единицы, и эти линкерные единицы связаны друг с другом при помощи реакции CuAAC, реакции SPAAC или реакции iEDDA. В вариантах осуществления изобретения первая линкерная единица содержит (1) центральную основу, (2) несколько первых элементов, соответственно связанных с остатками K центральной основы, и (3) конъюгирующую группу, связанную с N- или C-концом центральной основы, которая выбрана из группы, состоящей из азидной, пиколилазидной, алкиновой, тетразиновой, циклооктеновой и циклооктиновой групп. Аналогично, вторая линкерная единица содержит (1) центральную основу, (2) несколько вторых элементов, соответственно связанных с остатками K центральной основы, и (3) конъюгирующую группу, связанную с N- или C-концом центральной основы, которая выбрана из группы, состоящей из азидной, пиколилазидной, алкиновой, тетразиновой, циклооктеновой и циклооктиновой групп. Первая и вторая линкерные единицы могут быть связаны друг с другом при помощи реакции CuAAC, реакции SPAAC или реакции iEDDA между конъюгирующими группами.
[0120] В соответствии с некоторыми вариантами осуществления изобретения каждый из первых элементов представляет собой жирную кислоту или scFv специфичного по отношению к альбумину IgG, IgA или IgM; и каждый из вторых элементов представляет собой функциональный элемент, который обеспечивает терапевтическую пользу при лечении заболевания или патологического состояния; например, инсулин, инсулиноподобный фактор роста, агонист глюкагоноподобного пептида-1, соматостатин и аналоги соматостатина, кальцитонин, гормон роста, эритропоэтин, гонадотропин-рилизинг-фактор, гранулоцитарный колониестимулирующий фактор, аденозиндеаминаза, аспарагиназа, интерферон-α, интерферон-β, рецептор ФНО-α, рецептор IL-1, рецептор EGF, агалсидаза β, агалсидаза α, ларонидаза, идурсульфаза, альглюкозидаза α и галсульфаза, или их производное или вариант. Для пептидов или небольших белков, которые имеют только один остаток лизина, который не является существенным для биологической активности пептидов или белков, ε-аминогруппа остатка лизина обеспечивает функциональную группу для реакции с гетеробифункциональным сшивающим агентом, имеющим амино-реактивную группу, такую как N-гидроксисукцинимид (NHS), на одном конце, и функциональную группа для реакции клик-химии на другом конце. Поскольку все белки имеют несколько остатков лизина и их остатки цистеина находятся в парах, образующих дисульфидные связи, остатки лизина и цистеина не являются идеальными в качестве сайтов для присоединения функциональной группы для реакций клик-химии. Для такого белка остаток, доступный для растворителя на поверхности белка, который не требуется для биологической активности белка, может быть мутирован в остаток цистеина. Таким образом, этот остаток цистеина обеспечивает сульфгидрильную группу, которая может взаимодействовать с гетеробифункциональным сшивающим агентом с SH-реактивной функциональной группой, такой как малеимидная группа, на одном конце, и функциональной группой для реакции клик-химии на другом конце.
[0121] Альтернативно, первая линкерная единица содержит две конъюгирующие группы, соответственно связанные с ее N- и C-концами, где одна из конъюгирующих групп связана с функциональным элементом, а другая из конъюгирующих групп представляет собой азидную, пиколилазидную, алкиновую, тетразиновую, циклооктеновую или циклооктиновую группу.
[0122] В другом альтернативном варианте, как первая, так и вторая линкерная единица содержат две конъюгирующие группы, соответственно связанные с их N- и C-концами, где одна из конъюгирующих групп связана с функциональным элементом, а другая из конъюгирующих групп представляет собой азидную, пиколилазидную, алкиновую, тетразиновую, циклооктеновую или циклооктиновую группу. В этом случае функциональные элементы первой и второй линкерной единицы могут быть одинаковыми или разными.
[0123] II-(iii) Применение соединенной линкером молекулярной конструкции
[0124] Настоящее изобретение также относится к способу лечения различных заболеваний с использованием подходящей соединенной линкером молекулярной конструкции. Как правило, способ включает в себя этап введения субъекту, нуждающемуся в таком лечении, эффективного количества соединенной линкером молекулярной конструкции в соответствии с вариантами осуществления настоящего изобретения.
Экспериментальные примеры
[0125] Пример 1: Синтез азидсодержащего агониста глюкагоноподобного пептида-1 (GLP-1)
[0126] Активный GLP-1 человека представляет собой пептидный гормон, полученный в результате процессинга пептида проглюкагона (1-37). Амид GLP-1 (7-36) и GLP-1 (7-37) человека представляют собой две усеченные и эквипотентные биологически активные формы.
[0127] В этом примере получали азидсодержащий агонист GLP-1, у которого азидная группа была связана с молекулой агониста GLP-1 (SEQ ID NO:1) через соединение с остатком глутамата. В частности, γ-карбоксильная группа остатка глутамата была связана с ε-аминогруппой остатка лизина молекулы агониста GLP-1 (SEQ ID NO: 1), и α-аминогруппа остатка глутамата была модифицирована азидоацетильной группой (показано ниже).

[0128] Авторы настоящего изобретения осуществили дизайн молекулы азидсодержащего агониста GLP-1, и синтез этого вещества был передан на аутсорсинг в фирму Shanghai WuXi AppTech Co., Ltd. (Шанхай, Китай). В процедуре применяли ступенчатый процесс Fmoc SPPS (твердофазный пептидный синтез) с использованием химических реакций сочетания O-бензотриазол-N,N,N',N'-тетраметилуроний-гексафторфосфата (HBTU)/N,N-диизопропилэтиламина (DIEA)/N,N-диметилформамида (ДМФА), где HBTU служил в качестве активирующего реагента in situ для аминокислот, защищенных Fmoc, и DIEA использовался в качестве органического основания во время сочетания. В синтезе использовали Nα-Fmoc, аминокислоты с боковой цепью и смола 2-хлортритилхлорида (смола CTC). Использовали следующие стратегии защиты боковой цепи: Arg (Pbf), Trp (Boc), Thr (OtBu), Lys (N-Dde), Tyr (OtBu), Glu (OtBu), Gln (Trt), Ser (OtBu) ) His (Trt). Для каждого цикла сочетания, кроме первого цикла, использовали 3 ммоль Nα-Fmoc-аминокислоты, 6 ммоль DIEA и 2,85 ммоль-эквивалента HBTU. Защитную группу Fmoc на α-амине удаляли 20% раствором пиперидина в ДМФА (трехкратный объём пептидной смолы).
[0129] На этапе (i) пептидный синтез начинали путем ковалентного связывания первой аминокислоты со смолой: аминокислоту Fmoc-Gly-OH (1,0 ммоль, 297,5 мг) и смолу CTC (1,0 ммоль, замещение = 1,0 ммоль/г, 1,0 г) растворяли в дихлорметане (ДХМ), а затем добавляли DIEA (4,0 ммоль) и полученную смесь барботировали газообразным азотом. Затем в пептидную смолу, защищенную Fmoc, в качестве покрывающего реагента добавляли метанол (МеОН, 1,0 мл) и перемешивали в течение 0,5 часа для ковалентного связывания с непрореагировавшими карбокатионами на смоле СТС.
[0130] На этапе (ii) содержащий метанол защищенный раствор сливали и затем 3 раза промывали ДМФА. На этапе (iii) после промывки смолы защитную группу Fmoc на смоле СТС удаляли путем добавления 20% пиперидина в растворе ДМФА в течение 30 минут. На этапе (iv) полученный раствор сливали и промывали ДМФА 5 раз. На этапе (v) ручное связывание 2-й аминокислоты осуществляли путем добавления Fmoc-Arg(Pbf)-OH (3 экв.) и активирующего агента (HBTU) к смоле при барботировании газообразного азота в течение примерно 1 часа. Затем этапы (ii) - (v) повторяли каждый раз с другой аминокислотой в соответствии с пептидной последовательностью. Для каждого цикла этапов сочетания реакцию сочетания контролировали с помощью нингидриновой реакции.
[0131] Для отщепления пептида с защищенной боковой цепью, от смолы СТС, готовили 40,0 мл буфера для расщепления (5% TIS / 5% H2O / 90% TFA) и добавляли в колбу, содержащую смолу, при перемешивании в течение 2 часов. Неочищенный пептид осаждали в холодном трет-бутилметиловом эфире и центрифугировали в течение 3 минут при 6000 об/мин. Неочищенный пептид два раза промывали трет-бутилметиловым эфиром (всего 400,0 мл) и сушили в вакууме в течение 2 часов.
[0132] Азидсодержащий агонист GLP-1 очищали ВЭЖХ с обращенной фазой на препаративной НТ-колонке SB-фенил Agilent (250 мм х 30 мм; 7 мкм), используя в качестве подвижной фазы ацетонитрил и 0,075% трифторуксусную кислоту, линейный градиент от 0 до 60% ацетонитрила в течение 60 минут при скорости потока 20 мл/мин и температуре колонки 25°С.
[0133] Очищенный образец азидсодержащего агониста GLP-1 анализировали методом ВЭЖХ с обращенной фазой на колонке Supelco C18 (250 мм х 4,6 мм; 5 мкм), используя в качестве подвижной фазы ацетонитрил и 0,1% трифторуксусной кислоты, линейный градиент от 0% до 100% ацетонитрила в течение 30 минут при скорости потока 1,0 мл/мин и температуре колонки 25°C. На Фиг. 4А показан профиль аналитической ВЭЖХ с обращенной фазой азидсодержащего агониста GLP-1 с пиком азидсодержащего агониста GLP-1 при ОП 254 нм со временем удерживания 23,153 минуты.
[0134] Идентификацию образцов проводили с помощью масс-спектрометрии MALDI-TOF. Масс-спектрометрические анализы выполнялись на оборудовании Центра коллективного пользования в Институте молекулярной биологии (IMB), Академия Синика, Тайбэй, Тайвань. Измерения проводились на масс-спектрометре Bruker Autoflex III MALDI-TOF/TOF (Bruker Daltonics, Бремен, Германия).
[0135] Масс-спектроскопический анализ синтезированного таким образом азидсодержащего агониста GLP-1, приведенный на Фиг. 4B, показал, что молекулярная конструкция имеет молекулярную массу 3595,037 дальтон. Сокращения: Pbf, 2,2,4,6,7-пентаметилдигидробензофуран-5-сульфонилхлорид; Boc, трет-бутилоксикарбонил; tBu, трет-бутиловый эфир; Dde, 1-(4,4-диметил-2,6-диоксоциклогекс-1-илиден)этил; Trt, трифенилметил; TIS, триизопропилсилан; TFA, трифторуксусная кислота.
[0136] Пример 2: Синтез замещенного ε-аминоизомасляной кислотой (Aib) агониста глюкагоноподобного пептида-1 (GLP-1), имеющего азидную группу
[0137] В этом примере был получен Aib-замещенный агонист GLP-1, имеющий азидную группу (SEQ ID NO: 2) (как показано ниже), у которого остаток аланина в положении остатка 8 SEQ ID NO: 1 был заменен остатком Aib (однобуквенный код: U) для большей устойчивости к деградации дипептидилпептидазой IV (DPP 4). В этом примере γ-карбоксильная группа остатка глутамата была связана с ε-аминогруппой остатка лизина молекулы агониста GLP-1 (SEQ ID NO: 2), и α-аминогруппа остатка глутамата была модифицирована азидоацетильной группой (показано ниже).

[0138] Как и в Примере 1, авторы настоящего изобретения осуществили дизайн молекулы Aib-замещенного агониста GLP-1, имеющего азидную группу, и синтез этого вещества был передан на аутсорсинг в фирму Shanghai WuXi AppTech Co., Ltd. (Шанхай, Китай). Процедура синтеза была выполнена, как описано в предыдущем примере.
[0139] Очищенный образец Aib-замещенного агониста GLP-1, имеющего азидную группу, анализировали методом аналитической ВЭЖХ с обращенной фазой на колонке Supelco C18 (250 мм × 4,6 мм; 5 мкм), используя в качестве подвижной фазы ацетонитрил и 0,1%. трифторуксусную кислоту, линейный градиент ацетонитрила от 0% до 100% в течение 30 минут при скорости потока 1,0 мл/мин и температуре колонки 25°C. Идентификация образца проводилась с помощью масс-спектрометрии MALDI-TOF (данные не приводятся).
[0140] Пример 3: Синтез аналога соматостатина, имеющего остаток цистеина, для реакции сочетания
[0141] Как показано ниже, был осуществлен дизайн молекулы аналога соматостатина (SEQ ID NO: 3), содержащего свободный остаток цистеина для связывания с малеимидной группой связывающего фрагмента разветвленного линкера. Аналог соматостатина синтезировали стандартным твердофазным методом, который был осуществлен на аутсорсинге фирмой Ontores Biotechnologies Co., Ltd. (Ханчжоу, Китай). Аналог соматостатина имел чистоту более 95%.
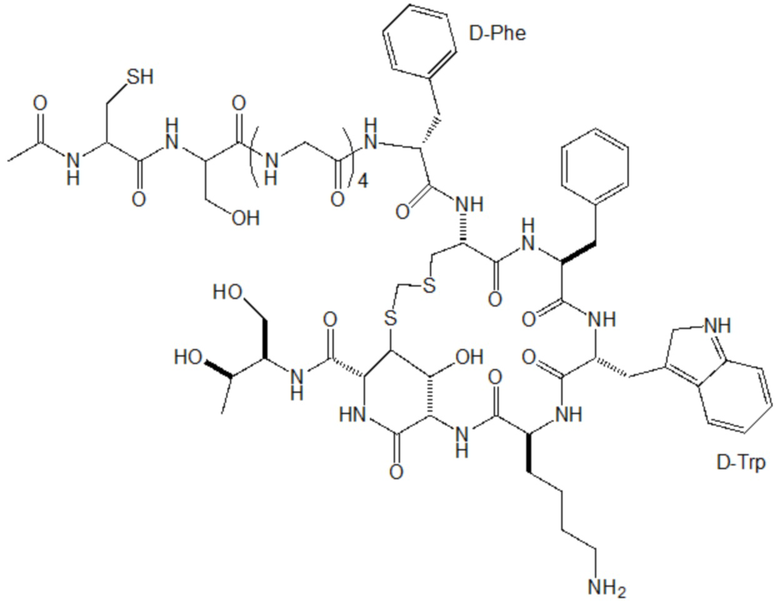
[0142] Идентификацию синтезированного пептида проводили при помощи масс-спектрометрии MALDI-TOF. На Фиг. 5 приведен результат масс-спектрометрии MALDI-TOF, который показал, что настоящая молекулярная конструкция имела молекулярную массу 1493,587 Дальтон.
[0143] Пример 4: Синтез DBCO-содержащего разветвленной линкерной единицы, конъюгированной с тремя аналогами соматостатина
[0144] Процедура синтеза DBCO-содержащего разветвленного линкера была следующей: на этапе (i) синтезированный пептид 2 (SEQ ID NO: 4) (Chinapepti Inc., Шанхай, Китай) растворяли в 100% безводном ДМСО в конечной концентрации 10 мМ. Для конъюгирования группы SH остатка цистеина с малеимид-PEG3-DBCO (Conju-probe Inc., Сан-Диего, США) для создания функциональной связывающей группы DBCO пептид и малеимид-PEG3-DBCO смешивали при соотношение 1/1 и выдерживают при комнатной температуре в течение 16 часов.
[0145] Идентификацию синтезированного DBCO-содержащего пептида 2 (показано ниже) проводили при помощи масс-спектрометрии MALDI-TOF.

[0146] На этапе (ii) синтезированный таким образом DBCO-содержащий пептид 2 затем растворяли в 100% ДМСО в конечной концентрации 10 мМ. DBCO-содержащий пептид 2 и органическое основание DABCO смешивали в молярном соотношении 1/5 в 100% ДМСО. Затем к раствору DBCO-содержащего пептида 2 добавляли сшивающий агент NHS-PEG12-Mal с конечным молярным соотношением 1/6 (DBCO-содержащий пептид 2:NHS-PEG12-Mal) в 100% безводном ДМСО. Реакционную смесь дополнительно инкубировали в течение ночи при комнатной температуре.
[0147] DBCO-содержащий пептид 2, конъюгированный с тремя связывающими фрагментами PEG12-Mal (показано ниже), очищали при помощи ВЭЖХ с обращенной фазой на колонке Supelco C18 (250 мм × 10 мм; 5 мкм), используя в качестве подвижной фазы ацетонитрил и 0,1% трифторуксусную кислоту, линейный градиент ацетонитрила от 0% до 100% в течение 30 минут, при скорости потока 3,0 мл/мин и температуре колонки 25°C.
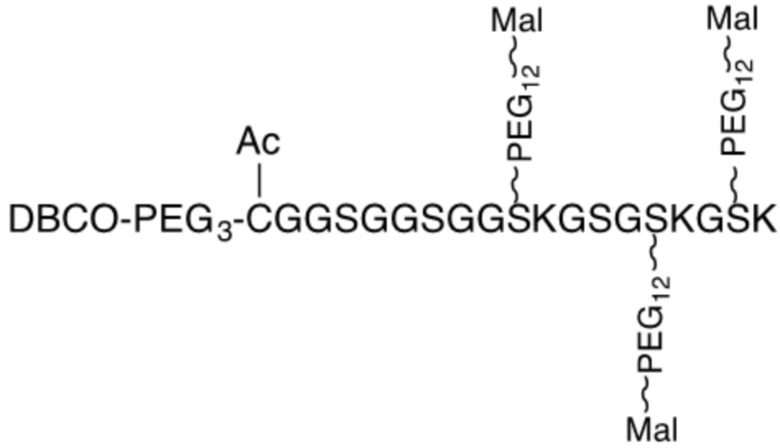
[0148] Масс-спектроскопический анализ синтезированного таким образом DBCO-содержащего пептида 2, конъюгированного с тремя связывающими фрагментами PEG12-Mal, показал, что молекулярная конструкция имеет молекулярную массу 4480,89 дальтон.
[0149] На этапе (iii) тиоловую группу аналога соматостатина из Примера 3 вводили в реакцию с DBCO-содержащим пептидом 2, конъюгированным с тремя связывающими фрагментами PEG12-Mal. Аналог соматостатина растворяли в 100% ДМСО в конечной концентрации 25 мМ, в то время как DBCO-содержащий пептид 2, конъюгированный с тремя связующими фрагментами, растворяли в 100% ДМСО в конечной концентрации 1 мМ. DBCO-содержащий пептид 2, конъюгированный с тремя связывающими фрагментами PEG12-Mal, добавляли к раствору соматостатина с конечной концентрацией 3,6 мМ (3,6-кратный молярный избыток по сравнению с 1 мМ раствором разветвленого линкера с DBCO-содержащим пептидом 2). Реакционную смесь инкубировали в течение ночи при комнатной температуре.
[0150] Содержащая DBCO разветвленная линкерная единица, конъюгированная с тремя аналогами соматостатина (3-соматостатин DBCO лекарственная группа), очищали при помощи высокоэффективной жидкостной хроматографии с обращенной фазой (ОФ-ВЭЖХ) на колонке Supelco C18 (250 мм x 10 мм; 5 мкм), используя в качестве подвижной фазы ацетонитрил и 0,1% трифторуксусную кислоту, линейный градиент от 0% до 100% ацетонитрила в течение 30 минут, при скорости потока 3,0 мл/мин и температуре колонки 25°C. Профиль элюции ВЭЖХ с обращенной фазой лекарственной группв 3-соматостатин DBCO показал, что ее элюирующий пик имеет время удерживания 22,38 минуты, отслеживаемое при ОП 254 нм посредством детектирования поглощения УФ-излучения, как показано на Фиг. 6А.
[0151] На фиг. 6В видно, что результат масс-спектроскопического анализа синтезированной таким образом лекарственной группы 3-соматостатин DBCO (показано ниже) показал, что молекулярная конструкция имела молекулярную масу 9,005 дальтон.
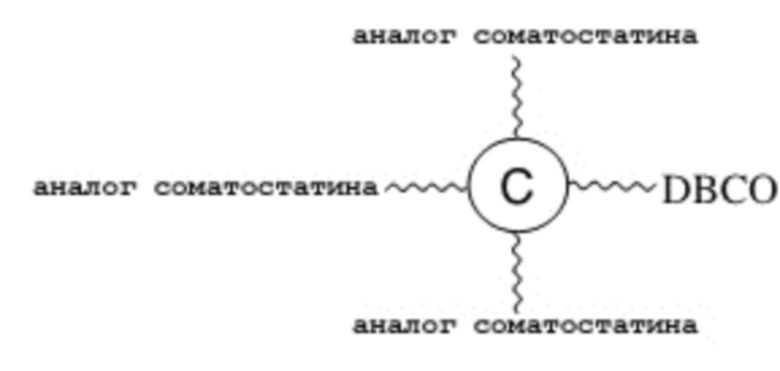
[0152] Пример 5: Синтез азидсодержащей разветвленной линкерной единицы с пептидом 3 в качестве пептидной основы (SEQ ID NO: 5) со связывающим фрагментом, ковалентно связанным с пептидом октреотидом (SEQ ID NO: 6)
[0153] В этом примере 3-октреотид азид-лекарственные группы получали с использованием стандартной Fmoc-химии путем ручного синтеза. Лекарственная група представляет собой азидсодержащую линкерную единицу с использованием пептида 3 в качестве пептидного ядра (SEQ ID NO: 5) и трех связывающих фрагментов, каждый из которых ковалентно связано с пептидом октреотидом (SEQ ID NO: 6). Авторы настоящего изобретения осуществили дизайн линкерной единиц и передали синтез 3-октреотид азид-лекарственных групп на аутсорсинг фирме Shanghai WuXi AppTech Co., Ltd. (Шанхай, Китай).
[0154] Синтезированная таким образом молекула, как показано ниже, состояла из разветвленной линкерной единицы, ковалентно связанной с тремя октреотидами и свободной азидной группой. Идентификация образцов проводили при помощи масс-спектрометрии MALDI-TOF.
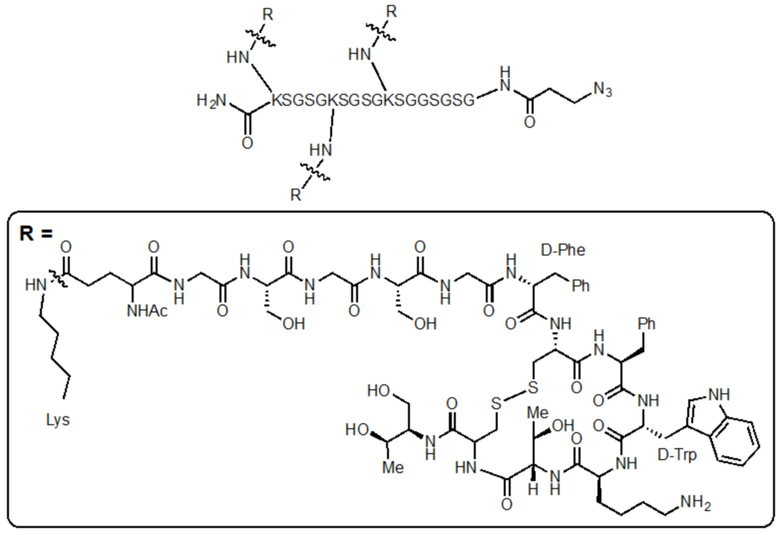
[0155] Пример 6: Синтез алкинсодержащей линкерной единицы, имеющей в качестве группы жирных кислот две пальмитоильные цепи
[0156] В этом примере получали алкинсодержащую группу жирных кислот, имеющую две пальмитоильные цепи (показано ниже).
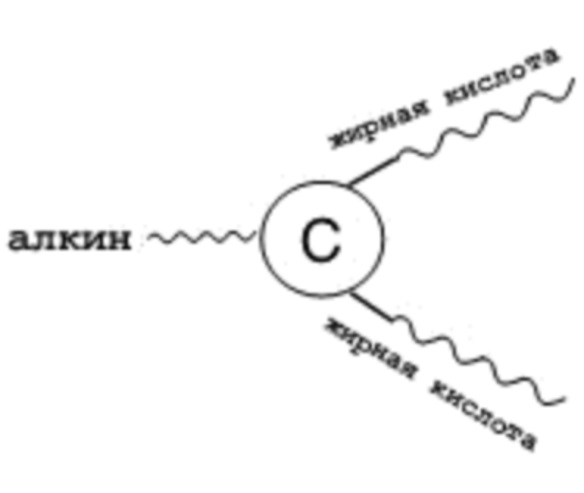
[0157] Пептидная основа (алкин-этил-Xaa4-K-Xaa4-K-OMe, SEQ ID NO: 7) имеет два остатка K и алкинилпропионильную группу, расположенную на ее N-конце. Наполнитель между двумя остатками K и N-концевой спейсер между алкиновой группой и первым остатком K представляют собой пегилированную аминокислоту с 4 повторами EG. Две пальмитоильные цепи были соответственно связаны с остатками K пептидной центральной основы посредством образования амидной связи между группой CO2H пальмитиновой кислоты и аминогруппой остатка K (показано ниже). Синтез этой новой молекулы - «алкин-EG4-2FA-C16» (сокращенно алкин-2FA) был проведен Shanghai WuXi AppTech Co., Ltd.
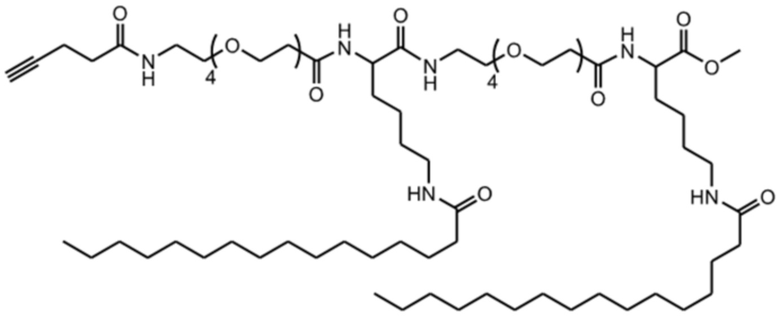
[0158] На этапе (i) пептидный синтез начинали путем ковалентного связывания первой аминокислоты со смолой: аминокислоту Fmoc-Lys(Dde)-OH (6,0 ммоль) и смолу СТС (3,0 ммоль) растворяли в дихлорметане (ДХМ), а затем добавляли DIEA (12,0 ммоль) и полученную смесь подвергали барботированию газообразным азотом в течение 2 часов.
[0159] На этапе (ii) раствор смеси пептид-смола сливали и промывали ДМФА 3 раза. На этапе (iii) после промывки смолы защитную группу Fmoc на смоле СТС удаляли путем добавления 20% пиперидина в растворе ДМФА в течение 30 минут. На этапе (iv) обработанный раствор сливали и промывали ДМФА 5 раз. На этапе (v) ручное связывание 2-й аминокислоты осуществляли путем добавления Fmoc-PEG4-OH (2 экв.) и активирующего агента (HBTU) к смоле в условиях барботирования газообразного азота в течение примерно 1 часа. Затем этапы (ii) - (v) повторяли каждый раз с другой аминокислотой в соответствии с пептидной последовательностью. Защитные группы Dde двух остатков лизина удаляли, добавляя 3% раствор N2H4/ДМФА к раствору пептидной смолы и инкубировали в течение 20 минут. В последнем цикле синтеза к смоле добавляли пальмитиновую кислоту (1,0 экв.) и активирующий агент (HBTU) при барботировании газообразного азота в течение примерно 1 часа.
[0160] Для отщепления пептида с защищенной боковой цепью, от смолы СТС, готовили расщепляющий буфер (95% TFA / 2,5% TIPS / 2,5% H2O) и добавляли в колбу, содержащую раствор пептидной смолы и перемешивали при комнатной температуре в течение 1 часа. Неочищенный пептид осаждали в холодном трет-бутилметиловом эфире и центрифугировали в течение 2 минут при 5000 об/мин. Неочищенный пептид еще два раза промывали трет-бутилметиловым эфиром и сушили в вакууме в течение 2 часов. Для получения метилового эфира С-конца неочищенный пептид растворяли в 4 н. HCl в растворе МеОН. Раствор реагировал в течение примерно 2 часов и результат реакции контролировали с помощью жидкостной хроматографии-масс-спектрометрии (ЖХМС). После того как реакция была завершена, реакцию гасили с помощью DIEA и доводили значение pH до 7,0. Полученный раствор сушили под вакуумом.
[0161] Алкинсодержащую линкерную единицу, имеющую две пальмитоильные цепи, очищали при помощи ВЭЖХ с обращенной фазой на препаративной колонке С4 Luna (250 мм × 25 мм; 10 мкм), используя в качестве подвижной фазы ацетонитрил и 0,075% трифторуксусную кислоту, линейную градиент от 55% до 90% ацетонитрила в течение 60 минут при скорости потока 20 мл/мин и температуре колонки 25°C. Масс-спектроскопический анализ синтезированной таким образом алкинсодержащей линкерной единицы, имеющей две алифатические цепи, как приведено на Фиг. 7, показал, что молекулярная конструкция имеет молекулярную массу 1340,104 дальтон. Сокращения: TIPS, триизопропилсилан.
[0162] Пример 7: Синтез четырех алкинсодержащих групп жирных кислот, вставленных с дополнительным остатком глутамата в качестве спейсера между остатком Lys и алифатической цепью в пептидной центральной основе
[0163] В этом примере были получены четыре дополнительных алкинсодержащих группы жирных кислот.
[0164] Как показано ниже, была получена одна из групп жирных кислот, названная «алкин-EG4-2E-2FA-C16», имеющая две пальмитоильные цепи. Пептидная центральная основа (алкин-этил-Xaa4-K-Xaa4-K-OMe, SEQ ID NO: 7) имеет два остатка лизина и группу алкина, расположенную на ее N-конце. Спейсеры между двумя остатками лизина и между алкинеэтильной группой и соседним остатком лизина представляют собой пегилированную аминокислоту с 4 повторами EG. Две пальмитоильные цепи были соответственно связаны с остатками лизина пептидной центральной основы через дополнительные глутаматные спейсеры, образующие амидные связи между гамма-CO2H-группой остатка глутамата и аминогруппой остатка лизина и между альфа-аминогруппой остатка глутамата и CO2H группой пальмитиновой кислоты.
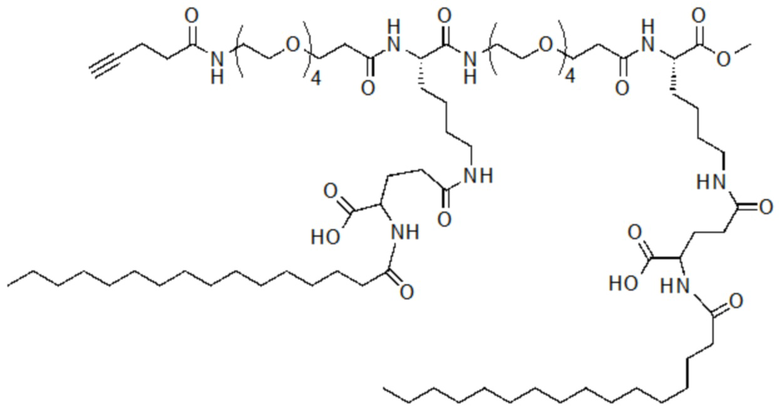
[0165] Получали группу жирных кислот алкин-EG4-2E-2FA-C16-кислоты (как показано ниже). Пептидная центральная основа (алкин-этил-Xaa4-K-Xaa4-K-OMe, SEQ ID NO: 7) имеет два остатка лизина и группу алкина, расположенную на ее N-конце. Спейсеры между двумя остатками лизина и между алкиновой группой и соседним остатком лизина представляют собой пегилированную аминокислоту с 4 повторами EG. Две пальмитоильные цепи с дикарбоновыми группами (то есть гексадекандиовая кислота или тапсиновая кислота) были соответственно связаны с остатками лизина пептидной центральной основы через дополнительные глутаматные спейсеры, образующие амидные связи между гамма-CO2H-группой остатка глутамата и аминогруппой остатка лизина и между альфа-аминогруппой остатка глутамата и одной из двух групп CO2H пальмитиновой кислоты.
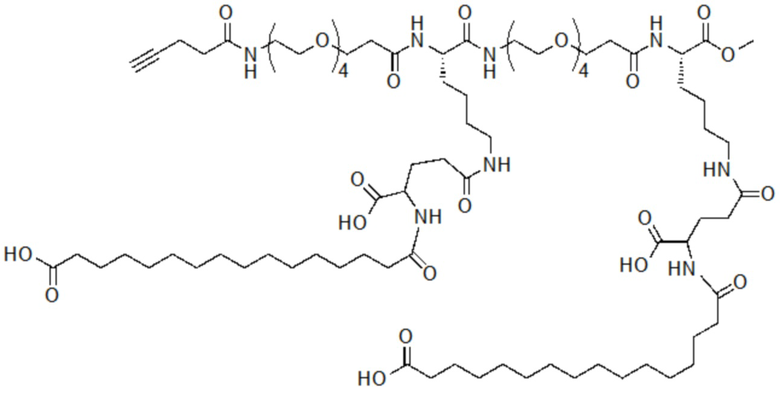
[0166] Получали группу алкин-EG2-2E-2FA-C16-жирной кислоты (как показано ниже). Пептидная центральная основа (алкин-этил-Xaa2-K-Xaa2-K-OMe, SEQ ID NO: 8) имеет два остатка лизина и группу алкина, расположенную на ее N-конце. Спейсеры между двумя остатками лизина и между алкиновой группой и соседним остатком лизина представляют собой пегилированную аминокислоту с 2 повторами EG. Две пальмитоильные цепи с дикарбоновыми группами были соответственно связаны с остатками лизина ядра пептидной центральной основы через дополнительные глутаматные спейсеры, образующие амидные связи между гамма-CO2H-группой остатка глутамата и аминогруппой остатка лизина и между альфа-аминогруппой остатка глутамата и одной из двух групп CO2H пальмитиновой кислоты.
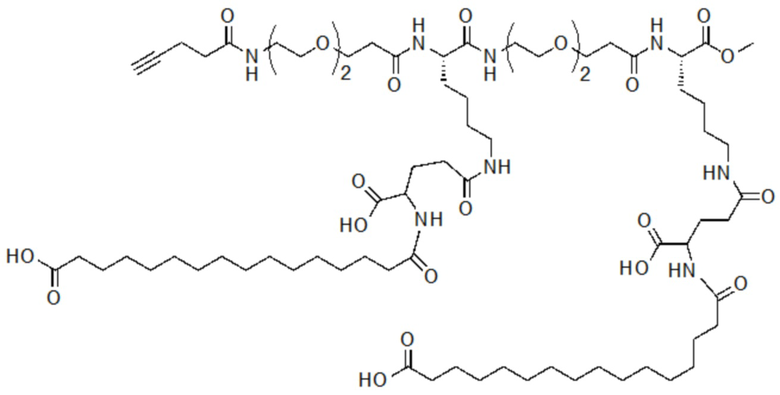
[0167] Получали группу алкин-EG2-2E-2FA-C18-жирной кислоты (как показано ниже). Пептидная центральная основа (алкин-этил-Xaa2-K-Xaa2-K-OMe, SEQ ID NO: 8) имеет два остатка лизина и группу алкина, расположенную на ее N-конце. Спейсеры между двумя остатками лизина и между алкиновой группой и соседним остатком лизина представляют собой пегилированную аминокислоту с 2 повторами EG. Две стеароильные цепи с дикарбоновыми группами (то есть октадекандиовая кислота) были соответственно связаны с остатками лизина пептидной центральной основы через дополнительные глутаматные спейсеры, образующие амидные связи между гамма-CO2H-группой остатка глутамата и аминогруппой остатка лизина и между альфа-аминогруппой остатка глутамата и одной из двух групп CO2H октадекандиовой кислоты.
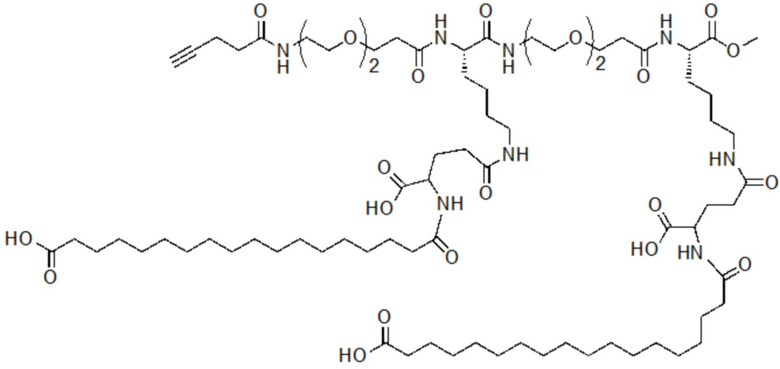
[0168] Аналогично Примеру 6, синтез этих четырех молекул группы жирных кислот - «алкин-EG4-2E-2FA-C16, алкин-EG4-2E-2FA-C16-кислота, алкин-EG2-2E-2FA-C16-кислота и алкин-EG2-2E-2FA-C18-кислота» был передан на аутсорсинг фирме Shanghai WuXi AppTech Co., Ltd.
[0169] Пример 8: Синтез молекулярной конструкции, состоящей из одного агониста GLP-1 и двух алифатических цепей (агонист GLP-1-Ala8-EG4-2FA-C16)
[0170] В этом примере азидсодержащий агонист GLP-1 из Примера 1 и алкинсодержащая линкерная единица, имеющая две пальмитоильные цепи из Примера 6, были связаны при помощи CuAAC между азидной и алкиновой группами с образованием «агониста GLP-1-Ala8-EG4-2FA-C16», как показано ниже.
[0171] Синтез был произведен на аутсорсинге фирмой Shanghai WuXi AppTech Co., Ltd. В кратком изложении, смесь азидсодержащего агониста GLP-1 из Примера 1 (850,0 мг, 236,4 мкмоль, 1,0 экв.) и алкинсодержащей линкерной единицы, содержащего два пальмитоильные цепи из Примера 6 (158,4 мг, 118,2 мкмоль, 0,5 экв.) в ДМСО (30,0 мл) дегазировали и продували газообразным азотом 3 раза, добавляли CuI (22,5 мг, 118,2 мкмоль, 0,5 экв.) и DIEA (61,1 мг, 472,8 мкмоль, 82,4 мкл, 2,0 экв.) и перемешивали эту смесь при температуре 25°С в течение 1 часа в атмосфере газообразного азота. Завершение реакции подтверждали жидкостной хроматографией с масс-спектрометрией (ЖХ-МС).
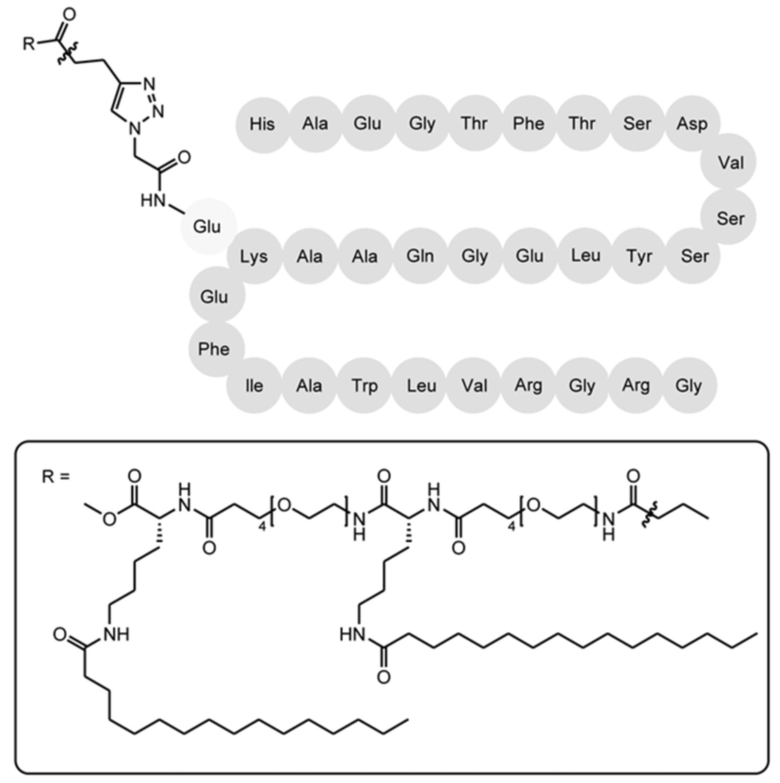
[0172] Агонист GLP-1-2FA очищали с помощью ВЭЖХ с обращенной фазой на колонке Luna C18 (200 мм x 25 мм; 10 мкм) и Gemini C18 (150 мм x 30 мм; 5 мкм) последовательно, используя в качестве подвижной фазы ацетонитрил и 0,075% трифторуксусную кислоту, линейный градиент от 40% до 70% ацетонитрила в течение 60 минут при скорости потока 20 мл/мин и температуре колонки 25°C. Продукт лиофилизировали с получением желаемого продукта (33,2 мг, выход 2,85%) в виде белого твердого вещества.
[0173] На Фиг. 8А изображен профиль элюции ВЭЖХ с обращенной фазой для очистки агониста GLP-1-2FA, где пик агониста GLP-1-2FA появляется при ОП 215 нм с временем удерживания 11,037 минут. Масс-спектроскопический анализ синтезированного таким образом агониста GLP-1-Ala8-EG4-2FA-C16, как изображено на Фиг. 8B, показал, что молекулярная конструкция агониста GLP-1-Ala8-EG4-2FA-C16 имела молекулярную массу 4937 Дальтон.
[0174] Пример 9: Синтез молекулярной конструкции, состоящей из одного агониста GLP-1 и двух пальмитоильных цепей с дополнительными остатками глутамата в качестве спейсеров (агонист GLP-1-Ala8-EG4-2E-2FA-C16)
[0175] В этом примере азидсодержащий агонист GLP-1 из Примера 1 и одна из групп алкинсодержащих жирных кислот (алкин-EG4-2E-2FA-C16) из Примера 7 были связаны при помощи CuAAC между азидной и алкиновой группами с образованием «агониста GLP-1-Ala8-EG4-2E-2FA-C16», как показано ниже.

[0176] Аналогично Примеру 8, синтез был передан на аутсорсинг фирме Shanghai WuXi AppTech Co., Ltd.
[0177] На Фиг. 9А показан профиль элюции ВЭЖХ с обращенной фазой для очистки агониста GLP-1-Ala8-EG4-2E-2FA-C16, где пик агониста GLP-1-EG4-2E-2FA-C16 появляется при ОП 215 нм с временем удерживания 34,53 минуты, этот пик обозначен стрелкой.
[0178] Масс-спектроскопический анализ синтезированного таким образом агониста GLP-1-EG4-2E-2FA-C16, как изображено на Фиг. 9B, показал, что молекулярная конструкция агонист GLP-1-Ala8-EG4-2E-2FA-C16 имела молекулярную массу 5194 дальтон.
[0179] Пример 10: Синтез молекулярной конструкции, состоящей из одного Aib-замещенного агониста GLP-1 и двух пальмитоильных цепей с дополнительными глутаматными остатками в качестве спейсеров (агонист GLP-1-Aib8-EG4-2E-2FA-C16)
[0180] В этом примере Aib-замещенный агонист GLP-1, имеющий азидную группу, из Примера 2 и одну из групп алкинсодержащих жирных кислот (алкин-EG4-2E-2FA-C16) из Примера 7, связывали при помощи CuAAC между азидной и алкиновой группами для получения «агониста GLP-1-Aib8-EG4-2E-2FA-C16», как показано ниже.
[0181] Аналогично Примеру 8 синтез был передан на аутсорсинг фирме Shanghai WuXi AppTech Co., Ltd.
[0182] На Фиг. 10А показан профиль элюции ВЭЖХ с обращенной фазой для очистки агониста GLP-1-Aib8-EG4-2E-2FA-C16, где пик агониста GLP-1-Aib-EG4-2E-2FA-C16 появляется при ОП 215 нм с временем удерживания 34,635 минут, этот пик обозначен стрелкой.
[0183] Масс-спектроскопический анализ синтезированного таким образом агониста GLP-1-Aib8-EG4-2E-2FA-C16, как изображено на Фиг. 10B, показал, что молекулярная конструкция агонист GLP-1-Aib8-EG4-2E-2FA-C16 имела молекулярную массу 5208 дальтон.
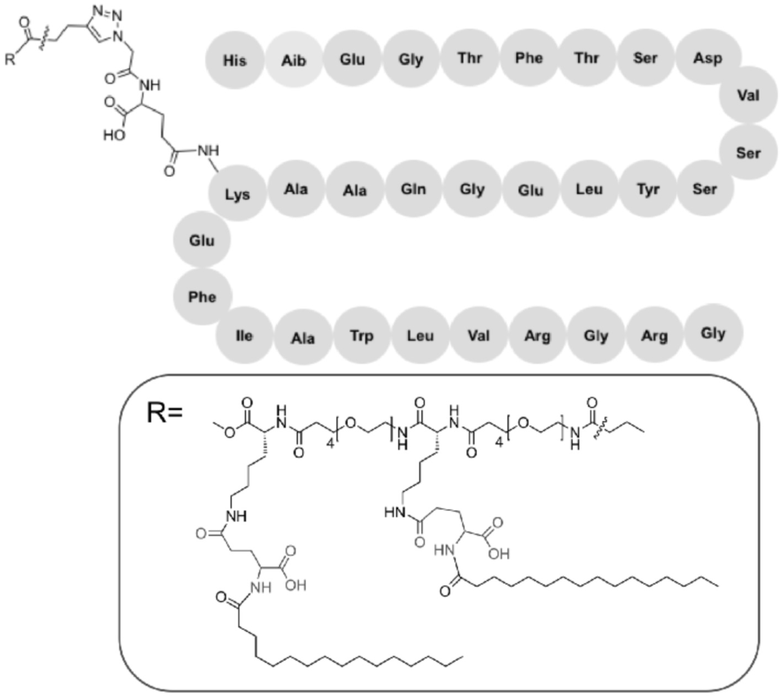
[0184] Пример 11: Синтез молекулярной конструкции, состоящей из одного Aib-замещенного агониста GLP-1 и двух цепей пальмитоил-дикарбоновой кислоты с дополнительными глутаматными остатками в качестве спейсеров (агонист GLP-1-Aib8-EG4-2E-2FA-C16-кислота)
[0185] В этом примере Aib-замещенный агонист GLP-1, имеющий азидную группу, из Примера 2 и одну из групп алкинсодержащих жирных кислот (алкин-EG4-2E-2FA-C16-кислота) из Примера 7, связывали при помощи CuAAC между азидной и алкиновой группами для получения «агониста GLP-1-Aib8-EG4-2E-2FA-C16-кислота», как показано ниже.
[0186] Аналогично Примеру 8, синтез был передан на аутсорсинг фирме Shanghai WuXi AppTech Co., Ltd.
[0187] На Фиг. 11А показан профиль элюции ВЭЖХ с обращенной фазой для очистки агониста GLP-1-Aib8-EG4-2E-2FA-C16-кислота, где пик агониста GLP-1-Aib8-EG4-2E-2FA-С16-кислота появляется при ОП 215 нм с временем удерживания 25,988 минут, этот пик обозначен стрелкой.
[0188] Масс-спектроскопический анализ синтезированного таким образом агониста GLP-1-Aib8-EG4-2E-2FA-C16-кислота, как изображено на Фиг. 11B, показал, что молекулярная конструкция агонист GLP-1-Aib8-EG4-2E-2FA-C16-кислота имела молеклярную массу 5267 дальтон.
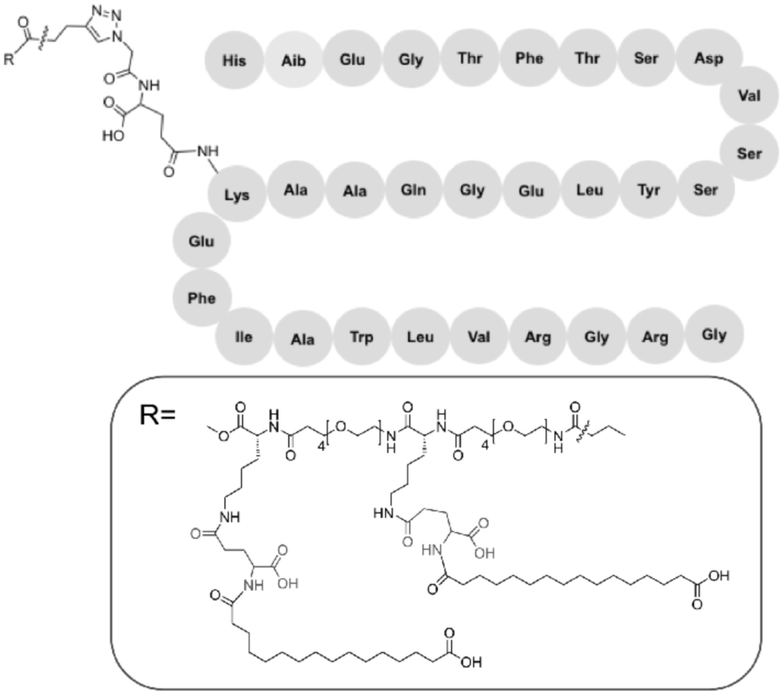
[0189] Пример 12: Синтез молекулярной конструкции, состоящей из одного Aib-замещенного агониста GLP-1 и двух цепей пальмитоил-дикарбоновой кислоты с дополнительными остатками глутамата в качестве спейсеров (агонист GLP-1-Aib8-EG2-2E-2FA-C16-кислота)
[0190] В этом примере Aib-замещенный агонист GLP-1, имеющий азидную группу, из Примера 2 и одну из групп алкинсодержащих жирных кислот (алкин-EG2-2E-2FA-C16-кислота) из Примера 7, связывали при помощи CuAAC между азидной и алкиновой группами для получения «агониста GLP-1-Aib8-EG2-2E-2FA-C16-кислота», как показано ниже.
[0191] Аналогично Примеру 8, синтез был передан на аутсорсинг фирме Shanghai WuXi AppTech Co., Ltd.
[0192] На Фиг. 12А показан профиль элюции ВЭЖХ с обращенной фазой для очистки агониста GLP-1-Aib8-EG2-2E-2FA-C16-кислота, где пик агониста GLP-1-Aib8-EG2-2E-2FA-С16-кислота появляется при ОП 215 нм с временем удерживания 26,0 минут, этот пик обозначен стрелкой.
[0193] Масс-спектроскопический анализ синтезированного таким образом агониста GLP-1-Aib8-EG4-2E-2FA-C16-кислота, как изображено на Фиг. 12B, показал, что молекулярная конструкция агонист GLP-1-Aib8-EG2-2E-2FA-C16-кислота имел молекулярную массу 5091 дальтон.
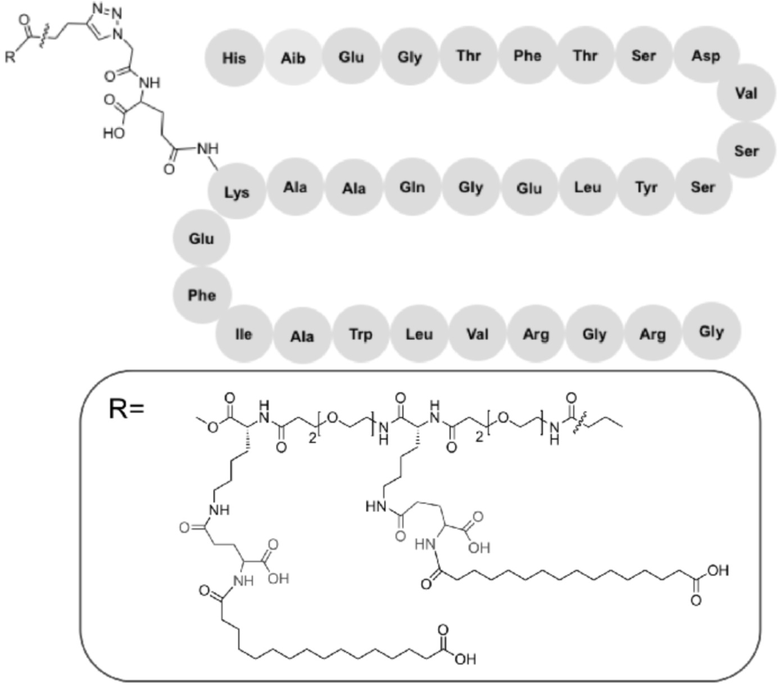
[0194] Пример 13: Синтез молекулярной конструкции, состоящей из одного Aib-замещенного агониста GLP-1 и двух цепей стеароил-дикарбоновой кислоты с дополнительными глутаматными остатками в качестве спейсеров (агонист GLP-1-Aib8-EG2-2E-2FA-C18-кислота)
[0195] В этом примере Aib-замещенный агонист GLP-1, имеющий азидную группу, из Примера 2 и одну из групп алкинсодержащих жирных кислот (алкин-EG2-2E-2FA-C18-кислота) из Примера 7, связывали при помощи CuAAC между азидной и алкинильной группами для получения «агониста GLP-1-Aib8-EG2-2E-2FA-C18-кислота», как показано ниже.
[0196] Аналогично Примеру 8, синтез был передан на аутсорсинг фирме Shanghai WuXi AppTech Co., Ltd.
[0197] На Фиг. 13А показан профиль элюции ВЭЖХ с обращенной фазой для очистки агониста GLP-1-Aib8-EG2-2E-2FA-C18-кислота, где пик агониста GLP-1-Aib8-EG2-2E-2FA-C18-кислота появляется при ОП 215 нм с временем удерживания 27,815 минут, этот пик обозначен стрелкой.
[0198] Масс-спектроскопический анализ синтезированного таким образом агониста GLP-1-Aib8-EG4-2E-2FA-C18-кислота, как изображено на Фиг. 13B, показал, что молекулярная конструкция агонист GLP-1-Aib8-EG2-2E-2FA-C18-кислота имеет молекулярную массу 5148 дальтон.
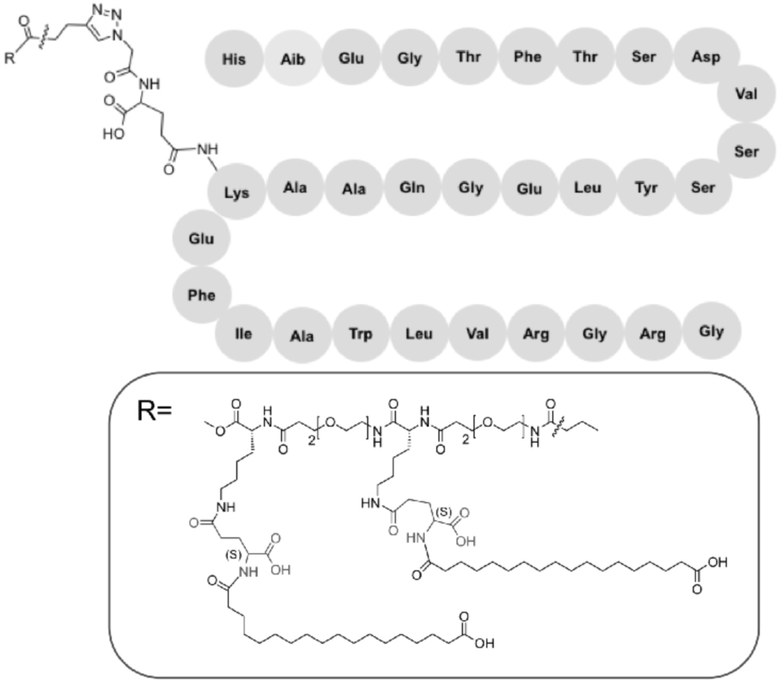
[0199] Пример 14: Синтез молекулярной конструкции, состоящей из разветвленной линкерной единицы, конъюгированной с тремя пептидами октреотида и двумя алифатическими цепями
[0200] В этом примере азидсодержащую разветвленную линкерную единицу, конъюгированную с тремя пептидами октреотида, из Примера 5 и одну из групп алкинсодержащих жирных кислот (алкин-EG4-2E-2FA-C16) из Примера 7, связывали при помощи CuAAC между азидной и алкинильной группами для получения молекулярной конструкции, состоящей из разветвленной линкерной единицы, конъюгированной с тремя пептидами октреотида и двумя алифатическими цепями, как показано ниже.
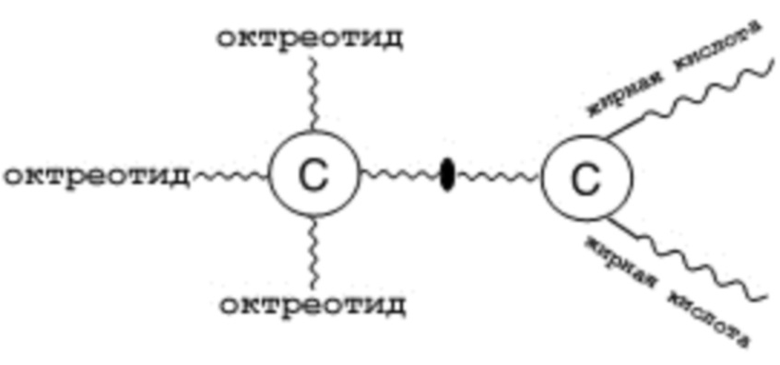
[0201] Процедуры синтеза были аналогичны процедурам, описанным в Примере 8. В кратком изложении, смесь азидсодержащей разветвленной линкерной единицы, конъюгированной с тремя пептидами октреотида, из Примера 5 (1,0 экв.) и алкинсодержащей линкерной единицы, имеющей две пальмитильные цепи, из Примера 7 (алкин-EG4-2E-2FA-C16) (0,5 экв.) в ДМСО (30,0 мл) дегазировали и продували газообразным азотом 3 раза, добавляли CuI (0,5 экв.) и DIEA (2,0 экв.) и перемешивали эту смесь при температуре 25°С в течение 1 часа в атмосфере газообразного азота. Завершение реакции подтверждали ЖХ-МС.
[0202] Синтезированная таким образом молекула, как показано ниже, состояла из разветвленной линкерной единицы, конъюгированной с тремя пептидами октреотида и двумя алифатическими цепями.
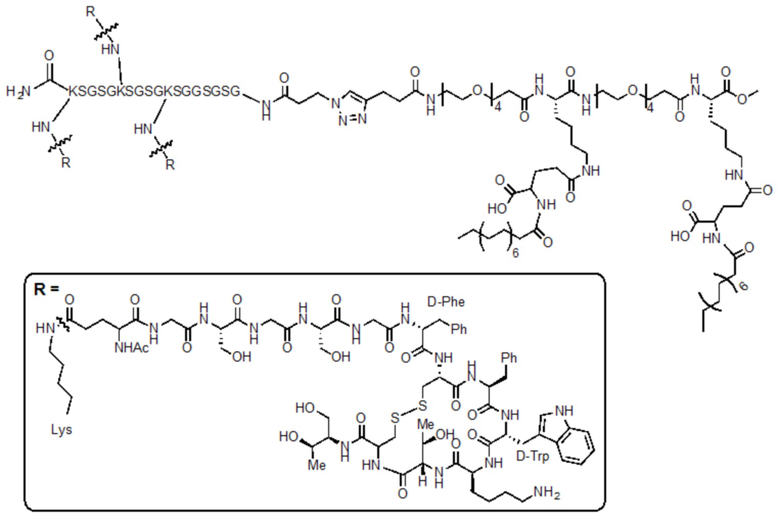
[0203] Пример 15: Характеристика связывания агониста GLP-1-EG4-2FA-C16 с рецептором GLP-1
[0204] В этом примере способность связывания агониста GLP-1-Ala8-EG4-2FA-C16 (сокращенно GLP-1-2FA) с рецептором GLP-1 исследовали с использованием ИФА.
[0205] В кратком изложении, 96-луночный планшет для микротитрования покрывали рекомбинантным слитым белком GLP-1R-IgG.Fc человека (GLP-1R) (приобретен у Sino Biological Inc., Тайбэй, Тайвань) в концентрации 10 мкг/мл, в количестве 50 мкл на лунку. После отмывания избытка рекомбинантного белка рецептора GLP-1 лунки блокировали 1% BSA в ФСБ, pH 7,4, содержащем 0,1% NaN3 в течение 1 часа, добавляли 50 мкл на лунку агониста GLP-1-EG4-2FA-C16, алкинсодержащей линкерной единицы, имеющей две пальмитоильные цепи (алкин-EG4-2FA-C16, сокращенно алкин-2FA), азидсодержащего агониста GLP-1 (GLP-1-азид) и лираглутид (Victoza, любезно предоствлен др. И-Чен Чанг, Институт медицинской геномики и протеомики, Национальный университет Тайваня) в двух концентрациях (1 мкг/мл и 10 мкг/мл). После промывания ФСБ добавляли мышиный mAb IgG анти-hGLP-1 (Abcam, Bristol, UK) в конечной концентрации 2 мкг/мл и инкубировали при температуре 37°C в течение 1 часа. После промывания ФСБ, pH 7,4, антитела, связанные с hGLP-1, детектировали с помощью HRP-конъюгированного козьего антимышиного IgG (H+L) (Jackson ImmunoResearch) при соотношении 1:10000 и инкубировали в течение 30 минут при температуре 37°C с последующей инкубацией с субстратом TMB (Clinical Science Products, Мэнсфилд, США). Реакцию останавливали добавлением 50 мкл 1 М HCl. Поглощение при длине волны 450 нм измеряли с помощью планшет-ридера. Каждый столбец представлет собой среднее значение ОП450 для дублированных образцов. Данные показали, что агонист GLP-1-2FA может специфически связываться с рекомбинантным рецептором GLP-1 (см. Фиг. 14). Пептид P1-P2, который является сегментом домена CεmX связанного с мембраной человека IgE, служил в качестве отрицательного контроля.
[0206] Пример 16: Характеристика связывания агониста GLP-1-Ala8-EG4-2FA-C16 с сывороточным альбумином человека (HSA)
[0207] В этом примере способность связывания агониста GLP-1-Ala8-EG4-2FA-C16 (сокращенно GLP-1-2FA) с HSA исследовали с использованием ИФА.
[0208] В кратком изложении, 96-луночный планшет для микротитрования покрывали белком HSA в концентрации 10 мкг/мл, 50 мкл на лунку в 1× ФСБ, pH 7,4 при температуре 37°C в течение 1 часа. Затем лунки блокировали 1% казеином в ФСБ, pH 7,4, содержащем 0,1% NaN3, в течение 1 часа и инкубировали с азидсодержащим агонистом GLP-1 (GLP-1-азид), алкин-EG4-2FA-C16 (алкин-2FA), лираглутидом или агонистои GLP-1-2FA в конечной концентрации 1 и 10 мкг/мл при температуре 37°С в течение 1 часа. После промывания ФСБ, pH 7,4, добавляли мышиное анти-hGLP-1 mAb (Abcam) в конечной концентрации 10 мкг/мл и инкубировали при температуре 37°C в течение 1 часа. После промывания ФСБ, pH 7,4, антитела, связанные с hGLP-1, детектировали с помощью HRP-конъюгированных козьих антимышиный IgG (H+L) антител (Jackson ImmunoResearch) при соотношении 1:10000 и инкубировали в течение 30 минут при температуре 37°C с последующей инкубацией с субстратом TMB (Clinical Science Products). Реакцию останавливали добавлением 50 мкл 1 М HCl. Поглощение при длине волны 450 нм измеряли с помощью планшет-ридера. Каждый столбец представляет собой среднее значение ОП450 для дублированных образцов. Было обнаружено, что GLP-1-2FA проявляет более высокую активность связывания с HSA, чем лираглутид (Фиг. 15). GLP-1-азид, алкин-2FA и только вторичные антитела служили отрицательным контролем.
[0209] Пример 17: Характеристика альбумин-связывающей активности агониста GLP-1-Ala8-EG4-2FA-C16 с HSA с использованием анализа диализного равновесия
[0210] Для дальнейшего изучения способности связывания агониста GLP-1-Ala8-EG4-2FA-C16 (GLP-1-2FA) с HSA в водном растворе проводили анализ диализного равновесия с использованием устройства для диализа Float-A-Lyzer G2 CE (Spectrum Europe BV, Бреда, Нидерланды), которое содержало 0,2 мл раствора HSA (150 мкМ) для инкубации с 30 мкМ лираглутида или агониста GLP-1-2FA. Диализные мешки имели диаметр 5 мм, внутренний объём 1 мл и молекулярную массу отсечки 20 кДа, что позволяло пропускать лираглутид (т.е. 3751,2 дальтон) или агонист GLP-1-2FA (т.е. 4937 дальтон) в и из диализного мешка. Устройство для диализа помещали в камеру, заполненную 4 мл буферного раствора для инкубации, и помещали на шейкер при комнатной температуре на ночь. Одну десятую объёма инкубационного раствора и контроля перед диализом наносили на модифицированный трициновый ДСН-ПААГ. Связанный с HSA агонист GLP-1-2FA или лираглутид в равновесном состоянии визуализировали и количественно определяли с помощью окрашивания кумасси-синим для сравнения относительной способности связывания агониста GLP-1-2FA с HSA и лираглутида с HSA.
[0211] Было обнаружено, что агонист GLP-1-2FA проявлял более высокую способность к связыванию с HSA, чем лираглутид в водном растворе (Фиг. 16A). Стрелка #1 обозначает HSA-связанный лираглутид; Стрелка #2 обозначает HSA-связанный агонист GLP-1-2FA; Стрелка № 3 обозначает HSA. Процент связанного с HSA агониста GLP-1-2FA или лираглутида в равновесии в ДСН-ПААГ показан на Фиг. 16B. Данные были представлены как среднее ± СКО образцов в трех повторностях.
[0212] Пример 18: Функциональный анализ аналогов GLP-1 на влияние на продуцирование GLP-1R-опосредованного цАМФ в клетках INS-1 крысы
[0213] Хорошо известно, что циклический АМФ (цАМФ) продуцируется в β-клетках в ответ на инкретины, высвобождаемые кишечником в ответ на потребление пищи. Гормон-пептид GLP-1 повышает уровни цАМФ путем активации специфичного связанного с G-белком рецептора, рецептора GLP-1, что приводит к стимуляции одной из семейства трансмембранных аденилилциклаз, чувствительных к G-белку.
[0214] В этом примере для оценки функциональной активности этих аналогов GLP-1 по отношению к рецептору GLP-1 на β-клетках проводили анализ цАМФ в клетках INS-1.
[0215] ИФА набор реагентов для определения цАМФ (Cayman Chemicals, Ann Arbor, США) использовали для измерения изменений уровня внутриклеточного цАМФ, вызванных пятью аналогами GLP-1, агонисты GLP-1-Ala8-EG4-2E-2FA-C16, GLP-1-Aib8-EG4-2E-2FA-C16, GLP-1-Aib8-EG4-2E-2FA-C16-кислота, GLP-1-Aib8-EG2-2E-2FA-C16-кислота и GLP-1-Aib8-EG2-2E-2FA-C18-кислота в соответствии с инструкциями производителя. В кратком изложении, в первый день 2 × 105 клеток INS-1 высевали в каждую лунку 24-луночного планшета (ThermoFisher Scientific, Waltham, США) с 500 мкл культуральной среды на лунку. На третий день аналоги GLP-1 настоящего изобретения в концентрации 100 нМ добавляли в лунки с 2,5 мМ глюкозы и инкубировали в течение 20 мин при температуре 37°С. В контрольные лунки добавляли 100 нМ лираглутида в качестве положительного контроля для продуцирования цАМФ и инкубировали в течение 20 мин при температуре 37°С. Глюкозу в более низкой концентрации (2,5 мМ) использовали в качестве отрицательного контроля, а глюкозу в более высокой концентрации (16 мМ) использовали в качестве контроля индуцированного глюкозой продуцирования цАМФ. После 20 минут инкубации среду удаляли путем аспирации и в каждую лунку добавляли 200 мкл 0,1 н. HCl. Клетки собирали с поверхности скребком и подвергали центрифугированию при 1000 × g в течение 10 минут при температуре 4°С. Супернатант переносили в новые пробирки и использовали для эксперимента в 96-луночном планшете. Уровни циклического АМФ в клетках измеряли при длине волны 420 нм с использованием устройства для считывания микропланшетов SpectraMax M2 (Molecular devices, San Jose, США).
[0216] На Фиг. 17 показано измерение цАМФ в клетках INS-1 при инкубации с пятью аналогами GLP-1, агонисты GLP-1-Ala8-EG4-2E-2FA-C16 (сокращенно Ala8-EG4-C16), GLP-1-Aib8-EG4-2E-2FA-C16 (сокращенно Aib8-EG4-C16), GLP-1-Aib8-EG4-2E-2FA-C16-кислота (сокращенно Aib8-EG4-C16-кислота), GLP-1-Aib8-EG2-2E-2FA-C16-кислота (сокращенно Aib8-EG2-C16-кислота) и GLP-1-Aib8-EG2-2E-2FA-C18-кислота (сокращенно Aib8-EG2-C18-кислота). Результат показал, что добавление этих синтезированных аналогов GLP-1 и лираглутида к клеткам INS-1 вызывало ожидаемое повышение клеточного уровня цАМФ, наблюдаемое в момент измерения (20 минут).
[0217] Пример 19: Вестерн-блот-анализ для выявления экспрессии активированной каспазы-3 в клетках INS-1
[0218] Расщепленная каспаза-3 играет ключевую роль в процессе апоптоза. В этом примере экспрессию каспазы-3 определяли с использованием вестерн-блоттинга.
[0219] Клетки INS-1, обработанные аналогами GLP-1, культивировали с хх мМ глюкозы и 500 мкл культуральной среды на лунку. Для иммуноблот-анализа белки разделяли с использованием ДСН-ПААГ, а затем переносили на поливинилиденфторидную (PVDF) мембрану. Мембрану исследовали с использованием антител против каспазы-3 (Cell Signaling Technology, Danvers, США), а затем вторичных антител, конъюгированных с пероксидазой хрена (HRP) (Epitomics, Burlingame, США). Мембрану визуализировали с использованием усовершенствованной системы хемилюминесценции (GE Healthcare Life Sciences, Бакингемшир, США). Уровни экспрессии белка были нормализованы против экспрессии β-актина.
[0220] Результаты, обобщенные на Фиг. 18А, показывают уровень экспрессии каспазы-3 при обработке аналогами GLP-1. На Фиг. 18В показана степень пониженного уровня экспрессии каспазы-3 в клетках INS-1 при инкубации с аналогами GLP-1. Результаты на Фиг. 18А и 18В показывают, что некоторые аналоги GLP-1, включая GLP-1-Aib8-EG4-2E-2FA-C16 (Aib8-EG4-C16) и GLP-1-Ala8-EG4-2E-2FA-C16 (Ala8-EG4-C16), могуь эффективно снижать уровень экспрессии каспазы-3 в клетках INS-1.
[0221] Пример 20: Анализ с аламаровым синим для определения жизнеспособности клеток INS-1
[0222] Культивируемые клетки INS-1 высевали с плотностью 2 × 104 клеток на лунку в 96-луночный планшет в культуральной среде, содержащей 10% фетальной бычьей сыворотки. Через 48 часов клетки дополнительно инкубировали в течение еще 24 часов для сывороточного голодания. Когда клетки находились в состоянии синхронизации, клетки культивировали в среде с 30 мМ глюкозы и обрабатывали 100 нМ аналогов GLP-1 или лираглутидом. Клетки, культивируемые в нормальной среде, использовали в качестве контроля.
После инкубации в течение 24, 48 и 72 часов жизнеспособность клеток затем определяли с помощью набора реагентов для определения жизнеспособности клеток с аламаровым синим (Invitrogen) в соответствии с инструкцией производителя.
[0223] Коэффициент пролиферации клеток (см. Фигуру 19) представлял собой отношение жизнеспособности клеток в несколько моментов времени по сравнению с 0 часом. Результат показал, что жизнеспособность клеток была значительно улучшена некоторыми аналогами GLP-1, включая GLP-1-Aib8-EG4-2E-2FA-C16-кислота (Aib8-EG4-C16-кислота), GLP-1-Aib8-EG4-2E-2FA-C16 (Aib8-EG4-C16) и GLP-1-Ala8-EG4-2E-2FA-C16 (Ala8-EG4-C16) по сравнению с лираглутидом.
[0224] Пример 21: In vivo анализ влияния аналогов GLP-1 на снижение концентрации глюкозы в крови у мышей db/db с диабетом типа II
[0225] 8-недельных мышей линии BKS.Cg- + Leprdb/+ Leprdb/ (db/db) приобретали в Национальном центре лабораторных животных (NARLabs) в Тайване. Во всех экспериментах четырех животных содержали в клетке в контролируемых условиях окружающей среды. Животным давали свободный доступ к питьевой воде и обычному рациону.
[0226] Для предварительного тестирования измерения уровня глюкозы в крови у мышей db/db, получавших аналоги GLP-1, была проведена процедура предварительного тестирования. Мышей объединили в группы по три мыши на группу, эти группы получали соответствующие образцы в концентрации 100 нмоль на кг массы тела. Мышам вводили однократные подкожные инъекции аналогов GLP-1, лираглутида или носителя (ФСБ).
[0227] Для измерения уровня глюкозы в крови отбирали образцы крови из хвостовой вены, и уровень глюкозы в крови немедленно измеряли с использованием коммерчески доступного метода ферментного электрода (ACCU-CHEK Active, Roche, Германия). Результат предварительного тестирования показал, что уровень глюкозы в крови у мышей db/db, получавших аналоги GLP-1, может быть значительно снижен некоторыми из этих аналогов GLP-1 в течение 96 часов по сравнению с мышами, получавшими лираглутид.
[0228] Следует понимать, что приведенное выше описание вариантов осуществления изобретения дано только в качестве примера, и что специалистами в данной области техники могут быть сделаны различные модификации. Приведенные выше описание, примеры и данные предоставляют собой полное описание структуры и применения примерных вариантов осуществления изобретения. Хотя различные варианты осуществления изобретения были описаны выше с определенной степенью детализации или со ссылкой на один или несколько отдельных вариантов осуществления изобретения, специалисты в данной области техники могут внести многочисленные изменения в раскрытые варианты осуществления изобретения, не отступая от сущности или объёма настоящего изобретения.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> ИММУНВОРК ИНК.
<120> ФАРМАЦЕВТИЧЕСКИЕ КОНСТРУКЦИИ С ПОВЫШЕННОЙ АФФИННОСТЬЮ
СВЯЗЫВАНИЯ С АЛЬБУМИНОМ
<130> P3063-1-PCT
<150> PCT/CN2018/106515
<151> 2018-09-19
<150> PCT/CN2017/102242
<151> 2017-09-19
<160> 8
<170> BiSSAP 1.3.6
<210> 1
<211> 31
<212> PRT
<213> Artificial Sequence
<220>
<223> Synthesized
<400> 1
His Ala Glu Gly Thr Phe Thr Ser Asp Val Ser Ser Tyr Leu Glu Gly
1 5 10 15
Gln Ala Ala Lys Glu Phe Ile Ala Trp Leu Val Arg Gly Arg Gly
20 25 30
<210> 2
<211> 32
<212> PRT
<213> Artificial Sequence
<220>
<223> Synthesized
<220>
<221> MOD_RES
<222> 2
<223> Aib
<400> 2
His Xaa Glu Gly Thr Phe Thr Ser Asp Val Ser Ser Tyr Leu Glu Gly
1 5 10 15
Gln Ala Ala Lys Leu Glu Phe Ile Ala Trp Leu Val Arg Gly Arg Gly
20 25 30
<210> 3
<211> 14
<212> PRT
<213> Artificial Sequence
<220>
<223> Synthesized
<400> 3
Cys Ser Gly Gly Gly Gly Phe Cys Phe Trp Lys Thr Cys Thr
1 5 10
<210> 4
<211> 19
<212> PRT
<213> Artificial Sequence
<220>
<223> Synthesized
<400> 4
Cys Gly Gly Ser Gly Gly Ser Gly Gly Ser Lys Gly Ser Gly Ser Lys
1 5 10 15
Gly Ser Lys
<210> 5
<211> 18
<212> PRT
<213> Artificial Sequence
<220> <223> Synthesized
<400> 5
Gly Ser Gly Ser Gly Gly Ser Lys Gly Ser Gly Ser Lys Gly Ser Gly
1 5 10 15
Ser Lys
<210> 6
<211> 14
<212> PRT
<213> Artificial Sequence
<220>
<223> Synthesized
<400> 6
Glu Gly Ser Gly Ser Gly Phe Cys Phe Trp Lys Thr Cys Thr
1 5 10
<210> 7
<211> 4
<212> PRT
<213> Artificial Sequence
<220>
<221> MOD_RES
<222> 1
<223> Xaa is a PEGylated amino acid with four EG units Xaa is coupled
with an alkynylpropionyl group
<220>
<223> Synthesized
<220>
<221> MOD_RES
<222> 3
<223> Xaa is a PEGylated amino acid with four EG units
<220>
<221> MOD_RES
<222> 4
<223> esterification
<400> 7
Xaa Lys Xaa Lys
1
<210> 8
<211> 38
<212> PRT
<213> Artificial Sequence
<220>
<221> MOD_RES
<222> 1
<223> Xaa is a PEGylated amino acid with two EG units Xaa is coupled with an
alkynylpropionyl group
<220>
<223> Synthesized
<220>
<221> MOD_RES
<222> 3
<223> Xaa is a PEGylated amino acid with two EG units
<220>
<221> MOD_RES
<222> 4
<223> esterification
<400> 8
Gly Leu Ala Gly Gly Ser Ala Gln Ser Gln Arg Ala Pro Asp Arg Val
1 5 10 15
Leu Cys His Ser Gly Gln Gln Gln Gly Leu Pro Arg Ala Ala Gly Gly
20 25 30
Ser Val Pro His Pro Arg
35
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| Линкерные звенья и содержащие их молекулярные конструкции | 2018 |
|
RU2752671C2 |
| МОЛЕКУЛЯРНЫЕ КОНСТРУКЦИИ С НАЦЕЛИВАЮЩИМИ И ЭФФЕКТОРНЫМИ ЭЛЕМЕНТАМИ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2016 |
|
RU2703952C2 |
| СОСТАВНОЙ ПОЛИПЕПТИД, ИМЕЮЩИЙ МЕТАЛЛСВЯЗЫВАЮЩИЙ МОТИВ, И СОДЕРЖАЩАЯ ИХ МОЛЕКУЛЯРНАЯ КОНСТРУКЦИЯ | 2020 |
|
RU2814475C2 |
| МОЛЕКУЛЯРНЫЕ КОНСТРУКЦИИ С НАЦЕЛИВАЮЩИМИ И ЭФФЕКТОРНЫМИ ЭЛЕМЕНТАМИ | 2016 |
|
RU2696378C2 |
| ПРИМЕНЕНИЕ ДОЛГОДЕЙСТВУЮЩИХ ПЕПТИДОВ GLP-1 | 2013 |
|
RU2657573C2 |
| АНАЛОГИ ГЛЮКАГОНА, ОБЛАДАЮЩИЕ ПОВЫШЕННОЙ РАСТВОРИМОСТЬЮ И СТАБИЛЬНОСТЬЮ В БУФЕРАХ С ФИЗИОЛОГИЧЕСКИМИ ЗНАЧЕНИЯМИ Ph | 2009 |
|
RU2560254C2 |
| ПЕПТИДНАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ПРОПИЛЕНГЛИКОЛЬ, ЯВЛЯЮЩАЯСЯ ОПТИМАЛЬНОЙ ДЛЯ ИЗГОТОВЛЕНИЯ И ПРИМЕНЕНИЯ В ИНЪЕКЦИОННЫХ УСТРОЙСТВАХ | 2004 |
|
RU2831321C2 |
| АНАЛОГИ ОКСИНТОМОДУЛИНА | 2009 |
|
RU2542362C2 |
| ТВЕРДЫЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ АГОНИСТ GLP-1 И СОЛЬ N-(8-(2-ГИДРОКСИБЕНЗОИЛ)АМИНО)КАПРИЛОВОЙ КИСЛОТЫ | 2019 |
|
RU2804318C2 |
| ПЕПТИДЫ ГЛЮКАГОНОВОГО СУПЕРСЕМЕЙСТВА, ОБЛАДАЮЩИЕ АКТИВНОСТЬЮ ОТНОСИТЕЛЬНО ЯДЕРНЫХ ГОРМОНАЛЬНЫХ РЕЦЕПТОРОВ | 2011 |
|
RU2604067C2 |
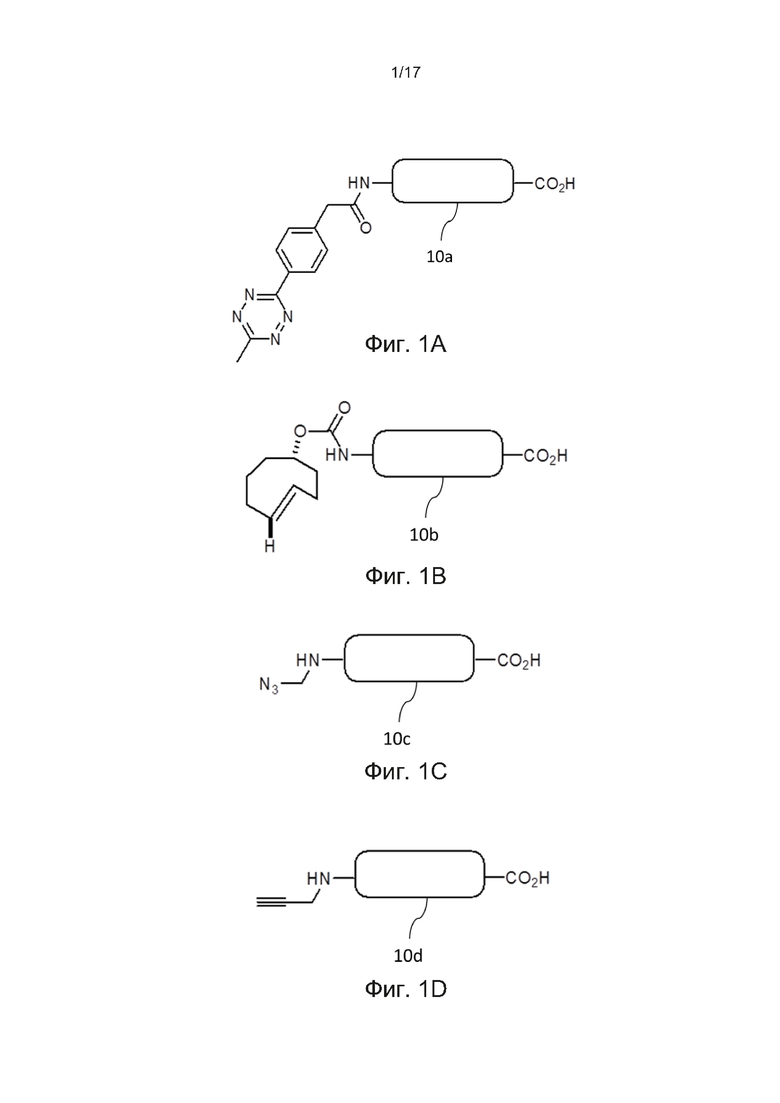
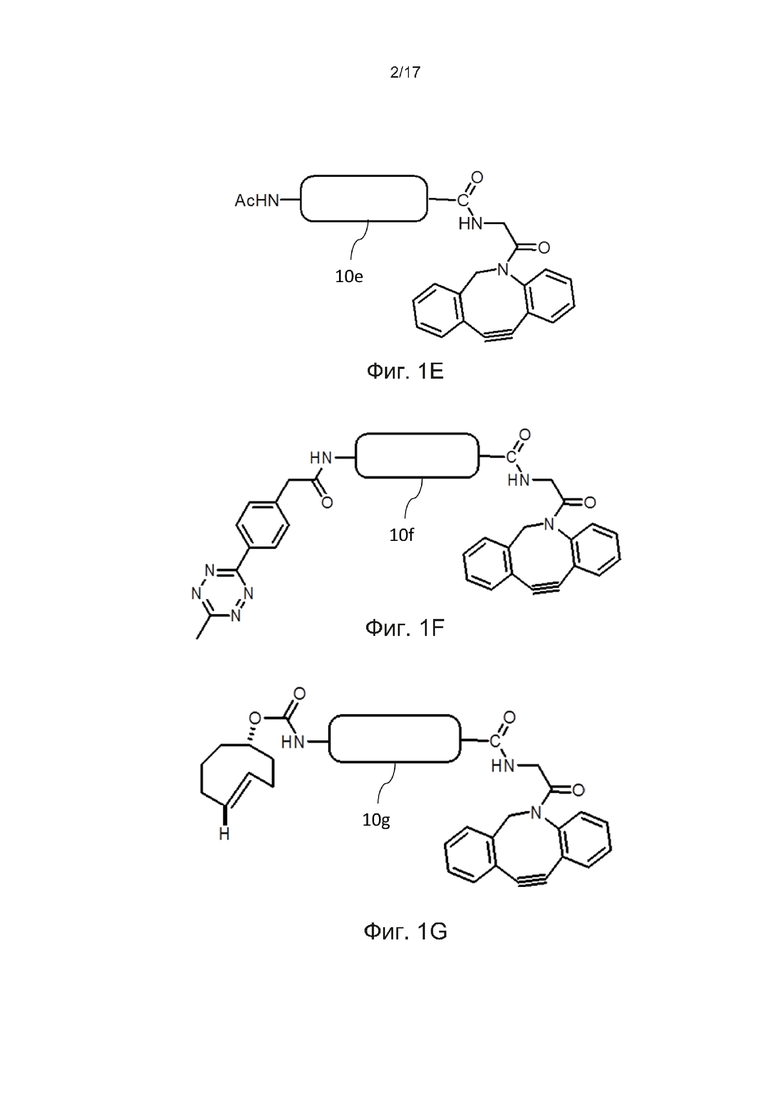
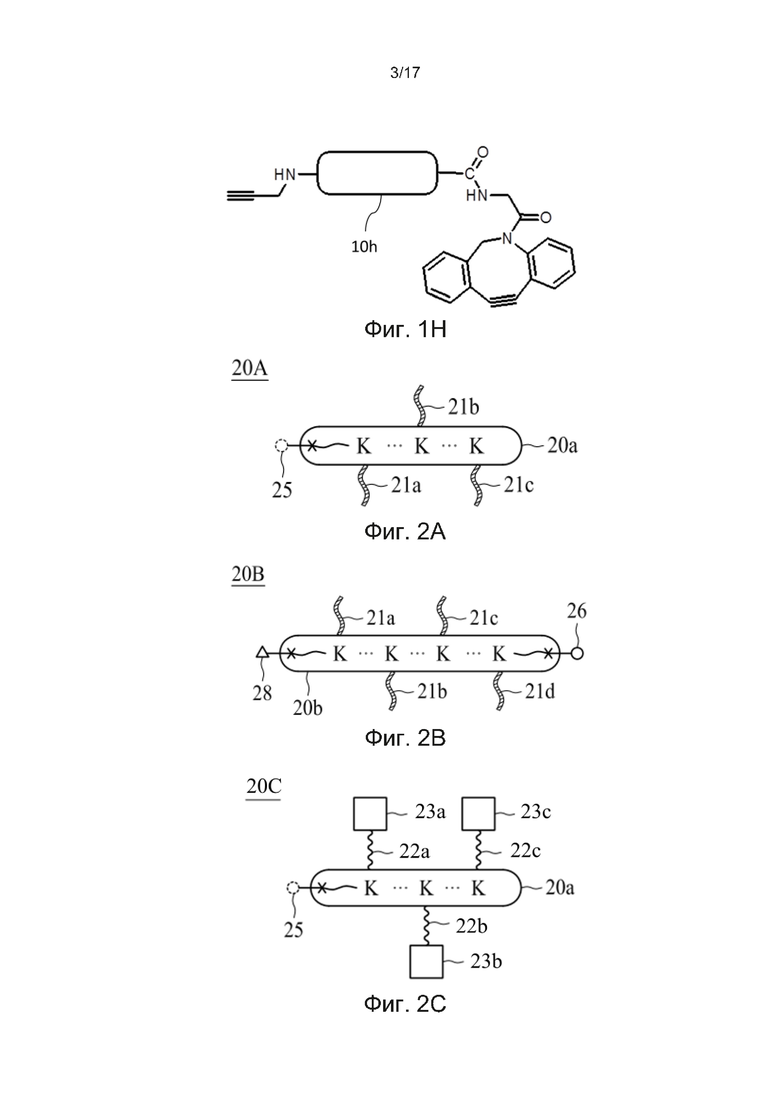
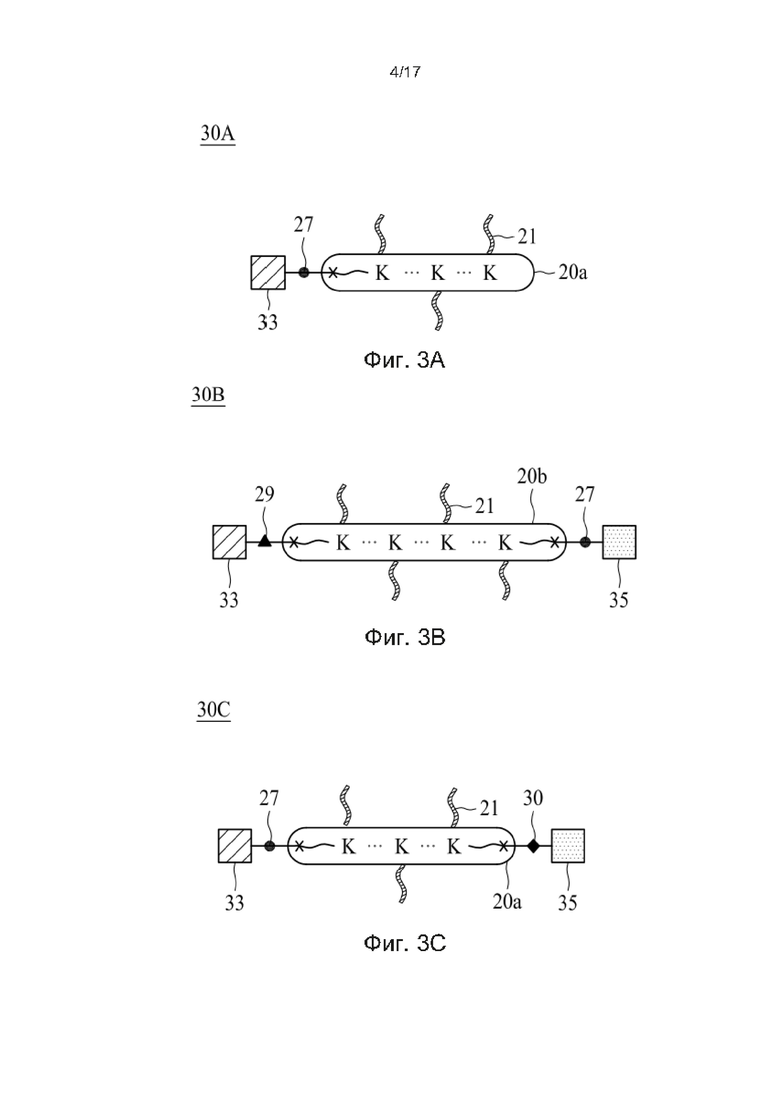
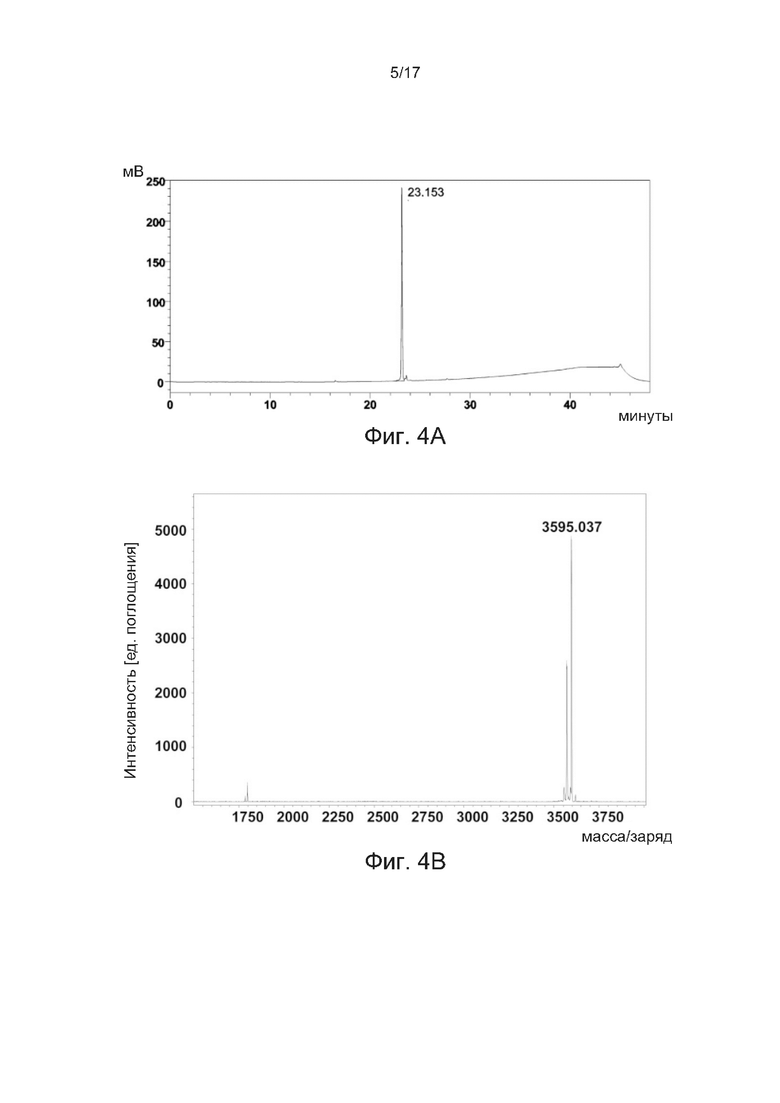
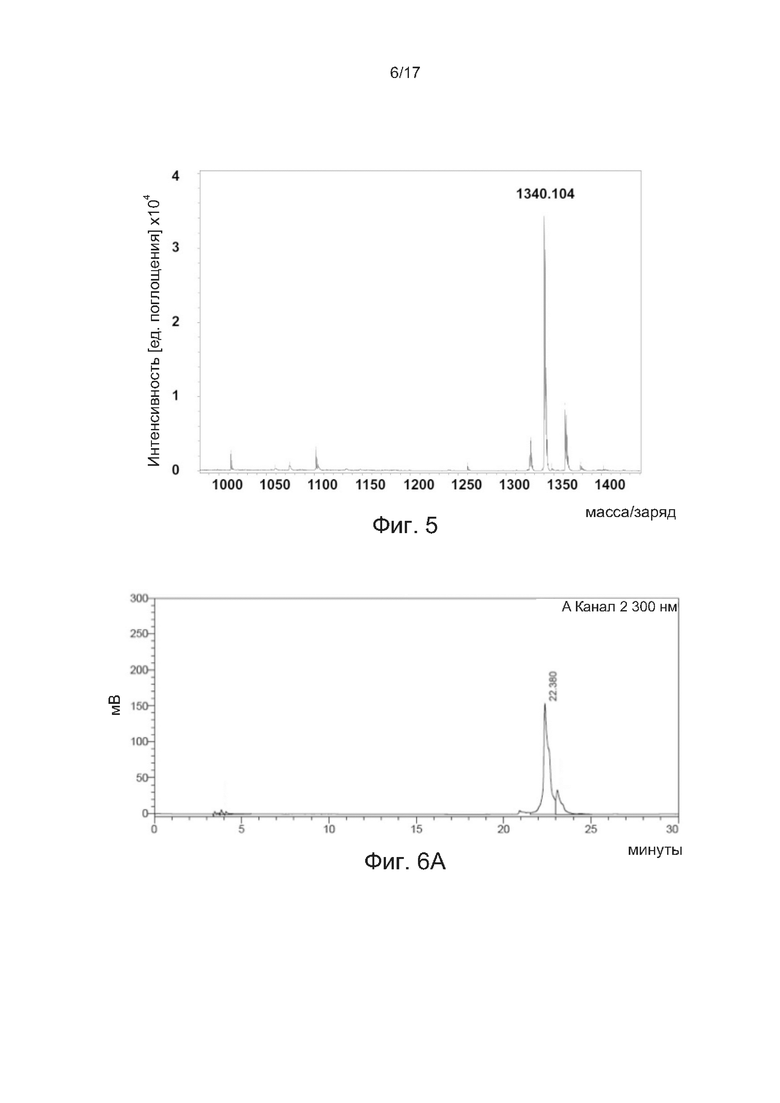
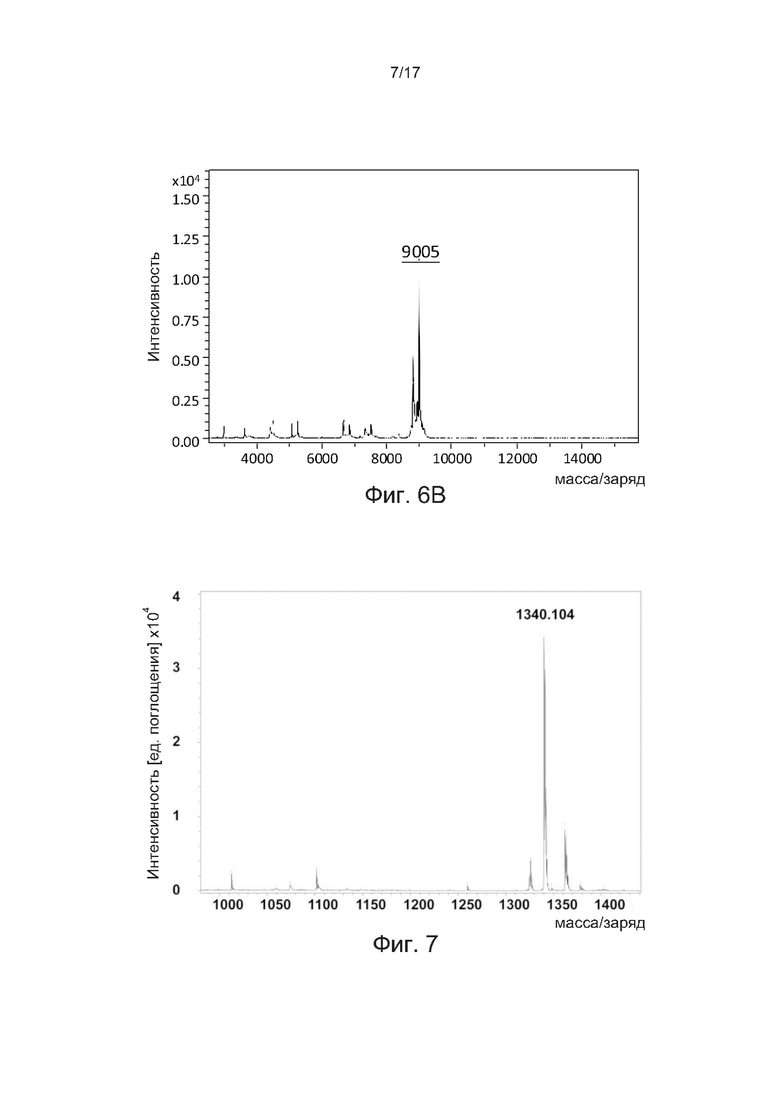
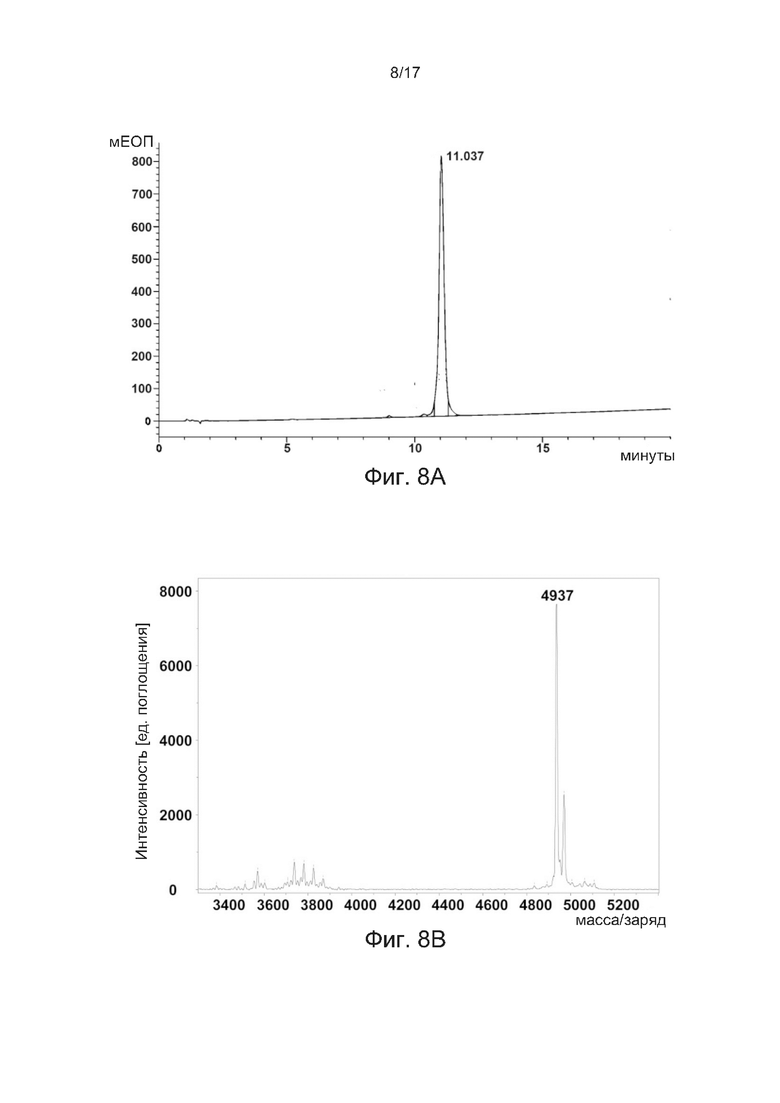
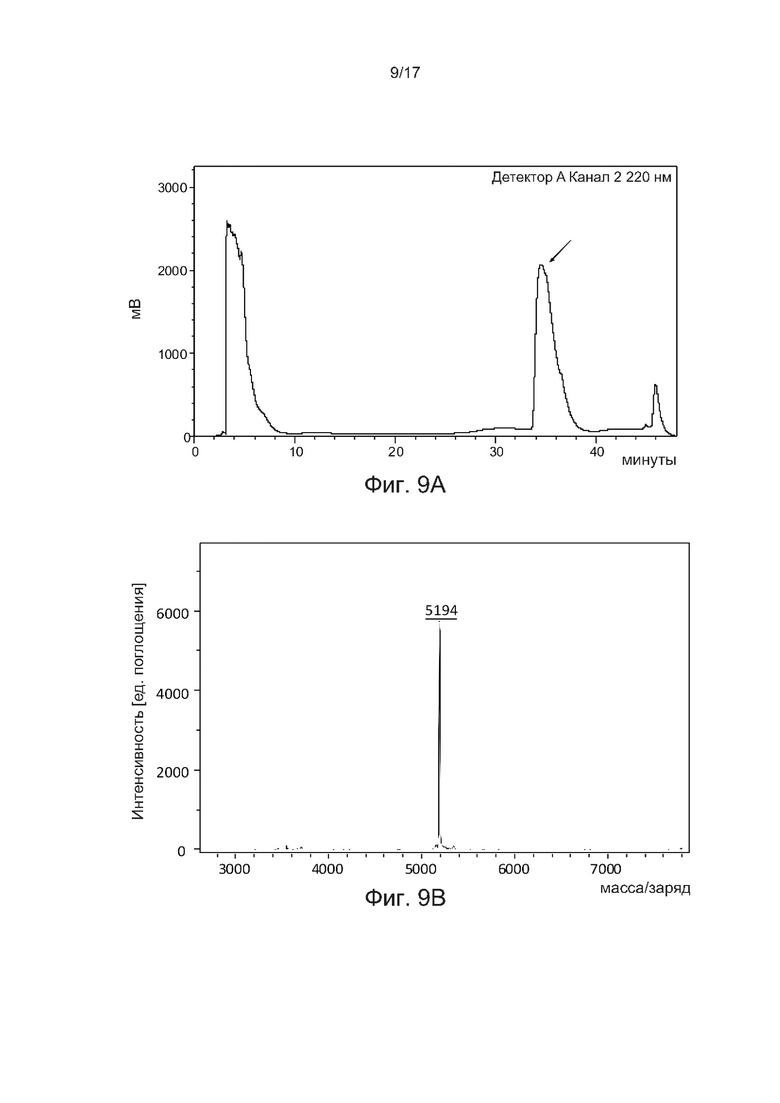
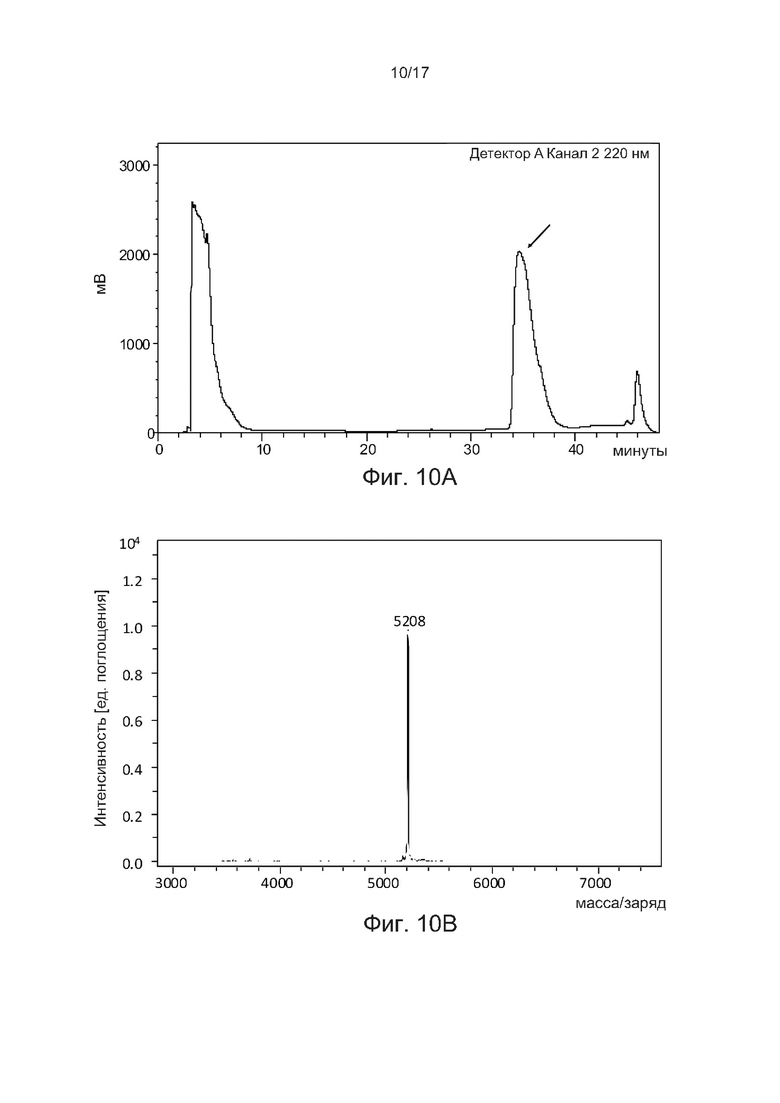
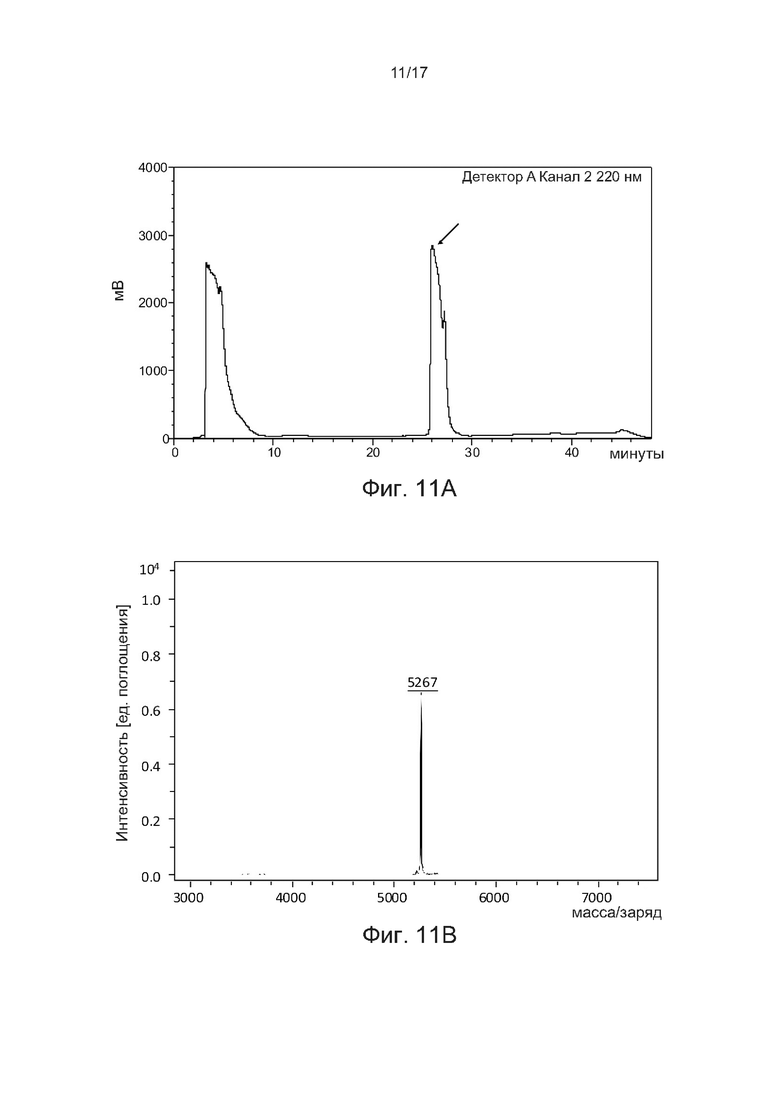
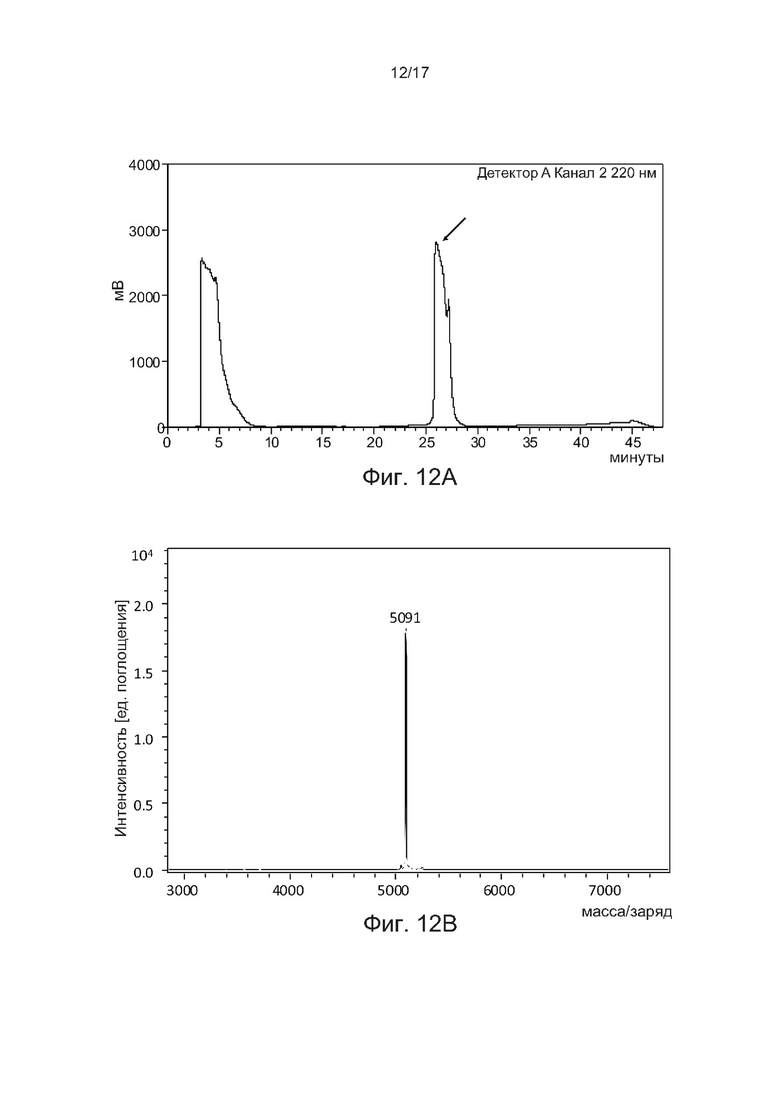
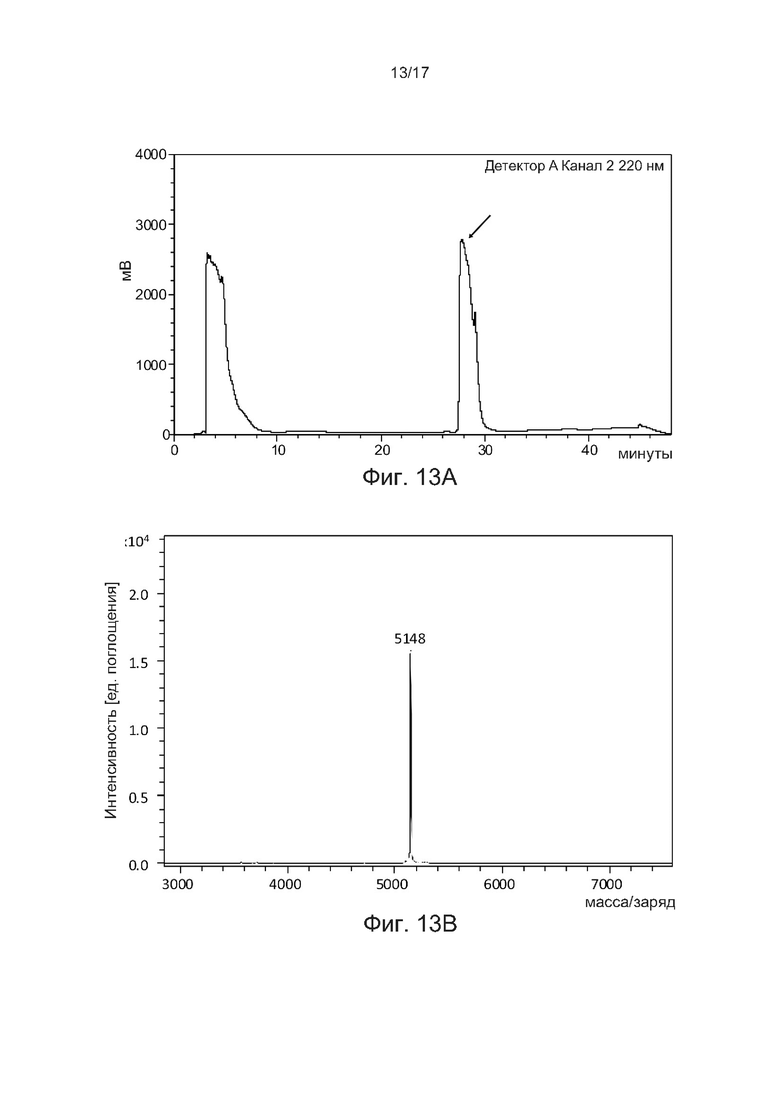
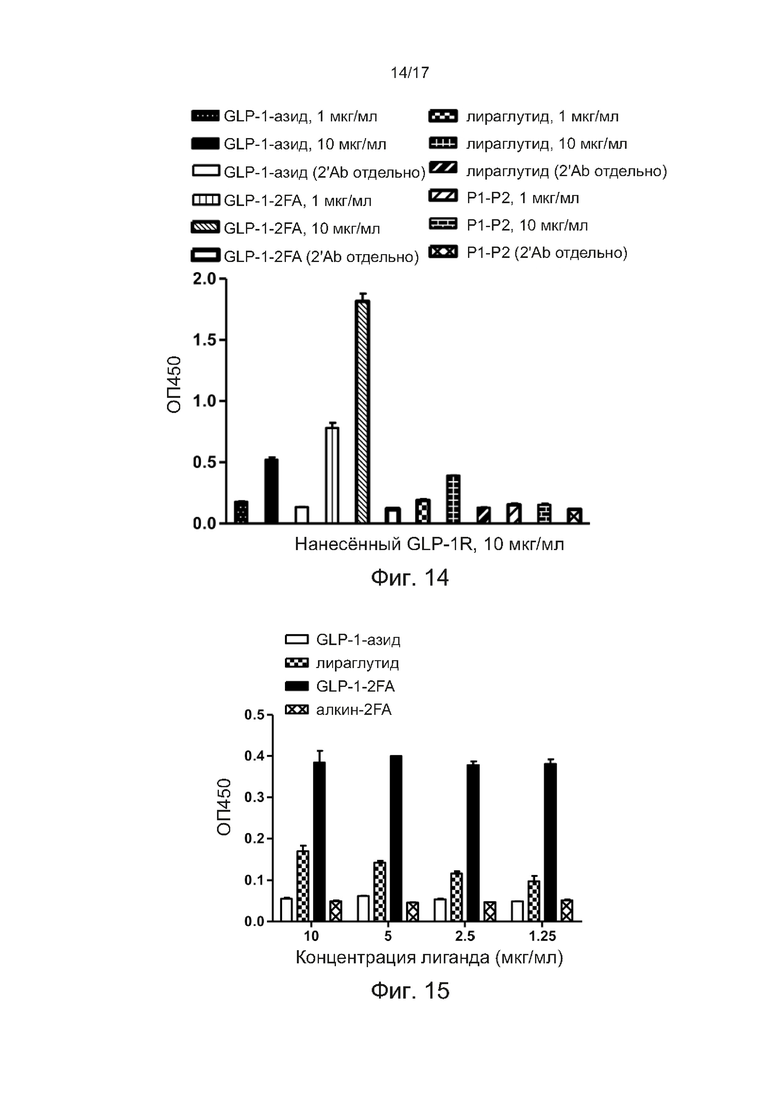
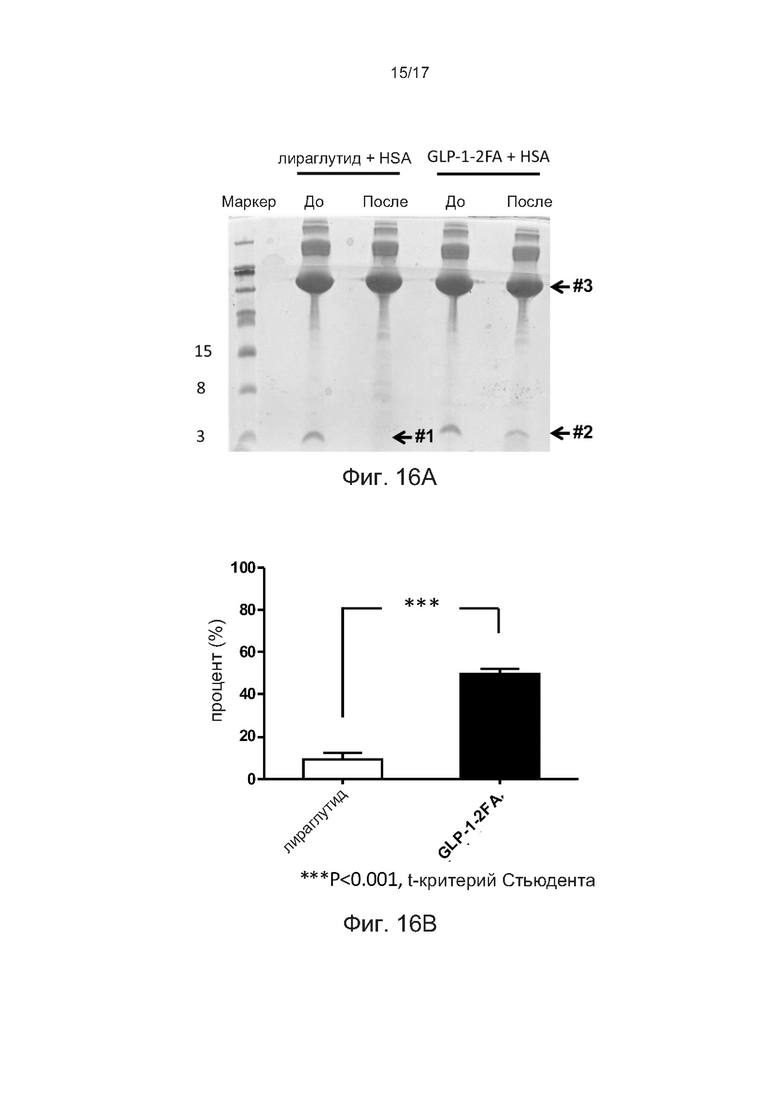
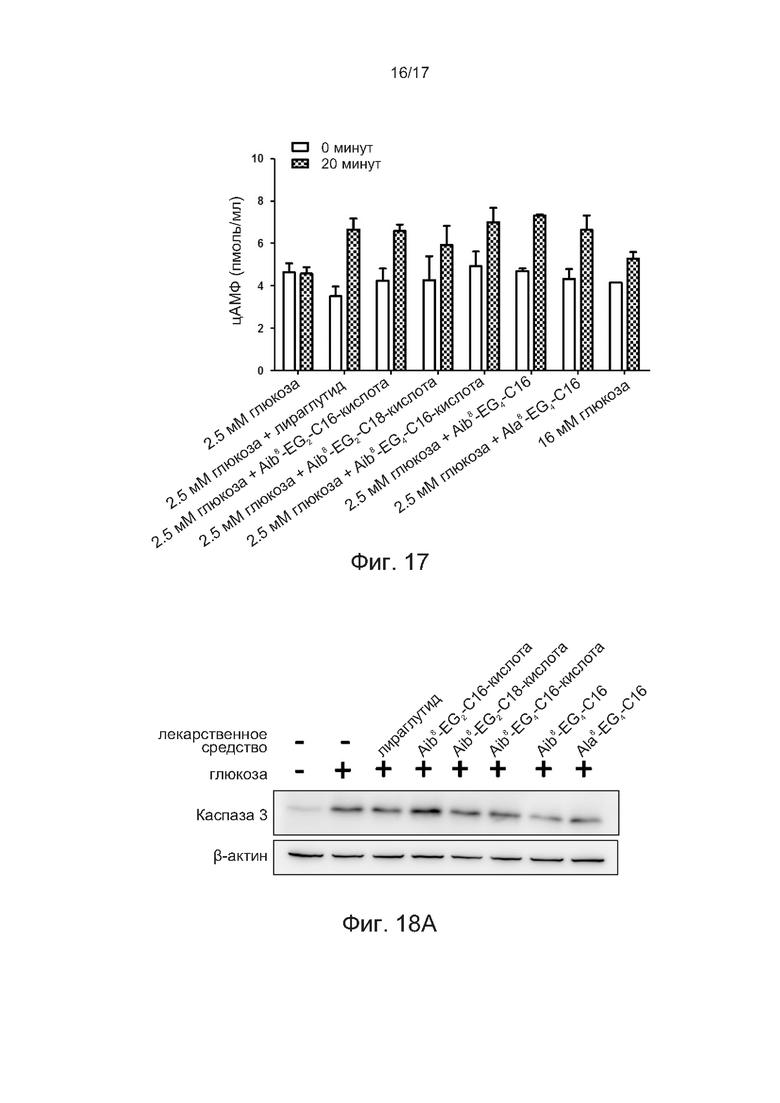
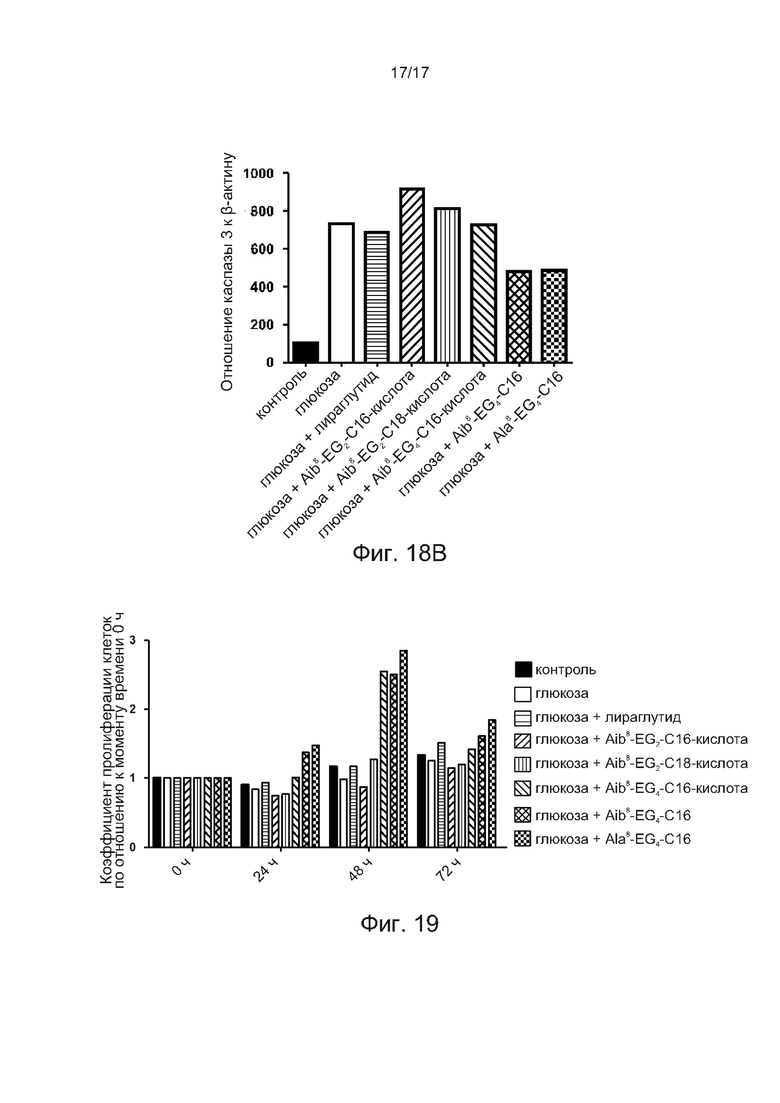
Изобретение относится к биотехнологии и представляет собой линкерную единицу, содержащую центральную основу и от 2 до 5 первых элементов, где каждый из первых элементов независимо представляет собой производное C16-20 жирной кислоты или производное C16-20 дикарбоновой жирной кислоты, и центральная основа содержит от 2 до 5 остатков лизина (K), где ε-аминогруппа остатка K ацилирована одним из первых элементов; необязательно, один или несколько наполнителей, где любые два из остатков K непосредственно следуют друг за другом или разделены наполнителем; необязательно, концевой спейсер, где концевые спейсеры представляют собой N-концевой спейсер, связанный с N-концом первого остатка K, или C-концевой спейсер, связанный с C-концом последнего остатка K; и каждый из наполнителей и концевых спейсеров независимо содержит (1) от 1 до 12 аминокислотных остатков, отличных от остатка K, или (2) пегилированную аминокислоту, имеющую от 1 до 12 повторов мономерных единиц этиленгликоля (EG); и конъюгирующий фрагмент, связанный с концевым остатком K, или, в случае присутствия концевого спейсера, концевым аминокислотным остатком концевого спейсера путем образования с ним амидной связи, где конъюгирующий фрагмент имеет конъюгирующую группу, выбранную из группы, состоящей из азидной, алкиновой, тетразиновой, циклооктеновой и циклооктиновой группы. Изобретение позволяет получить эффективно действующий линкер. 14 з.п. ф-лы, 19 ил, 21 пр.
1. Линкерная единица, содержащая центральную основу и от 2 до 5 первых элементов, где каждый из первых элементов независимо представляет собой производное C8-28 жирной кислоты или производное C8-28 дикарбоновой жирной кислоты, и центральная основа содержит:
от 2 до 5 остатков лизина (K), где ε-аминогруппа остатка K ацилирована одним из первых элементов;
необязательно, один или несколько наполнителей, где любые два из остатков K непосредственно следуют друг за другом или разделены наполнителем;
необязательно, концевой спейсер, где концевые спейсеры представляют собой N-концевой спейсер, связанный с N-концом первого остатка K, или C-концевой спейсер, связанный с C-концом последнего остатка K; и каждый из наполнителей и концевых спейсеров независимо содержит (1) от 1 до 12 аминокислотных остатков, отличных от остатка K, или (2) пегилированную аминокислоту, имеющую от 1 до 12 повторов мономерных единиц этиленгликоля (EG); и
конъюгирующий фрагмент, связанный с концевым остатком K, или, в случае присутствия концевого спейсера, концевым аминокислотным остатком концевого спейсера путем образования с ним амидной связи, где конъюгирующий фрагмент имеет конъюгирующую группу, выбранную из группы, состоящей из азидной, алкиновой, тетразиновой, циклооктеновой и циклооктиновой группы.
2. Линкерная единица по п. 1, где производное жирной кислоты получают из октановой кислоты, пеларгоновой кислоты, декановой кислоты, ундекановой кислоты, лауриновой кислоты, тридекановой кислоты, миристиновой кислоты, пентадекановой кислоты, пальмитиновой кислоты, маргариновой кислоты, стеариновой кислоты, нонадекановой кислоты, арахидиновой кислоты, геникозановой кислоты, бегеновой кислоты, трикозановой кислоты, лигноцериновой кислоты, пальмитолеиновой кислоты, олеиновой кислоты, линолевой кислоты, рицинолевой кислоты, вакценовой кислоты, эйкозапентаеновой кислоты (ЭПК) или докозагексановой кислоты (ДГК).
3. Линкерная единица по п. 2, где жирная кислота представляет собой производное миристиновой кислоты или пальмитиновой кислоты.
4. Линкерная единица по п. 1, где производное дикарбоновой жирной кислоты получают из субериновой кислоты, азелаиновой кислоты, себациновой кислоты, ундекандиовой кислоты, додекандиовой кислоты, брассиловой кислоты, тетрадекандиовой кислоты, пентадекандиовой кислоты, тапсиевой кислоты, гептадекандиовой кислоты или октадекандиовой кислоты.
5. Линкерная единица по п. 4, где производное дикарбоновой жирной кислоты представляет собой производное тетрадекандиовой кислоты или тапсиевой кислоты.
6. Линкерная единица по п. 1, где производное жирной кислоты или производное дикарбоновой жирной кислоты модифицировано остатком глутамата.
7. Линкерная единица по п. 1, дополнительно содержащая второй элемент, который связан с конъюгирующей группой при помощи катализируемой медью реакции азид-алкинового циклоприсоединения (CuAAC), реакции клик-химии активированных азида и алкина (SPAAC) или реакции Дильса-Алдера с обращенными электронными требованиями (iEDDA).
8. Линкерная единица по п. 7, где второй элемент выбран из группы, состоящей из инсулина, инсулиноподобного фактора роста, агониста глюкагоноподобного пептида-1, соматостатина и аналогов соматостатина, кальцитонина, гормона роста, эритропоэтина, гонадотропин-рилизинг-фактора, гранулоцитарного колониестимулирующего фактора, аденозиндеаминазы, аргининдеиминазы, аспарагиназы, интерферона-α, интерферона-β, растворимого рецептора ФНО-α, растворимого рецептора IL-1, растворимого рецептора EGF, агалсидазы β, агалсидазы α, ларонидазы, идурсульфазы, альглюкозидазы α и галсульфазы, или их производного или варианта.
9. Линкерная единица по п. 8, где аналог соматостатина представляет собой октреотид.
10. Линкерная единица по п. 7, где второй элемент представляет собой лекарственную группу, содержащую несколько молекул лекарственного средства.
11. Линкерная единица по п. 1, где циклооктеновая группа представляет собой норборнен или транс-циклооктен (TCO); и циклооктиновая группа представляет собой дибензоциклооктин (DBCO или DIBO), дифторированный циклооктин (DIFO), бициклононин (BCN) или дибензоазациклооктин (DIBAC).
12. Линкерная единица по п. 1, где тетразиновая группа представляет собой 1,2,3,4-тетразин, 1,2,3,5-тетразин или 1,2,4,5-тетразин или их производные.
13. Линкерная единица по п. 1, где азидная группа представляет собой пиколилазидную группу.
14. Линкерная единица по п. 1, где центральная основа содержит как N-концевой спейсер, так и C-концевой спейсер, и
когда конъюгирующая группа N-концевого спейсера представляет собой азидную, алкиновую или циклооктиновую группу; конъюгирующая группа C-концевого спейсера представляет собой тетразиновую или циклооктеновую группу; или
когда конъюгирующая группа N-концевого спейсера представляет собой тетразиновую или циклооктеновую группу, конъюгирующая группа C-концевого спейсера представляет собой азидную, алкиновую или циклооктиновую группу.
15. Линкерная единица по п. 1, дополнительно содержащая второй элемент и третий элемент, где
второй элемент связан с конъюгирующей группой N-концевого спейсера при помощи реакции азид-алкинового циклоприсоединения CuAAC или реакции клик-химии активированных азида и алкина SPAAC, а третий элемент связан с конъюгирующей группой C-концевого спейсера при помощи реакции Дильса-Алдера с обращенными электронными требованиями iEDDA; или
второй элемент связан с конъюгирующей группой N-концевого спейсера при помощи реакции Дильса-Алдера с обращенными электронными требованиями iEDDA, а третий элемент связан с конъюгирующей группой C-концевого спейсера при помощи реакции азид-алкинового циклоприсоединения CuAAC или реакции клик-химии активированных азида и алкина SPAAC.
| WO2016112870 A1, 21.07.2016 | |||
| ZORZI A et al., Acylated heptapeptide binds albumin with high affinity and application as tag furnishes long-acting peptides, Nat Commun | |||
| Автомобиль-сани, движущиеся на полозьях посредством устанавливающихся по высоте колес с шинами | 1924 |
|
SU2017A1 |
| RU2073011, 10.02.1997 | |||
| Фильтр для очистки нефти | 1925 |
|
SU2201A1 |
Авторы
Даты
2021-08-24—Публикация
2018-09-19—Подача