Изобретение относится к области медицинской химии и касается аминокислотных аналогов противоопухолевого антибиотика ребеккамицина. До настоящего времени сохраняется интерес к производным ребеккамицина как потенциальным противоопухолевым средствам, имеющим в том числе иммуномодулирующую активность [Экспериментальная онкология на рубеже веков. - 2003. - С. 281-294; Pindur U., Kim Y.S. et al. // Biochemistry. - 1999. - V. 38. - №. 21. - P. 8605-8611; Prudhomme M. // Current medicinal chemistry. - 2000. - V. 7. - №. 12. - P. 1189-1212; Prudhomme M. // European journal of medicinal chemistry. - 2003. - V. 38. - №. 2. - P. 123-140; Civenni G., Longoni N., et al. // Molecular Cancer Therapeutics. - 2016. - V. 15, - №. 5. - P. 806-8181].
Прототипом для заявляемого изобретения является способ получения китайскими авторами аналогов ребеккамицина N6-аминокислотных N12-β-D-глюкопиранозидов 5,7,12,13-тетрагидро-6Н-индоло[2,3-а]пирроло[3,4-с]карбазол-5,7-диона путем взаимодействия глюкозида индолофуранокарбазола с аминокислотой в диметилформамиде в течение часа при 150°С [CN 102125578А, 24.11.2010]. Для производного 2-[12-β-D-глюкопиранозил-5,7,12,13-тетрагидро-6Н-индоло[2,3-а]пирроло[3,4-с]карбазол-5,7-диона-6-ил]-3-фенилпропановой кислоты в тестах in vitro в концентрации 0,4⋅10-4 М отмечено 40% торможения роста клеток лейкоза К562; результатов изучения противоопухолевой активности in vivo N6-аминокислотных N12-β-D-глюкопиранозидов 5,7,12,13-тетрагидро-6Н-индоло[2,3-а]пирроло[3,4-с]карбазол-5,7-диона китайские авторы не привели.
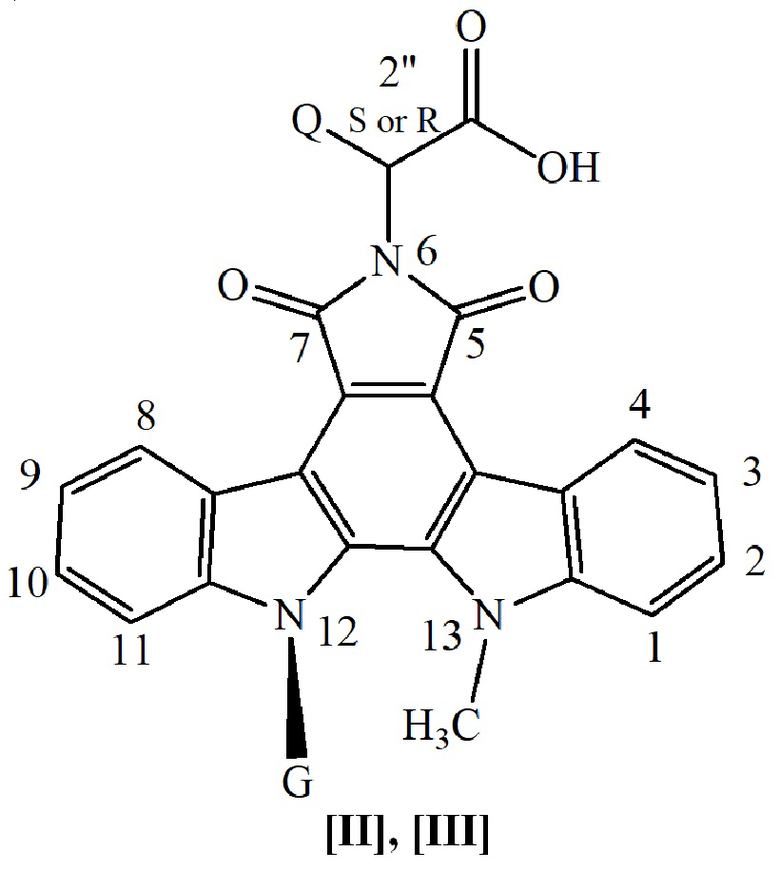
Способ получения аминокислотных аналогов противоопухолевого антибиотика ребеккамицина - производных N13-метил-{N12-β-D-ацилгликозил-5,7,12,13-тетрагидро-6Н-индоло[2,3-а]пирроло[3,4-с]карбазол-5,7-диона} формул [II], [III]
где G равно соответственно:
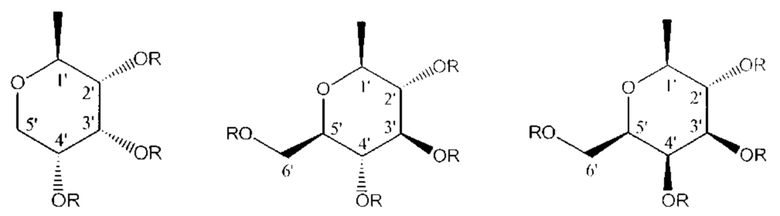
R=Ac для соединений формулы [II] и R=H для соединений формулы [III], n=3,4;
Q = боковая цепь аминокислоты, выбрана из -Н, -СН3 (2S или 2R), -СН(СН3)2 (2S или 2R), -СН2-ОН (2S или 2R), -СН(ОН)-СН3 (2S или 2R), -СН2-С6Н5 (2S или 2R), -СН2-р-С6Н4ОН (2S), -(СН2)2-S-CH3 (2S или 2R), -(СН2)2-SOCH3 (2S или 2R) -(СН2)2-СООН (2S), -(CH2)3-C(=NH)-NH(-NO2) (2S), -(CH2)4-NH-CO-O-CH2-C6H5 (2S), -CH2-Ind (2S или 2R).
Способ заключается в том, что соответствующий пер-О-ацетилированный N12-D-рибопиранозид, или N12-β-D-глюкопиранозид, или N12-β-D-галактопиранозид N13-метил-5,7,12,13-тетрагидро-6Н-индоло[2,3-а]фурано[3,4-с]карбазол-5,7-диона [I], синтезированный исходя из индолина по методике авторов [Мельник С.Я., Бахмедова А.А. и др. // Биоорганическая химия. - 1996. - Т. 22. - №6. - С. 458-467; Бахмедова А.А., Гараева Л.Д. и др. // Биоорганическая химия. - 1997. - Т. 23. - №8. - С. 667-6741
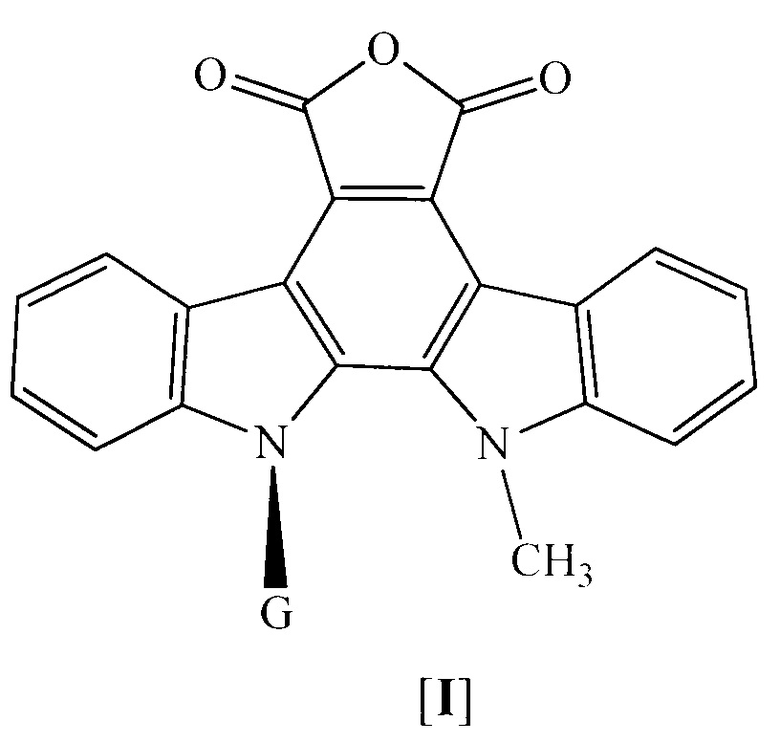
кипятят в сухом пиридине с аминокислотой в присутствии 3 молей хлоргидрата пиридина в течение 7-12 часов с контролем прохождения реакции по данным ТСХ на силуфоле; для направленного прохождения реакции в предложенных условиях требуется защита только азотсодержащих фрагментов боковой цепи Q аргинина (NO2/Arg) и лизина (Cbz/Lys); по окончании реакции пиридин упаривают, остаток кристаллизуют водой, затем методами экстракции и жидкостной хроматографией на силикагеле выделяют образовавшиеся N6-аминокислотные производные формулы [II]: пер-О-ацетилированные N12-β-D-рибопиранозиды, или N12-β-D-глюкопиранозиды, или N12-β-D-галактопиранозиды 5,7,12,13-тетрагидро-6Н-индоло[2,3-а]пирроло[3,4-с]карбазол-5,7-диона;
дезацетилирование углеводного остатка проводят действием безводного поташа в метаноле на ацетилгликозид формулы [II], фиксируют окончание реакции по данным ТСХ на силуфоле, затем добавляют воду до растворения осадка, вносят в раствор катеонит (Н+) до рН 5, смывают водой со смолы и упаривают досуха реакционную смесь; жидкостной хроматографией на силикагеле выделяют N6-аминокислотные производные формулы [III]: N12-β-D-рибопиранозиды, или N12-β-D-глюкопиранозиды, или N12-β-D-галактопиранозиды N13-метил-5,7,12,13-тетрагидро-6Н-индоло[2,3-а]пирроло[3,4-с]карбазол-5,7-диона.
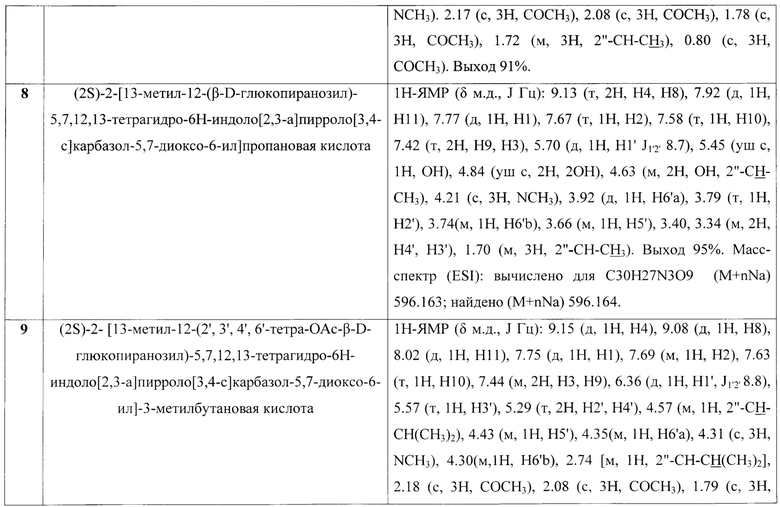
В таблице представлены характеристики полученных в ходе осуществления данного способа синтеза N6-аминокислотных производных N12-гликозидов N13-метил-5,7,12,13-тетрагидро-6Н-индоло[2,3-а]пирроло[3,4-с]карбазола [II], [III].
Структуры полученных производных подтверждены данными спектров 1Н-ЯМР и масс-спектров высокого разрешения ESI. Спектры 1Н-ЯМР записаны на приборе Bruker DRX-500 с программным обеспечением, внутренний стандарт - тетраметилсилан, химические сдвиги δ в DMSO-d6 (в отдельном случае в CDCl3) приведены в миллионных долях (м.д.), значения констант спин-спинового взаимодействия J1'2' приведены в герцах. Масс-спектры высокого разрешения зарегистрированы на приборе Bruker micrOTOF II методом электрораспылительной ионизации (ESI). Измерения выполнены на положительных (напряжение на капилляре 4500 V) или отрицательных (напряжение на капилляре 3200 V) ионах. Диапазон сканирования масс- m/z 50-3000Д, калибровка - внешняя или внутренняя (Electrospray Calibrant Solution, Fluka). Использовался шприцевой ввод вещества для растворов в воде или ацетонитриле, скорость потока - 3 мкл/мин. Газ-распылитель - азот (4 л/мин.), температура интерфейса - 180°С. Экспертный анализ сделан на основании наложения на экспериментальный спектр масс-спектров, рассчитанных математически по заданной формуле, учитывая совпадение экспериментальных значений для данного соединения с расчетными (M+nH), (M+nNa) и (М+nK). За ходом реакций следили с помощью тонкослойной хроматографии (ТСХ) на силуфоле (Silufol UV254) в системах бензол-этилацетат-этанол 50:25:1; 25:25:3; хлороформ-этанол 4:1; 5:3; 1:1. Жидкостную флеш-хроматографию на силикагеле L 5/40 мкм (Chemapol) проводили, используя градиент смеси растворителей хлороформ-ацетон 1:19 → 1:4; хлороформ-этанол 1:9 → 1:4.






























Биологические испытания N6-аминокислотных производных N12-гликозидов индоло[2,3-а]пирроло[3,4-с]карбазол-5,7-диона (АПГИК, представлены без расшифровки способа получения данных соединений), предваряли тесты in silico [Апрышко Г.Н. // Российский биотерапевтический журнал. - 2017. - Т. 16. - №4. - С. 46-541 с помощью прогностической программы PASS [Filimonov D.A. et al. // Chemistry of Heterocyclic Compounds. - 2014. - V. 50. - №. 3. - P. 483-499], в которых была определена низкая (диапазон 3-48%) вероятность цитотоксической активности рассмотренных соединений при высокой (57-75%) вероятности для них противоопухолевого эффекта. В этой же работе представлены данные изучения цитотоксической активности указанных соединений in vitro на клетках линий рака яичников SKOV3, карциномы молочной железы MCF7 и SKBR3, рака толстой кишки LS174T и НСТ116; в результате низкий показатель цитотоксической активности IC50>10 мкМ был подтвержден в МТТ-тесте и коррелировал с прогнозом in silico. В то же время компьютерный прогноз значимой вероятности противоопухолевой активности этих нуклеозидов был подтвержден результатами опытов на перевиваемых опухолях мышей in vivo в отношении гормонозависимых опухолей рака шейки матки РШМ-5 и аденокарциномы молочной железы Са-755. [Голубева И.С., Горюнова О.В. и др. // Российский биотерапевтический журнал. - 2018. - Т. 17. - №2. - С. 71-77; Golubeva I.S., Goryunova Q.V. // MedChem Russia - 2019. - 10.06.2019. - P. 3491. На опухоли РШМ-5 в дозе 100 мг/кг при внутрибрюшинном пятикратном введении каждые 24 часа все изученные соединения показали эффект торможения роста опухоли ТРО выше 52% до 12-го дня после окончания лечения. Производное L-треонина было изучено на опухоли рака шейки матки РШМ-5 в дозе 100 мг/кг, значения ТРО 84-58% наблюдались до 29 дня по окончании лечения без гибели животных.
| название | год | авторы | номер документа |
|---|---|---|---|
| Производное класса N-гликозидов индоло[2,3-а]пирроло[3,4-с]карбазол-5,7-дионов - N-{ 12-(β-D-ксилопиранозил)-5,7-диоксо-индоло[2,3-а]пирроло[3,4-с] карбазол-6-ил} пиридин-2-карбоксамид, обладающее цитотоксической и противоопухолевой активностью | 2017 |
|
RU2667906C1 |
| ПРОИЗВОДНЫЕ ИНДОЛОКАРБАЗОЛОВ, БЛОКИРУЮЩИЕ ВАСКУЛОГЕННУЮ МИМИКРИЮ В ОПУХОЛИ | 2014 |
|
RU2557554C1 |
| N-ГЛИКОЗИДЫ ИНДОЛО[2,3-a]ПИРРОЛО[3,4-c]КАРБАЗОЛОВ, ОБЛАДАЮЩИЕ ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ | 2014 |
|
RU2548045C1 |
| Средство для терапии опухолей | 2019 |
|
RU2726801C1 |
| СПОСОБ ПОЛУЧЕНИЯ N-ГЛИКОЗИДОВ ИНДОЛО[2,3-а]ПИРРОЛО[3,4-с]КАРБАЗОЛ-5,7-ДИОНОВ, ОБЛАДАЮЩИХ ЦИТОТОКСИЧЕСКОЙ И ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ | 2009 |
|
RU2427585C9 |
| ПРОТИВООПУХОЛЕВОЕ ЛЕКАРСТВЕННОЕ СРЕДСТВО ИНГИБИТОР ТОПОИЗОМЕРАЗЫ I | 2022 |
|
RU2786727C1 |
| ПРОТИВООПУХОЛЕВОЕ СРЕДСТВО | 2014 |
|
RU2572691C1 |
| ИНДОЛОПИРРОЛОКАРБАЗОЛЬНЫЕ ПРОИЗВОДНЫЕ САХАРОВ, СОДЕРЖАЩАЯ ИХ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ИНГИБИРОВАНИЯ РОСТА ОПУХОЛЕЙ | 1997 |
|
RU2167880C2 |
| ПРОИЗВОДНЫЕ ГЛИКОЗИДОВ ИНДОЛО[2,3-А]ПИРРОЛО[3,4-С]КАРБАЗОЛ-5,7-ДИОНОВ, ОБЛАДАЮЩИЕ ЦИТОТОКСИЧЕСКОЙ И ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ | 2003 |
|
RU2255089C1 |
| ПРОИЗВОДНЫЕ ИНДОЛОКАРБАЗОЛИМИДА, СМЕСЬ ИХ ИЗОМЕРОВ И ИХ СОЛИ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ С АКТИВНОСТЬЮ, ИНГИБИРУЮЩЕЙ ПРОТЕИНКИНАЗУ C ИЛИ КИНАЗУ ЛЕГКОЙ МИОЗИНОВОЙ ЦЕПИ ИЛИ ПОДАВЛЯЮЩЕЙ ИММУННЫЕ РЕАКЦИИ | 1993 |
|
RU2126007C1 |
Изобретение относится к способу получения аминокислотных аналогов противоопухолевого антибиотика ребеккамицина – производных N13-метилиндоло[2,3-а]пирроло[3,4-с]карбазол-5,7-диона формул [II] и [III], содержащих при N13-атоме азота гетероцикла метильную группу, при N12-атоме азота гетероцикла углеводные остатки пяти- или шестичленных сахаров и, независимо, остатки S- или R-аминокислот при N6 атоме азота гетероцикла. В формулах [II] и [III] G равно соответственно 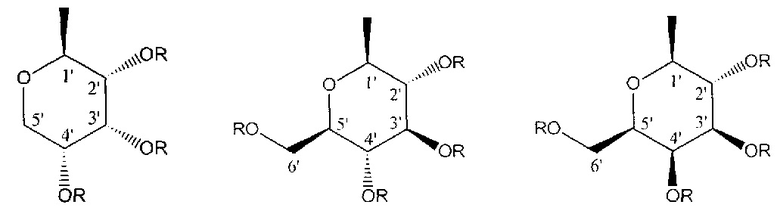 , R=Ac для соединений формулы [II] и R=H для соединений формулы [III]; n=3, 4; Q - боковая цепь аминокислоты, выбранная из -Н, -СН3 (2S или 2R), -СН(СН3)2 (2S или 2R), -СН2-ОН (2S или 2R), -CH(OH)-CH3(2S или 2R), -СН2-С6Н5 (2S или 2R), -СН2-р-С6Н4ОН (2S), -(СН2)2 -S-CH3 (2S или 2R), -(CH2)2-SOCH3 (2S или 2R) -(CH2)2-COOH (2S), -(CH2)3-C(=NH)-NH(-NO2) (2S), -(CH2)4-NH-CO-O-CH2-C6H5(2S), -CH2-Ind (2S или 2R, Ind – боковая цепь триптофана). Способ заключается в том, что соответствующий пер-О-ацетилированный N12-β-D-рибопиранозид индоло[2,3-а]фурано[3,4-с]карбазол-5,7-диона, или пер-О-ацетилированный N12-β-D-глюкопиранозид индоло[2,3-а]фурано[3,4-с]карбазол-5,7-диона, или пер-О-ацетилированный N12-β-D-галактопиранозид индоло[2,3-а]фурано[3,4-с]карбазол-5,7-диона формулы [I] кипятят в сухом пиридине с аминокислотой в присутствии 3 молей хлоргидрата пиридина в течение 7-12 часов с контролем прохождения реакции по данным ТСХ на силуфоле; для направленного прохождения реакции в предложенных условиях требуется защита только азотсодержащих фрагментов боковой цепи Q аргинина (NO2/Arg) и лизина (Cbz/Lys), по окончании реакции пиридин упаривают, остаток кристаллизуют водой, затем методами экстракции и жидкостной хроматографией на силикагеле выделяют образовавшиеся N6-аминокислотные производные формулы [II]: пер-О-ацетилированные N12-β-D-рибопиранозиды, или N12-β-D-глюкопиранозиды, или N12-β-D-галактопиранозиды индоло[2,3-а]пирроло[3,4-с]карбазол-5,7-диона. Дезацетилирование углеводного остатка проводят действием безводного поташа в метаноле на ацетилгликозид формулы [II], фиксируют окончание реакции по данным ТСХ на силуфоле, затем добавляют воду до растворения осадка, вносят в раствор катионит (Н+) до рН 5, смывают водой со смолы и упаривают досуха реакционную смесь; жидкостной хроматографией на силикагеле выделяют N6-аминокислотные производные формулы [III]: N12-β-D-рибопиранозиды, или N12-β-D-глюкопиранозиды, или N12-β-D-галактопиранозиды индоло[2,3-а]пирроло[3,4-с]карбазол-5,7-диона. 1 табл.
, R=Ac для соединений формулы [II] и R=H для соединений формулы [III]; n=3, 4; Q - боковая цепь аминокислоты, выбранная из -Н, -СН3 (2S или 2R), -СН(СН3)2 (2S или 2R), -СН2-ОН (2S или 2R), -CH(OH)-CH3(2S или 2R), -СН2-С6Н5 (2S или 2R), -СН2-р-С6Н4ОН (2S), -(СН2)2 -S-CH3 (2S или 2R), -(CH2)2-SOCH3 (2S или 2R) -(CH2)2-COOH (2S), -(CH2)3-C(=NH)-NH(-NO2) (2S), -(CH2)4-NH-CO-O-CH2-C6H5(2S), -CH2-Ind (2S или 2R, Ind – боковая цепь триптофана). Способ заключается в том, что соответствующий пер-О-ацетилированный N12-β-D-рибопиранозид индоло[2,3-а]фурано[3,4-с]карбазол-5,7-диона, или пер-О-ацетилированный N12-β-D-глюкопиранозид индоло[2,3-а]фурано[3,4-с]карбазол-5,7-диона, или пер-О-ацетилированный N12-β-D-галактопиранозид индоло[2,3-а]фурано[3,4-с]карбазол-5,7-диона формулы [I] кипятят в сухом пиридине с аминокислотой в присутствии 3 молей хлоргидрата пиридина в течение 7-12 часов с контролем прохождения реакции по данным ТСХ на силуфоле; для направленного прохождения реакции в предложенных условиях требуется защита только азотсодержащих фрагментов боковой цепи Q аргинина (NO2/Arg) и лизина (Cbz/Lys), по окончании реакции пиридин упаривают, остаток кристаллизуют водой, затем методами экстракции и жидкостной хроматографией на силикагеле выделяют образовавшиеся N6-аминокислотные производные формулы [II]: пер-О-ацетилированные N12-β-D-рибопиранозиды, или N12-β-D-глюкопиранозиды, или N12-β-D-галактопиранозиды индоло[2,3-а]пирроло[3,4-с]карбазол-5,7-диона. Дезацетилирование углеводного остатка проводят действием безводного поташа в метаноле на ацетилгликозид формулы [II], фиксируют окончание реакции по данным ТСХ на силуфоле, затем добавляют воду до растворения осадка, вносят в раствор катионит (Н+) до рН 5, смывают водой со смолы и упаривают досуха реакционную смесь; жидкостной хроматографией на силикагеле выделяют N6-аминокислотные производные формулы [III]: N12-β-D-рибопиранозиды, или N12-β-D-глюкопиранозиды, или N12-β-D-галактопиранозиды индоло[2,3-а]пирроло[3,4-с]карбазол-5,7-диона. 1 табл.
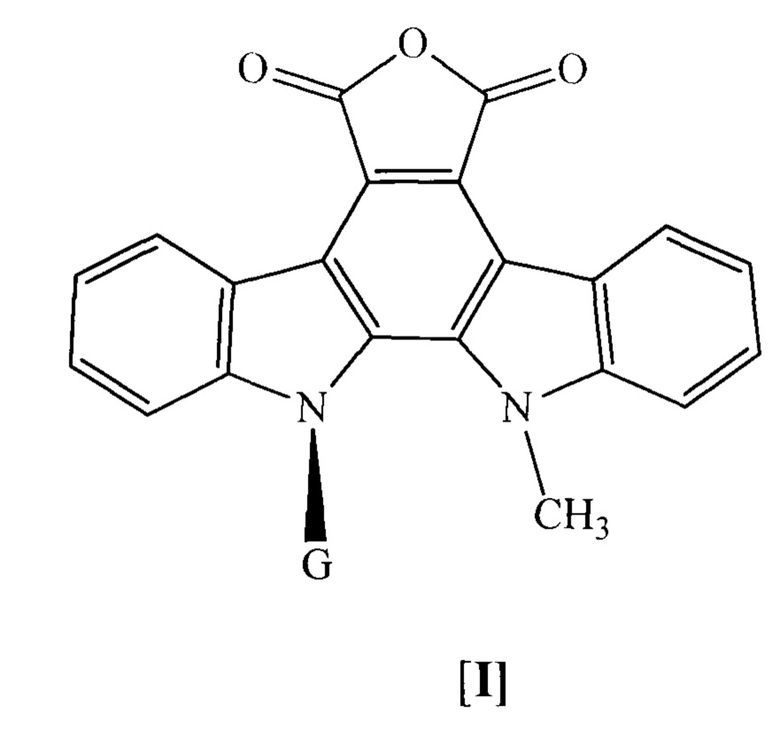
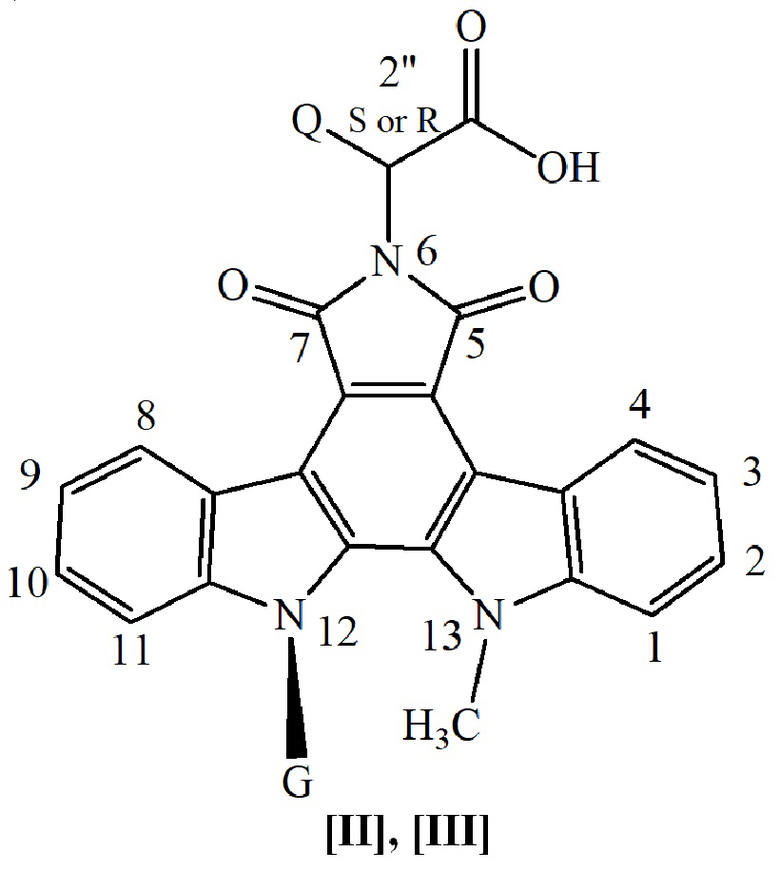
Способ получения аминокислотных аналогов противоопухолевого антибиотика ребеккамицина – производных N13-метилиндоло[2,3-а]пирроло[3,4-с]карбазол-5,7-диона формул [II] и [III], содержащих при N13-атоме азота гетероцикла метильную группу, при N12-атоме азота гетероцикла углеводные остатки пяти- или шестичленных сахаров и, независимо, остатки S- или R-аминокислот при N6 атоме азота гетероцикла
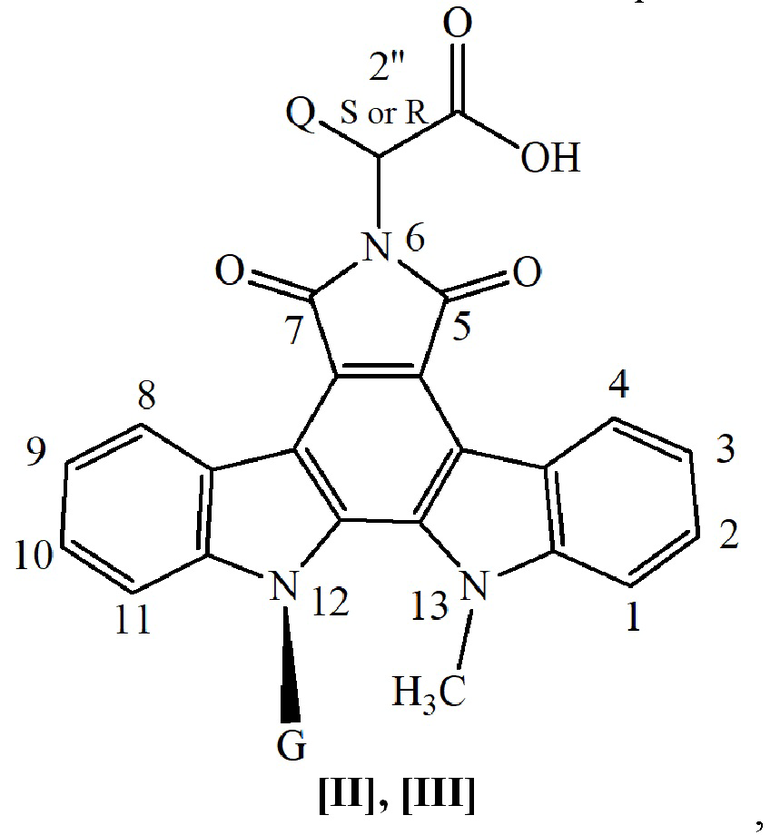
где G равно соответственно
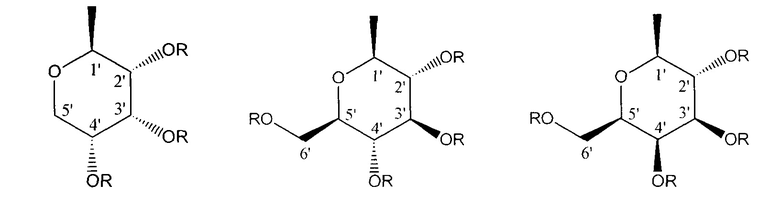 ,
,
R=Ac для соединений формулы [II] и R=H для соединений формулы [III], n=3, 4;
Q - боковая цепь аминокислоты, выбранная из -Н, -СН3 (2S или 2R), -СН(СН3)2 (2S или 2R), -СН2-ОН (2S или 2R), -CH(OH)-CH3(2S или 2R), -СН2-С6Н5 (2S или 2R), -СН2-р-С6Н4ОН (2S), -(СН2)2 -S-CH3 (2S или 2R), -(CH2)2-SOCH3 (2S или 2R) -(CH2)2-COOH (2S), -(CH2)3-C(=NH)-NH(-NO2) (2S), -(CH2)4-NH-CO-O-CH2-C6H5(2S), -CH2-Ind (2S или 2R, Ind – боковая цепь триптофана), заключающийся в том, что соответствующий пер-О-ацетилированный N12-β-D-рибопиранозид индоло[2,3-а]фурано[3,4-с]карбазол-5,7-диона, или пер-О-ацетилированный N12-β-D-глюкопиранозид индоло[2,3-а]фурано[3,4-с]карбазол-5,7-диона, или пер-О-ацетилированный N12-β-D-галактопиранозид индоло[2,3-а]фурано[3,4-с]карбазол-5,7-диона формулы [I]
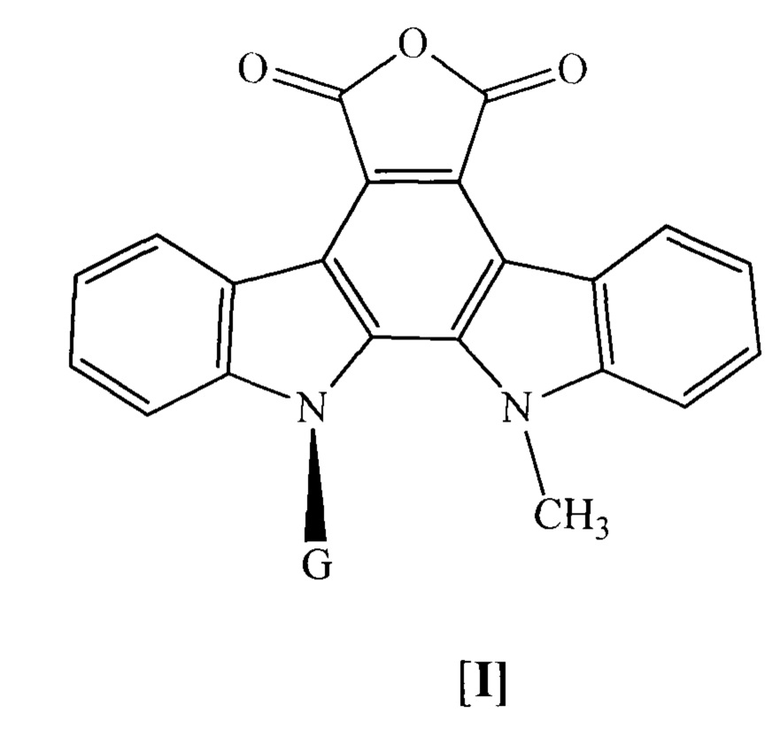
кипятят в сухом пиридине с аминокислотой в присутствии 3 молей хлоргидрата пиридина в течение 7-12 часов с контролем прохождения реакции по данным ТСХ на силуфоле; для направленного прохождения реакции в предложенных условиях требуется защита только азотсодержащих фрагментов боковой цепи Q аргинина (NO2/Arg) и лизина (Cbz/Lys), по окончании реакции пиридин упаривают, остаток кристаллизуют водой, затем методами экстракции и жидкостной хроматографией на силикагеле выделяют образовавшиеся N6-аминокислотные производные формулы [II]: пер-О-ацетилированные N12-β-D-рибопиранозиды, или N12-β-D-глюкопиранозиды, или N12-β-D-галактопиранозиды индоло[2,3-а]пирроло[3,4-с]карбазол-5,7-диона;
дезацетилирование углеводного остатка проводят действием безводного поташа в метаноле на ацетилгликозид формулы [II], фиксируют окончание реакции по данным ТСХ на силуфоле, затем добавляют воду до растворения осадка, вносят в раствор катионит (Н+) до рН 5, смывают водой со смолы и упаривают досуха реакционную смесь; жидкостной хроматографией на силикагеле выделяют N6-аминокислотные производные формулы [III]: N12-β-D-рибопиранозиды, или N12-β-D-глюкопиранозиды, или N12-β-D-галактопиранозиды индоло[2,3-а]пирроло[3,4-с]карбазол-5,7-диона.
| Г.Н | |||
| АПРЫШКО и др., Изучение свойств потенциальных противоопухолевых аминокислотных производных гликозидов индолокарбазолов, РОССИЙСКИЙ БИОТЕРАПЕВТИЧЕСКИЙ ЖУРНАЛ, 2017, Т | |||
| Устройство для электрической сигнализации | 1918 |
|
SU16A1 |
| Способ изготовления звездочек для французской бороны-катка | 1922 |
|
SU46A1 |
| СПОСОБ ПОЛУЧЕНИЯ N-ГЛИКОЗИДОВ ИНДОЛО[2,3-а]ПИРРОЛО[3,4-с]КАРБАЗОЛ-5,7-ДИОНОВ, ОБЛАДАЮЩИХ ЦИТОТОКСИЧЕСКОЙ И ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ | 2009 |
|
RU2427585C9 |
| N-ГЛИКОЗИДЫ ИНДОЛО[2,3-a]ПИРРОЛО[3,4-c]КАРБАЗОЛОВ, ОБЛАДАЮЩИЕ ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ | 2014 |
|
RU2548045C1 |
| И.С | |||
| ГОЛУБЕВА и др., Изучение in vivo потенциальных противоопухолевых свойств аминокислотных производных | |||
Авторы
Даты
2021-09-17—Публикация
2020-09-28—Подача