Изобретение относится к медицине, а именно к средствам, обладающим противоопухолевым действием.
Среди соединений, способных ингибировать ферменты ДНК-топоизомеразы, отвечающие за суперспирализацию ДНК и участвующие в процессе репликации и транскрипции, известны вещества различных химических групп. Особый интерес среди этих веществ представляют производные индолокарбазолов [Татарский В.В. Механизмы гибели опухолевых клеток при действии новых углеводных производных индолокарбазолов. Автореферат диссертации на соискание ученой степени ст. канд. биологических наук. Москва. 2010].
Известно средство из этой группы соединений бекатекарин, которое ингибирует топоизомеразы I и II и применяется в качестве противоопухолевого средства, при мелкоклеточном раке легкого [Schwandt A, Mekhail Т, Halmos В, O′Brien Т, Ma PC, Fu Р, Ivy Р, Dowlati A. Phase-II trial of rebeccamycin analog, a dual topoisomerase-I and -II inhibitor, in relapsed “sensitive” small cell lung cancer. J Thorac Oncol. 2012 Apr.; 7(4):751-4].
Задачей заявляемого изобретения является создание противоопухолевого средства из группы производных индолокарбазолов, позволяющего расширить спектр противоопухолевых препаратов.
Технический результат состоит в том, что создано новое противоопухолевое средство из группы производных индолокарбазолов, позволяющее расширить спектр противоопухолевых препаратов.
Поставленная задача достигается тем, что создано новое противоопухолевое средство из группы производных индолокарбазолов, включающее 6-амино-12-(α-L-арабинопиранозил)индоло[2,3-а]пирроло[3,4-с]карбазол-5,7-дион, диметилсульфоксид (ДМСО); поливинилпирролидон (ПВП) при следующем соотношении компонентов (мг):
Получение 6-амино-12-(α-L-арабинопиранозил)индоло[2,3-а]пирроло[3,4-с]карбазол-5,7-диона
К 0,55 г (0,9 ммоль) 13-формил-12-(2,3,4-три-О-ацетил-α-L-арабинопиранозил)индоло[2,3-а]фурано[3,4-с]карбазол-5,7-диона добавляли 3,2 мл (65,25 ммоль) гидразин-гидрата, смесь выдерживали при температуре 50°C в течение двух часов, охлаждали до 22°C, выливали в воду. Выпавший осадок отфильтровывали, промывали 10% спиртом. Выход 6-амино-12-(α-L-арабинопиранозил)индоло[2,3-а]пирроло[3,4-с]карбазол-5,7-диона составил 0,37 г (89%). Масс-спектр: М+ 457 m/z.
1Н-ЯМР (DMSO-d6, δ м.д.): 12.15 (с, 1H, NH-индол), 9.23 (д, 1H, Ar), 9.14 (д, 1Н, Ar), 7.94 (д, 1Н, Ar), 7.70 (д, 1Н, Ar), 7.62 (т, 1Н, Ar), 7.59 (т, 1H, Ar), 7.41 (т, 1Н, Ar), 7,37(т, 1H, Ar), 6.11 (д, 1Н, H1′, J1′2′ 9.1), 6.86, 5.38, 5.24 (3 уш с, 3Н, 2′,3′,4′-ОН), 4.99 (2Н, с, NH2), 4.20-4.05 (м, 3Н, Н2′, Н3′, Н5′′), 4.25 (м, 1Н, Н5′), 3.85 (м, 1Н, Н4′).
Способ получения заявляемого средства
К навеске 2970,0 мг 6-амино-12-(α-L-арабинопиранозил)индоло[2,3-а]пирроло[3,4-с]карбазол-5,7-диона добавляли 50,0 мл ДМСО, получали прозрачный раствор оранжевого цвета. Отдельно готовили 20% раствор ПВП в воде для инъекций. В водный раствор ПВП добавляли при постоянном перемешивании раствор 6-амино-12-(α-L-арабинопиранозил)индоло[2,3-а]пирроло[3,4-с]карбазол-5,7-диона в ДМСО. Полученный раствор стерилизовали при помощи фильтрации и разливали по 3,0 мл во флаконы вместимостью 20 мл и подвергали сублимационной сушке. По окончании лиофилизации флаконы закрывали пробками и укупоривали алюминиевыми колпачками.
Изобретение иллюстрируется примерами 1-3:
Пример 1.
Пример 2.
Пример 3.
Изучение противоопухолевой активности заявляемого средства
Исследование противоопухолевой активности заявляемого средства проводили на самках и самцах мышей гибридов первого поколения BDF1 (C57B1/6j×DBA/2), массой 18-20 грамма, полученных из питомника «Столбовая» РАМН.
Опухолевые клетки лимфолейкоза-Р388 перевивали мышам гибридам первого поколения BDF1 (C57B1/6×DBA/2) внутрибрюшинно асцитной жидкостью по 0,3 мл, содержащей 1×106 опухолевых клеток при разведении асцита в цитрате и среде 199. Введение заявляемого средства начинали через 24 часа после перевивки опухоли.
Опухолевую ткань эпидермоидной карциномы легкого Lewis (LLC) измельчали ножницами до гомогенной консистенции, добавляли среду 199 до соотношения 1:10. Полученную суспензию в объеме 0,5 мл вводили подкожно в область правой подмышечной впадины мышам - самцам BDF1. Введение заявляемого средства начинали через 48 час после перевивки опухоли.
Опытные группы при перевивке опухолевых клеток лимфолейкоза-Р388 состояли из 8 мышей. При перевивке опухолевой ткани эпидермоидной карциномы легкого Lewis опытные группы состояли из 9-10 мышей. Контрольные группы включали по 10-12 мышей, которые не получали заявляемого средства.
Критериями оценки противоопухолевой активности заявляемого средства служили: торможение роста опухоли (ТРО, %) и увеличение продолжительности жизни (УПЖ, %) опытных мышей по сравнению с контрольными.
Для оценки ТРО измеряли три максимальных взаимно перпендикулярных размера опухоли (длина, ширина, высота) у каждой мыши и вычисляли ее объем, а затем определяли средний объем опухолей в группе. Измерение объема опухоли проводили каждые 3 дня, начиная с 1 дня после окончания введения соединения, когда размеры опухолей у мышей контрольных групп были измеримыми.
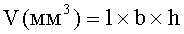
где: l - длина опухоли, мм;
b - ширина опухоли, мм;
h - высота опухоли, мм.
ТРО вычисляли по формуле:
ТРО(%)=(Vк-Vo)/Vk×100, где
Vк - средний объем опухолей в контрольной группе (мм3);
Vo - средний объем опухолей в опытной группе (мм3).
Сравнительную оценку противоопухолевой активности по УПЖ проводили после гибели мышей от опухолевого процесса. Сначала определяли среднюю продолжительность жизни (СПЖ) в днях в опытной и контрольной группах, а затем вычисляли УПЖ по формуле:
УПЖ(%)=(СПЖо-СПЖк)/СПЖк×100, где
СПЖк - средняя продолжительность жизни мышей в контрольной группе (дни);
СПЖо - средняя продолжительность жизни мышей в опытной группе (дни).
Минимальными критериями противоопухолевой активности служили: ТРО≥50% и УПЖ≥25%.
Статистическую значимость результатов оценивали по критерию Стьюдента-Фишера. Статистически значимой противоопухолевую активность считали при p≤0,05.
Заявляемое изобретение иллюстрировано таблицами 1-2.
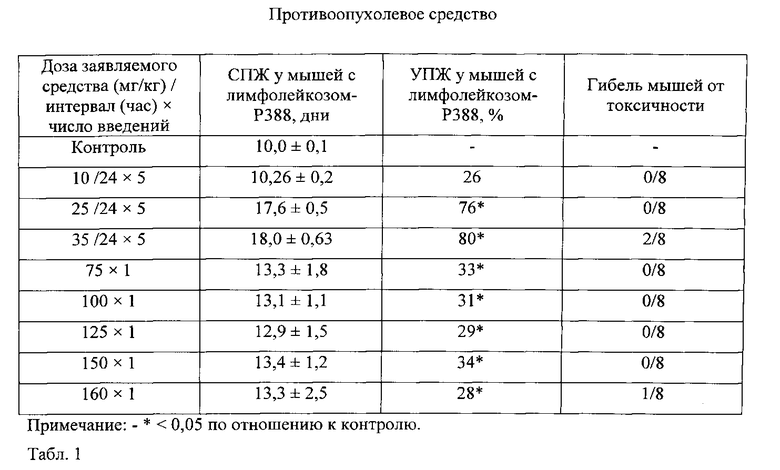
В табл. 1 представлена противоопухолевая активность заявляемого средства в зависимости от дозы и режима введения опытным мышам с лимфолейкозом-Р388. Показано, что при введении заявляемого средства в дозе 25 мг/кг при ежедневном применении в течение 5 дней выявлена высокая противоопухолевая активность, при этом УПЖ составило 76%. При введении заявляемого средства в дозе 35 мг/кг УПЖ составило 80%, но при этом отмечена гибель двух из 8 мышей. При однократном введении заявляемого средства в диапазоне доз от 75 мг/кг до 160 мг/кг не выявлено различий в терапевтическом эффекте: УПЖ варьировало от 28% до 34%. При введении заявляемого средства в дозе 160 мг/кг наблюдали гибель одной из 8 мышей.
Таким образом, режим введения заявляемого средства в дозе 25 мг/кг ежедневно в течение 5 дней у мышей с лимфолейкозом-Р388 являлся оптимальным.
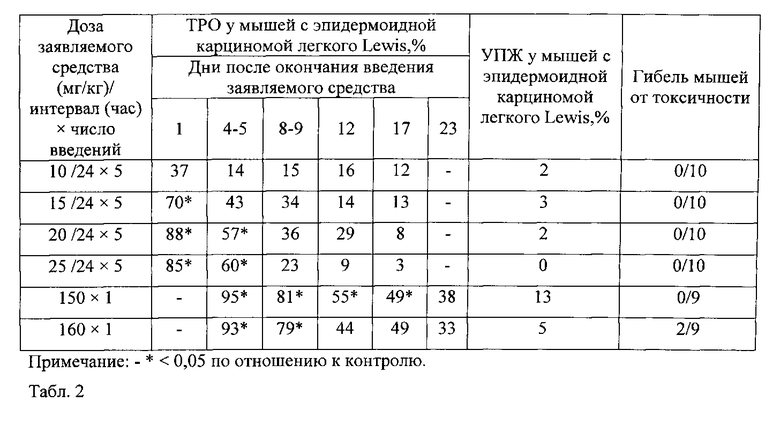
В табл. 2 представлена противоопухолевая активность заявляемого средства в зависимости от дозы и режима введения опытным мышам с эпидермоидной карциномой легкого Lewis (LLC). Показано, что при введении заявляемого средства в дозах 20 мг/кг и 25 мг/кг при ежедневном внутривенном введении в течение 5 дней выявлена статистически значимая противоопухолевая активность только в течение 5 дней после окончания его применения. ТРО на 1-й и 5-й дни после введения заявляемого средства в дозе 20 мг/кг составило 88% и 57%, соответственно. При применении заявляемого средства в дозе 25 мг/кг ТРО на 1-й и 5-й дни после введения составило 85% и 60%, соответственно. При однократном введении заявляемого средства в дозе 150 мг/кг достоверный противоопухолевый эффект сохранялся в течение 17 дней. При применении заявляемого средства в дозе 160 мг/кг наблюдали гибель двух из 9 мышей, соответственно.
Таким образом, введение заявляемого средства в дозе 150 мг/кг у мышей с эпидермоидной карциномой легкого Lewis (LLC) является оптимальным при однократном введении.
| название | год | авторы | номер документа |
|---|---|---|---|
| N-ГЛИКОЗИДЫ ИНДОЛО[2,3-a]ПИРРОЛО[3,4-c]КАРБАЗОЛОВ, ОБЛАДАЮЩИЕ ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ | 2014 |
|
RU2548045C1 |
| Производное класса N-гликозидов индоло[2,3-а]пирроло[3,4-с]карбазол-5,7-дионов - N-{ 12-(β-D-ксилопиранозил)-5,7-диоксо-индоло[2,3-а]пирроло[3,4-с] карбазол-6-ил} пиридин-2-карбоксамид, обладающее цитотоксической и противоопухолевой активностью | 2017 |
|
RU2667906C1 |
| СПОСОБ ПОЛУЧЕНИЯ N-ГЛИКОЗИДОВ ИНДОЛО[2,3-а]ПИРРОЛО[3,4-с]КАРБАЗОЛ-5,7-ДИОНОВ, ОБЛАДАЮЩИХ ЦИТОТОКСИЧЕСКОЙ И ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ | 2009 |
|
RU2427585C9 |
| Средство для терапии опухолей | 2019 |
|
RU2726801C1 |
| ПРОИЗВОДНЫЕ ИНДОЛОКАРБАЗОЛОВ, БЛОКИРУЮЩИЕ ВАСКУЛОГЕННУЮ МИМИКРИЮ В ОПУХОЛИ | 2014 |
|
RU2557554C1 |
| Способ лечения рака толстой кишки человека SW620 в эксперименте | 2017 |
|
RU2665168C1 |
| ПРОТИВООПУХОЛЕВОЕ ЛЕКАРСТВЕННОЕ СРЕДСТВО ИНГИБИТОР ТОПОИЗОМЕРАЗЫ I | 2022 |
|
RU2786727C1 |
| ПРОИЗВОДНЫЕ ГЛИКОЗИДОВ ИНДОЛО[2,3-А]ПИРРОЛО[3,4-С]КАРБАЗОЛ-5,7-ДИОНОВ, ОБЛАДАЮЩИЕ ЦИТОТОКСИЧЕСКОЙ И ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ | 2003 |
|
RU2255089C1 |
| Способ получения аминокислотных аналогов противоопухолевого антибиотика ребеккамицина | 2020 |
|
RU2755572C1 |
| ПРОТИВООПУХОЛЕВОЕ СРЕДСТВО | 2014 |
|
RU2569729C1 |
Изобретение относится к медицине, а именно к средствам, обладающим противоопухолевым действием. Предложено новое противоопухолевое средство, содержащее 6-амино-12-(α-L-арабинопиранозил)индоло[2,3-а]пирроло[3,4-с]карбазол-5,7-дион, диметилсульфоксид и поливинилпирролидон и при следующих соотношениях компонентов (мг):
Созданное новое противоопухолевое средство из группы производных индолокарбазолов позволяет расширить спектр противоопухолевых препаратов. 3 пр., 2 табл.
Противоопухолевое средство, содержащее 6-амино-12-(α-L-арабинопиранозил)индоло[2,3-а]пирроло[3,4-с]карбазол-5,7-дион, диметилсульфоксид и поливинилпирролидон и при следующих соотношениях компонентов (мг):
| Татарский В.В | |||
| Механизмы гибели опухолевых клеток при действии новых углеводных производных индолокарбазолов | |||
| Автореф.дис | |||
| на соиск | |||
| уч | |||
| ст | |||
| ст | |||
| канд | |||
| биологич | |||
| наук | |||
| Москва | |||
| Приспособление для суммирования отрезков прямых линий | 1923 |
|
SU2010A1 |
| Приспособление для набора, перевозки и смены, например, навоев, на быстроходных вертелках | 1955 |
|
SU103911A1 |
| Schwandt A, Mekhail Т, Halmos В, OBrien Т, Ma PC, Fu Р, Ivy Р, Dowlati A | |||
| Phase-II trial of rebeccamycin analog, a dual topoisomerase-I and | |||
Авторы
Даты
2016-01-20—Публикация
2014-10-09—Подача