Область техники.
Изобретение относится к экспериментальной медицине, а именно к моделированию в медицине, и может быть использовано для изучения патогенеза инсульта у человека и разработке эффективных технологий тромболитической и нейропротекторной терапии ишемического инсульта.
Уровень техники.
Ишемический инсульт занимает лидирующее место среди причин смертности, инвалидизации и социально-экономических потерь во всем мире.
Разработано множество экспериментальных моделей инсульта. Среди них модель тромбоэмболической ишемии является наиболее релевантной тромбоэмболическому инсульту у человека.
Известные модели тромбоэмболического инсульта различаются по способу формирования сгустка.
Известна модель, в которой для эмболии используют сгустки, спонтанно образованные из артериальной крови (Kudo М, Aoyama A, Ichimori S, Fukunaga N. An animal model of cerebral infarction. Homologous blood clot emboli in rats. Stroke. 1982 Jul-Aug;13(4):505-8. doi: 10.1161/01.str.13.4.505. PMID: 7101352). Сгустки получали следующим путем: 100 мкл крови, полученной путем пункции сердца, хранили 48 часов при комнатной температуре, сгусток отделяли от сыворотки и фрагментировали, пропуская 3 раза через иглу. 200 мкл суспензии (с физраствором) с фрагментами разного размера (до 100 мкл) использовали для эмболизации. Такие сгустки характеризуются высокой пластичностью.
Недостатками данного способа являются: низкая устойчивость тромба к действию собственной фибринолитической системы организма, высокий риск спонтанной реканализации тромба, и, как следствие, низкая воспроизводимость инфаркта мозга.
Известна также модель, в которой для эмболии используют индуцированные тромбином сгустки из аутокрови или аллогенной крови (Е Busch, K  , KA Hossmann Improved model of thromboembolic stroke and rt-PA induced reperfusion in the rat - Brain research, 1997. Volume 778, Issue 1,P. 16-24). Сгустки получали следующим образом: 0.6 ml артериальной крови смешивали с 0.15 ml тромбина (1 mg/ml, Sigma, St. Louis, MO, USA) и вводили в катетер РЕ50 (внутренний диаметр 0.58 mm, 50 cm). После этого сгустки удаляли из катетера, промывали физраствором, чтобы удалить клетки крови и исследовали под микроскопом, чтобы выбрать богатые фибрином участки. Эти сегменты разрезали на маленькие кусочки, чтобы получились цилиндрические сгустки размером 0.35×1.5 mm. 12 таких сгустков помещали в раствор альбумина (1 mg/ml) в фосфатном буфере. После полной ретракции (через 4 часа) сгустки вместе с раствором альбумина помещали в катетер РЕ50 длинной 1 м. Его соединяли с помощью иглы 22G с контуром, уже введенным в наружную сонную артерию (НСА). 12 сгустков один за другим вводили с интервалом 30 с. При этом общая сонная артерия (ОСА) была пережата.
, KA Hossmann Improved model of thromboembolic stroke and rt-PA induced reperfusion in the rat - Brain research, 1997. Volume 778, Issue 1,P. 16-24). Сгустки получали следующим образом: 0.6 ml артериальной крови смешивали с 0.15 ml тромбина (1 mg/ml, Sigma, St. Louis, MO, USA) и вводили в катетер РЕ50 (внутренний диаметр 0.58 mm, 50 cm). После этого сгустки удаляли из катетера, промывали физраствором, чтобы удалить клетки крови и исследовали под микроскопом, чтобы выбрать богатые фибрином участки. Эти сегменты разрезали на маленькие кусочки, чтобы получились цилиндрические сгустки размером 0.35×1.5 mm. 12 таких сгустков помещали в раствор альбумина (1 mg/ml) в фосфатном буфере. После полной ретракции (через 4 часа) сгустки вместе с раствором альбумина помещали в катетер РЕ50 длинной 1 м. Его соединяли с помощью иглы 22G с контуром, уже введенным в наружную сонную артерию (НСА). 12 сгустков один за другим вводили с интервалом 30 с. При этом общая сонная артерия (ОСА) была пережата.
Сгустки, полученные таким образом, характеризуются большей эластичностью, высокой плотностью фибриновой сети, чем в спонтанно образованных сгустках. Это имеет важное значение для воспроизводимости размера инфаркта.
Недостатками данного способа являются: очень сложная технология получения сгустков, вследствие чего подготовка к эксперименту занимает много времени; сама операция - введение катетера во внутреннюю сонную артерию (ВСА) через НСА - требует наличия в лаборатории дорогостоящего оборудования (операционного микроскопа); кроме того, полученные таким способом тромбы плохо поддаются тромболитической терапии.
Известен способ, при котором производится инъекция тромбина непосредственно в просвет средней мозговой артерии (СМА), характеризующийся тем, что тромб образуется в артерии (Orset С, Macrez R, Young AR, et al. Mouse model of in situ thromboembolic stroke and reperfusion. Stroke. 2007; 38 (10): 2771-2778; Arkelius K, Vivien D, Orset C, Ansar S. Validation of a stroke model in rat compatible with rt-PA-induced thrombolysis: new hope for successful translation to the clinic. Sci Rep.2020 Jul 22;10(1): 12191. doi: 10.1038/s41598-020-69081-0. PMID: 32699371; PMCID: PMC7376012). Животным под наркозом выполняли трепанацию черепа в височной области, иссекали твердую мозговую оболочку и обнажали СМА. С помощью специальной пипетки в просвет артерии вводили альфа-тромбин (0,75 ME), чем вызывали образование сгустка in situ. После стабилизации сгустка в течение 10-20 мин пипетку удаляли.
Недостатком данного способа является его инвазивность и то, что образование сгустков достаточно сложно стандартизировать, соответственно, ухудшается воспроизводимость инфаркта мозга.
Наиболее близким к заявляемому способу по совокупности совпадающих существенных признаков является способ моделирования окклюзии СМА сгустком аутологичной крови (Zhang Z, Zhang RL, Jiang Q, Raman SB, Cantwell L, Chopp M. A new rat model of thrombotic focal cerebral ischemia. J Cereb Blood Flow Metab. 1997 Feb;17(2):123-35. doi: 10.1097/00004647-199702000-00001. PMID: 9040491.) Принят в качестве прототипа.
В соответствии со способом-прототипом очаговый эмболический инсульт вызывали у крыс линии Вистар (350-450 г), под операционным микроскопом (Carl Zeiss, Inc., Thorpwood, NY, USA) выделяли правую и левую ОСА, правую НСА и ВСА. Дистальный конец НСА перевязывали. Правые ОСА и ВСА временно пережимали. Модифицированный катетер РЕ50 (внешний диаметр 0,3 мм), заполненный бычьим альфа-тромбином, вводили в просвет НСА через небольшой прокол. Петлю вокруг НСА с катетером затягивали. Катетер продвигали в просвет ВСА (в 2-3 мм от начала СМА). 10 мкл артериальной крови с помощью шприца отводили в катетер для образования сгустка. Через 10 мин правую и левую сонные артерии временно клипировали для уменьшения кровотока, а сгусток в катетере вводили в ВСА. Зажим на левой ОСА удаляли через 5 мин, из правой НСА извлекали катетер через 10 мин после инъекции. Правую НСА перевязывали.
Недостатками способа-прототипа, препятствующими достижению технических результатов заявляемого способа, является повышенная сложность выполнения операции, требующая наличия дорогостоящего операционного микроскопа, а также использование тромбина в качестве активатора тромбообразования.
Из уровня техники неизвестно использование тромбопластина в качестве активатора тромбообразования при моделировании эмболического инсульта у крыс.
Раскрытие изобретения
Заявляемое изобретение направлено на решение задачи усовершенствования модели тромбоэмболического инсульта, позволяющей доступными средствами, при наличии определенных технических навыков у экспериментатора, моделировать инфаркт головного мозга у крыс.
Моделирование ишемического инсульта головного мозга, также как в способе-прототипе, осуществляют путем формирования в шприце сгустка аутологичной крови и последующего введения сформированного сгустка через катетер в ВСА.
Особенность заявляемого способа заключается в том, что у подопытного животного под наркозом с одной стороны выделяют ОСА, НСА, крыловиднонебную артерию (КНА) и ВСА. ОСА, НСА и КНА перевязывают, в ОСА делают разрез выше места лигирования. Вставляют артериальный катетер и продвигают во ВСА на расстояние 14-18 мм от места бифуркации. В шприц с раствором тромбопластина и хлорида кальция отбирают кровь из ВСА и смешивают ее в шприце. Через 20 мин образовавшийся сгусток (100 мкл) вводят в ВСА через ОСА. Через 10 мин катетер вынимают, разрез ушивают.
Использование в эксперименте заявляемого способа позволяет достичь нескольких технических и экономических результатов:
- повышение релевантности модели тромбоэмболического инсульта по сравнению со способами, включающими использование тромбина, за счет использования тромбопластина, что обуславливает большую схожесть патогенеза ишемического инсульта у крысы с естественным течением инсульта у человека;
- высокая степень воспроизводимости за счет того, что введение сформированного сгустка осуществляют не через НСА, а через ОСА, что технически существенно легче выполнить;
- получение выраженных структурных и функциональных изменений мозга, что может способствовать разработке и исследованию эффективных технологий тромболитической и нейропротекторной терапии ишемического инсульта;
- уменьшение себестоимости проведения эксперимента за счет исключения необходимости применения дорогостоящего оборудования, в частности операционного микроскопа, по сравнению со способом Zhang Z, Zhang RL, Jiang Q, Raman SB, Cantwell L, Chopp M. A new rat model of thrombotic focal cerebral ischemia. J Cereb Blood Flow Metab. 1997 Feb; 17(2):123-35. doi: 10.1097/00004647-199702000-00001. PMID: 9040491.
Заявляемая модификация тромбоэмболической модели инсульта у крыс позволяет максимально устранить недостатки существующих моделей, получить воспроизводимый инфаркт головного мозга, что в дальнейшем будет способствовать разработке эффективных технологий тромболитической и нейропротекторной терапии ишемического инсульта.
Следует отметить, что индукция эмболии в проксимальной СМА является технически сложной операцией, при которой частота кровоизлияний в мозг и смертность довольно высоки.
При моделировании ишемии должны формироваться значимое снижение кровотока в пораженной артерии, стабильная и воспроизводимая зона нарушения перфузии и некроза ткани головного мозга, отчетливый неврологический дефицит; операция должна наносить минимальную травматизацию и выполняться быстро; модель должна быть проста в исполнении.
Авторами заявляемого способа была выбрана модель у крыс, поскольку она в наибольшей степени соответствует вышеуказанным требованиям. Заявляемый способ моделирования ишемического инсульта головного мозга включает следующие существенные отличительные признаки.
1. Для формирования фибринового сгустка крови используют раствор тромбопластина и CaCl2. Тогда как в большинстве известных способов для этого применяют тромбин. Тромбопластин (другое название - фактор свертывания крови III, тканевой фактор) играет роль активатора свертывания крови. Под действием тромбопластина образуется тромбин. При наличии в крови ионов кальция под действием тромбина происходит полимеризация растворимого фибриногена и образование бесструктурной сети волокон нерастворимого фибрина. Начиная с этого момента в волокнах фибрина начинают фильтроваться форменные элементы крови, придавая дополнительную жесткость всей системе, и образуя через некоторое время тромбоцитарно-фибриновый сгусток (физиологический тромб). Так, согласно инструкции к препарату (Тромбопластин, Диагем-П, Ренам НПО), при добавлении к цитратной плазме избытка тканевого тромбопластина и ионов кальция сгусток фибрина образуется в течение нескольких секунд (14-18 с). В нашем эксперименте сгусток крови формировался в шприце в течение 20 минут, затем его вводили через катетер во ВСА через разрез в ОСА.
2. Процедуру введения сгустка осуществляют не через НСА, а через ОСА, что технически существенно легче выполнить и не требует наличия дорогостоящего операционного микроскопа. В настоящее время при моделировании тромбоэмболического инсульта сгусток в большинстве случаев вводят через НСА.
3. При выполнении операции производят перманентное (постоянное) лигирование (перевязывание) сосудов мозга - ОСА, НСА и КНА для того, чтобы предотвратить кровотечение из поврежденной катером ОСА.
Краткое описание иллюстраций.
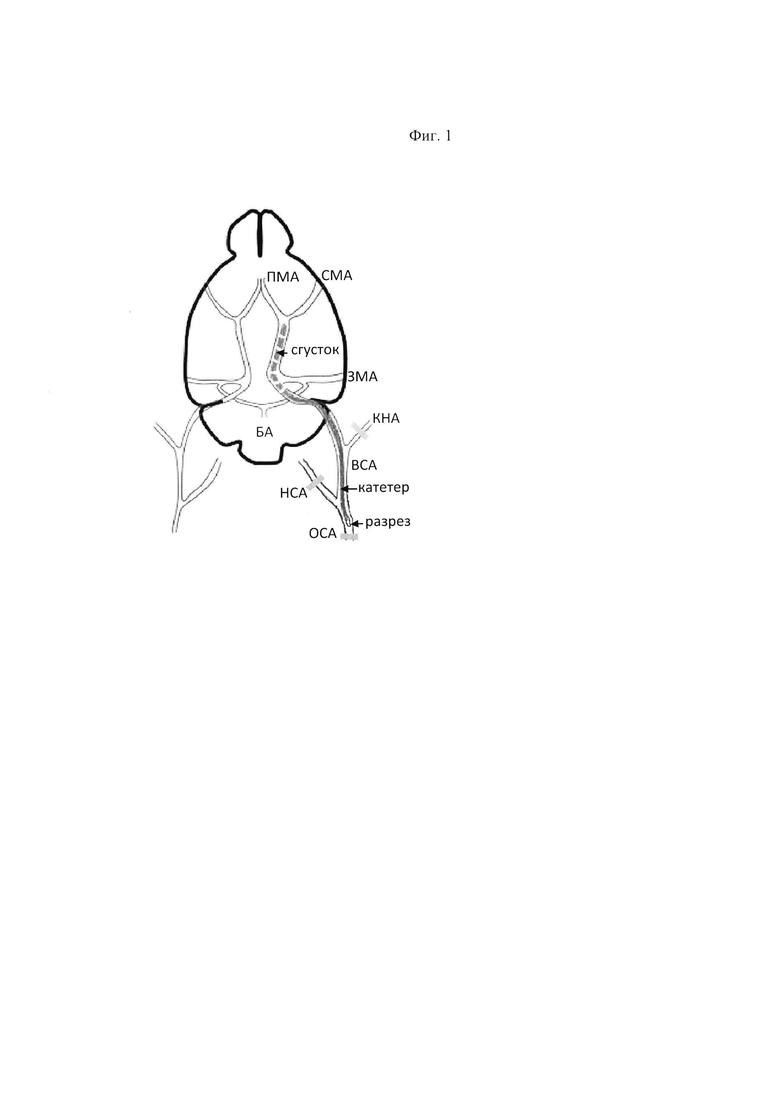
На Фиг. 1 представлена схема окклюзии СМА с использованием внутрисосудистого катетера и сгустка крови.
Обозначения: ОСА - общая сонная артерия, НСА - наружная сонная артерия, КНА -крыловиднонебная артерия, ВСА - внутренняя сонная артерия, СМА - средняя мозговая артерия, ПМА - передняя мозговая артерия, ЗМА - задняя мозговая артерия, БА - базиллярная артерия.
На Фиг. 2 представлены фронтальные срезы мозга, окрашенные гематоксилином и эозином.
А - Контроль.
На Фиг. 2 представлены фронтальные срезы мозга, окрашенные гематоксилином и эозином.
А - Контроль.
Б - 24 часа после эмболизации, зона инфаркта в области коры и таламуса бледно окрашена.
В - 72 часа после эмболизации, зона инфаркта в области таламуса и гиппокампа. Г - 6 суток после эмболизации, обширная зона инфаркта в области коры, таламуса и гиппокампа.
Д - тромбы в сосудах.
Описание процедуры эксперимента.
Фокальную ишемию головного мозга воспроизводили на крысах-самцах популяции Wistar (вес 250-400 г) в соответствии с протоколом, одобренным Локальным этическим комитетом ФГБНУ «Федеральный научно-клинический центр реаниматологии и реабилитологии» №1/20/3 от 11 марта 2020 г.
Животным под общей анестезией (раствор хлоралгидрата 6% 300 мг/кг в/б с дополнительными инъекциями (100 мг/кг) при снижении глубины анестезии) выбривали шерсть в области передней поверхности шеи. Кожу обрабатывали антисептиком. Выполняли срединный разрез кожи на передней поверхности шеи. Разрез обрабатывали раствором лидокаина. Левую ОСА выделяли тупым способом, на нее накладывали лигатуру (шелк 4.0). Ближе к основанию черепа выделяли левые НСА и ВСА. ВСА аккуратно отделяли от прилежащего к ней блуждающего нерва. Перевязывали НСА и КНА. Микрохирургическими ножницами делали небольшой надрез в ОСА на расстоянии 2 мм ниже места бифуркации (Фиг. 1).
Подготовленный составной катетер (внутрисосудистая часть - ПУ трубка 0,6×0,3×30 мм, внесосудистая часть - ПВХ трубка 1,0×0,7×70 мм) аккуратно заводили в ВСА через разрез в ОСА на расстояние 14-18 мм от места бифуркации ОСА на НСА и ВСА. Набирали 400 мкл артериальной крови в шприц, содержащий 50 мкл раствора тромбопластина и 50 мкл 4% раствора CaCl2. При этом использовали стандартный набор реагентов для определения протромбинового времени («Тромбопластин» Диагем-П, Ренам НПО). Шприц отсоединяли от катетера, катетер промывали раствором 0,9% NaCl. Через 20 мин образовавшийся в шприце сгусток объемом 100 мкл вводили через катетер в просвет ВСА (Фиг. 1). Через 10 мин катетер удаляли и операционную рану ушивали.
Животное переносили в клетку. Внутрибрюшинно вводили раствор парацетамола (1 мл) для обезболивания.
Ложнооперированным (контрольным) животным вводили аналогичный объем (100 мкл) физиологического раствора 0,9% NaCl.
Проводили оценку состояния животного в клетке (внешний вид и поведение) в первый час, а также через 6 ч, 24 ч, 72 ч и 6 суток после операции. Оценку неврологического статуса и поведения проводили с помощью модифицированной шкалы Бедерсона через 24 ч после операции. Более детальную оценку состояния проводили по 20-балльной шкале (Hunter AJ, Hatcher J, Virley D, Nelson P, Irving E, Hadingham SJ, Parsons AA: Functional assessments in mice and rats after focal stroke. Neuropharmacology 39 (2000) 806-816).
Через 6 ч, 24 ч, 72 ч и 6 суток осуществляли повторную анестезию, головной мозг извлекали и фиксировали в 10% формалине в течение 48 часов. Образцы мозга после стандартной обработки заключали в парафин. На ротационном микротоме изготавливали срезы толщиной 5-6 мкм, которые затем окрашивали гематоксилин-эозином. Проводили гистологическое исследование ткани мозга с целью выявления областей ишемического повреждения с помощью светового микроскопа Nikon Eclips Ni и программы NIS-Elements BR (Nikon Corp., Japan).
Общая летальность составила 22%, при этом операционная летальность была 5%, 16% экспериментальных животных погибли в первые 24 часа после операции. Клинические проявления в виде сужения зрачка и побледнения глаза на поврежденной стороне наблюдали у всех крыс с эмболией в отличие от ложнооперированных животных. 20-балльная оценка состояния крыс, проведенная через 24 часа после эмболизации, выявила нарушение моторных и поведенческих функций во всех группах животных с ишемическим инсультом в сравнении с ложнооперированными (р<0,05, критерий Манна-Уитни). При гистологическом анализе у ложнооперированных крыс не обнаружено различий между ипсилатеральным и контрлатеральным полушариями головного мозга. Через 6 часов после операции был выявлен обширный очаг некроза в области стриатума и коре ипсилатерального полушария у одной из 4-х крыс. Через 24 часа у всех подопытных крыс (n=3) в коре, гиппокампе и подкорковых областях обнаружены повреждения нейронов ипсилатерального полушария различной степени выраженности: ишемические изменения нейронов и некроз (Фиг. 2). Через 72 часа у четырех из шести подопытных животных также наблюдали патологические изменения нейронов левого полушария мозга - от отдельных небольших очагов поврежденных нейронов в коре и гиппокампе до значительных областей некроза в коре и таламо-стриатальной области (Фиг. 2). На 6-е сутки после ишемии у 4-х из 5-ти крыс были выявлены очаги некроза в стриатуме, коре и гиппокампе ипсилатерального полушария (Фиг. 2).
Использование заявляемого способа приводило к стойкому нарушению моторных и поведенческих функций у подопытных животных, а также к формированию очагов некроза в бассейне СМА ипсилатерального полушария головного мозга (сенсомоторная кора, таламо-стриатальная система, гиппокамп).
Таким образом, заявляемый способ моделирования ишемического инсульта имеет ряд преимуществ перед другими моделями, а именно, относительная дешевизна, легкость выполнения, относительно низкая летальность, получение выраженных структурных и функциональных изменений мозга, достаточно хорошая воспроизводимость.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ МОДЕЛИРОВАНИЯ ЗЛОКАЧЕСТВЕННОГО ИШЕМИЧЕСКОГО ИНСУЛЬТА | 2023 |
|
RU2822706C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ ЗЛОКАЧЕСТВЕННОГО ИШЕМИЧЕСКОГО ИНСУЛЬТА | 2022 |
|
RU2785608C1 |
| Способ деструкции эмбологенного матрикса в эксперименте. | 2020 |
|
RU2739669C1 |
| СПОСОБ РЕНТГЕНЭНДОВАСКУЛЯРНОЙ КОМБИНИРОВАННОЙ ТРОМБЭКТОМИИ ИЗ АРТЕРИЙ ГОЛОВНОГО МОЗГА | 2018 |
|
RU2670193C1 |
| Способ лечения острой окклюзии экстра- и интракраниального отделов внутренней сонной артерии в острейшем периоде ишемического инсульта | 2023 |
|
RU2811275C1 |
| Способ защиты головного мозга от ишемии при пережатии внутренней сонной артерии во время каротидной эндартерэктомии | 2022 |
|
RU2787458C1 |
| Способ установки временного внутрипросветного шунта с раздуваемыми баллонами и Т-образным портом при пережатии сонных артерий во время выполнения каротидной эндартерэктомии | 2022 |
|
RU2803385C1 |
| Способ открытого хирургического лечения ложной аневризмы зоны реконструкции после каротидной эндартерэктомии | 2021 |
|
RU2798714C2 |
| СПОСОБ ВОССТАНОВЛЕНИЯ КРОВОТОКА ПРИ СОЧЕТАННОМ ТРОМБОЗЕ ВНУТРЕННЕЙ СОННОЙ И СРЕДНЕЙ МОЗГОВОЙ АРТЕРИЙ | 2016 |
|
RU2629046C2 |
| Способ определения показания для применения временного шунта при выполнении каротидной эндартерэктомии | 2023 |
|
RU2809498C1 |

Изобретение относится к экспериментальной медицине. Способ моделирования фокального ишемического инсульта головного мозга у крыс включает формирование сгустка аутологичной крови и последующее введение сформированного сгустка через катетер во внутреннюю сонную артерию. При этом у подопытного животного под наркозом осуществляют перманентное лигирование сосудов мозга с одной стороны: общей сонной, наружной сонной и крыловиднонебной артерии. Вводят катетер через разрез в общей сонной артерии во внутреннюю сонную артерию на расстояние 14-18 мм от места бифуркации общей сонной артерии на наружную и внутреннюю сонные артерии. Отбирают 400 мкл артериальной крови. Формируют сгусток крови путем перемешивания в шприце артериальной крови с 50 мкл раствора тромбопластина и 50 мкл 4% раствора CaCl2. Через 20 мин образовавшийся сгусток объемом 100 мкл вводят через катетер во внутреннюю сонную артерию. Через 10 мин катетер удаляют и операционную рану ушивают. Изобретение обеспечивает повышение релевантности модели тромбоэмболического инсульта, высокую степень воспроизводимости, получение выраженных структурных и функциональных изменений мозга. 2 ил.
Способ моделирования фокального ишемического инсульта головного мозга у крыс, включающий формирование сгустка аутологичной крови и последующее введение сформированного сгустка через катетер во внутреннюю сонную артерию, отличающийся тем, что у подопытного животного под наркозом осуществляют перманентное лигирование сосудов мозга с одной стороны: общей сонной, наружной сонной и крыловиднонебной артерии, вводят катетер через разрез в общей сонной артерии во внутреннюю сонную артерию на расстояние 14-18 мм от места бифуркации общей сонной артерии на наружную и внутреннюю сонные артерии, отбирают 400 мкл артериальной крови, формируют сгусток крови путем перемешивания в шприце артериальной крови с 50 мкл раствора тромбопластина и 50 мкл 4% раствора CaCl2, через 20 мин образовавшийся сгусток объемом 100 мкл вводят через катетер во внутреннюю сонную артерию, через 10 мин катетер удаляют и операционную рану ушивают.
| СПОСОБ МОДЕЛИРОВАНИЯ ФОКАЛЬНОЙ ИШЕМИИ ГОЛОВНОГО МОЗГА | 2015 |
|
RU2639787C1 |
| ЕРШОВ В.И | |||
| и др | |||
| Математическое моделирование ишемического инсульта /Неврология, нейропсихиатрия, психосоматика, 2019; 11(4), стр | |||
| Способ сужения чугунных изделий | 1922 |
|
SU38A1 |
| ГАФАРОВА М.Э | |||
| ГЕМОСТАТИЧЕСКИЕ И ГЕМОРЕОЛОГИЧЕСКИЕ ФАКТОРЫ ПРИ ТРОМБОЛИТИЧЕСКОЙ ТЕРАПИИ ОСТРОГО ИШЕМИЧЕСКОГО ИНСУЛЬТА / Диссерт | |||
| на соиск | |||
| уч | |||
| степ | |||
| к.м.н., Москва, 2015 | |||
| ZHANG Z | |||
| et | |||
Авторы
Даты
2021-09-30—Публикация
2020-12-23—Подача