Настоящее изобретение касается нового терапевтического применения, включая введение низких дозировок высокоактивного лиганда H3-гистаминового рецептора.
В WO 2006/117609 описаны неимидазольные лиганды H3-гистаминового рецептора, имеющие формулу:
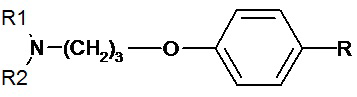
и их применение для лечения и/или предотвращения заболеваний ЦНС, таких как болезнь Альцгеймера; нарушение внимания; инсомния и нарушение запоминания; когнитивные расстройства в психиатрических патологиях; возрастные нарушения; депрессивные или астенические состояния; болезнь Паркинсона; синдром обструктивного апноэ во сне; деменция с тельцами Леви; сосудистая деменция; головокружение; укачивание; злоупотребление алкоголем и другими веществами; хроническая боль; ожирение; диабет и метаболический синдром; нарушения сна; стресс; психотропные нарушения; конвульсии; депрессия; нарколепсия; нарушения гипоталамо-гипофизной секреции, мозгового кровообращения и/или в иммунной системе; и/или для облегчения работы по ночам или для адаптации к смене часового пояса у здоровых людей.
В WO 2006/117609 описано, что указанные лиганды, в целом, подходят для введения людям в единичных дозированных формах, обычно от 0,1 мг до 1000 мг в сутки, предпочтительно от 1 до 500 мг с введением от одного до четырех раз в сутки, и еще более предпочтительно - от 10 мг до 300 мг два раза в сутки.
Сходным образом, питолизант, другой неимидазольный Н3-антагонист, одобренный для лечения нарколепсии, продается в единичных дозированных формах (таблетки с покрытием), содержащих 4,5 мг и 18 мг. Оптимальная одобренная терапевтическая дозировка может составлять до 36 мг в сутки.
В целом, является желательным выявление потенциальных лекарственных препаратов, обладающих максимально возможной активностью. Более высокая активность обычно ассоциируется с высокой селективностью к мишени, низкими рисками связывания с нецелевыми мишенями и, благодаря этому, более высокой безопасностью при клиническом применении.
Таким образом, является желательным выявление потенциальных лекарственных препаратов, обладающих максимально возможной активностью, при этом характеризующихся как можно более низкой эффективной дозировкой.
Среди H3-лигандов, раскрытых в WO 2006/117609, и вопреки раскрытым дозировкам H3-лигандов, авторы настоящего изобретения обнаружили, что (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид, имеющий формулу:
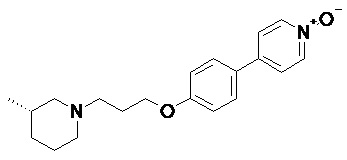
(A)
именуемый в настоящем тексте “соединение (A)”,
неожиданно демонстрирует выдающийся профиль, позволяющий использовать весьма низкие эффективные дозировки.
В одном варианте осуществления настоящее изобретение касается (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксида, имеющего формулу (A):

(A)
или его фармацевтически приемлемых солей и/или сольватов указанного соединения (A) или его солей, для применения для лечения и/или предотвращения у людей заболеваний, выбранных из следующих: болезнь Альцгеймера; нарушение внимания; инсомния и нарушение запоминания; когнитивные расстройства в психиатрических патологиях; когнитивные расстройства, расстройства настроения и концентрации, в особенности у пожилых пациентов; депрессивные или астенические состояния; болезнь Паркинсона; синдром обструктивного апноэ во сне; деменция с тельцами Леви; сосудистая деменция; головокружение; укачивание; ожирение; диабет и метаболический синдром; нарушения сна; стресс; психотропные нарушения; эпилепсия; депрессия; нарколепсия с катаплексией или без неё; злоупотребление веществами, в частности злоупотребление алкоголем, предотвращение синдрома отмены при злоупотреблении веществами; когнитивные нарушения при аутизме; хроническая боль и хроническая усталость; постинсультная усталость; расстройства настроения, концентрации и когнитивные расстройства, нарушения внимания и концентрации при СДВГ (синдром дефицита внимания и гиперактивности) у детей или взрослых или после инсульта; нарушения гипоталамо-гипофизной секреции, мозгового кровообращения и/или в иммунной системе; избыточная дневная сонливость, такая как избыточная дневная сонливость и усталость, связанная с болезнью Альцгеймера, синдром обструктивного апноэ во сне или деменция; и/или для облегчения работы по ночам или для адаптации к смене часового пояса у здоровых людей.
где указанное применение включает введение (A) человеку в дозировке от 10 до 90 мкг в сутки (в пересчете на соединение (A) в форме свободного основания).
В настоящем изобретении раскрыт также способ предотвращения и/или лечения перечисленных выше заболеваний, включающий введение пациенту, нуждающемуся в этом, соединения (A) в дозировке от 10 до 90 мкг в сутки (в пересчете на соединение (A) в форме свободного основания), с фармацевтически приемлемым носителем или вспомогательным веществом.
В одном варианте осуществления применение нацелено на лечение и/или предотвращение нарушений сна, таких как бессонница, нарушений инициирования и поддержания сна, фрагментации сна, парасомнии; нарушения фазы быстрого движения глаз во сне, нарушение дыхания во сне, суточная аритмия, нарколепсия с катаплексией или без неё, избыточная дневная сонливость (включая «приступы непреодолимого сна»), такая как усталость или избыточная дневная сонливость, связанная с болезнью Паркинсона, обструктивным апноэ во сне или деменцией. Другим применением является лечение и/или предотвращение злоупотребления веществами, в частности злоупотребления алкоголем. Другое применение предназначено для лечения и/или профилактики настроения, когнитивных нарушений и когнитивных расстройств, вызванных инсультом. Другое применение - для лечения и/или предотвращения нарушения внимания и концентрации при СДВГ или после инсульта.
В одном варианте осуществления соединение (A) находится в форме соответствующего основания, как показано в формуле (A). В альтернативном варианте соединение (A) может находиться в форме его фармацевтически приемлемых солей, таких как гидрохлорид, оксалат, дигидрохлорид, гидробромид, дигидробромид, нафталин-1,5-дисульфонат, сульфат, этан-1,2-дисульфонат, цикламат, толуолсульфонат, паратолуолсульфонат, тиоцианат, нитрат, метансульфонат, додецилсульфат, нафталин-2-сульфонат, бензолсульфонат, дихлорацетат, глицерофосфат, 2-гидроксиэтансульфонат, аспартат, малеат, фосфат, этансульфонат, камфор-10-сульфонат, глутамат, альгинат, памоат, 2-оксо-глутарат, 1-гидрокси-2-нафтоат, малонат, гентизат, салицилат, тартрат, фумарат, галактарат, цитрат, глюкуронат, лактобионат, 4-аминосалицилат, гликолят, сесквигликолят, глюкогептаноат, пироглутамат, манделат, малат, гиппурат, формиат, глюконат, лактат, олеат, аскорбат, бензоат, сукцинат, 4-ацетамидобензоат, глутарат, циннамат, адипат, себакат, камфорат, ацетат, капроат, никотинат, изобутират, пропионат, карат, лаурат, пальмитат, стеарат, ундецен-10-оат, каприлат, оротат, карбонат, 5-сульфосалицилат, 1-гидрокси-2-нафтоат, 3-гидрокси-2-нафтоат; и/или сольватов, таких как гидраты, этанолят, гемиэтанолят.
Соответственно, термин “соединение (A)” при использовании в настоящем изобретении относится также к его фармацевтически приемлемым солям и/или к сольватам указанного соединения, имеющего формулу (A), или его солей, если специально не указано иное. В частности, необходимо особо отметить дигидрохлоридную соль этого соединения.
Термин “соединение (A) в форме свободного основания” относится к изображенному выше соединению (A).
В одном варианте осуществления соединение (A) может находиться в форме следующих фармацевтически приемлемых солей:
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид дигидрохлорид тетрагидрат;
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид оксалат;
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид L-тартрат и его тригидрат;
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид памоат;
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид фумарат;
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид пара-толуолсульфонат и его сестерцигидрат (2,5)
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид 1,5-нафталиндисульфонат и его гемиэтанолят моногидрат;
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид фосфат;
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид бромгидрат;
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид 1,2-этандисульфонат;
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид сульфат;
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид дибромгидрат;
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид оротат и его дигидрат;
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид 5-сульфосалицилат;
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид 1-гидрокси-2-нафтоат и его моногидрат;
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид 3-гидрокси-2-нафтоат;
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид (сескви)гликолят и его моногидрат.
В одном варианте осуществления соединение находится в форме тетрагидрата дигидрохлорида соединения (A).
Тетрагидрат соединения (A) устойчив при относительной влажности от по меньшей мере 30% до 70%, что является улучшенным свойством в сравнении с гигроскопичной природой ранее описанного дигидрохлорида. Тетрагидрат соединения (A) устойчив также при температурах в диапазоне от 20°C до 40°C.
Тетрагидрат соединения (A) имеет одно или больше из перечисленных ниже отличительных свойств:
В одном варианте осуществления тетрагидратная форма соединения (A) имеет пик плавления около 191°C при измерении методом капиллярной трубки.
В другом варианте осуществления анализ методом дифференциальной сканирующей калориметрии показывает два эндотермических события с температурой начала около 53°C и 83°C, которые соответствуют потере четырех молекул воды; последнее событие наблюдается с температурой начала около 191°C.
В другом варианте осуществления содержание воды в тетрагидрате соединения (A) составляет от 14 до 16%, обычно около 15,3±0,7вес.%.
В одном варианте осуществления тетрагидратная форма соединения (A) имеет одну или больше из приведенных ниже линий в порошковой рентгеновской дифрактограмме (XRPD):
(2-Тета°)
(Ангстрем)
(импульсы)
(%)
Более конкретно, следующие пики:
(°)
(ангстрем)
Было показано, что тетрагидратная форма дигидрохлоридной соли соединения (A) очень устойчива.
Тетрагидрат дигидрохлорида соединения (A) можно получить обычными методами, такими осаждение из растворителя при концентрировании, добавлении антирастворителя и/или понижении температуры.
В одном варианте осуществления тетрагидрат дигидрохлоридной соли соединения (A) можно получить способом, включающим следующие стадии:
- растворение дигидрохлорида (A) в воде;
- упаривание до выделения твердого вещества; и
- сушка полученного твердого вещества до финального содержания воды 15,3±0,7вес.%.
В альтернативном варианте тетрагидрат дигидрохлорида соединения (A) можно получить следующим образом:
- добавление водной соляной кислоты к основанию (A);
- добавление ацетона;
- добавление затравочных кристаллов и образование твердого вещества;
- фильтрование; и
- сушка полученного твердого вещества до финального содержания воды 15,3±0,7вес.%.
В одном варианте осуществления суточная дозировка соединения (A) для введения человеку составляет от 20 до 50 мкг в сутки, предпочтительно от 30 до 45 мкг свободного основания в сутки (в пересчете на соединение (A) в форме свободного основания).
В другом варианте осуществления способ по настоящему изобретению может включать введение указанных дозировок соединения (A) с частотой от одного раза в 3 дня, одного раза в 2 дня (qod) до одного раза в сутки (qd). Предпочтительно введение осуществляется один раз в сутки.
Следует понимать, что дозировка по настоящему изобретению представляет собой суммарную дозировку всех доз, вводимых в течение суток.
Идентификация пациентов, нуждающихся в лечении описанных в настоящем тексте заболеваний и патологических состояний, находится в рамках знаний и способностей квалифицированного специалиста в данной области. Квалифицированный клиницист может легко выявить с применением клинических тестов, физического обследования, генетических тестов и медицинской/наследственной истории, тех субъектов, которые нуждаются в таком лечении.
Актуальный уровень дозировок соединения, имеющего формулу (А) по настоящему изобретению, может варьироваться таким образом, чтобы получить количество действующего вещества, которое эффективно для достижения желаемого терапевтического ответа для конкретной композиции и способа введения. Выбираемый уровень дозировки, таким образом, зависит от целевого терапевтического эффекта, способа введения, от желаемой длительности лечения и других факторов, например состояния пациента.
Терапевтически эффективное количество может быть легко определено лечащим врачом с применением общеизвестных методик, а также на основе результатов, полученных при аналогичных обстоятельствах. При определении терапевтически эффективного количества квалифицированный диагност рассматривает несколько факторов, включая (но не ограничиваясь только ими) вид субъекта; его вес, возраст и общее состояние здоровья; конкретное заболевание, которым страдает субъект; степень выраженности или тяжести заболевания; отклик конкретного субъекта; конкретное применяемое соединение; путь введения; характеристики биодоступности вводимого препарата; выбранный режим дозирования; применение сопутствующих лекарственных препаратов, и другие имеющие значение обстоятельства.
Количество соединения (A), которое требуется для достижения желаемого биологического эффекта, варьируется в зависимости от ряда факторов, включая дозировку применяемого лекарственного средства, тип заболевания, тяжесть течения заболевания и пациента и путь введения.
Говоря в общем, предпочтительная дозировка вводимого лекарственного средства будет зависеть от таких переменных, как тип и степень развития заболевания или нарушения, общее состояние здоровья конкретного пациента, относительная биологическая эффективность выбранного соединения, применение адъювантов и путь введения. Суточная дозировка соединения (A) обычно меньше 90 мкг (в пересчете на свободное основание) в сутки на пациента.
Согласно другому варианту осуществления способ по настоящему изобретению включает также введение одного или более других действующих веществ, выбранных из антипаркинсонических лекарственных средств, таких как леводопа, ропинорол, лизурид, бромокриптин, прамиксепол, или выбранных из противонарколептических или предполагаемых противонарколептических лекарственных средств из другого класса, включая модафинил.
Соединение (A) можно вводить в состав фармацевтических композиций путем смешивания с одним или больше фармацевтически приемлемыми вспомогательными веществами.
Композиции можно вводить в виде однократных дозированных форм и можно готовить любым из способов, хорошо известных в фармацевтике, например как описано в Remington: The Science and Practice of Pharmacy, 20th ed.; Gennaro, A. R., Ed.; Lippincott Williams & Wilkins: Philadelphia, PA, 2000.
Соединение (A) можно вводить различными способами, такими как пероральный; парентеральный, включая подкожное, внутримышечное, внутривенное введение; сублингвально, наружно; местно; внутритрахейно; интраназально; чрезкожно или ректально, при этом действующее вещество комбинируют с фармацевтически приемлемым вспомогательным веществом или растворителем в составе фармацевтической композиции.
В другом варианте осуществления настоящее изобретение также касается фармацевтической композиции, содержащей соединение (A) и фармацевтически приемлемое вспомогательное вещество или растворитель, для применения в лечении и/или предотвращении перечисленных выше нарушений, где соединение (A) вводят в дозировке от 10 до 70 мкг в сутки (в пересчете на соединение (A) в форме свободного основания).
В случае наружного применения композиции по настоящему изобретению могут применяться в виду кремов, гелей, мазей или лосьонов.
В частности, препараты, подходящие для парентерального введения, являются стерильными и включают эмульсии, суспензии, водные и неводные растворы для инъекций, которые могут содержать суспендирующие агенты, загустители и антиоксиданты, буферные добавки, бактериостатические добавки и вещества, делающие препараты изотоничными, они имеют надлежащим образом отрегулированный рН, подходящий для крови реципиента.
Согласно настоящему изобретению предпочтительно применяют соединения или композиции для перорального введения в виде подходящих препаратов. Препараты, подходящие для перорального приема пациентом, включают единичные дозированные формы, такие как капсулы, например мягкие или твердые желатиновые капсулы, таблетки, каждая из которых содержит определенное количество соединения, имеющего формулу (А). Они также включают порошки, гранулы, растворы или суспензии в водном или неводном растворителе, или эмульсии типа масло-в-воде или вода-в-масле.
Термин “фармацевтические” или “фармацевтически приемлемые” относится к молекулам и композициям, которые не вызывают побочной, аллергической или другой нежелательной реакции при введении животному или человеку.
При использовании в настоящем изобретении термин “фармацевтически приемлемое вспомогательное вещество, растворитель или носитель” включает, в частности, разбавители, адъюванты, вспомогательные вещества или растворители. Применение таких ингредиентов для фармацевтически активных субстанций хорошо известно в данной области.
В контексте настоящего изобретения термин “лечение” означает обращение, облегчение, подавление развития или профилактику расстройства или патологического состояния, к которому применяется данный термин, или одного или более симптомов такого расстройства или патологического состояния.
Термин “терапевтически эффективное количество” означает количество соединения/лекарственного средства по настоящему изобретению, эффективное для достижения желаемого терапевтического эффекта.
Согласно настоящему изобретению термин “пациент” или “пациент, нуждающийся в этом” относится к человеку или млекопитающему, не являющемуся человеком, страдающему или подверженному перечисленным выше заболеваниям. Предпочтительно пациентом является человек.
Соединение (A) можно вводить в однократных дозированных формах, где термин «однократная доза» означает единичную дозу, которую можно вводить пациенту и которую можно легко производить и упаковывать, при этом она остается физически и химически стабильной однократной дозированной формой, содержащей активное соединение в чистом виде или в составе фармацевтически приемлемой композиции.
Подходящие однократные дозированные формы включают формы для перорального приема, сублингвального, буккального, внутритрахейного, внутриглазного, интраназального введения, для введения в виде ингаляции, для наружного, чрезкожного, подкожного, внутримышечного или внутривенного введения, а также для ректального введения и введения в виде имплантов.
Суточную дозировку от 10 до 90 мкг согласно настоящему изобретению можно достичь путем введения половины однократной дозированной формы, введения одной однократной дозированной формы или двух или более однократных дозированных форм, в соответствии с доступными на рынке однократными дозированными формами, необходимой суточной дозировкой и частотой введения, предписанной лечащим врачом.
Некоторые соли соединения (A) являются новыми. В другом варианте осуществления настоящее изобретение касается также следующих соединений:
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид дигидрохлорид тетрагидрат;
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид L-тартрат и его тригидрат;
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид памоат;
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид фумарат;
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид пара-толуолсульфонат и его сестерцигидрат (2,5)
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид 1,5-нафталиндисульфонат и его гемиэтанолят моногидрат;
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид фосфат;
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид бромгидрат;
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид 1,2-этандисульфонат;
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид сульфат;
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид дибромгидрат;
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид оротат и его дигидрат;
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид 5-сульфосалицилат;
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид 1-гидрокси-2-нафтоат и его моногидрат;
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид 3-гидрокси-2-нафтоат;
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид (сескви)гликолят и его моногидрат.
Описанные ниже примеры приведены для иллюстрации неограничивающих вариантов осуществления настоящего изобретения.
Примеры
Пример 1. Данные фармакокинетики у человека
Cмакс соединения (A) при пероральном приеме один раз в сутки в дозировках 60 или 90 мкг достигалась примерно через 2,5-3,5 часа после введения в День 1 и День 10, среднее значение составляло 121 и 171 пг/мл после однократной дозировки, и 172 и 344 пг/мл после повторной дозы 60 и 90 мкг, соответственно.
Влияние соединения (A) на бодрствование в низкой дозировке (30 мкг/сутки) подтверждалось задержкой в засыпании при укладывании в постель ночью, в то время как повторяющийся прием по 90 мкг один раз в сутки в течение 10 дней приводил к некоторой бессоннице.
Среднее значение t1/2 составляло около 33 часов при определении в День 10 после нескольких введений. Общий клиренс (Clss/F) снижался на 65% и 74% после повторного приема 60 и 90 мкг соединения (A), соответственно. Уровень соединения (A) в плазме крови после введения 60 мкг был выше после повторного введения (День 10), чем после однократного введения (День 1), что отражается значением Cмакс на 42% выше и значением AUC0-24ч на 73% выше. Процент аккумулирования после повторного введения был более выражен для дозировки 90 мкг, где наблюдалось повышение Cмакс на 101%, а AUC0-24ч.- на 113%.
Судя по средним нормализованным по дозе соотношениям Cмакс и AUC0-24ч, содержание соединения (A) в крови у людей-добровольцев имело тенденцию к росту, превышающую пропорциональную дозозависимость, при увеличении дозировки с 60 до 90 мкг один раз в сутки, при сравнении показателей в День 1 и День 10.
Судя по результатам, равновесная концентрация достигается после 7-8 дней лечения при дозировке 60 мкг.
Пример 2. Определение активной дозы соединения (A)
Терапевтическую активность лекарств, представляющих собой антагонисты/обратные агонисты H3-гистаминового рецептора, можно предсказать, оценивая степень занятости их мишеней в мозге, т.е. H3-рецепторов.
Эту степень связывания с лекарственными препаратами у человека можно надежно измерить в ходе замещения ими связанной селективной радиоактивной метки, меченой радиоактивным изотопом с коротким временем жизни, таким как 11-С. В этом случае методика ПЭТ-изображения позволяет неинвазивно измерить занятость рецептора. Данная методика требует введения позитронно-активной радиометки, которая связывается с рецептором, после чего измеряют это связывание на ПЭТ-сканере. Были разработаны радиоактивные лиганды, селективные для H3-рецептора, среди которых [11C]GSK189254 является антагонистом H3-гистаминового рецептора, имеющим высокое сродство. Он характеризуется высокой степенью проникновения в мозг и периодом полувыведения в конечной фазе 1,6 + 0,4 часов. Эту метку недавно применяли для характеристики дозозависимой занятости для новых антагонистов H3-гистаминового рецептора, что подтвердило возможность применения [11C]-GSK189254 для измерения занятости H3-рецепторов у человека с помощью ПЭТ (Ashworth, S., et al., Evaluation of 11C-GSK189254 as a novel radioligand for the H3 receptor in humans using PET. J Nucl Med, 2010. 51(7): p. 1021-9).
Этот метод позволяет предсказать терапевтическую дозу нового обратного агониста/антагониста Н3-рецептора в две стадии: 1) определяют степень занятости рецептора, вызванную дозой, гарантирующей терапевтическую эффективность известного лекарственного средства А; 2) определяют дозу нового лекарственного средства В, обеспечивающую такую же занятость рецептора, какую обеспечивает А в терапевтической дозировке.
Эту стратегию применяли путем сравнения занятости H3R у здоровых добровольцев, получавших питолисант - одобренный и доступный на рынке обратный агонист H3R - в его максимальной пероральной терапевтической дозировке 40мг, с занятостью при введении нескольких дозировок соединения (А).
Занятость H3R после приема 40 мг питолисанта у 6 здоровых добровольцев была равна 82,33 ± 8,71%.
Как показано ниже, была обнаружена очень близкая занятость H3R при дозировке 60 мкг соединения (A), и даже при дозировке 30 мкг соединения (A) все еще наблюдалась очень высокая степень занятости, особенно после повторения приема один раз в сутки в течение 10 дней, когда достигается равновесная концентрация.
Поскольку исследования зависимости эффекта от дозы для питолисанта показали терапевтическую активность при различных патологиях (нарколепсия, избыточная дневная сонливость, связанная с болезнью Паркинсона, или обструктивное нарушение дыхания во сне) при пероральных дозировках от 20 до 40 мг, то приведенные выше результаты приводят к заключению, что терапевтическая доза соединения (A) составляет около 30 - 60 мкг. Таким образом получается, что активность соединения (А) в 1000 раз выше, чем у имеющегося на рынке лекарственного средства питолисанта.
Температуры плавления определяли на приборе Büchi для измерения температуры плавления в капилляре.
Протонные ЯМР-спектры записывали на ЯМР-приборе Varian с рабочей частотой 400 МГц. Значения химических сдвигов δ выражены в миллионных долях. Для обозначения мультиплетности сигналов используются следующие сокращения: с = синглет, д = дублет, т = триплет, кв = квадруплет, м = мультиплет, мс = массив (нагромождение). Записанные спектры соответствуют предложенным структурам.
Инфракрасные спектры (диапазон 4000-450 см-1) записывали на Фурье-ИК спектрометре THERMO Electron Corporation Nicolet 380, оснащенном системой с нарушенным полным отражением. Длины волн приведены в см-1.
Пример 3. (3S)-4-{4-[3-(3-Метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид дигидрохлорид тетрагидрат.
(3S)-4-{4-[3-(3-Метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид дигидрохлорид (210 г) и воду (200 г) загружали в колбу для упаривания. Температуру бани в системе для упаривания устанавливали равной примерно 40°C, и смесь перемешивали до полного растворения осадка. Упаривали воду до отделения продукта в твердой форме.
Колбу для упаривания, содержащую продукт, переносили в полочную вакуумную сушилку и сушили продукт при 30°C. Продукт переносили из колбы для упаривания в контейнер для сушки и продолжали сушку при 30°C до достижения содержания воды в продукте 15,3±0,5 вес.%.
Пример 4. (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид дигидрохлорид тетрагидрат
Загружали ацетон (10 кг) и (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил} пиридин 1-оксид (2,5 кг). Устанавливали температуру равной 30-40°C. Смесь перемешивали до растворения (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил} пиридин 1-оксида, фильтровали под давлением и упаривали. Добавляли раствор хлористоводородной кислоты (32%, 1,84 кг, 2,1 экв.) в воде (2 кг). Устанавливали температуру равной 22-30°C и добавляли ацетон (6 - 7 литров). После внесения затравочных кристаллов добавляли ацетон до общего количества 20 кг при 22-30°C. Полученную суспензию перемешивали при 18-24°C в течение 1-2 часов и фильтровали. Осадок на фильтре промывали смесью ацетона (3,5 кг) и воды (240 г). Продукт сушили в полочной вакуумной сушилке в токе азота (Tмакс = 30°C) до достижения содержания воды 15,0 - 16,5 вес.%.
Пример 5. (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид в виде свободного основания
К (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид дигидрохлориду добавляли этилацетат, воду, концентрированный гидроксид натрия и карбонат натрия для высвобождения свободного основания. Фазы фильтровали через слой целита и декантировали. Органическую фазу промывали насыщенным водным раствором хлорида натрия, сушили над сульфатом магния, фильтровали и упаривали при пониженном давлении, получая (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил} пиридин 1-оксид в виде свободного основания. Полученное свободное основание кипятили в диизопропиловом эфире и оставляли кристаллизоваться при комнатной температуре. Полученный твердый осадок отфильтровывали и сушили при 40°C в вакууме в течение двух дней, получая чистый (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид в виде свободного основания в виде белого твердого вещества, с температурой плавления 91°C.
1H ЯМР (ДМСО-d6): 8,17 (д, 2H), 7,69 (д, 2H), 7,68 (д, 2H), 7,00 (д, 2H), 4,02 (т, 2H), 2,72 (м, 2H), 2,35 (т, 2H), 1,90-1,70 (мс, 3H), 1,65-1,35 (мс, 5H), 0,85-0,75 (мс, 4H).
ИК (основные полосы): 2929, 2766, 1606, 1473, 1465, 1241, 1177, 1061, 1029, 822, 569, 515.
Пример 6. (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид оксалат
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид в виде свободного основания растворяли в ацетоне и добавляли раствор одного эквивалента щавелевой кислоты в ацетоне. Полученную белую суспензию перемешивали 15 часов при комнатной температуре, фильтровали, промывали ацетоном и сушили при 40°C в вакууме в течение двух дней, получая (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил} пиридин 1-оксид оксалат в виде беловатого твердого вещества с температурой плавления 102°C.
1H ЯМР (D2O): 8,12 (д, 2H), 7,65 (д, 2H), 7,58 (д, 2H), 6,95 (д, 2H), 4,06 (м, 2H), 3,41 (м, 1H), 3,34 (м, 1H), 3,16 (м, 2H), 2,70 (т, 1H), 2,43 (т, 1H), 2,150 (м, 2H), 1,85-1,50 (мс, 4H), 0,98 (м, 1H), 0,79 (с, 3H).
ИК (основные полосы): 2963, 2501, 1704, 1602, 1470, 1449, 1409, 1391, 1287, 1256, 1225, 1169, 1052, 826, 815, 766, 695, 574, 449.
Пример 7. (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид L-тартрат тригидрат
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид в виде свободного основания растворяли в этаноле и добавляли раствор одного эквивалента L-винной кислоты в этаноле. Полученную белую суспензию обрабатывали ультразвуком и затем перемешивали 15 часов при комнатной температуре, фильтровали, промывали этанолом и сушили при 45°C в вакууме 15 часов, получая (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид L-тартрат тригидрат в виде белого твердого вещества с температурой плавления 86°C.
1H ЯМР (D2O): 8,19 (д, 2H), 7,73 (д, 2H), 7,66 (д, 2H), 7,02 (д, 2H), 4,40 (с, 2H), 4,12 (м, 2H), 3,46 (м, 1H), 3,39 (м, 1H), 3,21 (м, 2H), 2,75 (т, 1H), 2,45 (т, 1H), 2,15 (м, 2H), 1,89-1,61 (мс, 4H), 1,05 (м, 1H), 0,84 (с, 3H).
ИК (основные полосы): 2982, 2882, 2500, 1650, 1600, 1470, 1260, 1213, 1114, 1070, 1046, 883, 674, 576, 477.
Пример 8. (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид памоат
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид в виде свободного основания и один эквивалент памоевой кислоты кипятили в этаноле. Полученную желтую суспензию перемешивали 15 часов при комнатной температуре и фильтровали. Полученный твердый осадок (который содержит избыток кислоты) кипятили в этаноле, фильтровали в горячем виде, фильтрат упаривали при пониженном давлении и затем растворяли остаток в минимальном количестве горячего этанола. Добавляли метил-трет-бутиловый эфир для осаждения соли. После перемешивания при комнатной температуре в течение 2 дней, фильтрования, промывки метил-трет-бутиловым эфиром и фильтрования, полученное твердое вещество сушили при 45°C в вакууме 15 часов, получая (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид памоат в виде желтого твердого вещества с температурой плавления 179°C.
1H ЯМР (ДМСО-d6): 8,24 (с, 2H), 8,17 (д, 2H), 8,14 (д, 2H), 7,71-7,65 (мс, 6H), 7,18 (м, 2H), 7,06-7,01 (мс, 4H), 4,69 (с, 2H), 4,09 (т, 2H), 2,77 (т, 1H), 2,14 (м, 2H), 1,85-1,61 (мс, 4H), 1,07 (м, 1H), 0,88 (с, 3H). Отсутствующие сигналы закрыты пиками дейтерированного растворителя.
ИК (основные полосы): 2984, 2500, 1644, 1567, 1510, 1445, 1392, 1354, 1214, 1196, 810, 751, 596, 482, 401.
Пример 9. (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид фумарат
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид в виде свободного основания растворяли в горячем ацетоне и добавляли раствор одного эквивалента фумаровой кислоты в горячем ацетоне. Полученную белую смолу кипятили и затем перемешивали 15 часов при комнатной температуре, получая белое твердое вещество. После фильтрования, промывки ацетоном и сушки при 45°C в вакууме в течение 15 часов получали (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил} пиридин 1-оксид фумарат в виде белого твердого вещества с температурой плавления 135°C.
1H ЯМР (ДМСО-d6): 8,18 (д, 2H), 8,14 (д, 2H), 7,70 (д, 2H), 7,68 (д, 2H), 7,01 (д, 2H), 6,53 (с, 2H), 4,04 (т, 2H), 2,90 (м, 2H), 2,56 (м, 2H), 2,06-1,85 (мс, 3H), 1,75 (м, 1H), 1,70-1,50 (мс, 3H), 1,49 (м, 1H), 0,88 (м, 1H), 0,82 (с, 3H).
ИК (основные полосы): 3161, 2500, 1713, 1656, 1574, 1470, 1403, 1339, 1257, 1235, 1144, 1110 1038, 983, 918, 840, 790, 756, 627, 573, 454.
Пример 10. (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид пара-толуолсульфонат сестерцигидрат (2,5)
В суспензию (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксида в виде свободного основания в воде добавляли раствор одного эквивалента пара-толуолсульфокислоты в воде. Полученную гомогенную фазу лиофилизовывали и оставляли при комнатной температуре на открытом воздухе на два дня, получая (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид пара-толуолсульфонат сестерцигидрат в виде беловатого твердого вещества с температурой плавления 201°C.
1H ЯМР (D2O): 8,10 (д, 2H), 7,62 (д, 2H), 7,55 (д, 2H), 7,49 (д, 2H), 7,17 (д, 2H), 6,92 (д, 2H), 4,40 (с, 2H), 4,03 (т, 2H), 3,37 (м, 1H), 3,30 (м, 1H), 3,14 (м, 2H), 2,71 (м, 1H), 2,44 (м, 1H), 2,20 (с, 3H), 2,06 (м, 2H), 1,85-1,50 (мс, 4H), 1,00 (м, 1H), 0,79 (с, 3H).
ИК (основные полосы): 2541, 2353, 1651, 1601, 1469, 1402, 1284, 1224, 1205, 1163, 1119, 1030, 1007, 943, 850, 820, 680, 628, 559, 521, 487.
Пример 11. (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид 1,5-нафталиндисульфонат моногидрат гемиэтанолят
В раствор (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксида в виде свободного основания в этаноле добавляли раствор одного эквивалента 1,5-нафталиндисульфокислоты в этаноле. Полученную суспензию перемешивали при комнатной температуре в течение 15 часов, фильтровали, промывали этанолом и сушили при 40°C в вакууме в течение двух дней, получая (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид 1,5-нафталиндисульфонат моногидрат гемиэтанолят в виде белого твердого вещества с температурой плавления 276°C.
1H ЯМР (D2O): 8,65 (д, 2H), 8,11 (д, 2H), 8,00 (д, 2H), 7,60 (д, 2H), 7,53 (м, 2H), 7,49 (м, 2H), 6,86 (д, 2H), 3,98 (т, 2H), 3,37 (м, 1H), 3,29 (м, 1H), 3,09 (м, 2H), 2,64 (т, 1H), 2,36 (т, 1H), 2,05 (м, 2H), 1,80-1,50 (мс, 4H), 0,95 (м, 1H), 0,77 (с, 3H).
ИК (основные полосы): 3026, 1601, 1487, 1416, 1261, 1213, 1114, 1030, 983, 806, 764, 665, 609, 580, 526, 502.
Пример 12. (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид фосфат
В суспензию (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксида в виде свободного основания в воде добавляли один эквивалент 85%-ной фосфорной кислоты в воде. Полученную гомогенную фазу лиофилизовывали и оставляли при комнатной температуре на открытом воздухе на два дня, получая (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид фосфат в виде белого твердого вещества с температурой плавления 116°C.
1H ЯМР (D2O): 8,11 (д, 2H), 7,64 (д, 2H), 7,57 (д, 2H), 6,95 (д, 2H), 4,05 (м, 2H), 3,42 (м, 1H), 3,34 (м, 1H), 3,15 (м, 2H), 2,70 (т, 1H), 2,43 (т, 1H), 2,10 (м, 2H), 1,85-1,50 (мс, 4H), 0,99 (м, 1H), 0,79 (с, 3H).
ИК (основные полосы): 2975, 2883, 2398, 2351, 1603, 1470, 1259, 1216, 1046, 932, 871, 812, 524, 502, 485, 450.
Пример 13. (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид бромгидрат
В раствор (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксида в виде свободного основания в тетрагидрофуране добавляли один эквивалент 48%-ной бромистоводородной кислоты в воде. Полученную суспензию перемешивали при комнатной температуре в течение 15 часов, упаривали при пониженном давлении и дважды подвергали азеотропной отгонке с этанолом, получая липкое твердое вещество. После разбавления в горячем ацетонитриле, упаривания при пониженном давлении и сушки 40°C в вакууме в течение двух дней получали (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид бромгидрат в виде белого твердого вещества с температурой плавления 76°C.
1H ЯМР (D2O): 8,15 (д, 2H), 7,68 (д, 2H), 7,62 (д, 2H), 6,98 (д, 2H), 4,09 (т, 2H), 3,44 (м, 1H), 3,36 (м, 1H), 3,18 (м, 2H), 2,72 (м, 1H), 2,45 (м, 1H), 2,13 (м, 2H), 1,85-1,55 (мс, 4H), 1,05 (м, 1H), 0,82 (с, 3H).
ИК (основные полосы): 3390, 2930, 2633, 2541, 2360, 1604, 1469, 1227, 1173, 1054, 1029, 945, 821, 568, 518, 487.
Пример 14. (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид 1,2-этандисульфонат
В суспензию (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксида в виде свободного основания в воде добавляли раствор одного эквивалента 1,2 этандисульфокислоты в воде. Полученную гомогенную фазу лиофилизовывали и оставляли при комнатной температуре на открытом воздухе на два дня, получая гигроскопичное твердое вещество. Растирание в тетрагидрофуране, фильтрование и упаривание при 40°C в вакууме в течение двух дней дает (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид 1,2-этандисульфонат в виде бежевого твердого вещества с температурой плавления 155°C.
1H ЯМР (D2O): 8,16 (д, 2H), 7,69 (д, 2H), 7,61 (д, 2H), 6,98 (д, 2H), 4,08 (т, 2H), 3,44 (м, 1H), 3,36 (м, 1H), 3,18 (м, 2H), 2,72 (м, 1H), 2,45 (т, 1H), 2,12 (м, 2H), 1,85-1,55 (мс, 4H), 1,02 (м, 1H), 0,81 (с, 3H).
ИК (основные полосы): 3390, 2944, 2726, 2355, 1600, 1472, 1218, 1166, 1131, 1022, 997, 823, 760, 544, 524, 500.
Пример 15. (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид сульфат
В суспензию (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксида в виде свободного основания в воде добавляли один эквивалент 5н. водного раствора серной кислоты. Полученную гомогенную фазу лиофилизовывали и оставляли при комнатной температуре на открытом воздухе на два часа, получая (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид сульфат в виде беловатого твердого вещества с температурой плавления 71°C.
1H ЯМР (D2O): 8,14 (д, 2H), 7,67 (д, 2H), 7,61 (д, 2H), 6,97 (д, 2H), 4,08 (т, 2H), 3,42 (м, 1H), 3,35 (м, 1H), 3,18 (м, 2H), 2,73 (м, 1H), 2,45 (м, 1H), 2,12 (м, 2H), 1,85-1,55 (мс, 4H), 1,03 (м, 1H), 0,82 (с, 3H).
ИК (основные полосы): 3377, 2931, 2357, 1604, 1470, 1285, 1229, 1174, 1027, 945, 821, 602, 568, 518, 487.
Пример 16. (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид дибромгидрат
В раствор (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксида в виде свободного основания в этаноле добавляли два эквивалента 48%-ной водной бромистоводородной кислоты в воде. В полученный раствор для осаждения добавляли этилацетат и перемешивали при комнатной температуре в течение 15 часов. После фильтрования, промывки этилацетатом и сушки при 40°C в вакууме в течение 15 часов получали (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид дибромгидрат в виде беловатого твердого вещества с температурой плавления 215°C.
1H ЯМР (D2O): 8,24 (д, 2H), 7,76 (д, 2H), 7,67 (д, 2H), 7,03 (д, 2H), 4,13 (т, 2H), 3,49 (м, 1H), 3,41 (м, 1H), 3,25 (м, 2H), 2,78 (м, 1H), 2,50 (т, 1H), 2,18 (м, 2H), 1,90-1,60 (мс, 4H), 1,08 (м, 1H), 0,87 (с, 3H).
ИК (основные полосы): 2930, 2632, 2352, 1601, 1471, 1410, 1292, 1261, 1210, 1182, 1050, 945, 823, 704, 678, 625, 569, 502, 485.
Пример 17. (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид оротат дигидрат
В суспензию (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксида в виде свободного основания в воде добавляли суспензию одного эквивалента оротовой кислоты в воде. Полученную гомогенную фазу лиофилизовывали и оставляли при комнатной температуре на открытом воздухе на 24 часа, получая (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид оротат дигидрат в виде белого твердого вещества с температурой плавления 125°C.
1H ЯМР (D2O): 8,14 (д, 2H), 7,66 (д, 2H), 7,59 (д, 2H), 6,95 (д, 2H), 5,98 (с, 1H), 4,07 (т, 2H), 3,43 (м, 1H), 3,36 (м, 1H), 3,18 (м, 2H), 2,72 (м, 1H), 2,45 (м, 1H), 2,11 (м, 2H), 1,85-1,55 (мс, 4H), 1,04 (м, 1H), 0,82 (с, 3H).
ИК (основные полосы): 2957, 2789, 1667, 1633, 1605, 1472, 1409, 1355, 1285, 1226, 1176, 819, 765, 572, 539, 418.
Пример 18. (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид 5-сульфосалицилат
В раствор (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксида в виде свободного основания в этаноле добавляли раствор одного эквивалента дигидрата 5-сульфосалициловой кислоты в этаноле. Полученную суспензию перемешивали при комнатной температуре в течение 20 часов, фильтровали, промывали этанолом и сушили при 45°C в вакууме 24 часа, получая (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси] фенил}пиридин 1-оксид 5-сульфосалицилат в виде белого твердого вещества с температурой плавления 213°C.
1H ЯМР (D2O): 8,13 (д, 2H), 8,06 (с, 1H), 7,67 (д, 1H), 7,63 (д, 2H), 7,53 (д, 2H), 6,90 (д, 2H), 6,86 (д, 2H), 4,04 (м, 2H), 3,42 (м, 1H), 3,34 (м, 1H), 3,16 (м, 2H), 2,70 (м, 1H), 2,43 (м, 1H), 2,09 (м, 2H), 1,85-1,55 (мс, 4H), 1,02 (м, 1H), 0,81 (с, 3H).
ИК (основные полосы): 2963, 2671, 2556, 2358, 1667, 1602, 1471, 1366, 1290, 1240, 1164, 1149, 1117, 1021, 878, 771, 667, 584, 503.
Пример 19. (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид 1-гидрокси-2-нафтоат моногидрат
В раствор (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксида в виде свободного основания в этаноле добавляли раствор одного эквивалента 1-гидрокси-2-нафтоевой кислоты в этаноле и воде. Полученную гомогенную фазу лиофилизовывали и оставляли при комнатной температуре на открытом воздухе на 24 часа, получая (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид 1-гидрокси-2-нафтоат моногидрат в виде бежевого твердого вещества с температурой плавления 140°C.
1H ЯМР (ДМСО-d6): 8,18 (д, 2H), 8,15 (м, 1H), 7,75-7,65 (мс, 6H), 7,43 (м, 1H), 7,35 (м, 1H), 7,01 (д, 2H), 6,97 (д, 2H), 4,08 (т, 2H), 3,10 (м, 2H), 2,60 (м, 1H), 2,10 (м, 2H), 1,85-1,60 (мс, 4H), 1,02 (м, 1H), 0,87 (с, 3H). Отсутствующие сигналы закрыты пиками дейтерированного растворителя.
ИК (основные полосы): 3500, 2356, 1609, 1580, 1471, 1402, 1367, 1313, 1239, 1175, 1035, 984, 806, 774, 578, 491, 447, 426.
Пример 20. (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид 3-гидрокси-2-нафтоат
В раствор (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксида в виде свободного основания в этаноле добавляли раствор одного эквивалента 3-гидрокси-2-нафтоевой кислоты в этаноле. Полученную гомогенную фазу упаривали при пониженном давлении, получая маслянистый остаток. Затем добавляли ацетон, и раствор упаривали при пониженном давлении, получая желтое твердое вещество. Добавляли минимальное количество ацетона и каплю воды, и полученную суспензию обрабатывали ультразвуком и перемешивали при комнатной температуре в течение 20 часов. После фильтрования, промывки ацетоном и сушки в вакууме при 45°C в течение 24 часов получали (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид 3-гидрокси-2-нафтоат в виде беловатого твердого вещества с температурой плавления 199°C.
1H ЯМР (ДМСО-d6): 8,26 (с, 1H), 8,18 (д, 2H), 7,72 (д, 1H), 7,70-7,65 (мс, 4H), 7,56 (д, 2H), 7,31 (т, 1H), 7,13 (т, 1H), 7,01 (д, 2H), 6,94 (с, 1H), 4,08 (т, 2H), 3,11 (м, 2H), 2,64 (м, 1H), 2,11 (м, 2H), 1,85-1,60 (мс, 4H), 1,02 (м, 1H), 0,87 (с, 3H). Отсутствующие сигналы закрыты пиками дейтерированного растворителя.
ИК (основные полосы): 2931, 2355, 1645, 1603, 1519, 1464, 1446, 1351, 1238, 1173, 841, 818, 739, 594, 577, 478.
Пример 21. (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид сесквигликолят моногидрат
В раствор (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксида в виде свободного основания в тетрагидрофуране добавляли раствор одного эквивалента гликолевой кислоты в тетрагидрофуране. Полученную суспензию перемешивали при комнатной температуре в течение 24 часов. После фильтрования, промывки тетрагидрофураном и сушки в вакууме при 45°C в течение 24 часов получали (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид сесквигликолят моногидрат в виде беловатого твердого вещества с температурой плавления 82°C.
1H ЯМР (D2O): 8,19 (д, 2H), 7,71 (д, 2H), 7,65 (д, 2H), 7,01 (д, 2H), 4,12 (т, 2H), 3,48 (м, 1H), 3,41 (м, 1H), 3,22 (м, 2H), 2,76 (м, 1H), 2,49 (т, 1H), 2,17 (м, 2H), 1,90-1,60 (мс, 4H), 1,06 (м, 1H), 0,86 (с, 3H).
ИК (основные полосы): 3258, 3102, 2930, 2356, 1603, 1470, 1411, 1287, 1232, 1177, 1059, 947, 819, 696, 568, 509, 456.
Пример 22. Сравнительные данные фармакокинетики у мышей.
Соединения вводили самцам домовой мыши в дозировке около 1 мг основания на килограмм. Через 24 часа брали образцы плазмы крови и мозга. Результаты приведены в таблице 1 с нормализацией на 1 мг основания на килограмм.
Таблица 1. Данные фармакокинетики для описанных в Примерах соединений
В определенной степени, описанные в Примерах соединения показывают одинаковую скорость абсорбции. Соотношения значений AUC для Примеров и значения AUC для дигидрохлорида тетрагидрата приведены в таблице 2. Все соотношения попадают в диапазон от 0,6 до 1,2, что соответствует близости их значений, с учетом экспериментальной погрешности в этих тестах.
Таблица 2. Соотношение значений AUC в плазме
Выдающийся результат был получен для памоата (Пример 8). Памоатные (эмбонатные) соли обычно используются для получения лекарственных средств с замедленным высвобождением (см., например зипадера/зипрекса релпревв - памоат оланзапина, который принимают раз в 2-4 недели).
Пример 8 показывает близкое значение AUC и время достижения Cмакс в сравнении с дигидрохлоридом тетрагидрата (Пример 4).
Таким образом, соединение A по настоящему изобретению позволяет применять низкие дозировки, вне зависимости от его солей и/или их сольватов.
Пример 1. диаграмма XRPD для (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил} пиридин 1-оксид L-тартрата
2-Тета °
Ангстрем
импульсы
%
Пример 2. диаграмма XRPD для (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксида памоата
2-Тета °
Ангстрем
импульсы
%
Пример 3: диаграмма XRPD для (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксида фумарата
2-Тета °
Ангстрем
импульсы
%
Пример 4. диаграмма XRPD для (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксида пара-толуолсульфоната
2-Тета °
Ангстрем
импульсы
%
Пример 5. диаграмма XRPD для (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксида 1,5-нафталиндисульфоната
2-Тета °
Ангстрем
импульсы
%
Пример 6: диаграмма XRPD для (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил} пиридин 1-оксида фосфата
2-Тета °
Ангстрем
импульсы
%
Пример 7. диаграмма XRPD для (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксида бромгидрата фаза A
2-Тета °
Ангстрем
импульсы
%
Пример 8. диаграмма XRPD для (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксида бромгидрата фаза B
2-Тета °
Ангстрем
импульсы
%
Пример 9. диаграмма XRPD для (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил} пиридин 1-оксида 1,2-этандисульфоната
2-Тета °
Ангстрем
импульсы
%
Пример 10. диаграмма XRPD для (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксида сульфата фаза A
2-Тета °
Ангстрем
импульсы
%
Пример 11. диаграмма XRPD для (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксида сульфата фаза B
2-Тета °
Ангстрем
импульсы
%
Пример 12. диаграмма XRPD для (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксида оротата
2-Тета °
Ангстрем
импульсы
%
Пример 13. диаграмма XRPD для (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксида 5-сульфосалицилата
2-Тета °
Ангстрем
импульсы
%
Пример 14. диаграмма XRPD для (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксида 1-гидрокси-2-нафтоата
2-Тета °
Ангстрем
импульсы
%
Пример 15. диаграмма XRPD для (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксида 3-гидрокси-2-нафтоата фаза A
2-Тета °
Ангстрем
импульсы
%
Пример 16. диаграмма XRPD для (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксида 3-гидрокси-2-нафтоата фаза B
2-Тета °
Ангстрем
импульсы
%
Пример 17. диаграмма XRPD для (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил} пиридин 1-оксида гликолята
2-Тета °
Ангстрем
импульсы
%
| название | год | авторы | номер документа |
|---|---|---|---|
| ТЕТРАГИДРАТ Н3-ЛИГАНДА, СПОСОБ ЕГО ПОЛУЧЕНИЯ И СОДЕРЖАЩИЕ ЕГО ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ | 2018 |
|
RU2771753C2 |
| НОВЫЕ ПРОИЗВОДНЫЕ ПИПЕРИДИНА | 2006 |
|
RU2417985C2 |
| КОНДЕНСИРОВАННОЕ 4-ОКСОПИРИМИДИНОВОЕ ПРОИЗВОДНОЕ | 2005 |
|
RU2358969C2 |
| СОЛИ И КРИСТАЛЛИЧЕСКИЕ ФОРМЫ | 2014 |
|
RU2654855C2 |
| ТРИЦИКЛИЧЕСКОЕ СОЕДИНЕНИЕ И ЕГО ФАРМАЦЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ | 2020 |
|
RU2833354C1 |
| НОВОЕ ПРОИЗВОДНОЕ 3-ГИДРОКСИ-5-АРИЛИЗОТИАЗОЛА | 2010 |
|
RU2567755C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ПРОИЗВОДНЫЕ ПИРИДОНА | 2012 |
|
RU2585287C2 |
| ПРОИЗВОДНЫЕ АМИНОПИРИДИНА И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ СЕЛЕКТИВНЫХ ИНГИБИТОРОВ ALK-2 | 2022 |
|
RU2803084C1 |
| НЕСТЕРОИДНЫЕ МОДУЛЯТОРЫ ГЛЮКОКОРТИОДИДНЫХ РЕЦЕПТОРОВ ДЛЯ МЕСТНОЙ ДОСТАВКИ ЛЕКАРСТВ | 2016 |
|
RU2731618C2 |
| ПРОИЗВОДНЫЕ ПИПЕРАЗИНИЛПИПЕРИДИНА В КАЧЕСТВЕ АНТАГОНИСТОВ ХЕМОКИНОВОГО РЕЦЕПТОРА | 2005 |
|
RU2369604C2 |
Изобретение относится к применению (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксида или его фармацевтически приемлемой соли и/или сольвата указанного соединения (A) или его соли для лечения и/или предотвращения у людей заболеваний, выбранных из следующих: болезнь Альцгеймера; нарушение внимания; инсомния и нарушение запоминания; когнитивные расстройства в психиатрических патологиях; когнитивные расстройства, расстройства настроения и концентрации, в особенности у пожилых пациентов; депрессивные или астенические состояния; болезнь Паркинсона; синдром обструктивного апноэ во сне; деменция с тельцами Леви; сосудистая деменция; головокружение; укачивание; ожирение; диабет и метаболический синдром; нарушения сна; стресс; психотропные нарушения; эпилепсия; депрессия; нарколепсия с катаплексией или без неё; нарушения гипоталамо-гипофизной секреции, мозгового кровообращения и/или в иммунной системе; избыточная дневная сонливость, такая как избыточная дневная сонливость и усталость, связанная с болезнью Паркинсона, синдромом обструктивного апноэ во сне или деменцией; и/или для облегчения работы по ночам или для адаптации к смене часового пояса у здоровых людей; злоупотребление веществами, в частности злоупотребление алкоголем; предотвращение синдрома отмены при злоупотреблении веществами; нарушения внимания; постинсультные усталость, расстройства настроения, концентрации и когнитивные расстройства; когнитивные нарушения при аутизме; хроническая боль и хроническая усталость; нарушения внимания и концентрации при СДВГ (синдром дефицита внимания и гиперактивности) у взрослых или после инсульта, где указанное применение включает введение соединения (A) или его фармацевтически приемлемых солей, и/или сольватов указанных солей или указанного соединения (A), взрослому человеку, с дозировкой свободного основания между 20 и 50 мкг в сутки (в пересчете на соединение (A) в форме свободного основания). 2 н. и 10 з.п. ф-лы, 38 пр., 2 табл.
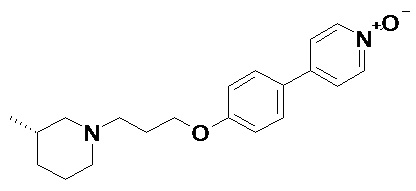
1. Применение (3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксида, имеющего формулу (A):
(A)
или его фармацевтически приемлемой соли и/или сольвата указанного соединения (A) или его соли, для лечения и/или предотвращения у людей заболеваний, выбранных из следующих: болезнь Альцгеймера; нарушение внимания; инсомния и нарушение запоминания; когнитивные расстройства в психиатрических патологиях; когнитивные расстройства, расстройства настроения и концентрации, в особенности у пожилых пациентов; депрессивные или астенические состояния; болезнь Паркинсона; синдром обструктивного апноэ во сне; деменция с тельцами Леви; сосудистая деменция; головокружение; укачивание; ожирение; диабет и метаболический синдром; нарушения сна; стресс; психотропные нарушения; эпилепсия; депрессия; нарколепсия с катаплексией или без неё; нарушения гипоталамо-гипофизной секреции, мозгового кровообращения и/или в иммунной системе; избыточная дневная сонливость, такая как избыточная дневная сонливость и усталость, связанная с болезнью Паркинсона, синдромом обструктивного апноэ во сне или деменцией; и/или для облегчения работы по ночам или для адаптации к смене часового пояса у здоровых людей; злоупотребление веществами, в частности злоупотребление алкоголем; предотвращение синдрома отмены при злоупотреблении веществами; нарушения внимания; постинсультные усталость, расстройства настроения, концентрации и когнитивные расстройства; когнитивные нарушения при аутизме; хроническая боль и хроническая усталость; нарушения внимания и концентрации при СДВГ (синдром дефицита внимания и гиперактивности) у взрослых или после инсульта, где указанное применение включает введение соединения (A) или его фармацевтически приемлемых солей, и/или сольватов указанных солей или указанного соединения (A), взрослому человеку, с дозировкой свободного основания между 20 и 50 мкг в сутки (в пересчете на соединение (A) в форме свободного основания).
2. Применение по п. 1, где нарушения сна включают бессонницу, нарушения инициирования и поддержания сна, фрагментацию сна, парасомнию; нарушения фазы быстрого движения глаз во сне, нарушение дыхания во сне, суточную аритмию, нарколепсию с катаплексией или без неё, избыточную дневную сонливость (включая «приступы непреодолимого сна»), такую как избыточная дневная сонливость, связанная с болезнью Паркинсона, обструктивным апноэ во сне или деменцией.
3. Применение по п. 1 или 2, где соединение (A) находится в форме его фармацевтически приемлемых солей, таких как гидрохлорид, оксалат, дигидрохлорид, гидробромид, дигидробромид, нафталин-1,5-дисульфонат, сульфат, этан-1,2-дисульфонат, цикламат, толуолсульфонат, паратолуолсульфонат, тиоцианат, нитрат, метансульфонат, додецилсульфат, нафталин-2-сульфонат, бензолсульфонат, дихлорацетат, глицерофосфат, 2-гидроксиэтансульфонат, аспартат, малеат, фосфат, этансульфонат, камфор-10-сульфонат, глутамат, альгинат, памоат, 2-оксо-глутарат, 1-гидрокси-2-нафтоат, малонат, гентизат, салицилат, тартрат, фумарат, галактарат, цитрат, глюкуронат, лактобионат, 4-аминосалицилат, гликолят, сесквигликолят, глюкогептаноат, пироглутамат, манделат, малат, гиппурат, формиат, глюконат, лактат, олеат, аскорбат, бензоат, сукцинат, 4-ацетамидобензоат, глутарат, циннамат, адипат, себакат, камфорат, ацетат, капроат, никотинат, изобутират, пропионат, карат, лаурат, пальмитат, стеарат, ундецен-10-оат, каприлат, оротат, карбонат, 5-сульфосалицилат, 1-гидрокси-2-нафтоат, 3-гидрокси-2-нафтоат; и/или сольватов, таких как гидраты, этанолят, гемиэтанолят.
4. Применение по пп. 1, 2 или 3, где соединение (A) находится в форме гидрохлорида.
5. Применение по любому из предшествующих пунктов, где соединение (A) находится в форме дигидрохлоридной соли.
6. Применение по любому из предшествующих пунктов, где соединение (A) находится в форме тетрагидрата дигидрохлорида.
7. Применение по любому из предшествующих пунктов, где суточная дозировка для введения человеку составляет от 30 до 45 мкг в сутки (в пересчете на соединение (A) в форме свободного основания).
8. Применение по любому из предшествующих пунктов, где соединение (A) вводят один раз в сутки или один раз в два дня.
9. Применение по любому из предшествующих пунктов, где соединение (A) вводят один раз в сутки.
10. Применение по любому из предшествующих пунктов, где соединение (A) вводят перорально.
11. Применение по любому из предшествующих пунктов, выбранное из группы, состоящей из следующих соединений:
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид дигидрохлорид тетрагидрат;
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид оксалат;
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид L-тартрат и его тригидрат;
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид памоат;
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид фумарат;
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид пара-толуолсульфонат и его сестерцигидрат (2,5);
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид 1,5-нафталиндисульфонат и его гемиэтанолят моногидрат;
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид фосфат;
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид бромгидрат;
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид 1,2-этандисульфонат;
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид сульфат;
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид дибромгидрат;
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид оротат и его дигидрат;
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид 5-сульфосалицилат;
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид 1-гидрокси-2-нафтоат и его моногидрат;
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид 3-гидрокси-2-нафтоат;
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид (сескви)гликолят и его моногидрат.
12. Соединение, выбранное из группы, состоящей из следующих соединений:
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид дигидрохлорид тетрагидрат;
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид L-тартрат и его тригидрат;
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид памоат;
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид фумарат;
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид пара-толуолсульфонат и его сестерцигидрат (2,5);
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид 1,5-нафталиндисульфонат и его гемиэтанолят моногидрат;
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид фосфат;
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид бромгидрат;
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид 1,2-этандисульфонат;
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид сульфат;
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид дибромгидрат;
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид оротат и его дигидрат;
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид 5-сульфосалицилат;
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид 1-гидрокси-2-нафтоат и его моногидрат;
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид 3-гидрокси-2-нафтоат;
(3S)-4-{4-[3-(3-метилпиперидин-1-ил)пропокси]фенил}пиридин 1-оксид (сескви)гликолят и его моногидрат.
| WO 2006117609 A2, 09.11.2006 | |||
| Устройство для предупреждения столкновений поездов | 1925 |
|
SU6254A1 |
| СПОСОБ ПОЛУЧЕНИЯ МЯГЧИТЕЛЕЙ ДЛЯ КАУЧУКОВИ РЕЗИН | 0 |
|
SU197840A1 |
| Модуляционное устройство | 1930 |
|
SU22746A1 |
Авторы
Даты
2021-10-25—Публикация
2018-03-21—Подача