Изобретение относится к области медицины, в частности к онкогематологии и может быть использовано для оценки динамики прироста донорских эритроцитов после трансплантации костного мозга и/или гемопоэтических стволовых клеток (ГСК) от неидентичного по системе АВО донора. Определение количества эритроцитов, имеющих фенотип донора, осуществляется методом агглютинации в геле путем сравнения относительного количества эритроцитов, экспрессирующих и неэкспрессирующих информативный антиген, со шкалой-идентификатором донорского химеризма.
Цель изобретения - разработка способа оценки посттрансплантационного химеризма при анализе экспрессии антигенов эритроцитов А и В.
Аллогенная трансплантация гемопоэтических стволовых клеток (аллоТГСК) - один из эффективных методов лечения тяжелых гематологических и онкологических заболеваний системы крови, а также ряда наследственных болезней. Результативность терапии доказана у пациентов с острыми лейкозами, хроническим миелолейкозом, злокачественными лимфомами, первичными иммунодефицитами [1, 2]. Потенциальный успех аллоТГСК, приводящий к долгосрочной выживаемости больных, зависит от функциональной активности гемопоэтических стволовых клеток и развития посттрансплантационных осложнений - отторжения трансплантата, реакции «трансплантат против хозяина», парциальной красноклеточной аплазии, рецидива основного заболевания, инфекционных осложнений [3, 4, 5]. Мониторинг приживления ГСК необходим для планирования сопроводительной терапии. Показателем, отражающим работу донорской кроветворной ткани, является посттрансплантационный химеризм. Существует ряд методов отслеживания донорского химеризма.
Известны способы оценки присутствия в организме различных клеточных линий на основании генетических маркеров. К ним относятся цитогенетический и FISH-анализ, которые могут применяться для определения химеризма только в тех ситуациях, когда донор и реципиент разного пола или пациент имеет хромосомные особенности. Такие ограничения приводят к редкому использованию данных методов [1, 6, 8].
Известен способ оценки донорского химеризма, основанный на выявлении индивидуальных отличий в структуре ДНК с применением ПЦР в реальном времени. В настоящее время для определения химеризма у больных после аллоТГСК данный метод считается наиболее востребованным, так как обладает возможностью ранней диагностики химеризма [7, 8]. Недостатком исследования структур ДНК является невозможность оценки функциональной состоятельности эритроидного ростка кроветворения и диагностики парциальной красноклеточной аплазии - тяжелого осложнения ТГСК.
Наиболее близким к предполагаемому изобретению является модифицированный микрометод дифференциальной агглютинации по Эшби, оценивающий количество эритроцитов в крови реципиента, экспрессирующих донорские антигены, с помощью камеры Горяева [9]. Данное исследование позволяет оценить работу эритроцитарного ростка донорского костного мозга, диагностировать парциальную красноклеточную аплазию. Недостатком этого метода является отсутствие автоматизации, необходимость дополнительных манипуляций, выходящих за рамки стандартных иммуногематологических исследований.
Техническим результатом заявляемого изобретения является создание способа диагностики донорского химеризма при исследовании антигенов системы АВО методом агглютинации в геле с моноклональными антителами анти-А, анти-В. Технология анализа экспрессии антигенов позволяет определить относительное количество эритроцитов, имеющих происхождение из донорского ростка кроветворения, отследить динамику прироста донорского химеризма после трансплантации ГСК, установить парциальную красноклеточную аплазию костного мозга. Преимущества данного метода заключаются в высокой скорости исполнения и использовании стандартных иммуногематологических методов исследования.
Для достижения поставленной цели в соответствии с аналогом [9] проводят типирование антигенов АВО донора и реципиента и выявляют различия экспрессии антигенов, позволяющие дифференцировать эритроциты, происходящие из ростков кроветворения донора и реципиента. В отличие от прототипа, в котором проводится подсчет количества связанных с антиэритроцитарными антителами клеток в камере Горяева с последующим расчетом % эритроцитов донора, в предлагаемом способе осуществляется анализ донорского химеризма на основании сопоставления результатов АВО-тестирования в гелевой карте со шкалой-идентификатором. Анализ химеризма проводится методом агглютинации в геле.
В процессе проведения патентно-информационного поиска не выявлено источников, порочащих новизну предполагаемого изобретения.
Заявляемое изобретение разработано в лаборатории иммуногематологии ФГБУН КНИИГиПК ФМБА России в соответствии с планом научно-исследовательской работы.
Способ осуществляется следующим образом.
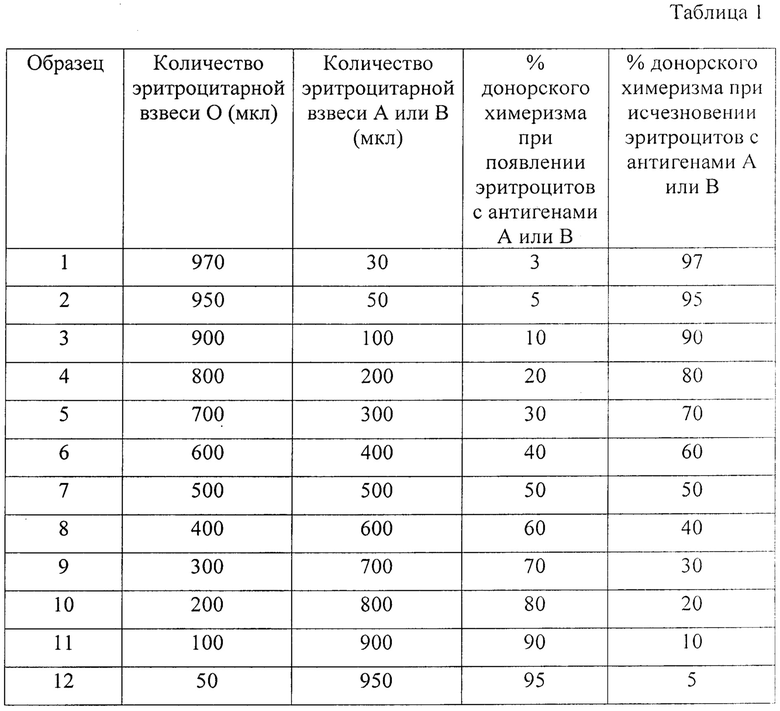
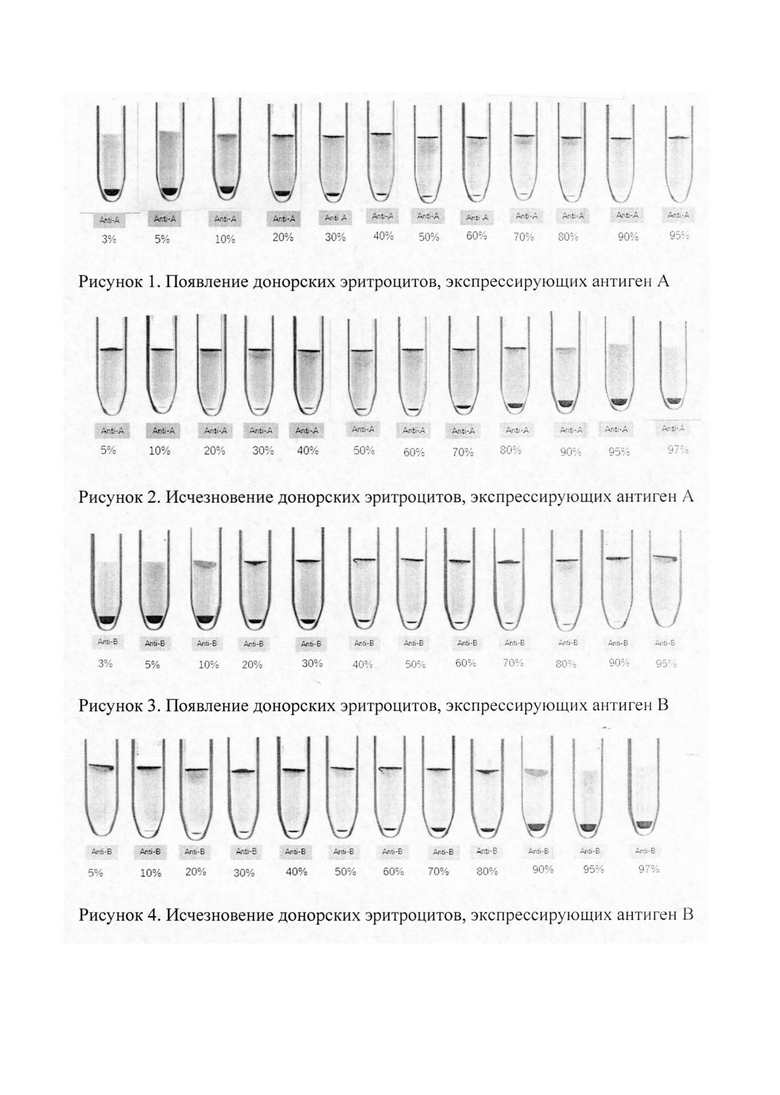
Этап 1. Создают шкалу-идентификатор процента донорского химеризма. С этой целью эритроциты из образцов крови доноров О, А и В трижды отмывают от плазмы в физиологическом растворе и ресуспензируют в растворе низкой ионной силы в соотношении 1:1. Перемешивают на вортексе. Маркируют пробирки с ЭДТА от 1 до 12. В соответствии с таблицей 1 в пробирки вносят заданный объем взвеси эритроцитов О и А группы (или О и В группы, в зависимости от установленного информативного маркера). Полученную смесь эритроцитов из каждой пробирки вносят в гелевые карты с соответствующими по специфичности моноклональными антителами. Центрифугируют и фотодокументируют результат. Формируют шкалу-идентификатор, отражающий различное процентное соотношение эритроцитов О и А (или О и В) в образце (рисунок 1, 2, 3, 4).
Этап 2. До трансплантации ГСК проводят типирование антигенов АВО эритроцитов донора и реципиента. Определяют информативные антигены, позволяющие установить различия эритроцитов донора и реципиента по системе АВО. Антиген считается информативным, если он выявлен в фенотипе реципиента и отсутствует в фенотипе донора или наоборот. Прогнозируют вектор донорского химеризма - появление или исчезновение эритроцитов, экспрессирующих информативный антиген.
Этап 3. После трансплантации ГСК исследование гемопоэтического химеризма проводят с 21 дня каждую неделю до +50 дня и далее по показаниям. Выполняют стандартное иммуногематологическое определение АВО-принадлежности крови реципиента. Анализируют процентное соотношение эритроцитов, экспрессирующих и не экспрессирующих информативные антигены. Оценку количественных значений химеризма осуществляют путем визуального сравнения результата исследования со шкалой-идентификатором процента донорского химеризма.
Представленные ниже клинические примеры подтверждают возможность использования заявляемого способа при оценке эритроцитарного химеризма после аллоТГСК.
Пример 1
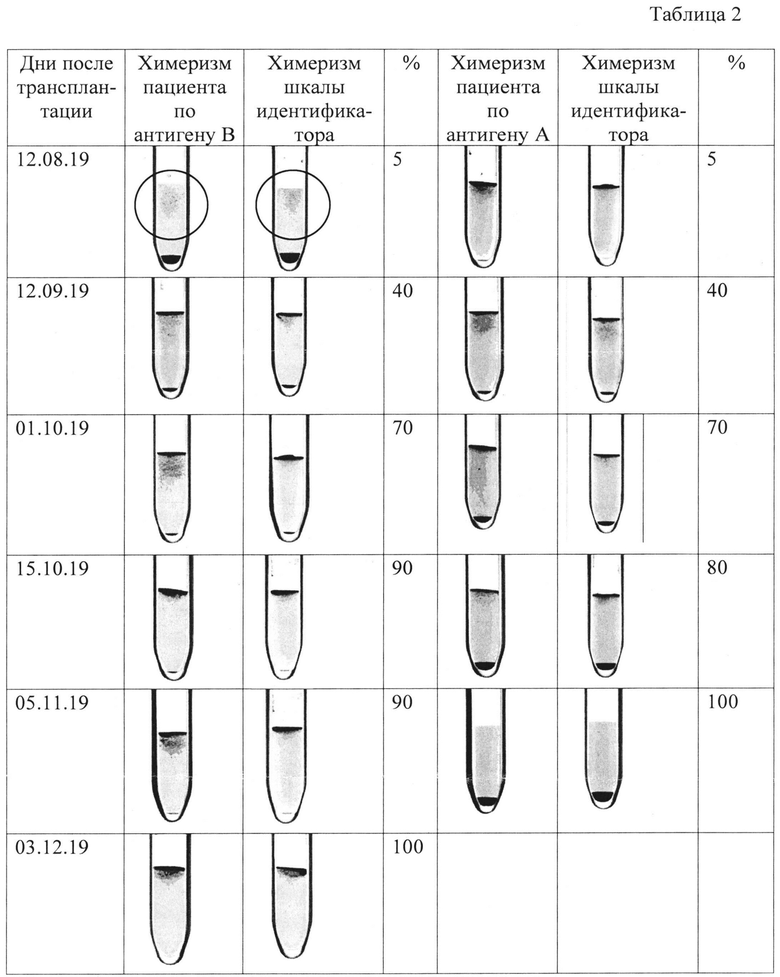
Пациент Г., 31 год с диагнозом: Острый лимфобластный лейкоз. Группа крови A ccDEE К- Cw-, анти-В антитела IgM - 1:8, IgG - не выявлены. Донор ГСК HLA-идентичный сиблинг с группой крови В ccDEe Κ- Cw-, анти-А антитела IgM - 1:32, IgG - не выявлены. Информативными были признаны антигены А и В, предполагалось появление клеток, экспрессирующих антиген В (B↑) и исчезновение эритроцитов, несущих антиген A (A↓) после трансплантации. АллоТГСК выполнена 26.07.2019. Трансфузионная тактика предусматривала трансфузии отмытых облученных эритроцитов О ccDEEK-. Исследования эритроцитарного химеризма выполнены на 17, 48, 67, 81, 102, 130, 360 дни после пересадки (таблица 2). Донорский химеризм 5% зарегистрирован на +17 день. Донорский химеризм 100% по антигену А установлен на +102 день, по антигену В - на +130 день. При обследовании через 1 год после трансплантации подтверждена полная ремиссия заболевания, донорский эритроцитарный химеризм - 100%. Больной ведет полноценную жизнь хорошего качества.
Пример 2
Пациентка П., 46 лет с диагнозом острый миелоцитарный лейкоз. Группа крови О CcDee К- Cw- (анти-А IgM - 1:8, IgG - 1:4). Донор ГСК родственный идентичный по системе HLA - A ccdee К- Cw-. Информативным признан антиген А, который экспрессировался на донорских эритроцитах и не экспрессировался на клетках реципиента. Предполагалось отслеживать появление клеток, имеющих в фенотипе антиген А (А↑). Аллогенная трансплантация ГСК выполнена 18.12.2019. При необходимости трансфузий эритроцитов переливались отмытые облученные эритроциты О ccdee К- Cw-. В течение 200 дней после ТГСК у реципиента не выявлялись эритроциты с фенотипом донора (таблица 3). Установлен диагноз: красноклеточная аплазия после аллогенной родственной совместимой ТГСК, ремиссия на основании трепанобиопсии +50 день после ТГСК. Скорректирована терапия. В течение 6 месяцев после трансплантации у пациентки наблюдалось постепенное снижение титров антиэритроцитарных анти-А антител. 06.07.20 (+201 день) было зафиксировано появление эритроцитов, характерных для донора ГСК, и последующее быстрое нарастание донорского химеризма. Анти-А антитела не выявлены. При обращении пациентки на +271 день после ТГСК выявлено 80% посттрансплантационных донорских эритроцитов. Пациентка активна, чувствует себя хорошо.
Список литературы
1. Блау О.В. Химеризм после аллогенной трансплантации гемопоэтических стволовых клеток. // Клиническая онкогематология 2013; 6(1): 34-39.
2. Лавритенко В.А., Майренко Ю.Е., Березовская Е.Ю. и др. Становление донорского химеризма у пациентов с первичными иммунодефицитами после аллогенной трансплантации гемопоэтических стволовых клеток. // Клиническая онкогематология 2018; 13(2): 82-92.
3. Lion F., Watzinger S., Preuner Η. et al. The EuroChimerism concept for a standardized approach to chimerism analysis after allogeneic stem cell transplantation// Leukemia, 2012, 26(8): 1821-1828.
4. Schäfer S.H., Finke J. Mismatched unrelated alternative donors for hematological malignancies. Semin Hematol 2016; 53 (2): 77-81.
5. Менделеева Л.П., Мишин Η.Ε., Клясова Γ.Α., Любимова Л.С. и др. Инфекции в течение первых 100 дней после трансплантации гемопоэтических клеток. // Гематология и трансфузиология 2007; 52 (4):8-15.
6. Fehse В., Chuchlovin Α., Kuhcke К. et al. Real-time quantitative Y chromosome-specific PCR (QYCS-PCR) for monitoring hematopoietic chimerism after sex-mismatched allogeneic stem cell transplantatoin// J. Hematother. Cell Res., 2001, 10(3): 419-425.
7. Bader P., Niethammer D., Willasch Α., Kreyenberg H., Klingebiel T. How and when should we monitor chimerism after allogeneic stem cell transplantation? Bone Marrow Transplant. 2005; 35(2): 107-19.
8. Лавриненко Β.Α., Савицкая Т.В., Волочник Ε.В. и др. Количественный анализ химеризма после аллогенной трансплантации гемопоэтических стволовых клеток молекулярно-генетическими методами // Онкогематология 2014; 9(2): 29-36.
9. Порешина Л.П. Эритроцитарный химеризм при аллогенной близкородственной трансплантации костного мозга // Автореферат дис... док. Биол. наук. - М., 2004. - 35 с.

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ определения уровня посттрансплантационного химеризма путем оценки экспрессии антигенов системы Резус и Келл в гелевых картах | 2021 |
|
RU2761100C1 |
| Способ определения посттрансплантационного химеризма при анализе точечных мутаций замены оснований в генах F2, F5, F7, F13, FGB, ITGA2, ITGB3, PAI-1 | 2017 |
|
RU2667006C1 |
| Способ определения гемопоэтического химеризма при исследовании однонуклеотидных полиморфизмов генов MTHER: 677, MTHER: 1298, MTR: 2756, MTRR: 66 | 2017 |
|
RU2667127C1 |
| Способ профилактики несостоятельности трансплантата аллогенного костного мозга или гемопоэтических стволовых клеток при наличии у реципиента донор-специфичных анти-HLA антител | 2022 |
|
RU2833126C2 |
| СПОСОБ ЛЕЧЕНИЯ РЕЦИДИВА ОСТРОГО МИЕЛОИДНОГО ЛЕЙКОЗА ПОСЛЕ ТРАНСПЛАНТАЦИИ АЛЛОГЕННЫХ ГЕМОПОЭТИЧЕСКИХ СТВОЛОВЫХ КЛЕТОК | 2013 |
|
RU2538799C1 |
| Способ оценки наличия неродственных доноров в виртуальном регистре произвольных размеров с прогнозированием возможности нахождения полностью или частично совместимого донора костного мозга и гемопоэтических стволовых клеток | 2024 |
|
RU2840759C1 |
| УСТРОЙСТВА И СПОСОБЫ ДЛЯ ОТБОРА КЛЕТОК, УСТОЙЧИВЫХ К АПОПТОТИЧЕСКИМ СИГНАЛАМ, И ОБЛАСТИ ИХ ПРИМЕНЕНИЯ | 2013 |
|
RU2630301C2 |
| КОМБИНИРОВАННАЯ ТЕРАПИЯ ДЛЯ СТАБИЛЬНОГО И ДОЛГОВРЕМЕННОГО ПРИЖИВЛЕНИЯ ТРАНСПЛАНТАТА С ИСПОЛЬЗОВАНИЕМ КОНКРЕТНЫХ ПРОТОКОЛОВ ДЛЯ Т/В-КЛЕТОЧНОЙ ДЕПЛЕЦИИ | 2012 |
|
RU2648354C2 |
| Т-КЛЕТКИ ЦЕНТРАЛЬНОЙ ПАМЯТИ ПРОТИВ ТРЕТЬЕЙ СТОРОНЫ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ИХ ПРИМЕНЕНИЕ В ТРАНСПЛАНТАЦИИ И ЛЕЧЕНИИ ЗАБОЛЕВАНИЙ | 2009 |
|
RU2506311C2 |
| Способ прогноза развития раннего рецидива у больных классической лимфомой Ходжкина | 2019 |
|
RU2702360C1 |
Изобретение относится к области медицины. Описан способ оценки эритроцитарного химеризма при исследовании антигенов АВО, включающий формирование шкалы-идентификатора процента донорского химеризма, типирование антигенов АВО эритроцитов донора и реципиента, определение информативных антигенов, мониторинг эритроцитарного химеризма после трансплантации аллогенных гемопоэтических стволовых клеток. Заявленный способ отличается тем, что производится сопоставление результатов АВО-тестирования реципиента со шкалой-идентификатором, причем в качестве детектирующего метода используют агглютинацию в гелевой колонке; наличие донорского химеризма диагностируют при обнаружении у реципиента эритроцитов, несущих антигены АВО донора; отсутствие донорского химеризма - при отсутствии у реципиента эритроцитов, экспрессирующих АВО антигены донора. Изобретение расширяет арсенал способов оценки состояния кроветворной системы пациента после трансплантации аллогенных гемопоэтических стволовых клеток, отслеживать динамику прироста донорского химеризма, устанавливать парциальную красноклеточную аплазию костного мозга, что необходимо для планирования и коррекции сопроводительной терапии больного. 4 ил., 3 табл., 2 пр.
Способ оценки эритроцитарного химеризма при исследовании антигенов АВО, включающий формирование шкалы-идентификатора процента донорского химеризма, типирование антигенов АВО эритроцитов донора и реципиента, определение информативных антигенов, мониторинг эритроцитарного химеризма после трансплантации аллогенных гемопоэтических стволовых клеток, отличающийся тем, что производится сопоставление результатов АВО-тестирования реципиента со шкалой-идентификатором, причем в качестве детектирующего метода используют агглютинацию в гелевой колонке; наличие донорского химеризма диагностируют при обнаружении у реципиента эритроцитов, несущих антигены АВО донора; отсутствие донорского химеризма - при отсутствии у реципиента эритроцитов, экспрессирующих АВО антигены донора.
| СПОСОБ ОПРЕДЕЛЕНИЯ БИОЛОГИЧЕСКОЙ СОВМЕСТИМОСТИ ЭРИТРОЦИТАРНОЙ МАССЫ КРОВИ ДОНОРА И КРОВИ РЕЦИПИЕНТА | 2001 |
|
RU2193197C1 |
| Способ определения посттрансплантационного химеризма при анализе точечных мутаций замены оснований в генах F2, F5, F7, F13, FGB, ITGA2, ITGB3, PAI-1 | 2017 |
|
RU2667006C1 |
| Способ определения гемопоэтического химеризма при исследовании однонуклеотидных полиморфизмов генов MTHER: 677, MTHER: 1298, MTR: 2756, MTRR: 66 | 2017 |
|
RU2667127C1 |
| Mehdi Alizadeh et al | |||
| Quantitative assessment of hematopoietic chimerism after bone marrow transplantation by real-time quantitative polymerase chain reaction | |||
| Blood, 2002, 99(12) p | |||
| ПРИБОР ДЛЯ ИЗМЕРЕНИЯ ВОЛЬТАМПЕР ИЛИ ВОЛЬТАМПЕРЧАСОВ В СЕТИ ПЕРЕМЕННОГО ТОКА | 1925 |
|
SU4618A1 |
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
| R.L | |||
| Niece A Differential Hemolysis | |||
Авторы
Даты
2021-10-26—Публикация
2020-10-28—Подача