Настоящее изобретение относится к новому диметоксибензилсульфо-производному хиназолин-4(3Н)-она, характеризующемуся высокой анальгетической, противопаркинсонической, анксиолитической и психостимулирующей активностью в сочетании с низкой токсичностью, и поэтому может найти применение в химико-фармацевтической промышленности и медицине. Оно касается применения бензил тиопроизводного хиназолин-4(3Н)-она для получения лекарственных средств, которые могут быть использованы как обезболивающие, противопаркинсонические, психостимулирующие препараты, дневные транквилизаторы. Соединение может быть использовано для получения лекарственных средств для лечения болевого синдрома; паркинсонизма; при неврозах, неврозоподобных состояниях, психосоматических нарушениях, сопровождающихся эмоционально-стрессорными расстройствами и астенией. Изобретение расширяет число средств, обладающих психостимулирующей активностью.
Предшествующий уровень техники
Результаты научного поиска веществ, воздействующих на центральную нервную систему, среди целенаправленно синтезированных биологически активных соединений, востребованы и определены актуальностью проблемы создания новых отечественных оригинальных лекарственных препаратов. Создание новых анальгезирующих лекарственных препаратов - безопасных и высокоэффективных - актуальной задача для фармакологии и фармации, решить которую возможно при синтезе и исследовании новых биологически активных соединений [1-4]. Известны производные 4-(3)хиназолинона, влияющие на ЦНС, однако обладающие значительной токсичностью [5].
При поиске нейротропных веществ делается акцент на целенаправленный синтез соединений, проявляющих агонистическую активность к дофаминовым рецепторам. Рост числа людей старших возрастных групп в структуре общества сопровождается увеличением частоты встречаемости болезни Паркинсона, ставшей социальной проблемой. При фармакотерапии болезни Паркинсона на ранних стадиях рекомендуется использование дофаминомиметических средств, способных проявлять нейропротекторную активность, защищать от негативного влияния нейроны и восстанавливать поврежденные нервные клетки. Нейропротекторная активность установлена для ряда производных хиназолинона-4 [6,7]. Интересными представляются исследователям гидрокси- и метоксифенильные производные хиназолинона-4, которые могут обладать дофаминергической активностью.
Создание новых лекарственных средств с противотревожным действием позволит улучшить лекарственное лечение тревожных нарушений, зачастую сопровождающих депрессивные расстройства и другие психоневрологические патологические состояния. Существующие анксиолитики оказывают выраженное седативное действие, амнестическое влияние, вызывают неблагоприятные изменения картины крови и т.д., не рекомендованы при деятельности, связанной с необходимостью концентрации внимания. В этой связи выигрышными будут соединения, сочетающие в спектре активности 2 и более видов положительного действия.
Наиболее близкие по структуре к заявляемому соединению - гидрокси- и метоксипроизводные 4-(3)хиназолинона, обладающие дофаминергической активностью [8].
Данные сведения свидетельствуют о перспективности поиска новых эффективных и безопасных обезболивающих, противопаркинсонических веществ, обладающих анксиолитическими свойствами, в ряду производных 3H-хиназолин-4-она.
Настоящее изобретение относится к новому сульфопроизводному хиназолин-4(3Н)-она, обладающему обезболивающей, противопаркинсонической, психостимулирующей способностью в сочетании с транквилизирующими свойствами и практически полным отсутствием токсичности.
Технический результат: получено новое сульфопроизводное 4-(3H)хиназолинона, обладающее анальгетическим действием, которое в тестах с формалином, «уксусные корчи» превосходит препараты сравнения метамизол натрия и лидокаин. Соединение проявляет противопаркинсонические свойства, превосходя в тесте галоперидоловой каталепсии антикаталептогенное действие бромокриптина, леводопы. Полученное соединение также обладает транквилизирующим действием, которое в тестах «приподнятый крестообразный лабиринт», «открытое поле», многопараметрическое тестирование превосходит референтный препарат диазепам. Вновь полученное соединение обладает психостимулирующим действием, превосходящим в тесте «боковое положение» прототип кофеин бензоат-натрий. Соединение 1 получено новым методом.
Заявляемый объект - 2-(3,4-диметоксибензил-6-сульфо)хиназолин-4(3Н)-он формулы (1), обладающий анальгетической, противопаркисонической, анксиолитической и психостимулирующей активностью.
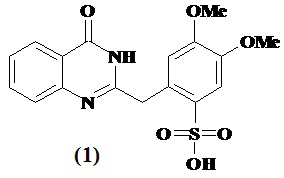
Способ получения 2-(3,4-диметоксибензил-6-сульфоно)-хиназолин-4(3Н)-она (1) основан на взаимодействии 2-(3,4-диметоксибензил)-(3Н)-хиназолин-4-она [9] с концентрированной серной кислотой при комнатной температуре с последующим выделением продукта реакции при разбавлении реакционной смеси водой.
СХЕМА ПОЛУЧЕНИЯ
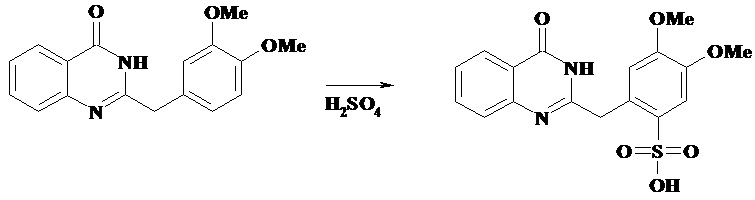
Новое соединение - тиопроизводное 4-(3Н)-хиназолинона - проявляет анальгетическое, противопаркинсоническое, анксиолитическое и психостимулирующее действие.
ПРИМЕР СИНТЕЗА
При комнатной температуре при перемешивании растворяют 3.0 г (0.01 моль) 2-(3,4-диметоксибензил)хиназолин-4(3Н)-она в 15 мл концентрированной серной кислоты. Гомогенную реакционную смесь выдерживают 10-12 часов при комнатной температуре и выливают в 150 г смеси воды со льдом. Отфильтровывают образовавшийся бесцветный осадок, тщательно промывают на фильтре водой и изопропиловым спиртом. Высушенный на воздухе продукт дальше используют без дополнительной очистки. Выход 80%. Т.пл.> 300 °C. 1H NMR (600 MHz, DMSO-d6 , δ, м.д.): 3.55 (s, 6H, 2OCH3), 4.70 (s, 2H, CH2), 6.94 (s, 1H, ar.), 7.38 (s, 1H, ar.), 7.20-7.55 (d.+t, 2H, ar.), 7.83 (t, 1H, ar.), 8.25 (d. 2H, ar.).
Оценка фармакологической активности
Фармакологическая активность соединения оценивалась по четырем направлениям. Было изучено обезболивающее, противопаркинсоническое, анксиолитическое, психостимулирующее действие соединения 1.
Для исследований использовались белые половозрелые крысы-самцы (по 5-11 в группе) и самки (по 10-12 в группе) линии Вистар массой 200-250 г, которых содержали при свободном доступе к воде и пище в стандартных условиях вивария. Уход, кормление, работу с животными осуществляли в соответствии с международными рекомендациями по защите позвоночных животных, применяемых для экспериментов либо в иных научных целях [10-12].
Контрольными животными в каждой серии опытов для каждой методики при оценке исследуемой активности являлись группы крыс - самок, самцов, которым вводили внутрибрюшинно растворитель в объеме 0,4 мл (1-2 капли твина-80 на 10 мл воды) либо физиологический раствор (группа контрольная для животных, получавших в аналогичных режимах прототипы - референсные препараты (метамизол натрия, лидокаин, бромокриптин, диазепам). Группы животных состояли из 5-12 особей (опытные, контрольные, препараты сравнения). Все растворы веществ во всех сериях исследований инъецировались интраперитонеально. С учетом хронотропной активности психотропных препаратов эксперименты проводили в дневное (с 12-00 до 17-00 ч) и вечернее время (с 18-00 до 20-00 ч) [13].
Статистический анализ результатов исследования проведен с применением пакетов компьютерных программ «Excel», «BIOSTAT», «Statistica 10». Определяли нормальность распределения полученных данных с применением критерия Шапиро-Уилка. t-критерий Стьюдента использовали при нормальном распределении полученных данных. При распределении данных исследования, отличных от нормального, применены критерии Краскела-Уоллиса, U-критерий Уилкоксона-Манна-Уитни. Был проведен сравнительный анализ, в ходе которого сопоставлены результаты опытных групп с данными контрольных животных (принятые равными 100%). Сравнительный анализ отличий в действии веществ у самок животных проводили также в стадиях эстрального цикла диэструс ½ и проэструс/эструс. Статистически значимыми приняты отличия при р<0‚05 для всех видов анализа [14-16 ].
Анальгезирующую активность соединения 1 изучали в тестах с формалином и «уксусные корчи»; противопаркинсоническое действие - на модели галоперидоловой каталепсии; транквилизирующую активность - в тестах приподнятого крестообразного лабиринта, «открытого поля», многопараметрического тестирования, психостимулирующую активность - на модели «бокового положения» [11,12].
Анальгетическая активность
Влияние заявляемого объекта на анальгезирующую активность проводилось на моделях ноцицептивных реакций, вызываемых химическими раздражителями (формалиновый тест и «уксусные корчи»). С помощью тестов оценивался периферический уровень болевой чувствительности [17].
Формалиновый тест позволяет оценить соматическую боль, индуцированную альгогенами, имитирует реакции при оперативных разрезах кожи. Первая (острая) стадия развивается сразу при воздействии болевого фактора, проявляется действием на первичные афференты боли; вторая (воспалительная) стадия - во времени отсрочена и вызвана воспалительным ответом. Болевая чувствительность моделировалась субплантарным введением 50 мкл водного раствора 2% формалина в тыльную поверхность задней правой лапки. В последующем в течение 60 минут наблюдения регистрировали ответные ноцицептивные реакции («flinches»: поднятие лапки, облизывание, покусывание места инъекции): 1) первые 10 минут от момента введения формалина (острая фаза); 2) с 10-й по 60-ю минуты болевой реакции (воспалительная фаза). Обезболивающий эффект исследуемого соединения определяли суммарно и отдельно для I и II фаз болевого ответа по снижению числа ответных реакций по отношению к показателям контрольной группы животных, принятых за 100%.
В условиях модели «Уксусные корчи» оценена выраженность перитовисцеральной боли. С помощью данной методики общепринятой висцеральной ноцицепции исследована периферическая противоболевая активность новых веществ с применением химического альгогена для раздражения ноцирецепторов брюшины и оценены специфические двигательные ответные реакции - «корчи». «Корчи» - это характерные болевые поведенческие ответы, которые возникают под воздействием химических раздражителей на серозные оболочки, проявляются сокращением и расслаблением абдоминальной мускулатуры, вытягиванием задних лапок, прогибом спины, сходны с перитонеальной болью. «Корчи» вызывали однократным инъецированием 1% раствора уксусной кислоты (0,5 мл/100 г массы тела животного; интраперитонеально). Обезболивающий эффект оценен по снижению числа «корчей» за 15 минут наблюдения после введения раствора уксусной кислоты (в % к показателям контрольной группы животных, принятым равными 100%).
Субстанцию 1 в дозе 0,2 от молекулярной массы в мг/кг (75,2 мг/кг), референсные препараты в терапевтически эффективных дозах: метамизол натрия - 55 мг/кг (Metamizolum natrium; анальгин, раствор для внутривенного и внутримышечного введения 500 мг/мл ампулы 2 мл; «Мосхимфармпрепараты им. Н. А. Семашко», Россия), лидокаин - 1 мг/кг (Lidocainum; ампулы 2% 2 мл; «Дальхимфарм», Россия) вводили внутрибрюшинно однократно за 40 минут до начала введения химических раздражителей. Доза исследованного соединения 1 и референсных препаратов подобраны методом титрования доз и с учетом литературных данных [18-19]. Самцам и самкам контрольных групп инъецировались соответственно солюбилизат твина-80 и дистиллированная вода (0,4 мл внутрибрюшинно) в аналогичных режимах. С учетом различий в активности лекарственных средств в зависимости от пола, фаз эстрального цикла исследования проведены у самцов и самок крыс, в том числе у самок в различных фазах эстрального цикла (ЭЦ). До начала тестирования по вагинальным мазкам самок животных определяли фазы эстрального цикла (проэструс / эструс (ПЭ) и диэструс ½ (Д)) [13]. Эксперименты проведены в дневное время.
При изучении анальгезирующей активности по тестам с формалином и «уксусные корчи» была отмечена высокая активность соединения 1 (таблица 1, 2). По сравнению с данными группы контрольных самцов при использовании соединения 1 в формалиновом тесте подавлялось ощущение боли, эффективнее аналогов: более чем в 1,42 раза метамизола натрия и в 2,61 раза - лидокаина. В тесте «уксусные корчи» при применении соединения 1 по сравнению с данными самцов контрольной группы ограничивалось ощущение боли эффективнее аналога лидокаина в 4,66 раза.
При тестировании «уксусных корчей» на фоне использования соединения 1 у самок статистически значимо ограничивалась частота болевых ответных реакций (таблица 3). При этом эффект соединения 1 был отчетливее по сравнению с действием лидокаина.
При анализе обезболивающей активности изучаемой субстанции 1 у самок животных с учетом фазы эстрального цикла отмечали статистически значимое снижение числа болевых реакций. При использовании у самок соединения 1 уменьшалось число болевых ответов в целом и на протяжении всех этапов тестирования с формалином, статистически значимо в стадии физиологического покоя - диэструсе ½ (таблица 4). При этом снижение частоты поднятий лапки, облизываний, покусываний места инъекции под влиянием соединения 1 было более выражено по сравнению с эффектами препарата сравнения.
В тесте «уксусные корчи» при введении соединения 1 достоверно ограничивалось число «корчей» у самок крыс, пребывающих в диэструсе ½ (таблица 5). При этом снижение числа «уксусных корчей» было более выражено по сравнению с действием лидокаина у самок животных в фазе эстрального цикла диэструс ½.
Следовательно, соединение 1 уменьшало частоту болевых ответов в тестах с формалином и «уксусные корчи» у самок животных, проявляя обезболивающую активность.
Вывод: соединение 1 обладает анальгезирующей активностью, превышающей действие препаратов сравнения метамизола натрия, лидокаина.
Антикаталептическая активность
Противопаркинсонический (антикаталептический) эффект соединения 1 изучали на половозрелых особях белых крысах самках (линии Вистар, массой 200-250 г, по 9-11 в группах) в тесте галоперидоловой каталепсии (галоперидол в дозе 1 мг/кг интраперитонеально) [13]. Соединение 1 в дозе 75,2 мг/кг (в суспензии с твин-80), референтные препараты бромокриптин (в дозе 0,125 мг/кг) (Bromocriptinum, таблетки 2,5 мг, «Gedeon Richter», Hungary), леводопа (в дозе 10 мг/кг) (Syndopa, таблетки 250 мг, Levodopum 250 мг + Carbidopum 25 мг, «Sun Pharmaceutical Industries Ltd.», India) вводились интраперитонеально одновременно с галоперидолом (Haloperidolum, таблетки 1,5 мг, «Биоком», Россия). Группам контрольных самок в аналогичном режиме вводился нейролептик. Опыты проводились в дневные часы.
Определена динимика двигательных нарушений у животных на фоне изученных веществ. Оценены изменения выраженности галоперидоловой каталепсии - латентных периодов времени (в секундах, с) вертикализации (в «позе лектора») - продолжительности сохранения животным вертикального положения на опоре. Установлены периоды времени, после которого животное убирала одну / вторую лапу: 1-й / 2-й результаты. Регистрация результатов проведена после введения солюбилизата соединения 1, раствора препаратов сравнения бромокриптина, синдопы через 30, 60, 120, 180 минут [11, 12]. Определены фазы эстрального цикла у самок крыс (проэструс / эструс, диэструс ½) по мазкам влагалищным.
При использовании сочетания соединения 1 с нейролептиком на 120-й и 180-й минутах теста ослаблялись двигательные нарушения, статистически значимо на 120-й минуте тестирования (таблицы 6, 7). Эффект был отчетливее, нежели при введении препаратов сравнения.
Вывод: соединение 1 обладает антикаталептогенной активностью, превышающей действие препаратов бромокриптина, леводопы в исследованных дозах.
Анксиолитическая активность
Оценку транквилизирующей активности соединения 1 по тесту «приподнятый крестообразный лабиринт» (ПКЛ) [20] проводили в экспериментальной установке, представляющей собой 4 рукава, размером 50×10 см, скрепленных под прямым углом друг с другом. Два противоположных рукава ПКЛ закрытые (огражденные с двух сторон, темные) и два других открытые (светлые). Лабиринт поднят над уровнем пола на высоту 0,5 м. Высота стенок в закрытых рукавах равна 10 см. Сверху рукава открыты. В месте пересечения (под прямым углом) рукавов находится площадка размерами 10×10 см. В ходе тестирования животных помещали на центральную площадку лабиринта и далее в течение 5 мин визуально регистрировали параметры поведения: общее число заходов в рукава лабиринта (открытые либо закрытые) и время нахождения в них (с). Анксиолитическую активность исследуемого соединения определяли по учащению заходов животного в светлые (открытые) рукава и увеличению времени пребывания в них, снижению количества заглядываний и времени нахождения в темных (закрытых) рукавах [11, 12].
Исследование выполнено на белых крысах самцах. Cоединение 1 в дозе 37,6 мг/кг (0,1 от молекулярной массы в мг/кг), референтный препарат - прототип диазепам в дозах 0,1 и 0,5 мг/кг (Diazepamum, раствор для внутривенного и внутримышечного введения 10 мг/2 мл; ампулы 2 мл; «Relanium», «Polfа», Poland) инъецировали однократно интраперитонеально за 40 минут до начала тестирования. Контрольным самцам в аналогичных режимах инъецировали внутрибрюшинно физиологический раствор.
При введении соединения 1 ограничивалось время нахождения в темных рукавах лабиринта при одновременном снижении частоты заходов в них по сравнению с параметрами поведения контрольных животных группы К1. На фоне влияния соединения 1 количество заходов в темные рукава статистически значимо было меньше, нежели под влиянием диазепама в исследованной дозе (таблица 8). Также учащался медленный груминг на фоне соединения 1 (889%, P=0,05).
Вывод. Соединение 1 проявляло анксиолитическое антифобическое действие у самцов крыс в перекрестном крестообразном лабиринте. При этом антифобическое влияние соединения 1 было более выражено, нежели у препарата сравнения диазепама в исследованной дозе.
При исследовании противотревожной активности соединения 1 по методике «открытого поля» [21] регистрировали: 1) латентный период выхода из центра поля; 2) горизонтальную двигательную активность - число пересеченных секторов; 3) вертикальную активность - количество вертикальных стоек; 4) исследовательскую активность - число обследованных отверстий - «норок» (обнюхивание); 5) быстый груминг - количество актов быстрого умывания; 6) число болюсов. Время проведения эксперимента составляло 2 мин. По совокупности повышения латентного периода выхода из центра поля, снижения вертикальной и горизонтальной активности судили о «седативном» действии вещества, при повышении исследовательской активности, ограничении частоты быстрого груминга и числа фекальных болюсов (вегетативная представленность стресса) - «противотревожном» действии [22].
Оценка действия соединения 1 на поведение самцов крыс в тесте «открытое поле» выявила статистически значимое повышение исследовательской активности и урежаение частоты быстрого груминга, что свидетельствовало о снижении эмоциональности животных. По сравнению с влиянием диазепама на фоне применения соединения 1 статистически значимо больше было количество исследованных «норок», достоверно снижалась частота быстрого груминга (таблица 9). Также на фоне использования соединения 1 учащался медленный груминг (333%, P=0,01).
Вывод. При тестировании самцов крыс в открытом поле соединение 1 проявляло противотревожное действие. Противотревожный эффект был выраженнее по сравнению с влиянием диазепама в исследованных дозах.
Многопараметрическое тестирование
В последние годы получили распространение психофармакологические методы оценки транквилизирующей активности психотропных лекарственных средств, основанные на регистрации поведенческого ответа грызунов, подвергнутых стресс-воздействиям. Наряду с методикой конфликтной ситуации применяются дискриминационные тесты. В каждом из методов оценивается изменение определенного поведенческого ответа у животных, который рассматривается как проявление тревожности, надежно воспроизводится стимулами, провоцирующими тревожность у человека, и подавляется транквилизаторами [11, 12].
С целью комплексного исследования эмоционального поведенческого статуса у животных был использован многопараметрический метод оценки тревожно-фобических состояний. Метод учитывает характер видоспецифического реагирования грызунов на серию этологически адекватных тест-стимулов, провоцирующих проявления страха и тревоги, не вызывающих возникновение сильных конкурентных мотиваций, легко воспроизводимых при неоднократном повторении опытов [23]. Многопараметрическое тестирование позволяет выявить основные особенности изменения поведенческой активности и оценить анксиолитический эффект при использовании методических приемов, получить системное, целостное представление о действии испытуемого вещества.
В основе тестов многопараметрического метода положены ситуации, формирующие у животных ответные реакции на страх и тревогу: 1) столкновение с неизвестными объектом («неживым») или ситуацией (1-4 тесты) и 2) манипуляции руки экспериментатора (5-8 тесты). Алгоритм тестирования был единым: последовательно от 1 к 8 тесту.
Первый - «step-down» тест характеризует инстинктивно-оборонительное поведение животного. Тестирование проводилось следующим образом: на ровную горизонтальную ярко освещенную поверхность устанавливали параллелепипед из органического стекла размером 20×14×14 см (бокс). Крысу помещали на верхнюю часть бокса и начинали отсчет времени, за которое животное спускалось на пол всеми четырьмя лапами. В случае, когда крыса оставалась наверху бокса в течение 180 с, действие считалось не выполненным, тест завершали, давая оценку в 3 балла.
Во втором тестировании используется двухкамерный бокс размером 20×20×30 см с перегородкой, в центре которой имеется отверстие 7×10 см. Крысу помещали в одно из отделений бокса и фиксировали время, за которое она переходила в другой отсек, пересекая линию перегородки всеми четырьмя лапами.
Третье тестирование проводили с помощью «домика», представляющего собой камеру из прозрачного органического стекла размером 16×15×15 см, одна из стен которой имела открывающееся отверстие для свободного выхода животного из замкнутого пространства. Крысу помещали в «домик», закрывали отверстие и устанавливали в центре ярко освещенной площадки. Через 15 секунд «домик» открывали и фиксировали время выхода животного.
Исследования по тестам 4-8 проводили в «открытом поле».
В четвертом тесте оценивали возникновение страха и тревоги перед открытым и незнакомым пространством, связываемое со снижение двигательной активности. Животное помещали в центр поля и регистрировали время, в течение которого крыса пересекала четыре центральных квадрата всеми лапами. Если животное не покидало центр поля за 60 с, действие считалось не выполненным, тест завершали, но продолжали наблюдение (5-8 тесты).
Пячение животных оценивали на действие руки экспериментатора. Спонтанное пячение и пячение, вызванное любым внешним раздражителем, наблюдается часто у крыс с патологическим чувством страха и тревоги, что является достоверным показателем эмоционального состояния животного.
Тесты 5 - 8 позволяют оценить поведение животного на действие руки экспериментатора: приближение и поглаживание. Тестирование проводили, медленно приближая руку к морде крысы, чтобы животное видело руку. Приближение и поглаживание проводили 2-3 раза подряд. Интенсивность ответной реакции оценивалась в пределах от 0 до 3 баллов (в тестах шкалы применялось дискретное ранжирование с интервалом в 1 балл). Большей выраженности ответной реакции соответствовала большая (в баллах) оценка, отсутствию реакции - низшая оценка, и, следовательно, более низкий тревожно-фобический уровень.
Ответы оценивали в баллах: по тестам 1-2: 0 - 0 < t < 30 c; 1 - 30 < t < 60 c; 2 - 60 < t < 180 c; 3 - не спускается (не проходит) за 180 с. По тесту 3: 0 - 0 < t < 15 c; 1 - 15 < t < 30 c; 2 - 30 < t < 180 c; 3 - не выходит за 180 с. По тесту 4: 0 - 0 < t < 15 c; 1 - 15 < t < 30 c; 2 - 30 < t < 60 c; 3 - не выходит за 60 с. В случае колебаний у животного при выполнении тестов 2 и 3 (незавершенный переходили выход, выглядывание) оценку увеличивали на 0,5 балла. При невыполнении крысой действий по тестам 1-4 давали оценку 3 балла. Интервалы между тестами 1-3 составляли 15-20 минут.
По тестам 5-8 отсутствие реакций животного в ответ на «живой объект» оценивалось по минимуму - 0 баллов. При возникновении реакции на контактный раздражитель (поглаживание) присуждали меньшее число баллов - 1, чем на дистантный (приближение руки) - 2 балла. Сохранение указанных реакций (в случае возникновения) после прекращения действия раздражителей оценивалось по максимуму - 3 балла.
Суммарный показатель по тестам 1-4 (ИДА - индекс двигательной активности) позволяет оценить «седативный» (повышение показателя, снижение двигательной активности) или активирующий (снижение показателей, повышение двигательной активности) эффект. Суммарный показатель по тестам 5-8 (индекс эмоциональной реактивности-ИЭР) позволяет судить о «противотревожном» (снижение показателей, уменьшение эмоциональной реактивности) или «анксиогенном» (повышение показателей, рост эмоциональности) действии исследуемого вещества [22, 24].
На фоне использовании соединения 1 у самцов животных отмечалось повышение латентного времени выхода из центра поля, вместе с тем, ускорялись переходы через отверстие бокса. При этом статистически значимо снижалась интенсивность реакций пячения, затаивания, вокализации и прижимания ушей, достоверно снижался индекс эмоциональной реактивности (ИЭР). В группе животных, получавших диазепам, снижалось латентное время выполнения тестов по отношению к данным контрольной группы, ограничивался ИДА. По сравнению с влиянием диазепама на фоне применения соединения 1 снижалась выраженность ответных реакций животных при воздействии раздражителей, снижался показатель эмоциональной реактивности (таблица 10).
Вывод. При многопараметрическом тестировании самцов крыс соединение 1 при однократном введении проявляло противотревожное действие. Противотревожный эффект был выраженнее по сравнению с влиянием диазепама в исследованных дозах.
Психостимулирующая активность
Психостимулирующий эффект соединения 1 изучали на половозрелых особях белых крыс самцов (линии Вистар, массой 200-250 г, по 7-10 в группах) в тесте «бокового положения» [11, 12]. Методика позволяет выявить наличие психостимулирующего / гипногенного действия веществ по боковому положению животных на фоне высоких доз гипнотических препаратов. Основана методика на способности животных оставаться в «некомфортной» позе под действием высоких доз гипногенных веществ. Животные контрольной группы при переворачивании в неудобную для них позу на спине немедленно рефлекторно возвращаются к нормальному положению. При наличии у изучаемых веществ снотворного действия животные остаются в «боковом положении» - неудобной позе на боку либо на спине. В ходе наблюдения исследователи регистрируют латентный период времени возникновения бокового положения и его продолжительность.
Соединение 1 в дозе 75,2 мг/кг (в суспензии с твин-80), вводили внутрибрюшинно однократно за 45 минут до введения раствора тиопентала-натрия в дозе 30 мг/кг (Thiopentalum Natrium, лиофилизат для приготовления раствора для внутривенного введения; 1,0 г активного вещества во флаконе вместимостью 20 мл; «СИНТЕЗ», ОАО, Россия). Аналогично введены референтные препараты: кофеин бензоат-натрия в дозе 0,5 мг/кг (Coffeinum natrii benzoas; раствор для инъекций 100 мг/мл ампулы 1 мл; «Новосибхимфарм АО», Россия) и аминазин в дозе 0,7 мг/кг мг/кг (Chlorpromazinum; раствор для инъекций 25 мг / мл, ампулы 1 мл; «Новосибхимфарм АО», Россия). Дозы исследованных соединений и референтных препаратов подобраны методом титрования доз и с учетом литературных данных. Животным контрольной группы инъецирован один тиопентал-натрий 30 мг/кг внутрибрюшинно.
При использовании сочетания соединения 1 и тиопентала-натрия отмечались не уснувшие животные (таблица 11). Кроме того, статистически значимо снижалась продолжительность сна. Эффект был отчетливее, нежели при введении препарата сравнения с психостимулирующем действием кофеина бензоата-натрия.
Вывод: соединение 1 обладает психостимулирующей активностью, превышающей действие препарата кофеина бензоата-натрия в исследованной дозе.
Острая токсичность
Определение острой токсичности и расчет LD50 у мышей самцов и самок осуществляли по методу Беренса и установили, что для соединения (I) для мышей самок LD50=1526,85 мг/кг массы тела животных, для мышей самцов LD50=750 мг/кг массы тела животных при внутрибрюшинном введении.
LD50 метамизола натрия для мышей - 250 мг/кг (внутрибрюшинно) [25]. LD50 лидокаина: для крыс равен 317 мг/кг, для мышей составил 220 мг/кг (перорально) [26]. LD50 бромокриптина: для крыс - 72 мг/кг (внутривенно) [27]; бромокриптина мезилата: для крыс - 10,5 мг/кг (внутривенно), мышей - 189 мг/кг (внутривенно) [28].
LD50 диазепама для мышей - 700 мг/кг, крыс - 1200 мг/кг (перорально) [29].
Таким образом, исследуемое соединение (1) является малотоксичным, относится к IV классу токсичности по Сидорову К.К. (1973) [30].
Вывод. Результаты исследований показывают, что изучаемое соединение 1 обладает обезболивающей, антикаталептической, транквилизирующей и психостимулирующей активностью.
Список источников
1. The Concise Guide to PHARMACOLOGY 2015/16: G Protein-Coupled Receptors. CGTP Collaborators [Теxt] / S. P. H. Alexander [et all] // Br. J. Pharmacol. - 2015. - Vol. 172. - P. 5744-5869. doi: 10.1111/bph.13348.
2. Al-Hasani R. Molecular Mechanisms of Opioid Receptor-Dependent Signaling and Behavior / R. Al-Hasani, M. R. Bruchas // Anesthesiology. - 2011. - Vol. 115. - P. 1363-1381.
3. Simonson B. Pharmacology and anti-addiction effects of the novel κ opioid receptor agonist Mesyl Sal B, a potent and long-acting analogue of salvinorin / B. Simonson [et all] // Br. J. Pharmacol. - 2015. - Vol. 172. - P. 515-531. doi: 10.1111/bph.12692.
4. Емельянова Т.Г. Противовоспалительная и анальгетическая активности дипептида Tyr-Pro и его аналогов / Т. Г. Емельянова [и др.] // Академический журнал Западной Сибири. - 2014. - Т. 10, № 4 (53). - С. 88-89.
5. Guzman D.S. Evaluation of thermal antinociceptive effects and pharmacokinetics after intramuscular administration of butorphanol tartrate to American kestrels (Falco sparverius) / D. S. Guzman, T. L. Drazenovich, B. KuKanich, G. H. Olsen //American journal of veterinary research. - 2014. - Vol. 75, № 1. - P. 11-18.
6. Кодониди И.П. Синтез и биологическая активность N-гетероциклических производных 1,4-дигидро-4-оксопиримидина / И. П. Кодониди [и др.] // Вопросы биологической, медицинской и фармацевтической химии. - 2012. - №4. - С. 19-26.
7. Aminoquinazoline cannabinoid receptor modulators for treatment of disease and their preparation / Gahman, Timothy C.; Thomas, David J.; Lang, Hengyuan; Massari, Mark E. // PCT Int. Appl. (2008), WO 2008157500 A1 20081224.
8. Овакимян А.Г., Бичеров А.А., Кодониди И.П., Оганесян Э.Т., Манвелян Э.А., Бичеров А.В., Зайченко С.Б., Тюрин Р.В., Манвелян М.М. Прогноз, синтез и изучение дофаминергической активности гидрокси- и метоксифенильных производных 4-(3)хиназолинона // Современные проблемы науки и образования. - 2015. - № 2-2. - С. 511.
9. Манвелян Э.А., Манвелян М.М., Оганесян Э. Т., Кодониди И.П., Зайченко С.Б., Бичеров А.А., Бичеров А.В. 2-бензилпроизводное 4-(3 H)-хиназолинона, обладающее анальгезирующим, противопаркинсоническим, антигипоксантным, транквилизирующим действием. - Патент на изобретение №2715884. Дата выдачи: 24.01.2020.
10. Червонская Г.П., Панкратова Г.П., Миронова Л.Л. Этика медико-биологического эксперимента в доклинических исследованиях // Токсикологический вестник. - 1998. - №3. - C. 2-8.
11. Руководство по проведению доклинических исследований лекарственных средств. Часть первая / под общей редакцией А.Н. Миронова. - М.: Гриф и К, 2012. - 944 с.
12. Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ [Текст] / под ред. Р. У. Хабриева. - М., 2005. - 512 с.
13. Манвелян Э.А., Батурин В.А., Колодийчук Е.В. Гендерные различия в эффективности психотропных и кардиотропных лекарственных средств: монография. - Ставрополь, 2016. - 130 с.
14. Гланц С. Медико-биологическая статистика: [пер. с англ.]. - Москва: Практика, 1999.
15. Реброва О.Ю. Статистический анализ медицинских данных. Применение пакета прикладных программ STATISTICA. - Москва: МедиаСФЕРА, 2006.
16. Гржибовский А.М., Иванов С.В., Горбатова М.А. Сравнение количественных данных двух независимых выборок с использованием программного обеспечения STATISTICA и SPSS: параметрические и непараметрические критерии // Наука и Здравоохранение. - 2016. - № 2. - С. 5-29.
17. Воронина Т.А., Гузеватых Л.С. Mетодические рекомендации по изучению анальгетической активности лекарственных средств // Руководство по проведению доклинических исследований лекарственных средств. - М.: Гриф и К, 2012. - С. 197-218.
18. Средство, обладающее местноанестезирующим действием Пат. 2313341 Рос. Федерация: МПК A61K31/4188/ A61P23/02 / Галенко-Ярошевский А. П. [и др.]; заявители и патентообладатели ФГОУ ВПО «Южный федеральный университет», Негосударственное ОУ ВПО «Кубанский медицинский институт», ФГУ «Межотраслевой научно-технический комплекс «Микрохирургия глаза» им. акад. С.Н. Федорова» Фед. агентства по здравоохр. и соц. развитию; №2006140600/15; Заявл. 16. 11. 2006; опубл. 27.12.2007. Бюл. № 38 - 8 с: ил.
19. Дубровин А.Н. [и др.]. Синтез и свойства 2-замещенных амидов цинхониновой кислоты // Современные проблемы науки и образования. - 2012. - № 4. https://science-education.ru/ru/article/view?id=6630.
20. Rodgers R.J., Johnson N.J. Factor analysis of spatiotemporal and ethological measures in the murine elevated plus-maze test of anxiety // Pharmacol. Biochem. Behav. - 1995. - Vol. 52, N2. - P. 297-303.
21. Буреш Я., Бурешова О., Хьюстон Дж.П. - Методики и основные эксперименты по изучению мозга и поведения. - Москва: Высшая школа, 1991. - 398 с.
22. Манвелян Э.А., Анисимова Н.А., Батурин В.Α. Половая диссимиляция поведения при стресс-воздействии различной интенсивности и изменении функции надпочечников (монография), Ставрополь, 2013. - 107 с.
23. Многопараметровый метод комплексной оценки тревожно-фобических состояний у крыс / Родина В. И. [и др.] // Журн. высш. нерв. деятельности им. И.П. Павлова. - 1993. - №5. - С.1006-1017.
24. Оганесян Э.Т., Кодониди И.П., Сочнев В.С., Манвелян Э.А., Сыса В.Ю., Манвелян М.М. Новое N-арилсульфамидное производное о-бензоиламинобензойной кислоты, обладающее анксиолитической, актопротекторной и антидепрессивной активностью. - Патент на изобретение №2643356. Дата выдачи: 1.02.2018.
25. SAFETY DATA SHEET. Metamizole (sodium salt). Режим доступа: https://www.caymanchem.com/msdss/15771m.pdf (дата обращения 24.12.2018).
26. Toxicological Data on Ingredients: Lidocaine. Режим доступа: http:// www.sciencelab.com/msds.php?msdsId=9924492 (дата обращения 18.12.2018).
27. Material Safety Data Sheet. Bromocriptin. sc-337602. Режим доступа: http://datasheets.scbt.com/sc-337602.pdf (дата обращения 24.12.2018).
28. Material Safety Data Sheet. Bromocriptine (mesylate). sc-200395. Режим доступа: http://datasheets.scbt.com/sc-200395.pdf (дата обращения 24.12.2018).
29. Diazepam International Programme on Chemical Safety Poisons Information. Режим доступа: http://www.inchem.org/documents/pims/pharm/pim181.htm(дата обращения 6.06.2018).
30. Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ / под ред. В. П. Фисенко [и др.] - М.: ИАА Ремедиум, 2000. - 398 с.
Исследование выполнено при поддержке Фонда содействия развитию малых форм предприятий в научно-технической сфере (Фонда содействия инновациям; договор №12575ГУ/2017 от 18.04.2018).
Таблица 1 - Влияние соединения 1 на показатели формалинового теста у самцов крыс (%)
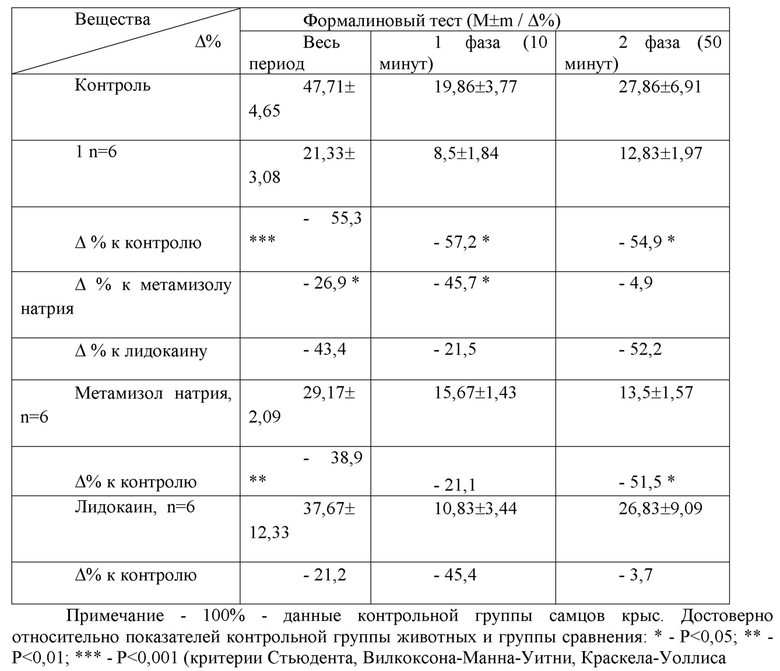
Таблица 2 - Влияние соединения 1 на показатели теста «уксусные корчи» у самцов крыс (%)
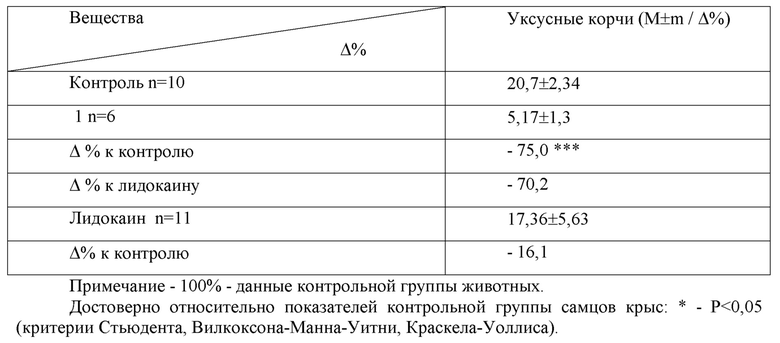
Таблица 3 - Влияние соединения 1 на показатели теста «уксусные корчи» у самок крыс
Примечание - 100% - данные контрольной группы животных. Достоверно относительно показателей контрольной группы самок крыс и группы сравнения: * - P<0,05, ** - P<0,01 (критерии Стьюдента, Вилкоксона-Манна-Уитни, Краскела-Уоллиса).
Таблица 4 - Влияние соединения 1 на показатели формалинового теста у самок крыс (в стадии диэструс ½)
Примечания - 100% - данные контрольных групп самок в стадии эстрального цикла диэструс ½. Достоверно относительно группы самок крыс, получавших растворитель, и групп сравнения в фазе эстрального цикла диэструс ½: * - P<0,05; *** - P<0,001 (критерии Стьюдента, Вилкоксона-Манна-Уитни, Краскела-Уоллиса).
Таблица 5 - Влияние соединения 1 на число «уксусных корчей» у самок крыс в стадиях диэструс ½ и проэструс / эструс
Примечания - 100% - данные контрольных групп самок в соответствующих фазах эстрального цикла. Достоверно относительно контрольной группы самок крыс в соответствующих стадиях эстрального цикла: * - P<0,05 (критерии Стьюдента, Вилкоксона-Манна-Уитни, Краскела-Уоллиса).
Таблица 6 - Влияние соединения 1 на каталептогенную активность галоперидола (с) у крыс самок
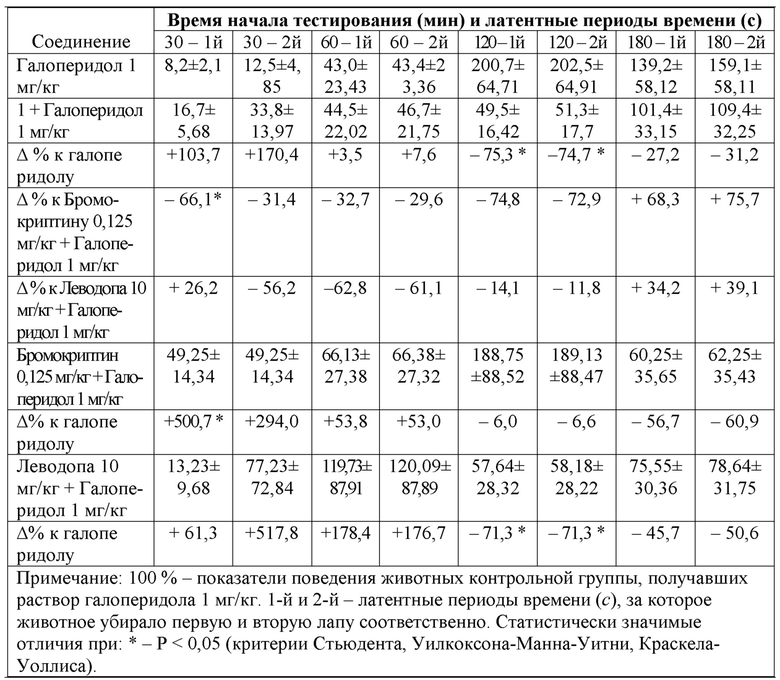
Таблица 7 - Влияние соединения 1 на каталептогенную активность галоперидола (с) у крыс самок в стадии эстрального цикла проэструс/эструс
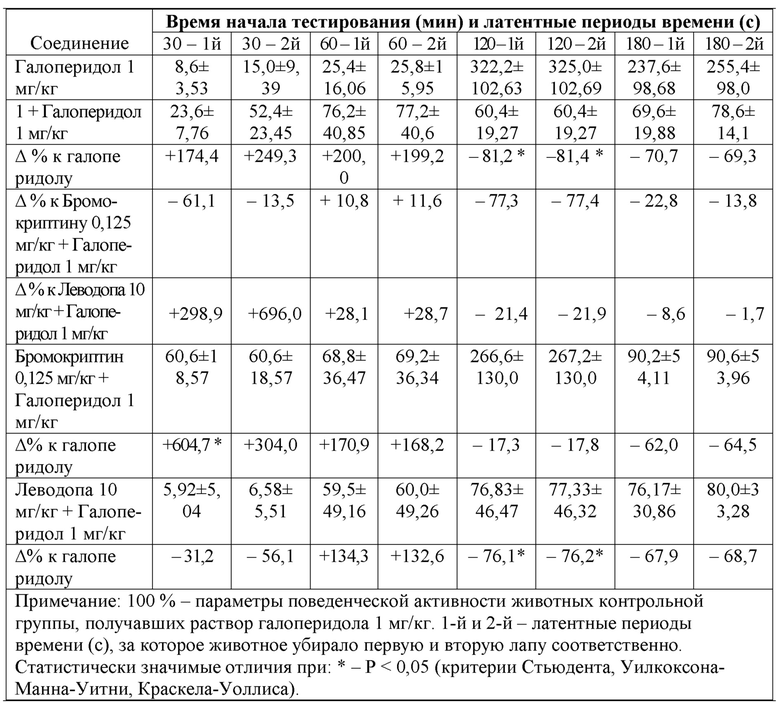
Таблица 8 - Действие соединения 1 и диазепама на показатели поведения крыс в приподнятом крестообразном лабиринте
Примечание - 100% - показатели поведения самцов крыс, получавших растворитель (раствор твина-80; К1 - контрольная группа для животных, получавших соединение 1) и физиологический раствор (К2 - контрольная группа для крыс, получавших диазепам). * - отличия статистически значимы по отношению к данным соответствующей контрольной группы: * - при р<0,05; ** - при р<0,01; # - отличия статистически значимы по отношению к данным группы, получавшей диазепам (критерий Уилкоксона-Манна-Уитни).
Таблица 9 - Действие соединения 1 на показатели поведения самцов крыс в «открытом поле» при однократном введении
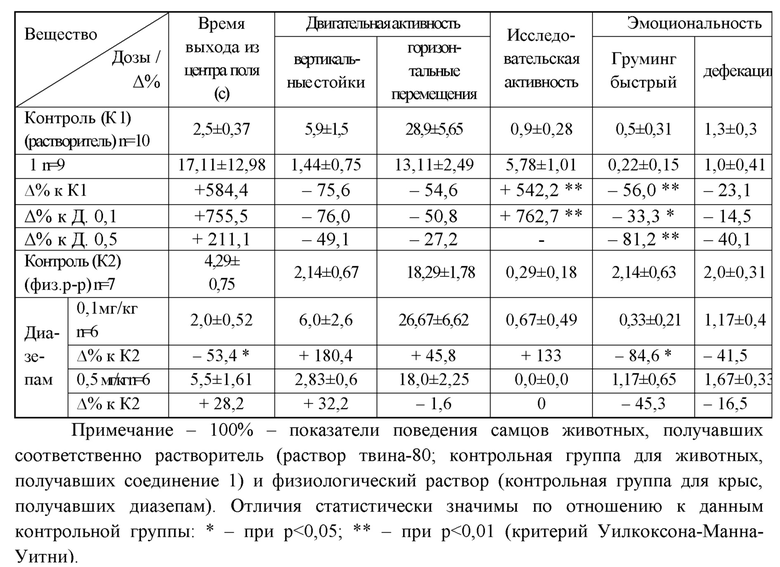
Таблица 10 - Действие соединения 1 на показатели поведения самцов крыс при многопараметрическом тестировании
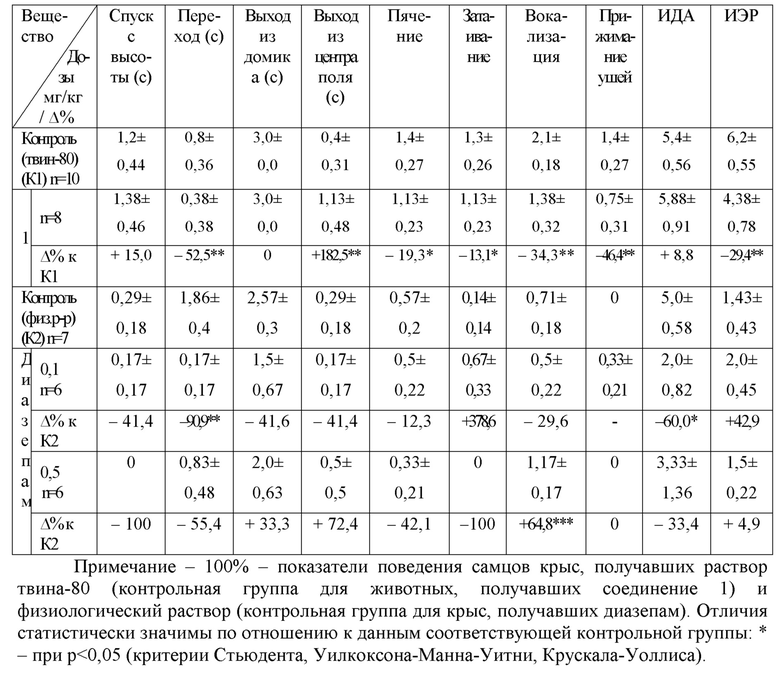
Таблица 11. Действие соединения 1 на показатели поведения самцов крыс в тесте «боковое положение»
| название | год | авторы | номер документа |
|---|---|---|---|
| 2-бензилпроизводное 4-(3Н)хиназолинона, обладающее анальгезирующим, противопаркинсоническим, антигипоксантным, транквилизирующим действием | 2019 |
|
RU2715884C1 |
| СРЕДСТВО ДЛЯ СТИМУЛЯЦИИ ГЕНЕРАТИВНОЙ ФУНКЦИИ | 2014 |
|
RU2564016C1 |
| НОВОЕ N-АРИЛСУЛЬФАМИДНОЕ ПРОИЗВОДНОЕ О-БЕНЗОИЛАМИНОБЕНЗОЙНОЙ КИСЛОТЫ, ОБЛАДАЮЩЕЕ АНКСИОЛИТИЧЕСКОЙ, АКТОПРОТЕКТОРНОЙ И АНТИДЕПРЕССИВНОЙ АКТИВНОСТЬЮ | 2016 |
|
RU2643356C2 |
| СПОСОБ РЕГУЛЯЦИИ ВОСПРОИЗВОДИТЕЛЬНОЙ ФУНКЦИИ У САМОК | 1994 |
|
RU2076593C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ УГНЕТЕНИЯ ГАРМОНАЛЬНОЙ АКТИВНОСТИ ЯИЧНИКОВ | 1999 |
|
RU2191584C2 |
| СРЕДСТВО ДЛЯ УЛУЧШЕНИЯ РЕПРОДУКТИВНОЙ ФУНКЦИИ | 2012 |
|
RU2487705C1 |
| ПРИМЕНЕНИЕ СОЛЕЙ ВОЛЬФРАМА (VI) ДЛЯ ЛЕЧЕНИЯ ЖЕНСКОГО БЕСПЛОДИЯ У МЛЕКОПИТАЮЩИХ, НЕ СТРАДАЮЩИХ ДИАБЕТОМ | 2014 |
|
RU2635507C2 |
| СРЕДСТВО ДЛЯ УЛУЧШЕНИЯ РЕПРОДУКТИВНОЙ ФУНКЦИИ | 2012 |
|
RU2489142C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ ПОЛИКИСТОЗНЫХ ЯИЧНИКОВ | 2007 |
|
RU2337411C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ ЖЕНСКОГО АНОВУЛЯТОРНОГО БЕСПЛОДИЯ НА КРЫСАХ | 2015 |
|
RU2571896C2 |
Изобретение относится к области органической химии, а именно к гетероциклическому соединению 2-(3,4-диметоксибензил-6-сульфо)хиназолин-4(3Н)-он, соответствующий формуле (1). Также изобретение относится к способу его получения. Технический результат: получено новое гетероциклическое соединение, обладающее анальгезирующей, противопаркинсонической, транквилизирующей, психостимулирующей активностью. 2 н.п. ф-лы, 11 табл.
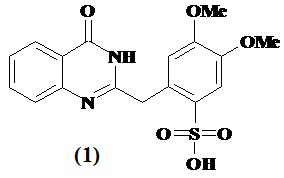
1. Способ получения 2-(3,4-диметоксибензил-6-сульфо)хиназолин-4(3Н)-она 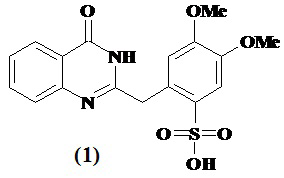
соответствующего формуле (1), в которой Ме - метильный радикал, основанный на взаимодействии 2-(3,4-диметоксибензил)-(3Н)-хиназолин-4-она с концентрированной серной кислотой при комнатной температуре с последующим выделением продукта реакции при разбавлении реакционной смеси водой.
2. 2-(3,4-диметоксибензил-6-сульфо)хиназолин-4(3Н)-он, соответствующий формуле (1), обладающий анальгезирующей, противопаркинсонической, транквилизирующей, психостимулирующей активностью.
| 2-бензилпроизводное 4-(3Н)хиназолинона, обладающее анальгезирующим, противопаркинсоническим, антигипоксантным, транквилизирующим действием | 2019 |
|
RU2715884C1 |
| ПРОИЗВОДНЫЕ ХИНАЗОЛИНА, ОБЛАДАЮЩИЕ АНТИДЕПРЕССИВНОЙ, АНКСИОЛИТИЧЕСКОЙ И НООТРОПНОЙ АКТИВНОСТЬЮ | 2012 |
|
RU2507199C1 |
| Автомат для отпуска жидкости | 1929 |
|
SU23670A1 |
| WO 2008157500 A1, 24.12.2008. | |||
Авторы
Даты
2021-10-28—Публикация
2021-03-22—Подача