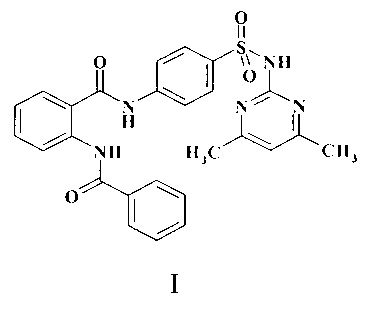
Изобретение относится к области химико-фармацевтической промышленности и медицины и касается соединений, которые могут быть использованы для создания лекарственных средств анксиолитического действия. Технический результат: получено новое производное о-бензоиламинобензойной кислоты, соединение формулы I, обладающее анксиолитическим действием. Также предложен способ его синтеза.
Предшествующий уровень техники
Известно что в настоящее время наиболее часто в медицинской практике для лечения неврозов и неврозоподобных состояний, психопатий, аффективных, депрессивных, психосоматических нарушений, сопровождаемых эмоционально-стрессорными и тревожными расстройствами, являются анксиолитические лекарственные средства различных фармакологических групп.
Производные дифенилметана (Бенактизин, гидроксизин и др.) активно подавляют холинергические системы мозга, в связи с чем, их называют также центральными холинолитиками. Производные пропандиола, к примеру мепротан, выраженного влияния на бензодиазепиновые и холинергические рецепторы не оказывают.
Наиболее употребляемыми остаются препараты группы бензодиазепинов, такие как феназепам, диазепам и др. Известно, что в ЦНС существуют специфические "бензодиазепиновые" рецепторы, для которых бензодиазепины являются экзогенными лигандами. Механизм действия анксиолитиков бензодиазепиновой структуры основан на аллостерическом взаимодействии с ГАМК-бензодиазепиновым рецепторным комплексом, потенцируя центральное тормозное влияние ГАМК. Вместе с тем, транквилизаторы этого ряда обладают высокой токсичностью, рядом нежелательных побочных лекарственных реакций, среди которых сонливость, головокружение, мышечная слабость, головная боль, а в некоторых случаях путанность сознания. При длительном применении этих препаратов развивается лекарственная зависимость и нарушение памяти [http://www.vidal.ru/drugs/molecule/309].
Вследствие этого актуальной задачей является поиск новых соединений, обладающих выраженным анксиолитическим действием и низкой токсичностью.
Среди производных 1,3-диазинона-4 и их ациклических аддуктов, производных антраниловой кислоты, обнаружено немало соединений, обладающих анксиолитическими свойствами и низкой токсичностью. К ним относятся производные о-бензоиламинобензойной кислоты [Манвелян Э.А., Сыса В.Ю., Кодониди И.П., Оганесян Э.Т., Сочнев B.C., Бандура А.Ф. Влияние амидов о-бензоиламинобензойной кислоты, производных предшественников хиназолинона-4, на поведение самцов крыс в приподнятом крестообразном лабиринте // / Медицинский вестник северного Кавказа, 2014. Т. 9. №4 (36). С. 378-379; Кодониди И.П., Оганесян Э.Т., Жогло Е.Н., Сочнев B.C., Ивченко А.В., Манвелян Э.А., Сыса В.Ю. Целенаправленный синтез амидов о-бензоиламинобензойной кислоты, в качестве предшественников хиназолинонов-4, обладающих влиянием на ЦНС // / Новые направления в химии гетероциклических соединений: тез. докл. 3 междунар. науч. конф. - Ставрополь, 2013. - С. 280-281; Э.А. Манвелян, В.Ю. Сыса, И.П. Кодониди, Э.Т. Оганесян. Действие амидов орто-бензоиламинобензойной кислоты, производных предшественников хиназолинона-4, на поведение самцов крыс в «открытом поле» // Наука. Инновации. Технологии. - Ставрополь: Изд-во СКФУ, 2014. - №1. - С. 212-220.] и производные хиназолинона-4 [Бандура А.Ф., Арльт А.В., Воронков А.В., Сочнев B.C., Кодониди М.И., Золотых Д.С., Луговой И.С., Базганов А.Ю. Молекулярное моделирование и анксиолитическая активность гетерилзамещенных 2,3-Дигидро-1Н-хиназолин-4-она // / Современные проблемы науки и образования. - 2014. - №4; URL: www.science-education.ru/118-14147]. Известны производные пиримидинов, обладающие психотропным действием [Igrashi, Jun-Etsu, Nishimura.// РСТ Jnt Appl. WO 963/488 A1, 10 Oct. 1996, 116 pp.], и соли 4-оксо-1,4-дигидропиримидина, обладающие психостимулирующей, антидепрессантной [Cashyap M.M.//J. labelled Compd. Radiopharm. - 1989 - Vol.22. - №12 - P. 1239-1250; C.A. - 1987 - Vol. 106-18475a], антиаллергической и иммуностимулирующей активностью [Патент №2015975].
Наиболее близкими по структуре к заявляемому объекту являются 2-бензоиламино-N-(4-сульфамоилфенил)-бензамид, обладающие выраженным влиянием на ЦНС [[Е.А. Manvelyan, V.Yu. Sysa, М.М. Manvelyan. Pharmacological evaluation of the spectrum of psychotropic activity of new synthesized derivatives if 4-oxopyrimidine and am-ides of orto-benzoyl amino-benzoic acid, predecessors of quinazoline-4 // Pharmacy and pharma-cology-2015. - Volume III. - Suplement 1. - P.72-73. http://www.pmedpharm.ru/content/files/ (дата обращения 04.12.2015)], 2-стирилпроизводные 1Н-пиримидин-4-она].
Эти данные свидетельствуют о перспективности поиска новых высокоэффективных и малотоксичных анксиолитических веществ в ряду производных 1,3-диазинона-4 и их ациклических предшественников.
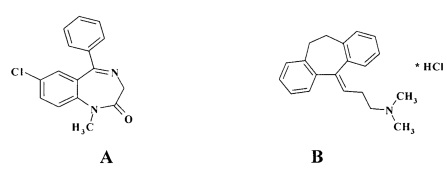
Фармакологическое действие соединения 1 было изучено в сравнении с двумя прототипами по каждому типу действия. Для оценки анксиолитической и актопротекторной активности прототипом был выбран диазепам (А); для оценки антидепрессивной активности прототипом выступал препарат амитриптилин (В). Такой выбор объясняется тем, что классическая методология изучения анксиолитических средств сложилась на основе исследования фармакологических свойств препаратов бензодиазепинового ряда. К таковым относится эталонный и хорошо изученный в различных модельных ситуациях диазепам, специфически связывающийся с безодиазепиновым сайтом ГАМКА-рецепторного комплекса. В связи с этим, в качестве препарата сравнения выбран диазепам. Антидепрессивная активность новых синтезированных соединений также оценивается в сравнении с эталонными и хорошо исследованными антидепрессантами, к которым относится амитриптилин, имеющий трициклическую структуру и неизбирательно блокирующий нейрональный захват серотонина и норадреналина [Манвелян Э.А., Батурин В.А. Влияние диазепама на поведение эпифизэктомированных крыс в условиях конфликтной ситуации и при многопараметрическом тестировании // Ставропольская гос. мед. академия. - Ставрополь, 1995. Деп. в ВИНИТИ 18.09.95, №2584-В95, - 13 с.; Манвелян Э.А. Роль эпифизарных механизмов в реализации специфической психотропной активности бензодиазепиновых транквилизаторов: автореф. дисс… канд. фарм. наук, Пятигорск, 1997. - 22 с.; Манвелян Э.А., Батурин В.А. Половые и хронобиологические различия в активности диазепама у крыс в тесте конфликтной ситуации // Эксперим. и клин, фармакол. - 2008. - №4. - С. 11-13; Манвелян Э.А., Батурин В.А. Особенности действия амитриптилина на плавательное поведение интакных и овариоэктомированных самок крыс в разное время суток // Биомедицина». - 2008. - №2. - с. 59-62; Батурин В.А., Манвелян Э.А. Хронобиологические особенности плавательного поведения интактных и овариоэктомированных крыс // Российский физиологический журнал им. И.М. Сеченова. - 2008 г. - №11. - Т. 94. - С. 1270-1276; Миронов А.Н., Бунятян Н.Д. Руководство по проведению доклинических исследований лекарственных средств: в 2 т./ под ред. А.Н. Миронова. - Москва: Гриф. и К., 2012, - 944 с.]
Настоящее изобретение относится к новым синтетическим N-арилсульфамидным производным обензоиламинобензойной кислоты, обладающим высокой анксиолитической активностью в сочетании с практически полным отсутствием токсичности.
Технический результат: получено новое производное о-бензоиламинобензойной кислоты, обладающее выраженной анксиолитической активностью, которое в тестах конфликтной ситуации, приподнятого крестообразного лабиринта, многопараметрического тестирования, «открытое поле» превосходит препарат сравнения диазепам (табл. 1). Новое соединение также обладает антидепрессивной активностью, превосходящей в тесте принудительного плавания прототип амитриптилин. В отличие от амитриптилина и диазепама, заявляемое вещество при хроническом введении не влияет на лейкоцитарную формулу крови.
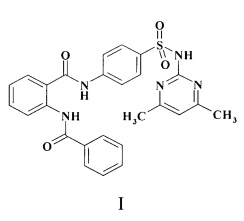
Заявляемый объект - 2-бензоиламино-N-[4-(4,6-сульфамоил)-фенил]-бензамид формулы (I), обладающий анксиолитическим, антидепрессивным действием.
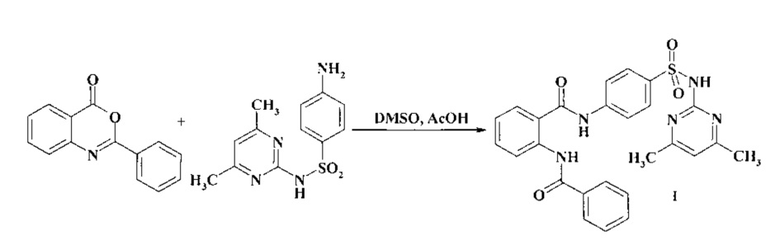
Способ получения 2-бензоиламино-N-[4-(4,6-диметилпиримидин-2-илсульфамоил)-фенил]-бензамида (1) основан на взаимодействии 2-фенилбензо[d][1,3]оксазин-4-она с 2-(4-аминобензолсульфамидо)-4,6-диметилпиримидином при нагревании в среде ледяной уксусной кислоты и диметилформамида.
Новое соединение проявляет выраженную анксиолитическую, антиконфликтную, антидепрессивную активность
ПРИМЕР СИНТЕЗА
2-Бензоиламино-N-[4-(4,6-диметилпиримидин-2-илсульфамоил)-фенил]-бензамид (1)
Смесь 2,23 г (0,01 моль) 2-фенилбензо[d][1,3]оксазин-4-она, 2,78 г и (0,01 моль) 2-(4-аминобензолсульфамидо)-4,6-диметилпиримидина, 7 мл ледяной уксусной кислоты и 0,5 мл диметилформамида кипятят 40 мин. Охлаждают, осадок отфильтровывают, промывают эфиром диэтиловым. Получают 3.67 г 2-бензоиламино-N-[4-(4,6-диметилпиримидин-2-илсульфамоил)-фенил]-бензамида, который подвергают перекристаллизации из этанола. Выход 76%. Вещество представляет собой белый кристаллический порошок, без запаха, нерастворим в воде, трудно растворим в этаноле, нерастворим в эфире. Тпл. 255-257°С (из этанола).
Спектр 1Н ЯМР (300 МГц), δ, м.д. в DMSO-d6: 2,15 (с, 6Н, СН3); 6,33 (с, 1Н, АrН); 7,18-7,24 (т, 1Н, Аr); 7,52-7,59 (м, 4Н, АrН); 7,88-8,01 (м, 6Н, ArH); 8,63-8,65 (д, 1Н, АrН); 10,73 (с, 1H, NH); 11,24 (с, уш., 1H, NH-SO2); 11,79 (с, 1Η, ΝΗ).
Найдено (%): С 63,28; Η 4,71; N 14,08; О 12,94; S 6,51.
C26H23N5O4S. Вычислено (%): С 62,26; H 4,62; N 13.96; О 12,76; S 6,39.
Оценка фармакологической активности
Фармакологическая активность препарата оценивалась по трем направлениям. Было изучено анксиолитическое, актопротекторное и антидепрессивное действие соединения 1.
Для исследований использовались белые половозрелые крысы-самцы Вистар массой 200-250 г, которые содержались в стандартных условиях вивария при свободном доступе к воде и пище вне экспериментального периода. Уход, кормление, работа с животными осуществлялись согласно международным рекомендациям о защите позвоночных животных, используемых для экспериментов или в иных научных целях [Г.П. Червонская, Г.П. Панкратова, Л.Л. Миронова, Токсикол. вестник, 3,2-8 (1998)].
Контрольной в каждой серии экспериментов для каждой методики при оценке исследуемой активности была группа самцов животных, получавших 0,4 мл внутрибрюшинно раствора твина-80 (1-2 капли на 10 мл воды) или физиологический раствор (контрольная группа для животных, получавших диазепам, амитриптилин) в аналогичных режимах. Группы животных (опытные, контрольные, препараты сравнения) включали 5-12 особей. Все растворы веществ во всех сериях исследований инъецировались внутрибрюшинно. Эксперименты проводили в вечернее время с 18-00 до 20-00 ч.
Статистическую обработку результатов проводили, используя стандартные параметрические и непараметрические критерии (t-критерий Стьюдента, критерии Манна-Уитни, Уилкинсона, Крускала-Уоллиса). При проверке данных на нормальность распределения использовался W-критерий Шапиро-Уилка. Проводили относительный сравнительный анализ, сопоставляя опытные данные с контрольными результатами, принятыми за 100%. Для всех видов анализа статистически значимыми считали различия при р<0,05 [С. Гланц. Медико-биологическая статистика: [пер. с англ.]. Практика, Москва (1999); О.Ю. Реброва. Статистический анализ медицинских данных. Применение пакета прикладных программ STATISTICА, МедиаСФЕРА, Москва (2006)].
Анксиолитическую активность соединения 1 изучали в тестах конфликтной ситуации, приподнятого крестообразного лабиринта, открытого поля, многопараметрического тестирования; актопротекторную активность оценивали в тестах открытого поля, многопараметрического тестирования; антидепрессивное действие - в условиях принудительного плавания [Т.А. Воронина, С.Б. Середенин, Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ, Р.У. Хабриев (ред.), Медицина, Москва (2005), с. 253-262; А.Н. Миронов, Н.Д. Бунятян, Руководство по проведению доклинических исследований лекарственных средств: в 2 т./ А.Н. Миронов. – Гриф. и К., Москва (2012); Родина В.И. Многопараметровый метод комплексной оценки тревожно-фобических состояний у крыс / В.И. Родина [и др.] // Журн. высш. нерв. деятельности им. Павлова. - 1993. - №5. - С. 1006-1017].
Анксиолитическая активность
Влияние заявляемого объекта на анксиолитическую активность проводилось по тесту конфликтной ситуации.
Эксперимент в условиях конфликтной ситуации начинался с водной депривации в течение 48 ч (животные получали сухой корм). Далее на протяжении 3 дней в течение 10 мин в одно и то же вечернее время суток животных обучали приемам взятия воды из поилки в экспериментальной камере [Манвелян Э.Α., Тарасов А.В. Установка для создания конфликтной ситуации у лабораторных животных (крыс). (Удостоверение на рац. предл.). // Ставропольский медицинский институт. Удост. на рац. Предл. №745 от 28.06.93]. В день проведения опыта на поилку подавали электрический ток силой 0,5 мА, позволяющий выявить анксиолитическое действие средней силы. В экспериментальной камере одновременно регистрировали несколько показателей, отражающих различные стороны поведения крысы в неврогенной ситуации. Анксиолитическую активность соединения 1 в конфликтной ситуации исследовали при введении в дозе 50 мг/кг. Вещество вводили однократно за 30 мин до начала исследования. Препарат сравнения диазепам применяли в дозах 0,1 и 0,5 мг/кг. Группы животных (опытная, контрольные, препарат сравнения) включали 6-8 особей.
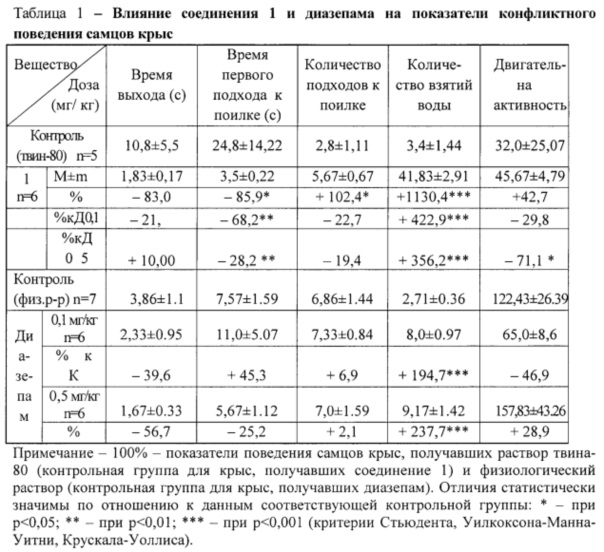
При изучении анксиолитической активности по тесту конфликтной ситуации была отмечена более высокая активность соединения 1 по сравнению с препаратом диазепамом (таблица 1).
По сравнению с данными группы контрольных самцов при использовании вещества 1 более чем в 12 раз возрастала питьевая активность животных (1230%, р<0,001). Антиконфликтная активность исследуемого соединения была более выражена и по сравнению с действием диазепама в дозах 0,1 и 0,5 мг/кг. Количество подходов к поилке при этом статистически значимо увеличивалось примерно в 2 раза по отношению к данным контрольной группы. Наряду с этим латентность выхода и время первого подхода к поилке ограничивались. При этом снижение латентного периода первого подхода было статистически значимым по сравнению с соответствующими контрольными данными и с влиянием эталонного транквилизатора сравнения.
Общая двигательная активность животных, регистрируемая по показаниям счетчиков, имела тенденцию к повышению на фоне соединения 1 (143%). Диазепам в дозе 0,1 мг/кг снижал двигательную активность животных (до 53%).
Вывод: вещество 1 обладает антиконфликтной активностью, статически значимо превышающей действие эталонного препарата сравнения диазепама. Соединение 1 также проявляет антиамнестическое действие, в отличие от диазепама.
Оценку анксиолитической активности соединения 1 по тесту «приподнятый крестообразный лабиринт» (ПКЛ) проводили в экспериментальной установке, представляющей собой 4 рукава, скрепленных друг с другом под прямым углом, размером 50·10 см. Два противоположных рукава ПКЛ закрытые (огражденные с двух сторон) и два других открытые. Лабиринт поднят над уровнем пола на высоту 0.5 м. Высота стенок в закрытых рукавах - 10 см. Сверху все рукава открыты. В месте перпендикулярного пересечения рукавов находится площадка размером 10×10 см. При тестировании в ПКЛ животных помещали на центральную площадку лабиринта и в течение 5 мин визуально регистрировали следующие параметры поведения: общее число заходов в открытые (светлые) или закрытые (темные) рукава лабиринта и время нахождения в них (с). Анксиолитический эффект вещества оценивали по учащению заходов животного в открытые (светлые) рукава и увеличению времени нахождения в них, а также ограничению частоты заглядываний и времени нахождения в закрытых рукавах [Rodgers R.J., Johnson №.J. Factor analysis of spatiotemporal and ethological measures in the murine elevated plus-maze test of anxiety // Pharmacol. Biochem. Behav. - 1995. - V. 52, №2. - P. 297-303].
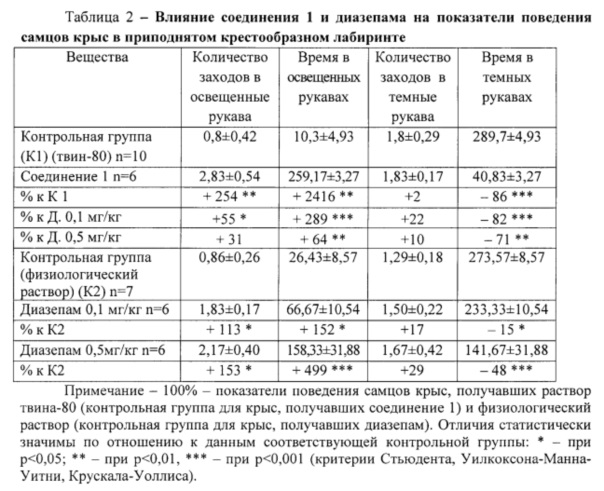
При использовании вещества 1 в дозе 50 мг/кг статистически значимо повышалось количество заходов самцов крыс и время нахождения в открытых рукавах при одновременном существенном снижении времени нахождения в темных рукавах ПКЛ по сравнению с данными контрольной группы К1 и групп животных, получавших диазепам (таблица 2).
Вывод. Соединение 1 проявляло анксиолитическое и антифобическое действие у самцов крыс в ПКЛ. При этом противотревожное и антифобическое влияние вещества 1 было более выражено, нежели у препарата сравнения диазепама.
При исследовании противотревожной активности соединения 1 по методике «открытого поля» [Буреш Я. Методики и основные эксперименты по изучению мозга и поведения / Я. Буреш, О. Бурешова, Дж. П. Хьюстон. - М.: Высш. шк., 1991. - 398 с.] регистрировали: 1) латентность выхода из центра поля; 2) горизонтальную двигательную активность - количество пересеченных секторов 4 лапами; 3) вертикальную активность - количество вертикальных стоек; 4) число обследованных отверстий - норок (обнюхивание); 5) груминг; 6) число болюсов. Время проведения эксперимента составляло 2 мин. По совокупности повышения латентности выхода из центра поля, снижения вертикальной и горизонтальной активности судили о «седативном» действии вещества, а при повышении исследовательской активности, снижении частоты груминга и числа фекальных болюсов (вегетативная представленность стресса) - «противотревожном» влиянии [Калуев А.В., 1998; Казакова С.Б. с соавт., 2007; Воронина Т.А. и соавт., 2008; Манвелян Э.А. Анисимова Н.А., Батурин В.Α. Половая диссимиляция поведения при стресс-воздействии различной интенсивности и изменении функции надпочечников (монография), Ставрополь: Изд-во СКФУ, 2013, - 107 с.].
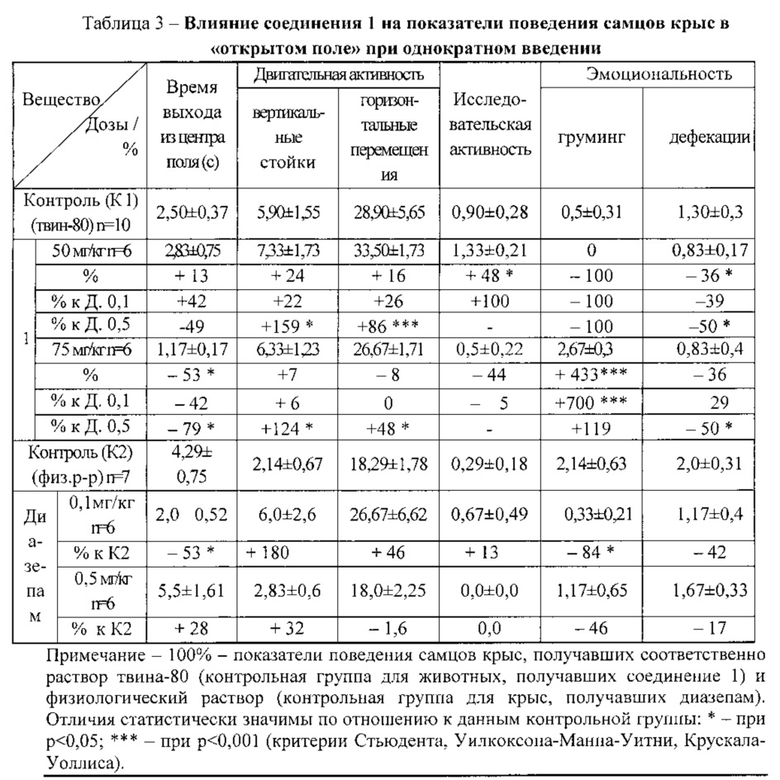
Оценка влияния соединения 1 при однократном введении в дозе 50 мг/кг на поведение самцов крыс в условиях «открытого поля» выявила тенденцию к увеличению числа вертикальных стоек и пересеченных линий по сравнению с контрольными животными, получавшими растворитель (таблица 3). Вместе с тем, животные статистически значимо чаще исследовали «норки», у них отсутствовал груминг, урежались вегетативные реакции (ограничивалось число фекальных болюсов), что свидетельствовало о снижении эмоциональности животных. По сравнению с влиянием диазепама в дозе 0,5 мг/кг на фоне применения соединения 1 статистически значимо выше были двигательная вертикальная и горизонтальная, а также исследовательская активность, отсутствовал груминг, снижалась вдвое частота вегетативных реакций.
При введении соединения 1 в дозе 75 мг/кг наблюдалось ограничение латентного периода выхода крыс из центра открытого поля и учащение груминга по отношению к данным контрольной группы. По сравнению с влиянием диазепама в дозе 0,5 мг/кг на фоне использования вещества 1 статистически значимо выше были локомоторная вертикальная и горизонтальная, исследовательская активность, существенно снижались латентность выхода из центра поля и частота вегетативных реакций.
Вывод. При тестировании самцов крыс в открытом поле соединение 1 при однократном введении в дозе 50 мг/кг проявляло противотревожное и активирующее действие, в дозе 75 мг/кг - активирующее влияние. Активирующий эффект был выраженнее по сравнению с влиянием диазепама.
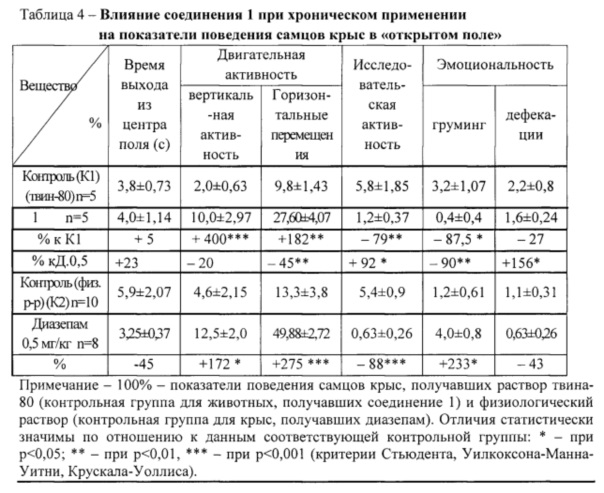
При хроническом (14 дней) использовании соединения 1 в дозе 50 мг/кг было отмечено статистически значимое повышение двигательной горизонтальной и вертикальной активности животных в открытом поле. Вместе с тем, наблюдалось ограничение исследовательской активности, частоты груминга, реже отмечались вегетативные эмоциональные реакции (таблица 4).
Вывод. При хроническом введении в дозе 50 мг/кг отмечалось активирующее и противотревожное влияние соединения 1 при тестировании самцов крыс в открытом поле. На фоне соединения 1 более выражена была исследовательская активность по сравнению с действием диазепама.
Для комплексной оценки тревожно-фобического статуса у крыс использовали многопараметрическое тестирование - МПТ [Родина В.И. Многопараметровый метод комплексной оценки тревожно-фобических состояний у крыс / В.И. Родина [и др.] // Журн. высш. нерв. деятельности им. Павлова. - 1993. - №5. - С. 1006-1017]. С этой целью каждой крысе в специальной камере предъявляли в определенной последовательности 8 тестов: определение латентных периодов: 1 - спуска с высоты, 2 - прохождения через отверстие, 3 - выхода из темного «домика», 4 - выхода из центра «открытого поля»; реакцию на смену освещенности: а также реакции на руку экспериментатора; 5 - пячение-2, 6 - затаивание, 7 - вокализация, 8 - прижимание ушей. Ответ на каждый тест оценивали от 0 до 3 баллов: большая оценка в баллах соответствовала более выраженной ответной реакции у животного. По изменению суммарного показателя по тестам 1-4 (ИДА - индекс двигательной активности) судили о «седативном» (повышение показателей, снижение двигательной активности) или активирующем (снижение показателей, повышение двигательной активности) эффекте, а по изменению показателей по тестам 5-9 (ИЭР - индекс эмоциональной реактивности - о «противотревожном» (снижение показателей и снижение эмоциональной реактивности) или «анксиогенном» (повышение показателей и повышение эмоциональной реактивности) эффекте использованного вещества.
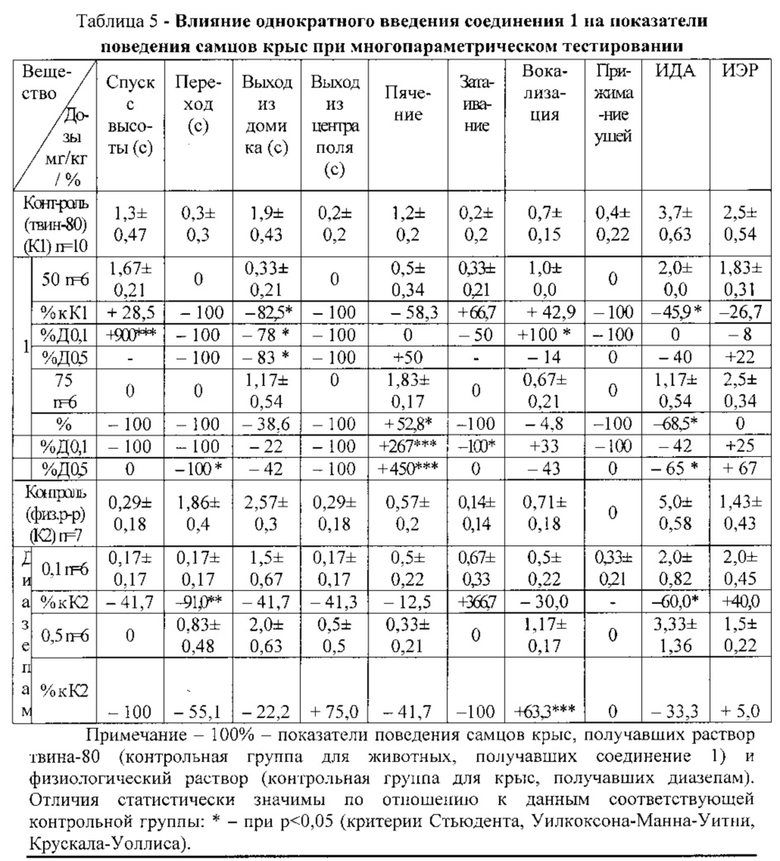
В условиях МПТ при однократном введении в дозе 50 мг/кг соединения 1 ускорялись переходы в боксе, выход из «домика» и центра освещенного «поля» по сравнению с животными контрольной группы (таблица 5). Анализ реактивности самцов выявил отсутствие или заметное ограничение интенсивности реакций пячения, отсутствие прижимания ушей при манипуляциях руки экспериментатора. По сравнению с влиянием диазепама в дозе 0,5 мг/кг при введении вещества 1 статистически значимо снижалась латентность выполнения тестов, отсутствовали или были менее выражены эмоциональные реакции.
При увеличении дозы (75 мг/кг) исследуемого соединения животные немедленно покидали высоту, совершали переходы в боксе и покидали центр «поля», быстрее выходили из «домика» по сравнению с контрольными животными. У самцов отсутствовали реакции затаивания и прижимания ушей, были менее выражены реакции вокализации в ответ на действия «живого объекта», однако учащалось пячение. По сравнению с влиянием диазепама в дозе 0,5 мг/кг при использовании субстанции 1 статистически значимо ограничивались латентные периоды выполнения тестов, отсутствовали либо были менее интенсивны ответные реакции на действия экспериментатора, был ниже ИДА.
Вывод. С учетом спектра поведенческой активности, суммарных ИДА и ИЭР, выявлено активирующее и противотревожное действие субстанции 1 при однократном введении в дозах 50 и 75 мг/кг при многопараметрическом тестировании. Действие соединения 1 от влияния диазепама отличалось выраженным активирующим эффектом.
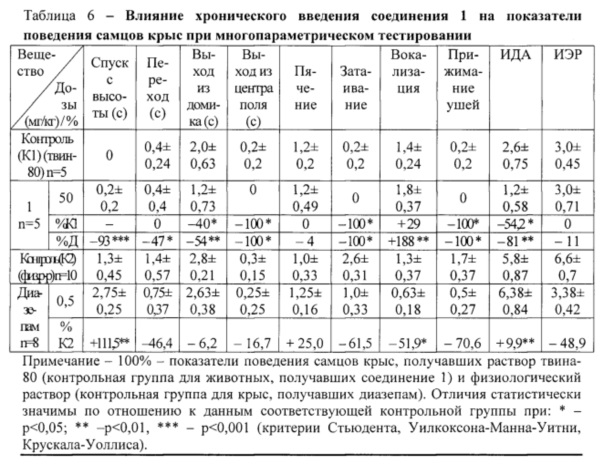
При хроническом (14 дней) использовании соединения 1 в дозе 50 мг/кг повышалось время спуска животных с высоты, однако одновременно снижалась латентность выхода из «домика» и центра «поля» по сравнению с данными контрольной группы. Также, на фоне субстанции 1 не регистрировались реакции затаивания и прижимания ушей, снижался ИДА (таблица 6). По сравнению с влиянием диазепама при использовании вещества 1 статистически значимо снижались латентные периоды выполнения предъявляемых тестов, отсутствовали реакции затаивания и прижимания ушей, однако чаще отмечалась вокализация в ответ на действия руки экспериментатора. При этом суммарный ИДА достоверно снижался, что свидетельствовало об активирующем действии соединения 1. На фоне действия диазепама ИДА повышался.
Вывод. При хроническом введении соединение 1 в дозе 50 мг/кг оказывало активирующее влияние на поведение самцов крыс при многопараметрическом тестировании. Препарат сравнения диазепам при аналогичном тестировании проявлял седативное действие.
Антидепрессивное действие
Оценка принудительного плавания по R.D. Porsolt (1977) проводилась с использованием биоритмологической модели, предложенной научной школой Арушаняна Э.Б. (1986) и компьютерной регистрацией параметров плавания [Щетинин Е.В., Батурин В.А., Арушанян Э.Б., Ованесов К.Б., Попов А.В. Биоритмологический подход к оценке принудительного плавания как экспериментальной модели «депрессивного» состояния // Журн. высш. нервн. деят. -1989. - №.5. - С. 959-964].
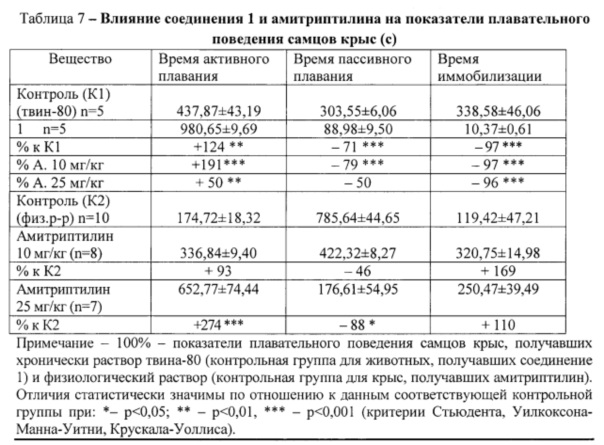
Хроническое введение соединения 1 в дозе 50 мг/кг приводило к статистически значимому увеличению продолжительности активного плавания животных по сравнению с показателями контрольной группы крыс - К1. Одновременно ограничивалась продолжительность пассивного плавания и иммобилизации (таблица 7).
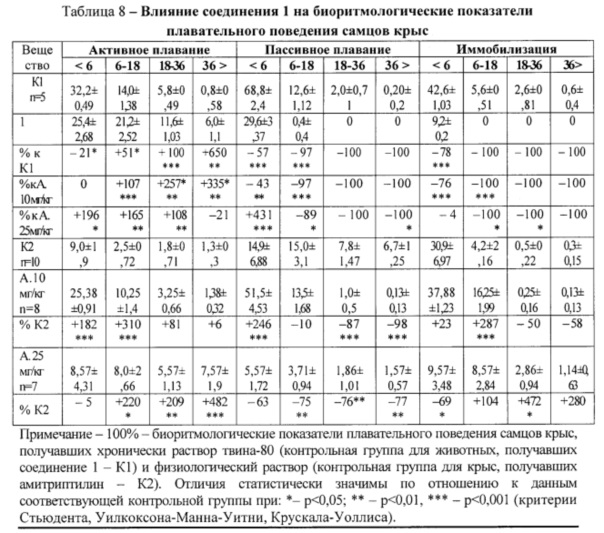
Хронобиологический анализ выявил уменьшение в структуре плавания коротких периодик активного, пассивного плавания и иммобилизации, но учащение средних и продолжительных циклов активного плавания (таблица 8).
По сравнению с действием амитриптилина на фоне соединения 1 увеличивалась продолжительность активного и уменьшалась длительность пассивного плавания и иммобилизации при преимущественном учащении периодик активного, ограничении ритмов средней продолжительности пассивного плавания, снижении частоты или отсутствии коротких, средних и длинных периодик иммобилизации.
Вывод. Соединение 1 в условиях принудительного плавания проявляет антидепрессивное действие, более выраженное по сравнению с влиянием препарата сравнения амитриптилина.
Хроническая токсичность
Проводили оценку влияния хронического применения соединения 1 на лейкоцитарную формулу периферической крови. Мазки крови животных исходные, до введения соединений (К1) и групп крыс, получавших хронически 14 дней раствор твина-80 (К2), соединение 1 в дозе 50 мг/кг, диазепам (0,5 мг/кг), амитриптилин (10 мг/кг), окрашивали по методу Романовского-Гимзы [Крамарь Л.В., Карпухина О.А. Оценка показателей общего анализа крови у детей при инфекционном мононуклеозе различной этиологии. // Современные проблемы науки и образования. - 2012. - №6. - С. 3-4]. Подсчет лейкоцитарной формулы включал определение относительного количества отдельных лейкоцитов [Мустафина Ж.Г., Крамаренко Ю.С., Кобцева В.Ю. Интегральные гематологические показатели в оценке иммунологической реактивности организма у больных с офтальмологией // Клин. лаб. диагностика. 1999. №5. 47-48].
При анализе лейкоцитарной формулы крови самцов крыс, получавших хронически соединение 1, было установлено повышение количества сегментоядерных клеток при ограничении числа эозинофилов и лимфоцитов. Других достоверных изменений не было выявлено ни по отношению к исходному уровню К1, ни по сравнению с контрольной группой К2 (таблица 9).
Хроническое использование диазепама приводило к увеличению количества эозинофилов по сравнению с К1 и числа моноцитов по отношению к контрольной группе К2, также снижалось число юных форм и палочкоядерных клеток по отношению к К1 и К2.
Применение амитриптилина сопровождалось появлением базофилов и увеличением количества сегментоядерных клеток, отсутствием юных форм и снижением уровня эозинофилов, палочкоядерных клеток по сравнению с исходным уровнем К1 и контрольной группой К2. Кроме того, по сравнению с К1 регистрировались увеличение содержания лимфоцитов и снижение числа моноцитов.
При использовании соединения 1 по сравнению с действием диазепама увеличилось количество юных форм, снизилось содержание эозинофилов. На фоне вещества 1, по сравнению влиянием амитриптилина, отсутствовали базофилы, появились юные формы, увеличилось количество эозинофилов, палочкоядерных клеток и моноцитов, снизилось содержание лимфоцитов.
Вывод. Соединение 1 при хроническом применении на лейкоцитарную формулу крови оказывало менее выраженное влияние в отличие от диазепама и амитриптилина.
Острая токсичность
Определение острой токсичности и расчет LD50 осуществляли по методу Кербера и установили, что для соединения (1) LD50 составляет 3476,4 мг/кг массы тела животных (мышей). LD50 диазепама для мышей - 240 мг/кг массы [Патент №1814291 A1]. LD50 амитриптилина для мышей - 280 (перорально) и 26 мг/кг (внутривенно) массы [Химическая энциклопедия. Режим доступа: http://www.xumuk.ru/encyklopedia/241.html (дата обращения 25.05.2016)], для крыс (внутрижелудочно) - 500,0±40,8 мг/кг [Дронова Ю.М. Фармакологическая коррекция олипифатом острых отравлений психотропными средствами: автореф. дисс… канд. мед. наук, Курск, 2005, - 22 с.]. Таким образом, исследуемое соединение (1) является относительно безвредным, относится к VI классу токсичности по Сидорову К.К. (1973). [Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ / под ред. В.П. Фисенко [и др.] - М.: ИАА Ремедиум, 2000, - 398 с.].
Вывод. Результаты проведенных исследований показывают, что изучаемое соединение обладает анксиолитической, актопротекторной и антидепрессивной активностью.
| название | год | авторы | номер документа |
|---|---|---|---|
| Диметоксибензилсульфопроизводное хиназолин-4(3Н)-она, обладающее анальгезирующей, противопаркинсонической, анксиолитической, психостимулирующей активностью | 2021 |
|
RU2758333C1 |
| 2-бензилпроизводное 4-(3Н)хиназолинона, обладающее анальгезирующим, противопаркинсоническим, антигипоксантным, транквилизирующим действием | 2019 |
|
RU2715884C1 |
| ПРОИЗВОДНЫЕ 4,6-ДИМЕТИЛ-2,3-ДИГИДРО-1Н-ПИРАЗОЛО[4,3-c]ПИРИДИН-3-ОНОВ И ЭФИРЫ 2,6-ДИМЕТИЛ-4-ФЕНИЛ-ГИДРАЗИНОНИКОТИНОВЫХ КИСЛОТ В КАЧЕСТВЕ ПРОМЕЖУТОЧНЫХ ПРОДУКТОВ ДЛЯ ИХ СИНТЕЗА, ОБЛАДАЮЩИЕ АНТИДЕПРЕССАНТНОЙ И АНКСИОЛИТИЧЕСКОЙ АКТИВНОСТЬЮ | 2007 |
|
RU2394034C2 |
| ФЕНИЛГИДРАЗИД (4-ФЕНИЛ-2-ПИРРОЛИДОН-1-ИЛ)-УКСУСНОЙ КИСЛОТЫ, ОБЛАДАЮЩИЙ НООТРОПНОЙ, АНТИДЕПРЕССИВНОЙ И АНКСИОЛИТИЧЕСКОЙ АКТИВНОСТЬЮ | 2010 |
|
RU2440981C1 |
| Фармацевтическая композиция на основе N-бутил-N-метил-1-фенилпирроло[1,2-а]пиразин-3-карбоксамида | 2023 |
|
RU2811453C1 |
| Анксиолитическое средство | 2017 |
|
RU2655929C1 |
| ПРОИЗВОДНЫЕ ХИНАЗОЛИНА, ОБЛАДАЮЩИЕ АНТИДЕПРЕССИВНОЙ, АНКСИОЛИТИЧЕСКОЙ И НООТРОПНОЙ АКТИВНОСТЬЮ | 2012 |
|
RU2507199C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ АНКСИОЛИТИЧЕСКИМ ДЕЙСТВИЕМ, НА ОСНОВЕ ГИДРИРОВАННЫХ ПИРИДО(4,3-b)ИНДОЛОВ (ВАРИАНТЫ), ФАРМАКОЛОГИЧЕСКОЕ СРЕДСТВО НА ЕГО ОСНОВЕ И СПОСОБ ЕГО ПРИМЕНЕНИЯ | 2007 |
|
RU2338533C1 |
| СОЛИ 2-ЭТИЛ-6-МЕТИЛ-3-ОКСИПИРИДИНА С ОРГАНИЧЕСКИМИ КАРБОНОВЫМИ КИСЛОТАМИ, ОБЛАДАЮЩИЕ АНКСИОЛИТИЧЕСКОЙ, АНТИДЕПРЕССИВНОЙ, ПРОТИВОГИПОКСИЧЕСКОЙ, АНТИАМНЕСТИЧЕСКОЙ И АНТИОКСИДАНТНОЙ АКТИВНОСТЬЮ, И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2002 |
|
RU2284993C2 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ АНТИДЕПРЕССИВНЫМ, АНКСИОЛИТИЧЕСКИМ И НООТРОПНЫМ ДЕЙСТВИЕМ | 2010 |
|
RU2437659C1 |
Изобретение относится к новому 2-бензоиламино-N-[4-(4,6-диметилпиримидин-2-илсульфамоил)-фенил]-бензамиду формулы (I), обладающему анксиолитическим, актопротекторным и антидепрессивным действием. Соединение может быть использовано для получения лекарственных средств для лечения неврозов, неврозоподобных состояний, психопатий, аффективных, депрессивных, психосоматических нарушений, сопровождаемых эмоционально-стрессорными и тревожными расстройствами. Соединение соответствует формуле (I) 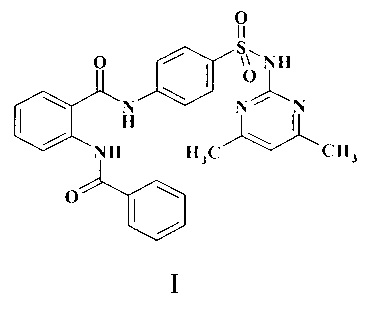 ,
,
является малотоксичным, а при хроническом применении оказывает менее выраженное влияние на лейкоцитарную формулу крови в отличие от диазепама. 1 з.п. ф-лы, 9 табл., 1 пр.
1. 2-Бензоиламино-N-[4-(4,6-диметилпиримидин-2-илсульфамоил)фенил]-бензамид
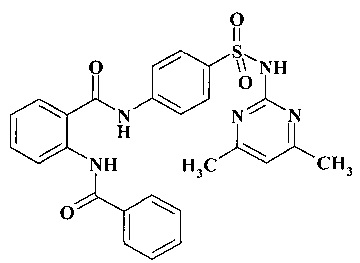
(I)
2. 2-Бензоиламино-N-[4-(4,6-диметилпиримидин-2-илсульфамоил)фенил]-бензамид, соответствующий формуле (I) по п.1, обладающий анксиолитической, актопротекторной и антидепрессивной активностью.
| ПРОИЗВОДНЫЕ 4-ОКСО-1,4-ДИГИДРОПИРИМИДИНА, ОБЛАДАЮЩИЕ АНТИАЛЛЕРГИЧЕСКОЙ И ИММУНОТРОПНОЙ АКТИВНОСТЬЮ | 1992 |
|
RU2015975C1 |
| DE 19710609 A1, 17.09.1998 | |||
| Прямоточный котел | 1948 |
|
SU77994A1 |
Авторы
Даты
2018-02-01—Публикация
2016-06-22—Подача