Область изобретения
Изобретение относится к области молекулярной биологии, вирусологии и биотехнологии, в частности, к диагностике инфекционных заболеваний, а именно к тест-системе для выявления SARS-CoV-2, Influenza virus A, Influenza virus B методом одношаговой полимеразной цепной реакции с обратной транскрипцией (далее по тексту - «ОТ-ПЦР»).
Предшествующий уровень техники
Пандемия COVID-19, вызванная новым коронавирусом SARS-CoV-2, продолжает оказывать серьезное влияние на общественное здравоохранение и социальные системы во всем мире. Поскольку клинические проявления и основные эпидемиологические признаки COVID-19 схожи с гриппом, важно обеспечить раннее выявление и соответствующее лечение обоих респираторных заболеваний, так как в будущем есть вероятность их совместного распространения. Система здравоохранения и общество в целом должны быть готовы к одновременным эпидемиям COVID-19 и гриппа. В частности, необходимо обеспечить наличие эффективного эпидемиологического надзора и диагностического потенциала для мониторинга данных инфекций, поскольку это будет лежать в основе решений о надлежащем клиническом лечении.
Таким образом, разработка мультиплекса грипп-ковид является актуальной проблемой современного здравоохранения.
Целью создания предлагаемого набора является расширение арсенала средств, используемых для диагностики гриппа и COVID-19, повышение эффективности такой диагностики, а также упрощение процесса диагностики, путем создания мультиплексной системы.
На сегодняшний день известны различные тест-системы для выявления нового коронавируса SARS-CoV-2 методом иммуноферментного анализа (далее по тексту - «ИФА») [1-5], а также ИФА тест-системы для одновременного обнаружения SARS-CoV-2 и вирусов гриппа[6-9]. При этом для обеспечения раннего выявления заболевания следует рассматривать способы и тест-системы, основанные на полимеразной цепной реакции (далее по тексту - «ПЦР), так как ИФА позволяет определить наличие антител (IgM и IgG) к SARS-CoV-2 и такой анализ может обнаружить наличие заболевания только через 1-2 недели после заражения. Использование ОТ-ПЦР для детекции РНК вируса SARS-CoV-2 позволяет обнаруживать патоген в наиболее значимый период времени - тогда, когда человек распространяет вирус: как до заражения (2-3 дня), так и после (5-8 дней). Также ОТ-ПЦР эффективен с точки зрения раннего выявления заболевания благодаря высокой чувствительности - возможности обнаружения малого количества молекул РНК SARS-CoV-2
Так, известен набор олигонуклеотидных праймеров и меченного флуоресцентным красителем олигонуклеотидного зонда для выявления РНК вируса SARS-CoV-2 [10], характеризующийся следующей структурой: прямой праймер SARS-CoV-2_up: 5’-TTGAAGTTTAATCCACCTGCT-3’; обратный праймер SARS-CoV-2_low: 5’-ACCGTTCAAGACTCTTTTGC-3’; меченный флуоресцентным красителем олигонуклеотидный зонд: 5’-(R6G)-CTTATTACAGAGCAAGGGCTGGTGAAG-(RTQ2)-3’. Также изобретение раскрывает набор реагентов для выявления РНК вируса SARS-CoV-2 методом ОТ-ПЦР, содержащий обратную транскриптазу (MMLV-ревертазу), Таq-полимеразу, эквимолярную смесь четырех дезоксинуклеотидтрифосфатов, внутренний контрольный образец, отрицательный контрольный образец, набор олигонуклеотидных праймеров и флуоресцентно-меченый олигонуклеотидный зонд, положительный контрольный образец, в качестве которого используется синтетическая РНК, последовательность которой соответствует области гибридизации олигонуклеотидных праймеров, при этом олигонуклеотидные праймеры и зонд используют в лиофильно высушенном состоянии.
Кроме того, известен набор олигодезоксирибонуклеотидных праймеров и флуоресцентно-меченого зонда для идентификации РНК коронавируса человека 2019-nCoV методом ПЦР с гибридизационно-флуоресцентной детекцией в режиме реального времени [11], содержащий одну пару олигонуклеотидов, обладающих активностью прямого и обратного праймеров в полимеразной цепной реакции, а также флуоресцентно-меченый ДНК-зонд, имеющие следующую первичную последовательность: прямой (F) 5'-TAGACATCATGCTAATGAGTACAGAT-3' 26; обратный (R) 5'-TGAAGTCTTGTAAAAGTGTTCCAG-3' 24; флуоресцентно-меченый ДНК-зонд (Z): 5'-ROX-GCTTATAACATGATGATCTCAGCTGGC-BHQ1-3' 27.
Также известен набор олигодезоксирибонуклеотидных праймеров и флуоресцентно-меченого ДНК-зонда для идентификации коронавирусов человека SARS и 2019-nCoV методом ОТ-ПЦР с гибридизационно-флуоресцентной детекцией [12], содержащий одну пару олигонуклеотидов, обладающих активностью прямого и обратного праймеров в полимеразной цепной реакции, а также флуоресцентно-меченый ДНК-зонд, имеющие следующую первичную последовательность: прямой (F4) и обратный (R5) праймеры F4: 5'-GTTGCAACTGAGGGAGCCTTG-3' 21 и R5: 5'-GAGAAGAGGCTTGACTGCCG-3' 20; флуоресцентно-меченый ДНК-зонд (Pb1) Pb1: 5'-FAM-TACACCAAAAGATCACATTGGCACCCG-BHQ1-3' 27.
Также известен лиофилизированный реагент для ПЦР в отношении COVID-19, FluA и FluB [13], со следующей структурой: последовательность прямого праймера для COVID-19: 5’-AGAATGGAGAACGCAGTGGG-3 ’; последовательность обратного праймера для COVID-19: 5’-TGAGAGCGGTGAACCAAGAC-3 ’; TaqMan зонд для COVID-19: 5’-FAM-CGCGATCAAAACAACGTCGGCC-BHQ13’, последовательность прямого праймера для FluA: 5’-5’-GTTGGTRATGAAACGRAAACGGG-3’; последовательность обратного праймера для FluA: 5’-CCGAATYCTTTTGGTCGCTGT-3’; TaqMan зонд для FluA: 5’-VIC-CTCTAGCATACTTACTGACAGC-MGB-3’, последовательность прямого праймера для FluB: 5’-CACAAATGCAACCAGACCTGC-3’; последовательность обратного праймера для FluB: 5’-GGGGAGAGAAAATTCTCCTGCAT-3’; TaqMan зонд для FluB: 5’-Cy5-TTAGACAGRATAGCTGCTGGCA-MGB-3’, последовательность прямого праймера для GAPDH: 5’-ACTTAGAGAAGGGGTGGGCT-3’; последовательность обратного праймера для GAPDH: 5’-ACGCTTGTACACTCAGCATCA-3’; TaqMan зонд для GAPDH: 5’-ROX-ccctgtccagttaatttctgacctttactcctgC-BHQ2-3’.
Также известен набор для ОТ-ПЦР и способ обнаружения вируса гриппа A, вируса гриппа B и коронавируса SARS-CoV-2 [14], включающий набор лиофилизированных реагентов и специфических праймеров для обнаружения вируса гриппа А, вируса гриппа В и коронавируса SARS-CoV-2, а также соответствующие зонды.
Таким образом, известно несколько типов тест-систем для обнаружения вируса гриппа А, В и коронавируса SARS-CoV-2.
Описание фигур
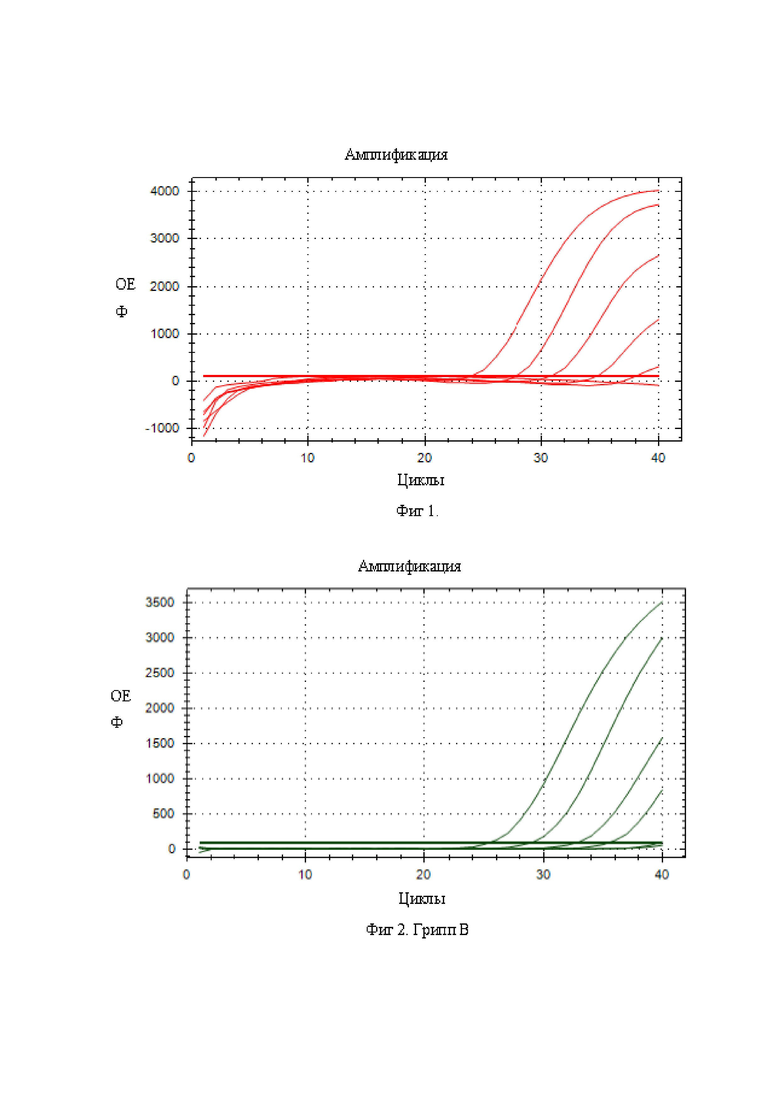
Фиг. 1 приведены результаты мультиплексного анализа вируса Гриппа A.
Фиг. 2 приведены результаты мультиплексного анализа вируса Гриппа В.
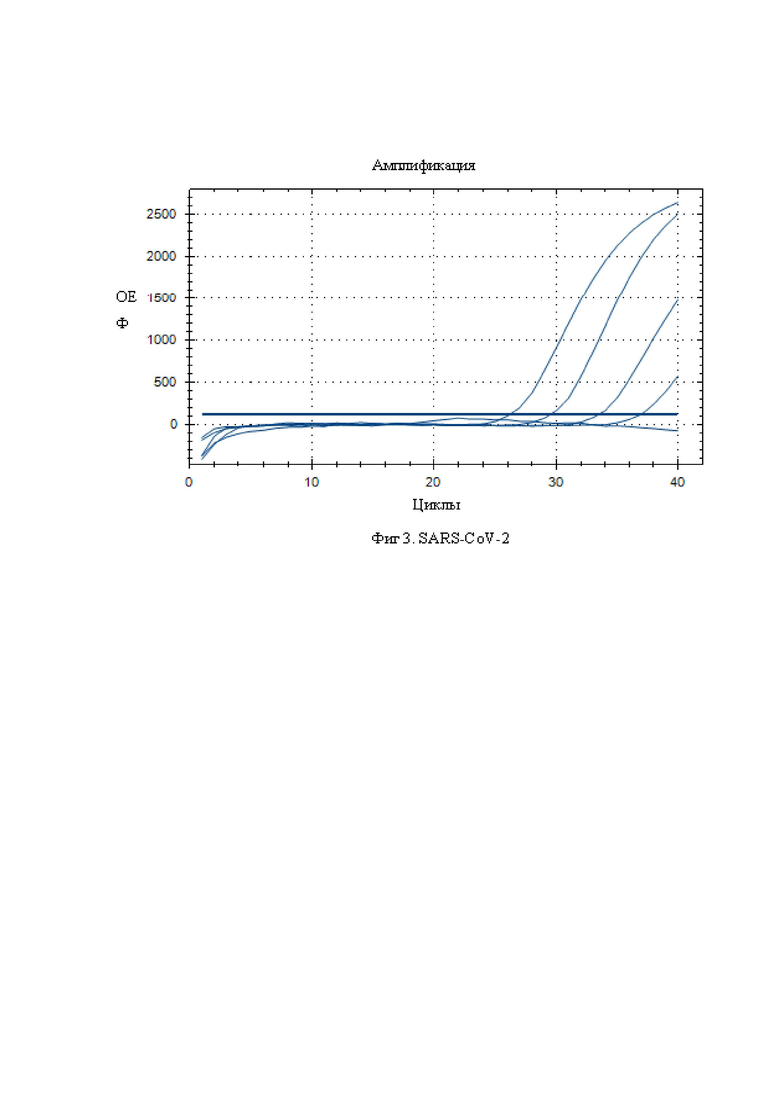
Фиг. 3 приведены результаты мультиплексного анализа вируса SARS-CoV-2.
Описание изобретения
Технической проблемой является необходимость расширения арсенала средств мультиплексного анализа для диагностики гриппа и COVID-19.
Технический результат состоит в реализации возможности эффективного мультиплексного анализа для диагностики гриппа и COVID-19 методом полимеразной цепной реакции с обратной транскрипцией.
Технический результат достигается тем, что тест-система для выявления SARS-CoV-2, Influenza virus A, Influenza virus B методом одношаговой полимеразной цепной реакции с обратной транскрипцией включает набор олигонуклеотидных праймеров и флуоресцентных зондов со следующей структурой:
прямой праймер вируса гриппа В ATTCTTCAATgAAgAAggAAC (SEQ ID NO: 1)
обратный праймер вируса гриппа В CTCCCAACACggTAgATA (SEQ ID NO: 2)
флуоресцентный зонд вируса гриппа В (R6G)-TCCCATCATCATyCCAgg-(BHQ-1) (SEQ ID NO: 3)
прямой праймер вируса гриппа А CACCAAAyCATgArggAATA (SEQ ID NO: 4)
обратный праймер вируса гриппа А gCTCATgTTgATTCCCAC (SEQ ID NO: 5)
флуоресцентный зонд вируса гриппа А (ROX)-TgCAggTCCTrTAgAATCTrTCCACTC-(BHQ-2) (SEQ ID NO: 6)
прямой праймер SARS-CoV-2 AgAgCTATgAATTgCAgAC (SEQ ID NO: 7)
обратный праймер SARS-CoV-2 gggAAATACAAAATTTggACA (SEQ ID NO: 8)
флуоресцентный зонд SARS-CoV-2 (FAM)-AATTggCAAAgAAATTTgACACCTTCA-(BHQ-1) (SEQ ID NO: 9)
Сущность изобретения состоит в том, что с помощью вышеприведенных праймеров и зондов определяют присутствие в пробе РНК вирусов гриппа В, гриппа А и SARS-CoV-2. Этот процесс включает выделение РНК исследуемой пробы, проведение обратной транскрипции и ПЦР с учетом результатов в режиме реального времени, согласно изобретению.
Заявляемая тест-система была получена путем конструирования диагностических праймеров и флуоресцентно-меченного зонда на консервативный участок гена ORF1 в случае SARS-CoV-2 и гена PB1 в случае гриппа А и гриппа В; оптимизации концентраций компонентов реакционной смеси и условий проведения ПЦР; проверки специфичности.
На начальном этапе были подобраны и синтезированы по 3 пары специфических олигонуклеотидных праймеров и зондов для гибридизационно-флуоресцентной детекции продуктов ПЦР для SARS-CoV-2 и Influenza virus A, и 2 пары для Influenza virus B. Для этого в базе данных GISAID (https://www.gisaid.org) был выбран наиболее консервативный участок генома SARS-CoV-2, Influenza virus A, Influenza virus B. Подбор и анализ свойств олигонуклеотидных праймеров и флуоресцентного зонда проводился с использованием программного обеспечения Beacon designer. Анализ специфичности проводили в BLAST (Nucleotide BLAST: Search nucleotide databases using a nucleotide query (nih.gov) Nucleotide BLAST: Search nucleotide databases using a nucleotide query (nih.gov). Были проанализированы все имеющиеся в базе данных последовательности. Далее, после ряда экспериментов по проверке на чувствительность, были отобраны лучшие пары праймеров для каждого патогена (таблица 1).
Для оптимизации работы тест-системы была проведена серия экспериментов по подбору рабочей концентрации праймеров и поставлен эксперимент с градиентом температуры отжига праймеров для подбора оптимального значения в условиях мультиплексной реакции. По результатам экспериментов оптимальная концентрация праймеров и зондов составила
600 нМ, оптимальная температура отжига 58°С.
Анализ результатов был произведён с помощью программного обеспечения прибора, используемого для проведения ПЦР с гибридизационно-флуоресцентной детекцией в режиме реального времени. Результаты интерпретировали на основании наличия или отсутствия пересечения кривой флуоресценции с установленной на соответствующем уровне пороговой линией, что соответствует наличию или отсутствию значения порогового цикла Ct, причем результат считали положительным в случае, если кривая накопления флуоресценции для соответствующего образца имела характерную сигмовидную форму и пересекала пороговую линию.
Аналитическую специфичность набора оценивали с помощью панели нуклеиновых кислот 12 респираторных вирусов (таблица 2) из собственной коллекции. В результате исследования перекрестных реакций не зафиксировано.
Таким образом, в результате проведенных исследований был разработан и апробирован набор для выявления РНК коронавируса вида SARS-CoV-2, а также РНК вирусов гриппа A и гриппа B.
Заявляемое изобретение поясняется примером.
Пример 1
Диагностика проводилась согласно МУ 1.3.2569-09 «Организация работы лабораторий, использующих методы амплификации нуклеиновых кислот при работе с материалом, содержащим микроорганизмы I-IV групп патогенности». Материалом для исследования служили клинические и биологические образцы. Экстракция производилась согласно инструкции производителя набора для выделения.
После экстракции РНК приступали к постановке одношаговой ОТ-ПЦР в режиме реального времени. Был использован набор «БиоМастер ОТ-ПЦР-РВ (Х2)» фирмы Biolabmix (Новосибирск). Для этого готовился ПЦР-микс, состоящий из смеси праймеров и зондов, буферного раствора, дистиллированной стерильной воды и фермента. Пропись реакции на один образец: 12,5 мкл 2х буфера; по 0,15 мкл праймеров и зондов (рабочая концентрация 100 пикомоль/мкл); 1 мкл фермента 25х БиоМастер-микс; 5,15 мкл дистиллированной стерильной воды; 5 мкл РНК. Конечный объем реакционной смеси составлял 25 мкл. Для контроля замешивания реакционной смеси и прохождения ПЦР дополнительно ставили положительный и отрицательный контроли.
Микропробирки, плашку или стрипы переносили в программируемый амплификатор с функцией амплификации в режиме реального времени с наличием 3 каналов детекции флуоресценции (FAM/Green, HEX/Yellow, ROX/Orange). По каналу FAM/Green детектировался SARS-CoV-2, по каналу HEX/Yellow детектировался грипп В, по каналу ROX/Orange детектировался грипп А. Режим амплификации представлен в таблице 3.
Также результаты мультиплексного анализа показаны на фигурах, в частности на фиг. 1 показаны результаты анализа вируса Гриппа A, на фиг. 2 - гриппа B, на фиг. 3 - SARS-CoV-2.
Таким образом было показано, что заявляемый набор позволяет достоверно выявлять РНК коронавируса вида SARS-CoV-2, Influenza virus A и Influenza virus B в клинических пробах.
После проведения необходимых экспериментов авторы заявляют набор, с помощью которого возможен анализ РНК, выделенной из биологических образцов (кровь и ее производные, мазок из носоглотки, мазок из ротоглотки, мокрота), методом одношаговой ОТ-ПЦР в режиме реального времени. Данный метод подходит для выявления целевых фрагментов РНК генома коронавируса вида SARS-CoV-2, а также вирусов гриппа А и гриппа B, с использованием набора олигонуклеотидных праймеров и соответствующих флуоресцентно-меченных зондов, комплементарных участку гена ORF1 SARS-CoV-2 и гена PB1 гриппа А и В.
Список литературы
1. Способ использования рекомбинантных белков SARS-COV-2 в составе тест-системы для иммуноферментного анализа с определением уровней антител классов IgM, IgG, IgA В сыворотке/плазме крови больных COVID-19: патент RU2730897, Российская Федерация, заявка RU2020121770, заявл. 01.07.2020, опубл. 26.08.2020.
2. Набор для выявления вируса SARS-CoV методом ОТ-ПЦР в реальном времени: патент RU2744198, Российская Федерация, заявка RU2020118246, заявл. 25.05.2020, опубл. 03.03.2021.
3. Тест-система и способ для выявления РНК коронавируса SARS-COV-2, вируса-возбудителя коронавирусного заболевания 2019 COVID-19, методом полимеразной цепной реакции в режиме реального времени (Варианты): патент RU2731390, Российская Федерация, заявка RU2020113326, заявл. 12.04.2020, опубл. 02.09.2020.
4. Диагностический маркер и его применение в диагностике COVID-19 и выявлении предшествующей инфекции: заявка CN111999508, Китайская Народная Республика, 25.09.2020, опубл. 27.11.2020.
5. Набор для диагностики и обнаружения коронавируса нового типа: заявка TR202006563, Турецкая Республика, заявл. 27.04.2020, опубл. 21.09.2020.
6. Тест-полоска для комбинированного выявления гриппа и COVID-19: заявка CN111537727, Китайская Народная Республика, заявл. 04.06.2020, опубл. 14.08.2020.
7. Набор реагентов для обнаружения новых коронавирусов и вирусов гриппа: патент CN111254228, Китайская Народная Республика, заявка CN202010370223, заявл. 06.05.2020, опубл. 09.06.2020.
8. Набор «три в одном» для обнаружения нового коронавируса, антигена вируса гриппа A и антигена вируса гриппа B, а также методы их приготовления и использования: заявка CN112557655, Китайская Народная Республика, заявл. 06.01.2021, опубл. 26.03.2021.
9. Набор для тестирования лиофилизированных новых коронавирусов, вирусов гриппа и вирусов гепатита и метод обнаружения: заявка CN111778362, Китайская Народная Республика, заявл. 10.08.2020, опубл. 16.10.2020.
10. Набор реагентов для выявления РНК вируса SARS-CoV-2, возбудителя нового коронавирусного заболевания COVID-2019, методом обратной транскрипции-полимеразной цепной реакции в реальном времени: патент RU2732608, Российская Федерация, заявка RU2020114301, заявл. 09.04.2020, опубл. 21.09.2020.
11. Набор олигодезоксирибонуклеотидных праймеров и флуоресцентно-меченого зонда для идентификации РНК коронавируса человека 2019-nCoV методом ПЦР с гибридизационно-флуоресцентной детекцией в режиме реального времени: патент RU2734300, Российская Федерация, заявка RU2020120618, заявл. 16.06.2020, опубл. 14.10.2020.
12. Набор олигодезоксирибонуклетидных праймеров и флуоресцентно-меченого зонда для идентификации РНК коронавирусов человека SARS и 2019-nCoV методом ОТ-ПЦР с гибридизационно-флуоресцентной детекцией в режиме реального времени: патент RU2733665, Российская Федерация, заявка RU2020120619, заявл. 16.06.2020, опубл. 06.10.2020.
13. Лиофилизированный реагент для ПЦР (полимеразной цепной реакции) для обнаружения вирусов COVID-19, FluA и FluB и способ его получения: заявка CN111647688, Китайская Народная Республика, заявл. 18.06.2020 , опубл. 11.09.2020.
14. Флуоресцентный реагент ОТ-ПЦР и метод обнаружения вируса гриппа A, вируса гриппа B и коронавируса SARS-CoV-2: заявка CN112410469, Китайская Народная Республика, заявл. 23.11.2020, опубл. 26.02.2020.
| название | год | авторы | номер документа |
|---|---|---|---|
| Тест-система для выявления SARS-CoV-2 линии Омикрон методом одношаговой полимеразной цепной реакции с обратной транскрипцией | 2021 |
|
RU2772362C1 |
| Тест-система на основе полимеразной цепной реакции с обратной транскрипцией для выявления SARS-CoV-2 линии Омикрон с определением субварианта BA.1 | 2022 |
|
RU2779025C1 |
| Набор реагентов для выявления РНК вируса SARS-CoV-2 методом прямой полимеразной цепной реакции в режиме реального времени | 2022 |
|
RU2795939C2 |
| Набор реагентов для выявления РНК вируса SARS-CoV-2, возбудителя нового коронавирусного заболевания COVID-2019, методом обратной транскрипции-полимеразной цепной реакции в реальном времени | 2020 |
|
RU2732608C1 |
| Набор олигонуклеотидов и способ мультиплексной полимеразной цепной реакции в режиме реального времени для выявления РНК SARS-CoV-2 | 2021 |
|
RU2752902C1 |
| НАБОР РЕАГЕНТОВ ДЛЯ ОБНАРУЖЕНИЯ РНК SARS-COV-2 МЕТОДОМ ПЕТЛЕВОЙ ИЗОТЕРМИЧЕСКОЙ АМПЛИФИКАЦИИ В РЕАЛЬНОМ ВРЕМЕНИ (КОВИГЕН-LAMP) | 2022 |
|
RU2779189C1 |
| Тест-система для обнаружения РНК вируса SARS-CoV-2 в биоматериале от животных, пищевых продуктах и объектах окружающей среды методом полимеразной цепной реакции в режиме реального времени | 2021 |
|
RU2756474C1 |
| Набор олигодезоксирибонуклетидных праймеров и флуоресцентно-меченого зонда для идентификации РНК коронавирусов человека SARS и 2019-nCoV методом ОТ-ПЦР с гибридизационно-флуоресцентной детекцией в режиме реального времени | 2020 |
|
RU2733665C1 |
| Тест-система и способ для выявления РНК коронавируса SARS-COV-2, вируса-возбудителя коронавирусного заболевания 2019 COVID-19, методом полимеразной цепной реакции в режиме реального времени (Варианты) | 2020 |
|
RU2731390C1 |
| Набор олигодезоксирибонуклеотидных праймеров и флуоресцентно-меченого зонда для идентификации РНК коронавируса человека 2019-nCoV методом ПЦР с гибридизационно-флуоресцентной детекцией в режиме реального времени | 2020 |
|
RU2734300C1 |
Изобретение относится к области молекулярной биологии, вирусологии и биотехнологии. Описана тест-система для выявления SARS-CoV-2, Influenza virus A и Influenza virus B методом одношаговой полимеразной цепной реакции с обратной транскрипцией. Тест-система включает олигонуклеотидные праймеры и флуоресцентные зонды со следующей структурой: прямой праймер вируса гриппа В ATTCTTCAATgAAgAAggAAC; обратный праймер вируса гриппа В CTCCCAACACggTAgATA; флуоресцентный зонд вируса гриппа В (R6G)-TCCCATCATCATyCCAgg-(BHQ-1); прямой праймер вируса гриппа А CACCAAAyCATgArggAATA; обратный праймер вируса гриппа А gCTCATgTTgATTCCCAC; флуоресцентный зонд вируса гриппа А (ROX)-TgCAggTCCTrTAgAATCTrTCCACTC-(BHQ-2); прямой праймер SARS-CoV-2 AgAgCTATgAATTgCAgAC; обратный праймер SARS-CoV-2 gggAAATACAAAATTTggACA; флуоресцентный зонд SARS-CoV-2 (FAM)-AATTggCAAAgAAATTTgACACCTTCA-(BHQ-1). Технический результат состоит в реализации возможности эффективного мультиплексного анализа для диагностики гриппа и COVID-19 методом полимеразной цепной реакции с обратной транскрипцией. 2 з.п. ф-лы, 3 ил., 3 табл., 1 пр.
1. Тест-система для выявления SARS-CoV-2, Influenza virus A и Influenza virus B методом одношаговой полимеразной цепной реакции с обратной транскрипцией, включающая набор олигонуклеотидных праймеров и флуоресцентных зондов со следующей структурой:
2. Тест-система по п. 1, отличающаяся тем, что оптимальная концентрация праймеров и зондов составляет 600 нМ.
3. Тест-система по п. 1, отличающаяся тем, что оптимальная температура отжига составляет 58°С.
| US 20210040571 A1, 11.02.2021 | |||
| CN 111593142 A, 28.08.2020 | |||
| Тест-система и способ для выявления РНК коронавируса SARS-COV-2, вируса-возбудителя коронавирусного заболевания 2019 COVID-19, методом полимеразной цепной реакции в режиме реального времени (Варианты) | 2020 |
|
RU2731390C1 |
| Ученые создали комбинированную тест-систему для коронавируса и гриппа, 27 октября 2020 [Найдено в интернет 01.10.2021] https://www.interfax.ru/russia/734387. | |||
Авторы
Даты
2021-12-08—Публикация
2021-09-07—Подача