Группа изобретений относится к медицине, а именно к стоматологии и может быть использована для лечения и профилактики стоматологических заболеваний, сформированных как до, так и после прорезывания зубов, включая некариозные поражения твердых тканей зубов, гиперестезию, начальные формы кариеса, терапию осложнений после ортодонтического лечения и отбеливания, в том числе профилактику этих состояний.
Перспективным направлением в стоматологии является разработка малоинвазивных технологий, которые позволяют применять лечебные программы на ранних стадиях заболевания, купируя его (Гилева О. С., Муравьева М.А., Свистков А.Л., Изюмов Р.И., Левицкая А.Д., 2017). Наиболее эффективным методом, основанным на применении малоинвазивных технологий, является лечение пациентов с использованием устройств для доставки, локального удерживания и прецизионного воздействия лекарственных препаратов непосредственно на патологический очаг зуба. Это позволяет в большинстве случаев отказаться от методик, связанных с ротационно-механическим препарированием кариозных и некариозных поражений твердых тканей зубов, которые приводят к удалению не только пораженных патологическим процессом тканей, но и неповрежденных, окружающих его, а также снизить частоту рецидива заболевания, развития осложнений и неудовлетворительных результатов лечения (Расулов Г.М., 2004).
Известно стоматологическое устройство, используемое в качестве внутриротовой системы доставки лекарственных препаратов (патент US8505541 от 13.08.2013), представляющее собой U-образную каппу с одним каналом для зубной дуги, имеющую расположенные в канале углубления, в которые устанавливаются вкладыши с лекарственным веществом. Устройство изготавливается методом вакуумной термоформовки сополимера этиленвинилацетата (EVA) с учетом параметров зубной дуги пациента.
Однако устройство имеет ряд недостатков:
1. Невозможно использовать на двух челюстях одновременно;
2. Является массивным из-за необходимости применения внутренних вкладышей, фиксирующихся в углублениях канала, что доставляет дополнительный дискомфорт пациенту во время лечения;
3. Устройство необходимо снимать во время приема пищи;
4. Изготавливается из пластмассы, такой как сополимер этиленвинилацетата (EVA), что часто вызывает аллергические реакции мягких тканей полости рта.
5. Не обеспечивает прецизионной аппликации и депонирования лекарственного препарата только в патологическом очаге твердых тканей зубов;
6. Использование устройства может привести к травмированию зубодесневой связки избытком лекарственного вещества, выходящим за пределы дефекта твердых тканей зуба.
В качестве прототипа выбран патент US6607382 «Методы и системы для одновременной репозиции зубов и доставки вещества». В одном из вариантов своего осуществления с целью доставки лекарственного препарата без одновременного изменения положения зубов, описана индивидуальной формы съемная каппа из эластичного материала, внутренняя поверхность которой соответствует внешней поверхности зубов пациента, имеющая на своей внутренней поверхности резервуар для лекарственного препарата. Устройство изготавливается путем 3D-сканирования гипсового слепка зубного ряда пациента, загрузки полученных данных в программное обеспечение, компьютерного моделирования трехмерной модели макета челюсти пациента с учетом объемных параметров резервуара для лекарственного препарата, SLA 3D-печати макета челюсти пациента, вакуумного термоформования из эластичного материала, заполнения резервуара устройства лекарственным препаратом.
Прототип имеет следующие недостатки:
1. Создание трехмерной модели зубного ряда пациента осуществляется с использованием гипсовых слепков, что снижает прецизионность устройства.
2. Способ изготовления устройства не обеспечивает возможности создания резервуара для лекарственного препарата, прецизионно соответствующего патологическому очагу твердых тканей зуба, что может приводить к повреждению зубодесневой связки лекарственным препаратом, воздействию лекарственного препарата на неповрежденные ткани зуба, контакту лекарственного вещества с ротовой жидкостью и нарушению ее pH среды.
3. Создание резервуара для лекарственного препарата производится без учета размеров частиц его основного действующего вещества, что не позволяет достигнуть дозированной концентрации лекарственного препарата в зоне патологического очага.
4. Материал, из которого изготавливается устройство, не позволяет его использовать постоянно, что приводит к вымыванию лекарственного препарата ротовой жидкостью при периодическом снимании каппы, отсутствию возможности длительной аппликации лекарственного вещества, снижению клинической эффективности устройства.
5. При изготовлении устройства не обеспечивается возможность изменения его толщины, в зависимости от клинической ситуации, что может приводит к разрушению каппы в процессе лечения, развитию дисфункции височно-нижнечелюстного сустава.
Задача предлагаемой группы изобретений - создание устройства и способа его изготовления, лишенных недостатков прототипа.
Технический результат - повышение эффективности лечения за счет высокоточного дозирования лекарственного препарата и его длительной аппликации только в области патологического очага твердых тканей зубов, возможности одновременного применения устройства на обеих челюстях постоянно на весь период лечения.
Технический результат достигается тем, что устройство для доставки лекарственного вещества в патологические очаги твердых тканей зубов выполнено в виде съемной каппы из эластомерного термопластичного полиуретана, внутренняя поверхность которой соответствует внешней поверхности зубов пациента и имеет в проекции каждого патологического очага области, состоящие из множеств микрорезервуаров диаметром 0,1-0,5 мм.
Предпочтительно устройство для доставки лекарственного вещества в патологические очаги твердых тканей зубов выполняют из эластомерного термопластичного полиуретана толщиной 0,5-0,75 мм.
Технический результат достигается также тем, что в способе изготовления устройства для доставки лекарственного вещества в патологические очаги твердых тканей зубов, включающем компьютерное моделирование трехмерной модели макета челюсти пациента с учетом объемных параметров резервуара для лекарственного препарата, SLA 3D-печать макета челюсти, вакуумное термоформование из эластичного материала, патологические очаги определяют интраорально с использованием лазерного флуоресцентного анализа, границы выявленных патологических очагов выделяют грифелем, выполняют интраоральное 3D-сканирование зубных рядов пациента, выполняют компьютерное моделирование патологического очага с учетом выделенных границ, моделируют шары диаметром 0,1-0,5 мм, однослойно заполняют шарами области патологических очагов, выполняют булеву операцию по объединению модели патологических очагов и шаров их заполняющих.
Предложенная группа изобретений поясняется графическими материалами, где:
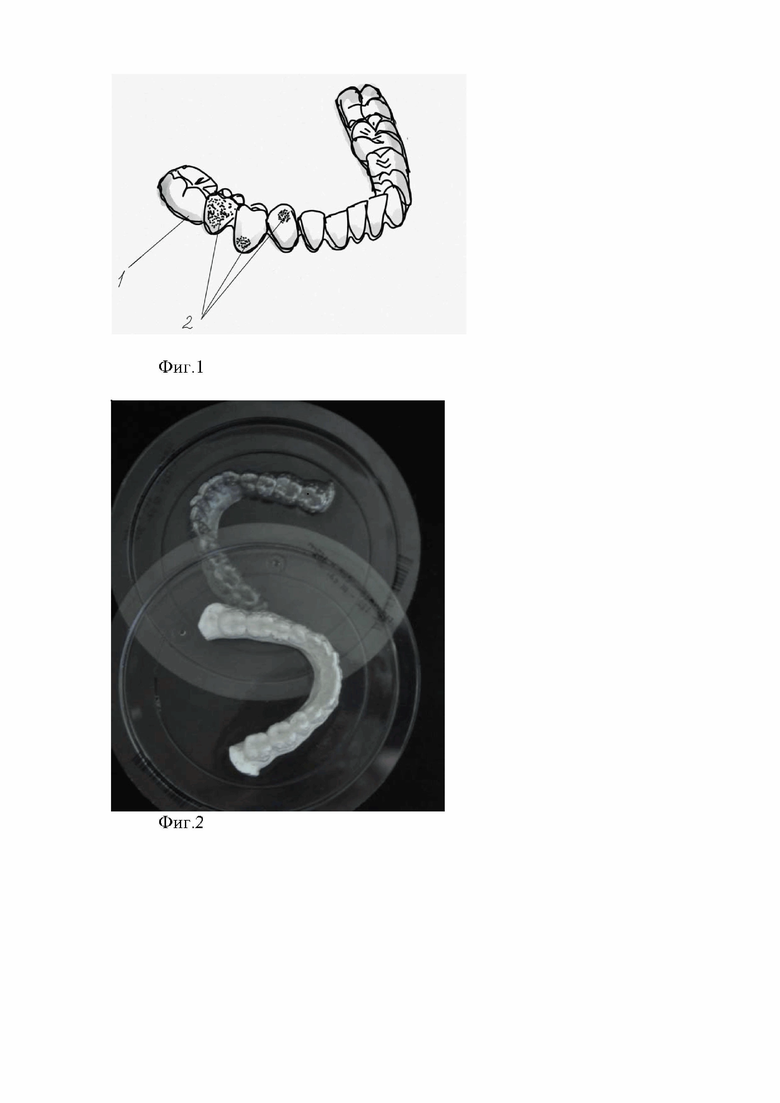
Фиг. 1 - рисунок устройства для доставки лекарственного вещества в патологические очаги твердых тканей зубов.
Фиг. 2 - фотография устройства, полученного в результате вакуумного термоформования, и напечатанная на 3D-принтере модель челюсти, на которой было произведено обжатие.
Устройство для доставки лекарственного вещества в патологический очаг твердых тканей зубов представляет собой индивидуальной формы съемную каппу 1 выполненную из эластомерного термопластичного полиуретана. Внутренняя поверхность каппы соответствует внешней поверхности зубов пациента и имеет область множества микрорезервуаров диаметром 0,1-0,5 мм в проекции каждого патологического очага 2 (Фиг.1).
Устройство для доставки лекарственного вещества в патологические очаги твердых тканей зубов изготавливают следующим образом. На клиническом приеме, пациенту, нуждающемуся в изготовлении устройства, проводят окрашивание каждого патологического очага твердых тканей зуба с использованием жидкостей для визуализации повреждения подповерхностных слоев твердых тканей зубов и лазерный флуоресцентный анализ патологического очага. Определяют лекарственный препарат, планируемый к использованию, фиксируют максимальное значение размера частиц действующего вещества. Очерчивают границы патологического очага грифелем для визуализации границ при интраоральном 3D-сканировании. Проводят интраоральное 3D-сканирование зубного ряда с точностью до 15 микрон соответствия биологическому объекту, что позволяет получить его трехмерную модель, на которой детально воспроизведена анатомия челюсти, поверхность зубов и десен, визуализированы границы патологического очага и его топологическое размещение. Детализированную виртуальную модель зубного ряда загружают в программное обеспечение для компьютерного моделирования. На трехмерной модели выполняют гибридное параметрическое моделирование каждого патологического очага с учетом границ, обведенных до 3D-сканирования грифелем. Выполняют моделирование шаров диаметром равным 70 максимальных размеров основного действующего вещества лекарственного препарата, выраженного в мм, округленного до одного знака после запятой. При этом, если полученное значение менее 0,1 мм, то диаметр шара принимают равным 0,1 мм, а если полученное значение более 0,5 мм, то диаметр шара принимают равным 0,5 мм. Заполняют шарами однослойно каждый патологический очаг. Затем осуществляют булеву операцию по объединению трехмерной модели и шаров, прецизионно заполняющих каждый патологический очаг. Получают модель челюсти пациента с выпуклостями в области каждого патологического очага. Выполняют ее SLA 3D-печать. Методом вакуумного формования эластомерного термопластичного полиуретана толщиной 0,5-0,75 мм с использованием напечатанного макета челюсти пациента выполняют создание персонифицированного устройства (Фиг.2). В результате вакуумного формования в проекции каждого патологического очага формируют область, представленную множеством микрорезервуаров для доставки лекарственного средства. Устройство шлифуют, полируют.
Клинический пример 1.
На терапевтическое лечение поступила пациентка О., 29 лет.
Жалобы: на быстропроходящую боль от температурных раздражителей в области зубов 3.4,3.3,4.3,4.4, боль от химических раздражителей в области 34 зуба.
Объективно: КПУ (кариес, пломба, удаленный) = 7; ИГР-У (степень гигиены полости рта) = 2; PMA (для оценки тяжести гингивита, а в последующем и регистрации динамики процесса) - 1; индекс рецессии десны - 2, ИР (индекс реминерализации эмали) - 2, Индекс распространенности и выраженности гиперестезии - 40 (генерализованная форма), ИИГЗ (индекс интенсивности гиперестезии зубов) = 1,5 ( гиперестезия I степени). На вестибулярной̆ поверхности 4.3, 4.4, 3.3, 3.4 зубов обнаружены клиновидные дефекты, с гладким и плотным дном. Дополнительным методом диагностики стала электроодонтодиагностика (ЭОД) аппаратом ЭОД-10.
Пациентке произведено окрашивание патологического очага каждого зуба с использованием метиленового синего. Затем выполнен лазерный флуоресцентный анализ патологических очагов с использованием аппарата - KaVo «DIAGNOdent Pen». Границы каждого очага обведены грифелем. В результате интраорального 3D-сканирования зубного ряда пациентки с точностью 15 микрон соответствия биологическому объекту получена его трехмерная модель, на которой детально воспроизведена анатомия челюсти больной, структура ее зубов и десен, а также топологическое размещение поврежденных участков твердых тканей зуба.
Для контроля эффективности лечения выполнена электроодонтодиагностика (ЭОД) поврежденных зубов. Получены следующие значения:
4.3. - ЭОД = 6 мкА; 4.4 - ЭОД = 7мкА; 3.3. ЭОД = 6мкА; 3.4. - ЭОД = 5мкА.
Далее детализированную виртуальную модель зубного ряда, полученную c использованием интраорального 3D-сканирования, загрузили в программное обеспечение для компьютерного моделирования Autodesk Meshmixer и выполнили гибридное параметрическое моделирование каждого патологического очага с учетом границ, обозначенных грифелем. Для лечебного воздействия выбран препарат Biorepair Desensitizing Enamel Repairer Treatment, способный образовывать гомогенный слой на поверхности зуба, проникать в микроповреждения эмали, а входящий в его состав гидроксиапатит microRepair взаимодействует с гидроксиапатитом зуба, химически связывается с ним, восстанавливает и реминерализируяет. Размер микрокристаллов гидроксиапатита в выбранном препарате от 20 до 100 нм (100 нм=0,0001 мм), 70×0,0001=0,007, поэтому диаметр шаров принят равным 0,1 мм. Выполнено моделирование шара, который размножили для однослойного заполнения каждого патологического очага. Выполнили булеву операцию по объединению модели челюсти и шаров, однослойно заполняющих патологические очаги. Получили модель челюсти пациентки с выпуклостями в области каждого патологического очага пораженных зубов. После этого была произведена SLA 3D-печать макета челюсти пациентки с наличием множества выпуклостей округлой формы в области патологических очагов зубов 3.4, 3.3, 4.4, 4.3. Поскольку устройство изготавливалось только для нижней челюсти использован эластомерный термопластичный полиуретан DURAN® (Scheu Dental, Германия) 0,75×125 мм. Методом вакуумного формования с использованием напечатанной модели изготовлено индивидуальное устройство. В проекции областей, соответствующих патологическим очагам зубов 3.4, 3.3, 4.4, 4.3, сформировано множество микрорезервуаров. Затем осуществлена шлифовка, полировка устройства. Устройство обработано антисептиком. После этого микрорезервуары устройства были заполнены препаратом Biorepair Desensitizing Enamel Repairer Treatment. Пациентке продемонстрированно дозирование и введение препарата в устройство, правила фиксирования его на зубах, гигиенический уход. Курс лечения составил 7 дней.
На контрольном осмотре пациентка жалоб не предъявляет.
Объективно: КПУ = 7; ИГР-У = 0; PBI - 0; PMA - 0; индекс рецессии десны - 2, ИР (индекс реминерализации эмали) - 1, Индекс распространенности и выраженности гиперестезии- 3.5 (ограниченная форма гиперестезии), ИИГЗ = 0 (отсутствие гиперестезии). Зондирование безболезненно. Зуб 4.3 ЭОД = 4 мкА; зуб 4.4 - ЭОД = 4 мкА; зуб 3.3 - ЭОД = 3мкА; зуб 3.4. - ЭОД = 2мкА.
Клиническое улучшение индексов реминерализации, выраженности гиперестезии, улучшение показаний объективных методов диагностики таких как электроодонтодиагностика, лазерный флуоресцентный анализ, свидетельствуют об эффективности применяемого лечения.
Клинический пример 2.
На терапевтическое лечение поступил пациент В., 34 года.
Жалобы: на быстропроходящую боль от температурных раздражителей в области зубов 2.2, 2.3, 2.4; 3.2, 3.3, 3.4 боль от химических раздражителей в области 3.3 и 2.2 зуба.
Объективно: КПУ (кариес, пломба, удаленный) = 12; ИГР-У (степень гигиены полости рта) = 4 (неудовлетворительная); PMA (для оценки тяжести гингивита, а в последующем и регистрации динамики процесса) - 2; индекс рецессии десны - 3, ИР (индекс реминерализации эмали) - 1, Индекс распространенности и выраженности гиперестезии - 40 (генерализованная форма), ИИГЗ (индекс интенсивности гиперестезии зубов) = 2,3 (гиперестезия II степени). На вестибулярной̆ поверхности зубов 2.3, 2.4; 3.2, 3.4 диагностированы клиновидные дефекты, с гладким и плотным дном, на зубах 2.2., 3.3. - начальный кариес, располагающийся в пределах эмали. Дополнительным методом диагностики стала электроодонтодиагностика (ЭОД) - аппарат ЭОД-10 (оценить электропроводимость зуба).
Произведено окрашивание патологического очага каждого зуба с использованием метиленового синего на зубах, пораженных клиновидным дефектом и Caries marker (Voco, GmbH, Германия) на зубах с диагностированным кариозным процессом. Затем выполнен лазерный флуоресцентный анализ патологических очагов с использованием аппарата - KaVo «DIAGNOdent Pen, видимые границы дефектов обведены грифелем.
С помощью интраорального 3D-сканирования зубных рядов верхней и нижней челюсти пациента, с точностью 15 микрон соответствия биологическому объекту, получены трехмерные модели челюстей, на которых, детально воспроизведены анатомические особенности больного, структура его зубов, десен, альвеолярного отростка, визуализированы границы патологических очагов.
Для контроля эффективности лечения выполнена электроодонтодиагностика (ЭОД) поврежденных зубов, лазерный флуоресцентный анализ зубов: 2.3. - ЭОД = 6 мкА; 2.4 ЭОД = 6 мкА; 3.2.- ЭОД 7 мкА; 3.4.- ЭОД = 7 мкА, 2.2. - ЭОД = 6 мкА, 3.3. - ЭОД = 6 мкА.
Далее детализированные виртуальные модели зубных рядов, полученные c использованием интраорального 3D-сканирования загрузили в программное обеспечение для компьютерного моделирования Autodesk Meshmixer и выполнили гибридное параметрическое моделирование каждого патологического очага.
В качестве лечебного средства для воздействия на очаги некариозного генеза, выбран 10% раствор глюконата кальция, способный повысить содержание минералов и укрепить эмаль. Действующее вещество - глюконат кальция, в выбранном препарате для лечения зубов с клиновидным дефектом размер частиц составляет от 3 до 4 мкм. 4 мкм=0,004 мм. 70×0,004=0,28 мм, округляя до одного знака после запятой получено значение 0,3 мм. Для патологических очагов зубов 2.3, 2.4; 3.2, 3.4 выполнили моделирование шара диаметром 0,3 мм, который размножили для однослойного заполнения каждого патологического очага некариозного генеза.
Затем был произведен расчет оптимального размера микрополостей устройства для лечения кариозного процесса с использованием препарата «Фторлак», способного предотвращать развитие кариозного процесса, насыщать эмаль минералами (основное действующее вещество натрия фторид от 6 до 7 мкм). 4 мкм=0,007 мм. 70×0,007=0,49 мм, округляя до одного знака после запятой 0,5 мм. Для патологических очагов зубов 2.2., 3.3 выполнили моделирование шара диаметром 0,5 мм, который размножили для однослойного заполнения патологических очагов кариозного генеза.
Затем выполнили булеву операцию по объединению трехмерной модели зубных рядов пациента со смоделированными патологическими очагами и шаров, заполняющих патологические очаги. После этого была произведена SLA 3D-печать макета челюстей пациента с наличием выпуклостей округлой формы в области патологических очагов зубов 2.2, 2.3, 2.4; 3.2, 3.3, 3.4 и изготовление методом вакуумной формовки персонифицированных устройств на верхнюю и нижнюю челюсти из эластомерного термопластичного полиуретана (DURAN® ,Scheu Dental, Германия) имеющего параметры 0,5 × 125 мм, с наличием микрорезервуаров в области зубов 2.2, 2.3, 2.4; 3.2, 3.3, 3.4. Затем осуществлены шлифовка, полировка устройств, последующее орошение антисептиком. После этого микрорезервуары устройства в проекции зубов 2.2., 3.3 были заполнены препаратом «Фторлак», а в проекции зубов 2.3, 2.4; 3.2, 3.4 - 10% раствором глюконата кальция. Пациенту продемонстрированно как вводить препараты в устройство, правила фиксирования его на зубах. Курс лечения составил 6 дней.
На контрольном осмотре пациент жалоб не предъявляет.
Объективно: КПУ = 12; ИГР-У = 0; PBI - 0; PMA - 0; индекс рецессии десны - 2, ИР (индекс реминерализации эмали) - 1, Индекс распространенности и выраженности гиперестезии - 3.5 (ограниченная форма гиперестезии), ИИГЗ = 0 (отсутствие гиперестезии). Зондирование безболезненно. Зуб 2.2 - ЭОД = 4 мкА; зуб 2.3. - ЭОД = 3 мкА; зуб 2.4 - ЭОД = 2 мкА; зуб 3.2.- ЭОД = 4 мкА, зуб 3.3. - ЭОД = 3 мкА; зуб 3.4.- ЭОД = 3 мкА.
Клиническое улучшение индексов реминерализации, выраженности гиперестезии, результаты объективных методов диагностики такие как электроодонтодиагностика, лазерный флуоресцентный анализ, свидетельствуют об эффективности применения группы изобретений.
Преимущества персонифицированного устройства.
Данное устройство соответствует современным требованиям международных трендов в медицине - малоинвазивности, при высоком органосохраняющем результате. Реализуется персонифицированный подход к выбору патогенетического лечения в каждой конкретной клинической ситуации. Возможность лечения и профилактики одновременно нескольких нозологических форм патологии твердых тканей зубов с применением персонифицированного устройства с доставкой и депонированием разных лекарственных форм. Использование устройства минимизирует травму слизистой оболочки полости рта, десны и круговой связки зуба при максимальном лечебном результате. Применение устройства повышает эффективность лечения, помогает достичь желаемого результата в более короткий срок. Использование устройства снижает расход лекарственного препарата. Разработанное персонифицированное устройство не вызывает у пациента дискомфорта при использовании, жевании и речи, не меняет эстетических параметров лица. Прецизионность устройства к тканям зуба достигается с помощью использования аддитивных технологий и 3D-печати.
Данное изобретение позволяет в зависимости от заболевания, стадии повреждения твердых тканей зуба производить индивидуальные лечебные или профилактические программы, размещать лекарственные вещества, различных форм (мази, лаки, гели, порошки) доставляя и депонируя их непосредственно в области повреждения твердых тканей зуба. Данное изобретение позволяет изготавливать персонифицированное устройство толщиной 0,5 мм, при необходимости лечения верхнего и нижнего зубного ряда, что снимает нагрузку с височно-нижнечелюстного сустава, дает возможность носить его в периоды приема пищи, сна, предотвращая бруксизм (скрежетание зубами). Данное устройство можно изготавливать толщиной 0.75 мм, в том случае если устройство применяется на одной из челюстей, при этом сохраняются его прочностные характеристики, устройство выдерживает жевательные нагрузки, не перегружая височно-нижнечелюстной сустав. Персонифицированное устройство предотвращает прямой контакт лекарственного вещества с ротовой жидкостью, его вымывание, не создавая конфликт pH среды. Устройство легко поддается качественной антисептической обработке и гигиеническому уходу.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ лечения зубочелюстных аномалий | 2023 |
|
RU2815154C1 |
| Способ лечения гиперестезии зубов у пациентов на фоне соматических заболеваний | 2017 |
|
RU2638293C1 |
| СПОСОБ ЛЕЧЕНИЯ ЭРОЗИИ ЗУБОВ | 2013 |
|
RU2541054C1 |
| Способ протезирования пациентов с полным отсутствием зубов и устройство для осуществления способа | 2022 |
|
RU2780935C1 |
| СПОСОБ МЕСТНОГО ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ СЛИЗИСТОЙ ОБОЛОЧКИ ПОЛОСТИ РТА, НОСА И ТКАНЕЙ ПАРОДОНТА ПРИ ВОСПАЛЕНИИ | 2005 |
|
RU2302247C2 |
| Способ моделирования гиперестезии твердых тканей зубов | 2018 |
|
RU2675358C1 |
| СПОСОБ ЛЕЧЕНИЯ КЛИНОВИДНЫХ ДЕФЕКТОВ ЗУБОВ | 2013 |
|
RU2562575C2 |
| СПОСОБ ЛЕЧЕНИЯ БИОГЕЛЕМ ЛАМИФАРЭН ХРОНИЧЕСКИХ ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЙ ПАРОДОНТА У ЛИЦ МОЛОДОГО ВОЗРАСТА | 2013 |
|
RU2539191C1 |
| Способ резекции верхушек корней зубов | 2022 |
|
RU2807941C1 |
| Способ оценки окклюзионных взаимоотношений зубных рядов | 2021 |
|
RU2784783C1 |
Группа изобретений относится к медицине, а именно к устройству для доставки лекарственного вещества в патологические очаги твердых тканей зубов и способу его изготовления. Устройство выполнено в виде съемной каппы из полиуретана, внутренняя поверхность которой соответствует внешней поверхности зубов пациента и имеет в проекции каждого патологического очага области из микрорезервуаров диаметром 0,1-0,5 мм. Способ включает компьютерное моделирование макета челюсти пациента с учетом параметров резервуара для лекарственного препарата, SLA 3D-печать макета и вакуумное термоформование. Патологические очаги определяют с использованием лазерного флуоресцентного анализа, их границы выделяют грифелем, после чего выполняют 3D-сканирование зубных рядов пациента. Моделирование патологического очага проводят с учетом выделенных границ, моделируют шары диаметром 0,1-0,5 мм, затем заполняют шарами области патологических очагов и объединеняют модель патологических очагов и шары. Достигается повышение эффективности лечения за счет высокоточного дозирования лекарственного препарата и его длительной аппликации только в области патологического очага твердых тканей зубов, а также возможности одновременного применения устройства на обеих челюстях постоянно на весь период лечения. 2 н. и 1 з.п. ф-лы, 2 ил.
1. Устройство для доставки лекарственного вещества в патологические очаги твердых тканей зубов, выполненное в виде съемной каппы из эластомерного термопластичного полиуретана, внутренняя поверхность которой соответствует внешней поверхности зубов пациента и имеет в проекции каждого патологического очага области, состоящие из микрорезервуаров диаметром 0,1-0,5 мм.
2. Устройство по п. 1, отличающееся тем, что устройство выполнено из эластомерного термопластичного полиуретана толщиной 0,5-0,75 мм.
3. Способ изготовления устройства для доставки лекарственного вещества в патологические очаги твердых тканей зубов, включающий компьютерное моделирование трехмерной модели макета челюсти пациента с учетом объемных параметров резервуара для лекарственного препарата, SLA 3D-печать макета челюсти, вакуумное термоформование из эластичного материала, отличающийся тем, что патологические очаги определяют интраорально с использованием лазерного флуоресцентного анализа, границы выявленных патологических очагов выделяют грифелем, выполняют интраоральное 3D-сканирование зубных рядов пациента, выполняют компьютерное моделирование патологического очага с учетом выделенных границ, моделируют шары диаметром 0,1-0,5 мм, однослойно заполняют шарами области патологических очагов, выполняют булеву операцию по объединению модели патологических очагов и шаров их заполняющих.
| US 6607382 B1, 19.08.2003 | |||
| ДЕНТАЛЬНАЯ НАКЛАДКА | 2017 |
|
RU2668690C2 |
| WO 2019068032 A1, 04.04.2019 | |||
| DE 69003135 D1, 14.10.1993 | |||
| US 8505541 B2, 13.08.2013 | |||
| US 7118376 B2, 10.10.2006. | |||
Авторы
Даты
2021-12-13—Публикация
2021-03-22—Подача