Изобретение относится к области медицины, производным пиррола, а именно новому биологически активному 2-амино-1-бензамидо-5-(3,3-диметил-2-оксобутилиден)-4-оксо-4,5-дигидро-1Н-пиррол-3-карбоксамиду (2-АБПК) I формулы:
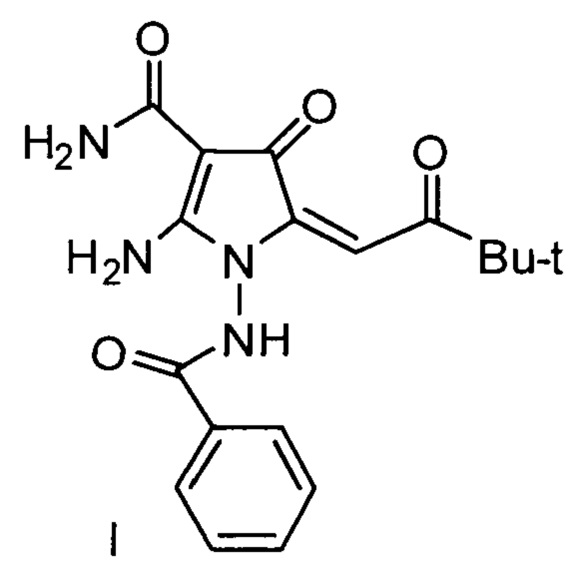
который может найти применение в медицине в качестве лекарственного противоопухолевого препарата.
Ближайшим структурным аналогом к заявленному соединению являются соединения общей формулы II, проявляющие противоопухолевую активность этиловые эфиры 2-амино-1-бензоиламино-4-оксо-5-(2-оксо-2-арил-этилиден)-4,5-дигидро-1Н-пирролидин-3-карбоновых кислот [Патент №2607920 Российская Федерация, МПК C07D 417/00, А61К 31/195. Этиловые эфиры 2-амино-1-бензоиламино-4-оксо-5-(2-оксо-2-арил-этилиден)-4,5-дигидро-1Н-пирролидин-3-карбоновых кислот, проявляющие противоопухолевую активность, и способ их получения: №2015120527: заявл. 29.05.2015: опубл. 11.01.2017 / С.С. Зыкова, Н.М. Игидов, М.В. Киселев, С.В. Бойчук, А.Р. Галембикова]:
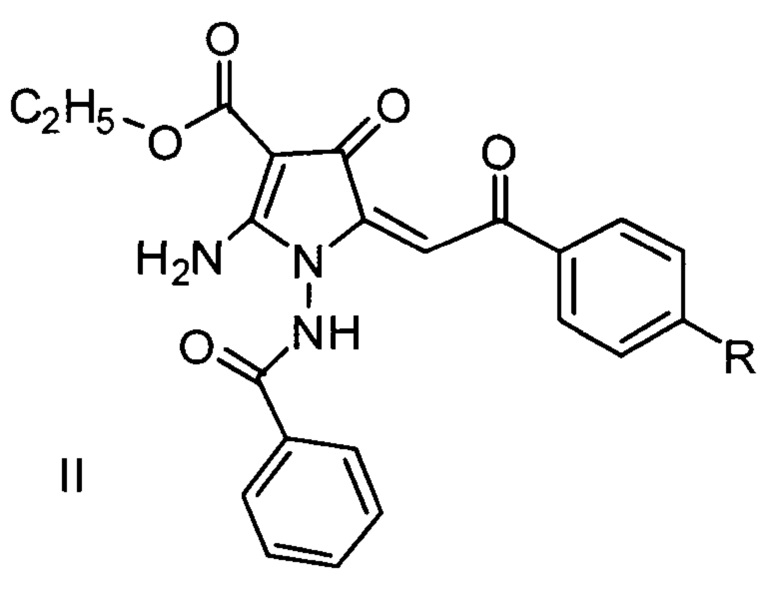
В качестве эталона сравнения нами взят противоопухолевый препарат - паклитаксел [Патент №2059631, МПК C07D 305/14, А61K 31/195. Производные таксола и фармацевтическая композиция, обладающая противоопухолевой активностью: №91 5010248: заявл. 29.11.1991: опубл. 10.05.1996 / Валентине Дж. Стелла, Абрахам Е. Мэтью].
Заявляемое соединение 2-АБПК в тесте острой токсичности на мышах при внутрибрюшинном введении в виде суспензии в 2% крахмальной слизи имеет токсичность более 1000 мг/кг [Колла В.Э., Сыропятов Б.Я. Дозы лекарственных средств и химических соединений для лабораторных животных, М.: Медицина. - 1998. - 263 с.].
Целью предлагаемого изобретения является синтез нового, ранее не описанного 2-амино-1-бензамидо-5-(3,3-диметил-2-оксобутилиден)-4-оксо-4,5-дигидро-1Н-пиррол-3-карбоксамида (2-АБПК) (I) проявляющего цитотоксическую активность в отношении сарком мягких тканей и гастроинтестинальных стромальных опухолей (ГИСО).
Поставленная цель достигается получением 2-амино-1-бензамидо-5-(3,3-диметил-2-оксобутилиден)-4-оксо-4,5-дигидро-1Н-пиррол-3-карбоксамида (I) взаимодействием N-(5-(трет-бутил)-2-оксофуран-3(2Н)-илиден)бензогидразида (II) с цианоацетамидом в присутствии триэтиламина в среде толуола по схеме:
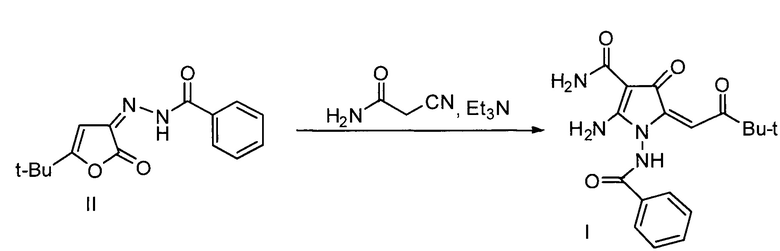
Методика получения 2-амино-1-бензамидо-5-(3,3-диметил-2-оксобутилиден)-4-оксо-4,5-дигидро-1Н-пиррол-3-карбоксамида (I). Смесь 1.36 г (0.005 моль) N-(5-(трет-бутил)-2-оксофуран-3(2Н)-илиден)бензогидразида (II), 0.42 г (0.005 моль) цианоацетамида и 0.5 г (0.005 моль) триэтиламина кипятили в 60 мл бензола в течение 25 минут. Выпавший при охлаждении осадок отфильтровывали и перекристаллизовывали из этанола. Получали 0.99 г (выход 56%) кристаллического вещества (I) с Тпл 230-231°С. C18H20N4O4. ИК-спектр, v/см-1, вазелиновое масло: 3408 (NH), 3318 (NH), 3204 (NH), 1679 (С=O), 1648 (С=O), 1591 (С=С). Спектр ЯМР 1Н (ДМСО-d6), δ, м.д.: 1.02 с (9Н, С(СН3)3), 6.42 с (1Н, СН), 7.01 уш. с (1H, NH), 7.34 уш. с (1Н, NH), 7.65 м (5Н, аром.), 8.70 уш. с (1Н, NH), 9.15 с (1H, NH), 10.86 с (1Н, NH).
Спектр ЯМР 13С, δ, м.д., ДМСО-d6: 25.98, 87.47, 101.80, 128.02, 128.05, 131.16, 132.08, 141.20, 164.90, 165.52, 167.01, 179.99, 204.57.
Масс-спектр, m/z (Iотн., %): 356 (74.7) [М]+., 300 (19.2) [М-2СО)]+, 299 (38.9) [М- t-BuCO]+, 282 (23.7) [М-2СО-Н2O]+, 271 (12.0) [M-t-BuCO]+, 105 (100.0) [PhCO]+, 77 (20.9) [Ph]+, 271 (14.3) [t-Bu]+.
Заявляемое соединение представляет собой светло-желтое кристаллическое вещество, растворимое в ДМСО, ДМФА, уксусной кислоте, при нагревании - в этиловом спирте, устойчивое при хранении.
Изобретение подтверждается следующими графическими материалами, на которых представлено:
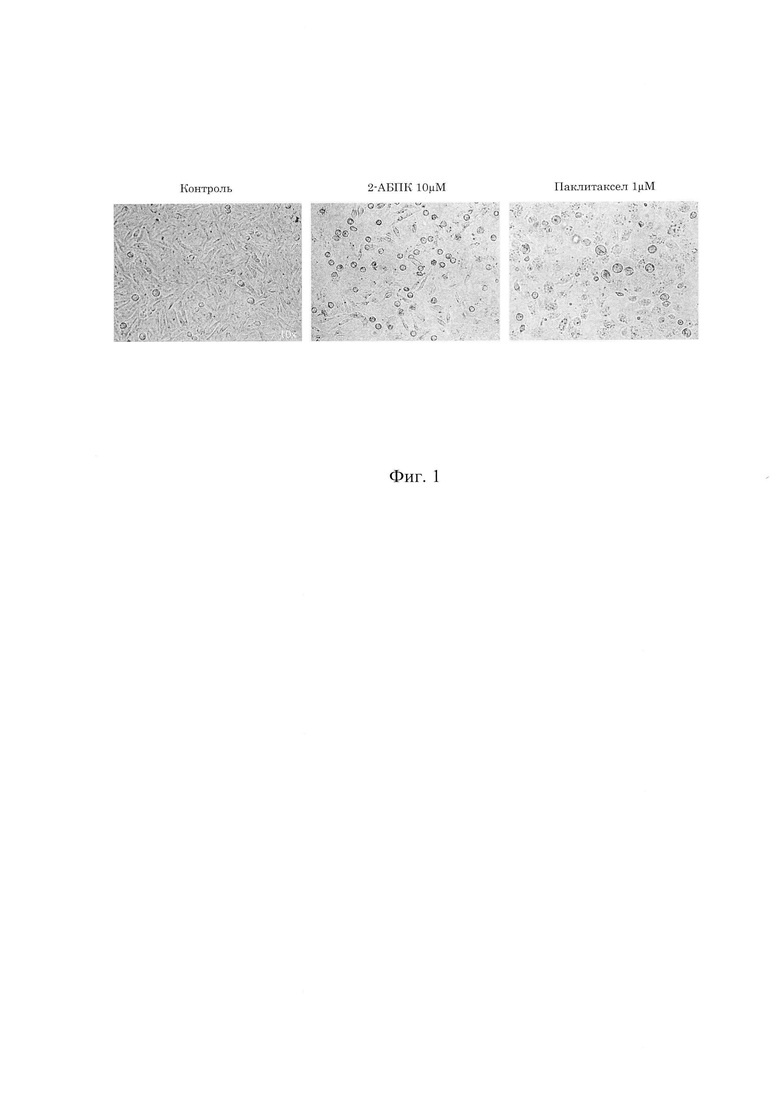
На фиг. 1 - микрофотографии клеток ГИСО (GIST T1-R), проинкубированных с 2-АБПК (10 μМ) и паклитакселом (1 μМ) в течение 24 часов.
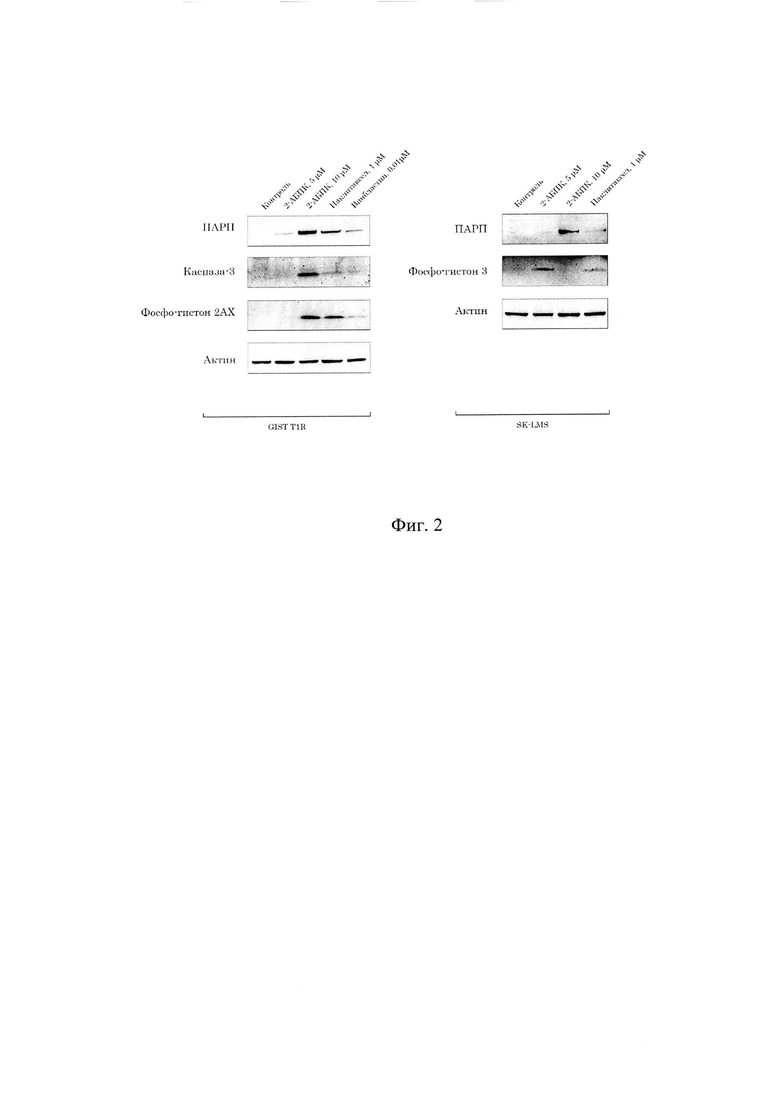
На фиг. 2 - расщепленные формы каспазы-3 и ПАРП, фосфорилированные формы гистонов 2АХ и 3 в клеточных линиях GIST Т1-IM-R (левая панель) и SK-LMS-1 (правая панель), инкубированных в течение 48 часов с 2-АБПК (5 и 10 μМ), паклитакселом (1 μМ) и винбластином (0,01 μМ). В качестве контроля загрузки использовался β-актин.
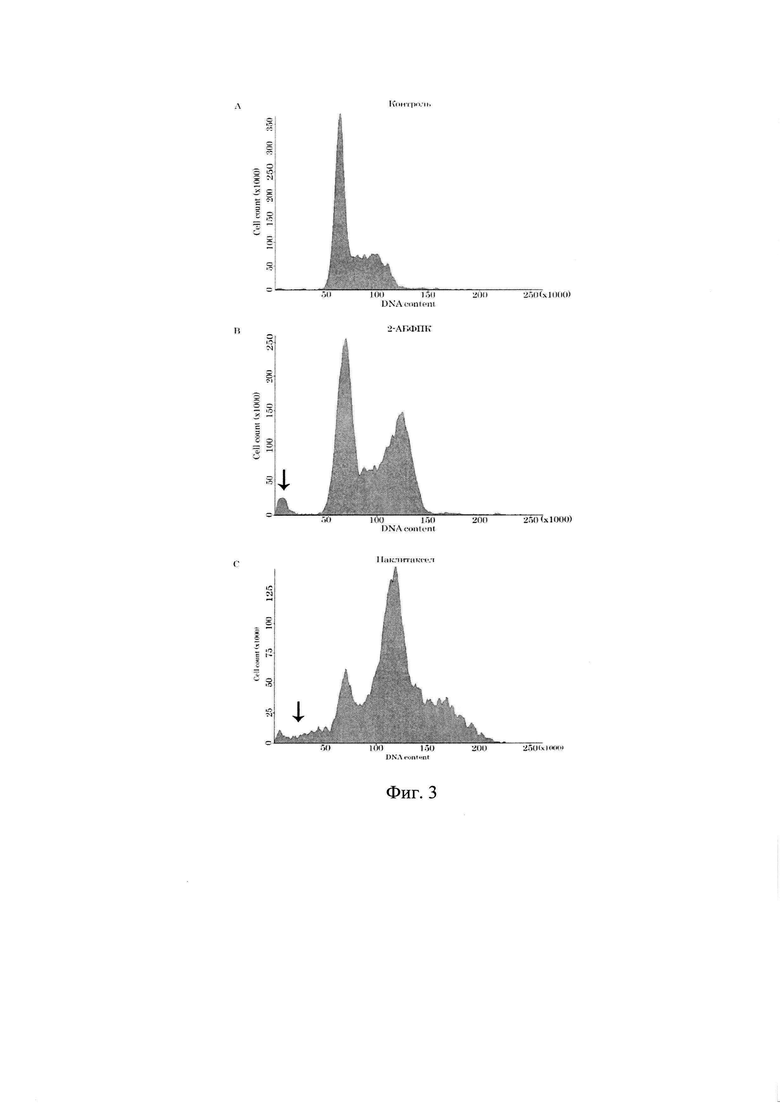
На фиг. 3 - гистограммы проточной цитометрии клеточного цикла линии GIST T1-IM-R, инкубированных с 2-АБПК (10 μМ) и паклитакселом (1 μМ) в течение 48 часов.
По результатам микроскопии клеточных линий сарком мягких тканей, в том числе лейомиосаркомы, рабдомиосаркомы, фибросаркомы (SK-LMS-1, RD, НТ1080, соответственно), и ГИСО (GIST T1-R) было выявлено следующее морфологическое изменение - переход формы клеток на округлую. Это может свидетельствовать о задержке клеток в фазе митоза. Соответствующие изменения были обнаружены при инкубации клеток с паклитакселом (препарат сравнения), который инициирует гибель клеток по механизму апоптоза (Фиг. 1).
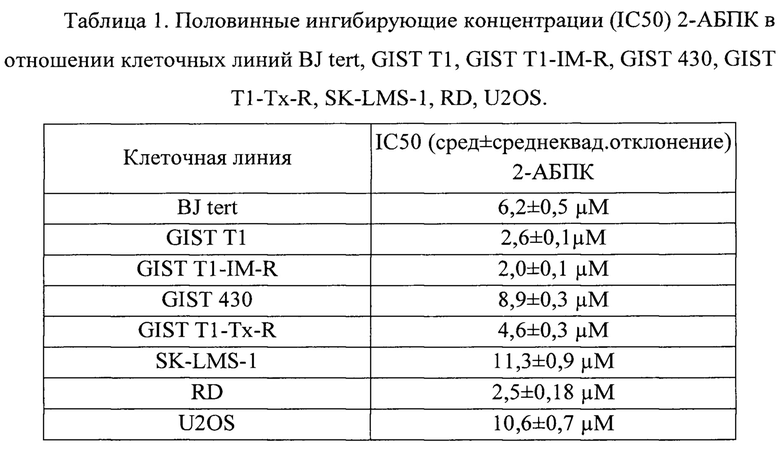
Половинные ингибирующие концентрации (IC50) для 2-АБПК, определенные с помощью MTS-теста в отношении клеточных линий сарком мягких тканей (SK-LMS-1, RD, НТ1080), а также наивных, иматиниб- и паклитаксел-резистентных клеточных линий ГИСО (GIST T1, GIST T1-R, GIST 430 и GIST Tx-R) и нетрансформированных фибробластов человека (ВJ tert) представлены в табл.1. Большая цитотоксическая активность исследуемого соединения в отношении ряда опухолевых клеточных линий, в том числе паклитаксел-резистентных ГИСО, по сравнению с нетрансформированными фибробластами человека свидетельствует о широком терапевтическом окне 2-АБПК, что делает его потенциальным кандидатом для терапии опухолей с приобретенной резистентностью к паклитакселу.
Гибель клеток по механизму апоптоза была подтверждена методом иммуноблоттинга, о чем свидетельствовали повышенные уровни расщепленных форм каспазы-3 и поли-АДФ-рибоза-полимеразы (ПАРП) в клеточных линиях GIST T1-IM-R и SK-LMS-1, обработанных 2-АБПК, паклитакселом и винбластином (положительный контроль). Важно отметить, что выраженность апоптоза, вызванного 2-АБПК, была существенно выше по сравнению с паклитакселом и винбластином. Апоптоз клеток, инкубированных с 2-АБПК, может быть вызван либо индукцией двухцепочечных разрывов ДНК, что доказывает повышенный уровень фосфорилированной формы гистона 2АХ (Фиг. 2, левая панель), либо явлением «митотической катастрофы», маркером которой является повышение уровня фосфорилированной формы гистона 3. (Фиг. 2, правая панель).
С помощью проточной цитометрии (Flow Cytometer BD FACSCanto II) был произведен анализ клеточного цикла клеток GIST T1-IM-R. Таким образом, в образцах, инкубированных 48 часов с 2-АБПК и паклитакселом (положительный контроль) было обнаружено повышенное количество гиподиплоидных клеток (subG1), что свидетельствуют о проапоптотической активности 2-АБПК.
Репрезентативные гистограммы проточной цитометрии (Фиг. 3) иллюстрируют распределение клеточного цикла GIST T1-IM-R, инкубированных с 2-АБПК (10 μМ) и паклитакселом (1 μМ) в течение 48 часов. Эксперимент был выполнен трехкратно, в каждом случае было подсчитано не менее 150000 клеток. Об апоптозе клеток, инкубированных в присутствии 2-АБПК и паклитакселом, свидетельствует пик subG1 (отмечен стрелкой). Результаты количественной оценки приведены в таблице 2.

Таким образом, результаты проведенных исследований указывают на то, что 2-АБПК проявляет цитотоксическую и проапоптотическую активность в отношении сарком мягких тканей и гастроинтестинальных стромальных опухолей (ГИСО).
Изобретение относится к применению 2-амино-1-бензамидо-5-(3,3-диметил-2-оксобутилиден)-4-оксо-4,5-дигидро-1Н-пиррол-3-карбоксамида I указанной ниже формулы для получения лекарственного противоопухолевого препарата. Соединение проявляет цитотоксическую активность в отношении сарком мягких тканей и гастроинтестинальных стромальных опухолей. 3 ил., 2 табл.

Применение 2-амино-1-бензамидо-5-(3,3-диметил-2-оксобутилиден)-4-оксо-4,5-дигидро-1Н-пиррол-3-карбоксамида I формулы

для получения лекарственного противоопухолевого препарата.
| I | |||
| A | |||
| KIZIMOVA ET AL., Synthesis of New 2-Aminopyrrole Derivatives by Reaction of Furan-2,3-diones 3-Acylhydrazones with CH-Nucleophiles, RUSSIAN JOURNAL OF GENERAL CHEMISTRY, 2020, Vol | |||
| Пожарный двухцилиндровый насос | 0 |
|
SU90A1 |
| Затвор для дверей холодильных камер | 1920 |
|
SU182A1 |
| S | |||
| S | |||
| ZYKOVA ET AL., Synthesis and cytotoxic activity of ethyl 2-amino-1-benzamido-4-oxo-5-(2-oxo-2-arylethylidene)- | |||
Авторы
Даты
2022-02-01—Публикация
2020-10-12—Подача