Предлагаемое изобретение относится к области новых средств, конкретно, к соединениям N-алкил-N-{[3-алкил-3,8-диазабицикло[3.2.1]окта-1(7),5-диен-8-ил]метил}аминам, обладающие цитотоксической активностью в отношении клеточной линии HEK 293 общей формулы (1):

Известны [К.С. Ковалева, О.И. Яровая, А.В. Шернюков, В.В. Зарубаев, А.А. Штро, Я.Р. Оршанская, Н.Ф. Салахутдинов. Синтез новых гетероциклических производных дегидроабиетиламина и их биологическая активность // ХГС, 2017, 53(3), 364-370] производные дегидроабиетиламина общей формулы (2), обладающие цитотоксической активностью в отношении линии клеток почки эмбриона человека HEK 293.
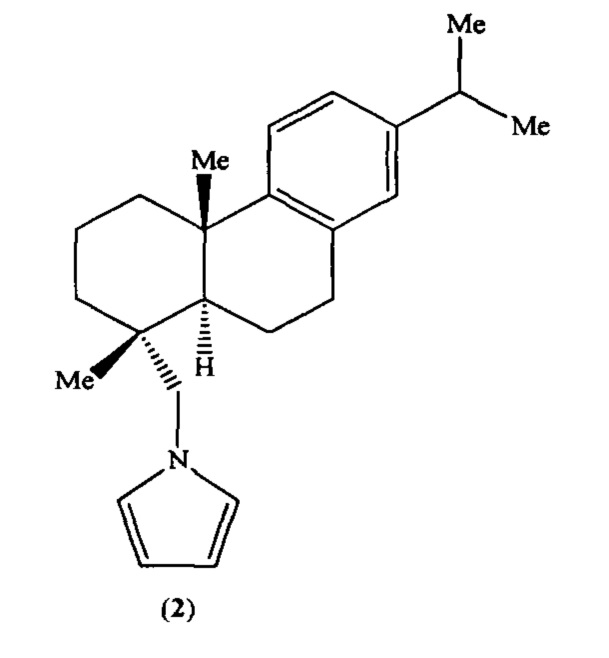
Синтез соединений общей формулы (2) базируется на использовании труднодоступных исходных реагентов.
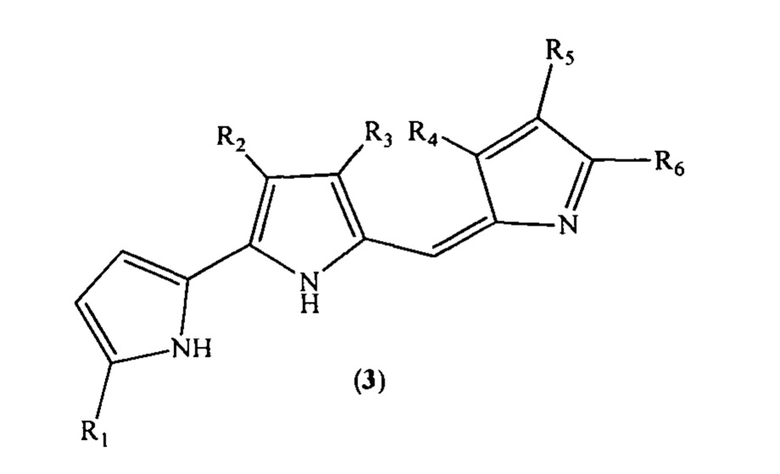
Известно, что пирролиденметильные производные (3), обладающие антибактериальной, антибиотической, антимикробной и/или цитотоксической активностью [J. Antibiotics 24, 636 (1971); Mar. Biol. 34, 223 (1976); Can. J. Microbiol. 22, 658 (1976); Can. J. Chem. 56, 1155 (1978); Tetrahedron Letters 24, 2797 (1983) J. Antibiotics 38, 128 (1985); Gen. Microbiol 132, 1899 (1986); J. Antibiotics 28, 194 (1975); Nature 213, 903 (1967); Tetrahedron Letters 24, 2701 (1983); J. Antibiotics 39, 1155 (1986); J. 6 1280 429-A и J 0 2250 828-A], проявляют иммуносупрессивное действие [Патент RU 2145957, 2000. Д. Дория, А.Ь. Изетта, М. Тиболла, М. Форсаньеро, М. Феррари, Д. Трицио].
Обнаружено, что производные пиррола - этиловый эфир 2-амино-1-бензоиламино-5-(2-(4-хлорфенил или 3,4-диметоксифенил)-2-оксоэтилиден)-4-оксо-4,5-дигидро-1Н-пиррол-3 карбоновой кислоты (4) проявляют цитотоксическую активность по отношению к некоторым клеточным линиям опухолей соединительной ткани, а именно гастроинтестинальных стромальных (ГИСТ) опухолей, остеосаркомы U2-OS и лейомиосаркомы SK-LMS-1 [Зыкова С.С., Галембикова А.Р., Рамазанов Б.Р., Одегова Т.Ф., Игидов Н.М., Киселев М.А., Бойчук С.В. Цитотоксическая активность этиловых эфиров 2-амино-1-бензоиламино-4-оксо-5-(2-оксо-2арилэтилиден)-4,5-дигидро-1Н-пиррол-3-карбоновых кислот // Хим. фарм. журн., 2015, №12, 19-23].
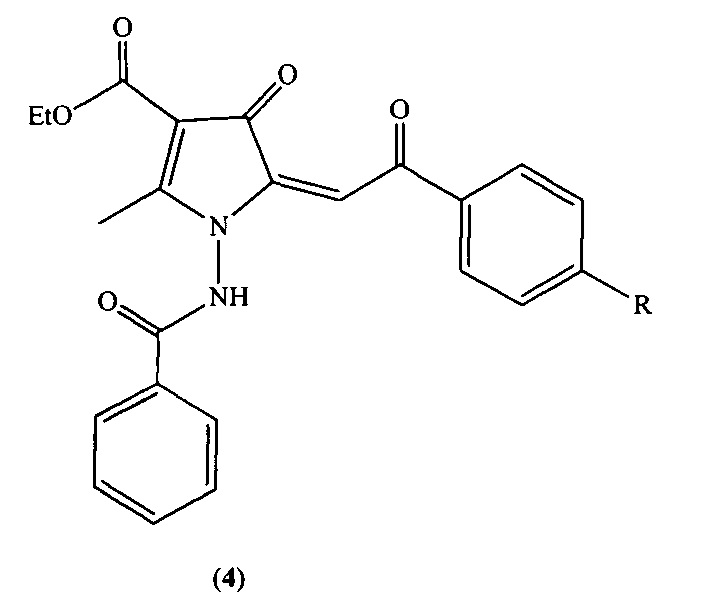
Показан выраженный дозозависимый цитотоксический эффект данных соединений в дозах 10 и 20 мкМ, в значительной степени превышающий эффект препарата сравнения (паклитаксела), а также известного противоопухолевого препарата этопозида, являющегося ингибитором топоизомеразы II типа. Эффект был обнаружен на опухолевых клеточных линиях гастроинтестинальных стромальных опухолей ГИСО-882 и Т-1, остеосаркомы U2-OS, рака легкого H1299, рака шейки матки HeLa S3. Синтез соединений многостадиен.
Новые производные пиррола (5), имеющие уреидогруппу, аминокарбонильную группу и/или бициклическую гетероциклическую группу, проявляют ингибирующую активность относительно продукции IL-6, что позволяет использовать их при лечении ряда заболеваний, включая опухолевые [Патент RU 2500669, 2012. Х. Еномото, М. Мюраи, Н. Кавасима, М. Ямамото, К. Кавасима].

Известны производные пиррола формулы (6)
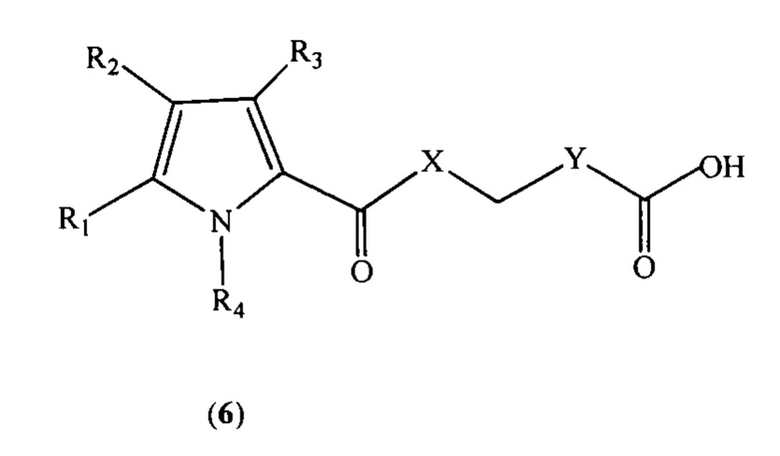
где R1 и R3 - арил(гетарил)-заместители, R2 - амино, амидо, нитро-группы, X=NH, О, S; Y=NH СН2. Соединения (6) обладают способностью ингибировать гистондеацетилазу, что позволяет использовать их при лечении рака [Патент RU 2416600, 2011. Коссио Мора, Эстельер Бадоса, Зубиа Оласкоага, Отайги Анса].
Известны производные пиррола (7) как лекарственные вещества для моделирования активности стероидных ядерных рецепторов [Патент RU 2470916, 2012, Канне Б., Чен Д., Дэримпл Л.Э., Флэт Б.Т., Форсайт Т.П. и др.]

где R1 и R2 = водород, галоген, циан, алкил, R3 = водород, галоген, циан, алкенил; R4 = водород, -C(O)R9 или -S(O)2R9.
Подобные соединения показывают ЕС50 или IC50 обычно менее 10 мкМ, а в некоторых вариантах менее 1 мкМ, 0,5 мкМ, 250 нМ, 100 нМ или 50 нМ. Эти соединения применяются в случае избытка или недостатка лигандов стероидных рецепторов или в случае активности стероидных рецепторов, например, болезнь Аддисона, синдром Кушинга, синдром Конна, синдром Тернера, заместительная гормонотерапия, менопауза, гипогонадизм, соматопауза, андропауза, виропауза, а также при расстройствах, относящихся к раку, включающие гормонозависимые злокачественные опухоли, например, рак молочной железы [патент США №6306832], рак предстательной железы [патент США №5656651], доброкачественная гиперплазия предстательной железы [патент США №5656651], рак яичника, рак эндометрия [патент США №6593322], лейкоз [патент США №6696459] и лимфома [патент США №6667299], болезни или расстройства, связанные с фиброзом [патент США №6716829, патент США №6391867].
Известен препарат сунитиниб, производное пиррола N-[2-(диэтиламино)этил]-5-[(Z)-(5-фтор-1,2-дигидро-2-оксо-3Н-индол-3-илиден)метил]-2,4-диметил-1H-пиррол-3-карбоксамид (8), обладающий ингибирующей активностью различных тирозинкиназ, участвующих в процессах роста опухолей, патологического ангиогенеза и образования метастазов.

Синтез соединения (8) многостадиен.
Наиболее близким структурным прототипом к предлагаемому изобретению является противомикробное средство 2,3-дигидро-1H-имидазо[1,5-а]пиррол [W.J. Burke, G.N. Hammer. 2,3-Dihydro-1H-imidazo[1.5-a]pyrroles. Condensation of Pyrroles and Formaldehyde and Primary Amines // J. Am. Chem. Soc, 1954, 76 (5), P. 1294-1296], полученное реакцией 3-карбэтокси-2,4-диметилпиррола с формальдегидом (37% водный раствор) и циклогексиламином в среде 1,4-диоксана при температуре 95°С в течение 1 ч по схеме:

Применение соединений общей формулы (9) в качестве средства с цитотоксической активностью неизвестно.
Задачей изобретения является расширение арсенала биологически активных веществ, в том числе обладающих цитотоксической активностью.
Результат достигается тем, что предлагаются N-алкил-N-{[3-алкил-3,8-диазабицикло[3.2.1]окта-1(7),5-диен-8-ил]метил}амины, обладающие цитотоксической активностью в отношении клеточной линии HEK293 общей формулы (1). Способ получения соединений формулы (1) основан на циклоконденсации доступных первичных алкиламинов, параформальдегида и пиррола [Э.М. Бикбулатова, В.Р. Ахметова, Ахмадиев Н.С., Р.В. Кулакова, А.Г. Ибрагимов. Катализируемые переходными металлами реакции С,С- и С,N-циклоаминометилирования пиррола и индола // ХГС, 2018, 54 (5), 520 -527].
Реакция проходит по схеме:
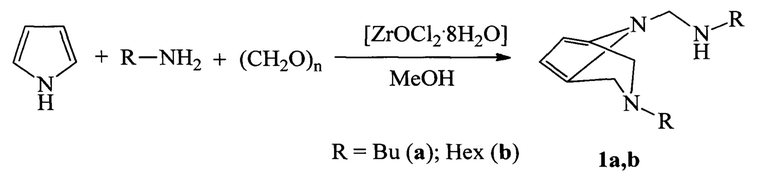
Синтез соединений 1а,b осуществлен следующим образом.
Пример 1. Способ получения N-алкил-N-{[3-алкил-3,8-диазабицикло[3.2.1]окта-1(7),5-диен-8-ил]метил}аминов общей формулы (1) заключается в перемешивании пиррола с первичными алкиламинами общей формулы R-NH2 (где R=Bu, Hex) и параформальдегидом в присутствии катализатора ZrOCl2⋅8Н2O при мольном соотношении пиррол : первичный амин : параформальдегид : ZrOCl2⋅8Н2O = 1:2:3:0.05 в среде метанола при температуре 0°С и атмосферном давлении в течение 6 ч. Затем реакционную смесь пропускают через слой SiO2, упаривают на роторном испарителе, остаток очищают колоночной хроматографией (элюент циклогексан-СНС13-EtOAc, 1:2:5), выделяют N-алкил-N-{[3-алкил-3,8-диазабицикло[3.2.1]окта-1(7),5-диен-8-ил]метил}амины общей формулы (1) с выходами 57% 1a (Rf 0.61), 51% 1b (Rf 0.72).
Спектральные характеристики соединений (1а,b).
N-Бутил-N-{[3-бутил-3,8-диазабицикло[3.2.1]окта-1(7),5-диен-8-ил]метил}амин (1а). Оранжевое масло, Rf 0.61. ИК спектр, ν, см-1: 617, 792, 1141, 1193, 1242, 1593, 3045, 3340. Спектр ЯМР 1Н, δ, м. д. (J, Гц): 0.92 (6Н, т, 2J=7.4, 2СН3); 1.31-1.38 (4Н, м, СН2); 1.42-1.49 (4Н, м, СН2); 2.50 (2Н, т, 2J=7.4, NCH2Pr); 3.48 (2Н, т, 2J=7.4, NHCH2Pr); 3.64 (4Н, уш. с, N(CH2CPyr)2); 4.86 (2Н, с, NCH2NH); 6.00 (2Н, с, Н Руг); 9.15 (1Н, с, NH). Спектр ЯМР 13С, δ, м. д.: 13.7 (СН3); 14.0 (СН3); 20.4 (СН2); 20.7 (СН2); 29.8 (СН2); 49.9 (NHCH2Et); 50.9 (N(CH2CPyr)2); 52.6 (NCH2Et); 74.6 (NCH2NH); 107.1 и 127.6 (CPyr). Масс-спектр, m/z (Iотн, %): 249 [M]+ (20), 163 [M-CH3(CH2)3NHCH2] (70), 121 [M-C8H18N] (100), 80 [M-C10H21N2] (50), 42 [M-C13H23N2] (20). Найдено, %: С 72.18; H 10.95; N 16.81. C15H27N3. Вычислено, %: С 72.24; Н 10.91; N 16.85.
N-Гексил-N-{[3-гексил-3,8-диазабицикло[3.2.1]окта-1(7),5-диен-8-ил]метил}амин (1b). Оранжевое масло, Rf 0.72. ИК спектр, v, см-1: 628, 729, 1078, 1150, 1200, 1215, 1270, 1660, 3101, 3379. Спектр ЯМР 1Н, δ, м. д. (J, Гц): 0.92 (6Н, т, 2J=7.4, 2СН3); 1.21-1.25 (2Н, м), 1.32-1.37 (4Н, м) и 1.39-1.50 (2Н, м, 8СН2); 2.42 (4Н, т, 2J=7.4, 2NCH2); 3.58 (4Н, уш. с, N(СН2СPyr)2); 4.44 (2Н, с, NCH2NH); 5.93 (2Н, с, Н Pyr); 7.29 (1Н, с, NH). Спектр ЯМР 13С, δ, м. д.: 13.9 (2СН3); 22.3 (2СН2); 27.0 (2СН2); 27.2 (2СН2); 31.5 (2СН2); 49.9 (NHCH2); 50.9 (N(CH2CPyr)2); 52.6 (NCH2); 74.6 (NCH2NH); 107.8 и 128.6 (СPyr). Найдено, m/z: 305.128 [M]+. C19H35N3. Вычислено, m/z: 305.282 [М]+. Найдено, %: С 74.64; Н 11.59; N 13.72. C19H35N3. Вычислено, %: С 74.70; Н 11.55; N 13.75.
Скрининг цитотоксичности соединений 1а,b проведен СО-ADD (The Community Organization for Antimicrobial Drug Discovery) при финансовой поддержке Wellcome Trust (Великобритания) и Университетом Квинсленда (Австралия).
Синтезированные соединения 1а,b протестированы на токсичность в отношении клеток HEK 293.
Анализ цитотоксичности
Методика
Клетки HEK 293 подсчитывали вручную в гемоцитометре Нейбауэра и затем высевали в 384-луночные планшеты, содержащие соединения, чтобы получить плотность 5000 клеток / лунка в конечном объеме 50 мкл. В качестве питательной среды использовали DMEM с добавлением 10% FBS, и клетки инкубировали вместе с соединениями в течение 20 часов при 37°С в 5% СO2.
Анализ
Цитотоксичность (или жизнеспособность клеток) измеряли по флуоресценции, например: 560/10 нм, em: 590/10 нм (F560 / 590), после добавления 5 мкл 25 мкг / мл ресазурина (конечная концентрация 2,3 мкг / мл) и после инкубации в течение еще 3 ч при 37°С в 5% СO2. Интенсивность флуоресценции измеряли с помощью планшет-ридера Tecan Ml000 Pro, используя автоматический расчет усиления.
СС50 (концентрация при 50% цитотоксичности) рассчитывали путем подбора кривой зависимости значений ингибирования от log (концентрации) с использованием сигмоидальной функции доза-ответ с переменными подгоночными значениями для дна, верха и наклона. Кроме того, максимальный процент цитотоксичности указан как DMax, что указывает на любые соединения с частичной цитотоксичностью.
Подгонка кривой была реализована с использованием компонента доза-ответ Pipeline Pilot, что привело к значениям, подобным инструментам подбора кривой, таким как Prism от GraphPad и XlFit от IDBS. Любое значение с> обозначает образец без активности (низкое значение DMах) или образцы со значениями СС50 выше максимальной протестированной концентрации (более высокое значение DMax).
Цитотоксические образцы были классифицированы по СС50≤32 мкг / мл или СС50≤10 мкМ в обоих повторностях (n=2 на разных планшетах). Кроме того, образцы были помечены как частично цитотоксические, если DMах≥50%, даже при СС50> максимальной протестированной концентрации.

Технический результат - получение биологически активных новых соединений, обладающих цитотоксической активностью. N-Алкил-N-{[3-алкил-3,8-диазабицикло[3.2.1]окта-1(7),5-диен-8-ил]метил}амины общей формулы (1) проявляют цитотоксическую активность в отношении клеточной линии HEK 293.
N-алкил-N-{[3-алкил-3,8-диазабицикио[3.2.1]окта-1 (7),5-диен-8-ил]метил}амины общей формулы (1) вызывают гибель 50% клеток, СС50 (мг/мл) в отношении линии клеток почки эмбриона человека HEK 293 в опытах in-vitro (таблица).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ N-АЛКИЛ-N-{ [3-АЛКИЛ-3,8-ДИАЗАБИЦИКЛО[3.2.1]ОКТА-1(7),5-ДИЕН-8-ИЛ]МЕТИЛ} АМИНОВ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ СРЕДСТВ С АНТИМИКРОБНОЙ АКТИВНОСТЬЮ | 2018 |
|
RU2739761C2 |
| СПОСОБ ПОЛУЧЕНИЯ N-АЛКИЛ-N,N-ДИ(АЛКАДИИНИЛ)АМИНОВ | 2015 |
|
RU2626008C2 |
| СПОСОБ ПОЛУЧЕНИЯ N-АЛКИЛ-О-АЛКИЛКАРБАМАТОВ | 2007 |
|
RU2359958C2 |
| N, N', N'-ТРИЗАМЕЩЕННЫЕ ИЗОСЕЛЕНОМОЧЕВИНЫ | 2010 |
|
RU2434852C1 |
| ПРОИЗВОДНЫЕ БЕНЗОТРИАЗОЛА В КАЧЕСТВЕ МОДУЛЯТОРОВ АКТИВНОСТИ TNF | 2014 |
|
RU2677696C1 |
| ЛЕЧЕНИЕ ГИДРАДЕНИТА ИНГИБИТОРАМИ JAK | 2020 |
|
RU2805595C1 |
| Производные пиридоксина и ацетона с противоопухолевой активностью | 2017 |
|
RU2639879C1 |
| ИНГИБИТОР НЕКОТОРЫХ ПРОТЕИНКИНАЗ | 2016 |
|
RU2732952C2 |
| ФАРМАЦЕВТИЧЕСКИЕ СОЕДИНЕНИЯ | 2019 |
|
RU2821941C2 |
| ЦИТОТОКСИЧЕСКИЕ ЛИНЕЙНЫЕ ГЕТЕРОЦИКЛИЧЕСКИЕ ПРОИЗВОДНЫЕ АНТРАЦЕНДИОНА, СОДЕРЖАЩИЕ В БОКОВОЙ ЦЕПИ ЦИКЛИЧЕСКИЕ ДИАМИНЫ, АКТИВНЫЕ В ОТНОШЕНИИ ОПУХОЛЕВЫХ КЛЕТОК С МНОЖЕСТВЕННОЙ ЛЕКАРСТВЕННОЙ УСТОЙЧИВОСТЬЮ | 2009 |
|
RU2412166C1 |
Изобретение относится к применению N-алкил-N-{[3-алкил-3,8-диазабицикло[3.2.1]окта-1(7),5-диен-8-ил]метил}аминов общей формулы (1) в качестве средства, обладающего цитотоксической активностью в отношении клеточной линии HEK 293. 1 табл., 1 пр.

Применение N-алкил-N-{[3-алкил-3,8-диазабицикло[3.2.1]окта-1(7),5-диен-8-ил]метил}аминов общей формулы (1)
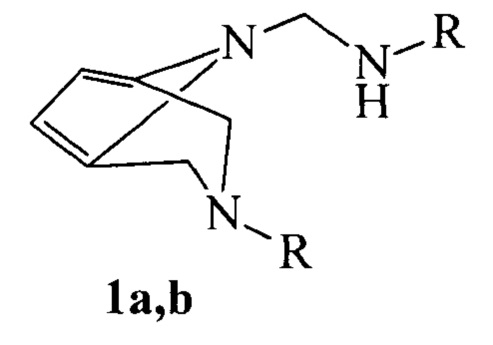 ,
,
где R=Bu (а), Hex (b),
в качестве средства, обладающего цитотоксической активностью в отношении клеточной линии HEK 293.
| V.R | |||
| AKHMETOVA ET AL., Transition metal-catalyzed C,C- and C,N-cycloaminomethylation reactions of pyrrole and indole, CHEMISTRY OF HETEROCYCLIC COMPOUNDS, 2018, 54(5), pp.520-527 | |||
| Э.М | |||
| БИКБУЛАТОВА И ДР., Мультикомпонентный синтез новых пиперазино[c,d]пирроловых и пиримидино[c,d]индоловых соединений, АКТУАЛЬНЫЕ ПРОБЛЕМЫ ОРГАНИЧЕСКОЙ ХИМИИ 2018, |
Авторы
Даты
2020-07-09—Публикация
2019-09-24—Подача