Область техники
Настоящее изобретение относится к области органической химии и фармакологии и касается новых несимметричных производных полифенолов динафталинового ряда, способа их получения и применения.
Предшествующий уровень техники
Полифенолы динафталинового ряда в течение длительного времени являются объектом многочисленных исследований. Наибольшее количество публикаций в этой области посвящено природному полифенолу госсиполу (1) и продуктам его синтетических превращений (апогоссипол (2), госсиполон (3), апогоссиполон (4)). Для данных соединений проводились исследования по противовирусной (Biochem. Pharmacol., 1993, 46, 251-255), противоопухолевой (Mol. Pharmacol., 1990, 37, 840-847), противогрибковой и антиоксидантной (Biochem. Pharmacol., 1989, 38, 2859-2865) активностям.
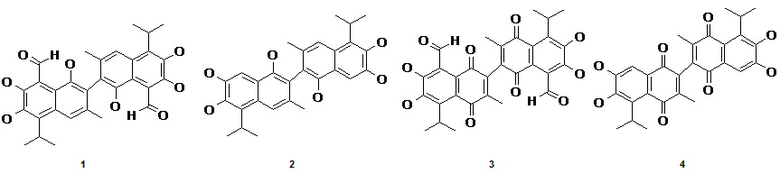
Помимо вышеупомянутых, синтезированы многочисленные производные госсипола (J. Am. Oil Chem. Soc. 2006, 83, 4, 269-301), являющиеся продуктами его синтетической модификации по альдегидным (азометиновые производные (5)), фенольным (алкильные эфиры (6)), продукты окисления (госсиполон (7)), щелочной деструкции нафталинового кольца (госcиндан (8) и др.). Для подавляющего большинства продуктов при этом характерно наличие двух одинаковых (симметричных) нафталиновых или иных фрагментов.
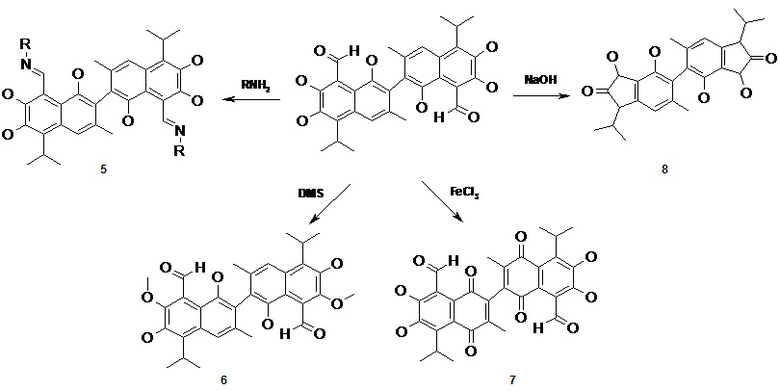
Однако, на сегодняшний день известно сравнительно небольшое количество полифенолов динафталинового ряда, содержащих два структурно различных нафталиновых фрагмента. Основным направлениям исследований несимметричных производных госсипола посвящен обзор К.З. Тилябаева (Химия растительного сырья, 2013, №3, 17-31). Наиболее широко в этой области представлены несимметричные основания Шиффа (9), а также моно-азапроизводные, получаемые по реакции с соответствующими солями диазония (10).
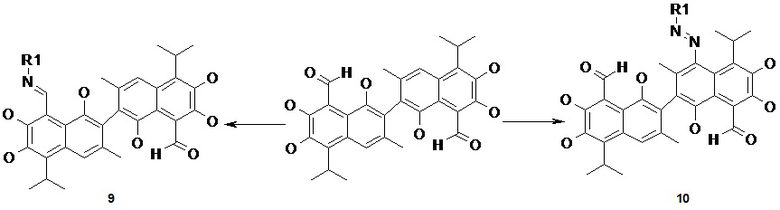
Кроме этого, синтезированы несимметричные производные госсипола путем модификации гидроксильной группы (11, 12) (Chin. Chem. Lett., 1992, vol. 3, 165-166; Yin J. Chemical modification and biological activity exploration of the natural product- gossypol: PhD dissertation in Food technology, Graduate School of Clemson University, USA, 2010), а также галогенпроизводные (13) (J. Org. Chem., 1992, vol. 57, 2316-2320).
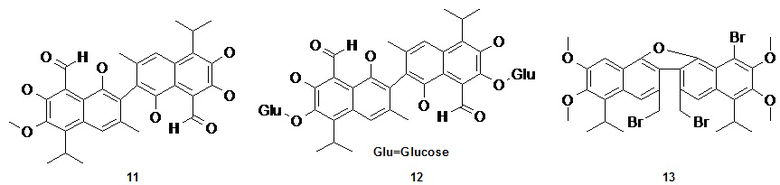
Отдельно упоминается возможность получения несимметричных производных госсипола на основе его таутомерных форм (14, 15) (Curr. Sci., 1973, 42, 821-822; Proceedings of the Alfred Benzon Symposium 26: Copenhagen, 1988, 75-100).
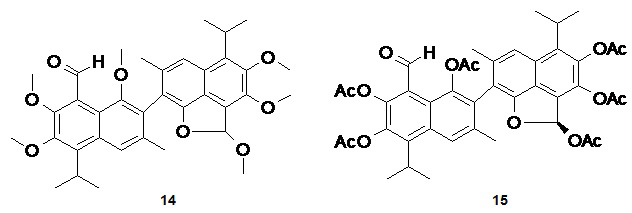
Наиболее близкими к настоящему изобретению являются описанные в работе (Yao. Xue. Xue. Bao., 1987, Aug 22, 8, 597-602) альдегидные производные (16), получаемые путем многостадийного синтеза, включающего формилирование по Гаттерману-Адамсу. В этой же работе упоминается потенциальная возможность получения моноальдегида госсипола (17) по реакции в водном растворе щелочи в присутствии гидросульфита натрия.

Таким образом, сохраняется необходимость в разработке новых несимметричных производных полифенолов динафталинового ряда и нетрудоемких способов их получения.
Сущность изобретения
Задачей настоящего изобретения является разработка новых несимметричных производных динафталиновых полифенолов и способов их получения.
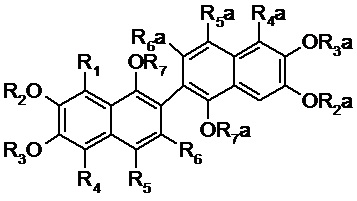
1) Настоящее изобретение относится к новым несимметричным производным динафталиновых полифенолов общей формулы I:
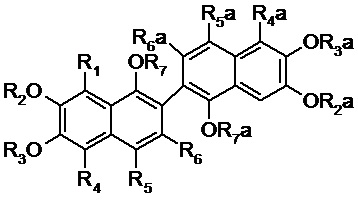
I
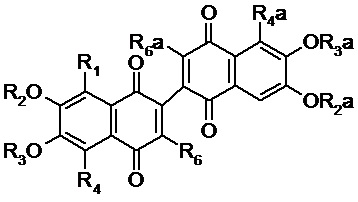
или общей формулы II
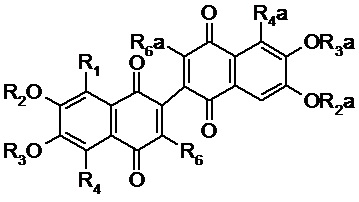
II
их таутомерным формам, фармацевтически приемлемым солям и сольватам, где:
R1 представляет собой: C(O)H, C=N-R8, С=N-NН-R8, С=N-NН-С(О)R8;
где R8 представляет собой: H; линейные и разветвленные С1-С20 алкилы, содержащие заместители в количестве от 0 до 10; линейные и разветвленные С2-С20 алкенилы и С2-С20 алкинилы с количеством двойных и (или) тройных связей от 1 до 9, содержащие заместители в количестве от 0 до 10; незамещенные и замещенные циклические системы с числом атомов в цикле от 3 до 20, содержащие заместители в количестве от 0 до 10, количеством двойных и (или) тройных связей от 0 до 10 и количеством гетероатомов (N, S, O) от 0 до 10; незамещенные и замещенные арилы с заместителями в количестве от 0 до 5, незамещенные и замещенные гетероароматические соединения с числом атомов в цикле от 3 до 12 и количеством гетероатомов (N, S, O) от 1 до 6, содержащие заместители в количестве от 0 до 10; насыщенные, ненасыщенные и (или) ароматические полициклические системы, содержащие от 2 до 5 циклов с числом атомов в цикле от 3 до 8, количеством двойных и (или) тройных связей от 0 до 10 и количеством гетероатомов (N, S, O) от 0 до 10 и заместители в количестве от 0 до 20;
R2, R3, R2a, R3a, R7, R7a независимо представляют собой R8 или C(O)R8;
R5 и R5a независимо представляют собой H или N=N-R9;
где R9 представляет собой: незамещенные и замещенные арилы с заместителями в количестве от 0 до 5, незамещенные и замещенные гетероароматические соединения с числом атомов в цикле от 3 до 12 и количеством гетероатомов (N, S, O) от 1 до 6, содержащие заместители в количестве от 0 до 10; насыщенные, ненасыщенные и (или) ароматические полициклические системы, содержащие от 2 до 5 циклов с числом атомов в цикле от 3 до 8 и количеством гетероатомов (N, S, O) от 0 до 10 и заместители в количестве от 0 до 20;
R4, R4a, R6 и R6a независимо представляют собой H, линейные и разветвленные С1-С10 алкилы;
где заместители представляют собой Н, F, Cl, Br, I, NO2, CN, SO3H, SO3M, SO2Cl, CF3, CCl3, CBr3, CI3, C(O)H, COOH, COOМ, C(O)Cl, C(O)Br, C(O)I, R8, COOR8, C(O)R8, OH, OR8, ОС(О)R8, OC(O)NR8R10, ОSO2R8, NH2, NR8R10, N+(R8R10R11), NR8C(O)R10, NR8SO2R10, NR8C(O)NR10R11, SR8, S(O)R8, SO2R8, CH=NR8;
где R10, R11 независимо представляют собой: H; линейные и разветвленные С1-С20 алкилы, содержащие заместители в количестве от 0 до 10; линейные и разветвленные С2-С20 алкенилы и С2-С20 алкинилы с количеством двойных и (или) тройных связей от 1 до 9, содержащие заместители в количестве от 0 до 10; незамещенные и замещенные циклические системы с числом атомов в цикле от 3 до 20, содержащие заместители в количестве от 0 до 10, количеством двойных и (или) тройных связей от 0 до 10 и количеством гетероатомов (N, S, O) от 0 до 10; незамещенные и замещенные арилы с заместителями в количестве от 0 до 5, незамещенные и замещенные гетероароматические соединения с числом атомов в цикле от 3 до 12 и количеством гетероатомов (N, S, O) от 1 до 6, содержащие заместители в количестве от 0 до 10; насыщенные, ненасыщенные и (или) ароматические полициклические системы, содержащие от 2 до 5 циклов с числом атомов в цикле от 3 до 8, количеством двойных и (или) тройных связей от 0 до 10 и количеством гетероатомов (N, S, O) от 0 до 10 и заместители в количестве от 0 до 20;
где М представляет собой Li, Na, K, Cs, Rb.
2) В другом аспекте настоящее изобретение относится к соединениям, структуры которых приведены в Таблице 1.
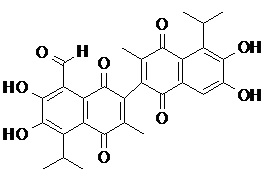

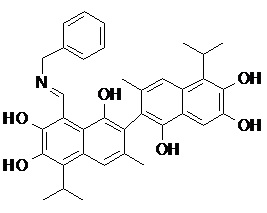
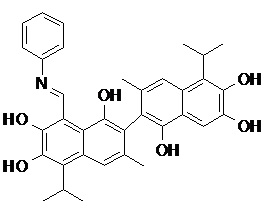

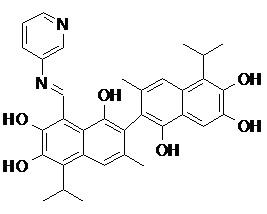
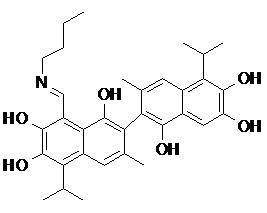

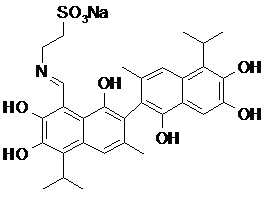
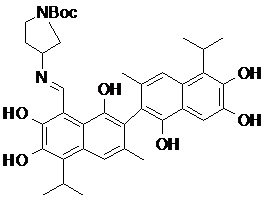
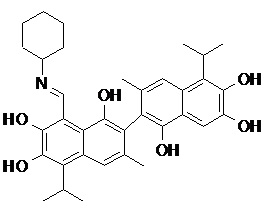

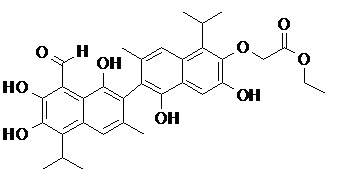
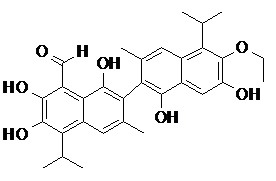
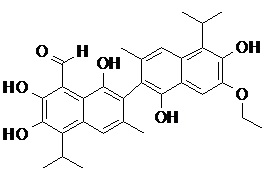
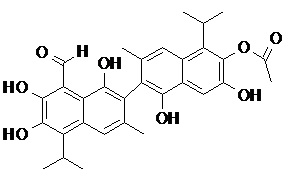

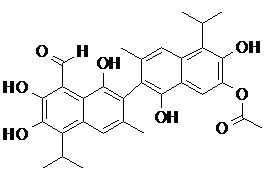
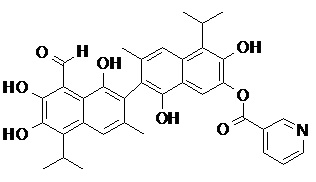
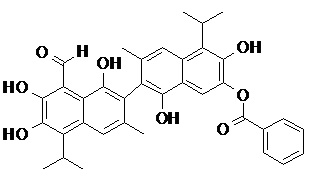
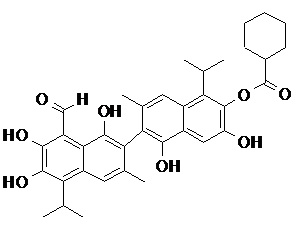
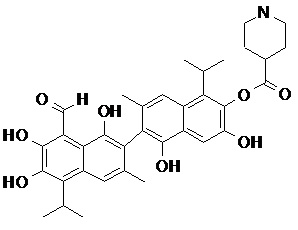
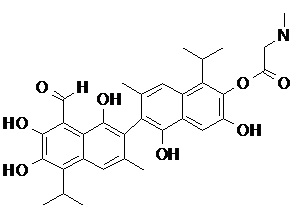
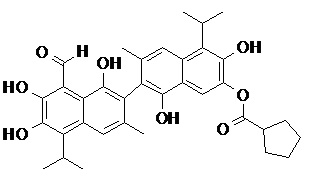
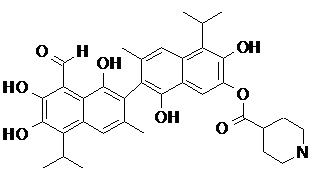
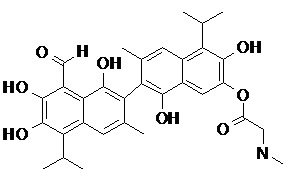
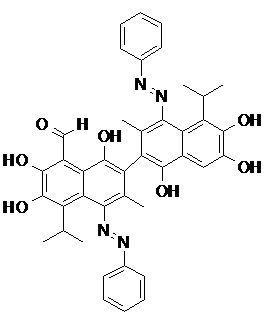
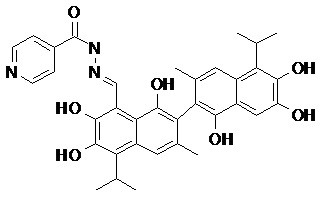
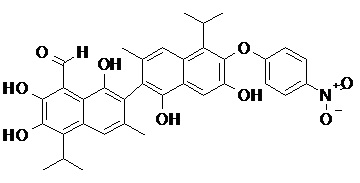
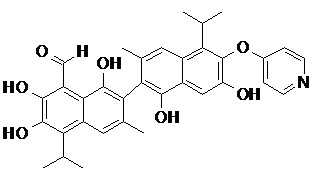
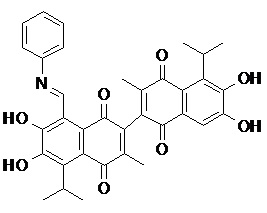
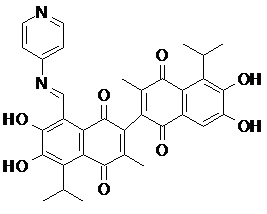
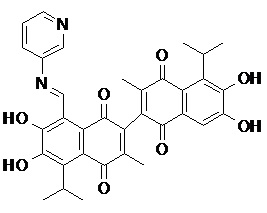
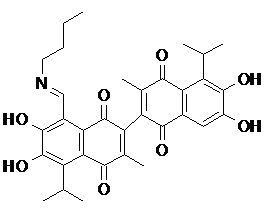
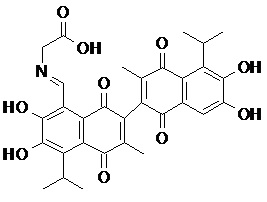
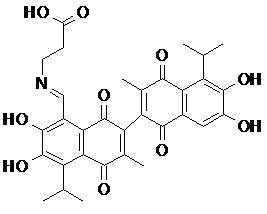
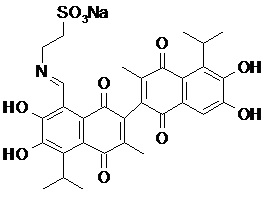

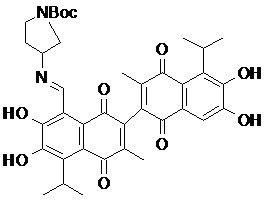
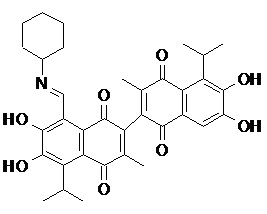
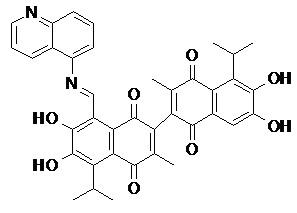
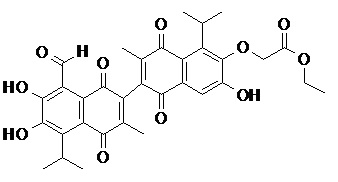
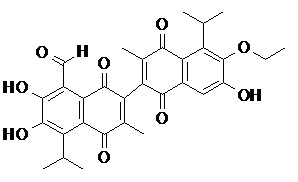
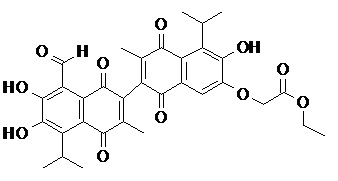
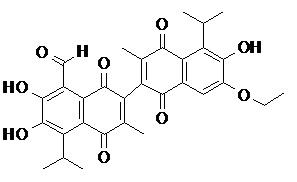
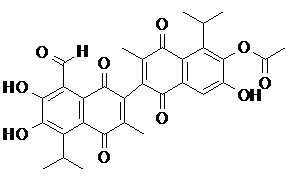
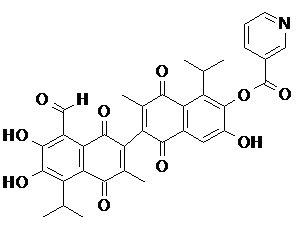
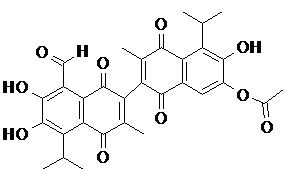
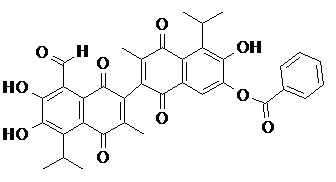
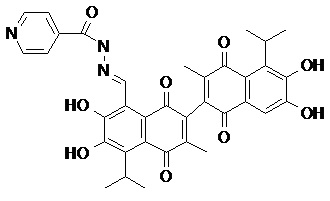
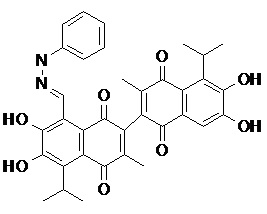
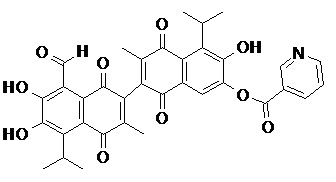
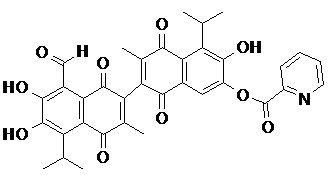
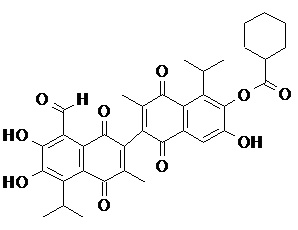
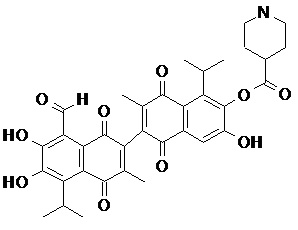
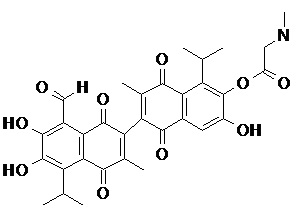
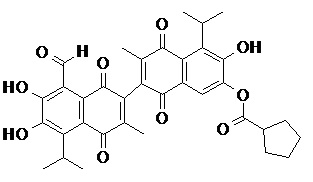
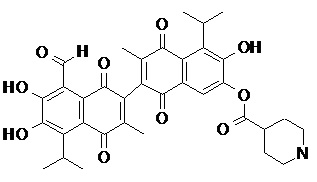
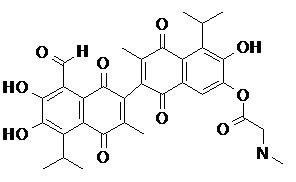
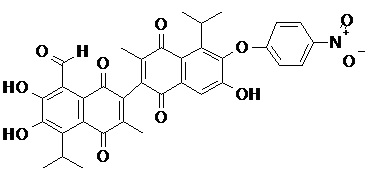
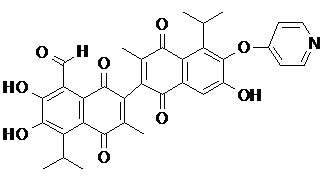
3) В еще одном другом аспекте настоящее изобретение относится к способу получения соединений общей формулы (I) по пункту (1), включающему стадии:
-обработки производного госсипола, необязательно в форме его сольвата, водным раствором гидроксида щелочного и/или щелочноземельного металла;
- обработки полученной реакционной смеси органическими и/или неорганическими кислотами до рН=0,1-10, предпочтительно 3-5;
-выделения и очистки полученного продукта;
- и, в случае необходимости, последующую обработку полученного продукта реакционным агентом, который выбирают из группы, содержащей: алифатические, ароматические или гетероароматические амины; алкилирующие агенты; ацилирующие агенты; соли диазония; и
- выделение и очистку целевого продукта.
Предпочтительно, производное госсипола представляет собой госсипол, госсиполуксусную кислоту, метиловые эфиры госсипола.
Предпочтительно, производное госсипола обрабатывают водным раствором гидроксида калия или натрия.
Предпочтительно, концентрация водного раствора гидроксида щелочного и щелочноземельного металла составляет 0,1-50 мас. %, предпочтительно 10-30 мас.%.
Предпочтительно, обработку алифатическими, ароматическими или гетероароматическими аминами проводят в растворителе, таком как изопропанол, диэтиловый эфир, диоксан или тетрагидрофуран.
Предпочтительно, в качестве алкилирующих агентов используют ароматические или алифатические галогенпроизводные или алкилсульфаты, и обработку проводят в присутствии органических и/или неорганических оснований, таких как карбонат цезия, этилат натрия, трет-бутилат калия, триэтиламин или гидрид натрия, в растворителе, таком как изопропанол, диэтиловый эфир или тетрагидрофуран.
Предпочтительно, в качестве ацилирующего агента используют карбоновые кислоты или галогенангидриды, и обработку проводят в присутствии органических и/или неорганических оснований, таких как карбонат калия, карбонат цезия, метилат натрия, этилат натрия, трет-бутилат калия, триэтиламин, диизопропиламин или гидрид натрия, необязательно в присутствии реагентов сочетания, таких как карбонилдиимидазол, ДЦК, в растворителе, таком как хлороформ, тетрагидрофуран или диоксан.
Предпочтительно, обработку солями диазония проводят в водной среде и/или растворителе, таком как этанол или диэтиловый эфир.
4) В еще одном другом аспекте настоящее изобретение относится к способу получения соединений общей формулы (II) по пункту (1), включающему стадии:
-обработки производного госсипола, необязательно в форме его сольвата, водным раствором гидроксида щелочного и/или щелочноземельного металла;
- обработки полученной реакционной смеси органическими и/или неорганическими кислотами до рН=0,1-10, предпочтительно 3-5;
-выделения и очистки полученного продукта;
-последующей обработки полученного продукта перекисью водорода в концентрации 0,1-99,8% в органических и/или неорганических кислотах; или
-последующей обработки полученного продукта соединениями трехвалентного железа в присутствии органического растворителя и/или органической или неорганической кислоты;
-выделения и очистки полученного продукта; и
- в случае необходимости, последующую обработку полученного продукта реакционным агентом, который выбирают из группы, содержащей: алифатические, ароматические или гетероароматические амины; алкилирующие агенты и ацилирующие агенты; и
- выделение и очистку целевого продукта.
Предпочтительно, производное госсипола представляет собой госсипол, госсиполуксусную кислоту, метиловые эфиры госсипола.
Предпочтительно, производное госсипола обрабатывают водным раствором гидроксида калия или натрия.
Предпочтительно, концентрация водного раствора гидроксида щелочного и щелочноземельного металла составляет 0,1-50 мас. %, предпочтительно 10-30 мас.%.
Предпочтительно, перекись водорода используют в концентрации 1-30 мас.% и обработку проводят в среде уксусной кислоты.
Предпочтительно, соединение трехвалетного железа представляет собой хлорид железа (III) в твердом виде или в водном растворе и обработку проводят в среде ацетона и/или уксусной кислоты.
Предпочтительно, обработку алифатическими, ароматическими или гетероароматическими аминами проводят в растворителе, таком как изопропанол, диэтиловый эфир, диоксан или тетрагидрофуран.
Предпочтительно, в качестве алкилирующих агентов используют ароматические или алифатические галогенпроизводные или алкилсульфаты и обработку проводят в присутствии органических и неорганических оснований, таких как карбонат цезия, этилат натрия, трет-бутилат калия, триэтиламин или гидрид натрия, в растворителе, таком как изопропанол, диэтиловый эфир или тетрагидрофуран.
Предпочтительно, в качестве ацилирующего агента используют карбоновые кислоты или галогенангидриды и обработку проводят в присутствии органических и/или неорганических оснований, таких как карбонат калия, карбонат цезия, метилат натрия, этилат натрия, трет-бутилат калия, триэтиламин, диизопропиламин или гидрид натрия, необязательно в присутствии реагентов сочетания, таких как карбонилдиимидазол, ДЦК, в растворителе, таком как хлороформ, тетрагидрофуран или диоксан.
5) В еще одном другом аспекте настоящее изобретение относится к противовирусному средству, представляющему собой соединение общей формулы (I) или (II) по пункту (1) или соединения по пункту (2).
В предпочтительном варианте настоящее изобретение относится к противовирусному средству, эффективному в отношении вирусов гриппа, герпеса, гепатита, ВИЧ.
Описание чертежей
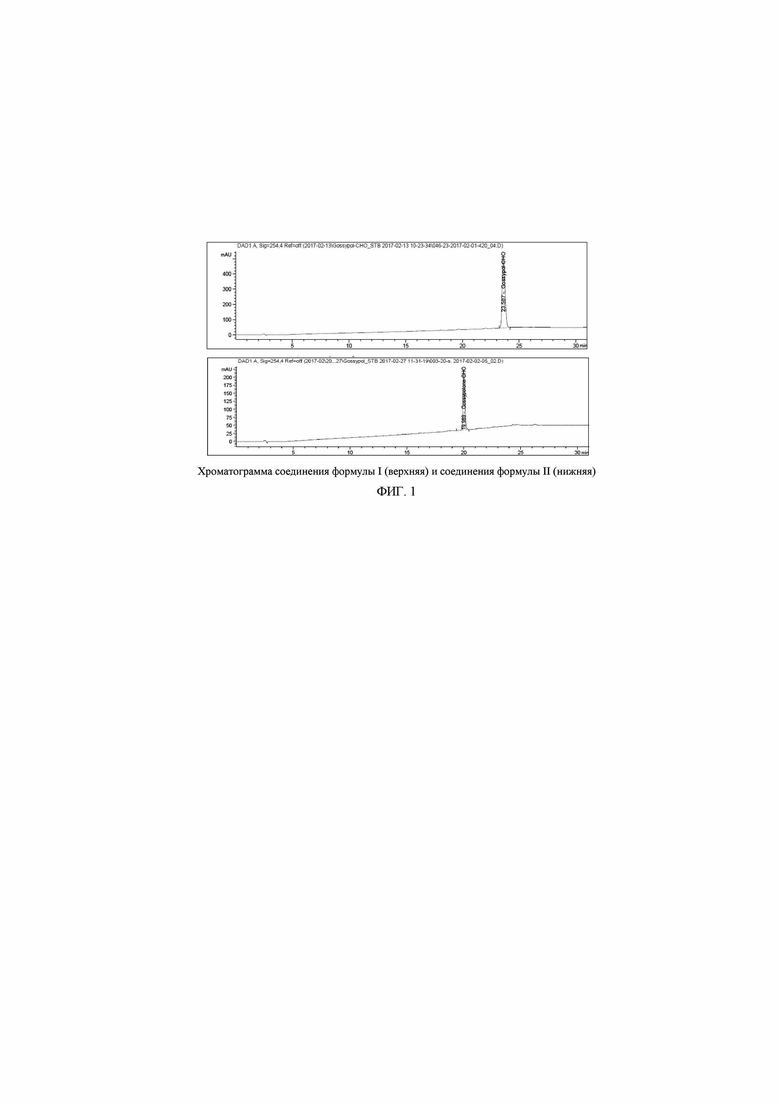
На Фиг. 1 представлены хроматограмма соединения формулы I и хроматограмма соединения формулы II.
На Фиг. 2 представлены масс-спектр соединения формулы I и масс-спектр соединения формулы II.
На Фиг. 3 представлены УФ-спектр соединения формулы I и УФ-спектр соединения формулы II.
На Фиг. 4 представлена хроматограмма (+) и (-) изомера соединения формулы I.
На Фиг. 5 представлены ИК-спектр госсипола и соединения формулы I в таблетке калия бромида.
Подробное описание изобретения
В контексте настоящего описания:
термин «С1-С20 алкил» означает линейную или разветвленную углеводородную цепь, содержащую 1-20 атомов углерода, предпочтительно 1-10 атомов углерода, содержащую заместители в количестве 0-10, предпочтительно 1-3 заместителя, в частности, метил, этил, н-пропил, изопропил, н-бутил, изобутил, С2Н4СООН, 3-метоксибензил;
термины «С2-С20 алкенил» и «С2-С20 алкинил» означают линейную или разветвленную углеводородную цепь, содержащую 2-20 атомов углерода, предпочтительно 2-7 атомов углерода, с количеством двойных и (или) тройных связей 1-9, предпочтительно 1-3 двойных и (или) тройных связи, содержащую заместители в количестве 0-10, предпочтительно 0-3 заместителя, в частности, СН2СH=СНС2H4OCH3, СН2СH=СНС6H5, СН2С≡СН, СН2С≡СС6H5;
термин «циклическая система» означает неароматическую моноциклическую структуру с числом атомов в цикле 3-20, предпочтительно 5-7 атомов, содержащую заместители в количестве 0-10, предпочтительно 0-3 заместителя, количеством двойных и (или) тройных связей 0-10, предпочтительно 0-2 связи, и количеством гетероатомов (N, S, O) 0-10, предпочтительно 0-2 гетероатома, в частности, тетрагидропиран-4-ил, циклогептил, тетрагидротиопиран-4-ил, пирролидин-2-он-3-ил, 1-этилазепан-2-он-3-ил;
термин «арил» означает шестичленное ароматическое соединение бензольного ряда, содержащее заместители в количестве 0-5, предпочтительно 0-3 заместителя, в частности 4-карбоксифенил, 3-гидрокси-4-метоксифенил, 3-метилфенил;
термин «гетероароматическое соединение» означает моноциклическую ароматическую структуру с числом атомов в цикле от 3 до 12, предпочтительно 5-7 атомов, количеством гетероатомов (N, S, O) от 1 до 6, предпочтительно 0-2 гетероатома, содержащую заместители в количестве от 0 до 10, предпочтительно 0-3 заместителя, в частности пиридазин-4-ил, пиразин-2-ил, пиримидин-5-ил;
термин «полициклическая система» означает ароматическое и (или) неароматическое конденсированное циклическое соединение, содержащее 2-5 циклов, предпочтительно 2-3 цикла, с числом атомов в цикле 3-8, предпочтительно 5-7 атомов в цикле, количеством двойных и (или) тройных связей 0-10, предпочтительно 0-3 двойных и (или) тройных связей, количеством гетероатомов (N, S, O) 0-10, предпочтительно 0-4 гетероатома, и содержащее заместители в количестве от 0 до 20, предпочтительно 0-3 заместителя, в частности, хинолин-6-ил, 1-ацетилиндолин-6-ил, имидазо[1,2-a]пиримидин-3-ил;
термин «сольваты» означает продукты присоединения растворителя или реагента к растворенному веществу, а также клатраты-соединения включения молекул растворителя или реагента в полости кристаллической структуры другого вещества, существующие в растворе и (или) твердом состоянии, в частности госсиполуксусная кислота, клатрат госсипола с изобутилацетатом, клатрат бис-о-толуидингоссипола с 1,4-диоксаном;
термин «фармацевтически приемлемые соли» означает вещества, которые в водных растворах диссоциируют на катионы и анионы кислотных остатков, в частности хлориды, сульфаты, ацетаты, карбонаты, оксалаты, карбоксилаты, алкоголяты, феноляты, аммонийные соли, пиридиниевые соли;
термин «гидроксид щелочного металла» означает соединение, состоящее из щелочного металла и гидроксильной группы, в частности, гидроксид лития, гидроксид натрия, гидроксид калия;
термин «гидроксид щелочноземельного металла» означает соединение, состоящее из щелочноземельного металла и гидроксильной группы, в частности, гидроксид кальция, гидроксид магния, гидроксид бария;
термин «органическая кислота» означает органическое соединение, проявляющее кислотные свойства, в частности, муравьиная кислота, уксусная кислота, щавелевая кислота, п-толуолсульфоновая кислота, лимонная кислота, винная кислота;
термин «неорганическая кислота» означает неорганическое соединение, проявляющее кислотные свойства, в частности, соляная кислота, серная кислота, ортофосфорная кислота, хлорная кислота, угольная кислота, азотная кислота;
термин «алифатический амин» означает органическое соединение, принадлежащее к классу аминов и отличающееся содержанием неароматических заместителей у атома азота, в частности, метиламин, морфолин, изопентиламин, бензиламин, глицин, 4-аминопиперидин;
термин «ароматический амин» означает производное ароматических углеводородов, в котором один или несколько атомов водорода замещены на аминогруппу, в частности, 2-метил- 4-метоксианилин, 3-фторанилин, 3-этоксианилин, 4-нитроанилин;
термин «гетероароматический амин» означает производное органических гетероароматических соединений, в котором один или несколько атомов водорода замещены на аминогруппу, в частности 4-аминопиримидин, метил 2-амино-6,7-дигидро-5H-пирроло[1,2-A]имидазол-3-карбоксилат, 1-Н-индол-3-амин, 5-аминоиндол, 5-аминоиндан, 6-амино-2,2-диметил-хроман-4-он;
термин «алкилирующий агент» означает вещество, позволяющее ввести алкильную группу в молекулу, в частности, бензилбромид, диметилсульфат, метилйодид, этил-4-бромбутират;
термин «ацилирующий агент» означает вещество, позволяющее ввести ацильную группу в молекулу, в частности, уксусный ангидрид, п-этоксибензоилхлорид, трифторуксусный ангидрид, циклопентанкарбонил хлорид, ацетил бромид;
термин «соль диазония» означает соединение формулы R-[N+≡N]X-, где R-арил или гетарил, а Х-анион соответствующей кислоты, в частности хлорид фенилдиазония, гидросульфат п-метоксифенилдиазония;
термин «метиловый эфир госсипола» означает производное госсипола в любой таутомерной форме, в котором один или несколько атомов водорода гидроксильной группы замещены на метил, в частности, 1,1',7,7'-тетрагидрокси-5,5'-диизопропил-6,6'-диметокси-3,3'-диметил-2,2'-бинафталин-8,8'-дикарбальдегид, 6,6',7,7'-тетрагидрокси-5,5'-диизопропил-1,1'-диметокси-3,3'-диметил-2,2'-бинафталин-8,8'-дикарбальдегид;
термин «алифатическое галогенпроизводное» означает любое неароматическое органическое соединение, в котором один и (или) несколько атомов водорода замещены на галоген, в частности, бромистый этил, циклопентилхлорид, 3,5-диметоксибензил бромид;
термин «ароматическое галогенпроизводное» означает любое ароматическое и (или) гетероароматическое органическое соединение, в котором один и (или) несколько атомов водорода замещены на галоген, в частности, 1-фтор-4-нитрофторбензол, 2-хлоропиридин, 2-бромо-1,3,4-тиодиазол;
термин «органическое основание» означает любое органическое соединение, способное принимать положительно заряженные ионы, в частности триэтиламин, 4-метилморфолин, N-этилдиизопропиламин, трет-бутилат калия;
термин «неорганическое основание» означает любое неорганическое соединение, способное принимать положительно заряженные ионы, в частности, карбонат натрия, гидроксид калия, ацетат натрия, гидроксид натрия, гидрокарбонат натрия, карбонат цезия, карбонат калия;
термин «карбоновая кислота» означает органическое соединение, содержащее в структуре как минимум одну группу СООН, в частности, уксусная кислота, муравьиная кислота, лимонная кислота, трифторуксусная кислота, бензойная кислота;
термин «галогенангидрид» означает органическое соединение, состоящее из остатка карбоновой кислоты, гидроксильная группа которой замещена на галоген, в частности, циклопропанкарбонил хлорид, 4,4,4-трифторбутирил бромид, 5-метилникотиноил хлорид;
термин «реагент сочетания» означает соединение, применяемое в органическом синтезе для активации карбоксильной группы, в частности, карбонилдиимидазол, 1-этил-3-(3-диметиламинопропил)карбодиимид, 1,3-дициклогексилкарбодиимид;
термин «таутомерные формы» означает вещества одного химического состава, способные к самопроизвольному превращению в структурные изомеры-таутомеры путем миграции атомной группы между несколькими центрами в молекуле, в частности, приведенные ниже (А - альдегид, В - кетон, С- полуацеталь; D - имин, F - енамин).
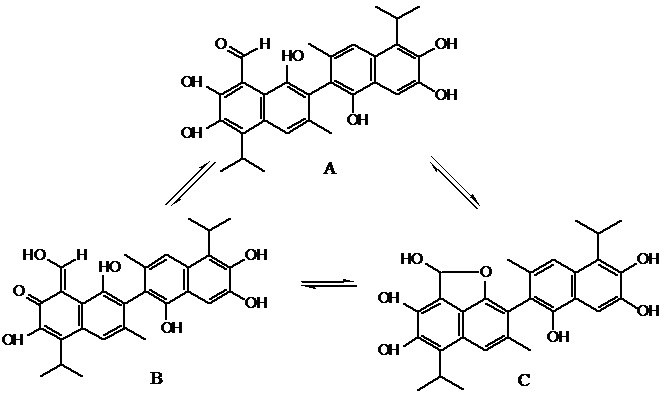
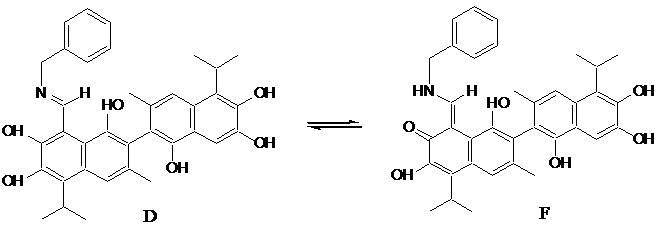
Предложенное изобретение иллюстрируется следующими примерами.
Получение соединения I (1,1',6,6',7,7'-гексагидрокси-5,5'-диизопропил-3,3'-диметил-2,2'-бинафталин-8-карбальдегид).

Способ 1: В химический стакан объемом 3000 мл наливают 1500 мл 17% раствора гидроксида натрия, после чего при перемешивании на магнитной мешалке добавляют 70 г (0,12 моль) госсиполуксусной кислоты (ГУК). Реакционную массу перемешивают при комнатной температуре в течение 8 часов, после чего выдерживают без перемешивания 15 часов. Затем реакционную массу подкисляют уксусной кислотой до рН=4. Далее выпавший осадок фильтруют и промывают 2 раза дистиллированной водой, после чего сушат в сухожаровом шкафу при 50°С до постоянной массы. Полученный порошок очищают перекристаллизацией или хроматографическими методами. Получают продукт в виде желтого порошка. Выход - 35 г (53%).
ЯМР 1H (CDCl3,, м.д., J, Гц): 1.51-1.54 м (12H, 4CH3, 2 i-Pr), 2.10 с (3H, СН3), 2.13 с (3H, СН3), 3.85-3.90 м (2H, 2CH, 2 i-Pr), 5.24 c (1H, OH), 5.86 c (1H, OH), 5.91 c (1H, OH), 5.98 c (1H, OH), 6.39 c (1H, OH), 7.45 c (1H, CH ), 7.62 c (1H, CH), 7.74 c (1H, CH), 11.12 c (1H, CHO), 15.15 (1H, OH); ЯМР 13С (CDCl3, δ, м.д.): 199.6 (C, HC=O), 156.1 (C, Ph-OH), 150.4 (C, Ph-OH), 149.4 (C, Ph-OH), 143.3 (C, Ph-OH), 142.7 (C, Ph-OH), 134.3 (C, Ph-OH), 134.2 (C, Ph-i-Pr), 132.8 (C, Ph-i-Pr), 130.3 (C, Ph-CH3), 129.4 (C, Ph-CH3), 129.1 (C, Ph), 128.3 (C, Ph), 125.9 (CH, Ph), 125.4 (CH, Ph), 117.8 (C, Ph-Ph), 116.9 (C, Ph-Ph), 114.5 (C, Ph), 111.9 (C, Ph), 110.8 (C, Ph-CH=O), 103.2 (CH, Ph), 27.2 (CH, i-Pr), 27.0 (CH, i-Pr), 20.0-20.9 (4+2, 4CH3,×2 i-Pr+2 CH3, ×2 Ph-CH3); ESI-MS m/z: 489.2 [M-H]-(C29H30O7, Mr=490.2); UV-VIS: λmax/nm: 249, 289, 379.
Получение соединения II (6,6',7,7'-тетрагидрокси-5,5'-диизопропил-3,3'-диметил-1,1',4,4'-тетраоксо-1,1',4,4'-тетрагидро-2,2'-бинафталин-8-карбальдегид).

Раствор 4,0 г (0,008 моль) соединения I в 100 мл ацетона и 200 мл уксусной кислоты нагревают на паровой бане с добавлением 150 мл 10% водного раствора гексагидрат хлорида железа III в течение нескольких минут. Раствор охлаждают и добавляют 250 мл воды. Выпавший темный осадок, содержащий соединения железа, удаляют обработкой смесью эфира и водного раствора 20% серной кислоты. Очищенный фенол экстрагируют эфиром, отделяют эфирный слой, сушат сульфатом натрия и досуха упаривают. Полученный порошок очищают перекристаллизацией или хроматографическими методами. Получают продукт в виде оранжевого порошка. Выход 3,1 г (69%).
В плоскодонную колбу емкостью 50 мл помещают 1,7 г (0,0035 моль) соединения I, добавляют 17 мл уксусной кислоты и 2 мл 30%-ого раствора перекиси водорода. Перемешивают реакционную массу при комнатной температуре в течение 24 часов. Далее реакционную массу выливают в 100 мл дистиллированной воды, экстрагируют 3 раза порциями хлороформа по 20 мл, объединенный органический слой промывают 2 раза порциями дистиллированной воды по 30 мл. Органический слой отделяют, сушат сульфатом натрия и упаривают досуха. Полученный порошок очищают перекристаллизацией или хроматографическими методами. Получают продукт в виде оранжевого порошка. Выход 1,0 г (54%).
ЯМР 1H (CDCl3,, м.д., J, Гц): 1.35-1.44 м (12H, 4CH3, 2 i-Pr), 2.02 с (3H, СН3), 2.03 с (3H, СН3), 4.09-4.14 м (1H, CH, 1 i-Pr), 4.28-4.33 м (1H, CH, 1 i-Pr), 6.23 c (1H, OH), 6.59 с (1H, OH), 6.93 c (1H, OH), 7.46 c (1H, CH), 10.53 c (1H, CHO), 12.93 (1H, OH); ЯМР 13С (DMSO-d6, CDCl3, δ, м.д.): 198.2 (C, HC=O), 186.9 (C, C=O), 186.8 (C, C=O), 184.3 (C, C=O), 182.7 (C, C=O), 153.0 (C, Ph-OH), 150.8 (C, Ph-OH), 150.7 (C, Ph-OH), 149.0 (C, Ph-OH), 147.9 (C, Ph- i-Pr), 146.4 C, Ph- i-Pr), 141.7 (C, Ph-CH3), 138.8 (C, Ph-CH3), 137.4 (C, Ph), 137.3 (C, Ph), 127.7 (C, Ph-Ph), 126.7 (C, Ph-Ph), 126.4 (C, Ph), 125.1 (C, Ph), 116.7 (C, Ph-CH=O), 111.3 (CH, Ph), 28.6 (CH, i-Pr), 27.3 (CH, i-Pr), 19.8-20.2 (4C, 4CH3, i-Pr), 15.1 (C, Ph-CH3), 14.7 (C, Ph-CH3); ESI-MS m/z: 517.2 [M-H]- (C29H26O9, Mr=518.2); UV-VIS: λmax/nm: 277, 368.
Получение соединения III (этил [(8-формил-1,1',6,6',7'-пентагидрокси-5,5'-диизопропил-3,3'-диметил-2,2'-бинафталин-7-ил)окси]ацетат).

В пробирку помещают 10 мл тетрагидрофурана, 1,00 г (2,0 ммоль) соединения I, 0,50 г (4,0 ммоль) трет-бутилата калия, после чего перемешивают реакционную смесь в течение 20 минут. Затем к раствору прибавляют 0,90 г (4,00 ммоль) этилйодацетата и перемешивают реакционную смесь при нагревании в течение 8 часов. Реакционную смесь выливают в 50 мл воды, подкисляют уксусной кислотой до рН 5, экстрагируют 2 раза порциями хлороформа по 10 мл. Объединенные органические слои сушат сульфатом натрия и концентрируют в вакууме. Полученный порошок очищают перекристаллизацией или хроматографическими методами. Получают продукт в виде желтого порошка. Выход 0,30 г (27%).
ЯМР 1H (CDCl3, м.д., J, Гц): 1.29-1.32 т (2H, CH2COOCH2CH3, 2J=7.1), 1.54-1.58 м (12H, 4CH3, 2 i-Pr), 2.12 с (3H, СН3), 2.14 с (3H, 2СН3), 3.84-3.91 м (2H, 2CH, 2 i-Pr), 4.27-4.31 к (2H, CH2COOCH2CH3, J=7.1), 4.79 c (2H, CH2COOCH2CH3), 5.17 c (1H, OH), 5.74 с (1H, OH), 6.41 с (1H, OH), 6.84 c (1H, OH), 7.45 c (1H, CH), 7.66 c (1H, CH), 7.75 c (1H, CH), 11.14 c (1H, CHO), 15.24 (1H, OH); ESI-MS m/z: 575.2 [M-H]- (C33H39O9, Mr=576.2).
Получение соединения IV(8-(бензилимино)метил-5,5'-диизопропил-3,3'-диметил-2,2'-бинафталин-1,1',6,6',7,7'-гексол).

В пробирку наливают 1 мл диэтилового эфира, добавляют 0,100 г (0,2 ммоль) соединения I и добавляют 0,022 г бензиламина (0,2 ммоль). Далее перемешивают реакционную массу при комнатной температуре 2 часа. Выпавший осадок фильтруют и промывают диэтиловым эфиром. Получают продукт в виде желтого порошка. Выход 0,060 г (48%).
ЯМР 1H (DMSO-d6, м.д., J, Гц): 1.38-1.41 м (12H, 4CH3, 2 i-Pr), 1.90 с (3H, СН3), 1.92 с (3H, СН3), 3.67-3.79 м (2H, 2CH, 2 i-Pr), 4.71 c (2H, C6H5CH2N), 7.25-7.43 м (8H+3H, C6H5CH2N, CH), 7.45 c (1H, OH), 7.63 c (1H, OH), 7.88 c (1H, OH), 8.25 c (1H, OH), 8.33 c (1H, OH), 9.82-9.84 д (1H, CNСH), 13.48 (1H, OH).
Получаемые продукты были проанализированы следующими методами:
Высокоэффективная жидкостная хроматография с УФ-спектрофотометрическим и масс-спектрометрическим детектированием (ВЭЖХ-УФ-МС)
Метод использовали для установления структуры и определения молекулярной массы, полученных соединений, а так же с целью установления количественного состава и чистоты. Анализ проводили на жидкостном хроматографе Agilent 1260 с последовательным детектированием на диодно-матричном и масс-селективном детекторах. Разделение проводили на хроматографической колонке Zorbax Eclipse Plus C18 производства Agilent, используя в качестве элюентов 0,1% раствор муравьиной кислоты в воде и ацетонитрил в градиентном режиме элюирования. В используемом одноквадрупольном масс-спектрометрическом детекторе ионизация осуществляется методом электрораспыления, детектирование проводили в режиме регистрации отрицательных ионов. Детектирование на диодно-матричном детекторе выполняли при длине волны 254 нм и регистрировали УФ-спектр в диапазоне от 200 до 400 нм.
Энантиомерный состав продукта определяли на хроматографе Waters, оснащенном спектрофотометрическим детектором. Разделение проводили на хиральной колонке Chiralart Cellulose-SB производства YMC, используя в качестве элюента смесь 10 мМ калия фосфата однозамещенного и ацетонитрила в изократическом режиме элюирования.
Чистота полученных продуктов была показана методом ВЭЖХ. Как видно из приведенных хроматограмм (фиг.1), выделенные продукты I и II не содержит родственных примесей в значительных количествах.
В полученном масс-спектре основного пика I со временем удерживания 23,6 мин в качестве основного присутствует псевдомолекулярный ион m/z 489, что соответствует депротонированной молекуле [M-H]-. В масс-спектре основного пика II со временем удерживания 20,0 мин присутствует основной молекулярный ион ион с m/z [M-H]-=517, а так же фрагмент соответствующий иону [M-2H+Na]- c массой 539 (фиг.2).
I и II имеют характеристичные УФ-спектры (фиг.3). В спектре I присутствуют три максимума при 249 нм, 289 нм и 370 нм. В УФ-спектре II имеется один ярко выраженный максимум при 277 нм.
Наличие в молекуле I связи С-С, которая соединяет два нафталиновых цикла, вокруг которой затруднено свободное вращение за счет объемных заместителей, приводит к тому, что I может существовать в виде двух энантиомеров.
Хроматограмма, приведенная на фиг.4, показывает, что продукт представляет собой рацемическую смесь, состоящую из (+) и (-) форм I, присутствующих примерно в равных количествах.
Инфракрасная спектроскопия с преобразованием Фурье (ИК)
Метод ИК-спектроскопии использовали с целью подтверждения структуры полученных соединений. Регистрацию спектров проводили на спектрометре Spectrum 65 производства Perkin Elmer в диске с калия бромидом, в области от 4000 до 400 см-1.
ИК-спектр I имеет характерные для данной структуры полосы (фиг.5). В ИК-спектре сигнал при 3482 см-1 соответствует валентным колебаниям OH-групп нафталиновых колец. Группа сигналов в диапазоне 2960-2873 см-1 соответствует колебаниям ненасыщенных и CH-групп бензольных колец и метильных групп CH3-. В отличие от ИК-спектра госсипола отсутствует ярко выраженная полоса при волновом числе 2609 см-1, соответствующая валентным колебаниям CH-фрагмента альдегидных групп, а так же происходит смещение и значительное уменьшение интенсивности полосы при 1711 см-1, принадлежащей валентным колебаниям C=O альдегидных групп. Полосы при волновых числах 1614, 1578 и 1502 см-1 соответствуют колебаниям атомов углерода при двойной связи нафталиновых колец. Деформационные колебания метильных групп CH3- изопропильного фрагмента представлены полосами 1441 и 1385 см-1. Полосы поглощения 1338 см-1 и 1303 см-1 принадлежат деформационным колебаниям нафталиновых колец относительно друг друга, а 1122 см-1 и 1053 см-1 деформационным колебаниям 1,2 - замещенных фенилов.
Спектроскопия ядерного магнитного резонанса (ЯМР)
Спектры ЯМР 1Н и 13С регистрировали на приборе Bruker Avance-400 (рабочая частота 400 и 100 МГц, соответственно). В качестве внутреннего стандарта использовали сигнал хлороформа (H=7.24, С=77.10 м.д).
Строение I и II было полностью подтверждено данными спектроскопии ЯМР 1Н и 13C. В ЯМР 1Н спектрах присутствуют все характеристичные сигналы для данных структур. В спектре 1Н II происходит смещение сигнала атома водорода альдегидной группы с δH=11.12 м.д. до δH=10.53 м.д. и сигнала, образующего с ней внутримолекулярную водородную связь, атома водорода фенольного гидроксила с δH=15.15 м.д. до δH=12.93 м.д. по сравнению со спектрами госсипола и I. По сравнению со спектром госсипола, имеющего синглетный сигнал при δH=7.80 м.д., соответствующий двум протонам СН-фрагментов каждого из нафталиновых колец, для I наблюдается три сигнала при δH=7.45 м.д., δH=7.62 м.д. и δH=7.74 м.д. из-за отсутствия одной альдегидной группы и нарушения симметрии молекулы. В молекуле II присутствует один такой протон, что проявляется в виде синглета с химическим сдвигом 7.46 м.д. ЯМР 1Н I имеет набор из 5 синглетных сигналов, принадлежащих фенольным гидроксилам: δH=5.24 м.д., δH=5.86 м.д., δH=5.91 м.д., δH=5.98 м.д., δH=6.39 м.д., для II таких сигнала три: δH=6.23 м.д., δH=6.59 м.д. и δH=6.93 м.д., что полностью согласуется с формулами данных веществ. Обе молекулы имеют в ЯМР 1Н спектре в сильном поле наборы сигналов, принадлежащих изопропильным и метильным группам, для которых наблюдается небольшое смещение в слабое поле для молекулы II.
Определение цитотоксических свойств несимметричных производных госсипола.
В 96-луночные плоскодонные тест-планшеты помещают клетки в количестве 10000 клеток на лунку в объеме 100 мкл полной среды, содержащей 10% эмбриональной телячьей сыворотки (ЭТС). Клетки культивируют в течение суток в ламинарном шкафу в темноте. Затем из лунок тест-планшетов удаляют жидкую среду пипеткой, оставляя иммобилизованные живые клетки. Взамен жидкой среды в лунки вносят по 100 мкл разведений тестируемых препаратов, приготовленных на полной среде. Каждое разведение дублируют в 3-4 повторностях. На планшете готовят 4 контрольные лунки, в которые добавляют по 100 мкл свежей полной среды, не содержащей тестируемых препаратов. Планшет помещают в ламинарный шкаф и клетки культивируют в течение 3 сут. Затем из лунок удаляют жидкое содержимое, вносят по 100 мкл полной среды и по 20 мкл ЭТС, перемешивают в насадке пипетки и инкубируют 3,5 часа в ламинарном шкафу в темноте, после чего на спектрофотометре Sunrise (Tecan) измеряют относительную оптическую плотность раствора в каждой лунке при 492 нм относительно его поглощения при длине волны сравнения 620 нм. Цитотоксичность СС50 рассчитывают по стандартной методике: Terry L. Riss and Richard A. Moravec «Use of multiple assay endpoints to investigate the effects of incubation time, dose of toxin, and plating density in cellbased cytotoxicity assays». ASSAY and Drug Development Technologies Volume 2, Number 1, 2004 р.51-62.
Исследование in vitro противовирусного действия несимметричных производных госсипола на штаммах вируса гриппа А.
список сокращений:
ТЦД50 - тканевая цитопатогенная доза, вызывающая гибель 50% клеток монослоя
ЦПД - цитопатическое действие
ТК50 - токсическая доза препарата, вызывающая гибель 50% клеток монослоя
ЭК50 - эффективная доза препарата, при которой выживает 50% клеток монослоя
Методика
К клеткам MDCK, достигшим монослоя на 96-луночных культуральных планшетах, добавляли исследуемые препараты в серийных разведениях. После этого клетки заражали вирусом гриппа в дозе 10ТЦД50/лунку. Для определения ТК50 клетки с теми же концентрациями препаратов заражены не были. Инфицированные клетки инкубировали в течение 48 часов, при этом в контроле ЦПД достигает 100%. После этого клетки окрашивали красителем МТЗ, оптическую плотность считывали на планшетном ридере. Точные значения ТК50 и ЭК50 были определены путем построения нелинейной регрессии данных. Химиотерапевтический индекс рассчитывали по формуле ХТИ=ТК50/ЭК50.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ N-ГИДРОКСИЛСУЛЬФОНАМИДА КАК НОВЫЕ ФИЗИОЛОГИЧЕСКИ ПРИМЕНИМЫЕ ДОНОРЫ НИТРОКСИЛА | 2008 |
|
RU2485097C2 |
| ПРОИЗВОДНЫЕ N-ГИДРОКСИЛСУЛЬФОНАМИДА В КАЧЕСТВЕ НОВЫХ ФИЗИОЛОГИЧЕСКИ ПОЛЕЗНЫХ ДОНОРОВ НИТРОКСИЛА | 2007 |
|
RU2616292C2 |
| МЕТАЛЛООРГАНИЧЕСКОЕ СОЕДИНЕНИЕ ПЕРЕХОДНОГО МЕТАЛЛА, БИСЦИКЛОПЕНТАДИЕНИЛЬНАЯ ЛИГАНДНАЯ СИСТЕМА, КАТАЛИТИЧЕСКАЯ СИСТЕМА И ПОЛУЧЕНИЕ ПОЛИОЛЕФИНОВ | 2004 |
|
RU2362779C2 |
| ПРОИЗВОДНЫЕ N-ГИДРОКСИЛСУЛЬФОНАМИДА В КАЧЕСТВЕ НОВЫХ ФИЗИОЛОГИЧЕСКИ ПОЛЕЗНЫХ ДОНОРОВ НИТРОКСИЛА | 2007 |
|
RU2448087C2 |
| НИЗКОМОЛЕКУЛЯРНЫЕ ИНГИБИТОРЫ N-КОНЦЕВОЙ АКТИВАЦИИ РЕЦЕПТОРА АНДРОГЕНОВ | 2009 |
|
RU2519948C2 |
| НОВЫЕ АНАЛОГИ СС-1065 И ИХ КОНЪЮГАТЫ | 2009 |
|
RU2562232C2 |
| ПИРАЗОЛО[1,5-a]ПИРИМИДИНЫ, ПРИМЕНЯЕМЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ ПРОТЕИНКИНАЗ | 2005 |
|
RU2417996C2 |
| ПРОТИВОГЕЛЬМИНТНЫЕ АЗА-БЕНЗОТИОФЕНОВЫЕ И АЗА-БЕНЗОФУРАНОВЫЕ СОЕДИНЕНИЯ | 2020 |
|
RU2833610C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИМЕРОВ С РАЗЛИЧНОЙ СТРУКТУРОЙ ПУТЕМ ИНИЦИАЦИИ АМИНАМИ | 2011 |
|
RU2592848C2 |
| КАРОТЕНОИДНОЕ ПРОИЗВОДНОЕ, ЕГО ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМАЯ СОЛЬ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ЕГО | 2015 |
|
RU2693455C2 |




Настоящее изобретение относится к несимметричным производным полифенолов динафталинового ряда общей Формулы (I) или общей Формулы (II), к способам их получения и к их применению в качестве противовирусного средства, эффективного в отношении вируса гриппа А
I
II.
В формуле I R1 представляет собой: C(O)H, CH=N-R8, где R8 представляет собой: линейный и разветвленный С1-С20 алкил, замещённый фенилом; R2, R3, R3a, R5, R5a, R7, R7a представляют собой H; R2a представляет собой: H, линейный и разветвленный С1-С20 алкил, замещённый COOR8a, где R8a представляет собой: H, линейный и разветвленный С1-С20 алкил; R4, R4a, R6 и R6a независимо представляют собой линейный и разветвленный С1-С10 алкил. В формуле II R1 представляет собой: C(O)H; R2, R3, R2a, R3a представляют собой Н; R4, R4a, R6 и R6a независимо представляют собой H, линейный или разветвленный С1-С10 алкил. 6 н. и 10 з.п. ф-лы, 5 ил., 2 табл.
1. Соединение общей формулы I:
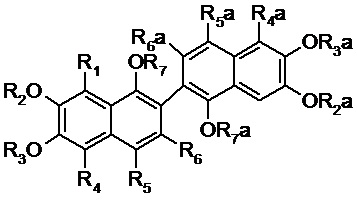
I
где
R1 представляет собой: C(O)H, CH=N-R8;
где R8 представляет собой: линейный и разветвленный С1-С20 алкил, замещённый фенилом;
R2, R3, R3a, R5, R5a, R7, R7a представляют собой H;
R2a представляет собой: H; линейный и разветвленный С1-С20 алкил, замещённый COOR8a;
где R8a представляет собой: H; линейный и разветвленный С1-С20 алкил;
R4, R4a, R6 и R6a независимо представляют собой линейный и разветвленный С1-С10 алкил;
или общей формулы II
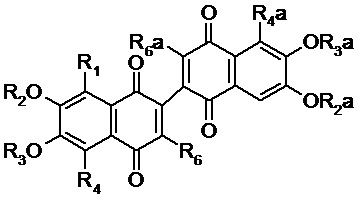
II
где
R1 представляет собой: C(O)H;
R2, R3, R2a, R3a представляют собой Н;
R4, R4a, R6 и R6a независимо представляют собой H, линейный или разветвленный С1-С10 алкил;
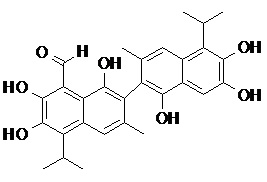
при условии, что следующее соединение исключено
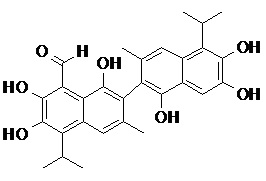
2. Соединение, имеющее структуру, представленную в Таблице 1:
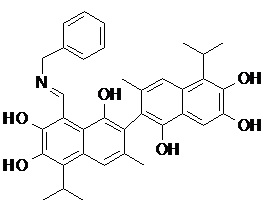

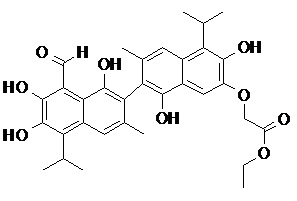
3. Способ получения соединения общей формулы (I) по п.1, включающий стадии:
- обработки госсиполуксусной кислоты водным раствором гидроксида щелочного и/или щелочноземельного металла;
- обработки полученной реакционной смеси органическими и/или неорганическими кислотами до рН=0,1-10;
- выделения и очистки полученного продукта;
- и, в случае необходимости, последующей обработки полученного продукта реакционным агентом, который выбирают из группы, содержащей: алифатические амины, ароматические амины или алкилирующие агенты; и
- выделения и очистки целевого продукта.
4. Способ по п.3, где обработку полученной реакционной смеси органическими и/или неорганическими кислотами проводят до рН=3-5.
5. Способ по п.3 или 4, где госсиполуксусную кислоту обрабатывают водным раствором гидроксида калия или натрия.
6. Способ по любому из пп.3-5, где концентрация водного раствора гидроксида щелочного и/или щелочноземельного металла составляет 0,1-50 мас.%, предпочтительно 10-30 мас.%.
7. Способ по любому из пп.3-6, где обработку алифатическими или ароматическими аминами проводят в растворителе, таком как изопропанол, диэтиловый эфир, диоксан или тетрагидрофуран.
8. Способ по любому из пп.3-6, где в качестве алкилирующих агентов используют ароматические или алифатические галогенпроизводные или алкилсульфаты и обработку проводят в присутствии органических и/или неорганических оснований, таких как карбонат цезия, этилат натрия, трет-бутилат калия, триэтиламин или гидрид натрия, в растворителе, таком как изопропанол, диэтиловый эфир или тетрагидрофуран.
9. Способ получения соединения общей формулы (II) по п.1, включающий стадии:
- обработки госсиполуксусной кислоты водным раствором гидроксида щелочного и/или щелочноземельного металла;
- обработки полученной реакционной смеси органическими и/или неорганическими кислотами до рН=0,1-10;
- выделения и очистки полученного продукта;
- последующей обработки полученного продукта перекисью водорода в концентрации 0,1-99,8 мас.% в органических и/или неорганических кислотах; или
- последующей обработки полученного продукта соединениями трехвалентного железа в присутствии органического растворителя и/или органической или неорганической кислоты;
- выделения и очистки целевого продукта.
10. Способ по п.9, где обработку полученной реакционной смеси органическими и/или неорганическими кислотами проводят до рН=3-5.
11. Способ по п.9 или 10, где госсиполуксусную кислоту обрабатывают водным раствором гидроксида калия или натрия.
12. Способ по любому из пп.9-11, где концентрация водного раствора гидроксида щелочного и/или щелочноземельного металла составляет 0,1-50 мас.%, предпочтительно 10-30 мас.%.
13. Способ по любому из пп.9-12, где перекись водорода используют в концентрации 1-30 мас.% и обработку проводят в среде уксусной кислоты.
14. Способ по любому из пп.9-12, где соединение трехвалентного железа представляет собой хлорид железа (III) в твердом виде или в водном растворе и обработку проводят в среде ацетона и/или уксусной кислоты.
15. Противовирусное средство, эффективное в отношении вируса гриппа А, представляющее собой соединение по п.1.
16. Применение соединения формулы

в качестве противовирусного средства, эффективного в отношении вируса гриппа А.
| CN 101327201 A, 24.12.2008 | |||
| SHELEEY, M.D | |||
| et al | |||
| "Structure-activity studies on gossypol in tumor cell lines" Anti-Cancer Drugs, 2000, 11(3), 209-216 | |||
| Database CA [online] AIHUA, K | |||
| et al | |||
| "Synthesis of gossypol unsymmetric derivatives and their antiferttility activity by oral administration" Zhongguo Yaowu Huaxue Zazhi, 1993, 3(2), 47-100, 1993, |
Авторы
Даты
2022-02-10—Публикация
2017-12-26—Подача