Настоящее изобретение относится к области молекулярной биологии и иммунологии, а именно к разработке вакцин и адъювантов для них. В частности, настоящее изобретение относится к применению пептида, усиливающего секрецию соматотропного гормона, выбранного из синтетического пептида, высвобождающего соматотропный гормон, GHRP-6 и его структурного аналога A233, в качестве молекулярного адъюванта для вакцин.
Уровень техники
Вещества, усиливающие секрецию соматотропного гормона, (GHS) (Davenport et al. 2005, Pharmacol. Rev. 57: 541-546) представляют собой семейство химических соединений, которое включает в себя пептидильные и непептидильные молекулы, которые стимулируют секрецию соматотропного гормона (СТГ) in vitro и in vitro (Tannenbaum and Bowers, 2001, Endocrine 14: 21-27).
Грелин является эндогенным лигандом рецептора веществ, усиливающих секрецию соматотропного гормона (GHS-R) (Kojima et al., 1999, Nature 402: 656-660). Он участвует во многих процессах, включая, среди прочего, регулирование энергетического баланса, аппетита, метаболических сигналов (Dixit and Taub, 2005, Exp. Gerontoly 40: 900-910). Кроме того, он оказывает противовоспалительное действие, модулирует фагоцитоз и способствует тимопоэзу, а также ослаблению септического шока (Hattori, 2009, J. Clin. Endocrinol. Metab. 86: 4284-4291).
Помимо стимуляции секреции СТГ, GHS регулируют аппетит и увеличение веса у млекопитающих, птиц и рыб (Kaiya et al., 2008, Comp. Biochem. Physiol. A 149: 109-128). Они также обладают кардиозащитными свойствами, улучшая показатели сердечной функции в нескольких исследованиях in vivo и подавляя пролиферацию раковых клеток (Locatelli и Rossoni, 1999, Endocrinol. 140: 4024-4031; Tivesten and Bollano, 2000, Endocrinol. 141: 60 -66; Cassoni et al., 2001, J. Clin. Endocrinol. Metab. 86: 1738-1745). Кроме того, они участвуют в таких процессах, как воспаление и старение (Hattori, 2009, J. Clin. Endocrinol. Metab. 86: 4284-4291).
Известно, что гексамер GHRP-6 (аминокислотная последовательность которого представляет собой His-D-Trp-Ala-Trp-D-Phe-Lys-NH2) является чрезвычайно мощным и безопасным химическим соединением, вызывая высвобождение соматотропного гормона у млекопитающих и птицы (Bowers et al., 1984, Endocrinol. 114: 1537-45), а также у ракообразных (Европейский патент NO:EP1477181 B1).
У животных моделей были описаны примеры противовоспалительного действия грелина (Smith et al., 2005, Trends Endocrinol. Metab. 16, 436-442). В большинстве этих исследований было высказано предположение, что использование ацилированного грелина подавляло экспрессию и/или выработку провоспалительных цитокинов, вне зависимости от патологии или дозы, и применяемой схемы лечения (Baatar et al., 2011, Molecular and Cellular Endocrinology 340: 44-58). Ранее выдвигались предроложения о его роли в снижении смертности и воспалительных эффектов, вызываемых липополисахаридами (ЛПС), как in vivo, так и in vitro, а также сепсиса у модельных грызунов (Dixit et al., 2004, J. Clin. Invest. 114: 57-66; Taub, 2007, Vitam. Horm. 77: 325-346).
В исследованиях, проводимых на мышиной модели хронического воспаления, грелин и синтетический агонист GHRP-2 значительно ингибировали высвобождение интерлейкина 6 (IL-6) и азотной кислоты из активированных макрофагов и ослабляли артрит (Granado et al., 2005, Am. J. Physiol. Endocrinol. Metab. 288: E486-E492). Кроме того, аналогичные исследования, которые были проведены, подтверждили противовоспалительные эффекты этих химических соединений (González-Rey et al., 2006, Gastroenterol. 130 (6), 1707-1720).
В работе, выполненной Lofti и сотрудниками в 2011 году (Lofti et al., 2011, Kafkas Univ Vet Fak Derg 17 (6): 949-952), инъекция грелина в яйцеклетку оказала влияние на количество лейкоцитов в крови недавно вылупившихся цыплят.При дозе 100 нг на 10-й день инкубации это привело к увеличению количества гетерофилов, базофилов и эозинофилов, а также к соотношения гетерофилов/лимфоцитов, в то же время это приводило к уменьшению количество лимфоцитов.
В случае костистых рыб исследования in vitro показали, что обработка лейкоцитов радужной форели (Oncorhynchus mykiss) грелином увеличивает продукцию супероксид-аниона, уровни рибонуклеиновой кислоты СТГ-мессенджера и супероксиддисмутазы в этих клетках (Yada et al., 2006, Endocrinol. 189: 57-65). В этом исследовании сообщалось, что предшествующая инкубация с антагонистом рецептора вещества, усиливающего секрецию соматотропного гормона, [D-Lys3]-GHRP-6, и иммуно-нейтрализация СТГ снижали выработку этих активных форм кислорода (O2•-), что свидетельствует о том, что действие грелина на лейкоциты опосредуются секрецией соматотропного гормона (Yada et al., 2007, Endocrinol. 152: 353-358). С другой стороны, исследования in vitro, проведенные с аналогом пептида GHRP-6, усиливающего секрецию соматотропного гормона, A233, показали, стимуляцию продуцирования индикаторов фагоцитарной активности, таких как супероксидный анион, в лейкоцитах тилапии (Oreochromis sp.) (Martínez et al., 2012, J. of Endocrinol. 214: 409-419). В том же исследовании было доказано, что введение А233 в иммерсионных ваннах стимулирует параметры антиоксидантной защиты с помощью фермента супероксиддисмутазы у личинок тилапии (Oreochromis sp.), а также титры лектина и антипротеазную активность. В других экспериментах, проведенных на молоди тилапии, перорально получавшей GHRP-6, наблюдалось увеличение титров лектина и количества интраэпителиальных лимфоцитов слизистой оболочки желудка (Martínez et al., 2016, Aquaculture 452 304-310). Этот последний параметр относится к врожденной иммунной системе, неспецифичен и не связан с введением определенного антигена.
Защитный иммунитет против различных патогенов требует ответов, которые могут быть получены с помощью соответствующего адъюванта вакцины (Awate et al., 2013, Frontiers in Immunology 4: 1-10). Поэтому необходимо выявить и разработать новые адъюванты, чтобы разрабатывать вакцины против патогенов, которые до сих пор были невосприимчивы к традиционным стратегиям вакцинации, и преодолеть ограничения нескольких доступных лицензированных адъювантов (Harandi et al., 2010, Vaccine 28(12): 2363-6; Pérez et al., 2012, Braz J Med Biol Res 45(8): 681-92).
Многие адъюванты потенцируют сильный неспецифичный воспалительный ответ, повышают иммуногенность совместно вводимых антигенов, но могут также вызывать нежелательные эффекты, в этих случаях необходимо разработать новые адъюванты, которые вызывают более специфичный и прямой иммунный ответ, чтобы получить оптимальную и безопасную защиту, обеспечиваемую вакцинами.
Подробное описание изобретения
Настоящее изобретение решает вышеупомянутую проблему, предлагая адъювант, способный эффективно усиливать иммунный ответ на совместно вводимый антиген. Настоящее изобретение относится к применению пептида, усиливающего секрецию соматотропного гормона, идентифицированного как SEQ ID NO: 1 (GHRP-6) или SEQ ID NO: 2 (A233), в качестве молекулярного адъюванта при изготовлении вакцины, которая применяется в различных стратегиях иммунизации. В одном варианте осуществления настоящего изобретения указанная вакцина используется для профилактики заболеваний, вызванных инфекционными агентами. В конкретном варианте осуществления изобретения эти заболевания поражают млекопитающих, птиц или рыб; и инфекционные агенты могут быть в числе прочего вирусами, бактериями и эктопаразитами.
В контексте настоящего изобретения термин «молекулярный адъювант» относится к веществу, способному положительно модулировать иммунный ответ против вакцинного антигена, что приводит к усилению этого ответа. На сегодняшний день нет исследований, демонстрирующих или предполагающих применение грелина или его аналогов в качестве молекулярного адъюванта. Напротив, было предложено применение грелина для лечения воспалительных заболеваний (González-Rey et al., 2006, Gastroenterology 130 (6), 1707-1720; Baatar et al., 2011, Mol Cell Endocrinol 340: 44-58). Принимая во внимание эту известную информацию, неожиданным является эффект, обнаруженный в настоящем изобретении, который демонстрирует, что введение GHRP-6 или A233 в комбинации с вакцинным антигеном стимулирует специфичный иммунный ответ против указанного антигена.
В другом варианте осуществления изобретения также описана вакцинная композиция, содержащая пептид, усиливающий секрецию соматотропного гормона, идентифицированный как SEQ ID NO: 1 (GHRP-6) или SEQ ID NO: 2 (A233), по меньшей мере, вакцинный антиген и фармакологически приемлемые носители или разбавители. Вакцинная композиция согласно настоящему изобретению может содержать другие химические соединения, которые действуют как вакцинные адъюванты, которые известны специалистам в данной области техники. В число этих адъювантов входят, например, соли алюминия и масляные адъюванты.
Чтобы проиллюстрировать различные варианты осуществления изобретения, вакцинные композиции, раскрытые в этих вариантах, включают различные антигены и пептиды GHRP-6 или A233. В число антигенов, которые комбинируются с GHRP-6 или его структурным аналогом A233, входят овальбумин (OVA), капсидный белок вируса Денге-2 (C2), пептид pP0 из Rhipicephalus sanguineus (Rodríguez-Mallón et al., 2012; Vaccine 30: 1782-1789), химерный белок P0-my32 (слитый полипептид двух антигенов Lepeophtheirus salmonis) и слитый полипептид P0 из L. salmonis и T-клеточных эпитопов (P0-TT). Не ограничивая настоящее изобретение, композиции вводили мышам, птицам и рыбам, и впервые был продемонстрирован адъювантный эффект для указанных пептидов, усиливающих секрецию соматотропного гормона. Неожиданно было обнаружено, что введение GHRP-6 или A233 в сочетании с антигеном повышает уровни антиген-специфичных антител у нескольких видов животных.
В одном варианте осуществления изобретения вакцинный антиген выбран из группы, состоящей из пептидов, белков, вирусов и аттенуированных бактерий. В одном предпочтительном варианте осуществления изобретения указанные вакцины вводят млекопитающим, птицам или рыбе. В более предпочтительном варианте осуществления изобретения вакцинную композицию настоящего изобретения вводят перорально или путем инъекции. В конкретном варианте осуществления изобретения в вакцинной композиции пептид SEQ ID NO: 1 или SEQ ID NO: 2 находится в концентрации 50-600 мкг/кг комбикорма, когда вакцина вводится перорально рыбам.
Настоящее изобретение также относится к способу усиления иммунного ответа против вакцинного антигена, который характеризуется введением эффективного количества пептида, усиливающего секрецию соматотропного гормона, идентифицированного как SEQ ID NO: 1 (GHRP-6) или SEQ ID NO: 2 (A233), в качестве молекулярного адъюванта указанных антигенов. В одном варианте осуществления изобретения вакцинный антиген используется для предотвращения заболеваний, вызываемых инфекционными агентами. В конкретном варианте осуществления указанного способа пептид с последовательностью SEQ ID NO: 1 или SEQ ID NO: 2 используют в дозе 50-600 мкг/кг комбикорма, когда вакцинный антиген и адъювантный пептид вводят перорально. В другом варианте осуществления указанного способа пептид с последовательностью SEQ ID NO: 1 или SEQ ID NO: 2, используют в дозе 0,1-40 мкг/г массы тела животного, если вакцинный антиген и пептид, действующий в качестве молекулярного адъюванта, вводят инъекцией. Для целей настоящего изобретения пептиды GHRP-6 и A233, известные как пептиды, усиливающего секрецию СТГ, получают химическим синтезом.
Как показано в различных вариантах осуществления изобретения, увеличение иммунного ответа против представляющего интерес антигена повышает уровень защиты от различных инфекционных агентов, включая вирусные, бактериальные и эктопаразитные возбудители.
Краткое описание чертежей.
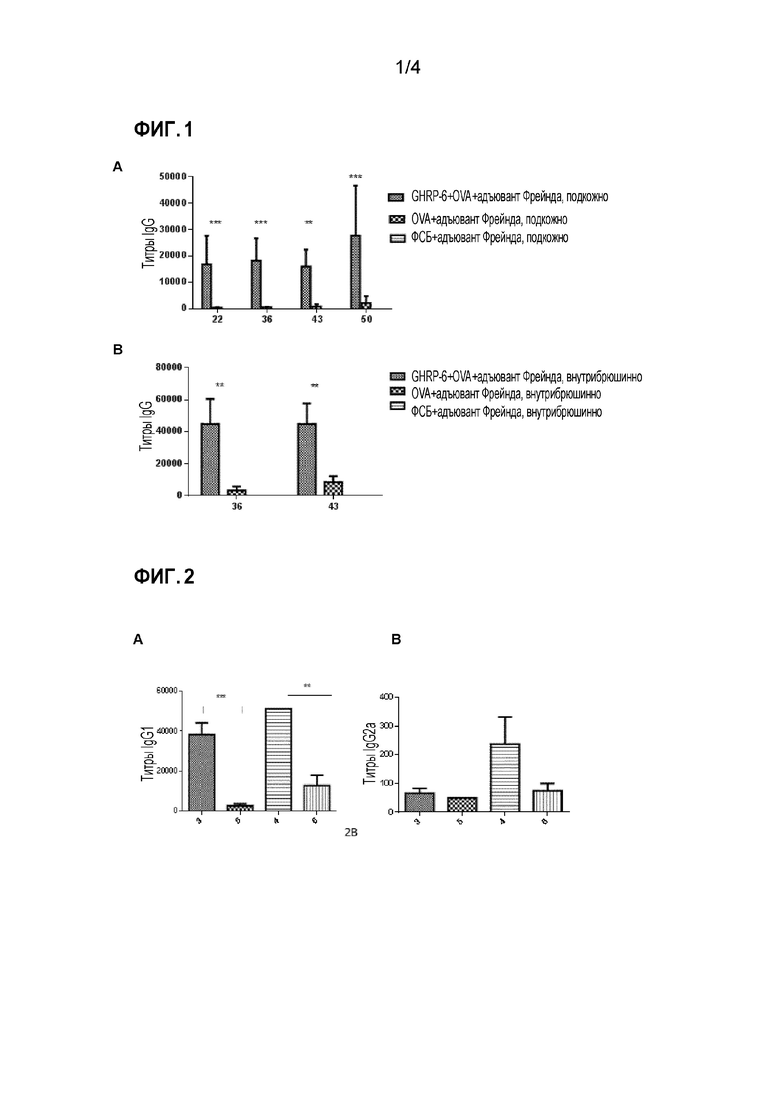
Фигура 1. Гуморальный ответ у мышей, иммунизированных OVA, GHRP-6 и адъювантом Фрейнда, или OVA и адъювантом Фрейнда. А. Титры иммуноглобулина G (IgG) в группах, иммунизированных подкожным путем (подкожно). B. Титры IgG в группах, иммунизированных внутрибрюшинным путем (внутрибрюшинно). Представлены медиана и стандартное отклонение в каждой группе. ** обозначает p<0,0014; *** обозначает p<0,001.
Фигура 2. Гуморальный ответ у мышей, иммунизированных OVA, GHRP-6 и адъювантом Фрейнда, подкожно и внутрибрюшинно. (Группы 3 и 4 соответственно); или OVA и адъювантом Фрейнда, подкожно и внутрибрюшинно (группы 5 и 6 соответственно). A. Титры IgG1. B. Титры IgG2a. Представлены медиана и стандартное отклонение в каждой группе. ** обозначает р<0,0014; *** обозначает р<0,001.
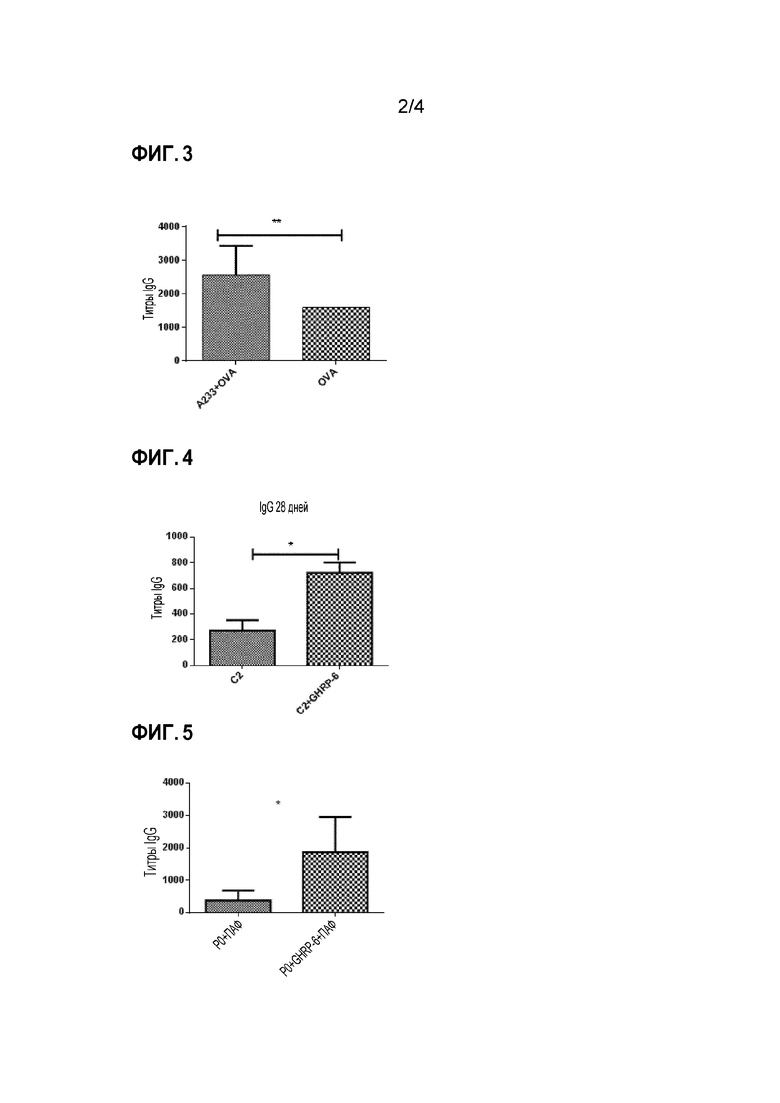
Фигура 3. Титры IgG у мышей, иммунизированных пептидом А233, OVA и адъювантом Фрейнда; или OVA и адъювантом Фрейнда, внутрибрюшинным способом. Показаны уровни антител, обнаруженных в сыворотке, полученной на 22-й день графика иммунизации. Представлены медиана и стандартное отклонение в каждой группе. ** обозначает р<0,0014.
Фигура 4. Титры IgG (обнаруженые на 28-й день графика иммунизации) в группах, иммунизированных С2 и алюминием; или C2, GHRP-6 и алюминием, подкожным способом. Представлены медиана и стандартное отклонение в каждой группе. * обозначает р<0,05.
Фигура 5. Титры IgG у мышей, иммунизированных Р0 и адъювантом Фрейнда; или P0, GHRP-6 и адъювантом Фрейнда, внутрибрюшинным способом в день 36 графика иммунизации. Представлены медиана и стандартное отклонение в каждой группе. * обозначает р<0,05.
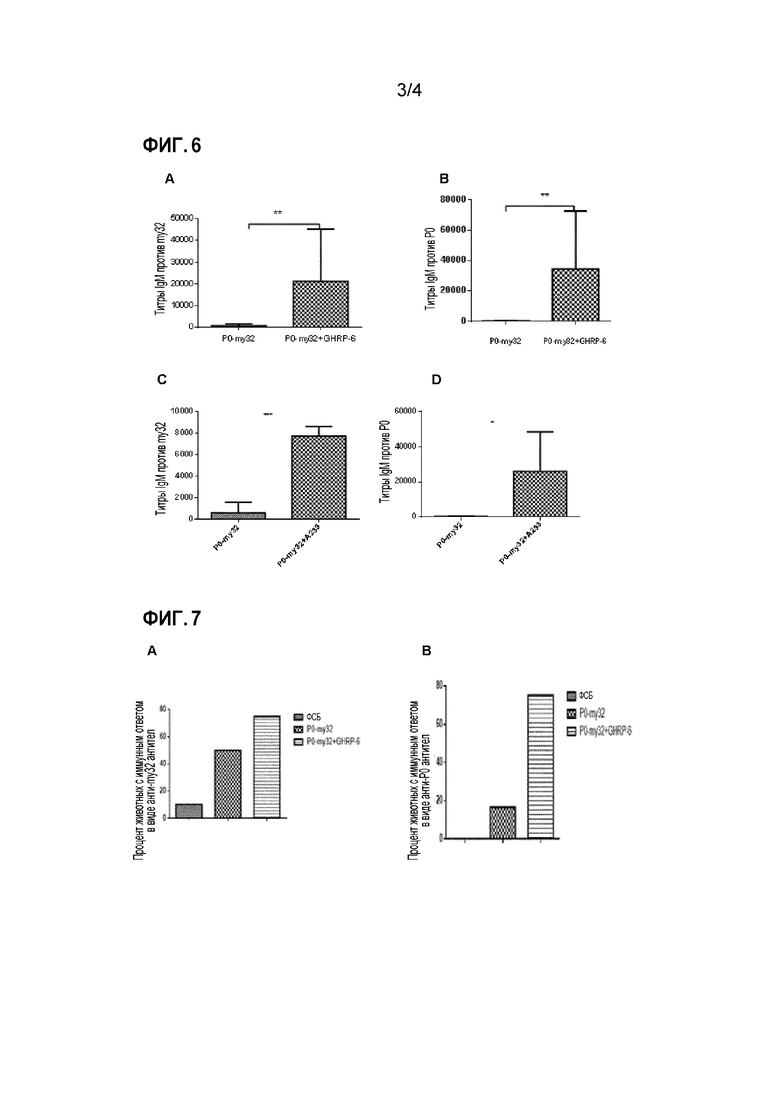
Фигура 6. Титры иммуноглобулина М (IgM) у тилапии, иммунизированной P0-my32 или P0-my32 в комбинации с GHRP-6 или пептидом A233, обнаруженные на 28-й день эксперимента, иммуногены вводили внутрибрюшинно. А. и С.Титры IgM против my-32. B и D. Титры IgM против P0. На А и В показаны титры у животных, получавших лечение с или без GHRP-6, а на С и D представлены титры у животных, получавших лечение с или без А233. Представлены медиана и стандартное отклонение в каждой группе. * обозначает р<0,01; ** обозначает р<0,0014; *** обозначает р<0,001.
Фигура 7. Процент тилапии с титрами IgM более 1:1000 после иммунизации препаратом P0-my32, включающим Montanide ISA 50 или P0-my32, включающим GHRP-6 и Montanide ISA 50, на 28-й день эксперимента. A. Процент животных, ответивших на анти-my32. B. Процент животных, ответивших на P0.
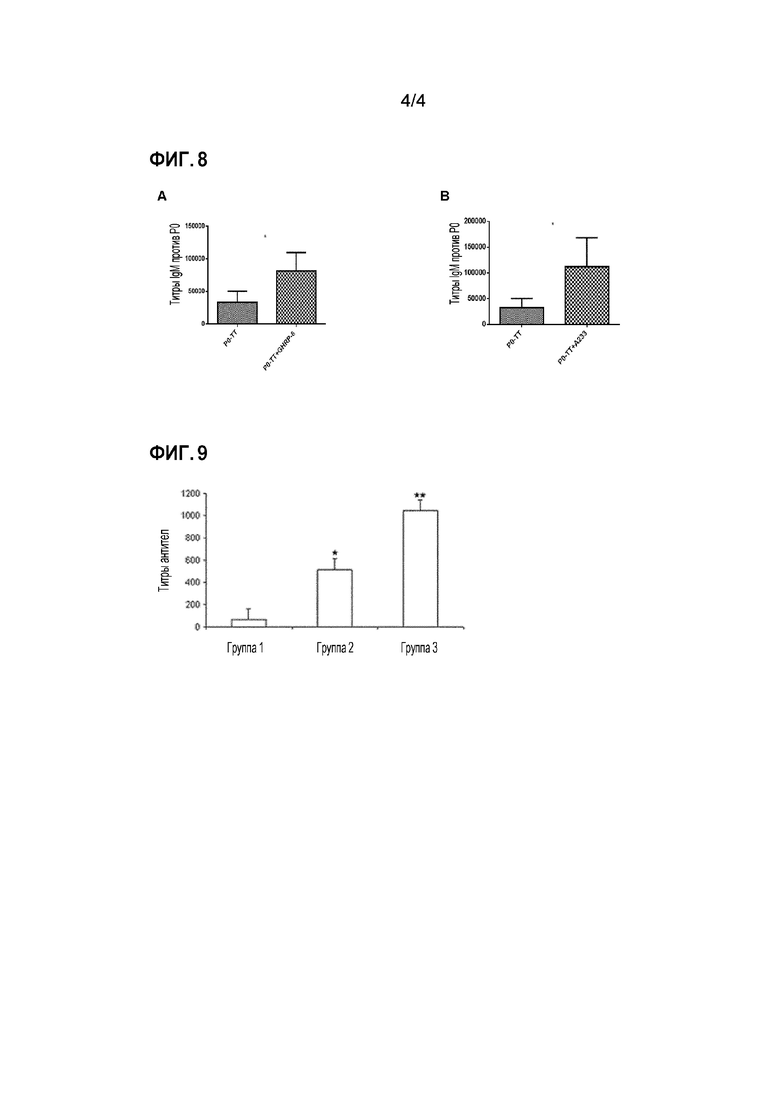
Фигура 8. Ответ антител IgM у клариевого сома, иммунизированного P0-TT или P0-TT в присутствии GHRP-6 или пептида A233, на 28-й день эксперимента, где рыбу иммунизировали внутрибрюшинно. А. Титры анти-Р0 антител в группах оценочного эксперимента с GHRP-6 в качестве адъюванта. B. Титры анти-P0 антител в группах оценочного эксперимента с A233 в качестве адъюванта. Все иммуногены были объединены с Montanide ISA 50.
Фигура 9. Титры агглютинирующих антител против Aeromonas hydrophila у карпа обыкновенного. Значения оси Y представляют медианное значение ± стандартную ошибку. * обозначает р<0,05; ** обозначает р<0,01. Группа 1: Инъекция ФСБ, Группа 2: инъекция инактивированных формалином клеток A. hydrophila, Группа 3: инъекция инактивированных формалином клеток A. hydrophila и GHRP-6 (20 мкг на рыбу). Все иммуногены были объединены с Montanide ISA 50.
Примеры
Пример 1. Влияние совместного введения GHRP-6 на гуморальный иммунный ответ против OVA
В этом эксперименте было использовано тридцать шесть самок мышей линии BALB/c. Животных распределили на шесть опытных групп по 6 животных в каждой. Три группы иммунизировали подкожно, а остальные - внутрибрюшинно. Во всех группах иммуногены эмульгировали с адъювантом Фрейнда.
Группа 1: Плацебо (фосфатно-солевой буфер, сокращенно ФСБ). подкожное введение.
Группа 2: Плацебо (ФСБ). внутрибрюшинное введение.
Группа 3: GHRP-6 в дозе 10 мкг/животное и OVA в дозе 5 мкг/животное. подкожное введение.
Группа 4: GHRP-6 в дозе 10 мкг/животное и OVA в дозе 5 мкг/животное. внутрибрюшинное введение.
Группа 5: OVA 5 мкг/животное. подкожное введение.
Группа 6: OVA 5 мкг/животное. внутрибрюшинное введение.
Мыши получали 150 мкл иммуногена во всех группах, которые вводили животным в дни 1 и 15 графика иммунизации. Забор крови проводили в дни 0 (неиммунная сыворотка), 8, 15, 22, 36, 43 и 50. Оценивали общие титры IgG, IgG1 и IgG2a. Полный адъювант Фрейнда (ПАФ) использовали при первой иммунизации, а неполный адъювант Фрейнда (НАФ) - при следующей иммунизации.
Животные группы, подкожно иммунизированной GHRP-6 и OVA, имели более высокие титры (со статистической значимостью: p<0,05), чем у животных, получавших OVA без GHRP-6 тем же путем, в дни 22, 36, 43 и 50 эксперимента (Фигура 1А). Животные, которым вводилм те же иммуногены, но внутрибрюшинным способом, имели такое же поведение на 36 и 43 дни эксперимента (Фигура 1В).
Титры IgG1 и IgG2a определяли в сыворотке, полученной на 36-й день, в группах, иммунизированных OVA с или без GHRP-6, подкожным и внутрибрюшинным способом. (Фигуры 2А и 2В). Не наблюдалось значимых различий в титрах IgG2a между группами, получавшими GHRP-6, и группами, которые не получали указанный пептид, усиливающий секрецию соматотропного гормона, для обоих способов введения (Фигура 2А и 2 В). Значимые различия наблюдались для IgG1 в случае обоих способов введения, будучи выше в группах, вакцинированных в присутствии GHRP-6.
Отношение IgG1/IgG2a как показатель дифференциальной реактивности к ответу Th2 или Th1, соответственно, было значительно выше в группе, иммунизированной внутрибрюшинным способом, с OVA в присутствии GHRP-6 и адъюванта Фрейнда, по сравнению с группой, которой вводили только OVA и адъювант Фрейнда. Это соотношение показано в таблице 1, где данные представляют собой среднее отношение IgG1/IgG2a, соответствующее шести животным в группе.
Таблица 1. Соотношение IgG1/IgG2a в обеих группах, иммунизированных внутрибрюшинным способом введения.
* означает значимые различия р<0,05.
Пример 2. Влияние совместного введения пептида A233 на гуморальный иммунный ответ против OVA.
Чтобы оценить, оказывает ли пептид A233 адъювантное действие на OVA, использовали 18 самок мышей линии BALB/c. Мыши получали 150 мкл иммуногена во всех группах внутрибрюшинным способом введения, которые давали животным в дни 1 и 15 графика иммунизации. Образцы крови отбирали в дни 0 (неиммунная сыворотка), 8, 15, 22, 36, 43 и 50. Оценивали титры общего IgG, присутствующего в сыворотке. Животных иммунизировали 5 мкг OVA/животное и 10 мкг A233/животное (Группа 2) или 5 мкг OVA/животное (Группа 3). Контрольной группе вводили ФСБ (Группа 1). Все иммуногены были эмульгированы с адъювантом Фрейнда.
У животных, которым инъецировали OVA и пептид A233, наблюдалось значительное увеличение титров анти-OVA-антител по сравнению с животными, иммунизированными только OVA, на 22-й день схемы иммунизации (Фигура 3).
Пример 3. Влияние совместного введения GHRP-6 на гуморальный иммунный ответ против антигена C2.
Антиген С2, капсидный белок вируса Денге, был получен в виде рекомбинантного белка в Escherichia coli с молекулярной массой 15 кДа. Для оценки гуморального и клеточного иммунного ответа у мышей, вакцинированных С2, в присутствии или в отсутствие GHRP-6 были отобраны 24 самки мышей линии BALB/c в возрасте 6 недель. Они были распределены на 3 группы. Каждое животное получало иммуноген согласно своей опытной группе:
Группа 1: 10 мкг С2
Группа 2: 10 мкг С2, вводимого совместно с 10 мкг GHRP-6.
Группа 3: ФСБ
Во всех группах иммуногены дополнительно содержали гидроксид алюминия, также известный как квасцы. Иммунизации проводили подкожным способом в дни 0, 15 и 30 графика иммунизации. Образцы крови отбирали в дни 0 (до иммунизации), 7, 16, 21, 28 и 35, чтобы оценить общие титры IgG.
На Фигуре 4 показано, что на 28-й день графика иммунизации группа 2, получавшая С2 и GHRP-6, показала значительное увеличение титра анти-С2 IgG по сравнению с группой 1, получавшей С2 и адъювантный гидроксид алюминия, без GHRP-6.
Пример 4. Влияние совместного введения GHRP-6 на гуморальный иммунный ответ против пептида P0 R. sanguineus.
Пептид P0 представляет собой фрагмент, соответствующий области меньшей идентичности по последовательности между рибосомальным белком P0 клеща R. sanguineus и его хозяином-млекопитающим. Для оценки гуморального иммунного ответа, стимулируемого совместным введением GHRP-6 и P0, было отобрано 24 самки мышей линии BALB/c 6-недельного возраста, которые были разделены на три группы по 8 мышей. Каждое животное получало 150 мкл иммуногена путем внутрибрюшинного введения в дни 1, 15 и 29 графика иммунизации. В первой иммунизации использовали ПАФ, а НАФ использовали в двух других введениях.
Группа 1. Контроль (ФСБ)
Группа 2. 100 мкг Р0.
Группа 3. 100 мкг P0 совместно вводили с 200 мкг GHRP-6.
Образцы крови отбирали в дни 0 (неиммунная сыворотка), 8, 16, 21, 28, 36, 43, 50 и 58, чтобы определить уровни общего IgG. У животных, иммунизированных P0, в присутствии GHRP-6 наблюдалось значительное увеличение титров IgG по сравнению с животными, которые не получали GHRP-6, как видно на Фигуре 5, где показано уровни анти-P0 антитела на 36 дней графика иммунизации.
Пример 5. Влияние совместного введения GHRP-6 или пептида A233 на гуморальный иммунный ответ против белка P0-my32 у тилапии (Oreochromis sp.)
Химерный белок P0-my32 был получен путем клонирования комплементарной дезоксирибонуклеиновой кислоты (кДНК), кодирующей 35-аминокислотный пептид рибосомального белка P0 L. salmonis, слитой с N-концевым концом кДНК, кодирующей белок my32 того же эктопаразита (Carpio et al., 2013; Exp. Parasitol 135: 188-199), в вектор, предназначенный для индуцированной экспрессии представляющих интерес генов в бактерии-хозяине E.coli. Этот белок был синтезирован в бактерии и очищен в виде слитого белка с гистидиновой меткой с помощью аффинной хроматографии с хелатом металла.
Для выполнения эксперимента по иммунизации были сформированы 6 опытных групп мальков мужского пола Oreochromis niloticus, по 15 животных в каждой. Во всех группах иммуноген вводили внутрибрюшинно с Montaide ISA 50 в качестве адъюванта. Опытные группы получали следующие иммуногены:
Группа 1: ФСБ
Группа 2: P0-my32 (1 мкг/г веса рыбы)
Группа 3: P0-my32 (1 мкг/г веса рыбы) совместно с 20 мкг GHRP-6
Группа 4: P0-my32 (1 мкг/г веса рыбы) совместно с 20 мкг A233
Группа 5: P0-my32 (1 мкг г веса рыбы). Рыбу в этой группе кормили комбикормом, содержащим 100 мкг GHRP-6 на кг корма, два раза в день, за одну неделю до и одну неделю после инъекционного введения my32.
В ходе эксперимента рыбу в группах 1-4 кормили два раза в день сбалансированным коммерческим комбикормом, не содержащим лекарственных препаратов, из расчета 1% от их массы тела. Иммунизации проводили в дни 0 и 14 графика. Образцы крови отбирали в дни 0, 21, 28 и 35 от начала эксперимента.
У тилапии, инъецированной P0-my32 в присутствии GHRP-6, наблюдалось увеличение титров антител IgM против my32 по сравнению с группой, инъецированной P0-my32. Это увеличение было статистически значимым, как показано на Фигуре 6А, где показаны уровни антител в сыворотках, выделенных на 28 день. Такой же эффект наблюдался для титра анти-P0 IgM (Фигура 6 В). Совместное введение А233 с химерным антигеном также позволило увеличить титры IgM по отношению к двум компонентам по сравнению с контрольной группой (Фигуры 6С и 6D). Группа, которой вводили P0-my32 и одновременно давали комбикорм, содержащий GHRP-6, также показала увеличение титров по сравнению с группой, которой вводили химерный белок, которой давали немодифицированный корм (Таблица 2).
Таблица 2. Влияние совместного введения GHRP-6 в корм на титры анти-my32 и анти-P0 IgM
* означает значимые различия между группами р<0,05.
Кроме того, в группе, которой вводили содержащий GHRP-6 иммуноген путем внутрибрюшинной инъекции, (Группа 3), число отвечающих на вакцинацию животных с титрами IgM более 1:1000 было выше для обоих компонентов химерного белка по сравнению с группой, получавшей P0-my32, но не получавшей пептид GHRP-6 (Группа 2). Это видно на Фигурах 7А и 7 В.
Пример 6. Влияние совместного введения GHRP-6 или A233 и белка P0-TT на гуморальный иммунный ответ у клариевого сома (Clarias gariepinus).
Химерный белок P0-TT основан на: a) пептиде pP0, состоящем из 35 аминокислот, соответствующих области, менее консервативной между рибосомальным белком P0 L. salmonis и тем же белком в одном из его хозяев, Salmo salar и b) двух Т-клеточных эпитопах, происходящих из вируса кори и столбнячного анатоксина, соответственно. Для эксперимента были сформированы 4 опытных группы C. gariepinus, по 12 животных в каждой. Этих животных внутрибрюшинно иммунизировали 1 мкг белка P0-TT на грамм веса животного (Группа 2) или той же дозой химерного белка P0-TT (1 мкг/г веса животного), вводимыми одновременно с 20 мкг или GHRP-6 или A233 на животное (Группы 3 и 4 соответственно), в общем объеме 120 мкл. Контрольная группа (Группа 1) получала такой же объем ФСБ. Иммуногены, соответствующие всем группам, эмульгировали с масляным адъювантом Montanide ISA 50. Иммунизацию проводили в тех же условиях, в дни 0 и 14 графика введения. Образцы крови брали в дни 0, 21, 28 и 35, от начала эксперимента.
У клариевых сомов, иммунизированных P0-TT и GHRP-6, наблюдалось увеличение титров антител против P0 IgM по сравнению с группой, которой вводили P0-TT без пептида GHRP-6, что имело статистическую значимость на 28 день (Фигура 8А). Тот же эффект наблюдался для титров, полученных после введения P0-TT и A233 (Фигура 8B).
Пример 7. Демонстрация адъювантного действия GHRP-6 на гуморальный иммунный ответ карпа обыкновенного (Cyprinus carpio) против бактерии Aeromonas hydrophila.
Эксперимент проводили с карпами (C. carpio) массой 40±10 г. Эти животные содержались в 600-литровых аквариумах при температуре 28±2°C. Были сформированы три опытные группы по 10 карпов в каждой, которым внутрибрюшинно вводили следующие иммуногены:
Группа 1: ФСБ+Montanide ISA 50.
Группа 2: Инактивированные клетки A. hydrophila (1×108 колониеобразующих единиц, сокращенно КОЕ)+Montanide ISA 50.
Группа 3: Инактивированные клетки A. hydrophila (1×108 КОЕ)+20 мкг GHRP-6/на рыбу + Montanide ISA 50.
Рыбу инъецировали в дни 0 и 14, и образцы крови брали из хвостовой вены в дни 0 и 21. Результаты показали, что титры агглютинирующих антител против A. hydrophila были значительно выше в группе, иммунизированной бактерией и GHRP-6, по сравнению с группой, иммунизированной бактерией без пептида GHRP-6 (Фигура 9). Эти результаты подтверждают действие GHRP-6 в качестве молекулярного адъюванта у рыб. Получение клеток A. hydrophila и измерение титров антител проводили в соответствии с ранее описанной методикой (Yin et al. ((1996) Fish & Shellfish Immunol. 6, 57-69).
Пример 8. Эксперимент с контролируемым заражением на рыбах, иммунизированных инактивированной бактерией Aeromonas hydrophila и инактивированной бактерией, вводимой совместно с пептидом GHRP-6.
Эксперимент проводили с обыкновенным карпом (C. carpio) массой 30±5 г. Эти животных содержали в 250-литровых аквариумах при температуре 30±2°C. Были сформированы три опытные группы, по 20 карпов в каждой, и животным внутрибрюшинно вводили:
Группа 1: ФСБ + Montanide ISA 50
Группа 2: Инактивированные клетки A. hydrophila (1×108 КОЕ) + Montanide ISA 50
Группа 3: Инактивированные клетки A. hydrophila (1×108 КОЕ) + 20 мкг GHRP-6/ на рыбу + Montanide ISA 50.
Рыбу инъецировали в дни 0 и 14. Заражение проводили на 21 день путем внутрибрюшинной инъекции летальной дозы 50 (ЛД50) бактерии, и смертность в каждой группе регистрировали в течение 7 дней. Относительную выживаемость (ОВ) рассчитывали как:
ОВ(%) = (% смертности в контроле - % смертности иммунизированных животных)/(% смертности в контроле)×100.
В результате 65% ОВ было получено в Группе 2 и 95% ОВ в Группе 3, демонстрируя, что введение GHRP-6 увеличивает выживаемость у рыб, вакцинированных и зараженных патогеном.
Пример 9. Демонстрация адъювантного действия GHRP-6 на гуморальный иммунный ответ цыплят на бычий сывороточный альбумин.
В этом эксперименте использовали пятнадцать новорожденных цыплят-бройлеров, гибрида EB34 Cronish × White Plymoth Rock, и они были разделены на три опытные группы по 5 животных в каждой. Животных иммунизировали внутрибрюшинным способом, на 12 и 18 дни схемы иммунизации, 5 мкг БСА на животное (Группа 2) или 5 мкг БСА и 20 мкг GHRP-6 на животное (Группа 3). Контрольная группа (Группа 1) была иммунизирована ФСБ. Уровни антител IgY в сыворотке крови определяли на 25 день эксперимента. Были выявлены статистически значимые различия между титрами антител у животных из группы, иммунизированной БСА, и группы, получавшей БСА и GHRP-6 (Таблица 3).
Таблица 3. Ответ антиген-специфичных антител IgY в сыворотке крови кур, иммунизированных БСА.
Данные показывают среднее и стандартное отклонение максимальных значений оптической плотности, определенных методом непрямого ИФА.
--->
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> CENTRO DE INGENIERIA GENETICA Y BIOTECNOLOGIA
<120> Применение пептида, усиливающего секрецию соматотропного
гормона, в качестве адъювант вакцины
<130> Адъюванты, усиливающие секрецию соматотропного гормона
<140>
<141>
<150> CU 2016-0161
<151> 2016-11-01
<160> 2
<170> Патентная версия 2.1
<210> 1
<211> 6
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: GHRP-6,
Trp(2) и Phe(5) являются D-аминокислотами
<220>
<221> Модифицированные_остатки
<222> (6)
<223> Амидирование
<400> 1
His Trp Ala Trp Phe Lys
1 5
<210> 2
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: пептид
A233, содержит лактамную связь между Lys и Asp
<400> 2
Gly Lys Phe Asp Leu Ser Pro Glu His Gln
1 5 10
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| ВАКЦИННАЯ КОМПОЗИЦИЯ ДЛЯ БОРЬБЫ С ЗАРАЖЕНИЯМИ ЭКТОПАРАЗИТАМИ | 2011 |
|
RU2585226C2 |
| ПРИМЕНЕНИЕ РАСАР В КАЧЕСТВЕ МОЛЕКУЛЯРНОГО АДЪЮВАНТА ДЛЯ ВАКЦИН | 2012 |
|
RU2580294C2 |
| АМИНОКИСЛОТНЫЕ ПОСЛЕДОВАТЕЛЬНОСТИ ДЛЯ КОНТРОЛЯ ПАТОГЕНОВ | 2012 |
|
RU2636001C2 |
| ХИМЕРНЫЕ АНТИГЕНЫ ДЛЯ ВАКЦИНЫ ПРОТИВ ВИРУСА ГЕПАТИТА С | 2013 |
|
RU2639504C2 |
| СПОСОБ ДЛЯ ПРИМЕНЕНИЯ В ТЕРАПИИ | 2010 |
|
RU2579659C2 |
| ИММУНОСТИМУЛИРУЮЩИЕ ОЛИГОНУКЛЕОТИДЫ | 2009 |
|
RU2477753C2 |
| Иммуностимулирующие олигонуклеотиды | 2012 |
|
RU2610690C2 |
| УСИЛЕНИЕ ИММУННОГО ОТВЕТА И НАПРАВЛЕННОСТИ НА МИШЕНЬ С ПОМОЩЬЮ АНТИГЕНОВ И/ИЛИ ЛЕКАРСТВА | 2008 |
|
RU2548685C2 |
| ИММУНОГЕННАЯ КОМПОЗИЦИЯ LHRH И ЕЕ ПРИМЕНЕНИЕ У СВИНЕЙ | 2014 |
|
RU2745720C2 |
| ПЕПТИДНАЯ ВАКЦИНА ДЛЯ ПРЕДУПРЕЖДЕНИЯ И ИММУНОТЕРАПИИ ДЕМЕНЦИИ АЛЬЦГЕЙМЕРОВСКОГО ТИПА | 2013 |
|
RU2696566C2 |
Изобретение относится к применению GHRP-6 и его структурного аналога в качестве молекулярных адъювантов для вакцин. Вакцины могут быть использованы для профилактики заболеваний, вызываемых инфекционными агентами, такими как вирусы, бактерии и эктопаразиты, которые поражают млекопитающих, птиц и водные организмы. GHRP-6 и его аналог A233 эффективны в качестве адъювантов, когда они комбинируются с данным антигеном, так как они усиливают специфичный иммунный ответ против него. 3 н. и 6 з.п. ф-лы, 9 ил., 3 табл., 9 пр.
1. Применение пептида, усиливающего секрецию соматотропного гормона, идентифицированного как SEQ ID NO: 1 или SEQ ID NO: 2, в качестве молекулярного адъюванта в получении вакцины для профилактики заболеваний, вызываемых инфекционными агентами, которые поражают млекопитающих, птиц или рыб.
2. Вакцинная композиция для профилактики заболеваний, вызываемых инфекционными агентами, которые поражают млекопитающих, птиц или рыб, содержащая пептид, усиливающий секрецию соматотропного гормона, идентифицированный как SEQ ID NO: 1 или SEQ ID NO: 2, в качестве молекулярного адъюванта, по меньшей мере один вакцинный антиген и фармакологически приемлемые носители или разбавители.
3. Композиция по п.2, где вакцинный антиген выбран из группы, состоящей из пептидов, белков, вирусов и аттенуированных бактерий.
4. Композиция по п.3, которую вводят перорально или путем инъекции.
5. Композиция по п.4, где пептид с последовательностью SEQ ID NO: 1 или SEQ ID NO: 2 находится в концентрации 50-600 мкг/кг комбикорма, когда вакцина вводится перорально рыбам.
6. Способ усиления иммунного ответа против вакцинного антигена, где эффективное количество пептида, усиливающего секрецию соматотропного гормона, идентифицированного как SEQ ID NO: 1 или SEQ ID NO: 2, вводят в качестве молекулярного адъюванта указанного антигена, и где вакцинный антиген и указанные пептиды, усиливающие секрецию соматотропного гормона, присутствуют в одной и той же вакцинной композиции.
7. Способ по п.6, где вакцинный антиген используется для профилактики заболеваний, вызываемых инфекционными агентами, которые поражают млекопитающих, птиц или рыб.
8. Способ по п.6, где пептид с последовательностью SEQ ID NO: 1 или SEQ ID NO: 2 используют в дозе 50-600 мкг/кг комбикорма, когда вакцинный антиген и адъювантный пептид вводят перорально.
9. Способ по п.6, где пептид с последовательностью SEQ ID NO: 1 или SEQ ID NO: 2 используют в дозе 0,1-40 мкг/г массы тела животного, если вакцинный антиген и пептид, действующий в качестве молекулярного адъюванта, вводят инъекцией.
| WO 2012041981 A2, 05.04.2012 | |||
| СОЕДИНЕНИЯ, ПРЕДСТАВЛЯЮЩИЕ СОБОЙ ПЕПТИДНЫЕ АНАЛОГИ СТИМУЛЯТОРОВ СЕКРЕЦИИ ГОРМОНА РОСТА, И СОДЕРЖАЩИЕ ИХ ПРЕПАРАТЫ | 2007 |
|
RU2416618C2 |
| REBECA MARTINEZ ET AL, "Comparative proteomic analysis of growth hormone secretagogue A233 treatment of murine macrophage cells J774A.2 indicates it has a role in antiviral innate response", BIOCHEMISTRY AND BIOPHYSICS REPORTS, 2016-03-01, vol | |||
| Кипятильник для воды | 1921 |
|
SU5A1 |
| REBECA MARTINEZ ET AL, | |||
Авторы
Даты
2022-03-23—Публикация
2017-10-30—Подача