Область техники
Настоящее изобретение относится к области биотехнологии, в частности к получению антимикробных пептидов и их применению для борьбы с патогенами. Применение антимикробных пептидов позволяет эффективно бороться с заболеваниями, вызванными патогенами. Более того, такие пептиды усиливают иммунный ответ, индуцированный различными антигенами, входящими в состав вакцин.
Предшествующий уровень техники
Рыбы обладают мощной системой врожденного иммунитета, которая первой включается в борьбу с широким спектром патогенов (Subramanian et al. (2008) Fish and Shellfish Immunol. 25:625-632), а также слабо развитой адаптивной иммунной системой (Magnadottir, (2010) Mar Biotechnol. 12:361-379). Одним из способов, который применяют рыбы для борьбы с патогенами, является секреция антимикробных пептидов (АМП), представляющая собой один из механизмов врожденного иммунитета. АМП лежат в основе системы врожденного иммунитета и защищают от разнообразных бактерий, грибков, вирусов и других патогенов, вызывающих инфекционные заболевания (Solomon, (2008) Lancet Neurol. 7:116-118). Обычно АМП секретируются в слюну, слизь, кровоток и в другие области, которые являются мишенями патогенов (Noga et al. (2010) Comp Biochem Physiol D: Genom Proteom. 6:44-54).
АМП подразделяются на пять категорий в зависимости от аминокислотного состава и структуры. Категории включают в себя анионные пептиды, линейные пептиды с амифифильной α-спиральной структурой, катионные пептиды, обогащенные специфическими аминокислотами, пептидные фрагменты и пептиды с остатками цистеина, которые образую внутримолекулярные связи (Brogden (2005) Nat Rev Microbiol. 3:238-50; Boman (2000) Immunol Rev. 173:5-16). Анионные пептиды образуются в милимолярных количествах, используют цинк в качестве кофактора и проявляют антимикробную активность в отношении грамположительных и грамотрицательных бактерий. Линейные и катионные пептиды с амфифильной α-спиралью состоят из менее чем 40 аминокислотных остатков и имеют трехмерную структуру с шарнирной областью посередине. Будучи неструктурированными в растворе, эти молекулы формируют вторичную структуру в виде α-спирали при контакте с мембранами (Brogden (2005) Nat Rev Microbiol. 3:238-50). Пептиды из другой группы, состоящей из линейных катионных пептидов, обогащенных специфическими аминокислотами, не содержат остатков цистеина и благодаря этому обладают очень гибкой структурой в растворе (Brogden (2005) Nat Rev Microbiol. 3:238-50). Четвертая группа объединяет заряженные пептиды, представляющие собой фрагменты более крупных белков. Такие пептиды проявляют антимикробную активность и обладают структурой, схожей с таковой в других группах пептидов (Bellamy et al. (1992) J Appl Bacteriol. 73:472-9; Zanetti et al. (1995) FEBS Lett. 374:1-5). Пятая группа включает приблизительно 380 пептидов, которые содержат шесть консервативных остатков цистеина, формирующих внутримолекулярные связи и структуру β-слоя (Brogden (2005) Nat Rev Microbiol. 3:238-50). В эту группу входят дефензины и гепсидин (Boman et al. (2000) Immunol Rev. 173:5-16).
В то время как АМП обычно классифицируют на основании структурных отличий, существует несколько характеристик, общих для этих пептидов. Так, например, длина пептидов обычно не превышает 60 аминокислот, пептиды обладают широким спектром антимикробной активности в физиологических условиях и заряжены положительно (Zasloff (2002) Nature 415:389-395). Большинство амфифильных АМП формируют структуру, которая обусловливает механизм их действия, основанный на взаимодействии с липидами клеточной мембраны таких патогенов, как бактерии и оболочечные вирусы (Shai (2002) Biopolymers 66: 236-48; Jelinek and Kolusheva (2005) Curr. Protein Pept. Sci. 6: 103-14). Такое взаимодействие вызывает быструю дестабилизацию/пермеабилизацию липидной мембраны патогенов. Некоторые наблюдения позволяют предположить, что механизм действия АМП, кроме формирования пор, может быть связан с ингибированием синтеза клеточной стенки, нуклеиновых кислот и белков и даже с ингибированием активности ферментов (Brogden et al. (2005) Nat. Immunol. 6: 558-64; Campagna et al. (2007) Biochemistry 46: 1771-8).
Способность микроорганизмов развивать устойчивость к антибиотикам и существование заболеваний, вызываемых патогенами, для которых отсутствует адекватное лечение, делают необходимым поиск новых молекул, обладающих антимикробной активностью.
Таким образом, важной проблемой, которую необходимо решить, является разработка новых антимикробных продуктов, в частности белков и/или пептидов, способных эффективно бороться с широким спектром патогенов и влияющих на врожденный и приобретенный иммунитет, которые представляют собой важные аспекты с точки зрения медицины человека и ветеринарии, в том числе аквакультуры.
Подробное описание изобретения
Настоящее изобретение решает описанную выше проблему, предлагая новый вариант лечения и борьбы с инфекциями, вызванными патогенами, в том числе бактериями, вирусами и грибками. Настоящее изобретение впервые описывает антимикробные пептиды, определяемые SEQ ID NO: 1, 2 и 3. Также предметом изобретения являются аминокислотные последовательности, содержащие аминокислотные последовательности, описанные SEQ ID NO: 1, 2 и 3, или аминокислотную последовательность, с по меньшей мере 80% идентичностью с пептидами, описанными SEQ ID NO: 1, 2 и 3.
Три пептида были выделены и секвенированы из белкового экстракта жабр тилапии (Oreochromis niloticus) и названы Ореохромицин I, Ореохромицин II и Ореохромицин III. Эти пептиды ранее не были описаны в литературе, и в настоящем изобретении обозначены как SEQ ID NO: 1, 2 и 3. Указанные пептиды обладают антимикробной активностью в отношении грамположительных бактерий, грамотрицательных бактерий, вирусов и грибков. Пептиды, являющиеся предметом настоящего изобретения, могут быть получены при выделении из их естественного источника. Кроме того, пептиды могут быть получены в результате химического синтеза или при применении технологии рекомбинантных дезоксирибонуклеиновых кислот (ДНК).
В одном из вариантов осуществления данного изобретения антимикробные пептиды получают в результате рекомбинантной экспрессии в бактериях, дрожжах или клетках высших организмов. Такие антимикробные пептиды можно экспрессировать в разных хозяйских системах и затем выделить из них. В конкретном случае осуществления изобретения антимикробные пептиды можно экспрессировать в дрожжах. В предпочтительном варианте осуществления экспрессия с применением технологии рекомбинантных ДНК осуществляется в Pichia pastoris, предпочтительно в культуральном супернатанте. Антимикробные пептиды, являющиеся предметом настоящего изобретения, также можно экспрессировать в бактериях. В другом предпочтительном варианте осуществления изобретения экспрессия с применением технологии рекомбинантных ДНК осуществляется в Escherichia coli. Пептиды, являющиеся предметом настоящего изобретения, можно получить, применяя способы выделения белков из хозяев, которые широко известны специалистам в данной области техники и включают хроматографические методы, промывку осадка и другие.
Применение антимикробных пептидов имеет преимущества по сравнению с другими антимикробными агентами из-за небольшого размера антимикробных пептидов (~5 кДа), их лучшей адсорбции через кожу и слизь водных организмов при применении в виде иммерсии, что является экономически выгодным способом введения препаратов в аквакультуре, а также из-за низкого уровня загрязнения окружающей среды. Другим преимуществом является способность антимикробных пептидов стимулировать активность врожденного и приобретенного иммунитета и увеличивать сопротивляемость инфекциям, вызванным патогенными агентами.
На основании аминокислотной последовательности каждого пептида были разработаны вырожденные олигонуклеотиды для амплификации с помощью полимеразной цепной реакции (ПЦР) нуклеотидных последовательностей, кодирующих каждый зрелый пептид. Таким образом, другим предметом настоящего изобретения является нуклеиновая кислота, которая содержит последовательность нуклеиновой кислоты из группы, состоящей из SEQ ID NO: 4, 5 и 6.
Другим предметом настоящего изобретения является нуклеиновая кислота, кодирующая пептиды, содержащие аминокислотные последовательности, описанные SEQ ID NO: 1, 2 и 3, или аминокислотную последовательность с по меньшей мере 80% идентичностью с пептидами, описанными SEQ ID NO: 1, 2 или 3.
Настоящее изобретение также описывает композицию для борьбы с патогенами, содержащую пептиды, описанные SEQ ID NO: 1, 2 и 3, или пептиды с по меньшей мере 80% идентичностью с пептидами, описанными SEQ ID NO: 1, 2 или 3.
В одном из вариантов осуществления данного изобретения антимикробные пептиды с заявленными последовательностями (и содержащие их композиции) могут применяться для борьбы с широким спектром патогенов, в том числе бактериальных патогенов (Aeromonas, Pseudomonas, Corynebacteria, Enterobacteria, Haemophilus, Mycobacteria, Nocardia, Myxobacteria, Streptomyces, Vibrio и других); вирусных патогенов (вируса инфекционного некроза гемопоэтической ткани, вируса инфекционного некроза поджелудочной железы, вируса геморрагической септицемии, иридовируса, вируса геморрагии карпа, вируса весенней виремии карпа, рабдовируса Hirame или рабдовируса Snakehead, вируса лимфоцистоза, вируса инфекционной анемии лососевых и других), грибков и оомицетов (Saprolegnia, Achlya, Ychthyosporidium hoferi и других).
В одном из способов осуществления изобретения пептиды Ореохромицин I, Ореохромицин II и Ореохромицин III, а также пептиды, имеющие 80% идентичность с ними, входят в состав композиций, применяемых для борьбы с патогенами в разных организмах, в том числе в млекопитающих и водных организмах. Такие композиции вводят для борьбы с патогенами как в профилактических, так и в терапевтических целях. Способы введения включают все способы, применяемые для введения лекарственных препаратов человеку и для введения препаратов и добавок животным, которые широко известны специалистам в данной области техники. В одном из вариантов осуществления изобретения композиции для борьбы с патогенами вводят перорально, парентерально или в виде иммерсионных ванн.
Также аспектом данного изобретения является применение пептида, содержащего аминокислотную последовательность из группы, состоящей из SEQ ID NO: 1, SEQ ID NO: 2 и SEQ ID NO: 3, или аминокислотную последовательность с по меньшей мере 80% идентичностью с SEQ ID NO: 1, SEQ ID NO: 2 или SEQ ID NO: 3, для производства композиции для борьбы с патогенами.
Другим аспектом изобретения является описание способа борьбы с патогенами, заражающими несколько организмов, который характеризуется введением эффективного количества пептида, содержащего аминокислотную последовательность из группы, состоящей из SEQ ID NO: 1, SEQ ID NO: 2 и SEQ ID NO: 3, или аминокислотную последовательность, с по меньшей мере 80% идентичностью с SEQ ID NO: 1, SEQ ID NO: 2 или SEQ ID NO: 3, указанным организмам.
В конкретном случае осуществления изобретения пептиды, являющиеся предметом настоящего изобретения, вводят рыбам в виде периодических инъекций в концентрации от 0,1 до 10 мкг на рыбу; в виде иммерсионных ванн с интервалом 1-15 дней (каждый день или через день) в пресной или в морской воде при концентрации пептида от 0,01 до 0,1 мг/л воды. Также пептиды можно давать в виде добавок к корму рыб в концентрации около 50-750 мкг/кг корма. Во всех случаях достигается значительное увеличение сопротивляемости заболеваниям, вызванных патогенами, в том числе вирусами, бактериями, грибками и другими.
Кроме того, настоящее изобретение описывает пептиды, которые могут быть применены в качестве молекулярных адъювантов вакцин. В контексте настоящего изобретения термин «молекулярный адъювант» относится к белковой молекуле, способной модулировать иммунный ответ на антиген вакцины, вызывая усиление иммунного ответа.
Таким образом, изобретение также включает композицию вакцины, содержащую пептид, включающую аминокислотную последовательность из группы, состоящей из SEQ ID NO: 1, SEQ ID NO: 2 и SEQ ID NO: 3, или аминокислотную последовательность с по меньшей мере 80% идентичностью с SEQ ID NO: 1, SEQ ID NO: 2 или SEQ ID NO: 3, в качестве молекулярного адъюванта и антигена вакцины.
Другим аспектом изобретения является описание способа повышения иммунного ответа на антиген вакцины с применением пептида, содержащего аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 1, SEQ ID NO: 2 и SEQ ID NO: 3, или аминокислотную последовательность с по меньшей мере 80% идентичностью с SEQ ID NO: 1, SEQ ID NO: 2 или SEQ ID NO: 3, в качестве молекулярного адъюванта вакцины.
Краткое описание чертежей
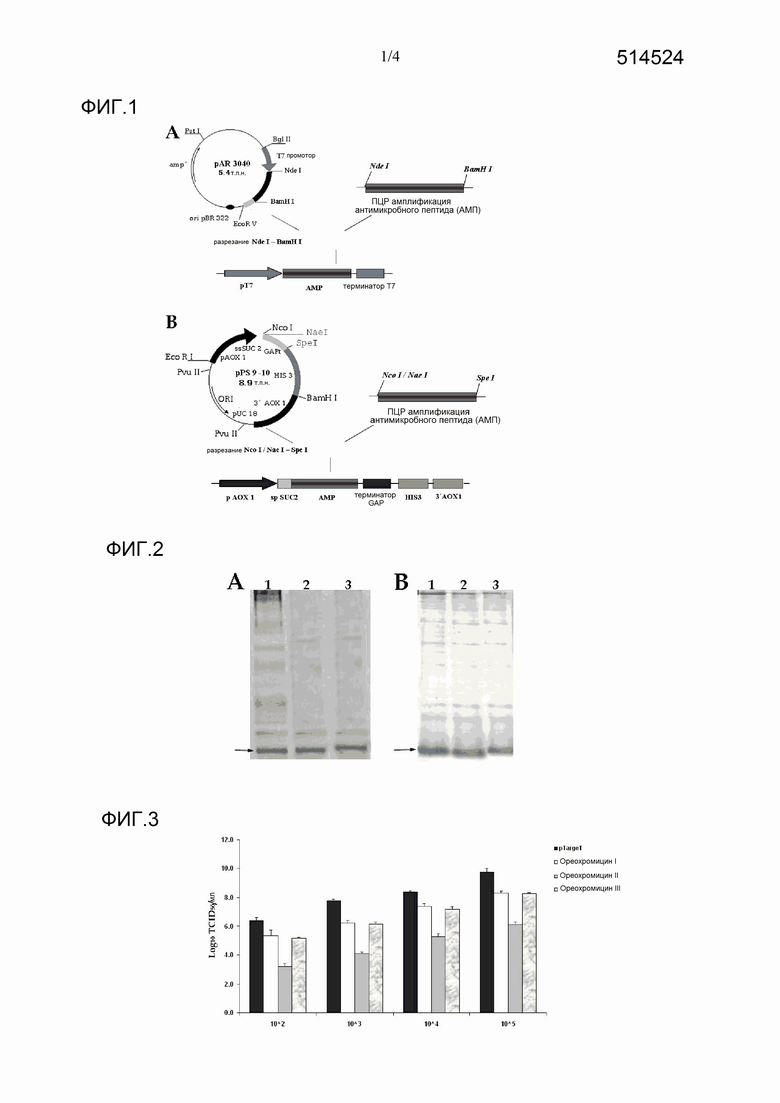
Фигура 1. Схема клонирования антимикробных пептидов в экспрессионные векторы для Е. coli (Фиг. 1А) и для дрожжей Р. pastoris (Фиг. 1В).
Фигура 2. Очистка антимикробных пептидов из культурального супернатанта P. pastoris (Фиг. 2А) и из супернатанта разрушенных Е. coli (Фиг. 2В). Дорожка 1: Ореохромицин I; Дорожка 2: Ореохромицин II, Дорожка 3: Ореохромицин III.
Фигура 3. Противовирусная активность антимикробных пептидов Ореохромицина I, Ореохромицина II и Ореохромицина III. Клетки ЕРС (папулезная эпителиома карпов), рассаженные в 24-луночные планшеты, трансфицировали в течение 24 ч 1 мкг pTargeT-Oreochromicin I, pTargeT-Oreochromicin II, pTargeT-Oreochromicin III или pTargeT в качестве контроля. Через 24 ч после трансфекции добавляли разное количество вируса Rana grylio (RGV) (105 50% инфекционных доз вируса (доля заражения 50% культуральной ткани (TCID50)/мл, 104 TCID50/мл, 103 TCID50/мл и 102 TCID50/мл), через 48 ч собирали культуральные супернатанты и определяли вирусные титры.
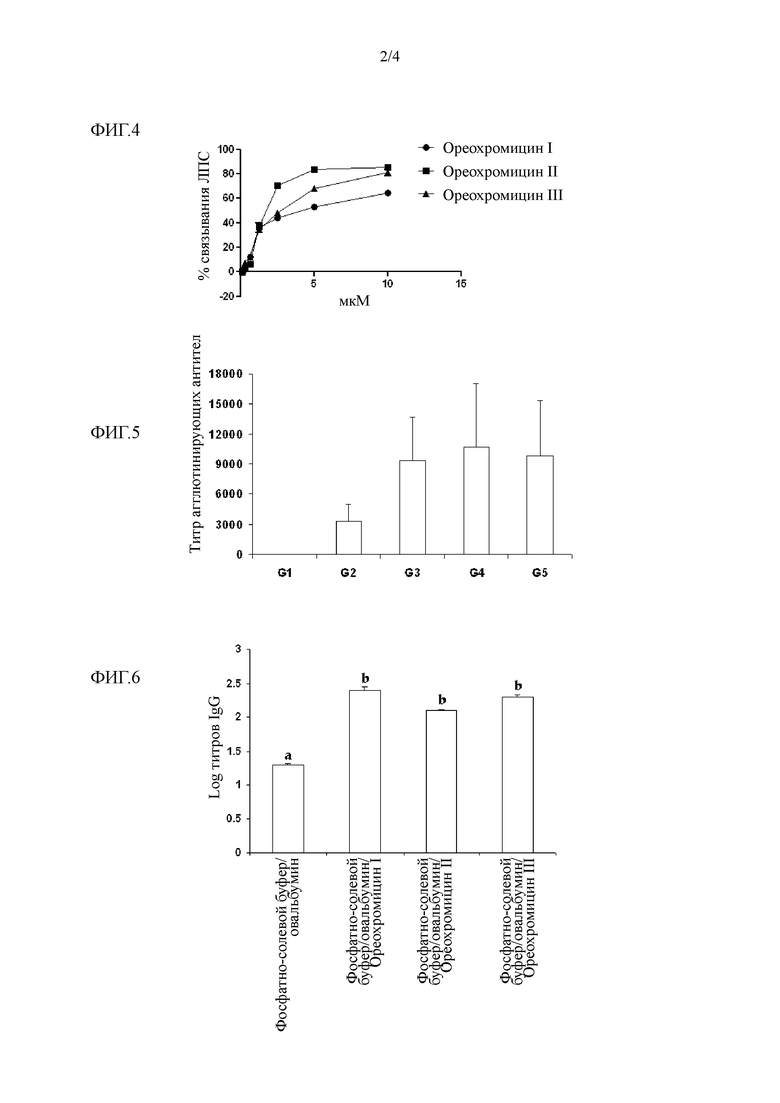
Фигура 4. Кривая насыщения при связывании антимикробных пептидов Ореохромицина I, Ореохромицина II, Ореохромицина III с липополисахаридом (ЛПС). Концентрация, при которой происходило связывание 50% пептида (Ореохромицина I, Ореохромицина II и Ореохромицина III) (эффективная концентрация ЕС50) составляла 1,23 мкМ, 1,41 мкМ и 2,99 мкМ соответственно.
Фигура 5. Титры антител против Aeromonas hydrophila в тилапии (n=12). Значения представляют собой среднее ± стандартную ошибку.
Фигура 6. Титры всех иммуноглобулинов G (IgG), индуцированных в мышах при иммунизации овальбумином, введенным одновременно с пептидами Ореохромицином I, Ореохромицином II и Ореохромицином III. Были созданы четыре экспериментальные группы, по 6 животных в каждой. В группе отрицательного контроля животным внутрибрюшинно вводили фосфатно-солевой буфер/овальбумин в дни 0 и 7 в дозировке 6 мкг овальбумина в 0,2 мл фосфатно-солевого буфера. В группах получавших также пептиды (фосфатно-солевой буфер/овальбумин + пептид) животным в дни 0 и 7 внутрибрюшинно инъецировали 6 мкг овальбумина + 0,5 мкг каждого пептида в 0,2 мл фосфатно-солевого буфера. Буквы обозначают статистически достоверные отличия. Значения представляют собой среднее ± стандартную ошибку (n=6).
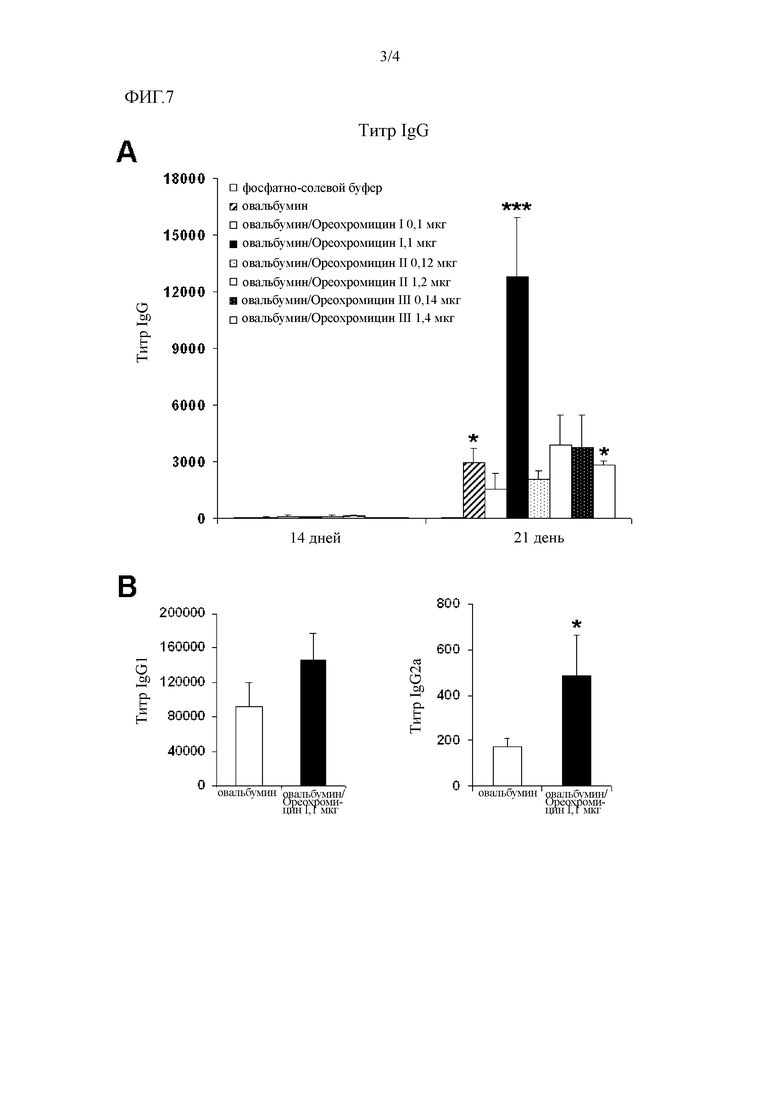
Фигура 7. Титры всех иммуноглобулинов G (IgG) (A), IgG1 и IgG2a (В), индуцированных в мышах при иммунизации овальбумином, введенным совместно с пептидами Ореохромицином I, Ореохромицином II и Ореохромицином III. Самцов мышей Balb/c (8 в группе) иммунизировали, делая в дни 0 и 14 внутрибрюшинную инъекцию только овальбумина (5 мкг/животное) или овальбумина в сочетании с пептидами в дозировке 0,238×1020 молекул/животное (эквивалентное 0,1, 0,12 и 0,14 мкг/животное Ореохромицина I, II и III, соответственно) и 2,38×1020 молекул/животное (эквивалентное 1, 1,2 и 1,4 мкг/животное Ореохромицина I, II и III, соответственно). В группе отрицательного контроля животным внутрибрюшинно вводили 0,1 мл фосфатно-солевого буфера. Овальбумин-специфичный гуморальный иммунный ответ (общий уровень IgG) исследовали на 14 и 21 дни после первой иммунизации. Титры антител IgG1 и IgG2a анализировали на 21 день после первой иммунизации. Титры антител, специфичных к овальбумину, определяли методом твердофазного иммуноферментного анализа (ELISA). (А) Титры всех IgG. Столбики представляют собой титр IgG ± стандартную ошибку (n=8). Статистический анализ проводили по критерию Краскела-Уолеса и критерию Данна для множественного сравнения. Звездочками отмечены достоверные отличия от группы получавших фосфатно-солевой буфер (* соответствует р<0,05, *** соответствует р<0,001). (В) Титры IgG1 и IgG2a. Столбики представляют собой титр антител ± стандартную ошибку (n=8). Статистический анализ проводили по критерию Манна-Уитни (* соответствует р<0,05).
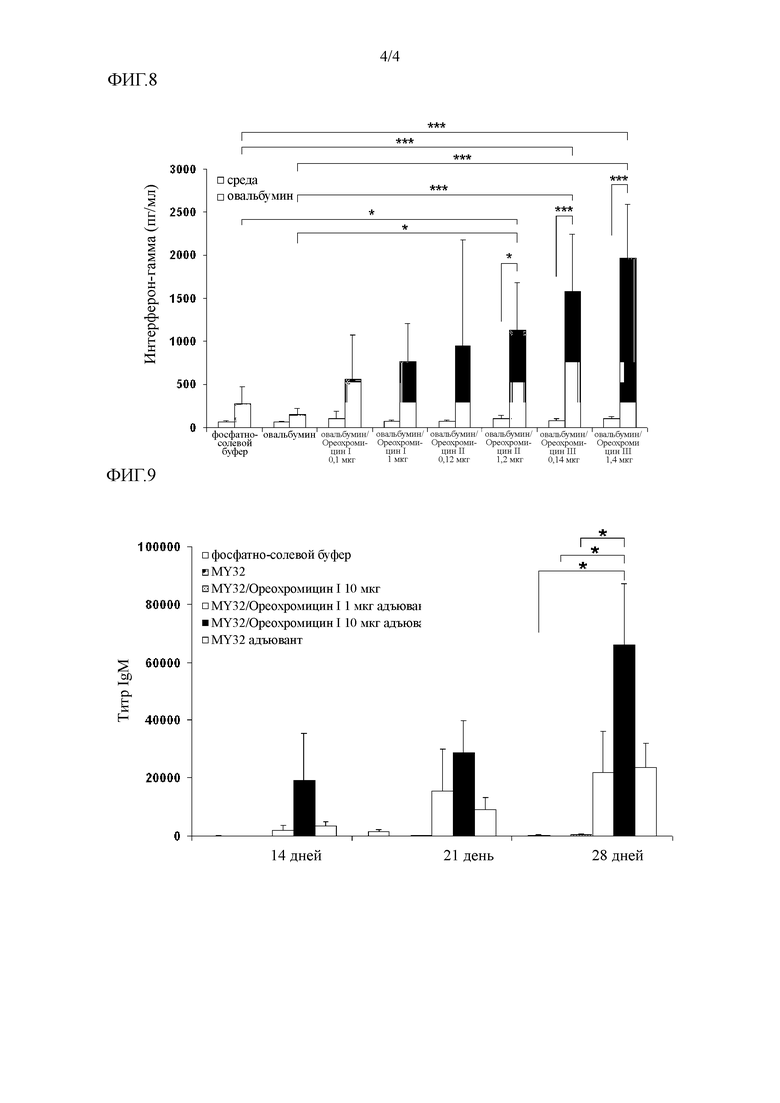
Фигура 8. Секреция IFN-γ клетками селезенки, выделенными из иммунизированных животных. По оси ординат отложена концентрация интерферона-γ в культуральном супернатанте сплиноцитов, стимулированных овальбумином (10 мкг/мл). Столбики представляют собой концентрацию интерферона-γ ± стандартную ошибку (n=5). Статистический анализ данных проводили с помощью дисперсионного анализа и критерия Бонферонни для множественного сравнения (*: р<0,05, ***: р<0,001).
Фигура 9. Титры IgM, индуцированных при иммунизации тилапии (О. niloticus) белком MY32, введенным одновременно с антимикробным пептидом Ореохромицином I. Рыб (10 рыб в группе) иммунизировали, делая внутрибрюшинную инъекцию в дни 0 и 14. Животным из группы отрицательного контроля вводили 0,3 мл фосфатно-солевого буфера. Специфичный гуморальный иммунный ответ на MY32 исследовали на 14, 21 и 28 дни после первой иммунизации. Титры антител IgM, специфичных к MY32, определяли методом твердофазного иммуноферментного анализа (ELISA). Столбики представляют собой титр антител IgM ± стандартную ошибку (n=10). Статистический анализ данных проводили с помощью дисперсионного анализа и критерия Ньюмана-Кейлса для множественного сравнения (* соответствует р<0,05).
Примеры
Пример 1. Выделение и очистка антимикробных пептидов из экстрактов жабр тилапии.
Жаберные лепестки тилапии (Oreochromis niloticus) измельчали в жидком азоте, полученный порошок нагревали при 100°С в течение 10 мин и оставляли остывать. Экстракцию белков проводили, добавляя 150 мл раствора 2М HCl, 10% (объем/объем) муравьиную кислоту, 2% (масса/объем) NaCl и 1% (объем/объем) трихлоруксусную кислоту, затем гомогенизировали в течение 1-2 мин. Гомогенат центрифугировали при 20000×g в течение 30 мин, доводили рН супернатанта до 4,0 и фильтровали. Полученный фильтрат применяли в качестве кислотного экстракта и наносили на колонку Sep-Pak С18 (Waters, Милфорд, штат Массачусетс, США). После промывки 0,1% (объем/объем) трифторуксусной кислотой фракцию, соответствующую пептидам, элюировали 80% ацетонитрилом/0,1% трифторуксусной кислотой. Элюат высушивали и растворяли в 1М уксусной кислоте, и сорбировали на носителе SP-Sephadex С-25. В результате последовательной ступенчатой элюции 1М уксусной кислотой, 2М пиридином и смесью 2М пиридин/уксусная кислота (рН 5,0) получали пять фракций. Определяли антимикробную активность каждой фракции и для последующей очистки выбирали фракцию 2.
Выбранную фракцию лиофилизировали и растворяли в 40% ацетонитриле, содержащем 0,1% трифторуксусной кислоты. Аликвоту раствора наносили на колонку TSKgel G2000SW (гель-фильтрация, высокоэффективная жидкостная хроматография (ВЭЖХ)) и элюировали 40% ацетонитрилом, содержащим 0,1% трифторуксусной кислоты. Эту же фракцию повторно наносили на колонку, образующуюся фракцию с молекулярным весом менее 5 кДа, обладающую антимикробной активностью, лиофилизировали и анализировали с помощью обратно-фазовой хроматографии и масс-спектрометрии с ионизацией электрораспылением. Молекулярный вес данной фракции определяли с помощью гель-электрофореза с Трицином-доделсульфатом натрия (16,5% Т/3% С) (сокращенно электрофорез в ПААГ с Трицином-додецилсульфатом натрия).
Разделение белков с помощью ВЭЖХ производили в системе Hewlett-Packard НР1100. В качестве растворителя А применяли 5% ацетонитрил, содержащий 0,1% трифторуксусной кислоты, в качестве растворителя В - 80% ацетонитрил, содержащий 0,085% трифторуксусной кислоты. Фракцию А разводили растворителем А и проводили обратно-фазовую ВЭХЖ на колонке С8-3 (4,6×150 мм). Градиент был образован 0-2 мин 0% растворителем В, 2-5 мин 0-20% растворителем В, 5-55 мин 20-47% растворителем В, и 55-80 мин 47-100% растворителем В. Полученные фракции, обладающие антимикробной активностью, лиофилизировали, растворяли в 5 мМ KH2PO4/Н3РО4 (рН 3,0), содержащем 25% ацетонитрила, и наносили на колонку PolySulfoethyl Aspartamide (4,6×200 мм). Фракции элюировали линейным градиентом KCl. Молекулярный вес фракций, которые обладали наибольшей антимикробной активностью, составлял 2527,3, 2981,9 и 3654,6 Да. Эти пептиды были названы Ореохромицином I, II и III соответственно. Определяли аминокислотную последовательность каждого пептида, обладающего антимикробной активностью, и обозначали их как SEQ ID NO: 1, 2 и 3, соответственно. Далее проанализировали последовательности с помощью программы BlastX и обнаружили, что данные пептиды не были описаны ранее.
Пример 2. Конструирование векторов для внутриклеточной экспрессии антимикробных пептидов в Е. coli и для внеклеточной экспрессии в дрожжах P. pastoris
Комплементарные ДНК (кДНК) получали из рибонуклеиновой кислоты (РНК), выделенной из жабр тилапии (О. niloticus) с помощью реакции обратной транскрипции. Реакции проводили в соответствии с инструкциями к набору реактивов «Обратнотранскриптазная система» (Promega, США). Вкратце, 4 мкг тотальной РНК помещали в микроцентрифужную пробирку без нуклеаз и инкубировали 10 мин при 70°С. Затем добавляли остальные компоненты реакции (4 мкл 25 мМ MgCl2, 2 мкл смеси 10 мМ дезоксинуклеотидтрифосфатов, 2 мкл 10-кратного буфера для обратной транскриптазы, 0,5 мкл ингибитора рибонуклеаз, 1 мкл олиго(дТ) 500 мкг/мл, 20 единиц обратной транскриптазы и вода, предварительно обработанная диэтилполикарбонатом, до конечного объема 20 мкл). Реакционную смесь инкубировали в течение 15 мин при 42°С и останавливали реакцию при 95°С в течение 5 мин.
Нуклеотидную последовательность, кодирующую зрелую область антимикробного пептида, амплифицировали с помощью ПЦР, применяя полученные кДНК и вырожденные синтетические олигонуклеотиды, подобранные на основании аминокислотной последовательности каждого пептида. Во всех случаях получали фрагмент ДНК нужного размера. Фрагменты ДНК выделяли из агарозного геля и вставляли в коммерческий вектор pGEM-TEasy (Промега) для секвенирования. Последовательности ДНК, кодирующие пептиды, обозначали номерами 4, 5 и 6.
Последовательности ДНК, кодирующие антимикробные пептиды, вставляли в экспрессионный вектор pAR 3040 для Е. coli по сайтам для эндонуклеаз рестрикции NdeI/BamHI (Фигура 1А). Для амплификации фрагментов, соответствующих каждому пептиду, применяли олигонуклеотиды, узнающие специфичные последовательности на 5'- и 3'-концах и несущие сайты узнавания для эндонуклеаз рестрикции, которые применяли для клонирования в экспрессионный вектор. Для каждого пептида выбирали один рекомбинантный клон, которым трансформировали штамм BL21DE3 Е. coli, а для индукции экспрессии гена под контролем Т7 промотора применяли 1 мМ изопропил-β-D-1-тиогалактопиранозид (ИПТГ). Ген экспрессировали при 37°С в течение 6 ч. Экспрессию рекомбинантных пептидов проверяли с помощью электрофореза в ПААГ с Трицином-додецилсульфатом натрия и масс-спектрометрии с ионизацией электрораспылением.
Векторы pPS9 и pPS10 и специфичные олигонуклеотиды, узнающие последовательности на 5'- и 3'-концах пептидов и несущие сайты узнавания для эндонуклеаз рестрикции, применяли для создания вектора для экспрессии антимикробных пептидов в P. pastoris. Для клонирования в вектор pPS9 использовали сайты NcoI и SpeI, для клонирования в вектор pPS10 - сайты NaeI и SpeI. Такая схема клонирования не добавляет аминокислоты к исследуемому белку (Фигура 1В).
Плазмиды линеаризовали перед трансформацией штамма МР36 Р. pastoris. Трансформацию проводили с помощью электропорации. Штамм МР36 представляет собой ауксотрофный мутант his3, который приобретает фенотип His+ после трансформации.
Клоны трансформантов идентифицировали с помощью дот-блота. С помощью Саузерн блота определяли, в каком из клонов произошла интеграция путем замещения гена AOX1 P. pastoris на экспрессионную кассету рекомбинантной плазмиды, что соответствовало фенотипу Muts (низкий уровень потребления метанола) и His+. Дрожжи P. pastoris секретируют небольшое количество собственных белков, среда для из культивирования не нуждается в белковых добавках, поэтому можно ожидать, что гетерологичный белок, секретируемый во внеклеточную среду, будет составлять основную часть общего белка в среде (более 80%) (Tschopp et al. (1987) Bio/Technology 5:1305-1308).
Экспрессию пептидов в P. pastoris проводили в объеме 5 л, добавляя в среду метанол. Экспрессию рекомбинантных пептидов и отсутствие дефектов проверяли с помощью электрофореза в ПААГ с Трицином-додецилсульфатом натрия и масс-спектрометрии с ионизацией электрораспылением.
Пример 3. Очистка и исследование биологической активности антимикробных пептидов
Антимикробные пептиды, полученные рекомбинантным способом, очищали из супернатанта разрушенных Е. coli или из культурального супернатанта P. pastoris. Сначала проводили диализ в 25 мМ ацетате натрия (рН 4,5), применяя мембрану с порами размером 1 кДа. Продукт диализа наносили на катионообменную смолу CM-Sepharose Fast Flow, уравновешенную 25 мМ ацетатом натрия (рН 4,5), и элюировали белки 1М хлоридом натрия, 50 мМ Трисом (рН 7,6). Фракции, содержащие пептиды, собирали и концентрировали, применяя систему ультрафильтрации и мембрану с размером пор 1 кДа. Детектирование проводили при длине волны 254 нм. Степень очистки проверяли с помощью электрофореза в ПААГ с Трицином-додецилсульфатом натрия, белки визуализировали после окрашивания Кумасси голубым (Фигура 2).
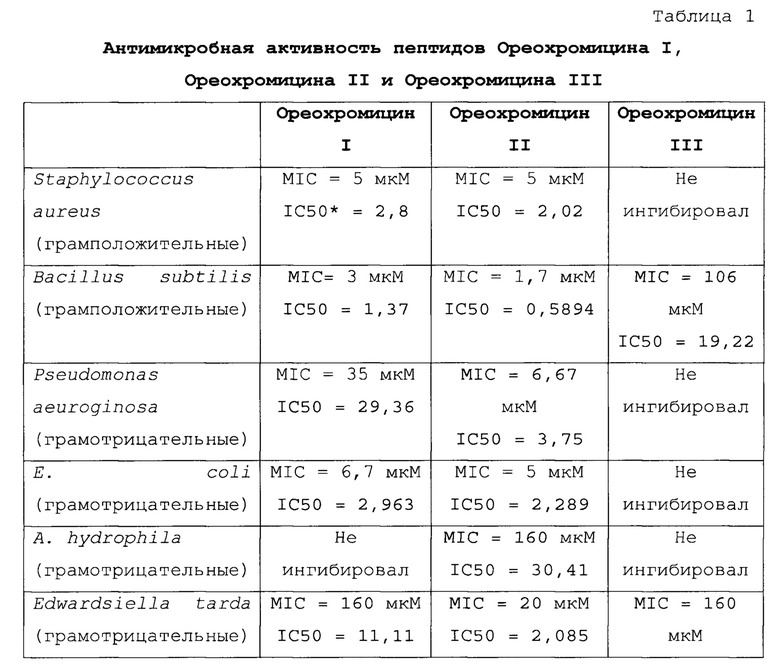
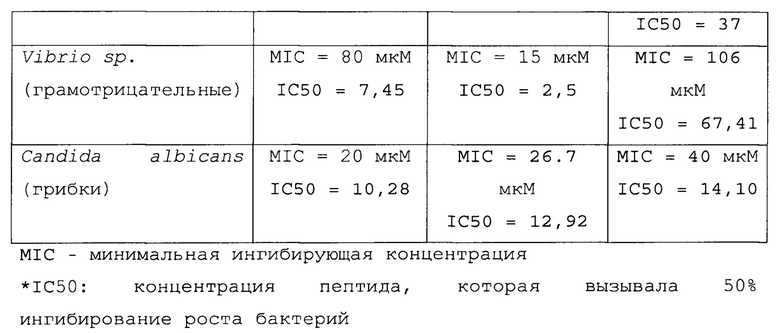
Пептиды, являющиеся предметом настоящего изобретения, также получали с помощью химического синтеза, применяя способы, известные специалистам в данной области техники. Антимикробную активность пептидов определяли способом микроразведений. Для определения минимальной ингибирующей концентрации каждый пептид разводили в соотношении 1:2. Десять микролитров каждого разведенного пептида инкубировали с 90 мкл суспензии бактерий или дрожжей (5×105 КОЕ (колониеобразующих единиц) в мл) в среде Мюллера-Хинтона (для бактерий) или в среде Сабуро (для грибков) в течение 18 ч при 28°С (в случае патогенов рыб и грибков) или при 37°С (в случае патогенов млекопитающих). Минимальную ингибирующую концентрацию определяли как наименьшую концентрацию пептида, при которой происходит ингибирование роста бактерий. Все исследования были проведены в трех повторностях, среду для культивирования (без микроорганизмов) и микроорганизмы без добавления пептидов применяли в качестве контроля. Результаты представлены в Таблице 1.
Пример 4. Определение сопротивляемости заражению Aeromonas hydrophila тилапий, предварительно обработанных антимикробными пептидами
Введение пептидов с помощью внутрибрюшинной инъекции
Далее проводили определение способности антимикробных пептидов повышать сопротивляемость заболеваниям in vivo. В первом исследовании изучали 130 тилапий (О. niloticus) весом 10 г, которые были распределены случайным образом в 13 экспериментальных групп, по 10 животных в группе. Исследование проводили с целью определения минимальной продолжительности терапии, которая необходима для повышения выживания рыб при заражении A. hydrophila. Каждый пептид вводили внутрибрюшинно в количестве 1 мкг на рыбу в течение 2, 4, 8 и 15 дней. Дополнительно была создана группа животных, которым вводили фосфатно-солевой буфер в качестве контроля. Экспериментальные группы:
Группа 1: фосфатно-солевой буфер.
Группа 2: Ореохромицин I вводили в течение 2 дней подряд.
Группа 3: Ореохромицин I вводили в течение 4 дней подряд.
Группа 4: Ореохромицин I вводили в течение 8 дней подряд.
Группа 5: Ореохромицин I вводили в течение 15 дней подряд.
Группа 6: Ореохромицин II вводили в течение 2 дней подряд.
Группа 7: Ореохромицин II вводили в течение 4 дней подряд.
Группа 8: Ореохромицин II вводили в течение 8 дней подряд.
Группа 9: Ореохромицин II вводили в течение 15 дней подряд.
Группа 10: Ореохромицин III вводили в течение 2 дней подряд.
Группа 11: Ореохромицин III вводили в течение 4 дней подряд.
Группа 12: Ореохромицин III вводили в течение 8 дней подряд.
Группа 13: Ореохромицин III вводили в течение 15 дней подряд.
После введения пептидов проводили тест с нагрузкой, делая внутрибрюшинную инъекцию средней летальной дозы (LD50) А. hydrophila, и оценивали уровень смертности в течение 7 дней. Вычисляли относительную долю выживаемости (%) по следующей формуле:
Относительная доля выживаемости (%) = (% смертности в контроле - % смертности в опыте) / (% смертности в контроле) × 100
В результате у рыб, обработанных Ореохромицином I и Ореохромицином III в течение 15 дней, был повышен уровень выживаемости (измеренный как относительная доля выживаемости) на 45% по сравнению с контрольными рыбами, обработанными фосфатно-солевым буфером. При этом в группе получавших Ореохромицин II в течение 8 дней уровень выживаемости (относительная доля выживаемости) был повышен на 48% по сравнению с контрольными рыбами, обработанными фосфатно-солевым буфером.
Второе исследование проводили для определения оптимальной дозы пептида, необходимой для повышения выживаемости рыб после заражения A. hydrophila. Исследовали 130 тилапий (О. niloticus) весом 10 г, которые были распределены случайным образом в 13 экспериментальных групп, по 10 животных в группе. Каждый пептид вводили в количестве 0,5, 1, 5 и 10 мкг на рыбу в течение 15 дней. Экспериментальные группы:
Группа 1: фосфатно-солевой буфер.
Группа 2: Ореохромицин I 0,5 мкг/рыба.
Группа 3: Ореохромицин I 1 мкг/рыба.
Группа 4: Ореохромицин I 5 мкг/рыба.
Группа 5: Ореохромицин I 10 мкг/рыба.
Группа 6: Ореохромицин II 0,5 мкг/рыба.
Группа 7: Ореохромицин II 1 мкг/рыба.
Группа 8: Ореохромицин II 5 мкг/рыба.
Группа 9: Ореохромицин II 10 мкг/рыба.
Группа 10: Ореохромицин III 0,5 мкг/рыба.
Группа 11: Ореохромицин III 1 мкг/рыба.
Группа 12: Ореохромицин III 5 мкг/рыба.
Группа 13: Ореохромицин III 10 мкг/рыба.
Через 15 дней введения пептидов проводили тест с нагрузкой, делая внутрибрюшинную инъекцию LD50 A. hydrophila, и оценивали уровень смертности в течение 7 дней. Относительную долю выживаемости рассчитывали, как описано выше. На 7 день после заражения все пептиды оказывали дозозависимый эффект, а доля выживаемости составляла от 84% до 88% по сравнению с контрольной группой, получавшей только фосфатно-солевой буфер, в которой уровень выживаемости составлял 10%.
Введение пептидов с помощью иммерсионных ванн
Исследование проводили для определения действия каждого пептида, вводимого посредством иммерсионных ванн, на выживаемость рыб после заражения A. hydrophila. Исследовали 1300 личинок тилапий (О. niloticus) в возрасте 5 дней после выхода из икры, которые были распределены случайным образом в 13 экспериментальных групп, по 100 личинок в группе. Каждый пептид вводили в количестве 0,01, 0,05, 0,1 и 0,5 мг пептида на литр воды в течение 15 дней. Экспериментальные группы:
Группа 1: фосфатно-солевой буфер.
Группа 2: Ореохромицин I 0,01 мг/л.
Группа 3: Ореохромицин I 0,05 мг/л.
Группа 4: Ореохромицин I 0,1 мг/л.
Группа 5: Ореохромицин I 0,5 мг/л.
Группа 6: Ореохромицин II 0,01 мг/л.
Группа 7: Ореохромицин II 0,05 мг/л.
Группа 8: Ореохромицин II 0,1 мг/л.
Группа 9: Ореохромицин II 0,5 мг/л.
Группа 10: Ореохромицин III 0,01 мг/л.
Группа 11: Ореохромицин III 0,05 мг/л.
Группа 12: Ореохромицин III 0,1 мг/л.
Группа 13: Ореохромицин III 0,5 мг/л.
Через 15 дней введения пептидов проводили тест с нагрузкой введением с помощью иммерсионных ванн LD50 A. hydrophila и оценивали уровень смертности в течение 10 дней. Относительную долю выживаемости рассчитывали, как описано выше. На 10 день после заражения все пептиды оказывали дозозависимый эффект, а доля выживаемости составляла от 76% до 89% по сравнению с контрольной группой, получавшей только фосфатно-солевой буфер, в которой уровень выживаемости составлял 18%.
Пероральное введение в виде добавок к корму
Исследование проводили для определения действия каждого пептида, вводимого перорально в виде добавки к корму, на выживаемость рыб после заражения A. hydrophila. Исследовали 130 тилапий (О. niloticus) весом 10 г, которые были распределены случайным образом в 13 экспериментальных групп, по 10 животных в группе. Каждый пептид вводили в количестве 50, 250, 500 и 750 мкг/кг корма в течение 30 дней. Экспериментальные группы:
Группа 1: фосфатно-солевой буфер.
Группа 2: Ореохромицин I 50 мкг/кг.
Группа 3: Ореохромицин I 250 мкг/кг.
Группа 4: Ореохромицин I 500 мкг/кг.
Группа 5: Ореохромицин I 750 мкг/кг.
Группа 6: Ореохромицин II 50 мкг/кг.
Группа 7: Ореохромицин II 250 мкг/кг.
Группа 8: Ореохромицин II 500 мкг/кг.
Группа 9: Ореохромицин II 750 мкг/кг.
Группа 10: Ореохромицин III 50 мкг/кг.
Группа 11: Ореохромицин III 250 мкг/кг.
Группа 12: Ореохромицин III 500 мкг/кг.
Группа 13: Ореохромицин III 750 мкг/кг.
Через 30 дней введения пептидов проводили тест с нагрузкой, делая внутрибрюшинную инъекцию LD50 A. hydrophila, и оценивали уровень смертности в течение 10 дней. Относительную долю выживаемости (%) рассчитывали, как описано выше. На 10 день после заражения все пептиды оказывали дозозависимый эффект, а доля выживаемости составляла от 80% до 95% по сравнению с контрольной группой, получавшей только фосфатно-солевой буфер, в которой уровень выживаемости составлял 13%.
Пример 5. Определение сопротивляемости мышей заражению Staphylococcus aureus или Pseudomonas aeruginosa
Изучали способность антимикробных пептидов Ореохромицина I и Ореохромицина II защищать мышей от летальной дозы бактерий S. aureus и P. aeruginosa. Данное исследование проводили на самцах мышей (ICR) в возрасте 4 недель весом 25 г. Бактерии выращивали в триптонно-соевой среде при 37°С в течение 8 ч.
Количество бактерий, необходимое для достижения 90% и 100% уровня смертности, получали при разведении культуры в фосфатно-солевом буфере. Количество жизнеспособных колоний оценивали по уровню поглощения при 550 нм и проверяли с помощью посева серии разведений инокулята. В зависимости от исследуемого микроорганизма и способа введения применяли дозировку 4,5×106 и 1,4×109 КОЕ/мышь.
15 мышей инфицировали каждой дозой и наблюдали за уровнем выживаемости в течение 7-10 дней после инъекции. В первом исследовании мышам вводили 0,5 мл фосфатно-солевого буфера (отрицательный контроль) или фосфатно-солевой буфер, содержащий отдельные антимикробные пептиды, посредством внутрибрюшинной инъекции сразу после внутрибрюшинной инъекции бактерий. Во втором исследовании вводили S. aureus внутривенно. Сразу после введения бактерий мышам внутривенно вводили 0,2 мл фосфатно-солевого буфера или фосфатно-солевой буфер, содержащий антимикробные пептиды.
В результате было обнаружено, что пептиды Ореохромицин I и Ореохромицин II, введенные внутрибрюшинно в дозе 0,5 мг/кг, снижали уровень смертности, вызванной S. aureus и P. aeruginosa с 90-100% в контрольной группе до 5-29% в группах получавших пептиды. В случае внутривенного введения S. aureus, и введения пептида в количестве 2,5 мг/кг уровень смертности снижался с 90-100% в контроле до 18-40% в группах получавших пептиды.
Пример 6. Активность антимикробных пептидов в отношении инфекции, вызванной иридовирусом
Клетки ЕРС (папулезная эпителиома карпобразных) инкубировали при 28°С, 5% СО2 и относительной влажности 95% в среде RPMI-1640, содержащей 10% фетальной бычьей сыворотки, 1 мМ пирувата, 2 мМ глутамина, 100 ед./мл пенициллина и 100 мкг/мл стрептомицина. Антимикробные пептиды, являющиеся предметом настоящего изобретения, амплифицировали с помощью ПЦР, применяя специфичные праймеры, узнающие последовательности на 5'- и 3'-концах, и вставляли в вектор pTargeT для получения плазмид pTargeT-Oreochromicin I, pTargeT-Oreochromicin II и pTargeT-Oreochromicin III.
Клетки ЕРС выращивали до 90% конфлюэнтности и проводили транзиентную трансфекцию векторами, содержащими гены, кодирующие антимикробные пептиды, и пустым вектором pTargeT при концентрации ДНК 1 мкг/мл, применяя липофектамин 2000. Экспрессию антимикробных пептидов в трансфицированных клетках анализировали методом обратной транскрипции. ПЦР-продукты визуализировали в 2% агарозном геле, окрашенном бромистым этидием. Через 24 ч после трансфекции каждую лунку 3 раза промывали фосфатно-солевым буфером и обрабатывали разным количеством вируса Rana grylio (RGV). Через 48 ч после заражения собирали супернатанты из каждой лунки и 3 раза проводили их замораживание и оттаивание. Для определения титров RGV готовили серию разведений супернатантов бессывороточной среды и титровали клетки на ЕРС. Каждое разведение исследовали в трех повторностях. Данные представляют собой среднее ± стандартную ошибку. Различия между группами оценивали с помощью дисперсионного анализа и критерия Данна для множественного сравнения.
При заражении клеток 105, 104, 103 и 102 TCID50/мл RGV значительные цитопатические эффекты наблюдали через 48 ч инкубации в клетках, трансфицированных пустым вектором pTargeT, по сравнению с остальными клетками, экспрессирующими антимикробные пептиды. Титры вирусов в клетках, экспрессирующих антимикробные пептиды, были существенно ниже, чем титры в клетках, трансфицированных пустым вектором (р<0,01) (Фигура 3).
Пример 7. Нейтрализация ЛПС антимикробными пептидами
Кроме антимикробной активности и возможности повышения сопротивляемости заболеваниям изучали способность антимикробных пептидов, являющихся предметом настоящего изобретения, нейтрализовать ЛПС, применяя тест с лизатом амебоцитов мечехвоста. Данный тест позволяет зарегистрировать наличие ЛПС, которые не были нейтрализованы. Различные концентрации пептидов инкубировали с 0,5 ед./мл ЛПС при 37°С в течение 30 мин. ЛПС без пептидов применяли в качестве положительного контроля в исследовании. Затем добавляли 100 мкл смеси до равного объема лизата амебоцитов мечехвоста. Кинетику помутнения раствора измеряли на приборе Tube Reader ATi-321 (Lab Kinetics, Великобритания). Как показано на фигуре 4, антимикробные пептиды, являющиеся предметом настоящего изобретения, обладают способностью нейтрализовать ЛПС по дозозависимому механизму. Эффективная концентрация (ЕС50) пептидов Ореохромицина I, Ореохромицина II и Ореохромицина III составляла 1,23 мкМ, 1,41 мкМ и 2,99 мкМ соответственно.
Пример 8. Применение антимикробных пептидов Ореохромицина I, Ореохромицина II и Ореохромицина III в качестве молекулярных адъювантов
Исследовали пять экспериментальных групп, по 12 тилапий (О. niloticus) в каждой. Тилапий весом 50 г инъецировали внутрибрюшинно фосфатно-солевым буфером, клетками A. hydrophila, инактивированными формалином и клетками A. hydrophila, инактивированными формалином, с добавлением каждого пептида в концентрации 1 мкг/рыба. Инъекции проводили в дни 0 и 14. Кровь из хвостовой вены рыб отбирали в дни 0 и 21 и хранили сыворотку при -20°С до дальнейшего применения.
Титр агглютинирующих антител против A. hydrophila определяли с помощью реакции агглютинации в 96-луночных планшетах. Готовили серию разведений образцов сыворотки (50 мкл) в фосфатно-солевом буфере, добавляли в каждую лунку 50 мкл клеток A. hydrophila, инактивированных формалином (4×109 клетки/мл), и тщательно перемешивали. Планшеты инкубировали в течение ночи при комнатной температуре перед исследованием агглютинации. Титр агглютинирующих антител выражали как обратную величину наибольшего разведения сыворотки, вызывающего агглютинацию.
Уровень выработки агглютинирующих антител против А. hydrophila представлен на фигуре 5. Наблюдение за средним титром агглютинирующих антител на неделе 3 после иммунизации показывает, что титры в группах рыб, инъецированных инактивированными бактериальными клетками, введенными совместно с антимикробными пептидами, были выше таковых в группах рыб, инъецированных только бактериями (р<0,001) или фосфатно-солевым буфером (р<0,0001). Более того, наблюдались достоверные различия титров антител между группами рыб, инъецированными фосфатно-солевым буфером и только бактериями (р<0,001).
Пример 9. Эффект одновременной иммунизации овальбумином и антимикробными пептидами Ореохромицином I, Ореохромицином II и Ореохромицином III на гуморальный и клеточный иммунный ответ в мышах
А. График первой иммунизации
Были отобраны 24 мыши BALB/c весом 20 г, которых разделили на 4 экспериментальные группы, по 6 животных в каждой. Мышей из группы отрицательного контроля (фосфатно-солевой буфер/овальбумин) инъецировали внутрибрюшинно в дни 0 и 7 дозой 6 мкг овальбумина в 0,2 мл фосфатно-солевого буфера. Мышей из групп, обработанных пептидами (фосфатно-солевой буфер/овальбумин + пептид), инъецировали внутрибрюшинно в дни 0 и 7 дозой 6 мкг овальбумина + 0,5 мкг пептида в 0,2 мл фосфатно-солевого буфера. В день 15 протокола иммунизации отбирали кровь и оценивали общий титр IgG.
Фигура 6 показывает общие титры IgG, индуцированных при иммунизации мышей овальбумином, вводимым одновременно с каждым из пептидов. У животных из группы фосфатно-солевой буфер/овальбумин + пептид титр специфичных к овальбумину IgG был статистически выше, чем в контрольной группе. Такой эффект наблюдался в случае всех пептидов.
В. График второй иммунизации
Были отобраны 64 мыши BALB/c в возрасте 6 недель, которых разделили на 8 экспериментальных групп, по 8 животных в каждой. Иммуногены вводили внутрибрюшинно в объеме 0,1 мл. Антимикробные пептиды вводили в эквимолярном количестве (0,238×1020 молекул и 2,38×1020 молекул). Экспериментальные группы:
Группа 1: мышей иммунизировали фосфатно-солевым буфером.
Группа 2: мышей иммунизировали овальбумином в дозировке 5 мкг/животное.
Группа 3: мышей иммунизировали овальбумином в дозировке 5 мкг/животное + Ореохромицином I в дозировке 0,1 мкг/животное, эквивалентной 0,238×1020 молекулам/животное.
Группа 4: мышей иммунизировали овальбумином в дозировке 5 мкг/животное + Ореохромицином I в дозировке 1 мкг/животное, эквивалентной 2,38×1020 молекулам/животное.
Группа 5: мышей иммунизировали овальбумином в дозировке 5 мкг/животное + Ореохромицином II в дозировке 0,12 мкг/животное, эквивалентной 0,238×1020 молекулам/животное.
Группа 6: мышей иммунизировали овальбумином в дозировке 5 мкг/животное + Ореохромицином II в дозировке 1,2 мкг/животное, эквивалентной 2,38×1020 молекулам/животное.
Группа 7: мышей иммунизировали овальбумином в дозировке 5 мкг/животное + Ореохромицином III в дозировке 0,14 мкг/животное, эквивалентной 0,238×1020 молекулам/животное.
Группа 8: мышей иммунизировали овальбумином в дозировке 5 мкг/животное + Ореохромицином III в дозировке 1,4 мкг/животное, эквивалентной 2,38×1020 молекулам/животное.
Животных иммунизировали в дни 0 и 14, кровь отбирали в дни 0, 14 и 21. Сыворотку крови животных применяли для определения титров специфичных антител (общего уровня IgG, IgG1 и IgG2a). В день 59 от начала эксперимента извлекали селезенку из мышей для определения клеточного иммунного ответа на антиген овальбумина. Селезенку экстрагировали в асептических условиях, выделяли сплиноциты и рассаживали их в количестве 2×105 клеток при концентрации 2×106 клеток/мл в 96-луночный планшет с круглым дном. Клетки стимулировали конкавалином А (5 мкг/мл) или овальбумином (10 мкг/мл) и инкубировали при 37°С, 5% СО2 в течение 4 дней. Культуральные супернатанты собирали и применяли для анализа уровня интерлейкина-4 и интерферона-γ методом твердофазного иммуноферментного анализа (ELISA).
Фигуры 7А и В показывают титры всех IgG, IgG1 и IgG2a, индуцированных при иммунизации мышей овальбумином, вводимым одновременно с пептидами Ореохромицином I, II и III. У животных из группы фосфатно-солевой буфер/овальбумин + Ореохромицин I в дозировке 1 мкг/животное титр специфичных IgG к овальбумину был статистически выше, чем в группе отрицательного контроля (р<0,001) (Фигура 7А). У животных из групп фосфатно-солевой буфер/овальбумин и фосфатно-солевой буфер/овальбумин + Ореохромицин III в дозировке 1,4 мкг/животное титр всех IgG был также статистически выше, чем в группе отрицательного контроля (р<0,05). Аналогично титры специфичных к овальбумину IgG2a в группе иммунизированных фосфатно-солевым буфером/овальбумином + Ореохромицином I в дозировке 1 мкг/животное были значительно выше, чем в группе иммунизированных только овальбумином через 21 день после первой иммунизации (р<0,05) (Фигура 7В).
Культуральные супернатанты сплиноцитов, стимулированных овальбумином, из иммунизированных животных анализировали методом твердофазного иммуноферментного анализа (ELISA) для определения концентрации интерферона-γ и интерлейкина-4. Как показано на фигуре 8, наибольший уровень интерферона-γ наблюдается у животных, иммунизированных овальбумином, вводимым одновременно с пептидом Ореохромицином III, и эффект является дозозависимым. Уровни были статистически выше, чем уровни, наблюдаемые в сплиноцитах животных, иммунизированных только овальбумином или фосфатно-солевым буфером (р<0,001). Более того, уровни секреции интерферона-γ у животных, иммунизированных овальбумином, вводимым одновременно с Ореохромицином II в дозировке 1,2 мкг/животное, были значительно выше, чем уровни, наблюдаемые в сплиноцитах из животных, иммунизированных только овальбумином или фосфатно-солевым буфером (р<0,05) (Фигура 8). Секреция интерлейкина-4 не наблюдалась ни в одной из групп в заданных экспериментальных условиях.
Пример 10. Действие одновременной иммунизации антигеном MY32 и пептидом Ореохромицином Oreochromicin I на гуморальный иммунный ответ в тилапии
Для оценки действия пептида Ореохромицина I как молекулярного адъюванта в тилапии применяли в качестве вакцинального антигена белок MY32, описанный ранее (Carpio et al. (2011) Vaccine 29: 2810-2820).
Были составлены шесть экспериментальных групп, по 10 тилапий (О. niloticus) весом 45 г в каждой. Применяли внутрибрюшинный способ введения, иммуноген вводили в объеме 0,3 мл. Экспериментальные группы:
Группа 1: рыб иммунизировали фосфатно-солевым буфером.
Группа 2: рыб иммунизировали белком MY32 в дозировке 1 мкг/г веса тела.
Группа 3: рыб иммунизировали белком MY32 в дозировке 1 мкг/г веса тела и одновременно пептидом Ореохромицином I в дозировке 10 мкг/рыба.
Группа 4: рыб иммунизировали белком MY32 в дозировке 1 мкг/г веса тела и одновременно пептидом Ореохромицином I в дозировке 1 мкг/рыба с добавлением адъюванта Монтанид 888.
Группа 5: рыб иммунизировали белком MY32 в дозировке 1 мкг/г веса тела и одновременно пептидом Ореохромицином I в дозировке 10 мкг/рыба с добавлением адъюванта Монтанид 888.
Группа 6: рыб иммунизировали белком MY32 в дозировке 1 мкг/г веса тела с добавлением адъюванта Монтанид 888.
Животных иммунизировали в дни 0 и 14, кровь отбирали в дни 0, 14, 21 и 28. Сыворотку крови животных применяли для определения титров специфичных антител IgM.
Фигура 9 показывает титры IgM, индуцированных при иммунизации рыб антигеном MY32, вводимым одновременно с пептидом Ореохромицином I. У животных из группы MY32 + Ореохромицин I в дозировке 10 мкг/животное с добавлением адъюванта Монтанида 888 титр специфичных IgM к MY32 был статистически больше, чем в группах иммунизированных фосфатно-солевым буфером, MY32 и MY32, вводимым одновременно с пептидом Ореохромицином I в дозировке 10 мкг/рыба (р<0,05) (Фигура 9). Достоверные различия между остальными экспериментальными группами не наблюдались.


Настоящие изобретения относятся к антимикробным пептидам, выделенным и очищенным из экстрактов жабр тилапии (Oreochromis niloticus), а также способам и композициям, в которых они могут быть использованы. Представленные пептиды можно получить в результате химического синтеза или экспрессии в гетерологичной системе, такой как бактерии и дрожжи, применяя традиционные молекулярно-биологические технологии. Пептиды обладают антимикробной активностью в отношении различных организмов, включающих грамположительные бактерии, грамотрицательные бактерии, грибки и вирусы. Изобретения позволяют эффективно усиливать иммунный ответ, индуцированный различными антигенами, и контролировать ход заболеваний, вызванных патогенами. 7 н. и 9 з.п. ф-лы, 9 ил., 1 табл., 10 пр.
1. Пептид с антимикробной активностью, отличающийся тем, что содержит аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 1, 2 и 3, или аминокислотную последовательность с по меньшей мере 80% идентичностью с SEQ ID NO: 1, SEQ ID NO: 2 или SEQ ID NO: 3.
2. Пептид по п. 1, полученный выделением из естественного источника, химическим синтезом или технологией рекомбинантных ДНК.
3. Пептид по п. 2, полученный при экспрессии в бактериях, дрожжах или в клетках высших организмов.
4. Нуклеиновая кислота, которая кодирует аминокислотную последовательность, содержащую последовательность, определенную как SEQ ID NO: 1, SEQ ID NO: 2 и SEQ ID NO: 3, или аминокислотную последовательность с по меньшей мере 80% идентичностью с SEQ ID NO: 1, SEQ ID NO: 2 или SEQ ID NO: 3.
5. Композиция с антимикробной активностью для борьбы с бактериями, вирусами и грибковыми патогенами, характеризующаяся тем, что содержит пептид с последовательностью, определенной как SEQ ID NO: 1, SEQ ID NO: 2 или SEQ ID NO: 3, или аминокислотную последовательность с по меньшей мере 80% идентичностью с SEQ ID NO: 1, SEQ ID NO: 2 или SEQ ID NO: 3.
6. Композиция по п. 5, в которой пептид получают выделением из естественного источника, химическим синтезом или технологией рекомбинантных ДНК.
7. Композиция по п. 5, которую применяют для борьбы с патогенами, поражающими млекопитающих и водные организмы, и применяют в профилактических или терапевтических целях.
8. Композиция по п. 5, которую вводят перорально, парентерально или в виде иммерсионных ванн.
9. Применение пептида, содержащего аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 1, SEQ ID NO: 2 и SEQ ID NO: 3, или аминокислотную последовательность с по меньшей мере 80% идентичностью с SEQ ID NO: 1, SEQ ID NO: 2 или SEQ ID NO: 3, для получения композиции с антимикробной активностью для борьбы с бактериями, вирусами и грибковыми патогенами.
10. Способ борьбы с бактериями, вирусами и грибковыми патогенами в живых организмах, который характеризуется введением эффективного количества пептида, содержащего аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 1, SEQ ID NO: 2 и SEQ ID NO: 3, или аминокислотную последовательность с по меньшей мере 80% идентичностью с SEQ ID NO: 1, SEQ ID NO: 2 или SEQ ID NO: 3, указанным организмам.
11. Способ по п. 10, в котором пептид вводят в профилактических или терапевтических целях.
12. Способ по п. 10, в котором пептид вводят млекопитающим или водным организмам.
13. Способ по п. 12, в котором пептид вводят рыбам, предпочтительно в виде периодических инъекций в концентрации от 0,1 до 10 мкг пептида/рыба, в виде иммерсионных ванн в концентрации от 0,01 до 0,1 мг пептида/литр воды или в виде добавки к корму в концентрации около 50-750 мкг/кг корма.
14. Вакцинная композиция, содержащая пептид с антимикробной активностью, который содержит аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 1, SEQ ID NO: 2 и SEQ ID NO: 3, или аминокислотную последовательность с по меньшей мере 80% идентичностью с SEQ ID NO: 1, SEQ ID NO: 2 или SEQ ID NO: 3, в качестве молекулярного адъюванта, и вакцинный антиген.
15. Вакцинная композиция по п. 14, в которой пептид, применяемый в качестве вакцинного адъюванта, и антиген вводятся одновременно, отдельно или последовательно в рамках одного графика иммунизации.
16. Способ усиления иммунного ответа на вакцинный антиген, характеризующийся применением пептида, содержащего аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 1, SEQ ID NO: 2 и SEQ ID NO: 3, или аминокислотную последовательность с по меньшей мере 80% идентичностью с SEQ ID NO: 1, SEQ ID NO: 2 или SEQ ID NO: 3, в качестве молекулярного адъюванта в вакцине.
| TW 200825098 A, 16.06.2008 | |||
| CN 101111256 A, 23.01.2008 | |||
| ПЕПТИДЫ ЛАТАРЦИНЫ, ПРОЯВЛЯЮЩИЕ АНТИМИКРОБНУЮ АКТИВНОСТЬ | 2005 |
|
RU2302467C1 |
Авторы
Даты
2017-11-17—Публикация
2012-10-01—Подача