Область техники, к которой относится изобретение
Изобретение относится к биотехнологии, в частности к способу увеличения продуктивности стабильных клеточных линий – продуцентов рекомбинантных антител и может быть использовано при получении стабильных клеточных линий на основе СНО клеток для получения терапевтических рекомбинантных антител IgG и IgA класса.
Уровень техники
Для целей фарминдустрии требуется высокий уровень экспрессии рекомбинантных терапевтических иммуноглобулинов в СНО клетках. Имеется несколько стратегий по улучшению продуктивности клеточных линий млекопитающих в бессывороточных средах. Однако при высокой плотности клеток продукция рекомбинантных антител может снижаться из-за накопления в среде культивирования продуктов метаболитов клеток. Кроме того, следует принимать во внимание, что различные клоны-продуценты и созданные на их основе клеточные линии, имеют особенности использования питательных элементов, основанные на специфике метаболизма.
Ионы аммония являются токсичными отходами метаболизма клеток, которые накапливаются в клеточных культуральных средах главным образом в результате метаболизма глутамина и аспарагина. С одной стороны, глутамин является важным источником углерода и азота в среде для культуры клеток животных, с другой - метаболизм глутамина или его аналога является источником аммония в культуре, так как он самопроизвольно разлагается на аммоний. Содержание аммония оказывает отрицательное влияние на культуру клеток животных, так как рост клеток может быть замедлен даже низкими концентрациями аммония. Так снижение содержания аммония на 40% в фазе экспоненциального роста увеличивает концентрацию клеток на 50% (C.Dyring, H.A.Hansen, C.Emborg “The influence of ammonium on t-pa production from chinese hamster ovary (CHO) cells”, Animal Cell Technology Products of Today, Prospects for Tomorrow, 1994, pp.155-157). Важным фактором является также то, что хлорид аммония вызывает увеличение внутриклеточного рН, что может влиять на гликозилирование продуцируемых гликопротеинов (B.Thorens, P.Vassalli “Chloroquine and ammonium chloride prevent terminal glycosylation of immunoglobulins in plasma cells without affecting secretion”,1986, Nature, v. 321, 618–620).
Аналогичное негативное воздействие на клеточные культуры путем ингибирования роста клеток за счет изменения осмоляльности и рН также оказывает и лактат, накапливающийся в питательной среде. (H. J. Cruz, C.M. Freitas, P.M. Alves, J.L. Moreira, M.J. Carrondo “Effects of ammonia and lactate on growth, metabolism, and productivity of BHK cells”, Enzyme Microb. Tech., 2000, 27, 43–52; M.S. Lao, D. Toth “Effects of ammonium and lactate on growth and metabolism of a recombinant Chinese hamster ovary cell culture”. Biotechnol. Prog., 1997, 13, 688–691).
Из уровня техники известно, что снижение уровня лактата в культуральной среде способствует повышению однородности и продуктивности стабильных клеточных линий (V. Argentova, T. Aliev, D. Dolgikh, M. Kirpichnikov “Effects of succinic acid supplementation on stable cell line growth, aggregation, and production of recombinant antibodies of IgG and IgA.” Curr Pharm Biotechnol. 2020; 21(10), 990-996. doi: 10.2174/1389201021666200312130957).
Лактат как продукт метаболизма анаэробного гликолиза может определяться косвенно, используя измерение активности лактатдегидрогеназы (LDH). В некоторых работах сообщается что, при определенных условиях клеточные культуры могут переключаться на более энергоэффективный путь при потреблении лактата (V.S. Martínez, S. Dietmair, L.E. Quek, M.P. Hodson, P. Gray, L.K. Nielsen “Flux balance analysis of CHO cells before and after a metabolic switch from lactate production to consumption”, Biotechnol. Bioeng., 2013, 110, 660–666; C. Altamirano, A. Illanes, S. Becerra, J.J. Cairo, F. Godia “Considerations on the lactate consumption by CHO cells in the presence of galactose”, J. Biotechnol., 2006, 125, 547–556).
Из уровня техники известен способ получения стабильных клеточных линий (М.Ф. Кроуфорд, Т. Кристен, М. Янг “Способ получения стабильных клеточных линий, экспрессирующих высокие уровни представляющего интерес белка”, N17398, 28.12.2012, C12N15/65, C12N15/67, C12N15/79, WO2009/010534 2009.01.22, Мерк Сероно С.А.(US)), заключающийся в отборе кандидатов-продуцентов по FACS-скринингу клеток на продуктивность. Недостатком данного способа является то, что в способе при получении клонов-продуцентов не учитывается уровень метаболитов, аммония и лактата, в культуре, так как при дальнейшем масштабировании и культивировании возможен отбор клонов-кандидатов, имеющих повышенную выработку продуктов метаболизма: аммония и/или лактата. Данная особенность клонов-продуцентов приводит к понижению плотности клеток в культуре, уменьшению периода культивирования и, как следствие, пониженному уровню продукции требуемого рекомбинантного иммуноглобулина. Процесс отбора по параметрам метаболизма на поздних этапах получения стабильной клеточной линии ведет к потере клонов-кандидатов, имеющих больший потенциал, или требует дополнительного времени на новые раунды отбора.
Наиболее близким к заявляемому способу является способ получения стабильных клеточных линий из адаптированных клеток, продуцирующих меньше аммония в присутствии достаточной концентрации экзогенного лактата, чем в его отсутствии (M.S. Croughan, N. W. Freund “Strategy to reduce lactic acid production and control PH in animal cell culture “, US8470552B2, Jun. 25, 2013). Однако недостатком данного способа является то, что в способе получения адаптированных клеток-продуцентов, растущих в присутствии экзогенного лактата в среде, не учитывают уровень продуктов метаболизма самих клеток. Отбор клонов происходит на основе селекции клонов, способных расти на определенных концентрациях экзогенного, то есть добавленного, лактата. В качестве экзогенного лактата в среду добавляли различные соли лактата.
Таким образом, известные способы не обеспечивают возможность получения стабильных клонов-продуцентов/клеточных линий с особенностями метаболизма по уровню выделения в среду разных количеств метаболитов - аммония и лактата. В случае стандартного отбора клонов-кандидатов для получения стабильной клеточной линии основным критерием выбора является продуктивность, когда в конце отбора остаётся небольшое количество кандидатов, которые оцениваются уже по другим параметрам качества, таким как продолжительность времени культивирования, плотность культуры, агрегирование. Однако такой подход увеличивает время и повышает риски получения клеточной линии с повышенной выработкой продуктов метаболизма- аммония и лактата.
Технической проблемой является отсутствие способа отбора стабильных клонов- продуцентов для получения стабильной клеточной линии-продуцента рекомбинантных антител не только с высокой продуктивностью, но и с увеличенным сроком культивирования и продукцией рекомбинантных антител.
Раскрытие изобретения
Техническим результатом заявляемого изобретения является получение стабильных клонов-продуцентов / стабильных клеточных линий с увеличенной продуктивностью и c пониженной наработкой метаболитов, лактата и аммония, за счет чего происходит более эффективное нарабатывание рекомбинантных белков в среде и увеличение продолжительности времени культивирования клеточных линий-продуцентов за счет снижения уровня метаболитов в среде культивирования.
Технический результат достигается способом получения стабильной клеточной линии-продуцента рекомбинатных белков, включающим культивирование клонов-продуцентов рекомбинантных антител IgG1 на основе клеточной линии СНО DG44 (dhfr) и проведение оценки продуктивности и метаболизма клонов, при этом указанный способ включает следующие этапы:
а) выделение из множества трансфектантов кандидатов клонов–продуцентов с использованием прибора ClonePix на основании связывания флуоресцентной метки с экспрессируемыми антителами;
б) определение для каждого клеточного клона/клеточной линии первого множества клеточных клонов/клеточных линий продуцирующей способности;
в) определение для каждого клеточного клона/клеточной линии первого множества клеточных клонов/клеточных линий уровня метаболизма (лактата и аммония);
г) выбор индивидуальных субклонов в количестве 2-5 на основании факторов продуктивности и метаболизма для второго этапа;
д) получение моноклональных стабильных кандидатов субклонов–продуцентов/клеточных линий методом лимитирующего разведения;
е) определение для каждого клеточного субклона/клеточной линии второго множества клеточных клонов/клеточных линий продуцирующей способности и уровня метаболизма (лактата и аммония);
ж) выбор стабильного моноклона-продуцента/моноклональной стабильной клеточной линии с оптимальным сочетанием продуцирующей способности и уровня метаболизма;
з) культивирование стабильного моноклона-продуцента/ стабильной клеточной линии.
При этом первое множество клеток и второе множество клеток являются одним и тем же множеством клеток СНО DG44.
Оценку продуктивности проводят способом ИФА, а оценку метаболизма проводят путем определения концентрации аммония и лактатдегидрогиназы в культуральной среде. В качестве среды для культивирования используют среды, обеспечивающие рост клонов, например среды DMEM-F12, IMDM, OptiCHO. Культивирование клеточных линий проводят в инкубаторе при 37C°, 5-8% СО2 и 100% влажности. Для культивирования отбирают стабильные клоны-продуценты/ стабильные клеточные линии уровень продуктивности иммуноглобулина которых составляет более 30 мкг/мл и при культивировании которых концентрация лактата в среде культивирования составляет не более 60 нмоль/мл и концентрация аммония не более 90 нмоль/мл.
Таким образом, заявляемый способ отбора стабильного клеточного клона/стабильной клеточной линии, заключается в селекции клонов-кандидатов по двум критериям: продуктивности и метаболизму и, таким образом, совмещает способ отбора по анализу продуктов метаболизма клеток - аммония и лактата, выделяемых клонами–кандидатами, с результатами продуктивности клонов.
Предложенный способ позволяет оптимизировать процесс получения клеточных линий-продуцентов рекомбинантных антител, созданных на основе клеток СНО. Клеточные линии-продуценты, созданные на основании данного способа, будут обладать как пониженным метаболизмом глутамина и глюкозы, и выделением продуктов их распада, так и повышенной продуктивностью, и концентрацией клеток.
Это особенно актуально при культивировании в больших объемах сред. Предложенный способ позволяет экономить дорогостоящие питательные среды, так как в одном объеме среды при более продолжительном культивировании происходит наработка большего количества антител.
Настоящее изобретение позволяет быстро генерировать пул стабильных клонов-продуцентов/стабильных клеточных линий, так как процесс проходит с применением многофакторного отбора. Таким образом, потребуется меньше времени для получения пула стабильных клонов по сравнению с традиционными методами, то есть использование метода отбора стабильных клонов по их метаболизму наряду с продуктивностью позволяет генерировать стабильные клоны-продуценты/ стабильные клеточные линии с повышенной продуктивностью и увеличенным временем культивирования по сравнению со способом, который не учитывает особенности метаболизма стабильных клонов-продуцентов/стабильных клеточных линий. Это представляется важным в области биотехнологии, поскольку более быстрое получение стабильной клеточной линии-продуцента и увеличение продукции рекомбинантных антител означает экономию времени, сред культивирования.
Краткое описание чертежей
Изобретение поясняется следующими графическими материалами.
На фиг.1 показаны результаты анализа по определению содержания аммония в среде культивирования при выращивании клонов-кандидатов на этапе первичного отбора.
На фиг.2 показаны результаты анализа по определению содержания ЛДГ в среде культивирования при выращивании клонов-кандидатов на этапе первичного отбора.
На фиг.3 представлена диаграмма продуктивности клеточной культуры клонов-кандидатов, экспрессирующих антитело IgG1 в среде культивирования на этапе первичного отбора.
На фиг.4 приведена диаграмма сравнения уровня аммония в среде культивирования при выращивании суб-клонов на этапе вторичного отбора.
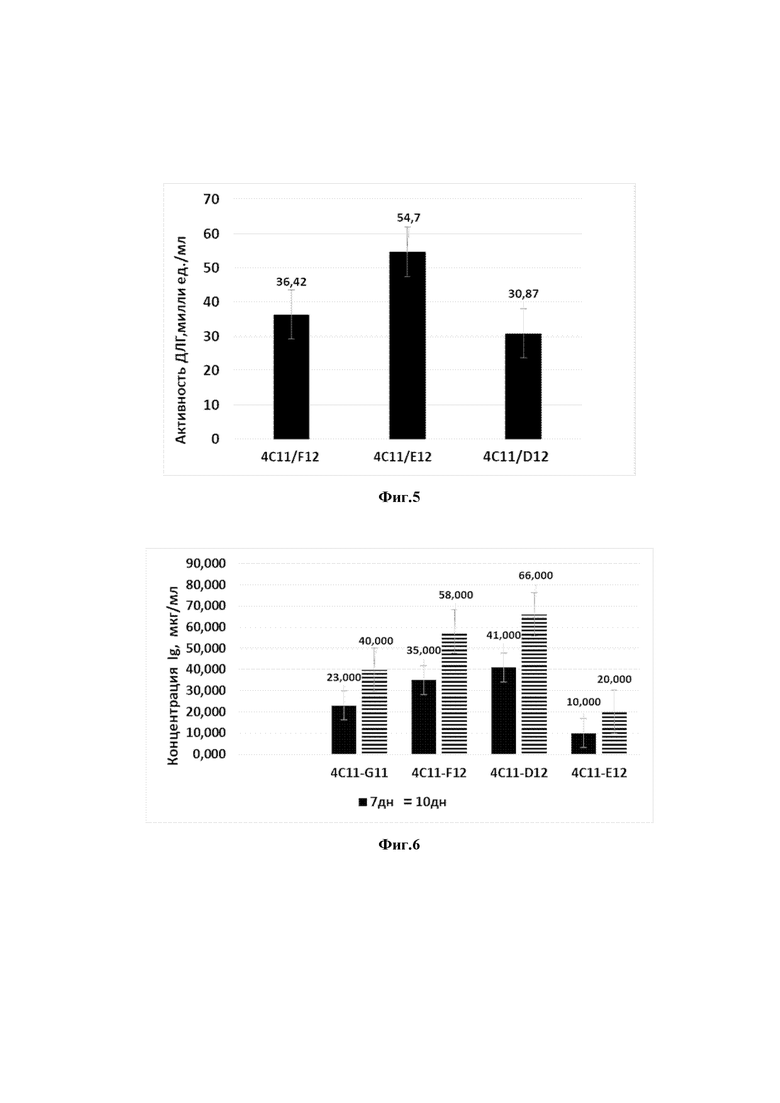
На фиг.5 приведена диаграмма сравнения уровня ЛДГ в среде культивирования при выращивании клонов-кандидатов на этапе вторичного отбора.
На фиг.6 приведена диаграмма сравнения продукции IgG в среде культивирования при выращивании клонов-кандидатов на этапе вторичного отбора.
Осуществление изобретения
Для целей настоящего изобретения термины "стабильная клеточная линия” и "стабильный клеточный клон " используются взаимозаменяемо.
Заявляемый способ получения стабильной клеточной линии путем отбора стабильных клонов-кандидатов с пониженной выработкой метаболитов позволяет выявить оптимальные клоны-кандидаты на раннем этапе процесса получения стабильной клеточных линии. Таким образом, стабильная клеточная линия, отобранная заявляемым способом, будет обладать продолжительным временем культивирования, повышенной плотностью клеточной культуры и, как следствие, увеличенной продуктивностью.
Для осуществления изобретения могут быть использования любые клетки линии СНО (клетки яичников китайского хомячка). Альтернативно могут быть использованы такие родительские клеточные линии как CHO–DUKX, CHO-DG44, CHO-S, CHO-K как в суспензионном, так и в адгезионном состоянии. Для получения трансфектантов могут быть применены любые методы трансфекции и использованы любые трансфицирующие реагенты.
Культивирование клеточных линий производят в стандартных условиях в инкубаторе при 37C°, 5-8% СО2 и 100% влажности. Суспензионное культивирование производят в планшетах, колбах Эрленмейера на орбитальном шейкере с частотой вращения 120-130 об/мин, либо в спиннер-флаконах или биореакторе (ферментере). Среду подбирают в зависимости от использованной клеточной линии. Это могут быть как среды на основе базовых DMEM-F12, IMDM, так и рекомендованные коммерческим производителем для конкретной клеточной линии.
Отбор клеток после стабильной трансфекции производят с помощью клональной селекции на полутвердой среде (Semi-Solid media, “Molecular Devices”, UK) по предложенной методике с использованием приборов ClonePix и CloneSelect Imager фирмы “Molecular Devices” (UK). Далее клоны выращивают на среде СD OptiCHO (Invitrogen, Thermo Fisher Sci., USA) при стандартных условиях выращивания. Альтернативно могут быть использованы как среды на основе базовых сред DMEM-F12, IMDM, так и рекомендованные коммерческим производителем для конкретной клеточной линии. Клоны выращивают в среднем в течение 10-14 дней.
Метаболизм глутамина вызывает аккумуляцию аммония в клеточной культуре, что замедляет рост клеток и отрицательно влияет на плотность клеточной культуры. Лактат является продуктом гликолиза, в частности глюкозы. Избыток лактата в клеточной культуре способен вызывать также снижение концентрации клеток и способствовать образованию агрегатов. Увеличение продукции антител, а также плотности культуры клеток и их жизнеспособности, может быть достигнуто за счет снижение уровня лактата и аммония в культуральной среде.
Для определения уровня аммиака или аммония в клеточной среде проводят измерение общего уровня ионов аммония и аммиака в образцах на 10-14 день культивирования с использованием набора по определению количества аммиака или аммония в культуральной жидкости. Концентрацию аммиака или аммония в нмоль/мкл (мМ) в тестируемых образцах вычисляют по формуле:
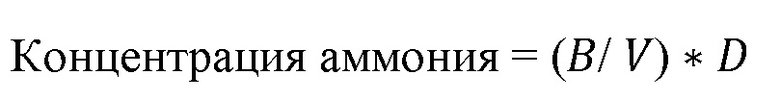
где: B – количество аммиака или аммония в образце в лунке, вычисленное по стандартной кривой в нмоль;
V – объем образца в лунке (мкл);
D – коэффициент разбавления пробы.
Параллельно проводят определение уровня лактата в культуральной среде. Для этого проводят измерение лактатдегидрогеназы (ЛДГ) с помощью набора для определения лактата в культуральной среде род. Вычисление активности ЛДГ проводят по формуле:
ЛДГ активность = B × фактор разведения образцов/(время реакции) × V,
где B – количество (нмоль) выработанного NADH/ (Tнач – Tконеч), V - объем.
На следующем этапе отбора проводят сравнение с показателем продуктивности клонов-кандидатов. Для дальнейшего культивирования отбирают не менее 2-5 клонов с пониженным содержанием лактата и аммония в культуральной среде и высоким показателем продуктивности относительно других клонов. Клоны, обладающие низкой продуктивностью менее 30 мкг/мл или повышенным уровнем метаболизма, более 60 нмоль/мл по лактату и более 90 нмоль/мл по аммонию, в процессе отбора отбраковываются.
Изобретение иллюстрируется примерами конкретного выполнения, которые более подробно описывают возможность осуществления заявляемого изобретения с достижением заявляемого технического результата.
Пример 1. Первичный отбор клонов - кандидатов на основании анализа метаболической активности
В экспериментах использовали клоны-продуценты рекомбинантных антител IgG1 на основе клеточной линии СНО DG44 (dhfr-) (Invitrogen, Thermo Fisher Sci., USA). Клоны выращивали на среде OptiCHO (Invitrogen, Thermo Fisher Sci., США). Для определения влияния уровня аммиака в культуральной среде на продуктивность, эксперимент проводили в формате статических культур в 6-луночных планшетах в инкубаторе при стандартных условиях выращивания при 37C° и 8% СО2 при непрерывном перемешивании 120 об/мин.
Метаболизм глутамина вызывает аккумуляцию аммония в клеточной культуре, что замедляет рост клеток и отрицательно влияет на плотность клеточной культуры.
Для определения уровня аммиака в клеточной среде проводили измерение общего уровня ионов аммония и аммиака в образцах с использованием набора” Ammonia Assay Kit” (Abcam, Великобритания) на 10 день культивирования. При физиологическом рН почти весь аммиак существует в виде аммония в растворе. Химическое уравнение, определяющее соотношение между аммиаком и аммонием, таково: NH3 + H2O ↔ NH4+ + OH-/
Концентрацию аммиака или аммония в нмоль/мкл (мМ) в тестируемых образцах вычисляли по формуле:
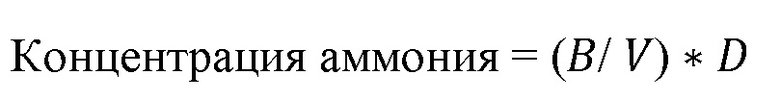
где: B – количество аммиака или аммония в образце в лунке, вычисленное по стандартной кривой в нмоль;
V – объем образца в лунке (мкл);
D – коэффициент разбавления пробы.
Для сравнения уровня аммония в среде культивирования были отобраны клоны-кандидаты 4C10, 2D2, 4C11, 1F2, 6F8. На Фиг.1 показаны результаты анализа по определению аммония в среде на 10 день культивирования. Наименьшее количество аммония в культуральной среде в диапазоне 82.28-87.25 нмоль/мл наблюдается у клонов 2D2, 4C11, и 6F8. Клоны 4С10 и 1А2 показали максимальное значение 92.47 и 90.41 нмоль/мл, соответственно.
Для определения влияния уровня лактата в культуральной среде на продуктивность, эксперимент также проводили в формате статических культур в 6-луночных планшетах при стандартных условиях выращивания, приведенных выше. Лактат как метаболит анаэробного гликолиза можно измерить косвенно, используя активность лактатдегидрогеназы (ЛДГ). Для определения уровня лактата в среде культивирования проводили измерение лактатдегидрогеназы (ЛДГ) с помощью коммерческого набора (Lactate Dehydrogenase Activity Assay Kit, Sigma). Вычисление активности ЛДГ проводили по формуле:
ЛДГ активность = B × фактор разведения образцов/(время реакции) × V,
где B - количество (нмоль) выработанного NADH/ (Tнач – Tконеч), V - объем.
На Фиг.2 показаны результаты по определению лактата в среде на 10 день культивирования. Содержание лактата в культуральной среде при выращивании клонов-кандидатов 4С11, 6F8 и 4С10 было наименьшим и составило 47.13, 53.29 и 74.71 нмоль/мл соответственно. Таким образом, на основании анализа продуктов метаболизма: лактата и аммония клон 1F2 демонстрирует увеличенный выход продуктов метаболизма, а клоны 4С11 и 6F8 - наименьший уровень. На основании совместного анализа на содержание лактата и аммония в среде культивирования проводили предварительный отбор по метаболизму в клонах. Клон 1F2, продемонстрировавший увеличенный уровень аммония 90.14 нмоль/мл и лактата 106.02 нмоль/мл не проходит отбор, так как увеличенное содержание аммония и лактата в культуральной среде замедляет рост клеток, снижает концентрацию клеток в культуре и ее продуктивность.
Пример 2. Первичный отбор клонов–кандидатов на основании сравнительного анализа продуктивности и плотности клеточной культуры
На следующем этапе отбора проводили сравнение с показателем продуктивности клонов-кандидатов. На Фиг.3 представлена диаграмма продуктивности клонов-кандидатов на первичном этапе отбора. Для клонов-продуцентов антител IgG1 наибольшую продуктивность 37.0, 42,0 и 40,0 мкг/мл показали клоны 4С10, 2D2, 4С11, соответственно. Продуктивность клона 6F8 является наименьшей и составляла 33.0 мкг/мл, что вместе с высокими показателями по уровню метаболизма дает отрицательный показатель отбора. В результате сравнения продуктивности и уровня метаболитов для клонов-кандидатов были выбраны наилучшие клоны по трем показателям: 4С11 и 2D2. Клон 2D2 выбран на основании наибольшего результата по продуктивности 42 мкг/мл и самого низкого показателя уровня аммония - 82.28 нмоль/мл. Клон 1F2 на основании данных по низкой продуктивности (33 мкг/мл) и высоких показателях уровня метаболизма, исключен из вторичного этапа отбора.
Выбранные клоны 4С11 и 2D2 имели пониженный уровень клеточного метаболизма и повышенную продуктивность антител. Далее для определения характера роста клоны культивировали способом статических культур в стандартных условиях в шейкер-флаконах в объеме 25 мл среды при ротационном перемешивании 125 об/мин. Клеточная культура клона 4С11 демонстрировала гомогенный суспензионный рост, в то время как культура клона 2D2 при продолжительном культивировании образовывала агрегаты (Табл.1), что связано с повышенной в 2 раза выработкой лактата (85.54 нмоль/мл), по сравнению с клоном 2D2 (47.13 нмоль/мл). В связи со всеми полученными результатами для вторичного отбора были выбран клон 4С11.
Табл.1. Динамика концентрации клеток в культурах клонов-продуцентов.
Пример 3. Второй этап отбора клонов-продуцентов по уровню продукции рекомбинантных антител и анализу метаболизма для выбора оптимального клона-продуцента рекомбинантных антител
На втором этапе с использованием способа лимитирующего разведения, от клона 4С11 были получены его суб-клоны. Выбранные клоны были подвергнуты вторичному отбору с проведением анализа на содержание аммония и лактата, в результате чего выбраны следующие суб-клоны: 4С11/G11, 4C11/F12, 4C11/D12 и 4C11/E12. Результаты, приведенные на Фиг.4 и Фиг.5, показывают, что суб-клоны 4С11/F12 и 4С11/D12 обладали более низкой продукцией лактата и аммония: 93,36 и 87.24 нмоль аммония, а также лактата - 36.42 и 30.87 нмоль/мл соответственно. Суб-клоны 4С11/G11 и 4С11/Е12 имели более высокие показатели уровня аммония и лактата, что отрицательно влияло на рост и плотность клеточной культуры.
С данными по метаболизму суб-клонов коррелировали показатели продукции иммуноглобулина (Фиг.6). Суб-клоны 4C11/F12 и 4C11/D12 с низкими уровнями клеточного метаболизма показывали уровень продукции иммуноглобулинов на уровне 58 мкг/мл и 66 мкг\мл соответственно. Так продуктивность субклона 4C11/D12 по сравнению в суб-клонами 4C11/G11 и 4C11/E12 выше в 1.65 и 3.3 раза соответственно.
Определение ростовых характеристик суб-клонов проводили способом статических культур. Данные по концентрации клеток культуры и продолжительности культивирования продемонстрированы в Табл. 2. Результаты по плотности клеточных культур суб-клонов 4C11/F12 и 4C11/E12 показывают, что их плотность нарастала до максимальной плотности 2.34х106 кл/мл, но затем резко снижалась до 3.0х105 и 1.5х105 кл/мл, соответственно. Таким образом, на 14 день культуры практически прекращали рост, что объясняется повышенным содержанием продуктов распада при метаболизме глутамина и глюкозы - аммонием и лактатом, замедляющим рост и продуктивность. Наилучший результат достигался при выращивании суб-клона 4C11/D12, который демонстрировал поступательное повышение и стабильный уровень плотности культуры клеток на 14 день культивирования (7.0х105кл/мл), жизнеспособность, высокую продуктивность,что коррелировало с пониженным уровнем клеточного метаболизма. Таким образом плотность клеточной культуры клона с пониженным метаболизмом в 2.3 и 4.6 раза, соответственно, выше по сравнению с клонами, обладающими повышенным метаболизмом. Полученная плотность 7.0х105 кл/мл на 14 день культивирования для клона с пониженным метаболизмом позволяло продолжить культивирование и наработку рекомбинантых антител.
Табл.2. Концентрация клеток клеточных культур суб-клонов продуцентов.
Таким образом, использование комбинированного отбора клонов-продуцентов на основании продуктивности и анализа продуктов метаболизма (аммония и лактата) позволяет более эффективно и быcтрее разрабатывать стабильные клеточные линии-продуценты рекомбинантных иммуноглобулинов G.
| название | год | авторы | номер документа |
|---|---|---|---|
| РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК рАР227, КОДИРУЮЩАЯ ПОЛИПЕПТИД РЕКОМБИНАНТНОГО ФАКТОРА VIII СВЕРТЫВАЕМОСТИ КРОВИ ЧЕЛОВЕКА, ЛИНИЯ КЛЕТОК Cricetulus griseus CHO 2H5 - ПРОДУЦЕНТ РЕКОМБИНАНТНОГО ФАКТОРА VIII СВЕРТЫВАЕМОСТИ КРОВИ ЧЕЛОВЕКА И СПОСОБ ПОЛУЧЕНИЯ ПОЛИПЕПТИДА, ОБЛАДАЮЩЕГО АКТИВНОСТЬЮ ФАКТОРА VIII | 2012 |
|
RU2500818C1 |
| Способ получения рекомбинантного фолликулостимулирующего гормона человека, клеточная линия - продуцент и плазмидные экспрессионные векторы | 2019 |
|
RU2697273C1 |
| СРЕДА ДЛЯ КУЛЬТИВИРОВАНИЯ КЛЕТОК БЕЗ БЕЛКОВ И БЕЗ СЫВОРОТКИ | 2009 |
|
RU2536244C2 |
| СРЕДА, НЕ СОДЕРЖАЩАЯ БЕЛКОВ И СЫВОРОТКИ, И СПОСОБ КУЛЬТИВИРОВАНИЯ КЛЕТОК МЛЕКОПИТАЮЩИХ В ТАКОЙ СРЕДЕ | 2000 |
|
RU2380412C2 |
| Композиция для предотвращения агрегирования и повышения однородности культуры, увеличения продуктивности клеточных линий-продуцентов рекомбинантных белков | 2018 |
|
RU2731988C2 |
| КЛЕТОЧНАЯ ЛИНИЯ huFSHIK, СЕКРЕТИРУЮЩАЯ РЕКОМБИНАНТНЫЙ ЧЕЛОВЕЧЕСКИЙ ФСГ | 2012 |
|
RU2502798C2 |
| СРЕДА ДЛЯ КУЛЬТИВИРОВАНИЯ КЛЕТОК БЕЗ БЕЛКОВ И БЕЗ СЫВОРОТКИ | 2000 |
|
RU2266325C2 |
| СИНТЕТИЧЕСКАЯ ДНК, КОДИРУЮЩАЯ ЭРИТРОПОЭТИН ЧЕЛОВЕКА, СОДЕРЖАЩИЙ ЕЁ ВЕКТОР, СПОСОБ ПОЛУЧЕНИЯ ШТАММА-ПРОДУЦЕНТА ЭРИТРОПОЭТИНА, ШТАММ-ПРОДУЦЕНТ ЭРИТРОПОЭТИНА | 2014 |
|
RU2548806C1 |
| ШТАММ КУЛЬТИВИРУЕМЫХ КЛЕТОК CHO-IL7/13 - ПРОДУЦЕНТ ИНТЕРЛЕЙКИНА-7 ЧЕЛОВЕКА | 2012 |
|
RU2562169C2 |
| ШТАММ КЛЕТОК ЯИЧНИКОВ КИТАЙСКОГО ХОМЯЧКА - ПРОДУЦЕНТ РЕКОМБИНАНТНОГО АНТИТЕЛА ПРОТИВ ФАКТОРА НЕКРОЗА ОПУХОЛИ АЛЬФА ЧЕЛОВЕКА | 2014 |
|
RU2556816C1 |
Изобретение относится к способу получения стабильной клеточной линии-продуцента рекомбинантных белков. Способ предусматривает культивирование клонов-продуцентов рекомбинантных иммуноглобулинов на основе клеточной линии СНО DG44 (dhfr-) и проведение оценки продуктивности и метаболизма клонов. Способ позволяет получать линии с пониженным клеточным метаболизмом продуктов гликолиза - лактата и метаболизма глутамина - аммония. Стабильные клеточные линии-продуценты с пониженным уровнем выделения аммония и лактата способны к более продолжительному росту, повышению плотности и однородности культуры. 4 з.п. ф-лы, 2 табл., 3 пр., 6 ил.
1. Способ получения стабильной клеточной линии-продуцента рекомбинатных белков, включающий культивирование клонов-продуцентов рекомбинантных иммуноглобулинов на основе клеточной линии СНО DG44 (dhfr-) и проведение оценки продуктивности и метаболизма клонов, при этом указанный способ включает следующие этапы:
а) выделение из множества трансфектантов кандидатов клонов–продуцентов с использованием прибора ClonePix;
б) определение для каждого клеточного клона/клеточной линии первого множества клеточных клонов/клеточных линий продуцирующей способности иммуноглобулинов;
в) определение для каждого клеточного клона/клеточной линии первого множества клеточных клонов/ клеточных линий уровня лактата и аммония;
г) выбор индивидуальных субклонов в количестве 2-5 на основании факторов продуктивности и метаболизма для второго этапа;
д) получение моноклональных стабильных кандидатов субклонов–продуцентов/клеточных линий методом лимитирующего разведения;
е) определение для каждого клеточного субклона/клеточной линии второго множества клеточных клонов/клеточных линий продуцирующей способности и уровня метаболизма;
ж) выбор стабильного моноклона-продуцента / моноклональной стабильной клеточной линии с уровнем продукции иммуноглобулина более 30 мкг/мл, и при культивировании которых концентрация лактата в среде культивирования составляет не более 60 нмоль/мл и концентрация аммония не более 90 нмоль/мл;
з) культивирование стабильного моноклона-продуцента / стабильной клеточной линии.
2. Способ по п. 1, характеризующийся тем, что оценку продуктивности проводят способом ИФА.
3. Способ по п. 1, характеризующийся тем, что оценку метаболизма проводят путем определения концентрации аммония и лактатдегидрогиназы в культуральной среде.
4. Способ по п. 1, характеризующийся тем, что для культивирования используют среды DMEM-F12, IMDM, OptiCHO.
5. Способ по п. 1, характеризующийся тем, что культивирование клеточных линий проводят в инкубаторе при 37C°, 5-8% СО2 и 100% влажности.
| US 8470552 B2, 25.06.2013 | |||
| WO 2009010534 A1, 22.01.2009 | |||
| CN 108018302 A, 11.05.2018 | |||
| Безмен | 1929 |
|
SU19812A1 |
| PEREIRA S | |||
| ET AL | |||
| Impact of CHO Metabolism on Cell Growth and Protein Production: An Overview of Toxic and Inhibiting Metabolites and Nutrients | |||
| Biotechnol J | |||
| Способ получения цианистых соединений | 1924 |
|
SU2018A1 |
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
| Способ получения цианистых соединений | 1924 |
|
SU2018A1 |
| Найдено | |||
Авторы
Даты
2022-03-24—Публикация
2020-12-31—Подача