Область техники, к которой относится настоящее изобретение
Настоящее изобретение относится к новому ингибитору индуцируемого гипоксией фактора 1α (HIF-1α), способу его получения и фармацевтической композиции для профилактики или лечения связанного с ангиогенезом заболевания глаз, содержащей его в качестве активного ингредиента.
Предшествующий уровень техники настоящего изобретения
Термин «ангиогенез» относится к механизму, с помощью которого образуются новые кровеносные сосуды из существующих кровеносных сосудов, представляет собой явление, которое редко возникает в нормальных физиологических условиях и строго контролируется, и в основном происходит во время эмбрионального развития в процессе развития оплодотворенных яиц, заживление ран у взрослых, изменения репродуктивных органов во время женского репродуктивного цикла и т.п.
У взрослых эндотелиальные клетки капилляров делятся относительно плохо и, как правило, делятся со скоростью от нескольких месяцев до нескольких лет. Ангиогенез происходит как сложный процесс за счет взаимодействия нескольких типов клеток с водорастворимыми факторами и компонентами внеклеточного матрикса.
Чрезмерный прогресс ангиогенеза, который строго контролируется таким образом, может вызывать различные заболевания. Новые кровеносные сосуды, образующиеся в опухолях, обеспечивают пути к другим органам, способствуя тем самым метастазированию, и, как известно, играют решающую роль в таких заболеваниях, как возрастная макулярная дегенерация, диабетическая ретинопатия, ретинопатия недоношенных, неоваскулярная глаукома, псориаз, ревматоидный артрит или хроническое воспаление, помимо опухолей.
Фактор роста сосудистого эндотелия (VEGF) представляет собой известный фактор, который играет ключевую роль в ангиогенезе, и известно, что VEGF может регулироваться регуляторным фактором транскрипции, называемым «HIF-1α» (индуцируемый гипоксией фактор 1, альфа) (патентный документ 1).
Следовательно, существует необходимость в разработке ингибиторов HIF-1α и способов лечения, облегчения или профилактики заболеваний или симптомов, связанных с ними.
Раскрытие настоящего изобретения
Техническая задача
Соответственно, одной из целей настоящего изобретения является предоставление соединения, которое способно эффективно ингибировать HIF-1α и, таким образом, применяться в качестве фармацевтической композиции для профилактики или лечения связанного с ангиогенезом заболевания глаз.
Другой целью настоящего изобретения является предоставление способа получения соединения.
Другой целью настоящего изобретения является предоставление фармацевтической композиции для профилактики или лечения связанного с ангиогенезом заболевания глаз, содержащей соединение в качестве активного ингредиента.
Еще цель настоящего изобретения состоит в том, чтобы предоставить композицию функциональной оздоровительной продукции для профилактики или облегчения связанного с ангиогенезом заболевания глаз, содержащую соединение в качестве активного ингредиента.
Техническое решение
В соответствии с настоящим изобретением вышеуказанные и другие задачи могут быть достигнуты путем предоставления соединения, представленного следующей Формулой (1), или его сольвата, гидрата, оптического изомера или фармацевтически приемлемой соли:
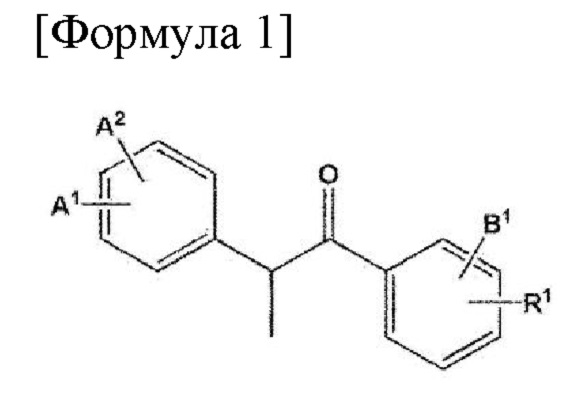
где А1 и А2, каждый независимо, представляют собой -Н, -ОН, -NO2, -CN, галоген, С1-10 алкил с прямой или разветвленной цепью или С1-10 алкокси с прямой или разветвленной цепью;
В1 представляет собой -Н, -ОН, -NO2, -CN, галоген, С1-10 алкил с прямой или разветвленной цепью или С1-10 алкокси с прямой или разветвленной цепью; а также
R1 представляет собой -Н, -ОН, -NO2, -CN, галоген, С1-10 алкил с прямой или разветвленной цепью, С1-10 алкокси с прямой или разветвленной цепью, С3-10 циклоалкилокси, ди-С1-10 алкиламино с прямой или разветвленной цепью, гетероциклоалкил с 5-10-членным кольцом, содержащий по меньшей мере один гетероатом, выбранный из группы, состоящей из N, О и S, или С1-5 алкиламино из С6-10 арила, незамещенного или замещенного по меньшей мере одним -CN.
В соответствии с другим аспектом настоящего изобретения предоставлен способ получения соединения.
В соответствии с другим аспектом настоящего изобретения предоставлена фармацевтическая композиция для профилактики или лечения связанного с ангиогенезом заболевания глаз, содержащая соединение в эффективном количестве в качестве активного ингредиента.
В соответствии с другим аспектом настоящего изобретения предоставлена композиция функциональной оздоровительной продукции для профилактики или облегчения связанного с ангиогенезом заболевания глаз, содержащая соединение в качестве активного ингредиента.
Положительные эффекты
Соединение, представленное в варианте осуществления настоящего изобретения, способно эффективно ингибировать HIF-1α и, таким образом, применимо в качестве фармацевтической композиции для профилактики или лечения связанного с ангиогенезом заболевания глаз.
Описание графических материалов
Фиг. 1 представляет собой график, на котором показаны результаты анализа ингибирующей активности против ангиогенеза соединения Примера согласно варианту осуществления настоящего изобретения.
Фиг. 2 представляет собой график, на котором показаны результаты анализа регулятор ной активности HIF-1α (индуцируемого гипоксией фактора 1α) соединения Примера согласно варианту осуществления настоящего изобретения.
Фиг. 3 представляет собой график, на котором показаны результаты анализа ингибирующей активности против неоваскуляризации сетчатки вследствие гипоксии соединения Примера согласно варианту осуществления настоящего изобретения.
Лучший вариант
В настоящем изобретении предложено соединение, представленное следующей формулой (1), или его сольват, гидрат, оптический изомер или фармацевтически приемлемая соль:
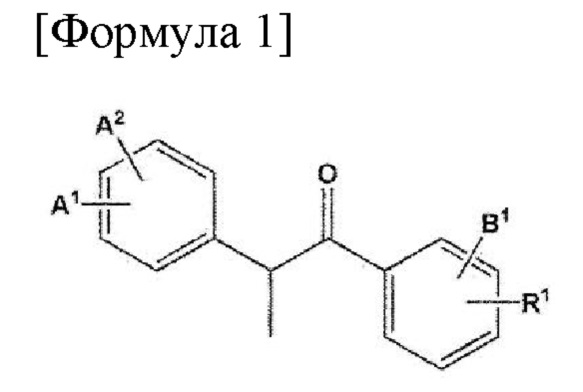
где А1 и А2, каждый независимо, представляют собой -Н, -ОН, -NO2, -CN, галоген, С1-10 алкил с прямой или разветвленной цепью или С1-10 алкокси с прямой или разветвленной цепью;
В1 представляет собой -Н, -ОН, -NO2, -CN, галоген, С1-10 алкил с прямой или разветвленной цепью или С1-10 алкокси с прямой или разветвленной цепью; а также
R1 представляет собой -Н, -ОН, -NO2, -CN, галоген, С1-10 алкил с прямой или разветвленной цепью, С1-10 алкокси с прямой или разветвленной цепью, С3-10 циклоалкилокси, ди-С1-10 алкиламино с прямой или разветвленной цепью, гетероциклоалкил с 5-10-членным кольцом, содержащий по меньшей мере один гетероатом, выбранный из группы, состоящей из N, О и S, или С1-5 алкиламино из С6-10 арила, незамещенного или замещенного по меньшей мере одним -CN.
Согласно варианту осуществления в настоящем изобретении предоставлено соединение формулы (1) или его сольват, гидрат, оптический изомер или фармацевтически приемлемая соль, где В1 представляет собой С1-10 алкокси с прямой или разветвленной цепью, a R1 представляет собой гетероциклоалкил с 5-10-членным кольцом, содержащий по меньшей мере один гетероатом, выбранный из группы, состоящей из N, О и S, или С1-5 алкиламино из С6-10 арила, незамещенного или замещенного по меньшей мере одним -CN.
Согласно варианту осуществления в настоящем изобретении предоставлено соединение формулы (1) или его сольват, гидрат, оптический изомер или фармацевтически приемлемая соль, где В1 представляет собой С1-10 алкокси с прямой или разветвленной цепью, a R1 представляет собой гетероциклоалкил с 5-членным кольцом, содержащий N или бензиламино, замещенный по меньшей мере одним -CN.
Принцип изобретения
Соединение, представленное Формулой 1 настоящего изобретения, можно использовать в форме фармацевтически приемлемой соли, и в качестве соли можно использовать соль присоединения кислоты, образованную фармацевтически приемлемой свободной кислотой. Соль присоединения кислоты получается из такой неорганической кислоты, как соляная кислота, азотная кислота, фосфорная кислота, серная кислота, бромистоводородная кислота, йодистоводородная кислота, азотистая кислота и фосфоновая кислота, такой нетоксичной органической кислоты, как алифатический моно- и дикарбоксилат, фенилзамещенный алканоат, гидроксиалканоат и алкандиоат, ароматическая кислота, алифатическая и ароматическая сульфоновая кислота, и такой органической кислоты, как трифторуксусная кислота, ацетат, бензойная кислота, лимонная кислота, молочная кислота, малеиновая кислота, глюконовая кислота, метансульфоновая кислота, 4-толуолсульфоновая кислота, винная кислота и фумаровая кислота.
Примеры фармацевтически нетоксичной соли включают в себя сульфат, пиросульфат, бисульфат, сульфит, бисульфит, нитрат, фосфат, моногидрофосфат, дигидрофосфат, метафосфат, пирофосфат, хлорид, бромид, йодид, фторид, ацетат, пропионат, деканоат, каприлат, акрилат, формиат, изобутират, капрат, гептаноат, пропиолат, оксалат, малонат, сукцинат, суберат, себацат, фумарат, малеат, бутин-1,4-диоат, гексан-1,6-диоат, бензоат, хлорбензоат, метилбензоат, динитробензоат, гидроксибензоат, метоксибензоат, фталат, терефталат, бензолсульфонат, толуолсульфонат, хлорбензолсульфонат, ксилолсульфонат, фенилацетат, фенилпропионат, фенилбутират, цитрат, лактат, β-гидроксибутират, гликолят, малат, тартрат, метансульфонат, пропансульфонат, нафталин- 1-сульфонат, нафталин-2-сульфонат, манделат и т.п.
Соль присоединения кислоты согласно настоящему изобретению может быть получена обычным способом, например, может быть получена растворением производного формулы 1 в органическом растворителе, таком как метанол, этанол, ацетон, метиленхлорид или ацетонитрил, добавлением органической или неорганической кислоты и фильтрованием полученного осадка с последующей сушкой или приготовлением путем выпаривания растворителя и избытка кислоты при пониженном давлении с последующей сушкой и кристаллизацией в присутствии органического растворителя.
Кроме того, фармацевтически приемлемую соль металла можно получить с использованием основания. Соль щелочного или щелочноземельного металла получают, например, растворением соединения в избыточном количестве раствора гидроксида щелочного металла или гидроксида щелочноземельного металла, фильтрованием нерастворенной соли соединения и выпариванием и сушкой фильтрата. В настоящее время фармацевтически предпочтительно приготовить соль натрия, калия или кальция в качестве соли металла. Кроме того, соответствующую соль получают реакцией соли щелочного или щелочноземельного металла с соответствующей солью серебра (например, нитратом серебра).
Кроме того, настоящее изобретение включает в себя все соединение, представленное Формулой 1, и его фармацевтически приемлемую соль, а также сольват, оптический изомер, гидрат и т.п., которые могут быть получены из них.
Кроме того, в настоящем изобретении предусмотрен способ получения соединения.
Кроме того, согласно одному варианту осуществления в настоящем изобретении предусмотрена фармацевтическая композиция для профилактики или лечения связанного с ангиогенезом заболевания глаз, содержащая соединение в эффективном количестве в качестве активного ингредиента. В настоящем документе некоторые конкретные примеры связанного с ангиогенезом заболевания глаз, включают в себя, без ограничения, макулярную дегенерацию, окклюзию вены сетчатки, диабетическую ретинопатию, ишемическую ретинопатию и т.п.
Соединение, представленное Формулой 1, или его фармацевтически приемлемая соль могут вводиться в форме любого из различных пероральных и парентеральных составов после клинического введения. Состав готовят с использованием обычно используемого разбавителя или вспомогательного вещества, такого как наполнитель, разбавитель, связующее вещество, смачивающее средство, разрыхлитель или поверхностно-активное вещество. Твердые препараты для перорального введения включают в себя таблетки, пилюли, порошки, гранулы, капсулы и т.п., и эти твердые препараты получают путем смешивания по меньшей мере одного соединения по меньшей мере с одним вспомогательным веществом, таким как крахмал, карбонат кальция, сахароза, лактоза или желатин. Кроме того, в дополнение к простым вспомогательным веществам также используются смазывающие вещества, такие как стеарат магния и тальк. Жидкие препараты для перорального введения включают в себя суспензии, пероральные растворители и жидкости, эмульсии, сиропы и т.п., а также могут быть включены различные вспомогательные вещества, такие как смачивающие вещества, подсластители, ароматизаторы и консерванты, в дополнение к воде и жидкому парафину, которые обычно используются в простых разбавителях. Составы для парентерального введения включают в себя стерильные водные растворы, неводные растворители, суспензии и эмульсии. В качестве неводных растворителей и суспензий могут быть использованы пропиленгликоль, полиэтиленгликоль, растительное масло, такое как оливковое масло, и сложный эфир для инъекций, такой как этилолеат.
Фармацевтическая композиция, содержащая представленное Формулой 1 соединение или его фармацевтически приемлемую соль в качестве активного ингредиента, может вводиться парентерально, и парентеральное введение может осуществляться путем подкожной инъекции, внутривенной инъекции, внутримышечной инъекции или внутригрудной инъекции.
В это время, чтобы приготовить состав для парентерального введения представленное Формулой 1 соединение или его фармацевтически приемлемую соль смешивают с водой вместе со стабилизатором или буфером для приготовления раствора или суспензии, и оттуда получают однократную дозировку в ампуле или флаконе. Композиция может быть стерилизована и/или может содержать вспомогательные лекарственные вещества, такие как консерванты, стабилизаторы, гидратирующие средства или ускорители эмульгирования, а также соли и/или буферы для контроля осмотического давления и другие терапевтически эффективные вещества, и может быть составлена обычным способом, таким как смешивание, гранулирование или нанесение покрытия.
Составы для перорального введения включают в себя, например, таблетки, пилюли, твердые/мягкие капсулы, жидкости/растворы, суспензии, эмульсии, сиропы, гранулы, эликсиры и пастилки. Эти составы содержат, помимо активного ингредиента, разбавители (например, лактозу, декстрозу, сахарозу, маннит, сорбит, целлюлозу и/или глицин) и смазывающие вещества (такие как диоксид кремния, тальк, стеариновая кислота и их соли магния или кальция и/или или полиэтиленгликоль). Таблетки могут содержать связующее вещество, такое как силикат магния и алюминия, крахмальная паста, желатин, метилцеллюлоза, карбоксиметилцеллюлоза натрия и/или поливинилпирролидин, и в некоторых случаях могут содержать разрыхлители или кипящие смеси, такие как крахмал, агар, альгиновая кислота или альгинат натрия, и/или абсорбенты, красители, ароматизаторы и подсластители.
Кроме того, согласно варианту осуществления в настоящем изобретении предусмотрена композиция функциональной оздоровительной продукции для профилактики или облегчения связанного с ангиогенезом заболевания глаз, содержащая соединение в качестве активного ингредиента.
Соединение, представленное Формулой 1 в соответствии с настоящим изобретением, может быть добавлено в пищу или может использоваться в комбинации с другим пищевым продуктом или ингредиентом пищевого продукта и может быть соответствующим образом использовано в соответствии с обычным способом. Количество смешанного активного ингредиента может быть соответствующим образом определено в соответствии с целью его использования (для профилактики или улучшения). Как правило, соединение может быть добавлено в продукт диетического питания в количестве от 0,1 до 90 частей по массе по отношению к общей массе продукта питания. Однако в случае длительного приема в целях здоровья и гигиены или в целях регулирования здоровья количество может быть ниже диапазона, определенного выше, и нет проблем с точки зрения безопасности, поэтому активный ингредиент может использоваться в количестве, превышающем указанный выше диапазон.
Кроме того, композиция функционального оздоровительного напитка по настоящему изобретению особо не ограничивается другими ингредиентами, за исключением того, что композиция функционального оздоровительного напитка содержит соединение в качестве основного ингредиента в заранее определенном соотношении и может содержать любой из различных ароматизаторов или натуральных углеводов, в качестве дополнительного ингредиента, как и обычные напитки. Примеры природных углеводов включают в себя: моносахариды, такие как глюкоза и фруктоза; дисахариды, такие как мальтоза и сахароза; и полисахариды, например, обычные сахара, такие как декстрин и циклодекстрин, и сахарные спирты, такие как ксилит, сорбит и эритрит. Примеры ароматизаторов, которые могут быть успешно использованы помимо описанных выше, включают в себя натуральные ароматизаторы (тауматин, экстракт стевии (например, ребаудиозид А, глицирризин и т.п.)) и синтетические ароматизаторы (сахарин, аспартам и т.п.). Соотношение природного углевода, как правило, составляет приблизительно от 1 до 20 г, предпочтительно приблизительно от 5 до 12 г, на 100 г композиции по настоящему изобретению.
Кроме того, в дополнение к описанным выше веществам соединение, представленное Формулой 1 в соответствии с настоящим изобретением, включает в себя различные питательные вещества, витамины, минералы (электролиты), ароматизаторы, такие как синтетические ароматизаторы и натуральные ароматизаторы, красители и наполнители (сыр, шоколад и т.п.), пектиновую кислоту и ее соли, альгиновую кислоту и ее соли, органические кислоты, защитные коллоидные загустители, регуляторы рН, стабилизаторы, консерванты, глицерин, спирты, газирующие средства, используемые в газированных напитках, и т.п. Кроме того, соединение, представленное Формулой 1 настоящего изобретения, может содержать мякоть для производства натуральных фруктовых соков, фруктовых напитков и овощных напитков.
Иллюстративные соединения, представленные в одном варианте осуществления настоящего изобретения, способны эффективно ингибировать HIF-1α и, таким образом, применимы в эффективном количестве в качестве фармацевтической композиции для профилактики или лечения связанного с ангиогенезом заболевания глаз, что будет подтверждено примерами и экспериментальными примерами, описанными ниже.
Далее настоящее изобретение будет подробно описано со ссылкой на примеры и экспериментальные примеры.
Однако примеры и экспериментальные примеры, описанные ниже, представлены только для иллюстрации настоящего изобретения, и настоящее изобретение этим не ограничивается.
<Пример 1> Получение 2-(3,4-диметоксифенил)-1-(4-гидрокси-2-метоксифенил)этан-1-она (31)
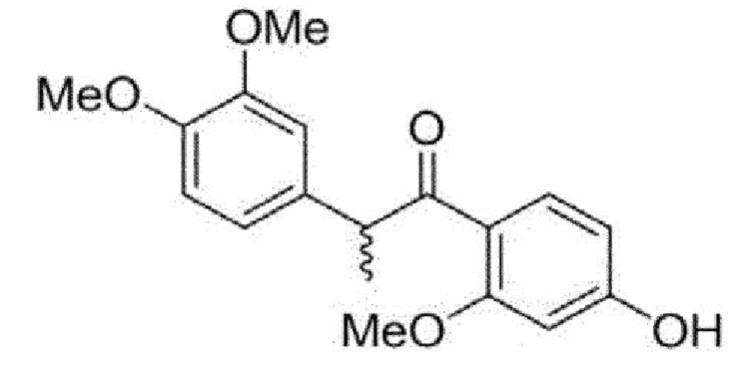
Раствор 2 н. HCl (10,0 мл) добавляли к раствору (877 мг, 2,4 ммоль) 2-(3,4-диметоксифенил)-1-(2-метокси-4-метоксиметокси)фенил)этан-1-она в метаноле. Реакционную смесь перемешивали при температуре 60°С в течение 4 часов и экстрагировали EtOAc. Органический слой собирали, промывали рассолом, сушили над безводным MgSO4 и концентрировали при пониженном давлении. Остаток очищали колоночной флэш-хроматографией на силикагеле (EtOAc/н-гексан = 1:1) с получением указанного в заголовке соединения (723 мг, 94%).
1H-ЯМР (CDCl3, 300 МГц) δ 7,71 (д, J=8,7 Гц, 1H), 6,79-6,71 (м, 3Н), 6,40-6,37 (м, 2Н), 5,52 (с, 1H), 4,19 (с, 2Н), 3,86 (с, 3Н), 3,82 (с, 6Н), 3,82 (с, 3Н).
<Пример 2> Получение 1-(2,4-диметоксифенил)-2-(3,4-диметоксифенил)пропан-1-она (32а)
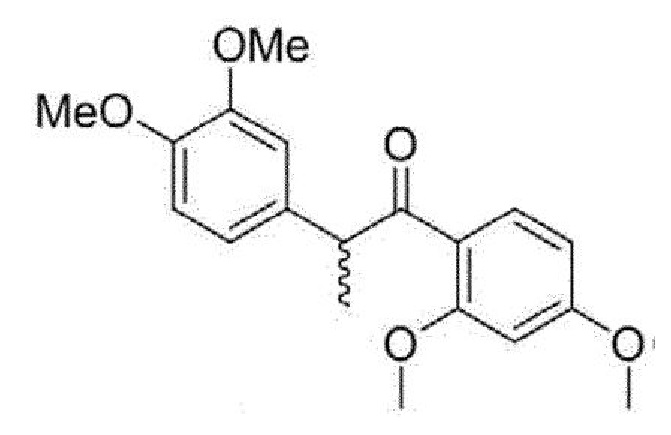
Карбонат цезия (52 мг, 0,2 ммоль) и йодметан (12,0 мкл, 0,2 ммоль) добавляли при температуре 0°С к раствору соединения примера 1 в ацетонитриле (1,0 мл). Реакционную смесь перемешивали при температуре 0°С в течение 20 минут, а затем перемешивали при комнатной температуре (приблизительно от 20 до 23°С) в течение 1 часа. Реакционную смесь обрабатывали водой для прекращения реакции и экстрагировали EtOAc. Органический слой собирали, промывали рассолом, сушили над безводным MgSO4 и концентрировали при пониженном давлении. Остаток очищали колоночной флэш-хроматографией на силикагеле (EtOAc/н-гексан=1:2) с получением указанного в заголовке соединения в виде желтого масла (25 мг, 71%).
1Н-ЯМР (CDCl3, 500 МГц) δ 7,60 (д, J=8,7 Гц, 1H), 6,72 (м, 3H), 6,42 (дд, J=8,7, 2,2 Гц, 1H), 6,35 (д, J=2,2 Гц, 1H), 4,68 (кв, J=7,0 Гц, 1H), 3,81 (с, 3H), 3,80 (с, 3H), 3,79 (с, 3H), 1,44 (д, J=7,0 Гц, 3H); 13С-ЯМР (CDCl3, 125 МГц) δ 201,8, 163,9, 159,8, 148,7, 147,6, 134,6, 132,8, 121,5, 120,2, 111,2, 111,0, 104,9, 98,3, 55,8, 55,7, 55,4, 55,3, 50,6, 19,1; HR-MS (ESI) вычислено для С19Н23О5 (М+Н+) 331,1540, обнаружено 331,1537.
<Пример 3> Получение 2-(3,4-диметоксифенил)-1-(4-этокси-2-метоксифенил)пропан-1-она (32b)
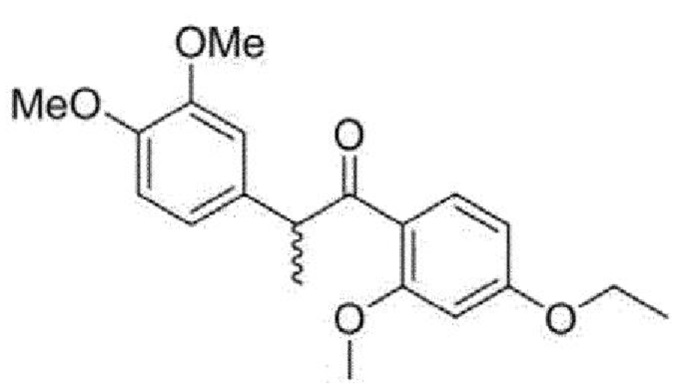
Указанное в заголовке соединение получали в виде бледно-желтого масла (10 мг, 91%) посредством процесса, аналогичного примеру 2, за исключением того, что использовали йодэтан (5,0 мкл, 0,1 ммоль) вместо йодметана.
1Н-ЯМР (CDCl3, 800 МГц) δ 7,60 (д, J=8,7 Гц, 1H), 6,73 (м, 3H), 6,41 (дд, J=8,7, 2,2 Гц, 1H), 6,35 (д, J=2,2 Гц, 1H), 4,68 (кв, J=6,9 Гц, 1H), 4,01 (кв, J=7,0 Гц, 1H), 3,81 (с, 6Н), 3,80 (с, 3H), 1,44 (д, J=7,0 Гц, 3H), 1,38 (т, J=7,0 Гц, 3H); 13С-ЯМР (CDCl3, 200 МГц) δ 201,8, 163,3, 159,8, 148,7, 147,5, 134,6, 132,8, 121,2, 120,2, 111,1, 110,9, 105,4, 98,8, 63,6, 55,7, 55,7, 55,3, 50,5, 19,1, 14,6; HR-MS (ESI) вычислено для С20Н25О5 (М+Н+) 345,1697, обнаружено 345,1695.
<Пример 4> Получение 1-(4-(циклогексилокси)-2-метоксифенил)-2-(3,4-диметоксифенил)пропан-1-она (32с)
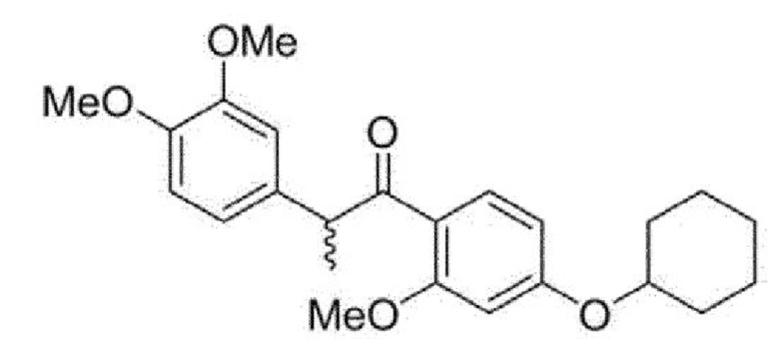
Раствор диэтилазодикарбоксилата (0,02 мл, 0,1 ммоль) в ТГФ (1,0 мл) добавляли к раствору соединения примера 1 (26 мг, 0,1 ммоль), циклогексанола (9 мкл, 0,1 ммоль) и трифенилфосфина (22 мг, 0,1 ммоль) в ТГФ (1,0 мл). Реакционную смесь перемешивали в течение одного дня и концентрировали при пониженном давлении. Остаток очищали колоночной флэш-хроматографией на силикагеле (EtOAc/н-гексан = 1:6) с получением указанного в заголовке соединения в виде бесцветного масла (42 мг, 43%).
1Н-ЯМР (CDCl3, 500 МГц) δ 7,59 (д, J=8,7 Гц, 1H), 6,73 (м, 3H), 6,41 (дд, J=8,7, 2,1 Гц, 1H), 6,34 (д, J=2,1 Гц, 1H), 4,69 (кв, J=6,9 Гц, 1H), 4,26-4,22 (м, 1H), 3,80 (с, 6Н), 3,79 (с, 3H), 1,96-1,90 (м, 2Н), 1,79-1,73 (м, 2Н), 1,54-1,46 (м, 2Н), 1,33-1,27 (м, 4Н); 13С-ЯМР (CDCl3, 125 МГц) δ 201,7, 162,4, 160,0, 148,8, 147,6, 134,7, 132,8, 121,0, 120,2, 111,2, 111,0, 106,3, 100,0, 75,4, 55,8 (два атома углерода), 55,3, 50,5, 31,7, 31,6, 25,4, 23,6 (два атома углерода), 19,2; HR-MS (ESI) вычислено для С24Н31О5 (М+Н+) 399,2166, обнаружено 399,2164.
<Пример 5> Получение 2-(3,4-диметоксифенил)-1-(4-(диметиламино)-2-метоксифенил)пропан-1-она (34а)
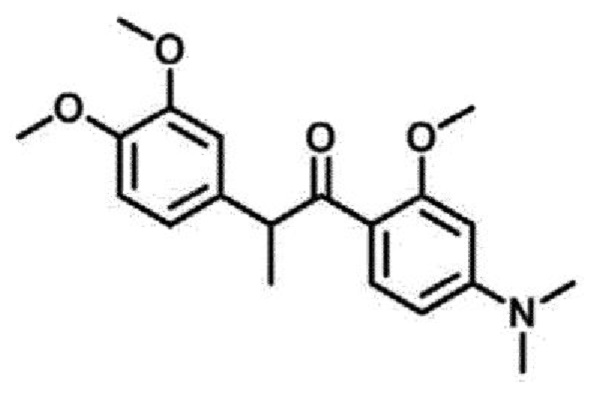
4-(2-(3,4-диметоксифенил)пропаноил)-3-метоксифенилтрифторметансульфонат (20 мг, 0,04 ммоль) обрабатывали диметиламином (2,0 М раствор ТГФ, 0,23 мл, 0,5 ммоль) для проведения аминирования, и полученный продукт очищали колоночной флэш-хроматографией на силикагеле (EtOAc/н-гексан = от 1:3 до 1:1) с получением указанного в заголовке соединения в виде желтого масла (6 мг, 41%).
1Н-ЯМР (CDCl3, 800 МГц) δ 7,71 (д, J=8,9 Гц, 1H), 6,79 (с, 1H), 6,78 (д, J=8,2 Гц, 1H), 6,72 (д, J=8,2 Гц, 1H), 6,22 (дд, J=8,9, 2,2 Гц, 1H), 5,98 (д, J=2,0 Гц, 1Н), 4,74 (кв, J=7,0 Гц, 1H), 3,82 (с, 3H), 3,81 (с, 3H), 3,79 (с, 3H), 2,99 (с, 6Н), 1,42 (д, J=7,0 Гц, 3H); 13С-ЯМР(COCl3, 200 МГц) δ 200,3, 160,7, 154,4, 148,6, 147,3, 135,6, 133,2, 120,1, 115,9, 111,1, 110,9, 104,3, 93,8, 55,7 (два атома углерода), 54,9, 50,0, 40,0 (два атома углерода), 19,6; HR-MS (ESI) вычислено для C20H26NO4 (М+Н+) 344,1856, обнаружено 344,1860.
<Пример 6> Получение 2-(3,4-диметоксифенил)-1-(2-метокси-4-(пирролидин-1-ил)фенил)пропан-1-она (34b)
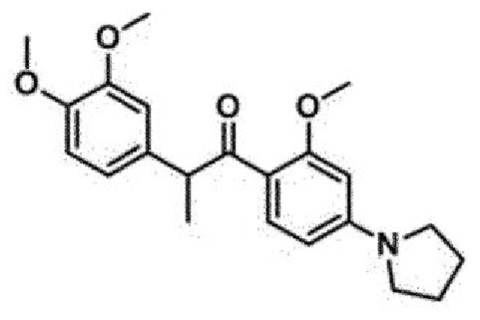
4-(2-(3,4-диметоксифенил)пропаноил)-3-метоксифенилтрифторметансульфонат (20 мг, 0,04 ммоль) обрабатывали пирролидином (7 мкл, 0,1 ммоль) для проведения аминирования, и полученный продукт очищали с помощью колоночной флэш-хроматографии на силикагеле (EtOAc/н-гексан = от 1:2 до 1:1) с получением указанного в заголовке соединения в виде бледно-желтого масла (19 мг, 90%).
1Н ЯМР (CDCl3, 300 МГц) δ 7,67 (дд, J=8,7, 1,2 Гц, 1H), 6,75-6,65 (м, 3H), 6,04 (дд, J=8,7, 2,0 Гц, 1H), 5,79 (с, 1H), 4,69 (кв, J=6,9 Гц, 1H), 3,77-3,72 (м, 9Н), 3,24-3,22 (м, 4Н), 1,97-1,90 (м, 4Н), 1,37 (д, 3Н, J=6,9 Гц); 13С ЯМР (CDCl3, 200 МГц) δ 200,1, 160,9, 152,0, 148,6, 147,3, 135,7, 133,4, 120,1, 115,3, 111,1, 110,9, 104,4, 93,6, 55,7 (два атома углерода), 54,9, 49,9, 47,5 (два атома углерода), 25,3 (два атома углерода), 19,7; HR-MS (FAB) вычислено для C22H28NO4 (М+Н+) 370,2018, обнаружено 370,2032.
<Пример 7> Получение 2-(3,4-диметоксифенил)-1-(2-метокси-4-(пиперидин-1-ил)фенил)пропан-1-она (34с)
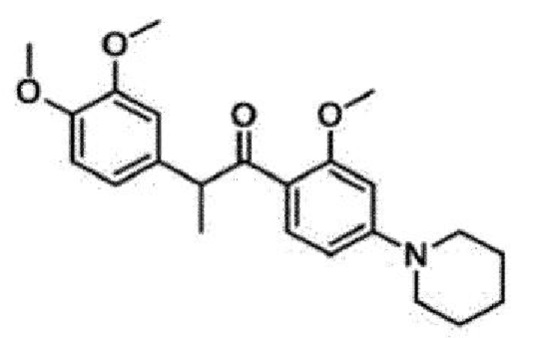
4-(2-(3,4-диметоксифенил)пропаноил)-3-метоксифенилтрифторметансульфонат (20 мг, 0,04 ммоль) обрабатывали пиперидином (8 мкл, 0,1 ммоль) для проведения аминирования, и полученный продукт очищали с помощью колоночной флэш-хроматографии на силикагеле (EtOAc/н-гексан=1:2) с получением указанного в заголовке соединения в виде бледно-желтого масла (10 мг, 45%).
1Н-ЯМР (CDCl3, 300 МГц) δ 7,61 (д, J=8,7 Гц, 1H), 6,73-6,65 (м, 3H), 6,35 (дд, J=8,7, 2,1 Гц, 1H), 6,16 (д, J=1,8 Гц, 1H), 4,67 (кв, J=6,9 Гц, 1H), 3,76 (с, 6Н), 3,75 (с, 3H), 3,21-3,20 (м, 4Н), 1,65-1,60 (м, 6Н) 1,37 (д, 3Н, J=6,9 Гц); 13С ЯМР (CDCl3, 200 МГц) δ 200,5, 160,4, 155,5, 148,6, 147,3, 135,3, 133,0, 120,1, 117,4, 111,1, 110,9, 106,8, 96,8, 55,7 (два атома углерода), 55,0, 50,1, 48,8 (два атома углерода), 25,4 (два атома углерода), 24,3, 19,5; HR-MS (FAB) вычислено для C23H30NO4 (М+Н+) 384,2175, обнаружено 384,2170.
<Пример 8> Получение 2-(3,4-диметоксифенил)-1-(2-метокси-4-морфолинофенил)пропан-1-она (34d)
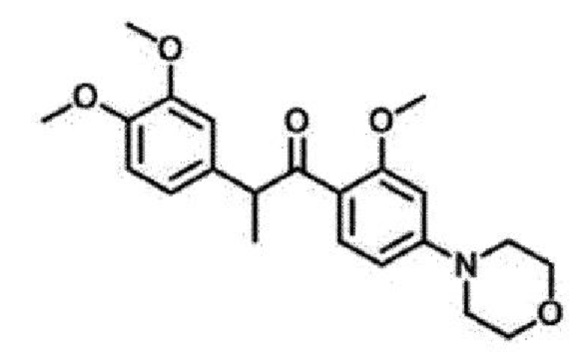
4-(2-(3,4-диметоксифенил)пропаноил)-3-метоксифенилтрифторметансульфонат (20 мг, 0,04 ммоль) обрабатывали морфолином (4 мг, 0,04 ммоль) для проведения аминирования, и полученный продукт очищали с помощью колоночной флэш-хроматографии на силикагеле (EtOAc/н-гексан = от 1:2 до 2:1) с получением указанного в заголовке соединения в виде желтого масла (7 мг, 53%).
1Н-ЯМР (CDCl3, 800 МГц) δ 7,65 (д, J=8,8 Гц, 1H), 6,75 (м, 2Н), 6,72 (д, J=8,0 Гц, 1H), 6,40 (дд, J=8,9, 2,2 Гц, 1Н), 6,23 (д, J=2,2 Гц, 1H), 4,70 (кв, J=6,9 Гц, 1H), 3,82 (с, 3H), 3,90-3,70 (м, 10Н), 3,22 (дд, J=5,9, 3,9 Гц, 4Н), 1,43 (д, J=7,0 Гц, 3H); 13С-ЯМР (CDCl3, 200 МГц) δ 200,9, 160,1, 155,2, 148,7, 147,4, 135,0, 132,9, 120,2, 119,0, 111,1, 110,9, 106,6, 96,9, 66,5 (два атома углерода), 55,7, 55,7, 55,1, 50,3, 47,7 (два атома углерода), 19,4; HR-MS (ESI) вычислено для C22H28NO5 (М+Н+) 386,1962, обнаружено 386,1963.
<Пример 9> Получение 1-(4-(бензиламино)-2-метоксифенил)-2-(3,4-диметоксифенил)пропан-1-она (34е)
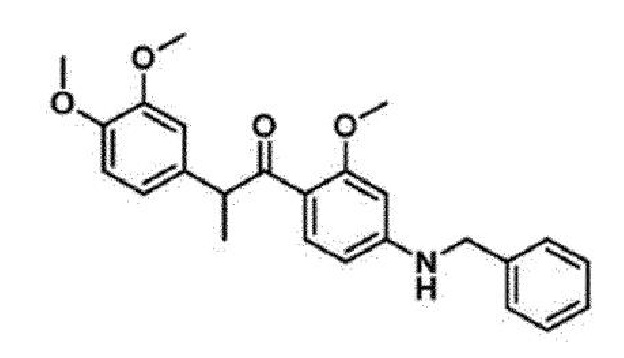
4-(2-(3,4-диметоксифенил)пропаноил)-3-метоксифенилтрифторметансульфонат (20 мг, 0,04 ммоль) обрабатывали бензиламином (0,01 мл, 0,084 ммоль) для проведения аминирования, и полученный продукт очищали с помощью колоночной флэш-хроматографии на силикагеле (EtOAc/н-гексан=1:2) с получением указанного в заголовке соединения в виде желтого масла (20 мг, 88%).
1H-ЯМР (ацетон-d6, 300 МГц) δ 7,55 (д, 1H, J=8,6 Гц), 7,39-7,36 (м, 2Н), 7,33-7,28 (м, 2Н), 7,22 (м, 1H), 6,86 (д, 1H, J=1,8 Гц), 6,78-6,70 (м, 2Н), 6,26-6,18 (м, 3H), 4,78 (кв, 1H, J=6,9 Гц), 4,40 (д, 2Н, J=5,6 Гц), 3,79 (с, 3H), 3,74 (с, 3H), 3,71 (с, 3H), 1,33 (д, 3Н, J=6,9 Гц); 13С-ЯМР (CDCl3, 200 МГц) δ 200,4, 160,8, 152,9, 148,7, 147,4, 138,3, 135,4, 133,5, 128,8 (два атома углерода), 127,5, 127,4 (два атома углерода), 120,1, 117,4, 111,2, 110,9, 105,1, 94,7, 55,8 (два атома углерода), 55, 50, 47,7, 19,6; HRMS (FAB) вычислено для C25H28NO4 (М+Н+): 406,2018, обнаружено: 406,2024.
<Пример 10> Получение 4-(((4-(2-(3,4-диметоксифенил)пропаноил)фенил)амино)метил)бензонитрила (34f)
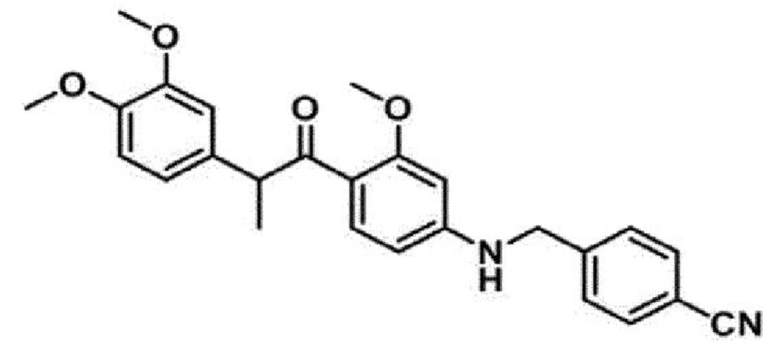
4-(2-(3,4-диметоксифенил)пропаноил)-3-метоксифенилтрифторметансульфонат (20 мг, 0,04 ммоль) обрабатывали 4-цианобензиламином (10,8 мг, 0,082 ммоль) для проведения аминирования, и полученный продукт очищали с помощью колоночной флэш-хроматографии на силикагеле (EtOAc/н-гексан=1:2) с получением указанного в заголовке соединения в виде желтого масла (16 мг, 91%).
1Н-ЯМР (CDCl3, 800 МГц) δ 7,61 (д, 1H, J=8,6 Гц), 7,60 (д, 2Н, J=8,2 Гц), 7,41 (д, 2Н, J=8,2 Гц), 6,76 (с, 1H), 6,74 (д, 1H, J=1,9 Гц), 6,72 (д, 1H, J=8,0 Гц), 6,10 (дд, 1H, J=8,6, 2,2 Гц), 5,94 (д, 1H, J=2,1 Гц), 4,68 (кв, 1H, J=7,0 Гц), 4,58 (т, 1H, J=5,8 Гц), 4,42 (д, 2Н, J=5,8 Гц), 3,80 (с, 3H), 3,80 (с, 3H), 3,72 (с, 3H), 1,41 (д, 3Н, J=7,0 Гц); 13С-ЯМР (CDCl3, 200 МГц) δ 200,6, 160,6, 152,2, 148,7, 147,4, 144,1, 135,2, 133,6, 132,6 (два атома углерода), 127,6 (два атома углерода), 120,2, 118,6, 118,1, 111,4, 111,2, 110,9, 105,0, 95,1, 55,8 (два атома углерода), 55,0, 50,2, 47,2, 19,6; HRMS (ESI) вычислено для C26H26N2O4 (М+Н+): 430,1893, обнаружено: 430,1887.
<Пример 11> Получение 2-(3,4-диметоксифенил)-1-(4-(пирролидин-1-ил)фенил)пропан-1-она (37а)
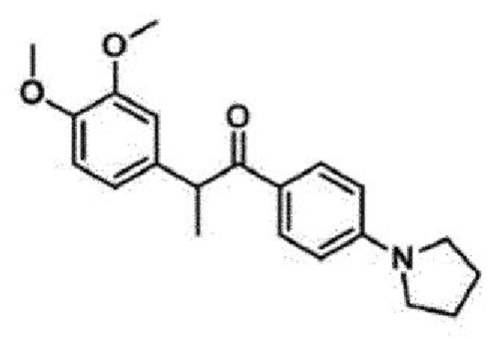
1-(4-бромфенил)-2-(3,4-диметоксифенил)пропан-1-он (23 мг, 0,1 ммоль) обрабатывали пирролидином (15 мкл, 0,2 ммоль) для проведения аминирования, и полученный продукт очищали с помощью колоночной флэш-хроматографии на силикагеле (EtOAc/н-гексан=1:6) с получением указанного в заголовке соединения в виде бледно-желтого масла (11 мг, 57%).
1Н-ЯМР (CDCl3, 500 МГц) δ 7,87 (д, J=8,9 Гц, 2Н), 6,83 (дд, J=8,1, 1,8 Гц, 1H), 6,79 (д, J=1,8 Гц, 1H), 6,74 (д, J=8,2 Гц, 1H), 6,42 (д, J=8,9 Гц, 2Н), 4,55 (кв, J=6,8 Гц, 1H), 3,82 (с, 3H), 3,79 (с, 3H), 3,29 (т, J=6,6 Гц, 4Н), 2,00-1,96 (м, 4Н), 1,46 (д, J=6,8 Гц, 3H); 13С ЯМР (CDCl3, 125 МГц) δ 198,4, 150,7, 149,0, 147,6, 135,3, 131,0, 131,0, 123,8, 119,8, 111,3, 110,6, 110,6, 110,5, 55,8, 55,8, 47,4, 47,4, 46,2, 25,3, 25,3, 19,6; HR-MS (FAB) вычислено для C21H26NO3 (М+Н+) 340,1913, обнаружено 340,1904.
<Пример 12> Получение 2-(3,4-диметоксифенил)-1-(4-морфолинофенил)пропан-1-она (37b)

1-(4-бромфенил)-2-(3,4-диметоксифенил)пропан-1-он (23 мг, 0,1 ммоль) обрабатывали морфолином (5 мг, 0,1 ммоль) для проведения аминирования, и полученный продукт очищали с помощью колоночной флэш-хроматографии на силикагеле (EtOAc/н-гексан = от 1:2 до 1:1) с получением указанного в заголовке соединения в виде желтого масла (12 мг, 80%).
1Н-ЯМР (CDCl3, 800 МГц) δ 7,88 (д, J=9,1 Гц, 2Н), 6,81 (дд, J=8,2, 2,1 Гц, 1H), 6,76 (м, 4Н), 4,54 (кв, J=6,8 Гц, 1H), 3,82 (с, 3H), 3,79 (с, 6Н), 3,23 (т, J=5,0 Гц, 4Н), 1,45 (д, J=6,9 Гц, 3H); 13С-ЯМР (CDCl3, 200 МГц) δ 198,7, 153,9, 149,1, 147,7, 134,7, 130,7 (два атома углерода), 127,1, 119,9, 113,2 (два атома углерода), 111,3, 110,5, 66,5 (два атома углерода), 55,8, 55,8, 47,4 (два атома углерода), 46,7, 19,5; HR-MS (ESI) вычислено для C21H26NO4 (М+Н+) 356,1856, обнаружено 356,1851.
<Пример 13> Получение 2-(2-фторфенил)-1-(4-(пиперидин-1-ил)фенил)пропан-1-она (41а)
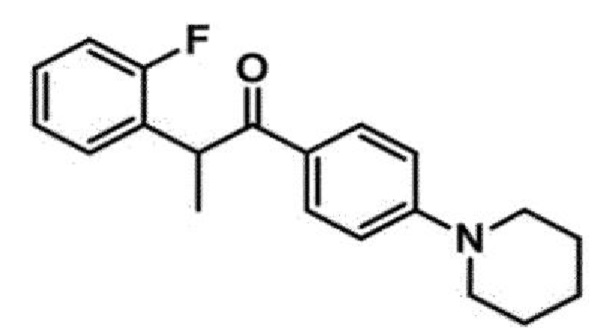
1-(4-бромфенил)-2-(2-фторфенил)пропан-1-он (31 мг, 0,1 ммоль) обрабатывали пиперидином (15 мкл, 0,2 ммоль) для проведения аминирования, и полученный продукт очищали с помощью колоночной флэш-хроматографии на силикагеле (EtOAc/н-гексан=1:5) с получением указанного в заголовке соединения в виде желтого твердого вещества (24 мг, 68%).
1H-ЯМР (CDCl3, 800 МГц) δ 7,85 (д, 2Н, J=9,0 Гц), 7,24-7,22 (м, 1H), 7,15-7,12 (м, 1H), 7,02 (д, 1H, J=8,3 Гц), 7,01 (д, 1H, J=8,2 Гц), 6,76 (д, 2Н, J=9,0 Гц), 4,96 (кв, 1H, J=6,9 Гц), 3,30 (с, 4Н), 1,61 (с, 6Н), 1,47 (д, 3Н, J=6,9 Гц); 13С-ЯМР (CDCl3, 200 МГц) δ 197,8, 159,6 (д, JC-F=243 Гц), 154,2, 130,7, 129,3, 129,2, 128,9 (д, JC-F=3,9 Гц), 128,2, 128,1, 125,2, 124,5 (д, JC-F=3,3 Гц), 115,4 (д, JC-F=22,5 Гц), 113,2, 48,4, 38,4, 38,4, 25,3 (два атома углерода), 24,3, 18,2;
<Пример 14> Получение 1-(4-(бензиламино)фенил)-2-(2-фторфенил)пропан-1-она (41b)
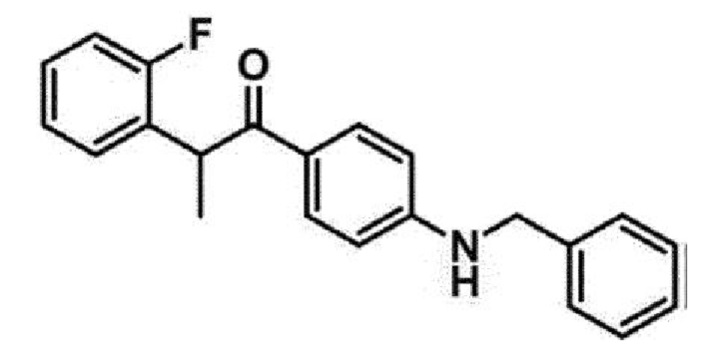
1-(4-бромфенил)-2-(2-фторфенил)пропан-1-он (24 мг, 0,1 ммоль) обрабатывали морфолином (13 мкл, 0,1 ммоль) для проведения аминирования, и полученный продукт очищали с помощью колоночной флэш-хроматографии на силикагеле (EtOAc/н-гексан=1:5) с получением указанного в заголовке соединения в виде белого твердого вещества (18 мг, 71%).
1H-ЯМР (CDCl3, 600 МГц) δ 7,83-7,82 (м, 2Н), 7,33-7,25 (м, 5Н), 7,22-7,21 (м, 2Н), 7,15-7,12 (м, 2Н), 7,02-6,99 (м, 2Н), 6,52-6,51 (м, 2Н), 4,94 (кв, 1H, J=8,6 Гц), 4,53 (широкий, 1H), 4,33 (с, 2Н), 1,46 (д, 3Н, J=6,9 Гц); 13С-ЯМР (CDCl3, 150 МГц) δ 197,7, 159,6 (д, JC-F=243 Гц), 151,8, 138,1, 131,0, 131,0, 129,2 (д, JC-F=15,0 Гц), 128,8 (д, JC-F=4,3 Гц), 128,7, 128,7, 128,1 (d, JC-F=7,8 Гц), 127,5, 127,3, 127,3, 125,6, 124,5 (d, JC-F=3,5 Гц), 115,3 (d, JC-F=22,2 Гц), 111,6, 111,6, 47,5, 38,3 (д, JC-F=2,1 Гц), 18,2; HRMS (ESI) вычислено для C22H21FNO (М+Н+): 334,1607, обнаружено: 334,1611.
<Пример 15> Получение 2-(2-фторфенил)-1-(2-метокси-4-(пиперидин-1-ил)фенил)пропан-1-она
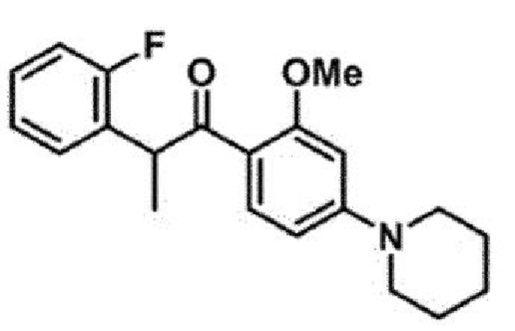
LR-MS (ESI) вычислено для C21H25FNO2 (M+H+) 342,4, обнаружено 342,4.
<Пример 16> Получение 4-(((4-(2-(2-фторфенил)пропаноил)-3-метоксифенил)амино)метил)бензонитрила
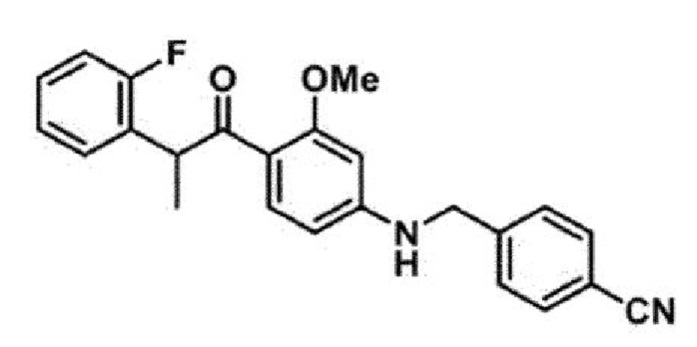
LR-MS (ESI) вычислено для C24H22FN2O2 (М+Н+) 389,4, обнаружено 389,4.
Структуры соединений примеров 1-16 описанных выше соединений показаны в таблице 1 ниже:
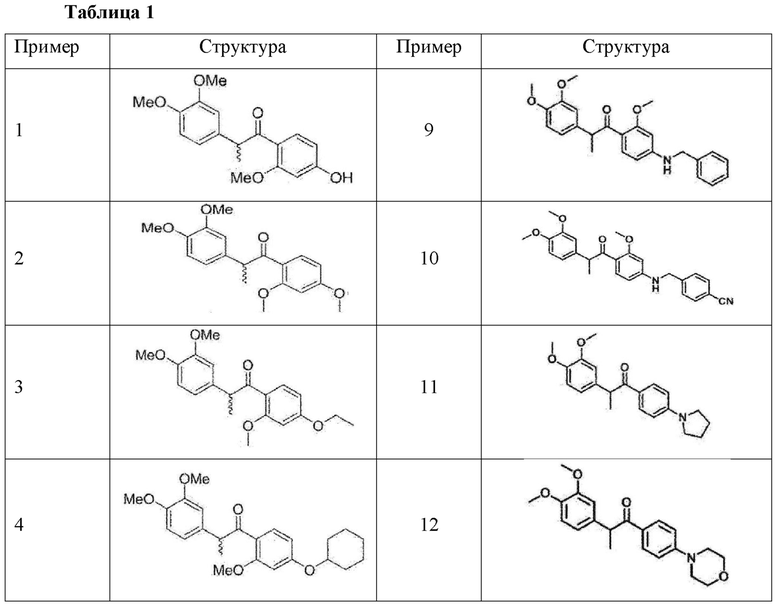
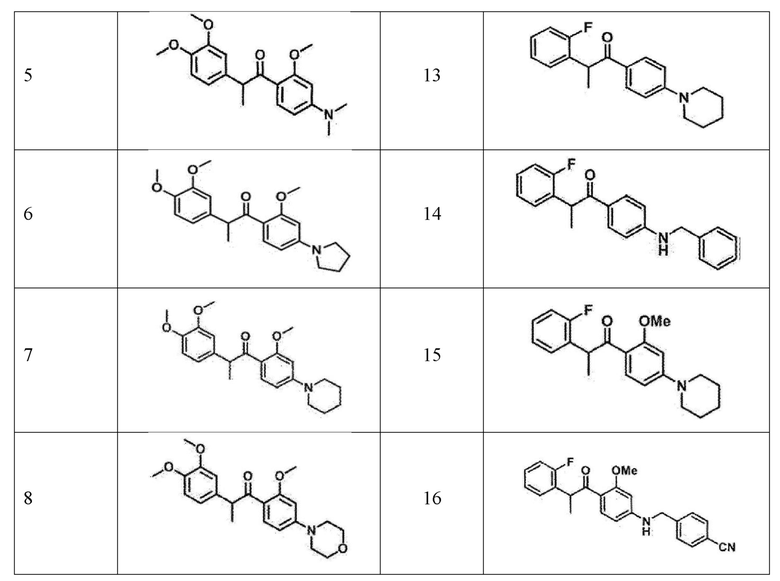
<Сравнительный пример 1> Получение соединения SH-1242 (2)
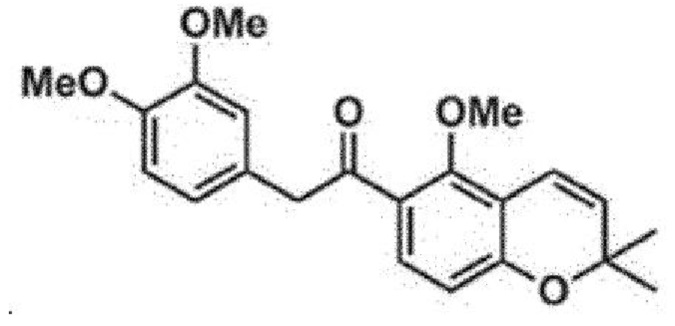
Соединение сравнительного примера 1 получали со ссылкой на литературу ((J. Mol. Med. (Berl.) 2014, 92, 1083-1092 (Опосредованная гипоксией неоваскуляризация сетчатки и транссудация в сетчатке при сахарном диабете подавляется дестабилизацией HIF-1α с помощью SH-1242 и SH-1280, новых ингибиторов hsp90)).
Экспериментальный пример 1> Оценка ингибирующей активности HIF-1α (in vitro)
Следующий эксперимент проводили для оценки ингибирующей активности против HIF-1α (индуцируемого гипоксией фактора 1α) соединения Примера согласно варианту осуществления настоящего изобретения.
Результаты показаны в таблице 2 ниже.
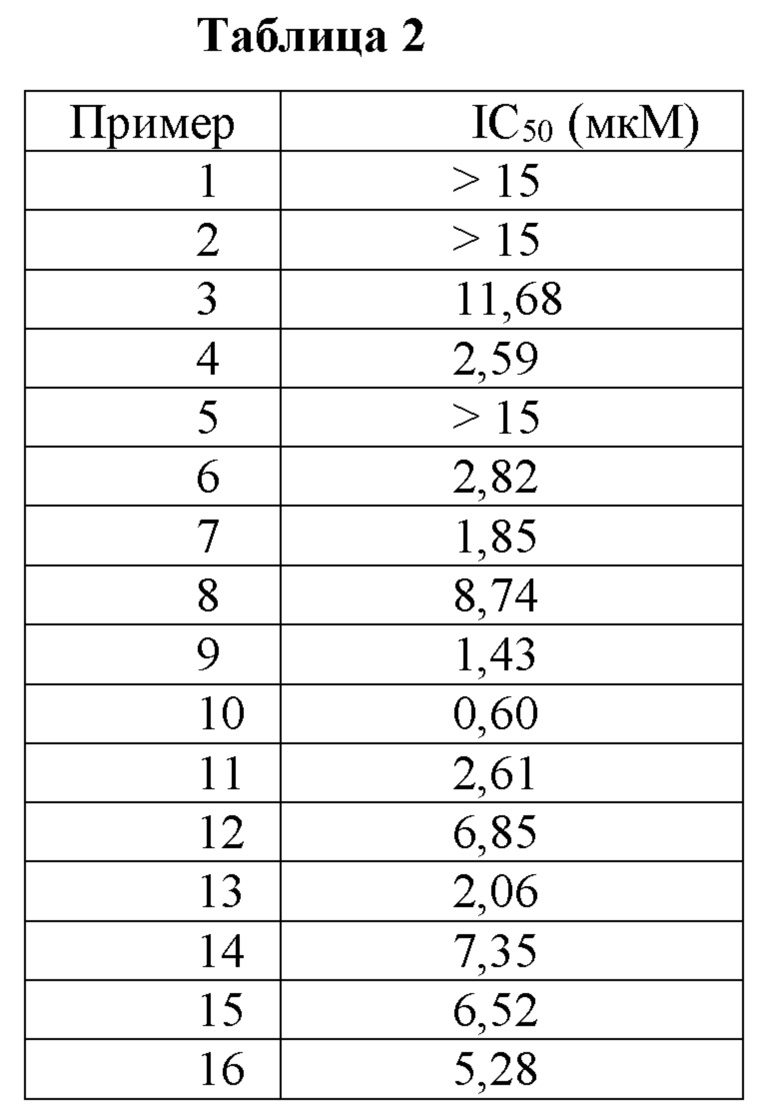
Как видно из таблицы 2 выше, соединение Примера согласно варианту осуществления настоящего изобретения проявляет превосходную ингибирующую активность против HIF-1α (индуцируемого гипоксией фактора 1α). В частности, среди соединений Примера соединение примера 10 проявляет лучшую ингибирующую активность против HIF-1α.
<Экспериментальный пример 2> Оценка ингибирующей активности против ангиогенеза (in vitro)
Следующий эксперимент проводили для того, чтобы оценить ингибирующую активность против ангиогенеза соединения Примера согласно варианту осуществления настоящего изобретения.
Результаты показаны на фиг. 1.
Фиг. 1 представляет собой график, на котором показаны результаты анализа ингибирующей активности против ангиогенеза соединения Примера согласно варианту осуществления настоящего изобретения, причем соединение 2 представляет собой соединение сравнительного примера 1, а соединение 34f представляет собой соединение примера 10.
Как видно из фиг. 1, соединение примера 10 согласно настоящему изобретению обладает лучшей ингибирующей активностью против ангиогенеза, чем соединение сравнительного примера 1.
<Экспериментальный пример 3> Оценка регуляторной активности HIF-1α (in vitro)
Следующий эксперимент проводили для оценки регуляторной активности HIF-1α (индуцируемого гипоксией фактора 1α) соединения Примера согласно варианту осуществления настоящего изобретения.
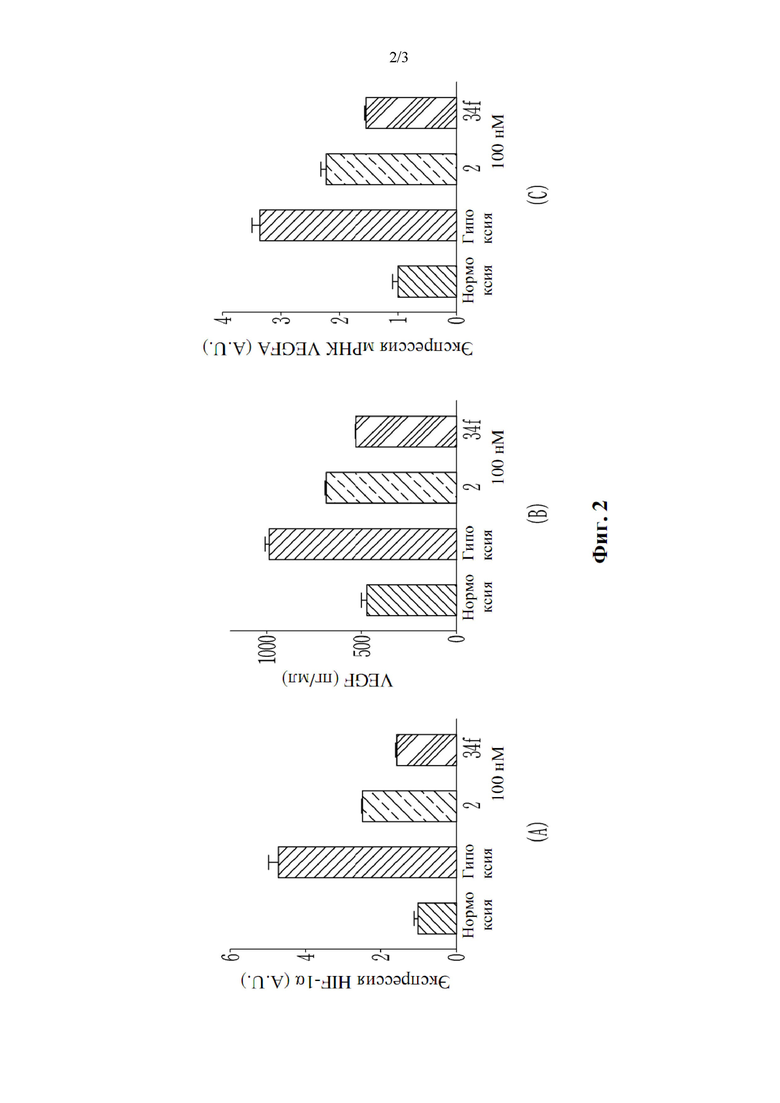
Результаты показаны на фиг. 2.
Фиг. 2 представляет собой график, на котором показаны результаты анализа регуляторной активности HIF-1α (индуцируемого гипоксией фактора 1α) соединения Примера согласно варианту осуществления настоящего изобретения, причем соединение 2 представляет собой соединение сравнительного примера 1, а соединение 34f представляет собой соединение примера 10.
Как видно из фиг. 2, соединение примера 10 согласно настоящему изобретению обладает лучшей регулирующей активностью HIF-1α, чем соединение сравнительного примера 1.
<Экспериментальный пример 4> Оценка ингибирующей активности против вызванной гипоксией неоваскуляризации сетчатки.
Следующий эксперимент проводили для того, чтобы оценить ингибирующую активность против вызванной гипоксией неоваскуляризации сетчатки соединения Примера согласно варианту осуществления настоящего изобретения.
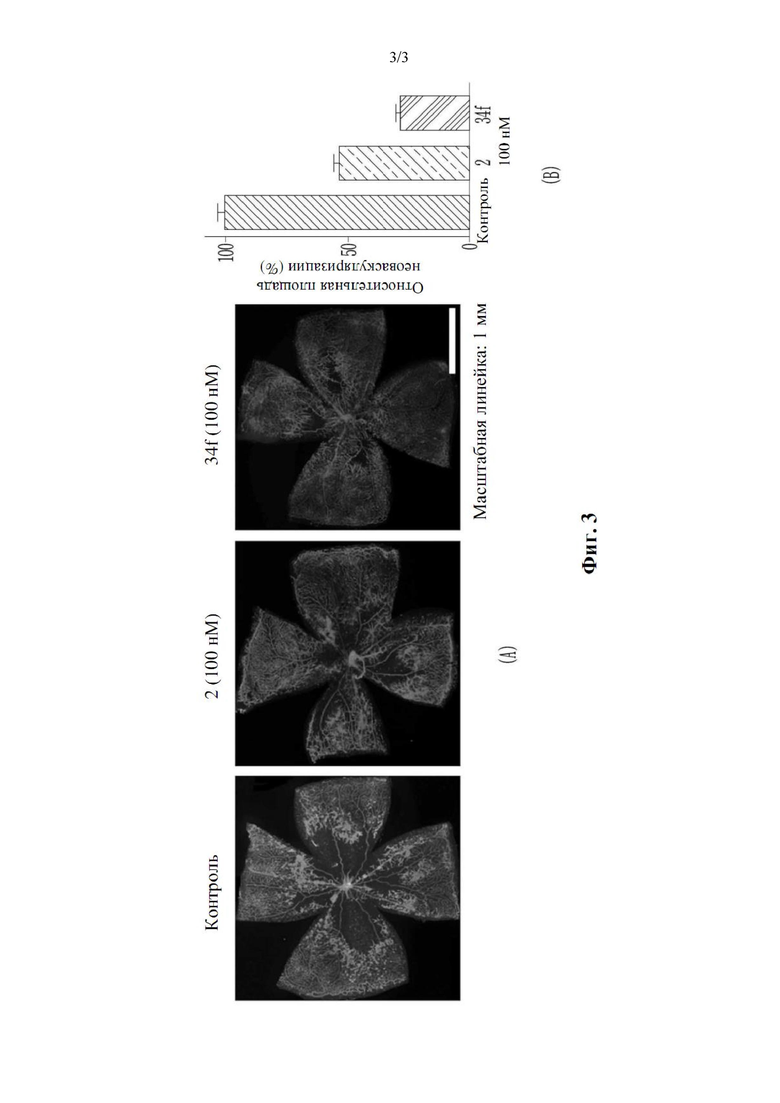
Результаты показаны на фиг. 3.
Фиг. 3 представляет собой график, на котором показаны результаты анализа ингибирующей активности против вызванной гипоксией неоваскуляризации сетчатки соединения Примера согласно варианту осуществления настоящего изобретения, причем соединение 2 представляет собой соединение сравнительного примера 1, а соединение 34f представляет собой соединение примера 10.
Как видно из фиг. 3, соединение примера 10 согласно настоящему изобретению обладает лучшей ингибирующей активностью против вызванной гипоксией неоваскуляризации сетчатки, чем соединение сравнительного примера 1.
<Пример состава 1> Приготовление фармацевтического состава
1-1. Приготовление порошка
Описанные выше ингредиенты смешивают, и полученную смесь загружают в воздухонепроницаемую ткань для приготовления порошка.
1-2. Приготовление таблетки
Описанные выше ингредиенты смешивают, и полученную смесь подвергают таблетированию в соответствии с обычным способом приготовления таблеток для получения таблетки.
1-3. Приготовление капсулы
Описанные выше ингредиенты смешивают обычным способом приготовления капсулы, и полученную смесь загружают в желатиновую капсулу для получения капсулы.
1-4. Приготовление инъекции
Инъекцию готовят, загружая количества описанных выше ингредиентов в каждую дозу (2 мл) в соответствии с обычным способом приготовления инъекции.
1-5. Приготовление жидкости/раствора
В соответствии с обычным способом приготовления жидкости каждый ингредиент растворяют в очищенной воде, к полученному раствору добавляют соответствующее количество лимонного ароматизатора, ингредиенты смешивают вместе, добавляют очищенную воду, чтобы довести общее количество до 100 мл, и полученную смесь загружают в коричневый флакон с последующей стерилизацией для приготовления жидкости.
| название | год | авторы | номер документа |
|---|---|---|---|
| ИНГИБИТОРЫ ПРОЛИЛГИДРОКСИЛАЗЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2007 |
|
RU2429226C9 |
| ГЕТЕРОЦИКЛИЧЕСКИЕ МОДУЛЯТОРЫ АКТИВНОСТИ HIF ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ | 2013 |
|
RU2698197C2 |
| ИНГИБИТОРЫ ПРОЛИЛГИДРОКСИЛАЗЫ | 2010 |
|
RU2518071C2 |
| СОЕДИНЕНИЯ АЗАЛАКТАМА В КАЧЕСТВЕ ИНГИБИТОРОВ HPK1 | 2021 |
|
RU2819642C1 |
| НОВЫЕ ПРОИЗВОДНЫЕ ПИРИДИНА, СПОСОБ ИХ ПОЛУЧЕНИЯ И СОДЕРЖАЩАЯ ИХ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2004 |
|
RU2366659C2 |
| ИНДАЗОЛЬНЫЕ СОЕДИНЕНИЯ В КАЧЕСТВЕ ИНГИБИТОРОВ КИНАЗЫ FGFR, ИХ ПОЛУЧЕНИЕ И ПРИМЕНЕНИЕ | 2015 |
|
RU2719428C2 |
| ИНГИБИТОРНЫЕ СОЕДИНЕНИЯ | 2013 |
|
RU2673079C2 |
| ИНГИБИТОРЫ ПРОТЕИНКИНАЗЫ MKK4 ДЛЯ СТИМУЛЯЦИИ РЕГЕНЕРАЦИИ ПЕЧЕНИ ИЛИ УМЕНЬШЕНИЯ ИЛИ ПРЕДОТВРАЩЕНИЯ ГИБЕЛИ ГЕПАТОЦИТОВ | 2019 |
|
RU2788000C2 |
| ИНГИБИТОРЫ ТИРОЗИНФОСФАТАЗЫ БЕЛКА ЧЕЛОВЕКА И СПОСОБЫ ПРИМЕНЕНИЯ | 2007 |
|
RU2435763C2 |
| ИНГИБИТОРЫ СЕТР | 2006 |
|
RU2513107C2 |

Настоящее изобретение относится к соединению, представленному следующей Формулой (1), которое используется для лечения или профилактики возрастной макулярной дегенерации, диабетической ретинопатии, ретинопатии недоношенных или неоваскулярной глаукомы, к содержащей данное соединение фармацевтической композиции и к способу лечения или профилактики возрастной макулярной дегенерации, диабетической ретинопатии, ретинопатии недоношенных или неоваскулярной глаукомы с использованием данного соединения.
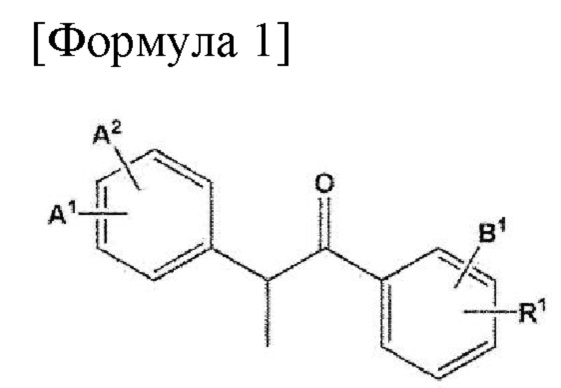
В формуле 1 А1 и А2, каждый независимо, представляют собой -Н, галоген или метокси; В1 представляет собой –Н или метокси; R1 представляет собой С3-10 циклоалкилокси, гетероциклоалкил с 5- или 6-членным кольцом, содержащий по меньшей мере один гетероатом, выбранный из группы, состоящей из N, О и S, или бензиламино; причем бензильная группа может опционально быть замещена по меньшей мере одним -CN. Технический результат – предоставлено соединение для профилактики или лечения связанного с ангиогенезом заболевания глаз. 3 н. и 3 з.п. ф-лы, 3 ил., 2 табл., 21 пр.
1. Соединение, представленное следующей Формулой (1):
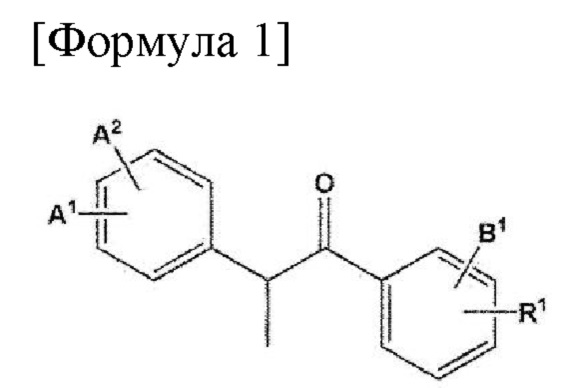
где А1 и А2, каждый независимо, представляют собой -Н, галоген или метокси;
В1 представляет собой –Н или метокси; а также
R1 представляет собой С3-10 циклоалкилокси, гетероциклоалкил с 5- или 6-членным кольцом, содержащий по меньшей мере один гетероатом, выбранный из группы, состоящей из N, О и S, или бензиламино;
причем бензильная группа может опционально быть замещена по меньшей мере одним
-CN.
2. Соединение по п. 1, в котором А1 и А2 представляют собой метокси или А1 представляет собой Н и А2 представляет собой F.
3. Соединение по п. 1, причем соединение формулы 1 выбрано из группы, состоящей из следующих соединений:
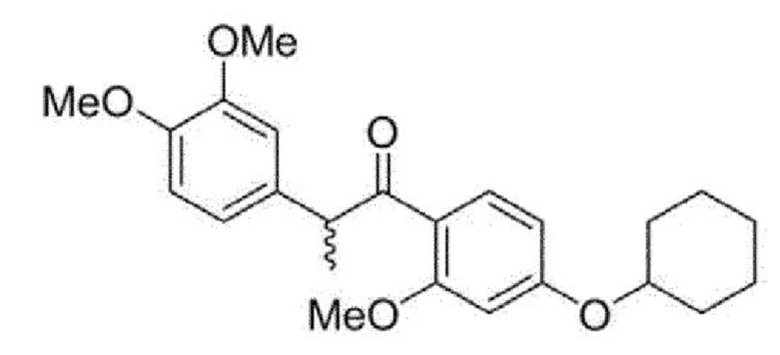

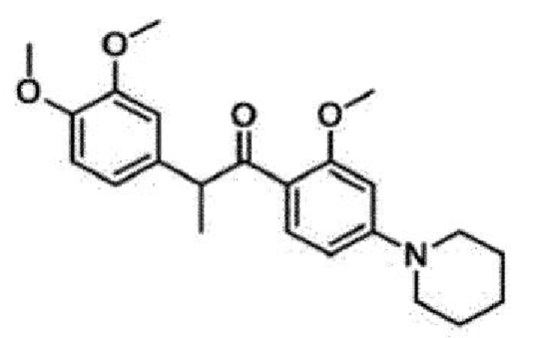
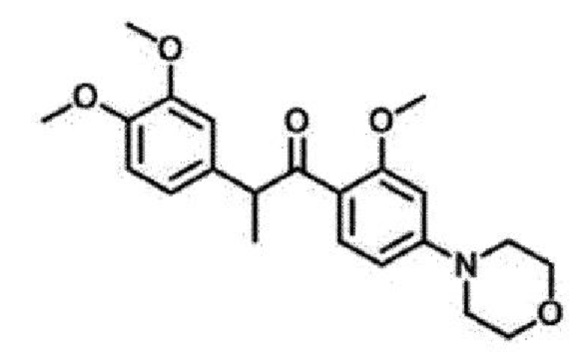
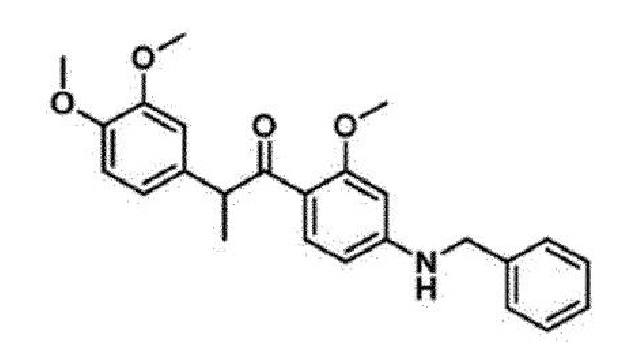
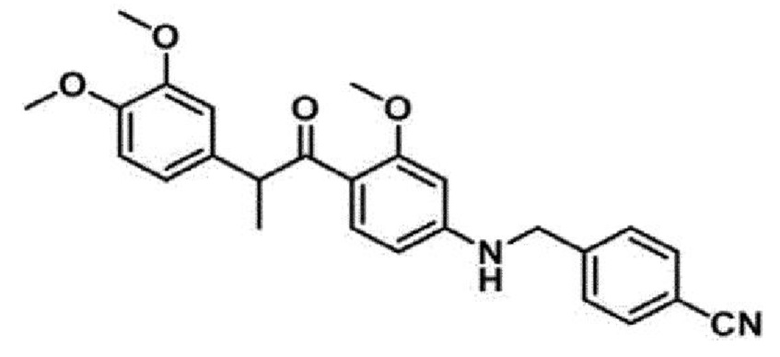
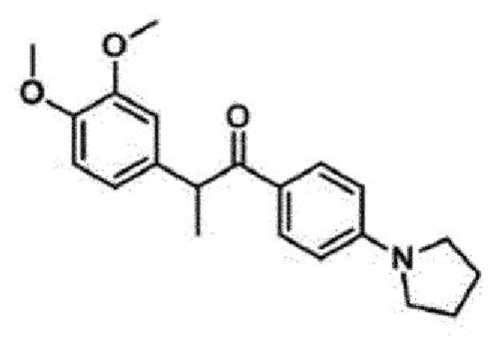
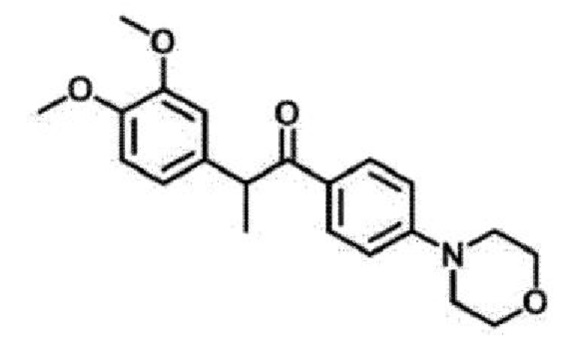
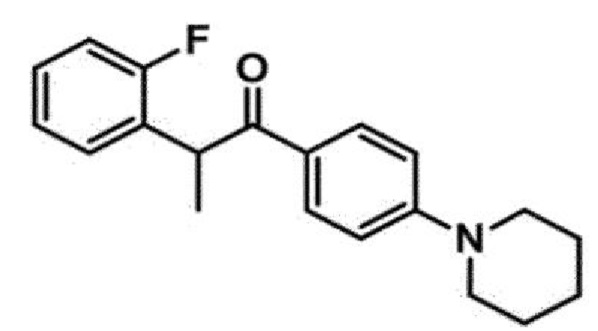

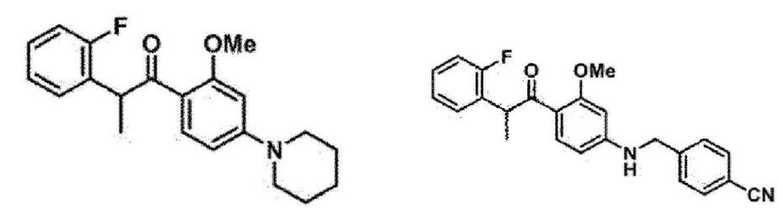
4. Фармацевтическая композиция для лечения или профилактики возрастной макулярной дегенерации, диабетической ретинопатии, ретинопатии недоношенных или неоваскулярной глаукомы, содержащая в качестве активного ингредиента соединение, представленное следующей Формулой (1):

где А1 и А2, каждый независимо, представляют собой -Н, галоген или метокси;
В1 представляет собой –Н или метокси; а также
R1 представляет собой С3-10 циклоалкилокси, гетероциклоалкил с 5- или 6-членным кольцом, содержащий по меньшей мере один гетероатом, выбранный из группы, состоящей из N, О и S, или бензиламино;
причем бензильная группа может опционально быть замещена по меньшей мере одним
-CN.
5. Фармацевтическая композиция по п.4, причем соединение согласно Формуле (1) выбрано из группы, состоящей из следующих соединений:










 .
.
6. Способ лечения или профилактики возрастной макулярной дегенерации, диабетической ретинопатии, ретинопатии недоношенных или неоваскулярной глаукомы у субъекта, предусматривающий введение субъекту в качестве активного ингредиента фармацевтически эффективного количества соединения по п.1.
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
| Hong, Hyo Jeong et al | |||
| A Versatile Synthesis of O-Desmethylangolensin Analogues from Methoxy-Substituted Benzoic Acids | |||
| Journal of the Korean Chemical Society, 2014, 58(6), 569-574 | |||
| Salakka, A | |||
| et al | |||
| Synthesis of α-methyldeoxybenzoins | |||
| Journal of the Chemical Society, 1999, Perkin Transactions 1, (18), 2601-2604 | |||
Авторы
Даты
2022-04-14—Публикация
2019-08-12—Подача