Область техники, к которой относится изобретение
[0001]
Настоящее изобретение относится к новому конденсированному пиримидиновому соединению, обладающему RET-ингибирующей активностью, или его соли и к фармацевтической композиции, содержащей такое соединение или соль.
Перекрестная ссылка на родственные заявки
Настоящая заявка испрашивает приоритет согласно Японской патентной заявки № 2016-031919, поданной 23 февраля 2016 года, и Японской патентной заявки № 2016-140801, поданной 15 июля 2016 года, которые включены в настоящую заявку посредством ссылки во всей их полноте. Настоящее изобретение относится к новому конденсированному пиримидиновому соединению, обладающему RET-ингибирующей активностью, или его соли и к фармацевтической композиции, содержащей такое соединение или соль.
Предпосылки создания изобретения
[0002]
Различные протеинкиназы присутствуют in vivo, и известно, что они вовлечены в целый ряд функциональных регуляций. RET представляет собой рецепторную тирозинкиназу, идентифицированную как тирозинкиназа протоонкогенов. RET связывается с нейротрофическим фактором глиальных клеток (GDNF) и GDNF рецептором с образованием комплекса, который позволяет RET осуществлять физиологические функции через внутриклеточную передачу сигналов фосфорилирования (Непатентная литература 1). В одном исследовании сообщалось, что в нормальных тканях RET способствует развитию почек и нейрогенезу в эмбриональном периоде развития (Непатентная литература 2). Некоторые исследования показывают, что в раковых заболеваниях, таких как рак легкого, рак щитовидной железы, рак молочной железы, рак поджелудочной железы и рак предстательной железы, транслокация, мутация и сверхэкспрессия RET усиливает его активацию, таким образом, способствуя клеточному росту, образованию опухоли или инфильтрации ткани (Непатентная литература 3, 4, 5, 6, 7, и 8). Кроме того, известно, что RET является плохим прогностическим фактором рака, и, как показано в некоторых сообщениях, транслокация RET и повышенный уровень его активации также обратно коррелируют с прогнозом при раке (Непатентная литература 9, 10, 11, и 12).
[0003]
Поэтому считают, что ингибитор, способный ингибировать активность RET, является полезным в качестве терапевтического средства для лечения заболеваний, ассоциированных с аномально усиленными сигнальными путями RET.
[0004]
Ожидается, например, что при раке с вовлечением транслоцированного, мутантного и сверхэкспрессируемого RET the введение лекарственного средства, способного специфическим образом ингибировать RET, будет селективно и интенсивно подавлять пролиферацию раковых клеток и способствовать лечению, продлению жизни и улучшению качества жизни раковых пациентов.
[0005]
В качестве таких соединений, обладающих ингибирующей RET активностью, известно PP1 (Непатентная литература 13). В PP1 п-толильная группа связана с конденсированным кольцевым пиримидиновым скелетом. Известно, что PP1 демонстрирует высокую ингибиторную активность против не только RET, но также Src (Непатентная литература 14), c-Kit, Bcr-Abl (Непатентная литература 15 и 16) и других. Например, в качестве побочных эффектов, ингибирование Src может привести к аномально усиленному костеобразованию, а ингибирование Lck может подавлять T-клетки (Непатентная литература 17 и 18). Поскольку мультикиназные ингибиторы ингибируют не только RET, но также различные сигнальные пути для ингибирования клеточного роста и другие функции, есть опасения, связанные с такими ингибиторами, касающиеся различных возможных побочных эффектов, в связи с чем может потребоваться уменьшение дозы и/или лекарственные каникулы, приводя, таким образом, к недостаточной ингибиторной активности в отношении RET. С точки зрения уменьшения побочных эффектов, желательны ингибиторы RET, которые обладают высокой ингибиторной активностью против RET с низкой ингибиторной активностью против других киназ.
[0006]
Непатентная литература 19 и Патентная литература 1 раскрывают вещество с конденсированным пиримидиновым скелетом, с которым кольцевая структура связана через амидную связь. Это соединение описано как обладающее ингибиторной активностью против киназы Aurora.
[0007]
Патентная литература 2 раскрывает пирролопиримидиновое производное, которое селективно ингибирует Tie-2, TrkA и член его семейства TrkB.
[0008]
Патентная литература 3 раскрывает пирролопиримидиновое производное, которое селективно ингибирует Tie-2 и члены его семейства.
[0009]
Патентная литература 4 раскрывает пирролопиримидиновое производное, которое представляет собой модулятор калиевых каналов.
[0010]
Патентная литература 5 раскрывает пирролопиримидиновое производное, которое обладает терапевтическим эффектом на диабет.
[0011]
Патентная литература 6 и 7 раскрывают гетероциклическое замещенное циклопентановое соединение, которое ингибирует аденозинкиназу.
[0012]
Патентная литература 8 раскрывает пирролопиримидиновое производное, которое содержит винильную группу или этинильную группу.
[0013]
Патентная литература 9 раскрывает конденсированное пиримидиновое производное, которое обладает ингибиторной активностью против BTK.
[0014]
Однако никакая Патентная литература из указанных выше конкретно не раскрывает или даже не предполагает соединение, ингибирующее RET, с конденсированным пиримидиновым скелетом, которое содержит амино группу в 4-положении и кольцо, присоединенное через амидную связь.
Перечень ссылочных документов
Патентная литература
[0015]
Патентная литература 1: WO2007/067781 Брошюра
Патентная литература 2: WO2004056830A1 Брошюра
Патентная литература 3: WO2005047289A1 Брошюра
Патентная литература 4: WO2011018894A1 Брошюра
Патентная литература 5: WO2015078417A1 Брошюра
Патентная литература 6: Патент США № 5665721
Патентная литература 7: WO9640686A1 Брошюра
Патентная литература 8: WO2014184069A1 Брошюра
Патентная литература 9: WO2015022926A1 Брошюра
Непатентная литература
[0016]
Непатентная литература 1: Lois M. Mulligan, Nature Rev., 14(3): pp. 173-186, (2014)
Непатентная литература 2: Carlos F. Ibanez, Cold Spring Harb Perspect Biol., 5(2): pp. 1-10, (2013)
Непатентная литература 3: Takashi Kohno, Nature Med., 18(3): pp. 375-377, (2012)
Непатентная литература 4: Massimo Santoro, Eur J Endocrinol., 155: pp. 645-653, (2006)
Непатентная литература 5: Marjan Zarif Yeganeh, Asian Pac J Cancer Prev., 16(6): pp. 2107-2117, (2015)
Непатентная литература 6: Albana Gattelli, EMBO Mol Med., 5: pp. 1335-1350, (2013)
Непатентная литература 7: Yoshinori Ito, Surgery, 138: pp. 788-794, (2005)
Непатентная литература 8: Dawn M. Dawson, J Natl Cancer Inst., 90: pp. 519-523, (1998)
Непатентная литература 9: Weijing Cai, Cancer, 119: pp. 1486-1494, (2013)
Непатентная литература 10: Rossella Elisei, J Clin Endocrinol Metab., 93(3): pp. 682-687, (2008)
Непатентная литература 11: Albana Gattelli, EMBO Mol Med., 5: pp. 1335-1350, (2013)
Непатентная литература 12: Q Zeng, J. Int. Med. Res., 36: pp. 656-664, (2008)
Непатентная литература 13: Francesca Carlomagno, Cancer Res., 62(4): pp. 1077-1082, (2002)
Непатентная литература 14: Johannes Waltenberger, Circ Res., 85(1): pp. 12-22, (1999)
Непатентная литература 15: Louise Tatton, J Biol Chem., 278(7): pp. 4847-4853, (2003)
Непатентная литература 16: Markus Warmuth, Blood. 101(2): pp. 664-672, (2003)
Непатентная литература 17: Carolyn Lowe, Proc Natl Acad Sci USA, 90(10): pp. 4485-9, (1993)
Непатентная литература 18: Thierry Molina, Nature, 357(6374): pp. 161-4, (1992)
Непатентная литература 19: McClellan WJ, Bioorganic & Medicinal Chemistry Letters 21: pp. 5620-5624 (2011)
Непатентная литература 20: Front Oncol. 2015 Dec 21; 5:278
Непатентная литература 21: Nature Reviews Clinical Oncology, vol. 9, no. 2, pp. 98-109, 2012
Сущность изобретения
Техническая задача
[0017]
Целью настоящего изобретения является обеспечение нового соединения или его соли, которые селективно и сильно ингибируют RET, и фармацевтической композиции, включающей их.
Решение задачи
[0018]
Авторы настоящего изобретения провели широкие исследования для достижения указанной выше цели, и в результате обнаружили, что ряд соединений, представленных формулами (I) и (I') ниже, показывают отличную ингибиторную активность против RET и селективность в отношении определенных киназ и являются полезными в качестве фармацевтического препарата для лечения RET-связанных заболеваний, таких как злокачественные опухоли. Таким образом, было создано настоящее изобретение.
[0019]
Более определенно, настоящее изобретение обеспечивает соединение, представленное формулой (I) ниже, или его соль:
[0020]

[0021]
где в формуле (I) A представляет собой
[0022]

[0023]
где R1 представляет собой
галоген,
циано,
нитро,
замещенный или незамещенный C1-C6 алкил,
замещенный или незамещенный C1-C6 алкокси,
замещенный или незамещенный C2-C6 алкенил,
замещенный или незамещенный C2-C6 алкинил,
замещенный или незамещенный амино или
замещенную или незамещенную 4-10-членную моноциклическую или полициклическую ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы,
Y представляет собой N или CH, и
n представляет собой целое число, имеющее значение от 0 до 2,
где, когда n имеет значение 2, два R1 могут быть одинаковыми или отличными друг от друга;
в формуле A2 группа:
[0024]

[0025]
образует, вместе с фенилом или пиридинилом, с которым эта группа связана, полициклический C8-C14 ароматический углеводород или 8-14-членную полициклическую ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы;
R2 представляет собой
замещенный или незамещенный C3-C10 алкил,
замещенный или незамещенный C3-C7 циклоалкил,
замещенный или незамещенный C4-C12 связанный мостиковой связью циклоалкил,
замещенный или незамещенный C2-C6 алкенил,
замещенный или незамещенный C3-C7 циклоалкенил или
замещенную или незамещенную 4-10-членную моноциклическую или полициклическую насыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы,
при условии, что, когда каждая группа, представленная как R2, содержит заместитель, этот заместитель не должен представлять собой замещенную или незамещенную насыщенную гетероциклическую группу, которая может содержать по меньшей мере один одинаковый или разный гетероатом, выбранный из кислорода и серы, и содержит по меньшей мере один атом азота; и
X представляет собой
N или
CR3, где R3 представляет собой
водород,
галоген,
циано,
нитро,
замещенный или незамещенный C1-C6 алкил,
замещенный или незамещенный C1-C6 алкокси,
замещенный или незамещенный C1-C6 алкилтио,
замещенный или незамещенный C3-C7 циклоалкил,
замещенный или незамещенный C2-C6 алкенил,
замещенный или незамещенный C2-C6 алкинил,
замещенный или незамещенный амино,
замещенный или незамещенный карбамоил,
замещенный или незамещенный C6-C14 ароматический углеводород или
замещенную или незамещенную 4-10-членную моноциклическую или полициклическую насыщенную или ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы.
[0026]
Настоящее изобретение также обеспечивает соединение, представленное формулой (I') ниже, или его соль:
[0027]

[0028]
где в формуле (I') A представляет собой
[0029]
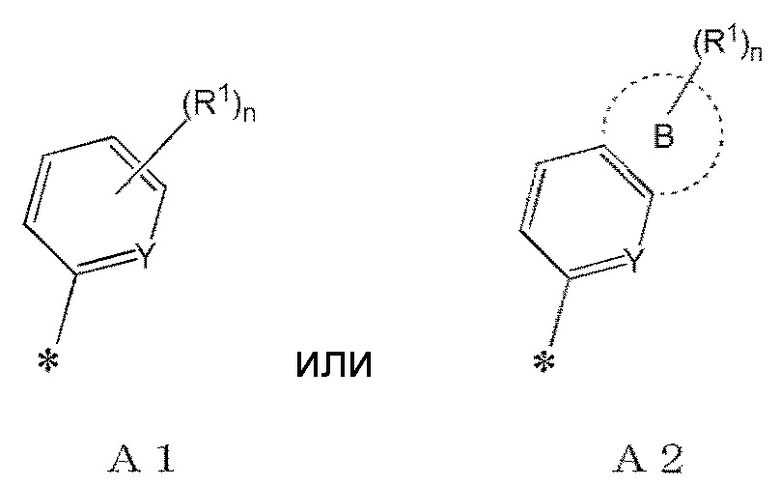
[0030]
где R1 представляет собой
галоген,
циано,
нитро,
замещенный или незамещенный C1-C6 алкил,
замещенный или незамещенный C1-C6 алкокси,
замещенный или незамещенный C2-C6 алкенил,
замещенный или незамещенный C2-C6 алкинил,
замещенный или незамещенный амино или
замещенную или незамещенную 4-10-членную моноциклическую или полициклическую ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы,
Y представляет собой N или CH, и
n представляет собой целое число, имеющее значение от 0 до 2,
где, когда n имеет значение 2, два R1 могут быть одинаковыми или отличными друг от друга;
в формуле A2 группа:
[0031]

[0032]
образует, вместе с фенилом или пиридинилом, с которым эта группа связана, полициклический C8-C14 ароматический углеводород или 8-14-членную полициклическую ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы;
R2 представляет собой
замещенный или незамещенный C3-C10 алкил,
замещенный или незамещенный C3-C4 циклоалкил,
замещенный или незамещенный C4-C12 связанный мостиковой связью циклоалкил,
замещенный или незамещенный C2-C6 алкенил,
замещенный или незамещенный C3-C4 циклоалкенил или
замещенную или незамещенную 4-10-членную моноциклическую или полициклическую насыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы,
при условии, что, когда каждая группа, представленная как R2, содержит заместитель, этот заместитель не должен представлять собой замещенную или незамещенную насыщенную гетероциклическую группу, которая может содержать по меньшей мере один одинаковый или разный гетероатом, выбранный из кислорода и серы, и содержит по меньшей мере один атом азота; и
X представляет собой
N или
CR3, где R3 представляет собой
водород,
галоген,
циано,
нитро,
замещенный или незамещенный C1-C6 алкил,
замещенный или незамещенный C1-C6 алкокси,
замещенный или незамещенный C1-C6 алкилтио,
замещенный или незамещенный C3-C7 циклоалкил,
замещенный или незамещенный C2-C6 алкенил,
замещенный или незамещенный C2-C6 алкинил,
замещенный или незамещенный амино,
замещенный или незамещенный карбамоил,
замещенный или незамещенный C6-C14 ароматический углеводород или
замещенную или незамещенную 4-10-членную моноциклическую или полициклическую насыщенную или ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы.
[0033]
Настоящее изобретение также обеспечивает медицинское применение, например, ингибитора RET, фармацевтической композиции и противоопухолевого средства, все из которых включают соединение, представленное формулой (I) или (I') выше, или его соль.
Полезные эффекты изобретения
[0034]
Настоящее изобретение обеспечивает новое соединение, представленное формулой (I) или (I') выше, или его соль, которые оба полезны в качестве ингибиторов RET.
[0035]
Было обнаружено, что соединения или соли по настоящему изобретению обладают превосходной ингибиторной активностью против RET и селективностью в отношении определенных киназ. Следовательно, соединения или соли по настоящему изобретению не приводят к побочным эффектам, которые могут быть вызваны ингибированием, например, Src, Lck, Aurora B, EGFR и подобных киназ, отличных от RET, и являются полезными в качестве средства для профилактики и/или лечения заболеваний, связанных с RET (например, рака).
Краткое описание чертежей
[0036]
Фиг. 1 иллюстрирует изменения относительного объема опухоли, наблюдаемые с течением времени в Примере испытаний 10.
Фиг. 2 иллюстрирует изменения относительного объема опухоли, наблюдаемые с течением времени в Примере испытаний 10.
Фиг. 3 иллюстрирует изменения средней массы тела, наблюдаемые с течением времени в Примере испытаний 10.
Фиг. 4 иллюстрирует изменения средней массы тела, наблюдаемые с течением времени в Примере испытаний 10.
Описание вариантов осуществления
[0037]
Соединения по настоящему изобретению, представленные формулами (I) и (I') выше, представляют собой соединения, имеющие конденсированный пиримидиновый скелет, содержащий амино группу в положении 4, с бензольным кольцом, пиридиновым кольцом или конденсированным кольцом, содержащим бензольное кольцо или пиридиновое кольцо, через амидную связь, и являются новыми соединениями, которые не раскрыты ни в одном из указанных выше документов предшествующего уровня техники.
[0038]
В настоящем описании * представляет собой положение связывания, если не указано иное. Например, когда A в формуле (I) или (I') представляет собой A1 ниже:
[0039]

[0040]
предполагается, что A1 связан с карбамоильной группой в формуле (I) или (I') в положении, показанным *.
[0041]
В настоящем описании, указанная выше группа:
[0042]

[0043]
также просто указана как группа B или B фрагмент.
[0044]
В настоящем описании следующая часть:
[0045]
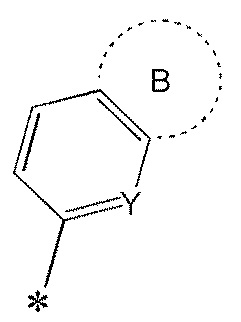
[0046]
где группа B и Y имеют значение, определенное выше;
формулы A2 ниже:
[0047]

[0048]
где группа B, Y и R1 имеют значение, определенное выше;
представляет собой полициклический C8-C14 ароматический углеводород, содержащий бензольное кольцо (Y представляет собой CH) или пиридиновое кольцо (Y представляет собой N), представленное следующей формулой:
[0049]

[0050]
или 8-14-членную полициклическую ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы. Иными словами, в A2 следующая группа:
[0051]

[0052]
означает кольцо, содержащее 0-2 атома азота, атома кислорода, или атома серы в качестве гетероатомов. Группа B образует, вместе с фенилом или пиридинилом, полициклический C8-C14 ароматический углеводород или 8-14-членную полициклическую ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы.
[0053]
В настоящем описании, если не указано иное, примеры ʺзаместителяʺ включают дейтерий, галоген, гидрокси, циано, нитро, алкил, галогенoалкил, гидроксиалкил, алкокси, алкоксиалкил, циклоалкил, циклоалкил-алкил, связанный мостиковой связью циклоалкил, аралкил, алкенил, циклоалкенил, алкинил, галогенoалкокси, циклоалкокси, циклоалкил-алкокси, аралкилокси, алкилтио, циклоалкил-алкилтио, амино, моно- или диалкиламино, циклоалкиламино, циклоалкил-алкиламино, аралкиламино, ароматический углеводород амино, ациламино, алкоксикарбониламино, аралкилоксикарбониламино, ацил, ацилокси, алкилсилилокси, оксо, карбоксил, алкоксикарбонил, аралкилоксикарбонил, карбамоил, насыщенную или ненасыщенную гетероциклическую группу, ароматический углеводород, насыщенный гетероциклический окси, ненасыщенный гетероциклический окси и т.д. Когда присутствует заместитель из перечисленных выше, количество таких заместителей типично составляет один, два или три.
[0054]
В настоящем описании примеры ʺгалогенаʺ включают фтор, хлор, бром и иод.
[0055]
В настоящем описании ʺалкилʺ относится к линейному или разветвленному насыщенному углеводороду. Примеры включают метил, этил, н-пропил, изопропил, н-бутил, втор-бутил, изобутил, трет-бутил, 1-метилпропил, н-пентил, изопентил, трет-пентил, пентан-3-ил, н-гексил, 1,1-диметилпропил, 1,1,2,2-тетраметилэтил, н-гептил, 1,1,2,2-тетраметилпропил, н-октил, н-нонил, н-децил и т.д.; и, более конкретно, включают C1-C10 алкил, C3-C10 алкил, C1-C6 алкил, C1-C4 алкил, C3-C8 алкил, C3-C6 алкил и т.д.
[0056]
В настоящем описании ʺгалогенoалкилʺ относится к алкилу, указанному выше, содержащему один или несколько (например, 1-10, 1-7, или 1-5) атомов галогена, указанных выше. Примеры включают фторметил, дифторметил, трифторметил, трихлорметил, фторэтил, 1,1,1-трифторэтил, монофтор-н-пропил, перфтор-н-пропил, перфторизопропил, монофтор-н-бутил, монофтор-н-пентил, монофтор-н-гексил и т.д.; и, более конкретно, включают галогенo C1-C6 алкил, галогенo C1-C4 алкил и т.д.
[0057]
В настоящем описании ʺгидроксиалкилʺ относится к алкилу, указанному выше, содержащему одну или несколько (например, 1-5, 1-3, или 1) гидрокси групп. Примеры включают гидроксиметил, гидроксиэтил (1-гидроксиэтил или 2-гидроксиэтил), гидроксипропил, гидроксибутил, гидроксипентил, гидроксигексил и т.д.; и, более конкретно, включают гидрокси C1-C6 алкил, гидрокси C1-C4 алкил и т.д.
[0058]
В настоящем описании ʺалкоксиʺ относится к окси, с которым связан указанный выше алкил. Примеры включают метокси, этокси, н-пропокси, изопропокси, н-бутокси, изобутокси, трет-бутокси, н-пентилокси, изопентилокси, н-гексилокси и т.д.; и, более конкретно, включают C1-C6 алкокси, C1-C4 алкокси и т.д.
[0059]
В настоящем описании ʺалкоксиалкилʺ относится к алкилу, указанному выше, содержащему одну или несколько (например, 1-5, предпочтительно 1-3, и более предпочтительно 1) алкокси групп, указанных выше. Примеры включают метоксиметил, этоксиметил, н-пропоксиметил, н-бутоксиметил, 2-метоксиэтил, 1-метокси-н-пропил, 3-метокси-н-пропил, 2-этокси-н-бутил, 4-метокси-н-бутил, 5-метокси-н-пентил, 6-метокси-н-гексил и т.д.; и, более конкретно, включают C1-C4 алкокси C1-C6 алкил, C1-C4 алкокси C1-C4 алкил и т.д.
[0060]
В настоящем описании ʺциклоалкилʺ относится к моноциклическому или полициклическому (например, бициклическому или трициклическому) насыщенному углеводороду. Примеры включают моноциклический циклоалкил, такой как циклопропил, циклобутил, циклопентил, циклогексил и циклогептил; полициклический циклоалкил, такой как спиро[3.3]гептил, спиро[3.4]октил и диспиро[5.1.78.26]гептадеканил; и, более конкретно, включают C3-C7 циклоалкил, C3-C5 циклоалкил и т.д. В настоящем изобретении ʺциклоалкилʺ должен определяться независимо от ʺсвязанного мостиковой связью циклоалкилаʺ, описанного ниже. Поэтому в настоящем изобретении ʺсвязанный мостиковой связью циклоалкилʺ исключается из ʺциклоалкилаʺ.
[0061]
В настоящем описании ʺциклоалкил-алкилʺ относится к алкилу, указанному выше, содержащему одну или несколько (например, 1-3 и предпочтительно 1) циклоалкильных групп, указанных выше. Примеры включают циклопропилметил, циклобутилметил, циклопентилметил, циклогексилметил, циклогептилметил и т.д.; и, более конкретно, включают C3-C7 циклоалкил-замещенный C1-C10 алкил, C3-C7 циклоалкил-замещенный C1-C6 алкил и т.д.
[0062]
В настоящем описании ʺсвязанный мостиковой связью циклоалкилʺ относится к полициклическому (например, бициклическому или трициклическому) насыщенному углеводороду, в котором по меньшей мере два (например, два или три) насыщенных углеводородных кольца содержат по меньшей мере два атома углерода, общих со смежным кольцом. Примеры включают бицикло[1.1.0]бутил (бицикло[1.1.0]бутан-1-ил или бицикло[1.1.0]бутан-2-ил), бицикло[1.1.1]пентил (бицикло[1.1.1]пентан-1-ил или бицикло[1.1.1]пентан-2-ил), бицикло[3.1.0]гексил (бицикло[3.1.0]гексан-1-ил, бицикло[3.1.0]гексан-2-ил, бицикло[3.1.0]гексан-3-ил, или бицикло[3.1.0]гексан-6-ил), бицикло[2.2.1]гептил (бицикло[2.2.1]гептан-1-ил, бицикло[2.2.1]гептан-2-ил, или бицикло[2.2.1]гептан-7-ил), бицикло[3.1.1]гептил (бицикло[3.1.1]гептан-1-ил, бицикло[3.1.1]гептан-2-ил, бицикло[3.1.1]гептан-3-ил или бицикло[3.1.1]гептан-6-ил), бицикло[4.4.0]децил (бицикло[4.4.0]декан-2-ил, бицикло[4.4.0]декан-3-ил и т.д.), адамантил (адамантан-1-ил или адамантан-2-ил) и т.д.; и, более конкретно, включают C4-C12 связанный мостиковой связью циклоалкил, C5-C10 связанный мостиковой связью циклоалкил и т.д.
[0063]
В настоящем описании ʺароматический углеводородʺ относится к моноциклическому или полициклическому (например, бициклическому или трициклическому) кольцевому заместителю, включающему углерод и водород, содержащему ненасыщенную связь и содержащему 4e+2 количество электронов (e представляет собой целое число, имеющее значение 1 или больше) в циклической π электронной системе. Примеры включают фенил, нафтил, антраценил, фенантрил, флуоренил, тетрагидронафтил и т.д.; и, более конкретно, включают C6-C14, C6-C10 и C8-C14 ароматические углеводороды.
[0064]
В настоящем описании ʺаралкилʺ относится к алкилу, указанному выше, содержащему одну или несколько (например, 1-3 и предпочтительно 1) ароматических углеводородных групп, указанных выше. Примеры включают бензил, фенетил, дифенилметил (бензгидрил), трифенилметил (тритил), нафтилметил, флуоренилметил и т.д.; и, более конкретно, включают C7-C14 аралкил, C6-C14 ароматический углеводород-замещенный C1-C6 алкил (C1-C6 алкил, содержащий один или несколько C6-C14 ароматических углеводородов) и т.д.
[0065]
В настоящем описании ʺалкенилʺ относится к линейному или разветвленному ненасыщенному углеводороду, содержащему по меньшей мере одну (например, 1 или 2, или 1) двойную связь. Примеры включают винил, аллил, 1-пропенил, 2-метил-2-пропенил, изопропенил, 1-, 2- или 3-бутенил, 2-, 3-, или 4-пентенил, 2-метил-2-бутенил, 3-метил-2-бутенил, 5-гексенил, 3-метил-3-бутенил и т.д.; и, более конкретно, включают C2-C6 алкенил, C2-C4 алкенил и т.д.
[0066]
В настоящем описании ʺциклоалкенилʺ относится к моноциклическому или полициклическому (например, бициклическому или трициклическому) ненасыщенному углеводороду, содержащему по меньшей мере одну (например, 1 или 2, или 1) двойную связь. Примеры включают циклопропенил (например, 2-циклопропен-1-ил), циклобутенил (например, 2-циклобутен-1-ил), циклопентенил (например, 2-циклопентен-1-ил и 3-циклопентен-1-ил), циклопентадиенил (например, 2,4-циклопентадиен-1-ил), циклогексенил (например, 3-циклогексен-1-ил), циклогептенил (например, 3-циклогептен-1-ил) и т.д.; и, более конкретно, включают C3-C7 циклоалкенил и т.д.
[0067]
В настоящем описании ʺалкинилʺ относится к линейному или разветвленному ненасыщенному углеводороду, содержащему по меньшей мере одну (например, 1 или 2, или 1) тройную связь. Примеры включают этинил, 1- или 2-пропинил, 1-, 2-, или 3-бутинил, 1-метил-2-пропинил и т.д.; и, более конкретно, включают C2-C6 алкинил, C2-C4 алкинил и т.д.
[0068]
В настоящем описании ʺгалогенoалкоксиʺ относится к алкокси, указанному выше, содержащему один или несколько (например, 1-10, 1-7, или 1-5) атомов галогена. Примеры включают фторметокси, дифторметокси, трифторметокси, трихлорметокси, фторэтокси, 1,1,1-трифторэтокси, монофтор-н-пропокси, перфтор-н-пропокси, перфтор-изопропокси и т.д.; и, более конкретно, включают галогенo C1-C6 алкокси, галогенo C1-C4 алкокси и т.д.
[0069]
В настоящем описании ʺциклоалкоксиʺ относится к окси, с которым связан указанный выше циклоалкил. Примеры включают циклопропокси, циклобутокси, циклопентилокси, циклогексилокси, циклогептилокси и т.д.; и, более конкретно, включают C3-C7 циклоалкокси.
[0070]
В настоящем описании ʺциклоалкил-алкоксиʺ относится к алкокси, указанному выше, содержащему одну или несколько (например, 1-3 и предпочтительно 1) циклоалкильных групп, указанных выше. Примеры включают циклопропилметокси, циклобутилметокси, циклопентилметокси, циклогексилметокси, циклогептилметокси и т.д.; и, более конкретно, включают C3-C7 циклоалкил-замещенный C1-C4 алкокси (C1-C4 алкокси, содержащий одну или несколько (например, 1-3 и предпочтительно 1) C3-C7 циклоалкильных групп).
[0071]
В настоящем описании ʺаралкилоксиʺ относится к алкокси, указанному выше, содержащему одн или несколько (например, 1-3 и предпочтительно 1) ароматических углеводородных групп, указанных выше. Примеры включают бензилокси, фенетилокси, нафтилметилокси, флуоренилметилокси и т.д.; и, более конкретно, включают C7-C14 аралкилокси.
[0072]
В настоящем описании ʺалкилтиоʺ относится к меркапто, в котором водород замещен алкилом, указанным выше. Примеры включают метилтио, этилтио, н-пропилтио, изопропилтио, н-бутилтио, изобутилтио, трет-бутилтио, н-пентилтио, изопентилтио, гексилтио и т.д.; и, более конкретно, включают C1-C6 алкилтио, C1-C4 алкилтио и т.д.
[0073]
В настоящем описании ʺциклоалкил-алкилтиоʺ относится к алкилтио, указанному выше, содержащему одну или несколько (например, 1-3 и предпочтительно 1) циклоалкильных групп, указанных выше. Примеры включают циклопропилметилтио, циклобутилметилтио, циклопентилметилтио, циклогексилметилтио, циклогептилметилтио и т.д.; и, более конкретно, включают C3-C7 циклоалкил-замещенный C1-C4 алкилтио (C1-C4 алкилтио, содержащий одну или несколько (например, 1-3 и предпочтительно 1) C3-C7 циклоалкильных групп).
[0074]
В настоящем описании ʺмоноалкиламиноʺ относится к амино, содержащему одну алкильную группу, указанную выше. Примеры включают метиламино, этиламино, н-пропиламино, изопропиламино, н-бутиламино, изобутиламино, трет-бутиламино, н-пентиламино, изопентиламино, гексиламино и т.д.; и, более конкретно, включают моно(C1-C6 алкил)амино.
[0075]
В настоящем описании ʺдиалкиламиноʺ относится к амино, содержащему две алкильные группы, указанные выше. Примеры включают диметиламино, этилметиламино, диэтиламино, ди(н-пропил)амино, диизопропиламино, ди(н-бутил)амино, диизобутиламино, ди(трет-бутил)амино, ди(н-пентил)амино, диизопентиламино, дигексиламино и т.д.; и, более конкретно, включают ди(C1-C6 алкил)амино.
[0076]
В настоящем описании, ʺалкиламиноʺ, как таковой, включает как моноалкиламино, так и диалкиламино.
[0077]
В настоящем описании ʺциклоалкиламиноʺ относится к амино, содержащему одну или две циклоалкильные группы, указанные выше. Примеры включают циклопропиламино, циклобутиламино, циклопентиламино, циклогексиламино, циклогептиламино, дициклобутиламино и т.д.; и, более конкретно, включают C3-C7 циклоалкил-замещенный амино (амино, содержащий одну или две C3-C7 циклоалкильные группы).
[0078]
В настоящем описании ʺциклоалкил-алкиламиноʺ относится к амино, содержащему одну или две циклоалкил-алкильные группы, указанные выше. Примеры включают N-циклопропилметиламино, N-циклобутилметиламино, N-циклопентилметиламино, N-циклогексилметиламино, N-циклогептилметиламино и т.д.; и, более конкретно, включают N-C3-C7 циклоалкил-замещенный C1-C4 алкиламино (амино, содержащий одну или две ʺC1-C4 алкильные группы, содержащие одну или несколько (например, 1-3 и предпочтительно 1) C3-C7 циклоалкильных группʺ).
[0079]
В настоящем описании ʺаралкиламиноʺ относится к амино, содержащему одну или две аралкильные группы, указанные выше. Примеры включают бензиламино, фенетиламино, нафтилметиламино, флуоренилметиламино и т.д.; и, более конкретно, включают C7-C14 аралкил-замещенный амино.
[0080]
В настоящем описании ʺароматический углеводород аминоʺ относится к амино, содержащему одну или две ароматические углеводородные группы, указанные выше. Примеры включают фениламино, нафтиламино, антрацениламино, фенантриламино, флуорениламино, тетрагидронафтиламино и т.д.; и, более конкретно, включают C6-C14 ароматический углеводород-замещенный амино.
[0081]
В настоящем описании ʺацилʺ относится к формилу, алкилкарбонилу, циклоалкилкарбонилу, аралкилкарбонилу или ароматический углеводород карбонилу.
[0082]
В настоящем описании ʺалкилкарбонилʺ относится к карбонилу, содержащему алкил, указанный выше. Примеры включают метилкарбонил, этилкарбонил, н-пропилкарбонил, изопропилкарбонил, н-бутилкарбонил, изобутилкарбонил, трет-бутилкарбонил, н-пентилкарбонил, изопентилкарбонил, гексилкарбонил и т.д.; и, более конкретно, включают (C1-C6 алкил)карбонил (карбонил, содержащий C1-C6 алкил).
[0083]
В настоящем описании ʺциклоалкилкарбонилʺ относится к карбонилу, содержащему циклоалкил, указанный выше. Примеры включают циклопропилкарбонил, циклобутилкарбонил, циклопентилкарбонил, циклогексилкарбонил, циклогептилкарбонил и т.д.; и, более конкретно, включают (C3-C7 циклоалкил)карбонил (карбонил, содержащий C3-C7 циклоалкил).
[0084]
В настоящем описании ʺаралкилкарбонилʺ относится к карбонилу, содержащему аралкил, указанный выше. Примеры включают бензилкарбонил, фенетилкарбонил, нафтилметилкарбонил, флуоренилметилкарбонил и т.д.; и, более конкретно, включают (C7-C14 аралкил)карбонил (карбонил, содержащий C7-C14 аралкил).
[0085]
В настоящем описании ʺароматический углеводород карбонилʺ включают карбонил, содержащий ароматический углеводород, указанный выше. Примеры включают фенилкарбонил, нафтилкарбонил, флуоренилкарбонил, антрилкарбонил, бифенилилкарбонил, тетрагидронафтилкарбонил, хроманилкарбонил, 2,3-дигидро-1,4-диоксанафталенилкарбонил, инданилкарбонил, фенантрилкарбонил и т.д.; и, более конкретно, включают (C6-C14 ароматический углеводород)карбонил.
[0086]
В настоящем описании ʺациламиноʺ относится к амино, содержащему одну или две ацильные группы, указанные выше.
Примеры включают N-формиламино, N-метилкарбониламино, N-этилкарбониламино, N-н-пропилкарбониламино, N-изопропилкарбониламино, N-н-бутилкарбониламино, N-изобутилкарбониламино, N-трет-бутилкарбониламино, N-н-пентилкарбониламино, N-изопентилкарбониламино, N-гексилкарбониламино, N,N-диметилкарбониламино, N-циклопропилкарбониламино, N-циклобутилкарбониламино, N-циклопентилкарбониламино, N-циклогексилкарбониламино, N-циклогептилкарбониламино, N-бензилкарбониламино, N-фенетилкарбониламино, N-нафтилметилкарбониламино, N-флуоренилметилкарбониламино и т.д.; и, более конкретно, включают N-формиламино, N-(C1-C6 алкил)карбонил-замещенный амино (амино, содержащий одну или две (C1-C6 алкил)карбонильные группы), N-(C3-C7 циклоалкил)карбонил-замещенный амино (амино, содержащий одну или две (C3-C7 циклоалкил)карбонильные группы), (C7-C14 аралкил)карбонил-замещенный амино (амино, содержащий одну или две (C7-C14 аралкил)карбонильные группы) и т.д.
[0087]
В настоящем описании ʺацилоксиʺ относится к формилокси, алкилкарбонилокси, циклоалкилкарбонилокси, аралкилкарбонилокси, или ароматический углеводород карбонилокси.
[0088]
В настоящем описании ʺалкилкарбонилоксиʺ относится к окси, содержащему алкилкарбонил, указанный выше. Примеры включают метилкарбонилокси, этилкарбонилокси, н-пропилкарбонилокси, изопропилкарбонилокси, н-бутилкарбонилокси, изобутилкарбонилокси, трет-бутилкарбонилокси, н-пентилкарбонилокси, изопентилкарбонилокси, н-гексилкарбонилокси и т.д.; и, более конкретно, включают (C1-C6 алкил)карбонилокси.
[0089]
В настоящем описании ʺциклоалкилкарбонилоксиʺ относится к окси, содержащему циклоалкилкарбонил, указанный выше. Примеры включают циклопропилкарбонилокси, циклобутилкарбонилокси, циклопентилкарбонилокси, циклогексилкарбонилокси, циклогептилкарбонилокси и т.д.; и, более конкретно, включают C3-C7 циклоалкил-замещенный карбонилокси (карбонилокси, содержащий C3-C7 циклоалкил).
[0090]
В настоящем описании ʺаралкилкарбонилоксиʺ относится к окси, содержащему циклоалкилкарбонил, указанный выше. Примеры включают бензилкарбонилокси, 1-фенетилкарбонилокси, 2-фенетилкарбонилокси, нафтилметилкарбонилокси, флуоренилметилкарбонилокси и т.д.; и, более конкретно, включают (C7-C14 аралкил)карбонилокси (карбонилокси, содержащий C7-C14 аралкил).
[0091]
В настоящем описании ʺароматический углеводород карбонилоксиʺ относится к окси, содержащему ароматический углеводород карбонил, указанный выше. Примеры включают фенилкарбонилокси, нафтилкарбонилокси, флуоренилкарбонилокси, антрилкарбонилокси, бифенилилкарбонилокси, тетрагидронафтилкарбонилокси, хроманилкарбонилокси, 2,3-дигидро-1,4-диоксанафталенилкарбонилокси, инданилкарбонилокси, фенантрилкарбонилокси и т.д.; и, более конкретно, включают (C6-C14 ароматический углеводород)карбонилокси.
[0092]
В настоящем описании ʺалкилсилилоксиʺ относится к силилокси, содержащему алкил, указанный выше, и необязательно содержащему фенил. Примеры включают окси, с которым связан трет-бутилдифенилсилил, триметилсилил, триэтилсилил, трет-бутилдиметилсилил, триизопропилсилил, трет-бутилдифенилсилил, или т.п.; и, более конкретно, включают моно-C1-C6 алкилсилилокси (силилокси, замещенный одной C1-C6 алкильной группой), ди-C1-C6 алкилсилилокси (силилокси, замещенный двумя C1-C6 алкильными группами) и три-C1-C6 алкилсилилокси (силилокси, замещенный тремя C1-C6 алкильными группами). В настоящем описании ʺC1-C6 алкилсилилоксиʺ, как таковой, включает все из моно-C1-C6 алкилсилилокси, ди-C1-C6 алкилсилилокси и три-C1-C6 алкилсилилокси.
[0093]
В настоящем описании ʺалкоксикарбонилʺ относится к карбонилу, содержащему алкокси, указанный выше. Примеры включают метоксикарбонил, этоксикарбонил, н-пропоксикарбонил, изопропоксикарбонил, н-бутоксикарбонил, изобутоксикарбонил, трет-бутоксикарбонил, н-пентилоксикарбонил, изопентилоксикарбонил, н-гексилоксикарбонил и т.д.; и, более конкретно, включают (C1-C6 алкокси)карбонил.
[0094]
В настоящем описании ʺалкоксикарбониламиноʺ относится к амино, содержащему одну или две алкоксикарбонильные группы, указанные выше. Примеры включают метоксикарбониламино, этоксикарбониламино, н-пропоксикарбониламино, изопропоксикарбониламино, н-бутоксикарбониламино, изобутоксикарбониламино, трет-бутоксикарбониламино, н-пентилоксикарбониламино, изопентилоксикарбониламино, н-гексилоксикарбониламино, ди(метоксикарбонил)амино и т.д.; и, более конкретно, включают (C1-C6 алкокси)карбонил-замещенный амино (амино, содержащий одну или две (C1-C6 алкокси)карбонильные группы).
[0095]
В настоящем описании ʺаралкилоксикарбонилʺ относится к карбонилу, содержащему аралкилокси, указанный выше. Примеры включают бензилоксикарбонил, 1-фенетилоксикарбонил, 2-фенетилоксикарбонил, нафтилметилоксикарбонил, флуоренилметилоксикарбонил и т.д.; и, более конкретно, включают (C7-C14 аралкил)оксикарбонил.
[0096]
В настоящем описании ʺаралкилоксикарбониламиноʺ относится к амино, содержащему одну или две аралкилоксикарбонильные группы, указанные выше. Примеры включают бензилоксикарбониламино, 1-фенетилоксикарбониламино, 2-фенетилоксикарбониламино, нафтилметилоксикарбониламино, флуоренилметилоксикарбониламино и т.д.; и, более конкретно, включают (C7-C14 аралкил)оксикарбонил-замещенный амино (амино, содержащий одну или две (C7-C14 аралкил)оксикарбонильные группы).
[0097]
В настоящем описании ʺнасыщенная гетероциклическая группаʺ относится к моноциклической или полициклической (например, бициклической или трициклической) насыщенной гетероциклической группе, содержащей один или несколько (например, 1-3) одинаковых или отличных друг от друга гетероатомов, выбранных из азота, кислорода и серы. Примеры включают морфолино, 1-пирролидинил, пиперидино, пиперазинил, 4-метил-1-пиперазинил, тетрагидрофуранил, тетрагидропиранил, тетрагидротиофенил, тиазолидинил, оксазолидинил, 7-азабицикло[2.2.1]гепт-2-ил, 2,6-диоксабицикло[3.2.1]окт-7-ил, 7-оксабицикло[2.2.1]гептан и т.д.; и, более конкретно, включают 4-10-членные, 8-14-членные, 8-10-членные и 4-6-членные насыщенные гетероциклические группы.
[0098]
В настоящем описании ʺненасыщенная гетероциклическая группаʺ относится к моноциклической или полициклической (например, бициклической или трициклической) полностью или частично ненасыщенной гетероциклической группе, содержащей один или несколько (например, 1-3) одинаковых или отличных друг от друга гетероатомов, выбранных из азота, кислорода и серы. Примеры включают имидазолил, тиенил, фурил, пирролил, оксазолил, изоксазолил, тиазолил, изотиазолил, тиадиазолил, пиразолил, триазолил, тетразолил, пиридинил, пиразил, пиримидинил, пиридазинил, индолил, изоиндолил, индазолил, триазолoпиридинил, бензоимидазолил, бензоксазолил, бензотиазолил, бензотиенил, бензофуранил, пуринил, хинолил, изохинолил, хиназолинил, хиноксалинил, метилендиоксифенил, этилендиоксифенил, дигидробензофуранил, дигидротиазолил, бензотиофенил и т.д.; и, более конкретно, включают 4-10-членные, 8-14-членные, 8-10-членные и 4-6-членные ненасыщенные гетероциклические группы.
[0099]
В настоящем описании ʺнасыщенный гетероциклический оксиʺ относится к окси, содержащему насыщенное гетероциклическое кольцо, указанное выше. Примеры включают морфолинилокси, 1-пирролидинилокси, пиперидиноокси, пиперазинилокси, 4-метил-1-пиперазинилокси, тетрагидрофуранилокси, тетрагидропиранилокси, тетрагидротиофенилокси, тиазолидинилокси и оксазолидинилокси; и, более конкретно, включают 4-10-членный, 8-14-членный, 8-10-членный и 4-6-членный насыщенный гетероциклический окси.
[0100]
В настоящем описании ʺненасыщенный гетероциклический оксиʺ относится к окси, содержащему ненасыщенное гетероциклическое кольцо, указанное выше. Примеры включают имидазолилокси, тиенилокси, фурилокси, пирролилокси, оксазолилокси, изоксазолилокси, тиазолилокси, изотиазолилокси, тиадиазолилокси, пиразолилокси, триазолилокси, тетразолилокси, пиридинилокси, пиразилокси, пиримидинилокси, пиридазинилокси, индолилокси, изоиндолилокси, индазолилокси, триазолoпиридинилокси, бензоимидазолилокси, бензоксазолилокси, бензотиазолилокси, бензотиенилокси, бензофуранилокси, пуринилокси, хинолилокси, изохинолилокси, хиназолинилокси, хиноксалинилокси, метилендиоксифенилокси, этилендиоксифенилокси, дигидробензофуранилокси, дигидротиазолилокси, бензотиофенилокси и т.д.; и, более конкретно, включают 4-10-членный, 8-14-членный, 8-10-членный и 4-6-членный ненасыщенный гетероциклический окси.
[0101]
Термин ʺCa-Cbʺ в описании, относящийся к заместителю, указывает, что заместитель содержит a-b-количество атомов углерода. Например, ʺC1-C6 алкилʺ относится к алкилу, содержащему 1-6 атомов углерода, и ʺC6-C14 ароматический углеводород оксиʺ относится к окси, с которым связан ароматический углеводород, содержащий 6-14 атомов углерода. Кроме того, термин ʺa-b-членныйʺ указывает, что количество атомов (количество кольцевых членов), которые образуют кольцо, составляет от а до b. Например, ʺ4-10-членная насыщенная гетероциклическая группаʺ относится к насыщенной гетероциклической группе с 4-10-членным кольцом. Кроме того, следующая формула:
[0102]

[0103]
представляет ʺC5 связанный мостиковой связью циклоалкил.ʺ
[0104]
В настоящем описании, когда существуют несклько вариантов для заместителей, которые содержит каждая группа, определенная в Формулах (I) и (I'), каждая группа может содержать одинаковые или разные типы заместителей, если не указано иное. Например, ʺC1-C6 алкил, который замещен галогеном или гидроксиʺ, включает не только C1-C6 алкил, который замещен галогеном только, и C1-C6 алкил, который замещен гидрокси только, но также C1-C6 алкил, который замещен и галогеном и гидрокси, если не указано иное. Кроме того, ʺC1-C6 алкил, который замещен галогеном или гидроксиʺ включает, например, C1-C6 алкил, который замещен двумя или более видами атомов галогена (например, фтор и хлор).
[0105]
A1 предпочтительно представляет собой
[0106]

[0107]
более предпочтительно
[0108]

[0109]
и еще более предпочтительно
[0110]

[0111]
[0112]
A2 предпочтительно представляет собой
[0113]

[0114]
[0115]
Заместители, такие как R1, R2, R3, R4, R5, R6 и R7, в формулах, представляющих соединения по настоящему изобретению, объясняются подробно ниже. В объяснении заместителей, заместители, такие как R1, R2, R3, R4, R5, R6 и R7, относятся к соответствующим заместителям в формуле (I) или (I'), если не указано иное.
[0116]
R1, R1a, R1b и R1c каждый представляет собой
галоген,
циано,
нитро,
замещенный или незамещенный C1-C6 алкил,
замещенный или незамещенный C1-C6 алкокси,
замещенный или незамещенный C2-C6 алкенил,
замещенный или незамещенный C2-C6 алкинил,
замещенный или незамещенный амино или
замещенную или незамещенную 4-10-членную моноциклическую или полициклическую ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы.
[0117]
Примеры ʺзаместителяʺ, когда группы, представленные как R1, R1a, R1b и R1c, каждая содержит заместитель, включают заместители, указанные выше, и их количество типично составляет один, два или три.
[0118]
Примеры ʺгалогенаʺ, представленн как R1, R1a, R1b и R1c, включают группы, указанные выше; предпочтительно фтор, хлор и бром; более предпочтительно фтор и хлор; и еще более предпочтительно фтор.
[0119]
Примеры ʺC1-C6 алкилаʺ в ʺзамещенном или незамещенном C1-C6 алкилеʺ, представленном как R1, R1a, R1b и R1c, включают группы, указанные выше, предпочтительно C1-C4 алкил, более предпочтительно метил или н-пропил, и еще более предпочтительно метил.
[0120]
Примеры ʺзаместителяʺ в ʺзамещенном или незамещенном C1-C6 алкилеʺ, представленном как R1, R1a, R1b и R1c, включают группы, указанные выше;
предпочтительно гидрокси, C1-C6 алкокси, где водород, содержащийся в алкокси, может быть замещен 1 или несколькими атомами дейтерия, C1-C6 алкилтио или C6-C14 ароматический углеводород;
более предпочтительно C1-C6 алкокси, где водород, содержащийся в алкокси, может быть замещен 1 или несколькими атомами дейтерия, или C1-C6 алкилтио;
еще более предпочтительно C1-C4 алкокси, где водород, содержащийся в алкокси, может быть замещен 1 или несколькими атомами дейтерия; и
еще более предпочтительно метокси.
[0121]
Количество заместителей конкретно не ограничивается, но предпочтительно составляет 0-3, и более предпочтительно 1.
[0122]
ʺЗамещенный или незамещенный C1-C6 алкилʺ, представленный как R1, R1a, R1b и R1c, предпочтительно представляет собой C1-C6 алкил, который может быть замещен ʺгидрокси, C1-C6 алкокси, где водород, содержащийся в алкокси, может быть замещен 1 или несколькими атомами дейтерия, C1-C6 алкилтио или C6-C14 ароматическим углеводородомʺ;
более предпочтительно C1-C6 алкил, который может быть замещен ʺC1-C6 алкокси, где водород, содержащийся в алкокси, может быть замещен 1 или несколькими атомами дейтерия, или C1-C6 алкилтиоʺ;
еще более предпочтительно C1-C6 алкил, который замещен ʺC1-C6 алкокси, где водород, содержащийся в алкокси, может быть замещен 1 или несколькими атомами дейтерия, или C1-C6 алкилтиоʺ;
еще более предпочтительно C1-C4 алкил, который замещен одним ʺC1-C4 алкокси, где водород, содержащийся в алкокси, может быть замещен 1 или несколькими атомами дейтерияʺ;
даже еще более предпочтительно C1-C4 алкил, который замещен одним C1-C4 алкокси; и
даже еще более предпочтительно метоксиметил.
[0123]
ʺC1-C6 алкоксиʺ в ʺзамещенном или незамещенном C1-C6 алкоксиʺ, представленном как R1, R1a, R1b и R1c, включают группы, указанные выше, предпочтительно C1-C4 алкокси, и более предпочтительно метокси.
[0124]
Примеры ʺзаместителяʺ в ʺзамещенном или незамещенном C1-C6 алкоксиʺ, представленном как R1, R1a, R1b и R1c, включают группы, указанные выше, предпочтительно галоген, и более предпочтительно фтор.
[0125]
Когда заместитель в ʺзамещенном или незамещенном C1-C6 алкоксиʺ, представленно как R1, R1a, R1b и R1c, представляет собой галоген, количество заместителей конкретно не ограничивается, но предпочтительно составляет 1-3, и более предпочтительно 3.
[0126]
ʺЗамещенный или незамещенный C1-C6 алкоксиʺ, представленный как R1, R1a, R1b и R1c, предпочтительно представляет собой C1-C6 алкокси, который может быть замещен галогеном, более предпочтительно C1-C6 алкокси, еще более предпочтительно C1-C4 алкокси, и еще более предпочтительно метокси.
[0127]
Примеры ʺC2-C6 алкенилаʺ в ʺзамещенном или незамещенном C2-C6 алкенилеʺ, представленном как R1, R1a, R1b и R1c, включают группы, указанные выше, предпочтительно C2-C4 алкенил, и более предпочтительно винил и 1-пропенил.
[0128]
Примеры ʺзаместителяʺ в ʺзамещенном или незамещенном C2-C6 алкенилеʺ, представленном как R1, R1a, R1b и R1c, включают группы, указанные выше.
[0129]
ʺЗамещенный или незамещенный C2-C6 алкенилʺ, представленный как R1, R1a, R1b и R1c, предпочтительно представляет собой C2-C6 алкенил, более предпочтительно C2-C4 алкенил, еще более предпочтительно винил и 1-пропенил, и наиболее предпочтительно 1-пропенил.
[0130]
ʺC2-C6 алкинилʺ в ʺзамещенном или незамещенном C2-C6 алкинилеʺ, представленном как R1, R1a, R1b и R1c, включает группы, указанные выше, предпочтительно C2-C4 алкинил, и более предпочтительно этинил.
[0131]
Примеры ʺзаместителяʺ в ʺзамещенном или незамещенном C2-C6 алкинилеʺ, представленном как R1, R1a, R1b и R1c, включает группы, указанные выше.
[0132]
ʺЗамещенный или незамещенный C2-C6 алкинилʺ, представленный как R1, R1a, R1b и R1c, предпочтительно представляет собой C2-C6 алкинил, более предпочтительно C2-C4 алкинил, и еще более предпочтительно этинил.
[0133]
Примеры ʺзаместителяʺ в ʺзамещенном или незамещенном аминоʺ, представленном как R1, R1a, R1b и R1c, включают группы, указанные выше;
предпочтительно 4-10-членную моноциклическую или полициклическую ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или C6-C14 ароматический углеводород;
более предпочтительно 4-6-членную моноциклическую или полициклическую ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или C6-C10 ароматический углеводород;
еще более предпочтительно 4-6-членную моноциклическую ненасыщенную гетероциклическую группу, содержащую один атом азота, или C6-C10 ароматический углеводород; и
еще более предпочтительно фенил или пиридинил.
[0134]
Количество заместителей конкретно не ограничивается, но предпочтительно составляет 1.
[0135]
ʺЗамещенный или незамещенный аминоʺ, представленный как R1, R1a, R1b и R1c, предпочтительно представляет собой амино, который может быть замещен ʺодной или несколькими 4-10-членными моноциклическими или полициклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы; или C6-C14 ароматическим углеводородомʺ;
более предпочтительно амино, который может быть замещен ʺодной или несколькими 4-6-членными моноциклическими или полициклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или C6-C10 ароматическим углеводородомʺ;
еще более предпочтительно амино, который замещен одной ʺ4-6-членной моноциклической ненасыщенной гетероциклической группой, содержащей один атом азота, или C6-C10 ароматическим углеводородом ʺ; и
еще более предпочтительно амино, который замещен одной ʺфенильной или пиридинильной группойʺ
[0136]
Примеры ʺ4-10-членной моноциклической или полициклической ненасыщенной гетероциклической группы, содержащей 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ в ʺзамещенной или незамещенной 4-10-членной моноциклической или полициклической ненасыщенной гетероциклической группе, содержащей 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ, представленной как R1, R1a, R1b и R1c, включают группы, указанные выше. ʺ4-10-членная моноциклическая или полициклическая ненасыщенная гетероциклическая группа, содержащая 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ, предпочтительно представляет собой 4-6-членную моноциклическую ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы. Конкретные примеры включают пиразолил, фурил, оксазолил и т.д. ʺ4-10-членная моноциклическая или полициклическая ненасыщенная гетероциклическая группа, содержащая 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ, более предпочтительно представляет собой 4-6-членную моноциклическую ненасыщенную гетероциклическую группу, содержащую один атом кислорода; еще более предпочтительно фурил; и еще более предпочтительно фуран-2-ил.
[0137]
Примеры ʺзаместителяʺ в ʺзамещенной или незамещенной 4-10-членной моноциклической или полициклической ненасыщенной гетероциклической группе, содержащей 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ, представленной как R1, R1a, R1b и R1c, включают группы, указанные выше.
[0138]
ʺЗамещенная или незамещенная 4-10-членная моноциклическая или полициклическая ненасыщенная гетероциклическая группа, содержащая 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ, представленная как R1, R1a, R1b и R1c, предпочтительно представляет собой 4-6-членную моноциклическую ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы; более предпочтительно 4-6-членную моноциклическую ненасыщенную гетероциклическую группу, содержащую один атом кислорода; еще более предпочтительно фурил; и еще более предпочтительно фуран-2-ил.
[0139]
R1 предпочтительно представляет собой
галоген,
циано,
нитро,
C1-C6 алкил, который может быть замещен ʺгидрокси, C1-C6 алкокси, где водород, содержащийся в алкокси, может быть замещен 1 или несколькими атомами дейтерия, C1-C6 алкилтио или C6-C14 ароматическим углеводородомʺ,
C1-C6 алкокси, который может быть замещен галогеном,
C2-C6 алкенил,
C2-C6 алкинил,
амино, который может быть замещен ʺодной или несколькими 4-10-членными моноциклическими или полициклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или C6-C14 ароматическим углеводородомʺ, или
4-10-членную моноциклическую или полициклическую ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы.
R1 более предпочтительно представляет собой
галоген,
циано,
нитро,
C1-C6 алкил, который может быть замещен ʺC1-C6 алкокси, где водород, содержащийся в алкокси, может быть замещен 1 или несколькими атомами дейтерия, или C1-C6 алкилтиоʺ,
C1-C6 алкокси, который может быть замещен галогеном,
C2-C6 алкенил,
C2-C6 алкинил,
амино, который может быть замещен ʺодной или несколькими 4-10-членными моноциклическими или полициклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или C6-C14 ароматическим углеводородомʺ, или
4-10-членную моноциклическую или полициклическую ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы.
R1 еще более предпочтительно представляет собой
галоген,
C1-C6 алкил, который может быть замещен ʺC1-C6 алкокси, где водород, содержащийся в алкокси, может быть замещен 1 или несколькими атомами дейтерия, или C1-C6 алкилтиоʺ,
C1-C6 алкокси,
C2-C6 алкенил,
C2-C6 алкинил,
амино, который может быть замещен ʺодной или несколькими 4-6-членными моноциклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или C6-C10 ароматическим углеводородомʺ, или
4-6-членную моноциклическую ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы.
R1 еще более предпочтительно представляет собой
галоген,
C1-C6 алкил, который замещен ʺC1-C6 алкокси, где водород, содержащийся в алкокси, может быть замещен 1 или несколькими атомами дейтерия, или C1-C6 алкилтиоʺ,
C2-C6 алкенил,
C2-C6 алкинил или
4-6-членную моноциклическую ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы.
R1 еще более предпочтительно представляет собой
галоген,
C1-C4 алкил, который замещен одним C1-C4 алкокси, где водород, содержащийся в алкокси, может быть замещен 1 или несколькими атомами дейтерия,
C2-C6 алкенил,
C2-C6 алкинил или
4-6-членную моноциклическую ненасыщенную гетероциклическую группу, содержащую один атом кислородаʺ.
R1 еще более предпочтительно представляет собой C1-C4 алкил, который замещен одним C1-C4 алкокси.
R1 еще более предпочтительно представляет собой галоген или метоксиметил.
[0140]
R1a предпочтительно представляет собой
циано,
нитро,
C1-C6 алкил, который может быть замещен ʺгидрокси, C1-C6 алкокси, где водород, содержащийся в алкокси, может быть замещен 1 или несколькими атомами дейтерия, или C1-C6 алкилтиоʺ,
C1-C6 алкокси, который может быть замещен галогеном,
C2-C6 алкенил,
C2-C6 алкинил,
амино, который может быть замещен ʺодной или несколькими 4-10-членными моноциклическими или полициклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или C6-C14 ароматическим углеводородомʺ, или
4-10-членную моноциклическую или полициклическую ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы.
R1a более предпочтительно представляет собой
C1-C6 алкил, который может быть замещен ʺC1-C6 алкокси, где водород, содержащийся в алкокси, может быть замещен 1 или несколькими атомами дейтерия, или C1-C6 алкилтиоʺ,
C2-C6 алкенил,
C2-C6 алкинил,
амино, который может быть замещен ʺодной или несколькими 4-10-членными моноциклическими или полициклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или C6-C14 ароматическим углеводородомʺ, или
4-10-членную моноциклическую или полициклическую ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы.
R1a еще более предпочтительно представляет собой
C1-C6 алкил, который может быть замещен ʺC1-C6 алкокси, где водород, содержащийся в алкокси, может быть замещен 1 или несколькими атомами дейтерия, или C1-C6 алкилтиоʺ,
C2-C6 алкенил,
C2-C6 алкинил,
амино, который может быть замещен ʺодной или несколькими 4-6-членными моноциклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или C6-C10 ароматическим углеводородомʺ, или
4-6-членную моноциклическую ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы.
R1a еще более предпочтительно представляет собой
C1-C6 алкил, который замещен ʺC1-C6 алкокси, где водород, содержащийся в алкокси, может быть замещен 1 или несколькими атомами дейтерия, или C1-C6 алкилтиоʺ,
C2-C6 алкенил,
C2-C6 алкинил или
4-6-членную моноциклическую ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы.
R1a еще более предпочтительно представляет собой
C1-C4 алкил, который замещен одним C1-C4 алкокси, где водород, содержащийся в алкокси, может быть замещен 1 или несколькими атомами дейтерия,
C2-C6 алкенил,
C2-C6 алкинил или
4-6-членную моноциклическую ненасыщенную гетероциклическую группу, содержащую один атом кислорода.
R1a еще более предпочтительно представляет собой C1-C4 алкил, который замещен одним C1-C4 алкокси.
R1a еще более предпочтительно представляет собой метоксиметил.
[0141]
R1b предпочтительно представляет собой галоген, C1-C6 алкил или C1-C6 алкокси, более предпочтительно галоген, и еще более предпочтительно фтор.
[0142]
R1c предпочтительно представляет собой C1-C6 алкокси, более предпочтительно C1-C4 алкокси, и еще более предпочтительно метокси.
[0143]
Примеры ʺзаместителяʺ, когда каждая группа, представленная как R2, содержит заместитель, включают группы, указанные выше, и количество заместителей типично составляет один, два или три. Однако в настоящем изобретении заместитель, который содержит каждая группа, представленная как R2, не должен представлять собой ʺзамещенную или незамещенную насыщенную гетероциклическую группу, которая может содержать по меньшей мере один одинаковый или разный гетероатом, выбранный из кислорода и серы, и содержит по меньшей мере один атом азотаʺ. Когда каждая группа, представленная как R2, содержит заместитель, примеры заместителя, который может содержать насыщенная гетероциклическая группа в ʺзамещенной или незамещенной насыщенной гетероциклической группе, которая может содержать по меньшей мере один одинаковый или разный гетероатом, выбранный из кислорода и серы, и содержит по меньшей мере один атом азотаʺ, исключенной из ʺзаместителяʺ, включают группы, указанные выше; однако, заместитель, который может содержать насыщенная гетероциклическая группа, включает по меньшей мере алкил. Поэтому, когда каждая группа, представленная как R2, содержит заместитель, этот ʺзаместительʺ исключает, например, следующие:
[0144]

[0145]
[0146]
Примеры ʺC3-C10 алкилаʺ в ʺзамещенном или незамещенном C3-C10 алкилеʺ, представленном как R2, включают группы, указанные выше, предпочтительно разветвленный C3-C8 алкил, более предпочтительно разветвленный C3-C6 алкил, и еще более предпочтительно трет-бутил.
[0147]
Примеры ʺзаместителяʺ в ʺзамещенном или незамещенном C3-C10 алкилеʺ, представленном как R2, включают группы, указанные выше. Однако ʺзаместительʺ предпочтительно представляет собой галоген, C1-C6 алкокси, C3-C7 циклоалкил или ʺ4-10-членную моноциклическую или полициклическую ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ;
более предпочтительно галоген, C3-C7 циклоалкил или ʺ4-10-членную моноциклическую или полициклическую ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ;
еще более предпочтительно галоген или C3-C7 циклоалкил;
еще более предпочтительно галоген; и
еще более предпочтительно фтор.
[0148]
Количество заместителей конкретно не ограничивается, но предпочтительно составляет 0-3, и более предпочтительно 0 или 1.
[0149]
ʺЗамещенный или незамещенный C3-C10 алкилʺ, представленный как R2, предпочтительно представляет собой C3-C10 алкил, который может быть замещен ʺгалогеном, C1-C6 алкокси, C3-C7 циклоалкилом или одной или несколькими 4-10-членными моноциклическими или полициклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ;
более предпочтительно C3-C10 алкил, который может быть замещен ʺгалогеном, C3-C7 циклоалкилом или одной или несколькими 4-10-членными моноциклическими или полициклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ;
еще более предпочтительно разветвленный C3-C8 алкил, который может быть замещен ʺгалогеном или C3-C7 циклоалкиломʺ;
еще более предпочтительно разветвленный C3-C6 алкил, который может быть замещен галогеном;
даже еще более предпочтительно разветвленный C3-C6 алкил, который может быть замещен одним атомом галогена; и
еще более предпочтительно трет-бутил, который может быть замещен фтором.
[0150]
В формуле (I) примеры ʺC3-C7 циклоалкилаʺ в ʺзамещенном или незамещенном C3-C7 циклоалкилеʺ, представленном как R2, включают группы, указанные выше, предпочтительно C3-C5 циклоалкил, более предпочтительно C3-C4 циклоалкил, и еще более предпочтительно циклопропил.
[0151]
В формуле (I') примеры ʺC3-C4 циклоалкилаʺ в ʺзамещенном или незамещенном C3-C4 циклоалкилеʺ, представленном как R2, включают группы, указанные выше, и предпочтительно циклопропил.
[0152]
В формулах (I) и (I') примеры ʺзаместителяʺ в ʺзамещенном или незамещенном C3-C7 циклоалкилеʺ и ʺзамещенном или незамещенном C3-C4 циклоалкилеʺ, представленном как R2, включают группы, указанные выше;
предпочтительно галоген, C1-C6 алкил, C3-C7 циклоалкил или галогенo C1-C6 алкил;
более предпочтительно C1-C6 алкил, C3-C7 циклоалкил или галогенo C1-C6 алкил;
еще более предпочтительно C1-C4 алкил или C3-C5 циклоалкил;
еще более предпочтительно метил или циклопропил; и
еще более предпочтительно метил.
[0153]
Количество заместителей конкретно не ограничивается, но предпочтительно составляет 0-3, более предпочтительно 0-2, и еще более предпочтительно 1.
[0154]
ʺЗамещенный или незамещенный C3-C7 циклоалкилʺ, представленный как R2 в формуле (I), предпочтительно представляет собой C3-C7 циклоалкил, который может быть замещен ʺгалогеном, C1-C6 алкилом, C3-C7 циклоалкилом или галогенo C1-C6 алкиломʺ;
более предпочтительно C3-C7 циклоалкил, который может быть замещен ʺC1-C6 алкилом, C3-C7 циклоалкилом или галогенo C1-C6 алкиломʺ;
еще более предпочтительно C3-C7 циклоалкил, который может быть замещен ʺC1-C4 алкилом или C3-C5 циклоалкиломʺ;
еще более предпочтительно C3-C5 циклоалкил, который может быть замещен одним ʺC1-C4 алкилом или C3-C5 циклоалкиломʺ;
еще более предпочтительно C3-C4 циклоалкил, который может быть замещен одним ʺC1-C4 алкилом или C3-C5 циклоалкиломʺ;
еще более предпочтительно циклопропил, который может быть замещен одним ʺметилом или циклопропиломʺ; и
еще более предпочтительно
[0155]

[0156]
[0157]
ʺЗамещенный или незамещенный C3-C4 циклоалкилʺ, представленный как R2 в формуле (I'), предпочтительно представляет собой C3-C4 циклоалкил, который может быть замещен ʺгалогеном, C1-C6 алкилом, C3-C7 циклоалкилом или галогенo C1-C6 алкиломʺ;
более предпочтительно C3-C4 циклоалкил, который может быть замещен ʺC1-C6 алкилом, C3-C7 циклоалкилом или галогенo C1-C6 алкиломʺ;
еще более предпочтительно C3-C4 циклоалкил, который может быть замещен ʺC1-C4 алкилом или C3-C5 циклоалкиломʺ;
еще более предпочтительно C3-C4 циклоалкил, который может быть замещен одним ʺC1-C4 алкилом или C3-C5 циклоалкиломʺ;
даже еще более предпочтительно циклоалкил, который может быть замещен одним ʺметилом или циклопропиломʺ; и
еще более предпочтительно
[0158]
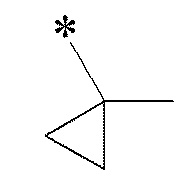
[0159]
[0160]
Примеры ʺC4-C12 связанного мостиковой связью циклоалкилаʺ в ʺзамещенном или незамещенном C4-C12 связанном мостиковой связью циклоалкилеʺ, представленном как R2, включают группы, указанные выше, предпочтительно C5-C10 связанный мостиковой связью циклоалкил, и более предпочтительно
[0161]

[0162]
[0163]
Примеры ʺзаместителяʺ в ʺзамещенном или незамещенном C4-C12 связанном мостиковой связью циклоалкилеʺ, представленном как R2, включают группы, указанные выше.
[0164]
ʺЗамещенный или незамещенный C4-C12 связанный мостиковой связью циклоалкилʺ, представленный как R2, предпочтительно представляет собой C4-C12 связанный мостиковой связью циклоалкил, более предпочтительно C5-C10 связанный мостиковой связью циклоалкил, и более предпочтительно
[0165]

[0166]
[0167]
Примеры ʺC2-C6 алкенилаʺ в ʺзамещенном или незамещенном C2-C6 алкенилеʺ, представленном как R2, включают группы, указанные выше, предпочтительно C2-C4 алкенил, и более предпочтительно изопропенил.
[0168]
Примеры ʺзаместителяʺ в ʺзамещенном или незамещенном C2-C6 алкенилеʺ, представленном как R2, включают группы, указанные выше, предпочтительно галоген, и более предпочтительно фтор.
[0169]
Количество заместителей конкретно не ограничивается, но предпочтительно составляет 1.
[0170]
ʺЗамещенный или незамещенный C2-C6 алкенилʺ, представленный как R2, предпочтительно представляет собой C2-C6 алкенил, который может быть замещен галогеном, более предпочтительно C2-C4 алкенил, который может быть замещен фтором, и еще более предпочтительно фторизопропенил.
[0171]
В формуле (I) примеры ʺC3-C7 циклоалкенилаʺ в ʺзамещенном или незамещенном C3-C7 циклоалкенилеʺ, представленном как R2, включают группы, указанные выше, и предпочтительно циклопентенил.
[0172]
В формуле (I') примеры ʺC3-C4 циклоалкенилаʺ в ʺзамещенном или незамещенном C3-C4 циклоалкенилеʺ, представленном как R2, включают группы, указанные выше.
[0173]
В формулах (I) и (I') примеры ʺзаместителяʺ в ʺзамещенном или незамещенном C3-C7 циклоалкенилеʺ и ʺзамещенном или незамещенном C3-C4 циклоалкенилеʺ, представленном как R2, включают группы, указанные выше.
[0174]
В формуле (I) ʺзамещенный или незамещенный C3-C7 циклоалкенилʺ, представленный как R2, предпочтительно представляет собой C3-C7 циклоалкенил, и более предпочтительно циклопентенил.
[0175]
В формуле (I') ʺзамещенный или незамещенный C3-C4 циклоалкенилʺ, представленный как R2, предпочтительно представляет собой C3-C4 циклоалкенил.
[0176]
Примеры ʺ4-10-членной моноциклической или полициклической насыщенной гетероциклической группы, содержащей 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ, в ʺзамещенной или незамещенной 4-10-членной моноциклической или полициклической насыщенной гетероциклической группе, содержащей 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ, представленной как R2, включают группы, указанные выше.
[0177]
ʺЗаместительʺ в ʺзамещенной или незамещенной 4-10-членной моноциклической или полициклической насыщенной гетероциклической группе, содержащей 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ, представленной как R2, включают группы, указанные выше.
[0178]
R2 в формуле (I) предпочтительно представляет собой
замещенный или незамещенный C3-C10 алкил,
замещенный или незамещенный C3-C7 циклоалкил,
замещенный или незамещенный C4-C12 связанный мостиковой связью циклоалкил,
замещенный или незамещенный C2-C6 алкенил или
замещенный или незамещенный C3-C7 циклоалкенил,
при условии, что, когда каждая группа, представленная как R2, содержит заместитель, этот заместитель не должен представлять собой ʺзамещенную или незамещенную насыщенную гетероциклическую группу, которая может содержать по меньшей мере один одинаковый или разный гетероатом, выбранный из кислорода и серы, и содержит по меньшей мере один атом азота.ʺ
R2 более предпочтительно представляет собой
C3-C10 алкил, который может быть замещен ʺгалогеном, C1-C6 алкокси, C3-C7 циклоалкилом или одной или несколькими 4-10-членными моноциклическими или полициклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ,
C3-C7 циклоалкил, который может быть замещен ʺгалогеном, C1-C6 алкилом, C3-C7 циклоалкилом или галогенo C1-C6 алкиломʺ,
C4-C12 связанный мостиковой связью циклоалкил,
C2-C6 алкенил, который может быть замещен галогеном, или
C3-C7 циклоалкенил.
R2 еще более предпочтительно представляет собой
C3-C10 алкил, который может быть замещен ʺгалогеном, C3-C7 циклоалкилом или одной или несколькими 4-10-членными моноциклическими или полициклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ,
C3-C7 циклоалкил, который может быть замещен ʺC1-C6 алкилом, C3-C7 циклоалкилом или галогенo C1-C6 алкиломʺ,
C4-C12 связанный мостиковой связью циклоалкил или
C3-C7 циклоалкенил.
R2 еще более предпочтительно представляет собой
C3-C10 алкил, который может быть замещен ʺгалогеном, C3-C7 циклоалкилом или одной или несколькими 4-10-членными моноциклическими или полициклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ,
C3-C7 циклоалкил, который может быть замещен ʺC1-C6 алкилом, C3-C7 циклоалкилом или галогенo C1-C6 алкиломʺ, или
C4-C12 связанный мостиковой связью циклоалкил.
R2 еще более предпочтительно представляет собой
разветвленный C3-C8 алкил, который может быть замещен ʺгалогеном или C3-C7 циклоалкиломʺ,
C3-C7 циклоалкил, который может быть замещен ʺC1-C4 алкилом или C3-C5 циклоалкиломʺ, или
C4-C12 связанный мостиковой связью циклоалкил.
R2 еще более предпочтительно представляет собой
разветвленный C3-C6 алкил, который может быть замещен галогеном, или
C3-C7 циклоалкил, который может быть замещен ʺC1-C4 алкилом или C3-C5 циклоалкиломʺ.
R2 еще более предпочтительно представляет собой
разветвленный C3-C6 алкил, который может быть замещен галогеном, или
C3-C5 циклоалкил, который может быть замещен ʺC1-C4 алкилом или C3-C5 циклоалкиломʺ.
R2 еще более предпочтительно представляет собой C3-C5 циклоалкил, который может быть замещен одним C1-C4 алкилом.
R2 еще более предпочтительно представляет собой
[0179]

[0180]
[0181]
Кроме того, R2 в формуле (I') предпочтительно представляет собой
замещенный или незамещенный C3-C10 алкил,
замещенный или незамещенный C3-C4 циклоалкил,
замещенный или незамещенный C4-C12 связанный мостиковой связью циклоалкил,
замещенный или незамещенный C2-C6 алкенил или
замещенный или незамещенный C3-C4 циклоалкенил,
при условии, что, когда каждая группа, представленная как R2, содержит заместитель, этот заместитель не должен представлять собой ʺзамещенную или незамещенную насыщенную гетероциклическую группу, которая может содержать по меньшей мере один одинаковый или разный гетероатом, выбранный из кислорода и серы, и содержит по меньшей мере один атом азотаʺ.
R2 более предпочтительно представляет собой
C3-C10 алкил, который может быть замещен ʺгалогеном, C1-C6 алкокси, C3-C7 циклоалкилом или одной или несколькими 4-10-членными моноциклическими или полициклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ,
C3-C4 циклоалкил, который может быть замещен ʺгалогеном, C1-C6 алкилом, C3-C7 циклоалкилом или галогенo C1-C6 алкиломʺ,
C4-C12 связанный мостиковой связью циклоалкил,
C2-C6 алкенил, который может быть замещен галогеном, или
C3-C4 циклоалкенил.
R2 еще более предпочтительно представляет собой
C3-C10 алкил, который может быть замещен ʺгалогеном, C3-C7 циклоалкилом или одной или несколькими 4-10-членными моноциклическими или полициклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ,
C3-C4 циклоалкил, который может быть замещен ʺC1-C6 алкилом, C3-C7 циклоалкилом или галогенo C1-C6 алкиломʺ,
C4-C12 связанный мостиковой связью циклоалкил или
C3-C4 циклоалкенил.
R2 еще более предпочтительно представляет собой
C3-C10 алкил, который может быть замещен ʺгалогеном, C3-C7 циклоалкилом или одной или несколькими 4-10-членными моноциклическими или полициклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ,
C3-C4 циклоалкил, который может быть замещен ʺC1-C6 алкилом, C3-C7 циклоалкилом или галогенo C1-C6 алкиломʺ, или
C4-C12 связанный мостиковой связью циклоалкил.
R2 еще более предпочтительно представляет собой
разветвленный C3-C8 алкил, который может быть замещен ʺгалогеном или C3-C7 циклоалкиломʺ,
C3-C4 циклоалкил, который может быть замещен ʺC1-C4 алкилом или C3-C5 циклоалкиломʺ, или
C4-C12 связанный мостиковой связью циклоалкил.
R2 еще более предпочтительно представляет собой
разветвленный C3-C6 алкил, который может быть замещен галогеном, или
C3-C4 циклоалкил, который может быть замещен ʺC1-C4 алкилом или C3-C5 циклоалкиломʺ.
R2 еще более предпочтительно представляет собой
C3-C4 циклоалкил, который может быть замещен одним C1-C4 алкилом.
R2 еще более предпочтительно представляет собой
[0182]
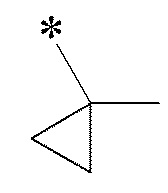
[0183]
[0184]
Предпочтительно, когда R2 связан с атомом азота, который содержится в пирролопиримидиновом или пиразолoпиримидиновом скелете в формулах (I) и (I'), через атом углерода из атомов, содержащихся в R2, и когда количество атомов водорода, которые содержит атом углерода, составляет 0 или 1. То есть, предпочтительно, когда в следующей части формул (I) и (I'):
[0185]

[0186]
атом углерода, содержащийся в R2, и указанный выше атом азота связаны вместе, и когда атом углерода содержит 0 или 1 атом водорода. В R2 количество атомов водорода, которые содержит атом углерода, более предпочтительно составляет 0.
[0187]
Примеры ʺзаместителяʺ, когда каждая группа, представленная как R3, содержит заместитель, включают группы, указанные выше и их количество типично составляет один, два или три.
[0188]
Примеры ʺгалогенаʺ, представленного как R3, включают группы, указанные выше; и предпочтительно фтор, хлор и бром.
[0189]
Примеры ʺC1-C6 алкилаʺ в ʺзамещенном или незамещенном C1-C6 алкилеʺ, представленном как R3, включают группы, указанные выше, предпочтительно C1-C4 алкил, более предпочтительно метил или этил, и еще более предпочтительно метил.
[0190]
Примеры ʺзаместителяʺ в ʺзамещенном или незамещенном C1-C6 алкилʺ, представленном как R3, включают группы, указанные выше, и предпочтительно гидрокси или оксо.
[0191]
Количество заместителей конкретно не ограничивается, но предпочтительно составляет 0 или 1, и более предпочтительно 0.
[0192]
ʺЗамещенный или незамещенный C1-C6 алкилʺ, представленный как R3, предпочтительно представляет собой C1-C6 алкил, который может быть замещен гидрокси или оксо группой, более предпочтительно C1-C4 алкил, который может быть замещен гидрокси или оксо группой, еще более предпочтительно C1-C4 алкил, и еще более предпочтительно метил.
[0193]
ʺC1-C6 алкоксиʺ в ʺзамещенном или незамещенном C1-C6 алкоксиʺ, представленном как R3, включают группы, указанные выше, предпочтительно C1-C4 алкокси, и более предпочтительно метокси или этокси.
[0194]
Примеры ʺзаместителяʺ в ʺзамещенном или незамещенном C1-C6 алкоксиʺ, представленном как R3, включают группы, указанные выше;
предпочтительно галоген, C1-C6 алкокси, C3-C7 циклоалкил, или 4-10-членную моноциклическую насыщенную гетероциклическую группу, которая может быть замещена окси группой и содержит 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы;
более предпочтительно галоген, C1-C4 алкокси, C3-C7 циклоалкил или или 4-10-членную моноциклическую насыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы;
еще более предпочтительно C1-C4 алкокси, C3-C7 циклоалкил, или или 4-10-членную моноциклическую насыщенную гетероциклическую группу, содержащую один атом кислорода; и
еще более предпочтительно тетрагидрофуранил.
[0195]
Количество заместителей конкретно не ограничивается, но предпочтительно составляет 0 или 1, и более предпочтительно 1.
[0196]
ʺЗамещенный или незамещенный C1-C6 алкоксиʺ, представленный как R3, предпочтительно представляет собой C1-C6 алкокси, который может быть замещен ʺгалогеном, C1-C6 алкокси, C3-C7 циклоалкилом или одной или несколькими 4-10-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены оксо и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ;
более предпочтительно C1-C4 алкокси, который может быть замещен ʺгалогеном, C1-C4 алкокси, C3-C7 циклоалкилом или одной или несколькими 4-6-членными моноциклическими насыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ;
еще более предпочтительно C1-C4 алкокси, который может быть замещен ʺC1-C4 алкокси, C3-C7 циклоалкилом или одной или несколькими 4-6-членными моноциклическими насыщенными гетероциклическими группами, содержащими один атом кислородаʺ;
еще более предпочтительно C1-C4 алкокси, который может быть замещен ʺодной или несколькими 4-6-членными моноциклическими насыщенными гетероциклическими группами, содержащими один атом кислородаʺ; и
еще более предпочтительно этокси или тетрагидрофуранилметокси.
[0197]
ʺC1-C6 алкилтиоʺ в ʺзамещенном или незамещенном C1-C6 алкилтиоʺ, представленном как R3, включает группы, указанные выше, предпочтительно C1-C4 алкилтио, и более предпочтительно метилтио.
[0198]
Примеры ʺзаместителяʺ в ʺзамещенном или незамещенном C1-C6 алкилтиоʺ, представленном как R3, включают группы, указанные выше.
[0199]
Количество заместителей конкретно не ограничивается, но предпочтительно составляет 0 или 1, и более предпочтительно 0.
[0200]
ʺЗамещенный или незамещенный C1-C6 алкилтиоʺ, представленный как R3, предпочтительно представляет собой C1-C6 алкилтио, более предпочтительно C1-C4 алкилтио, и еще более предпочтительно метилтио.
[0201]
ʺC3-C7 циклоалкилʺ в ʺзамещенном или незамещенном C3-C7 циклоалкилеʺ, представленном как R3, включает группы, указанные выше, и предпочтительно циклопропил.
[0202]
Примеры ʺзаместителяʺ в ʺ ʺзамещенном или незамещенном C3-C7 циклоалкилеʺ, представленном как R3, включают группы, указанные выше.
[0203]
ʺЗамещенный или незамещенный C3-C7 циклоалкилʺ, представленный как R3, предпочтительно представляет собой C3-C7 циклоалкил, более предпочтительно C3-C5 циклоалкил, и еще более предпочтительно циклопропил.
[0204]
Примеры ʺC2-C6 алкенилаʺ в ʺзамещенном или незамещенном C2-C6 алкенилеʺ, представленном как R3, включают группы, указанные выше, предпочтительно C2-C4 алкенил, и еще более предпочтительно винил.
[0205]
Примеры ʺзаместителяʺ в ʺзамещенном или незамещенном C2-C6 алкенилеʺ, представленном как R3, включают группы, указанные выше, и предпочтительно гидрокси.
[0206]
Количество заместителей конкретно не ограничивается, но предпочтительно составляет 0 или 1, и более предпочтительно 0.
[0207]
ʺЗамещенный или незамещенный C2-C6 алкенилʺ, представленный как R3, предпочтительно представляет собой C2-C6 алкенил, который может быть замещен ʺгидроксиʺ;
более предпочтительно C2-C4 алкенил, который может быть замещен ʺгидроксиʺ;
еще более предпочтительно C2-C4 алкенил; и
еще более предпочтительно винил.
[0208]
Примеры ʺC2-C6 алкинилаʺ в ʺзамещенном или незамещенном C2-C6 алкинилеʺ, представленном как R3, включают группы, указанные выше, предпочтительно C2-C4 алкинил, и более предпочтительно этинил или пропинил.
[0209]
Количество тройных связей в ʺC2-C6 алкинилеʺ предпочтительно представляет собой 1, и положение тройной связи предпочтительно находится между атомом углерода, связанным с 7H-пирроло[2,3-d]пиримидиновым скелетом, и атомом углерода, смежным с этим атомом углерода.
[0210]
Примеры ʺзаместителяʺ в ʺзамещенном или незамещенном C2-C6 алкинилнʺ, представленном как R3, включают группы, указанные выше, и предпочтительно
гидрокси,
C1-C6 алкокси,
амино, который может быть замещен группой R4,
C1-C6 алкилсилилокси,
C3-C7 циклоалкил, который может быть замещен ʺгидрокси или оксоʺ,
C6-C14 ароматический углеводород, который может быть замещен группой R5,
одну или несколько 4-10-членных моноциклических насыщенных гетероциклических групп, которые могут быть замещены группой R6 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы,
одну или несколько 4-10-членных моноциклических или полициклических ненасыщенных гетероциклических групп, которые могут быть замещены группой R7 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или
ненасыщенный гетероциклический окси, который может быть замещен галогеном, где ненасыщенное гетероциклическое кольцо представляет собой 4-10-членное моноциклическое или полициклическое ненасыщенное гетероциклическое кольцо, содержащее 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы.
[0211]
ʺC1-C6 алкоксиʺ, указанный выше в качестве примера заместителя в ʺ ʺзамещенном или незамещенном амещенный C2-C6 алкинилеʺ, представленном как R3, предпочтительно представляет собой C1-C4 алкокси, и более предпочтительно метокси.
[0212]
R4 в ʺамино, который может быть замещен группой R4ʺ, указанном выше в качестве примера заместителя в ʺзамещенном или незамещенном C2-C6 алкинилеʺ, представленном как R3, предпочтительно представляет собой C1-C6 алкил, C1-C4 алкокси C1-C6 алкил или карбамоил, который может быть замещен C3-C7 циклоалкилом.
ʺАмино, который может быть замещен группой R4ʺ, указанный выше в качестве примера заместителя в ʺзамещенном или незамещенном C2-C6 алкинилеʺ, представленном как R3, предпочтительно представляет собой амино, который может быть замещен группой R4, где R4 представляет собой C1-C4 алкил или C1-C4 алкокси C1-C4 алкил; и
более предпочтительно амино, который может быть замещен группой R4, где R4 представляет собой метил или метоксиэтил.
[0213]
ʺC1-C6 алкилсилилоксиʺ, указанный выше в качестве примера заместителя в ʺзамещенном или незамещенном C2-C6 алкинилеʺ, представленном как R3, предпочтительно представляет собой три-C1-C6 алкилсилилокси, и более предпочтительно трет-бутилдиметилсилилокси.
[0214]
C3-C7 циклоалкил, который может быть замещен ʺгидрокси или оксоʺ, указанный выше в качестве примера заместителя в ʺзамещенном или незамещенном C2-C6 алкинилеʺ, представленном как R3, предпочтительно представляет собой C3-C7 циклоалкил, который может быть замещен ʺгидрокси.ʺ
[0215]
R5 в ʺC6-C14 ароматическом углеводороде, который может быть замещен группой R5ʺ, указанном выше в качестве примера заместителя в ʺзамещенном или незамещенном C2-C6 алкинилеʺ, представленном как R3, предпочтительно представляет собой
галоген,
C1-C4 алкиламино, который может быть замещен одной или несколькими 4-10-членными моноциклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или
C1-C6 алкокси.
[0216]
ʺC6-C14 ароматический углеводород, который может быть замещен группой R5ʺ, указанный выше в качестве примера заместителя в ʺзамещенном или незамещенном C2-C6 алкинилеʺ, представленном как R3, предпочтительно представляет собой фенил, который может быть замещен группой R5, где R5 представляет собой галоген, метиламино, который может быть замещен одной или несколькими 4-6-членными моноциклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или C1-C4 алкокси; и
более предпочтительно фенил, который может быть замещен группой R5, где R5 представляет собой галоген.
[0217]
R6 в ʺодной или нескольких 4-10-членных моноциклических насыщенных гетероциклических группах, которые могут быть замещены группой R6 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ, указанных выше в качестве примера заместителя в ʺзамещенном или незамещенном C2-C6 алкинилеʺ, представленном как R3, предпочтительно представляет собой гидрокси, C1-C6 алкил, C1-C6 алкокси или оксо.
[0218]
ʺОдна или несколько 4-10-членных моноциклических насыщенных гетероциклических групп, которые могут быть замещены группой R6 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ, указанные выше в качестве примера заместителя в ʺзамещенном или незамещенном C2-C6 алкинилеʺ, представленном как R3, предпочтительно представляют собой ʺодну или несколько 4-6-членных моноциклических насыщенных гетероциклических групп, которые может быть замещены группой R6 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ, где R6 представляет собой гидрокси, C1-C4 алкил, C1-C4 алкокси или оксо;
более предпочтительно ʺодну или несколько 4-6-членных моноциклических насыщенных гетероциклических групп, которые может быть замещены группой R6 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы,ʺ где R6 представляет собой гидрокси, C1-C4 алкил или оксо;
еще более предпочтительно ʺодну или несколько 4-6-членных моноциклических насыщенных гетероциклических групп, которые могут быть замещены группой R6 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ, где R6 представляет собой гидрокси или метил; и
еще более предпочтительно морфолино, тетрагидропиранил, пирролидинил, пиперидинил или оксетанил, который может быть замещен группой R6, где R6 представляет собой гидрокси или метил.
[0219]
R7 в ʺодной или нескольких 4-10-членных моноциклических или полициклических ненасыщенных гетероциклических группах, которые могут быть замещены группой R7 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ, указанных выше в качестве примера заместителя в ʺзамещенном или незамещенном C2-C6 алкинилеʺ, представленном как R3, представляет собой галоген, циано, C1-C6 алкил, C1-C6 алкокси или амино.
[0220]
ʺОдна или несколько 4-10-членных моноциклических или полициклических ненасыщенных гетероциклических групп, которые могут быть замещены группой R7 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ предпочтительно представляют собой ʺодну или несколько 4-10-членных моноциклических или бициклических ненасыщенных гетероциклических групп, которые могут быть замещены группой R7 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ, где R7 представляет собой галоген, циано, C1-C4 алкил, C1-C4 алкокси или амино;
более предпочтительно ʺодну или несколько 4-10-членных моноциклических или бициклических ненасыщенных гетероциклических групп, которые могут быть замещены группой R7 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ, где R7 представляет собой C1-C4 алкил или амино; и
еще более предпочтительно пиразолил, имидазо[1,2-b]пиридазинил, имидазолил, пиридинил, тиазолил или фуро[3,2-b]пиридинил, который может быть замещен группой R7, где R7 представляет собой C1-C4 алкил или амино.
[0221]
ʺНенасыщенный гетероциклический окси, который может быть замещен галогеном, где ненасыщенное гетероциклическое кольцо представляет собой 4-10-членное моноциклическое или полициклическое ненасыщенное гетероциклическое кольцо, содержащее 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ, указанный выше в качестве примера заместителя в ʺзамещенном или незамещенном C2-C6 алкинилеʺ, представленном как R3, предпочтительно представляет собой ʺненасыщенный гетероциклический окси, который может быть замещен галогеном, где ненасыщенное гетероциклическое кольцо представляет собой 4-6-членное моноциклическое ненасыщенное гетероциклическое кольцо, содержащее 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ, и
более предпочтительно ʺпиридинилокси, который может быть замещен галогеномʺ.
[0222]
Количество заместителей в ʺC2-C6 алкинилеʺ в ʺзамещенном или незамещенном C2-C6 алкинилеʺ, представленном как R3, конкретно не ограничивается, но предпочтительно составляет 1.
[0223]
ʺЗамещенный или незамещенный C2-C6 алкинилʺ, представленный как R3, предпочтительно представляет собой C2-C6 алкинил, который может быть замещен
ʺгидрокси,
C1-C6 алкокси,
амино, который может быть замещен группой R4, где R4 представляет собой C1-C6 алкил, C1-C4 алкокси C1-C6 алкил или карбамоил, который может быть замещен C3-C7 циклоалкилом,
C1-C6 алкилсилилокси,
C3-C7 циклоалкилом, который может быть замещен ʺгидрокси или оксоʺ,
C6-C14 ароматическим углеводородом, который может быть замещен группой R5, где R5 представляет собой галоген, C1-C4 алкиламино, который может быть замещен одной или несколькими 4-10-членными моноциклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или C1-C6 алкокси,
одной или несколькими 4-10-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены группой R6 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R6 представляет собой гидрокси, C1-C6 алкил, C1-C6 алкокси или оксо,
одной или несколькими 4-10-членными моноциклическими или полициклическими ненасыщенными гетероциклическими группами, которые могут быть замещены группой R7 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R7 представляет собой галоген, циано, C1-C6 алкил, C1-C6 алкокси или амино, или
ненасыщенным гетероциклическим окси, который может быть замещен галогеном, где ненасыщенное гетероциклическое кольцо представляет собой 4-10-членное моноциклическое или полициклическое ненасыщенное гетероциклическое кольцо, содержащее 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ,
при условии, что положение тройной связи C2-C6 алкинила находится между атомом углерода, связанным с 7H-пирроло[2,3-d]пиримидиновым скелетом, и атомом углерода, смежным с этим атомом углерода;
более предпочтительно C2-C6 алкинил, который может быть замещен
ʺгидрокси,
C1-C4 алкокси,
амино, который может быть замещен группой R4, где R4 представляет собой C1-C4 алкил, C1-C4 алкокси C1-C4 алкил или карбамоил, который может быть замещен C3-C5 циклоалкилом,
три-C1-C6 алкилсилилокси,
C3-C7 циклоалкилом, который может быть замещен ʺгидрокси или оксоʺ,
фенилом, который может быть замещен группой R5, где R5 представляет собой галоген, метиламино, который может быть замещен одной или несколькими 4-6-членными моноциклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или C1-C4 алкокси,
одной или несколькими 4-6-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены группой R6 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R6 представляет собой гидрокси, C1-C4 алкил, C1-C4 алкокси или оксо,
одной или несколькими 4-10-членными моноциклическими или бициклическими ненасыщенными гетероциклическими группами, которые могут быть замещены группой R7 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R7 представляет собой галоген, циано, C1-C4 алкил, C1-C4 алкокси или амино, или
ненасыщенным гетероциклическим окси, который может быть замещен галогеном, где ненасыщенное гетероциклическое кольцо представляет собой 4-6-членное моноциклическое ненасыщенное гетероциклическое кольцо, содержащее 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ,
при условии, что положение тройной связи C2-C6 алкинила находится между атомом углерода, связанным с 7H-пирроло[2,3-d]пиримидиновым скелетом, и атомом углерода, смежным с этим атомом углерода;
еще более предпочтительно C2-C6 алкинил, который может быть замещен
ʺгидрокси,
C1-C4 алкокси,
амино, который может быть замещен группой R4, где R4 представляет собой C1-C4 алкил, C1-C4 алкокси C1-C4 алкил или карбамоил, который может быть замещен C3-C5 циклоалкилом,
три-C1-C6 алкилсилилокси,
C3-C7 циклоалкилом, который может быть замещен ʺгидрокси или оксоʺ,
фенилом, который может быть замещен группой R5, где R5 представляет собой галоген,
ʺодной или несколькими 4-6-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены группой R6 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ, где R6 представляет собой гидрокси, C1-C4 алкил, C1-C4 алкокси или оксо,
ʺодной или несколькими 4-10-членными моноциклическими или бициклическими ненасыщенными гетероциклическими группами, которые могут быть замещены группой R7 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ, где R7 представляет собой галоген, циано, C1-C4 алкил, C1-C4 алкокси или амино, или
ненасыщенным гетероциклическим окси, который может быть замещен галогеном, где ненасыщенное гетероциклическое кольцо представляет собой 4-6-членное моноциклическое ненасыщенное гетероциклическое кольцо, содержащее 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ,
при условии, что положение тройной связи C2-C6 алкинила находится между атомом углерода, связанным с 7H-пирроло[2,3-d]пиримидиновым скелетом, и атомом углерода, смежным с этим атомом углерода;
еще более предпочтительно C2-C6 алкинил, который может быть замещен
ʺгидрокси,
амино, который может быть замещен группой R4, где R4 представляет собой C1-C4 алкил или C1-C4 алкокси C1-C4 алкил,
C3-C7 циклоалкилом, который может быть замещен гидрокси,
фенилом, который может быть замещен группой R5, где R5 представляет собой галоген,
ʺодной или несколькими 4-6-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены группой R6 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ, где R6 представляет собой гидрокси, C1-C4 алкил или оксо, или
ʺодной или несколькими 4-10-членными моноциклическими или бициклическими ненасыщенными гетероциклическими групп, которые могут быть замещены группой R7 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы,ʺ где R7 представляет собой галоген, циано, C1-C4 алкил, C1-C4 алкокси или аминоʺ,
при условии, что положение тройной связи C2-C6 алкинила находится между атомом углерода, связанным с 7H-пирроло[2,3-d]пиримидиновым скелетом, и атомом углерода, смежным с этим атомом углерода; и
еще более предпочтительно C2-C6 алкинил, который может быть замещен
ʺгидрокси,
амино, который может быть замещен группой R4, где R4 представляет собой метил или метоксиэтил,
C3-C7 циклоалкилом, который может быть замещен гидрокси,
ʺодной или несколькими 4-6-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены группой R6 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ, где R6 представляет собой гидрокси или метил, или
ʺодной или несколькими 4-10-членными моноциклическими или бициклическими ненасыщенными гетероциклическими группами, которые могут быть замещены группой R7 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ, где R7 представляет собой C1-C4 алкил или аминоʺ,
при условии, что положение тройной связи C2-C6 алкинила находится между атомом углерода, связанным с 7H-пирроло[2,3-d]пиримидиновым скелетом, и атомом углерода, смежным с этим атомом углерода.
[0224]
Предпочтительные конкретные примеры включают
[0225]

[0226]
[0227]
Примеры ʺзаместителяʺ в ʺзамещенном или незамещенном аминоʺ, представленном как R3, включают группы, указанные выше.
[0228]
Примеры ʺзаместителяʺ в ʺзамещенном или незамещенном карбамоилеʺ, представленном как R3, включают группы, указанные выше.
[0229]
Примеры ʺC6-C14 ароматического углеводородаʺ в ʺзамещенном или незамещенном C6-C14 ароматическом углеводородеʺ, представленном как R3, включают группы, указанные выше, и предпочтительно фенил.
[0230]
Примеры ʺзаместителяʺ в ʺзамещенном или незамещенном C6-C14 ароматическом углеводородеʺ, представленном как R3, включают группы, указанные выше;
предпочтительно
гидрокси,
C1-C6 алкил, который может быть замещен гидрокси,
формил или
одну или несколько 4-10-членных моноциклических насыщенных гетероциклических групп, которые могут быть замещены C1-C6 алкилом и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы;
более предпочтительно
гидрокси,
C1-C4 алкил, который может быть замещен гидрокси,
формил или
одну или несколько 4-6-членных моноциклических насыщенных гетероциклических групп, которые могут быть замещены C1-C4 алкилом и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы;
еще более предпочтительно
гидрокси,
C1-C4 алкил, который может быть замещен гидрокси, или
формил; и
еще более предпочтительно
гидрокси или
C1-C4 алкил, который может быть замещен гидрокси.
[0231]
Количество заместителей конкретно не ограничивается, но предпочтительно составляет 0 или 1, и более предпочтительно 1.
[0232]
ʺЗамещенный или незамещенный C6-C14 ароматический углеводородʺ, представленный как R3, предпочтительно представляет собой C6-C14 ароматический углеводород, который может быть замещен
ʺгидрокси,
C1-C6 алкилом, который может быть замещен гидрокси,
формилом или
одной или несколькими 4-10-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены C1-C6 алкилом и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ;
более предпочтительно фенил, который может быть замещен
ʺгидрокси,
C1-C4 алкилом, который может быть замещен гидрокси,
формилом или
одной или несколькими 4-6-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены C1-C4 алкилом и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ;
еще более предпочтительно фенил, который может быть замещен
ʺгидрокси,
C1-C4 алкилом, который может быть замещен гидрокси, или
формиломʺ; и
еще более предпочтительно фенил, который может быть замещен
ʺгидрокси или
C1-C4 алкилом, который может быть замещен гидроксиʺ.
[0233]
Примеры ʺ4-10-членной моноциклической или полициклической насыщенной гетероциклической группы, содержащей 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ в ʺзамещенной или незамещенной 4-10-членной моноциклической или полициклической насыщенной гетероциклической группе, содержащей 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ, представленной как R3, включают группы, указанные выше.
[0234]
Примеры ʺзаместителяʺ в ʺзамещенной или незамещенной 4-10-членной моноциклической или полициклической насыщенной гетероциклической группе, содержащей 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ, представленной как R3, включают группы, указанные выше.
[0235]
ʺ4-10-членная моноциклическая или полициклическая ненасыщенная гетероциклическая группа, содержащая 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ в ʺзамещенной или незамещенной 4-10-членной моноциклической или полициклической ненасыщенной гетероциклической группе, содержащей 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ, представленной как R3, включает группы, указанные выше; предпочтительно 4-6-членную моноциклическую или полициклическую ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы; более предпочтительно 4-6-членную моноциклическую ненасыщенную гетероциклическую группу, содержащую один ли два атома азота; и еще более предпочтительно пиразолил.
[0236]
Примеры ʺзаместителяʺ в ʺзамещенной или незамещенной 4-10-членной моноциклической или полициклической ненасыщенной гетероциклической группе, содержащей 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ, представленной как R3, включают группы, указанные выше;
предпочтительно галоген, C1-C6 алкил, который может быть замещен гидрокси, или амино, который может быть замещен группой C1-C6 алкил(карбонил);
более предпочтительно галоген, C1-C4 алкил, который может быть замещен гидрокси, или амино, который может быть замещен группой C1-C4 алкил(карбонил); и
еще более предпочтительно фтор, метил, который может быть замещен гидрокси, или ацетиламино.
[0237]
Количество заместителей конкретно не ограничивается, но предпочтительно составляет 0 или 1, и более предпочтительно 1.
[0238]
ʺЗамещенная или незамещенная 4-10-членная моноциклическая или полициклическая ненасыщенная гетероциклическая группа, содержащая 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ, представленная как R3, предпочтительно представляет собой 4-6-членную моноциклическую ненасыщенную гетероциклическую группу, которая может быть замещена ʺгалогеном, C1-C6 алкилом, который может быть замещен гидрокси, или амино, который может быть замещен группой C1-C6 алкил(карбонил)ʺ, и содержит 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы;
более предпочтительно 4-6-членную моноциклическую ненасыщенную гетероциклическую группу, которая может быть замещена ʺгалогеном, C1-C4 алкилом, который может быть замещен гидрокси, или амино, который может быть замещен группой C1-C4 алкил(карбонил)ʺ, и содержит 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы;
еще более предпочтительно 4-6-членную моноциклическую ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы;
еще более предпочтительно 4-6-членную моноциклическую ненасыщенную гетероциклическую группу, содержащую один ли два атома азота; и
еще более предпочтительно пиразолил.
[0239]
R3 предпочтительно представляет собой
водород,
галоген,
циано,
замещенный или незамещенный C1-C6 алкил,
замещенный или незамещенный C1-C6 алкокси,
замещенный или незамещенный C1-C6 алкилтио,
замещенный или незамещенный C3-C7 циклоалкил,
замещенный или незамещенный C2-C6 алкенил,
замещенный или незамещенный C2-C6 алкинил, при условии, что положение тройной связи C2-C6 алкинила находится между атомом углерода, связанным с 7H-пирроло[2,3-d]пиримидиновым скелетом, и атомом углерода, смежным с этим атомом углерода,
замещенный или незамещенный C6-C14 ароматический углеводород или
замещенную или незамещенную 4-10-членную моноциклическую ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы.
R3 более предпочтительно представляет собой
водород,
галоген,
циано,
C1-C6 алкил, который может быть замещен гидрокси или оксо группой,
C1-C6 алкокси, который может быть замещен
ʺгалогеном,
C1-C6 алкокси,
C3-C7 циклоалкилом или
одной или несколькими 4-10-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены оксо и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ,
C1-C6 алкилтио,
C3-C7 циклоалкил,
C2-C6 алкенил, который может быть замещен ʺгидроксиʺ,
C2-C6 алкинил, который может быть замещен
ʺгидрокси,
C1-C6 алкокси,
амино, который может быть замещен группой R4, где R4 представляет собой C1-C6 алкил, C1-C4 алкокси C1-C6 алкил или карбамоил, который может быть замещен C3-C7 циклоалкилом,
C1-C6 алкилсилилокси,
C3-C7 циклоалкилом, который может быть замещен ʺгидрокси или оксоʺ,
C6-C14 ароматическим углеводородом, который может быть замещен группой R5, где R5 представляет собой галоген, C1-C4 алкиламино, который может быть замещен одной или несколькими 4-10-членными моноциклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или C1-C6 алкокси,
одной или несколькими 4-10-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены группой R6 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R6 представляет собой гидрокси, C1-C6 алкил, C1-C6 алкокси или оксо,
одной или несколькими 4-10-членными моноциклическими или полициклическими ненасыщенными гетероциклическими группами, которые могут быть замещены группой R7 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R7 представляет собой галоген, циано, C1-C6 алкил, C1-C6 алкокси или амино, или
ненасыщенным гетероциклическим окси, который может быть замещен галогеном, где ненасыщенное гетероциклическое кольцо представляет собой 4-10-членное моноциклическое или полициклическое ненасыщенное гетероциклическое кольцо, содержащее 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ,
при условии, что положение тройной связи C2-C6 алкинила находится между атомом углерода, связанным с 7H-пирроло[2,3-d]пиримидиновым скелетом, и атомом углерода, смежным с этим атомом углерода,
C6-C14 ароматический углеводород, который может быть замещен
ʺгидрокси,
C1-C6 алкилом, который может быть замещен гидрокси,
формилом или
одной или несколькими 4-10-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены C1-C6 алкилом и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ, или
4-6-членную моноциклическую ненасыщенную гетероциклическую группу, которая может быть замещена
ʺгалогеном,
C1-C6 алкилом, который может быть замещен гидрокси, или
амино, который может быть замещен группой C1-C6 алкил(карбонил)ʺ,
и содержит 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы.
R3 еще более предпочтительно представляет собой
водород,
галоген,
циано,
C1-C4 алкил, который может быть замещен гидрокси или оксо группой,
C1-C6 алкокси, который может быть замещен
ʺгалогеном,
C1-C6 алкокси,
C3-C7 циклоалкилом или
одной или несколькими 4-10-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены оксо и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы,
C1-C4 алкилтио,
C3-C5 циклоалкил,
C2-C6 алкенил, который может быть замещен ʺгидроксиʺ,
C2-C6 алкинил, который может быть замещен
ʺгидрокси,
C1-C6 алкокси,
амино, который может быть замещен группой R4, где R4 представляет собой C1-C6 алкил, C1-C4 алкокси C1-C6 алкил или карбамоил, который может быть замещен C3-C7 циклоалкилом,
C1-C6 алкилсилилокси,
C3-C7 циклоалкилом, который может быть замещен ʺгидрокси или оксоʺ,
C6-C14 ароматическим углеводородом, который может быть замещен группой R5, где R5 представляет собой галоген, C1-C4 алкиламино, который может быть замещен одной или несколькими 4-10-членными моноциклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или C1-C6 алкокси,
одной или несколькими 4-10-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены группой R6 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R6 представляет собой гидрокси, C1-C6 алкил, C1-C6 алкокси, или оксо,
одной или несколькими 4-10-членными моноциклическими или полициклическими ненасыщенными гетероциклическими группами, которые могут быть замещены группой R7 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R7 представляет собой галоген, циано, C1-C6 алкил, C1-C6 алкокси или амино, или
ненасыщенным гетероциклическим окси, который может быть замещен галогеном, где ненасыщенное гетероциклическое кольцо представляет собой 4-10-членное моноциклическое или полициклическое ненасыщенное гетероциклическое кольцо, содержащее 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ,
при условии, что положение тройной связи C2-C6 алкинила находится между атомом углерода, связанным с 7H-пирроло[2,3-d]пиримидиновым скелетом, и атомом углерода, смежным с этим атомом углерода,
C6-C14 ароматический углеводород, который может быть замещен
ʺгидрокси,
C1-C6 алкилом, который может быть замещен гидрокси,
формилом или
одной или несколькими 4-10-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены C1-C6 алкилом и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ, или
4-6-членную моноциклическую ненасыщенную гетероциклическую группу, которая может быть замещена
ʺгалогеном,
C1-C6 алкилом, который может быть замещен гидрокси, или
амино, который может быть замещен группой C1-C6 алкил(карбонил)ʺ,
и содержит 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы.
R3 еще более предпочтительно представляет собой
водород,
галоген,
циано,
C1-C4 алкил,
C1-C6 алкокси, который может быть замещен
ʺгалогеном,
C1-C6 алкокси,
C3-C7 циклоалкилом или
одной или несколькими 4-10-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены оксо и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ,
C1-C4 алкилтио,
C3-C5 циклоалкил,
C2-C4 алкенил, который может быть замещен ʺгидрокси,ʺ
C2-C6 алкинил, который может быть замещен
ʺгидрокси,
C1-C4 алкокси,
амино, который может быть замещен группой R4, где R4 представляет собой C1-C4 алкил, C1-C4 алкокси C1-C4 алкил или карбамоил, который может быть замещен C3-C5 циклоалкилом,
три-C1-C6 алкилсилилокси,
C3-C7 циклоалкилом, который может быть замещен ʺгидрокси или оксоʺ,
фенилом, который может быть замещен группой R5, где R5 представляет собой галоген, метиламино, который может быть замещен одной или несколькими 4-6-членными моноциклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или C1-C4 алкокси,
одной или несколькими 4-6-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены группой R6 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R6 представляет собой гидрокси, C1-C4 алкил, C1-C4 алкокси или оксо,
одной или несколькими 4-10-членными моноциклическими или бициклическими ненасыщенными гетероциклическими группами, которые могут быть замещены группой R7 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R7 представляет собой галоген, циано, C1-C4 алкил, C1-C4 алкокси или амино, или
ненасыщенным гетероциклическим окси, который может быть замещен галогеном, где ненасыщенное гетероциклическое кольцо представляет собой 4-6-членное моноциклическое ненасыщенное гетероциклическое кольцо, содержащее 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ,
при условии, что положение тройной связи C2-C6 алкинила находится между атомом углерода, связанным с 7H-пирроло[2,3-d]пиримидиновым скелетом, и атомом углерода, смежным с этим атомом углерода,
фенил, который может быть замещен
ʺгидрокси,
C1-C4 алкилом, который может быть замещен гидрокси,
формилом или
одной или несколькими 4-6-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены C1-C4 алкилом и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ, или
4-6-членную моноциклическую ненасыщенную гетероциклическую группу, которая может быть замещена
ʺгалогеном,
C1-C4 алкилом, который может быть замещен гидрокси, или
амино, который может быть замещен группой C1-C4 алкил(карбонил)ʺ,
и содержит 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы.
R3 еще более предпочтительно представляет собой
водород,
галоген,
C1-C4 алкил,
C1-C4 алкокси, который может быть замещен
ʺгалогеном,
C1-C4 алкокси,
C3-C7 циклоалкилом или
одной или несколькими 4-6-членными моноциклическими насыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы,ʺ
C1-C4 алкилтио,
C2-C4 алкенил,
C2-C6 алкинил, который может быть замещен
ʺгидрокси,
C1-C4 алкокси,
амино, который может быть замещен группой R4, где R4 представляет собой C1-C4 алкил, C1-C4 алкокси C1-C4 алкил или карбамоил, который может быть замещен C3-C5 циклоалкилом,
три-C1-C6 алкилсилилокси,
C3-C7 циклоалкилом, который может быть замещен ʺгидрокси или оксоʺ,
фенилом, который может быть замещен группой R5, где R5 представляет собой галоген,
ʺодной или несколькими 4-6-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены группой R6 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ, где R6 представляет собой гидрокси, C1-C4 алкил, C1-C4 алкокси или оксо,
ʺодной или несколькими 4-10-членными моноциклическими или бициклическими ненасыщенными гетероциклическими группами, которые могут быть замещены группой R7 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ, где R7 представляет собой галоген, циано, C1-C4 алкил, C1-C4 алкокси, или амино, или
ненасыщенным гетероциклическим окси, который может быть замещен галогеном, где ненасыщенное гетероциклическое кольцо представляет собой 4-6-членное моноциклическое ненасыщенное гетероциклическое кольцо, содержащее 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ,
при условии, что положение тройной связи C2-C6 алкинила находится между атомом углерода, связанным с 7H-пирроло[2,3-d]пиримидиновым скелетом, и атомом углерода, смежным с этим атомом углерода,
фенил, который может быть замещен
ʺгидрокси,
C1-C4 алкилом, который может быть замещен гидрокси, или
формиломʺ, или
4-6-членную моноциклическую ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы.
R3 еще более предпочтительно представляет собой
водород,
галоген,
C1-C4 алкокси, который может быть замещен
ʺC1-C4 алкокси,
C3-C7 циклоалкилом или
одной или несколькими 4-6-членными моноциклическими насыщенными гетероциклическими группами, содержащими один атом кислородаʺ,
C1-C4 алкилтио,
C2-C4 алкенил,
C2-C6 алкинил, который может быть замещен
ʺгидрокси,
амино, который может быть замещен группой R4, где R4 представляет собой C1-C4 алкил или C1-C4 алкокси C1-C4 алкил,
C3-C7 циклоалкилом, который может быть замещен ʺгидрокси или оксоʺ,
фенилом, который может быть замещен группой R5, где R5 представляет собой галоген,
ʺодной или несколькими 4-6-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены группой R6 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ, где R6 представляет собой гидрокси, C1-C4 алкил или оксо, или
одной или несколькими 4-10-членными моноциклическими или бициклическими ненасыщенными гетероциклическими группами, которые могут быть замещены группой R7 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R7 представляет собой галоген, циано, C1-C4 алкил, C1-C4 алкокси или аминоʺ,
при условии, что положение тройной связи C2-C6 алкинила находится между атомом углерода, связанным с 7H-пирроло[2,3-d]пиримидиновым скелетом, и атомом углерода, смежным с этим атомом углерода,
фенил, который может быть замещен
ʺгидрокси или
C1-C4 алкилом, который может быть замещен гидроксиʺ, или
4-6-членную моноциклическую ненасыщенную гетероциклическую группу, содержащую 1 или 2 атома азота.
R3 еще более предпочтительно представляет собой
C1-C4 алкокси, который может быть замещен ʺодной или несколькими 4-6-членными моноциклическими насыщенными гетероциклическими группами, содержащими один атом кислородаʺ, или
C2-C6 алкинил, который может быть замещен
ʺгидрокси,
амино, который может быть замещен группой R4, где R4 представляет собой метил или метоксиэтил,
C3-C7 циклоалкилом, который может быть замещен гидрокси,
ʺодной или несколькими 4-6-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены группой R6 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ, где R6 представляет собой гидрокси или метил, или
одной или несколькими 4-10-членными моноциклическими или бициклическими ненасыщенными гетероциклическими группами, которые могут быть замещены группой R7 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R7 представляет собой C1-C4 алкил или аминоʺ,
при условии, что положение тройной связи C2-C6 алкинила находится между атомом углерода, связанным с 7H-пирроло[2,3-d]пиримидиновым скелетом, и атомом углерода, смежным с этим атомом углерода.
[0240]
X предпочтительно представляет собой CR3, когда A представляет собой A1, и X предпочтительно представляет собой N, когда A представляет собой A2.
Y предпочтительно представляет собой CH, когда A представляет собой A1 или A2.
[0241]
Когда A представляет собой A1, n предпочтительно имеет значение 1 или 2, и более предпочтительно 1. Когда A представляет собой A2, n предпочтительно имеет значение 0 или 1, и более предпочтительно 1.
[0242]
m представляет собой целое число, имеющее значение 0 или 1, и предпочтительно 0.
[0243]
l представляет собой целое число, имеющее значение 1-3, и предпочтительно 2.
[0244]
Когда A представляет собой A1 и n имеет значение 2, положения связывания R1 предпочтительно включают одно пара-положение и одно орто- или мета-положение, и более предпочтительно одно мета-положение и одно пара-положение. Когда A представляет собой A1 и n имеет значение 1, положение связывания R1 предпочтительно представляет собой пара- или мета-положение, и наиболее предпочтительно пара-положение. В настоящем описании, если не указано иное, положение связывания (орто-, мета- или пара-положение) R1 относится к положению атома углерода, связанного с карбамоильной группой в формулах (I) и (I'), из атомов углерода, содержащихся в A1 (более определенно, атома углерода, указанного стрелкой:
[0245]
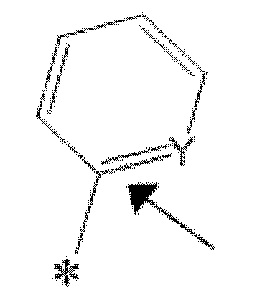
[0246]
[0247]
Даже когда A представляет собой
[0248]
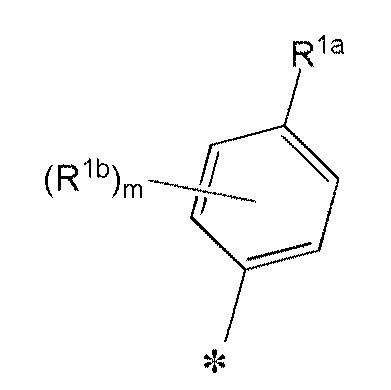
[0249]
и m имеет значение 1, положение связывания R1b предпочтительно представляет собой мета положение.
[0250]
A1 предпочтительно представляет собой
[1]
[0251]

[0252]
где R1 представляет собой
галоген,
циано,
нитро,
замещенный или незамещенный C1-C6 алкил,
замещенный или незамещенный C1-C6 алкокси,
замещенный или незамещенный C2-C6 алкенил,
замещенный или незамещенный C2-C6 алкинил,
замещенный или незамещенный амино или
замещенную или незамещенную 4-10-членную моноциклическую или полициклическую ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы;
Y представляет собой N или CH; и
n представляет собой целое число, имеющее значение 1 или 2.
A1 более предпочтительно представляет собой
[0253]

[0254]
где R1 представляет собой
галоген,
циано,
нитро,
C1-C6 алкил, который может быть замещен ʺгидрокси, C1-C6 алкокси, где водород, содержащийся в алкокси, может быть замещен 1 или несколькими атомами дейтерия, C1-C6 алкилтио или C6-C14 ароматическим углеводородомʺ,
C1-C6 алкокси, который может быть замещен галогеном,
C2-C6 алкенил,
C2-C6 алкинил,
амино, который может быть замещен ʺодной или несколькими 4-10-членными моноциклическими или полициклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или C6-C14 ароматическим углеводородомʺ, или
4-10-членную моноциклическую или полициклическую ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы;
Y представляет собой N или CH; и
n представляет собой целое число, имеющее значение 1 или 2.
[2]
A1 еще более предпочтительно представляет собой
[0255]

[0256]
где R1a представляет собой
C1-C6 алкил, который может быть замещен ʺC1-C6 алкокси, где водород, содержащийся в алкокси, может быть замещен 1 или несколькими атомами дейтерия, или C1-C6 алкилтиоʺ,
C2-C6 алкенил,
C2-C6 алкинил,
амино, который может быть замещен ʺодной или несколькими 4-10-членными моноциклическими или полициклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или C6-C14 ароматическим углеводородомʺ, или
4-10-членную моноциклическую или полициклическую ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы;
R1b представляет собой галоген, C1-C6 алкил или C1-C6 алкокси; и
m представляет собой целое число, имеющее значение 0 или 1.
[3]
A1 еще более предпочтительно представляет собой
[0257]

[0258]
где R1a представляет собой
C1-C6 алкил, который может быть замещен ʺC1-C6 алкокси, где водород, содержащийся в алкокси, может быть замещен 1 или несколькими атомами дейтерия, или C1-C6 алкилтиоʺ,
C2-C6 алкенил,
C2-C6 алкинил,
амино, который может быть замещен ʺодной или несколькими 4-6-членными моноциклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или C6-C10 ароматическим углеводородомʺ, или
4-6-членную моноциклическую ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы;
R1b представляет собой галоген, C1-C6 алкил или C1-C6 алкокси; и
m представляет собой целое число, имеющее значение 0 или 1.
[4]
A1 еще более предпочтительно представляет собой
[0259]

[0260]
где R1a представляет собой
C1-C6 алкил, который замещен ʺC1-C6 алкокси, где водород, содержащийся в алкокси, может быть замещен 1 или несколькими атомами дейтерия, или C1-C6 алкилтиоʺ,
C2-C6 алкенил,
C2-C6 алкинил или
4-6-членную моноциклическую ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы;
R1b представляет собой галоген; и
m представляет собой целое число, имеющее значение 0 или 1.
[5]
A1 еще более предпочтительно представляет собой
[0261]
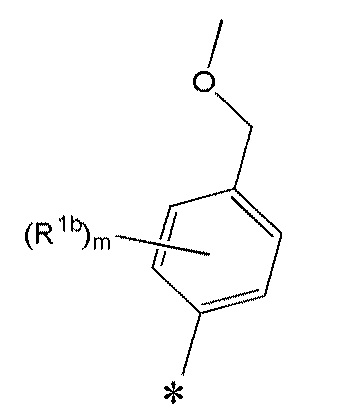
[0262]
где R1b представляет собой галоген; и
m представляет собой целое число, имеющее значение 0 или 1.
[6]
A1 еще более предпочтительно представляет собой
[0263]

[0264]
[0265]
Когда A представляет собой A2, и следующая часть:
[0266]

[0267]
где группа B и Y имеют значение, определенное выше;
представляет собой полициклический C8-C14 ароматический углеводород, примеры полициклического C8-C14 ароматического углеводорода включают группы, указанные выше; предпочтительно бициклический C8-C10 ароматический углеводород; более предпочтительно
[0268]
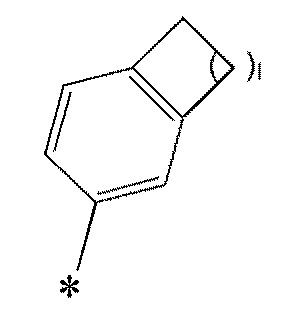
[0269]
где l имеет значение, определенное выше;
и еще более предпочтительно
[0270]

[0271]
[0272]
Когда A представляет собой A2, и следующая часть:
[0273]
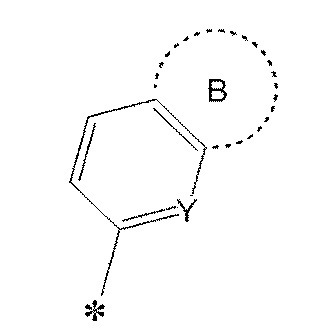
[0274]
где группа B и Y имеют значение, определенное выше;
представляет собой 8-14-членную полициклическую ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, примеры 8-14-членной полициклической ненасыщенной гетероциклической группы, содержащей 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, включают группы, указанные выше; предпочтительно 8-10-членную бициклическую ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы; более предпочтительно an 8-10-членную бициклическую ненасыщенную гетероциклическую группу, содержащую один гетероатом, выбранный из азота, кислорода и серы; и еще более предпочтительно
[0275]

[0276]
[0277]
A2 предпочтительно представляет собой
[0278]

[0279]
где R1 представляет собой замещенный или незамещенный C1-C6 алкокси;
Y представляет собой CH; и
n представляет собой целое число, имеющее значение 0 или 1.
A2 более предпочтительно представляет собой
[0280]

[0281]
где R1c представляет собой C1-C6 алкокси; l представляет собой целое число, имеющее значение 1-3; и n представляет собой целое число, имеющее значение 0 или 1; или
8-10-членную бициклическую ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы.
A2 еще более предпочтительно представляет собой
[0282]

[0283]
A2 еще более предпочтительно представляет собой
[0284]
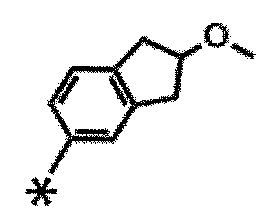
[0285]
[0286]
A более предпочтительно представляет собой A1, а не A2.
[0287]
Предпочтительные варианты осуществления настоящего изобретения описаны ниже в [1] - [6].
[1] Более предпочтительным является соединение, представленное формулой (I), или его соль, где
когда A представляет собой A1,
R1 представляет собой
галоген,
циано,
нитро,
замещенный или незамещенный C1-C6 алкил,
замещенный или незамещенный C1-C6 алкокси,
замещенный или незамещенный C2-C6 алкенил,
замещенный или незамещенный C2-C6 алкинил,
замещенный или незамещенный амино или
замещенную или незамещенную 4-10-членную моноциклическую или полициклическую ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы;
Y представляет собой N или CH;
n представляет собой целое число, имеющее значение 1 или 2;
R2 представляет собой
замещенный или незамещенный C3-C10 алкил,
замещенный или незамещенный C3-C7 циклоалкил,
замещенный или незамещенный C4-C12 связанный мостиковой связью циклоалкил,
замещенный или незамещенный C2-C6 алкенил или
замещенный или незамещенный C3-C7 циклоалкенил,
при условии, что, когда каждая группа, представленная как R2, содержит заместитель, этот заместитель не должен представлять собой замещенную или незамещенную насыщенную гетероциклическую группу, которая может содержать по меньшей мере один одинаковый или разный гетероатом, выбранный из кислорода и серы, и содержит по меньшей мере один атом азота; и
X представляет собой
N или
CR3, где R3 представляет собой
водород,
галоген,
циано,
замещенный или незамещенный C1-C6 алкил,
замещенный или незамещенный C1-C6 алкокси,
замещенный или незамещенный C1-C6 алкилтио,
замещенный или незамещенный C3-C7 циклоалкил,
замещенный или незамещенный C2-C6 алкенил,
замещенный или незамещенный C2-C6 алкинил, при условии, что положение тройной связи C2-C6 алкинила находится между атомом углерода, связанным с 7H-пирроло[2,3-d]пиримидиновым скелетом, и атомом углерода, смежным с этим атомом углерода,
замещенный или незамещенный C6-C14 ароматический углеводород или
замещенную или незамещенную 4-10-членную моноциклическую ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы; и
когда A представляет собой A2,
R1 представляет собой замещенный или незамещенный C1-C6 алкокси;
Y представляет собой CH;
n представляет собой целое число, имеющее значение 0 или 1;
R2 представляет собой замещенный или незамещенный C3-C7 циклоалкил; и
X представляет собой N.
[0288]
[1-2] Более предпочтительным является соединение, представленное формулой (I), или его соль, где
когда A представляет собой A1,
R1 представляет собой
галоген,
циано,
нитро,
C1-C6 алкил, который может быть замещен ʺгидрокси, C1-C6 алкокси, где водород, содержащийся в алкокси, может быть замещен 1 или несколькими атомами дейтерия, C1-C6алкилтио или C6-C14 ароматическим углеводородомʺ,
C1-C6 алкокси, который может быть замещен галогеном,
C2-C6 алкенил,
C2-C6 алкинил,
амино, который может быть замещен ʺодной или несколькими 4-10-членными моноциклическими или полициклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или C6-C14 ароматическим углеводородомʺ, или
4-10-членную моноциклическую или полициклическую ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы;
Y представляет собой N или CH;
n представляет собой целое число, имеющее значение 1 или 2;
R2 представляет собой
C3-C10 алкил, который может быть замещен ʺгалогеном, C1-C6 алкокси, C3-C7 циклоалкилом или одной или несколькими 4-10-членными моноциклическими или полициклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ,
C3-C7 циклоалкил, который может быть замещен ʺгалогеном, C1-C6 алкилом, C3-C7 циклоалкилом или галогенo C1-C6 алкиломʺ,
C4-C12 связанный мостиковой связью циклоалкил,
C2-C6 алкенил, который может быть замещен галогеном, или
C3-C7 циклоалкенил; и
X представляет собой
N или
CR3, где R3 представляет собой
водород,
галоген,
циано,
C1-C6 алкил, который может быть замещен гидрокси или оксо группой,
C1-C6 алкокси, который может быть замещен
ʺгалогеном,
C1-C6 алкокси,
C3-C7 циклоалкилом или
одной или несколькими 4-10-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены оксо и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ,
C1-C6 алкилтио,
C3-C7 циклоалкил,
C2-C6 алкенил, который может быть замещен ʺгидрокси,ʺ
C2-C6 алкинил, который может быть замещен
ʺгидрокси,
C1-C6 алкокси,
амино, который может быть замещен группой R4, где R4 представляет собой C1-C6 алкил, C1-C4 алкокси C1-C6 алкил или карбамоил, который может быть замещен C3-C7 циклоалкилом,
C1-C6 алкилсилилокси,
C3-C7 циклоалкилом, который может быть замещен ʺгидрокси или оксоʺ,
C6-C14 ароматическим углеводородом, который может быть замещен группой R5, где R5 представляет собой галоген, C1-C4 алкиламино, который может быть замещен одной или несколькими 4-10-членными моноциклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или C1-C6 алкокси,
одной или несколькими 4-10-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены группой R6 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R6 представляет собой гидрокси, C1-C6 алкил, C1-C6 алкокси или оксо,
одной или несколькими 4-10-членными моноциклическими или полициклическими ненасыщенными гетероциклическими группами, которые могут быть замещены группой R7 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R7 представляет собой галоген, циано, C1-C6 алкил, C1-C6 алкокси или амино, или
ненасыщенным гетероциклическим окси, который может быть замещен галогеном, где ненасыщенное гетероциклическое кольцо представляет собой 4-10-членное моноциклическое или полициклическое ненасыщенное гетероциклическое кольцо, содержащее 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ,
при условии, что положение тройной связи C2-C6 алкинила находится между атомом углерода, связанным с 7H-пирроло[2,3-d]пиримидиновым скелетом, и атомом углерода, смежным с этим атомом углерода,
C6-C14 ароматический углеводород, который может быть замещен
ʺгидрокси,
C1-C6 алкилом, который может быть замещен гидрокси,
формилом или
одной или несколькими 4-10-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены C1-C6 алкилом и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ, или
4-6-членную моноциклическую ненасыщенную гетероциклическую группу, которая может быть замещена
ʺгалогеном,
C1-C6 алкилом, который может быть замещен гидрокси, или
амино, который может быть замещен группой C1-C6 алкил(карбонил)ʺ,
и содержит 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы; и
когда A представляет собой A2,
R1 представляет собой замещенный или незамещенный C1-C6 алкокси;
Y представляет собой CH;
n представляет собой целое число, имеющее значение 0 или 1;
R2 представляет собой замещенный или незамещенный C3-C7 циклоалкил; и
X представляет собой N.
[0289]
[2] Более предпочтительным является соединение, представленное формулой (I), или его соль, где
когда A представляет собой A1,
A1 представляет собой
[0290]

[0291]
где R1a представляет собой
C1-C6 алкил, который может быть замещен ʺC1-C6 алкокси, где водород, содержащийся в алкокси, может быть замещен 1 или несколькими атомами дейтерия, или C1-C6 алкилтиоʺ,
C2-C6 алкенил,
C2-C6 алкинил,
амино, который может быть замещен ʺодной или несколькими 4-10-членными моноциклическими или полициклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или C6-C14 ароматическим углеводородомʺ, или
4-10-членную моноциклическую или полициклическую ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы;
R1b представляет собой галоген, C1-C6 алкил или C1-C6 алкокси;
m представляет собой целое число, имеющее значение 0 или 1;
R2 представляет собой
C3-C10 алкил, который может быть замещен ʺгалогеном, C3-C7 циклоалкилом или одной или несколькими 4-10-членными моноциклическими или полициклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ,
C3-C7 циклоалкил, который может быть замещен ʺC1-C6 алкилом, C3-C7 циклоалкилом или галогенo C1-C6 алкиломʺ,
C4-C12 связанный мостиковой связью циклоалкил или
C3-C7 циклоалкенил; и
X представляет собой
N или
CR3, где R3 представляет собой
водород,
галоген,
циано,
C1-C4 алкил, который может быть замещен гидрокси или оксо группой,
C1-C6 алкокси, который может быть замещен
ʺгалогеном,
C1-C6 алкокси,
C3-C7 циклоалкилом или
одной или несколькими 4-10-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены оксо и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ,
C1-C4 алкилтио,
C3-C5 циклоалкил,
C2-C6 алкенил, который может быть замещен ʺгидроксиʺ,
C2-C6 алкинил, который может быть замещен
ʺгидрокси,
C1-C6 алкокси,
амино, который может быть замещен группой R4, где R4 представляет собой C1-C6 алкил, C1-C4 алкокси C1-C6 алкил или карбамоил, который может быть замещен C3-C7 циклоалкилом,
C1-C6 алкилсилилокси,
C3-C7 циклоалкилом, который может быть замещен ʺгидрокси или оксоʺ,
C6-C14 ароматическим углеводородом, который может быть замещен группой R5, где R5 представляет собой галоген, C1-C4 алкиламино, который может быть замещен одной или несколькими 4-10-членными моноциклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или C1-C6 алкокси,
одной или несколькими 4-10-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены группой R6 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R6 представляет собой гидрокси, C1-C6 алкил, C1-C6 алкокси или оксо,
одной или несколькими 4-10-членными моноциклическими или полициклическими ненасыщенными гетероциклическими группами, которые могут быть замещены группой R7 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R7 представляет собой галоген, циано, C1-C6 алкил, C1-C6 алкокси или амино, или
ненасыщенным гетероциклическим окси, который может быть замещен галогеном, где ненасыщенное гетероциклическое кольцо представляет собой 4-10-членное моноциклическое или полициклическое ненасыщенное гетероциклическое кольцо, содержащее 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ,
при условии, что положение тройной связи C2-C6 алкинила находится между атомом углерода, связанным с 7H-пирроло[2,3-d]пиримидиновым скелетом, и атомом углерода, смежным с этим атомом углерода,
C6-C14 ароматический углеводород, который может быть замещен
ʺгидрокси,
C1-C6 алкилом, который может быть замещен гидрокси,
формилом или
одной или несколькими 4-10-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены C1-C6 алкилом и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или
4-6-членную моноциклическую ненасыщенную гетероциклическую группу, которая может быть замещена
ʺгалогеном,
C1-C6 алкилом, который может быть замещен гидрокси, или
амино, который может быть замещен группой C1-C6 алкил(карбонил)ʺ,
и содержит 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы; и
когда A представляет собой A2,
A2 представляет собой
[0292]

[0293]
где R1c представляет собой C1-C6 алкокси; l представляет собой целое число, имеющее значение 1-3; и n представляет собой целое число, имеющее значение 0 или 1;
R2 представляет собой C3-C7 циклоалкил; и
X представляет собой N.
[0294]
[3] Еще более предпочтительным является соединение, представленное формулой (I), или его соль, где
A представляет собой
[0295]
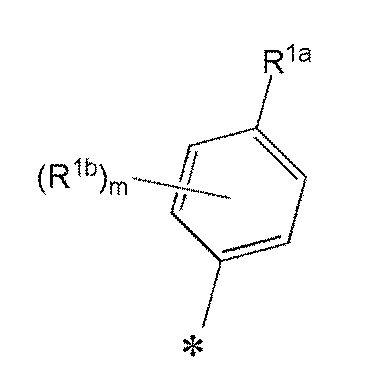
[0296]
где R1a представляет собой
C1-C6 алкил, который может быть замещен ʺC1-C6 алкокси, где водород, содержащийся в алкокси, может быть замещен 1 или несколькими атомами дейтерия, или C1-C6 алкилтиоʺ,
C2-C6 алкенил,
C2-C6 алкинил,
амино, который может быть замещен ʺодной или несколькими 4-6-членными моноциклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или C6-C10 ароматическим углеводородомʺ, или
4-6-членную моноциклическую ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы;
R1b представляет собой галоген, C1-C6 алкил или C1-C6 алкокси;
m представляет собой целое число, имеющее значение 0 или 1;
R2 представляет собой
C3-C10 алкил, который может быть замещен ʺгалогеном, C3-C7 циклоалкилом или одной или несколькими 4-10-членными моноциклическими или полициклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ,
C3-C7 циклоалкил, который может быть замещен ʺC1-C6 алкилом, C3-C7 циклоалкилом или галогенo C1-C6 алкиломʺ, или
C4-C12 связанный мостиковой связью циклоалкил; и
X представляет собой
N или
CR3, где R3 представляет собой
водород,
галоген,
циано,
C1-C4 алкил,
C1-C6 алкокси, который может быть замещен
ʺгалогеном,
C1-C6 алкокси,
C3-C7 циклоалкилом или
одной или несколькими 4-10-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены оксо и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ,
C1-C4 алкилтио,
C3-C5 циклоалкил,
C2-C4 алкенил, который может быть замещен ʺгидроксиʺ,
C2-C6 алкинил, который может быть замещен
ʺгидрокси,
C1-C4 алкокси,
амино, который может быть замещен группой R4, где R4 представляет собой C1-C4 алкил, C1-C4 алкокси C1-C4 алкил, или карбамоил, который может быть замещен C3-C5 циклоалкилом,
три-C1-C6 алкилсилилокси,
C3-C7 циклоалкилом, который может быть замещен ʺгидрокси или оксоʺ,
фенилом, который может быть замещен группой R5, где R5 представляет собой галоген, метиламино, который может быть замещен одной или несколькими 4-6-членными моноциклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или C1-C4 алкокси,
одной или несколькими 4-6-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены группой R6 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R6 представляет собой гидрокси, C1-C4 алкил, C1-C4 алкокси или оксо,
одной или несколькими 4-10-членными моноциклическими или бициклическими ненасыщенными гетероциклическими группами, которые могут быть замещены группой R7 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R7 представляет собой галоген, циано, C1-C4 алкил, C1-C4 алкокси или амино, или
ненасыщенным гетероциклическим окси, который может быть замещен галогеном, где ненасыщенное гетероциклическое кольцо представляет собой 4-6-членное моноциклическое ненасыщенное гетероциклическое кольцо, содержащее 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ,
при условии, что положение тройной связи C2-C6 алкинила находится между атомом углерода, связанным с 7H-пирроло[2,3-d]пиримидиновым скелетом, и атомом углерода, смежным с этим атомом углерода,
фенил, который может быть замещен
ʺгидрокси,
C1-C4 алкилом, который может быть замещен гидрокси,
формилом или
одной или несколькими 4-6-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены C1-C4 алкилом и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ, или
4-6-членную моноциклическую ненасыщенную гетероциклическую группу, которая может быть замещена
ʺгалогеном,
C1-C4 алкилом, который может быть замещен гидрокси, или
амино, который может быть замещен группой C1-C4 алкил(карбонил)ʺ,
и содержит 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы.
[0297]
[4] Еще более предпочтительным является соединение, представленное формулой (I), или его соль, где
A представляет собой
[0298]

[0299]
где R1a представляет собой
C1-C6 алкил, который замещен ʺC1-C6 алкокси, где водород, содержащийся в алкокси, может быть замещен 1 или несколькими атомами дейтерия, или C1-C6 алкилтиоʺ,
C2-C6 алкенил,
C2-C6 алкинил или
4-6-членную моноциклическую ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы;
R1b представляет собой галоген;
m представляет собой целое число, имеющее значение 0 или 1;
R2 представляет собой
разветвленный C3-C8 алкил, который может быть замещен ʺгалогеном или C3-C7 циклоалкиломʺ
C3-C7 циклоалкил, который может быть замещен ʺC1-C4 алкилом или C3-C5 циклоалкиломʺ, или
C4-C12 связанный мостиковой связью циклоалкил; и
X представляет собой
N или
CR3, где R3 представляет собой
водород,
галоген,
C1-C4 алкил,
C1-C4 алкокси, который может быть замещен
ʺгалогеном,
C1-C4 алкокси,
C3-C7 циклоалкилом или
одной или несколькими 4-6-членными моноциклическими насыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ,
C1-C4 алкилтио,
C2-C4 алкенил,
C2-C6 алкинил, который может быть замещен
ʺгидрокси,
C1-C4 алкокси,
амино, который может быть замещен группой R4, где R4 представляет собой C1-C4 алкил, C1-C4 алкокси C1-C4 алкил или карбамоил, который может быть замещен C3-C5 циклоалкилом,
три-C1-C6 алкилсилилокси,
C3-C7 циклоалкилом, который может быть замещен ʺгидрокси или оксоʺ,
фенилом, который может быть замещен группой R5, где R5 представляет собой галоген,
ʺодной или несколькими 4-6-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены группой R6 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ, где R6 представляет собой гидрокси, C1-C4 алкил, C1-C4 алкокси или оксо,
ʺодной или несколькими 4-10-членными моноциклическими или бициклическими ненасыщенными гетероциклическими группами, которые могут быть замещены группой R7 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ, где R7 представляет собой галоген, циано, C1-C4 алкил, C1-C4 алкокси или амино, или
ненасыщенным гетероциклическим окси, который может быть замещен галогеном, где ненасыщенное гетероциклическое кольцо представляет собой 4-6-членное моноциклическое ненасыщенное гетероциклическое кольцо, содержащее 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ,
при условии, что положение тройной связи C2-C6 алкинила находится между атомом углерода, связанным с 7H-пирроло[2,3-d]пиримидиновым скелетом, и атомом углерода, смежным с этим атомом углерода,
фенил, который может быть замещен
ʺгидрокси,
C1-C4 алкилом, который может быть замещен гидрокси, или
формиломʺ, или
4-6-членную моноциклическую ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы.
[0300]
[5] Еще более предпочтительным является соединение, представленное формулой (I), или его соль, где
A представляет собой
[0301]

[0302]
где R1b представляет собой галоген;
m представляет собой целое число, имеющее значение 0 или 1;
R2 представляет собой
разветвленный C3-C6 алкил, который может быть замещен галогеном, или
C3-C7 циклоалкил, который может быть замещен ʺC1-C4 алкилом или C3-C5 циклоалкиломʺ;
X представляет собой CR3, где R3 представляет собой
водород,
галоген,
C1-C4 алкокси, который может быть замещен
ʺC1-C4 алкокси,
C3-C7 циклоалкилом или
одной или несколькими 4-6-членными моноциклическими насыщенными гетероциклическими группами, содержащими один атом кислородаʺ,
C1-C4 алкилтио,
C2-C4 алкенил,
C2-C6 алкинил, который может быть замещен
ʺгидрокси,
амино, который может быть замещен группой R4, где R4 представляет собой C1-C4 алкил или C1-C4 алкокси C1-C4 алкил,
C3-C7 циклоалкилом, который может быть замещен гидрокси,
фенилом, который может быть замещен группой R5, где R5 представляет собой галоген,
ʺодной или несколькими 4-6-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены группой R6 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ, где R6 представляет собой гидрокси, C1-C4 алкил или оксо, или
одной или несколькими 4-10-членными моноциклическими или бициклическими ненасыщенными гетероциклическими группами, которые могут быть замещены группой R7 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R7 представляет собой галоген, циано, C1-C4 алкил, C1-C4 алкокси или аминоʺ,
при условии, что положение тройной связи C2-C6 алкинила находится между атомом углерода, связанным с 7H-пирроло[2,3-d]пиримидиновым скелетом, и атомом углерода, смежным с этим атомом углерода,
фенил, который может быть замещен
ʺгидрокси или
C1-C4 алкилом, который может быть замещен гидроксиʺ, или
4-6-членную моноциклическую ненасыщенную гетероциклическую группу, содержащую 1 или 2 атома азота.
[0303]
[6] Еще более предпочтительным является соединение, представленное формулой (I), или его соль, где
A представляет собой
[0304]
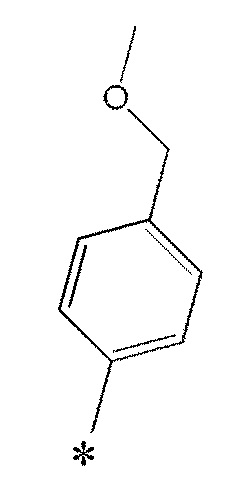
[0305]
R2 представляет собой
C3-C5 циклоалкил, который может быть замещен одним C1-C4 алкилом; и
X представляет собой CR3, где R3 представляет собой
C1-C4 алкокси, который может быть замещен ʺодной или несколькими 4-6-членными моноциклическими насыщенными гетероциклическими группами, содержащими один атом кислородаʺ, или
C2-C6 алкинил, который может быть замещен
ʺгидрокси,
амино, который может быть замещен группой R4, где R4 представляет собой метил или метоксиэтил,
C3-C7 циклоалкилом, который может быть замещен гидрокси,
ʺодной или несколькими 4-6-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены группой R6 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ, где R6 представляет собой гидрокси или метил, или
одной или несколькими 4-10-членными моноциклическими или бициклическими ненасыщенными гетероциклическими группами, которые могут быть замещены группой R7 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R7 представляет собой C1-C4 алкил или аминоʺ,
при условии, что положение тройной связи C2-C6 алкинила находится между атомом углерода, связанным с 7H-пирроло[2,3-d]пиримидиновым скелетом, и атомом углерода, смежным с этим атомом углерода.
[0306]
Другой предпочтительный вариант осуществления настоящего изобретения описан ниже.
Предпочтительным является соединение, представленное формулой (I), или его соль, где A представляет собой
[0307]

[0308]
R2 представляет собой
C3-C10 алкил, который может быть замещен ʺгалогеном, C3-C7 циклоалкилом или одной или несколькими 4-10-членными моноциклическими или полициклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ,
C3-C7 циклоалкил, который может быть замещен ʺC1-C6 алкилом, C3-C7 циклоалкилом или галогенo C1-C6 алкиломʺ, или
C4-C12 связанный мостиковой связью циклоалкил; и
X представляет собой
N или
CR3, где R3 представляет собой
водород,
галоген,
циано,
C1-C4 алкил,
C1-C6 алкокси, который может быть замещен
ʺгалогеном,
C1-C6 алкокси,
C3-C7 циклоалкилом или
одной или несколькими 4-10-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены оксо и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ,
C1-C4 алкилтио,
C3-C5 циклоалкил,
C2-C4 алкенил, который может быть замещен ʺгидроксиʺ,
C2-C6 алкинил, который может быть замещен
ʺгидрокси,
C1-C4 алкокси,
амино, который может быть замещен группой R4, где R4 представляет собой C1-C4 алкил, C1-C4 алкокси C1-C4 алкил или карбамоил, который может быть замещен C3-C5 циклоалкилом,
три-C1-C6 алкилсилилокси,
C3-C7 циклоалкилом, который может быть замещен with ʺгидрокси или оксоʺ,
фенилом, который может быть замещен группой R5, где R5 представляет собой галоген, метиламино, который может быть замещен одной или несколькими 4-6-членными моноциклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или C1-C4 алкокси,
одной или несколькими 4-6-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены группой R6 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R6 представляет собой гидрокси, C1-C4 алкил, C1-C4 алкокси или оксо,
одной или несколькими 4-10-членными моноциклическими или бициклическими ненасыщенными гетероциклическими группами, которые могут быть замещены группой R7 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R7 представляет собой галоген, циано, C1-C4 алкил, C1-C4 алкокси или амино, или
ненасыщенным гетероциклическим окси, который может быть замещен галогеном, где ненасыщенное гетероциклическое кольцо представляет собой 4-6-членное моноциклическое ненасыщенное гетероциклическое кольцо, содержащее 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ,
при условии, что положение тройной связи C2-C6 алкинила находится между атомом углерода, связанным с 7H-пирроло[2,3-d]пиримидиновым скелетом, и атомом углерода, смежным с этим атомом углерода,
фенил, который может быть замещен
ʺгидрокси,
C1-C4 алкилом, который может быть замещен гидрокси,
формилом или
одной или несколькими 4-6-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены C1-C4 алкилом и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или
4-6-членную моноциклическую ненасыщенную гетероциклическую группу, которая может быть замещена
ʺгалогеном,
C1-C4 алкилом, который может быть замещен гидрокси, или
амино, который может быть замещен группой C1-C4 алкил(карбонил)ʺ,
и содержит 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы.
[0309]
Более предпочтительным является соединение, представленное формулой (I), или его соль, где A представляет собой
[0310]
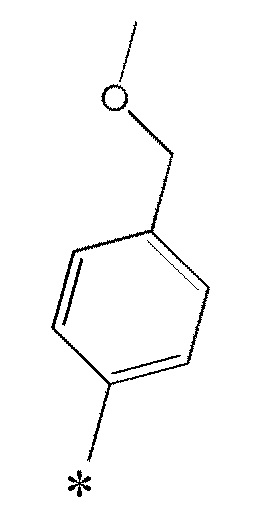
[0311]
R2 представляет собой
разветвленный C3-C8 алкил, который может быть замещен ʺгалогеном или C3-C7 циклоалкиломʺ
C3-C7 циклоалкил, который может быть замещен ʺC1-C4 алкилом или C3-C5 циклоалкиломʺ, или
C4-C12 связанный мостиковой связью циклоалкил; и
X представляет собой
N или
CR3, где R3 представляет собой
водород,
галоген,
C1-C4 алкил,
C1-C4 алкокси, который может быть замещен
ʺгалогеном,
C1-C4 алкокси,
C3-C7 циклоалкилом или
одной или несколькими 4-6-членными моноциклическими насыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ,
C1-C4 алкилтио,
C2-C4 алкенил,
C2-C6 алкинил, который может быть замещен
ʺгидрокси,
C1-C4 алкокси,
амино, который может быть замещен группой R4, где R4 представляет собой C1-C4 алкил, C1-C4 алкокси C1-C4 алкил или карбамоил, который может быть замещен C3-C5 циклоалкилом,
три-C1-C6 алкилсилилокси,
C3-C7 циклоалкилом, который может быть замещен ʺгидрокси или оксоʺ,
фенилом, который может быть замещен группой R5, где R5 представляет собой галоген,
ʺодной или несколькими 4-6-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены группой R6 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ, где R6 представляет собой гидрокси, C1-C4 алкил, C1-C4 алкокси или оксо,
ʺодной или несколькими 4-10-членными моноциклическими или бициклическими ненасыщенными гетероциклическими группами, которые могут быть замещены группой R7 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ, где R7 представляет собой галоген, циано, C1-C4 алкил, C1-C4 алкокси или амино, или
ненасыщенным гетероциклическим окси, который может быть замещен галогеном, где ненасыщенное гетероциклическое кольцо представляет собой 4-6-членное моноциклическое ненасыщенное гетероциклическое кольцо, содержащее 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ,
при условии, что положение тройной связи C2-C6 алкинила находится между атомом углерода, связанным с 7H-пирроло[2,3-d]пиримидиновым скелетом, и атомом углерода, смежным с этим атомом углерода,
фенил, который может быть замещен
ʺгидрокси,
C1-C4 алкилом, который может быть замещен гидрокси, или
формиломʺ, или
4-6-членную моноциклическую ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы.
[0312]
Еще один предпочтительный вариант осуществления настоящего изобретения описан ниже.
[1] Предпочтительным является соединение, представленное формулой (I'), или его соль, где
когда A представляет собой A1,
R1 представляет собой
галоген,
циано,
нитро,
замещенный или незамещенный C1-C6 алкил,
замещенный или незамещенный C1-C6 алкокси,
замещенный или незамещенный C2-C6 алкенил,
замещенный или незамещенный C2-C6 алкинил,
замещенный или незамещенный амино или
замещенную или незамещенную 4-10-членную моноциклическую или полициклическую ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы;
Y представляет собой N или CH;
n представляет собой целое число, имеющее значение 1 или 2;
R2 представляет собой
замещенный или незамещенный C3-C10 алкил,
замещенный или незамещенный C3-C4 циклоалкил,
замещенный или незамещенный C4-C12 связанный мостиковой связью циклоалкил,
замещенный или незамещенный C2-C6 алкенил или
замещенный или незамещенный C3-C4 циклоалкенил,
при условии, что, когда каждая группа, представленная как R2, содержит заместитель, этот заместитель не должен представлять собой замещенную или незамещенную насыщенную гетероциклическую группу, которая может содержать по меньшей мере один одинаковый или разный гетероатом, выбранный из кислорода и серы, и содержит по меньшей мере один атом азота; и
X представляет собой
N или
CR3, где R3 представляет собой
водород,
галоген,
циано,
замещенный или незамещенный C1-C6 алкил,
замещенный или незамещенный C1-C6 алкокси,
замещенный или незамещенный C1-C6 алкилтио,
замещенный или незамещенный C3-C7 циклоалкил,
замещенный или незамещенный C2-C6 алкенил,
замещенный или незамещенный C2-C6 алкинил, при условии, что положение тройной связи C2-C6 алкинила находится между атомом углерода, связанным с 7H-пирроло[2,3-d]пиримидиновым скелетом, и атомом углерода, смежным с этим атомом углерода,
замещенный или незамещенный C6-C14 ароматический углеводород или
замещенную или незамещенную 4-10-членную моноциклическую ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы; и
когда A представляет собой A2,
R1 представляет собой замещенный или незамещенный C1-C6 алкокси;
Y представляет собой CH;
n представляет собой целое число, имеющее значение 0 или 1;
R2 представляет собой замещенный или незамещенный C3-C7 циклоалкил; и
X представляет собой N.
[0313]
[1-2] Более предпочтительным является соединение, представленное формулой (I'), или его соль, где
когда A представляет собой A1,
R1 представляет собой
галоген,
циано,
нитро,
C1-C6 алкил, который может быть замещен ʺгидрокси, C1-C6 алкокси, где водород, содержащийся в алкокси, может быть замещен 1 или несколькими атомами дейтерия, C1-C6 алкилтио или C6-C14 ароматическим углеводородомʺ,
C1-C6 алкокси, который может быть замещен галогеном,
C2-C6 алкенил,
C2-C6 алкинил,
амино, который может быть замещен ʺодной или несколькими 4-10-членными моноциклическими или полициклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или C6-C14 ароматическим углеводородомʺ, или
4-10-членную моноциклическую или полициклическую ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы;
Y представляет собой N или CH;
n представляет собой целое число, имеющее значение 1 или 2;
R2 представляет собой
C3-C10 алкил, который может быть замещен ʺгалогеном, C1-C6 алкокси, C3-C7 циклоалкилом или одной или несколькими 4-10-членными моноциклическими или полициклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ,
C3-C4 циклоалкил, который может быть замещен ʺгалогеном, C1-C6 алкилом, C3-C7 циклоалкилом или галогенo C1-C6 алкиломʺ,
C4-C12 связанный мостиковой связью циклоалкил,
C2-C6 алкенил, который может быть замещен галогеном, или
C3-C4 циклоалкенил; и
X представляет собой
N или
CR3, где R3 представляет собой
водород,
галоген,
циано,
C1-C6 алкил, который может быть замещен гидрокси или оксо группой,
C1-C6 алкокси, который может быть замещен
ʺгалогеном,
C1-C6 алкокси,
C3-C7 циклоалкилом или
одной или несколькими 4-10-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены оксо и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ,
C1-C6 алкилтио,
C3-C7 циклоалкил,
C2-C6 алкенил, который может быть замещен ʺгидрокси,ʺ
C2-C6 алкинил, который может быть замещен
ʺгидрокси,
C1-C6 алкокси,
амино, который может быть замещен группой R4, где R4 представляет собой C1-C6 алкил, C1-C4 алкокси C1-C6 алкил или карбамоил, который может быть замещен C3-C7 циклоалкилом,
C1-C6 алкилсилилокси,
C3-C7 циклоалкилом, который может быть замещен ʺгидрокси или оксоʺ,
C6-C14 ароматическим углеводородом, который может быть замещен группой R5, где R5 представляет собой галоген, C1-C4 алкиламино, который может быть замещен одной или несколькими 4-10-членными моноциклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или C1-C6 алкокси,
одной или несколькими 4-10-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены группой R6 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R6 представляет собой гидрокси, C1-C6 алкил, C1-C6 алкокси или оксо,
одной или несколькими 4-10-членными моноциклическими или полициклическими ненасыщенными гетероциклическими группами, которые могут быть замещены группой R7 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R7 представляет собой галоген, циано, C1-C6 алкил, C1-C6 алкокси или амино, или
ненасыщенным гетероциклическим окси, который может быть замещен галогеном, где ненасыщенное гетероциклическое кольцо представляет собой 4-10-членное моноциклическое или полициклическое ненасыщенное гетероциклическое кольцо, содержащее 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ,
при условии, что положение тройной связи C2-C6 алкинила находится между атомом углерода, связанным с 7H-пирроло[2,3-d]пиримидиновым скелетом, и атомом углерода, смежным с этим атомом углерода,
C6-C14 ароматический углеводород, который может быть замещен
ʺгидрокси,
C1-C6 алкилом, который может быть замещен гидрокси,
формилом или
одной или несколькими 4-10-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены C1-C6 алкилом и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ, или
4-6-членную моноциклическую ненасыщенную гетероциклическую группу, которая может быть замещена
ʺгалогеном,
C1-C6 алкилом, который может быть замещен гидрокси, или
амино, который может быть замещен группой C1-C6 алкил(карбонил)ʺ,
и содержит 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы; и
когда A представляет собой A2,
R1 представляет собой замещенный или незамещенный C1-C6 алкокси;
Y представляет собой CH;
n представляет собой целое число, имеющее значение 0 или 1;
R2 представляет собой замещенный или незамещенный C3-C7 циклоалкил; и
X представляет собой N.
[0314]
[2] Еще более предпочтительным является соединение, представленное формулой (I'), или его соль, где
когда A представляет собой A1,
A1 представляет собой
[0315]

[0316]
где R1a представляет собой
C1-C6 алкил, который может быть замещен ʺC1-C6 алкокси, где водород, содержащийся в алкокси, может быть замещен 1 или несколькими атомами дейтерия, или C1-C6 алкилтиоʺ,
C2-C6 алкенил,
C2-C6 алкинил,
амино, который может быть замещен ʺодной или несколькими 4-10-членными моноциклическими или полициклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или C6-C14 ароматическим углеводородомʺ, или
4-10-членную моноциклическую или полициклическую ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы;
R1b представляет собой галоген, C1-C6 алкил или C1-C6 алкокси;
m представляет собой целое число, имеющее значение 0 или 1;
R2 представляет собой
C3-C10 алкил, который может быть замещен ʺгалогеном, C3-C7 циклоалкилом или одной или несколькими 4-10-членными моноциклическими или полициклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ,
C3-C4 циклоалкил, который может быть замещен ʺC1-C6 алкилом, C3-C7 циклоалкилом или галогенo C1-C6 алкиломʺ,
C4-C12 связанный мостиковой связью циклоалкил или
C3-C4 циклоалкенил; и
X представляет собой
N или
CR3, где R3 представляет собой
водород,
галоген,
циано,
C1-C4 алкил, который может быть замещен гидрокси или оксо группой,
C1-C6 алкокси, который может быть замещен
ʺгалогеном,
C1-C6 алкокси,
C3-C7 циклоалкилом или
одной или несколькими 4-10-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены оксо и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ,
C1-C4 алкилтио,
C3-C5 циклоалкил,
C2-C6 алкенил, который может быть замещен ʺгидрокси,ʺ
C2-C6 алкинил, который может быть замещен
ʺгидрокси,
C1-C6 алкокси,
амино, который может быть замещен группой R4, где R4 представляет собой C1-C6 алкил, C1-C4 алкокси C1-C6 алкил или карбамоил, который может быть замещен C3-C7 циклоалкилом,
C1-C6 алкилсилилокси,
C3-C7 циклоалкилом, который может быть замещен ʺгидрокси или оксоʺ,
C6-C14 ароматическим углеводородом, который может быть замещен группой R5, где R5 представляет собой галоген, C1-C4 алкиламино, который может быть замещен одной или несколькими 4-10-членными моноциклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или C1-C6 алкокси,
одной или несколькими 4-10-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены группой R6 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R6 представляет собой гидрокси, C1-C6 алкил, C1-C6 алкокси или оксо,
одной или несколькими 4-10-членными моноциклическими или полициклическими ненасыщенными гетероциклическими группами, которые могут быть замещены группой R7 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R7 представляет собой галоген, циано, C1-C6 алкил, C1-C6 алкокси или амино, или
ненасыщенным гетероциклическим окси, который может быть замещен галогеном, где ненасыщенное гетероциклическое кольцо представляет собой 4-10-членное моноциклическое или полициклическое ненасыщенное гетероциклическое кольцо, содержащее 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ,
при условии, что положение тройной связи C2-C6 алкинила находится между атомом углерода, связанным с 7H-пирроло[2,3-d]пиримидиновым скелетом, и атомом углерода, смежным с этим атомом углерода,
C6-C14 ароматический углеводород, который может быть замещен
ʺгидрокси,
C1-C6 алкилом, который может быть замещен гидрокси,
формилом или
одной или несколькими 4-10-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены C1-C6 алкилом и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или
4-6-членную моноциклическую ненасыщенную гетероциклическую группу, которая может быть замещена
ʺгалогеном,
C1-C6 алкилом, который может быть замещен гидрокси, или
амино, который может быть замещен группой C1-C6 алкил(карбонил)ʺ,
и содержит 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы; и
когда A представляет собой A2,
A2 представляет собой
[0317]

[0318]
где R1c представляет собой C1-C6 алкокси; l представляет собой целое число, имеющее значение от 1-3; и n представляет собой целое число, имеющее значение 0 или 1;
R2 представляет собой C3-C7 циклоалкил; и
X представляет собой N.
[0319] [3] Еще более предпочтительным является соединение, представленное формулой (I'), или его соль, где
A представляет собой
[0320]

[0321]
где R1a представляет собой
C1-C6 алкил, который может быть замещен ʺC1-C6 алкокси, где водород, содержащийся в алкокси, может быть замещен 1 или несколькими атомами дейтерия, или C1-C6 алкилтиоʺ,
C2-C6 алкенил,
C2-C6 алкинил,
амино, который может быть замещен ʺодной или несколькими 4-6-членными моноциклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или C6-C10 ароматическим углеводородомʺ, или
4-6-членную моноциклическую ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы;
R1b представляет собой галоген, C1-C6 алкил или C1-C6 алкокси;
m представляет собой целое число, имеющее значение 0 или 1;
R2 представляет собой
C3-C10 алкил, который может быть замещен ʺгалогеном, C3-C7 циклоалкилом или одной или несколькими 4-10-членными моноциклическими или полициклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ,
C3-C4 циклоалкил, который может быть замещен ʺC1-C6 алкилом, C3-C7 циклоалкилом или галогенo C1-C6 алкиломʺ, или
C4-C12 связанный мостиковой связью циклоалкил; и
X представляет собой
N или
CR3, где R3 представляет собой
водород,
галоген,
циано,
C1-C4 алкил,
C1-C6 алкокси, который может быть замещен
ʺгалогеном,
C1-C6 алкокси,
C3-C7 циклоалкилом или
одной или несколькими 4-10-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены оксо и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ,
C1-C4 алкилтио,
C3-C5 циклоалкил,
C2-C4 алкенил, который может быть замещен ʺгидроксиʺ,
C2-C6 алкинил, который может быть замещен
ʺгидрокси,
C1-C4 алкокси,
амино, который может быть замещен группой R4, где R4 представляет собой C1-C4 алкил, C1-C4 алкокси C1-C4 алкил или карбамоил, который может быть замещен C3-C5 циклоалкилом,
три-C1-C6 алкилсилилокси,
C3-C7 циклоалкилом, который может быть замещен with ʺгидрокси или оксоʺ,
фенилом, который может быть замещен группой R5, где R5 представляет собой галоген, метиламино, который может быть замещен одной или несколькими 4-6-членными моноциклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или C1-C4 алкокси,
одной или несколькими 4-6-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены группой R6 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R6 представляет собой гидрокси, C1-C4 алкил, C1-C4 алкокси или оксо,
одной или несколькими 4-10-членными моноциклическими или бициклическими ненасыщенными гетероциклическими группами, которые могут быть замещены группой R7 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R7 представляет собой галоген, циано, C1-C4 алкил, C1-C4 алкокси или амино, или
ненасыщенным гетероциклическим окси, который может быть замещен галогеном, где ненасыщенное гетероциклическое кольцо представляет собой 4-6-членное моноциклическое ненасыщенное гетероциклическое кольцо, содержащее 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ,
при условии, что положение тройной связи C2-C6 алкинила находится между атомом углерода, связанным с 7H-пирроло[2,3-d]пиримидиновым скелетом, и атомом углерода, смежным с этим атомом углерода,
фенил, который может быть замещен
ʺгидрокси,
C1-C4 алкилом, который может быть замещен гидрокси,
формилом или
одной или несколькими 4-6-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены C1-C4 алкилом и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ, или
4-6-членную моноциклическую ненасыщенную гетероциклическую группу, которая может быть замещена
ʺгалогеном,
C1-C4 алкилом, который может быть замещен гидрокси, или
амино, который может быть замещен группой C1-C4 алкил(карбонил)ʺ,
и содержит 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы.
[0322]
[4] Еще более предпочтительным является соединение, представленное формулой (I'), или его соль, где
A представляет собой
[0323]

[0324]
где R1a представляет собой
C1-C6 алкил, который замещен ʺC1-C6 алкокси, где водород, содержащийся в алкокси, может быть замещен 1 или несколькими атомами дейтерия, или C1-C6 алкилтиоʺ,
C2-C6 алкенил,
C2-C6 алкинил или
4-6-членную моноциклическую ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы;
R1b представляет собой галоген;
m представляет собой целое число, имеющее значение 0 или 1;
R2 представляет собой
разветвленный C3-C8 алкил, который может быть замещен ʺгалогеном или C3-C7 циклоалкиломʺ
C3-C4 циклоалкил, который может быть замещен ʺC1-C4 алкилом или C3-C5 циклоалкиломʺ, или
C4-C12 связанный мостиковой связью циклоалкил; и
X представляет собой
N или
CR3, где R3 представляет собой
водород,
галоген,
C1-C4 алкил,
C1-C4 алкокси, который может быть замещен
ʺгалогеном,
C1-C4 алкокси,
C3-C7 циклоалкилом или
одной или несколькими 4-6-членными моноциклическими насыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ,
C1-C4 алкилтио,
C2-C4 алкенил,
C2-C6 алкинил, который может быть замещен
ʺгидрокси,
C1-C4 алкокси,
амино, который может быть замещен группой R4, где R4 представляет собой C1-C4 алкил, C1-C4 алкокси C1-C4 алкил или карбамоил, который может быть замещен C3-C5 циклоалкилом,
три-C1-C6 алкилсилилокси,
C3-C7 циклоалкилом, который может быть замещен ʺгидрокси или оксоʺ,
фенилом, который может быть замещен группой R5, где R5 представляет собой галоген,
ʺодной или несколькими 4-6-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены группой R6 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ, где R6 представляет собой гидрокси, C1-C4 алкил, C1-C4 алкокси или оксо,
ʺодной или несколькими 4-10-членными моноциклическими или бициклическими ненасыщенными гетероциклическими группами, которые могут быть замещены группой R7 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ, где R7 представляет собой галоген, циано, C1-C4 алкил, C1-C4 алкокси или амино, или
ненасыщенным гетероциклическим окси, который может быть замещен галогеном, где ненасыщенное гетероциклическое кольцо представляет собой 4-6-членное моноциклическое ненасыщенное гетероциклическое кольцо, содержащее 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ,
при условии, что положение тройной связи C2-C6 алкинила находится между атомом углерода, связанным с 7H-пирроло[2,3-d]пиримидиновым скелетом, и атомом углерода, смежным с этим атомом углерода,
фенил, который может быть замещен
ʺгидрокси,
C1-C4 алкилом, который может быть замещен гидрокси, или
формиломʺ, или
4-6-членную моноциклическую ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы.
[0325]
[5] Еще более предпочтительным является соединение, представленное формулой (I'), или его соль, где
A представляет собой
[0326]

[0327]
где R1b представляет собой галоген;
m представляет собой целое число, имеющее значение 0 или 1;
R2 представляет собой
разветвленный C3-C6 алкил, который может быть замещен галогеном, или
C3-C4 циклоалкил, который может быть замещен ʺC1-C4 алкилом или C3-C5 циклоалкиломʺ;
X представляет собой CR3, где R3 представляет собой
водород,
галоген,
C1-C4 алкокси, который может быть замещен
ʺC1-C4 алкокси,
C3-C7 циклоалкилом или
одной или несколькими 4-6-членными моноциклическими насыщенными гетероциклическими группами, содержащими один атом кислородаʺ,
C1-C4 алкилтио,
C2-C4 алкенил,
C2-C6 алкинил, который может быть замещен
ʺгидрокси,
амино, который может быть замещен группой R4, где R4 представляет собой C1-C4 алкил или C1-C4 алкокси C1-C4 алкил,
C3-C7 циклоалкилом, который может быть замещен гидрокси,
фенилом, который может быть замещен группой R5, где R5 представляет собой галоген,
ʺодной или несколькими 4-6-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены группой R6 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ, где R6 представляет собой гидрокси, C1-C4 алкил или оксо, или
одной или несколькими 4-10-членными моноциклическими или бициклическими ненасыщенными гетероциклическими группами, которые могут быть замещены группой R7 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R7 представляет собой галоген, циано, C1-C4 алкил, C1-C4 алкокси или аминоʺ,
при условии, что положение тройной связи C2-C6 алкинила находится между атомом углерода, связанным с 7H-пирроло[2,3-d]пиримидиновым скелетом, и атомом углерода, смежным с этим атомом углерода,
фенил, который может быть замещен
ʺгидрокси или
C1-C4 алкилом, который может быть замещен гидроксиʺ, или
4-6-членную моноциклическую ненасыщенную гетероциклическую группу, содержащую 1 или 2 атома азота.
[0328]
[6] Еще более предпочтительным является соединение, представленное формулой (I'), или его соль, где
A представляет собой
[0329]

[0330]
R2 представляет собой
C3-C4 циклоалкил, который может быть замещен одним C1-C4 алкилом; и
X представляет собой CR3, где R3 представляет собой
C1-C4 алкокси, который может быть замещен ʺодной или несколькими 4-6-членными моноциклическими насыщенными гетероциклическими группами, содержащими один атом кислородаʺ, или
C2-C6 алкинил, который может быть замещен
ʺгидрокси,
амино, который может быть замещен группой R4, где R4 представляет собой метил или метоксиэтил,
C3-C7 циклоалкилом, который может быть замещен гидрокси,
ʺодной или несколькими 4-6-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены группой R6 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ, где R6 представляет собой гидрокси или метил, или
ʺодной или несколькими 4-10-членными моноциклическими или бициклическими ненасыщенными гетероциклическими группами, которые могут быть замещены группой R7 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ, где R7 представляет собой C1-C4 алкил или аминоʺ,
при условии, что положение тройной связи C2-C6 алкинила находится между атомом углерода, связанным с 7H-пирроло[2,3-d]пиримидиновым скелетом, и атомом углерода, смежным с этим атомом углерода.
[0331]
Еще один предпочтительный вариант осуществления настоящего изобретения описан ниже.
Предпочтительным является соединение, представленное формулой (I'), или его соль, где
A представляет собой
[0332]

[0333]
R2 представляет собой
C3-C10 алкил, который может быть замещен ʺгалогеном, C3-C7 циклоалкилом или одной или несколькими 4-10-членными моноциклическими или полициклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ,
C3-C4 циклоалкил, который может быть замещен ʺC1-C6 алкилом, C3-C7 циклоалкилом или галогенo C1-C6 алкиломʺ, или
C4-C12 связанный мостиковой связью циклоалкил; и
X представляет собой
N или
CR3, где R3 представляет собой
водород,
галоген,
циано,
C1-C4 алкил,
C1-C6 алкокси, который может быть замещен
ʺгалогеном,
C1-C6 алкокси,
C3-C7 циклоалкилом или
одной или несколькими 4-10-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены оксо и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ,
C1-C4 алкилтио,
C3-C5 циклоалкил,
C2-C4 алкенил, который может быть замещен ʺгидроксиʺ,
C2-C6 алкинил, который может быть замещен
ʺгидрокси,
C1-C4 алкокси,
амино, который может быть замещен группой R4, где R4 представляет собой C1-C4 алкил, C1-C4 алкокси C1-C4 алкил или карбамоил, который может быть замещен C3-C5 циклоалкилом,
три-C1-C6 алкилсилилокси,
C3-C7 циклоалкилом, который может быть замещен ʺгидрокси или оксоʺ,
фенилом, который может быть замещен группой R5, где R5 представляет собой галоген, метиламино, который может быть замещен одной или несколькими 4-6-членными моноциклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или C1-C4 алкокси,
одной или несколькими 4-6-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены группой R6 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R6 представляет собой гидрокси, C1-C4 алкил, C1-C4 алкокси или оксо,
одной или несколькими 4-10-членными моноциклическими или бициклическими ненасыщенными гетероциклическими группами, которые могут быть замещены группой R7 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R7 представляет собой галоген, циано, C1-C4 алкил, C1-C4 алкокси или амино, или
ненасыщенным гетероциклическим окси, который может быть замещен галогеном, где ненасыщенное гетероциклическое кольцо представляет собой 4-6-членное моноциклическое ненасыщенное гетероциклическое кольцо, содержащее 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ,
при условии, что положение тройной связи C2-C6 алкинила находится между атомом углерода, связанным с 7H-пирроло[2,3-d]пиримидиновым скелетом, и атомом углерода, смежным с этим атомом углерода,
фенил, который может быть замещен
ʺгидрокси,
C1-C4 алкилом, который может быть замещен гидрокси,
формилом или
одной или несколькими 4-6-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены C1-C4 алкилом и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или
4-6-членную моноциклическую ненасыщенную гетероциклическую группу, которая может быть замещена
ʺгалогеном,
C1-C4 алкилом, который может быть замещен гидрокси, или
амино, который может быть замещен группой C1-C4 алкил(карбонил)ʺ,
и содержит 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы.
[0334]
Более предпочтительным является соединение, представленное формулой (I'), или его соль, где
A представляет собой
[0335]

[0336]
R2 представляет собой
разветвленный C3-C8 алкил, который может быть замещен ʺгалогеном или C3-C7 циклоалкиломʺ
C3-C4 циклоалкил, который может быть замещен ʺC1-C4 алкилом или C3-C5 циклоалкиломʺ, или
C4-C12 связанный мостиковой связью циклоалкил; и
X представляет собой
N или
CR3, где R3 представляет собой
водород,
галоген,
C1-C4 алкил,
C1-C4 алкокси, который может быть замещен
ʺгалогеном,
C1-C4 алкокси,
C3-C7 циклоалкилом или
одной или несколькими 4-6-членными моноциклическими насыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ,
C1-C4 алкилтио,
C2-C4 алкенил,
C2-C6 алкинил, который может быть замещен
ʺгидрокси,
C1-C4 алкокси,
амино, который может быть замещен группой R4, где R4 представляет собой C1-C4 алкил, C1-C4 алкокси C1-C4 алкил или карбамоил, который может быть замещен C3-C5 циклоалкилом,
три-C1-C6 алкилсилилокси,
C3-C7 циклоалкилом, который может быть замещен ʺгидрокси или оксоʺ,
фенилом, который может быть замещен группой R5, где R5 представляет собой галоген,
ʺодной или несколькими 4-6-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены группой R6 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ, где R6 представляет собой гидрокси, C1-C4 алкил, C1-C4 алкокси или оксо,
ʺодной или несколькими 4-10-членными моноциклическими или бициклическими ненасыщенными гетероциклическими группами, которые могут быть замещены группой R7 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ, где R7 представляет собой галоген, циано, C1-C4 алкил, C1-C4 алкокси или амино, или
ненасыщенным гетероциклическим окси, который может быть замещен галогеном, где ненасыщенное гетероциклическое кольцо представляет собой 4-6-членное моноциклическое ненасыщенное гетероциклическое кольцо, содержащее 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ,
при условии, что положение тройной связи C2-C6 алкинила находится между атомом углерода, связанным с 7H-пирроло[2,3-d]пиримидиновым скелетом, и атомом углерода, смежным с этим атомом углерода,
фенил, который может быть замещен
ʺгидрокси,
C1-C4 алкилом, который может быть замещен гидрокси, или
формиломʺ, или
4-6-членную моноциклическую ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы.
[0337]
Еще один предпочтительный вариант осуществления настоящего изобретения описан ниже.
[0338]
Предпочтительными являются соединения, представленные формулами (I) и (I'), или их соли, где
A представляет собой
[0339]

[0340]
R2 представляет собой
[0341]
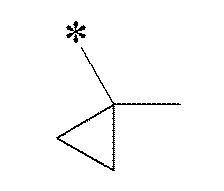
[0342]
X представляет собой CR3, где R3 предпочтительно представляет собой
водород,
галоген,
циано,
замещенный или незамещенный C1-C6 алкил,
замещенный или незамещенный C1-C6 алкокси,
замещенный или незамещенный C1-C6 алкилтио,
замещенный или незамещенный C3-C7 циклоалкил,
замещенный или незамещенный C2-C6 алкенил,
замещенный или незамещенный C2-C6 алкинил, при условии, что положение тройной связи C2-C6 алкинила находится между атомом углерода, связанным с 7H-пирроло[2,3-d]пиримидиновым скелетом, и атомом углерода, смежным с этим атомом углерода,
замещенный или незамещенный C6-C14 ароматический углеводород или
замещенную или незамещенную 4-10-членную моноциклическую ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы;
более предпочтительно
водород,
галоген,
замещенный или незамещенный C1-C6 алкокси или
замещенный или незамещенный C2-C6 алкинил, при условии, что положение тройной связи C2-C6 алкинила находится между атомом углерода, связанным с 7H-пирроло[2,3-d]пиримидиновым скелетом, и атомом углерода, смежным с этим атомом углерода;
еще более предпочтительно
водород,
галоген,
замещенный или незамещенный метокси,
замещенный или незамещенный этокси,
замещенный или незамещенный этинил или
замещенный или незамещенный пропинил, при условии, что положение тройной связи находится между атомом углерода, связанным с 7H-пирроло[2,3-d]пиримидиновым скелетом, и атомом углерода, смежным с этим атомом углерода;
еще более предпочтительно
метокси или этокси, который может быть замещен
ʺC1-C6 алкокси,
C3-C7 циклоалкилом или
одной или несколькими 4-10-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены оксо и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ, или
этинил или пропинил, который может быть замещен
ʺгидрокси,
C1-C6 алкокси,
амино, который может быть замещен группой R4, где R4 представляет собой C1-C6 алкил, C1-C4 алкокси C1-C6 алкил или карбамоил, который может быть замещен C3-C7 циклоалкилом,
C1-C6 алкилсилилокси,
C3-C7 циклоалкилом, который может быть замещен ʺгидрокси или оксоʺ,
C6-C14 ароматическим углеводородом, который может быть замещен группой R5, где R5 представляет собой галоген, C1-C4 алкиламино, который может быть замещен одной или несколькими 4-10-членными моноциклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или C1-C6 алкокси,
одной или несколькими 4-10-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены группой R6 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R6 представляет собой гидрокси, C1-C6 алкил, C1-C6 алкокси, или оксо,
одной или несколькими 4-10-членными моноциклическими или полициклическими ненасыщенными гетероциклическими группами, которые могут быть замещены группой R7 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R7 представляет собой галоген, циано, C1-C6 алкил, C1-C6 алкокси или амино, или
ненасыщенным гетероциклическим окси, который может быть замещен галогеном, где ненасыщенное гетероциклическое кольцо представляет собой 4-10-членное моноциклическое или полициклическое ненасыщенное гетероциклическое кольцо, содержащее 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ,
при условии, что положение тройной связи находится между атомом углерода, связанным с 7H-пирроло[2,3-d]пиримидиновым скелетом, и атомом углерода, смежным с этим атомом углерода; и
еще более предпочтительно
этинил или пропинил, который может быть замещен
ʺгидрокси,
амино, который может быть замещен группой R4, где R4 представляет собой C1-C4 алкил или C1-C4 алкокси C1-C4 алкил,
C3-C7 циклоалкилом, который может быть замещен гидрокси,
фенилом, который может быть замещен группой R5, где R5 представляет собой галоген,
ʺодной или несколькими 4-6-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены группой R6 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ, где R6 представляет собой гидрокси, C1-C4 алкил, или оксо, или
ʺодной или несколькими 4-10-членными моноциклическими или бициклическими ненасыщенными гетероциклическими группами, которые могут быть замещены группой R7 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серыʺ, где R7 представляет собой галоген, циано, C1-C4 алкил, C1-C4 алкокси, или аминоʺ,
при условии, что положение тройной связи находится между атомом углерода, связанным с 7H-пирроло[2,3-d]пиримидиновым скелетом, и атомом углерода, смежным с этим атомом углерода.
[0343]
Конкретные примеры соединений по настоящему изобретению включают, но не ограничиваются этим, соединения, полученные в примерах, описанных ниже.
[0344]
Предпочтительными примерами соединений по настоящему изобретению являются следующие:
(1) 4-амино-7-(трет-бутил)-N-(4-(метоксиметил)фенил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид;
(2) 4-амино-7-(1-фтор-2-метилпропан-2-ил)-N-(4-(метоксиметил)фенил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид;
(3) 4-амино-N-(4-(метоксиметил)фенил)-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид;
(4) 4-амино-6-бром-N-[4-(метоксиметил)фенил]-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид;
(5) 4-амино-6-хлор-N-[4-(метоксиметил)фенил]-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид;
(6) 4-амино-N-(4-(метоксиметил)фенил)-7-(1-метилциклопропил)-6-винил-7H-пирроло[2,3-d]пиримидин-5-карбоксамид;
(7) 4-амино-6-фтор-N-(4-(метоксиметил)фенил)-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид;
(8) 4-амино-N-[4-(метоксиметил)фенил]-7-(1-метилциклопропил)-6-(3-морфолинопроп-1-ин-1-ил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид;
(9) 4-амино-6-(4-гидрокси-4-метилпент-1-ин-1-ил)-N-[4-(метоксиметил)фенил]-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид;
(10) 4-амино-N-[4-(метоксиметил)фенил]-7-(1-метилциклопропил)-6-((тетрагидро-2H-пиран-4-ил)этинил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид;
(11) 4-амино-N-[4-(метоксиметил)фенил]-7-(1-метилциклопропил)-6-(3-(пирролидин-1-ил)проп-1-ин-1-ил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид;
(12) (R)-4-амино-N-[4-(метоксиметил)фенил]-7-(1-метилциклопропил)-6-((тетрагидрофуран-2-ил)метокси)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид;
(13) 4-амино-N-[4-(метоксиметил)фенил]-6-((1-метил-1H-пиразол-4-ил)этинил)-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид;
(14) 4-амино-6-(имидазо[1,2-b]пиридазин-3-илэтинил)-N-[4-(метоксиметил)фенил]-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид;
(15) 4-амино-N-(4-(метоксиметил)фенил)-6-((1-метил-1H-пиразол-3-ил)этинил)-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид;
(16) 4-амино-N-(4-(метоксиметил)фенил)-6-((1-метил-1H-имидазол-5-ил)этинил)-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид;
(17) 4-амино-N-[4-(метоксиметил)фенил]-7-(1-метилциклопропил)-6-(пиридин-3-илэтинил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид;
(18) 4-амино-N-(4-(метоксиметил)фенил)-7-(1-метилциклопропил)-6-(проп-1-ин-1-ил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид;
(19) 4-амино-N-[4-(метоксиметил)фенил]-7-(1-метилциклопропил)-6-(3-(пиперидин-1-ил)проп-1-ин-1-ил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид;
(20) 4-амино-6-этокси-N-(4-(метоксиметил)фенил)-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид;
(21) 4-амино-6-((1-гидроксициклопентил)этинил)-N-(4-(метоксиметил)фенил)-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид;
(22) 4-амино-N-(4-(метоксиметил)фенил)-7-(1-метилциклопропил)-6-(3-тиоморфолинопроп-1-ин-1-ил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид;
(23) 4-амино-N-(4-(метоксиметил)фенил)-7-(1-метилциклопропил)-6-(3-(тетрагидро-2H-пиран-4-ил)проп-1-ин-1-ил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид;
(24) 4-амино-6-((6-аминопиридин-3-ил)этинил)-N-(4-(метоксиметил)фенил)-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид;
(25) 4-амино-6-((1,3-диметил-1H-пиразол-4-ил)этинил)-N-(4-(метоксиметил)фенил)-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид;
(26) 4-амино-N-(4-(метоксиметил)фенил)-7-(1-метилциклопропил)-6-((1-метилпиперидин-4-ил)этинил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид;
(27) 4-амино-6-(3-(диметиламино)проп-1-ин-1-ил)-N-(4-(метоксиметил)фенил)-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид;
(28) 4-амино-N-(3-фтор-4-(метоксиметил)фенил)-7-(1-метилциклопропил)-6-((тетрагидро-2H-пиран-4-ил)этинил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид; и
(29) 4-амино-N-(3-фтор-4-(метоксиметил)фенил)-7-(1-метилциклопропил)-6-(3-морфолинопроп-1-ин-1-ил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид.
Более предпочтительными примерами соединений по настоящему изобретению являются следующие:
(8) 4-амино-N-[4-(метоксиметил)фенил]-7-(1-метилциклопропил)-6-(3-морфолинопроп-1-ин-1-ил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид;
(10) 4-амино-N-[4-(метоксиметил)фенил]-7-(1-метилциклопропил)-6-((тетрагидро-2H-пиран-4-ил)этинил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид;
(12) (R)-4-амино-N-[4-(метоксиметил)фенил]-7-(1-метилциклопропил)-6-((тетрагидрофуран-2-ил)метокси)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид; и
(13) 4-амино-N-[4-(метоксиметил)фенил]-6-((1-метил-1H-пиразол-4-ил)этинил)-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид.
Настоящее изобретение также обеспечивает ингибитор RET, включающий соединение или его соль по настоящему изобретению, например, соединение или его соль в соответствии с любым из представленных выше пунктов [1] - [6] в качестве активного ингредиента.
[0345]
Настоящее изобретение также обеспечивает фармацевтическую композицию, включающую соединение или его соль по настоящему изобретению, например, соединение или его соль в соответствии с любым из представленных выше пунктов [1] - [6].
[0346]
Настоящее изобретение также обеспечивает фармацевтическую композицию для профилактики или лечения заболевания, которое можно лечить путем ингибирования RET, при этом фармацевтическая композиция включает соединение или его соль по настоящему изобретению, например, соединение или его соль в соответствии с любым из представленных выше пунктов [1] - [6].
[0347]
Настоящее изобретение также обеспечивает противоопухолевое средство, включающее соединение или его соль по настоящему изобретению, например, соединение или его соль в соответствии с любым из представленных выше пунктов [1] - [6].
[0348]
Настоящее изобретение также обеспечивает противоопухолевое средство для лечения злокачественной опухоли с повышенной активацией RET, при этом противоопухолевое средство включает соединение или его соль по настоящему изобретению, например, соединение или его соль в соответствии с любым из представленных выше пунктов [1] - [6].
[0349]
Настоящее изобретение также обеспечивает соединение или его соль по настоящему изобретению, например, соединение или его соль в соответствии с любым из представленных выше пунктов [1] - [6], для применения для профилактики или лечения злокачественной опухоли.
[0350]
Настоящее изобретение также обеспечивает соединение или его соль по настоящему изобретению, например, соединение или его соль в соответствии с любым из представленных выше пунктов [1] - [6], для применения для профилактики или лечения злокачественной опухоли с повышенной активацией RET.
[0351]
Настоящее изобретение также обеспечивает применение соединения или его соли по настоящему изобретению, например, соединения или его соли в соответствии с любым из представленных выше пунктов [1] - [6], для получения противоопухолевого средства.
[0352]
Настоящее изобретение также обеспечивает применение соединения или его соли по настоящему изобретению, например, соединения или его соли в соответствии с любым из представленных выше пунктов [1] - [6], для получения противоопухолевого средства для лечения злокачественной опухоли с повышенной активацией RET.
[0353]
Настоящее изобретение также обеспечивает применение соединения или его соли по настоящему изобретению, например, соединения или его соли в соответствии с любым из представленных выше пунктов [1] - [6], для получения ингибитора RET.
[0354]
Настоящее изобретение также обеспечивает применение соединения или его соли по настоящему изобретению, например, соединения или его соли в соответствии с любым из представленных выше пунктов [1] - [6], для профилактики или лечения злокачественной опухоли.
[0355]
Настоящее изобретение также обеспечивает применение соединения или его соли по настоящему изобретению, например, соединения или его соли в соответствии с любым из представленных выше пунктов [1] - [6], для профилактики или лечения злокачественной опухоли с повышенной активацией RET.
[0356]
Настоящее изобретение также обеспечивает способ для профилактики или лечения злокачественной опухоли, включающий введение млекопитающему соединения или его соли по настоящему изобретению, например, соединения или его соли в соответствии с любым из представленных выше пунктов [1] - [6].
[0357]
Настоящее изобретение также обеспечивает способ для профилактики или лечения злокачественной опухоли, включающий введение млекопитающему соединения или его соли по настоящему изобретению, например, соединения или его соли в соответствии с любым из представленных выше пунктов [1] - [6], где злокачественная опухоль представляет собой злокачественную опухоль с повышенной активацией RET.
[0358]
Настоящее изобретение также обеспечивает способ для ингибирования RET, включающий введение млекопитающему соединения или его соли по настоящему изобретению, например, соединения или его соли в соответствии с любым из представленных выше пунктов [1] - [6].
[0359]
Далее описаны способы для получения соединений по настоящему изобретению.
[0360]
Соединения (I) и (I') по настоящему изобретению можно получить, например, способами получения, описанными ниже, или способами, описанными в примерах. Однако способы для получения Соединений (I) и (I') по настоящему изобретению не ограничиваются этими примерами реакций.
[0361]
Способ получения 1
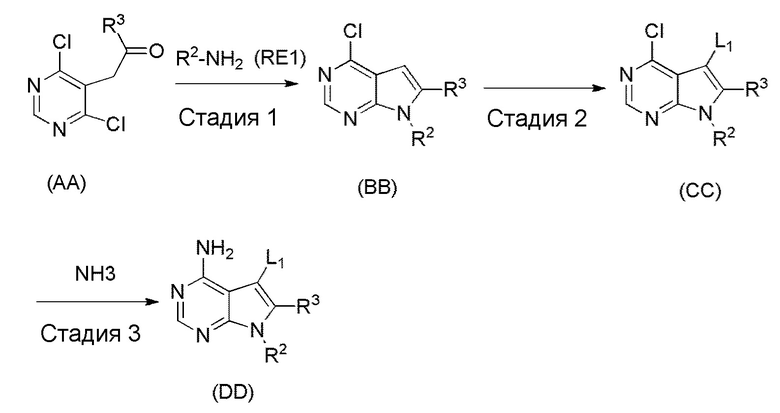
[0362]
где L1 представляет собой удаляемую группу, и R2 и R3 имеют значение, определенное выше.
Стадия 1
На этой стадии синтезируют соединение, представленное формулой (BB), из соединения, представленного формулой (AA). Соединение, представленное формулой (AA), можно получить от коммерческих поставщиков, или его можно получить известным способом.
[0363]
Стадию 1 осуществляют с использованием амино соединения, представленного формулой (RE1), или его соли в количестве обычно 0,5-5 моль, предпочтительно 0,9-1,5 моль, на моль соединения, представленного формулой (AA).
[0364]
На этой стадии при необходимости можно добавить основание. Примеры оснований включают неорганические основания, такие как гидрокарбонат натрия, карбонат натрия, карбонат калия, карбонат цезия, гидроксид цезия, гидрид натрия и гидрид калия; органические амины, такие как триметиламин, триэтиламин, трипропиламин, диизопропилэтиламин, N-метилморфолин, пиридин, 4-(N,N-диметиламино)пиридин, лутидин и коллидин; и т.п. Количество основания, которое используют, как правило, составляет 1-100 моль, предпочтительно 1-10 моль, на моль соединения, представленного формулой (AA). Амино соединение можно получить от коммерческих поставщиков, или его можно получить известным способом. Кроме того, реакцию можно промотировать путем добавления кислоты в процессе реакции, при необходимости. Примеры кислот включают муравьиную кислоту, уксусную кислоту, хлористоводородную кислоту, фосфорную кислоту и т.п. Количество используемой кислоты, как правило, составляет 1-100 моль, предпочтительно 1-20 моль, на моль соединения, представленного формулой (AA).
[0365]
Реакционный растворитель конкретно не ограничивается, и можно использовать любой растворитель, который не оказывает отрицательного влияния на реакцию. Примеры растворителя включают спирты (например, метанол и этанол), углеводороды (например, бензол, толуол и ксилол), галогенированные углеводороды (например, метиленхлорид, хлороформ и 1,2-дихлорэтан), нитрилы (например, ацетонитрил), простые эфиры (например, 1,2-диметоксиэтан и тетрагидрофуран), апротонные полярные растворители (например, N,N-диметилформамид, диметилсульфоксид и гексаметилфосфорамид), воду и их смеси.
[0366]
Время реакции, как правило, находится в пределах 0,1-100 часов, предпочтительно 0,5-24 часа. Температура реакции, как правило, находится в пределах 0-120°C, предпочтительно 50-120°C.
[0367]
Полученное таким образом соединение, представленное формулой (BB), можно подвергнуть следующей стадии после, или без, выделения и очистки из реакционной смеси известными способами разделения и очистки, такими как концентрирование, концентрирование под вакуумом, кристаллизация, экстракция растворителем, повторное осаждение и хроматография.
[0368]
Стадия 2
На этой стадии синтезируют соединение, представленное формулой (CC), из соединения, представленного формулой (BB).
[0369]
Стадию 2, как правило, осуществляют с использованием галогенирующего реагента в количестве 1-10 моль, предпочтительно 1-5 моль, на моль соединения, представленного формулой (BB).
[0370]
Примеры галогенирующих реагентов включают N-иодсукцинимид, N-бромсукцинимид, N-хлорсукцинимид, иод, бром и т.п. Реакционный растворитель конкретно не ограничивается, и можно использовать любой растворитель, который не оказывает отрицательного влияния на реакцию. Примеры растворителя включают толуол, бензол, тетрагидрофуран, 1,4-диоксан, диметилформамид, диметилацетамид, N-метилпирролидинон, диметилсульфоксид и их смеси.
[0371]
Примеры удаляемой группы, представленной как L1, включают хлор, бром, иод и т.п.
[0372]
Температура реакции, как правило, находится в пределах от -78 до 200°C, предпочтительно 0-50°C. Время реакции, как правило, находится в пределах от 5 минут до 6 дней, предпочтительно от 10 минут до 3 дней.
[0373]
Полученное таким образом соединение, представленное формулой (CC), можно подвергнуть следующей стадии после, или без, выделения и очистки из реакционной смеси известными способами разделения и очистки, такими как концентрирование, концентрирование под вакуумом, кристаллизация, экстракция растворителем, повторное осаждение и хроматография.
[0374]
Стадия 3
На этой стадии получают соединение, представленное формулой (DD), путем взаимодействия соединения, представленного формулой (CC), с аммиаком или его солью.
[0375]
Количество аммиака или его соли, используемое на этой стадии, как правило, составляет от эквимолярного до избыточного молярного количества на моль соединения, представленного формулой (CC).
[0376]
Реакционный растворитель конкретно не ограничивается, и можно использовать любой растворитель, который не оказывает отрицательного влияния на реакцию. Примеры растворителя включают воду, метанол, этанол, изопропанол, трет-бутиловый спирт, тетрагидрофуран, 1,4-диоксан, диметилформамид, N-метилпирролидон, 1,2-диметоксиэтан, диметилсульфоксид и их смеси.
[0377]
Температура реакции, как правило, находится в пределах 0-200°C, предпочтительно от комнатной температуры до 150°C. Время реакции, как правило, находится в пределах от 5 минут до 7 дней, предпочтительно от 30 минут до 4 дней.
[0378]
Полученное таким образом соединение, представленное формулой (DD), можно подвергнуть следующей стадии после, или без, выделения и очистки из реакционной смеси известными способами разделения и очистки, такими как концентрирование, концентрирование под вакуумом, кристаллизация, экстракция растворителем, повторное осаждение и хроматография.
[0379]
Способ получения 2
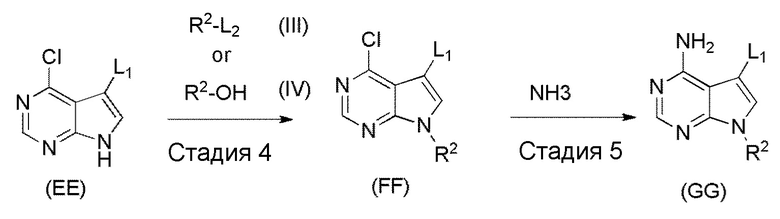
[0380]
где L1 и L2 каждый представляет собой удаляемую группу, и R2 имеет значение, определенное выше.
Стадия 4
На этой стадии получают соединение, представленное формулой (FF), с использованием соединения, представленного формулой (EE), и соединения, представленного формулой (III) или (IV). Соединение, представленное формулой (EE), можно получить от коммерческих поставщиков, или его можно получить известным способом.
[0381]
Когда соединение, представленное формулой (III), используют в качестве алкилирующего реагента, соединение, представленное формулой (FF), можно получить в присутствии основания. В формуле (III) L2 представляет собой удаляемую группу, такую как хлор, бром, иод, эфир метансульфоновой кислоты или эфир п-толуолсульфоновой кислоты. Соединение, представленное формулой (III), можно получить от коммерческих поставщиков, или его можно получить известным способом. Используемое количество соединения, представленного формулой (III), как правило, составляет 1-10 моль, предпочтительно 1-5 моль, на моль соединения, представленного формулой (EE).
[0382]
Примеры оснований включают неорганические основания, такие как гидрокарбонат натрия, карбонат натрия, карбонат калия, карбонат цезия, гидроксид цезия, гидрид натрия и гидрид калия; органические амины, такие как триметиламин, триэтиламин, трипропиламин, диизопропилэтиламин, N-метилморфолин, пиридин, 4-(N,N-диметиламино)пиридин, лутидин и коллидин; и т.п. Количество основания, которое используют, как правило, составляет 1-100 моль, предпочтительно 1-10 моль, на моль соединения, представленного формулой (EE).
[0383]
Реакционный растворитель конкретно не ограничивается, и можно использовать любой растворитель, который не оказывает отрицательного влияния на реакцию. Примеры растворителя включают N,N-диметилформамид, N,N-диметилацетамид, диметилсульфоксид, тетрагидрофуран, 1,4-диоксан, N-метилпирролидин-2-он, ацетонитрил и т.п. Эти растворители можно использовать отдельно или в смеси.
[0384]
Время реакции, как правило, находится в пределах 0,1-100 часов, предпочтительно 0,5-24 часа. Температура реакции находится в пределах от 0°C до температуры кипения реакционного растворителя, предпочтительно 0-100°C.
[0385]
Когда соединение формулы (IV) используют в качестве алкилирующего реагента, соединение, представленное формулой (FF), можно получить через реакцию Мицунобу. Эту стадию, как правило, можно осуществить известным способом, например, способом, раскрытым в Chemical Reviews, Vol. 109, p. 2551 (2009). Например, эту стадию можно осуществить в присутствии реагента Мицунобу и фосфинового реагента в растворителе, который не оказывает отрицательного влияния на реакцию. Эту стадию, как правило, осуществляют с использованием соединения, представленного формулой (IV), в количестве 1-10 моль, предпочтительно 1-5 моль, на моль соединения, представленного формулой (EE).
[0386]
Примеры реагентов Мицунобу включают диэтилазодикарбоксилат, диизопропилазодикарбоксилат и т.п. Количество используемого реагента Мицунобу, как правило, составляет 1-10 моль, предпочтительно 1-5 моль, на моль соединения, представленного формулой (EE).
[0387]
Примеры фосфиновых реагентов включают трифенилфосфин и трибутилфосфин. Количество используемого фосфинового реагента как правило, составляет 1-10 моль, предпочтительно 1-5 моль, на моль соединения, представленного формулой (EE).
[0388]
Реакционный растворитель конкретно не ограничивается, и можно использовать любой растворитель, который не оказывает отрицательного влияния на реакцию. Примеры растворителя включают толуол, бензол, тетрагидрофуран, 1,4-диоксан, диметилформамид, диметилацетамид, N-метилпирролидинон, диметилсульфоксид и их смеси.
[0389]
Температура реакции, как правило, находится в пределах от -78 до 200°C, предпочтительно 0-50°C. Время реакции, как правило, находится в пределах от 5 минут до 3 дней, предпочтительно от 10 минут до 48 часов.
[0390]
Полученное таким образом соединение, представленное формулой (FF), можно подвергнуть следующей стадии после, или без, выделения и очистки из реакционной смеси известными способами разделения и очистки, такими как концентрирование, концентрирование под вакуумом, кристаллизация, экстракция растворителем, повторное осаждение и хроматография.
[0391]
Стадия 5
На этой стадии получают соединение, представленное формулой (GG), путем взаимодействия соединения, представленного формулой (FF), с аммиаком или его солью.
[0392]
Количество аммиака или его соли, используемое на этой стадии, как правило, составляет от эквимолярного до избыточного молярного количества на моль соединения, представленного формулой (FF).
[0393]
Реакционный растворитель конкретно не ограничивается, и можно использовать любой растворитель, который не оказывает отрицательного влияния на реакцию. Примеры растворителя включают воду, метанол, этанол, изопропанол, трет-бутиловый спирт, тетрагидрофуран, 1,4-диоксан, диметилформамид, 1,2-диметоксиэтан, N-метилпирролидон, диметилсульфоксид и их смеси.
[0394]
Температура реакции, как правило, находится в пределах 0-200°C, предпочтительно от комнатной температуры до 150°C. Время реакции, как правило, находится в пределах от 5 минут до 7 дней, предпочтительно от 30 минут до 4 дней.
[0395]
Полученное таким образом соединение, представленное формулой (GG), можно подвергнуть следующей стадии после, или без, выделения и очистки из реакционной смеси известными способами разделения и очистки, такими как концентрирование, концентрирование под вакуумом, кристаллизация, экстракция растворителем, повторное осаждение и хроматография.
[0396]
Способ получения 3

[0397]
где L1 и L2 каждый представляет собой удаляемую группу, и R2 имеет значение, определенное выше.
Стадия 6
На этой стадии получают соединение, представленное формулой (WW), с использованием соединения, представленного формулой (QQ) и соединения, представленного формулой (III) или (IV). Соединение, представленное формулой (QQ), можно получить от коммерческих поставщиков, или его можно получить известным способом. Когда соединение, представленное формулой (III), используют в качестве алкилирующего реагента, соединение, представленное формулой (WW), можно получить в присутствии основания. В формуле (III) L2 представляет собой удаляемую группу, такую как хлор, бром, иод, эфир метансульфоновой кислоты, или эфир п-толуолсульфоновой кислоты; и можно получить от коммерческих поставщиков, или можно получить известным способом. Количество соединения, представленного формулой (III), которое используют, как правило, составляет 1-10 моль, предпочтительно 1-5 моль, на моль соединения, представленного формулой (QQ).
[0398]
Примеры оснований включают неорганические основания, такие как гидрокарбонат натрия, карбонат натрия, карбонат калия, карбонат цезия, гидроксид цезия, гидрид натрия и гидрид калия; органические амины, такие как триметиламин, триэтиламин, трипропиламин, диизопропилэтиламин, N-метилморфолин, пиридин, 4-(N,N-диметиламино)пиридин, лутидин и коллидин; и т.п. Количество основания, которое используют, как правило, составляет 1-100 моль, предпочтительно 2-10 моль, на моль соединения, представленного формулой (QQ). Примеры реакционного растворителя включают N,N-диметилформамид, N,N-диметилацетамид, диметилсульфоксид, тетрагидрофуран, 1,4-диоксан, N-метилпирролидин-2-он, ацетонитрил и т.п. Эти растворители можно использовать отдельно или в смеси.
[0399]
Время реакции, как правило, находится в пределах 0,1-100 часов, предпочтительно 0,5-24 часа. Температура реакции находится в пределах от 0°C до температуры кипения растворителя, предпочтительно 0-100°C.
[0400]
Когда соединение формулы (IV) используют в качестве алкилирующего реагента, соединение, представленное формулой (WW), можно получить через реакцию Мицунобу. Эту стадию, как правило, можно осуществить известным способом, например, способом, раскрытым в Chemical Reviews, Vol. 109, p. 2551 (2009). Например, эту стадию можно осуществить в присутствии реагента Мицунобу и фосфинового реагента в растворителе, который не оказывает отрицательного влияния на реакцию. Эту стадию, как правило, осуществляют с использованием соединения, представленного формулой (IV), в количестве обычно 1-10 моль, предпочтительно 1-5 моль, на моль соединения, представленного формулой (QQ).
[0401]
Примеры реагентов Мицунобу включают диэтилазодикарбоксилат, диизопропилазодикарбоксилат и т.п. Количество используемого реагента Мицунобу как правило, составляет 1-10 моль, предпочтительно 1-5 моль, на моль соединения, представленного формулой (QQ). Примеры фосфиновых реагентов включают трифенилфосфин и трибутилфосфин. Количество используемого фосфинового реагента как правило, составляет 1-10 моль, предпочтительно 1-5 моль, на моль соединения, представленного формулой (QQ).
[0402]
Реакционный растворитель конкретно не ограничивается, и можно использовать любой растворитель, который не оказывает отрицательного влияния на реакцию. Примеры растворителя включают толуол, бензол, тетрагидрофуран, 1,4-диоксан, диметилформамид, диметилацетамид, N-метилпирролидинон, диметилсульфоксид и их смеси.
[0403]
Температура реакции, как правило, находится в пределах от -78 до 200°C, предпочтительно 0-50°C. Время реакции, как правило, находится в пределах от 5 минут до 3 дней, предпочтительно от 10 минут до 48 часов.
[0404]
Полученное таким образом соединение, представленное формулой (WW), можно подвергнуть следующей стадии после, или без, выделения и очистки из реакционной смеси известными способами разделения и очистки, такими как концентрирование, концентрирование под вакуумом, кристаллизация, экстракция растворителем, повторное осаждение и хроматография.
[0405]
Способ получения 4
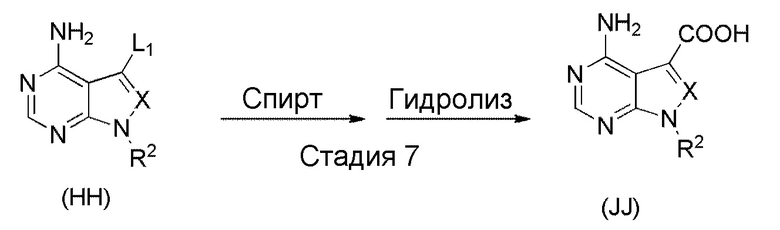
[0406]
где L1 представляет собой удаляемую группу, и R2 и X имеют значение, определенное выше.
Стадия 7
На этой стадии получают соединение, представленное формулой (JJ), путем взаимодействия соединения, представленного формулой (HH), в атмосфере оксида углерода в присутствии спирта, с использованием, например, переходного металла и, необязательно, основания в растворителе, который не оказывает отрицательного влияния на реакцию.
[0407]
Соединение, представленное формулой (HH), можно получить путем осуществления стадий 1-3, стадий 4 и 5 или стадии 6 способа получения, раскрытого в настоящей заявке.
[0408]
На этой стадии давление оксида углерода, как правило, составляет 1 атм - 20 атм, предпочтительно 1 атм - 10 атм.
[0409]
Количество используемого спиртового соединения, как правило, составляет от 1 до избыточного молярного количества на моль соединения, представленного формулой (HH). Примеры спиртовых соединений включают метанол, этанол, пропанол, изопропиловый спирт, диэтиламиноэтанол, изобутанол, 4-(2-гидроксиэтил)морфолин, 3-морфолинопропанол, диэтиламинопропанол и т.п.
[0410]
Примеры катализаторов на основе переходных металлов, используемых на этой стадии, включают палладиевые катализаторы (например, ацетат палладия, трис(бензилиденацетон)дипалладий, бис(трифенилфосфин)палладий(II) дихлорид, комплекс 1,1'-бис(дифенилфосфино)ферроцен-палладий(II) дихлорид-дихлорметан и т.д.). При необходимости, добавляют лиганд (например, трифенилфосфин, xantphos, три-трет-бутилфосфин и т.д.). Количество катализатора на основе переходного металла варьируется в зависимости от типа катализатора. Например, количество используемого катализатора на основе переходного металла, как правило, составляет 0,0001-1 моль, предпочтительно 0,001-0,5 моль, на моль соединения, представленного формулой (HH). Количество используемого лиганда, как правило, составляет 0,000 1-4 моль, предпочтительно 0,01-2 моль, на моль соединения, представленного формулой (HH).
[0411]
Кроме того, при необходимости можно добавить основание в ходе указанной выше реакции. Примеры оснований включают органические основания, такие как триэтиламин, диизопропилэтиламин, пиридин, лутидин, коллидин, 4-диметиламинопиридин, N-метилморфолин, трет-бутират калия, трет-бутират натрия, метоксид натрия, этоксид натрия, гексаметилдисилазид лития, гексаметилдисилазид натрия, гексаметилдисилазид калия и бутиллитий; и неорганические основания, такие как гидрокарбонат натрия, карбонат натрия, карбонат калия, карбонат цезия, гидроксид натрия и гидрид натрия. Количество основания, которое используют, как правило, составляет 0,1-50 моль, предпочтительно 1-20 моль, на моль соединения, представленного формулой (HH).
[0412]
Реакционный растворитель конкретно не ограничивается, и можно использовать любой растворитель, который не оказывает отрицательного влияния на реакцию. Примеры растворителя включают углеводороды (например, бензол, толуол и ксилол), нитрилы (например, ацетонитрил), простые эфиры (например, 1,2-диметоксиэтан, тетрагидрофуран и 1,4-диоксан), спирты (например, метанол и этанол), апротонные полярные растворители (например, диметилформамид, диметилацетамид, N-метилпирролидинон, диметилсульфоксид и гексаметилфосфорамид), воду и их смеси. Время реакции, как правило, находится в пределах 0,1-100 часов, предпочтительно 0,5-24 часа. Температура реакции, как правило, составляет 0°C-200°C, предпочтительно 0-150°C.
[0413]
Сложноэфирную форму, соответствующую используемому спирту, или смесь сложноэфирной формы и карбоновокислотного соединения (JJ) можно подвергнуть реакции гидролиза для преобразования таким образом сложноэфирной формы или смеси в соединение, представленное формулой (JJ). Гидролиз осуществляют с использованием основания. Примеры оснований включают органические основания, такие как диэтиламин, диизопропиламин, трет-бутират калия, трет-бутират натрия, метоксид натрия, этоксид натрия, гексаметилдисилазид лития, гексаметилдисилазид натрия, гексаметилдисилазид калия и бутиллитий; и неорганические основания, такие как гидрокарбонат натрия, карбонат натрия, карбонат калия, карбонат цезия, гидроксид натрия, гидроксид калия, гидроксид лития и гидроксид кальция.
[0414]
Реакционный растворитель конкретно не ограничивается, и можно использовать любой растворитель, который не оказывает отрицательного влияния на реакцию. Примеры растворителя включают углеводороды (например, бензол, толуол и ксилол), нитрилы (например, ацетонитрил), простые эфиры (например, 1,2-диметоксиэтан, тетрагидрофуран и 1,4-диоксан), спирты (например, метанол и этанол), апротонные полярные растворители (например, диметилформамид, диметилацетамид, N-метилпирролидинон, диметилсульфоксид и гексаметилфосфорамид), воду и их смеси.
[0415]
Время реакции, как правило, находится в пределах 0,1-100 часов, предпочтительно 0,5-24 часа. Температура реакции находится в пределах от 0°C до температуры кипения растворителя, предпочтительно 0-150°C.
[0416]
Полученное таким образом соединение, представленное формулой (JJ), можно подвергнуть следующей стадии после, или без, выделения и очистки из реакционной смеси известными способами разделения и очистки, такими как концентрирование, концентрирование под вакуумом, кристаллизация, экстракция растворителем, повторное осаждение и хроматография.
[0417]
Способ получения 5
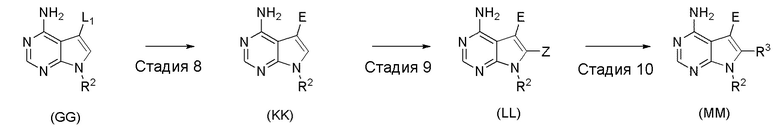
[0418]
где L1 представляет собой удаляемую группу; E представляет собой сложный эфир, циано или карбоновокислотный эквивалент, такой как карбоксамид; Z представляет собой галоген; и R2 и R3 имеют значение, определенное выше.
Стадия 8
На этой стадии получают сложноэфирное производное или циано производное, представленное формулой (KK), путем взаимодействия соединения, представленного формулой (GG), в атмосфере оксида углерода в присутствии спирта или с использованием циано соединения, такого как цианид меди или цианид цинка, с использованием, например, катализатора на основе переходного металла и, необязательно, основания в растворителе, который не оказывает отрицательного влияния на реакцию.
[0419]
Соединение, представленное формулой (GG), можно получить путем осуществления стадий 1-3 или стадий 4 и 5 способа получения, раскрытого в настоящей заявке.
[0420]
При получении сложноэфирного производного давление оксида углерода как правило, составляет 1 атм - 20 атм, предпочтительно 1 атм - 10 атм. Количество используемого спиртового соединения в качестве реагирующего вещества составляет от 1 до избыточного молярного количества, предпочтительно 1-200 моль, на моль соединения, представленного формулой (GG). Примеры спиртовых соединений включают метанол, этанол, пропанол, изопропиловый спирт, диэтиламиноэтанол, изобутанол, 4-(2-гидроксиэтил)морфолин, 3-морфолинопропанол, диэтиламинопропанол и т.п.
[0421]
При получении циано производного, примеры циано соединения, используемого в качестве реагирующего вещества, включают цианид меди, цианид цинка, три-н-бутилцианоолово и т.п. Количество используемого циано соединения, как правило, составляет 1-100 моль, предпочтительно 1-10 моль, на моль соединения, представленного формулой (GG).
[0422]
Примеры катализаторов на основе переходных металлов, используемых на этой стадии, как для получения сложноэфирного производного, так и для получения циано производного включают палладиевые катализаторы (например, ацетат палладия, тетракис(трифенилфосфин)палладий, трис(бензилиденацетон)дипалладий, бис(трифенилфосфин)палладий(II) дихлорид, комплекс 1,1'-бис(дифенилфосфино)ферроцен-палладий(II) дихлорид-дихлорметан и т.д.). При необходимости, добавляют лиганд (например, трифенилфосфин, xantphos, три-трет-бутилфосфин и т.д.). Количество катализатора на основе переходного металла варьируется в зависимости от типа катализатора. Например, количество используемого катализатора на основе переходного металла, как правило, составляет 0,0001-1 моль, предпочтительно 0,001-0,5 моль, на моль соединения, представленного формулой (GG). Количество используемого лиганда как правило, составляет 0,000 1-4 моль, предпочтительно 0,01-2 моль, на моль соединения, представленного формулой (GG).
[0423]
Кроме того, при необходимости можно добавить основание в ходе указанной выше реакции. Примеры оснований включают органические основания, такие как триэтиламин, диизопропилэтиламин, пиридин, лутидин, коллидин, 4-диметиламинопиридин, N-метилморфолин, трет-бутират калия, трет-бутират натрия, метоксид натрия, этоксид натрия, гексаметилдисилазид лития, гексаметилдисилазид натрия, гексаметилдисилазид калия и бутиллитий; и неорганические основания, такие как гидрокарбонат натрия, карбонат натрия, карбонат калия, карбонат цезия, гидроксид натрия и гидрид натрия. Количество основания, которое используют, как правило, составляет 0,1-50 моль, предпочтительно 1-20 моль, на моль соединения, представленного формулой (GG).
[0424]
Реакционный растворитель конкретно не ограничивается, и можно использовать любой растворитель, который не оказывает отрицательного влияния на реакцию. Примеры растворителя включают углеводороды (например, бензол, толуол и ксилол), нитрилы (например, ацетонитрил), простые эфиры (например, диметоксиэтан, тетрагидрофуран и 1,4-диоксан), спирты (например, метанол и этанол), апротонные полярные растворители (например, диметилформамид, диметилацетамид, N-метилпирролидинон, диметилсульфоксид и гексаметилфосфорамид), воду и их смеси. Время реакции, как правило, находится в пределах 0,1-100 часов, предпочтительно 0,5-24 часа. Температура реакции находится в пределах 0°C-200°C, предпочтительно 0-150°C. Полученное таким образом соединение, представленное формулой (KK), можно подвергнуть следующей стадии после, или без, выделения и очистки из реакционной смеси известными способами разделения и очистки, такими как концентрирование, концентрирование под вакуумом, кристаллизация, экстракция растворителем, повторное осаждение и хроматография.
[0425]
Стадия 9
На этой стадии получают галогенированное соединение (LL) путем обработки соединения, представленного формулой (KK), галогенирующим агентом.
[0426]
Эту стадию, как правило, осуществляют с использованием галогенирующего реагента в количестве обычно 1-10 моль, предпочтительно 1-5 моль, на моль соединения, представленного формулой (KK).
[0427]
Примеры галогенирующих реагентов включают 1-хлорметил-4-фтор-1,4-диазониабицикло[2.2.2]октан бис(тетрафторборат), N-иодсукцинимид, N-бромсукцинимид, N-хлорсукцинимид, иод, бром и т.п. Реакционный растворитель конкретно не ограничивается, и можно использовать любой растворитель, который не оказывает отрицательного влияния на реакцию. Примеры растворителя включают дихлорметан, хлороформ, толуол, бензол, тетрагидрофуран, 1,4-диоксан, диметилформамид, диметилацетамид, N-метилпирролидинон, диметилсульфоксид и их смеси.
[0428]
Примеры галогена, представленного как Z, включают фтор, хлор, бром, иод и т.п.
[0429]
Температура реакции, как правило, находится в пределах от -78 до 200°C, предпочтительно от 0 до 50°C. Время реакции, как правило, находится в пределах от 5 минут до 6 дней, предпочтительно от 10 минут до 3 дней.
[0430]
Полученное таким образом соединение, представленное формулой (LL), можно подвергнуть следующей стадии после, или без, выделения и очистки из реакционной смеси известными способами разделения и очистки, такими как концентрирование, концентрирование под вакуумом, кристаллизация, экстракция растворителем, повторное осаждение и хроматография.
[0431]
Кроме того, E можно преобразовать в другую группу E, если это потребуется, известным способом, таким как гидролиз или сольволиз. Например, циано можно преобразовать в карбоксамид путем гидролиза, и циано или карбоксамид можно преобразовать в сложный эфир путем сольволиза.
[0432]
Стадия 10
На этой стадии получают соединение, представленное формулой (MM), подвергая соединение, представленное формулой (LL), реакции сочетания с боратным производным, производным борной кислоты, производным олова, ацетиленовым производным, солью щелочного металла, солью щелочно-земельного металла, алкоксидом или тиоалкоксидом, который содержит R3, с использованием, например, переходного металла и, необязательно, основания в растворителе, который не оказывает отрицательного влияния на реакцию.
[0433]
Количество используемого боратного производного, производного борной кислоты, производного олова, ацетиленового производного, соли щелочного металла, соли щелочно-земельного металла, алкоксида или тиоалкоксида, который содержит R3, как правило, составляет 1-100 моль, предпочтительно 1-20 моль. Примеры катализаторов на основе переходных металлов, используемых на этой стадии, включают палладиевые катализаторы (например, ацетат палладия, тетракис(трифенилфосфин)палладий, трис(бензилиденацетон)дипалладий, бис(трифенилфосфин)палладий(II) дихлорид, комплекс 1,1'-бис(дифенилфосфино)ферроцен-палладий(II) дихлорид-дихлорметан и т.д.). При необходимости, добавляют лиганд (например, трифенилфосфин, xantphos, 2-дициклогексилфосфино-2',4',6'-триизопропилбифенил, 2-дициклогексилфосфино-2',6'-диметоксибифенил, трициклогексилфосфин, три-трет-бутилфосфин и т.д.). Примеры медных катализаторов включают иодид меди, бромид меди и хлорид меди. Количество катализатора на основе переходного металла варьируется в зависимости от типа катализатора. Например, количество используемого катализатора на основе переходного металла, как правило, составляет 0,0001-1 моль, предпочтительно 0,001-0,5 моль, на моль соединения, представленного формулой (LL). Катализаторы на основе переходного металла можно использовать в комбинации, при необходимости. Количество используемого лиганда, как правило, составляет 0,0001-4 моль, предпочтительно 0,01-2 моль, на моль соединения, представленного формулой (LL).
[0434]
Кроме того, при необходимости можно добавить основание в ходе указанной выше реакции. Примеры оснований включают органические основания, такие как триэтиламин, диизопропилэтиламин, пиридин, лутидин, коллидин, 4-диметиламинопиридин, N-метилморфолин, трет-бутират калия, трет-бутират натрия, метоксид натрия, этоксид натрия, гексаметилдисилазид лития, гексаметилдисилазид натрия, гексаметилдисилазид калия и бутиллитий; и неорганические основания, такие как гидрокарбонат натрия, карбонат натрия, карбонат калия, карбонат цезия, фосфат калия, гидроксид натрия и гидрид натрия. Количество основания, которое используют, как правило, составляет 0,1-50 моль, предпочтительно 1-20 моль, на моль соединения, представленного формулой (LL).
[0435]
Реакционный растворитель конкретно не ограничивается, и можно использовать любой растворитель, который не оказывает отрицательного влияния на реакцию. Примеры растворителя включают углеводороды (например, бензол, толуол и ксилол), нитрилы (например, ацетонитрил), простые эфиры (например, диметоксиэтан, тетрагидрофуран и 1,4-диоксан), спирты (например, метанол, этанол и этиленгликоль), апротонные полярные растворители (например, диметилформамид, диметилацетамид, N-метилпирролидинон, диметилсульфоксид и гексаметилфосфорамид), воду и их смеси.
[0436]
Время реакции, как правило, находится в пределах 0,1-100 часов, предпочтительно 0,5-24 часа. Температура реакции находится в пределах от 0°C до температуры кипения растворителя, предпочтительно 0-160°C.
[0437]
Полученное таким образом соединение, представленное формулой (MM), можно подвергнуть следующей стадии после, или без, выделения и очистки из реакционной смеси известными способами разделения и очистки, такими как концентрирование, концентрирование под вакуумом, кристаллизация, экстракция растворителем, повторное осаждение и хроматография.
[0438]
Способ получения 6

[0439]
где E, R2 и R3 имеют значение, определенное выше.
Стадия 11
На этой стадии получают карбоновокислотное соединение, представленное формулой (NN), путем гидролиза соединения, представленного формулой (MM).
[0440]
Гидролиз осуществляют с использованием основания или кислоты. Примеры оснований включают органические основания, такие как диэтиламин, диизопропиламин, трет-бутират калия, трет-бутират натрия, метоксид натрия, этоксид натрия, гексаметилдисилазид лития, гексаметилдисилазид натрия, гексаметилдисилазид калия и бутиллитий; и неорганические основания, такие как гидрокарбонат натрия, карбонат натрия, карбонат калия, карбонат цезия, гидроксид натрия, гидроксид калия, гидроксид лития и гидроксид кальция. Примеры кислоты включают хлористоводородную кислоту, серную кислоту, фосфорную кислоту и т.п.
[0441]
Реакционный растворитель конкретно не ограничивается, и можно использовать любой растворитель, который не оказывает отрицательного влияния на реакцию. Примеры растворителя включают углеводороды (например, бензол, толуол и ксилол), нитрилы (например, ацетонитрил), простые эфиры (например, диметоксиэтан, тетрагидрофуран и 1,4-диоксан), спирты (например, метанол, этанол и этиленгликоль), апротонные полярные растворители (например, диметилформамид, диметилацетамид, N-метилпирролидинон, диметилсульфоксид и гексаметилфосфорамид), воду и их смеси.
[0442]
Время реакции, как правило, находится в пределах 0,1-100 часов, предпочтительно 0,5-24 часа. Температура реакции находится в пределах от 0°C до температуры кипения растворителя, предпочтительно 0-160°C.
[0443]
Полученное таким образом соединение, представленное формулой (NN), можно подвергнуть следующей стадии после, или без, выделения и очистки из реакционной смеси известными способами разделения и очистки, такими как концентрирование, концентрирование под вакуумом, кристаллизация, экстракция растворителем, повторное осаждение и хроматография.
[0444]
Способ получения 7

[0445]
где A, R2 и X имеют значение, определенное выше.
Стадия 12
На этой стадии получают соединение, представленное формулой (RR), осуществляя реакцию амидирования с использованием соединения, представленного формулой (JJ), и соединения, представленного формулой (VII). Эту стадию осуществляют в присутствии подходящего агента конденсации или активирующего агента в качестве амидирующего реагента, с использованием соединения формулы (VII) в количестве обычно 0,5-10 моль, предпочтительно 1-3 моль, на моль соединения, представленного формулой (JJ).
[0446]
Реакционный растворитель конкретно не ограничивается, и можно использовать любой растворитель, который не оказывает отрицательного влияния на реакцию. Примеры растворителя включают изопропанол, трет-бутиловый спирт, толуол, бензол, метиленхлорид, хлороформ, тетрагидрофуран, 1,4-диоксан, диметилформамид, диметилацетамид, N-метилпирролидинон, диметилсульфоксид, ацетонитрил и их смеси.
[0447]
Температура реакции, как правило, находится в пределах от -78 до 200°C, предпочтительно от 0 до 100°C. Время реакции, как правило, находится в пределах от 5 минут до 7 дней, предпочтительно от 5 минут до 3 дней, более предпочтительно от 5 минут до 10 часов.
[0448]
Примеры агентов конденсации и активирующих агентов включают дифенилфосфорилазид, N,N'-дициклогексилкарбодиимид, бензотриазол-1-илокси-трисдиметиламинофосфониевую соль, 4-(4,6-диметокси-1,3,5-триазин-2-ил)-4-метилморфолиний хлорид, 1-этил-3-(3-диметиламинопропил)карбодиимид, комбинацию 1-этил-3-(3-диметиламинопропил)карбодиимида и 1-гидроксибензотриазола, 2-хлор-1,3-диметилимидазолиний хлорид, (диметиламино)-N,N-диметил(3H-[1,2,3]триазолo[4,5-b]пиридин-3-илокси)метаниминий гексафторфосфат, 1,1-карбонилдиимидазол, имид N-гидроксиянтарной кислоты и т.п.
[0449]
Кроме того, при необходимости можно добавить основание в ходе указанной выше реакции. Примеры оснований включают органические основания, такие как триэтиламин, диизопропилэтиламин, пиридин, лутидин, коллидин, 4-диметиламинопиридин, трет-бутират калия, трет-бутират натрия, метоксид натрия, этоксид натрия, гексаметилдисилазид лития, гексаметилдисилазид натрия, гексаметилдисилазид калия, диазабициклоундецен, диазабициклононен и бутиллитий; и неорганические основания, такие как гидрокарбонат натрия, карбонат натрия, карбонат калия, карбонат цезия, гидроксид натрия и гидрид натрия. Количество добавляемого основания, как правило, составляет 1-100 моль, предпочтительно 1-10 моль, на моль соединения, представленного формулой (JJ).
[0450]
После завершения реакции можно добавить основание, такое как раствор гидроксида натрия, для осуществления последующей обработки.
[0451]
Полученное таким образом соединение, представленное формулой (RR), можно выделить и очистить известными способами разделения и очистки, такими как концентрирование, концентрирование под вакуумом, кристаллизация, экстракция растворителем, повторное осаждение и хроматография.
[0452]
Способ получения 8

[0453]
где L1 представляет собой удаляемую группу, и A, R2 и X имеют значение, определенное выше.
Стадия 13
На этой стадии получают соединение, представленное формулой (RR), путем взаимодействия соединения, представленного формулой (HH), в присутствии соединения (VII) в атмосфере оксида углерода с использованием, например, переходного металла и, необязательно, основания в растворителе, который не оказывает отрицательного влияния на реакцию.
[0454]
На этой стадии давление оксида углерода как правило, составляет 1 атм - 20 атм, предпочтительно 1 атм - 10 атм.
[0455]
Примеры катализаторов на основе переходных металлов, используемых на этой стадии, включают палладиевые катализаторы (например, ацетат палладия, трис(дибензилиденацетон)дипалладий, бис(трифенилфосфин)палладий(II) дихлорид, комплекс 1,1'-бис(дифенилфосфино)ферроцен-палладий(II) дихлорид-дихлорметан и т.д.). При необходимости добавляют лиганд (например, трифенилфосфин, xantphos, три-трет-бутилфосфин и т.д.). Количество катализатора на основе переходного металла варьируется в зависимости от типа катализатора. Например, количество используемого катализатора на основе переходного металла, как правило, составляет 0,0001-1 моль, предпочтительно 0,001-0,5 моль, на моль соединения, представленного формулой (HH). Количество используемого лиганда как правило, составляет 0,000 1-4 моль, предпочтительно 0,01-2 моль, на моль соединения, представленного формулой (HH).
[0456]
Кроме того, при необходимости можно добавить основание в ходе указанной выше реакции. Примеры оснований включают органические основания, такие как триэтиламин, диизопропилэтиламин, пиридин, лутидин, коллидин, 4-диметиламинопиридин, N-метилморфолин, трет-бутират калия, трет-бутират натрия, метоксид натрия, этоксид натрия, гексаметилдисилазид лития, гексаметилдисилазид натрия, 1,8-диазабицикло[5.4.0]ундец-7-ен, гексаметилдисилазид калия и бутиллитий; и неорганические основания, такие как гидрокарбонат натрия, карбонат натрия, карбонат калия, карбонат цезия, гидроксид натрия и гидрид натрия. Количество основания, которое используют, как правило, составляет 0,1-50 моль, предпочтительно 1-20 моль, на моль соединения, представленного формулой (HH).
[0457]
Реакционный растворитель конкретно не ограничивается, и можно использовать любой растворитель, который не оказывает отрицательного влияния на реакцию. Примеры растворителя включают углеводороды (например, бензол, толуол и ксилол), нитрилы (например, ацетонитрил), простые эфиры (например, диметоксиэтан, тетрагидрофуран и 1,4-диоксан), спирты (например, метанол и этанол), апротонные полярные растворители (например, диметилформамид, диметилацетамид, N-метилпирролидинон, диметилсульфоксид и гексаметилфосфорамид), воду и их смеси. Время реакции, как правило, находится в пределах 0,1-100 часов, предпочтительно 0,5-24 часа. Температура реакции находится в пределах 0°C-250°C, предпочтительно 0-200°C.
[0458]
Полученное таким образом соединение, представленное формулой (RR), можно выделить и очистить известными способами разделения и очистки, такими как концентрирование, концентрирование под вакуумом, кристаллизация, экстракция растворителем, повторное осаждение и хроматография.
[0459]
Способ получения 9

[0460]
где A, Z и R2 имеют значение, определенное выше.
На этой стадии получают соединение, представленное формулой (TT) из соединения, представленного формулой (OO), с использованием подходящего галогенированного реагента.
[0461]
Эту стадию, как правило, осуществляют с использованием галогенированного реагента в количестве обычно 1-10 моль, предпочтительно 1-5 моль, на моль соединения, представленного формулой (OO).
[0462]
Примеры галогенирующих реагентов включают 1-хлорметил-4-фтор-1,4-диазониабицикло[2.2.2]октан бис(тетрафторборат), N-иодсукцинимид, N-бромсукцинимид, N-хлорсукцинимид, иод, бром и т.п. Реакционный растворитель конкретно не ограничивается, и можно использовать любой растворитель, который не оказывает отрицательного влияния на реакцию. Примеры растворителя включают углеводороды (например, бензол, толуол и ксилол), нитрилы (например, ацетонитрил), простые эфиры (например, диметоксиэтан, тетрагидрофуран и 1,4-диоксан), апротонные полярные растворители (например, диметилформамид, диметилацетамид, N-метилпирролидинон, диметилсульфоксид и гексаметилфосфорамид), хлороформ, дихлорметан, тетрахлорид углерода и их смеси.
[0463]
Примеры галогена, представленного как Z, включают фтор, хлор, бром, иод и т.п.
[0464]
Температура реакции, как правило, находится в пределах от -78 до 200°C, предпочтительно от -10 до 50°C. Время реакции, как правило, находится в пределах от 5 минут до 6 дней, предпочтительно от 10 минут до 3 дней.
[0465]
Полученное таким образом соединение, представленное формулой (TT) можно выделить и очистить известными способами разделения и очистки, такими как концентрирование, концентрирование под вакуумом, кристаллизация, экстракция растворителем, повторное осаждение и хроматография.
[0466]
Способ получения 10

[0467]
где A, R2 и R3 имеют значение, определенное выше.
На этой стадии получают соединение, представленное формулой (UU), подвергая соединение, представленное формулой (PP), реакции сочетания с боратным производным, производным борной кислоты, производным олова, ацетиленовым производным, солью щелочного металла или солью щелочно-земельного металла, содержащими R3, с использованием, например, переходного металла и, необязательно, основания в растворителе, который не оказывает отрицательного влияния на реакцию.
[0468]
Количество используемого боратного производного, производного борной кислоты, производного олова, ацетиленового производного, соли щелочного металла, соли щелочно-земельного металла, алкоксида, или тиоалкоксида, который содержит R3, как правило, составляет 1-100 моль, предпочтительно 1-20 моль. Примеры катализаторов на основе переходных металлов, используемых на этой стадии, включают палладиевые катализаторы (например, ацетат палладия, тетракис(трифенилфосфин)палладий, трис(бензилиденацетон)дипалладий, бис(трифенилфосфин)палладий(II) дихлорид, комплекс 1,1'-бис(дифенилфосфино)ферроцен-палладий(II) дихлорид-дихлорметан и т.д.). При необходимости добавляют лиганд (например, трифенилфосфин, xantphos, 2-дициклогексилфосфино-2',4',6'-триизопропилбифенил, 2-дициклогексилфосфино-2',6'-диметоксибифенил, трициклогексилфосфин, три-трет-бутилфосфин и т.д.). При необходимости можно использовать медный катализатор. Примеры медных катализаторов включают иодид меди, бромид меди и хлорид меди. Количество катализатора на основе переходного металла варьируется в зависимости от типа катализатора. Например, количество используемого катализатора на основе переходного металла, как правило, составляет 0,0001-1 моль, предпочтительно 0,001-0,5 моль, на моль соединения, представленного формулой (PP). Можно использовать катализаторы на основе переходных металлов, или, при необходимости, их можно использовать в комбинации. Количество используемого лиганда как правило, составляет 0,0001-4 моль, предпочтительно 0,01-2 моль, на моль соединения, представленного формулой (PP).
[0469]
Кроме того, при необходимости можно добавить основание в ходе указанной выше реакции. Примеры оснований включают органические основания, такие как триэтиламин, диизопропилэтиламин, диизопропиламин, пиридин, лутидин, коллидин, 4-диметиламинопиридин, N-метилморфолин, трет-бутират калия, трет-бутират натрия, метоксид натрия, этоксид натрия, гексаметилдисилазид лития, гексаметилдисилазид натрия, гексаметилдисилазид калия и бутиллитий; и неорганические основания, такие как гидрокарбонат натрия, карбонат натрия, карбонат калия, карбонат цезия, фосфат калия, гидроксид натрия и гидрид натрия. Количество основания, которое используют, как правило, составляет 0,1-50 моль, предпочтительно 1-20 моль, на моль соединения, представленного формулой (PP).
[0470]
Реакционный растворитель конкретно не ограничивается, и можно использовать любой растворитель, который не оказывает отрицательного влияния на реакцию. Примеры растворителя включают углеводороды (например, бензол, толуол и ксилол), нитрилы (например, ацетонитрил), простые эфиры (например, диметоксиэтан, тетрагидрофуран и 1,4-диоксан), спирты (например, метанол, этанол, этиленгликоль и изопропанол), апротонные полярные растворители (например, диметилформамид, диметилацетамид, N-метилпирролидинон, диметилсульфоксид и гексаметилфосфорамид), воду и их смеси.
[0471]
Время реакции находится в пределах 0,1-100 часов, предпочтительно 0,5-48 часов. Температура реакции находится в пределах от 0°C до температуры кипения растворителя, предпочтительно 0-160°C.
[0472]
Полученное таким образом соединение, представленное формулой (UU), можно подвергнуть следующей стадии после, или без, выделения и очистки из реакционной смеси известными способами разделения и очистки, такими как концентрирование, концентрирование под вакуумом, кристаллизация, экстракция растворителем, повторное осаждение и хроматография.
[0473]
Когда соединения по настоящему изобретению имеют изомеры, такие как оптические изомеры, стереоизомеры, региоизомеры и ротационные изомеры, смеси любого из изомеров включены в объем соединений по настоящему изобретению. Например, когда соединения по настоящему изобретению имеют оптические изомеры, оптический изомер, выделенный из рацемической смеси, также включен в объем соединений по настоящему изобретению. Каждый из таких изомеров может быть получен в виде единственного соединения известными способами синтеза и разделения (например, концентрация, экстракция растворителем, колоночная хроматография, перекристаллизация и т.д.).
[0474]
Соединения или соли по настоящему изобретению могут находиться в форме кристаллов. Монокристаллы и полиморфные смеси включены в объем соединений или их солей по настоящему изобретению. Такие кристаллы могут быть получены кристаллизацией в соответствии со способом кристаллизации, известным per se в данной области. Соединения или соли по настоящему изобретению могут быть в форме сольватов (например, гидратов) или в несольватированной форме. Любая из таких форм включена в объем соединений или их солей по настоящему изобретению. Соединения, меченные изотопом (например, 2H, 3H, 13C, 14C, 35S, 125I и т.д.), также включены в объем соединений или их солей по настоящему изобретению.
[0475]
Пролекарства соединений или их солей по настоящему изобретению относятся к соединениям, которые могут преобразовываться в соединения или их соли по настоящему изобретению посредством реакции с ферментом, желудочной кислотой и т.п. в физиологических условиях in vivo, то есть, соединения, которые могут преобразовываться в соединения или их соли по настоящему изобретению путем ферментативного окисления, восстановления, гидролиза или т.п.; или соединения, которые могут быть преобразовываться в соединения или их соли по настоящему изобретению путем гидролиза под действием желудочной кислоты или т.п. Кроме того, пролекарства соединений или их солей по настоящему изобретению могут представлять собой соединения, которые могут преобразовываться в соединения или их соли по настоящему изобретению в физиологических условиях, как описано в "Iyakuhin no Kaihatsu [Development of Pharmaceuticals])," Vol. 7, Molecular Design, опубликованном в 1990 году компанией Hirokawa Shoten Co., стр. 163-198.
[0476]
Соли соединений по настоящему изобретению относятся к обычным солям, используемым в области органической химии. Примеры таких солей включают соли присоединения оснований к карбоксильной группе, когда соединение содержит карбоксильную группу, и кислотно-аддитивные соли, образованные с аминогруппой или основной гетероциклической группой, когда соединение содержит аминогруппу или основную гетероциклическую группу.
[0477]
Примеры кислотно-аддитивных солей включают соли неорганических кислот, такие как гидрохлорид, сульфат, нитрат, фосфат и перхлорат; соли органических кислот, такие как ацетат, формиат, малеат, фумарат, тартрат, цитрат, аскорбат и трифторацетат; и сульфонаты, такие как метансульфонат, изетионат, бензолсульфонат и п-толуолсульфонат.
[0478]
В настоящем описании, ʺRETʺ означает RET (реаранжированную во время трансфекции) тирозинкиназу и включает RET человека и RET отличного от человека млекопитающего, предпочтительно RET человека. Кроме того, термин ʺRETʺ включает изоформы. Кроме того, что касается RET, известно, что существует три типа белков, т.е. RET9, RET43 и RET51, из-за разницы в сплайсинге карбокси конца (Trends в Genetics, 2006, Vol. 22, pp. 627-636). Помимо этих трех типов белков, ʺRETʺ включает все варианты сплайсинга, которые в настоящее время известны и будут известны в будущем, при условии, что они содержат АТФ-связывающий сайт RET.
[0479]
Примеры человеческого RET включают полипептид, включающий аминокислотную последовательность, кодируемую GenBank Accession number: NM_020975, и полипептид, включающий аминокислотную последовательность, кодируемую GenBank Accession number: NM_020630.
[0480]
Кроме того, примеры гена, который кодирует RET, включают полинуклеотид, включающий последовательность оснований 191-3535 последовательности оснований, представленной GenBank Accession number: NM_020975, полинуклеотид, включающий последовательность оснований 191-3409 последовательности оснований, представленной GenBank Accession number: NM_020630, и т.п.
[0481]
Кроме того, RET по настоящему изобретению может иметь транслокации и мутации (включая точечные мутации, делеционные мутации и инсерционные мутации), при условии, что он обладает киназной активностью RET.
[0482]
Транслокации RET в настоящем изобретении включают случай где весь RET белок, или его часть, обладающий RET киназной активностью, слит с целым или частью другого белка (например, KIF5B белка, CCDC6 белка, NCOA4 белка или TRIM33 белка) с образованием слитого белка, и предпочтительно CCDC6-RET и KIF5B-RET (CCDC6-RET означает, что часть CCDC6 белка и часть RET белка слиты в этом порядке; то же относится к описанному ниже) (Drilon A, Cancer Discov., 3 (6), pp. 630-635 (2013)).
[0483]
Мутации RET в настоящем изобретении могут представлять собой точечные мутации, делеционные мутации или инсерционные мутации, при условии, что RET обладает RET киназной активностью. Мутации RET включают полипептиды, обладающие RET киназной активностью и включающие аминокислотную последовательность, мутированную путем замены, делеции или добавления одной или нескольких аминокислот, или путем комбинации вышеперечисленных, в аминокислотной последовательности RET, например, аминокислотной последовательности, кодируемой GenBank Accession number: NM_020975, или аминокислотной последовательности, кодируемой GenBank Accession number: NM_020630.
[0484]
Области для мутации не ограничиваются, при условии, что RET обладает RET киназной активностью. АТФ-связывающая область или область-gatekeeper может быть мутирована. Область остатка, смежного с шарнирной областью, с которой связан АТФ протеинкиназы, называется gatekeeper областью. Аминокислотный остаток этой области сильно влияет на пространственную конфигурацию АТФ-связывающего кармана. Аминокислота gatekeeper области в RET представляет собой 804-й валин аминокислотной последовательности, кодируемой GenBank accession number: NM_020975 или GenBank accession number: NM_020630. Были сообщения о RET V804L мутации и RET V804M мутации у пациентов с раком щитовидной железы (Bolino A, Oncogene, 10, pp. 2415-2419, (1995) и т.д.).
[0485]
Известно также, что длительное введение ингибитора протеинкиназы часто приводит к спонтанным мутациям в аминокислотных остатках gatekeeper области (Kobayashi S, N Engl J Med., 352 (8): pp. 786-792, (2005) и т.д.). Поэтому длительное введение ингибитора RET может привести к мутации в 804-м валине в gatekeeper области (Cranston AN, Cancer Res., 66 (20): pp. 10179-10187, (2006)). Мутации в gatekeeper области приобретают резистентность к ингибитору и поэтому могут вызывать серьезные терапевтические проблемы. Действительно, научные исследования показали, что клетки, полученные путем введения мутации V804L или мутации V804M в RET, демонстрируют резистентность к Вандетанибу, который является лекарственным средством, обладающим RET-ингибирующей активностью (Carlomagno F, Oncogene, 23, pp. 6056-6063, (2004)).
[0486]
Эти резистентные мутантные RET предпочтительно представляют собой RET, имеющие V804L, V804M, V804E, Y806C, Y806E, Y806S, Y806H или Y806N, в которых 804-й валин, который является gatekeeper областью, или его соседний 806-й тирозин заменен другой аминокислотой; и более предпочтительно RET, имеющий V804L или V804M, в котором 804-й валин заменен лейцином или метионином.
[0487]
Кроме того, RET по настоящему изобретению может иметь мутации в областях, отличных от gatekeeper области, при условии, что он обладает RET киназной активностью. Примеры включают, но не ограничиваются этим, RET, содержащий C618S, C620R, C630R, C634R, C634W, C634Y, C691S, E768D, A883F, A883S, E884V, S891A, S891L или M918T (например, C618S представляет собой RET, в котором 618-й цистеин заменен серином; то же относится к описанному ниже) в аминокислотной последовательности, кодируемой GenBank accession number: NM_020975 или GenBank accession number: NM_020630. Предпочтительным является C634W.
[0488]
Присутствие мутаций RET можно определить путем анализа последовательности гена RET или последовательности мРНК, которая представляет собой генный транскрипт RET. Примеры анализа последовательности включают дидезоксинуклеотидный метод с обрывом цепи (Sanger et al. (1977) Proc. Natl. Acad. Sci. USA 74:5463) и т.п. Последовательность также можно анализировать с использованием подходящего ДНК секвенатора.
[0489]
Присутствие мутаций RET также можно анализировать, например, с использованием in situ гибридизации, нозерн-блот анализа, ДНК-микрочипа, ОТ-ПЦР, SSCP-ПЦР (ПЦР с анализом конформационного полиморфизма одноцепочечных фрагментов ДНК) или т.п. Эти анализы можно осуществить стандартным способом (Clinical Cancer Research, 8, 457-463, 2002).
[0490]
Кроме того, присутствие мутаций RET можно анализировать, например, иммунохимическим методом (например, иммуногистохимический метод, метод иммунопреципитации, вестерн-блоттинг, метод проточной цитометрии, ELISA, радиоиммуноанализ, или т.п.). Эти анализы можно осуществить стандартным способом.
[0491]
Для анализа присутствия RET мутаций методом ПЦР можно сконструировать последовательность праймера стандартным способом. Последовательность праймера можно сконструировать с использованием, например, Primer Expression (Perkin-Elmer Applied Biosystems).
[0492]
Благодаря их превосходной активности ингибирования RET, соединения или соли по настоящему изобретению полезны в качестве фармацевтических препаратов для профилактики и лечения связанных с RET заболеваний. Примеры ʺсвязанных с RET заболеванийʺ включают заболевания, число случаев которых можно уменьшить, и симптомы которых можно устранить, облегчить и/или полностью вылечить путем устранения, подавления и/или ингибирования функции RET. Примеры таких заболеваний включают, но не ограничиваются этим, злокачественные опухоли и т.д. Предпочтительные примеры злокачественных опухолей включают злокачественные опухоли с усиленной активацией RET, более предпочтительно немелкоклеточный рак легкого, рак молочной железы, колоректальный рак или рак щитовидной железы с сверхактивированным RET.
[0493]
Фраза ʺповышенная активация RETʺ указывает на то, что активированное состояние RET усиливается из-за, например, транслокаций и мутаций (включая точечные мутации, делеционные мутации и инсерционные мутации) RET гена и чрезмерной экспрессии (включая повышенное число копий RET гена, сверхэкспрессию матричной РНК RET, увеличение RET белков и конститутивно активированные RET белки).
[0494]
Тип рака и опухоли, подлежащих лечению соединениями или их солями по настоящему изобретению, конкретно не ограничивается. Примеры включают эпителиальные раковые заболевания (рак органов дыхания, рак органов пищеварения, рак репродуктивных органов, рак органов секреции и т.д.), саркомы, гемопоэтические опухоли, опухоли центральной нервной системы и опухоли периферических нервов.
[0495]
Конкретные примеры типа рака включают рак головы и шеи, рак щитовидной железы, рак пищевода, рак желудка, рак двенадцатиперстной кишки, рак печени, рак желчных путей (желчного пузыря, холангиокарцинома и т.д.), рак поджелудочной железы, колоректальный рак (рак толстой кишки, рак прямой кишки и т.д.), рак легких (немелкоклеточный рак легкого, мелкоклеточный рак легкого, мезотелиома и т. д.), рак молочной железы, рак яичников, рак матки (рак шейки матки, рак эндометрия и т.д.), рак почек, рак почечных лоханок и уретры, рак мочевого пузыря, рак предстательной железы, тестикулярную опухоль, лейкоз, злокачественную лимфому, множественную миелому, остеосаркому, саркому мягких тканей, рак кожи, опухоль головного мозга, опухоль надпочечников, нейробластому и т.п. Рак, являющийся мишенью, предпочтительно представляет собой рак легкого (немелкоклеточный рак легкого, мелкоклеточный рак легкого, мезотелиома и т.д.), колоректальный рак (рак толстой кишки, рак прямой кишки и т.д.), рак щитовидной железы, рак молочной железы, опухоль головного мозга и лейкоз; и особенно предпочтительно немелкоклеточный рак легкого, рак молочной железы, колоректальный рак и рак щитовидной железы.
[0496]
Когда соединения или их соли по настоящему изобретению используют в качестве фармацевтических препаратов, при необходимости может быть добавлен фармацевтический носитель, с образованием, таким образом, подходящей лекарственной формы в соответствии с профилактическими и лечебными целями. Примеры лекарственной формы включают пероральные препараты, инъекции, суппозитории, мази, пластыри и т.п.; предпочтительно пероральные препараты. Такие лекарственные формы могут быть образованы способами, обычно известными специалистам в данной области.
[0497]
В качестве фармацевтического носителя, различные обычные органические или неорганические вещества-носители, используемые в качестве веществ для получения препаратов, можно добавить в смесь в качестве наполнителя, связующего, разрыхлителя, смазывающего вещества или агента покрытия в твердых препаратах; или в качестве растворителя, солюбилизирующего агента, суспендирующего агента, изотонического агента, регулятора рН/буфера или успокаивающего средства в жидких препаратах. Кроме того, при необходимости можно использовать добавки для фармацевтических препаратов, такие как антисептики, антиоксиданты, красители, подсластители и стабилизаторы.
[0498]
При получении твердого препарата для перорального введения к соединению по настоящему изобретению, необязательно, можно добавить эксципиент, связующее, разрыхлитель, смазывающее вещество, краситель, подсластитель и т.п.; и полученную смесь можно сформулировать в виде таблеток, таблеток с покрытием, гранул, порошков, капсул и т.д., в соответствии с обычным способом.
[0499]
При получении препарата для инъекций, при необходимости, к соединению по настоящему изобретению можно добавить регулятор рН, буфер, стабилизатор, изотонический агент, местный анестетик и т.п.; и полученную смесь можно сформулировать в виде препарата для подкожных, внутримышечных и внутривенных инъекций в соответствии с обычным способом.
[0500]
Количество соединения по настоящему изобретению, которое должно быть включено в каждую из таких единичных лекарственных форм, зависит от состояния пациента, которому вводят соединение, лекарственной формы и т.д. Как правило, в случае перорального средства, инъекции и суппозитория, количество соединения по настоящему изобретению предпочтительно составляет от 0,05 до 1000 мг, от 0,01 до 500 мг и от 1 до 1000 мг, соответственно, на единичную стандартную лекарственную форму.
[0501]
Суточная доза лекарственного средства в такой дозированной форме зависит от состояния, массы тела, возраста, пола и т.д. пациента и не может быть обобщена. Например, суточная доза соединения по настоящему изобретению для взрослого (масса тела 50 кг) может составлять обычно от 0,05 до 5000 мг, и предпочтительно от 0,1 до 1000 мг; и предпочтительно ее вводят в виде одной дозы или в двух-трех дробных доз в день.
[0502]
Соединения или соли по настоящему изобретению обладают превосходной ингибиторной активностью в отношении RET и полезны в качестве противоопухолевых средств. Описанный в настоящей заявке RET предпочтительно представляет собой RET в состоянии ʺповышенной активацииʺ, как описано выше. Кроме того, в предпочтительном варианте осуществления соединения или соли по настоящему изобретению обладают высокой селективностью в отношении RET и имеют преимущественно небольшое количество побочных эффектов, вызываемых ингибированием нецелевых мишеней, таких как Src, Lck, EGFR и Aurora B. Aurora B является киназой, участвующей в клеточном делении. Клиническое испытание средства, обладающего активностью ингибирования Aurora B, показало, что часто возникают побочные эффекты на систему клеток крови, такие как нейтропения (Непатентная литература 20). Кроме того, известно, что ингибиторы, специфические в отношении EGFR, совместно вызывают побочные эффекты, такие как кожные заболевания или желудочно-кишечные расстройства (Непатентная литература 21).
[0503]
В предпочтительном варианте осуществления соединения или их соли по настоящему изобретению также обладают превосходными эффектом ингибирования клеточного роста на клетки, изначально имеющие RET-резистентные мутации, где существующие ингибиторы RET с меньшей долей вероятности будут работать. Кроме того, соединения или соли по настоящему изобретению обладают превосходными эффектом ингибирования клеточного роста на клетки с приобретенными RET-резистентными мутациями из-за длительного введения ингибиторов RET и обеспечивают возможность длительного введения.
[0504]
Кроме того, в предпочтительном варианте осуществления соединения или соли по настоящему изобретению обладают превосходной стабильностью в микросомах печени. Поэтому можно ожидать отличной экспозиции препарата в кровотоке, и нет никакого беспокойства по поводу ингибирования Cyp.
[0505]
Кроме того, в предпочтительном варианте осуществления соединения или соли по настоящему изобретению обладают превосходной пероральной абсорбцией. Поэтому наблюдается достаточная концентрация в плазме, и соединения или соли по настоящему изобретению полезны в качестве пероральных фармацевтических препаратов.
Примеры
[0506]
Далее настоящее изобретение описано более подробно со ссылкой на Примеры. Однако настоящее изобретение не ограничивается этими примерами.
[0507]
В примерах использовали коммерчески доступные реагенты, если не указано иное. Для колоночной хроматографии на силикагеле использовали следующие колонки: Purif-Pack (зарегистрированная торговая марка) SI, изготовитель Moritex Corp.; KP-Sil (зарегистрированная торговая марка) заполненная диоксидом кремния колонка, изготовитель Biotage; HP-Sil (зарегистрированная торговая марка) заполненная диоксидом кремния колонка, изготовитель Biotage; или HP-Sphere (зарегистрированная торговая марка) заполненная диоксидом кремния колонка изготовитель Biotage. Для колоночной хроматографии на щелочном силикагеле использовали Purif-Pack (зарегистрированная торговая марка) NH, изготовитель Moritex Corp., или KP-NH (зарегистрированная торговая марка) заполненную колонку, изготовитель Biotage. Для препаративной тонкослойной хроматографии использовали Kieselgel TM 60F 254, Art. 5744, изготовитель Merck, или пластину с NH2 силикагелем 60F254, изготовитель Wako. ЯМР спектры измеряли с использованием спектрометра модели AL400 (400 МГц; изготовитель JEOL), Mercury 400 (400 МГц; изготовитель Agilent Technologies, Inc.) или спектрометра модели Inova 400 (400 МГц; изготовитель Agilent Technologies, Inc.), снабженного OMNMR зондом (Protasis). Измерение осуществляли с использованием тетраметилсилана в качестве внутреннего стандарта, когда тетраметилсилан содержался в дейтерированном растворителе; в иных случаях ЯМР растворитель использовали в качестве внутреннего стандарта. Все δ значения представлены в м.д. Реакцию в условиях микроволнового нагрева осуществляли с использованием Initiator изготовитель Biotage.
[0508]
ЖХМС спектры измеряли с использованием Acquity SQD (квадрупольный), изготовитель Waters Corporation, в следующих условиях.
Колонка: Acquity UPLC (зарегистрированная торговая марка) BEH C18, 2,1×50 мм, 1,7 мкм (изготовитель Waters Corporation)
МС детекция: ESI положительный режим
УФ детекция: 254 и 210 нм
Скорость потока в колонке: 0,5 мл/мин
Подвижная фаза: Вода/ацетонитрил (0,1% муравьиной кислоты)
Объем вводимой пробы: 1 мкл градиент
Очистку препаративной обращенно-фазовой ВЭЖХ осуществляли с использованием препаративной системы разделения, доступной от Gilson, Inc.
Колонка: CombiPrep Pro C18, 50×30 мм дл.диам., S-5 мкм (изготовитель YMC)
УФ детекция: 254 нм
Скорость потока в колонке: 40 мл/мин
Подвижная фаза: Вода/ацетонитрил (0,1% муравьиной кислоты)
Объем вводимой пробы: 0,1-1 мл
[0509]
Далее представлены используемые аббревиатуры и их значения.
s: синглет
d: дублет
t: триплет
q: квартет
dd: двойной дублет
dt: двойной триплет
td: тройной дублет
tt: тройной триплет
ddd: двойной дублет дублетов
ddt: двойной триплет дублетов
dtd: двойной дублет триплетов
tdd: тройной дублет дублетов
m: мультиплет
br: широкий
brs: широкий синглет
brd: широкий дублет
CDI: карбонилдиимидазол
DMSO-d6: дейтерированный диметилсульфоксид
CDCl3: дейтерированный хлороформ
CD3OD: дейтерированный метанол
THF: тетрагидрофуран
DMF: N,N-диметилформамид
DMA: N,N-диметилацетамид
NMP: 1-метил-2-пирролидинон
DMSO: диметилсульфоксид
HATU: (диметиламино)-N,N-диметил(3H-[1,2,3]триазолo[4,5-b]пиридин-3-илокси)метаниминий гексафторфосфат
DIAD: диизопропилазодикарбоксилат
DIPEA: диизопропилэтиламин
DME: 1,2-диметоксиэтан
[0510]
Ссылочный пример 1: Синтез 4-амино-1-циклопентил-1H-пиразолo[3,4-d]пиримидин-3-карбоновой кислоты
Стадия 1: Синтез 1-циклопентил-3-иод-1H-пиразолo[3,4-d]пиримидин-4-амина
[0511]

1-циклопентил-3-иод-1H-пиразолo[3,4-d]пиримидин-4-амин
[0512]
Суспензию 3,0 г 3-иод-1H-пиразолo[3,4-d]пиримидин-4-амина, синтезированн в соответствии с процедурой, описанной в международной публикации № WO2007/126841, 3,4 г иодциклопентана и 4,8 г карбоната калия в 30 мл DMF нагревали до 80°C и перемешивали в течение 18 часов. После охлаждения полученной смеси до комнатной температуры добавляли 200 мл воды с последующим фильтрованием осадка. Осадок промывали водой и сушили, таким образом получая 3,7 г указанного в заголовке соединения.
Физические свойства: m/z[M+H]+ 330,1.
[0513]
Стадия 2: Синтез 4-амино-1-циклопентил-1H-пиразолo[3,4-d]пиримидин-3-карбоновой кислоты
[0514]
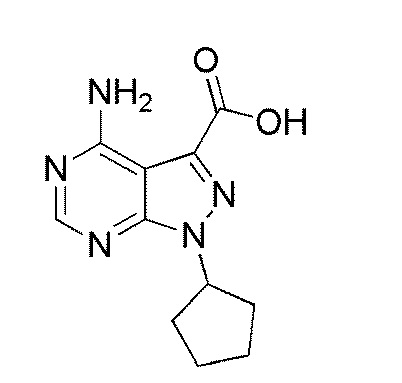
4-амино-1-циклопентил-1H-пиразолo[3,4-d]пиримидин-3-карбоновая кислота
[0515]
21 г 1-циклопентил-3-иод-1H-пиразолo[3,4-d]пиримидин-4-амина, полученного на стадии 1, 42 мл 2-диэтиламиноэтанола и 2,24 г Pd(PPh3)2Cl2 растворяли в 120 мл ΝΜΡ и атмосферу внутри системы заменяли оксидом углерода, с последующим нагреванием до 120°C. После перемешивания в течение 2 часов полученную смесь охлаждали до комнатной температуры и добавляли 50 мл метанола. Затем добавляли 19 мл 5N водного раствора гидроксида натрия и перемешивали в течение 30 минут. После добавления воды водный слой промывали этилацетатом и промытый водный слой доводили хлористоводородной кислотой до pH 3. Полученный осадок собирали фильтрованием, промывали водой и сушили, таким образом получая 9,8 г указанного в заголовке соединения.
Физические свойства: m/z[M+H]+ 248,3.
[0516]
Ссылочный пример 2: Синтез 1-(адамантан-2-ил)-4-амино-1H-пиразолo[3,4-d]пиримидин-3-карбоновой кислоты
Стадия 1: Синтез 1-(адамантан-2-ил)-3-иод-1H-пиразолo[3,4-d]пиримидин-4-амина
[0517]

1-(адамантан-2-ил)-3-иод-1H-пиразолo[3,4-d]пиримидин-4-амин
[0518]
2,3 мл диизопропилазодикарбоксилата добавляли к раствору 1,5 г 3-иод-1H-пиразолo[3,4-d]пиримидин-4-амина, 2,6 г 2-адамантанола и 3,0 г трифенилфосфина в 30 мл THF при комнатной температуре, с последующим перемешиванием в течение ночи. После концентрирования остаток очищали хроматографией на силикагеле (гексан → гексан/этилацетат=1/1), таким образом получая 1,87 г указанного в заголовке соединения.
Физические свойства: m/z[M+H]+ 396,2.
[0519]
Стадия 2: Синтез 1-(адамантан-2-ил)-4-амино-1H-пиразолo[3,4-d]пиримидин-3-карбоновой кислоты
[0520]

1-(адамантан-2-ил)-4-амино-1H-пиразолo[3,4-d]пиримидин-3-карбоновая кислота
[0521]
1,8 г 1-(адамантан-2-ил)-3-иод-1H-пиразолo[3,4-d]пиримидин-4-амина, полученного на стадии 1, 3,0 мл 2-диэтиламиноэтанола и 160 мг Pd(PPh3)2Cl2 растворяли в 5 мл ΝΜΡ и атмосферу внутри системы заменяли оксидом углерода, с последующим нагреванием до 120°C. После перемешивания в течение 2 часов полученную смесь охлаждали до комнатной температуры и добавляли 5 мл метанола. Затем добавляли 2,3 мл 5N водного раствора гидроксида натрия и перемешивали в течение 30 минут. После добавления воды водный слой промывали этилацетатом и промытый водный слой доводили хлористоводородной кислотой до pH 3. Полученный осадок собирали фильтрованием, промывали водой и сушили, таким образом получая 0,3 г указанного в заголовке соединения.
Физические свойства: m/z[M+H]+ 314,2.
[0522]
Ссылочный пример 3: Синтез 4-амино-1-(трет-бутил)-1H-пиразолo[3,4-d]пиримидин-3-карбоновой кислоты
Стадия 1: Синтез метил 4-амино-1-(трет-бутил)-1H-пиразолo[3,4-d]пиримидин-3-карбоксилата
[0523]

метил 4-амино-1-(трет-бутил)-1H-пиразолo[3,4-d]пиримидин-3-карбоксилат
[0524]
3,33 г триэтиламина и 1,35 г комплекса 1,1'-бис(дифенилфосфино)ферроцен-палладий(II) дихлорид-дихлорметан добавляли к суспензии 4,45 г 3-бром-(1-трет-бутил)-1H-пиразолo[3,4-d]пиримидин-4-амина в 45 мл метанола. Смесь перемешивали в атмосфере оксида углерода в автоклаве при 0,5 МПа и при 100°C в течение 3 часов. После охлаждения реакционный раствор концентрировали, растворяли в хлороформе, промывали водой и сушили над безводным сульфатом натрия. Высушенную смесь затем фильтровали и концентрировали. Полученный остаток очищали колоночной хроматографией на силикагеле (гексан-этилацетат) и концентрировали. Полученный осадок суспендировали и промывали смесью гексан-этилацетат. После фильтрования осадок сушили при 70°C при пониженном давлении, таким образом получая 2,37 г указанного в заголовке соединения.
Физические свойства: m/z[M+H]+ 250,1.
[0525]
Стадия 2: Синтез 4-амино-1-(трет-бутил)-1H-пиразолo[3,4-d]пиримидин-3-карбоновой кислоты
[0526]

4-амино-1-(трет-бутил)-1H-пиразолo[3,4-d]пиримидин-3-карбоновая кислота
[0527]
2,23 г метил-4-амино-1-(трет-бутил)-1H-пиразолo[3,4-d]пиримидин-3-карбоксилата, полученного на стадии 1, суспендировали в 33 мл метанола и добавляли 3,58 мл 5M водного раствора гидроксида натрия. Смесь перемешивали при нагревании с обратным холодильником в течение 30 минут. После охлаждения реакционный раствор нейтрализовали водным раствором 5M хлористоводородной кислоты и разбавляли водой, собирая полученный осадок фильтрованием. Полученный осадок сушили при 60°C при пониженном давлении, таким образом получая 2,05 г указанного в заголовке соединения.
Физические свойства: m/z[M+H]+ 236,3.
[0528]
Ссылочный пример 4: Синтез 4-амино-7-изопропил-7H-пирроло[2,3-d]пиримидин-5-карбоновой кислоты
Стадия 1: Синтез 4-хлор-5-иод-7-изопропил-7H-пирроло[2,3-d]пиримидина
[0529]
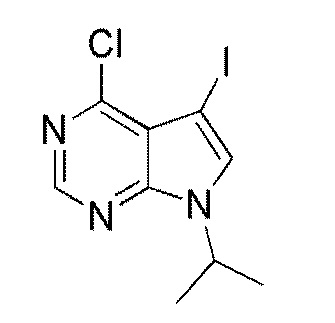
4-хлор-5-иод-7-изопропил-7H-пирроло[2,3-d]пиримидин
[0530]
5,79 мл диизопропилазодикарбоксилата добавляли к раствору 4,0 г 4-хлор-5-иод-7H-пирроло[2,3-d]пиримидина, 2,58 г пропан-2-ола и 7,51 г трифенилфосфина в 30 мл тетрагидрофурана. Реакционный раствор перемешивали в течение 18 часов. Реакционный раствор концентрировали и полученный остаток очищали хроматографией на силикагеле (гексан → гексан/этилацетат=1/1), таким образом получая 4,0 г указанного в заголовке соединения.
Физические свойства: m/z[M+H]+ 322,0.
[0531]
Стадия 2: Синтез 5-иод-7-изопропил-7H-пирроло[2,3-d]пиримидин-4-амина
[0532]

5-иод-7-изопропил-7H-пирроло[2,3-d]пиримидин-4-амин
[0533]
30 мл 1,2-диметоксиэтана и 30 мл 28% водного раствора аммиака добавляли к 3 г 4-хлор-5-иод-7-изопропил-7H-пирроло[2,3-d]пиримидина, полученного на стадии 1, и смесь перемешивали в нержавеющей стойкой к давлению трубке при 115°C в течение 18 часов. К реакционному раствору добавляли 300 мл воды и полученный осадок промывали водой, таким образом получая 2,0 г указанного в заголовке соединения.
Физические свойства: m/z[M+H]+ 303,1.
[0534]
Стадия 3: Синтез 4-амино-7-изопропил-7H-пирроло[2,3-d]пиримидин-5-карбоновой кислоты
[0535]

4-амино-7-изопропил-7H-пирроло[2,3-d]пиримидин-5-карбоновая кислота
[0536]
3,8 г 5-иод-7-изопропил-7H-пирроло[2,3-d]пиримидин-4-амина, полученного на стадии 2, 8,3 мл 2-диэтиламиноэтанола и 0,44 г Pd(PPh3)2Cl2 растворяли в 10 мл NMP и атмосферу внутри системы заменяли оксидом углерода, с последующим нагреванием до 120°C. После перемешивания в течение 2 часов реакционную смесь охлаждали до комнатной температуры и добавляли 7 мл метанола. Затем добавляли 3,5 мл 5N водного раствора гидроксида натрия и смесь перемешивали в течение 30 минут. После добавления воды водный слой промывали этилацетатом и доводили хлористоводородной кислотой до pH 3, с последующим фильтрованием полученного осадка. Отфильтрованный осадок промывали водой и сушили, таким образом получая 0,670 г указанного в заголовке соединения.
Физические свойства: m/z[M+H]+ 221,2.
[0537]
Ссылочный пример 5: Синтез 4-амино-7-(трет-бутил)-7H-пирроло[2,3-d]пиримидин-5-карбоновой кислоты
Стадия 1: Синтез 7-(трет-бутил)-4-хлор-7H-пирроло[2,3-d]пиримидина
[0538]
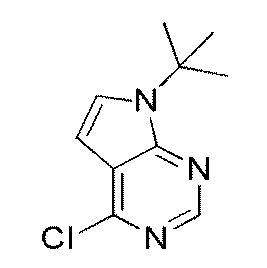
7-(трет-бутил)-4-хлор-7H-пирроло[2,3-d]пиримидин
[0539]
Смешанный раствор 29,3 г 2-(4,6-дихлорпиримидин-5-ил)ацетальдегида, 13,4 г трет-бутиламина и 29,7 г N,N-диизопропилэтиламина в 200 мл этанола перемешивали при нагревании с обратным холодильником в течение 2 часов. После охлаждения реакционную смесь концентрировали. Остаток разбавляли этилацетатом, промывали водой и затем промывали насыщенным водным раствором хлорида натрия. Полученный органический слой сушили над безводным сульфатом натрия, фильтровали и концентрировали. Полученный остаток очищали хроматографией на силикагеле, таким образом получая 21,5 г указанного в заголовке соединения.
Физические свойства: m/z[M+H]+ 210,0.
[0540]
Стадия 2: Синтез 7-(трет-бутил)-4-хлор-5-иод-7H-пирроло[2,3-d]пиримидина
[0541]

7-(трет-бутил)-4-хлор-5-иод-7H-пирроло[2,3-d]пиримидин
[0542]
46,7 г N-иодсукцинимида добавляли к раствору 36 г 7-(трет-бутил)-4-хлор-7H-пирроло[2,3-d]пиримидина, полученного на стадии 1, в 360 мл DMF и смесь перемешивали при комнатной температуре в течение 3 дней. Смесь разбавляли этилацетатом и промывали водой 3 раза, с последующей промывкой насыщенным водным раствором хлорида натрия. Полученный органический слой сушили над безводным сульфатом натрия, фильтровали и концентрировали. Полученный осадок суспендировали и промывали смесью гексан-этилацетат и фильтровали, с последующей сушкой при пониженном давлении, таким образом получая 45,5 г указанного в заголовке соединения.
Физические свойства: m/z[M+H]+ 335,9.
[0543]
Стадия 3: Синтез 7-(трет-бутил)-5-иод-7H-пирроло[2,3-d]пиримидин-4-амина
[0544]

7-(трет-бутил)-5-иод-7H-пирроло[2,3-d]пиримидин-4-амин
[0545]
Суспензию 52 г 7-(трет-бутил)-4-хлор-5-иод-7H-пирроло[2,3-d]пиримидина, полученного на стадии 2, в 180 мл THF и 180 мл 28% водного раствора аммиака перемешивали при 120°C в течение 14 часов в автоклаве. После охлаждения смесь разбавляли водой, собирая полученный осадок фильтрованием, с последующей сушкой при 60°C при пониженном давлении, таким образом получая 52 г указанного в заголовке соединения.
Физические свойства: m/z[M+H]+ 317,3.
[0546]
Стадия 4: Синтез метил 4-амино-7-(трет-бутил)-7H-пирроло[2,3-d]пиримидин-5-карбоксилата
[0547]

метил 4-амино-7-(трет-бутил)-7H-пирроло[2,3-d]пиримидин-5-карбоксилат
[0548]
Суспензию 15 г 7-(трет-бутил)-5-иод-7H-пирроло[2,3-d]пиримидин-4-амина, полученного на стадии 3, 1,94 г комплекса 1,1'-бис(дифенилфосфино)ферроцен-палладий(II) дихлорид-дихлорметан и 13,2 мл триэтиламина в 150 мл метанола перемешивали в атмосфере оксида углерода в автоклаве при 100°C и 0,45 МПа в течение 1,5 часов. После охлаждения реакционный раствор концентрировали и очищали хроматографией на силикагеле (гексан-этилацетат). После концентрирования полученный осадок суспендировали и промывали смесью гексан-этилацетат, фильтровали и сушили при пониженном давлении, таким образом получая 9,70 г указанного в заголовке соединения.
Физические свойства: m/z[M+H]+ 249,3.
[0549]
Стадия 5: 4-амино-7-(трет-бутил)-7H-пирроло[2,3-d]пиримидин-5-карбоновая кислота
[0550]
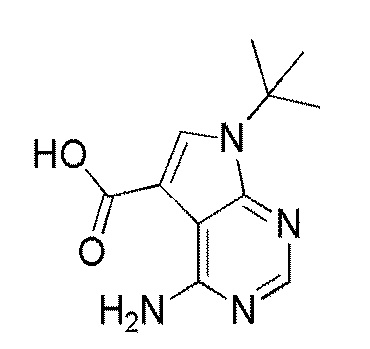
4-амино-7-(трет-бутил)-7H-пирроло[2,3-d]пиримидин-5-карбоновая кислота
[0551]
23,4 мл 5M водного раствора гидроксида натрия добавляли к суспензии 9,70 г метил-4-амино-7-(трет-бутил)-7H-пирроло[2,3-d]пиримидин-5-карбоксилата, полученного на стадии 4, в 97 мл метанола. Смесь перемешивали при нагревании с обратным холодильником в течение 2 часов. После охлаждения смесь нейтрализовали водным раствором 5M хлористоводородной кислоты. Полученный таким образом осадок разбавляли водой, фильтровали и сушили при 60°C при пониженном давлении, таким образом получая 8,0 г указанного в заголовке соединения.
Физические свойства: m/z[M+H]+ 235,2.
[0552]
Ссылочный пример 6: Синтез 7-(1-(фторметил)циклопропил)-5-иод-7H-пирроло[2,3-d]пиримидин-4-амина
Стадия 1: Синтез 4-хлор-7-(1-(фторметил)циклопропил)-7H-пирроло[2,3-d]пиримидина
[0553]
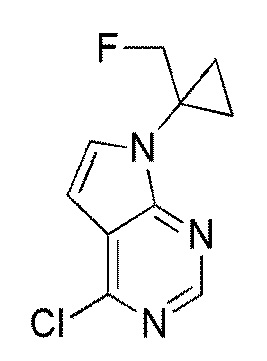
4-хлор-7-(1-(фторметил)циклопропил)-7H-пирроло[2,3-d]пиримидин
[0554]
Раствор смеси 1,3 г 2-(4,6-дихлорпиримидин-5-ил)ацетальдегида, 1,0 г 1-(фторметил)циклопропанамин гидрохлорида и 4,7 мл N,N-диизопропилэтиламина в 10 мл этанола перемешивали при нагревании с обратным холодильником в течение 2 часов. После охлаждения реакционный раствор концентрировали и полученный остаток очищали хроматографией на силикагеле (гексан → гексан/этилацетат=1/1), таким образом получая 1,1 г указанного в заголовке соединения.
Физические свойства: m/z[M+H]+ 226,0.
[0555]
Стадия 2: Синтез 4-хлор-7-(1-(фторметил)циклопропил)-5-иод-7H-пирроло[2,3-d]пиримидина
[0556]

4-хлор-7-(1-(фторметил)циклопропил)-5-иод-7H-пирроло[2,3-d]пиримидин
[0557]
1,2 г N-иодсукцинимида добавляли к раствору 1,0 г 4-хлор-7-(1-(фторметил)циклопропил)-7H-пирроло[2,3-d]пиримидина, полученного на стадии 1, в 10 мл DMF и смесь перемешивали при комнатной температуре в течение 18 часов. 10% водный раствор тиосульфата натрия добавляли к реакционному раствору для остановки реакции и реакционный раствор разбавляли водой. Полученный осадок промывали водой, фильтровали и сушили при пониженном давлении, таким образом получая 2,5 г указанного в заголовке соединения.
Физические свойства: m/z[M+H]+ 351,9.
[0558]
Стадия 3: Синтез 7-(1-(фторметил)циклопропил)-5-иод-7H-пирроло[2,3-d]пиримидин-4-амина
[0559]

7-(1-(фторметил)циклопропил)-5-иод-7H-пирроло[2,3-d]пиримидин-4-амин
[0560]
10 мл 1,2-диметоксиэтана и 10 мл 28% водного раствора аммиака добавляли к 2,5 г 4-хлор-7-(1-(фторметил)циклопропил)-5-иод-7H-пирроло[2,3-d]пиримидина, полученного на стадии 2, и смесь перемешивали в нержавеющей стойкой к давлению трубке при 115°C в течение 18 часов. К реакционному раствору добавляли 200 мл воды и полученный осадок промывали водой, таким образом получая 1,9 г указанного в заголовке соединения.
Физические свойства: m/z[M+H]+ 333,0.
[0561]
Ссылочный пример 7: Синтез 7-(трет-бутил)-5-иод-6-метил-7H-пирроло[2,3-d]пиримидин-4-амина
Стадия 1: Синтез 1-(4,6-дихлорпиримидин-5-ил)пропан-2-ола
[0562]

1-(4,6-дихлорпиримидин-5-ил)пропан-2-ол
[0563]
1 г 2-(4,6-дихлорпиримидин-5-ил)ацетальдегида растворяли в 20 мл THF и реактор охлаждали до -78°C. Медленно добавляли по каплям 4,36 мл раствора метилмагнийбромида в диэтиловом эфире (3 моль/л). При этой же температуре смесь перемешивали в течение 1 часа и медленно добавляли насыщенный водный раствор хлорида аммония для остановки реакции. Реакционную смесь перемешивали при комнатной температуре в течение 10 минут и помещали в делительную воронку, с последующим экстрагированием этилацетатом. Органический слой промывали насыщенным водным раствором хлорида натрия и затем сушили над сульфатом натрия для удаления растворителя. Остаток очищали хроматографией на щелочном силикагеле (гексан/этилацетат=1/0 → 3/1), таким образом получая 446 мг указанного в заголовке соединения.
Физические свойства: m/z[M+H]+ 207,0.
[0564]
Стадия 2: Синтез 1-(4,6-дихлорпиримидин-5-ил)пропан-2-она
[0565]

1-(4,6-дихлорпиримидин-5-ил)пропан-2-он
[0566]
246 мг 1-(4,6-дихлорпиримидин-5-ил)пропан-2-ола, полученного на стадии 1, растворяли в 2,5 мл дихлорметана и добавляли 1,0 г реагента Десса-Мартина, с последующим перемешиванием при комнатной температуре в течение 1 часа. К реакционному раствору добавляли 10% водный раствор тиосульфата натрия и насыщенный водный раствор бикарбоната натрия и смесь снова перемешивали в течение 30 минут. Реакционную смесь экстрагировали хлороформом и органический слой промывали водой и насыщенным водным раствором хлорида натрия, с последующим добавлением сульфата натрия для сушки. После удаления растворителя остаток очищали хроматографией на силикагеле (гексан/этилацетат=1/0 → 3/1), таким образом получая 198 мг указанного в заголовке соединения.
Физические свойства: m/z[M+H]+ 205,0.
[0567]
Стадия 3: Синтез 1-(4-(трет-бутиламино)-6-хлорпиримидин-5-ил)пропан-2-она
[0568]

1-(4-(трет-бутиламино)-6-хлорпиримидин-5-ил)пропан-2-он
[0569]
198 мг 1-(4,6-дихлорпиримидин-5-ил)пропан-2-она, полученного на стадии 2, 122 мкл трет-бутиламина и 252 мкл диизопропилэтиламина растворяли в 2 мл этанола и раствор перемешивали при 90°C в течение ночи.
Реакционную смесь концентрировали, затем остаток очищали хроматографией на силикагеле (гексан/этилацетат=1/0 → 3/1), таким образом получая 64 мг указанного в заголовке соединения.
Физические свойства: m/z[M+H]+ 242,1.
[0570]
Стадия 4: Синтез 7-(трет-бутил)-4-хлор-6-метил-7H-пирроло[2,3-d]пиримидина
[0571]

7-(трет-бутил)-4-хлор-6-метил-7H-пирроло[2,3-d]пиримидин
[0572]
64 мг 1-(4-(трет-бутиламино)-6-хлорпиримидин-5-ил)пропан-2-она, полученного на стадии 3, и 42 мкл уксусной кислоты растворяли в 5,5 мл этанола и взаимодействие раствора осуществляли в микроволновом реакторе при 120°C в течение 1 часа. После удаления растворителя остаток очищали хроматографией на силикагеле (гексан/этилацетат =1/0 → 4/1), таким образом получая 54 мг указанного в заголовке соединения.
Физические свойства: m/z[M+H]+ 224,1.
[0573]
Стадия 5: Синтез 7-(трет-бутил)-4-хлор-5-иод-6-метил-7H-пирроло[2,3-d]пиримидина
[0574]

7-(трет-бутил)-4-хлор-5-иод-6-метил-7H-пирроло[2,3-d]пиримидин
[0575]
7-(трет-бутил)-4-хлор-6-метил-7H-пирроло[2,3-d]пиримидин, полученный на стадии 4, растворяли в 1,5 мл DMF. Добавляли 64 мг N-иодсукцинимида и смесь перемешивали при комнатной температуре в течение ночи. К реакционному раствору добавляли 10% водный раствор тиосульфата натрия для остановки реакции, с последующим экстрагированием этилацетатом. Органический слой промывали водой и насыщенным водным раствором хлорида натрия и сушили над сульфатом натрия, с последующим удалением растворителя. Остаток очищали хроматографией на силикагеле (гексан/этилацетат=1/0 → 4/1), таким образом получая 69 мг указанного в заголовке соединения.
Физические свойства: m/z[M+H]+ 349,9.
[0576]
Стадия 6: 7-(трет-бутил)-5-иод-6-метил-7H-пирроло[2,3-d]пиримидин-4-амин
[0577]

7-(трет-бутил)-5-иод-6-метил-7H-пирроло[2,3-d]пиримидин-4-амин
[0578]
60 мг 7-(трет-бутил)-4-хлор-5-иод-6-метил-7H-пирроло[2,3-d]пиримидина, полученного на стадии 5, подвергали взаимодействию с 600 мкл DME и 600 мкл водного раствора аммиака в стойкой к давлению трубке при 115°C в течение 12 часов. После охлаждения воздухом к реакционной смеси добавляли воду. Полученный осадок фильтровали и сушили, таким образом получая 45 мг указанного в заголовке соединения.
Физические свойства: m/z[M+H]+ 331,0.
[0579]
Ссылочный пример 8: Синтез 3-фтор-4-(метоксиметил)анилина
[0580]

3-фтор-4-(метоксиметил)анилин
[0581]
5,71 г карбоната цезия и 3,64 мл иодметана добавляли к смешанному раствору 1,0 г (2-фтор-4-нитрофенил)метанолу в 20 мл THF и DMF (1:1) и смесь перемешивали в течение 18 часов. Полученную смесь растворяли в этилацетате, промывали водой и сушили над безводным сульфатом магния, с последующим фильтрованием и концентрированием. Полученный остаток очищали колоночной хроматографией на силикагеле (гексан-этилацетат) и реакционную смесь концентрировали, таким образом получая 0,76 г 2-фтор-1-(метоксиметил)-4-нитробензола. Затем 0,76 г 2-фтор-1-(метоксиметил)-4-нитробензола растворяли в 20 мл этанола и добавляли 400 мг палладия/углерод (палладий 10%), с последующим перемешиванием в атмосфере водорода в течение 18 часов. Нерастворимое вещество фильтровали и фильтрат концентрировали. Полученный остаток концентрировали, таким образом получая 567 мг указанного в заголовке соединения.
Физические свойства: m/z[M+H]+ 156,0.
[0582]
Ссылочный пример 9: Синтез метил 4-амино-6-бром-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксилата
[0583]
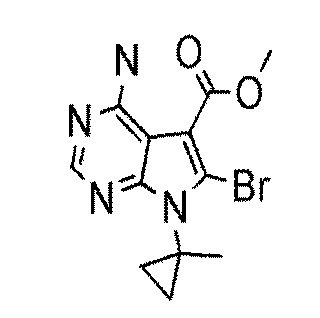
4-амино-6-бром-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксилат
[0584]
Стадия 1: Синтез 4-амино-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбонитрила
2,5 мл DMF добавляли к 234 мг 5-иод-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-4-амина, синтезированного в соответствии с процедурой стадий 1-3 в Ссылочном примере 5, с использованием 1-метилциклопропанамин гидрохлорида вместо трет-бутиламина, 131 мг цианида цинка и 86 мг тетракис(трифенилфосфин)палладия. Взаимодействие смеси осуществляли в микроволновом реакторе при 150°C в течение 20 минут. Нерастворимое вещество удаляли с использованием Целита и фильтрат распределяли между смесью толуол/этилацетат и водой. Органический слой промывали водой и насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия, с последующим фильтрованием и концентрировани. К остатку добавляли гексан и этилацетат и смесь перемешивали при комнатной температуре. Образовавшийся осадок фильтровали, таким образом получая 100 мг указанного в заголовке соединения.
Физические свойства: m/z[M+H]+ 214,2.
[0585]
Стадия 2: Синтез 4-амино-6-бром-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбонитрила
100 мг 4-амино-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбонитрила, полученного на стадии 1, растворяли в 5 мл DMF и добавляли 167 мг N-бромсукцинимида при охлаждении льдом, с последующим перемешиванием в течение 3,5 часов. Реакционный раствор распределяли между этилацетатом и 10% водным раствором тиосульфата натрия. Органический слой промывали водой и насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия, с последующим фильтрованием и концентрированием. Добавляли гексан и этилацетат для осаждения остатка и смесь перемешивали при охлаждении льдом. Образовавшийся осадок фильтровали, таким образом получая 96 мг указанного в заголовке соединения.
Физические свойства: m/z[M+H]+ 294,0.
[0586]
Стадия 3: 4-амино-6-бром-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид
96 мг 4-амино-6-бром-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбонитрила, полученного на стадии 2, растворяли в 3 мл DMSO и добавляли 90 мкл 4N водного раствора NaOH и 41 мкл 30% пероксида водорода, с последующим перемешиванием при комнатной температуре в течение 1 часа. Реакционный раствор распределяли между этилацетатом и 10% водным раствором тиосульфата натрия. Органический слой промывали водой и насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия, с последующим фильтрованием и концентрированием, таким образом получая 76 мг указанного в заголовке соединения.
Физические свойства: m/z[M+H]+ 312,0.
[0587]
Стадия 4: Синтез метил 4-амино-6-бром-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксилата
118 мг 4-амино-6-бром-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида, полученного на стадии 3, растворяли в 2 мл THF и добавляли 23 мг диметиламинопиридина и 415 мг ди-трте-бутилдикарбоната, с последующим перемешиванием при комнатной температуре в течение ночи. После удаления THF добавляли 2 мл метанола и затем добавляли 53 мг карбоната калия, с последующим перемешиванием при комнатной температуре в течение 7 часов. Реакционный раствор нейтрализовали 2N раствором HCl и распределяли между этилацетатом и водой. Органический слой промывали водой и насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия, с последующим фильтрованием и концентрированием. К остатку добавляли 2 мл дихлорметана и 2 мл трифторуксусной кислоты и смесь перемешивали при комнатной температуре в течение 1 часа. После удаления трифторуксусной кислоты остаток распределяли между этилацетатом и насыщенным водным раствором бикарбоната натрия. Органический слой промывали водой и насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия, с последующим фильтрованием и концентрированием. Остаток очищали на колонке с силикагелем (этилацетат/метанол=1/0 → 8/1), таким образом получая 50 мг указанного в заголовке соединения.
Физические свойства: m/z[M+H]+ 327,0.
[0588]
Ссылочный пример 10: Синтез метил 4-амино-1-(4,4-дифторциклогексил)-1H-пиразолo[3,4-d]пиримидин-3-карбоксилата
Стадия 1: Синтез 1-(4,4-дифторциклогексил)-3-иод-1H-пиразолo[3,4-d]пиримидин-4-амина
[0589]

1-(4,4-дифторциклогексил)-3-иод-1H-пиразолo[3,4-d]пиримидин-4-амин
[0590]
1,6 мл диизопропилазодикарбоксилата добавляли к раствору 1,6 г 3-иод-1H-пиразолo[3,4-d]пиримидин-4-амина, 1,0 г 4,4-дифторциклогексанола и 2,1 г трифенилфосфина в 50 мл THF при комнатной температуре и смесь перемешивали в течение ночи. После концентрирования смесь суспендировали и промывали метанолом, с последующим фильтрованием. Полученный осадок сушили при 60°C при пониженном давлении, таким образом получая 1,5 г указанного в заголовке соединения.
Физические свойства: m/z[M+H]+ 380,2.
[0591]
Стадия 2: Синтез метил 4-амино-1-(4,4-дифторциклогексил)-1H-пиразолo[3,4-d]пиримидин-3-карбоксилата
[0592]

метил 4-амино-1-(4,4-дифторциклогексил)-1H-пиразолo[3,4-d]пиримидин-3-карбоксилат
[0593]
Смешанный раствор 1,5 г 1-(4,4-дифторциклогексил)-3-иод-1H-пиразолo[3,4-d]пиримидин-4-амина, полученного на стадии 1, 330 мг комплекса 1,1'-бис(дифенилфосфино)ферроцен-палладий (II) дихлорид-дихлорметан и 3 мл N,N-диизопропиламина в 30 мл метанола перемешивали в атмосфере оксида углерода в автоклаве при 0,45 МПа при 100°C в течение 2 часов. После охлаждения реакционную смесь концентрировали и очищали колоночной хроматографией на силикагеле (проявляющий растворитель: гексан-этилацетат). Полученный неочищенный продукт снова очищали на щелочном силикагеле (проявляющий растворитель: гексан-этилацетат) и концентрировали. Полученный осадок суспендировали и промывали смесью гексан-этилацетат, фильтровали и сушили при пониженном давлении, таким образом получая 650 мг указанного в заголовке соединения.
Физические свойства: m/z[M+H]+ 312,1.
[0594]
Ссылочный пример 11: Синтез 4-амино-6-бром-N-(3-фтор-4-(метоксиметил)фенил)-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
[0595]

4-амино-6-бром-N-(3-фтор-4-(метоксиметил)фенил)-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид
[0596]
270 мг 4-амино-N-(3-фтор-4-(метоксиметил)фенил)-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида, показанного в Примере 48, растворяли в 4 мл DMF. Добавляли 195 мг N-бромсукцинимида при охлаждении льдом, с последующим перемешиванием при комнатной температуре в течение 15 минут. К реакционному раствору добавляли 10% водный раствор тиосульфата натрия и образовавшийся осадок фильтровали, с последующей промывкой водой, таким образом получая 245 мг указанного в заголовке соединения.
Физические свойства: m/z [M+H]+ 450,1.
[0597]
Ссылочный пример 12: Синтез 4-амино-1-фенил-1H-пиразолo[3,4-d]пиримидин-3-карбоновой кислоты
[0598]

4-амино-1-фенил-1H-пиразолo[3,4-d]пиримидин-3-карбоновая кислота
[0599]
300 мг 1-фенил-1H-пиразолo[3,4-d]пиримидин-4-амина и 453 мг брома растворяли в 2 мл воды и раствор перемешивали при комнатной температуре в течение 1 часа, с последующим перемешиванием при 100°C в течение 1 часа. К реакционному раствору добавляли водный раствор бикарбоната натрия и образовавшийся осадок собирали фильтрованием. Затем осадок промывали водой, таким образом получая 370 мг 3-бром-1-фенил-1H-пиразолo[3,4-d]пиримидин-4-амина. Раствор 370 мг полученного 3-бром-1-фенил-1H-пиразолo[3,4-d]пиримидин-4-амина, 104 мг комплекса 1,1'-бис(дифенилфосфино)ферроцен-палладий(II) дихлорид-дихлорметан и 500 мкл триэтиламина в 5 мл метанола перемешивали в атмосфере оксида углерода в автоклаве при 120°C в течение 4 часов. После охлаждения растворитель концентрировали при пониженном давлении. Полученный остаток растворяли в 5 мл метанола и добавляли 0,4 мл 5M водного раствора гидроксида натрия, с последующим перемешиванием при 50°C в течение 2 часов. После охлаждения растворитель концентрировали при пониженном давлении. Остаток нейтрализовали водным раствором 5M хлористоводородной кислоты и полученный таким образом осадок разбавляли водой, фильтровали и сушили при пониженном давлении, таким образом получая указанное в заголовке соединение.
Физические свойства: m/z [M+H]+ 256,1.
[0600]
Пример 1: Синтез 4-амино-1-циклопентил-N-(4-(метоксиметил)фенил)-1H-пиразолo[3,4-d]пиримидин-3-карбоксамида
30 мг 4-амино-1-циклопентил-1H-пиразолo[3,4-d]пиримидин-3-карбоновой кислоты, полученной на стадии 2 Ссылочного примера 1, 20 мг 4-(метоксиметил)анилина и 55 мг HATU растворяли в 1 мл DMF и добавляли 62 мкл диизопропилэтиламина. После перемешивания при комнатной температуре в течение 18 часов, к реакционному раствору добавляли воду, с последующим экстрагированием этилацетатом. Органический слой промывали водой и сушили над безводным сульфатом магния, с последующим концентрированием органического раствора при пониженном давлении. Остаток очищали хроматографией на силикагеле (хлороформ → хлороформ/метанол=10/1), таким образом получая 36 мг указанного в заголовке соединения.
[0601]
Пример 2: 4-амино-7-(трет-бутил)-N-(4-(метоксиметил)фенил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид
2,43 г HATU добавляли к раствору 1,00 г 4-амино-7-(трет-бутил)-7H-пирроло[2,3-d]пиримидин-5-карбоновой кислоты, полученной на стадии 5 Ссылочного примера 5, 878 мг 4-(метоксиметил)анилина и 2,23 мл N,N-диизопропилэтиламина в 20 мл DMF при комнатной температуре. Смесь перемешивали при комнатной температуре в течение ночи и добавляли водный раствор гидроксида натрия, с последующим экстрагированием хлороформом. Полученный органический слой сушили над безводным сульфатом натрия, фильтровали, концентрировали и очищали хроматографией на силикагеле. После концентрирования полученный осадок суспендировали и промывали метанолом, с последующим фильтрованием и сушкой при пониженном давлении, таким образом получая 1,12 г указанного в заголовке соединения.
[0602]
Пример 3: Синтез 4-амино-1-циклопентил-N-(4-((метилтио)метил)фенил)-1H-пиразолo[3,4-d]пиримидин-3-карбоксамида
В соответствии с процедурой синтеза Примера 1, используя 4-((метилтио)метил)анилин вместо 4-(метоксиметил)анилина, получали указанное в заголовке соединение (65%).
[0603]
Пример 4: Синтез 4-амино-1-циклопентил-N-(4-(фуран-2-ил)фенил)-1H-пиразолo[3,4-d]пиримидин-3-карбоксамида
В соответствии с процедурой синтеза Примера 1, используя 4-(фуран-2-ил)анилин вместо 4-(метоксиметил)анилина, получали указанное в заголовке соединение (60%).
[0604]
Пример 5: Синтез 4-амино-1-циклопентил-N-(4-(фениламино)фенил)-1H-пиразолo[3,4-d]пиримидин-3-карбоксамида
В соответствии с процедурой синтеза Примера 1, используя N-фенилбензол-1,4-диамин вместо 4-(метоксиметил)анилина, получали указанное в заголовке соединение (78%).
[0605]
Пример 6: Синтез 4-амино-1-циклопентил-N-(2-метокси-2,3-дигидро-1H-инден-5-ил)-1H-пиразолo[3,4-d]пиримидин-3-карбоксамида
В соответствии с процедурой синтеза Примера 1, используя 2-метокси-2,3-дигидро-1H-инден-5-амин вместо 4-(метоксиметил)анилина, получали указанное в заголовке соединение (88%).
[0606]
Пример 7: Синтез 4-амино-1-циклопентил-N-(4-винилфенил)-1H-пиразолo[3,4-d]пиримидин-3-карбоксамида
В соответствии с процедурой синтеза Примера 1, используя 4-виниланилин вместо 4-(метоксиметил)анилина, получали указанное в заголовке соединение (69%).
[0607]
Пример 8: Синтез 4-амино-N-(3-хлорфенил)-1-циклопентил-1H-пиразолo[3,4-d]пиримидин-3-карбоксамида
В соответствии с процедурой синтеза Примера 1, используя 3-хлоранилин вместо 4-(метоксиметил)анилина, получали указанное в заголовке соединение (61%).
[0608]
Пример 9: Синтез (E)-4-амино-1-циклопентил-N-(4-(проп-1-ен-1-ил)фенил)-1H-пиразолo[3,4-d]пиримидин-3-карбоксамида
В соответствии с процедурой синтеза Примера 1, используя (E)-4-(проп-1-ен-1-ил)анилин вместо 4-(метоксиметил)анилина, получали указанное в заголовке соединение (82%).
[0609]
Пример 10: Синтез 4-амино-1-(циклопент-3-ен-1-ил)-N-(4-(метоксиметил)фенил)-1H-пиразолo[3,4-d]пиримидин-3-карбоксамида
В соответствии с процедурами синтеза стадий 1 и 2 в Ссылочном примере 1, используя циклопент-3-ен-1-илметансульфонат вместо иодциклопентана, получали 4-амино-1-(циклопент-3-ен-1-ил)-1H-пиразолo[3,4-d]пиримидин-3-карбоновую кислоту.
В соответствии с процедурой Примера 1, используя 4-амино-1-(циклопент-3-ен-1-ил)-1H-пиразолo[3,4-d]пиримидин-3-карбоновую кислоту вместо 4-амино-1-циклопентил-1H-пиразолo[3,4-d]пиримидин-3-карбоновой кислоты, получали указанное в заголовке соединение (70%).
[00610]
Пример 11: Синтез 4-амино-N-(4-(метоксиметил)фенил)-1-(3-метилциклопентил)-1H-пиразолo[3,4-d]пиримидин-3-карбоксамида
В соответствии с процедурами синтеза стадий 1 и 2 в Ссылочном примере 1, используя 3-метилциклопентилметансульфонат вместо иодциклопентана, получали 4-амино-1-(3-метилциклопентил)-1H-пиразолo[3,4-d]пиримидин-3-карбоновую кислоту.
Реакцию осуществляли в соответствии с процедурой Примера 1, используя 4-амино-1-(3-метилциклопентил)-1H-пиразолo[3,4-d]пиримидин-3-карбоновую кислоту вместо 4-амино-1-циклопентил-1H-пиразолo[3,4-d]пиримидин-3-карбоновой кислоты. Реакционный раствор очищали препаративной обращенно-фазовой ВЭЖХ и концентрировали. Полученный осадок суспендировали и промывали смесью гексан-этилацетат, фильтровали и сушили при пониженном давлении, таким образом получая указанное в заголовке соединение (55%).
[0611]
Пример 12: Синтез 4-амино-1-циклобутил-N-(4-(метоксиметил)фенил)-1H-пиразолo[3,4-d]пиримидин-3-карбоксамида
В соответствии с процедурами синтеза стадий 1 и 2 в Ссылочном примере 1, используя бромциклобутан вместо иодциклопентана, получали 4-амино-1-циклобутил-1H-пиразолo[3,4-d]пиримидин-3-карбоновую кислоту.
В соответствии с процедурой Примера 1, используя 4-амино-1-циклобутил-1H-пиразолo[3,4-d]пиримидин-3-карбоновую кислоту вместо 4-амино-1-циклопентил-1H-пиразолo[3,4-d]пиримидин-3-карбоновой кислоты, получали указанное в заголовке соединение (82%).
[0612]
Пример 13: Синтез 4-амино-1-циклобутил-N-(4-((метилтио)метил)фенил)-1H-пиразолo[3,4-d]пиримидин-3-карбоксамида
В соответствии с процедурой синтеза Примера 12, используя 4-((метилтио)метил)анилин вместо 4-(метоксиметил)анилина, получали указанное в заголовке соединение (65%).
[0613]
Пример 14: Синтез 4-амино-1-(3,3-диметилциклобутил)-N-(4-(метоксиметил)фенил)-1H-пиразолo[3,4-d]пиримидин-3-карбоксамида
В соответствии с процедурами синтеза стадий 1 и 2 в Ссылочном примере 1, используя 3-бром-1,1-диметил-циклобутан вместо иодциклопентана, получали 4-амино-1-(3,3-диметилциклобутил)-1H-пиразолo[3,4-d]пиримидин-3-карбоновую кислоту.
В соответствии с процедурой Примера 1, используя 4-амино-1-(3,3-диметилциклобутил)-1H-пиразолo[3,4-d]пиримидин-3-карбоновую кислоту вместо 4-амино-1-циклопентил-1H-пиразолo[3,4-d]пиримидин-3-карбоновой кислоты, получали указанное в заголовке соединение (73%).
[0614]
Пример 15: Синтез 4-амино-1-изопропил-N-(4-((метилтио)метил)фенил)-1H-пиразолo[3,4-d]пиримидин-3-карбоксамида
В соответствии с процедурами синтеза стадий 1 и 2 в Ссылочном примере 1, используя 2-бромпропан вместо иодциклопентана, получали 4-амино-1-изопропил-1H-пиразолo[3,4-d]пиримидин-3-карбоновую кислоту.
В соответствии с процедурой Примера 1, используя 4-амино-1-изопропил-1H-пиразолo[3,4-d]пиримидин-3-карбоновую кислоту вместо 4-амино-1-циклопентил-1H-пиразолo[3,4-d]пиримидин-3-карбоновой кислоты и используя 4-((метилтио)метил)анилин вместо 4-(метоксиметил)анилина, получали указанное в заголовке соединение (63%).
[0615]
Пример 16: Синтез 4-амино-N-(4-((метилтио)метил)фенил)-1-(пентан-3-ил)-1H-пиразолo[3,4-d]пиримидин-3-карбоксамида
В соответствии с процедурами синтеза стадий 1 и 2 в Ссылочном примере 1, используя 3-бромпентан вместо иодциклопентана, получали 4-амино-1-(пентан-3-ил)-1H-пиразолo[3,4-d]пиримидин-3-карбоновую кислоту.
В соответствии с процедурой Примера 1, используя 4-амино-1-(пентан-3-ил)-1H-пиразолo[3,4-d]пиримидин-3-карбоновую кислоту вместо 4-амино-1-циклопентил-1H-пиразолo[3,4-d]пиримидин-3-карбоновой кислоты и используя 4-((метилтио)метил)анилин вместо 4-(метоксиметил)анилина, получали указанное в заголовке соединение (65%).
[0616]
Пример 17: 4-амино-1-циклогексил-N-(4-(метоксиметил)фенил)-1H-пиразолo[3,4-d]пиримидин-3-карбоксамид
В соответствии с процедурами синтеза стадий 1 и 2 в Ссылочном примере 1, используя бромциклогексан вместо иодциклопентана, получали 4-амино-1-циклогексил-1H-пиразолo[3,4-d]пиримидин-3-карбоновую кислоту.
В соответствии с процедурой Примера 1, используя 4-амино-1-циклогексил-1H-пиразолo[3,4-d]пиримидин-3-карбоновую кислоту вместо 4-амино-1-циклопентил-1H-пиразолo[3,4-d]пиримидин-3-карбоновой кислоты, получали указанное в заголовке соединение (16%).
[0617]
Пример 18: Синтез 4-амино-1-циклогексил-N-(4-((метилтио)метил)фенил)-1H-пиразолo[3,4-d]пиримидин-3-карбоксамида
В соответствии с процедурой Примера 17, используя 4-((метилтио)метил)анилин вместо 4-(метоксиметил)анилина, получали указанное в заголовке соединение (85%).
[0618]
Пример 19: Синтез 1-(адамантан-2-ил)-4-амино-N-(4-(метоксиметил)фенил)-1H-пиразолo[3,4-d]пиримидин-3-карбоксамида
38 мг 1-(адамантан-2-ил)-4-амино-1H-пиразолo[3,4-d]пиримидин-3-карбоновой кислоты, полученной на стадии 2 Ссылочного примера 2, 20 мг 4-(метоксиметил)анилина и 55 мг HATU растворяли в 1 мл DMF и добавляли 62 мкл диизопропилэтиламина. Смесь перемешивали при комнатной температуре в течение 18 часов и к реакционному раствору добавляли воду, с последующим экстрагированием этилацетатом. Органический слой промывали водой и сушили над безводным сульфатом магния, с последующим концентрированием органического раствора при пониженном давлении. Остаток очищали хроматографией на силикагеле (хлороформ → хлороформ/метанол=10/1), таким образом получая 26 мг указанного в заголовке соединения.
[0619]
Пример 20: Синтез 4-амино-N-(4-(метоксиметил)фенил)-1-(транс-4-метилциклогексил)-1H-пиразолo[3,4-d]пиримидин-3-карбоксамида
В соответствии с процедурами синтеза стадий 1 и 2 в Ссылочном примере 2, используя цис-4-метилциклогексанол вместо 2-адамантанола, получали 4-амино-1-(транс-4-метилциклогексил)-1H-пиразолo[3,4-d]пиримидин-3-карбоновую кислоту.
В соответствии с процедурой Примера 19, используя 4-амино-1-(транс-4-метилциклогексил)-1H-пиразолo[3,4-d]пиримидин-3-карбоновую кислоту вместо 1-(адамантан-2-ил)-4-амино-1H-пиразолo[3,4-d]пиримидин-3-карбоновой кислоты, получали указанное в заголовке соединение (82%).
[0620]
Пример 21: Синтез 4-амино-1-(1-фторпропан-2-ил)-N-(4-(метоксиметил)фенил)-1H-пиразолo[3,4-d]пиримидин-3-карбоксамида
В соответствии с процедурами синтеза стадий 1 и 2 в Ссылочном примере 2, используя 1-фторпропан-2-ол вместо 2-адамантанола, получали 4-амино-1-(1-фторпропан-2-ил)-1H-пиразолo[3,4-d]пиримидин-3-карбоновую кислоту.
В соответствии с процедурой Примера 19, используя 4-амино-1-(1-фторпропан-2-ил)-1H-пиразолo[3,4-d]пиримидин-3-карбоновую кислоту вместо 1-(адамантан-2-ил)-4-амино-1H-пиразолo[3,4-d]пиримидин-3-карбоновой кислоты, получали указанное в заголовке соединение (58%).
[0621]
Пример 22: Синтез 4-амино-1-(трет-бутил)-N-(4-(метоксиметил)фенил)-1H-пиразолo[3,4-d]пиримидин-3-карбоксамида
121 мг HATU добавляли к раствору 50 мг 4-амино-1-(трет-бутил)-1H-пиразолo[3,4-d]пиримидин-3-карбоновой кислоты, полученной на стадии 2 Ссылочного примера 3, 34 мг 4-(метоксиметил)анилина и 0,11 мл N,N-диизопропилэтиламина в 1 мл DMF при комнатной температуре. После перемешивания при комнатной температуре в течение 1 часа смесь разбавляли этилацетатом и промывали водой, с последующей промывкой насыщенным водным раствором хлорида натрия. Полученный органический слой сушили над безводным сульфатом натрия, с последующим фильтрованием и концентрированием. Полученный осадок суспендировали и промывали метанолом, фильтровали и сушили при пониженном давлении, таким образом получая 65 мг указанного в заголовке соединения.
[0622]
Пример 23: 4-амино-1-(трет-бутил)-N-(4-((метилтио)метил)фенил)-1H-пиразолo[3,4-d]пиримидин-3-карбоксамид
В соответствии с процедурой Примера 22, используя 4-((метилтио)метил)анилин вместо 4-(метоксиметил)анилина, получали указанное в заголовке соединение (77%).
[0623]
Пример 24: Синтез 4-амино-7-изопропил-N-(4-(метоксиметил)фенил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
67 мг 4-амино-7-изопропил-7H-пирроло[2,3-d]пиримидин-5-карбоновой кислоты, полученной на стадии 3 Ссылочного примера 4, 50 мг 4-(метоксиметил)анилин и 138 мг HATU растворяли в 1 мл DMF и добавляли 158 мкл диизопропилэтиламина. После перемешивания при комнатной температуре в течение 5 часов к реакционному раствору добавляли воду, с последующим экстрагированием хлороформом. Органический слой промывали водой и сушили над безводным сульфатом магния. Органический раствор концентрировали при пониженном давлении. Остаток очищали хроматографией на силикагеле (хлороформ → хлороформ/метанол=10/1), таким образом получая 76 мг указанного в заголовке соединения.
[0624]
Пример 25: Синтез 4-амино-7-циклопентил-N-(4-(метоксиметил)фенил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурами синтеза стадий 1-3 в Ссылочном примере 4, используя циклопентанол вместо пропан-2-ола, получали 4-амино-7-циклопентил-7H-пирроло[2,3-d]пиримидин-5-карбоновую кислоту.
В соответствии с процедурой Примера 24, используя 4-амино-7-циклопентил-7H-пирроло[2,3-d]пиримидин-5-карбоновую кислоту вместо 4-амино-7-изопропил-7H-пирроло[2,3-d]пиримидин-5-карбоновой кислоты, получали указанное в заголовке соединение (69%).
[0625]
Пример 26: Синтез 4-амино-7-(1-фтор-2-метилпропан-2-ил)-N-(4-(метоксиметил)фенил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид
В соответствии с процедурами синтеза стадий 1-5 в Ссылочном примере 5, используя 1-фтор-2-метилпропан-2-амин гидрохлорид вместо трет-бутиламина, получали 4-амино-7-(1-фтор-2-метилпропан-2-ил)-7H-пирроло[2,3-d]пиримидин-5-карбоновую кислоту.
В соответствии с процедурой Примера 2, используя 4-амино-7-(1-фтор-2-метилпропан-2-ил)-7H-пирроло[2,3-d]пиримидин-5-карбоновую кислоту вместо 4-амино-7-(трет-бутил)-7H-пирроло[2,3-d]пиримидин-5-карбоновой кислоты, получали указанное в заголовке соединение (67%).
[0626]
Пример 27: Синтез 4-амино-7-(трет-бутил)-N-(4-пропилфенил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид
В соответствии с процедурой Примера 2, используя 4-пропиланилин вместо 4-(метоксиметил)анилина, получали указанное в заголовке соединение (48%).
[0627]
Пример 28: Синтез 4-амино-7-(трет-бутил)-N-(4-(пиридин-2-иламино)фенил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурой Примера 2, используя N-(2-пиридил)бензол-1,4-диамин вместо 4-(метоксиметил)анилина, получали указанное в заголовке соединение (100%).
[0628]
Пример 29: Синтез 4-амино-7-(трет-бутил)-N-(4-((метилтио)метил)фенил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурой Примера 2, используя 4-((метилтио)метил)анилин вместо 4-(метоксиметил)анилина, получали указанное в заголовке соединение (29%).
[0629]
Пример 30: Синтез 4-амино-7-(трет-бутил)-N-(3-фтор-4-(метоксиметил)фенил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурой Примера 2, используя 3-фтор-4-(метоксиметил)анилин, полученный в Ссылочном примере 8, вместо 4-(метоксиметил)анилина, получали указанное в заголовке соединение (43%).
[0630]
Пример 31: Синтез 4-амино-7-(трет-бутил)-N-(3-хлор-4-(метоксиметил)фенил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурой Примера 2, используя 3-хлор-4-(метоксиметил)анилин вместо 4-(метоксиметил)анилина, получали указанное в заголовке соединение (27%).
[0631]
Пример 32: Синтез 4-амино-7-(трет-бутил)-N-(4-(метоксиметил)-3-метилфенил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурой Примера 2, используя 4-(метоксиметил)3-метил-анилин, который был получен с использованием (2-метил-4-нитрофенил)метанола вместо (2-фтор-4-нитрофенил)метанола в соответствии со Ссылочным примером 8, вместо 4-(метоксиметил) анилин, получали указанное в заголовке соединение (82%).
[0632]
Пример 33: Синтез 4-амино-7-(трет-бутил)-N-(2-метокси-4-(метоксиметил)фенил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурой Примера 2, используя 2-метокси-4-(метоксиметил)анилин, который был получен с использованием (3-метокси-4-нитрофенил)метанола вместо (2-фтор-4-нитрофенил)метанола в соответствии со Ссылочным примером 8, вместо 4-(метоксиметил)анилина, получали указанное в заголовке соединение (60%).
[0633]
Пример 34: Синтез 4-амино-7-(трет-бутил)-N-(4-этинилфенил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурой Примера 2, используя 4-(этинилфенил)анилин вместо 4-(метоксиметил)анилина, получали указанное в заголовке соединение (52%).
[0634]
Пример 35: 4-амино-7-(трет-бутил)-N-(4-((метокси-d3)-метил)фенил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид
В соответствии с процедурой Примера 2, используя 4-((метокси-d-3)метил)анилин, который был синтезирован с использованием (4-нитрофенил)метанола и метилиодида (d3) в соответствии со Ссылочным примером 8, вместо 4-(метоксиметил)анилина, получали указанное в заголовке соединение (45%).
[0635]
Пример 36: Синтез 4-амино-N-(4-(метоксиметил)фенил)-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурами синтеза стадий 1-5 в Ссылочном примере 5, используя 1-метилциклопропанамин гидрохлорид вместо трет-бутиламина, получали 4-амино-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоновую кислоту.
В соответствии с процедурой Примера 2, используя 4-амино-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоновую кислоту вместо 4-амино-7-(трет-бутил)-7H-пирроло[2,3-d]пиримидин-5-карбоновой кислоты, получали указанное в заголовке соединение (8%).
[0636]
Пример 37: Синтез 4-амино-7-(1-метилциклопропил)-N-(4-((метилтио)метил)фенил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурой Примера 36, используя 4-((метилтио)метил)анилин вместо 4-(метоксиметил)анилина, получали указанное в заголовке соединение (78%).
[0637]
Пример 38: Синтез 4-амино-N-(4-(метоксиметил)фенил)-7-(трет-пентил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурами синтеза стадий 1-5 в Ссылочном примере 5, используя 2-метилбутан-2-амин вместо трет-бутиламина, получали 4-амино-7-(трет-пентил)-7H-пирроло[2,3-d]пиримидин-5-карбоновую кислоту.
В соответствии с процедурой Примера 2, используя 4-амино-7-(трет-пентил)-7H-пирроло[2,3-d]пиримидин-5-карбоновую кислоту вместо 4-амино-7-(трет-бутил)-7H-пирроло[2,3-d]пиримидин-5-карбоновой кислоты, получали указанное в заголовке соединение (82%).
[0638]
Пример 39: Синтез 4-амино-N-(4-(метоксиметил)фенил)-7-(1-метилциклобутил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурами синтеза стадий 1-5 в Ссылочном примере 5, используя 1-метилциклобутанамин гидрохлорид вместо трет-бутиламина, получали 4-амино-7-(1-метилциклобутил)-7H-пирроло[2,3-d]пиримидин-5-карбоновую кислоту.
В соответствии с процедурой Примера 2, используя 4-амино-7-(1-метилциклобутил)-7H-пирроло[2,3-d]пиримидин-5-карбоновую кислоту вместо 4-амино-7-(трет-бутил)-7H-пирроло[2,3-d]пиримидин-5-карбоновой кислоты, получали указанное в заголовке соединение (69%).
[0639]
Пример 40: Синтез 4-амино-7-(1-фтор-2-метилпропан-2-ил)-N-(4-((метилтио)метил)фенил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурой Примера 26, используя 4-((метилтио)метил)анилин вместо 4-(метоксиметил)анилина, получали указанное в заголовке соединение (55%).
[0640]
Пример 41: Синтез 4-амино-7-(1-фтор-2-метилпропан-2-ил)-N-(3-фтор-4-(метоксиметил)фенил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурой Примера 26, используя 3-фтор-4-(метоксиметил)анилин, который был получен в Ссылочном примере 8, вместо 4-(метоксиметил)анилина, получали указанное в заголовке соединение (50%).
[0641]
Пример 42: Синтез 4-амино-N-(4-(метоксиметил)фенил)-7-(2-(тиофен-2-ил)пропан-2-ил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурами синтеза стадий 1-5 в Ссылочном примере 5, используя 2-(тиофен-2-ил)пропан-2-амин вместо трет-бутиламина, получали 4-амино-7-(2-(тиофен-2-ил)пропан-2-ил)-7H-пирроло[2,3-d]пиримидин-5-карбоновую кислоту.
В соответствии с процедурой Примера 2, используя 4-амино-7-(2-(тиофен-2-ил)пропан-2-ил)-7H-пирроло[2,3-d]пиримидин-5-карбоновую кислоту вместо 4-амино-7-(трет-бутил)-7H-пирроло[2,3-d]пиримидин-5-карбоновой кислоты, получали указанное в заголовке соединение (86%).
[0642]
Пример 43: Синтез 4-амино-7-(бицикло[2.2.1]гептан-2-ил)-N-(4-(метоксиметил)фенил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурами синтеза стадий 1-5 в Ссылочном примере 5, используя бицикло[2.2.1]гептан-2-амин вместо трет-бутиламина, получали 4-амино-7-(бицикло[2.2.1]гептан-2-ил)-7H-пирроло[2,3-d]пиримидин-5-карбоновую кислоту.
В соответствии с процедурой Примера 2, используя 4-амино-7-(бицикло[2.2.1]гептан-2-ил)-7H-пирроло[2,3-d]пиримидин-5-карбоновую кислоту вместо 4-амино-7-(трет-бутил)-7H-пирроло[2,3-d]пиримидин-5-карбоновой кислоты, получали указанное в заголовке соединение (67%).
[0643]
Пример 44: 4-амино-7-(бицикло[1.1.1.]пентан-1-ил)-N-(4-(метоксиметил)фенил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид
В соответствии с процедурами синтеза стадий 1-5 в Ссылочном примере 5, используя бицикло[1.1.1]пентан-1-амин гидрохлорид вместо трет-бутиламина, получали 4-амино-7-(бицикло[1.1.1.]пентан-1-ил)-7H-пирроло[2,3-d]пиримидин-5-карбоновую кислоту.
В соответствии с процедурой Примера 2, используя 4-амино-7-(бицикло[1.1.1.]пентан-1-ил)-7H-пирроло[2,3-d]пиримидин-5-карбоновую кислоту вместо 4-амино-7-(трет-бутил)-7H-пирроло[2,3-d]пиримидин-5-карбоновой кислоты, получали указанное в заголовке соединение (76%).
[0644]
Пример 45: Синтез 4-амино-7-(1-(фторметил)циклопропил)-N-(4-(метоксиметил)фенил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
Раствор 100 мг 7-(1-(фторметил)циклопропил)-5-иод-7H-пирроло[2,3-d]пиримидин-4-амина, полученного на стадии 3 Ссылочного примера 6, 100 мг 4-(метоксиметил)анилина, 90 мкл 1,8-диазабицикло[5.4.0]ундец-7-ена и 20 мг комплекса 1,1'-бис(дифенилфосфино)ферроцен-палладий(II) дихлорид-дихлорметан в 3 мл NMP перемешивали в атмосфере оксида углерода при 100°C в течение 4 часов. Реакционный раствор концентрировали и очищали хроматографией на силикагеле (гексан-этилацетат-метанол), таким образом получая 86 мг указанного в заголовке соединения.
[0645]
Пример 46: Синтез 4-амино-7-(1-(дифторметил)циклопропил)-N-(4-(метоксиметил)фенил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурами синтеза стадий 1-3 в Ссылочном примере 6, используя 1-(дифторметил)циклопропанамин гидрохлорид вместо 1-(фторметил)циклопропанамин гидрохлорида, получали 7-(1-(дифторметил)циклопропил)-5-иод-7H-пирроло[2,3-d]пиримидин-4-амин.
В соответствии с процедурой Примера 45, используя 7-(1-(дифторметил)циклопропил)-5-иод-7H-пирроло[2,3-d]пиримидин-4-амин вместо 7-(1-(фторметил)циклопропил)-5-иод-7H-пирроло[2,3-d]пиримидин-4-амина, получали указанное в заголовке соединение (80%).
[0646]
Пример 47: Синтез 4-амино-7-(1-этилциклопропил)-N-(4-(метоксиметил)фенил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурами синтеза стадий 1-3 в Ссылочном примере 6, используя 1-этилциклопропанамин гидрохлорид вместо 1-(фторметил)циклопропанамин гидрохлорида, получали 7-(1-этилциклопропил)-5-иод-7H-пирроло[2,3-d]пиримидин-4-амин.
В соответствии с процедурой Примера 45, используя 7-(1-этилциклопропил)-5-иод-7H-пирроло[2,3-d]пиримидин-4-амин вместо 7-(1-(фторметил)циклопропил)-5-иод-7H-пирроло[2,3-d]пиримидин-4-амина, получали указанное в заголовке соединение (60%).
[0647]
Пример 48: Синтез 4-амино-N-(3-фтор-4-(метоксиметил)фенил)-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурами синтеза стадий 1-3 в Ссылочном примере 6, используя 1-метилциклопропан гидрохлорид вместо 1-(фторметил)циклопропанамин гидрохлорида, получали 5-иод-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-4-амин.
В соответствии с процедурой Примера 45, используя 5-иод-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-4-амин вместо 7-(1-(фторметил)циклопропил)-5-иод-7H-пирроло[2,3-d]пиримидин-4-амина и используя 3-фтор-4-(метоксиметил)анилин, который был получен в Ссылочном примере 8, вместо 4-(метоксиметил)анилина, получали указанное в заголовке соединение (80%).
[0648]
Пример 49: Синтез 7-{[1,1-би(циклопропан)]-1-ил}-4-амино-N-(4-(метоксиметил)фенил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурами синтеза стадий 1-3 в Ссылочном примере 6, используя 1-циклопропилциклопропанамин гидрохлорид вместо 1-(фторметил)циклопропанамин гидрохлорида, получали 7-([1,1-би(циклопропан)]-1-ил)-5-иод-7H-пирроло[2,3-d]пиримидин-4-амин.
В соответствии с процедурой Примера 45, используя 7-([1,1-би(циклопропан)]-1-ил)-5-иод-7H-пирроло[2,3-d]пиримидин-4-амин вместо 7-(1-(фторметил)циклопропил)-5-иод-7H-пирроло[2,3-d]пиримидин-4-амина, получали указанное в заголовке соединение (50%).
[0649]
Пример 50: Синтез 4-амино-7-(1,1-дифтор-2-метилпропан-2-ил)-N-(4-(метоксиметил)фенил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурами синтеза стадий 1-3 в Ссылочном примере 6, используя 1,1-дифтор-2-метил-пропан-2-амин гидрохлорид вместо 1-(фторметил)циклопропанамин гидрохлорида, получали 7-(1,1-дифтор-2-метилпропан-2-ил)-5-иод-7H-пирроло[2,3-d]пиримидин-4-амин.
В соответствии с процедурой Примера 45, используя 7-(1,1-дифтор-2-метилпропан-2-ил)-5-иод-7H-пирроло[2,3-d]пиримидин-4-амин вместо 7-(1-(фторметил)циклопропил)-5-иод-7H-пирроло[2,3-d]пиримидин-4-амина, получали указанное в заголовке соединение (32%).
[0650]
Пример 51: Синтез 4-амино-7-(2,3-диметилбутан-2-ил)-N-(4-(метоксиметил)фенил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурами синтеза стадий 1-3 в Ссылочном примере 6, используя 2,3-диметилбутан-2-амин гидрохлорид вместо 1-(фторметил)циклопропанамин гидрохлорида, получали 7-(2,3-диметилбутан-2-ил)-5-иод-7H-пирроло[2,3-d]пиримидин-4-амин.
В соответствии с процедурой Примера 45, используя 7-(2,3-диметилбутан-2-ил)-5-иод-7H-пирроло[2,3-d]пиримидин-4-амин вместо 7-(1-(фторметил)циклопропил)-5-иод-7H-пирроло[2,3-d]пиримидин-4-амина, получали указанное в заголовке соединение (74%).
[0651]
Пример 52: Синтез 4-амино-N-(4-(метоксиметил)фенил)-7-(2,3,3-триметилбутан-2-ил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурами синтеза стадий 1-3 в Ссылочном примере 6, используя 2,3,3-триметилбутан-2-амин вместо 1-(фторметил)циклопропанамин гидрохлорида, получали 5-иод-7-(2,3,3-триметилбутан-2-ил)-7H-пирроло[2,3-d]пиримидин-4-амин.
В соответствии с процедурой Примера 45, используя 5-иод-7-(2,3,3-триметилбутан-2-ил)-7H-пирроло[2,3-d]пиримидин-4-амин вместо 7-(1-(фторметил)циклопропил)-5-иод-7H-пирроло[2,3-d]пиримидин-4-амина, получали указанное в заголовке соединение (80%).
[0652]
Пример 53: Синтез 4-амино-7-(2-циклопропилпропан-2-ил)-N-(4-(метоксиметил)фенил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурами синтеза стадий 1-3 в Ссылочном примере 6, используя 2-циклопропилпропан-2-амин гидрохлорид вместо 1-(фторметил)циклопропанамин гидрохлорида, получали 7-(2-циклопропилпропан-2-ил)-5-иод-7H-пирроло[2,3-d]пиримидин-4-амин.
В соответствии с процедурой Примера 45, используя 7-(2-циклопропилпропан-2-ил)-5-иод-7H-пирроло[2,3-d]пиримидин-4-амин вместо 7-(1-(фторметил)циклопропил)-5-иод-7H-пирроло[2,3-d]пиримидин-4-амина, получали указанное в заголовке соединение (30%).
[0653]
Пример 54: Синтез 4-амино-7-(2-циклопропилпропан-2-ил)-N-(3-фтор-4-(метоксиметил)фенил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурой Примера 53, используя 3-фтор-4-(метоксиметил)анилин вместо 4-(метоксиметил)анилина, получали указанное в заголовке соединение (40%).
[0654]
Пример 55: 4-амино-6-бром-N-[4-(метоксиметил)фенил]-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид
Стадия 1: Синтез 4-амино-6-бром-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоновой кислоты
3 мл THF, 3 мл метанола и 0,62 мл водного раствора гидроксида лития (4 моль/л) добавляли к 80 мг метил 4-амино-6-бром-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксилата, полученного в Ссылочном примере 9. Смесь перемешивали при комнатной температуре в течение ночи. Добавляли 10 мл воды и смесь нейтрализовали 2N водным раствором HCl с получением таким образом осадка. После удаления растворителя остаток перемешивали при охлаждении льдом в течение 30 минут и осадок фильтровали, таким образом получая 73 мг указанного в заголовке соединения.
Физические свойства: m/z[M+H]+ 313,0
Стадия 2: Синтез 4-амино-6-бром-N-[4-(метоксиметил)фенил]-7-(1-метилциклопропил)7H-пирроло[2,3-d]пиримидин-5-карбоксамида
10,1 мг 4-амино-6-бром-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоновой кислоты, полученной на стадии 1, растворяли в 1 мл DMF и добавляли 5,3 мг 4-(метоксиметил)анилина, 17 мкл DIPEA и 18,5 мг HATU, с последующим перемешиванием при комнатной температуре в течение ночи. Реакционный раствор распределяли между этилацетатом и водой и органический слой промывали 1N водным раствором NaOH, водой и насыщенным водным раствором хлорида натрия, с последующей сушкой над безводным сульфатом натрия. После фильтрования фильтрат концентрировали. Остаток очищали на колонке с силикагелем (этилацетат/метанол=1/0 → 8/1), таким образом получая 6,7 мг указанного в заголовке соединения.
[0655]
Пример 56: 4-амино-6-хлор-N-[4-(метоксиметил)фенил]-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид
Стадия 1: Синтез метил 4-амино-6-хлор-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксилата
111 мг метил 4-амино-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксилата, синтезированного в соответствии с процедурами стадий 1-4 в Ссылочном примере 5 с использованием 1-метилциклопропанамин гидрохлорида вместо трет-бутиламина, растворяли в 4,5 мл DMF и добавляли 90 мг N-хлорсукцинимида при комнатной температуре, с последующим перемешиванием в течение ночи. Реакционный раствор распределяли между этилацетатом и 10% водным раствором тиосульфата натрия и органический слой промывали водой и насыщенным водным раствором хлорида натрия, с последующей сушкой над безводным сульфатом натрия. После фильтрования фильтрат концентрировали. Остаток очищали на колонке с силикагелем (этилацетат/метанол=1/0 → 8/1), таким образом получая 45 мг указанного в заголовке соединения.
Физические свойства: m/z[M+H]+ 281,1
Стадия 2: Синтез 4-амино-6-хлор-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоновой кислоты
В соответствии с процедурой стадии 1 Примера 55, исходя из 36 мг метил 4-амино-6-хлор-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксилата, полученного на стадии 1, получали указанное в заголовке соединение (87%).
Физические свойства: m/z[M+H]+ 267,0
Стадия 3: Синтез 4-амино-6-хлор-N-[4-(метоксиметил)фенил]-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурой стадии 2 в Примере 55, используя 17,6 мг 4-амино-6-хлор-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоновой кислоты, полученной на стадии 2, получали указанное в заголовке соединение (47%).
[0656]
Пример 57: 4-амино-6-метокси-N-[4-(метоксиметил)фенил]-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид
Стадия 1: Синтез метил 4-амино-6-метокси-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксилата
1,66 г 4-амино-6-бром-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида, полученного на стадии 3 Ссылочного примера 9, растворяли в 27 мл THF и добавляли 327 мг диметиламинопиридина и 5,84 г ди-трет-бутилдикарбоната, с последующим перемешиванием при комнатной температуре в течение ночи. После удаления THF добавляли 25 мл метанола и затем добавляли 5 мл раствора 5M метоксида натрия в метаноле, с последующим перемешиванием при комнатной температуре в течение 1 часа. Реакционный раствор нейтрализовали 2N раствором HCl и распределяли между этилацетатом и водой. Органический слой промывали водой и насыщенным водным раствором хлорида натрия, с последующей сушкой над безводным сульфатом натрия. После фильтрования фильтрат концентрировали. К остатку добавляли 5 мл дихлорметана и 5 мл трифторуксусной кислоты и смесь перемешивали при охлаждении льдом в течение 1 часа. После удаления трифторуксусной кислоты остаток распределяли между этилацетатом и водным раствором бикарбоната натрия. Органический слой промывали водой и насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия, фильтровали и концентрировали. Остаток очищали на колонке с силикагелем (этилацетат/метанол=1/0 → 8/1), таким образом получая 400 мг указанного в заголовке соединения.
Физические свойства: m/z[M+H]+ 277,1
Стадия 2: Синтез 4-амино-6-метокси-N-[4-(метоксиметил)фенил]-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурами стадий 1 и 2 в Примере 55, исходя из метил 4-амино-6-метокси-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксилата, полученного на стадии 1, получали указанное в заголовке соединение (50%).
[0657]
Пример 58: 4-амино-6-циано-N-[4-(метоксиметил)фенил]-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид
Стадия 1: Синтез метил 4-амино-6-циано-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксилата
77 мг метил 4-амино-6-бром-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксилата, полученного в Ссылочном примере 9, растворяли в 2,5 мл DMF и добавляли 53 мг цианида меди, с последующим перемешиванием при 120°C в атмосфере азота в течение 9 часов. Реакционный раствор концентрировали и остаток очищали хроматографией на силикагеле (этилацетат/метанол=1/0 → 8/1), таким образом получая 40 мг указанного в заголовке соединения.
Физические свойства: m/z[M+H]+ 272,1
Стадия 2: Синтез 4-амино-6-циано-N-[4-(метоксиметил)фенил]-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурами стадий 1 и 2 в Примере 55, исходя из метил 4-амино-6-циано-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксилата, полученного на стадии 1, получали указанное в заголовке соединение (35%).
[0658]
Пример 59: Синтез 4-амино-6-бром-7-(1-метилциклопропил)-N-(4-((метилтио)метил)фенил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурой стадии 2 в Примере 55, используя 4-амино-6-бром-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоновую кислоту, полученную на стадии 1 Примера 55, и 4-((метилтио)метил)анилин, получали указанное в заголовке соединение (44%).
[0659]
Пример 60: 4-амино-7-(трет-бутил)-N-(4-(метоксиметил)фенил)-6-метил-7H-пирроло[2,3-d]пиримидин-5-карбоксамид
Стадия 1: Синтез 4-амино-7-(трет-бутил)-6-метил-7H-пирроло[2,3-d]пиримидин-5-карбоновой кислоты
В соответствии с процедурами стадий 4 и 5 в Ссылочном примере 5, используя 135 мг 7-(трет-бутил)-5-иод-6-метил-7H-пирроло[2,3-d]пиримидин-4-амина, полученного в Ссылочном примере 7, получали указанное в заголовке соединение (45%).
Физические свойства: m/z[M+H]+ 249,1
Стадия 2: Синтез 4-амино-7-(трет-бутил)-N-(4-(метоксиметил)фенил)-6-метил-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурой стадии 2 в Примере 55, используя 4-амино-7-(трет-бутил)-6-метил-7H-пирроло[2,3-d]пиримидин-5-карбоновую кислоту, полученную на стадии 1, получали указанное в заголовке соединение (30%).
[0660]
Пример 61: 4-амино-N-(4-(метоксиметил)фенил)-7-(1-метилциклопропил)-6-(пиридин-3-ил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид
Стадия 1: Синтез метил 4-амино-7-(1-метилциклопропил)-6-(пиридин-3-ил)-7H-пирроло[2,3-d]пиримидин-5-карбоксилата
50 мг метил 4-амино-6-бром-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксилата, полученного в Ссылочном примере 9, 56 мг 3-пиридинбороновой кислоты, 14 мг трис(дибензилиденацетон)дипалладия, 14 мг 2-(дициклогексилфосфино)-2',4',6'-три-изопропил-1,1'-бифенила и 49 мг карбоната натрия подвергали взаимодействию в смеси 1,5 мл 1,4-диоксана и 500 мкл воды при 120°C в течение 1 часа в микроволновом реакторе. К реакционному раствору добавляли хлороформ и нерастворимое вещество фильтровали, с последующим концентрированием. Остаток очищали хроматографией на силикагеле (этилацетат/метанол=1/0 → 8/1), таким образом получая 27 мг указанного в заголовке соединения.
Физические свойства: m/z[M+H]+ 324,1
Стадия 2: Синтез 4-амино-7-(1-метилциклопропил)-6-(пиридин-3-ил)-7H-пирроло[2,3-d]пиримидин-5-карбоновой кислоты
26 мг метил 4-амино-7-(1-метилциклопропил)-6-(пиридин-3-ил)-7H-пирроло[2,3-d]пиримидин-5-карбоксилата, полученного на стадии 1, суспендировали в 2 мл THF и 2 мл метанола. Добавляли 0,20 мл водного раствора гидроксида лития (4 моль/л) и перемешивали при комнатной температуре в течение ночи. Добавляли 10 мл воды и смесь нейтрализовали 2N водным раствором HCl, с последующим экстрагированием водного слоя хлороформом. Органический слой промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия, с последующим удалением растворителя, таким образом получая 13 мг указанного в заголовке соединения.
Физические свойства: m/z[M+H]+ 310,1
Стадия 3: Синтез 4-амино-N-(4-(метоксиметил)фенил)-7-(1-метилциклопропил)-6-(пиридин-3-ил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурой стадии 2 в Примере 55, используя 4-амино-7-(1-метилциклопропил)-6-(пиридин-3-ил)-7H-пирроло[2,3-d]пиримидин-5-карбоновую кислоту, полученную на стадии 2, получали указанное в заголовке соединение (9%) =.
[0661]
Пример 62: 4-амино-N-(4-(метоксиметил)фенил)-6-метил-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид
Стадия 1: Синтез метил 4-амино-6-метил-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксилата
30 мг метил 4-амино-6-бром-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксилата, полученного в Ссылочном примере 9, 55 мг метилбороновой кислоты, 8 мг трис(дибензилиденацетон)дипалладия, 5 мг трициклогексилфосфина и 58 мг трифосфата калия подвергали взаимодействию в смеси 1,5 мл 1,4-диоксана и 150 мкл воды при 120°C в течение 1 часа в микроволновом реакторе. К реакционному раствору добавляли хлороформ и нерастворимое вещество фильтровали с последующим концентрированием. Остаток очищали хроматографией на силикагеле (этилацетат/метанол=1/0 → 8/1), таким образом получая 20 мг указанного в заголовке соединения.
Физические свойства: m/z[M+H]+ 261,2
Стадия 2: Синтез 4-амино-N-(4-(метоксиметил)фенил)-6-метил-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурами стадий 1 и 2 в Примере 55, используя метил 4-амино-6-метил-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксилат, полученный на стадии 1, получали указанное в заголовке соединение (6%).
[0662]
Пример 63: 4-амино-6-циклопропил-N-(4-(метоксиметил)фенил)-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид
В соответствии с процедурами стадий 1 и 2 в Примере 62, используя метил 4-амино-6-бром-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксилат, полученный в Ссылочном примере 9, и циклопропилбороновую кислоту вместо метилбороновой кислоты, получали указанное в заголовке соединение (38%).
[0663]
Пример 64: 6-ацетил-4-амино-N-(4-(метоксиметил)фенил)-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид
Стадия 1: Синтез метил 6-ацетил-4-амино-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксилата
1 мл толуола добавляли к 60 мг метил 4-амино-6-бром-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксилата, полученного в Ссылочном примере 9, 75 мкл трибутил(1-этокси)олова и 21 мг тетракис(трифенилфосфин)палладия и взаимодействие смеси осуществляли при 130°C в течение 4 часов в микроволновом реакторе. Реакционный раствор концентрировали, затем остаток очищали амино-гель-хроматографией (гексан/этилацетат=10/4 → 0/1). Целевую фракцию концентрировали, затем добавляли 1 мл THF и 300 мкл раствора хлористоводородной кислоты (2 моль/л), с последующим перемешиванием при комнатной температуре в течение ночи. Затем смесь снова подвергали взаимодействию при 50°C в течение 4 часов. Реакционный раствор распределяли между этилацетатом и насыщенным водным раствором бикарбоната натрия и органический слой промывали водой и насыщенным водным раствором хлорида натрия, с последующей сушкой над безводным сульфатом натрия. После фильтрования фильтрат концентрировали, таким образом получая 45 мг указанного в заголовке соединения.
Физические свойства: m/z[M+H]+ 289,2
Стадия 2: Синтез 6-ацетил-4-амино-N-(4-(метоксиметил)фенил)-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурами стадий 1 и 2 в Примере 55, используя метил 6-ацетил-4-амино-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксилат, полученный на стадии 1, получали указанное в заголовке соединение (48%).
[0664]
Пример 65: 4-амино-N-(4-(метоксиметил)фенил)-7-(1-метилциклопропил)-6-винил-7H-пирроло[2,3-d]пиримидин-5-карбоксамид
Стадия 1: Синтез метил 4-амино-7-(1-метилциклопропил)-6-винил-7H-пирроло[2,3-d]пиримидин-5-карбоксилата
1,5 мл толуола добавляли к 90 мг метил 4-амино-6-бром-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксилата, полученного в Ссылочном примере 9, 97 мкл трибутилвинилолова и 32 мг тетракис(трифенилфосфин)палладия и взаимодействие смеси осуществляли при 130°C в течение 3 часов в микроволновом реакторе. Реакционный раствор концентрировали, затем остаток очищали амино-гель-хроматографией (гексан/этилацетат=4/1 → 3/5), таким образом получая 67 мг указанного в заголовке соединения.
Физические свойства: m/z[M+H]+ 273,2
Стадия 2: Синтез 4-амино-N-(4-(метоксиметил)фенил)-7-(1-метилциклопропил)-6-винил-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурами стадий 1 и 2 в Примере 55, используя метил 4-амино-7-(1-метилциклопропил)-6-винил-7H-пирроло[2,3-d]пиримидин-5-карбоксилат, полученный на стадии 1, получали указанное в заголовке соединение (27%).
[0665]
Пример 66: Синтез 4-амино-7-циклобутил-N-(4-(метоксиметил)фенил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурами синтеза стадий 1-5 в Ссылочном примере 5, используя циклобутанамин вместо трет-бутиламина, получали 4-амино-7-циклобутил-7H-пирроло[2,3-d]пиримидин-5-карбоновую кислоту.
В соответствии с процедурой Примера 2, используя 4-амино-7-циклобутил-7H-пирроло[2,3-d]пиримидин-5-карбоновую кислоту вместо 4-амино-7-(трет-бутил)-7H-пирроло[2,3-d]пиримидин-5-карбоновой кислоты, получали указанное в заголовке соединение (86%).
[0666]
Пример 67: Синтез 4-амино-N-(4-(метоксиметил)фенил)-1-(цис-2-метилциклопентил)-1H-пиразолo[3,4-d]пиримидин-3-карбоксамида
В соответствии с процедурами синтеза стадий 1 и 2 в Ссылочном примере 2, используя транс-2-метилциклопентанол вместо 2-адамантанол, получали 4-амино-1-(цис-2-метилциклопентил)-1H-пиразолo[3,4-d]пиримидин-3-карбоновую кислоту.
В соответствии с процедурой Примера 19, используя 4-амино-1-(цис-2-метилциклопентил)-1H-пиразолo[3,4-d]пиримидин-3-карбоновую кислоту вместо 1-(адамантан-2-ил)-4-амино-1H-пиразолo[3,4-d]пиримидин-3-карбоновой кислоты, получали указанное в заголовке соединение (52%).
[0667]
Пример 68: Синтез 4-амино-1-циклопентил-N-(4-этинилфенил)-1H-пиразолo[3,4-d]пиримидин-3-карбоксамида
В соответствии с процедурой синтеза Примера 1, используя 4-этиниланилин вместо 4-(метоксиметил)анилина, получали указанное в заголовке соединение (88%).
[0668]
Пример 69: Синтез 4-амино-6-фтор-N-(4-(метоксиметил)фенил)-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
50 мг 4-амино-N-(4-(метоксиметил)фенил)-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида, полученного в Примере 36, растворяли в 1,5 мл DMF и добавляли 151 мг 1-хлорметил-4-фтор-1,4-диазониабицикло[2.2.2]октан бис(тетрафторборат) при охлаждении льдом. Смесь затем перемешивали при охлаждении льдом и через 1 час добавляли 151 мг 1-хлорметил-4-фтор-1,4-диазониабицикло[2.2.2]октан бис(тетрафторборат). Смесь снова перемешивали в течение 1 часа и затем реакционный раствор распределяли между хлороформом и водой. Органический слой промывали водой и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом натрия, фильтровали и концентрировали. Остаток очищали на колонке с силикагелем (этилацетат/метанол=1/0 → 8/1), таким образом получая 2,7 мг указанного в заголовке соединения.
[0669]
Пример 70: Синтез 4-амино-1-циклопентил-N-(4-(трифторметокси)фенил)-1H-пиразолo[3,4-d]пиримидин-3-карбоксамида
В соответствии с процедурами синтеза Примера 1, используя 4-(трифторметокси)анилин вместо 4-(метоксиметил)анилина, получали указанное в заголовке соединение (45%).
[0670]
Пример 71: Синтез 4-амино-N-(3-бензилфенил)-1-циклопентил-1H-пиразолo[3,4-d]пиримидин-3-карбоксамида
В соответствии с процедурами синтеза Примера 1, используя 3-бензиланилин вместо 4-(метоксиметил)анилина, получали указанное в заголовке соединение (58%).
[0671]
Пример 72: Синтез 4-амино-1-циклопентил-N-(4-(оксазол-2-ил)фенил)-1H-пиразолo[3,4-d]пиримидин-3-карбоксамида
В соответствии с процедурами синтеза Примера 1, используя 4-(оксазол-2-ил)анилин вместо 4-(метоксиметил)анилина, получали указанное в заголовке соединение (32%).
[0672]
Пример 73: Синтез 4-амино-N-(4-цианофенил)-1-циклопентил-1H-пиразолo[3,4-d]пиримидин-3-карбоксамида
В соответствии с процедурой синтеза Примера 1, используя 4-аминобензонитрил вместо 4-(метоксиметил)анилина, получали указанное в заголовке соединение (69%).
[0673]
Пример 74: Синтез 4-амино-1-циклопентил-N-(4-нитрофенил)-1H-пиразолo[3,4-d]пиримидин-3-карбоксамида
В соответствии с процедурой синтеза Примера 1, используя 4-нитроанилин вместо 4-(метоксиметил)анилина, получали указанное в заголовке соединение (65%).
[0674]
Пример 75: Синтез 4-амино-N-(бензо[b]тиофен-5-ил)-1-циклопентил-1H-пиразолo[3,4-d]пиримидин-3-карбоксамида
В соответствии с процедурой синтеза Примера 1, используя бензо[b]тиофен-5-амин вместо 4-(метоксиметил)анилина, получали указанное в заголовке соединение (33%).
[0675]
Пример 76: Синтез 4-амино-1-циклопентил-N-(4-этинил-3-фторфенил)-1H-пиразолo[3,4-d]пиримидин-3-карбоксамида
В соответствии с процедурой синтеза Примера 1, используя 4-этинил-3-фторанилин вместо 4-(метоксиметил)анилина, получали указанное в заголовке соединение (34%).
[0676]
Пример 77: Синтез 4-амино-N-(4-бром-2-метилфенил)-1-циклопентил-1H-пиразолo[3,4-d]пиримидин-3-карбоксамида
В соответствии с процедурой синтеза Примера 1, используя 4-бром-2-метиланилин вместо 4-(метоксиметил)анилина, получали указанное в заголовке соединение (51%).
[0677]
Пример 78: Синтез 4-амино-1-(3-фторпроп-1-ен-2-ил)-N-(4-(метоксиметил)фенил)-1H-пиразолo[3,4-d]пиримидин-3-карбоксамида
В соответствии с процедурами синтеза стадий 1 и 2 в Ссылочном примере 2, используя 1,3-дифторпропан-2-ол вместо 2-адамантанола, получали 4-амино-1-(3-фторпроп-1-ен-2-ил)-1H-пиразолo[3,4-d]пиримидин-3-карбоновую кислоту.
В соответствии с процедурой Примера 19, используя 4-амино-1-(3-фторпроп-1-ен-2-ил)-1H-пиразолo[3,4-d]пиримидин-3-карбоновую кислоту вместо 1-(адамантан-2-ил)-4-амино-1H-пиразолo[3,4-d]пиримидин-3-карбоновой кислоты, получали указанное в заголовке соединение (90%).
[0678]
Пример 79: Синтез 4-амино-7-(1-метокси-2-метилпропан-2-ил)-N-(4-(метоксиметил)фенил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурами синтеза стадий 1-3 в Ссылочном примере 6, используя 1-метокси-2-метилпропан-2-амин вместо 1-(фторметил)циклопропанамин гидрохлорида, получали 5-иод-7-(1-метокси-2-метилпропан-2-ил)-7H-пирроло[2,3-d]пиримидин-4-амин.
В соответствии с процедурой Примера 45, используя 5-иод-7-(1-метокси-2-метилпропан-2-ил)-7H-пирроло[2,3-d]пиримидин-4-амин вместо 7-(1-(фторметил)циклопропил)-5-иод-7H-пирроло[2,3-d]пиримидин-4-амина, получали указанное в заголовке соединение (70%).
[0679]
Пример 80: Синтез N-(4-(1H-пиразол-3-ил)фенил)-4-амино-7-(трет-бутил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурой синтеза Примера 2, используя 4-(1H-пиразол-3-ил)анилин вместо 4-(метоксиметил)анилина, получали указанное в заголовке соединение (94%).
[0680]
Пример 81: Синтез 4-амино-7-(трет-бутил)-N-(5-(метоксиметил)пиридин-2-ил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурой Примера 45, используя 7-(трет-бутил)-5-иод-7H-пирроло[2,3-d]пиримидин-4-амин, полученный на стадии 3 Ссылочного примера 5, и 5-(метоксиметил)пиридин-2-амин, синтезированный в соответствии с процедурой, описанной в международной публикации № WO2010/058846, получали указанное в заголовке соединение (64%).
[0681]
Пример 82: Синтез 4-амино-1-(4,4-дифторциклогексил)-N-(4-(метоксиметил)фенил)-1H-пиразолo[3,4-d]пиримидин-3-карбоксамида
33 мг метил-4-амино-1-(4,4-дифторциклогексил)-1H-пиразолo[3,4-d]пиримидин-3-карбоксилата, полученного на стадии 2 Ссылочного примера 10, растворяли в 2 мл метанола. Добавляли 0,05 мл 5M водного раствора гидроксида натрия при комнатной температуре и смесь перемешивали при 60°C в течение 1 часа. После охлаждения добавляли 0,2 мл 5M водного раствора хлористоводородной кислоты и смесь концентрировали при пониженном давлении. Полученное твердое вещество суспендировали в 2 мл DMF и добавляли 17 мг 4-(метоксиметил)анилина, 60 мг HATU и 0,055 мл N,N-диизопропилэтиламина при комнатной температуре, с последующим перемешиванием при этой же температуре в течение 1 часа. Реакционный раствор разбавляли этилацетатом и промывали водой и насыщенным водным раствором хлорида натрия. Полученный органический слой сушили над безводным сульфатом натрия, фильтровали и концентрировали. Полученный остаток суспендировали в метаноле и фильтровали, с последующей сушкой при 60°C при пониженном давлении, таким образом получая 29 мг указанного в заголовке соединения.
[0682]
Пример 83: Синтез 4-амино-1-циклопентил-N-(4-(гидроксиметил)фенил)-1H-пиразолo[3,4-d]пиримидин-3-карбоксамида
1 мл трифторуксусной кислоты и 50 мкл воды добавляли к 90 мг 4-амино-1-циклопентил-N-(4-(метоксиметил)фенил)-1H-пиразолo[3,4-d]пиримидин-3-карбоксамида, полученного в Примере 1, и смесь перемешивали при 100°C в течение 1 часа. После охлаждения смесь концентрировали и к полученному остатку добавляли раствор аммиак-метанол, с последующим перемешиванием в течение 30 минут. После концентрирования полученный остаток очищали хроматографией на силикагеле (проявляющий растворитель: хлороформ/метанол) и концентрировали. Полученный осадок суспендировали и промывали метанолом и фильтровали, с последующей сушкой при пониженном давлении, таким образом получая указанное в заголовке соединение (58%).
[0683]
Пример 84: Синтез 4-амино-1-циклопентил-N-(isochroman-6-ил)-1H-пиразолo[3,4-d]пиримидин-3-карбоксамида
В соответствии с процедурой синтеза Примера 1, используя изохроман-6-амин вместо 4-(метоксиметил)анилина, получали указанное в заголовке соединение (60%).
[0684]
Пример 85: Синтез 4-амино-N-[4-(метоксиметил)фенил]-7-(1-метилциклопропил)-6-(3-морфолинопроп-1-ин-1-ил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
5,15 г 4-амино-6-бром-N-[4-(метоксиметил)фенил]-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида, показанного в Примере 55, растворяли в 50 мл DMF. Добавляли 228 мг иодида меди, 5,24 г 4-(проп-2-ин-1-ил)морфолина, 5,0 мл триэтиламина и 1,38 г тетракис(трифенилфосфин)палладия, с последующим дегазированием. Затем смесь перемешивали при 100°C в течение 2 часов. Растворитель удаляли из реакционного раствора и остаток очищали на колонке с силикагелем (хлороформ/метанол=1/0 → 8/1). Затем фракции, содержащие побочные продукты, концентрировали и снова очищали на колонке с силикагелем (этилацетат/метанол=1/0 → 4/1), таким образом получая 2,78 г указанного в заголовке соединения.
[0685]
Пример 86: Синтез 4-амино-6-(4-гидрокси-4-метилпент-1-ин-1-ил)-N-[4-(метоксиметил)фенил]-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурой Примера 85, используя 2-метилпен-4-тин-2-ол вместо 4-(проп-2-ин-1-ил)морфолина, получали указанное в заголовке соединение (36%).
[0686]
Пример 87: Синтез 4-амино-N-[4-(метоксиметил)фенил]-7-(1-метилциклопропил)-6-((тетрагидро-2H-пиран-4-ил)этинил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурой Примера 85, используя 4-этинилтетрагидро-2H-пиран вместо 4-(проп-2-ин-1-ил)морфолина, получали указанное в заголовке соединение (66%).
[0687]
Пример 88: Синтез 4-амино-N-[4-(метоксиметил)фенил]-7-(1-метилциклопропил)-6-(3-(пирролидин-1-ил)проп-1-ин-1-ил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурой Примера 85, используя 1-(про-2-пин-1-ил)пирролидин вместо 4-(проп-2-ин-1-ил)морфолина, получали указанное в заголовке соединение (46%).
[0688]
Пример 89: Синтез (R)-4-амино-N-[4-(метоксиметил)фенил]-7-(1-метилциклопропил)-6-((тетрагидрофуран-2-ил)метокси)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
721 мкл (R)-(-)-тетрагидрофурфурилового спирта добавляли к суспензии 371 мг гидрида натрия (60%) в 15 мл DMF при перемешивании при температуре охлаждения льдом. Смесь затем перемешивали при комнатной температуре в течение 30 минут. К смеси добавляли раствор 800 мг 4-амино-6-бром-N-[4-(метоксиметил)фенил]-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида, показанного в Примере 55, в 5 мл DMF и перемешивали при 80°C в течение ночи. После охлаждения реакционную смесь распределяли между этилацетатом и водой и органический слой промывали водой и насыщенным водным раствором хлорида натрия, с последующей сушкой над сульфатом натрия и удалением растворителя. Остаток очищали на колонке с силикагелем (этилацетат/метанол=1/0 → 8/1), таким образом получая 644 мг указанного в заголовке соединения.
[0689]
Пример 90: Синтез 4-амино-N-[4-(метоксиметил)фенил]-6-((1-метил-1H-пиразол-4-ил)этинил)-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
1,2 г 4-амино-6-бром-N-[4-(метоксиметил)фенил]-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида, показанного в Примере 55, растворяли в 40 мл DMF и добавляли 53 мг иодида меди, 890 мг 4-этинил-1-метил-пиразола, 2,3 мл триэтиламина и 320 мг тетракис(трифенилфосфин)палладия, с последующим дегазированием и перемешиванием при 110°C в течение 1,5 часа. К реакционному раствору добавляли насыщенный раствор бикарбоната натрия, с последующим экстрагированием хлороформом. Органический слой промывали водой и сушили над безводным сульфатом магния, с последующим концентрированием органического раствораителя при пониженном давлении. Остаток очищали препаративной обращенно-фазовой ВЭЖХ, таким образом получая 700 мг указанного в заголовке соединения.
[0690]
Пример 91: Синтез 4-амино-6-(имидазо[1,2-b]пиридазин-3-илэтинил)-N-[4-(метоксиметил)фенил]-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурой Примера 90, используя 3-этинилимидазо[1,2-b]пиридазин вместо 4-этинил-1-метил-пиразола, получали указанное в заголовке соединение (58%).
[0691]
Пример 92: Синтез 4-амино-N-(4-(метоксиметил)фенил)-6-((1-метил-1H-пиразол-3-ил)этинил)-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурой Примера 90, используя 3-этинил-1-метил-пиразол вместо 4-этинил-1-метил-пиразола, получали указанное в заголовке соединение (28%).
[0692]
Пример 93: Синтез 4-амино-N-(4-(метоксиметил)фенил)-6-((1-метил-1H-имидазол-5-ил)этинил)-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурой Примера 90, используя 5-этинил-1-метил-имидазол вместо 4-этинил-1-метил-пиразола, получали указанное в заголовке соединение (37%).
[0693]
Пример 94: Синтез 4-амино-N-[4-(метоксиметил)фенил]-7-(1-метилциклопропил)-6-(пиридин-3-илэтинил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурой Примера 90, используя 3-этинилпиридин вместо 4-этинил-1-метил-пиразола, получали указанное в заголовке соединение (34%).
[0694]
Пример 95: Синтез 4-амино-N-(4-(метоксиметил)фенил)-7-(1-метилциклопропил)-6-(проп-1-ин-1-ил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
6,6 мг иодида меди, 2,4 мл пропина (1,0 моль/л раствор в DMF), 146 мкл триэтиламина и 24 мг дихлорбистрифенилфосфинпалладия добавляли к 150 мг 4-амино-6-бром-N-[4-(метоксиметил)фенил]-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида, показанного в Примере 55. Смесь перемешивали при 80°C в течение 5 часов. Реакционный раствор распределяли между хлороформом и водой и фильтровали через фазовый разделитель. Фильтрат концентрировали и остаток очищали на колонке с силикагелем (этилацетат/метанол=1/0 → 8/1). Затем фракции, содержащие побочные продукты, концентрировали и снова очищали на колонке с силикагелем (хлороформ/метанол=1/0 → 8/1), таким образом получая 107 мг указанного в заголовке соединения.
[0695]
В соответствии с процедурой Примера 89, используя соединения, показанные в Таблице 1, вместо (R)-(-)-тетрагидрофурфурилового спирта, получали соединения 96-102 Примеров.
[0696]
[0697]
В соответствии с процедурой синтеза Примера 85, используя соединения, показанные в Таблице 2, вместо 4-(проп-2-ин-1-ил)морфолина, были получены соединения 103-105 Примеров.
[0698]
[0699]
В соответствии с процедурой синтеза Примера 36, используя соединения, показанные в Таблице 3, вместо 4-(метоксиметил)анилина, были получены соединения 106-108 Примеров.
[0700]
[0701]
Пример 109: Синтез (E)-4-амино-6-(3-гидроксипроп-1-ен-1-ил)-N-(4-(метоксиметил)фенил)-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурами стадий 1 и 2 в Примере 62, реакцию осуществляли с использованием (E)-трет-бутилдиметил((3-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)аллил)окси)силана вместо метил 4-амино-6-бром-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксилата, показанного в Ссылочном примере 9, и метилбороновой кислоты с получением указанного в заголовке соединения (4%).
[0702]
Пример 110: Синтез 4-амино-6-(3-гидроксипроп-1-ин-1-ил)-N-(4-(метоксиметил)фенил)-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
10 мг 4-амино-6-(3-((трет-бутилдиметилсилил)окси)проп-1-ин-1-ил)-N-(4-(метоксиметил)фенил)-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида, показанного в Примере 180, растворяли в 1,5 мл THF и добавляли 3,3 мкл уксусной кислоты и 29 мкл тетрабутиламмонийфторида (1,0 моль/л THF раствор), с последующим перемешиванием в течение 30 минут. Реакционный раствор концентрировали и остаток очищали на колонке с силикагелем (этилацетат/метанол=1/0 → 8/1), таким образом получая 6 мг указанного в заголовке соединения.
[0703]
В соответствии с процедурой синтеза Примера 90, используя соединения, показанные в Таблицах 4-7, вместо 4-этинил-1-метил-пиразола, были получены соединения 111-114, 118-126, 128-132, 134, 142-144, 151, 152, 155-163, 165, 166, 168-170, 172-178, 181-189, 191-193 и 195-200 Примеров.
[0704]
[0705]
[0706]
[0707]
[0708]
В соответствии с процедурой синтеза Примера 115, используя соединения, показанные в Таблице 8, вместо 4-((метилтио)метил)анилина, были получены соединения 116 и 117 Примеров.
[0709]
[0710]
Пример 115: Синтез 4-амино-6-этокси-7-(1-метилциклопропил)-N-(4-((метилтио)метил)фенил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурой синтеза Примера 59, используя 4-амино-6-этокси-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоновую кислоту, показанную на стадии 1 Примера 127, вместо 4-амино-6-бром-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоновой кислоты, получали указанное в заголовке соединение (64%).
[0711]
Пример 127: Синтез 4-амино-6-этокси-N-(4-(метоксиметил)фенил)-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
Стадия 1: Синтез 4-амино-6-этокси-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоновой кислоты
714 мг метил 4-амино-6-хлор-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксилата, показанного на стадии 1 Примера 56, растворяли в 12 мл THF и добавляли 155 мг диметиламинопиридина и 1,66 г трет-бутилдикарбоната, с последующим перемешиванием при 50°C в течение 1 часа.
[0712]
После удаления растворителя остаток распределяли между этилацетатом и водой и органический слой промывали водой и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом натрия и концентрировали. К остатку добавляли 20 мл этанола и 3 мл этоксида натрия (20% раствор в этаноле) и смесь перемешивали в течение ночи. К реакционному раствору добавляли 20 мл этанола и 12 мл 4N водного раствора гидроксида натрия и смесь перемешивали при 80°C в течение 6 часов. После охлаждения к реакционному раствору добавляли 30 мл воды и этанол удаляли через испаритель. Остаток доводили до pH 4 2N водным раствором HCl и образовавшийся осадок перемешивали при охлаждении льдом в течение 1 часа и фильтровали, таким образом получая 400 мг указанного в заголовке соединения.
[0713]
Стадия 2: Синтез 4-амино-6-этокси-N-(4-(метоксиметил)фенил)-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурой синтеза стадии 2 Примера 55, используя 4-амино-6-этокси-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоновую кислоту, полученную на стадии 1, вместо 4-амино-6-бром-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоновой кислоты, получали указанное в заголовке соединение (56%).
[0714]
Пример 133: Синтез 4-амино-N-(4-метоксиметил)фенил-7-(1-метилциклопропил)-6-(метилтио)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
100 мг 4-амино-6-бром-N-[4-(метоксиметил)фенил]-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида, показанного в Примере 55, растворяли в 1 мл DMF и добавляли 330 мкл натриевой соли метилмеркаптана (примерно 15% водный раствор) при комнатной температуре. После перемешивания в течение 30 минут смесь разбавляли водой и полученное твердое вещество фильтровали, промывали водой и сушили при 60°C при пониженном давлении, таким образом получая 87 мг указанного в заголовке соединения.
[0715]
Пример 135: Синтез 4-амино-N-(4-(метоксиметил)фенил)-7-(1-метилциклопропил)-6-((тетрагидрофуран-2-ил)метокси)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
100 мкл тетрагидрофурфурилового спирта добавляли к суспензии 52 мг гидрида натрия (60%) в 1 мл DMF при перемешивании, охлаждая при этом смесь льдом, и затем смесь перемешивали при комнатной температуре в течение 30 минут. Добавляли раствор 30 мг 4-амино-6-хлор-N-[4-(метоксиметил)фенил]-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида, показанного в Примере 56, в 1 мл DMF и смесь перемешивали при 80°C в течение ночи. После охлаждения реакционный раствор распределяли между этилацетатом и водой и органический слой промывали водой и насыщенным водным раствором хлорида натрия и сушили над сульфатом натрия, с последующим удалением растворителя. Остаток очищали на колонке с силикагелем (этилацетат/метанол=1/0 → 8/1) и ВЭЖХ, таким образом получая 32,2 мг указанного в заголовке соединения.
[0716]
В соответствии с процедурой синтеза Примера 135, используя соединения, показанные в Таблице 9, вместо тетрагидрофурфурилового спирта, были получены соединения 136-141 Примеров.
[0717]
[0718]
Пример 145: Синтез 4-амино-6-(4-(гидроксиметил)фенил)-N-(4-(метоксиметил)фенил)-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
100 мг 4-амино-6-бром-N-[4-(метоксиметил)фенил]-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида, показанного в Примере 55, 148 мг фосфата калия, 70 мг (4-(гидроксиметил)фенил)бороновой кислоты и 13 мг тетракис(трифенилфосфин)палладия перемешивали в смеси растворителей 2 мл диоксана и 0,2 мл воды при 130°C в течение 1 часа в микроволновом реакторе. К полученному реакционному раствору добавляли этилацетат и воду и органический слой отделяли. Полученный органический слой концентрировали при пониженном давлении и остаток очищали хроматографией на силикагеле (проявляющий растворитель: хлороформ-метанол). После концентрирования полученный остаток суспендировали в метаноле, фильтровали и сушили при пониженном давлении, таким образом получая 57 мг указанного в заголовке соединения.
[0719]
Пример 146: Синтез 4-амино-6-изопропокси-N-(4-(метоксиметил)фенил)-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
50 мг 4-амино-6-хлор-N-[4-(метоксиметил)фенил]-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида, показанного в Примере 56, растворяли в 1,5 мл DMF и добавляли 160 мг изопропоксида натрия, с последующим перемешиванием с нагреванием при 100°C в течение 8 часов. Реакционный раствор распределяли между этилацетатом и водой и органический слой концентрировали, с последующей очисткой остатка препаративной обращенно-фазовой ВЭЖХ, таким образом получая 2,9 мг указанного в заголовке соединения.
[0720]
В соответствии с процедурой синтеза Примера 145, используя соединения, показанные в Таблице 10, вместо [4-(гидроксиметил)фенил]бороновой кислоты, были получены соединения 147-150 и 203 Примеров.
[0721]
[0722]
Пример 153: Синтез 4-амино-6-(4-формилфенил)-N-(4-(метоксиметил)фенил)-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
Со ссылкой на Пример 145, реакцию осуществляли с использованием 4-формилфенилбороновой кислоты вместо (4-(гидроксиметил)фенил)бороновой кислоты. К полученному реакционному раствору добавляли этилацетат и воду и органический слой отделяли. Полученный органический слой концентрировали при пониженном давлении и остаток очищали хроматографией на силикагеле (проявляющий растворитель: хлороформ-метанол). После концентрирования полученный остаток суспендировали в метаноле, фильтровали и сушили при пониженном давлении, таким образом получая 23 мг указанного в заголовке соединения.
[0723]
Пример 154: Синтез 4-амино-N-(4-(метоксиметил)фенил)-7-(1-метилциклопропил)-6-фенил-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурой синтеза Примера 153, используя фенилбороновую кислоту вместо 4-формилфенилбороновой кислоты, получали указанное в заголовке соединение (44%).
[0724]
Пример 164: Синтез 4-амино-6-(3-(гидроксиметил)фенил)-N-(4-(метоксиметил)фенил)-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
100 мг 4-амино-6-бром-N-[4-(метоксиметил)фенил]-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида, показанного в Примере 55, 148 мг фосфата калия, 70 мг (3-(гидроксиметил)фенил)бороновой кислоты и 13 мг тетракис(трифенилфосфин)палладия перемешивали в смешанном растворителе, состоящем из 2 мл диоксана и 0,2 мл воды, при 140°C в течение 1 часа в микроволновом реакторе. К полученному реакционному раствору добавляли этилацетат и воду и органический слой отделяли. Полученный органический слой концентрировали при пониженном давлении и остаток очищали хроматографией на силикагеле (проявляющий растворитель: хлороформ-метанол). После концентрирования полученный остаток очищали снова препаративной обращенно-фазовой ВЭЖХ и подщелачивали насыщенным раствором бикарбоната натрия, с последующим экстрагированием хлороформом. Полученный органический слой концентрировали и остаток суспендировали в метаноле, фильтровали и сушили при пониженном давлении, таким образом получая 28 мг указанного в заголовке соединения.
[0725]
Пример 167: Синтез 4-амино-N-(4-(метоксиметил)фенил)-7-(1-метилциклопропил)-6-(1H-пиразол-4-ил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурой синтеза Примера 164, используя трет-бутил 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиразол-1-карбоксилат вместо [3-(гидроксиметил)фенил]бороновой кислоты, получали 16 мг указанного в заголовке соединения.
[0726]
Пример 171: Синтез 4-амино-N-(4-(метоксиметил)фенил)-7-(1-метилциклопропил)-6-(4-(4-метилпиперазин-1-ил)фенил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурой синтеза Примера 145, используя 1-метил-4-[4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)фенил]пиперазин вместо (4-(гидроксиметил)фенил)бороновой кислоты, получали 84 мг указанного в заголовке соединения.
[0727]
Пример 179: Синтез 4-амино-6-(6-(гидроксиметил)пиридин-3-ил)-N-(4-(метоксиметил)фенил)-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурой синтеза Примера 164, используя (6-(гидроксиметил)пиридин-3-ил)бороновую кислоту вместо (4-(гидроксиметил)фенил)бороновой кислоты, получали 47 мг указанного в заголовке соединения.
[0728]
Пример 180: Синтез 4-амино-6-(3-(трет-бутилдиметилсилил)окси)проп-1-ин-1-ил-N-(4-(метоксиметил)фенил)-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
50 мг 4-амино-6-бром-N-[4-(метоксиметил)фенил]-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида, показанного в Примере 55, растворяли в 1 мл DMF. Добавляли 2 мг иодида меди, 65 мг 2-пропин-1-ола, 50 мкл триэтиламина и 13 мг тетракис(трифенилфосфин)палладия и дегазировали, с последующим перемешиванием при 100°C в течение 1,5 часа. После завершения реакции реакционный раствор распределяли между хлороформом и водой и органический слой сушили над насыщенным раствором сульфата натрия, фильтровали и концентрировали. Остаток растворяли в 2 мл дихлорметана и затем добавляли 6 мг имидазола и 7 мг трет-бутилдиметилсилилхлорида, с последующим перемешиванием при комнатной температуре в течение 5 часов. Реакционный раствор концентрировали и остаток очищали колоночной хроматографией на силикагеле (этилацетат/метанол=1/0 → 8/1), таким образом получая 13 мг указанного в заголовке соединения.
[0729]
Пример 190: Синтез 4-амино-6-(6-фторпиридин-3-ил)-N-(4-(метоксиметил)фенил)-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурой Примера 164, используя (6-фторпиридин-3-ил)бороновую кислоту вместо (4-(гидроксиметил)фенил)бороновой кислоты, получали 47 мг указанного в заголовке соединения.
[0730]
Пример 194: Синтез 4-амино-N-(4-(метоксиметил)фенил)-7-(1-метилциклопропил)-6-(пиримидин-5-ил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
Со ссылкой на Пример 145, реакцию осуществляли с использованием 86 мг пиримидин-5-илбороновой кислоты вместо (4-(гидроксиметил)фенил)бороновой кислоты. К полученному реакционному раствору добавляли этилацетат и воду и органический слой отделяли. Полученный органический слой концентрировали при пониженном давлении и остаток очищали хроматографией на силикагеле (проявляющий растворитель: хлороформ-метанол). После концентрирования полученный остаток очищали снова препаративной обращенно-фазовой ВЭЖХ. После концентрирования остаток очищали снова хроматографией на силикагеле (хлороформ-метанол). Полученный остаток суспендировали в гексане-этилацетате, фильтровали и сушили при пониженном давлении, таким образом получая 10 мг указанного в заголовке соединения.
[0731]
Пример 201: Синтез 4-амино-6-хлор-7-(1-фтор-2-метилпропан-2-ил)-N-(4-(метоксиметил)фенил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
Стадия 1: Синтез метил 4-амино-6-хлор-7-(1-фтор-2- метилпропан-2-ил)-7H-пирроло[2,3-d]пиримидин-5-карбоксилата
Со ссылкой на процедуру синтеза стадии 1 в Примере 56, используя метил 4-амино-7-(1-фтор-2-метилпропан-2-ил)-7H-пирроло[2,3-d]пиримидин-5-карбоксилат, который был синтезирован с использованием 1-фтор-2-метилпропан-2-амин гидрохлорида вместо трет-бутиламина в соответствии с процедурами стадий 1-4 Ссылочного примера 5, вместо метил 4-амино-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин 5-карбоксилата, получали указанное в заголовке соединение (12%).
[0732]
Стадия 2: Синтез 4-амино-6-хлор-7-(1-фтор-2-метилпропан-2-ил)-7H-пирроло[2,3-d]пиримидин-5-карбоновой кислоты
В соответствии с процедурой синтеза стадии 2 в Примере 56, используя метил 4-амино-6-хлор-7-(1-фтор-2-метилпропан-2-ил)-7H-пирроло[2,3-d]пиримидин-5-карбоксилат, полученный на стадии 1, получали указанное в заголовке соединение (75%).
[0733]
Стадия 3: Синтез 4-амино-6-хлор-7-(1-фтор-2-метилпропан-2-ил)-N-(4-(метоксиметил)фенил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурой синтеза стадии 3 в Примере 56, используя 4-амино-6-хлор-7-(1-фтор-2-метилпропан-2-ил)-7H-пирроло[2,3-d]пиримидин-5-карбоновую кислоту, полученную на стадии 2, получали указанное в заголовке соединение (35%).
[0734]
Пример 202: Синтез 4-амино-7-(трет-бутил)-6-хлор-N-(4-(метоксиметил)фенил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
Стадия 1: метил 4-амино-6-хлор-7-(трет-бутил)-7H-пирроло[2,3-d]пиримидин-5-карбоксилат
Со ссылкой на процедуру синтеза стадии 1 в Примере 56, используя метил 4-амино-7-(трет-бутил)-7H-пирроло[2,3-d]пиримидин-5-карбоксилат, полученный на стадии 4 Ссылочного примера 5, вместо метил 4-амино-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксилата, получали указанное в заголовке соединение (11%).
[0735]
Стадия 2: Синтез 4-амино-6-хлор-7-(трет-бутил)-7H-пирроло[2,3-d]пиримидин-5-карбоновой кислоты
В соответствии с процедурой синтеза стадии 2 в Примере 56, используя метил 4-амино-6-хлор-7-(трет-бутил)-7H-пирроло[2,3-d]пиримидин-5-карбоксилат, полученный на стадии 1, получали указанное в заголовке соединение (74%).
[0736]
Стадия 3: Синтез 4-амино-7-(трет-бутил)-6-хлор-N-(4-(метоксиметил)фенил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурой синтеза стадии 3 в Примере 56, используя 4-амино-6-хлор-7-(трет-бутил)-7H-пирроло[2,3-d]пиримидин-5-карбоновую кислоту, полученную на стадии 2, получали указанное в заголовке соединение (46%).
[0737]
Пример 204: Синтез 4-амино-6-(1-гидроксиэтил)-N-(4-(метоксиметил)фенил)-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
23 мг 6-ацетил-4-амино-N-(4-(метоксиметил)фенил)-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида, показанного в Примере 64, растворяли в 2 мл метанола. Добавляли 7 мг борогидрида натрия при комнатной температуре и смесь перемешивали в течение 2 часов. Реакционный раствор распределяли между этилацетатом и водой и органический слой промывали водой и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом натрия, фильтровали и концентрировали. Остаток очищали на колонке с силикагелем (этилацетат/метанол=1/0 → 8/1), таким образом получая 13,6 мг указанного в заголовке соединения.
[0738]
Пример 205: Синтез 4-амино-N-(3-фтор-4-(метоксиметил)фенил)-7-(1-метилциклопропил)-6-((тетрагидро-2H-пиран-4-ил)этинил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурой синтеза Примера 90, используя 4-амино-6-бром-N-(3-фтор-4-(метоксиметил)фенил)-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид, показанный в Ссылочном примере 11, вместо 4-амино-6-бром-N-(4-(метоксиметил)фенил)-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида и используя 4-этинилтетрагидропиран вместо 4-этинил-1-метил-пиразола, получали указанное в заголовке соединение (53%).
[0739]
Пример 206: Синтез 4-амино-N-(3-фтор-4-(метоксиметил)фенил)-7-(1-метилциклопропил)-6-(3-морфолинопроп-1-ин-1-ил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурой синтеза Примера 205, используя 4-проп-2-инилморфолин вместо 4-этинилтетрагидропирана, получали указанное в заголовке соединение (42%).
[0740]
Пример 207: 4-амино-6-этил-N-(4-(метоксиметил)фенил)-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид
Стадия 1: Синтез метил 4-амино-6-этил-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксилата
20 мг метил 4-амино-7-(1-метилциклопропил)-6-винил-7H-пирроло[2,3-d]пиримидин-5-карбоксилата, показанного на стадии 1 Примера 65, растворяли в 5 мл этилацетата и добавляли 5 мг 10% палладия на углероде, с последующим перемешиванием в атмосфере водорода в течение 2 часов. Нерастворимое вещество фильтровали через Целит и фильтрат концентрировали, таким образом получая 20 мг указанного в заголовке соединения.
[0741]
Стадия 2: Синтез 4-амино-6-этил-N-(4-(метоксиметил)фенил)-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурами стадий 1 и 2 Примера 55, используя 4-амино-6-этил-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксилат, полученный на стадии 1, вместо метил 4-амино-6-бром-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксилата, получали указанное в заголовке соединение (26%).
[0742]
Сравнительный пример 1: Синтез 1-(трет-бутил)-3-(п-толуил)пиразолo[3,4-d]пиримидин-4-амина
В соответствии с процедурой синтеза, описанной в Tetrahedron Letters, 52(44), 5761-5763; 2011, получали указанное в заголовке соединение (30%).
[0743]
Сравнительный пример 2: Синтез 4-амино-7-циклопентил-N-(4-феноксифенил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
В соответствии с процедурами синтеза Примера 25, используя 4-феноксиланилин вместо 4-(метоксиметил)анилина, получали указанное в заголовке соединение (79%).
[0744]
Сравнительный пример 3: Синтез 4-амино-7-(трет-бутил)-N-(4-(метоксиметил)фенил)-N-метил-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
Стадия 1: Синтез N-[4-(метоксиметил)фенил]-2-нитро-бензолсульфонамида
1,9 г 2-нитробензолсульфонилхлорида добавляли к раствору 1,0 г 4-(метоксиметил)анилина и 1,5 мл триэтиламина в 10 мл хлороформа и смесь перемешивали в течение ночи. После концентрирования остаток очищали хроматографией на силикагеле (проявляющий растворитель: гексан-этилацетат), концентрировали и сушили при пониженном давлении, таким образом получая 1,89 г указанного в заголовке соединения.
[0745]
Стадия 2: Синтез N-[4-(метоксиметил)фенил]-N-метил-2-нитро-бензолсульфонамида
0,53 мл метилиодида добавляли к суспензии 1,84 г N-[4-(метоксиметил)фенил]-2-нитро-бензолсульфонамида, полученного на стадии 1, и 1,58 г карбоната калия в 20 мл DMF и смесь перемешивали при комнатной температуре в течение 2 часов. Реакционный раствор разбавляли этилацетатом и водой. После экстрагирования этилацетатом полученный органический слой промывали водой два раза и затем промывали насыщенным водным раствором хлорида натрия, с последующей сушкой над безводным сульфатом натрия. Полученный раствор фильтровали, концентрировали и сушили при пониженном давлении, таким образом получая 2,04 г указанного в заголовке соединения.
[0746]
Стадия 3: Синтез 4-(метоксиметил)-N-метил-анилина
1,59 мл 3-метилбензолтиола добавляли к суспензии 2,51 г N-[4-(метоксиметил)фенил]-N-метил-2-нитро-бензолсульфонамида, полученного на стадии 2, и 2,51 г карбоната калия в 10 мл DMF и смесь перемешивали при комнатной температуре в течение 5 часов. Реакционный раствор разбавляли этилацетатом-водой и экстрагировали этилацетатом. Полученный органический слой промывали водой два раза и затем промывали насыщенным водным раствором хлорида натрия, с последующей сушкой над безводным сульфатом натрия. Полученный раствор фильтровали и концентрировали и полученный остаток очищали хроматографией на силикагеле, концентрировали и сушили при пониженном давлении, таким образом получая 0,81 г указанного в заголовке соединения.
[0747]
Стадия 4: Синтез 4-амино-7-(трет-бутил)-N-(4-(метоксиметил)фенил)-N-метил-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
Раствор 59 мг 4-(метоксиметил)-N-метил-анилин, 48 мкл of 1,8-диазабицикло[5.4.0]ундец-7-ена, 12 мг комплекса 1,1'-бис(дифенилфосфино)ферроцен-палладий (II) дихлорид-дихлорметан и 50 мг 7-(трет-бутил)-5-иод-7H-пирроло[2,3-d]пиримидин-4-амина, показанного на стадии 3 Ссылочного примера 5, в 1 мл DMA перемешивали в атмосфере оксида углерода при 110°C в течение 1,5 часа. Реакционный раствор очищали хроматографией на силикагеле (проявляющий растворитель: хлороформ-метанол), концентрировали и очищали снова препаративной обращенно-фазовой системой. После концентрирования полученный остаток суспендировали и промывали смесью гексан-этилацетат, фильтровали и сушили при 60°C при пониженном давлении, таким образом получая 3,5 мг указанного в заголовке соединения.
[0748]
Сравнительный пример 4: Синтез 7-(трет-бутил)-N-(4-(метоксиметил)фенил)-4-(метиламино)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
Стадия 1: Синтез 7-(трет-бутил)-5-иод-N-метил-7H-пирроло[2,3-d]пиримидин-4-амина
400 мг 7-(трет-бутил)-4-хлор-5-иод-7H-пирроло[2,3-d]пиримидина, показанного на стадии 2 Ссылочного примера 5, добавляли к 10 мл раствора метиламина в THF и смесь перемешивали при 120°C в течение 12 часов в микроволновом реакторе. Полученный реакционный раствор концентрировали и очищали хроматографией на щелочном силикагеле (проявляющий растворитель: гексан-этилацетат), с последующим концентрированием, таким образом получая 400 мг указанного в заголовке соединения.
[0749]
Стадия 2: Синтез 7-(трет-бутил)-N-(4-(метоксиметил)фенил)-4-(метиламино)-7H-пирроло[2,3-d]пиримидин-5-карбоксамида
7-(трет-бутил)-5-иод-N-метил-7H-пирроло[2,3-d]пиримидин-4-амин, полученный на стадии 1, 103 мг 4-(метоксиметил)анилин, 90 мкл 1,8-диазабицикло[5.4.0]ундец-7-ена и 24 мг комплекса 1,1'-бис(дифенилфосфино)ферроцен-палладий(II) дихлорид-дихлорметан добавляли к 1 мл DMA и смесь перемешивали в атмосфере оксида углерода при 110°C в течение 2 часов. Полученный реакционный раствор очищали хроматографией на силикагеле (проявляющий растворитель: гексан-этилацетат), концентрировали и очищали снова хроматографией на щелочном силикагеле, с последующим концентрированием, таким образом получая 52 мг указанного в заголовке соединения.
[0750]
Сравнительный пример 5: Синтез 4-амино-N-(4-(метоксиметил)фенил)-1-фенил-1H-пиразолo[3,4-d]пиримидин-3-карбоксамида
В соответствии с процедурой синтеза Примера 1, используя 4-амино-1-фенил-1H-пиразолo[3,4-d]пиримидин-3-карбоновую кислоту, показанную в Ссылочном примере 12, вместо 4-амино-1-циклопентил-1H-пиразолo[3,4-d]пиримидин-3-карбоновой кислоты, получали указанное в заголовке соединение (33%).
[0751]
Таблицы 11-34 показывают структурные формулы и физические свойства соединений, полученных в Примерах и Сравнительных примерах.
[0752]
Таблица 11

[0753]
Таблица 12
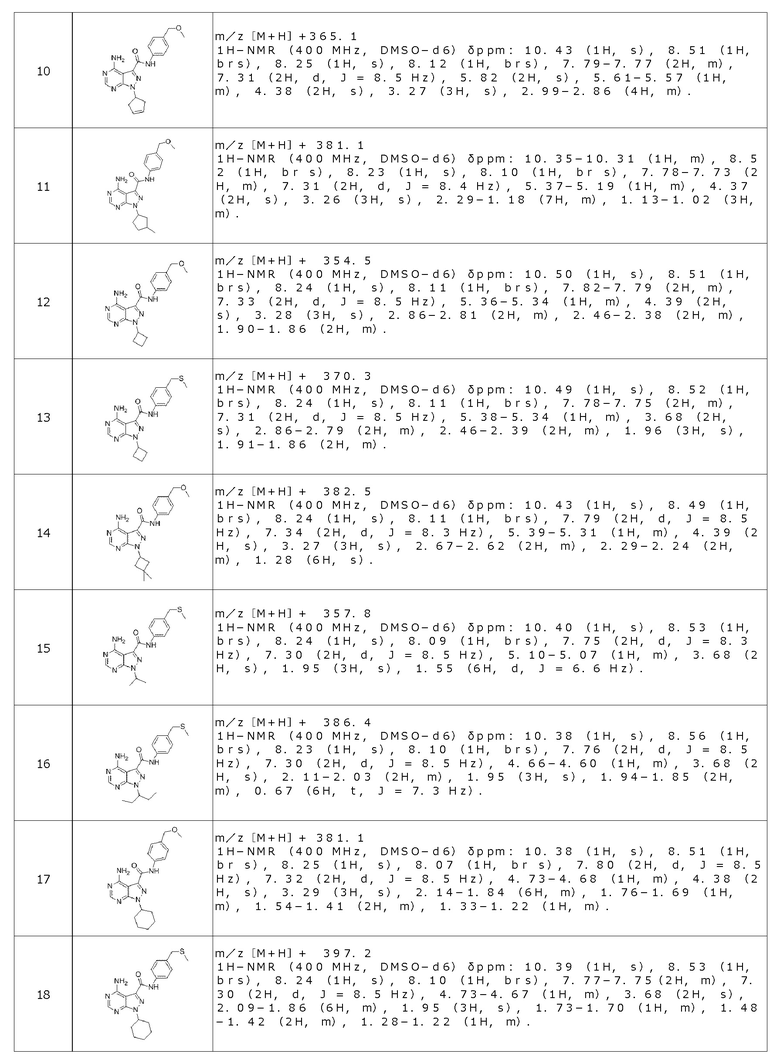
[0754]
Таблица 13
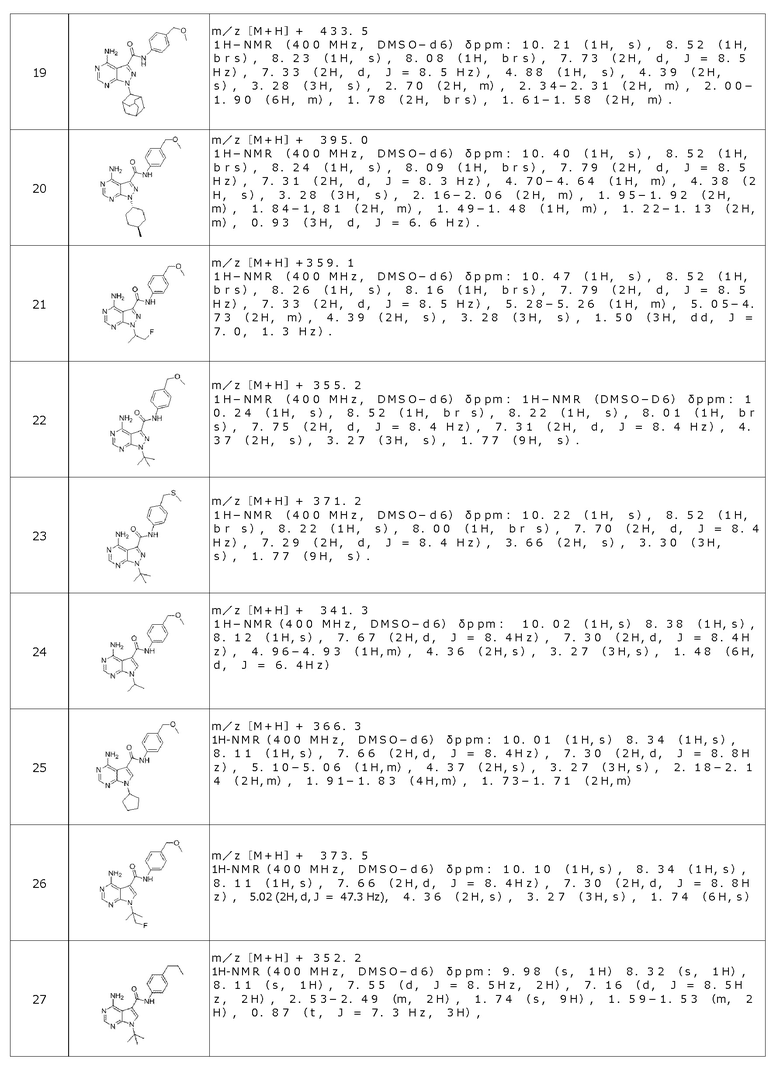
[0755]
Таблица 14

[0756]
Таблица 15

[0757]
Таблица 16

[0758]
Таблица 17

[0759]
Таблица 18
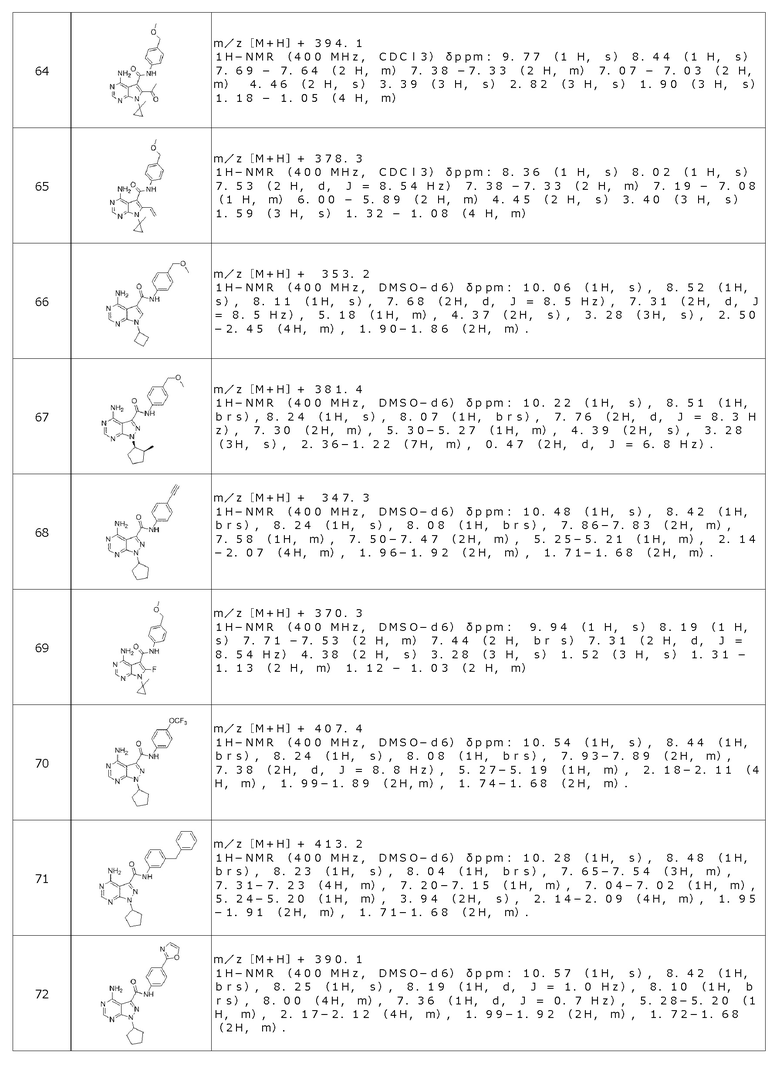
[0760]
Таблица 19

[0761]
Таблица 20

[0762]
Таблица 21

[0763]
Таблица 22

[0764]
Таблица 23
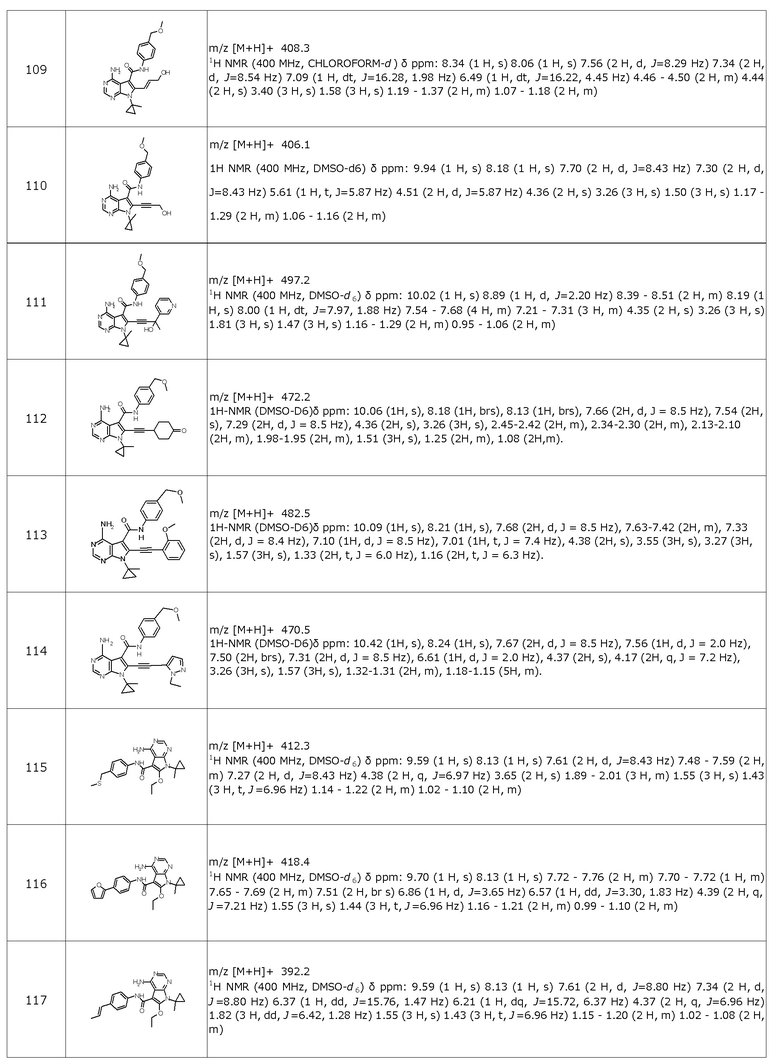
[0765]
Таблица 24

[0766]
Таблица 25

[0767]
Таблица 26

[0768]
Таблица 27

[0769]
Таблица 28

[0770]
Таблица 29

[0771]
Таблица 30

[0772]
Таблица 31
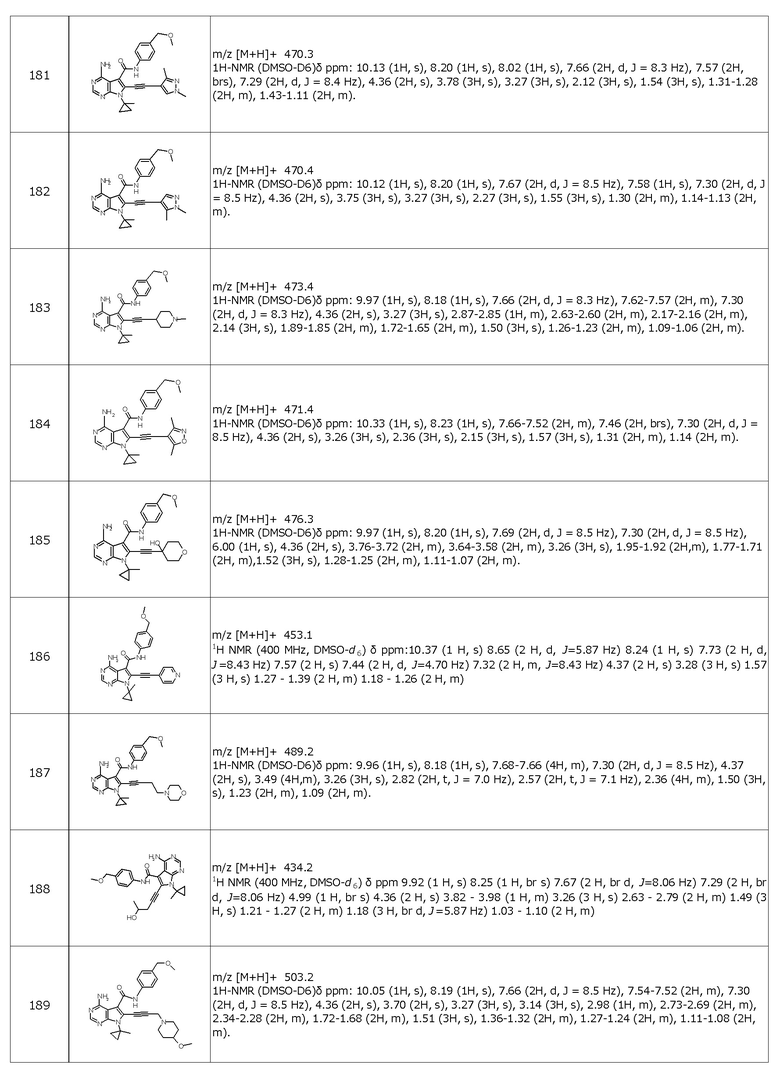
[0773]
Таблица 32

[0774]
Таблица 33
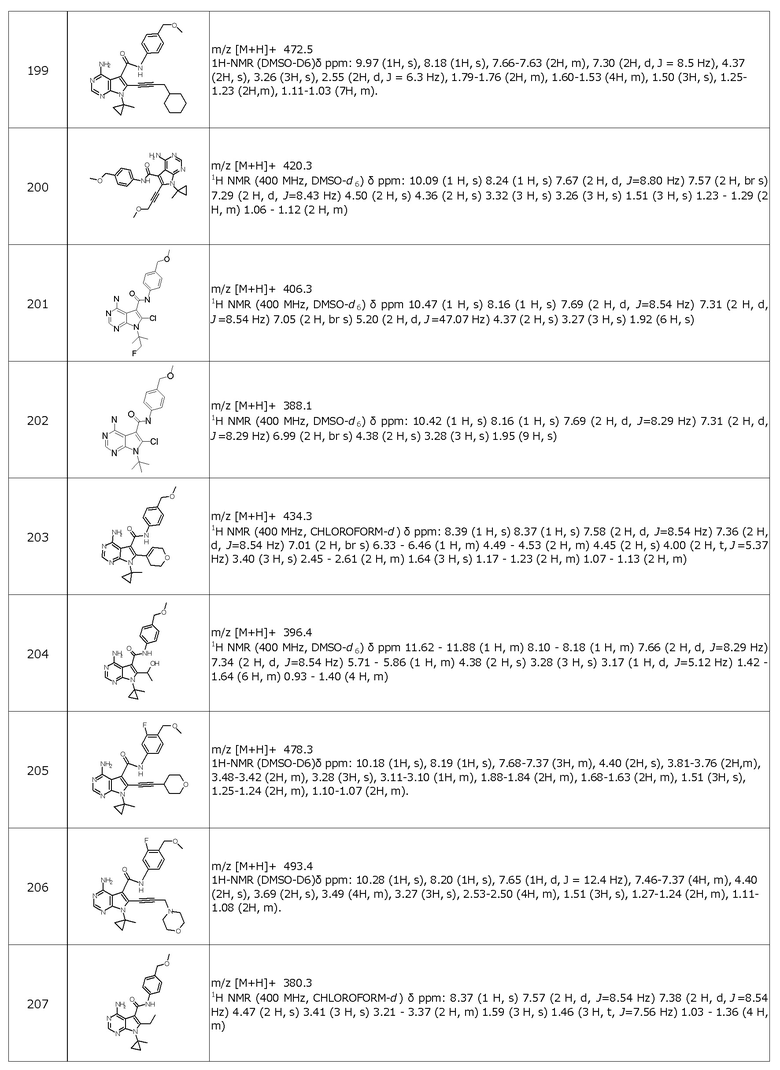
[0775]
Таблица 34

[0776]
Пример испытаний 1: Измерение ингибиторной активности против RET (in vitro)
Что касается условий для измерения in vitro ингибиторной активности соединений против киназной активности RET, веб-сайт AnaSpec указывает, что Srctide (GEEPLYWSFPAKKK) соответствует пептидному субстрату для реакции для измерения киназной активности RET. Таким образом, аминокислотная последовательность была частично модифицирована и биотинилирована для получения биотинилированных пептидов (биотин-EEPLYWSFPAKKK). Очищенный рекомбинантный человеческий RET белок, используемый в испытании, закупали у Carna Biosciences, Inc.
[0777]
Для измерения ингибиторной активности сначала соединения по настоящему изобретению индивидуально разбавляли диметилсульфоксидом (DMSO) постепенно. Затем RET белок, пептидный субстрат (конечная концентрация: 250 нМ), хлорид магния (конечная концентрация: 10 мМ), АТФ (конечная концентрация: 10 мкМ) и раствор соединения по настоящему изобретению в DMSO (конечная концентрация DMSO: 2,5%) добавляли к буферу для киназной реакции (13,5 мМ Tris, pH 7,5, 2 мМ дитиотреитола, 0,009% Tween-20). Каждую из смесей инкубировали при 25°C в течение 100 минут для осуществления киназной реакции. Затем добавляли EDTA с получением конечной концентрации 24 мМ для остановки реакции. Добавляли раствор для детекции, содержащий Eu-меченное антифосфотирозиновое антитело PT66 (PerkinElmer) и SureLight APC-SA (PerkinElmer), и каждой смеси давали выстояться при комнатной температуре в течение 2 часов или больше. В завершение, интенсивность флуоресценции под возбуждающим светом с длиной волны 337 нм измеряли с использованием PHERAstar FS (BMG Labtech) при двух длинах волн 620 нм и 665 нм. Уровень фосфорилирования рассчитывали из отношения интенсивности флуоресценции при двух длинах волн, и концентрацию соединения, при которой фосфорилирование ингибировалось на 50%, определяли как IC50 значение (нМ).
[0778]
Таблицы 35 и 36 показывают IC50 (нМ) ингибиторной активности против RET для Вандетаниба, соединений Примеров и соединений 2-5 Сравнительных примеров.
[0779]
Известно, что Вандетаниб обладает высокой ингибиторной активностью против RET (Carlomagno F. Cancer Res. 2002 Dec 15; 62(24): 7284-90). Было обнаружено, что соединения по настоящему изобретению или их соли, представленные соединениями Примеров, демонстрируют in vitro ингибиторную активность против RET на уровне, эквивалентном Вандетанибу или выше. В отличие от этого, соединения 2-5 Сравнительных примеров продемонстрировали значительно более низкую ингибиторную активность против RET.
[0780]
Таблица 35

[0781]
Таблица 36 (продолжение)

[0782]
Пример испытаний 2: Селективность в отношении RET по сравнению с другими киназами(in vitro)
Поскольку мультикиназные ингибиторы ингибируют не только RET, но также различные сигнальные пути для подавления клеточного роста и других функций, эти ингибиторы вызывают опасения, связанные с различными возможными побочными эффектами, в связи с чем может потребоваться уменьшение дозы или лекарственные каникулы, приводящие к недостаточной RET-ингибирующей активности. Далее обсуждается селективность соединений по настоящему изобретению или их солей в отношении RET по сравнению с другими киназами.
1) Измерение ингибиторной активности против RET
Ингибиторную активность против RET измеряли таким же способом, как в Примере испытаний 1.
2) Измерение ингибиторной активности против SRC
Что касается условий для измерения in vitro ингибиторной активности соединений против киназной активности SRC, прайс-лист расходуемых реагентов LabChip-серии от PerkinElmer показывает, что FL-Пептид 4 соответствует пептидному субстрату для измерения киназной активности SRC. Таким образом, FL-Пептид 4 использовали в качестве субстрата. Очищенный рекомбинантный человеческий SRC белок, используемый в испытании, закупали у Carna Biosciences, Inc.
[0783]
Для измерения ингибиторной активности сначала испытываемые соединения индивидуально разбавляли диметилсульфоксидом (DMSO) постепенно. Затем SRC белок, FL-Пептид 4 (конечная концентрация: 1,5 мкМ), хлорид магния (конечная концентрация: 10 мМ), АТФ (конечная концентрация: 15 мкМ) и раствор испытываемого соединения в DMSO (конечная концентрация DMSO: 5%) добавляли к реакционному буферу (100 мМ HEPES, pH 7,0, 1 мМ дитиотреитола, 0,003% Brij35, 0,04% Tween-20), содержащему коктейль ингибиторов фосфатаз (PhosSTOP, Roche) и коктейль ингибиторов протеаз (cOmplete Mini, EDTA-free, Roche) при рекомендованных концентрациях. Каждую смесь инкубировали при 30°C в течение 90 минут для осуществления киназной реакции. Затем добавляли EDTA, разбавленную разделительным буфером, доступным от PerkinElmer (конечная концентрация: 30 мМ), для остановки киназной реакции. В завершение, нефосфорилированные субстратные пептиды (S) и фосфорилированные пептиды (P) разделяли и осуществляли детекцию методом микроканального капиллярного электрофореза с использованием считывающего устройства EZ Reader II (PerkinElmer). Уровень фосфорилирования рассчитывали из высоты пиков S и P, и концентрацию соединения, при которой фосфорилирование ингибировалось на 50%, определяли как IC50 значение (нМ).
3) Измерение ингибиторной активности против LCK
Что касается условий для измерения in vitro ингибиторной активности соединений против киназной активности LCK, веб-сайт AnaSpec указывает, что Srctide (GEEPLYWSFPAKKK) соответствует пептидному субстрату для реакции для измерения киназной активности LCK. Таким образом, аминокислотная последовательность была частично модифицирована и биотинилирована для получения биотинилированных пептидов (биотин-EEPLYWSFPAKKK). Очищенный рекомбинантный человеческий LCK белок, используемый в испытании, закупали у Carna Biosciences, Inc.
[0784]
Для измерения ингибиторной активности сначала испытываемые соединения индивидуально разбавляли диметилсульфоксидом (DMSO) постепенно. Затем LCK белок, пептидные субстраты (конечная концентрация: 250 нМ), хлорид магния (конечная концентрация: 10 мМ), АТФ (конечная концентрация: 50 мкМ) и раствор испытываемого соединения в DMSO (конечная концентрация DMSO: 5%) добавляли к буферу для киназной реакции (13,5 мМ Tris, pH 7,5, 2 мМ дитиотреитола, 0,009% Tween-20). Каждую смесь инкубировали при 25°C в течение 60 минут для осуществления киназной реакции. Затем добавляли EDTA с получением конечной концентрации 40 мМ для остановки реакции. Добавляли раствор для детекции, содержащий Eu-меченное антифосфотирозиновое антитело PT66 (PerkinElmer) и SureLight APC-SA (PerkinElmer), и каждой смеси давали выстояться при комнатной температуре в течение 2 часов или больше. В завершение, измеряли интенсивность флуоресценции под возбуждающим светом с длиной волны 337 нм с использованием PHERAstar FS (BMG Labtech) при двух длинах волн 620 нм и 665 нм. Уровень фосфорилирования рассчитывали из отношения интенсивности флуоресценции при двух длинах волн, и концентрацию соединения, при которой фосфорилирование ингибировалось на 50%, определяли как IC50 значение (нМ).
4) Измерение ингибиторной активности против AURB (Aurora B)
In vitro ингибиторную активность соединений против AURB киназы измеряли со ссылкой на процедуру, описанную в JP2008-81492A. Очищенный рекомбинантный человеческий AURB белок, используемый в испытании, закупали у Carna Biosciences, Inc.
[0785]
Для измерения ингибиторной активности сначала испытываемые соединения индивидуально разбавляли диметилсульфоксидом (DMSO) постепенно. Затем AURB белок, FL-Пептид 21 (caliper Life Sciences, конечная концентрация: 100 нМ), хлорид магния (конечная концентрация: 1 мМ), АТФ (конечная концентрация: 40 мкМ) и раствор испытываемого соединения в DMSO (конечная концентрация DMSO: 5%) добавляли к буферному раствору для киназной реакции (20 мМ HEPES, pH 7,4, 2 мМ дитиотреитола, 0,01% Tween-20) и каждую смесь инкубировали при 25°C в течение 60 минут для осуществления киназной реакции. IMAP Прогрессивный Связывающий Реагент, разбавленный IMAP Прогрессивным Связывающим Буфером A (1:500 разведение, Molecular Devices, LLC.), добавляли для остановки киназной реакции. Реакционному раствору давали выстояться в темном месте при комнатной температуре в течение 120 минут и уровень фосфорилирования рассчитывали из степени поляризации флуоресценции, измеренной при помощи PHERAstar (BMG LABTECH, длина волны возбуждения: 485 нм, длиной волны детекции: 520 нм). Концентрацию соединения, при которой фосфорилирование ингибировалось на 50%, определяли как IC50 значение (нМ).
5) Измерение ингибиторной активности против EGFR
Что касается условий для измерения in vitro ингибиторной активности соединений против EGFR киназной активности, прайс-лист расходных реагентов LabChip (торговая марка) серии от PerkinElmer показывает, что FL-Пептид 22 соответствует пептидному субстрату для измерения киназной активности EGFR. Таким образом, со ссылкой на аминокислотную последовательность, получали биотинилированный пептид (биотин-EEPLYWSFPAKKK). Очищенный рекомбинантный человеческий EGFR белок, используемый в испытании, закупали у Carna Biosciences, Inc.
[0786]
Для измерения ингибиторной активности сначала испытываемые соединения индивидуально разбавляли диметилсульфоксидом (DMSO) постепенно. Затем EGFR белок, пептидный субстрат (конечная концентрация: 250 нМ), хлорид магния (конечная концентрация: 10 мМ), хлорид марганца (конечная концентрация: 10 мМ), АТФ (конечная концентрация: 1,5 мкМ) и раствор испытываемого соединения в DMSO (конечная концентрация DMSO: 2,5%) добавляли к буферному раствору для киназной реакции (Carna Biosciences, Inc.). Каждую смесь инкубировали при 25°C в течение 120 минут для осуществления киназной реакции. Затем добавляли EDTA с получением конечной концентрации 24 мМ для остановки реакции. Добавляли раствор для детекции, содержащий Eu-меченное антифосфотирозиновое антитело PT66 (PerkinElmer) и SureLight APC-SA (PerkinElmer), и каждой смеси давали выстояться при комнатной температуре в течение 2 часов или больше. В завершение, интенсивность флуоресценции под возбуждающим светом с длиной волны 337 нм измеряли с использованием PHERAstar FS (BMG Labtech) при двух длинах волн 620 нм и 665 нм. Уровень фосфорилирования рассчитывали из отношения интенсивности флуоресценции при двух длинах волн, и концентрацию соединения, при которой фосфорилирование ингибировалось на 50%, определяли как IC50 значение (нМ).
6) Селективность ингибирования в отношении RET
Из значений, полученных в разделах 1) - 5) выше, рассчитывали отношения SRC-ингибирующая активность IC50 (нМ)/RET-ингибирующая активность IC50 (нМ), LCK-ингибирующая активность IC50 (нМ)/RET-ингибирующая активность IC50 (нМ), AURB-ингибирующая активность IC50 (нМ)/RET-ингибирующая активность IC50 (нМ) и EGFR-ингибирующая активность IC50 (нМ)/RET-ингибирующая активность IC50 (нМ) и исследовали селективность ингибирования RET испытываемыми соединениями.
[0787]
Таблицы 37-44 показывают результаты. Таблицы 37-44 показывают, что соединения по настоящему изобретению или их соли, представленные соединениями Примеров, продемонстрировали более высокую селективность ингибирования RET относительно ингибирования SRC, LCK, Aurora B и EGFR, по сравнению с соединением 1 Сравнительных примеров. Соединения по настоящему изобретению или их соли также продемонстрировали отличную селективность ингибировани RET по сравнению с другими киназами (PI3K, TrkB). Таким образом, результаты дают основание предположить, что соединения по настоящему изобретению или их соли имеют низкий потенциал побочных эффектов, которые относят за счет ингибирования киназ, отличных от RET.
[0788]
Таблица 37

[0789]
Таблица 38 (продолжение)
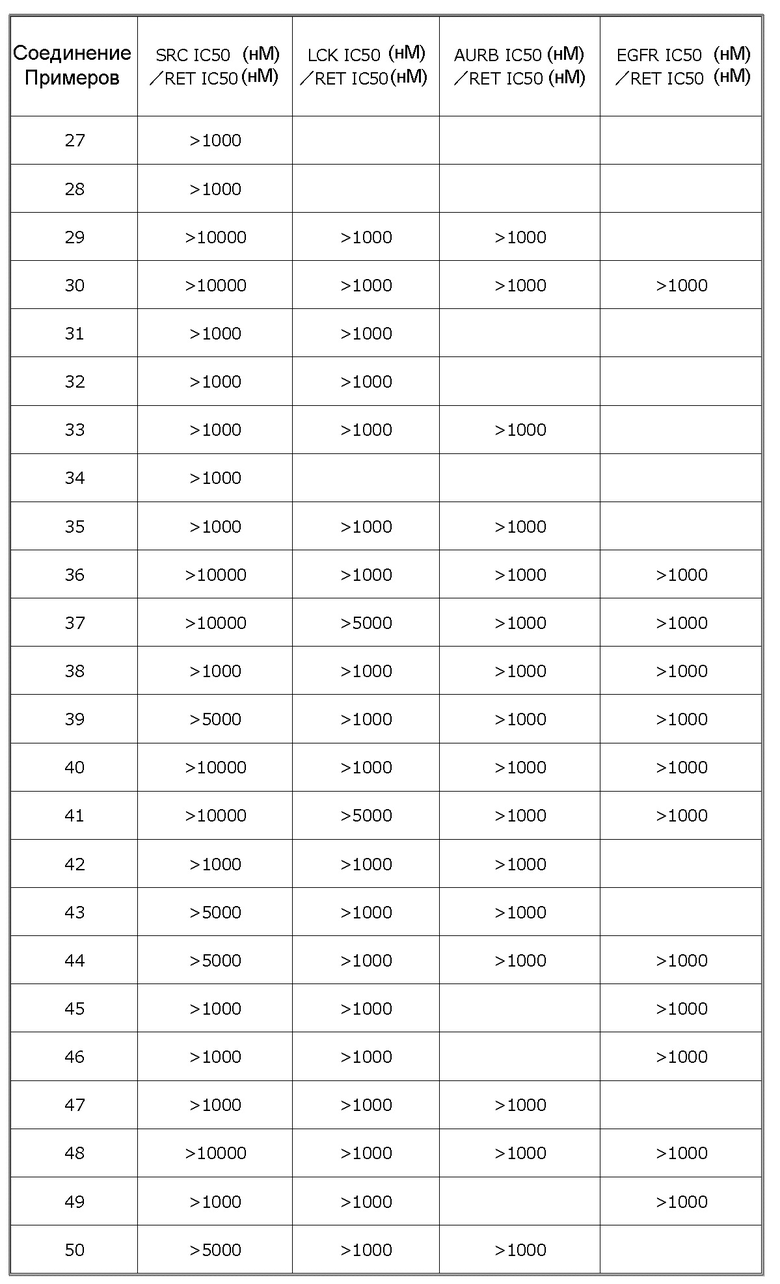
[0790]
Таблица 39 (продолжение)
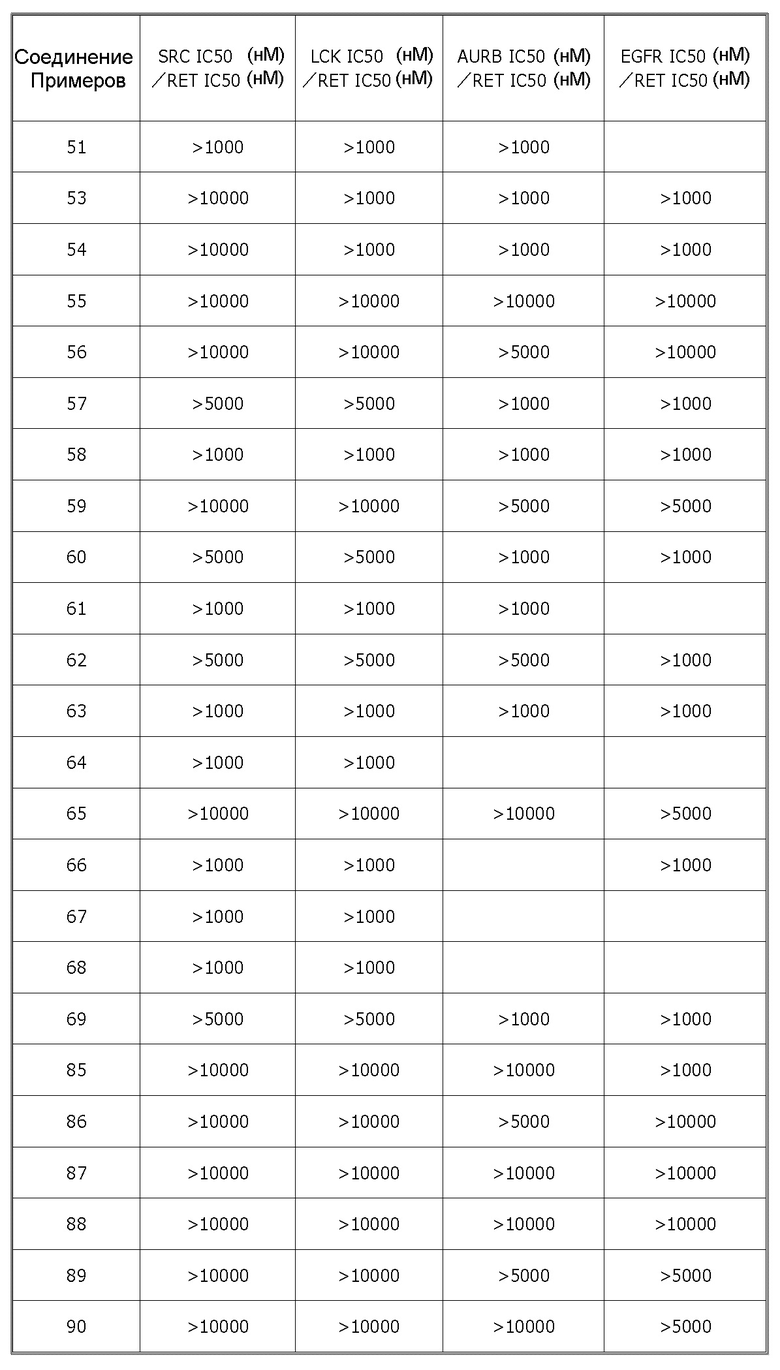
[0791]
Таблица 40 (продолжение)
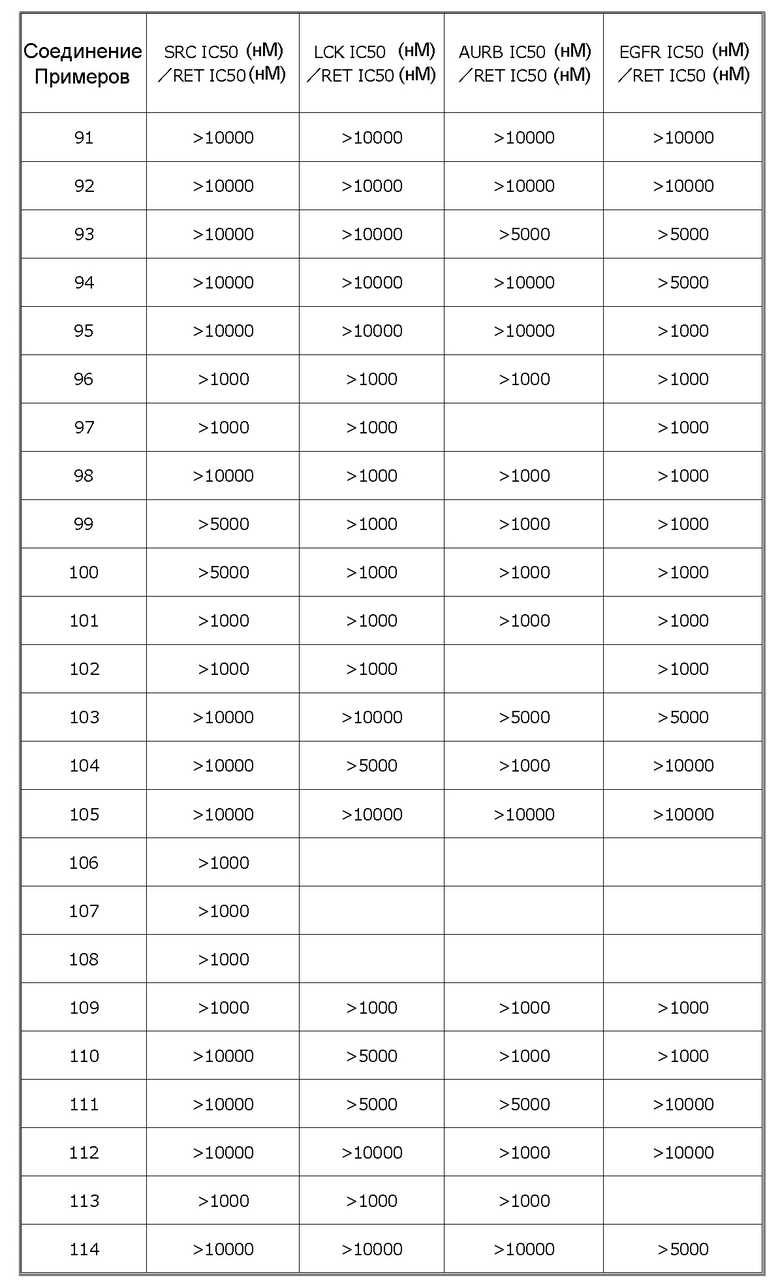
[0792]
Таблица 41 (продолжение)
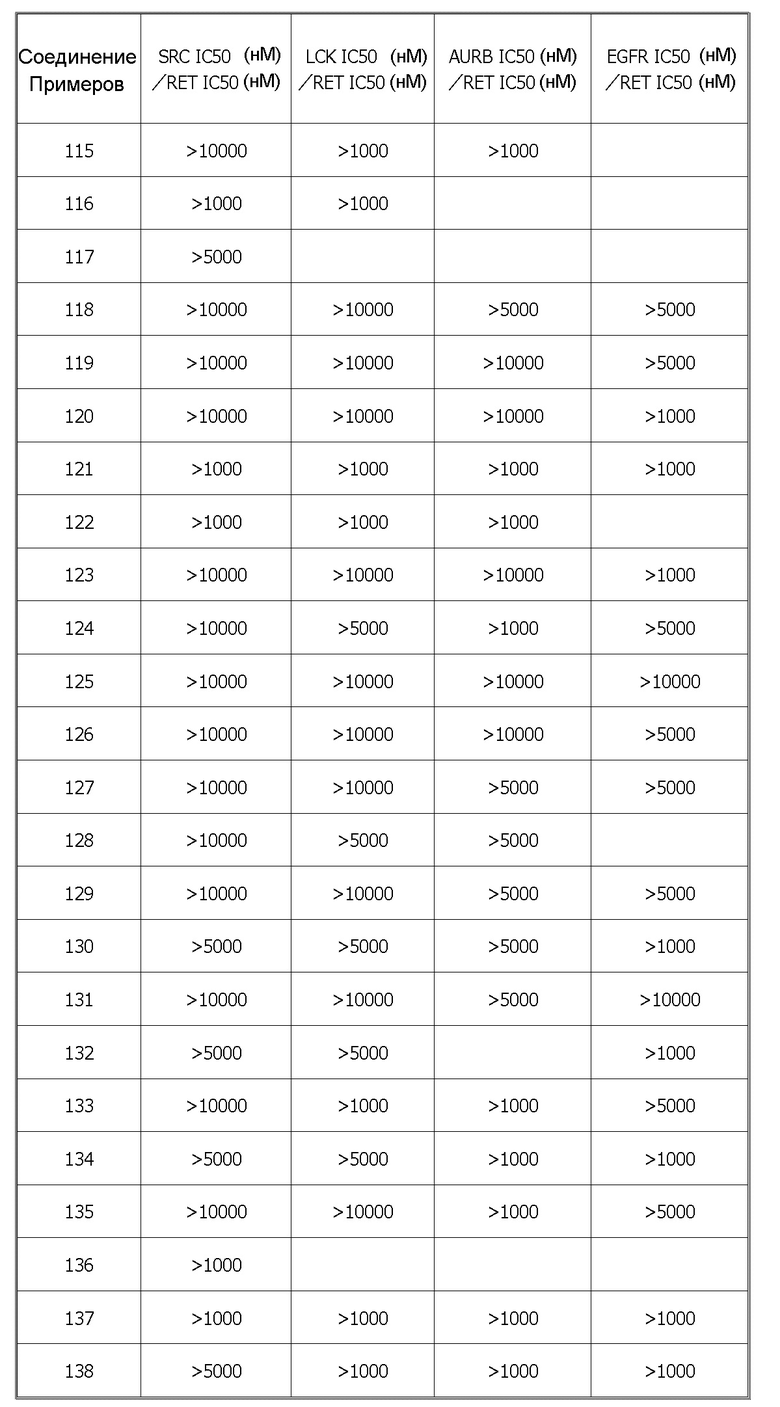
[0793]
Таблица 42 (продолжение)

[0794]
Таблица 43 (продолжение)

[0795]
Таблица 44 (продолжение)

Пример испытаний 3: Ингибиторная активность против мутации резистентности RET (in vitro)
1) Измерение ингибиторной активности против RET (V804L)
Что касается условий для измерения in vitro ингибиторной активности соединений против RET (V804L) (т.е. RET с V804L мутацией) киназной активности, веб-сайт AnaSpec указывает, что Srctide (GEEPLYWSFPAKKK) соответствует пептидному субстрату для реакции для измерения киназной активности RET. Таким образом, аминокислотная последовательность была частично модифицирована и биотинилирована для получения биотинилированных пептидов (биотин-EEPLYWSFPAKKK). Очищенный рекомбинантный человеческий RET (V804L) белок, используемый в испытании, закупали у Eurofins.
[0797]
Для измерения ингибиторной активности сначала испытываемые соединения индивидуально разбавляли диметилсульфоксидом (DMSO) постепенно. Затем RET (V804L) белок, пептидные субстраты (конечная концентрация: 250 нМ), хлорид магния (конечная концентрация: 10 мМ), АТФ (конечная концентрация: 10 мкМ) и раствор испытываемого соединения в DMSO (конечная концентрация DMSO: 5%) добавляли к буферу для киназной реакции (13,5 мМ Tris, pH 7,5, 2 мМ дитиотреитола, 0,009% Tween-20). Каждую из смесей инкубировали при 25°C в течение 120 минут для осуществления киназной реакции. Затем добавляли EDTA с получением конечной концентрации 40 мМ для остановки реакции. Добавляли раствор для детекции, содержащий Eu-меченное антифосфотирозиновое антитело PT66 (PerkinElmer) и SureLight APC-SA (PerkinElmer), и каждой смеси давали выстояться при комнатной температуре в течение 2 часов или больше. В завершение, интенсивность флуоресценции под возбуждающим светом с длиной волны 337 нм измеряли с использованием PHERAstar FS (BMG Labtech) при двух длинах волн 620 нм и 665 нм. Уровень фосфорилирования рассчитывали из отношения интенсивности флуоресценции при двух длинах волн, и концентрацию соединения, при которой фосфорилирование ингибировалось на 50%, определяли как IC50 значение (нМ).
1)Измерение ингибиторной активности Против RET (V804M)
RET (V804M) (т.е. RET с V804M мутацией) киназную активность измеряли с использованием очищенного рекомбинантного человеческого RET (V804M) белка, который закупали у Eurofins, с конечной концентрацией АТФ 13 мкМ в системе киназной реакции, следуя процедуре 1), что касается остальной части.
[0798]
Таблицы 45-48 показывают IC50 (нМ) значение ингибиторной активности против RET с мутацией резистентности для соединений Примеров, Вандетаниба и соединений 1-4 Сравнительных примеров.
[0799]
Известно, что Вандетаниб обладает высокой ингибиторной активностью против RET (Carlomagno F. Cancer Res. 2002 Dec 15; 62(24): 7284-90). Однако Вандетаниб продемонстрировал существенно низкую ингибиторную активность против RET (V804L) и RET (V804M).
[0800]
Соединения 1-4 Сравнительных примеров также продемонстрировали существенно низкую ингибиторную активность против RET (V804L) и RET (V804M).
[0801]
Были сообщения о том, что Алектиниб демонстрирует ингибиторный эффект в отношении RET (V804L) и имеет IC50 32 (нМ) in vitro (Mol Cancer Ther. 2014 Dec; 13 (12): 2910-8). Соединения по настоящему изобретению или их соли, представленные соединениями Примеров, продемонстрировали отличную ингибиторную активность против RET (V804L) на уровне, эквивалентном или выше чем у Алектиниба. Соединения по настоящему изобретению или их соли, представленные соединениями Примеров, также продемонстрировали высокую ингибиторную активность против RET (V804M). Результаты дают основание предположить, что соединения по настоящему изобретению или их соли обладают противоопухолевым эффектом на рак и опухоли, экспрессирующие RET с мутацией в его gatekeeper сайте (например, V804L и V804M).
[0802]
Таблица 45

[0803]
Таблица 46 (продолжение)

[0804]
Таблица 47 (продолжение)
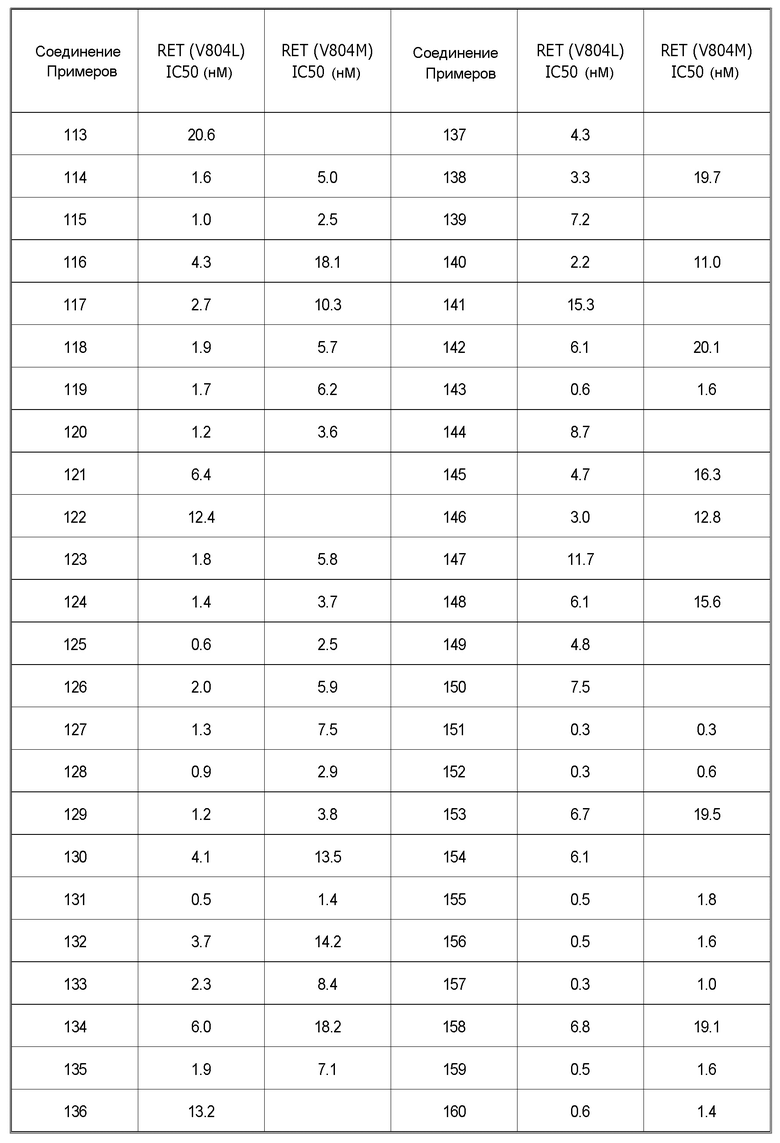
[0805]
Таблица 48 (продолжение)

[0806]
Пример испытаний 4: Оценка стабильности в микросомах печени
Растворы испытываемых соединений в DMSO/ацетонитриле (конечная концентрация каждого испытываемого соединения 1 мкМ, конечная концентрация DMSO 0,01%, и конечная концентрация ацетонитрила 1%) индивидуально добавляли к раствору смеси микросом печени (микросомы печени мыши с конечной концентрацией 0,25 мг/мл, фосфатно-калиевый буфер с конечной концентрацией 100 мМ и хлорид магния с конечной концентрацией 3 мМ) и каждую смесь предварительно инкубировали при 37°C в течение 5 минут. NADPH-генерирующую систему (глюкозо-6-фосфат с конечной концентрацией 10 мМ, окисленный никотинамидаденин динуклеотидфосфат с конечной концентрацией 1 мМ и глюкозо-6-фосфатдегидрогеназа с конечной концентрацией 1 Ед./мл) добавляли к части раствора каждой смеси и начинали метаболическую реакцию. После инкубации при 37°C в течение 30 минут добавляли двукратное количество этанола для остановки реакции, таким образом получая пост-реакционные образцы. Добавляли двукратное количество этанола к каждому из оставшихся растворов смеси и затем добавляли NADPH-генерирующую систему, таким образом получая пред-реакционные образцы. Пред-реакционные образцы и пост-реакционные образцы центрифугировали при 2000×g и их супернатант фильтровали через стеклянный фильтр. Каждый фильтрат затем вводили в систему ЖХ-МС/МС и определяли МС/МС пики испытываемых соединений. Из отношения пост-реакционного МС/МС пика к пред-реакционному МС/МС пику испытываемых соединений рассчитывали процент оставшихся испытываемых соединений (оставшийся %).
[0807]
Таблица 49 показывает результаты. В то время как соединения 1 и 2 Сравнительных примеров имели оставшийся процент 0% в любом случае, соединения по настоящему изобретению или их соли, представленные соединениями Примеров, имели высокий оставшийся процент. Это означает, что соединения по настоящему изобретению или их соли существенно более стабильны в микросомах печени мыши, чем соединения Сравнительных примеров.
[0808]
Таблица 49

[0809]
Пример испытаний 5: Оценка пероральной абсорбции
Соединения по настоящему изобретению суспендировали или растворяли в 0,5% HPMC и 0,1N хлористоводородной кислоте и перорально вводили BALB/cA мышам. В точке времени 0,5, 1, 2, 4 и 6 часов после перорального введения кровь мышей собирали из глазного дна для получения плазмы. Концентрацию соединений в полученной плазме измеряли при помощи ЖХ-МС/МС и оценивали пероральную абсорбцию.
[0810]
Результаты показывают, что концентрация соединений по настоящему изобретению в плазме была достаточной, что указывает на отличную пероральную абсорбцию.
[0811]
Пример испытаний 6: Оценка эффекта ингибирования клеточного роста (1)
Испытание цитотоксичности in vitro осуществляли на TT клетках (клеточная линия рака щитовидной железы человека с RET активирующей мутацией (C634W)).
[0812]
Суспензию TT клеток, полученную со средой Хэма F12K (kaighn's) (Life Technologies Japan), содержащей 10% FBS, инокулировали в каждую лунку 96-луночного плоскодонного микропланшета в количестве 5×103 клеток/лунка (0,15 мл) и культивировали в инкубаторе, содержащем 5% диоксида углерода, при 37°C в течение ночи (день 0). Соединения по настоящему изобретению индивидуально растворяли в диметилсульфоксиде с получением концентрации 10 мМ и затем разбавляли 10% FBS-содержащей RPMI1640 средой (изготовитель Wako Pure Chemical Industries, Ltd.), чтобы соединения по настоящему изобретению соответственно имели конечную концентрацию 40, 12, 4, 1,2, 0,4, 0,12, 0,04 и 0,012 мкМ. Соединения в разных концентрациях индивидуально добавляли в лунки содержащего TT клетки культурального планшета, описанного выше, в количестве 0,05 мл/лунка (день 1) и культивировали в инкубаторе, содержащем 5% диоксида углерода, при 37°C в течение 7 дней. После культивирования (день 8) 0,1 мл среды удаляли из каждой лунки и добавляли 0,1 мл CellTiter Glo 2.0 реагента (Promega Corporation), который представляет собой реагент для детекции внутриклеточного АТФ люминесцентным методом, с последующим встряхиванием в течение 1 минуты. После встряхивания каждой культуре давали выстояться при комнатной температуре в течение 15 минут и хемилюминесценцию измеряли с использованием люминометра, и использовали в качестве показателя количества жизнеспособных клеток. Процент роста от дня 1 при разных концентрациях соединений рассчитывали из следующих уравнений, в зависимости от значения Tдень 8 и Cдень 1, для определения концентрации (GI50 (нМ)) испытываемых соединений, способной подавлять клеточный рост на 50%.
1) Tдень 8≥Cдень 1
Процент роста (%)=(Tдень 8-Cдень 1)/(Cдень 8-Cдень 1)×100
2) Tдень 8<Cдень 1
Процент роста (%)=(Tдень 8-Cдень 1)/(Cдень 1)×100
T: Поглощение в лунке, в которую добавляли испытываемое соединение.
C: Поглощение в лунке, в которую не добавляли испытываемое соединение.
День 1: День, в который добавляли испытываемое соединение.
День 8: День, в который осуществляли оценку.
Таблица 50 показывает результаты. Соединения по настоящему изобретению продемонстрировали высокий эффект ингибирования роста TT клеток.
[0813]
Таблица 50
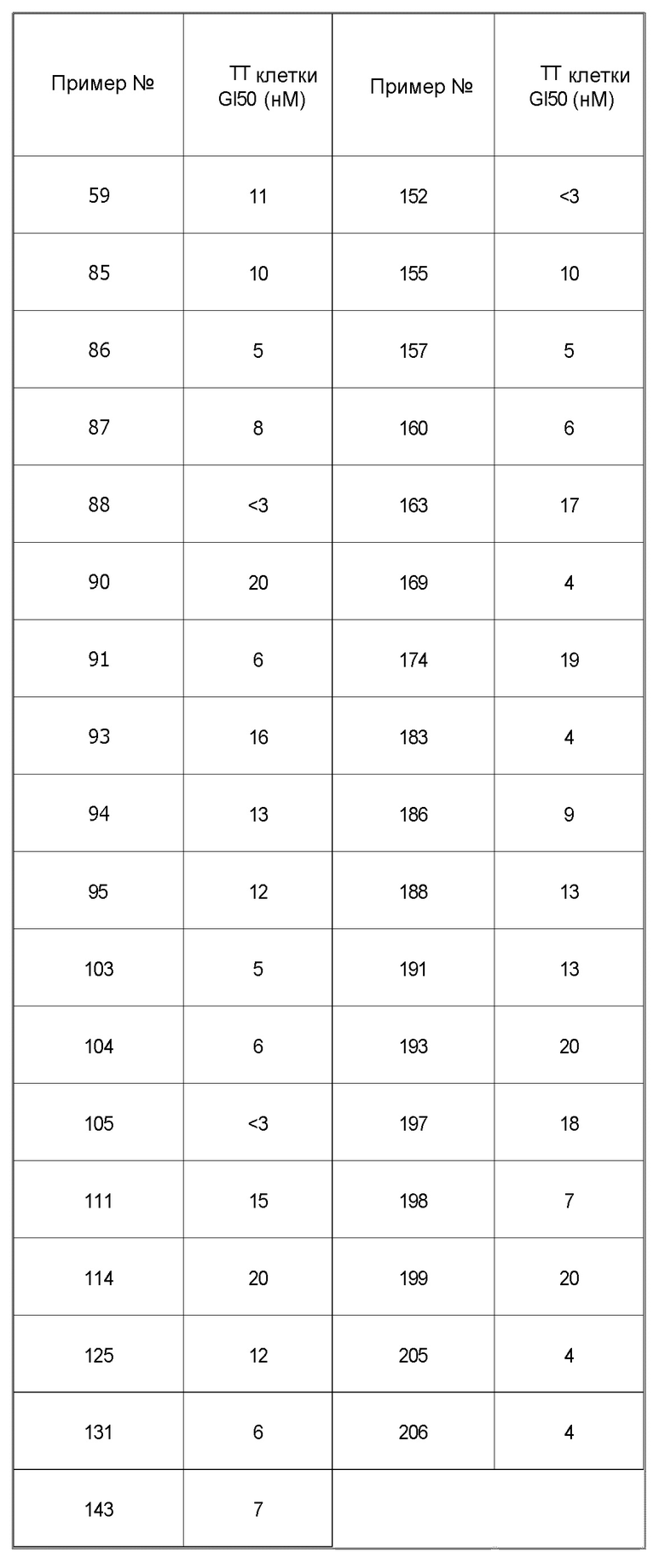
[0814]
Пример испытаний 7: Оценка эффекта ингибирования клеточного роста (2)
Испытание цитотоксичности in vitro осуществляли на LC-2/ad клетках (клеточная линия аденокарциномы легкого человека с CCDC6-RET гибридным геном).
[0815]
Суспензию LC-2/ad клеток, полученную с 10% FBS-содержащей RPMI1640 средой, инокулировани в каждую лунку 96-луночного плоскодонного микропланшета в количестве 5×103 клеток/лунка (0,15 мл) и культивировали в инкубаторе, содержащем 5% диоксида углерода, при 37°C в течение ночи (день 0). Соединения по настоящему изобретению индивидуально растворяли в диметилсульфоксиде с получением концентрации 10 мМ и затем разбавляли 10% FBS-содержащей RPMI1640 средой, чтобы соединения по настоящему изобретению соответственно имели конечную концентрацию 40, 12, 4, 1,2, 0,4, 0,12, 0,04 и 0,012 мкМ. Соединения в разных концентрациях индивидуально добавляли в каждую лунку содержащего LC-2/ad клетки культурального планшета, описанного выше, в количестве 0,05 мл/лунка (день 1) и культивировали в инкубаторе, содержащем 5% диоксида углерода, при 37°C в течение 7 дней. После культивирования (день 8), 0,1 мл среды удаляли из каждой лунки и добавляли 0,1 мл CellTiter Glo 2.0 реагента (Promega Corporation), который представляет собой реагент для детекции внутриклеточного АТФ люминесцентным методом, с последующим встряхиванием в течение 5 минут. После встряхивания каждой культуре давали выстояться при комнатной температуре в течение 15 минут и хемилюминесценцию измеряли с использованием люминометра и использовали как показатель количества жизнеспособных клеток. Концентрацию (GI50 (нМ)) определяли таким же способом, как в Примере испытаний 6, в зависимости от значения Tдень 8 и Cдень 1.
[0816]
Таблица 51 показывает результаты. Соединения по настоящему изобретению продемонстрировали высокий эффект ингибирования роста.
[0817]
Таблица 51

[0818]
Пример испытаний 8: Оценка эффекта ингибирования клеточного роста (3)
Испытание цитотоксичности in vitro осуществляли на Ba/F3_TEL-RET V804L клетках (Ba/F3 клетка, в которую был введен TEL-RET гибридный ген с gatekeeper мутацией V804L).
[0819]
Ba/F3_TEL-RET V804L клетки получали путем встраивания плазмидной ДНК, которую получали путем введения V804L мутации в RET ген TEL-RET гибридного гена в Ba/F3 клетки стандартным методом. Суспензию Ba/F3_TEL-RET V804L клеток, полученную с использованием 10% FBS-содержащей RPMI1640 среды, инокулировани в каждую лунку 96-луночного плоскодонного микропланшета в количестве of 1×103 клеток/лунка (0,075 мл). Соединения по настоящему изобретению индивидуально растворяли в диметилсульфоксиде с получением концентрации 10 мМ и затем разбавляли 10% FBS-содержащей RPMI1640 средой, чтобы соединения по настоящему изобретению соответственно имели конечную концентрацию 40, 12, 4, 1,2, 0,4, 0,12, 0,04 и 0,012 мкМ. Соединения в разных концентрациях индивидуально добавляли в каждую лунку содержащего Ba/F3_TEL-RET V804L клетки культурального планшета, описанного выше, в количестве 0,025 мл/лунка (день 1) и культивировали в инкубаторе, содержащем 5% диоксида углерода при 37°C в течение 4 дней. После культивирования (день 4) добавляли 0,1 мл CellTiter Glo 2.0 реагента (Promega Corporation), который представляет собой реагент для детекции внутриклеточного АТФ люминесцентным методом, с последующим встряхиванием в течение 5 минут. После встряхивания каждой культуре давали выстояться при комнатной температуре в течение 15 минут и хемилюминесценцию измеряли с использованием люминометра и использовали как показатель количества жизнеспособных клеток. Оценку осуществляли в день 4 и концентрацию (GI50 (нМ)) определяли таким же способом, как в Примере испытаний 6, в зависимости от значения Tдень 8 и Cдень 1.
[0820]
Таблица 52 показывает результаты. Значение GI50 Алектиниба, который известен как обладающий ингибиторным эффектом против RET V804L мутации, было 206 (нМ). Для сравнения, соединения по настоящему изобретению продемонстрировали значительно более высокий эффект ингибирования роста против Ba/F3_TEL-RET V804L клеток.
[0821]
Таблица 52

[0822]
Пример испытаний 9: Оценка эффекта ингибирования клеточного роста (4)
Испытание ингибирования клеточного роста in vitro осуществляли на Ba/F3_BCR-RET V804M клетках (Ba/F3 клетка, в которую был введен BCR-RET гибридный ген с gatekeeper мутацией V804M).
[0823]
Суспензию Ba/F3_BCR-RET V804M клеток, полученную с использованием RPMI1640 среды, содержащей 10% FCS и 2 нг/мл IL3 (Интерлейкин3), инокулировани в каждую лунку 384-луночного планшета в количестве 5×103 клеток/лунка (0,05 мл). Соединения по настоящему изобретению индивидуально растворяли в диметилсульфоксиде с получением концентрации 10 мМ и затем разбавляли средой, чтобы соединения по настоящему изобретению соответственно имели конечную концентрацию 1000, 300, 100, 30, 10, 3, 1 и 0,3 мкМ. Соединения в разных концентрациях индивидуально добавляли в каждую лунку содержащего Ba/F3_BCR-RET V804M клетки культурального планшета, описанного выше, в количестве 50 нл/лунка (день 1) и культивировали в инкубаторе, содержащем 5% диоксида углерода, при 37°C в течение 2 дней. После культивирования (день 3) добавляли 0,015 мл CellTiter Glo (Promega Corporation), который представляет собой реагент для детекции внутриклеточного АТФ люминесцентным методом, и хемилюминесценцию измеряли с использованием люминометра и использовали как показатель количества жизнеспособных клеток. Концентрацию соединения (IC50 (нМ)), при которой жизнеспособность клеток в день 3 ингибировалась на 50%, определяли из следующего уравнения.
[0824]
Процент выживания (%)=(Tдень 3)/(Cдень 3) × 100
T: Поглощение в лунке, в которую добавляли испытываемое соединение.
C: Поглощение в лунке, в которую не добавляли испытываемое соединение.
День 1: День, в который добавляли испытываемое соединение.
День 3: День, в который осуществляли оценку.
Таблица 53 показывает результаты. Соединения по настоящему изобретению продемонстрировали высокий эффект ингибирования роста на Ba/F3_BCR-RET V804M клетки.
[0825]
Таблица 53

[0826]
Пример испытаний 10: Оценка противоопухолевого эффекта in vivo с использованием мышиной модели с подкожно имплантированными TT клетками (человеческая клеточная линия рака щитовидной железы с RET-активирующей мутацией)
Человеческие клеточные линии рака щитовидной железы (TT) подкожно имплантировали в правый бок 6-7-недельным самцам мышей BALB/cA Jcl-nu/nu. Примерно через 2-3 недели после имплантации клеток измеряли длину (мм) и ширину (мм) опухолей, обнаруженных у мышей. Затем рассчитывали объем опухоли (объем опухоли: TV) и мышей делили на группы (n=5 или 6) таким образом, чтобы группы имели по существу равный средний TV. День, когда мышей делили на группы, определяли как ʺдень распределения по группамʺ (день 0 или 1).
[0827]
Испытываемые растворы, содержащие соединения по настоящему изобретению, получали при дозе 50, 100 или 150 мг/кг/день и перорально вводили мышам в течение последовательных 14 дней (первым днем введения был день 1). Контрольной группе вводили растворитель (0,5% HPMC/0,1N HCl).
[0828]
Для определения показателя противоопухолевого эффекта, TV каждой группы введения лекарственного средства измеряли в день 15 и объем опухоли в день 15 относительно объема опухоли в день распределения по группам (день 0 или 1) (относительный объем опухоли: RTV) и T/C (%) рассчитывали из следующих уравнений и оценивали противоопухолевый эффект. Когда группа, которой вводили какое-либо соединение по настоящему изобретению (группа обработки испытываемым соединением), демонстрировала статистически существенно меньший средний RTV (критерий Даннета, p<0,05), чем средний RTV контрольной группы, это определяли как присутствие противоопухолевого эффекта. Фиг. 1 и 2 и Таблицы 54 и 55 показывают результаты. На этих Фиг. символ ʺ*ʺ указывает на статистически значимую разницу.
TV (мм3)=(длина × ширина2)/2
RTV=(TV в день 15)/(TV в день 0 или день 1)
T/C(%)=(средний RTV группы обработки испытываемым соединением)/(средний RTV контрольной группы)×100
Для определения показателя токсичности, массу тела (масса тела: BW (г)) мышей измеряли в течение длительного периода времени и изменение средней массы тела (изменение массы тела: BWC (%)) от дня разделения на группы (день 0 или день 1) по день 15 рассчитывали из следующего уравнения (n: день, в который массу тела измеряли при 2 раза/неделя, и последним днем измерения был день 15, в который осуществляли конечную оценку). Фиг. 3 и 4 показывают результаты.
BWC (%)=[(BW в день n)-(BW в день 0 или день 1)]/(BW в день 0 или день 1)×100
Соединения по настоящему изобретению продемонстрировали замечательный противоопухолевый эффект на человеческу клеточную линию рака щитовидной железы TT с RET-активирующей мутацией, которую подкожно имплантировали бестимусным мышам. Токсичность, такую как потеря массы тела, не наблюдали.
[0829]
/день)
[0830]
/день)
| название | год | авторы | номер документа |
|---|---|---|---|
| КОНДЕНСИРОВАННОЕ ПИРИМИДИНОВОЕ СОЕДИНЕНИЕ ИЛИ ЕГО СОЛЬ | 2016 |
|
RU2729636C2 |
| ПРОИЗВОДНЫЕ КАРБОНОВОЙ КИСЛОТЫ, СОДЕРЖАЩИЕ 2,5-ЗАМЕЩЕННОЕ ОКСАЗОЛОПИРИМИДИНОВОЕ КОЛЬЦО | 2011 |
|
RU2564018C2 |
| ПРОИЗВОДНЫЕ КАРБОНОВОЙ КИСЛОТЫ, СОДЕРЖАЩИЕ 2,5,7-ЗАМЕЩЕННОЕ ОКСАЗОЛОПИРИМИДИНОВОЕ КОЛЬЦО | 2011 |
|
RU2560876C2 |
| ПРОИЗВОДНОЕ 7H-ПИРРОЛО[2,3-D]ПИРИМИДИН-4-АМИНА | 2020 |
|
RU2796605C2 |
| ПРОИЗВОДНЫЕ ГЕТЕРОЦИКЛИЧЕСКИХ КАРБОНОВЫХ КИСЛОТ, СОДЕРЖАЩИЕ 2,5,7-ЗАМЕЩЕННОЕ ОКСАЗОЛОПИРИМИДИНОВОЕ КОЛЬЦО | 2011 |
|
RU2554869C2 |
| ГЕТЕРОЦИКЛИЧЕСКИЕ ПРОИЗВОДНЫЕ КАРБОНОВЫХ КИСЛОТ, ИМЕЮЩИЕ 2,5-ЗАМЕЩЕННОЕ ОКСАЗОЛОПИРИМИДИНОВОЕ КОЛЬЦО | 2011 |
|
RU2559896C2 |
| 2,5-ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ ОКСАЗОЛОПИРИМИДИНА | 2011 |
|
RU2554874C2 |
| НОВЫЕ ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ, ИХ ПОЛУЧЕНИЕ, ИХ ПРИМЕНЕНИЕ И СОДЕРЖАЩИЕ ИХ ФАРМАЦЕВТИЧЕСКИЕ ПРЕПАРАТЫ | 1998 |
|
RU2240326C2 |
| АМИНО-ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ 3-ГЕТЕРОАРОИЛАМИНОПРОПИОНОВОЙ КИСЛОТЫ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ФАРМАЦЕВТИЧЕСКИХ СРЕДСТВ | 2012 |
|
RU2605600C2 |
| АЦИЛИРОВАННЫЕ АРИЛЦИКЛОАКИЛАМИНЫ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ФАРМАЦЕВТИЧЕСКИХ СРЕДСТВ | 2003 |
|
RU2337094C2 |

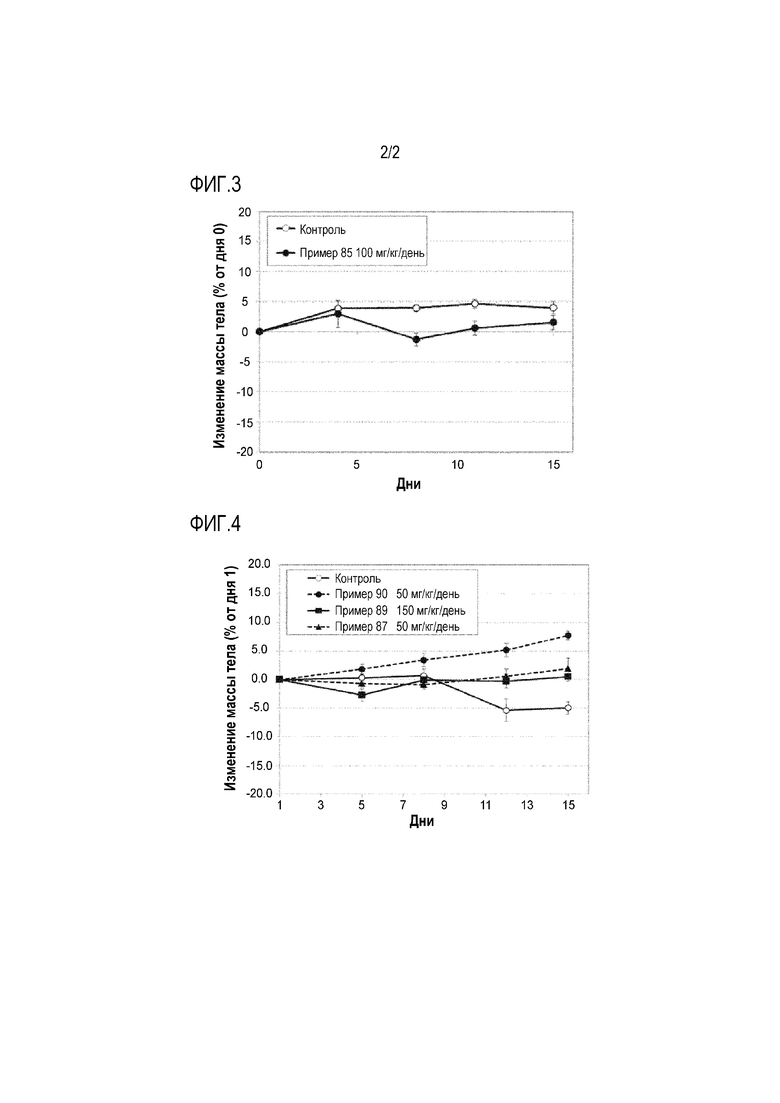
Группа изобретений относится к области органической химии и фармацевтики, а именно к новому конденсированному пиримидиновому соединению, обладающему RET-ингибирующей активностью. Раскрыто соединение, представленное формулой (I'), или его кислотно-аддитивная соль, где значения заместителей A, R2, X такие, как раскрыто в формуле изобретения. Кроме того, описан способ ингибирования RET, включающий введение соединения I, способ профилактики или лечения злокачественной опухоли, связанной с RET, применение соединения формулы (I) в качестве селективного ингибитора RET и для получения противоопухолевого средства, кроме того, раскрыта фармацевтическая композиция, обладающая свойствами селективного ингибитора RET. Технический результат: эффективное ингибирование RET для профилактики и/или лечения опухолей, связанных с RET заболеваний. 14 н. и 23 з.п. ф-лы, 4 ил., 56 табл., 217 пр.
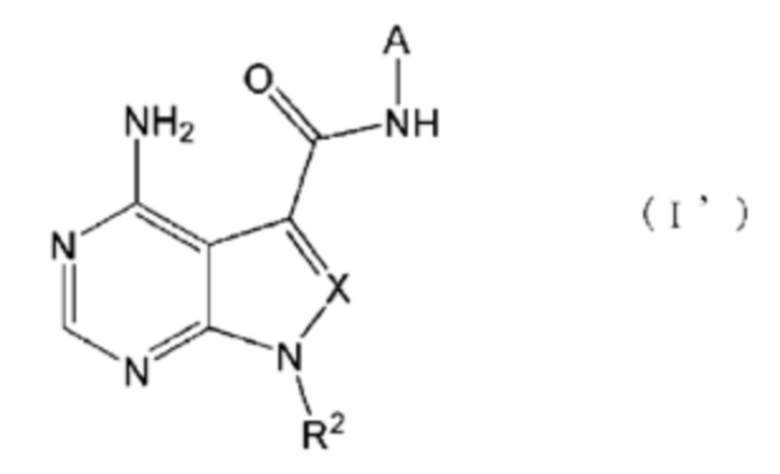
1. Способ ингибирования RET, включающий введение соединения, представленного формулой (I) ниже, или его кислотно-аддитивной соли млекопитающему:

где в формуле (I) A представляет собой

где R1 представляет собой
галоген,
циано,
нитро,
C1-C6 алкил, который может быть замещен C1-C6 алкоксигруппой или C1-C6 алкилтио, гидрокси, фенилом, где атом водорода, содержащийся в C1-C6 алкокси, может быть замещен 1 или более атомами дейтерия,
C1-C6 алкокси, замещенный или незамещенный галогеном, где атом водорода, содержащийся в C1-C6 алкокси, может быть замещен 1 или более атомами дейтерия,
C2-C6 алкенил, замещенный или незамещенный галогеном,
незамещенный C2-C6 алкинил,
амино, который может быть замещен одной или несколькими 4-6-членными моноциклическими или полициклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или различных гетероатомов, выбранных из азота, кислорода и серы, или C6-C10 ароматическим углеводородом, или
5-6-членную моноциклическую или полициклическую ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы,
Y представляет собой N или CH, и
n представляет собой целое число, имеющее значение от 0 до 2,
где, когда n имеет значение 2, два R1 могут быть одинаковыми или отличными друг от друга;
в формуле A2 группа:

образует вместе с фенилом или пиридинилом, с которым эта группа связана, дициклический C9-C10 ароматический углеводород или 9-10-членную дициклическую ненасыщенную гетероциклическую группу, содержащую 1 гетероатом, выбранный из кислорода или серы;
R2 представляет собой
C3-C10 алкил, который может быть замещен 1 или несколькими заместителями, выбранными из группы, состоящей из галогена, С1-С6 алкокси, С3-С7 циклоалкила и 4-10-членной моноциклической или полициклической ненасыщенной гетероциклической группы, содержащей 1-3 одинаковых или разных гетероатомов, выбранных из азота, кислорода и серы,
C3-C7 циклоалкил, который может быть замещен 1 или более заместителями, выбранными из группы, состоящей из С1-С6 алкила, С3-С7 циклоалкила, галоген-С1-С6 алкила и галогена,
C4-C10 связанный мостиковой связью циклоалкил,
C2-C6 алкенил, который может быть замещен галогеном,
C3-C7 циклоалкенил; и
X представляет собой
N или
CR3, где R3 представляет собой
(i) водород,
(ii) галоген,
(iii) циано,
(iv) C1-C4 алкил, который может быть замещен гидрокси или оксо,
(v) C1-C6 алкокси, который может быть замещен 1 или более заместителями, выбранными из группы, состоящей из
(v-1) галогена,
(v-2) C1-C6 алкокси,
(v-3) C3-C7 циклоалкила и
(v-4) одной или нескольких 5-6-членных моноциклических насыщенных гетероциклических групп, которые могут быть замещены оксо и содержат 1 гетероатом, выбранный из азота или кислорода,
(vi) незамещенный C1-C6 алкилтио,
(vii) незамещенный C3-C7 циклоалкил,
(viii) C2-C6 алкенил, который может быть замещен гидрокси,
(ix) C2-C6 алкинил, который может быть замещен 1 или более заместителями, выбранными из группы, состоящей из
(ix-1) гидрокси,
(ix-2) C1-C6 алкокси,
(ix-3) амино, которое может быть замещено группой(ами) R4, где R4 представляет собой по крайней мере один, выбранный из группы, состоящей из C1-C6 алкила, C1-C4 алкокси, C1-C6 алкила и карбамоила, который может быть замещен C3-C7 циклоалкилом,
(ix-4) C1-C6-алкилсилилокси,
(ix-5) C3-C7 циклоалкила, который может быть замещен гидрокси или оксо,
(ix-6) C6-ароматического углеводорода, который может быть замещен группой R5, где R5 представляет собой галоген, C1-C4 алкил, C1-C4 алкиламино, который может быть замещен одной или несколькими 4-10-членными моноциклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или разных гетероатомов, выбранных из азота, кислорода и серы, или C1-C6 алкокси,
(ix-7) одной или нескольких 4-6-членных моноциклических насыщенных гетероциклических групп, которые могут быть замещены группой(ами) R6 и содержат 1-2 идентичных или разных гетероатома, выбранных из азота, кислорода и серы, где R6 представляет собой гидрокси, C1-C6 алкил, C1-C6 алкокси или оксо,
(ix-8) одной или нескольких 4-10-членных моноциклических или дициклических ненасыщенных гетероциклических групп, которые могут быть замещены группой (группами) R7 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R7 представляет собой галоген, циано, C1-C6 алкил, C1-C6 алкокси или амино, и
(ix-9) ненасыщенной гетероциклилоксигруппы, которая может быть замещена галогеном, где ненасыщенное гетероциклическое кольцо представляет собой 4-10-членное моноциклическое или дициклическое ненасыщенное гетероциклическое кольцо, содержащее 1-2 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы,
при условии, что положение тройной связи C2-C6 алкинила находится между атомом углерода, связанным с 7H-пирроло[2,3-d]пиримидиновым скелетом, и атомом углерода, соседним с этим атомом углерода,
(x) C6 ароматический углеводород, который может быть замещен
(x-1) гидрокси,
(x-2) C1-C6 алкилом, который может быть замещен гидроксигруппой,
(x-3) формилом, или
(x-4) одной 5-6-членной моноциклической насыщенной гетероциклической группой, которая может быть замещена C1-C6 алкилом и содержать 1-2 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или
(xi) 5-6-членную моноциклическую или 9-10-членную дициклическую насыщенную или ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, которая может быть замещена
(xi-1) галогеном,
(xi-2) C1-C6 алкилом, который может быть замещен гидроксигруппой, или
(xi-3) амино, которое может быть замещено C1-C6 алкильной (карбонильной) группой.
2. Способ по п. 1, где, когда A представляет собой A1, A1 представляет собой

где R1a представляет собой
C1-C6 алкил, который может быть замещен группой C1-C6 алкокси или C1-C6 алкилтио, где водород, содержащийся в C1-C6 алкокси, может быть замещен 1 или несколькими атомами дейтерия,
C2-C6 алкенил,
C2-C6 алкинил,
амино, который может быть замещен одной или несколькими 4-6-членными моноциклическими или полициклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или C6-C10 ароматическим углеводородом, или
5-6-членную моноциклическую ненасыщенную гетероциклическую группу, содержащую 1-2 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы;
R1b представляет собой галоген, C1-C6 алкил или C1-C6 алкокси; и
m представляет собой целое число, имеющее значение от 0 или 1.
3. Способ по п. 1, где R2 представляет собой
C3-C10 алкил, который может быть замещен одним или несколькими заместителями, выбранными из группы, состоящей из галогена, C3-C7 циклоалкила и 4-10-членных моноциклических или полициклических ненасыщенных гетероциклических групп, содержащих 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы,
C3-C7 циклоалкил, который может быть замещен одним или несколькими заместителями, выбранными из группы, состоящей из C1-C6 алкила, C3-C7 циклоалкила и галогенo C1-C6 алкила,
C4-C10 связанный мостиковой связью циклоалкил или
C3-C7 циклоалкенил.
4. Способ по п. 1, где, когда X представляет собой CR3, R3 представляет собой
(i) водород,
(ii) галоген,
(iii) циано,
(iv) C1-C4 алкил, который может быть замещен группой гидрокси или оксо,
(v) C1-C6 алкокси, который может быть замещен одним или несколькими заместителями, выбранными из группы, состоящей из
(v-1) галогена,
(v-2) C1-C6 алкокси,
(v-3) C3-C7 циклоалкила и
(v-4) одной или нескольких 5-6-членных моноциклических насыщенных гетероциклических групп, которые могут быть замещены оксо и содержат 1 гетероатом, выбранный из азота или кислорода,
(vi) C1-C4 алкилтио,
(vii) C3-C5 циклоалкил,
(viii) C2-C6 алкенил, который может быть замещен группой гидрокси,
(ix) C2-C6 алкинил, который может быть замещен одним или несколькими заместителями, выбранными из группы, состоящей из
(ix-1) гидрокси,
(ix-2) C1-C6 алкокси,
(ix-3) амино, который может быть замещен группой R4, где R4 представляет собой C1-C6 алкил, C1-C4 алкокси C1-C6 алкил или карбамоил, который может быть замещен C3-C7 циклоалкилом,
(ix-4) C1-C6 алкилсилилокси,
(ix-5) C3-C7 циклоалкила, который может быть замещен группой гидрокси или оксо,
(ix-6) C6 ароматического углеводорода, который может быть замещен группой R5, где R5 представляет собой галоген, C1-C4 алкиламино, который может быть замещен одной или несколькими 4-10-членными моноциклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или C1-C6 алкокси,
(ix-7) одной или нескольких 4-6-членных моноциклических насыщенных гетероциклических групп, которые могут быть замещены группой R6 и содержат 1-2 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R6 представляет собой гидрокси, C1-C6 алкил, C1-C6 алкокси или оксо,
(ix-8) одной или нескольких 4-10-членных моноциклических или дициклических ненасыщенных гетероциклических групп, которые могут быть замещены группой R7 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R7 представляет собой галоген, циано, C1-C6 алкил, C1-C6 алкокси или амино, и
(ix-9) ненасыщенного гетероциклилокси, который может быть замещен галогеном, где ненасыщенное гетероциклическое кольцо представляет собой 4-10-членное моноциклическое или дициклическое ненасыщенное гетероциклическое кольцо, содержащее 1-2 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы,
при условии, что положение тройной связи C2-C6 алкинила находится между атомом углерода, связанным с 7H-пирроло[2,3-d]пиримидиновым скелетом, и атомом углерода, смежным с этим атомом углерода,
(x) C6 ароматический углеводород, который может быть замещен
(x-1) гидрокси,
(x-2) C1-C6 алкилом, который может быть замещен гидроксигруппой,
(x-3) формилом или
(x-4) одной или несколькими 5-6-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены C1-C6 алкилом и содержат 1-2 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или
(xi) 5-6-членную моноциклическую ненасыщенную гетероциклическую группу, которая может быть замещена
(xi-1) галогеном,
(xi-2) C1-C6 алкилом, который может быть замещен гидроксигруппой, или
(xi-3) амино, который может быть замещен группой C1-C6 алкил (карбонил),
и содержит 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы.
5. Способ по п. 1, где A представляет собой
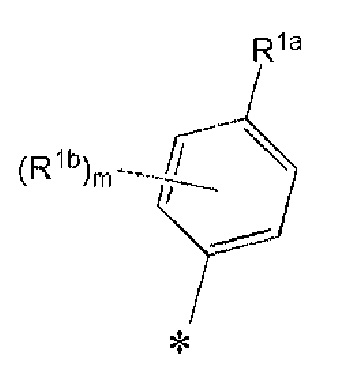
где R1a представляет собой
C1-C6 алкил, который может быть замещен группой C1-C6 алкокси или C1-C6 алкилтио, где водород, содержащийся в C1-C6 алкокси, может быть замещен 1 или несколькими атомами дейтерия,
C2-C6 алкенил,
C2-C6 алкинил,
амино, который может быть замещен одной или несколькими 4-6-членными моноциклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или C6-C10 ароматическим углеводородом, или
5-6-членную моноциклическую ненасыщенную гетероциклическую группу, содержащую 1-2 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы;
R1b представляет собой галоген, C1-C6 алкил или C1-C6 алкокси;
m представляет собой целое число, имеющее значение от 0 или 1;
R2 представляет собой
C3-C10 алкил, который может быть замещен одним или несколькими заместителями, выбранными из группы, состоящей из галогена, C3-C7 циклоалкила и одной или нескольких 4-10-членных моноциклических или полициклических ненасыщенных гетероциклических групп, содержащих 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы,
C3-C7 циклоалкил, который может быть замещен одним или несколькими заместителями, выбранными из группы, состоящей из C1-C6 алкила, C3-C7 циклоалкила и галогенo C1-C6 алкила, или
C4-C10 связанный мостиковой связью циклоалкил; и
X представляет собой
N или
CR3, где R3 представляет собой
(i') водород,
(ii') галоген,
(iii') циано,
(iv') C1-C4 алкил,
(v') C1-C6 алкокси, который может быть замещен одним или несколькими заместителями, выбранными из группы, состоящей из
(v-1') галогена,
(v-2') C1-C6 алкокси,
(v-3') C3-C7 циклоалкила и
(v-4') одной или нескольких 5-6-членных моноциклических насыщенных гетероциклических групп, которые могут быть замещены оксо и содержат 1 гетероатом, выбранный из азота или кислорода,
(vi') C1-C4 алкилтио,
(vii') C3-C5 циклоалкил,
(viii') C2-C4 алкенил, который может быть замещен гидроксигруппой,
(ix') C2-C6 алкинил, который может быть замещен одним или несколькими заместителями, выбранными из группы, состоящей из
(ix-1') гидрокси,
(ix-2') C1-C4 алкокси,
(ix-3') амино, который может быть замещен группой R4, где R4 представляет собой C1-C4 алкил, C1-C4 алкокси C1-C4 алкил или карбамоил, который может быть замещен C3-C5 циклоалкилом,
(ix-4') C1-C6 алкилсилилокси,
(ix-5') C3-C7 циклоалкила, который может быть замещен гидроксигруппой или оксо,
(ix-6') фенила, который может быть замещен группой R5, где R5 представляет собой галоген, метиламино, который может быть замещен одной или несколькими 4-6-членными моноциклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или C1-C4 алкокси,
(ix-7') одной или нескольких 4-6-членных моноциклических насыщенных гетероциклических групп, которые могут быть замещены группой R6 и содержат 1-2 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R6 представляет собой гидрокси, C1-C4 алкил, C1-C4 алкокси или оксо,
(ix-8') одной или нескольких 4-10-членных моноциклических или дициклических ненасыщенных гетероциклических групп, которые могут быть замещены группой R7 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R7 представляет собой галоген, циано, C1-C4 алкил, C1-C4 алкокси или амино, и
(ix-9') ненасыщенного гетероциклилокси, который может быть замещен галогеном, где ненасыщенное гетероциклическое кольцо представляет собой 4-6-членное моноциклическое ненасыщенное гетероциклическое кольцо, содержащее 1-2 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы,
при условии, что положение тройной связи C2-C6 алкинила находится между атомом углерода, связанным с 7H-пирроло[2,3-d]пиримидиновым скелетом, и атомом углерода, смежным с этим атомом углерода,
(x') фенил, который может быть замещен
(x-1') гидрокси,
(x-2') C1-C4 алкилом, который может быть замещен гидроксигруппой,
(x-3') формилом или
(x-4') одной 5-6-членной моноциклической насыщенной гетероциклической группой, которая может быть замещена C1-C4 алкилом и содержать 1-2 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или
(xi') 5-6-членную моноциклическую ненасыщенную гетероциклическую группу, которая может быть замещена
(xi-1') галогеном,
(xi-2') C1-C4 алкилом, который может быть замещен гидроксигруппой, или
(xi-3') амино, который может быть замещен группой C1-C4 алкил(карбонил),
и содержит 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы.
6. Способ по п. 1, где A представляет собой
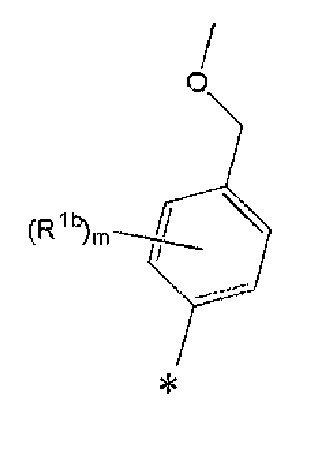
где R1b представляет собой галоген;
m представляет собой целое число, имеющее значение от 0 или 1;
R2 представляет собой
C3-C6 алкил, который может быть замещен галогеном, или
C3-C7 циклоалкил, который может быть замещен C1-C4 алкилом или C3-C5 циклоалкилом; и
X представляет собой CR3, где R3 представляет собой
(i'') водород,
(ii'') галоген,
(v') C1-C4 алкокси, который может быть замещен одним или несколькими заместителями, выбранными из группы, состоящей из
(v-2'') C1-C4 алкокси,
(v-3'') C3-C7 циклоалкила и
(v-4'') одной или нескольких 5-6-членных моноциклических насыщенных гетероциклических групп, содержащих один атом кислорода,
(vi'') C1-C4 алкилтио,
(viii') C2-C4 алкенил,
(ix') C2-C6 алкинил, который может быть замещен одним или несколькими заместителями, выбранными из группы, состоящей из
(ix-1'') гидрокси,
(ix-2'') амино, который может быть замещен группой R4, где R4 представляет собой C1-C4 алкил или C1-C4 алкокси C1-C4 алкил,
(ix-5'') C3-C7 циклоалкила, который может быть замещен гидроксигруппой,
(ix-6'') фенила, который может быть замещен группой R5, где R5 представляет собой галоген,
(ix-7'') одной или нескольких 4-6-членных моноциклических насыщенных гетероциклических групп, которые могут быть замещены группой R6 и содержат 1-2 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R6 представляет собой гидрокси, C1-C4 алкил или оксо, и
(ix-8'') одной или нескольких 4-10-членных моноциклических или дициклических ненасыщенных гетероциклических групп, которые могут быть замещены группой R7 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R7 представляет собой галоген, циано, C1-C4 алкил, C1-C4 алкокси или амино,
при условии, что положение тройной связи C2-C6 алкинила находится между атомом углерода, связанным с 7H-пирроло[2,3-d]пиримидиновым скелетом, и атомом углерода, смежным с этим атомом углерода,
(x'') фенил, который может быть замещен гидрокси или C1-C4 алкилом, который может быть замещен гидроксигруппой, или
(xi'') 5-6-членную моноциклическую ненасыщенную гетероциклическую группу, содержащую 1 или 2 атома азота.
7. Способ профилактики или лечения злокачественной опухоли, связанной с активностью RET, включающий введение соединения, представленного формулой (I) ниже, или его кислотно-аддитивной соли млекопитающему:

где в формуле (I) A представляет собой

где R1 представляет собой
галоген,
циано,
нитро,
C1-C6 алкил, который может быть замещен C1-C6 алкоксигруппой или C1-C6 алкилтио, гидрокси, фенилом, где атом водорода, содержащийся в C1-C6 алкокси, может быть замещен 1 или более атомами дейтерия,
C1-C6 алкокси, замещенный или незамещенный галогеном, где атом водорода, содержащийся в C1-C6 алкокси, может быть замещен 1 или более атомами дейтерия,
C2-C6 алкенил, замещенный или незамещенный галогеном,
незамещенный C2-C6 алкинил,
амино, который может быть замещен одной или несколькими 4-6-членными моноциклическими или полициклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или различных гетероатомов, выбранных из азота, кислорода и серы, или C6-C10 ароматическим углеводородом, или
5-6-членную моноциклическую ненасыщенную гетероциклическую группу, содержащую 1-2 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы,
Y представляет собой N или CH, и
n представляет собой целое число, имеющее значение от 0 до 2,
где, когда n имеет значение 2, два R1 могут быть одинаковыми или отличными друг от друга;
в формуле A2 группа:

образует вместе с фенилом или пиридинилом, с которым эта группа связана, дициклический C9-C10 ароматический углеводород или 9-10-членную дициклическую ненасыщенную гетероциклическую группу, содержащую 1 гетероатом, выбранный из кислорода или серы;
R2 представляет собой
C3-C10 алкил, который может быть замещен 1 или несколькими заместителями, выбранными из группы, состоящей из галогена, С1-С6 алкокси, С3-С7 циклоалкила и 4-10-членной моноциклической или полициклической ненасыщенной гетероциклической группы, содержащей 1-3 одинаковых или разных гетероатомов, выбранных из азота, кислорода и серы,
C3-C7 циклоалкил, который может быть замещен 1 или более заместителями, выбранными из группы, состоящей из С1-С6 алкила, С3-С7 циклоалкила, галоген-С1-С6 алкила и галогена,
C4-C10 связанный мостиковой связью циклоалкил,
C2-C6 алкенил, который может быть замещен галогеном,
C3-C7 циклоалкенил; и
X представляет собой
N или
CR3, где R3 представляет собой
(i) водород,
(ii) галоген,
(iii) циано,
(iv) C1-C4 алкил, который может быть замещен гидрокси или оксо,
(v) C1-C6 алкокси, который может быть замещен 1 или более заместителями, выбранными из группы, состоящей из
(v-1) галогена,
(v-2) C1-C6 алкокси,
(v-3) C3-C7 циклоалкила и
(v-4) одной или нескольких 5-6-членных моноциклических насыщенных гетероциклических групп, которые могут быть замещены оксо и содержат 1 гетероатом, выбранный из азота или кислорода,
(vi) незамещенный C1-C6 алкилтио,
(vii) незамещенный C3-C7 циклоалкил,
(viii) C2-C6 алкенил, который может быть замещен гидрокси,
(ix) C2-C6 алкинил, который может быть замещен 1 или более заместителями, выбранными из группы, состоящей из
(ix-1) гидрокси,
(ix-2) C1-C6 алкокси,
(ix-3) амино, которое может быть замещено группой(ами) R4, где R4 представляет собой по крайней мере один, выбранный из группы, состоящей из C1-C6 алкила, C1-C4 алкокси, C1-C6 алкила и карбамоила, который может быть замещен C3-C7 циклоалкилом,
(ix-4) C1-C6-алкилсилилокси,
(ix-5) C3-C7 циклоалкила, который может быть замещен гидрокси или оксо,
(ix-6) C6-ароматического углеводорода, который может быть замещен группой R5, где R5 представляет собой галоген, C1-C4 алкил, C1-C4 алкиламино, который может быть замещен одной или несколькими 4-10-членными моноциклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или разных гетероатомов, выбранных из азота, кислорода и серы, или C1-C6 алкокси,
(ix-7) одной или нескольких 4-6-членных моноциклических насыщенных гетероциклических групп, которые могут быть замещены группой(ами) R6 и содержат 1-2 идентичных или разных гетероатома, выбранных из азота, кислорода и серы, где R6 представляет собой гидрокси, C1-C6 алкил, C1-C6 алкокси или оксо,
(ix-8) одной или нескольких 4-10-членных моноциклических или дициклических ненасыщенных гетероциклических групп, которые могут быть замещены группой (группами) R7 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R7 представляет собой галоген, циано, C1-C6 алкил, C1-C6 алкокси или амино, и
(ix-9) ненасыщенной гетероциклилоксигруппы, которая может быть замещена галогеном, где ненасыщенное гетероциклическое кольцо представляет собой 4-10-членное моноциклическое или дициклическое ненасыщенное гетероциклическое кольцо, содержащее 1-2 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы,
при условии, что положение тройной связи C2-C6 алкинила находится между атомом углерода, связанным с 7H-пирроло[2,3-d]пиримидиновым скелетом, и атомом углерода, соседним с этим атомом углерода,
(x) C6 ароматический углеводород, который может быть замещен
(x-1) гидрокси,
(x-2) C1-C6 алкилом, который может быть замещен гидроксигруппой,
(x-3) формилом, или
(x-4) одной 5-6-членной моноциклической насыщенной гетероциклической группой, которая может быть замещена C1-C6 алкилом и содержать 1-2 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или
(xi) 5-6-членную моноциклическую или 9-10-членную дициклическую насыщенную или ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, которая может быть замещена
(xi-1) галогеном,
(xi-2) C1-C6 алкилом, который может быть замещен гидроксигруппой, или
(xi-3) амино, которое может быть замещено C1-C6 алкильной (карбонильной) группой.
8. Способ по п. 7, где, когда A представляет собой A1, A1 представляет собой

где R1a представляет собой
C1-C6 алкил, который может быть замещен группой C1-C6 алкокси или C1-C6 алкилтио, где водород, содержащийся в алкокси, может быть замещен 1 или несколькими атомами дейтерия,
C2-C6 алкенил,
C2-C6 алкинил,
амино, который может быть замещен одной или несколькими 4-6-членными моноциклическими или полициклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или C6-C10 ароматическим углеводородом, или
5-6-членную моноциклическую ненасыщенную гетероциклическую группу, содержащую 1-2 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы;
R1b представляет собой галоген, C1-C6 алкил или C1-C6 алкокси; и
m представляет собой целое число, имеющее значение от 0 или 1.
9. Способ по п. 7, где R2 представляет собой
C3-C10 алкил, который может быть замещен одним или несколькими заместителями, выбранными из группы, состоящей из галогена, C3-C7 циклоалкила и одной или нескольких 4-10-членных моноциклических или полициклических ненасыщенных гетероциклических групп, содержащих 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы,
C3-C7 циклоалкил, который может быть замещен одним или несколькими заместителями, выбранными из группы, состоящей из C1-C6 алкила, C3-C7 циклоалкила и галогенo C1-C6 алкила,
C4-C10 связанный мостиковой связью циклоалкил или
C3-C7 циклоалкенил.
10. Способ по п. 7, где, когда X представляет собой CR3, R3 представляет собой
(i) водород,
(ii) галоген,
(iii) циано,
(iv) C1-C4 алкил, который может быть замещен гидроксигруппой или оксо,
(v) C1-C6 алкокси, который может быть замещен одним или несколькими заместителями, выбранными из группы, состоящей из
(v-1) галогена,
(v-2) C1-C6 алкокси,
(v-3) C3-C7 циклоалкила и
(v-4) одной или нескольких 5-6-членных моноциклических насыщенных гетероциклических групп, которые могут быть замещены оксо и содержат 1 гетероатом, выбранный из азота или кислорода,
(vi) C1-C4 алкилтио,
(vii) C3-C5 циклоалкил,
(viii) C2-C6 алкенил, который может быть замещен гидроксигруппой,
(ix) C2-C6 алкинил, который может быть замещен одним или несколькими заместителями, выбранными из группы, состоящей из
(ix-1) гидрокси,
(ix-2) C1-C6 алкокси,
(ix-3) амино, который может быть замещен группой R4, где R4 представляет собой C1-C6 алкил, C1-C4 алкокси C1-C6 алкил или карбамоил, который может быть замещен C3-C7 циклоалкилом,
(ix-4) C1-C6 алкилсилилокси,
(ix-5) C3-C7 циклоалкила, который может быть замещен гидроксигруппой или оксо,
(ix-6) C6 ароматического углеводорода, который может быть замещен группой R5, где R5 представляет собой галоген, C1-C4 алкиламино, который может быть замещен одной или несколькими 4-10-членными моноциклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или C1-C6 алкокси,
(ix-7) одной или нескольких 4-6-членных моноциклических насыщенных гетероциклических групп, которые могут быть замещены группой R6 и содержат 1-2 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R6 представляет собой гидрокси, C1-C6 алкил, C1-C6 алкокси или оксо,
(ix-8) одной или нескольких 4-10-членных моноциклических или дициклических ненасыщенных гетероциклических групп, которые могут быть замещены группой R7 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R7 представляет собой галоген, циано, C1-C6 алкил, C1-C6 алкокси или амино, и
(ix-9) ненасыщенного гетероциклилокси, который может быть замещен галогеном, где ненасыщенное гетероциклическое кольцо представляет собой 4-10-членное моноциклическое или дициклическое ненасыщенное гетероциклическое кольцо, содержащее 1-2 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы,
при условии, что положение тройной связи C2-C6 алкинила находится между атомом углерода, связанным с 7H-пирроло[2,3-d]пиримидиновым скелетом, и атомом углерода, смежным с этим атомом углерода,
(x) C6 ароматический углеводород, который может быть замещен
(x-1) гидрокси,
(x-2) C1-C6 алкилом, который может быть замещен гидроксигруппой,
(x-3) формилом или
(x-4) одной 5-10-членной моноциклической насыщенной гетероциклической группой, которая может быть замещена C1-C6 алкилом и содержит 1-2 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или
(xi) 5-6-членную моноциклическую ненасыщенную гетероциклическую группу, которая может быть замещена
(xi-1) галогеном,
(xi-2) C1-C6 алкилом, который может быть замещен гидроксигруппой, или
(xi-3) амино, который может быть замещен группой C1-C6 алкил(карбонил),
и содержит 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы.
11. Способ по п. 7, где A представляет собой
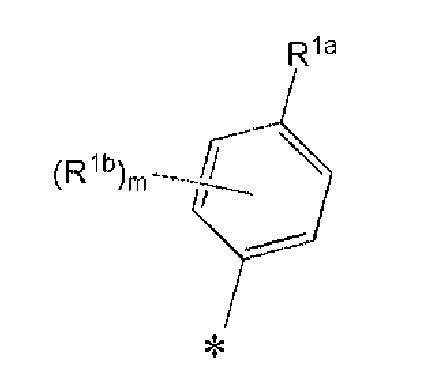
где R1a представляет собой
C1-C6 алкил, который может быть замещен группой C1-C6 алкокси или C1-C6 алкилтио, где водород, содержащийся в алкокси, может быть замещен 1 или несколькими атомами дейтерия,
C2-C6 алкенил,
C2-C6 алкинил,
амино, который может быть замещен одной или несколькими 4-6-членными моноциклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или C6-C10 ароматическим углеводородом, или
5-6-членную моноциклическую ненасыщенную гетероциклическую группу, содержащую 1-2 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы;
R1b представляет собой галоген, C1-C6 алкил или C1-C6 алкокси;
m представляет собой целое число, имеющее значение от 0 или 1;
R2 представляет собой
C3-C10 алкил, который может быть замещен одним или несколькими заместителями, выбранными из группы, состоящей из галогена, C3-C7 циклоалкила и одной или нескольких 4-10-членных моноциклических или полициклических ненасыщенных гетероциклических групп, содержащих 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы,
C3-C7 циклоалкил, который может быть замещен одним или несколькими заместителями, выбранными из группы, состоящей из C1-C6 алкила, C3-C7 циклоалкила и галогенo C1-C6 алкила, или
C4-C12 связанный мостиковой связью циклоалкил; и
X представляет собой
N или
CR3, где R3 представляет собой
(i') водород,
(ii') галоген,
(iii') циано,
(iv') C1-C4 алкил,
(v') C1-C6 алкокси, который может быть замещен одним или несколькими заместителями, выбранными из группы, состоящей из
(v-1') галогена,
(v-2') C1-C6 алкокси,
(v-3') C3-C7 циклоалкила и
(v-4') одной или нескольких 5-6-членных моноциклических насыщенных гетероциклических групп, которые могут быть замещены оксо и содержат 1 гетероатом, выбранный из азота или кислорода,
(vi') C1-C4 алкилтио,
(vii') C3-C5 циклоалкил,
(viii') C2-C4 алкенил, который может быть замещен гидроксигруппой,
(ix') C2-C6 алкинил, который может быть замещен одним или несколькими заместителями, выбранными из группы, состоящей из
(ix-1') гидрокси,
(ix-2') C1-C4 алкокси,
(ix-3') амино, который может быть замещен группой R4, где R4 представляет собой C1-C4 алкил, C1-C4 алкокси C1-C4 алкил или карбамоил, который может быть замещен C3-C5 циклоалкилом,
(ix-4') C1-C6 алкилсилилокси,
(ix-5') C3-C7 циклоалкила, который может быть замещен гидроксигруппой или оксо,
(ix-6') фенила, который может быть замещен группой R5, где R5 представляет собой галоген, метиламино, который может быть замещен одной или несколькими 4-6-членными моноциклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или C1-C4 алкокси,
(ix-7') одной или нескольких 4-6-членных моноциклических насыщенных гетероциклических групп, которые могут быть замещены группой R6 и содержат 1-2 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R6 представляет собой гидрокси, C1-C4 алкил, C1-C4 алкокси или оксо,
(ix-8') одной или нескольких 4-10-членных моноциклических или бициклических ненасыщенных гетероциклических групп, которые могут быть замещены группой R7 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R7 представляет собой галоген, циано, C1-C4 алкил, C1-C4 алкокси или амино, и
(ix-9') ненасыщенного гетероциклического окси, который может быть замещен галогеном, где ненасыщенное гетероциклическое кольцо представляет собой 4-6-членное моноциклическое ненасыщенное гетероциклическое кольцо, содержащее 1-2 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы,
при условии, что положение тройной связи C2-C6 алкинила находится между атомом углерода, связанным с 7H-пирроло[2,3-d]пиримидиновым скелетом, и атомом углерода, смежным с этим атомом углерода,
(x') фенил, который может быть замещен
(x-1') гидрокси,
(x-2') C1-C4 алкилом, который может быть замещен гидроксигруппой,
(x-3') формилом или
(x-4') одной или несколькими 5-6-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены C1-C4 алкилом и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или
(xi') 5-6-членную моноциклическую ненасыщенную гетероциклическую группу, которая может быть замещена
(xi-1') галогеном,
(xi-2') C1-C4 алкилом, который может быть замещен гидроксигруппой, или
(xi-3') амино, который может быть замещен группой C1-C4 алкил(карбонил),
и содержит 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы.
12. Способ по п. 7, где A представляет собой

где R1b представляет собой галоген;
m представляет собой целое число, имеющее значение от 0 или 1;
R2 представляет собой
C3-C6 алкил, который может быть замещен галогеном, или
C3-C7 циклоалкил, который может быть замещен C1-C4 алкилом или C3-C5 циклоалкилом; и
X представляет собой CR3, где R3 представляет собой
(i'') водород,
(ii'') галоген,
(v') C1-C4 алкокси, который может быть замещен одним или несколькими заместителями, выбранными из группы, состоящей из
(v-2'') C1-C4 алкокси,
(v-3'') C3-C7 циклоалкила и
(v-4'') одной или нескольких 5-6-членных моноциклических насыщенных гетероциклических групп, содержащих один атом кислорода,
(vi'') C1-C4 алкилтио,
(viii') C2-C4 алкенил,
(ix') C2-C6 алкинил, который может быть замещен одним или несколькими заместителями, выбранными из группы, состоящей из
(ix-1'') гидрокси,
(ix-2'') амино, который может быть замещен группой R4, где R4 представляет собой C1-C4 алкил или C1-C4 алкокси C1-C4 алкил,
(ix-5'') C3-C7 циклоалкила, который может быть замещен гидроксигруппой,
(ix-6'') фенила, который может быть замещен группой R5, где R5 представляет собой галоген,
(ix-7'') одной или нескольких 4-6-членных моноциклических насыщенных гетероциклических групп, которые могут быть замещены группой R6 и содержат 1-2 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R6 представляет собой гидрокси, C1-C4 алкил или оксо, и
(ix-8'') одной или нескольких 4-10-членных моноциклических или дициклических ненасыщенных гетероциклических групп, которые могут быть замещены группой R7 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R7 представляет собой галоген, циано, C1-C4 алкил, C1-C4 алкокси или амино,
при условии, что положение тройной связи C2-C6 алкинила находится между атомом углерода, связанным с 7H-пирроло[2,3-d]пиримидиновым скелетом, и атомом углерода, смежным с этим атомом углерода,
(x'') фенил, который может быть замещен гидрокси или C1-C4 алкилом, который может быть замещен гидроксигруппой, или
(xi'') 5-6-членную моноциклическую ненасыщенную гетероциклическую группу, содержащую 1 или 2 атома азота.
13. Применение соединения, представленного формулой (I) ниже, или его кислотно-аддитивной соли в качестве селективного ингибитора RET:

где в формуле (I) A представляет собой

где R1 представляет собой
галоген,
циано,
нитро,
C1-C6 алкил, который может быть замещен C1-C6 алкоксигруппой или C1-C6 алкилтио, гидрокси, фенилом, где атом водорода, содержащийся в C1-C6 алкокси, может быть замещен 1 или более атомами дейтерия,
C1-C6 алкокси, замещенный или незамещенный галогеном, где атом водорода, содержащийся в C1-C6 алкокси, может быть замещен 1 или более атомами дейтерия,
C2-C6 алкенил, замещенный или незамещенный галогеном,
незамещенный C2-C6 алкинил,
амино, который может быть замещен одной или несколькими 4-6-членными моноциклическими или полициклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или различных гетероатомов, выбранных из азота, кислорода и серы, или C6-C10 ароматическим углеводородом, или
5-6-членную моноциклическую ненасыщенную гетероциклическую группу, содержащую 1-2 одинаковых или отличных друг от друга гетероатома, выбранных из кислорода и серы,
Y представляет собой N или CH, и
n представляет собой целое число, имеющее значение от 0 до 2,
где, когда n имеет значение 2, два R1 могут быть одинаковыми или отличными друг от друга;
в формуле A2 группа:

образует вместе с фенилом или пиридинилом, с которым эта группа связана, дициклический C9-C10 ароматический углеводород или 9-10-членную дициклическую ненасыщенную гетероциклическую группу, содержащую 1 гетероатом, выбранный из кислорода или серы;
R2 представляет собой
C3-C10 алкил, который может быть замещен 1 или несколькими заместителями, выбранными из группы, состоящей из галогена, С1-С6 алкокси, С3-С7 циклоалкила и 4-10-членной моноциклической или полициклической ненасыщенной гетероциклической группы, содержащей 1-3 одинаковых или разных гетероатомов, выбранных из азота, кислорода и серы,
C3-C7 циклоалкил, который может быть замещен 1 или более заместителями, выбранными из группы, состоящей из С1-С6 алкила, С3-С7 циклоалкила, галоген-С1-С6 алкила и галогена,
C4-C12 связанный мостиковой связью циклоалкил,
C2-C6 алкенил, который может быть замещен галогеном,
C3-C7 циклоалкенил из кислорода и серы, и содержит по меньшей мере один атом азота; и
X представляет собой
N или
CR3, где R3 представляет собой
(i) водород,
(ii) галоген,
(iii) циано,
(iv) C1-C4 алкил, который может быть замещен гидрокси или оксо,
(v) C1-C6 алкокси, который может быть замещен 1 или более заместителями, выбранными из группы, состоящей из
(v-1) галогена,
(v-2) C1-C6 алкокси,
(v-3) C3-C7 циклоалкила и
(v-4) одной или нескольких 5-6-членных моноциклических насыщенных гетероциклических групп, которые могут быть замещены оксо и содержат 1 гетероатом, выбранный из азота или кислорода,
(vi) незамещенный C1-C6 алкилтио,
(vii) незамещенный C3-C7 циклоалкил,
(viii) C2-C6 алкенил, который может быть замещен гидрокси,
(ix) C2-C6 алкинил, который может быть замещен 1 или более заместителями, выбранными из группы, состоящей из
(ix-1) гидрокси,
(ix-2) C1-C6 алкокси,
(ix-3) амино, которое может быть замещено группой(ами) R4, где R4 представляет собой по крайней мере один, выбранный из группы, состоящей из C1-C6 алкила, C1-C4 алкокси, C1-C6 алкила и карбамоила, который может быть замещен C3-C7 циклоалкилом,
(ix-4) C1-C6-алкилсилилокси,
(ix-5) C3-C7 циклоалкила, который может быть замещен гидрокси или оксо,
(ix-6) C6-ароматического углеводорода, который может быть замещен группой R5, где R5 представляет собой галоген, C1-C4 алкил, C1-C4 алкиламино, который может быть замещен одной или несколькими 4-10-членными моноциклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или разных гетероатомов, выбранных из азота, кислорода и серы, или C1-C6 алкокси,
(ix-7) одной или нескольких 4-6-членных моноциклических насыщенных гетероциклических групп, которые могут быть замещены группой(ами) R6 и содержат 1-2 идентичных или разных гетероатома, выбранных из азота, кислорода и серы, где R6 представляет собой гидрокси, C1-C6 алкил, C1-C6 алкокси или оксо,
(ix-8) одной или нескольких 4-10-членных моноциклических или дициклических ненасыщенных гетероциклических групп, которые могут быть замещены группой (группами) R7 и содержат 1-3 одинаковых или разных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R7 представляет собой галоген, циано, C1-C6 алкил, C1-C6 алкокси или амино, и
(ix-9) ненасыщенной гетероциклилоксигруппы, которая может быть замещена галогеном, где ненасыщенное гетероциклическое кольцо представляет собой 4-10-членное моноциклическое или дициклическое ненасыщенное гетероциклическое кольцо, содержащее 1-2 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы,
при условии, что положение тройной связи C2-C6 алкинила находится между атомом углерода, связанным с 7H-пирроло[2,3-d]пиримидиновым скелетом, и атомом углерода, соседним с этим атомом углерода,
(x) C6 ароматический углеводород, который может быть замещен
(x-1) гидрокси,
(x-2) C1-C6 алкилом, который может быть замещен гидроксигруппой,
(x-3) формилом, или
(x-4) одной 5-6-членной моноциклической насыщенной гетероциклической группой, которая может быть замещена C1-C6 алкилом и содержать 1-2 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или
(xi) 5-6-членную моноциклическую или 9-10-членную дициклическую насыщенную или ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, которая может быть замещена
(xi-1) галогеном,
(xi-2) C1-C6 алкилом, который может быть замещен гидроксигруппой, или
(xi-3) амино, которое может быть замещено C1-C6 алкильной (карбонильной) группой.
14. Применение соединения, представленного формулой (I) ниже, или его кислотно-аддитивной соли, обладающего действиями селективного ингибитора REТ, для получения противоопухолевого средства:

где в формуле (I) A представляет собой

где R1 представляет собой
галоген,
циано,
нитро,
C1-C6 алкил, который может быть замещен C1-C6 алкоксигруппой или C1-C6 алкилтио, гидрокси, фенилом, где атом водорода, содержащийся в C1-C6 алкокси, может быть замещен 1 или более атомами дейтерия,
C1-C6 алкокси C1-C6 алкокси, замещенный или незамещенный галогеном, где атом водорода, содержащийся в C1-C6 алкокси, может быть замещен 1 или более атомами дейтерия,
C2-C6 алкенил, замещенный или незамещенный галогеном,
незамещенный C2-C6 алкинил,
амино, который может быть замещен одной или несколькими 4-6-членными моноциклическими или полициклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или различных гетероатомов, выбранных из азота, кислорода и серы, или C6-C10 ароматическим углеводородом, или
5-6-членную моноциклическую или полициклическую ненасыщенную гетероциклическую группу, содержащую 1-2 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы,
Y представляет собой N или CH, и
n представляет собой целое число, имеющее значение от 0 до 2,
где, когда n имеет значение 2, два R1 могут быть одинаковыми или отличными друг от друга;
в формуле A2 группа:

образует вместе с фенилом или пиридинилом, с которым эта группа связана, дициклический C9-C10 ароматический углеводород или 9-10-членную дициклическую ненасыщенную гетероциклическую группу, содержащую 1 гетероатом, выбранный из кислорода или серы;
R2 представляет собой
C3-C10 алкил, который может быть замещен 1 или несколькими заместителями, выбранными из группы, состоящей из галогена, С1-С6 алкокси, С3-С7 циклоалкила и 4-10-членной моноциклической или полициклической ненасыщенной гетероциклической группы, содержащей 1-3 одинаковых или разных гетероатомов, выбранных из азота, кислорода и серы,
C3-C7 циклоалкил, который может быть замещен 1 или более заместителями, выбранными из группы, состоящей из С1-С6 алкила, С3-С7 циклоалкила, галоген-С1-С6 алкила и галогена,
C4-C10 связанный мостиковой связью циклоалкил,
C2-C6 алкенил, который может быть замещен галогеном,
C3-C7 циклоалкенил; и
X представляет собой
N или
CR3, где R3 представляет собой
(i) водород,
(ii) галоген,
(iii) циано,
(iv) C1-C4 алкил, который может быть замещен гидрокси или оксо,
(v) C1-C6 алкокси, который может быть замещен 1 или более заместителями, выбранными из группы, состоящей из
(v-1) галогена,
(v-2) C1-C6 алкокси,
(v-3) C3-C7 циклоалкила и
(v-4) одной или нескольких 5-6-членных моноциклических насыщенных гетероциклических групп, которые могут быть замещены оксо и содержат 1 гетероатом, выбранный из азота или кислорода,
(vi) незамещенный C1-C6 алкилтио,
(vii) незамещенный C3-C7 циклоалкил,
(viii) C2-C6 алкенил, который может быть замещен гидрокси,
(ix) C2-C6 алкинил, который может быть замещен 1 или более заместителями, выбранными из группы, состоящей из
(ix-1) гидрокси,
(ix-2) C1-C6 алкокси,
(ix-3) амино, которое может быть замещено группой(ами) R4, где R4 представляет собой по крайней мере один, выбранный из группы, состоящей из C1-C6 алкила, C1-C4 алкокси, C1-C6 алкила и карбамоила, который может быть замещен C3-C7 циклоалкилом,
(ix-4) C1-C6-алкилсилилокси,
(ix-5) C3-C7 циклоалкила, который может быть замещен гидрокси или оксо,
(ix-6) C6-ароматического углеводорода, который может быть замещен группой R5, где R5 представляет собой галоген, C1-C4 алкил, C1-C4 алкиламино, который может быть замещен одной или несколькими 4-10-членными моноциклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или разных гетероатомов, выбранных из азота, кислорода и серы, или C1-C6 алкокси,
(ix-7) одной или нескольких 4-6-членных моноциклических насыщенных гетероциклических групп, которые могут быть замещены группой (ами) R6 и содержат 1-2 идентичных или разных гетероатома, выбранных из азота, кислорода и серы, где R6 представляет собой гидрокси, C1-C6 алкил, C1-C6 алкокси или оксо,
(ix-8) одной или нескольких 4-10-членных моноциклических или дициклических ненасыщенных гетероциклических групп, которые могут быть замещены группой (группами) R7 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R7 представляет собой галоген, циано, C1-C6 алкил, C1-C6 алкокси или амино, и
(ix-9) ненасыщенной гетероциклилоксигруппы, которая может быть замещена галогеном, где ненасыщенное гетероциклическое кольцо представляет собой 4-10-членное моноциклическое или дициклическое ненасыщенное гетероциклическое кольцо, содержащее 1-2 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы,
при условии, что положение тройной связи C2-C6 алкинила находится между атомом углерода, связанным с 7H-пирроло[2,3-d]пиримидиновым скелетом, и атомом углерода, соседним с этим атомом углерода,
(x) замещенный или незамещенный C6 ароматический углеводород, который может быть замещен
(x-1) гидрокси,
(x-2) C1-C6 алкилом, который может быть замещен гидроксигруппой,
(x-3) формилом, или
(x-4) одной 5-6-членной моноциклической насыщенной гетероциклической группой, которая может быть замещена C1-C6 алкилом и содержать 1-2 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или
(xi) 5-6-членную моноциклическую или 9-10-членную дициклическую насыщенную или ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, которая может быть замещена
(xi-1) галогеном,
(xi-2) C1-C6 алкилом, который может быть замещен гидроксигруппой, или
(xi-3) амино, которое может быть замещено C1-C6 алкильной (карбонильной) группой.
15. Применение соединения, представленного формулой (I) ниже, или его кислотно-аддитивной соли для ингибирования RET:

где в формуле (I) A представляет собой

где R1 представляет собой
галоген,
циано,
нитро,
C1-C6 алкил, который может быть замещен C1-C6 алкоксигруппой или C1-C6 алкилтио, гидрокси, фенилом, где атом водорода, содержащийся в C1-C6 алкокси, может быть замещен 1 или более атомами дейтерия,
C1-C6 алкокси, замещенный или незамещенный галогеном, где атом водорода, содержащийся в C1-C6 алкокси, может быть замещен 1 или более атомами дейтерия,
C2-C6 алкенил, замещенный или незамещенный галогеном,
незамещенный C2-C6 алкинил,
амино, который может быть замещен одной или несколькими 4-6-членными моноциклическими или полициклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или различных гетероатомов, выбранных из азота, кислорода и серы, или C6-C10 ароматическим углеводородом, или
5-6-членную моноциклическую ненасыщенную гетероциклическую группу, содержащую 1-2 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы,
Y представляет собой N или CH, и
n представляет собой целое число, имеющее значение от 0 до 2,
где, когда n имеет значение 2, два R1 могут быть одинаковыми или отличными друг от друга;
в формуле A2 группа:

образует вместе с фенилом или пиридинилом, с которым эта группа связана, дициклический C9-C10 ароматический углеводород или 9-10-членную дициклическую ненасыщенную гетероциклическую группу, содержащую 1 гетероатом, выбранный из кислорода или серы;
R2 представляет собой
C3-C10 алкил, который может быть замещен 1 или несколькими заместителями, выбранными из группы, состоящей из галогена, С1-С6 алкокси, С3-С7 циклоалкила и 4-10-членной моноциклической или полициклической ненасыщенной гетероциклической группы, содержащей 1-3 одинаковых или разных гетероатомов, выбранных из азота, кислорода и серы,
C3-C7 циклоалкил, который может быть замещен 1 или более заместителями, выбранными из группы, состоящей из С1-С6 алкила, С3-С7 циклоалкила, галоген-С1-С6 алкила и галогена,
C4-C10 связанный мостиковой связью циклоалкил,
C2-C6 алкенил, который может быть замещен галогеном,
C3-C7 циклоалкенил; и
X представляет собой
N или
CR3, где R3 представляет собой
(i) водород,
(ii) галоген,
(iii) циано,
(iv) C1-C4 алкил, который может быть замещен гидрокси или оксо,
(v) C1-C6 алкокси, который может быть замещен 1 или более заместителями, выбранными из группы, состоящей из
(v-1) галогена,
(v-2) C1-C6 алкокси,
(v-3) C3-C7 циклоалкила и
(v-4) одной или нескольких 5-6-членных моноциклических насыщенных гетероциклических групп, которые могут быть замещены оксо и содержат 1 гетероатом, выбранный из азота или кислорода,
(vi) незамещенный C1-C6 алкилтио,
(vii) незамещенный C3-C7 циклоалкил,
(viii) C2-C6 алкенил, который может быть замещен гидрокси,
(ix) C2-C6 алкинил, который может быть замещен 1 или более заместителями, выбранными из группы, состоящей из
(ix-1) гидрокси,
(ix-2) C1-C6 алкокси,
(ix-3) амино, которое может быть замещено группой(ами) R4, где R4 представляет собой по крайней мере один, выбранный из группы, состоящей из C1-C6 алкила, C1-C4 алкокси, C1-C6 алкила и карбамоила, который может быть замещен C3-C7 циклоалкилом,
(ix-4) C1-C6-алкилсилилокси,
(ix-5) C3-C7 циклоалкила, который может быть замещен гидрокси или оксо,
(ix-6) C6-ароматического углеводорода, который может быть замещен группой R5, где R5 представляет собой галоген, C1-C4 алкил, C1-C4 алкиламино, который может быть замещен одной или несколькими 4-10-членными моноциклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или разных гетероатомов, выбранных из азота, кислорода и серы, или C1-C6 алкокси,
(ix-7) одной или нескольких 4-6-членных моноциклических насыщенных гетероциклических групп, которые могут быть замещены группой(ами) R6 и содержат 1-2 идентичных или разных гетероатома, выбранных из азота, кислорода и серы, где R6 представляет собой гидрокси, C1-C6 алкил, C1-C6 алкокси или оксо,
(ix-8) одной или нескольких 4-10-членных моноциклических или дициклических ненасыщенных гетероциклических групп, которые могут быть замещены группой (группами) R7 и содержат 1-3 одинаковых или разных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R7 представляет собой галоген, циано, C1-C6 алкил, C1-C6 алкокси или амино, и
(ix-9) ненасыщенной гетероциклилоксигруппы, которая может быть замещена галогеном, где ненасыщенное гетероциклическое кольцо представляет собой 4-10-членное моноциклическое или дициклическое ненасыщенное гетероциклическое кольцо, содержащее 1-2 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы,
при условии, что положение тройной связи C2-C6 алкинила находится между атомом углерода, связанным с 7H-пирроло[2,3-d]пиримидиновым скелетом, и атомом углерода, соседним с этим атомом углерода,
(x) C6 ароматический углеводород, который может быть замещен
(x-1) гидрокси,
(x-2) C1-C6 алкилом, который может быть замещен гидроксигруппой,
(x-3) формилом, или
(x-4) одной 5-6-членной моноциклической насыщенной гетероциклической группой, которая может быть замещена C1-C6 алкилом и содержать 1-2 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или
(xi) 5-6-членную моноциклическую или 9-10-членную дициклическую насыщенную или ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, которая может быть замещена
(xi-1) галогеном,
(xi-2) C1-C6 алкилом, который может быть замещен гидроксигруппой, или
(xi-3) амино, которое может быть замещено C1-C6 алкильной (карбонильной) группой.
16. Применение соединения, представленного формулой (I) ниже, или его кислотно-аддитивной соли для профилактики или лечения злокачественной опухоли, связанной с активностью RET:
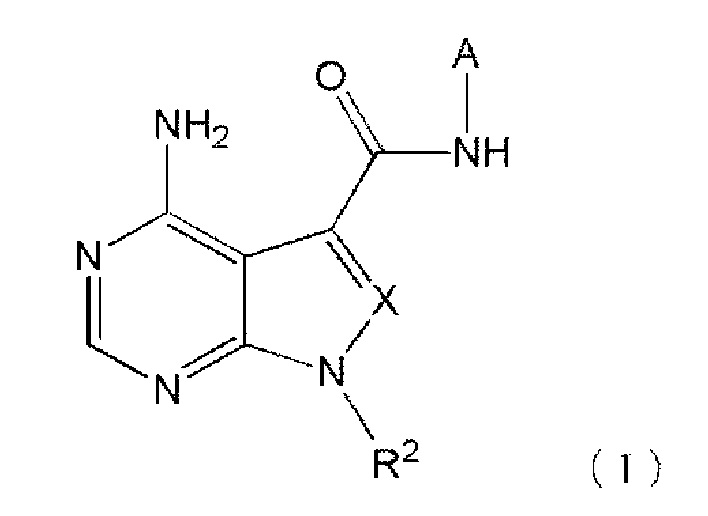
где в формуле (I) A представляет собой
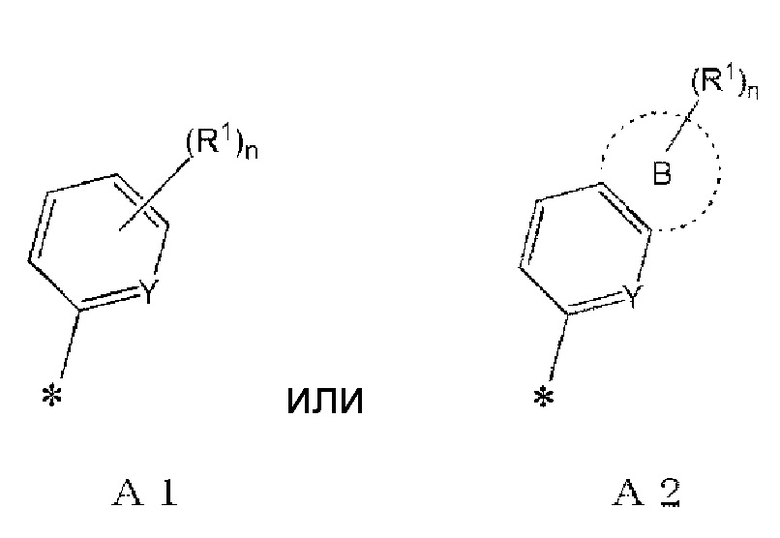
где R1 представляет собой
галоген,
циано,
нитро,
C1-C6 алкил, который может быть замещен C1-C6 алкоксигруппой или C1-C6 алкилтио, гидрокси, фенилом, где атом водорода, содержащийся в C1-C6 алкокси, может быть замещен 1 или более атомами дейтерия,
C1-C6 алкокси, замещенный или незамещенный галогеном, где атом водорода, содержащийся в C1-C6 алкокси, может быть замещен 1 или более атомами дейтерия,
C2-C6 алкенил, замещенный или незамещенный галогеном,
незамещенный C2-C6 алкинил,
амино, который может быть замещен одной или несколькими 4-6-членными моноциклическими или полициклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или различных гетероатомов, выбранных из азота, кислорода и серы, или C6-C10 ароматическим углеводородом, или
5-6-членную моноциклическую или ненасыщенную гетероциклическую группу, содержащую 1-2 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы,
Y представляет собой N или CH, и
n представляет собой целое число, имеющее значение от 0 до 2,
где, когда n имеет значение 2, два R1 могут быть одинаковыми или отличными друг от друга;
в формуле A2 группа:

образует вместе с фенилом или пиридинилом, с которым эта группа связана, дициклический C9-C10 ароматический углеводород или 9-10-членную дициклическую ненасыщенную гетероциклическую группу, содержащую 1 гетероатом, выбранный из кислорода или серы;
R2 представляет собой
C3-C10 алкил, который может быть замещен 1 или несколькими заместителями, выбранными из группы, состоящей из галогена, С1-С6 алкокси, С3-С7 циклоалкила и 4-10-членной моноциклической или полициклической ненасыщенной гетероциклической группы, содержащей 1-3 одинаковых или разных гетероатомов, выбранных из азота, кислорода и серы,
C3-C7 циклоалкил, который может быть замещен 1 или более заместителями, выбранными из группы, состоящей из С1-С6 алкила, С3-С7 циклоалкила, галоген-С1-С6 алкила и галогена,
C4-C10 связанный мостиковой связью циклоалкил,
C2-C6 алкенил, который может быть замещен галогеном,
C3-C7 циклоалкенил; и
X представляет собой
N или
CR3, где R3 представляет собой
(i) водород,
(ii) галоген,
(iii) циано,
(iv) C1-C6 алкил, который может быть замещен гидрокси или оксо,
(v) C1-C6 алкокси, который может быть замещен 1 или более заместителями, выбранными из группы, состоящей из
(v-1) галогена,
(v-2) C1-C6 алкокси,
(v-3) C3-C7 циклоалкила и
(v-4) одной или нескольких 5-6-членных моноциклических насыщенных гетероциклических групп, которые могут быть замещены оксо и содержат 1 гетероатом, выбранный из азота или кислорода,
(vi) незамещенный C1-C6 алкилтио,
(vii) незамещенный C3-C7 циклоалкил,
(viii) C2-C6 алкенил, который может быть замещен гидрокси,
(ix) C2-C6 алкинил, который может быть замещен 1 или более заместителями, выбранными из группы, состоящей из
(ix-1) гидрокси,
(ix-2) C1-C6 алкокси,
(ix-3) амино, которое может быть замещено группой(ами) R4, где R4 представляет собой по крайней мере один, выбранный из группы, состоящей из C1-C6 алкила, C1-C4 алкокси, C1-C6 алкила и карбамоила, который может быть замещен C3-C7 циклоалкилом,
(ix-4) C1-C6-алкилсилилокси,
(ix-5) C3-C7 циклоалкила, который может быть замещен гидрокси или оксо,
(ix-6) C6-ароматического углеводорода, который может быть замещен группой R5, где R5 представляет собой галоген, C1-C4 алкил, C1-C4 алкиламино, который может быть замещен одной или несколькими 4-10-членными моноциклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или разных гетероатомов, выбранных из азота, кислорода и серы, или C1-C6 алкокси,
(ix-7) одной или нескольких 4-6-членных моноциклических насыщенных гетероциклических групп, которые могут быть замещены группой(ами) R6 и содержат 1-2 идентичных или разных гетероатома, выбранных из азота, кислорода и серы, где R6 представляет собой гидрокси, C1-C6 алкил, C1-C6 алкокси или оксо,
(ix-8) одной или нескольких 4-10-членных моноциклических или дициклических ненасыщенных гетероциклических групп, которые могут быть замещены группой (группами) R7 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R7 представляет собой галоген, циано, C1-C6 алкил, C1-C6 алкокси или амино, и
(ix-9) ненасыщенной гетероциклилоксигруппы, которая может быть замещена галогеном, где ненасыщенное гетероциклическое кольцо представляет собой 4-10-членное моноциклическое или дициклическое ненасыщенное гетероциклическое кольцо, содержащее 1-2 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы,
при условии, что положение тройной связи C2-C6 алкинила находится между атомом углерода, связанным с 7H-пирроло[2,3-d]пиримидиновым скелетом, и атомом углерода, соседним с этим атомом углерода,
(x) C6 ароматический углеводород, который может быть замещен
(x-1) гидрокси,
(x-2) C1-C6 алкилом, который может быть замещен гидроксигруппой,
(x-3) формилом, или
(x-4) одной 5-6-членной моноциклической насыщенной гетероциклической группой, которая может быть замещена C1-C6 алкилом и содержать 1-2 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или
(xi) 5-6-членную моноциклическую или 9-10-членную дициклическую насыщенную или ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, которая может быть замещена
(xi-1) галогеном,
(xi-2) C1-C6 алкилом, который может быть замещен гидроксигруппой, или
(xi-3) амино, которое может быть замещено C1-C6 алкильной (карбонильной) группой.
17. Применение по любому из пп. 13-16, где, когда A представляет собой A1, A1 представляет собой
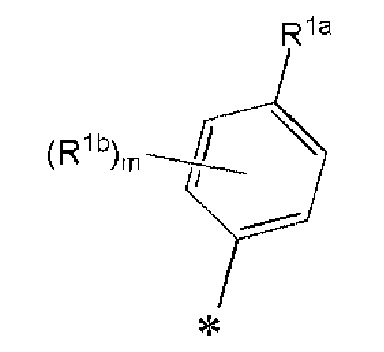
где R1a представляет собой
C1-C6 алкил, который может быть замещен группой C1-C6 алкокси или C1-C6 алкилтио, где водород, содержащийся в C1-C6 алкокси, может быть замещен 1 или несколькими атомами дейтерия,
C2-C6 алкенил,
C2-C6 алкинил,
амино, который может быть замещен одной или несколькими 4-6-членными моноциклическими или полициклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или C6-C10 ароматическим углеводородом, или
5-6-членную моноциклическую или полициклическую ненасыщенную гетероциклическую группу, содержащую 1-2 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы;
R1b представляет собой галоген, C1-C6 алкил или C1-C6 алкокси; и
m представляет собой целое число, имеющее значение от 0 или 1.
18. Применение по любому из пп. 13-16, где R2 представляет собой
C3-C10 алкил, который может быть замещен одним или несколькими заместителями, выбранными из группы, состоящей из галогена, C3-C7 циклоалкила и одной или нескольких 4-10-членных моноциклических или полициклических ненасыщенных гетероциклических групп, содержащих 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы,
C3-C7 циклоалкил, который может быть замещен одним или несколькими заместителями, выбранными из группы, состоящей из C1-C6 алкила, C3-C7 циклоалкила и галогенo C1-C6 алкила,
C4-C10 связанный мостиковой связью циклоалкил или
C3-C7 циклоалкенил.
19. Применение по любому из пп. 13-16, где, когда X представляет собой CR3, R3 представляет собой
(i) водород,
(ii) галоген,
(iii) циано,
(iv) C1-C4 алкил, который может быть замещен гидроксигруппой или оксо,
(v) C1-C6 алкокси, который может быть замещен одним или несколькими заместителями, выбранными из группы, состоящей из
(v-1) галогена,
(v-2) C1-C6 алкокси,
(v-3) C3-C7 циклоалкила и
(v-4) одной или нескольких 5-6-членных моноциклических насыщенных гетероциклических групп, которые могут быть замещены оксо и содержат 1 гетероатом, выбранный из азота или кислорода,
(vi) C1-C4 алкилтио,
(vii) C3-C5 циклоалкил,
(viii) C2-C6 алкенил, который может быть замещен гидроксигруппой,
(ix) C2-C6 алкинил, который может быть замещен одним или несколькими заместителями, выбранными из группы, состоящей из
(ix-1) гидрокси,
(ix-2) C1-C6 алкокси,
(ix-3) амино, который может быть замещен группой R4, где R4 представляет собой C1-C6 алкил, C1-C4 алкокси C1-C6 алкил или карбамоил, который может быть замещен C3-C7 циклоалкилом,
(ix-4) C1-C6 алкилсилилокси,
(ix-5) C3-C7 циклоалкила, который может быть замещен гидроксигруппой или оксо,
(ix-6) C6 ароматического углеводорода, который может быть замещен группой R5, где R5 представляет собой галоген, C1-C4 алкиламино, который может быть замещен одной или несколькими 4-10-членными моноциклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или C1-C6 алкокси,
(ix-7) одной или нескольких 4-6-членных моноциклических насыщенных гетероциклических групп, которые могут быть замещены группой R6 и содержат 1-2 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R6 представляет собой гидрокси, C1-C6 алкил, C1-C6 алкокси или оксо,
(ix-8) одной или нескольких 4-10-членных моноциклических или дициклических ненасыщенных гетероциклических групп, которые могут быть замещены группой R7 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R7 представляет собой галоген, циано, C1-C6 алкил, C1-C6 алкокси или амино, и
(ix-9) ненасыщенного гетероциклилокси, который может быть замещен галогеном, где ненасыщенное гетероциклическое кольцо представляет собой 4-10-членное моноциклическое или дициклическое ненасыщенное гетероциклическое кольцо, содержащее 1-2 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы,
при условии, что положение тройной связи C2-C6 алкинила находится между атомом углерода, связанным с 7H-пирроло[2,3-d]пиримидиновым скелетом, и атомом углерода, смежным с этим атомом углерода,
(x) C6 ароматический углеводород, который может быть замещен
(x-1) гидрокси,
(x-2) C1-C6 алкилом, который может быть замещен гидроксигруппой,
(x-3) формилом или
(x-4) одной или несколькими 5-6-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены C1-C6 алкилом и содержат 1-2 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или
(xi) 4-6-членную моноциклическую ненасыщенную гетероциклическую группу, которая может быть замещена
(xi-1) галогеном,
(xi-2) C1-C6 алкилом, который может быть замещен гидроксигруппой, или
(xi-3) амино, который может быть замещен группой C1-C6 алкил(карбонил),
и содержит 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы.
20. Применение по любому из пп. 13-16, где A представляет собой

где R1a представляет собой
C1-C6 алкил, который может быть замещен группой C1-C6 алкокси или C1-C6 алкилтио, где водород, содержащийся в C1-C6 алкокси, может быть замещен 1 или несколькими атомами дейтерия,
C2-C6 алкенил,
C2-C6 алкинил,
амино, который может быть замещен одной или несколькими 4-6-членными моноциклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или C6-C10 ароматическим углеводородом, или
5-6-членную моноциклическую ненасыщенную гетероциклическую группу, содержащую 1-2 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы;
R1b представляет собой галоген, C1-C6 алкил или C1-C6 алкокси;
m представляет собой целое число, имеющее значение от 0 или 1;
R2 представляет собой
C3-C10 алкил, который может быть замещен одним или несколькими заместителями, выбранными из группы, состоящей из галогена, C3-C7 циклоалкила и одной или нескольких 4-10-членных моноциклических или полициклических ненасыщенных гетероциклических групп, содержащих 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы,
C3-C7 циклоалкил, который может быть замещен одним или несколькими заместителями, выбранными из группы, состоящей из C1-C6 алкила, C3-C7 циклоалкила и галогенo C1-C6 алкила, или
C4-C10 связанный мостиковой связью циклоалкил; и
X представляет собой
N или
CR3, где R3 представляет собой
(i') водород,
(ii') галоген,
(iii') циано,
(iv') C1-C4 алкил,
(v') C1-C6 алкокси, который может быть замещен одним или несколькими заместителями, выбранными из группы, состоящей из
(v-1') галогена,
(v-2') C1-C6 алкокси,
(v-3') C3-C7 циклоалкила и
(v-4') одной или нескольких 5-6-членных моноциклических насыщенных гетероциклических групп, которые могут быть замещены оксо и содержат 1 гетероатом, выбранный из азота или кислорода,
(vi') C1-C4 алкилтио,
(vii') C3-C5 циклоалкил,
(viii') C2-C4 алкенил, который может быть замещен гидроксигруппой,
(ix') C2-C6 алкинил, который может быть замещен одним или несколькими заместителями, выбранными из группы, состоящей из
(ix-1') гидрокси,
(ix-2') C1-C4 алкокси,
(ix-3') амино, который может быть замещен группой R4, где R4 представляет собой C1-C4 алкил, C1-C4 алкокси C1-C4 алкил или карбамоил, который может быть замещен C3-C5 циклоалкилом,
(ix-4') C1-C6 алкилсилилокси,
(ix-5') C3-C7 циклоалкила, который может быть замещен гидроксигруппой или оксо,
(ix-6') фенила, который может быть замещен группой R5, где R5 представляет собой галоген, метиламино, который может быть замещен одной или несколькими 4-6-членными моноциклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или C1-C4 алкокси,
(ix-7') одной или нескольких 4-6-членных моноциклических насыщенных гетероциклических групп, которые могут быть замещены группой R6 и содержат 1-2 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R6 представляет собой гидрокси, C1-C4 алкил, C1-C4 алкокси или оксо,
(ix-8') одной или нескольких 4-10-членных моноциклических или дициклических ненасыщенных гетероциклических групп, которые могут быть замещены группой R7 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R7 представляет собой галоген, циано, C1-C4 алкил, C1-C4 алкокси или амино, и
(ix-9') ненасыщенного гетероциклического окси, который может быть замещен галогеном, где ненасыщенное гетероциклическое кольцо представляет собой 4-6-членное моноциклическое ненасыщенное гетероциклическое кольцо, содержащее 1-2 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы,
при условии, что положение тройной связи C2-C6 алкинила находится между атомом углерода, связанным с 7H-пирроло[2,3-d]пиримидиновым скелетом, и атомом углерода, смежным с этим атомом углерода,
(x') фенил, который может быть замещен
(x-1') гидрокси,
(x-2') C1-C4 алкилом, который может быть замещен гидроксигруппой,
(x-3') формилом или
(x-4') одной 5-6-членной моноциклической насыщенной гетероциклической группой, которая может быть замещена C1-C4 алкилом и содержит 1-2 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или
(xi') 5-6-членную моноциклическую ненасыщенную гетероциклическую группу, которая может быть замещена
(xi-1') галогеном,
(xi-2') C1-C4 алкилом, который может быть замещен гидроксигруппой, или
(xi-3') амино, который может быть замещен группой C1-C4 алкил(карбонил),
и содержит 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы.
21. Применение по любому из пп. 13-16, где A представляет собой

где R1b представляет собой галоген;
m представляет собой целое число, имеющее значение от 0 или 1;
R2 представляет собой
C3-C6 алкил, который может быть замещен галогеном, или
C3-C7 циклоалкил, который может быть замещен C1-C4 алкилом или C3-C5 циклоалкилом; и
X представляет собой CR3, где R3 представляет собой
(i'') водород,
(ii'') галоген,
(v') C1-C4 алкокси, который может быть замещен одним или несколькими заместителями, выбранными из группы, состоящей из
(v-2'') C1-C4 алкокси,
(v-3'') C3-C7 циклоалкила и
(v-4'') одной или нескольких 4-6-членных моноциклических насыщенных гетероциклических групп, содержащих один атом кислорода,
(vi'') C1-C4 алкилтио,
(viii') C2-C4 алкенил,
(ix') C2-C6 алкинил, который может быть замещен одним или несколькими заместителями, выбранными из группы, состоящей из
(ix-1'') гидрокси,
(ix-2'') амино, который может быть замещен группой R4, где R4 представляет собой C1-C4 алкил или C1-C4 алкокси C1-C4 алкил,
(ix-5'') C3-C7 циклоалкила, который может быть замещен гидроксигруппой,
(ix-6'') фенила, который может быть замещен группой R5, где R5 представляет собой галоген,
(ix-7'') одной или нескольких 4-6-членных моноциклических насыщенных гетероциклических групп, которые могут быть замещены группой R6 и содержат 1-2 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R6 представляет собой гидрокси, C1-C4 алкил или оксо, и
(ix-8'') одной или нескольких 4-10-членных моноциклических или бициклических ненасыщенных гетероциклических групп, которые могут быть замещены группой R7 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R7 представляет собой галоген, циано, C1-C4 алкил, C1-C4 алкокси или амино,
при условии, что положение тройной связи C2-C6 алкинила находится между атомом углерода, связанным с 7H-пирроло[2,3-d]пиримидиновым скелетом, и атомом углерода, смежным с этим атомом углерода,
(x'') фенил, который может быть замещен гидрокси или C1-C4 алкилом, который может быть замещен гидроксигруппой, или
(xi'') 5-6-членную моноциклическую ненасыщенную гетероциклическую группу, содержащую 1 или 2 атома азота.
22. Соединение, представленное формулой (I') ниже, или его кислотно-аддитивная соль:

где в формуле (I') A представляет собой

где R1 представляет собой галоген,
циано,
нитро,
C1-C6 алкил, который может быть замещен C1-C6 алкоксигруппой или C1-C6 алкилтио, гидрокси, фенилом, где атом водорода, содержащийся в C1-C6 алкокси, может быть замещен 1 или более атомами дейтерия,
C1-C6 алкокси, замещенный или незамещенный галогеном, где атом водорода, содержащийся в C1-C6 алкокси, может быть замещен 1 или более атомами дейтерия,
C2-C6 алкенил, замещенный или незамещенный галогеном,
незамещенный C2-C6 алкинил,
амино, который может быть замещен одной или несколькими 4-6-членными моноциклическими или полициклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или различных гетероатомов, выбранных из азота, кислорода и серы, или C6-C10 ароматическим углеводородом, или
5-6-членную моноциклическую ненасыщенную гетероциклическую группу, содержащую 1-2 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы,
Y представляет собой N или CH, и
n представляет собой целое число, имеющее значение от 0 до 2,
где, когда n имеет значение 2, два R1 могут быть одинаковыми или отличными друг от друга;
в формуле A2 группа:

образует вместе с фенилом или пиридинилом, с которым эта группа связана, дициклический C9-C10 ароматический углеводород или 9-10-членную дициклическую ненасыщенную гетероциклическую группу, содержащую 1 гетероатом, выбранный из кислорода или серы;
R2 представляет собой
C3-C10 алкил, который может быть замещен 1 или несколькими заместителями, выбранными из группы, состоящей из галогена, С1-С6 алкокси, С3-С7 циклоалкила и 4-10-членной моноциклической или полициклической ненасыщенной гетероциклической группы, содержащей 1-3 одинаковых или разных гетероатомов, выбранных из азота, кислорода и серы,
C3-C4 циклоалкил, который может быть замещен 1 или более заместителями, выбранными из группы, состоящей из С1-С6 алкила, С3-С7 циклоалкила, галоген-С1-С6 алкила и галогена,
C4-C10 связанный мостиковой связью циклоалкил,
C2-C6 алкенил, который может быть замещен галогеном,
C3-C4 циклоалкенил; и
X представляет собой
N или
CR3, где R3 представляет собой
(i) водород,
(ii) галоген,
(iii) циано,
(iv) C1-C6 алкил, который может быть замещен гидрокси или оксо,
(v) C1-C6 алкокси, который может быть замещен 1 или более заместителями, выбранными из группы, состоящей из
(v-1) галогена,
(v-2) C1-C6 алкокси,
(v-3) C3-C7 циклоалкила и
(v-4) одной или нескольких 5-6-членных моноциклических насыщенных гетероциклических групп, которые могут быть замещены оксо и содержат 1 гетероатом, выбранный из азота или кислорода,
(vi) незамещенный C1-C6 алкилтио,
(vii) незамещенный C3-C7 циклоалкил,
(viii) C2-C6 алкенил, который может быть замещен гидрокси,
(ix) C2-C6 алкинил, который может быть замещен 1 или более заместителями, выбранными из группы, состоящей из
(ix-1) гидрокси,
(ix-2) C1-C6 алкокси,
(ix-3) амино, которое может быть замещено группой(ами) R4, где R4 представляет собой по крайней мере один, выбранный из группы, состоящей из C1-C6 алкила, C1-C4 алкокси, C1-C6 алкила и карбамоила, который может быть замещен C3-C7 циклоалкилом,
(ix-4) C1-C6-алкилсилилокси,
(ix-5) C3-C7 циклоалкила, который может быть замещен гидрокси или оксо,
(ix-6) C6-ароматического углеводорода, который может быть замещен группой R5, где R5 представляет собой галоген, C1-C4 алкил, C1-C4 алкиламино, который может быть замещен одной или несколькими 4-10-членными моноциклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или разных гетероатомов, выбранных из азота, кислорода и серы, или C1-C6 алкокси,
(ix-7) одной или нескольких 4-6-членных моноциклических насыщенных гетероциклических групп, которые могут быть замещены группой(ами) R6 и содержат 1-2 идентичных или разных гетероатома, выбранных из азота, кислорода и серы, где R6 представляет собой гидрокси, C1-C6 алкил, C1-C6 алкокси или оксо,
(ix-8) одной или нескольких 4-10-членных моноциклических или дициклических ненасыщенных гетероциклических групп, которые могут быть замещены группой (группами) R7 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R7 представляет собой галоген, циано, C1-C6 алкил, C1-C6 алкокси или амино, и
(ix-9) ненасыщенной гетероциклилоксигруппы, которая может быть замещена галогеном, где ненасыщенное гетероциклическое кольцо представляет собой 4-10-членное моноциклическое или дициклическое ненасыщенное гетероциклическое кольцо, содержащее 1-2 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы,
при условии, что положение тройной связи C2-C6 алкинила находится между атомом углерода, связанным с 7H-пирроло[2,3-d]пиримидиновым скелетом, и атомом углерода, соседним с этим атомом углерода,
(x) C6 ароматический углеводород, который может быть замещен
(x-1) гидрокси,
(x-2) C1-C6 алкилом, который может быть замещен гидроксигруппой,
(x-3) формилом, или
(x-4) одной 5-6-членной моноциклической насыщенной гетероциклической группой, которая может быть замещена C1-C6 алкилом и содержать 1-2 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или
(xi) 5-6-членную моноциклическую или 9-10-членную дициклическую насыщенную или ненасыщенную гетероциклическую группу, содержащую 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, которая может быть замещена
(xi-1) галогеном,
(xi-2) C1-C6 алкилом, который может быть замещен гидроксигруппой, или
(xi-3) амино, которое может быть замещено C1-C6 алкильной (карбонильной) группой.
23. Соединение или его соль по п. 22, где, когда A представляет собой A1, A1 представляет собой

где R1a представляет собой
C1-C6 алкил, который является незамещенным или замещен группой C1-C6 алкокси или C1-C6 алкилтио, где водород, содержащийся в алкокси, может быть замещен 1 или несколькими атомами дейтерия,
C2-C6 алкенил,
C2-C6 алкинил,
амино, который может быть замещен одной или несколькими 4-6-членными моноциклическими или полициклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или C6-C10 ароматическим углеводородом, или
5-6-членную моноциклическую ненасыщенную гетероциклическую группу, содержащую 1-2 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы;
R1b представляет собой галоген, C1-C6 алкил или C1-C6 алкокси; и
m представляет собой целое число, имеющее значение от 0 или 1.
24. Соединение или его соль по п. 22, где R2 выбран из группы, состоящей из:
C3-C10 алкила, который является незамещенным или замещен одним или несколькими заместителями, выбранными из группы, состоящей из галогена, C3-C7 циклоалкила и одной или нескольких 4-10-членных моноциклических или полициклических ненасыщенных гетероциклических групп, содержащих 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы;
C3-C4 циклоалкила, который является незамещенным или замещен одним или несколькими заместителями, выбранными из группы, состоящей из C1-C6 алкила, C3-C7 циклоалкила и галогенo C1-C6 алкила,
C4-C10 связанного мостиковой связью циклоалкила; и
C3-C4 циклоалкенила.
25. Соединение или его соль по п. 22, где, когда X представляет собой CR3, R3 выбран из группы, состоящей из:
(i) водорода;
(ii) галогена;
(iii) циано;
(iv) C1-C4 алкила, который является незамещенным или замещен гидрокси- или оксогруппой;
(v) C1-C6 алкокси, который является незамещенным или замещен одним или несколькими заместителями, выбранными из группы, состоящей из
(v-1) галогена,
(v-2) C1-C6 алкокси,
(v-3) C3-C7 циклоалкила и
(v-4) одной или нескольких 5-6-членных моноциклических насыщенных гетероциклических групп, которые могут быть замещены оксо и содержат 1 гетероатом, выбранный из азота или кислорода;
(vi) C1-C4 алкилтио;
(vii) C3-C5 циклоалкила;
(viii) C2-C6 алкенила, который может быть замещен гидроксилом;
(ix) C2-C6 алкинила, который может быть замещен одним или несколькими заместителями, выбранными из группы, состоящей из
(ix-1) гидрокси;
(ix-2) C1-C6 алкокси;
(ix-3) амино, который может быть замещен группой R4, где R4 выбран из группы, состоящей из C1-C6 алкила, C1-C4 алкокси C1-C6 алкила и карбамоила, который является незамещенным или замещен C3-C7 циклоалкилом;
(ix-4) C1-C6 алкилсилилокси;
(ix-5) C3-C7 циклоалкила, который является незамещенным или замещен гидрокси- или оксогруппой,
(ix-6) C6 ароматического углеводорода, который может быть замещен группой R5, где R5 выбран из группы, состоящей из галогена; C1-C4 алкиламино, который является незамещенным или замещен одной или несколькими 4-10-членными моноциклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы; и C1-C6 алкокси;
(ix-7) одной или нескольких 4-6-членных моноциклических насыщенных гетероциклических групп, которые могут быть замещены группой R6 и содержат 1-2 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R6 выбран из группы, состоящей из гидрокси, C1-C6 алкила, C1-C6 алкокси и оксо;
(ix-8) одной или нескольких 4-10-членных моноциклических или дициклических ненасыщенных гетероциклических групп, которые могут быть замещены группой R7 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R7 выбран из группы, состоящей из галогена, циано, C1-C6 алкила, C1-C6 алкокси и амино; и
(ix-9) ненасыщенного гетероциклилокси, который является незамещенным или замещен галогеном, где ненасыщенное гетероциклическое кольцо представляет собой 4-10-членное моноциклическое или полициклическое ненасыщенное гетероциклическое кольцо, содержащее 1-2 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы;
где положение тройной связи C2-C6 алкинила находится между атомом углерода, связанным с 7H-пирроло[2,3-d]пиримидиновым скелетом, и атомом углерода, смежным с этим атомом углерода,
(x) C6 ароматического углеводорода, который может быть замещен
(x-1) гидрокси,
(x-2) C1-C6 алкилом, который может быть замещен гидроксилом,
(x-3) формилом или
(x-4) одной или несколькими 5-6-членными моноциклическими насыщенными гетероциклическими группами, которые могут быть замещены C1-C6 алкилом и содержат 1-2 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, и
(xi) 5-6-членной моноциклической ненасыщенной гетероциклической группы, которая может быть замещена одним или несколькими заместителями, выбранными из группы, состоящей из
(xi-1) галогена и
(xi-2) C1-C6 алкила, который может быть замещен гидроксигруппой, или
(xi-3) амино, который может быть замещен группой C1-C6 алкил(карбонил),
где указанная 5-6-членная моноциклическая ненасыщенная гетероциклическая группа содержит 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы.
26. Соединение или его соль по п. 22, где A представляет собой

где
R1a выбран из группы, состоящей из:
C1-C6 алкила, который является незамещенным или замещен группой C1-C6 алкокси или C1-C6 алкилтио, где водород, содержащийся в алкокси, может быть замещен 1 или несколькими атомами дейтерия,
C2-C6 алкенила,
C2-C6 алкинила,
амино, который может быть замещен одной или несколькими 4-6-членными моноциклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, или C6-C10 ароматическим углеводородом, или
5-6-членной моноциклической ненасыщенной гетероциклической группы, содержащей 1-2 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы;
R1b представляет собой галоген, C1-C6 алкил или C1-C6 алкокси;
m представляет собой целое число, имеющее значение от 0 или 1;
R2 выбран из группы, состоящей из:
C3-C10 алкила, который может быть замещен одним или несколькими заместителями, выбранными из группы, состоящей из галогена, C3-C7 циклоалкила и одной или нескольких 4-10-членных моноциклических или полициклических ненасыщенных гетероциклических групп, содержащих 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы,
C3-C4 циклоалкила, который может быть замещен одним или несколькими заместителями, выбранными из группы, состоящей из C1-C6 алкила, C3-C7 циклоалкила и галогенo C1-C6 алкила, и
C4-C10 связанного мостиковой связью циклоалкила; и
X представляет собой
N или
CR3, где R3 выбран из группы, состоящей из
(i') водорода,
(ii') галогена,
(iii') циано,
(iv') C1-C4 алкила,
(v') C1-C6 алкокси, который может быть замещен одним или несколькими заместителями, выбранными из группы, состоящей из
(v-1') галогена,
(v-2') C1-C6 алкокси,
(v-3') C3-C7 циклоалкила и
(v-4') одной или нескольких 5-6-членных моноциклических насыщенных гетероциклических групп, которые могут быть замещены оксо и содержат 1 гетероатом, выбранный из азота или кислорода,
(vi') C1-C4 алкилтио,
(vii') C3-C5 циклоалкила,
(viii') C2-C4 алкенила, который может быть замещен гидроксигруппой,
(ix') C2-C6 алкинила, который может быть замещен одним или несколькими заместителями, выбранными из группы, состоящей из:
(ix-1') гидрокси,
(ix-2') C1-C4 алкокси,
(ix-3') амино, который может быть замещен группой R4, где R4 представляет собой C1-C4 алкил, C1-C4 алкокси C1-C4 алкил, или карбамоил, который может быть замещен C3-C5 циклоалкилом,
(ix-4') C1-C6 алкилсилилокси,
(ix-5') C3-C7 циклоалкила, который может быть замещен гидроксигруппой или оксо,
(ix-6') фенила, который может быть замещен группой R5, где R5 выбран из группы, состоящей из галогена; метиламино, который может быть замещен одной или несколькими 4-6-членными моноциклическими ненасыщенными гетероциклическими группами, содержащими 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы; и C1-C4 алкокси;
(ix-7') одной или нескольких 4-6-членных моноциклических насыщенных гетероциклических групп, которые могут быть замещены группой R6 и содержат 1-2 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R6 представляет собой гидрокси, C1-C4 алкил, C1-C4 алкокси или оксо;
(ix-8') одной или нескольких 4-6-членных моноциклических или дициклических ненасыщенных гетероциклических групп, которые могут быть замещены группой R7 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R7 выбран из группы, состоящей из галогена, циано, C1-C4 алкила, C1-C4 алкокси и амино; и
(ix-9') ненасыщенного гетероциклилокси, который может быть замещен галогеном, где ненасыщенное гетероциклическое кольцо представляет собой 4-6-членное моноциклическое ненасыщенное гетероциклическое кольцо, содержащее 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы;
где положение тройной связи C2-C6 алкинила находится между атомом углерода, связанным с 7H-пирроло[2,3-d]пиримидиновым скелетом, и атомом углерода, смежным с этим атомом углерода;
(x') фенила, который может быть замещен одним или несколькими заместителями, выбранными из группы, состоящей из:
(x-1') гидроксила,
(x-2') C1-C4 алкила, который может быть замещен гидроксигруппой,
(x-3') формила и
(x-4') одной или нескольких 5-6-членных моноциклических насыщенных гетероциклических групп, которые могут быть замещены C1-C4 алкилом и содержат 1-2 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы; или
(xi') 5-6-членной моноциклической ненасыщенной гетероциклической группы, которая может быть замещена
(xi-1') галогеном,
(xi-2') C1-C4 алкилом, который может быть замещен гидроксигруппой, или
(xi-3') амино, который может быть замещен группой C1-C4 алкил(карбонил),
где указанная 5-6-членная моноциклическая ненасыщенная гетероциклическая группа содержит 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы.
27. Соединение или его соль по п. 22, где A представляет собой

где R1b представляет собой галоген;
m представляет собой целое число, имеющее значение от 0 или 1;
R2 представляет собой
C3-C6 алкил, который может быть замещен галогеном, или
C3-C4 циклоалкил, который может быть замещен C1-C4 алкилом или C3-C5 циклоалкилом; и
X представляет собой CR3, где R3 представляет собой
(i'') водород;
(ii'') галоген;
(v') C1-C4 алкокси, который может быть замещен одним или несколькими заместителями, выбранными из группы, состоящей из:
(v-2'') C1-C4 алкокси,
(v-3'') C3-C7 циклоалкила и
(v-4'') одной или нескольких 4-6-членных моноциклических насыщенных гетероциклических групп, содержащих один атом кислорода;
(vi'') C1-C4 алкилтио,
(viii') C2-C4 алкенил,
(ix') C2-C6 алкинил, который может быть замещен одним или несколькими заместителями, выбранными из группы, состоящей из:
(ix-1'') гидрокси;
(ix-2'') амино, который может быть замещен группой R4, где R4 представляет собой C1-C4 алкил или C1-C4 алкокси C1-C4 алкил;
(ix-5'') C3-C7 циклоалкила, который может быть замещен гидроксигруппой;
(ix-6'') фенила, который может быть замещен группой R5, где R5 представляет собой галоген,
(ix-7'') одной или нескольких 4-6-членных моноциклических насыщенных гетероциклических групп, которые могут быть замещены группой R6 и содержат 1-2 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R6 представляет собой гидрокси, C1-C4 алкил или оксо; и
(ix-8'') одной или нескольких 4-10-членных моноциклических или дициклических ненасыщенных гетероциклических групп, которые могут быть замещены группой R7 и содержат 1-3 одинаковых или отличных друг от друга гетероатома, выбранных из азота, кислорода и серы, где R7 представляет собой галоген, циано, C1-C4 алкил, C1-C4 алкокси или амино;
где положение тройной связи C2-C6 алкинила находится между атомом углерода, связанным с 7H-пирроло[2,3-d]пиримидиновым скелетом, и атомом углерода, смежным с этим атомом углерода;
(x'') фенил, который может быть замещен одним или несколькими заместителями, выбранными из группы, состоящей из гидрокси и C1-C4 алкила, который может быть замещен гидроксилом; или
(xi'') 5-6-членную моноциклическую ненасыщенную гетероциклическую группу, содержащую 1 или 2 атома азота.
28. Соединение по п. 22, выбранное из группы, состоящей из следующих:
(1) 4-амино-7-(трет-бутил)-N-(4-(метоксиметил)фенил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид;
(2) 4-амино-7-(1-фтор-2-метилпропан-2-ил)-N-(4-(метоксиметил)фенил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид;
(3) 4-амино-N-(4-(метоксиметил)фенил)-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид;
(4) 4-амино-6-бром-N-[4-(метоксиметил)фенил]-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид;
(5) 4-амино-6-хлор-N-[4-(метоксиметил)фенил]-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид;
(6) 4-амино-N-(4-(метоксиметил)фенил)-7-(1-метилциклопропил)-6-винил-7H-пирроло[2,3-d]пиримидин-5-карбоксамид;
(7) 4-амино-6-фтор-N-(4-(метоксиметил)фенил)-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид;
(8) 4-амино-N-[4-(метоксиметил)фенил]-7-(1-метилциклопропил)-6-(3-морфолинопроп-1-ин-1-ил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид;
(9) 4-амино-6-(4-гидрокси-4-метилпент-1-ин-1-ил)-N-[4-(метоксиметил)фенил]-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид;
(10) 4-амино-N-[4-(метоксиметил)фенил]-7-(1-метилциклопропил)-6-((тетрагидро-2H-пиран-4-ил)этинил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид;
(11) 4-амино-N-[4-(метоксиметил)фенил]-7-(1-метилциклопропил)-6-(3-(пирролидин-1-ил)проп-1-ин-1-ил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид;
(12) (R)-4-амино-N-[4-(метоксиметил)фенил]-7-(1-метилциклопропил)-6-((тетрагидрофуран-2-ил)метокси)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид;
(13) 4-амино-N-[4-(метоксиметил)фенил]-6-((1-метил-1H-пиразол-4-ил)этинил)-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид;
(14) 4-амино-6-(имидазо[1,2-b]пиридазин-3-илэтинил)-N-[4-(метоксиметил)фенил]-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид;
(15) 4-амино-N-(4-(метоксиметил)фенил)-6-((1-метил-1H-пиразол-3-ил)этинил)-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид;
(16) 4-амино-N-(4-(метоксиметил)фенил)-6-((1-метил-1H-имидазол-5-ил)этинил)-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид;
(17) 4-амино-N-[4-(метоксиметил)фенил]-7-(1-метилциклопропил)-6-(пиридин-3-илэтинил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид;
(18) 4-амино-N-(4-(метоксиметил)фенил)-7-(1-метилциклопропил)-6-(проп-1-ин-1-ил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид;
(19) 4-амино-N-[4-(метоксиметил)фенил]-7-(1-метилциклопропил)-6-(3-(пиперидин-1-ил)проп-1-ин-1-ил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид;
(20) 4-амино-6-этокси-N-(4-(метоксиметил)фенил)-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид;
(21) 4-амино-6-((1-гидроксициклопентил)этинил)-N-(4-(метоксиметил)фенил)-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид;
(22) 4-амино-N-(4-(метоксиметил)фенил)-7-(1-метилциклопропил)-6-(3-тиоморфолинопроп-1-ин-1-ил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид;
(23) 4-амино-N-(4-(метоксиметил)фенил)-7-(1-метилциклопропил)-6-(3-(тетрагидро-2H-пиран-4-ил)проп-1-ин-1-ил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид;
(24) 4-амино-6-((6-аминопиридин-3-ил)этинил)-N-(4-(метоксиметил)фенил)-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид;
(25) 4-амино-6-((1,3-диметил-1H-пиразол-4-ил)этинил)-N-(4-(метоксиметил)фенил)-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид;
(26) 4-амино-N-(4-(метоксиметил)фенил)-7-(1-метилциклопропил)-6-((1-метилпиперидин-4-ил)этинил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид;
(27) 4-амино-6-(3-(диметиламино)проп-1-ин-1-ил)-N-(4-(метоксиметил)фенил)-7-(1-метилциклопропил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид;
(28) 4-амино-N-(3-фтор-4-(метоксиметил)фенил)-7-(1-метилциклопропил)-6-((тетрагидро-2H-пиран-4-ил)этинил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид; и
(29) 4-амино-N-(3-фтор-4-(метоксиметил)фенил)-7-(1-метилциклопропил)-6-(3-морфолинопроп-1-ин-1-ил)-7H-пирроло[2,3-d]пиримидин-5-карбоксамид; и
соли этих соединений.
29. Соединение или его кислотно-аддитивная соль по любому из пп. 22-28 в качестве селективного ингибитора RET.
30. Фармацевтическая композиция, обладающая свойствами селективного ингибитора RET, включающая в эффективном количестве соединение или его кислотно-аддитивную соль по любому из пп. 22-28.
31. Соединение или его кислотно-аддитивная соль по любому из пп. 22-28, обладающая свойствами селективного ингибитора RET, для получения противоопухолевого средства.
32. Способ профилактики или лечения злокачественной опухоли, связанной только с активностью RET, включающий введение млекопитающему соединения или его кислотно-аддитивной соли по любому из пп. 22-28.
33. Способ ингибирования RET, включающий введение млекопитающему соединения или его кислотно-аддитивной соли по любому из пп. 22-28.
34. Применение соединения или его кислотно-аддитивной соли по любому из пп. 22-28 в качестве селективного ингибитора RET.
35. Применение соединения или его кислотно-аддитивной соли по любому из пп. 22-28 для получения противоопухолевого средства, где опухоль, которую необходимо предотвратить или лечить, связана только с активностью RET.
36. Применение соединения или его кислотно-аддитивной соли по любому из пп. 22-28 для ингибирования RET.
37. Применение соединения или его кислотно-аддитивной соли по любому из пп. 22-28 для профилактики или лечения злокачественной опухоли, связанной только с активностью RET.
| WO 2007067781 A2, 14.06.2007 | |||
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| Способ защиты переносных электрических установок от опасностей, связанных с заземлением одной из фаз | 1924 |
|
SU2014A1 |
| ABELHAMID, ABDOU O | |||
| et al., Heterocyclic synthesis using hydrazonoyl halides: synthesis of annulated pyrimidines, pyridazines and pyrazoles | |||
| Journal of Chemical Research, Synopses (6),208-209, 1993 | |||
| McCLELLAN, W | |||
| J | |||
| et al., Discovery of potent and | |||
Авторы
Даты
2022-04-21—Публикация
2017-02-22—Подача