Предлагаемое изобретение относится к области органической химии, конкретно к способу получения 1,4,7(8,9)-тритиа-2,9(10,11)-диазациклоалкан 1,1-диоксидов общей формулы (1):

Циклические производные сульфамидов перспективны в качестве противомикробных и антиоксидантных агентов [J.R. Badgujar, D.Н. More, Jy. S. Меshram. Synthesis, Antimicrobial and Antioxidant Activity of Pyrazole Based Sulfonamide Derivatives. Indian J. Microbiol., 2018, Vol 58, Issue 1, pp. 93-99], препаратов для лечения язвы желудка [В.С.Ross, J.D. Michael, С.J. Cousins Thiatriazine derivatives. Pat. EP №0104611 A3, 1985], являются антагонистами рецептора 5HT-1A [A. Tait, A. Luppi, S. Franchini, E. Preziosi, C. Parenti, M. Buccioni, G. Marucci, A. Leonardi, E. Poggesi, L. Brasili.l,2,4-Benzothiadiazine derivatives as al and 5-HT1A receptor ligands. Bioorganic & Medicinal Chemistry Letters 2005, 15, pp. 1185-1188], а также в качестве лекарства для лечения астмы и хронической обструктивной болезни легких (ХОБЛ) [A. Tait, A. Luppi, A. Hatzelmann, P. Fossa, L. Mosti. Synthesis, biological evaluation and molecular modelling studies on benzothiadiazine derivatives as PDE4 selective inhibitors. Bioorganic & Medicinal Chemistry 2005, 13, pp. 1393-1402] и агентов с противоопухолевыми и цитотоксическими свойствами [D. Vullo, A. Innocenti, I. Ni-shimori, J. Pastorek, A. Scozzafava, S. Pastorekova, С.T. Supuran. Carbonic an-hydrase inhibitors. Inhibition of the transmembrane isozyme XII with sulfonamides-a new target for the design of antitumor and antiglaucoma drags. Bioorganic & Medicinal Chemistry Letters 2005, 15, pp. 963-969].
Известен способ [R.М. Bannister, R. Jones, Ch.W. Rees, D.J. Williams 1,3,5,2,4-Trithiadiazines; a New Ring System. J. CHEM. SOC, CHEM. COMMUN., 1987, pp. 1546-1548] получения 1,3λ4δ2,5,2,4-тритиадиазинов (2) с выходом 6-50% реакцией алкандисульфенилдихлоридов с 1,3-бис(триметилсилил)-2λ4-диазатиа-1,2-диеном при кипячении в дихлорметане.

Известный способ не позволяет получать 1,4,7(8,9)-тритиа-2,9(10,11)-диазациклоалкан 1,1-диоксиды общей формулы (1).
Известен способ [R.R. Khairullina, A.R. Geniyatova, Т.V. Tyumkina, D.S. Karamzina, A.G. Ibragimov, U.М. Dzhemilev Synthesis of a new class of hete-rocycles l,7-dithia-3,5-diazacycloalkan(e)-4-(thi)ones using Cs- and Rb-containing catalysts. Tetrahedron, 2017, Vol 73, Issue 50, pp. 7079-7084] получения 1,7-дитиа-3,5-диазациклоалкан-4-(ти)онов (3) взаимодействием (тио)мочевины с бис(N,N-диметиламино)метаном и α,ω-дитиолами в присутствии RbNO3 или CS2CO3 в качестве катализатора с выходами 65-80% соответственно.

Известным способом не могут быть получены 1,4,7(8,9)-тритиа-2,9(10,11)-диазациклоалкан 1,1-диоксиды общей формулы (1).
Известен способ [P. Du, Н. Zhou, Yu. Sui, Q. Liu, K. Zou. Asymmetric synthesis of 3,4-dihydro-2H-1,2,4-benzothiadiazine-1,1-dioxides catalyzed by scandium(III)-inda-Pybox. Tetrahedron, 2016, 24, pp. 1573-1578] получения 3,4-дигидро-2H-1,2,4-бензотиадиазин-1,1-диоксидов (4) конденсацией 2-аминобензолсульфамидов с альдегидами в присутствии солей скандия с выходами 35-81% соответственно.
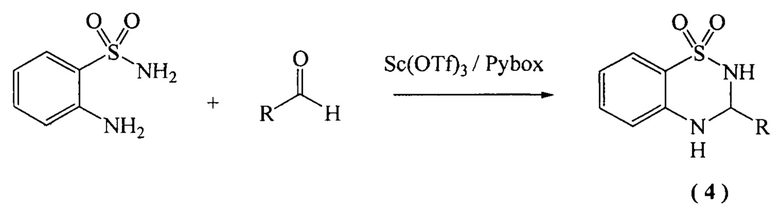
Известный способ не позволяет получать 1,4,7(8,9)-тритиа-2,9(10,11)-диазациклоалкан 1,1-диоксиды общей формулы (1).
Таким образом, в литературе отсутствуют сведения о 1,4,7(8,9)-тритиа-2,9(10,11)-диазациклоалкан 1,1-диоксидах общей формулы (1) и селективном их получении.
Предлагается новый способ селективного получения 1,4,7(8,9)-тритиа-2,9(10,11)-диазациклоалкан 1,1-диоксидов общей формулы (1).
Сущность способа заключается во взаимодействии сульфамида с формальдегидом (параформ) и α,ω-дитиолами, а именно 1,2-этан-, 1,3-пропан-, 1,4-бутандитиолами в присутствии в качестве катализатора Sm(NO3)3⋅6H2O, взятыми в мольном соотношении сульфамид: параформ: α,ω-дитиол: [кат]=10:(15-25):10:(1-3), предпочтительно 10:20:10:2, при температуре 60 - 80°С, предпочтительно 70°С, в течение 6.5 - 7.5 ч, предпочтительно 7 ч, в смеси растворителей хлороформ:этанол = 1:1. Выход 1,4,7(8,9)-тритиа-2,9(10,11)-диазациклоалкан 1,1-диоксидов общей формулы (1) составляет 31-70%. Реакция проходит по схеме:
Способ поясняется примерами:
Пример 1. В стеклянный реактор, снабженный магнитной мешалкой помещают сульфамид 0.096 г (1 ммоль), параформ 0.060 г (2 ммоль), EtOH (5 мл) и катализатор 0.088 г (0.2 ммоль) Sm(NO3)3⋅6H2O, 0.094 г (1 ммоль) 1,2-дитиола и CHCl3 (5 мл). Реакционную массу перемешивают 7 ч при температуре 70°С. Затем методом колоночной хроматографии на SiO2 выделяют 1,4,7,2,9-тритиадиазонан 1,1-диоксид общей формулы (1) с выходом 65%. Другие примеры, подтверждающие способ, приведены в таблице.

Спектральные характеристики 1,4,7(8,9)-тритиа-2,9(10,11)-диазациклоалкан 1,1-диоксидов общей формулы (1)
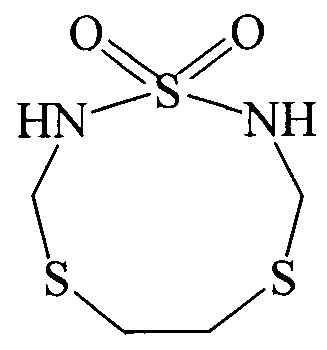
1,4,7-тритиа-2,9-диазонан 1,1-диоксид. Выход 65%, т.пл. 176-178°С. ИК-спектр (KBr), ν/cm-1: 3262 (N-H); 2923-2854 (СН); 1616, 1414 (NH); 1385 (СН); 1331 (S=O), 1300, 1206 (С-S); 1149 (S=O); 720 (C-S). Спектр ЯМР 1H, δ, м.д.: 2.83 с (4Н, CH2S); 4.10 уш.с (4Н, NCH2S); 7.66 т (2Н, NH, 3J=6.0 Гц). Спектр ЯМР 13С, δ, м.д.: 30.60 (CH2S); 44.81 (NCH2S). Масс-спектр MALDI TOF / TOF: m/z 212.828 [M-H]+. Масс-спектр (ХИАД), m/z (Iотн., %): 212.9 (100) [M-H]-.

1,4,8-тритиа-2,10-диазекан 1,1-диоксид. Выход 53%, вязкое, смолообразное вещество. ИК-спектр (KBr), ν/см-1: 3459 (N-H); 2923-2853 (СН); 1619, 1455 (NH); 1384 (СН); 1329 и 1150 (S=O); 1069 (C-N); 772 (C-S). Спектр ЯМР 1H, δ, м.д.: 1.83 м (2Н, CH2); 2.67 м (4Н, CH2S); 4.04 д (4Н, NCH2S, J=8.0 Гц); 7.61 т (2Н, NH, 3J=8.0 Гц). Спектр ЯМР 13С, δ, м.д.: 28.99 (CH2S); 29.52 (СН2); 44.76 (NCH2S). Масс-спектр, MALDI TOF / TOF: m/z 227.086 [M-H]+. Масс-спектр (ХИАД), m/z (Iотн., %): 270 [M+H+CH3CN]+, 150 [M-C4H8S2+H+CH3CN]+, 121 [M-CH4SO2+H+CH3CN]+.
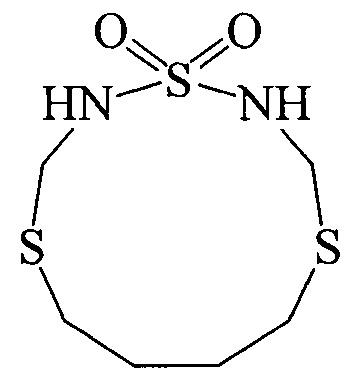
1,4,9-тритиа-2,11-диазациклоундекан 1,1-диоксид. Выход 39%, т.пл. 98-100°С.ИК-спектр (KBr), ν/cm-1: 3269 (N-H); 2924-2854 (СН); 1618, 1422 (NH); 1377 (СН); 1326 и 1147 (S=O); 1050 (C-N); 722 (C-S). Спектр ЯМР 1Н, δ, м.д.: 2.62 м (4Н, CH2); 2.61 м (4Н, CH2S); 4.03 уш.с (4Н, NCH2S); 7.59 уш.с (2Н, NH). Спектр ЯМР 13С, δ, м.д.: 28.36 (CH2S); 29.97 (СН2); 44.72 (NCH2S). Масс-спектр, MALDI TOF / TOF: m/z 241.148 [M-H]+.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения 1,6-бис-[алкил(арил)сульфониламино]-2,5-дитиагексана | 2023 |
|
RU2821791C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2- И 4-(1,5,3-ДИТИАЗОЦИНАН-3-ИЛ)ФЕНОЛОВ | 2011 |
|
RU2478627C2 |
| Способ получения 2-{ [({ 2-[({ [2-(аминокарбонил)фенил]амино} метил)тио]алкил} тио)-метил]амино} бензамидов | 2021 |
|
RU2779385C2 |
| СПОСОБ ПОЛУЧЕНИЯ 3-(о, м, n-ГАЛОГЕНФЕНИЛ)-3, 4-ДИГИДРО-2Н-БЕНЗО[f][1, 5, 3]ДИТИАЗЕПИНОВ | 2016 |
|
RU2632661C2 |
| СПОСОБ ПОЛУЧЕНИЯ 4-(о, м, п-ГАЛОГЕНФЕНИЛ)-2, 6-ДИТИА-4-АЗАБИЦИКЛО[5.3.1]УНДЕКА-1(11),7,9-ТРИЕНОВ | 2016 |
|
RU2626006C1 |
| СПОСОБ ПОЛУЧЕНИЯ 3-АРИЛ-1,5,3-ДИТИАЗОЦИНАНОВ | 2012 |
|
RU2538603C2 |
| СПОСОБ ПОЛУЧЕНИЯ 7,16,25-ТРИАРИЛ-7,8,16,17,25,26-ГЕКСАГИДРО-6Н,15Н,24Н-ТРИБЕНЗО[f,m,t][1,5,8,12,15,19]ГЕКСАОКСА[3,10,17]ТРИАЗАЦИКЛОХЕНИКОЗИНОВ | 2016 |
|
RU2632666C1 |
| СПОСОБ ПОЛУЧЕНИЯ N-(1,5,3-ДИТИАЗОЦИНАН-3-ИЛ)АМИДОВ | 2012 |
|
RU2496777C2 |
| СПОСОБ ПОЛУЧЕНИЯ 6-ГАЛОГЕНФЕНИЛ-2,4,8-ТРИТИА-6-АЗА-1,3(1,4)-ДИБЕНЗОЦИКЛООКТАФАНОВ | 2015 |
|
RU2605430C1 |
| СПОСОБ ПОЛУЧЕНИЯ 6-АРИЛ-2,4,8-ТРИТИА-6-АЗА-1,3(1,4)-ДИБЕНЗОЦИКЛООКТАФАНОВ | 2015 |
|
RU2605429C1 |
Изобретение относится к способу получения 1,4,7(8,9)-тритиа-2,9(10,11)-диазациклоалкан 1,1-диоксидов общей формулы (1), заключающемуся в том, что сульфамид подвергается взаимодействию с параформом и α,ω-дитиолами, выбранными из ряда 1,2-этан-, или 1,3-пропан-, или 1,4-бутандитиол, в присутствии в качестве катализатора Sm(NO3)3⋅6H2O, взятыми в мольном соотношении сульфамид:параформ:α,ω-дитиол:[Sm(NO3)3⋅6H2O]=10:(15-25):10:(1-3), при температуре 60-80°С в течение 6.5-7.5 ч в смеси растворителей хлороформ:этанол=1:1. Способ позволяет поучать соединения формулы (1) с выходом 31-70%. Технический результат: получение 1,4,7(8,9)-тритиа-2,9(10,11)-диазациклоалкан 1,1-диоксидов общей формулы (1). 1 табл., 1 пр.
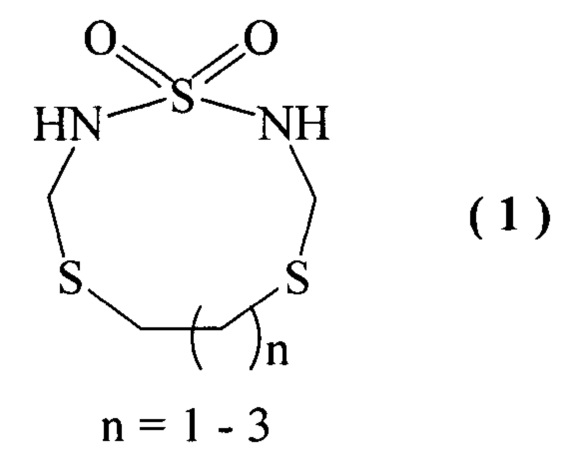
Способ получения 1,4,7(8,9)-тритиа-2,9(10,11)-диазациклоалкан 1,1-диоксидов общей формулы (1):
 ,
,
отличающийся тем, что сульфамид подвергается взаимодействию с параформом и α,ω-дитиолами, выбранными из ряда 1,2-этан-, или 1,3-пропан-, или 1,4-бутандитиол, в присутствии в качестве катализатора Sm(NO3)3⋅6H2O, взятыми в мольном соотношении сульфамид:параформ:α,ω-дитиол:[Sm(NO3)3⋅6H2O]=10:(15-25):10:(1-3), при температуре 60-80°С в течение 6.5-7.5 ч в смеси растворителей хлороформ:этанол=1:1.
| Г | |||
| Р | |||
| Хабибуллина и др | |||
| "Эффективный синтез N-(карбоксиалкил)замещенных дитиаза- и диоксадитиазациклоалканов циклоконденсацией аминокислот с формальдегидом и α,ω-дитиолами" Журнал органической химии, т | |||
| Веникодробильный станок | 1921 |
|
SU53A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| H | |||
| W | |||
| Roesky et al | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
2022-06-01—Публикация
2020-10-26—Подача