Изобретение относится к медицине, а именно к челюстно-лицевой хирургии и стоматологии. Изобретение направлено на лечение и профилактику развития рецидивов доброкачественных эпителиальных кистозных образований челюстей, а именно: одонтогенной кератокисты, фолликулярной кисты и доброкачественной одонтогенной опухоли эпителиального происхождения (амелобластома) [A61B17/24, A61L31/00].
На сегодняшний день в мировой клинической практике при хирургическом лечении вышеупомянутых кистозных образований используются несколько вариантов состава раствора Карнуа, то есть различные его модификации. Раствор Карнуа впервые использовался в качестве лекарственного средства в работах Катлера и Золлингера еще в 1933 г. Это мощный фиксирующий, гемостатический и прижигающий раствор. В растворе Карнуа большинство авторов не используют хлороформ, так как он активирует злокачественную трансформацию клеток и вызывает бесплодие. Кроме того, хлороформ официально запрещен FDA (Food and Drug Administration – Управление по санитарному надзору за качеством пищевых продуктов и медикаментов) на территории США. На территории Российской Федерации ни один из вышеперечисленных составов не применялся и не применяется на сегодняшний день.
По данным мировой литературы применяются следующие модификации раствора Карнуа:
СОСТАВ №1 (рекомендован Катлером и Золлингером в 1933 г.). Состав раствора: хлорид железа – 1 грамм; хлороформ – 3 мл; ледяная уксусная кислота – 1 мл; этиловый спирт 96% – 6 мл [Cutler E.C., Zollinger R. The use of sclerosing solutions in the treatment of cysts and fistulae // Am.J. Surg. 1933. Vol. 19. N 3. P. 411–418].
СОСТАВ №2. Состав раствора: этиловый спирт 96% – 3 мл; ледяная уксусная кислота – 1 мл [Madhulaxmi M., Abdul Wahab P.U. Carnoy`s solution as a surgical medicament in the treatment of KCOT // Int. J. Pharma Bio Sci. 2014. Vol. 5. N 1. P. 492–495].
СОСТАВ №3. Состав раствора: хлороформ – 3 мл; ледяная уксусная кислота – 1 мл; этиловый спирт 96% – 6 мл [Ecker J., ter Horst R., Koslovsky D. Current role of Carnoy’s solution in treating keratocystic odontogenic tumors // J. Oral Maxillofac. Surg. 2016. Vol 74. N 2. P. 278–282.].
Недостатками аналогов являются:
- для состава №1: наличие в составе хлороформа, который активирует злокачественную трансформацию клеток и вызывает бесплодие. Из-за этого хлороформ официально запрещен FDA (Food and Drug Administration) Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов на территории США;
- для составов №№1-3: с увеличением времени воздействия растворов на сосудистую стенку артерий и вен, повышается вероятность развития васкулопатий, пристеночных тромбов и фиброза [Saulacic N., Stajcic Z., Stajcic L.S., Piattelli A., Iizuka T., Lombardi T. Effects of Carnoy’s solution on blood vessels of the axillary fossa of rats // Int. J. Oral Maxillofac. Surg. 2009. Vol. 38. N 8. P. 876–879.]. Таким образом, после проведения удаления кистозного образования время нахождения раствора Карнуа в костной полости не должно превышать 5 мин;
- для составов №№1-3: с увеличением времени экспозиции (более 3 мин) растворов, происходят необратимые изменения в нервной ткани [Frerich B., Cornelius C.P., Wiethölter H. Critical time of exposure of the rabbit inferior alveolar nerve to Carnoy’s solution // J. Oral Maxillofac. Surg. 1994. Vol. 52. N 6. P. 599–606.] В связи с этим безопасное использование раствора Карнуа, прилежащего к нервным стволам не должно превышать 2–3 мин.
Наиболее близким по технической сущности (а также требованиям безопасности и эффективности) является СОСТАВ №4. Состав раствора: хлорид железа – 1 грамм; ледяная уксусная кислота – 1 мл; этиловый спирт 96% – 6 мл [Madhulaxmi M., Abdul Wahab P.U. Carnoy`s solution as a surgical medicament in the treatment of KCOT // Int. J. Pharma Bio Sci. 2014. Vol. 5. N 1. P. 492–495].
Для состава №4 характерны второй и третий приведенные выше недостатки аналогов, а именно вероятность развития васкулопатий, пристеночных тромбов и фиброза и необратимые изменения в нервной ткани с увеличением времени экспозиции раствора.
Основной технической проблемой прототипа является высокая вероятность возникновения рецидивов кистозного образования из-за низкой эффективности удаления остатков оболочек доброкачественных кистозных образований челюстей [В.В. Лебедев, С.Б. Буцан. Использование раствора Карнуа и его модификаций для уменьшения количества рецидивов после хирургического удаления кератокистозных одонтогенных опухолей и амелобластом: систематический обзор // Вестн. Моск. ун-та. сер. 16. Биология. 2019. Т. 74. № 2. С. 135–145].
Задачей изобретения является устранение недостатков прототипа.
Техническим результатом изобретения является уменьшение вероятности рецидивов кистозного образования.
Указанный технический результат достигается за счет того, что раствор для обработки костных полостей при кистозных образованиях в челюстно-лицевой области, включающий этиловый спирт с концентрацией 95% и уксусную кислоту с концентрацией 75% при объемном соотношении указанных компонент 2:1.
Краткое описание чертежей
На фиг. 1, 2 показана зависимость от времени экспозиции специального раствора в тканях одонтогенной кератокисты в флуоресцентном микроскопе (разрешение х20).
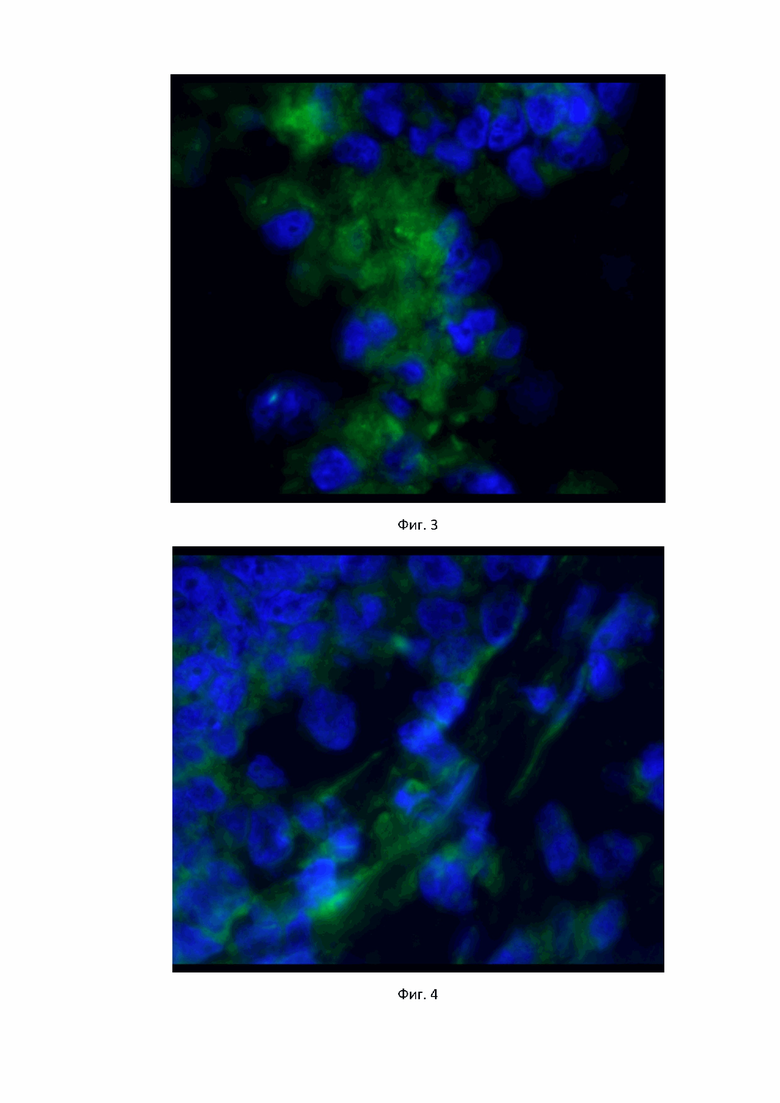
На фиг. 3, 4 показана зависимость от времени экспозиции специального раствора в тканях доброкачественной одонтогенной опухоли эпителиального происхождения в флуоресцентном микроскопе (разрешение х40).
На фиг. 5-9 показаны иллюстрации использования раствора для обработки костных полостей при кистозных образованиях в челюстно-лицевой области для клинического примера 1.
На фиг. 10-14 показаны иллюстрации использования раствора для обработки костных полостей при кистозных образованиях в челюстно-лицевой области для клинического примера 2.
Осуществление изобретения.
Раствор для обработки костных полостей при кистозных образованиях в челюстно-лицевой области состоит из следующих прекурсоров:
1) этилового спирта 95% (этанол) C2H5OH (регистрационный номер № 74/614/12, справочник лекарственных средств Видаль);
2) уксусной кислоты 75% (эссенция) CH3COOH (регистрационный номер ФС-001785 от 19.07.2018 г., ООО НПК "ФармХимКомплект" / Россия),
при объемном соотношении ингредиент 2:1.
При смешивании этилового спирта и уксусной кислотой (в обычных условиях без добавления реактива) образуется этиловый спирт уксусной кислоты (этилацетат):
CH3COOH + CH3CH2OH=CH3COOC2H5 + H2O
Этилацетат применяется как в медицине, так и в пищевой промышленности. Зарегистрирован в качестве пищевой добавки E1504 (ароматизатор).
Раствор для обработки костных полостей при кистозных образованиях в челюстно-лицевой области является бесцветной прозрачной жидкостью без посторонних включений и осадка. На вкус раствор кислый, имеет запах характерный для уксусной кислоты. При встряхивании не образует на поверхности пену. Активность раствора не снижается при хранении в обычных условиях.
Основной эффект и действие раствора для обработки костных полостей при кистозных образованиях в челюстно-лицевой области направлен на фиксацию и разрушение клеточной мембраны. Объектами воздействия являются клетки кистозных образований челюстей (доброкачественной одонтогенной опухоли эпителиального происхождения, одонтогенной кератокисты и фолликулярной кисты), состоящие из клеточной стенки, цитоплазмы и ядерного аппарата. Преобладающим механизмом воздействия является нарушение целостности клеточной стенки и ядерного аппарата, приводящее к нарушению деления клетки с повреждением цепочечной структуры молекулы ДНК.
Заявленный технический результат – уменьшение вероятности рецидивов кистозного образования подтверждается проведенными клиническими исследованиями, которые показали, что использование раствора для обработки костных полостей при кистозных образованиях в челюстно-лицевой области позволяет более эффективно удалять остатки оболочек доброкачественной одонтогенной опухоли эпителиального происхождения, одонтогенной кератокисты и фолликулярной кисты). Также проведенные клинические исследования показали, что заявленный раствор:
- не обладает побочными эффектами;
- безопасен при воздействии на окружающие ткани и сосудисто-нервные пучки (при времени экспозиции не более 3 мин), проходящие в проекции кистозного образования;
- при использовании отсутствует эффект остеомаляции и остеонекроза челюстей.
Для подтверждения заявленного технического результата (для оценки жизнедеятельности клеток кистозных образований челюстей) использовался специальный краситель 4,6-диамидино-2-фенилиндол (DAPI).
DAPI – это синий флуоресцентный краситель для окрашивания нуклеиновых кислот. Он связывается с двуцепочечной молекулой ДНК, взаимодействуя с кластерами в малой бороздке молекулы. В комплексе с ДНК флуоресценция DAPI в 20 раз сильнее. Спектральные свойства DAPI делают его удобным для определения жизнеспособности на проточном цитометре и флуоресцентном микроскопе, оборудованном ультрафиолетовым или фиолетовым лазером. Длина волны возбуждения красителя составляет 358 нм, длина волны максимума излучения - 461 нм. Плазматическая мембрана практически непроницаема для DAPI, поэтому он чрезвычайно плохо окрашивает живые клетки. Если же мембрана повреждена, краситель проникает в клетку и связывается с ДНК. В рекомендуемых условиях флуоресценция окрашенных мертвых клеток возбуждается фиолетовым лазером и детектируется в диапазоне длин волн 425-475 нм. Апоптотические, некротические и/или поврежденные клетки – источник помех при анализе жизнеспособности методом проточной цитометрии. DAPI позволяет окрасить нежизнеспособные клетки, оценить их количество и исключить соответствующие данные, в то время как живые клетки останутся неокрашенными (негативными).
В качестве эксперимента проведен ряд патогистологических исследований о влиянии раствора для обработки костных полостей при кистозных образованиях в челюстно-лицевой области на клеточную стенку кистозных образований челюстно-лицевой области. После удаления образования ее оболочка была фрагментирована на несколько частей. Одни фрагменты целиком помещены в специальный раствор на 3 сек, другие фрагментированные части на 3 мин. Для определения уровня проникновения раствора и визуализации живых и/или поврежденных клеток в тканях образования, взятые фрагменты помещены в среду с физиологическим раствором NaCl 0,9%. Оценивая проникновение раствора в различных тканях были взяты за основу фрагменты одонтогенной кератокисты и доброкачественной одонтогенной опухоли эпителиального происхождения.
На фиг. 1, 2 показана зависимость от времени экспозиции специального раствора в тканях одонтогенной кератокисты в флуоресцентном микроскопе (разрешение х20). На фиг. 1 время экспозиции раствора на ткани составляет 3 сек; на фиг. 2 время экспозиции раствора на ткани составляет 3 мин. При этом, клетки, окрашенные синим цветом (красителем DAPI) имеют поврежденную клеточную стенку и соответственно ядерный аппарат.
На фиг. 3, 4 показана зависимость от времени экспозиции специального раствора в тканях доброкачественной одонтогенной опухоли эпителиального происхождения в флуоресцентном микроскопе (разрешение х40). На фиг. 3 время экспозиции раствора на ткани составляет 3 сек; на фиг. 4 время экспозиции раствора на ткани составляет 3 мин. При этом, клетки, окрашенные синим цветом (красителем DAPI) имеют поврежденную клеточную стенку и соответственно ядерный аппарат
Из фиг. 1-4, видно, что при проведении патогистологического исследования с помощью флуоресцентного микроскопа и окраски тканей специальным красителем DAPI получаются результаты, которые показывают разницу времени экспозиции специального раствора на клетку каждого из кистозных образований. Обращает на себя внимание то, что при удерживании раствора в тканях в течение 3 мин происходит повреждение всех клеточных структур образования. Применение специального раствора в пределах костной полости после удаления оболочки гарантирует наиболее полное удаление оставшихся фрагментов кистозного образования и, таким образом, предупреждается рецидив основного заболевания в отдаленном послеоперационном периоде.
Клинические исследования
С 2018 по 2021 гг. проведено хирургическое лечение с использованием раствора для обработки костных полостей при кистозных образованиях в челюстно-лицевой области у 52 пациентов, возрастом от 20 до 60 лет с доброкачественной одонтогенной опухолью эпителиального происхождения (амелобластома), одонтогенной кератокистой и фолликулярной кистой. После проведенного оперативного вмешательства через 6, 12 и 36 месяцев проводилась контрольная компьютерная томография черепа для верификации, возможного, появления рецидива основного заболевания. Для оценки отдаленного рецидива кистозных образований челюстей проведение компьютерной томографии черепа проводится 1 раз в год. Результаты лечения представлены в таблице 1.
Таблица 1
Доброкачественная одонтогенная опухоль эпителиального происхождения и одонтогенная кератокиста – это доброкачественные, но тем не менее агрессивные образования челюстно-лицевой области, имеющие высокий процент рецидивов (доходящие до 60–80%). Хирургическое лечение вышеописанных образований может выполняться с помощью различных методик: 1) марсупиализации (частота рецидивов до 24,8%); 2) энуклеации с дополнительной терапией или без нее; терапия может включать в себя криотерапию жидким азотом (частота рецидивов до 23,1%), периферическую остэктомию (частота рецидивов до 20%), обработку костной полости специальным раствором (частота рецидивов от 0 до 6,6%); 3) краевой/сегментарной резекции челюсти (частота рецидивов от 0 до 2,5%). Несмотря на низкую частоту рецидивов при использовании краевой/сегментарной резекции челюстей, этот метод требует более длительного и дорогого анестезиологического и хирургического вмешательства, а также более продолжительного послеоперационного и реабилитационного периодов. Также необходимо отметить, что использование специального раствора необходимо применять исключительно в тех случаях, когда сохранена непрерывность верхней/нижней челюсти. При объемных поражениях кистозным образованием челюстей, выходящие за пределы костной полости и нарушением непрерывности рекомендовано использование больших реконструктивных операций с резекцией челюсти и одномоментным замещением образовавшегося дефекта костным аутотрансплантатом или силовой титановой реконструктивной пластиной.
Анализ клинических и морфологических исследований, приведенных в таблице 1, показывает отсутствие рецидивов кистозного образования и осложнений после использования раствора для обработки костных полостей при кистозных образованиях в челюстно-лицевой области.
Таким образом, проведенные клинические исследования подтверждают заявленный технический результат уменьшение вероятности рецидивов кистозного образования, по сравнению с аналогами и прототипом, а также другими известными способами лечения.
Рекомендации по применению раствора для обработки костных полостей при кистозных образованиях в челюстно-лицевой области.
Использование вышеописанного раствора необходимо применять исключительно в тех случаях, когда сохранена непрерывность верхней/нижней челюсти. При объемных поражениях кистозным образованием челюстей, выходящие за пределы костной полости и нарушением непрерывности рекомендовано использование резекции челюсти с одномоментным замещением образовавшегося дефекта костным аутотрансплантатом или силовой титановой реконструктивной пластиной.
Недостатком раствора для обработки костных полостей при кистозных образованиях в челюстно-лицевой области является раздражающее действие на интактную слизистую оболочку полости рта и продолжительном времени экспозиции (более 5 мин), что приводит к нарушению клеточной стенки сосудисто-нервных пучков, находящиеся в пределах костной полости. При попадании раствора на слизистую оболочку рекомендуется смыть раствор физиологическим раствором NaCl 0,9% комнатной температуры. При воздействии раствора на сосудисто-нервный пучок, проходящий в костной полости после удаления кистозного образования, время экспозиции не должно превышать более 3 мин.
Клинические примеры использования раствора для обработки костных полостей при кистозных образованиях в челюстно-лицевой области.
Клинический пример №1
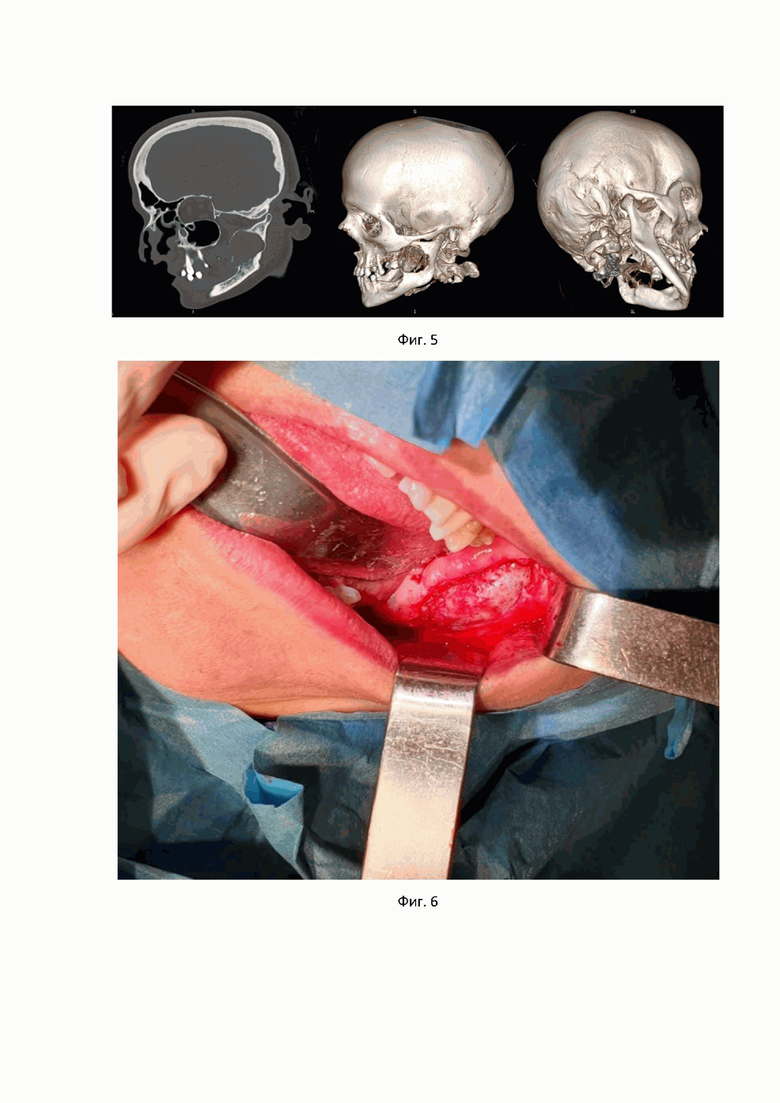
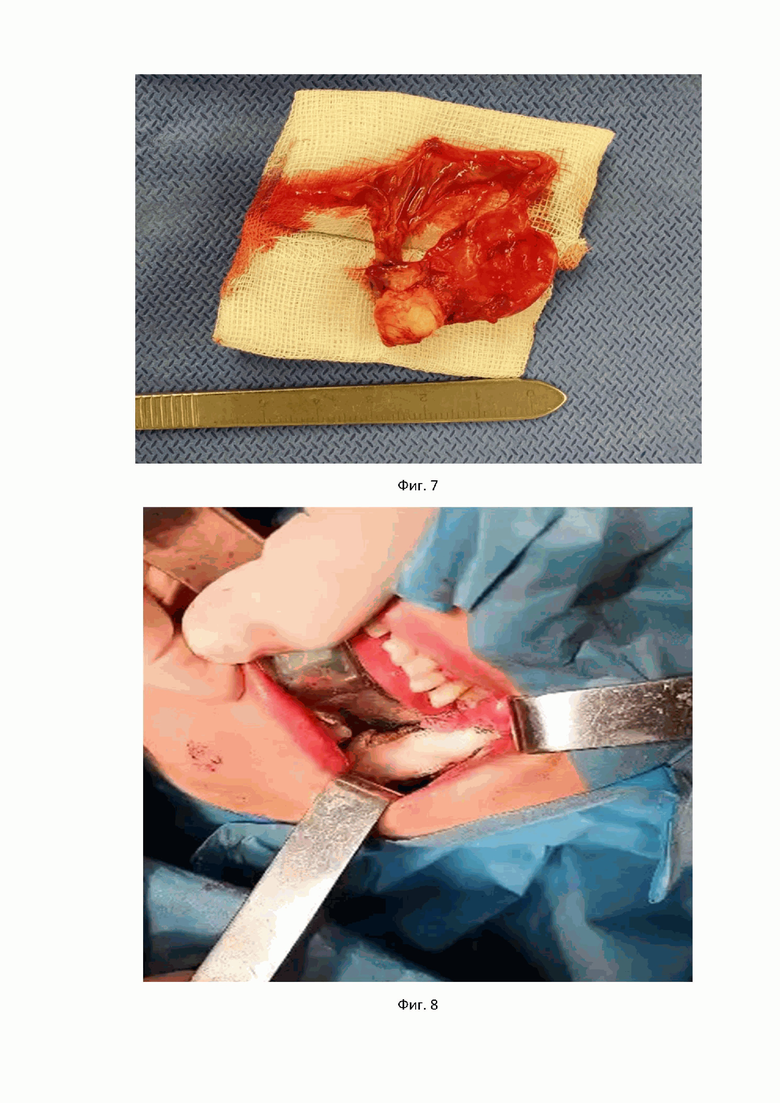
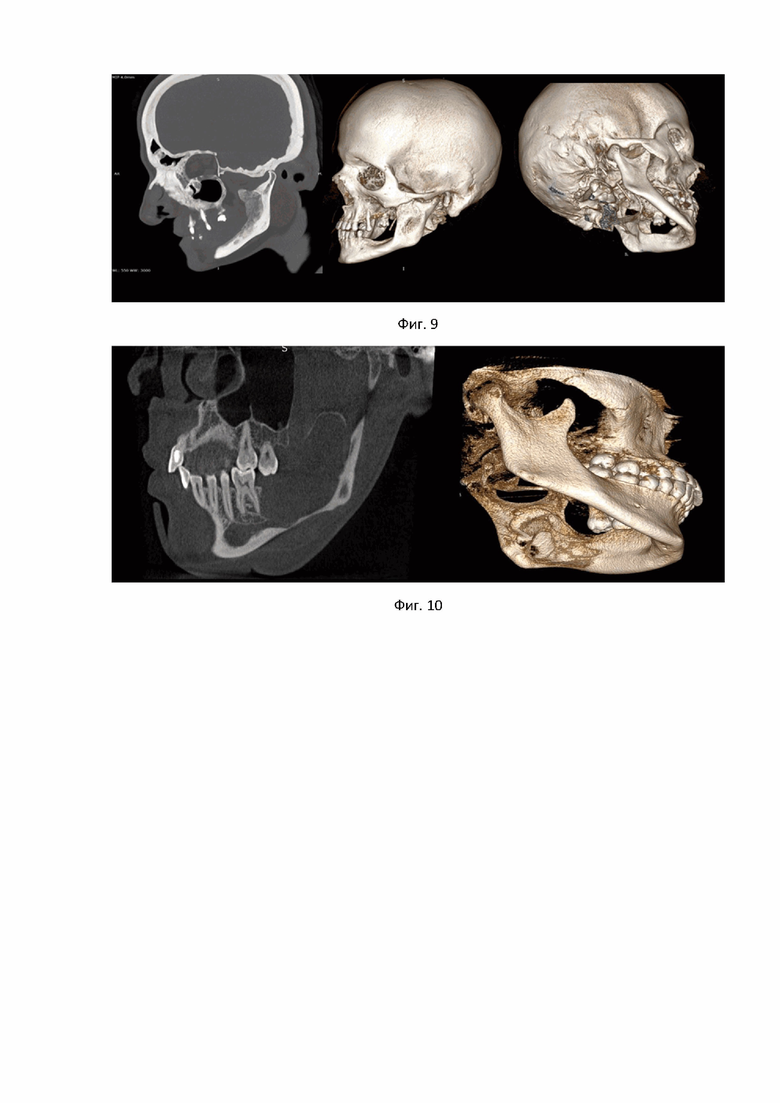
Пациентка У., обратилась клинику с жалобами на повторный рост новообразования в области нижней челюсти слева. Трижды пациентка оперирована в другой клинике по поводу десмоплатического варианта амелобластомы в области ветви нижней челюсти слева. В связи с рецидивом этого заболевания пациентка обратилась за лечением в нашу клинику. В нашей клинике была проведена мультиспиральная компьютерная томография (МСКТ) черепа (показано на фиг. 5.), по результатам которой в области ветви нижней челюсти слева визуализируется объемное полостное новообразование, размерами 38х29 мм с вовлечением в процесс венечного отростка. Далее был проведен классический внутриротовой доступ к амелобластоме в проекции ветви нижней челюсти слева. Была визуализирована оболочка опухоли, размерами 35х30 мм, которая в последующем выделена и удалена на всем протяжении. Образовавшаяся костная полость была обработана раствором для обработки костных полостей при кистозных образованиях в челюстно-лицевой области (время экспозиции в ране составило 3 мин) и активно промыта физиологическим раствором; проведен дополнительный кюретаж оставшихся фрагментов опухоли (показано на фиг. 6-8). Через 2 года после проведенного хирургического лечения у пациентки полностью восстановлена структура костной ткани. Отсутствие признаков рецидива десмопластического варианта амелобластомы подтверждается проведенной компьютерной томографией черепа (показано на фиг. 9).
Клинический пример №2
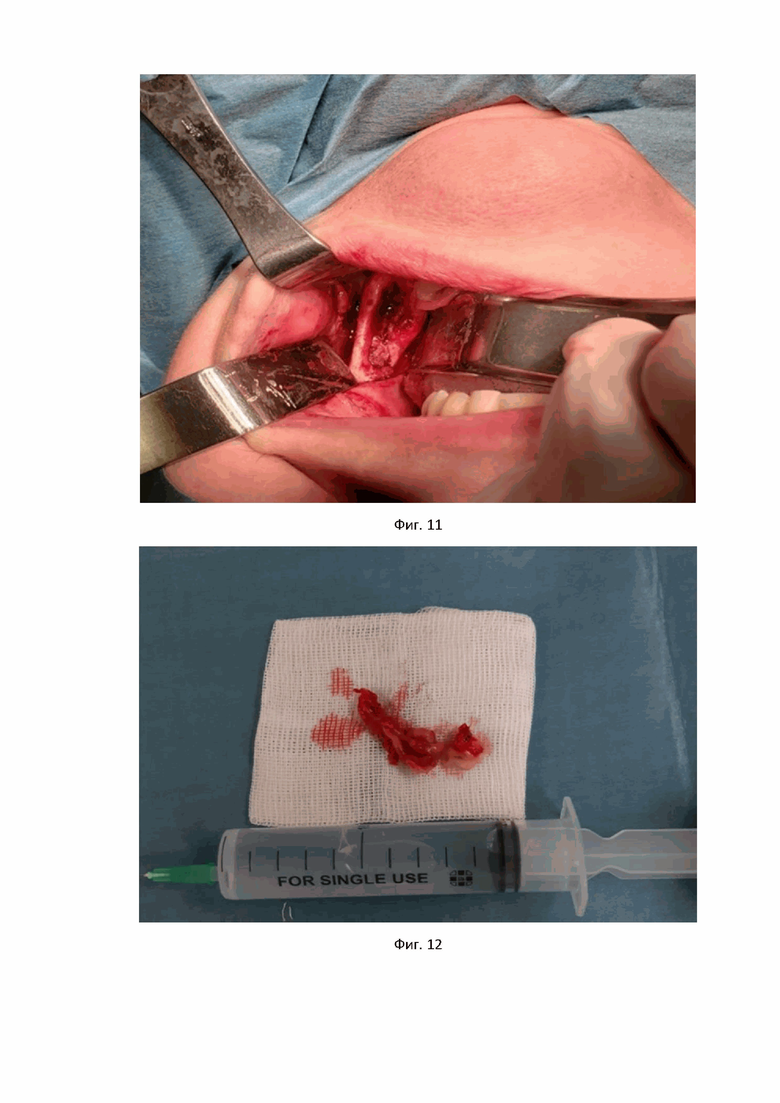
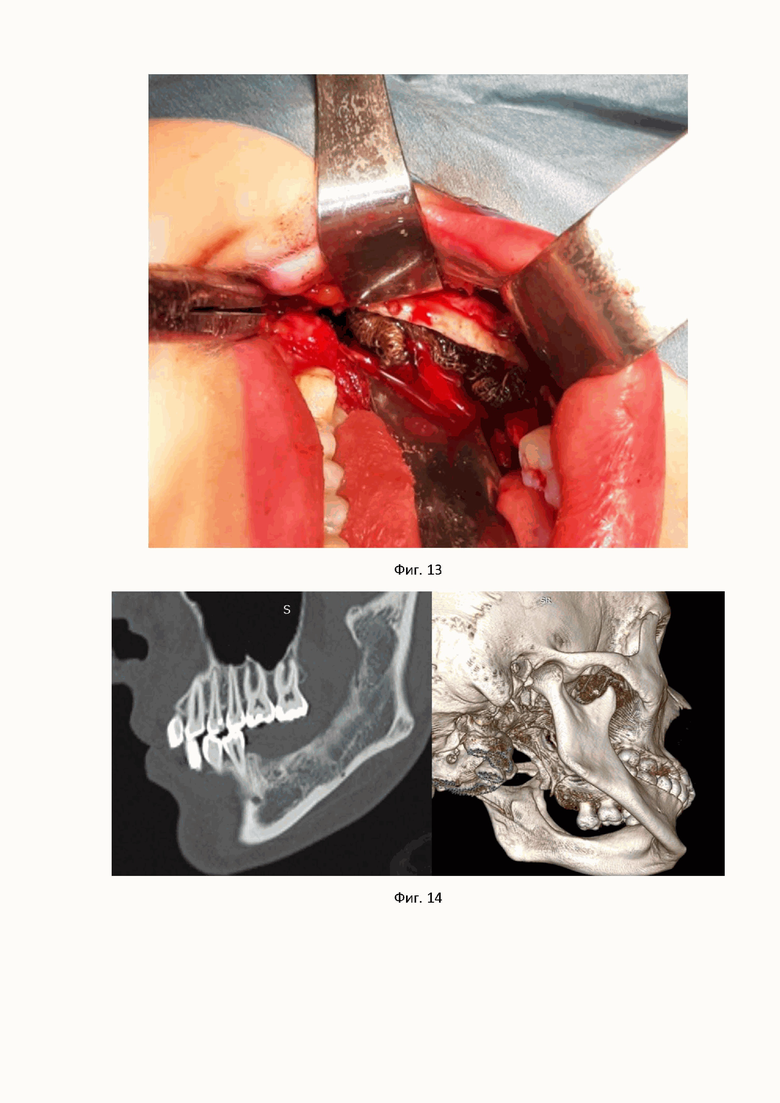
Пациентка О., обратилась с жалобами на периодически возникающие боли и отек в области нижней челюсти слева. Проведена компьютерная томография, по результатам которой было выявлено, что в области тела и ветви нижней челюсти слева имеется однокамерное образование, размерами 45х25 мм с деструкцией язычной кортикальной пластинки (показано на фиг. 10). До обращения в нашу клинику, пациентке неоднократно проводили кюретаж в проекции отсутствующих зубов 3.7 и 3.8 с кратковременным уменьшением болевого синдрома и отека в данной области. Патогистологических исследований не проводилось. Также стоит отметить истончение нижнего края нижней челюсти до 2 мм в проекции выявленного образования. Был проведен внутриротовой доступ к предполагаемому кистозному образованию в проекции тела и ветви нижней челюсти слева. Далее оболочка образования, размерами 35×20 была полностью выделена на всем протяжении и удалена. Образовавшаяся костная полость обработана раствором для обработки костных полостей при кистозных образованиях в челюстно-лицевой области (время экспозиции в ране составило 3 мин). Полость была активно промыта физиологическим раствором. Проведен дополнительный кюретаж оставшихся фрагментов оболочки образования (показано на фиг. 11-13). По данным патогистологического исследования был подтверждён диагноз: одонтогенная кератокиста. Через 1 год и 6 месяцев после проведенного хирургического лечения была восстановлена структура и архитектоника костной ткани. Отсутствие признаков рецидива кистозного образования подтверждается проведенной компьютерной томографией черепа (показано на фиг. 14).
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ устранения дефекта нижней челюсти и мягких тканей после хирургического лечения опухолей | 2021 |
|
RU2776041C1 |
| СПОСОБ ЦИСТОТОМИИ ЧЕЛЮСТНОЙ КИСТЫ | 2010 |
|
RU2442544C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ АМЕЛОБЛАСТОМЫ НИЖНЕЙ ЧЕЛЮСТИ | 2001 |
|
RU2222053C2 |
| Способ хирургического лечения кистозных образований нижней челюсти больших размеров | 2015 |
|
RU2610332C1 |
| Хирургический способ лечения одонтогенных кист нижней челюсти | 2021 |
|
RU2768472C1 |
| СПОСОБ ЛЕЧЕНИЯ КИСТ ЧЕЛЮСТЕЙ | 2014 |
|
RU2578161C2 |
| Способ лечения хронического одонтогенного верхнечелюстного синусита, осложненного наличием ороантрального сообщения | 2017 |
|
RU2649515C1 |
| Способ одномоментного устранения дефектов тела и ветви нижней челюсти | 2018 |
|
RU2689195C1 |
| Хирургический способ лечения одонтогенных кист верхней челюсти | 2022 |
|
RU2790935C1 |
| Способ одномоментной дентальной имплантации | 2023 |
|
RU2820001C1 |

Изобретение относится к медицине, а именно к челюстно-лицевой хирургии и стоматологии. Раствор для обработки костных полостей при кистозных образованиях в челюстно-лицевой области включает этиловый спирт с концентрацией 95% и уксусную кислоту с концентрацией 75% при объёмном соотношении указанных компонент 2:1. Изобретение обеспечивает уменьшение частоты рецидивов кистозного образования. 14 ил., 1 табл., 2 пр.
Раствор для обработки костных полостей при кистозных образованиях в челюстно-лицевой области, включающий этиловый спирт с концентрацией 95% и уксусную кислоту с концентрацией 75% при объёмном соотношении указанных компонент 2:1.
| ЛЕБЕДЕВ В.В., БУЦАН С.Б | |||
| Использование раствора Карнуа и его модификаций для уменьшения количества рецидивов после хирургического удаления кератокистозных одонтогенных опухолей и амелобластом: систематический обзор // Вестн | |||
| Моск | |||
| ун-та | |||
| сер | |||
| Устройство для электрической сигнализации | 1918 |
|
SU16A1 |
| Биология, Т | |||
| Приспособление в центрифугах для регулирования количества жидкости или газа, оставляемых в обрабатываемом в формах материале, в особенности при пробеливании рафинада | 0 |
|
SU74A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Способ обделки поверхностей приборов отопления с целью увеличения теплоотдачи | 1919 |
|
SU135A1 |
| Ручной прибор для загибания кромок листового металла | 1921 |
|
SU175A1 |
| SU 1608870 A1, 15.11.1994 | |||
| MADHULAXMI | |||
Авторы
Даты
2022-06-06—Публикация
2021-09-10—Подача