Изобретение относится к области медицины, фармакологии и химико-фармацевтической промышленности, а именно к новым соединениям общей формулы (I), нетоксичным терапевтически активным веществам для применения в терапии инфекционных и воспалительных заболеваний.
Многие вирусы поражают дыхательные пути, носовые ходы, горло, бронхи, легкие, в связи с чем такие вирусные инфекции собраны в группу острых респираторных вирусных инфекций (ОРВИ), поскольку обладают также и общностью клинических симптомов. Вирусы гриппа также относятся к группе ОРВИ, однако выделены в отдельную группу в связи с тем, что воздействуют системно на весь организм. Причиной ОРВИ могут быть более 200 различных вирусов, представителей 4 семейств РНК-содержащих вирусов (ортомиксовирусы, парамиксовирусы, коронавирусы и пикорнавирусы) и 2 семейств ДНК-содержащих вирусов (аденовирусы и герпесвирусы) [1, 2]. По частоте инфицирования грипп составляет около 15% (тип А - 12%, В - 3%), парагрипп и риновирусы - до 50%, аденовирус - до 5%, респираторно-синцитиальный вирус (РС) - 4%, микоплазма - около 2%, энтеровирусы - около 1%, смешанные инфекции - около 23% случаев. К группе высокого риска относятся дети, у которых заболевания респираторного тракта составляют до 90% всей инфекционной патологии и 65% от всех регистрируемых заболеваний [1, 3].
Для всех ОРВИ характерны симптомы общей интоксикации (головная боль, слабость, мышечные боли, потеря аппетита), повышенная температура, катаральные явления (заложенность носа, насморк, кашель, боль в горле). Локализация очага поражения во многом зависит от вида возбудителя. Так, риновирусные заболевания характеризуются преобладанием ринита, аденовирусные инфекции - ринофарингита, для парагриппа характерен фарингит, а для гриппа - трахеит, респираторно-синцитиальный вирус поражает бронхи. Возможны и другие симптомы, например, аденовирусы могут вызывать конъюнктивиты и кератиты. Обычно симптомы ОРВИ сохраняются в течение 3-7 дней (кашель может наблюдаться более длительное время), возможная длительность гриппа 1-2 недели. Среди осложнений выделяют ларингит, тонзиллит, фарингит и трахеит бактериальной природы, различные формы синуситов (гайморит, этмоидит, фронтит), а также отит, евстахиит, возможно развитие бронхита и пневмонии. Основные причины осложнений - нарушения иммунной защиты, приводящие к длительно протекающим иммунодефицитам, сочетающимся с резким снижением антибактериальной резистентности организма. При правильно выбранной тактике лечения ОРВИ риск развития осложнений заметно снижается [1-5].
Несмотря на успехи, достигнутые в медицине за последние десятилетия, в частности в лечении инфекционных заболеваний, ОРВИ и вирусы гриппа продолжают оставаться серьезной проблемой здравоохранения для большинства стран мира из-за чрезвычайно высокого уровня заболеваемости, обычно носящего характер сезонных эпидемий. ОРВИ и грипп занимают лидирующие положения по обращаемости за врачебной помощью детского и взрослого населения, временной утрате трудоспособности, количеству потребляемых лекарств за период болезни. В наибольшей степени сезонной заболеваемости подвержены дети, пожилые люди, лица с сопутствующими заболеваниями (различные иммунодефицитные состояния, заболевания легких, сердечно-сосудистой системы, печени, почек, сахарный диабет и пр.).
Самым эффективным способом контроля за сезонной заболеваемостью гриппом до настоящего времени остается вакцинация. Однако вакцины, эффективной против риновирусной инфекции, не существует.
Главный недостаток вакцинации и специфической противовирусной профилактики состоит в том, что их действие ограничено только вирусами гриппа, защита против других возбудителей ОРВИ отсутствует. Существует потребность в разработке новых средств и доступных терапевтических форм для лечения и профилактики гриппа и ОРВИ. При этом такие средства предпочтительно должны обладать способностью оказывать противовоспалительное действие в очагах локализации инфекции.
Таким образом, задачей настоящего изобретения являлось создание новых нетоксичных терапевтически активных веществ для применения в терапии инфекционных и воспалительных заболеваний.
Ниже приведены определения терминов, которые используются в описании настоящего изобретения.
«Лекарственное начало» (лекарственная субстанция, лекарственное вещество) означает физиологически активное вещество синтетического или иного (биотехнологического, растительного, животного, микробного и прочего) происхождения, обладающее фармакологической активностью и являющееся активным началом фармацевтической композиции, используемой для производства и изготовления лекарственного препарата (средства).
«Лекарственное средство (препарат)» - вещество (или смесь веществ в виде фармацевтической композиции) в виде таблеток, капсул, инъекций, мазей и других готовых форм, предназначенное для восстановления, исправления или изменения физиологических функций у человека и животных, а также для лечения и профилактики болезней, диагностики, анестезии, контрацепции, косметологии и прочего.
«Фармацевтическая композиция» обозначает композицию, включающую в себя по меньшей мере одно соединение общей формулы (I) и/или его оптические изомеры, и/или его фармацевтически приемлемые соли и, по крайней мере, один из компонентов, выбранных из группы, состоящей из фармацевтически приемлемых и фармакологически совместимых наполнителей, растворителей, разбавителей, носителей, вспомогательных, распределяющих средств, средств доставки. К группе перечисленных компонентов относятся консерванты, стабилизаторы, наполнители, дезинтегранты, увлажнители, эмульгаторы, суспендирующие агенты, загустители, подсластители, отдушки, ароматизаторы, антибактериальные агенты, фунгициды, лубриканты, регуляторы пролонгированной доставки, выбор и соотношение которых зависит от их природы, способа введения композиции и дозировки. Примерами суспендирующих агентов являются этоксилированный изостеариловый спирт, полиоксиэтилен, сорбитол и сорбитовый эфир, микрокристаллическая целлюлоза, метагидроксид алюминия, бентонит, агар-агар и трагакант, а также иные фармацевтически приемлемые поверхностно-активные вещества, и смеси этих веществ. Защита от действия микроорганизмов может быть обеспечена с помощью разнообразных антибактериальных и противогрибковых агентов, например, таких как бензиловый спирт, уротропин, этилендиаминтетрауксусная кислота, бензойная кислота, хлорбутанол, сорбиновая кислота, парабены, алкилпиридиний, бензетоний и их фармацевтически приемлемые соли и подобные им соединения. Композиция может включать также изотонические агенты, например, сахара, хлористый натрий и им подобные. Пролонгированное действие композиции может быть обеспечено с помощью агентов, замедляющих абсорбцию активного начала, например, таких как гидрофильные полимерные замедлители высвобождения, например, производные целлюлозы, полиэтиленоксид, желатин, поливиниловый спирт, поливинилпирролидон, альгинаты, карбомеры, гидрофобные замедлители высвобождения, такие как глицерилбегенат, моностеарат алюминия. Примерами подходящих носителей, растворителей, разбавителей и средств доставки являются вода, этанол, полиспирты, буферные растворы, а также их смеси, растительные масла (такие как оливковое масло) и инъекционные органические сложные эфиры (такие как этилолеат). Примерами наполнителей являются лактоза, молочный сахар, микрокристаллическая целлюлоза, цитрат натрия, карбонат кальция, фосфат кальция и им подобные. Для регулирования pH могут быть использованы различные органические и неорганические кислоты, такие как яблочная, аскорбиновая, лимонная, уксусная, янтарная, винная, фумаровая, молочная, аспарагиновая, глутаровая, глутаминовая, сорбиновая кислоты. Примерами диспергирующих агентов и распределяющих средств являются крахмал, альгиновая кислота и ее соли, силикаты. Примерами лубрикантов являются стеарат магния, лаурилсульфат натрия, тальк, коллоидный диоксид кремния, а также полиэтиленгликоль с высоким молекулярным весом. Фармацевтическая композиция для перорального, сублингвального, трансдермального, внутримышечного, внутривенного, подкожного, местного или ректального введения активного начала, одного или в комбинации с другим активным началом, может быть введена животным и людям в стандартной форме введения, в виде смеси с традиционными фармацевтическими носителями. Пригодные стандартные формы введения включают пероральные формы, такие как таблетки, желатиновые капсулы, пилюли, порошки, гранулы, жевательные резинки и пероральные растворы, эликсиры или суспензии, сублингвальные и трансбуккальные формы введения, аэрозоли, имплантаты, местные, трансдермальные, подкожные, внутримышечные, внутривенные, интраназальные или внутриглазные формы введения и ректальные формы введения.
«Фармацевтически приемлемая соль» означает относительно нетоксичные органические и неорганические соли кислот и оснований, заявленных в настоящем изобретении. Эти соли могут быть получены in situ в процессе синтеза, выделения или очистки соединений, или получены специально. В частности, соли оснований могут быть получены специально, исходя из очищенного свободного основания заявленного соединения и подходящей органической или неорганической кислоты. Примерами полученных таким образом солей являются гидрохлориды, гидробромиды, сульфаты, бисульфаты, фосфаты, нитраты, ацетаты, оксалаты, валериаты, олеаты, пальмитаты, стеараты, лаураты, бораты, бензоаты, лактаты, тозилаты, цитраты, малеаты, фумараты, сукцинаты, тартраты, мезилаты, малонаты, салицилаты, пропионаты, этансульфонаты, бензолсульфонаты, сульфаматы и им подобные [6]. Соли заявленных кислот также могут быть специально получены реакцией очищенной кислоты с подходящим основанием, при этом могут быть синтезированы соли металлов и аминов. К солям металлов относятся соли натрия, калия, кальция, бария, цинка, магния, лития и алюминия, наиболее желательными из которых являются соли натрия и калия. Подходящими неорганическими основаниями, из которых могут быть получены соли металлов, являются гидроксид, карбонат, бикарбонат и гидрид натрия, гидроксид и бикарбонат калия, поташ, гидроксид лития, гидроксид кальция, гидроксид магния, гидроксид цинка. В качестве органических оснований, из которых могут быть получены соли заявленных кислот, выбраны амины и аминокислоты, обладающие достаточной основностью, чтобы образовать устойчивую соль, и пригодные для использования в медицинских целях (в частности, они должны обладать низкой токсичностью). К таким аминам относятся аммиак, метиламин, диметиламин, триметиламин, этиламин, диэтиламин, триэтиламин, бензиламин, дибензиламин, дициклогексиламин, пиперазин, этилпиперидин, трис(гидроксиметил)аминометан и подобные им. Кроме того, для солеобразования могут быть использованы гидроокиси тетраалкиламмония, например, такие как холин, тетраметиламмоний, тетраэтиламмоний и им подобные. В качестве аминокислот могут быть использованы основные аминокислоты – лизин, орнитин и аргинин.
Фармацевтические композиции могут включать фармацевтически приемлемые эксципиенты. Под фармацевтически приемлемыми эксципиентами подразумеваются применяемые в сфере фармацевтики разбавители, вспомогательные агенты и/или носители. Фармацевтическая композиция наряду с действующим веществом по настоящему изобретению или его фармацевтически приемлемой солью может включать и другие активные субстанции, в том числе обладающие активностью, при условии, что они не вызывают нежелательных эффектов.
Термин «терапевтически эффективное количество» означает количество действующего вещества, которое (1) лечит или предупреждает конкретное заболевание, состояние или расстройство, (2) ослабляет, улучшает или устраняет один или более симптомов конкретного заболевания, состояния или расстройства, или (3) предупреждает или задерживает наступление одного или более симптомов конкретного заболевания, состояния или расстройства, изложенного в данном описании.
Термин «фармацевтически приемлемый» означает, что данное вещество или композиция, в отношении которых применяется этот термин, должны быть совместимы с точки зрения химии и/или токсикологии с другими ингредиентами, входящими в состав препарата, и безопасны для того, кого лечат этим веществом или композицией.
Термины «содержащий», «содержит» означает, что указанные комбинации, композиции и наборы включают перечисленные компоненты, но не исключают включение других компонентов.
Предметом настоящего изобретения являются новые соединения общей формулы (I):
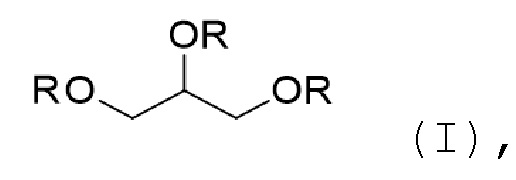
где 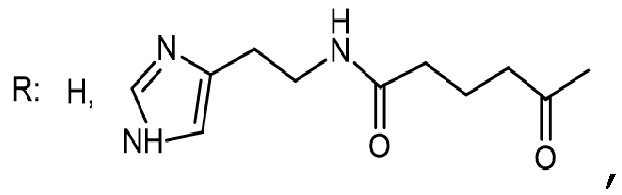 при этом хотя бы один из R представляет собой
при этом хотя бы один из R представляет собой 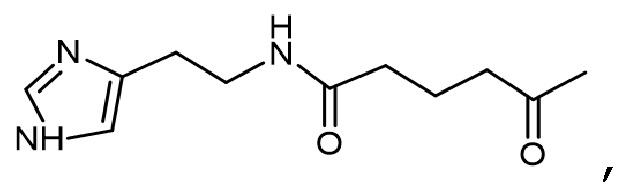
или их оптические изомеры или их фармацевтически приемлемые соли, которые могут быть использованы для лечения и/или профилактики заболеваний дыхательных путей.
Предметом настоящего изобретения также является способ лечения и/или профилактики заболеваний дыхательных путей, включающий введение пациенту, нуждающемуся в этом, эффективного количества по меньшей мере одного соединения формулы (I) или его оптического изомера, или его фармацевтически приемлемой соли.
Более предпочтительным является способ, характеризующийся тем, что заболевания выбраны из группы, состоящей из ринита, синусита, риносинусита, фарингита, назофарингита, тонзиллита, болезней голосовых складок и гортани, вазомоторного и аллергического ринита, бронхита, бронхиолита, пневмонии, бронхиальной астмы, хронической обструктивной болезни легких, муковисцидоза.
Более предпочтительным является способ, характеризующийся тем, что заболевания вызваны вирусом, выбранным из группы, состоящей из риновируса, респираторно-синцитиального вируса, вируса парагриппа, вируса гриппа, аденовируса, метапневмовируса, коронавируса, вируса Коксаки, энтеровируса, ротавируса, вируса герпеса.
Более предпочтительным является способ, характеризующийся тем, что по меньшей мере одно указанное соединение вводят пациенту от 5 до 10 дней.
Предметом настоящего изобретения также является фармацевтическая композиция для лечения и/или профилактики заболеваний дыхательных путей, причем упомянутая композиция содержит в терапевтически эффективном количестве по меньшей мере одно соединение общей формулы (I) или его оптический изомер, или его фармацевтически приемлемую соль, и по меньшей мере один фармацевтически приемлемый носитель.
Предметом настоящего изобретения также является лекарственное средство для лечения и/или профилактики заболеваний дыхательных путей в виде таблеток, капсул или сиропа, помещенных в фармацевтически приемлемую упаковку, причем упомянутое средство содержит в терапевтически эффективном количестве соединение общей формулы (I) или его оптический изомер, или его фармацевтически приемлемую соль, или фармацевтическую композицию, содержащую соединение общей формулы (I) или его оптический изомер, или его фармацевтически приемлемую соль.
Предметом настоящего изобретения также является применение соединения общей формулы (I) или его оптического изомера, или соли его оптического изомера для лечения и/или профилактики заболеваний дыхательных путей.
Предметом настоящего изобретения также является применение фармацевтической композиции согласно настоящему изобретению или лекарственного средства согласно настоящему изобретению для лечения и/или профилактики заболеваний дыхательных путей.
Авторам настоящего изобретения удалось синтезировать новые соединения общей формулы (I), которые обладают способностью связывать переходные металлы (обладают хелатирующими свойствами), а также способны инактивировать свободные радикалы (обладают антиоксидантными свойствами). Кроме того, соединения общей формулы (I) согласно настоящему изобретению способны стимулировать макрофаги, что является важным и необходимым звеном иммунитета, обладают противовирусными и противовоспалительными свойствами. Совокупность указанных свойств соединения общей формулы (I) согласно настоящему изобретению делает их перспективными объектами, которые могут быть использованы в терапевтических целях для лечения и/или профилактики инфекционных заболеваний, в том числе вирусных заболеваний, а также в качестве противовоспалительного средства.
Настоящее изобретение относится к cложным эфирам полиол-имидазолилэтиламидов пентандиовой кислоты общей формулы (I), которые могут использоваться в качестве нетоксичных противовирусных и противовоспалительных средств:
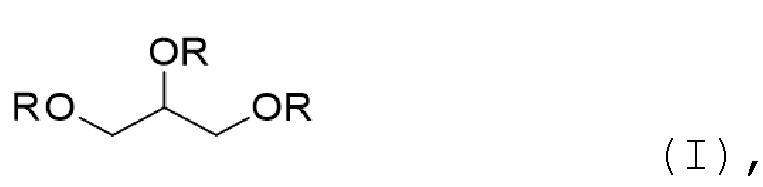
где
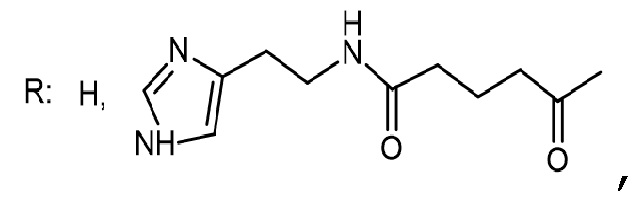 при этом хотя бы один из R представляет собой
при этом хотя бы один из R представляет собой 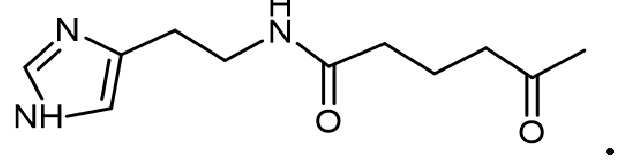
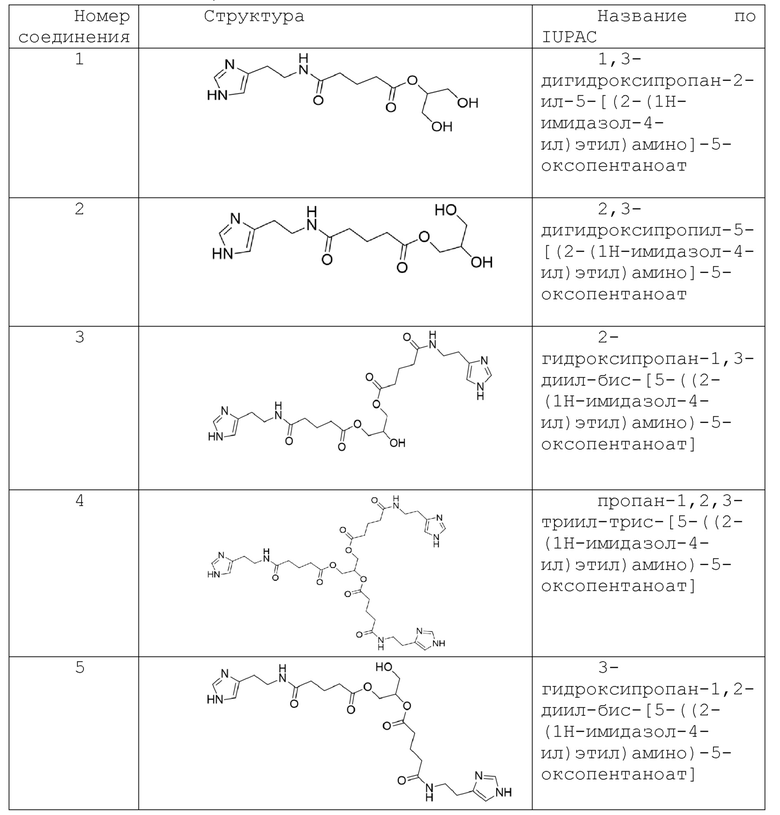
Наиболее предпочтительными являются соединения общей формулы (I), представленные в таблице 1.
Таблица 1. Наиболее предпочтительные соединения общей формулы (I) согласно настоящему изобретению.
Пример 1. Способ получения соединений общей формулы (I)
Соединения согласно настоящему изобретению получали в несколько стадий.
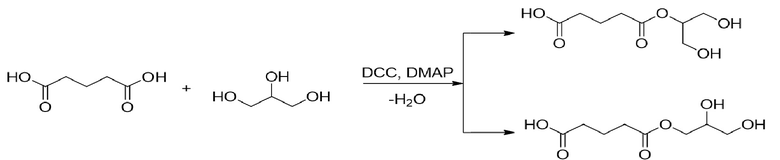
На первой стадии смешивали глутаровую кислоту с глицерином в мольном соотношении 1:1 в присутствии растворителя ацетонитрила. В качестве катализаторов использовали N,N'-дициклогексилкарбодиимид (DCC) и 4-диметиламинопиридин (DMAP). Реакционную смесь перемешивали в течение часа при 0°С. Полноту протекания реакции контролировали методом ТСХ. Реакционную смесь отогревали до комнатной температуры, осадок отфильтровали. Растворители удаляли в вакууме, остаток растворяли в хлористом метилене и пропускали через слой SiO2.
Продуктами реакции является смесь изомеров сложных эфиров 1,3-дигидроксипропан-2-ил пентаноата и 2,3-дигидроксипропил пентаноата.
Разделение продуктов проводили методом препаративной ВЭЖХ.
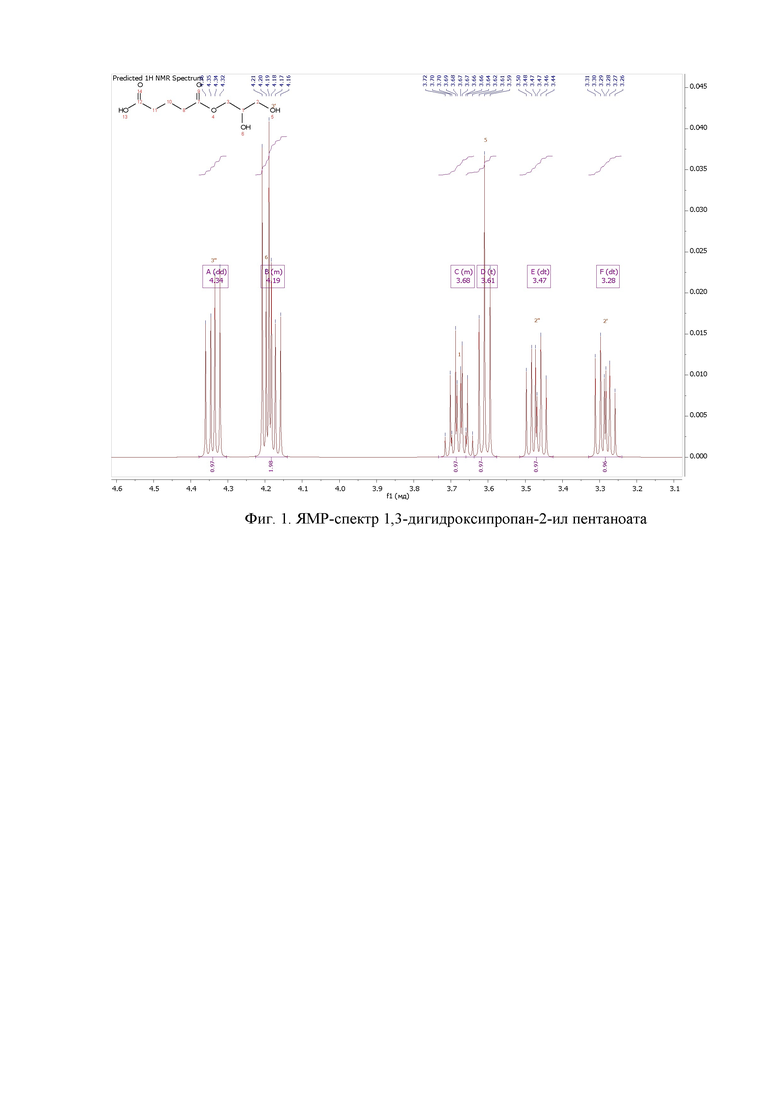
1,3-Дигидроксипропан-2-ил пентаноат получен с выходом 48,7%.
ЯМР: 1H (300 MHz, CDCl3) δ = 1.92 (p, 2H), 2.47 (t, 4H), 3.78-3.90 (m, 4H), 4.28 (t, 2H), 4.73-4.79 (m, 1H). ЯМР-спектр 1,3-дигидроксипропан-2-ил пентаноата см. на фиг. 1.
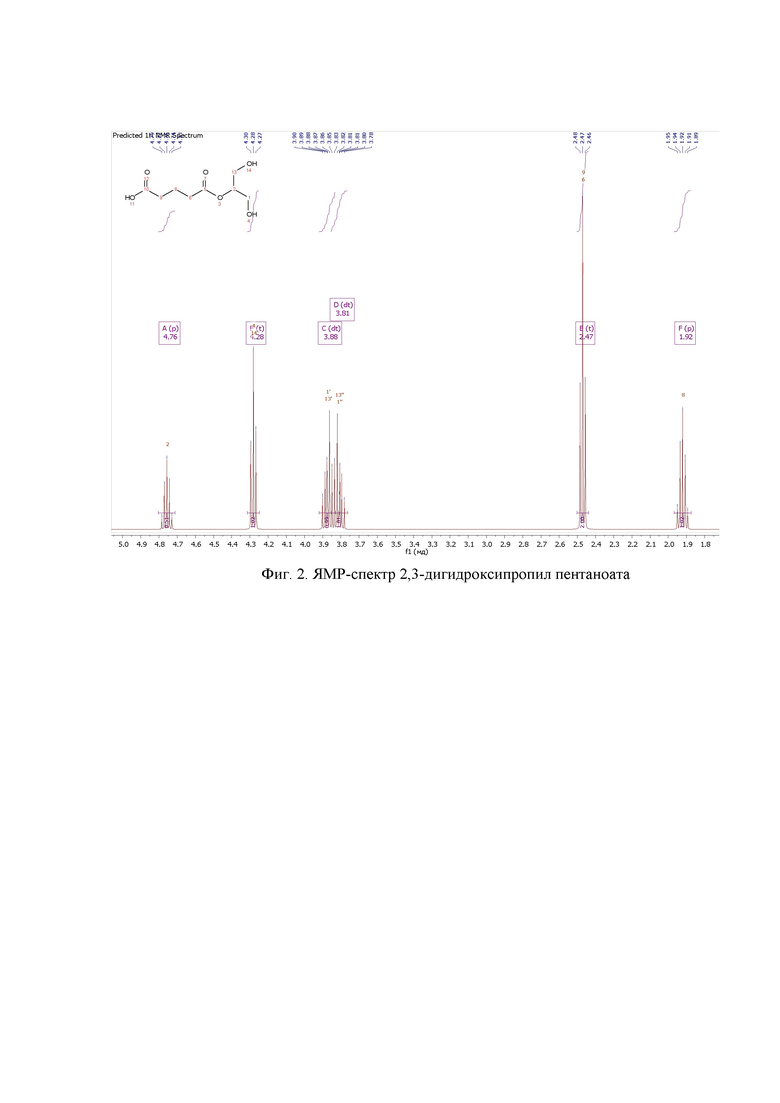
2,3-Дигидроксипропил пентаноат получен с выходом 46,9% .
ЯМР: 1H (300 MHz, CDCl3) δ = 1.86-1.95 (m, 2H), 2.43-2.55 (m. 4H), 3.28 (dt, 1H), 3.47 (dt, 1H), 3.61 (br, 1H), 3.64-3.72 (m, 1H), 4.16-4.21 (m, 2H), 4.34 (dd, 1H). ЯМР-спектр 2,3-дигидроксипропил пентаноата см. на фиг. 2.
Общая методика получения сложных эфиров полиол-имидазолилэтиламидов пентандиовой кислоты: к полученному на предыдущей стадии сложному эфиру в ацетонитриле добавляли гистамин в избытке. В качестве катализатора использовали DCC. Реакционную смесь перемешивали в течение часа при 0°С. Полноту протекания реакции контролировали методом ТСХ. Реакционную смесь отогревали до комнатной температуры, осадок отфильтровали. Растворители удаляли в вакууме, остаток растворяли в хлористом метилене и пропускали через слой SiO2. Продукт кристаллизовали из смеси изопропиловый спирт (ИПС) : гексан.
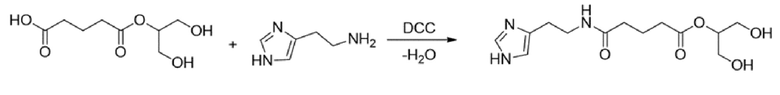
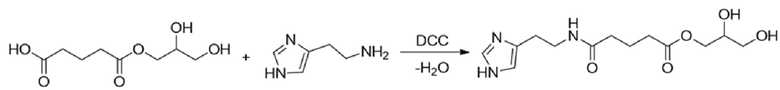
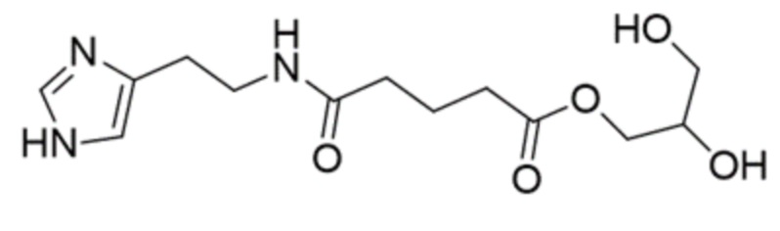
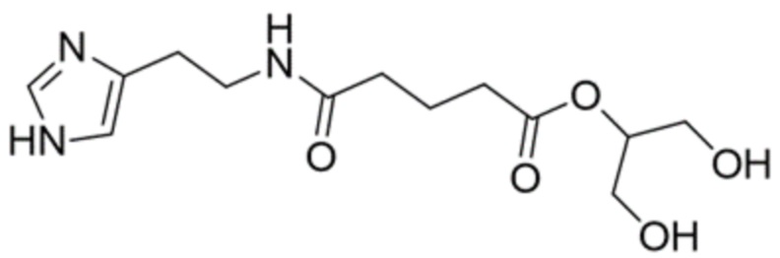
Продуктами данной реакции являются 1,3-дигидроксипропан-2-ил-5-[(2-(1H-имидазол-4-ил) этил) амино]-5-оксопентаноат и 2,3-дигидроксипропил-5-[(2-(1H-имидазол-4-ил) этил) амино]-5-оксопентаноат.
1,3-Дигидроксипропан-2-ил-5-[(2-(1H-имидазол-4-ил)этил)амино]-5-оксопентаноат получен с выходом 78,2%.
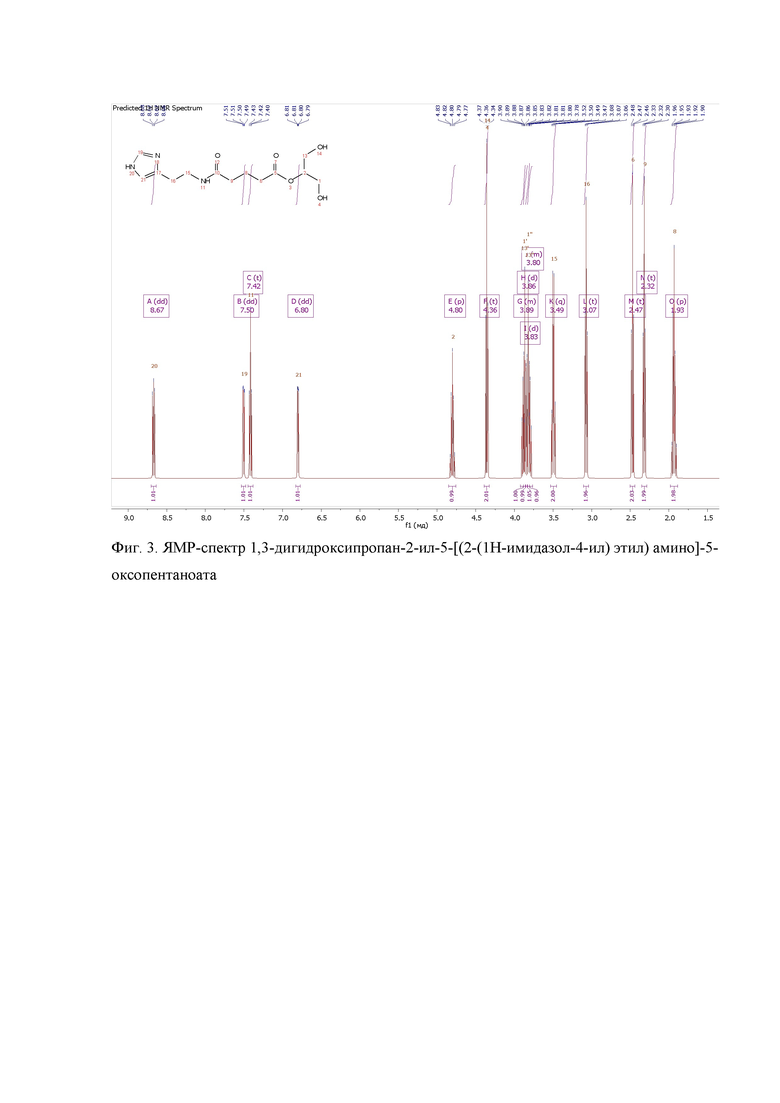
ЯМР: 1H (300 MHz, CDCl3) δ = 1.90-1.96 (m, 2H), 2.42 (t, 2H), 2.47 (t, 2H), 3.00-3.07 (m, 2H), 3.52-3.58 (m, 2H), 3.78-3.90 (m, 4H), 4.36 (t, 2H), 4.85 (p, 1H), 6.80 (dd, 1H), 7.35 (t, 1H), 7.50 (dd, 1H), 8.75 (m, 1H). ЯМР-спектр 1,3-дигидроксипропан-2-ил-5-[(2-(1H-имидазол-4-ил)этил)амино]-5-оксопентаноата см. на фиг. 3.
2,3-Дигидроксипропил-5-[(2-(1H-имидазол-4-ил) этил) амино]-5-оксопентаноат получен с выходом 81,5%.
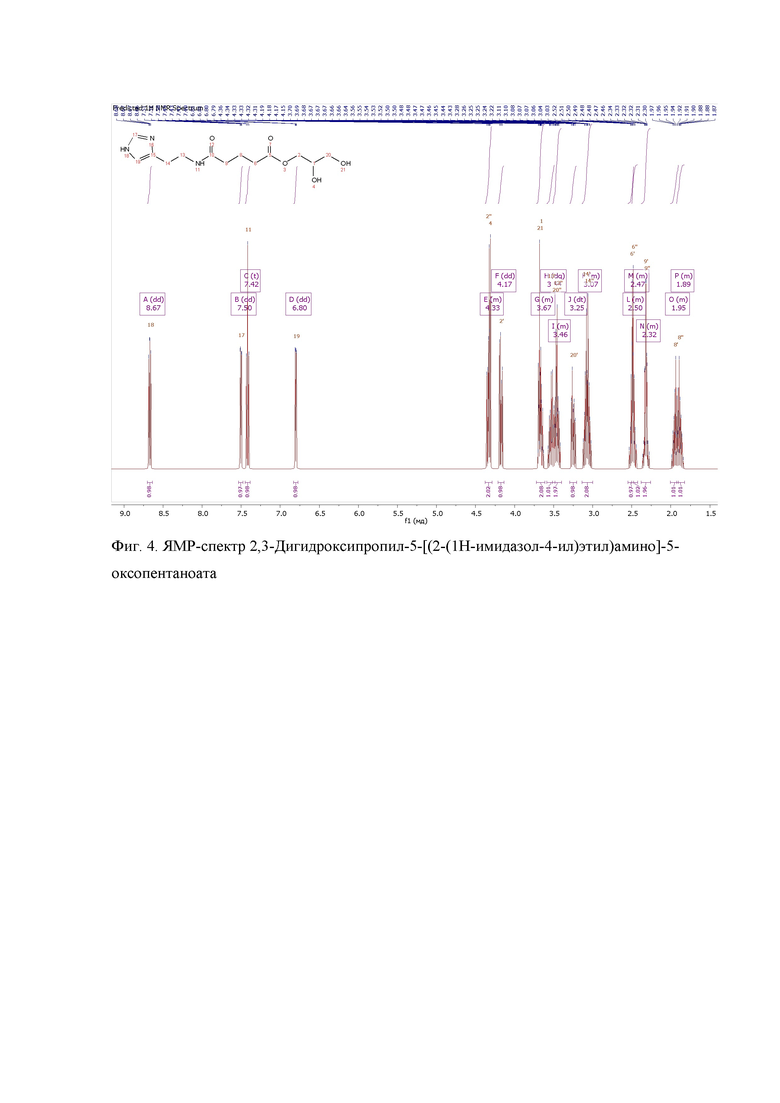
ЯМР: 1H (300 MHz, CDCl3) δ = 1.84-1.99 (m, 2H), 2.28-2.36 (m, 2H), 2.44-2.53 (m, 2H), 3.02-3.12 (m, 2H), 3.22-3.28 (m, 1H), 3.42-3.57 (m, 3H), 3.63-3.70 (m, 2H), 4.17 (dd, 1H), 4.31-4.36 (m, 2H), 6.85 (dd, 1H), 7.41 (t, 1H), 7.61 (dd, 1H), 8.80 (m, 1H). ЯМР-спектр 2,3-дигидроксипропил-5-[(2-(1H-имидазол-4-ил) этил) амино]-5-оксопентаноата см. на фиг. 4.
Пример 2. Противовирусное действие новых соединений общей формулы (I) согласно настоящему изобретению
Исследовали противовирусное действие новых соединений общей формулы (I) (соединения 1, 2, 3, 4, 5). Составы были приготовлены согласно примеру 1.
Противовирусное действие новых составов согласно настоящему изобретению в отношении адаптированного к мышам респираторно-синцитиального вируса человека.
Эксперимент проводили на белых беспородных мышах обоих полов массой 8-10 г, которых рандомизированно делили на 6 групп, в каждой группе по 10 животных: соединение 1, соединение 2, соединение 3, соединение 4, соединение 5 и группа контроля, получавшая плацебо. Животных содержали по пять особей в терморегулируемых боксах (с температурой в среднем 21°С) при 12-часовом цикле дня и ночи и с достаточным количеством воды и пищи. Для проведения исследований был использован респираторно-синцитиальный вирус человека (РС вирус), предварительно адаптированный к росту в легких мышей. Мышей инфицировали РС вирусом интраназально под легким эфирным наркозом в дозе 5,0 logTCID50, в объеме 0,05 мл для каждой мыши. О противовирусной эффективности новых соединений общей формулы (I) согласно настоящему изобретению судили посредством измерения вирусного титра в легких мышей экспериментальных групп по сравнению с группой контроля на 5-е и 7-е сутки инфицирования посредством титрования выделенной легочной суспензии мышей в культуре клеток Heр-2, по цитопатическому эффекту или действию (ЦПД) [7]. Животные получали лечение составами перорально при помощи зонда в дозе 50 мг в пересчете на человека, один раз в сутки в течение 7 дней, аналогичным образом, животные контрольной группы получали плацебо. Лечение начинали через сутки после инфицирования.
Таблица 2. Противовирусное действие новых соединений общей формулы (I) согласно настоящему изобретению в модели экспериментальной респираторно-синцитиальной вирусной инфекции у мышей.
*достоверное отличие инфекционного титра вируса в легких мышей экспериментальных групп (соединения 1-5) от инфекционного титра вируса в легких мышей контрольной группы, получавшей плацебо (р<0,05).
Представленные данные свидетельствуют о том, что новые соединения общей формулы (I) согласно настоящему изобретению обладают противовирусной активностью, что подтверждается снижением титров вирусов в легких мышей по сравнению с мышами контрольной группы, получавшими плацебо (статистический уровень значимости р<0,05).
Противовирусное действие новых составов согласно настоящему изобретению в отношении вируса гриппа.
Эксперимент проводили на белых беспородных мышах обоих полов массой 8-10 г, которых рандомизированно делили на 6 групп, в каждой группе по 10 животных: соединение 1, соединение 2, соединение 3, соединение 4, соединение 5 и группа контроля, получавшая плацебо. Животных содержали по пять особей в терморегулируемых боксах (с температурой в среднем 21°С) при 12-часовом цикле дня и ночи и с достаточным количеством воды и пищи. Для проведения исследований был использован вирус гриппа человека, тип A, штамм Aichi (аллантоисная жидкость), предварительно титрованный на мышах. Мышей инфицировали вирусом гриппа интраназально под легким эфирным наркозом в дозе 100 LD50, в объеме 0,05 мл для каждой мыши [7]. О противовирусной эффективности новых соединений общей формулы (I) согласно настоящему изобретению судили по изменению средней продолжительности жизни (СПЖ) мышей, выживаемости мышей и степени защиты от смертельной дозы вирусной инфекции, обеспечиваемой препаратом. Степень защиты, обеспечиваемой препаратом, вычислялась как разница между количеством выживших животных (в процентах) в экспериментальной группе, получавшей лечение соединениями 1-5, и количеством выживших животных (в процентах) в контрольной группе, получавшей плацебо. Животные получали лечение составами перорально при помощи зонда в дозе 50 мг в пересчете на человека, один раз в сутки в течение 3 дней до заражения и 10 дней после заражения, аналогичным образом, животные контрольной группы получали плацебо [8].
Таблица 3. Противовирусное действие новых соединений общей формулы (I) согласно настоящему изобретению в модели экспериментальной гриппозной инфекции у мышей.
* достоверное отличие средней продолжительности жизни и выживаемости у мышей экспериментальных групп (соединения 1-5) от аналогичных показателей у мышей контрольной группы, получавшей плацебо (р<0,05).
Представленные данные свидетельствуют о том, что новые соединения общей формулы (I) согласно настоящему изобретению обладают противовирусной активностью, что подтверждается увеличением СПЖ и выживаемости мышей экспериментальных групп по сравнению с мышами контрольной группы, получавшими плацебо (статистический уровень значимости р<0,05).
Противовирусное действие новых составов согласно настоящему изобретению в отношении риновируса.
Эксперимент проводили на белых беспородных мышах обоих полов массой 8-10 г, которых рандомизированно делили на 6 групп, в каждой группе по 10 животных: соединение 1, соединение 2, соединение 3, соединение 4, соединение 5 и группа контроля, получавшая плацебо. Животных содержали по пять особей в терморегулируемых боксах (с температурой в среднем 21°С) при 12-часовом цикле дня и ночи и с достаточным количеством воды и пищи. Для проведения исследований был использован риновирус человека, штамм HRV-1 (депонированный в ГКВ2730), предварительно титрованный на мышах. Мышей инфицировали риновирусом интраназально под легким эфирным наркозом в дозе 5,0 lgTCID50, в объеме 0,05 мл для каждой мыши. Для оценки противовирусной эффективности новых соединений общей формулы (I) согласно настоящему изобретению проводили измерения вирусного титра в легких мышей экспериментальных групп по сравнению с группой контроля на 2-е и 3-е сутки после инфицирования посредством титрования выделенной легочной суспензии мышей в культуре клеток HeLa по цитопатическому эффекту или действию (ЦПД) [7]. Животные получали лечение составами перорально при помощи зонда в дозе 30 мг в пересчете на человека один раз в сутки в течение 5 дней, аналогичным образом, животные контрольной группы получали плацебо. Лечение начинали через сутки после инфицирования.
Таблица 4. Противовирусное действие новых соединений общей формулы (I) согласно настоящему изобретению в модели экспериментальной риновирусной инфекции у мышей.
* достоверное отличие инфекционного титра вируса в легких мышей экспериментальных групп (соединения 1-5) от инфекционного титра вируса в легких мышей контрольной группы, получавшей плацебо (р<0,05).
Представленные данные свидетельствуют о том, что новые соединения общей формулы (I) согласно настоящему изобретению обладают противовирусной активностью, что подтверждается снижением титров вирусов в легких мышей по сравнению с мышами контрольной группы, получавшими плацебо (статистический уровень значимости р<0,05).
Пример 3. Исследование противовоспалительной активности соединений общей формулы (I) в модели каррагинанового отека лапы у крыс.
Эксперимент проводили на крысах линии Вистар обоих полов, которых рандомизированно делили на 6 групп, в каждой группе по 10 животных: соединение 1, соединение 2, соединение 3, соединение 4, соединение 5 и группа контроля, получавшая плацебо. Животных содержали по пять особей в терморегулируемых боксах (с температурой в среднем 21°С) при 12-часовом цикле дня и ночи и с достаточным количеством воды и пищи. Для проведения исследований была использована модель каррагинанового отека лапки крыс линии Вистар. Отек вызывали субплантарным введением 0,1 мл 1%-ного водного раствора λ-каррагинана в заднюю конечность животных опытных и контрольных групп. Животные экспериментальных групп получали исследуемые соединения сразу после индукции каррагинанового отека перрорально при помощи зонда в дозе 30 мг в пересчете на человека. Аналогичным образом животные контрольной группы получали плацебо. Оценку отека проводили измерением объема стопы с помощью механического онкометра до введения флагогена, через два часа после его введения и через четыре часа после его введения. О степени отека судили по разнице в объеме между отечной стопой и стопой до индукции воспаления. Противовоспалительную активность соединений общей формулы (I) определяли при помощи формулы А=(ΔVк-ΔVэ/ΔVк)·100%, где А – противовоспалительная активность в процентах; ΔVэ и ΔVк – разница межу отечной и нормальной стопами у животных экспериментальных и контрольной групп.
Таблица 5. Противовоспалительное действие соединений общей формулы (I) в модели каррагинанового отека лапы у крыс.
Представленные данные свидетельствуют о том, что при приеме соединений общей формулы (I) наблюдалось достоверное (р<0,05) снижение отека стопы у мышей экспериментальных групп, что свидетельствует о том, что соединения общей формулы (I) обладают противовоспалительной активностью.
Изобретение может быть использовано в медицине, химии, фармацевтической промышленности.
Список литературы
1. Рублева О.В.: «К вопросу о терапии и профилактике вирусных инфекций» // Русский медицинский журнал, 2012, Т. 20, №11, С. 571-574;
2. Ершов Ф.И., Гаращенко Т.И.: «Возможен ли контроль острых респираторных заболеваний у детей? (Новый взгляд на старую проблему)» // Актуальные вопросы оториноларингологии детского возраста и фармакотерапия болезней ЛОР-органов. Юбилейный сборник научных трудов, Москва, 2001;
3. Селькова Е.П.: «Профилактика и лечение острых респираторных вирусных инфекций. Применение амиксина» // Пособие для врачей, М., 2004;
4. Беляков К.В.: «Профилактика и лечение ОРВИ в современных городских условиях» // Consilium Provisorum, 2006, Т.04, №5;
5. Гендон Ю.З.: «Этиология острых респираторных заболеваний» // Вакцинация, 2001, №5(17), С. 4-5;
6. Berge S.M., Bighley L.D., Monkhouse D.C.: «Pharmaceutical Salts» // Journal of Pharmaceutical Sciences, 1997, V. 66, №1, P. 1-19;
7. Маркушин С.Г., Кост В.Ю., Ртищев А.А., Акопова И.И., Коптяева И.Б., Лисовская К.В.: «Особенности иммунного ответа мышей, иммунизированных различными типами кандидатов в живые гриппозные вакцины, на инфекцию, вызванную вирулентным штаммом вируса гриппа» // Эпидемиология и вакцинопрофилактика, 2016, №5(90), С. 79-85;
8. Полетаева А.В., Леванюк А.И., Сергеева Е.В.: «Влияние гормонов на иммунологическую реактивность. Обзор» // Экология человека, 2009, №7, С. 42-46.
Изобретение относится к области медицины, фармакологии и химико-фармацевтической промышленности, а именно к фармацевтической композиции для лечения и/или профилактики вирусных заболеваний дыхательных путей или воспалительных заболеваний, содержащей в терапевтически эффективном количестве соединение формулы (I), или его изомер формулы (II), или их фармацевтически приемлемую соль, и, по меньшей мере, один фармацевтически приемлемый носитель
 (I)
(I)
 (II). Также изобретение относится к лекарственному средству, содержащему данную фармацевтическую композицию и к применению фармацевтической композиции или лекарственного средства. Технический результат - создание новых нетоксичных терапевтически активных веществ для применения в терапии инфекционных и воспалительных заболеваний. 3 н.п. ф-лы, 5 табл., 3 пр., 4 ил.
(II). Также изобретение относится к лекарственному средству, содержащему данную фармацевтическую композицию и к применению фармацевтической композиции или лекарственного средства. Технический результат - создание новых нетоксичных терапевтически активных веществ для применения в терапии инфекционных и воспалительных заболеваний. 3 н.п. ф-лы, 5 табл., 3 пр., 4 ил.
1. Фармацевтическая композиция для лечения и/или профилактики вирусных заболеваний дыхательных путей или воспалительных заболеваний, содержащая в терапевтически эффективном количестве соединение формулы (I), или его изомер формулы (II), или их фармацевтически приемлемую соль, и, по меньшей мере, один фармацевтически приемлемый носитель
 (I)
(I)
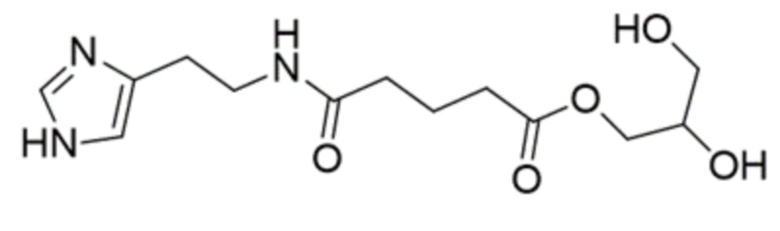 (II).
(II).
2. Лекарственное средство для лечения и/или профилактики вирусных заболеваний дыхательных путей или воспалительных заболеваний, выполненное в виде таблеток, капсул или сиропа, помещенных в фармацевтически приемлемую упаковку, содержащее в терапевтически эффективном количестве фармацевтическую композицию по п. 1.
3. Применение фармацевтической композиции по п. 1 или лекарственного средства по п. 2 для лечения и/или профилактики вирусных заболеваний дыхательных путей или воспалительных заболеваний.
| СПОСОБ ИНДУКЦИИ ДИФФЕРЕНЦИРОВКИ КЛЕТОК | 2002 |
|
RU2217196C2 |
| Устройство для закрепления лыж на раме мотоциклов и велосипедов взамен переднего колеса | 1924 |
|
SU2015A1 |
| Julia Quinton et al | |||
| Reaction Discovery by Using a Sandwich Immunoassay | |||
| Angewandte Chemie - International Edition, 2012, 51(25), 6144-6148 | |||
| Медицинская вирусология | |||
| Учебное пособие, под ред | |||
| д.м.н., профессора И.И | |||
| Генералова | |||
| Витебск, 2017, Раздел 2 | |||
| Челенкова И.Н | |||
| и др | |||
| Острые и | |||
Авторы
Даты
2022-07-27—Публикация
2020-06-18—Подача