Область техники, к которой относится изобретение
Изобретение относится к области медицины, в частности к нейрофизиологии, и может быть использовано в неврологии, травматологии и ортопедии при реабилитации больных после заболеваний и/или травматических повреждений головного мозга и/или спинного мозга, следствием которых является нарушение функции ходьбы. Изобретение также может быть использовано для лечения патологии органов дыхательной системы, кардиоваскулярной системы и терапии функций других внутренних органов человека.
Предпосылки изобретения
В настоящее время существуют неинвазивные (не требующие оперативного вмешательства) способы стимуляции спинного мозга, которые позволяют облегчить произвольную ходьбу, а также восстановить и обеспечить самостоятельное передвижение пациентов с нарушениями функции ходьбы, вызванными заболеваниями и/или травматическими повреждениями головного мозга и/или спинного мозга, и позволяют восстановить двигательные функции верхних и нижних конечностей пациентов.
Например, известен способ регуляции и восстановления самостоятельной ходьбы у пациентов с двигательной патологией различного генеза (RU2725090 C1). Способ включает одновременную непрерывную стимуляцию спинного мозга по меньшей мере на уровне позвонков Т11-Т12 и ритмическую стимуляцию корешков спинного мозга на уровне позвонков Т11 и L1, при которой уровень стимуляции и латерализации стимуляции зависит от фазы и скорости движения непораженной верхней и/или нижней конечности. При этом включение ритмической стимуляции корешков спинного мозга осуществляется за счет движения непораженной верхней и/или нижней конечности.
Неинвазивная электрическая стимуляция участков спинного мозга также используется у пациентов с нарушениями опорно-двигательного аппарата в рамках использования активного экзоскелета (RU2016144450 А). При этом накожная электрическая стимуляция осуществляется в районе грудных позвонков Т11, Т12 в зависимости от определенной фазы движения активного экзоскелета.
Также, существующий уровень техники использует накожную электрическую стимуляцию в процессе контроля дыхания у пациентов с острым нарушением дыхания при заболеваниях вирусного или бактериального происхождения (RU2750236 C1). Электростимуляцию используют для активации межреберных мышц, диафрагмы, абдоминальных мышц путем стимуляции корешков спинного мозга и сегментов грудного отдела спинного мозга с различными параметрами импульсов для каждого типа мышц. Перечисленные выше способы и другие известные способы чрескожной электрической стимуляции позволяют воздействовать на спинной мозг в нескольких сегментах одновременно. Для реализации возможности одновременной стимуляции спинного мозга в нескольких разных отделах по различным выбранным алгоритмам используются независимые электроды или системы электродов.
Так, для осуществления, например, способа накожной электростимуляции спинного мозга, раскрытого в RU2545440 C1, используется матрица в виде электродов, размещенных на эластичном электронейтральном основании в три столбца и образующих из каждых 3-х элементов горизонтальные ряды. При этом горизонтальные ряды электродов могут перемещаться и фиксироваться в продольном направлении. Электроды выполнены в виде мягких чашечек, которые заполняют токопроводящим электродным гелем. К подложке эластичному основанию электроды прикрепляются пружинящим жестким основанием, сквозь которое пропущен электрический проводник, подключенный к формирователю электрических стимулов. Для осуществления стимуляции матрицу электродов располагают накожно над позвоночником больного так, чтобы центральные электроды в тройках находились между остистыми отростками над спинным мозгом, а крайние электроды - симметрично справа и слева от центральной линии позвоночника над корешками спинного мозга. Матрицу можно располагать над поясничным утолщением спинного мозга, где расположен центр управления движениями ног, или над шейным утолщением спинного мозга, где находится центр управления движениями рук и который связан с нижележащим поясничным утолщением.
Конструкция подобной матрицы имеет ряд недостатков. Во-первых, конструкция самих электродов приводит к их быстрому изнашиванию и поломке. Во-вторых, жесткое основание электрода не позволяет повторять индивидуальные особенности формы человеческой спины. Это очень неудобно, так как матрицу приходится крепко приматывать к торсу пациентов, что ограничивает движения пациента во время реабилитационных сессий и оставляет глубокие следы на спине от краев матрицы.
Таким образом, для преодоления описанных выше проблем, существует потребность в разработке матрицы электродов, закрепляемой на спине пациента, для осуществления чрескожного мультисегментарного (многоуровневого) стимуляционного электрического воздействия, в том числе, во время движений, на структуры спинного мозга по определенному алгоритму.
Именно этому и посвящена настоящая заявка.
Раскрытие сущности изобретения
Целью настоящего изобретения является преодоление вышеперечисленных недостатков и создание гибкой и многофункциональной электродной матрицы, которая могла бы быть использована в различных применениях электрической стимуляции спинного мозга, при которой требуется мультисегментарное воздействие на спинной мозг.
Техническим результатом, достигаемым при осуществлении изобретения, является разработка электродной матрицы, закрепляемой на спине пациента, над позвоночником, для мультисегментарного (многоуровневого) стимуляционного электрического воздействие на структуры спинного мозга в диапазоне сегментов спинного мозга T1-S1
Технический результат изобретения достигается за счет того, что неинвазивная электродная матрица для мультисегментарной стимуляции спинного мозга содержит раму с направляющими, выполненную с возможностью плотного прилегания к спине пациента; по меньшей мере два сменных модуля с установленными в каждом из них телескопическими держателями электродов, причем электроды закреплены на торцах телескопических держателей, направленных к спине пациента, и являются съемными; по меньшей мере два основания сменных модулей, выполненных с возможностью перемещения вдоль направляющих рамы и фиксации на направляющих рамы в заданном положении; причем каждый из сменных модулей размещен в соответствующем основании и один из телескопических держателей является неподвижным, а остальные подвижные телескопические держатели имеют возможность продольного и вертикального перемещения относительно сменного модуля, в котором они установлены, таким образом, чтобы электроды находились в контакте с кожей пациента.
В некоторых вариантах осуществления изобретения рама выполнена в виде двух параллельно скрепленных элементов, имеющих изогнутую форму типа бумеранга, между которыми располагаются две направляющие, каждая из которых проходит через отверстия в обоих элементах в области изгиба.
В некоторых вариантах изобретения на обоих концах каждого из элементов закреплены опоры через шарнирные соединения.
В частных вариантах реализации изобретения опоры имеют подложку из медицинского силикона для плотного прилегания к телу пациента.
В частных вариантах осуществления изобретения параллельные элементы рамы имеют отверстия для крепления средств крепления матрицы электродов к телу пациента, выбранные из: пояс, бандаж, эластичные ремни.
В частных вариантах осуществления изобретения каждый сменный модуль фиксируется в основании сменного модуля посредством подпружиненных кнопок-защелок, расположенных с каждой стороны сменного модуля.
В некоторых вариантах осуществления изобретения в каждом из сменных модулей установлено по меньшей мере три телескопических держателя электродов.
В некоторых вариантах осуществления изобретения съемным электродом является кнопочный электрод круглой формы с токопроводящим адгезивным слоем.
Другим техническим результатом настоящего изобретения является применение неинвазивной электродной матрицы с использованием чрескожной электрической стимуляции спинного мозга для реабилитации двигательных функций пациента и/или для модуляции дыхательной, кардиоваскулярной или иной функции внутренних органов пациента и/или для диагностики функционального состояния вегетативной нервной системы пациента и/или для купирования спастического синдрома, обусловленного нарушением сегментарного аппарата спинного мозга.
Краткое описание чертежей
Прилагаемые чертежи, которые включены в состав настоящего описания и являются его частью, иллюстрируют варианты осуществления изобретения и совместно с вышеприведенным общим описанием изобретения и нижеприведенным подробным описанием вариантов осуществления служат для пояснения принципов настоящего изобретения. На чертежах одинаковые позиции применяются для обозначения одинаковых деталей или элементов конструкции.
На фиг. 1 изображен вид сверху матрицы электродов.
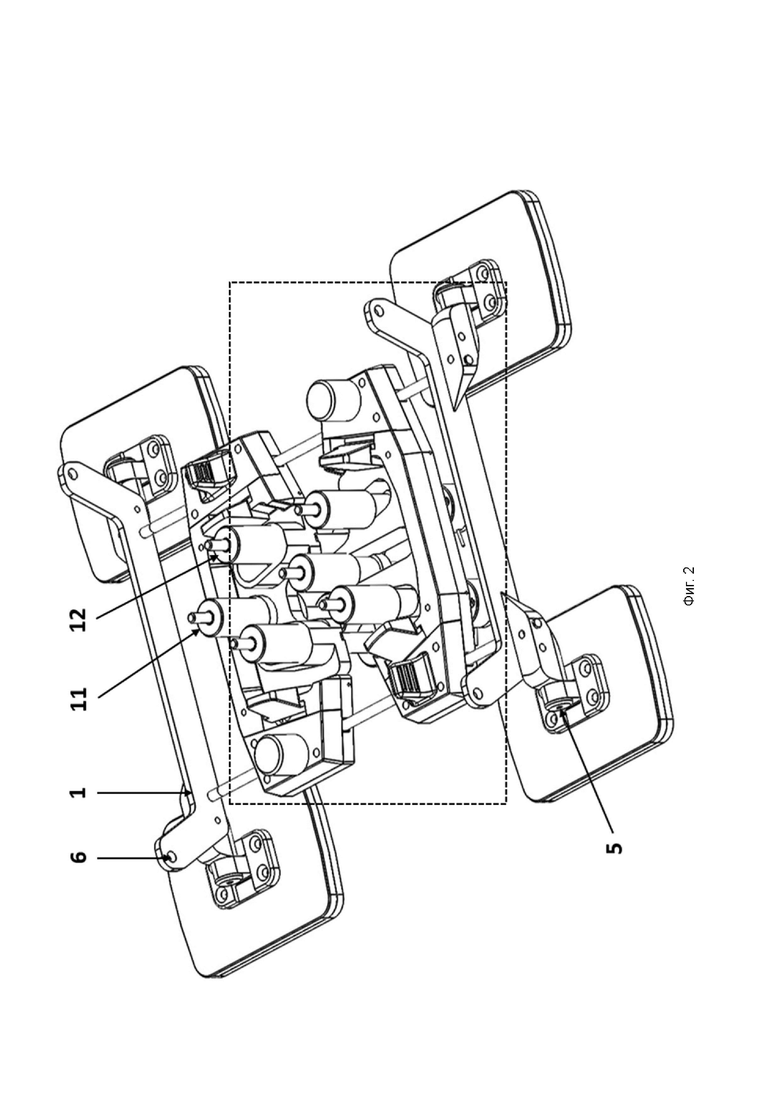
На фиг. 2 представлен вид сбоку матрицы электродов.
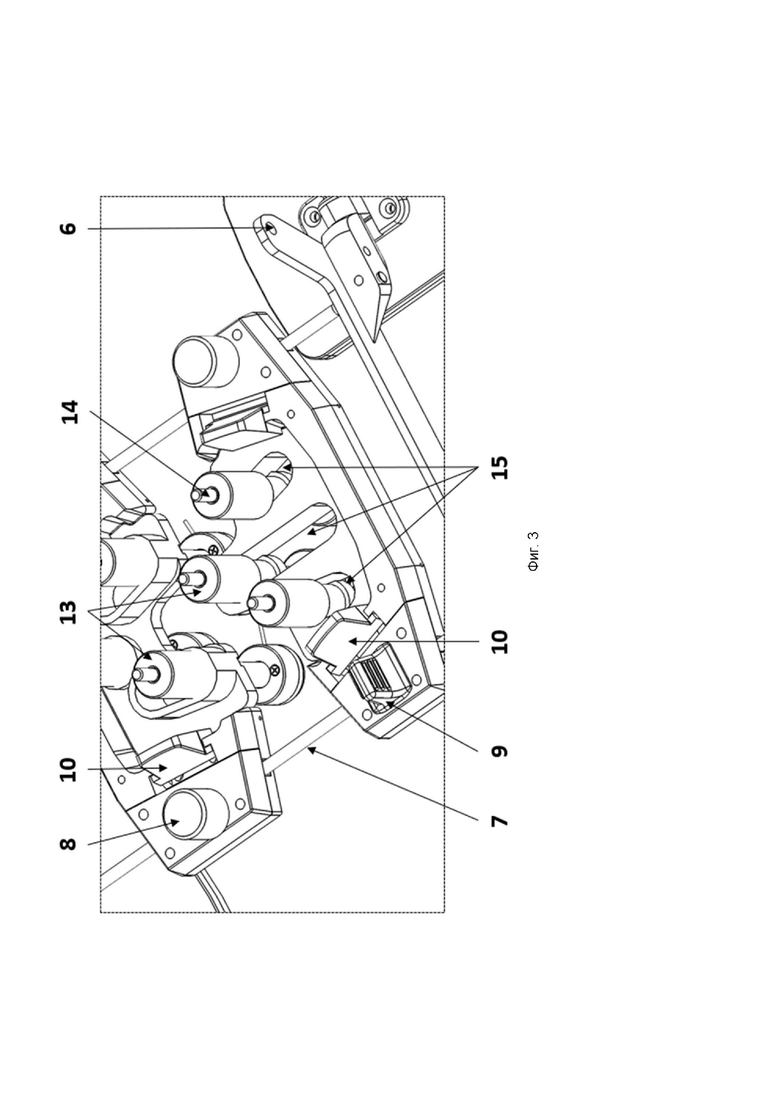
На фиг. 3 изображен вид матрицы электродов, на котором более подробно изображено крепление электродов на сменных модулях.
На фиг. 4 изображен вид матрицы со стороны, которая находится в контакте со спиной пациента.
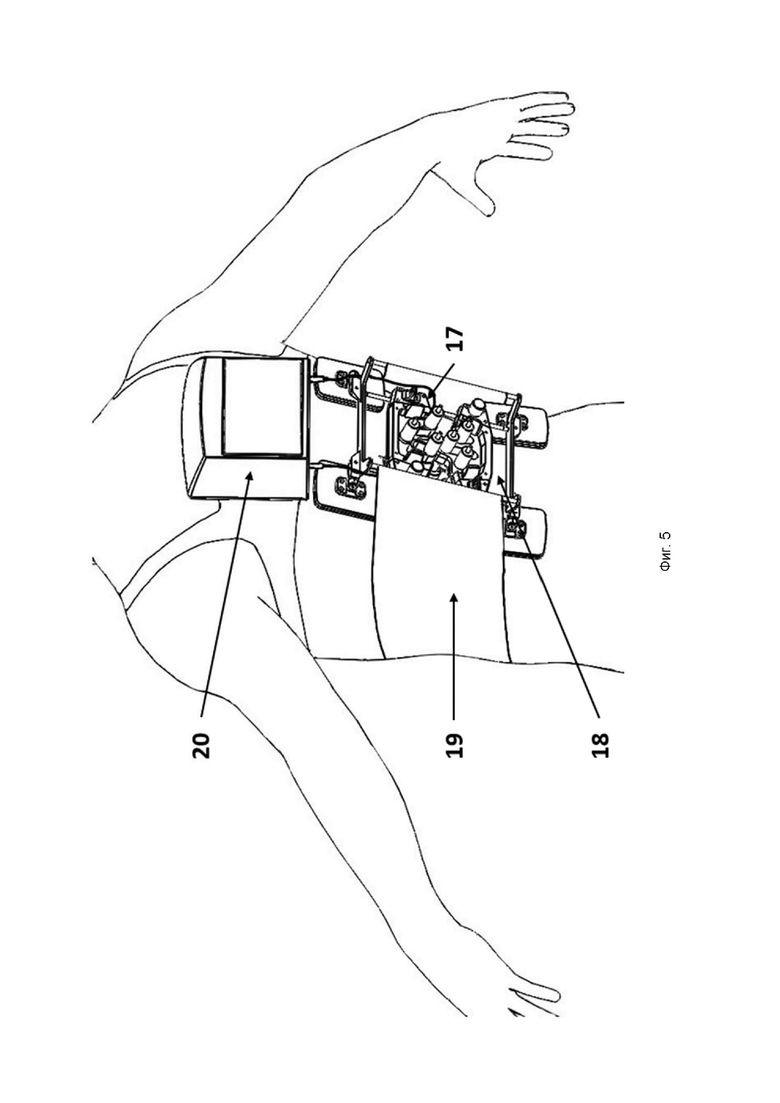
На фиг. 5 представлена матрица на спине пациента, подключаемая к внешнему элекростимулятору во время исследования.
На фиг. 6 изображена схема расположения электродов.
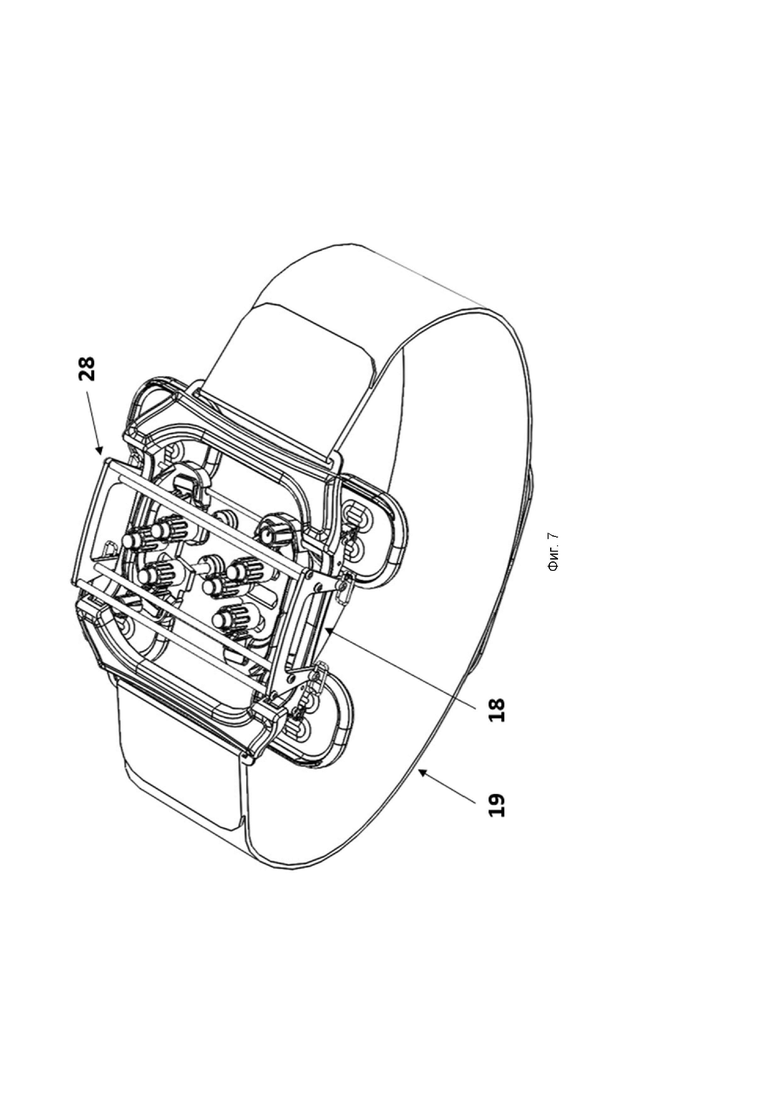
На фиг. 7 представлен один из вариантов осуществления защитной рамы-накладки для предохранения выступающих элементов из электродной матрицы.
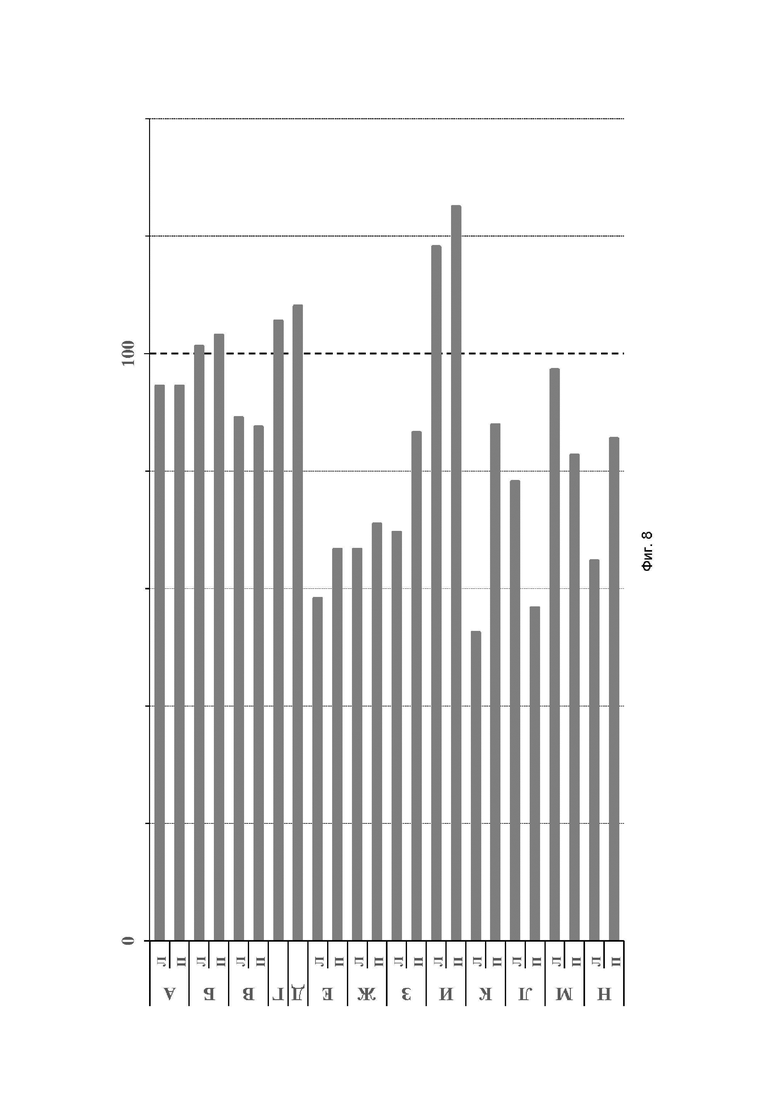
На фиг. 8 приведены относительные изменения (%) кинематических характеристик ходьбы пациента после реабилитационной процедуры у Пациента 1. Тестирование при ходьбе по беговой дорожке. А - длительность цикла шага, Б - длительность периода опоры с паретичной стороны, В - длительность опоры на одной ноге с паретичной стороны, Г - длина цикла шага, Д - скорость ходьбы, Е - высота подъема стопы с паретичной стороны, Ж, З, И - амплитуда сгибания / разгибания в тазобедренном, коленном, голеностопном суставах, соответственно, с паретичной стороны, К, Л, М и Н - амплитуда ЭМГ передней большеберцовой мышцы, латеральной головки икроножной мышцы, прямой мышцы бедра и двуглавой мышцы бедра, соответственно, с паретичной стороны.
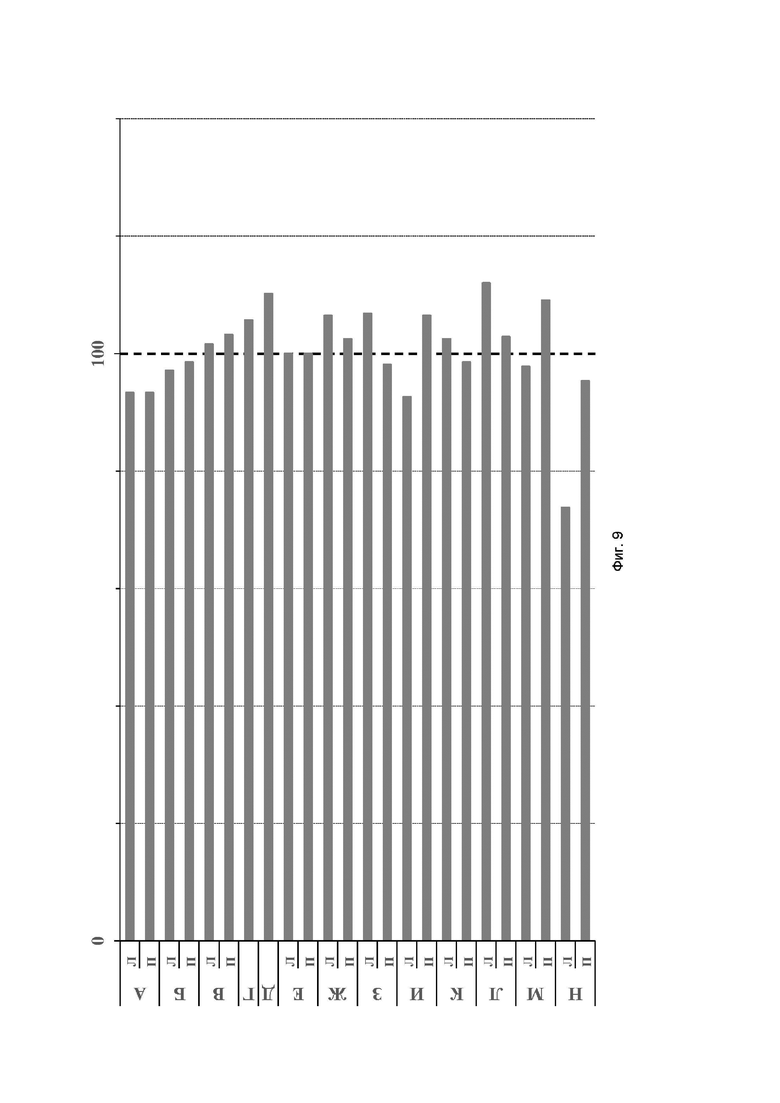
На фиг. 9 приведены относительные изменения (%) кинематических характеристик ходьбы пациента после реабилитационной процедуры у Пациента 2. Тестирование при ходьбе по полу. Остальные обозначения как на фиг. 7
Обозначения
На фигурах элементы обозначены следующими позициями:
1 - опора «бумеранг»,
2 - сменный модуль,
3 - основание сменного модуля,
4 - опора,
5 - шарнирное соединение,
6 - место крепления ремней или пояса,
7 - направляющая,
8 - ручка для перемещения основания сменного модуля,
9 - ручка-фиксатор положения основания модуля,
10 - кнопка-защелка сменного модуля,
11 - телескопический держатель электрода, закрепленный в модуле,
12 - телескопический держатель электрода с возможностью перемещения в модуле,
13 - ручка-фиксатор продольного положения держателя электрода,
14 - шток держателя электрода,
15 - прорезь в сменном модуле для свободного хода держателя электрода,
16 - сменные кнопочные электроды,
17 - проводники к стимулятору.
18 - матрица электродов в сборе,
19 - пояс,
20 - внешний электростимулятор нейропротеза,
21 - позвонок T11,
22 - позвонок T12,
23 - позвонок L1,
24 - позвонок L2,
25 - электрод над спинным мозгом,
26, 27 - электроды над корешками спинного мозга,
28 - крышка.
Термины и определения
Определения некоторых терминов, используемых в данном описании, приведены ниже. Если не определено отдельно, технические и научные термины в данной заявке имеют стандартные значения, общепринятые в научной и технической литературе.
В настоящем описании и в формуле изобретения термины «включает», «включающий» и «включает в себя», «имеющий», «снабженный», «содержащий» и другие их грамматические формы не предназначены для истолкования в исключительном смысле, а, напротив, используются в неисключительном смысле (т.е. в смысле «имеющий в своем составе»). В качестве исчерпывающего перечня следует рассматривать только выражения типа «состоящий из».
Под «регуляцией ходьбы», «контролем ходьбы» понимается управление характеристиками ходьбы в целом (скорость, амплитуда шага, длительность), и ее составляющими, например, фазами шагательного цикла (перенос, опора).
Под «облегчением ходьбы» понимается частный случай регуляции ходьбы, когда управление характеристиками ходьбы приводит к улучшению координации, увеличению устойчивости походки и скорости ходьбы.
Термин «стимуляция» относится к электрическому воздействию переменным током, при этом под «непрерывной стимуляцией» понимается стимуляция, начало и конец которой не зависят от ритмических движений неповрежденных (не затронутых патологическим процессом, ставшим причиной гемиплегии) рук и ног; под «прерывистой (ритмической) стимуляций» понимается стимуляция, начало и конец которой синхронизированы с ритмическими движениями неповрежденных рук и ног, при этом под «пространственно-избирательной стимуляцией» понимается прерывистая (ритмическая) стимуляция, при которой уровень стимуляции и латерализация (справа или слева) стимуляции зависят от фазы движений неповрежденных рук и ног, под «пространственно-временной стимуляцией» подразумевают пространственно-избирательную стимуляцию, при которой начало и конец этой стимуляции зависит от фазы движений неповрежденных рук и ног.
Термин «мультисегментарная стимуляция» относится к воздействию на спинной мозг, обозначает воздействие на уровне двух или более сегментов спинного мозга.
Кроме того, термины «первый», «второй», «третий» и т.д. используются просто как условные маркеры, не накладывая каких-либо численных или иных ограничений на перечисляемые объекты.
Термин «соединенный» означает функционально соединенный, при этом может быть использовано любое количество или комбинация промежуточных элементов между соединяемыми компонентами (включая отсутствие промежуточных элементов).
Подробное описание изобретения
Настоящее изобретение направлено на разработку электродной матрицы, закрепляемую в области позвоночника пациента, с помощью которой возможно осуществить чрескожную стимуляцию спинного мозга.
Схема электродной матрицы (далее - матрица) в сборе показана на фиг. 1. Матрица состоит из рамы , по меньшей мере двух сменных модулей (2) с присоединенному к каждому модулю электродами и соответствующих по меньшей двух оснований (3) сменных модулей, установленных на направляющие рамы матрицы.
Рама представляет собой два параллельных элемента (1), которые скреплены с помощью цилиндрических направляющих (7). Рама матрицы изготовлена из легкосплавных материалов для обеспечения прочности и минимизации массы и выполняет функцию опоры-направляющей для оснований (3) сменных модулей и непосредственно для самих сменных модулей (2).
Рама матрицы имеет в целом прямоугольную форму. Два параллельных элемента (1) являются идентичными, и каждый из них может быть выполнен как п-образная деталь или деталь, имеющая форму типа бумеранг (далее - опоры «бумеранг»), или деталь, имеющая любую другую изогнутую форму, при которой концы детали с обеих сторон приподняты на некоторую высоту в отношении основной части.
Между параллельными элементами (1) располагаются две цилиндрические направляющие (7), проходящие через отверстия в обоих элементах (1) в области изгиба. По направляющим (7) перемещаются основания (3) сменных модулей электродов.
К раме крепятся опоры (4). В частности, к каждому из параллельных элементов (1) закреплено по две опоры (4) с помощью шарнирного соединения (5). Входящие в состав матрицы четыре опоры (4) имеют подложку из медицинского силикона для максимально плотного нетравмирующего прилегания к телу пациента, в частности, к спине пациента. Опоры (4) матрицы самоустанавливаются (когда прикладывают матрицу к спине пациента, опоры занимают единственное возможное положение, когда они плотно прижаты к спине) за счет шарнирного соединения (5) и обеспечивают надежное позиционирование матрицы на теле пациента. В предпочтительном варианте осуществления изобретения свободное угловое перемещение шарнирного соединения (5) может быть в пределах телесного угла 15 угл. градусов. Каждый из опор «бумеранг» (1), входящая в состав рамы, имеет отверстия (6) по углам, которые предназначены для крепления пояса или ремней, притягивающих матрицу к телу пациента. Элемент (1) может иметь любую другую форму, которая приподнимает места крепления пояса или ремней над общей конструкцией рамы.
Основания (3) сменных модулей можно перемещать по направляющим (7), используя ручки (8) и фиксировать на направляющих, используя фиксаторы (9). В изображенном варианте изобретения на фиг. 1 фиксатор - это механический зажим на основе эксцентрического кулачка, который за счет сил трения возникающих в месте контакта кулачка и направляющей, удерживает основания модулей в заданном положении. При нажатии на фиксаторы (9) поверхность фиксаторов выходит из зацепления паза направляющей и позволяет перемещать основания (3) сменных модулей вдоль направляющих (7).
В основаниях (3) сменных модулей размещают сменные модули (2), фиксируя их там с помощью по меньшей мере четырех кнопок-защелок (10). Кнопки-защелки (10) сменных модулей подпружинены и позволяют быстро заменять модули (2) в основаниях (3), когда матрица находится на пациенте (при необходимости, например, поменять кнопочный электрод). Электроды присоединяются к каждому сменному модулю (2). Модуль (2) с электродами вставляется в раму матрицы. Если электрод оказался некачественным, что стало ясно после того, как начали стимуляцию, то необходимо извлечь модуль (2) из матрицы и заменить электрод.
Для удержания и позиционирования на теле пациента электродов в каждом из сменных модулей размещено по меньшей мере три телескопических держателя электрода (11, 12). Ручка-фиксатор (13) телескопического держателя электрода закрепляет продольное положения телескопического держателя относительно сменного модуля (2). Шток (14) телескопического держателя электрода имеет индикатор глубины погружения электрода под сменный модуль (2) и может использоваться для контроля прижатия электрода к телу пациента при установке матрицы.
Один из телескопических держателей электродов (11) зафиксирован в пределах одного из сменных модулей (2). Согласно изображенному варианту осуществления изобретения на фиг. 1-5, неподвижный телескопический держатель электрода (11) является центральным в верхнем сменном модуле (2), представляя собой «нулевую координату». Неподвижный телескопический держатель электрод (11) размещают, например, в случае использования электродной матрицы для регуляции двигательной активности, между позвонками Т11-Т12, над спинным мозгом. Фиксируют матрицу и подгоняют под анатомические особенности пациента положения всех остальных электродов, изменяя их продольное положение относительно друг друга и каждого из сменных модулей (2) и изменяя их глубину для контроля прижатия к телу пациента. При этом электродную матрицу возможно фиксировать в любом месте над позвоночником в пределах спины (грудной и поясничный отделы позвоночника/спинного мозга) в зависимости от ее применения.
Остальные пять телескопических держателей электродов (12) согласно предпочтительному варианту осуществления изобретения могут перемещаться по сменному модулю в пределах прорезей-направляющих (15). Такое перемещение позволяет точно позиционировать электроды, учитывая индивидуальные анатомические особенности пациента.
Каждый из телескопических держателей (11, 12) электродов на торце, направленном к спине пациента, имеют кнопочное крепление для фиксации съемных электродов с ответным кнопочным разъемом (16) (фиг.4). Держатели соединяют электроды со стимулятором проводниками (17) (частично проводник схематично показан на фиг. 4).
Каждый используемый в матрице электрод представляет собой кнопочный электрод круглой формы, диаметром 1,5 см - 2,5 см (или 0,5 дюйм - 1 дюйм), с токопроводящим адгезивным слоем. В качестве неограничивающего примера, например, могут быть использованы одноразовые электроды для ЭКГ регистрации или круглые стимуляционные многоразовые электроды типа Beurer 66102.
Процесс сборки матрицы перед использованием заключается в следующем.
1. Прикрепляют кнопочные электроды (16) к телескопическим держателям электродов (11, 12).
2. Сменные модули (2) устанавливают в основания сменных модулей (3) так, чтобы модуль с неподвижным держателем электрода (11) находился в верхнем основании сменного модуля (как на фиг. 1, 2, 4). После чего сменные модули фиксируют с помощью кнопок-защелок (10).
Расположение собранной матрицы (18) на пациенте продемонстрировано на фиг.5. Вблизи матрицы, на ремнях, расположен внешний стимулятор нейропротеза (20).
Возможный порядок позиционирования электродов в случае неограничивающего примера применения электродной матрицы для восстановления двигательной активности представлен ниже.
1. Неподвижный телескопический держатель электрода (11) закрепить в выбранной позиции, например, между позвонками T11-T12.
2. Подвижные телескопические держатели электродов (12) верхнего сменного модуля (2) располагают над корешками спинного мозга между позвонками T11-T12 и фиксируют с помощью ручек-фиксаторов (13).
3. Подвижные телескопические держатели электродов (12) нижнего сменного модуля (2) располагают между позвонками L1-L2 и над корешками спинного мозга между позвонками L1-L2 и фиксируют с помощью ручек-фиксаторов (13).
4. Матрицу притягивают к спине пациента и подгоняют по месту с помощью пояса, бандажа, эластичных ремней и т.п. (19).
Зафиксировав матрицу на спине пациента, дополнительную регулировку положения каждого из электродов (12) можно осуществлять, ослабив ручку-фиксатор электрода (13), переместив его в пределах прорези (15). Используя шток телескопического держателя электрода (14), электрод можно оттянуть на время от тела пациента, когда это необходимо (например, положить токопроводящий гель под электрод, если сопротивление кожи большое). Шток держателя электрода (14) и прорези (15) имеют шкалы. Это позволяет документировать расположение каждого из электродов на теле пациента и, при повторном использовании матрицы на пациенте, воспроизвести координаты расположения электродов, готовя матрицу к процедуре, что уменьшит длительность подготовки матрицы к стимуляции с участием пациента и сбережет физические ресурсы пациента для реабилитационной процедуры.
В некоторых вариантах осуществления изобретения, когда электродная матрица применяется для тяжелых пациентов, которые не могут самостоятельно стоять и/или ходить, матрицу снабжают крышкой (28) с целью предохранения выступающих элементов от ремней подвесной системы, на которую закрепляют пациента в некоторых тренажерах, обеспечивающих ходьбу. Крышка крепится к защитной раме-накладке, которая прикреплена к раме электродной матрицы. Один из неограничивающих примеров выполнения защитной рамы-накладки представлен на фиг. 7. Крышка (28) состоит из четырех параллельных цилиндрических осей, прикрепленных ортогонально к двум параллельным пластинам, которые имеют присоединительные пазы. Данные пазы входят в закрепление с втулками основания матрицы и осуществляют верное ее пространственное расположение и сопряжение с основанием матрицы. Фиксацию крышки осуществляет элементы подвесной система поддержки пациента за счет прижатия крышки к основанию матрицы.
Матрица может быть использована во всех случаях, когда необходима неинвазивная стимуляция спинного мозга и корешков спинного мозга на нескольких уровнях в диапазоне сегментов спинного мозга T1-S1, в том числе, когда начало и конец стимуляции надо согласовать с неким событием (начало движения конечности, начало записи сигнала внешним регистрирующим устройством). Матрицу можно фиксировать в любом месте над позвоночником в пределах спины (грудной и поясничный отделы позвоночника/спинного мозга).
Использование матрицы для стимуляции спинного мозга.
Например, предлагаемая в настоящем изобретении электродная матрица может быть использована для реабилитации пациента с помощью восстановления движений в составе экзоскелета, когда проводят чрескожную электрическую стимуляцию спинного мозга на нескольких уровнях спинного мозга, зависящую от определенной фазы движения активного экзоскелета или ног пациента. Так, электрическую стимуляцию спинного мозга осуществляют в районе грудных позвонков T11, Т12 в зависимости от определенной фазы движения активного экзоскелета. В одной из фаз движения активного экзоскелета неподвижный телескопический держатель электрода (11) матрицы может быть расположен на уровне Т11-Т12. При этом, если, например, надо будет восстанавливать функцию поддержания вертикальной стойки, то неподвижный телескопический держатель электрода (11) матрицы может быть расположен между L1-L2, а остальные электроды матрицы перемещают в пределах каждого сменного модуля матрицы и раздвигают сменные модули матрицы таким образом, чтобы стимулировать корешки спинного мозга на уровне L1-L2 справа или слева, если пациент начинает заваливаться вправо или влево.
Фаза движения определяется с помощью датчиков определения текущего положения составных элементов экзоскелета. Примером такого экзоскелета может служить, например, экзоскелет, раскрытый в RU2016144450 A. При этом, возможны варианты решений, когда чрескожная стимуляция в экзосклете зависит от определенной фазы движения ног пациента, и когда фазы движения ног определяют по датчикам, расположенным на ногах (RU 2020101607 А).
Другим альтернативным вариантом применения электродной матрицы является ее использование в системе для поддержания дыхательной функции. В уровне техники известны технические решения, которые позволяют осуществлять нейростимуляцию пациентов, подключенных к аппаратам искусственной вентиляции легких (например, RU2750236 C1). Электростимуляцию используют для активации межреберных мышц, диафрагмы, абдоминальных мышц путем стимуляции корешков спинного мозга и сегментов грудного отдела спинного мозга с различными параметрами импульсов для каждого типа мышц. При этом матрица может быть расположена следующим образом: неподвижный телескопический держатель электрода (11) матрицы зафиксирован между позвонками Т3-Т4, или Т4-Т5, или Т5-Т6, или Т6-Т7, или Т7-Т8, а остальные электроды расположены на уровне выше или ниже в зависимости от того, какую функцию (вдох или выдох) необходимо в первую очередь активировать. Вдох - уровни выше, выдох - уровни ниже.
Также электродная матрица может быть использована для одновременного воздействия на две и более физиологических систем человека, центры регуляции которых расположены в спинном мозге. Так, известна проблема резкого уменьшения артериального давления при вертикализации пациентов с травмой спинного мозга (ортостатическая гипотензия). Стимуляция на уровне поясничного утолщения, зависящая от фаз движения, обеспечит переход из положения сидя в положение стоя и устойчивую вертикальную позу у таких пациентов (Sayenko D. G. et al. Self-assisted standing enabled by non-invasive spinal stimulation after spinal cord injury //Journal of neurotrauma. - 2019. - Т. 36. - №. 9. - С. 1435-1450), а стимуляция в среднегрудном отделе позвоночника предотвратит резкое падение артериального давления и обморок (Phillips A. A. et al. An autonomic neuroprosthesis: noninvasive electrical spinal cord stimulation restores autonomic cardiovascular function in individuals with spinal cord injury //Journal of neurotrauma. - 2018. - Т. 35. - №. 3. - С. 446-451). Для регуляции функций кардиоваскулярной системы для предотвращения обмороков при вертикализации спинальных пациентов неподвижный телескопический держатель электрода (11) матрицы может фиксироваться на уровне Т7. Если решается иная кардиологическая проблема (например, аритмия), то неподвижный телескопический держатель электрода (11) матрицы может располагаться на уровне Т1 или Т5.
Матрица может быть использована при диагностике функционального состояния вегетативной нервной системы, когда осуществляют стимуляцию спинного мозга электрическим током и регистрируют вызванные кожные вегетативные потенциалы с электродов, расположенных в тех сегментах спинного мозга, в которых находятся центры регуляции той или иной вегетативной системы. Один из подобных способов диагностики вегетативной нервной системы раскрыт в RU2201710 C1. Для этого регистрируют вызванные кожные вегетативные потенциалы с электродов, расположенных по паравертебральным линиям с двух сторон от линии остистых отростков в межреберных промежутках на уровне позвонков T6-Т11 или ниже на уровне Т12-S1.
Поражение симпатического ствола диагностируют при увеличении амплитуды потенциала, снижении скорости проведения и уменьшении латентного периода потенциала относительно нормы. Поражение спинно-мозговых корешков диагностируют при увеличении латентного периода потенциала, снижении скорости проведения и уменьшении амплитуды потенциала. Полное нарушение проводимости сегментарного нерва диагностируют при отсутствии вызванного кожного потенциала на исследуемом уровне.
Так как в уровне техники продемонстрировано, что механизмы воздействия на спинной мозг при эпидуральной и при чрескожной электрической стимуляции одинаковые (Gerasimenko et al., Transcutaneous electrical spinal-cord stimulation in humans. // Ann. Phys. Rehabil. Med. - 2015. - V. 58, N4. - P. 225-231), то электродная матрица может применяться в тех случаях, когда сейчас применяется инвазивная (эпидуральная) электрическая стимуляция спинного мозга на нескольких уровнях. Например, матрица может быть использована для купирования спастического синдрома, обусловленного нарушением сегментарного аппарата спинного мозга в соответствии с RU2038099 C1. Для этого неподвижный телескопический держатель электрода (11) матрицы может фиксироваться на уровне позвонков T12-L1. Этот способ включает дозированное введение лекарственных препаратов в эпидуральное пространство на уровне поясничного утолщения и осуществляют стимуляцию спинного мозга выше и ниже поясничного утолщения.
Ниже приведен неограничивающий пример электродной матрицы согласно настоящему изобретению для восстановления локомоторных функций пациента.
Пример. Использование матрицы в реабилитации двигательных функций.
Целью двигательной реабилитации с использованием матрицы в составе нейропротеза (RU2725090) является улучшение навыка ходьбы, увеличение подвижности в суставах нижних конечностях, улучшение координации.
Реабилитационная процедура с использованием матрицы в составе нейропротеза может состоять из двух частей: тренировка на беговой дорожке и тренировка на неподвижной ровной твердой поверхности (например, ходьба по полу). Каждая часть процедуры может быть примерно одинаковой длительности. Общая длительность тренировки от 20 до 60 минут. Длительность зависит от общей тренированности/утомляемости, самочувствия пациента (уровень нагрузки - умеренный). Длительность тренировки для каждого пациента может увеличиваться от начала реабилитационного периода к его концу. Пациент во время процедуры может использовать привычные для него технические средства реабилитации (ортезы, трости, ходунки, костыли и т.п.). Возможно 12 процедур на реабилитационный курс. Возможные режимы: 20 мин для первых 1-3 процедур, увеличение длительности 30 мин для 4-6 процедур и до 40-60 мин для 7-12 процедур. После 1-2-дневного перерыва между процедурами длительность тренировки может быть уменьшена.
Перед началом тренировки накожно, над позвоночником, размещают матрицу электродов (фиг.5). Применяют одноразовые или индивидуальные для каждого пациента электроды с токопроводящей самоклеящейся поверхностью с кнопочным разъемом.
Используя возможности матрицы регулировать положение электродов с учетом анатомических особенностей пациента, располагают и закрепляют электроды следующим образом (фиг.6):
• по вертикальной осевой линии позвоночника между позвонками Т11 (21) и Т12 (22) - электрод (25), соединенный с неподвижным телескопическим держателем электрода (11),
• на 1-3 см латерально с пораженной стороны и вниз от межпозвоночной зоны между позвонками Т11 (21) и Т12 (22) - электрод (26), соединенный с подвижным телескопическим держателем электрода (12),
• на 1-3 см латерально с пораженной стороны и вниз от межпозвоночной зоны между позвонками L1 (23) и L2 (24) - электрод (27), соединенный с подвижным телескопическим держателем электрода (12).
В результате электрод (25) должен находиться над спинным мозгом, электроды (26) и (27) - над дорзальными корешками спинного мозга. Электроды на спине являются катодами. Два анода располагают над гребнями подвздошных костей справа и слева или один анод - на пораженной стороне над гребнем подвздошной кости. Аноды общие для всех катодов.
После установки матрицы электродов их подсоединяют к стимулятору для чрескожной электрической стимуляции (20) с помощью проводов (17).
Интенсивность стимуляции зависит от возбудимости спинальных нейронных сетей спинного мозга и от уровня болевой чувствительности пациента. Подбор интенсивности стимуляции осуществляет специалист, проводящий процедуру, сразу после начала тренировки (ходьбы пациента по полу или по беговой дорожке с комфортной скоростью). Интенсивность тока при избранной частоте стимуляции должна быть на уровне парастезии (ощущения покалывания, или жжения, или легкой болезненности, или тяжести в области катода). Или интенсивность на 5-10% меньше интенсивности парастезии. Интенсивность стимуляции в движении не должна вызывать неприятных или болезненных ощущений. В процессе тренировки возможно постепенное увеличение интенсивности стимуляции по мере адаптации пациента к ходьбе и текущей интенсивности стимуляции. Эти величины интенсивности тока должны находиться в диапазоне токов, вызывающих двигательные ответы мышц нижних конечностей на одиночные прямоугольные импульсы длительностью 1 мсек, которые определяют перед началом реабилитационного курса.
Частота стимуляции на уровне T11-T12 позвонков, электрод (25) - около 30 Гц. Частота стимуляции на уровне корешков спинного мозга в районе позвонка T12, электрод (26) - около 40 Гц, в районе позвонка L2, электрод (27) - около 15 Гц.
Форма импульса - биполярная, заполненная частотой ~5-10 кГц, или монополярная, заполненная частотой ~5-10 кГц.
В процессе тренировки интенсивность тока на электродах (26) и (27) равна нулю, если пациент стоит. При ходьбе каналы стимулятора, подключенные к этим электродам, включаются. На латеральный электрод (26) в области Т12 позвонка поступает ток в фазе переноса пораженной ноги, или в фазе опоры условно здоровой ноги, или во время опоры на средство технической реабилитации (трость, костыль и т.п.), которое пациент держит в условно здоровой руке. На латеральный электрод (27) в области позвонка L2 - в фазе опоры пораженной ноги, или в фазе переноса условно здоровой ноги, или отрыва от опоры средства технической реабилитации. Сигнал о фазе шага и об опоре/переносе средства технической реабилитации стимулятор получает от датчиков движения, которые перед процедурой закрепляют на ногах пациента и/или на средстве технической реабилитации (RU2725090; Гришин А.А., Боброва Е.В., Решетникова В.В., Мошонкина Т.Р., Герасименко Ю.П. Система детектирования фаз шагательного цикла и стимуляции спинного мозга как инструмент управления локомоцией человека // Медицинская техника. - 2020. - №5. - с. 10-14.)
Реабилитационные процедуры проходят в присутствии специалиста. Специалист следит за качеством ходьбы пациента, дает пациенту рекомендации для корректировки движений с целью увеличить устойчивость при ходьбе, специалист уменьшает или увеличивает скорость движения беговой дорожки. Возможны тренировки на беговой дорожке с частичной поддержкой веса тела (до 50%).
Пациент может самостоятельно использовать нейропротез после того, как специалист выставит и зафиксирует на матрице позиции электродов и подберет оптимальные для пациента интенсивности стимуляции и режим работы нейропротеза, обучит пациента или его близких управлять нейропротезом.
Клинические случаи
Пациент 1. 78 лет, мужчина, последствия острого нарушение мозгового кровообращения в правой среднемозговой артерии 1 год реабилитации. Левосторонний гемипарез. Левосторонняя гемигипостезия.
Проведена реабилитационная процедура с использованием нейропротеза, направленная на восстановление функции ходьбы. Катоды (∅ 2 см) зафиксировали по средней линии позвоночника между T11-T12 позвонками, левее и ниже на ~2,5 см от центра этого электрода, над корешком спинного мозга и левее и ниже на ~2 см от средней вертикальной линии между позвонками L1-L2. Аноды размером 5*10 см разместили над гребнями подвздошных костей справа и слева. Пациент ходил по беговой дорожке 25 мин с 4 остановками для отдыха на 1-2 мин. Скорость беговой дорожке подбирали так, чтобы пациент самостоятельно мог идти по движущейся ленте, не приближаясь к передней стойке дорожки и не откатываясь назад. Скорость в процессе процедуры меняли, чтобы ходьба была равномерной и комфортной для пациента. Стартовая комфортная скорость составила 0,2 м/сек (0,74 км/ч). В процессе ходьбы с нейропротезом скорость дорожки была увеличена до 0,3 м/сек (0,8 км/ч).
Интенсивность стимуляции по всем электродам ~50-70 мА. Частота стимуляции на уровне T11-T12 позвонков, по осевой линии, 30 Гц. Частота стимуляции на уровне корешков спинного мозга в районе позвонка T11-T12 40 Гц, в районе позвонка L1-L2 20 Гц.
Контроль результатов процедуры проводили на беговой дорожке. Пациент ходил без стимуляции по дорожке с комфортной скоростью ~1 мин непосредственно перед началом и сразу после окончания реабилитационной процедуры. Активность мышц ног и кинематические характеристики ходьбы регистрировали с помощью комплекса «Стэдис» (ООО «Нейрософт»). Перед началом первого исследования на теле пациента устанавливали на эластичных лентах 5 сенсоров, в состав которых входят акселерометры, которые регистрируют перемещение в пространстве звеньев тела, на которых они закреплены, а также усилители биологического сигнала для регистрации электрической активности мышц (электромиограммы, ЭМГ). Сенсоры устанавливали на спине, в области поясницы, а также билатерально на голень и бедро. Регистрировали ЭМГ следующих мышц: mm. tibialis anterior, gastrocnemius lateralis, quadriceps femoris (rectus femoris), biceps femoris (длинную и короткую головки). Для этого на перечисленные мышц крепили поверхностные одноразовые электроды с адгезивным слоем ∅ 35 мм (Kendall, Н135).
Абсолютные значения измеренных параметров до и после проведения одной реабилитационной процедуры представлены в Таблице 1. Относительные изменения представлены на фиг. 8, где 100% соответствуют величине параметра перед реабилитационной процедурой.
После процедуры у пациента увеличилась скорость ходьбы на 8% (фиг. 8, Д), что также проявилось в уменьшении длительности цикла шага на 6% (фиг. 8, А). Длина двойного шага увеличилась на 6% (фиг. 8, Г). При увеличении скорости ходьбы активность всех регистрируемых мышц заметно уменьшилась (от 3% до 47%, фиг. 8К-Н), что демонстрирует уменьшение метаболической стоимости локомоции и демонстрирует, что реабилитационная процедура оптимизировала нервную регуляцию мышц ног.
Пациент 2. 68 лет, мужчина, Последствия инфаркта головного мозга в бассейне правой средней мозговой артерии, произошедший за 8 месяцев до процедуры. Атеросклероз брахиоцефальных артерий со стенозированием, справа каротидная бифуркация на 30%. S-образная извитость обеих внутренних сонных артерий. Левосторонний гемипарез. Левосторонняя гемигипостезия. Вестибуло-атактический и астенический синдромы. Фоновое заболевание: Гипертоническая болезнь 3 степени.
Проведена реабилитационная процедура с использованием нейропротеза, направленная на восстановление функции ходьбы. Расположение стимулирующих электродов и режим стимуляции такие же, как у Пациента 1 Длительность ходьбы по беговой дорожке со стимуляцией 20 мин со скоростью 0,4 м/с (1,41 км/ч).
Контроль параметров ходьбы проводили на твердой поверхности, на полу - пациент ходил без стимуляции в комнате, где проводили реабилитацию, непосредственно перед началом и сразу после окончания процедуры. Пациент должен был идти с комфортной для него скоростью в течение ~1 мин, пройденный путь составил в обоих случаях ~30 м. Активность мышц ног и кинематические характеристики ходьбы регистрировали также, как и в случае с пациентом 1.
Абсолютные значения измеренных параметров до и после проведения одной реабилитационной процедуры представлены в Таблице 1, относительные изменения - на фиг.8.
После процедуры у пациента увеличилась скорость ходьбы на 10% (фиг. 9, Д), что также проявилось в уменьшении длительности цикла шага на 7% (фиг. 9, А). Длина двойного шага увеличилась на 6% (фиг. 9, Г). Увеличилась амплитуда движений в тазобедренном и коленном суставах с пораженной стороны (фиг. 9, Ж, З).
П1, П2 - пациенты, Л - слева, П - справа, ТЗБ - тазобедренный сустав, КЛН - коленный сустав, ГЛН - голеностопный сустав, TA - m. tibialis anterior (передняя большеберцовая мышца), GL - m. gastrocnemius lateralis (латеральная головка икроножной мышцы), RF - m. rectus femoris (прямая мышца бедра), BF - m. biceps femoris (двуглавая мышца бедра).
Таким образом, показано, что использование электродной матрицы согласно настоящему изобретению обеспечивает надежную и точную фиксацию на спине пациента набора электродов для стимуляции спинного мозга и корешков спинного мозга, а также и осуществление чрескожной мультисегментарной (многоуровневой) электрической стимуляции структур спинного мозга во время движений по определенному алгоритму.
Несмотря на то, что изобретение описано со ссылкой на раскрываемые варианты воплощения, для специалистов в данной области должно быть очевидно, что конкретные подробно описанные исследования приведены лишь в целях иллюстрирования настоящего изобретения, и их не следует рассматривать как каким-либо образом ограничивающие объем изобретения. Должно быть понятно, что возможно осуществление различных модификаций без отступления от сути настоящего изобретения.
Таблица 1
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ РЕГУЛЯЦИИ И ВОССТАНОВЛЕНИЯ САМОСТОЯТЕЛЬНОЙ ХОДЬБЫ У ПАЦИЕНТОВ С ДВИГАТЕЛЬНОЙ ПАТОЛОГИЕЙ РАЗЛИЧНОГО ГЕНЕЗА | 2019 |
|
RU2725090C1 |
| Способ и устройство контроля положения головы пациента и его коррекции путем неинвазивной нейростимуляции | 2022 |
|
RU2822711C2 |
| УСТРОЙСТВО ДЛЯ НЕИНВАЗИВНОЙ ЭЛЕКТРИЧЕСКОЙ СТИМУЛЯЦИИ СПИННОГО МОЗГА | 2015 |
|
RU2627359C2 |
| СПОСОБ МЕДИЦИНСКОЙ РЕАБИЛИТАЦИИ ПАЦИЕНТОВ СО СПАСТИЧЕСКОЙ ПАРАПЛЕГИЕЙ ВСЛЕДСТВИЕ ПОВРЕЖДЕНИЯ СПИННОГО МОЗГА НА ГРУДНОМ И ГРУДО-ПОЯСНИЧНОМ УРОВНЕ | 2023 |
|
RU2821772C1 |
| СПОСОБ НАКОЖНОЙ ЭЛЕКТРОСТИМУЛЯЦИИ СПИННОГО МОЗГА | 2012 |
|
RU2529471C2 |
| СПОСОБ РЕАБИЛИТАЦИИ ПАЦИЕНТОВ ПОСЛЕ ТРАВМ И ПОРАЖЕНИЙ ГРУДНОГО И ПОЯСНИЧНОГО ОТДЕЛОВ ПОЗВОНОЧНИКА | 2017 |
|
RU2650210C1 |
| Способ коррекции локомоторных функций человека после нарушения церебрального кровообращения ишемического генеза | 2020 |
|
RU2743222C1 |
| СПОСОБ НАКОЖНОЙ ЭЛЕКТРОСТИМУЛЯЦИИ СПИННОГО МОЗГА | 2014 |
|
RU2545440C1 |
| СПОСОБ РЕГУЛЯЦИИ ВИСЦЕРАЛЬНЫХ ФУНКЦИЙ ПАЦИЕНТА ПУТЕМ НЕИНВАЗИВНОЙ СТИМУЛЯЦИИ СПИННОГО МОЗГА | 2016 |
|
RU2642384C1 |
| КОСТЮМ ДЛЯ НЕЙРОМЫШЕЧНОЙ И СПИНАЛЬНОЙ ЭЛЕКТРИЧЕСКОЙ СТИМУЛЯЦИИ | 2017 |
|
RU2654285C1 |



Группа изобретений относится к медицине, а именно к неинвазивной электродной матрице для мультисегментарной стимуляции спинного мозга, и способу ее применения. Электродная матрица содержит раму с направляющими (1), два сменных модуля, два основания сменных модулей. Рама с направляющими выполнена с возможностью плотного прилегания к спине пациента. В каждом из сменных модулей установлены телескопические держатели электродов для стимуляции спинного мозга. При этом электроды закреплены на торцах телескопических держателей, направленных к спине пациента, и являются съемными. Основания сменных модулей выполнены с возможностью перемещения вдоль направляющих рамы и фиксации на направляющих рамы в заданном положении. Каждый из сменных модулей размещен в соответствующем основании. Один из телескопических держателей (11) является неподвижным, а остальные подвижными (12) и имеют возможность продольного и вертикального перемещения относительно сменного модуля, в котором они установлены, так чтобы электроды находились в контакте с кожей пациента. Неинвазивную электродную матрицу с использованием чрескожной электрической стимуляции спинного мозга применяют для реабилитации двигательных функций пациента, для модуляции функций внутренних органов пациента, для диагностики функционального состояния вегетативной нервной системы пациента, для купирования спастического синдрома, обусловленного нарушением сегментарного аппарата спинного мозга. За счет особенностей конструкции матрицы электродов для осуществления чрескожного мультисегментарного стимуляционного электрического воздействия обеспечивается возможность повторять индивидуальные особенности формы спины пациента при проведении реабилитационной сессии, в том числе во время движений, а также повышение износостойкости матрицы. 2 н. и 10 з.п. ф-лы, 9 ил., 1 табл.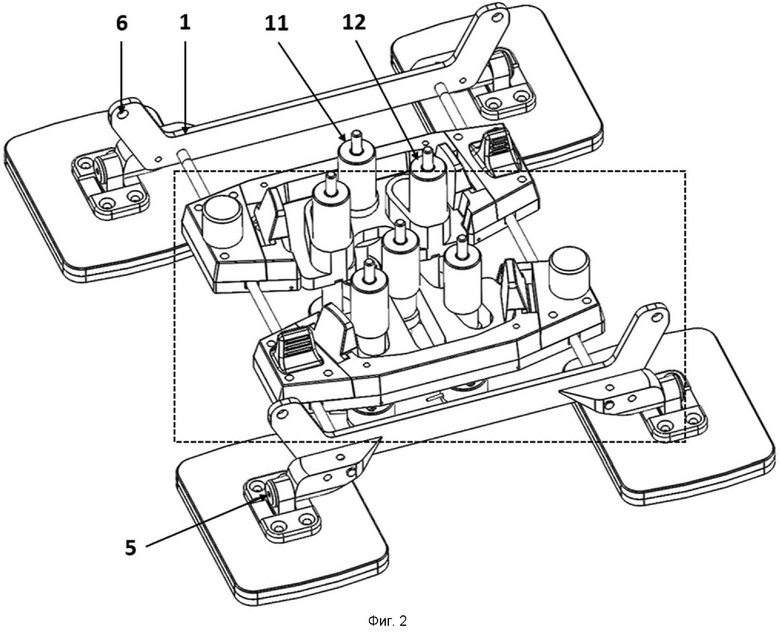
1. Неинвазивная электродная матрица для мультисегментарной стимуляции спинного мозга, содержащая:
раму с направляющими, выполненную с возможностью плотного прилегания к спине пациента,
по меньшей мере два сменных модуля с установленными в каждом из них телескопическими держателями электродов для стимуляции спинного мозга, причем указанные электроды закреплены на торцах телескопических держателей, направленных к спине пациента, и являются съемными,
по меньшей мере два основания сменных модулей, выполненных с возможностью перемещения вдоль направляющих рамы и фиксации на направляющих рамы в заданном положении,
причем
каждый из сменных модулей размещен в соответствующем основании, один из телескопических держателей является неподвижным, а остальные подвижные телескопические держатели имеют возможность продольного и вертикального перемещения относительно сменного модуля, в котором они установлены, таким образом, чтобы электроды находились в контакте с кожей пациента.
2. Неинвазивная электродная матрица по п. 1, в которой рама выполнена в виде двух параллельно скрепленных элементов, имеющих изогнутую форму типа бумеранга, между которыми располагаются две направляющие, каждая из которых проходит через отверстия в обоих элементах в области изгиба.
3. Неинвазивная электродная матрица по п. 2, в которой на обоих концах каждого из элементов закреплены опоры через шарнирные соединения.
4. Неинвазивная электродная матрица по п. 3, в которой опоры имеют подложку из медицинского силикона для плотного прилегания к телу пациента.
5. Неинвазивная электродная матрица по п. 2, в которой параллельные элементы рамы имеют отверстия для крепления средств крепления матрицы электродов к телу пациента, выбранных из следующего: пояс, бандаж, эластичные ремни.
6. Неинвазивная электродная матрица по п. 1, в которой каждый сменный модуль фиксируется в основании сменного модуля посредством подпружиненных кнопок-защелок, расположенных с каждой стороны сменного модуля.
7. Неинвазивная электродная матрица по п. 1, в которой в каждом из сменных модулей установлены по меньшей мере три телескопических держателя электродов.
8. Неинвазивная электродная матрица по п. 1, в которой сменный модуль имеет пазы для размещения, продольного перемещения вдоль них подвижных телескопических держателей электродов и вертикального перемещения относительно них подвижных телескопических держателей электродов.
9. Неинвазивная электродная матрица по п. 1, в которой каждый телескопический держатель имеет ручку-фиксатор для закрепления продольного положения держателя относительно сменного модуля и шток для регулирования вертикального перемещения держателя относительно сменного модуля.
10. Неинвазивная электродная матрица по п. 1, в которой на торцах телескопических держателей электродов выполнено кнопочное крепление для фиксации съемных электродов с ответным кнопочным разъемом.
11. Неинвазивная электродная матрица по п. 1, в которой съемным электродом является кнопочный электрод круглой формы с токопроводящим адгезивным слоем.
12. Применение неинвазивной электродной матрицы по п. 1 с использованием чрескожной электрической стимуляции спинного мозга для реабилитации двигательных функций пациента, и/или для модуляции функций внутренних органов пациента, и/или для диагностики функционального состояния вегетативной нервной системы пациента, и/или для купирования спастического синдрома, обусловленного нарушением сегментарного аппарата спинного мозга.
| СПОСОБ НАКОЖНОЙ ЭЛЕКТРОСТИМУЛЯЦИИ СПИННОГО МОЗГА | 2014 |
|
RU2545440C1 |
| US 2011208029 A1, 25.08.2011 | |||
| US 2017065814 A1, 09.03.2017 | |||
| WO 2019073003 A1, 18.04.2019 | |||
| US 2017027803 A1, 02.02.2017. | |||
Авторы
Даты
2022-08-12—Публикация
2021-09-07—Подача