Изобретение относится к области медицины, ветеринарии, фармации и фармакологии, а именно к седативному средству, действующим веществом в котором могут являться метиловые эфиры замещенных 3-ароил-4-oксо-1,4-дигидрохинолин-2-карбоновых кислот общей формулы 1, их соли или композиции на их основе и которое может найти применение для лечения людей и животных в качестве седативного средства.

Технический результат: получены соединения, обладающие седативным действием на основании результатов теста "открытое поле", что предполагает возможность его использования в медицине в качестве седативного средства.
В литературе имеются сведения о синтезе, физико-химических, спектральных характеристиках соединения, представленного формулой 1, а именно 1а [Ботева А.А. дис. … канд.фарм.наук. Пер.гос.фарм.академия, Пермь, 2008], описаны его анальгетические свойства и токсичность [Патент РФ 2634618 С1]. Однако в литературе отсутствую сведения о влиянии данных веществ на центральную нервную систему (ЦНС).
Центральным структурным фрагментом в соединениях общей формулы 1, применение которых является объектом данного изобретения, выступает 4-хинолоновый фрагмент, содержащий заместители в положениях 2 и 3 и не содержащий заместителя у атома азота.
Применяемые в медицине 4-хинолоны под названием фторхинолоны (розоксацин, налидиксовая и оксолиновая кислоты, ципрофлоксацин, эноксацин, норфлоксаци) имеют побочное действие, а именно влияние на ЦНС. Механизм этого действия может включать важнейший тормозной нейромедиатор центральной нервной системы – γ-аминомасляную кислоту (ГАМК) [P. R. Dodd , L. P. Davies, W. E. Watson, B. Nielsen, J. A. Dyer, L. S. Wong, G. A. Johnston. Pharmacol Toxicol. 1989; 64 (5): 404-11].
Из литературы известны 4-хинолоны, обладающие экспериментально подтвержденным влиянием на ЦНС, или такие, для которых можно предположить подобное влияние на основании действия этих веществ на соответствующие биологические мишени. Так, например: 6-замещенные пропиловые и бутиловые эфиры и амиды 4-oксо-1,4-дигидрохинолин-3-карбоновых кислот 2 являются высокоаффинными лигандами бензодиазепинового сайта рецепторов γ-аминомасляной кислоты, которая является одним из основных тормозных нейротрансмиттеров в центральной нервной системе и оказывает свое физиологическое действие путем связывания с тремя различными типами рецепторов в нейрональной мембране [E. Lager, P. Andersson, J. Nilsson, I. Pettersson, E. Ø. Nielsen, M. Nielsen, O. Sterner, T. Liljefors. J. Med. Chem. 2006, 49, 2526-2533]. Несколько соединений тестировали на подтипах рецепторов ГАМК – α1β2γ2S и α3β2γ2S. Были найдены два соединения, (2: Х=О, R=Et, Bz, R1 = i-C5H11, Et), проявляющие селективность к рецептору α1β2γ2S. Указанный рецептор отвечает за такие физиологические эффекты, как седация, анксиолитическая активность, мышечная релаксация и пр.
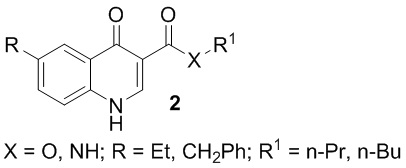
Исследования проводились на кортикальных мембранах крыс и на суспензии клеток HEK 293. Константа Ki находится в пределах 0.048-0.17 нмоль.
(4-Морфолин-4-ил-фенил)амиды 4-oксo-1,4-дигидрохинолин2-карбоновых кислот 3, содержащие в положении 8 пяти-, шести- или семичленный цикл с одним или двумя атомами азота, являются мощными антагонистами 5-гидрокситриптаминовых рецепторов (5HT1), а именно 5НТ1В рецепторов [C. L. Horchler, J. P. McCauley, Jr., J. E. Hall, D. H. Snyder, W. C. Moore, T. J. Hudzik, M. J. Chapdelaine. Bioorganic & Medicinal Chemistry 15 (2007) 939–950]. Данный подтип рецепторов отвечает за психические расстройства, связанные с серотонинергической нейротрансмиссией, такие как депрессия, тревога. Предполагается, что антагонисты терминальных авторецепторов 5HT1 (5HT1B / 1D) блокируют терминальные рецепторы 5HT1B, тем самым влияя на высвобождение 5-гидрокситриптамина и на увеличение его передачи на синапсы, что в конечном итоге обеспечивает быструю клиническую антидепрессивную активность [Briley, M.; Moret, C. Clin. Neuropharmacology 1993, 16, 387–400; Chenu, F.; Dailly, E.; Bourin, M. Drug Dev. Res. 2005, 65, 141–146; Mitchell, S. N.; Greenslade, R. G.; Cooper, J. Eur. J. Pharmacol. 2001, 432, 19– 27].
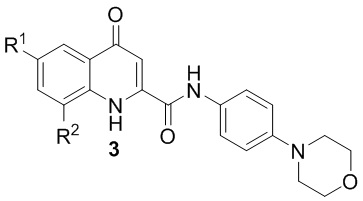
Биологическая активность структур 3 исследовалась на стабильно трансфицированной клеточной линий яичника китайского хомяка, экспрессирующей рецепторы 5HT1B. Константы Кi находятся в интервале 0.9-1000 нмоль [C. L. Horchler, J. P. McCauley, Jr., J. E. Hall, D. H. Snyder, W. C. Moore, T. J. Hudzik, M. J. Chapdelaine. Bioorganic & Medicinal Chemistry 15 (2007) 939–950].
Наиболее близким к заявляемому техническому решению по сущности и по достигаемым результатам является соединение 2, которое принято за прототип изобретения.
К основным недостаткам прототипа можно отнести отсутствие данных по токсичности соединений 2 и отсутствие подтвержденного in vivo влияния на ЦНС.
Технической задачей предлагаемого изобретения является расширение арсенала средств, обладающих седативной активностью на ЦНС и имеющих низкую токсичность.
Поставленная задача решается использованием химических соединений формулы 1, проявляющих выраженную седативную активность и обладающих низкой токсичностью.
Получение соединений общей формулы 1 реализуется известной реакцией термического разложения метиловых эфиров 3-ароил-4,5-диоксо-1-фенил-4,5-дигидро-1H-пиррол-2-карбоновых кислот, которая описана в [А. А. Ботева, О. П. Красных, И. В. Фефилова, Е. Б. Бабушкина, П. А. Слепухин. Известия Академии наук. Серия химическая (2014), № 3, 731-738].
Достоинствами изобретения являются:
1. Низкая токсичность веществ: LD50 вещества 1а более 500 мг/кг, а вещества 1b более 1750 мг/кг (таблица 3). Соединения относятся к 4 классу токсичности, т.е. являются малотоксичными [К.К. Сидоров, Токсикология новых промышленных веществ, Москва, (1973), вып. 13, с. 47-51]. Этим достоинством устраняется недостаток прототипа, связанный с отсутствием данных по токсичности. При этом токсичность заявляемых соединений значительно ниже, чем у применяемого в медицине диазепама (таблица 2).
2. Подтвержденное на животных влияние на ЦНС (таблица 1).
3. Отработанная схема получения веществ, высокие выходы, т.е. легкая синтетическая доступность веществ формулы 1.
Биологическая активность соединений формулы 1 изучалась путем определения острой токсичности и оценки влияния соединений на ЦНС тесте «открытое поле» [ А. Н. Миронов, Руководство по проведению доклинических исследований лекарственных средств. Часть первая. — М.: Гриф и К, 2012. — 944 с.], который регистрирует поведение животных в ответ на новые, потенциально опасные стимулы. Данный тест позволяет изучить изменения в ориентировочной, двигательной и исследовательской активности животных.
Тест «открытое поле» проводили на двух группах мышей линии CD-1. Каждая группа содержала по 10 особей (5 самок и 5 самцов). Вещество вводилось внутрибрюшинно в концентрации 0.1 ммоль/кг в 1% крахмальной слизи. Вторая группа животных являлась контрольной, ей вводили внутрибрюшинно 1% крахмальную слизь. Животные помещались в установку «открытое поле» через 60 минут после введения вещества и крахмальной слизи. В ходе эксперимента регистрировали следующие показатели: пересечение линий (в двух периферийных секторах), пересечение центрального сектора, стойки (с опорой и без), груминг (короткий - один или два коротких круговых движения лап животного вокруг носа и рта, длительный - более интенсивные умывания), дефекации, мочеиспускания и обследование отверстий – обнюхивание края отверстия и заглядывание в отверстия «по глаза» (Kalueff, Tuohimaa, 2004). Число поведенческих реакций, выраженное в процентах относительно количества аналогичных реакций у контрольной группы животных приведено в таблице 1. Было установлено, что вещества формулы 1 уменьшают локомоторную активность животных (по показателям пересеченных секторов и уменьшению количества стоек), при этом они не снижают их исследовательскую активность (количество исследованных отверстий не уменьшается), что может говорить о седативном эффекте. Влияния на вегетативную нервную систему (дефекация, уринация) не было обнаружено.
Исследование острой токсичности проводили на аутбредных белых мышах линии CD-1 массой 27-38 грамм. Вещества вводили внутрибрюшинно в 2 % крахмальной слизи и далее оценивали выживаемость животных в группе при постоянном мониторинге в течение 24 часов и последующем общем наблюдении в течение 14 дней. Установлено, что LD50 вещества 1а более 500 мг/кг, а вещества 1b более 1750 мг/кг (таблица 2). Соединения относятся к 4 классу токсичности, т.е. являются малотоксичными [К.К. Сидоров, Токсикология новых промышленных веществ, Москва, (1973), вып. 13, с. 47-51].
Токсичность эталона сравнения диазепама в разных источниках составляет 240-770 мг/кг при внутрибрюшинном способе введения [В.Э. Колла, Б.Я. Сыропятов, М., "Медицина", 1998 - 263с.] и 37 мг/кг [W. Frik, O. Strubelt, K. Wittmann. Strahlentherapie 127 (2) (1965) 245-252]. Таким образом, заявляемое вещество 1а по токсичности находится на уровне диазепама, а вещество 1b гораздо менее токсично, чем диазепам. Принимая во внимание тот факт, что седативные средства требуют длительного приема, снижение токсичности является критичным моментом.
Изобретение иллюстрируется следующими примерами.
ПРИМЕР 1:
Влияние на ЦНС метиловых эфиров замещенных 3-ароил-4-oксо-1,4-дигидрохинолин-2-карбоновых кислот общей формулы 1 в дозе 0,1 ммоль/кг
Таблица 1.
* - Р = 0.054
Уменьшение параметра по отношению к контролю (в %) рассчитывали для показателей, которые статистически значимо (р<0,05) отличались от значений в контрольной группе, по формуле:
Уменьшение параметра = 100*(среднее значение в группе с веществом – среднее значение в контрольной группе)/значение в контрольной группе.
ПРИМЕР 2:
Токсичность метиловых эфиров замещенных 3-ароил-4-oксо-1,4-дигидрохинолин-2-карбоновых кислот общей формулы 1
Таблица 2
37**
* - [В.Э. Колла, Б.Я. Сыропятов, М., "Медицина", 1998 - 263с.]
** - [W. Frik, O. Strubelt, K. Wittmann. Strahlentherapie 127 (2) (1965) 245-252]
ПРИМЕР 3:
Метиловый эфир 3-(3-бромбензоил)-6-фтор-4-oксо-1,4-дигидрохинолин-2-карбоновой кислоты 1а
5.5 ммоль метилового эфира 3-(3-бромбензоил)-1-(4-фторфенил)-4,5-диоксо-4,5-дигидро-1H-пиррол-2-карбоновой кислоты выдерживали в абсолютном дифенилоксиде при 200°С 7 минут (контроль за протеканием реакции осуществляли с помощью ТСХ). После охлаждения реакционной массы выпадал осадок, который промывали петролейным эфиром и перекристаллизовывали из ацетонитрила. Выход 62%, Тпл. = 242.8-244.0 °С (с разл.). ИК спектр (вазелиновое масло): 3360 (NH); 1744 (COOCH3); 1674 (ArCO); 1608 (C(4)=O, C=C)см-1. ЯМР 1H (300 МГц, DMSO-d6) δ 3.76 (c, 3H, OМе); 7.66-7.76 (м, 6Н, Ar); 8.07 (д.д, 1Н, Н(5), 3J = 9.9, 4J = 4.8); 12.54 (с, 1Н, NH). ЯМР 13C (125 MГц, DMSO-d6): 192.74; 174.96; 161.75; 160.13; 158.18, 139.15; 136.33; 136.21; 135.67; 130.87; 130.80; 127.67; 126.93; 126.87, 122.76; 122.69; 122.31, 122.11, 121.93, 121.07, 108.84, 108.66; 53.58. Анализ: вычислено для C18H11BrFNO4 C, 53.49; H, 2.74; Br, 19.77; F, 4.70; N, 3.47; Найдено: C, 53.43; H, 2.61; Br, 20.05; F, (не делали); N, 3.49.
ПРИМЕР 4:
Метиловый эфир 8-этил-3-(4-метилбензоил)-4-oксо-1,4-дигидрохинолин-2-карбоновой кислоты 1b
Синтезировали аналогично, в качестве растворителя использовали даутерм А. Выход: Т.пл. = 142 -143 °С (с разл.) (ацетонитрил). ИК спектр (ATR): 3400 (NH), 1717 (COOMe) ,1666 (COAr), 1620 (C(4)=O), 1607 (C=C) см-1. ЯМР 1H (400 МГц, ДМСО-d6) δ 10.82 (с, 1H, NH), 7.98 (д, J = 7.8 Гц, 1H, H-5), 7.70-7.68 (м, 3H, H-2',6', H-6'), 7.43-7.39 (м, 1H, H-7), 7.29 (д, J = 7.9 Гц, 2H, H-3',5'), 3.73 (с, 3H, OCH3), 3.04 (м, 2H, CH2), 2.38 (с, 3H, CH3), 1.31 (т, J = 7.4 Гц, 3H, CH3). ЯМР 13C (125 MГц, ДМСО-d6): 193.4, 175.6, 162.3, 143.5, 138.9, 136.8, 134.9, 133.1, 132.2, 129.0, 128.9, 125.9, 124.7, 122.9, 121.2, 53.3, 22.72, 21.1, 13.9. Анализ: вычислено для C21H19NO4 С, 72.19; Н, 5.48; N, 4.01; найдено: С, 71.97; Н, 5.48; N, 4.01.
| название | год | авторы | номер документа |
|---|---|---|---|
| СЕДАТИВНОЕ СРЕДСТВО НА ОСНОВЕ 3-(2-(4-ФТОРОФЕНИЛ)-2-ОКСОЭТИЛИДЕН)-3,4-ДИГИДРО-2Н-БЕНЗО[B][1,4]ОКСАЗИН-2-ОНА | 2021 |
|
RU2788047C1 |
| ПРИМЕНЕНИЕ 1-(2-ТИЕНИЛ)-4H-[1,2]ОКСАЗИНО[5,4-b]ХИНОЛИН-4,10(5H)-ДИОНА В КАЧЕСТВЕ СРЕДСТВА, ОБЛАДАЮЩЕГО РАДИКАЛСВЯЗЫВАЮЩЕЙ АКТИВНОСТЬЮ | 2023 |
|
RU2800388C1 |
| АНАЛЬГЕЗИРУЮЩЕЕ СРЕДСТВО | 2018 |
|
RU2711968C1 |
| АНАЛЬГЕЗИРУЮЩЕЕ СРЕДСТВО | 2016 |
|
RU2634618C1 |
| ПРОИЗВОДНЫЕ ПИРИДОНКАРБОНОВОЙ КИСЛОТЫ И КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 1993 |
|
RU2100351C1 |
| ПРОИЗВОДНЫЕ БЕНЗОТИАЗОЛА | 2005 |
|
RU2382782C2 |
| РАДИКАЛСВЯЗЫВАЮЩЕЕ СРЕДСТВО НА ОСНОВЕ ПРОИЗВОДНЫХ АЦИЛПИРОВИНОГРАДНЫХ КИСЛОТ | 2022 |
|
RU2800386C1 |
| АМИД 8-АМИНО-[1.2.4]ТРИАЗОЛО-[1.5-А]ПИРИДИН-6-КАРБОНОВОЙ КИСЛОТЫ И СОДЕРЖАЩЕЕ ЕГО ЛЕКАРСТВЕННОЕ СРЕДСТВО | 2002 |
|
RU2296763C2 |
| СПИРОЦИКЛИЧЕСКИЕ ЦИКЛОПРОПАНОВЫЕ АМИНОКИСЛОТЫ - АНАЛОГИ ГАММА-АМИНОМАСЛЯНОЙ КИСЛОТЫ, С ОГРАНИЧЕННОЙ КОНФОРМАЦИОННОЙ ПОДВИЖНОСТЬЮ И ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ НА ИХ ОСНОВЕ | 2011 |
|
RU2468000C2 |
| НОВОЕ ПРОИЗВОДНОЕ БЕНЗОАЗЕПИНА И ЕГО МЕДИЦИНСКОЕ ПРИМЕНЕНИЕ | 2013 |
|
RU2642783C2 |
Изобретение относится к применению метиловых эфиров замещенных 3-ароил-4-oксо-1,4-дигидрохинолин-2-карбоновых кислот формулы 1 в качестве седативного средства. Технический результат - седативный эффект, оказываемый соединением формулы 1. 2 табл., 3 пр.
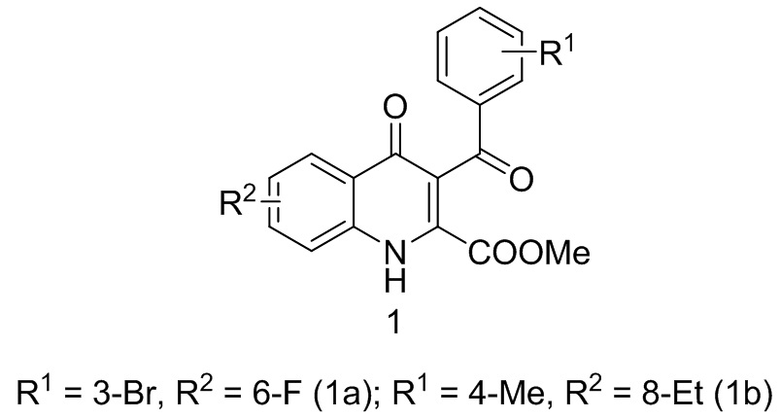
Применение метиловых эфиров замещенных 3-ароил-4-oксо-1,4-дигидрохинолин-2-карбоновых кислот формулы 1

в качестве седативного средства.
| E | |||
| Lager, P | |||
| Andersson, J | |||
| Nilsson, I | |||
| Pettersson, E | |||
| Nielsen, M | |||
| Nielsen, O | |||
| Sterner, T | |||
| Liljefors | |||
| J | |||
| Med | |||
| Chem | |||
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| WO 2009040377 A3, 02.04.2009 | |||
| Ботева А | |||
| А., Красных О | |||
| П., Томилов М | |||
| Ю., И Вахрин М., Бабушкина Е | |||
| Б., Одегова Т | |||
| Ф | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
Авторы
Даты
2022-09-28—Публикация
2021-12-23—Подача