Изобретение относится к микробиологии и фармацевтической химии и предназначено для фотодинамической инактивации граморицательных патогенных микроорганизмов, в том числе антибиотикорезистентной внутрибольничной микрофлоры, с использованием фотосенсибилизатора.
Антимикробная фотодинамическая терапия (АФДТ) представляет собой альтернативу привычным методам борьбы с патогенной микрофлорой, а также может быть использована, как эффективное дополнение к антибиотикотерапии. АФДТ представляет собой принципиально новую и отличную от антибиотикотерапии стратегию инактивации патогенной микрофлоры, основанную на селективном накоплении в микробных клетках окрашенных веществ - фотосенсибилизаторов (ФС). Эти вещества при воздействии видимого света определенной длины волны и соответствующей мощности генерируют активные формы кислорода, что позволяет проводить фотодинамическую инактивацию микроорганизмов путем запуска каскада фотохимических реакций.
Введенные в клиническую практику для лечения опухолей нейтральные и анионные макрогетероциклические ФС на основе порфиринов, хлоринов и фталоцианинов эффективны при фотодинамической инактивации в основном грамположительных микроорганизмов, однако грамотрицательные бактерии, имеющие внешнюю липополисахаридную мембрану, обычно оказываются малочувствительными к АФДТ.
Известно использование фотосенсибилизатора «Фотосенс» на основе сульфированного фталоцианина гидроксиалюминия для проведения АФДТ инфицированных ран и трофических язв с устойчивой к антибиотикам микрофлорой [Stranadko Е.Р., Tolstykh М.Р., Riabov M.V., Krivikhin D.V. (2003) Photodynamic therapy of persistent purulent wounds and trophic ulcers of lower extremeties. DC World Congress of the International Photodynamic Association. Abstracts. Miyazaki, P. 28].
Однако анионный характер предлагаемого ФС не позволяет эффективно проводить фотодинамическую инактивацию грамотрицательных бактерий.
Описано использование нейтральных и катионных цинковых комплексов фталоцианинов для фотодинамической инактивации Грам (-) микрооргазмов in vitro. Показано, что наличие катионных групп в молекуле ФС позволяет на несколько порядков уменьшить число колониеобразующих единиц кишечной палочки (КОЕ) [Scalise I, Durantini EN. Synthesis, properties, and photodynamic inactivation of escheric.iia coli using a cationic and a non-charged zn(ii) pyridyloxyphthalocyanine derivatives. Bioorg Med Chem 2005. 13. P. 3037-3045].
Однако использованные ФС не позволяют провести полную инактивацию патогенной микрофлоры и, кроме того, обладают заметной остаточной фототоксичностью.
Известно использование малотоксичных производных хлорина е6 (нейтральной, анионной и катионных форм) в отношении грамотрицательных и грамположительных бактерий in vitro [Drulis-Kawa Z, Bednarkiewicz A, Bugla G, Strek W, Doroszkiewicz W. // Adv Clin Exp Med 2006; 15(2). P. 279-83; Karygianni L, Ruf S, Folio M, Hellwig E, Bucher M, Anderson AC, Vach K, Al-Ahmad A. // Appl Environ Microbiol 2014; 80: 7324-7336; Mesquita MQ, Menezes JC, Neves MG, Tome AC, Cavaleiro JA, Cunha A, Almeida A, Hackbarth S, Roder B, Faustino MA. // Bioorg Med Chem Lett 2014; 24: 808-812; Kustov A.V, Belykh DV, Smimova NL, Venediktov EA, Kudayarova TV, Kruchin SO, Khudyaeva IS, Berezin DB. // Dyes & Pigments. 2018; 149: 553-559]. Несмотря на успешную фотоинактивацию Грам (+) патогенов, в отношении грамотрицательных микроорганизмов фотодинамическая инактивация оказалась недостаточно эффективной. Кроме того, все исследования проводились in vitro в отношении планктонных форм микроорганизмов.
Наиболее близким по совокупности существенных признаков к заявляемому изобретению является проведение фотодинамической инактивации микроорганизмов in vivo фотосенсибилизатором «Фотодитазин», который был использован для лечения длительно не заживающих ран, содержавших смешанную микрофлору, представленную как грамположительными, так и грамотрицательными бактериями [Гейниц А.В., Толстых П.И., Дербенев В.А. и др. Фотодинамическая терапия гнойных и длительно не заживающих ран. Пособие для врачей. М., 2004. 15 с.]. Оказалось, что после облучения уровень обсемененности снижался на два порядка с 107 до 105 КОЕ, однако фотоинактивации грамотрицательной микрофлоры отмечено не было.
Техническим результатом изобретения является уничтожение грамотрицательных патогенных микроорганизмов in vivo, в том числе антибиотикорезистентной внутрибольничной микрофлоры, путем проведения их фотодинамической инактивации.
Указанный результат достигается тем, что в способе фотодинамической инактивации грамотрицательных патогенных микроорганизмов in vivo, заключающемся в воздействии на них фотосенсибилизатора на основе хлорина е6, согласно изобретению, в качеств фотосенсибилизатора используют препарат на основе монокатионного производного хлорина е6:
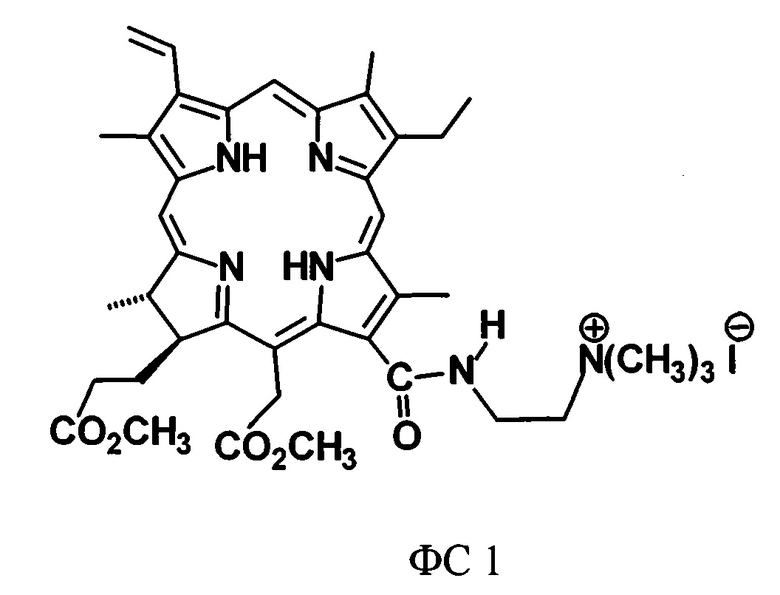
путем внесения в очаг воспаления его композиции с концентрацией фотосенсибилизатора 0,0035 моль/кг, содержащей 1 мас. % неионогенного ПАВ Твин 80 в качестве носителя, 0,1 мас. % динатриевой соли этилендиаминтетрауксусной кислоты (Na2H2Edta), 10 мас. % глицерина, 2 мас. % диметилсульфоксида и 1 мас. % альгината натрия, и облучения красным светом с длиной волны λ=660 нм и плотностью световой энергии 80 Дж/см2.
Технический результат достигается за счет того, что используемый фотосенсибилизатор способен к эффективной фотодинамической инактивации грамотрицательных микроорганизмов in vivo путем реализации следующих преимуществ:
1) наличие в структуре молекулы ФС 1 одной катионной группы позволяет обеспечить необходимую растворимость в водных растворах при достаточно высоком сродстве к липофильному окружению, в том числе к внешней мембране грамотрицательных бактерий;
2) наличие атома йода в структуре молекулы ФС 1 потенциально увеличивает фототоксичность в отношении патогенной микрофлоры путем продукции реактивных иодид-радикалов в процессе фотоинактивации;
3) использование Твин 80 в качестве носителя и Na2H2Edta позволяет увеличить агрегативную устойчивость фотосенсибилизатора в водных растворах, повысить фотостабильность молекул ФС и дестабилизировать внешнюю липополисахаридную мембрану грамотрицательных бактерий.
Предлагаемое изобретение может быть использовано для проведения фотодинамической инактивации грамотрицательных микроорганизмов in vivo, включая антибиотикорезистентную внутрибольничную патогенную микрофлору.
Для реализации фотодинамической инактивации с ФС 1 используют следующие вещества и устройства:
- фотосенсибилизатор;
- бидистиллированная вода;
- Твин 80 (Panreac, >98%);
- глицерин (Panreac, >98%);
- Na2H2Edta 2 Н2O (Panreac, >99%);
- диметилсульфоксид (Panreac, >99%);
- альгинат натрия (Aldrich, Pharm. sec. standard);
- диодный лазер или светодиодная панель с длиной волны 660 нм (ООО «Эломед» (Москва), ЗАО БМЦ (Минск)).
Фотоинактивация патогенных микроорганизмов реализуется путем внесения в очаг воспаления композиции с концентрацией фотосенсибилизатора 0,0035 моль/кг, содержащей 1 мас. % неионогенного ПАВ Твин 80 в качестве носителя, 0,1 мас. % динатриевой соли этилендиаминтетрауксусной кислоты (Na2H2Edta), 10 мас. % глицерина, 2 мас. % диметилсульфоксида и 1 мас. % альгината натрия, и облучения красным светом с длиной волны λ=660 нм и плотностью световой энергии 80 Дж/см2.
Сведения, подтверждающие возможность воспроизведения изобретения
Способ был апробирован путем фотодинамической инактивации грамотрицательных внутрибольничных антибиотикорезистентных микроорганизмов с помощью ФС 1 in vivo.
Суточные культуры тест-штаммов микроорганизмов на скошенном мясопептонном агаре смывали физиологическим раствором и доводили до концентрации 109 КОЕ в 1 мл. Посевную дозу 108 клеток в 1 мл готовили из исходной стандартной взвеси разведением. При моделировании инактивации in vivo 0,1 мл раствора с тест-культурой микроорганизмов (108 КОЕ/мл) наносилось на область ожога, полученного на спине лабораторных крыс женского пола породы Wistar или путем нанесения суспензии микроорганизмов на предплечье у добровольцев. Все работы проводились в специализированной лаборатории Ивановской государственной медицинской академии и были одобрены этическим комитетом ИвГМА (ЭК 2017.25.10).
Непосредственно перед проведением исследований лабораторные животные погружались в глубокий сон путем инъекции смеси препаратов Zoletil 100 (Virbac Sante Animale) and Rometar (Bioveta). После этого поверхность спины животных подвергалась эпиляции и далее специальным устройством, разогретым до температуры 220-230°С, осуществлялось несколько круговых ожогов радиусом 1 см, на каждый из которых через 5 минут наносилось 0,1 мл суспензии с культурой микроорганизмов. Через 20 минут на область каждого ожога наносилась композиция, с концентрацией ФС 0.0035 моль/кг и еще через 20-25 минут проводился сеанс антимикробной ФДТ путем облучения поверхности красным светом. По окончании сеанса биоматериал с каждого ожога собирался стерильным тампоном, начиная от центра к краю раневой поверхности, и высевался на соответствующие питательные среды. После окончания эксперимента находящимся в состоянии сна животным вводилась летальная доза указанных выше препаратов, после чего они утилизировались в установленном порядке.
При проведении фотоинактивации грамотрицательных микроорганизмов на поверхности кожи добровольцев, 0,1 мл раствора с тест-культурой микроорганизмов (108 КОЕ/мл) наносилось на область предплечья площадью ~4 см2. Через 20 минут на нее наносилась композиция ФС, и еще через 20-25 минут проводился сеанс антимикробной ФДТ путем облучения поверхности красным светом с длиной волны 660 нм. По окончании сеанса биоматериал с каждой области нанесения собирался стерильным тампоном, начиная от центра к краю раневой поверхности, и высевался на соответствующие питательные среды. Затем поверхность кожи смывалась и обрабатывалась антимикробным средством.
Результаты испытаний in vivo с заявленным ФС при фотоинактивации внутрибольничных антибиотикорезистентных грамотрицательных бактерий Pseudomonas aeroginosa и Е. coli у лабораторных животных в модели ожоговой раны и у добровольцев при нанесении на кожу приведены в таблице.
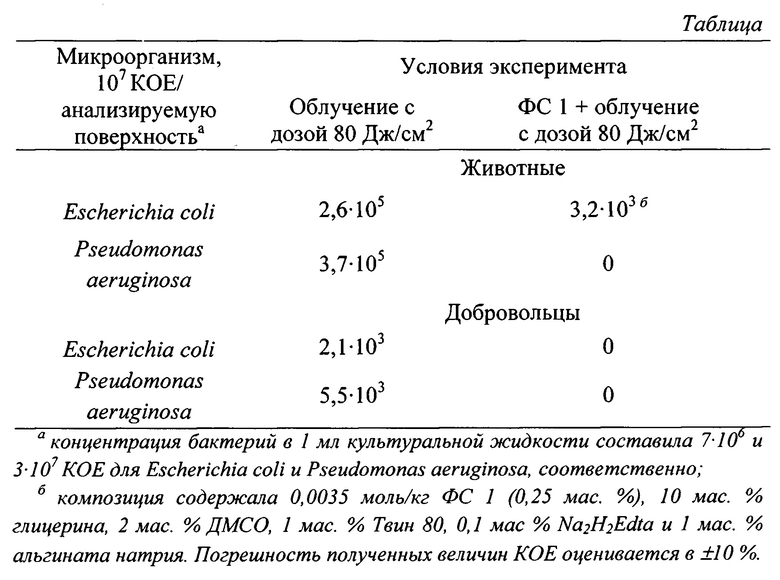
Как видно из таблицы, облучение ожоговой поверхности с дозой световой энергии 80 Дж/см2 без ФС 1 (контроль) снижает количество микроорганизмов на поверхности раны более чем на полтора порядка, указывая на наличие остаточного бактерицидного эффекта кожи у лабораторных животных. Использование ФС 1 позволяет полностью инактивировать патогенный микроорганизм Pseudomonas aeruginosa и почти на два порядка уменьшить число КОЕ у Е. coli за один сеанс ФДТ.
Исследования фотоинактивации микроорганизмов с поверхности кожи добровольцев показали, что облучение поверхности с дозой световой энергии 80 Дж/см2 без ФС 1 (контроль) снижает количество микроорганизмов на поверхности раны более чем на три порядка, указывая на наличие существенного бактерицидного эффекта кожи. Использование ФС 1 позволяет полностью инактивировать оба патогенных микроорганизма. Из приведенных в таблице данных можно сделать вывод о высокой эффективности инактивации Грам (-) микроорганизмов in vivo.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЛЕЧЕНИЯ НОЗОКОМИАЛЬНОГО СИНУСИТА У ПАЦИЕНТОВ В ОТДЕЛЕНИЯХ РЕАНИМАЦИИ И ИНТЕНСИВНОЙ ТЕРАПИИ | 2012 |
|
RU2503471C1 |
| Монокатионный хлориновый фотосенсибилизатор для фотодинамической инактивации опухолевых клеток | 2022 |
|
RU2792003C1 |
| Способ оптимизации фотодинамической терапии гнойных ран (варианты) | 2015 |
|
RU2609735C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ГНОЙНЫХ РАН МЕТОДОМ АНТИМИКРОБНОЙ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ | 2018 |
|
RU2678974C1 |
| ФОТОСЕНСИБИЛИЗАТОР ДЛЯ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ | 2013 |
|
RU2536966C1 |
| СПОСОБ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ ПЕРЕВИВНОЙ ОПУХОЛИ КАРЦИНОМА ЭРЛИХА МЫШЕЙ С ФОТОСЕНСИБИЛИЗАТОРОМ ХЛОРИНОВОГО РЯДА | 2022 |
|
RU2788766C2 |
| СПОСОБ ФОТОДИНАМИЧЕСКОЙ ИНАКТИВАЦИИ БАКТЕРИЙ | 2006 |
|
RU2316366C2 |
| ФОТОСТАБИЛЬНАЯ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ТЕРАПИИ ОЧАГОВ БАКТЕРИАЛЬНОГО ПОРАЖЕНИЯ | 2017 |
|
RU2662082C2 |
| СПОСОБ ФОТОИНАКТИВАЦИИ ВИРУСА ГРИППА А ПТИЦ ПОДТИПА H5N1 | 2007 |
|
RU2357770C1 |
| СПОСОБ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ ПЕРЕВИВНОЙ ПОВЕРХНОСТНОЙ СОЛИДНОЙ СОЕДИНИТЕЛЬНОТКАННОЙ САРКОМЫ М-1 КРЫС | 2019 |
|
RU2704202C1 |
Изобретение относится к микробиологии и медицине и предназначено для фотодинамической инактивации грамотрицательных патогенных микроорганизмов in vivo, в том числе антибиотикорезистентной внутрибольничной микрофлоры, с использованием фотосенсибилизатора, представляющего собой монокатионное производное хлорина е6, указанной ниже формулы, заключающейся во внесении в очаг воспаления композиции с концентрацией фотосенсибилизатора 0,0035 моль/кг, содержащей 1 мас. % неионогенного ПАВ Твин 80 в качестве носителя, 0,1 мас. % динатриевой соли этилендиаминтетрауксусной кислоты (Na2H2Edta), 10 мас. % глицерина, 2 мас. % диметилсульфоксида и 1 мас. % альгината натрия, и облучения красным светом с длиной волны λ=660 нм и плотностью световой энергии 80 Дж/см2. Техническим результатом изобретения является уничтожение патогенных грамотрицательных микроорганизмов, в том числе антибиотикорезистентной внутрибольничной микрофлоры in vivo, путем проведения их фотодинамической инактивации. 1 табл.
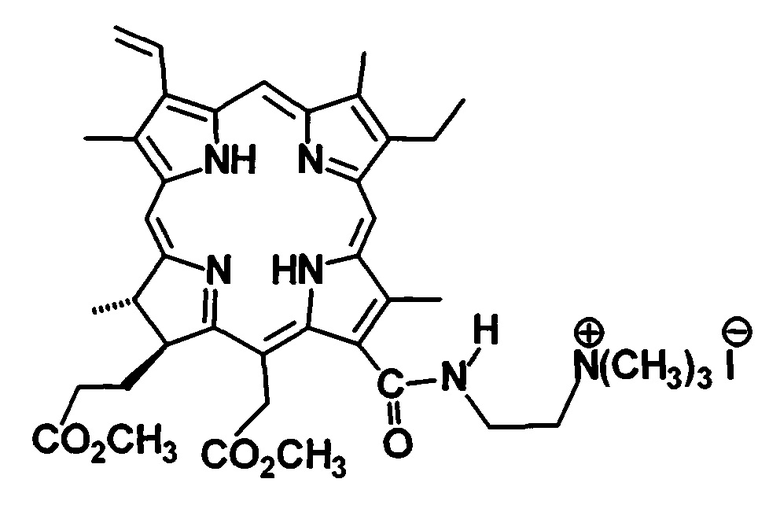
Способ фотодинамической инактивации грамотрицательных патогенных микроорганизмов in vivo, заключающийся в воздействии на них фотосенсибилизатора на основе хлорина е6, отличающийся тем, что для фотодинамической инактивации грамотрицательных патогенных микроорганизмов, в том числе антибиотикорезистентной внутрибольничной микрофлоры, в качестве фотосенсибилизатора используют препарат на основе монокатионного производного хлорина е6, формулы:
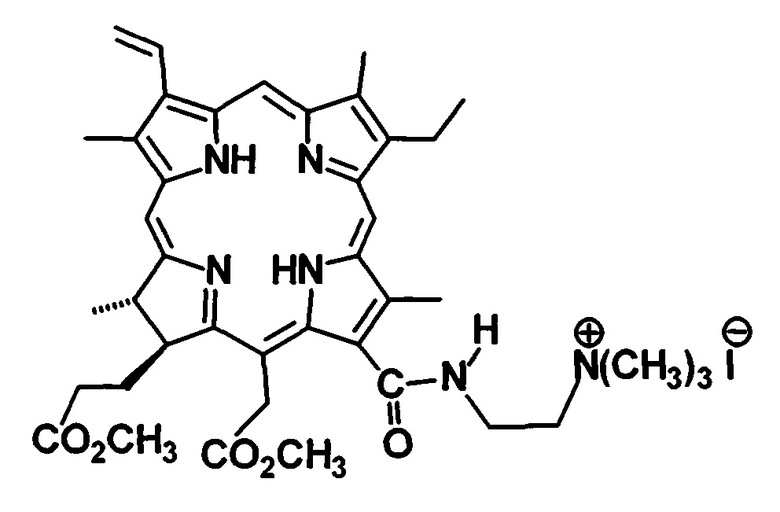
путем внесения в очаг воспаления его композиции с концентрацией фотосенсибилизатора 0,0035 моль/кг, содержащей 1 мас. % неионогенного ПАВ Твин 80 в качестве носителя, 0,1 мас. % динатриевой соли этилендиаминтетрауксусной кислоты (Na2H2Edta), 10 мас. % глицерина, 2 мас. % диметилсульфоксида и 1 мас. % альгината натрия, и облучения красным светом с длиной волны λ=660 нм и плотностью световой энергии 80 Дж/см2.
| Kustov, Andrey V | |||
| И др | |||
| "Synthesis and investigation of water-soluble chlorophyll pigments for antimicrobial photodynamic therapy", Dyes and Pigments, 2018, 149, с.553-559 | |||
| D | |||
| B | |||
| Капельная масленка с постоянным уровнем масла | 0 |
|
SU80A1 |
Авторы
Даты
2022-10-19—Публикация
2021-11-10—Подача