УРОВЕНЬ ТЕХНИКИ ИЗОБРЕТЕНИЯ
[0001] Область техники, к которой относится изобретение
[0002] Варианты осуществления настоящего изобретения относятся к растворам замка катетера и видам терапии с применением замков катетеров, при использовании тринатрийцитрата и этилового спирта, и, в частности, 4,0-15,0 массо-объемных % тринатрийцитрата в качестве антикоагулянтного компонента и/или антибактериального компонента и 15,0-25,0 объемных % этилового спирта в качестве антибактериального компонента.
[0003] Предшествующий уровень техники
[0004] Катетеры являются трубчатыми объектами, которые можно вводить в тело пациента для проведения различных видов лечения. Внутрисосудистые катетеры представляют собой обычную форму катетера, применяемого для проведения лечения через сосуды тела. Такие виды лечения могут включать в себя гемодиализ, внутрисосудистое охлаждение, внутрисосудистое ультразвуковое вмешательство и т.п. При этом, катетеризация и виды лечения, получающиеся в результате катетеризации, могут быть связаны с многочисленными рисками. Например, может происходить формирование биопленки вследствие размножения болезнетворных бактерии и/или роста грибов в, на катетере и/или вокруг катетера. Формирование биопленки может приводить к образованию тромбов, а также к инфекциям кровотока. В, на катетере и/или вокруг катетера может также происходить тромбообразование и/или образование эмболов. Например, образование кровяных сгустков может вызываться повреждением и воспалением эндотелия из-за процесса катетеризации. Другой риск может исходить от осаждения твердых частиц из растворов, применяемых в катетерной системе. Формирование биопленки, образование кровяных сгустков, и/или осаждение твердых частиц может быть следствием нарушения работы катетера, например, закупоркой катетера. Кроме того, любое из упомянутых состояний может дополнительно приводить к потенциальным опасностям для здоровья пациента.
[0005] Общим способом снижения рисков, связанных с катетеризацией и видами лечения, получающимися в результате катетеризации, может быть терапия с применением замка катетера, при которой в просвет катетера можно вводить раствор замка катетера (например, антибактериальные и/или антикоагулянтные растворы). Растворы замка катетера и виды терапии с применением замков катетеров можно использовать для уменьшения предрасположенности к возникновению любого из вышеупомянутых состояний и/или ослабления их воздействий. В общем, раствор замка катетера вводят в катетерную систему между сеансами использования, чтобы подавить образование бактерий и тромбообразование и тем самым замедлить формирование биопленки и нарушение работы катетера. Общеупотребительные растворы замка катетера могут включать в себя антибактериальные средства для уменьшения бактериемии и антикоагулянтные средства для снижения любой вероятности нарушения работы катетера.
[0006] Одним из недостатков существующих растворов и видов терапии является их неспособность эффективно снижать тенденции, приводящие к нарушению работы катетера. Другие недостатком является их неспособность эффективно снижать тенденции, приводящие к нарушению работы катетера, при одновременном ослаблении последствий, которые могут приводить к дискомфорту пациента и заболеванию пациента. Кроме того, многие существующие растворы замка катетера не способны предотвращать нарушение работы катетера без неблагоприятных воздействий на катетерную систему. Например, существующие растворы могут быть основаны на антибиотических средствах, чтобы создавать антибактериальные действия. Это может приводить к повышению резистентности к противомикробным препаратам, что может нанести ущерб пациенту, в частности, пациентам, связанным с длительным применением катетерной системы. Другие растворы могут производить антибактериальное и/или антикоагулянтное действия посредством использования средств, которые создают токсичную окружающую среду для пациента, приводящую к дискомфорту, заболеванию и другим осложнениям. Кроме того, многие растворы являются вредными для катетерной системы, вызывающими деградацию материалов и действующими как катализатор укорачивания срока службы составных частей катетерной системы.
[0007] В общем, существующие растворы замка катетера вынуждали врачей-практиков выбирать терапию с применением замка катетера, которая выбирает компромиссный отказ от одного требуемого действия в пользу другого. Например, существующие растворы замка катетера могут состоять из компонентов, которые либо более пригодны для выполнения антибактериальных функций, или более пригодны для выполнения антикоагулянтных функций, при этом сочетание данных компонентов не обнаруживают синергического действия какого-либо типа, смягчающего компромисс. В качестве другого примера, другие существующие растворы замка катетера могут демонстрировать эффективные антибактериальные действия, но создавать дискомфорт для пациента или оказывать вредное воздействие на катетер.
[0008] Варианты осуществления настоящего изобретения направлены на решение одной или более вышеупомянутых проблем.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[0009] Раскрываемый раствор замка катетера может включать в себя 4,0-15,0 массо-объемных % («масс./об. %») тринатрийцитрата. Тринатрийцитрат можно использовать в качестве антикоагулянтного компонента и/или антибактериального компонента раствора замка катетера. Раствор замка катетера может дополнительно включать в себя 15,0-25,0 об. % этилового спирта. Этиловый спирт можно использовать в качестве антибактериального компонента раствора замка катетера. Некоторые варианты осуществления могут включать в себя раствор замка катетера, содержащий водный раствор, содержащий 4,0-15,0 масс./об. % тринатрийцитрата и 15,0-25.0 об. % этилового спирта («раствор TCEA»). Другие отношения в пределах диапазона могут включать в себя 10,0 масс./об. % тринатрийцитрата и 20,0 об. % этилового спирта, которые могут образовать относительно менее сильный противомикробный раствор замка. В качестве другого примера можно использовать 10,0 масс./об. % тринатрийцитрата и 25,0 об. % этилового спирта для образования раствора замка с относительно более сильным противомикробным действием.
[0010] Предполагается, что настоящее изобретение предназначено для использования с катетерной системой, которая может быть постоянной катетерной системой или «долговременной» катетерной системой. Типичная катетерная система может включать в себя трубчатый стержень, имеющий наконечник, со сформированным в нем просветом, соединительную втулку, расширительную камеру, участок захвата и иглу. Использовать можно больше или меньше деталей катетерной системы. Например, настоящее изобретение можно применять с катетерной системой, состоящей, по существу, из трубчатого стержня. В качестве примера, катетерная система может включать в себя дополнительные компоненты, например, фильтр, пневмокамеру и т.п. Хотя настоящее изобретение может быть описано здесь как применяемое с катетерной системой, оно не обязательно ограничено таким применением. Раствор замка катетера и терапию с применением замка катетера можно использовать в любой ситуации, в которой желательно создать окружающую среду, в которой не происходит или, по существу, не происходит роста биопленки и/или коагуляции крови. Например, способ применения может включать в себя способ очистки от биопленки посредством введения раствора, включающего в себя тринатрийцитрат и этиловый спирт, в целевую окружающую среду и сохранения контакта между раствором тринатрийцитрата и этилового спирта и целевой окружающей средой, чтобы обеспечить, по меньшей мере, что-то одно из предотвращения формирования биопленки и устранения биопленки, которая сформировалась в целевой окружающей среде.
[0011] Варианты осуществления раствора замка катетера можно применять для исправления неудачного результата лечения во время медицинских процедур, которые могут использовать катетеры для проведения лечения. Данной цели можно достичь путем применения любого из раскрытых вариантов осуществления раствора замка катетера и/или любого из раскрытых вариантов осуществления терапии с применением замка катетера. Таким образом, раствор замка катетера и/или терапию с применением замка катетера можно использовать для предотвращения формирования биопленки и/или полного устранения биопленки, которая сформировалась внутри катетерной системы. Например, предварительные испытания in vitro показывают, что один только тринатрийцитрат в концентрации 10,0 масс./об. % не оказывал влияния на выживаемость бактерий. Этиловый спирт в концентрации 15,0 об. % уменьшал количество бактериальных клеток с 107 до 102 и не подвергал лизису все бактериальные клетки. Один тринатрийцитрат не подавляет бактериальные клетки или не обеспечивает подходящего средства для их лизиса. Тем не менее, сочетание этанола в концентрации 15,0 об. % с тринатрийцитратом в концентрации 10,0 масс./об. % вызывало полный лизис бактериальных клеток (ниже порога обнаружения). Кроме того, такая же или подобная дозировка может сдерживать или предотвращать коагуляцию посредством хелатного комплекса ионов кальция с ионами цитрата в крови для прерывания свертывания крови.
[0012] В некоторых вариантах осуществления раствор замка катетера можно вводить в просвет катетера, когда катетер не используют для проведения лечения, и/или когда катетер не введен в тело пациента. Например, раствор замка катетера можно применять между сеансами диализа катетерной системы, используемой для гемодиализа. Раствор замка катетера можно оставлять находящимся внутри просвета (т.е. выдерживать внутри просвета) в течение периода, когда катетер не используется и/или не введен в пациента. В некоторых вариантах осуществления раствор замка катетера можно оставлять находящимся в просвете в течение предварительно заданного периода времени, независимо от того, как долго катетер не будет использован и/или остается снаружи пациента.
[0013] Применение раствора замка катетера, содержащего, по меньшей мере, раствор TCEA, может почти устранить или полностью устранить биопленку, существующую внутри просвета. Такой раствор может также предотвращать формирование биопленки. Кроме того, такой раствор можно использовать с незначительной или отсутствующей деградацией материалов, являющихся материалами катетера, под действием раствора замка катетера. Возможно образование растворов замка катетера с, по меньшей мере, раствором TCEA, имеющие уровень pH, который полезен для катетера, что дополнительно ограничивает вредные воздействия на материал катетера. Кроме того, раствор TCEA может создавать дополнительные преимущества для катетерной системы и/или пациента благодаря тому, что не вызывает преципитации белков плазмы крови, не создает дискомфорта для пациента, значительно снижает степень нарушения работы катетера и обладает способностью к использованию при терапии с применением замков катетеров, включающих использование глицерилтринитратов («GTN»). Как подробно изложено ниже, различные варианты осуществления растворов замка катетера и видов терапии с применением замков катетеров могут предотвращать или, по меньшей мере, значительно снижать риски, связанные с инфекциями кровотока, нарушением работы катетерной системы, образованием эмболов, дискомфортом для пациента и заболеванием пациента. Кроме того, растворы замка катетера с, по меньшей мере, некоторым количеством раствора TCEA могут обеспечивать тринатрийцитратный компонент в качестве антикоагулянтного средства и/или антибактериального средства, а тринатрийцитрат в пределах раскрытых диапазонов для образования TCEA может производить неожиданный результат усиления противомикробного действия этилового спирта.
[0014] Дополнительные варианты осуществления настоящего изобретения можно применять в связи с другими средствами замка катетера и видами терапии с применением замков катетеров. Эти средства и виды терапии могут включать в себя, но без ограничения, тромболитические средства, растворы гепарина, физиологические растворы, растворы соляной кислоты, другие хелатирующие средства, другие спирты, другие средства разрушения биопленок, методы промывки, методы применения положительного давления, виды фибринолитической терапии и т.п. Отмечено, что применение других средств в растворах замка катетера, например, гепарина, может стимулировать прилипание биопленки к поверхности катетера, и поэтому следует проявлять осторожность при использовании раствора TCEA в сочетании с другими средствами в растворах замка катетера. Другие побочные действия гепарина могут включать в себя усиление кровотечения, кожную сыпь, головную боль, симптомы простуды и желудочное расстройство. Менее распространенным побочным действием может быть снижение прочности костей, если пациенты испытывают воздействие гепарина в течение длительных периодов времени (например, периодов времени продолжительностью несколько месяцев или более). Упомянутые побочные действия могут усиливаться при использовании с пациентами в состоянии беременности. Редко встречающимся побочным действием гепарина является состояние, называемое гепарин-индуцированной тромбоцитопенией («HIT»). Состояние HIT иногда неправильно называют «аллергией на гепарин». Состояние HIT является автоиммунным процессом с развитием тромбоцитопении. Данное состояние встречается у небольшого числа пациентов (приблизительно 3-5% пациентов, подлежащих лечению гепарином), но оно характеризуется очень серьезными симптомами, включая ухудшение свертываемости крови и развитие новых сгустков крови, что может привести к инсульту, инфаркту миокарда, тромбозу глубоких вен и смерти.
[0015] Хотя приведенные потенциальные преимущества и возможны благодаря техническим решениям, предлагаемым в настоящей заявке, их получение не обязательно. Раскрываемые растворы замка катетера и виды терапии с применением растворов замка катетера можно реализовывать для получения технических преимуществ, независимо от того, добиваются ли или получают вышеупомянутые потенциальные преимущества по-отдельности или в сочетании.
[0016] Дополнительные признаки, аспекты, цели, преимущества и возможные применения настоящего изобретения будут понятны в результате изучения примерных вариантов осуществления и примеров, описанных ниже в связи с фигурами, и прилагаемой формулы изобретения.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0017] Вышеприведенные и другие цели, аспекты, признаки, преимущества и возможные применения настоящего изобретения станут понятнее из нижеприведенного подробного описания изобретения, представленного в связи со следующими чертежами, на которых:
[0018] Фиг. 1 - график, изображающий результаты испытаний, относящиеся к синергическим антибактериальным действиям тринатрийцитрата и этилового спирта в растворе, и, в частности, график колониеобразующих единиц бактериального штамма в зависимости от растворов, имеющих различные концентрации тринатрийцитрата и этилового спирта.
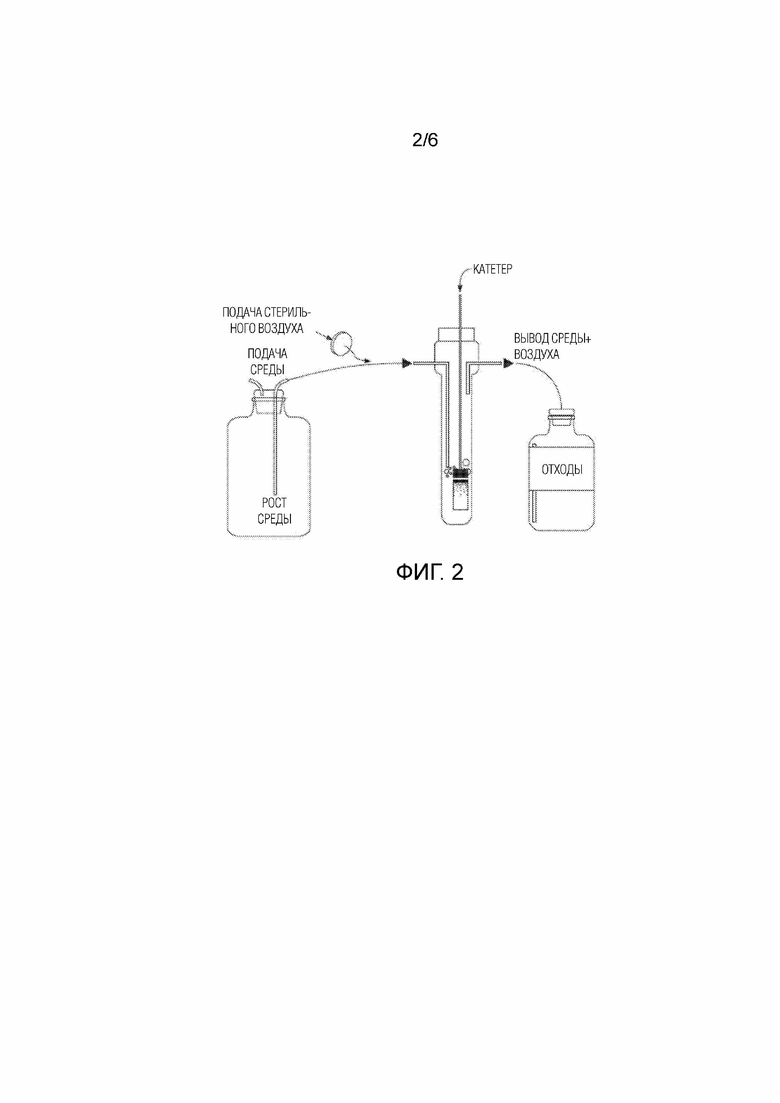
[0019] Фиг. 2 - изображение примерной экспериментальной установки для определения, может ли примерный раствор замка катетера уничтожать жизнеспособные бактерии и предотвращать возобновление роста биопленки.
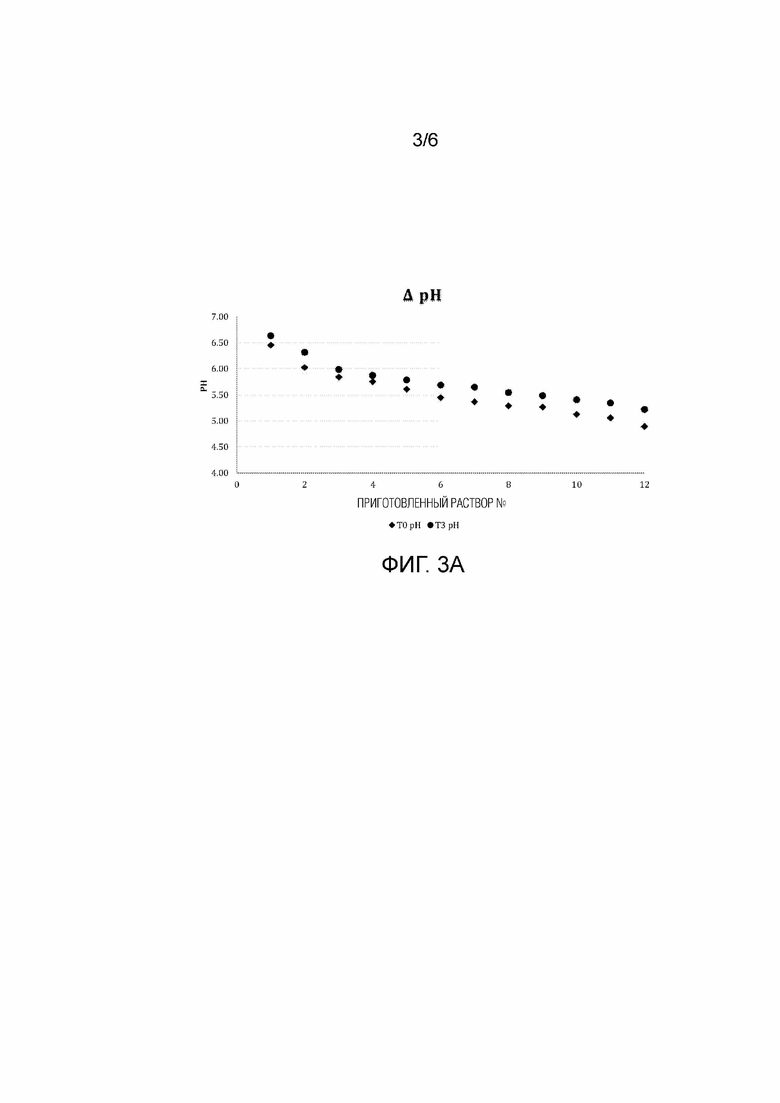
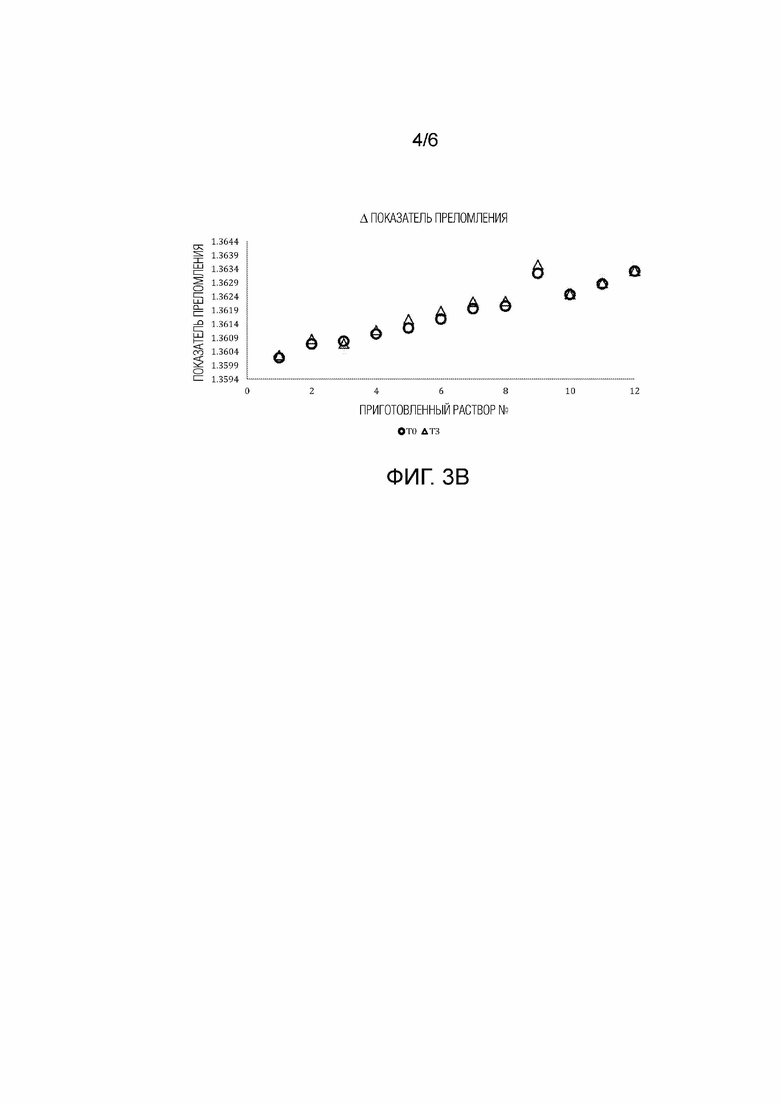
[0020] Фиг. 3A-3D - результаты стабильности двенадцати примерных составленных растворов в процессе примерного исследования с ускоренным старением, где фиг. 3A представляет изменение уровня pH, фиг. 3B представляет изменение RI, фиг. 3C представляет изменение плотности, и фиг. 3D представляет потерю веса.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0021] Нижеприведенное описание представляет вариант осуществления, планируемого к настоящему времени для выполнения настоящего изобретения. Данное описание не подлежит интерпретации в ограничивающем смысле, но составлено только с целью описания общих признаков и признаков настоящего изобретения. Объем настоящего изобретения следует определять со ссылкой на формулу изобретения.
[0022] Следует иметь в виду, что раствор замка катетера используется с водой для инъекций («WFI»), и, следовательно, раствор замка катетера может быть водным раствором. Дополнительно следует иметь в виду, что раствор содержит приблизительно 75% воды. Варианты осуществления раскрываемого раствора замка катетера могут содержать тринатрийцитрат в водном растворе. Другие варианты осуществления раствора замка катетера могут содержать этиловый спирт в водном растворе. Некоторые варианты осуществления могут содержать тринатрийцитрат и этиловый спирт в водном растворе. Примерный вариант осуществления называется в настоящей заявке «раствором TCEA», который может содержать водный раствор, содержащий тринатрийцитрат, имеющий концентрацию в пределах от 4,0 до 15,0 массо-объемных % («масс./об. %») и этиловый спирт, имеющий концентрацию в пределах от 15,0 до 25,0 объемных % («об. %»). Концентрации тринатрийцитрата измеряются в единицах массы тринатрийцитрата на суммарный объем раствора. Концентрации этилового спирта измеряются в единицах объема этанола на суммарный объем раствора. В рамках различных вариантов осуществления тринатрийцитратный компонент можно использовать как антикоагулянтное средство и/или антибактериальное средство. Кроме того, этиловоспиртовой компонент можно использовать как антибактериальное средство. При ссылке на антибактериальное действие в настоящем раскрытии подразумевается, что данное действие охватывает также противомикробные действия, антибиотические действия, противогрибковые действия и антисептические действия.
[0023] Как видно из фиг. 1, раствор замка катетера с водным раствором, содержащим концентрацию тринатрийцитрата в пределах от 4,0 до 15.0 масс./об. % оказывает умеренное антибактериальное действие. Раствор замка катетера с водным раствором, содержащим концентрацию этилового спирта в пределах от 15,0 до 25,0 об. % также оказывает умеренное антибактериальное действие. Однако, раствор замка катетера, содержащий, по меньшей мере, раствор TCEA, оказывает значительное антибактериальное действие и может почти устранять или полностью устранять биопленку в окружающей среде, сохраняющей контакт с раствором TCEA, в течение предварительно заданного периода времени. Следует отметить, что тринатрийцитратный компонент можно использовать в качестве антикоагулянтного средства и/или антибактериального средства. Кроме того, использование тринатрийцитрата в пределах раскрытых диапазонов для образования раствора TCEA может производить неожиданный результат усиления противомикробного действия этилового спирта.
[0024] График на фиг. 1 представляет полученные данные испытаний, обнаруживающие синергическое антибактериальные действия тринатрийцитрата и этилового спирта, при формировании раствора TCEA. Например, выполняли предварительный количественный анализ характеристик противодействия биопленкам раствора TCEA, содержащего тринатрийцитрат в концентрации 10,0 масс./об. % и этиловый спирт (т.е. этанол или EtOH) в концентрациях 15,0, 20,0 и 25,0 об. %. Испытания выполняли следующим образом.
[0025] Тест-растворы
Этанол 15%, 20% и 25% (об.)+тринатрийцитрат 10% (масс./об.)
Контрольные растворы: Этанол 15%, 20% и 25%
Тринатрийцитрат 10%
Вода для инъекций
Испытуемый материал был представлен сегментами, каждый по 1 сантиметру в длину, стерильных катетеров Chronoflex («сегментами катетера»). Используемые штаммы были staphylococcus aureus (золотистыми стафилококками) CIP 65.25 (метициллин-резистентными).
[0026] План исследования
[0027] Биопленки формировались в аэрируемых микроферментерах, с сегментами катетера, закрепленными на внутреннем съемном предметном стекле микроферментеров. Штаммы из фондов хранения в замороженном состоянии культивировали в триптиказо-соевом бульоне («TSB»). Для засевания микроферментеров, содержащих сегменты катетера, использовали инокулят в количестве 108 клеток. Для получения режима непрерывного потока через культуру применяли непрерывный поток 54 миллиметров в час («мл/ч») бульона TSB и постоянную аэрацию стерильным сжатым воздухом под давлением 0,3 бар (0,03 МПа). Через 24 часа инкубации, сегменты катетера извлекали из инкубатора и отделяли от соответствующего им устройства микроферментера. Затем, каждый сегмент катетера тщательно промывали в 1 мл физиологического раствора.
[0028] Для определения числа жизнеспособных клеток в биопленках, сформированных на сегментах катетера, до воздействия на них или помещения их в контакт с тест-растворами (т.е. до лечения), биопленки (в трех параллельных анализах для каждого штамма) ресуспендировали в TSB путем разрушения ультразвуком и интенсивного перемешивания. Выполняли последовательные разбавления полученных суспензий и высевали на соответствующие планшеты с агаровой средой, чтобы определять число жизнеспособных клеток после инкубации в течение ночи при 37 градусах Цельсия («°C»).
[0029] Параллельно, испытуемые сегменты катетера помещали в пробирку, содержащую 1 мл разных растворов замков: (i) этанол в концентрациях 15%, 20% и 25% (об.); (ii) тринатрийцитрат в концентрации 10% (об.); (iii) смешанные растворы этанола/тринатрийцитрата (15%-10%, 20%-10%, 25%-10% (об.)), в которых концентрации этанола равнялись 15%, 20% и 25%, и концентрация тринатрийцитрата была 10%; и (iv) воду для инъекций в качестве контрольного раствора. Для каждого организма эксперименты повторяли в трех параллельных анализах, и, в течение каждой обработки, испытуемые сегменты катетера подвергали воздействию разных растворов в течение 24 часов при 37°C. Затем, сегменты катетера извлекали, однократно споласкивали физиологическим раствором, и число прилипших жизнеспособных микроорганизмов определяли, как описано выше. На фиг. 1 число жизнеспособных клеток выражено числом колониеобразующих единиц («КОЕ»), и число бактерий выражено десятичным логарифмом, lg10. (Следует отметить: фиг. 1 представляет КОЕ как UFC, что является сокращением от unit formant colonie и является такой же единицей измерения, как и КОЕ). Предел обнаружения в экспериментальных условиях составляет 10 КОЕ на сегмент KT, поэтому порог обнаружения равен 10 КОЕ на сегмент KT. KT означает образец катетера, используемый при испытании, и его длина может быть в пределах от 3 до 5 сантиметров. KT может быть образцом катетера, который отрезан (обычно, длиной 1 метр) и помещен в устройство микроферментера так, чтобы на поверхности катетера формировалась биопленка. После того, как биопленка сформировалась и размещалась в контакте с испытуемым раствором замка катетера, получают измеренное число жизнеспособных бактериальных клеток, все еще присутствующих на поверхности катетера. Предел обнаружения равен 10 колониеобразующим единицам на один образец катетера.
[0030] Результаты
Таблица I
Примечание: Этанол обозначен как EtOH; тринатрийцитрат обозначен как цитрат.
[0031] Из данных, представленных в таблице I и на фиг. 1, видно, что один тринатрийцитрат в концентрации 10,0 масс./об. % не влиял на выживаемость бактерий. Кроме того, один EtOH в концентрации 15 об. % не осуществлял лизиса всех бактериальных клеток. Тем не менее, EtOH в концентрациях 15, 20 и 25 об. %, смешанный с тринатрийцитратом в концентрации 10 масс./об. %, вызывал полный лизис бактериальных клеток. Следует отметить, что порог обнаружения равен 10 КОЕ на сегмент KT, и потому наблюдение полного лизиса бактериальные клетки находится ниже порога обнаружения. Результаты предварительного тестирования предполагают, что значительного различия между 20 об. % и 25 об. % EtOH in-vitro не существуют. Однако, в реальной клинической практике, вследствие утечек, испарения и т.п., более высокая концентрация EtOH может создавать дополнительно усиленное противомикробное действие. Например, использование 20 об. % и 25 об. % EtOH дало более значительный результат лизиса бактерий, чем использование 15 об. % EtOH. Значительного различия между результатами лизиса бактерий при использовании 20 об. % и 25 об. % одного только EtOH не отмечается.
[0032] Окружающую среду, сохраняющую контакт с раствором замка катетера, который может содержать раствор TCEA, в течение предварительно заданного периода времени, можно именовать целевой окружающей средой. Целевая окружающая среда может находиться внутри, по меньшей мере, участка катетерной системы, например, в просвете катетерной системы. Таблица I показывает, что почти все болезнетворные бактерии и/или грибы, которые образовались в просвете катетера, могут уничтожаться после прихода в контакт с раствором TCEA, с почти полным устранением или полным устранением биопленки, содержащей бактерии и/или грибы. Раствор замка катетера оказывает как антикоагулянтное, так и противомикробное действие, в отличие от некоторых существующих растворов замков катетеров и видов терапии с применением замков катетеров, которые используют один гепарин или один тринатрийцитрат, применяемый в разных концентрациях от низкой до высокой. Более высокие концентрации тринатрийцитрата могут оказывать противомикробное действие, но могут иметь более сильные побочные действия на пациента, по сравнению с настоящим раскрытым раствором замка катетера.
[0033] Благоприятные действия настоящего раскрытого раствора замка катетера можно отнести на счет этиловоспиртового компонента, способного проникать в биопленку и уничтожать микроорганизмы, грибы и другие патогены посредством денатурирования белков. Хотя замечено, что этиловый спирт может оказывать антибиотическое действие, этиловый спирт не является антибиотиком. Таким образом, применение этилового спирта не повышает резистентность к противомикробным препаратам. Примерами микроорганизмов, уничтожаемых этиловым спиртом, могут включать в себя, но без ограничения, S. Aureus (золотистый стафилококк), S. Epidermidis (эпидермальный стафилококк), Klebsiella pneumonia (клебсиеллу пневмонии), P. Aeruginosa (синегнойную палочку), Candida spp. (дрожжеподобные грибы) и т.п. Кроме того, такая же или сходная дозировка может предотвращать или, по меньшей мере, задерживает коагуляцию хелатного комплекса ионов кальция с ионами цитрата в крови, чтобы прекращать свертывание крови.
[0034] Как описано выше, совместное использование тринатрийцитрата и этилового спирта в приведенных концентрациях для образования раствора TCEA производит неожиданный результат почти устранения или полного устранения биопленки и/или предотвращения, по меньшей мере, любого значительного формирования биопленки в целевой окружающей среде. Например, специалисты в данной области техники не ожидают, что такие низкие, как 25,0 об. %, концентрации этилового спирта покажут эффективные антибактериальные действия, не говоря уже об эффективности антибактериальных действий при концентрациях этилового спирта ниже, чем 25,0 об. %. Кроме того, как показано выше, результаты испытаний с различными сочетаниями тринатрийцитрата и этилового спирта не показывают нелинейной зависимости, связанной со сложением двух умеренных антибактериальных действий, и, в частности, никакой нелинейной зависимости, предполагающей, что какое-нибудь сочетание приведет к значительному антибактериальному действию. Кроме того, известные теории микробиологии или химии не предполагают синергических действий, связанных с антибактериальными свойствами, при сочетании тринатрийцитрата с этиловым спиртом таким образом.
[0035] Раствор замка катетера с этиловым спиртом в концентрациях всего или ниже, чем 25,0 об. % может быть также полезнее для катетера. Этиловый спирт может вызывать деградацию материалов, являющихся материалами, широко используемыми для изготовления катетеров, (например, силикона, полиуретана, полиэтилена, политетрафторэтилена, карботана и т.п.). Авторы настоящего изобретения обнаружили, что растворы с концентрациями, по меньшей мере, 70 об. % этилового спирта оказывали вызывающие деградацию материалов воздействия на материалы катетера. Поэтому, пониженные концентрации этилового спирта могут быть лучше с точки зрения деградации материалов. Например, применение раствора замка катетера с концентрациями этилового спирта всего или ниже, чем 25,0 об. % могут совсем не вызывать деградации материалов или, по меньшей мере, не вызывать такой деградации материалов, которая сокращает срок службы катетера. Минимизация или даже предотвращение деградации материалов, обусловленной раствором замка катетера, может поддерживать сохранность материалов и структурную целостность катетерной системы и, следовательно, не создавать непредвиденной деформации катетерной системы.
[0036] Раствор замка катетера с концентрациями этилового спирта всего ниже, чем 25,0 об. % может быть дополнительно выгоден для катетерной системы и/или пациента тем, что концентрации этилового спирта выше 25,0 об. % обычно могут вызывать возникновение преципитации белков плазмы крови, а возникновение преципитации белков плазмы крови приводит к повышенному риску нарушения работы катетера и/или образования эмболов. Кроме того, применение концентраций этилового спирта выше 25,0 об. % может вызывать другие побочные действия, например дискомфорт и болезненные ощущения у пациента (например, тошноту, головную боль, привкус спирта, угнетение дыхания и т.п.).
[0037] Раствор TCEA можно дополнительно применять для образования раствора замка катетера, имеющего уровень pH в пределах от 4,0 до 8,0, что также может быть полезно для катетерной системы, так как растворы, имеющие уровни pH за пределами приведенного диапазона могут вызывать деградацию материалов, составляющих материал катетера, и повышать риск непредвиденной деформации катетерной системы. Кроме того, уровни pH за пределами диапазона от 4,0 до 8,0 могут приводить к индуцированной преципитации, что может порождать нарушение работы катетерной системы и/или потенциальные опасности для пациента.
[0038] Раствор TCEA можно дополнительно применять для образования раствора замка катетера без добавления глицерилтринитратов («GTN»). Например, тринатрийцитрат является частично нерастворимым в этиловом спирте, и поэтому использование GTN может быть необязательно для сдерживания и/или уменьшения формирования осадка тринатрийцитрата в растворе замка катетера, имеющего концентрацию этилового спирта в пределах от 15,0 до 25,0 об. %. Таким образом, раствор замка катетера может быть образован без риска преципитации тринатрийцитрата, при этом раствор замка катетера содержит, максимально, 25,0 масс./об. % этилового спирта и не содержит GTN. Другими словами, раствор замка катетера, содержащий, по меньшей мере, некоторое количество раствора TCEA, можно применять в качестве антибактериального средства и/или антикоагулянтного средства, проявляющего любое из преимуществ или все преимущества, описанные в настоящей заявке, в целевой окружающей среде, при этом целевая окружающая среда не содержит GTN или, по меньшей мере, не содержит GTN, которые добавлялись бы для предотвращения образования осадка. Преимуществом отсутствия GTN в составе может быть образование раствора замка катетера с меньшим числом компонентов. Это может приводить к повышению эконмической выгоды при одинаковом лечебном действии. Кроме того, некоторые индивидуумы характеризуются аллергической реакцией на GTN, воздействия GTN на материал и свойства катетера не известны, и изготовление GTN может быть затруднительным.
[0039] Примерное исследование, проведенное авторами настоящего изобретения, касалось стабильности раствора замка катетера, содержащего 10,0 масс./об. % тринатрийцитрата и 25,0% этилового спирта. Кроме того, с такими же соотношениями компонентов провели испытание на ускоренное старение. Тринатрийцитрат может очень эффективно предотвращать тромбоз катетера (т.е. может быть эффективным антикоагулянтным средством). При приготовлении раствора замка катетера, авторы настоящего изобретения обнаружили, что тринатрийцитрат в меньших концентрациях может быть более растворимым в этиловом спирте. Кроме того, растворы тринатрийцитрата, имеющие концентрации от 30,0 масс./об. % и 46,7 масс./об. % могут значительно ослаблять размножение бактериальных клеток (т.е. могут быть эффективным антибактериальным средством), но не могут ликвидировать бактерии. Растворы этилового спирта, импеющие концентрацию 25,0 об. % могут подавлять образование, но не могут устранять зрелые биопленки (например, золотистых стафилококков). Растворы этилового спирта, имеющие концентрацию выше 40,0% могут подавлять размножение бактерий (т.е. могут быть эффективным антибактериальным средством). Растворы этилового спирта, имеющие концентрацию выше 60,0% могут обеспечивать полную ликвидацию жизнеспособных бактерий. Большую скорость уничтожения бактерий этиловым спиртом можно использовать, чтобы не давать бактериям прочно устраиваться на поверхности катетеров и, тем самым, предотвращать рост биопленки.
[0040] Во время исследования, раскрываемый раствор замка катетера испытывали для определения, может ли он уничтожать жизнеспособные бактерии и предотвращать возобновление роста биопленки. (Смотри фиг. 2). Раствор замка катетера испытывали на золотистом стафилококке (метициллин-резистентном). Растворы с одним только тринатрийцитратом (10 масс./об. %) не оказывали влияния на выживаемость бактерий. Растворы с одним только EtOH (15 об. %) не обеспечивали лизис всех бактериальных клеток. Растворы, содержащие смесь EtOH (15 об. %), смешанного с тринатрийцитратом (10 масс./об. %), вызывали полный лизис бактериальных клеток (до уровня ниже порога обнаружения).
[0041] В процессе разработки примерного препарата, авторы настоящего изобретения приготовили двенадцать растворов, содержащих 10,0 масс./об. % тринатрийцитрата, 25,0 об. % этанола и разные количества лимонной кислоты. В качестве контрольных растворов приготовили также отдельные растворы, содержащие 10,0 масс./об. % тринатрийцитрата (растворяли 25 грамм тринатрийцитрата в 125 миллилитрах воды и регулировали уровень pH в пределах от 5,0 до 7.0; доводили водой объем до 250 миллилитров) и 25,0 об. % этилового спирта (добавляли 125 миллилитров этилового спирта в 500-миллиметровый пикнометр (VF) и доливали водой). Уровни pH и значения показателя преломления («RI») измеряли через некоторые интервалы на протяжении приготовлений образцов, результаты которых представлены в таблице II.
Таблица II
[0042] Процедуру исследования стабильности вышеописанных примерных препаратов выполняли следующим образом.
Подготовка шприца и пакета:
Шприц наполняли вручную и закручивали колпачки
Использовали существующие упаковочные материалы компании DuraLock-C (приемники/пакеты)
Приемники/пакеты маркировали
Пакеты содержали 5/2,5-мл шприцы
Подготовили всего 25 шприцов на каждый контрольный момент времени. В сумме 75 шприцов для каждого испытуемого раствора.
Шприцы: 1-15: 3-мл шприцы Sanxin с красными колпачками Sanxin
Шприцы: 16-25: 3-мл шприцы BD с синими колпачками Vitalmed
Всего 15 пакетов для каждой подготовки образца
Пакеты герметизировали
Стерилизованные образцы:
Образцы стерилизовали гамма-излучением
После возврата в приемники, пакеты и образцы проверяли на наличие какого-либо осадка
Образцы помещали в камеру (условия):
Образцы помещали в камеру при 40°C/не более, чем 25% относительной влажности
Контрольными моментами времени при ускоренном старении являются 0 месяцев, 3 месяца, и 6 месяцев
Температура и влажность, контролируемые в камере
T0=0 месяцев, T3=3 месяца, T6=6 месяцев
[0043] На фиг. 3A-3D и в таблице Table III представлены результаты для двенадцати примерных составленных растворов. Как можно видеть, при добавлении тринатрийцитрата, уровень pH снижается, RI (показатель преломления) повышается, и плотность повышается. Статистически значимого отличия по плотности (суммы концентрации компонентов по массе в растворе) образцов T3 от образцов T0 не было. Внешне растворы были прозрачными (т.е. образцы T0 и образцы T3 имели прозрачность как у воды). Извлекаемый объем для образцов T0 был, в 25 из 25 выполнений, >2,5 мл. Извлекаемый объем для образцов T3 был, в 23 из 25 выполнений, >2,5 мл. Колпачки не уплотнялись надлежащим образом, и на внешней поверхности колпачка образовалась соль. Таким образом, результаты предполагают, что раствор с 10 масс./об. % тринатрийцитрата и 25 об. % этанола остается стабильным и растворимым по прошествии трех месяцев (ускоренный срок=1 год реального времени).
Таблица III
[0044] Как описано выше, различные раскрытые растворы замка катетера и виды терапии с применением замков катетеров можно применять для предотвращения или смягчения нарушения работы катетера. Одной формой нарушения работы катетера является образование закупорки катетера. Закупорки могут происходить в любое время в течение катетеризации и/или в любое время в течение проведения лечения через катетерную систему. Например, стержень катетера, вставленный в тело пациента, может оказаться покрытым плазмой и фибрином, при этом тромбоциты и лейкоциты начинают прилипать к стержню, создавая возможность образования колоний бактерий, дополнительного образования фибрина, свертывания крови и, затем, тромбоза. Тромбообразование может происходить в просвете катетера, на поверхности наконечника катетера и/или вблизи от наконечника катетера, что приводит к нарушению работы катетера вследствие закупорки. После образования на поверхности, формирующий закупорку тромб может прилипать к внутренней поверхности и/или наружной поверхности катетерной системы, при этом тромб препятствует потоку внутри катетерной системы. Закупорка внутри катетерной системы может происходить, где кровь и/или существующие эмболы оттекают обратно внутри просвета через наконечник, что приводит к преграждению потока. Применение растворов замка катетера, содержащих TCEA, может предотвращать или, по меньшей мере, значительно снижать риск закупорок типа тромбов посредством подавления тромбообразования, как описано выше.
[0045] Закупорки могут также возникать в результате преципитации белков плазмы крови, преципитации твердых частиц из компонентов раствора замка катетера, преципитации твердых частиц из составляющих для проведения лечения, применяемого с катетерной системой, и других механизмов формирования осадка. Упомянутые осадки могут порождать закупорки подобно тому, как описано выше. Упомянутые осадки, равно как и тромбообразования, также могут приводить к потенциальным опасностям для пациента, даже если из них не сформировалось никакой закупорки. Например, образовавшийся осадок и/или образовавшийся тромб могут проникнуть в кровоток и вызвать эмболию. Применение растворов замка катетера, содержащих раствор TCEA, может предотвращать или, по меньшей мере, значительно снижать риск образования осадка, как описано выше.
[0046] Раскрываются диапазоны изменения концентраций для каждого компонента раствора TCEA. Диапазоны раскрываются потому, что предполагается, что относительные концентрации тринатрийцитрата и этилового спирта будут обеспечивать различные требуемые действия. Например, хотя меньшая концентрация этилового спирта может быть, в общем, полезнее для уменьшения деформации катетерной системы, снижения риска преципитации и ослабления других побочных действий, этиловый спирт проявляет выраженную эффективность при уничтожении многих типов микроорганизмов, без приобретения данными организмами резистентности к противомикробному действию этилового спирта. Таким образом, концентрация этилового спирта вблизи верхней границы диапазона (например, вблизи 25,0 об. %) может быть необходима для максимального усиления антибактериальных действий, а концентрация этилового спирта вблизи нижней границы диапазона (например, вблизи 15,0 об. %) может быть необходима для минимизации дискомфорта пациента или деформации катетерной системы. Для согласования с состоянием пациента и типом катетерной системы можно использовать другие относительные концентрации компонентов.
[0047] В качестве примера, отношения в пределах диапазона могут включать в себя 10,0 масс./об. % тринатрийцитрата и 20,0 об. % этилового спирта, которые могут создавать раствор замка со сравнительно менее сильным противомикробным действием. В качестве другого примера, 10,0 масс./об. % тринатрийцитрата и 25,0 об. % этилового спирта можно использовать для образования раствора замка со сравнительно более сильным противомикробным действием.
[0048] Терапия с применением замка катетера может включать в себя способ применения с раствором замка катетера для обеспечения любого из требуемых действий на целевую окружающую среду. Терапия с применением замка катетера может включать в себя введение раствора замка катетера внутрь просвета, при этом целевой окружающей средой являются объем, ограниченный просветом, и/или внутренняя поверхность просвета. В некоторых вариантах осуществления раствор замка катетера можно вводить внутрь просвета в то время, когда катетер не используют для проведения лечения пациента (например, между сеансами диализа катетерной системы, используемой для гемодиализа). Терапия с применением замка катетера может дополнительно включать в себя этап промывки, этап применения положительного давления и т.п.
[0049] Как описано выше, применение раствора замка катетера не должно ограничиваться применением с катетерной системой. Например, способ применения может включать в себя способ очистки от биопленки посредством введения раствора, включающего в себя тринатрийцитрат и этиловый спирт, в целевую окружающую среду и сохранения контакта между раствором тринатрийцитрата и этилового спирта и целевой окружающей средой, чтобы обеспечить, по меньшей мере, что-то одно из предотвращения формирования биопленки и устранения биопленки, которая сформировалась в целевой окружающей среде.
[0050] В примерном варианте осуществления катетерную систему можно сначала промыть некоторым объемом воды, 0,9% водного раствора хлорида натрия или физиологическим раствором, чтобы достаточно удалить продукты распада, фибрин, осадки и другие отложения (например, липидов, лекарств и т.п.), которые могут существовать внутри катетерной системы. Объем промывочной жидкости может составлять, приблизительно, 5,0-10 мл, но, в общем, будет зависеть от катетерной системы и условий целевой окружающей среды. Затем, в катетерную систему можно ввести некоторый объем раствора замка катетера, который может быть ограничен просветом, ограничен другим участком катетерной системы или введен во всю катетерную систему целиком. Раствор замка катетера можно оставлять находящимся (или выдерживать) в целевой окружающей среде в течение предварительно заданного периода времени. В качестве альтернативы или дополнительно, раствор замка катетера можно оставлять находящимся в целевой окружающей среде, чтобы поддерживать раскрытое состояние просвета, раскрытое состояние наконечника и/или раскрытое состояние другого участка катетерной системы. В общем, это будет зависеть от целевой окружающей среды, катетерной системы и соответственных компонентов раствора TCEA.
[0051] В общем, объем раствора замка катетера, используемый для данной терапии с применением замка катетера, может быть количеством, которое будет обеспечивать достаточный контакт с целевой окружающей средой, чтобы получать требуемый результат. Данное количество раствора замка катетера может быть количеством, которое будет обеспечивать, чтобы достаточный контакт между раствором замка катетера и целевой окружающей средой поддерживался в течение предварительно заданного периода времени. Например, данное количество раствора замка катетера может быть количеством, которого будет достаточно для заполнения всего просвета катетера, при условии, что просвет является целевой окружающей средой. Например, 0,03 мл раствора замка катетера можно использовать для заполнения просвета периферического катетера, 0,4 мл раствора замка катетера можно использовать для заполнения просвета среднего катетера диаметром 4 Френч (4/3 мл) и т.п. Кроме того, если целевой окружающей средой является катетерная система в целом, а не только просвет, и катетерная система включает в себя дополнительный участок (например, порт венозного доступа), то возможно включение объема резервуара порта и любых других соединительных частей порта. Кроме того, если раствор замка катетера может вытекать из катетерной системы, то терапия с применением замка катетера может включать в себя введение дополнительного раствора замка катетера, чтобы обеспечивать поддерживание достаточного контакта между раствором замка катетера и целевой окружающей средой в течение требуемого периода времени. Например, если целевой окружающей средой является просвет, и раствор замка катетера может вытекать из целевой окружающей среды, то может выполняться введение дополнительных 15-20% раствора замка катетера сверх количества, необходимого для заполнения просвета.
[0052] Период времени, в течение которого раствор замка катетера остается или выдерживается внутри катетерной системы, может зависеть от многих факторов. В общем, период времени будет сроком, в течение которого катетерная система не используется для проведения лечения. Применение раствора замка катетера таким образом можно назвать «запиранием катетера». При типичном сеансе диализа, период времени между сеансами может быть 12-24 часов, и, следовательно, раствор замка катетера может выдерживаться внутри катетерной системы течение данного срока.
[0053] Дополнительный этап промывки можно выполнять после запирания катетера и/или перед проведением лечения через катетерную систему. Например, раствор замка катетера можно аспирировать из катетерной системы методами промывки, подобными описанным выше. Аспирацию можно выполнять, чтобы «обновить» раствор замка катетера (т.е. вымыть раствор замка катетера и ввести ввести большее количество такого же или другого раствора замка катетера). Аспирацию можно дополнительно выполнять для подготовки катетерной системы к проведению лечения пациента (например, проведению лекарственного лечения). Если раствор замка катетера можно вводить в кровоток без риска причинения вреда пациенту, то аспирацию можно не выполнять (т.е. раствор замка катетера можно протолкнуть в кровоток пациента вместо извлечения из катетерной системы, без выпуска в кровоток). Введение раствора TCEA в кровоток можно выполнять при минимальных побочных воздействий на пациента, и, следовательно, аспирация может не входить в терапию с применением замка катетера, если аспирацию выполнять нежелательно. Это объясняется тем, что раствор замка катетера, содержащий раствор TCEA, не может значительно повышать риск токсического воздействия на пациента, при выпуске в кровоток пациента.
[0054] Хотя предполагается, что целевая окружающая среда должна находиться внутри, по меньшей мере, участка просвета катетерной системы, целевая окружающая среда может быть любым участком катетерной системы (например, внешней поверхностью стержня катетера, участком фильтра, участком пневмокамеры, резервуаром порта венозного доступа и т.п.) и/или объемом пространства снаружи катетерной системы (например, внутри тела пациента и снаружи катетерной системы). Например, раствор замка катетера может быть токсичным, и поэтому соответствующую терапию с применением замка катетера можно разработать так, чтобы блокировать раствор замка катетера от проникновения в кровоток путем его удерживания внутри катетерной система, если только не выполняется контролируемое вымывание (т.е. аспирация) из катетерной системы. В некоторых вариантах осуществления терапия с применением замка катетера может быть такой, чтобы раствор замка катетера удерживался в локальной области конкретной биопленки, которое областью внутри катетерной системы (например, внутри просвета, внутри фильтра и т.п.). В других вариантах осуществления раствор замка катетера может быть менее токсичным или даже нетоксичным, и поэтому можно разработать терапию с применением замка катетера, допускающую введение, по меньшей мере, небольшого количества раствора замка катетера в кровоток (намеренно или случайно), без причинения повреждения или вреда пациенту. В дополнительных вариантах осуществления можно разработать терапию с применением замка катетера, обеспечивающую проникновение раствора замка катетера в кровоток, чтобы проводить лечение в той или иной форме.
[0055] Дополнительные варианты осуществления могут включать в себя режимы промывки, запирания, аспирации и/или обновления. Данные режимы могут включать в себя обновление раствора замка катетера через заданные периоды времени, при этом катетерная система заперта и не использовалась в течение длительного периода времени. Например, в случае типичного сеанса диализа, катетерную систему можно промыть после сеанса диализа, затем запереть на период 12-24 часов, с обновлением, при этом, раствора замка катетера через каждые 8 часов, и затем снова промыть, чтобы подготовить катетерную систему для последующего лечения, связанного с диализом, после периода запирания.
[0056] Дополнительные варианты осуществления могут включать в себя раствор замка катетера, предварительно заправленный в стерилизованные шприцы, при этом каждый шприц в первом наборе шприцов содержит первый окрашенный колпачок, и каждый шприц во втором наборе шприцов содержит второй окрашенный колпачок. В качестве примера, первый цвет может быть красным, и второй цвет может быть синим. Красный(ые) колпачок(ки) можно использовать для обозначения шприца(ов), предназначенного(ых) для использования с катетерами, предназначенными для артериальных просветов. Синий(ие) колпачок(ки) можно использовать для обозначения шприца(ов), предназначенного(ых) для использования с катетерами, предназначенными для венозных просветов.
[0057] Дополнительные варианты осуществления терапии с применением замка катетера могут включать в себя применение положительного давления в катетерной системе, чтобы сдерживать и/или предотвращать втекание крови или другого материала в катетерную систему. Например, можно использовать методы, обеспечивающие проявление положительного перепада давления внутри катетерной системы перед прекращением проведения лечения, чтобы минимизировать, тем самым, риск втекания крови, когда проведение лечения заканчивается. Применение положительного давления возможно также до и/или после каждой стадии режима терапии с применением замка катетера.
[0058] Примерные растворы будут тестироваться для оценки характеристик противодействия биопленкам смеси этанола 25% с цитратом (от 5 до 15%) применительно к формированию биопленки и зрелым биопленкам, с использованием нескольких репрезентативных патогенов. Испытания для получения таких результатов представлены в двух примерах.
Пример I
Испытуемые растворы:
Этанол 25% (об.)+тринатрийцитрат 5% - 10% и 15%
Контрольные растворы: Этанол 25%, тринатрийцитрат 5%, тринатрийцитрат 10%, тринатрийцитрат 15%, физиологический раствор
Испытуемый материал:
Сегменты (каждый длиной 1 см) стерильных катетеров (из материалов ChronoflexTM, CarbothaneTM, силикона, TecothaneTM и Pellethane®).
Штаммы:
Staphylococcus epidermidis (эпидермальный стафилококк) CIP 68.21
Staphylococcus aureus (золотистый стафилококк) CIP 65.25 (метициллин-резистентный)
Pseudomonas aeruginosa (синегнойная палочка) ATCC 27853
Klebsiella pneumoniae (клебсиелла пневмонии) LM21
Candida albicans (дрожжеподобные грибы) SC5314
[0059] Бактериальные штаммы выращивают в лизогенном бульоне (LB) и минимальной среде (M63B1), и грибковые виды выращивают в 0,67% основе азотного агара для классификации дрожжей (Yeast Nitrogen Based (YNB), DifcoTM), дополненной 0,4% глюкозой.
[0060] Измерение действия на зрелую биопленку (с возрастом 24 часа)
[0061] Биопленки формируют в аэрируемых микроферментерах, как описано в «Natural conjugative plasmids induce bacterial biofilm development» by Ghigo JM, Nature, 2001 Jul 26; 412(6845):442-5. Биопленки формируются на сегментах катетера, закрепленных на внутренних съемных предметных стеклах микроферментеров. Штаммы из фондов хранения в замороженном состоянии культивировали в среде M63B1 с добавлением 0,4% глутамата (Glu) или YNB с добавлением 0,4% Glu в течение ночи. Для засевания микроферментеров, содержащих сегменты катетера, использовали инокулят в количестве 109 бактерий палочковидных бактерий, 108 кокков или 107 клеток Candida albicans. Для получения режима непрерывного потока через культуру применяли непрерывный поток 100 мл/ч либо среды M63B1 с добавлением 0,4% Glu (бактериальные штаммы), либо среды YNB с добавлением 0,4% Glu (дрожжевые грибы) и постоянную аэрацию стерильным сжатым воздухом (0,3 бар (0,03 МПа). Такая интенсивная подача свежей среды исключает заметный рост планктона. Через 24 часа инкубации, сегменты извлекали из инкубатора и отделяли от устройства.
[0062] Затем, каждый сегмент катетера тщательно промывали в 1 мл физиологического раствора. Для определения числа жизнеспособных клеток в биопленках, сформированных на сегментах катетера, биопленки (в трех параллельных анализах для каждого штамма) ресуспендировали в 5 мл минимальной среды M63B1 или среды YNB путем разрушения ультразвуком и интенсивного перемешивания. Выполняли последовательные разбавления полученных суспензий и высевали на соответствующие планшеты с агаровой средой, чтобы определять число жизнеспособных клеток [колониеобразующих единиц (КОЕ)] после инкубации в течение ночи при 37°C. Число бактерий выражено десятичным логарифмом (lg10).
[0063] Предел обнаружения в экспериментальных условиях равен 1,6·lg10 (40 КОЕ) на сегмент KT. Параллельно, испытуемые сегменты помещают в пробирки, содержащие 1 мл разных растворов замка: (i) этанол 25%, (ii) тринатрийцитрат 5%, 10%, 15%, (iii) смешанные растворы этанола/цитрата (25%-5%, 25%-10%, 25%-15%) и (iv) 0,9% хлорид натрия в качестве контрольного раствора. Для каждого организма, эксперименты повторяли в трех параллельных анализах, и, в течение каждой обработки, испытуемые сегменты катетера подвергают воздействию разных растворов в течение 4, 24 и 48 часов при 37°C. Затем, сегменты катетера извлекают, однократно споласкивают физиологическим раствором, и число прилипших жизнеспособных микроорганизмов (КОЕ) определяют, как описано выше.
Пример II
Испытуемые растворы:
Этанол 25% (об.)+тринатрийцитрат 5% - 10% и 15%
Контрольные растворы: Этанол 25%, тринатрийцитрат 5%, тринатрийцитрат 10%, тринатрийцитрат 15%, физиологический раствор
Испытуемый материал:
Сегменты (каждый длиной 1 сантиметр) стерильных катетеров (из материалов ChronoflexTM, CarbothaneTM, силикона, TecothaneTM и Pellethane®).
Штаммы:
Staphylococcus epidermidis (эпидермальный стафилококк) CIP 68.21
Staphylococcus aureus (золотистый стафилококк) CIP 65.25 (метициллин-резистентный)
Pseudomonas aeruginosa (синегнойная палочка) ATCC 27853
Klebsiella pneumoniae (клебсиелла пневмонии) LM21
Candida albicans (дрожжеподобные грибы) SC5314
[0064] Измерение действия на формирования биопленки
[0066] Растворы: (i) этанол 25%, (ii) тринатрийцитрат 5%, 10%, 15%, (iii) смешанные растворы этанола/цитрата (25%-5%, 25%-10%, 25%-15%) и (iv) 0,9% хлорид натрия в качестве контрольного раствора.
[0066] Сегменты катетера (каждый длиной 1 см) помещали в 24-луночные планшеты.
[0067] Контрольные растворы и растворы-замки засевали бактерийными/грибковыми суспензиями, чтобы получить мутность, эквивалентную мутности 0.5 по стандарту МакФарланда (начальные плотности 1×106 КОЕ/мл, разбавление 1/100) в бульоне LB (бактерии) или среде YNB с добавлением 0,4% Glu (грибы).
[0068] 0,5 мл раствора замка (или контрольного раствора) с инокулятом вносят в каждую лунку, содержащую сегменты. Планшеты помещают на встряхиватель с 90 об/мин и инкубируют при 37°C в течение 72 ч. Каждые 24 ч питательную среду пополняют свежим питательным раствором для поддержки развития микроорганизма в устройстве.
[0069] Для определения обсемененности бактериями на каждом сегменте катетера через 72 ч, сегменты переносили в лунки, наполненные 500 мкл физиологического раствора, и помещали обратно на встряхиватель на 1 мин, чтобы удалить остаточные организмы с поверхностей сегментов.
[0070] Затем сегменты помещали в 0,5 мл физиологического раствора и облучали ультразвуком в течение 5 мин, чтобы разрушить любую биопленку. Образцы из полученного раствора высевали на планшеты с агаровой средой LB и инкубировали в течение 72 ч. Планшеты проверяли через каждые 24 ч на наличие жизнеспособных колоний. Нижний предел обнаружения равен 1,6 lg10 (40 КОЕ). Все штаммы тестировали в двух параллельных анализах в отдельные дни.
[0071] С учетом вышеизложенных принципов изобретения, специалистам в данной области техники будет очевидно, что возможны многочисленные модификации и варианты описанных примеров и вариантов осуществления. Раскрытые примеры и варианты осуществления представлены только для иллюстрации. Другие альтернативные варианты осуществления могут включать в себя некоторые или все признаки, раскрытые в настоящей заявке. Поэтому, цель состоит в охране всех таких модификаций и альтернативных вариантов осуществления, которые могут находиться в пределах истинного объема настоящего изобретения, который должен быть задан как полный объем охраны настоящего изобретения. Кроме того, раскрытие диапазона значений означает раскрытие каждого числового значения в пределах данного диапазона, включая конечные точки.



Изобретение относится к области медицины, а именно к способу обработки катетеров от биоплёнки. Способ обработки от биопленки, содержащий следующие этапы: вводят раствор, содержащий 4,0-15,0 массо-объемных % («масс./об. %») тринатрийцитрата и 15,0-25,0 об/об. % этилового спирта, в целевую окружающую среду; и поддерживают контакт между раствором и целевой окружающей средой, чтобы обеспечить по меньшей мере одно из предотвращения формирования биопленки и устранения биопленки, которая сформировалась в целевой окружающей среде; и при этом целевая окружающая среда свободна от осадка тринатрийцитрата, при этом раствор имеет уровень pH в диапазоне от 4,0 до 8,0, причем целевая окружающая среда является по меньшей мере участком катетерной системы, причем раствор не содержит глицерилтринитратов (GTN). Вышеуказанное изобретение позволяет предотвратить формирование биоплёнки и/или устранить биоплёнку, сформировавшуюся внутри катетерной системы, и таким образом значительно снизить риски, связанные с инфекциями кровотока, нарушением работы катетерной системы, образованием эмболов, дискомфортом для пациента и заболеванием пациента. 12 з.п. ф-лы, 6 ил., 3 табл., 2 пр.
1. Способ обработки от биопленки, содержащий следующие этапы:
вводят раствор, содержащий 4,0-15,0 массо-объемных % («масс./об. %») тринатрийцитрата и 15,0-25,0 об/об. % этилового спирта, в целевую окружающую среду; и
поддерживают контакт между раствором и целевой окружающей средой, чтобы обеспечить, по меньшей мере, одно из предотвращения формирования биопленки и устранения биопленки, которая сформировалась в целевой окружающей среде; и
при этом целевая окружающая среда свободна от осадка тринатрийцитрата, при этом
раствор имеет уровень pH в диапазоне от 4,0 до 8,0,
причем целевая окружающая среда является, по меньшей мере, участком катетерной системы,
причем раствор не содержит глицерилтринитратов (GTN).
2. Способ по п. 1, в котором этап поддержки контакта может создавать стерильную целевую окружающую среду, которая не содержит средства, повышающего свертываемость крови.
3. Способ по любому из пп. 1, 2, в котором целевая окружающая среда не содержит глицерилтринитратов («GTN»).
4. Способ по любому из пп. 1-3, в котором раствор не содержит гепарина.
5. Способ по п. 1, в котором этап поддержки контакта может предотвращать тромбообразование внутри катетерной системы.
6. Способ по любому из пп. 1-5, дополнительно содержащий аспирацию раствора после этапа поддержания контакта.
7. Способ по любому из пп. 1-6, дополнительно содержащий, по меньшей мере, один этап из следующих:
обеспечивают поступление по меньшей мере части раствора в кровоток пациента после этапа поддержания контакта; и
продвигают по меньшей мере часть раствора для поступления в кровоток пациента после этапа поддержания контакта; и
при этом поступление раствора в кровоток не подвергает пациента риску токсичного воздействия.
8. Способ по любому из пп. 1-7, дополнительно содержащий промывку, по меньшей мере, участка катетерной системы перед введением раствора.
9. Способ по любому из пп. 1-8, дополнительно содержащий обновление раствора после того, как прошел предварительно заданный период времени в течение этапа поддержки контакта.
10. Способ по любому из пп. 1-9, дополнительно содержащий применение положительного давления внутри, по меньшей мере, участка катетерной системы в течение, по меньшей мере, одного периода из до этапа введения и после этапа поддержки контакта.
11. Способ по любому из пп. 1-10, в котором введение раствора содержит введение водного раствора, содержащего 8,0-12,0 массо-объемных % тринатрийцитрата и 18,0-22,0 об/об. % этилового спирта.
12. Способ по любому из пп. 1-11, в котором введение раствора содержит введение водного раствора, содержащего 8,0-12,0 массо-объемных % тринатрийцитрата и 23,0-25,0 об/об. % этилового спирта.
13. Способ по любому из пп. 1-12, в котором введение раствора содержит введение водного раствора, содержащего 4,0-10,0 массо-объемных % тринатрийцитрата и 25,0 об/об. % этилового спирта.
| US 6679870 B1, 20.01.2004 | |||
| TАKLA T | |||
| ET AL, Effectiveness of 30% ethanol/4 % trisodium citrate locking solution in preventing biofilm formation by organisms causing haemodialysis catheter-related infections // Journal of antimicrobial chemotherapy, Oxford university press, vol.62, no.5, 2008, p.1024-1026 | |||
| US 20050215978 A1, 29.09.2005 | |||
| РАСТВОР ЗАМКА КАТЕТЕРА, СОДЕРЖАЩИЙ ЦИТРАТ И ПАРАБЕН | 2006 |
|
RU2399375C2 |
Авторы
Даты
2022-11-22—Публикация
2017-02-06—Подача