Изобретение относится к медицине, а именно к хирургической стоматологии и челюстно-лицевой хирургии, и может быть применимо для пластики соустья верхнечелюстной пазухи и полости рта, возникшего при удалении первого или второго моляра верхней челюсти.
Перфорация дна полости верхнечелюстного синуса является одним из наиболее распространенных осложнений, возникающих непосредственно в ходе операции удаления больших коренных зубов на верхней челюсти. Возникающее вследствие этого сообщение между полостью рта и полостью носа необходимо как можно скорее устранить, наиболее оптимальным способом, сохраняющим оригинальную архитектонику мягких тканей и способствующим полному восстановлению костной ткани альвеолярного отростка верхней челюсти. На сегодняшний день существуют способы пластики перфораций верхне-челюстного синуса, многие из которых имеют лишь незначительные различия в технике проведения. Все они преследуют цель: закрытие перфорационного отверстия, недопущение рецидивов, предупреждения формирования ороантральных соустий и свищей, и, как следствие, лечение одонтогенного перфоративного верхнечелюстного синусита.
Все эти методы можно подразделить на три основные группы:
1 - пластика местными тканями;
2 - пластика с использованием аутотрансплантатов;
3 - пластика с использованием различных синтетических, аллогенных или ксеногенных материалов.
Однако каждый из данных методов имеет множество недостатков.
Существует метод закрытия перфорации верхнечелюстного синуса коронарно смещенным лоскутом со щеки (Губайдуллина Е.Я., Анютин Р.Г., Анютин Р.Г., А.Н. Дорошенко, А.А. Мосейко) «Одонтогенные свищи верхнечелюстной пазухи»: автореф. дис. … канд. мед. наук / Е.Я. Губайдуллина. - М., 1959. - 19 с.
На этапах проведения этого метода над лункой удаленного зуба выкраивают трапециевидный лоскут. Лоскут отсекают от надкостницы (для лучшей мобилизации и перемещения в область дефекта). Далее - ставший мобильным лоскут перемещают на небную поверхность и фиксируют швами.
Недостатком метода является вероятность ишемии трансплантата, вследствие малого размера питающей ножки. Кроме того, данный метод предполагает сильную мобилизацию мягких тканей альвеолярного отростка верхней челюсти с вестибулярной стороны, что влечет за собой потерю прикрепленной кератинизированной десны, и как следствие, проблемы с пародонтом соседних здоровых зубов при их наличии и/или ухудшается архитектоника протезного ложа при беззубом альвеолярном отростке. Кроме того, этот метод пластики обеспечивает только мягкотканую регенерацию в области перфорации.
Существует способ, в котором авторы (Н.А. Каримкулов, Д.Е. Мухаммаджонова Устранение перфорации гайморовой пазухи с пластикой надкостнично-субэпителиальным небным лоскутом на ножке / Н.А. Каримкулов, Д.Е. Мухаммаджонова. - Текст: непосредственный // Молодой ученый. - 2018. - №26 (212). - С.69-72. - URL: https://moluch.ru/archive/212/51848/ (дата обращения: 19.08.2021)) предлагают в преддверии рта выкраивать толстый слизисто-надкостничный лоскут, деэпителизировать его конец, и подвести его под
отслоенную слизистую оболочку у лунки с небной стороны, и после этого фиксировать швами к краю перфорации.
Данный способ обладает так же рядом недостатков: 1 - постоянное натяжение лоскута нарушает его кровоснабжение; 2 - значительная травматизация тканей вследствие широкого разреза и отсепаровки надкостницы при формировании трапециевидного лоскута; 3 - тканевой экссудат в послеоперационном периоде давит на раневую поверхность лоскута, препятствуя нормальному его приживлению; 4. - не формируется внутренняя эпителиальная выстилка со стороны синуса, в результате заживления в области внутреннего отверстия свища образуется рубец, лишенный эпителия и, как следствие, нарушается мукоциллиарный транспорт в синусе. Минусом данной методики является возникновение складки слизистой оболочки, которая может явиться препятствием для протезирования, особенно с использованием съемного пластиночного протеза, наличие длительных парестезий отдельных областей средней зоны лица в послеоперационном периоде.
Есть сообщение о применении мембраны из пчелиного воска, (Погосян Ю.М., Бурназян С.С., Погосян А.Ю., Хачатрян Г.Э./ Клиническое обоснование применения мембраны из пчелиного воска при комплексном лечении хронических гайморитов - 'Вестник Хирургии Армении" им. Г.С. Тамазяна, N1, 2011 г. Трехмесячный научно-практический журнал. - с 77 -83) в сочетании с богатой тромбоцитами плазмой, с целью пластического закрытия одонтогенной перфорации верхнечелюстного синуса. Суть метода: для разграничения полости синуса с полостью рта применяется мембрана из пчелиного воска, лунка удаленного зуба заполняется богатой тромбоцитами плазмой в комбинации с аллогенным размельченным аллогенным деминерализованным костным материалом. Со стороны полости рта выкраивается привычный трапециевидный слизисто-надкостничный лоскут, и фиксируется к слизистой оболочке небного края лунки.
Относительно недавно предложены варианты пластики перфорации верхнечелюстного синуса с использованием синтетических остеопластических (Зекерьяев Р.С., Сирак С.В. Опыт использования остеопластических материалов для пластики дефекта альвеолярного отростка верхней челюсти при перфорации верхнечелюстного синуса // Научное обозрение. Медицинские науки. - 2014. - №1. - С.126-126; URL: https://science-medicine.ru/ru/article/view?id=180 (дата обращения: 23.08.2021) материалов на основе коллагена, и резорбируемых коллагеновых мембран. Суть данного метода в том, что в перфоративный канал помещается остеопластический материал (коллапан, остеодант К, Biooss, и пр.). Непосредственно перфорация при этом ушивается по какой-либо стандартной методике. Преимущества данного метода состоит в возможность восстановления костной ткани в области перфорации. Недостатком является некотролируемая миграция в полость синуса гранул остеопластического материала, что, учитывая высокую склонность большинства материалов к воспалению, может привести к развитию хронического или острого ятрогенного верхнечелюстного синусита, возможно с формированием стойкого свища.
Существует модификация данного метода с использованием коллагеновых резорбируемых мембран, в попытке герметизации полости синуса вводимых в перфоративный канал и фиксируемых к Шнейдеровой мембране. Однако учитывая сложность фиксации мембраны к слизистой оболочке синуса, а также возможную бионесовместимость с организмом больного, полностью исключить миграцию инородных тел в синус, исключить не возможно. Кроме того, последующее закрытие перфорации с мобилизацией местных тканей приводит, как уже сказано выше к уменьшению области прикрепленной кератинизированной десны.
Наиболее близким по сути, взятым за прототип, является способ «Применения свободного аутогенного костного трансплантата при хирургическом лечении одонтогенных синуситов с ороантральным
сообщением» (О. Маланчук, Ш.Ю. Гарляускайте, Д.Н. Кеян. Применение свободного аутогенного костного трансплантата при хирургическом лечении одонтогенных синуситов с ороантральным сообщением // "Вюник стоматологи ", 2012 - №3. - с. 65-68.), предложенный О. Маланчук, Ш.Ю. Гарляускайте, Д.Н. Кеян в 2012 году. К недостаткам применения свободного аутогенного костного трансплантата относится наличие донорской зоны, т.е. двух операционных полей - дополнительная травматизация пациента, ограниченность объема необходимого пластического материала, трудоемкость его выделения.
Основным недостатком всех выше перечисленных методов пластики перфорации (соустья) верхнечелюстного синуса является то, что ни в одном из предложенных способов не происходит восстановления непрерывности зубного ряда и восстановления жевательной эффективности.
Метод аутотрансплантации третьего моляра является одним из возможных решений при необходимости заменить отсутствующий зуб бокового ряда. Преимущества метода: эстетика, сохранение формы зубной дуги и ее целостности, рост и развитие, и функционирование челюстно-лицевой области без аномалий, сохранение жевательной функции, нормальная речь, возможность избежать использования чужеродных материалов для восстановления жевательной эффективности.
Проведенный поиск показал отсутствие в отечественной литературе и зарубежной научной литературе сочетания способов аутотрансплантации третьего моляра и пластики соустья (перфорации) верхнечелюстного синуса. Аутотрансплантация третьего моляра - альтернатива традиционным методам пластики перфорации верхнечелюстного синуса при условии подходящего зуба-донора.
Задачей изобретения является создание способа пластики перфорации (соустья) верхнечелюстного синуса, возникшего в результате
удаления первого или второго моляра верхней челюсти, с использованием аутотрансплантации третьего моляра и «аутомембраны» PRF или APRF, восстановление жевательной эффективности и непрерывности зубного ряда, проведение профилактики и лечения одонтогенного перфоративного верхнечелюстного синусита.
Техническим результатом изобретения является 100% закрытие перфорации верхнечелюстного синуса, восстановление непрерывности зубного ряда и жевательной эффективности, возможность избежать дорогостоящего восстановительного лечения с использованием дентальных имплантатов и без применения костно-пластических манипуляций (операций). Лечение и профилактика одонтогенного перфоративного верхнечелюстного синусита.
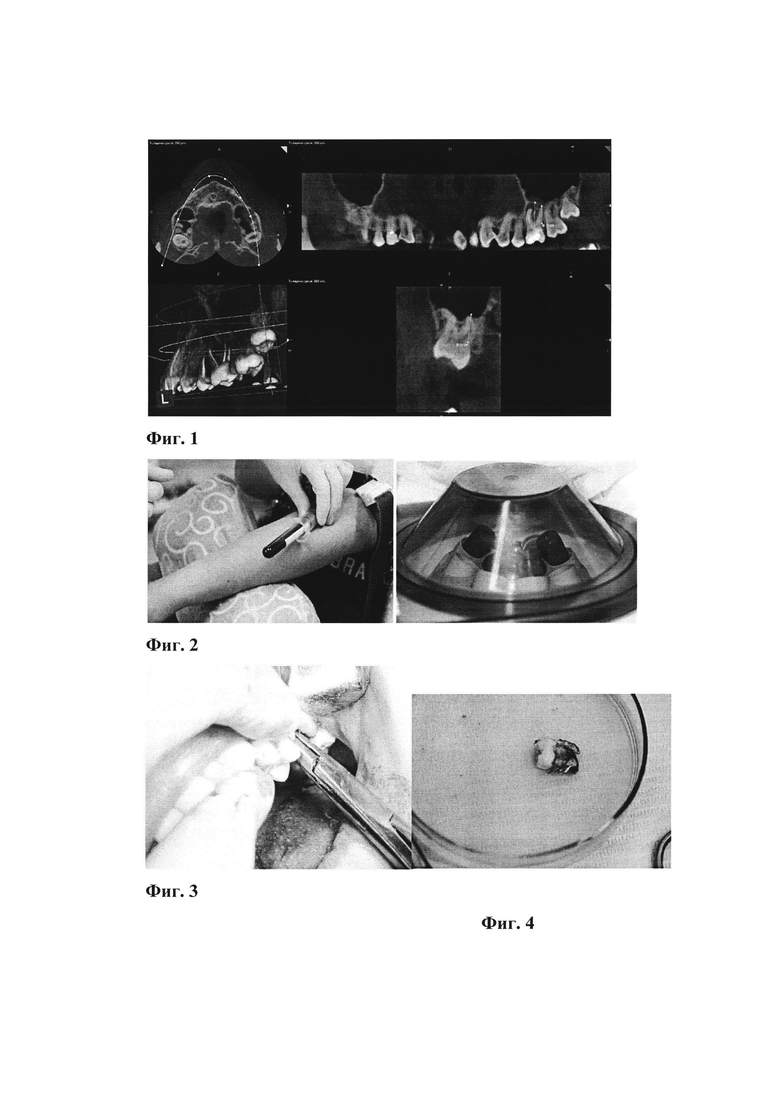
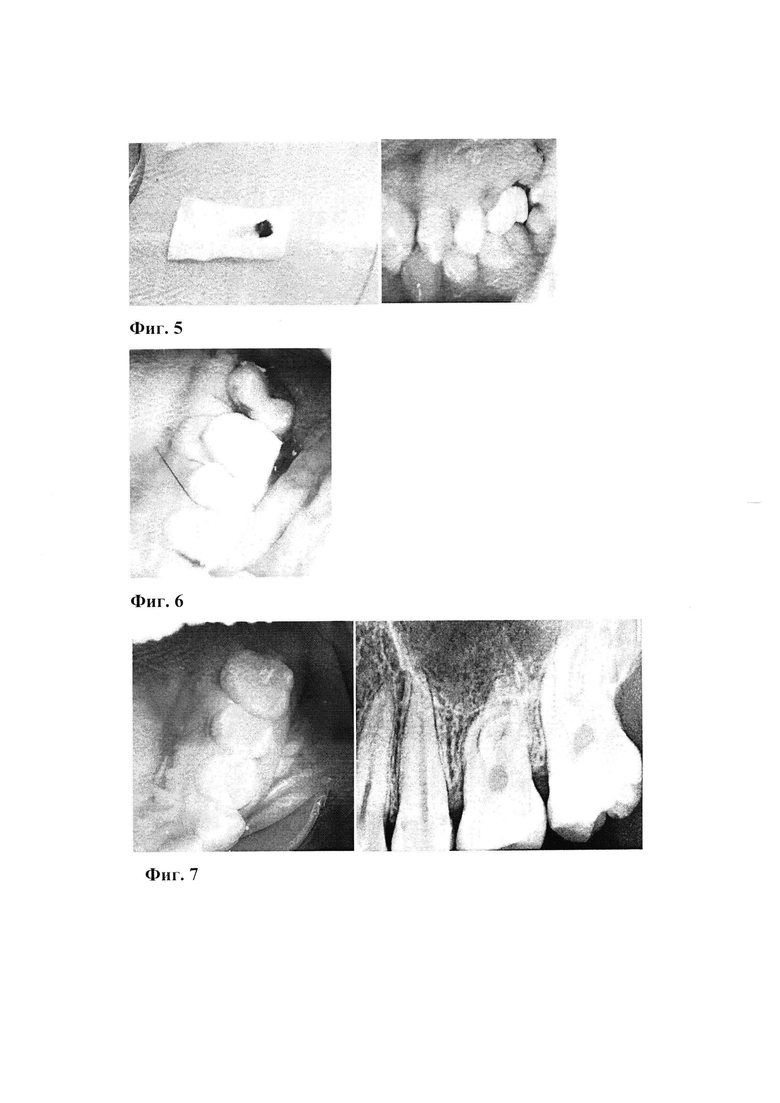
Изобретение иллюстрируется фотографиями, где на фиг. 1 - Измерения длины корней 3-го моляра и зуба, подлежащего удалению, в программе Radiant DICOM Viewer, на фиг. 2 - Забор венозной крови пациента и ее центрифугирование. На фиг. 3 - Коррекция межкорневых перегородок с применением «костных кусачек». На фиг. 4 - Удаленный 3-й моляр в чашке «Петри», на фиг. 5 - мембрана PRF и позиционирование 3-го (28 зуба) моляра в лунке 1-го моляра (26 зуба), на фиг. 6 - швы в зоне пластики. На фиг. 7 - Клинический осмотр и рентгенодиагностика. Вид через 6 месяцев после пластики.
Этапы выполнения способа:
1. Проводят лучевую диагностику зоны предполагаемого хирургического вмешательства с использованием метода компьютерной дентальной томографии. Измерения длины корней 3-го моляра и зуба, подлежащего удалению, проводят в программе Radiant DICOM Viewer с целью предварительного планирования хирургической операции (Фиг. 1).
2. Определяют местоположение 3го моляра верней челюсти, степень его прорезывания и архитектонику его корней. Определяют
местоположение корней 1 или 2 моляра верхней челюсти, подлежащего удалению вследствие хронического одонтогенного процесса, распространяющегося на верхнечелюстной синус.
3. Производят забор венозной крови пациента с цель получения плазмы, богатой тромбоцитами и фибрином в безвибрационной центрифуге (методика PRF или APRF) и создания аутомембраны (Фиг. 2).
4. Под инфильтрационным обезболиванием производят атравматичное удаление первого или второго моляра верхней челюсти (зуба, подлежащего удалению) с разделением корней и отслаиванием слизисто-надкостничного лоскута. Проводят аккуратную обработку зоны соустья лунки зуба и дна верхнечелюстной пазухи. Удаляют нежизнеспособные осколки костной ткани в лунке удаленного зуба, воспалительные грануляции, коррекцию межлуночковых (межкорневых) перегородок проводят с применением «костных кусачек»» и остеотома в соответствии со строением аутотрансплантируемого 3-го моляра (Фиг. 3).
5. Через перфорационное отверстие, возникшее при удалении корней первого или второго моляра верхней челюсти, проводят аспирацию (отсасывание, откачивание) жидкого содержимого верхнечелюстной пазухи (при его наличии). Производят орошение лунки зуба и нижних отделов верхнечелюстного синуса стерильным физиологическим раствором.
6. Производят атравматичное удаление ретинированного или дистопированного третьего моляра верхней челюсти, ранее не функционировавшего. После удаления зуб помещают в чашку «Петри» со стерильным физиологическим раствором, смешанным с PRF или APRF гелем, с цель предотвращения гибели сосудисто-нервного пучка, волокон периодонтальной связки и высушивания твердых тканей зуба (Фиг. 4).
7. Полученную мембрану PRF или APRF размещают на дне лунки, уделенного первого или второго моляра верхней челюсти, закрывая перфорационное отверстие и соустье с верхнечелюстной пазухой. Затем в лунке размещают третий моляр (зуб мудрости), стараясь заглубить его на 1,5-2 мм ниже окклюзионной поверхности стоящих рядом зубов (зуб располагается вне окклюзионных контактов) (Фиг. 5).
Накладываются простые узловые и перекрестные швы на края лунки удаленных зубов (фиг. 6). Аутотрансплантируемый третий моляр шинируется (стабилизируется) с помощью ортодонтической проволоки и фотополимеризующего жидкотекучего композита к соседним зубам.
Назначается антибактериальная и противовоспалительная терапия сроком на 7 дней. Назначается антибактериальный назальный спрей («Изофра», «Полидекса с фенилэфрином», «Фюзафюнжин») на 7 дней и ротовые ванночки с антисептиком (хлоргекседин водный) сроком на 10 дней. Также рекомендовано обрабатывать слизистую оболочку в области зоны хирургии противовоспалительными и антибактериальными гелями для полости рта («Аргокол», «Асепта», «Холисал») в течение 7 дней после хирургии. Пациенту рекомендуют щадящую диету и ограничение приема жесткой и грубой пищи с исключением жевания на стороне оперативного вмешательства сроком до 10 дней.
Контрольные осмотры проводят через сутки и на 4-е сутки после оперативного вмешательства. Швы снимают на 10 сутки. Снятие шины производят через 4 недели после оперативного вмешательства. Энододонтическое лечение (лечение каналов) аутотрансплантируемого третьего моляра проводится через 6-8 недель после хирургического лечения по показаниям (если сохраняется болевая реакция при перкуссии и имеются признаки гибели сосудисто-нервного пучка).
8. Рентгенодиагностические мероприятия проводятся через 1,5 месяца и через 6 месяцев (Фиг. 7) после проведенного хирургического лечения.
Несомненным преимуществом предлагаемого способа является:
1. 100% гарантия закрытия ороантрального сообщения.
2. Восстановление непрерывности зубного ряда и жевательной эффективности.
3. Возможность провести профилактику и лечение одонтогенного перфоративного верхнечелюстного синусита.
4. Возможность избежать применения аллогенных, ксеногенных, синтетических и других чужеродных трансплантатов для восстановления целостности верхнечелюстной пазухи и полости рта.
5. Возможность избежать дорогостоящего восстановительного лечения с использованием дентальных имплантатов и масштабных костно-пластических манипуляций.
В способе пластики перфорации (соустья) верхнечелюстного синуса с использованием аутотрансплантации (аутотрансплантата) третьего моляра дополнительно использована методика получения и использования PRF или APRF геля и аутомембраны, получаемых из венозной крови пациента, непосредственно на этапах проведения хирургического лечения. Фибрин, обогащенный тромбоцитами (PRF) представляет собой концентрат тромбоцитов второго поколения, полученный в ходе одиночного центрифугирования без использования антикоагулянтов. Полученный PRF-сгусток является физиологической трехмерной матрицей, насыщенной тромбоцитами и лейкоцитами. Альфа-гранулы, секретируемые тромбоцитами, которые находятся в мембране, выделяют специфические факторы роста, которые способствуют медленной и естественной резорбции самой структуры мембраны (15
дней). Данные факторы включают тромбоцитарный фактор роста (PDGF- platelet-derived growth factor), трансформирующий фактор роста-b (TGF-b-transforming growth factor-b), фактор роста эндотелия сосудов (VEGF- vascular endothelial growth factor), эпидермальный фактор роста (EGF - epidermal growth factor) и инсулиноподобный фактор роста-1 (IGF-1- insulin-like growth factor-1). Получение APRF базируется на аналогичном протоколе, при котором лишь изменяется структура используемой пробирки из пластиковой на стеклянную, что помогает увеличить эффект хелирования. Кроме того, в ходе получения APRF уменьшается время и параметры самого центрифугирования (от 2700 об./12 мин до 1200 об./8 мин). Изменяя эти параметры, Choukroun и коллеги обнаружили, что полученные таким образом APRF-мембраны содержат увеличенное количество фактора VEGF (ответственного за более быструю неоваскуляризацию области вмешательства), моноцитов (ответственных за высвобождение BMP) и внеклеточный матрикса (фибронектина). Omar и Rocher установили, что моноциты являются критически важным источником аутогенного костного морфогенетического белка-2 (ВМР-2) и костного морфогенетического белка-7 (ВМР-7), что объясняет улучшенные характеристики APRF по сравнению с PRF.
Предлагаемый способ иллюстрируется клиническими примерами. Клинические примеры:
Пациентка Ю., 22 года, обратилась в клинику стоматологии с жалобами на боли и разрушение 26 зуба, периодическую заложенность носа. После проведения клинических и рентгенологических (лучевых) методов обследования поставлен диагноз - хронический периодонтит 26 зуб (К04.5), хронический верхнечелюстной одонтогенный синусит слева (J32.0), ретенция 28 зуба (К01.0). Целесообразность и эффективность перелечивания 26 зуба является сомнительной, принято решение об удалении 26 и аутотрансплантации 28 зуба в лунку удаленного 26 зуба.
Вследствие хронического одонтогенного процесса в проекции верхушек корней 26 зуба и «пневматичного» анатомического строения верхней челюсти пациентки, произошло вскрытие верхнечелюстной пазухи в проекции медиального щечного корня с формированием соустья. Через перфорационное отверстие провели аспирацию жидкого содержимого верхнечелюстной пазухи. Произвели орошение лунки зуба и нижних отделов верхнечелюстного синуса стерильным физиологическим раствором. Перед началом хирургических манипуляций у пациентки провели забор венозной крови в стерильную пробирку для получения геля/мембраны по методике PRF. Проведено фрагментарное удаление 26 зуба с разделением корней, проведена медикаментозная обработка лунки и нижнего отдела верхнечелюстной пазухи через перфорационное отверстие в проекции медиального щечного корня. Проведено атравматичное удаление ретинированного 28 зуба, ранее не функционировавшего. После удаления зуб помещен в чашку «Петри» со стерильным физиологическим раствором, смешанным с PRF гелем, с цель предотвращения гибели сосудисто-нервного пучка, периодонтальных волокон и высушивания твердых тканей зуба. Мембрану PRF разместили на дне лунки, уделенного первого моляра верхней челюсти (26 зуба), закрыв перфорационное отверстие и соустье с верхнечелюстной пазухой. 28 зуб разместили в лунке 26, заглубив его на 1,5 мм ниже окклюзионной поверхности стоящих рядом. Для оптимизации расположения корней аутотрансплактируемого 3го моляра, была проведена коррекция межкорневых перегородок лунки 26 зуба с использованием «костных кусачек» и остеотома. Наложены простые узловые и перекрестные швы на края лунки удаленного 28 зуба и аутотрансплантированного зуба. Аутотрансплантируемый третий моляр стабилизирован с помощью ортодонтической проволоки и фотополимеризующего жидкотекучего композита к соседним зубам. Назначено антибактериальное и противовоспалительная лечение на 7 дней. Назначается антибактериальный назальный спрей «Изофра», на 7 дней.
Ротовые ванночки с антисептиком (хлоргекседин водный) на 10 дней. Рекомендовано обрабатывать слизистую оболочку в области зоны хирургии противовоспалительными и антибактериальными гелями для полости рта «Аргокол», в течение 7 дней после хирургии. Пациентке рекомендована щадящая диета и ограничение приема жесткой и грубой пищи с исключением жевания на стороне оперативного вмешательства сроком до 10 дней. Контрольные осмотры проводились через сутки и на 4-е сутки после оперативного вмешательства. Швы сняты на 10 сутки. Демонтаж шины, фиксирующей аутотрансплантарованый зуб, провели через 4 недели после оперативного вмешательства. Энододонтическое лечение аутотрансплатированного зуба не проводилось, т.к. зуб не демонстрирует признаков гибели сосудисто-нервного пучка. Рентгенодиагностические мероприятия проведены через 1,5 месяца и через 6 месяцев после хирургического лечения. Отмечается восстановление жевательной эффективности, нет ороантрального соустья, нет признаков воспаления верхнечелюстной пазухи.
Пациент К., 24 года, обратилась в клинику стоматологии с жалобами на боли и разрушение 17 зуба, периодическую заложенность носа. После проведения клинических и рентгенологических (лучевых) методов обследования поставлен диагноз - хронический периодонтит 17 зуб (К04.5), хронический верхнечелюстной одонтогенный синусит справа (J32.0), ретенция 18 зуба (К01.0). Целесообразность и эффективность перелечивания 17 зуба является сомнительной, принято решение об удалении 17 и аутотрансплантации 18 зуба в лунку удаленного 17 зуба. Вследствие хронического одонтогенного процесса в проекции верхушек корней 17 зуба и «пневматичного» анатомического строения верхней челюсти пациента, произошло вскрытие верхнечелюстной пазухи в проекции небного корня с формированием соустья. Через перфорационное отверстие провели аспирацию жидкого содержимого верхнечелюстной пазухи. Произвели орошение лунки зуба и нижних отделов
верхнечелюстного синуса стерильным физиологическим раствором. Перед началом хирургических манипуляций у пациента провели забор венозной крови в стерильную пробирку для получения геля/мембраны по методике APRF. Проведено фрагментарное удаление 17 зуба с разделением корней, проведена медикаментозная обработка лунки и нижнего отдела верхнечелюстной пазухи через перфорационное отверстие в проекции медиального небного корня. Проведено атравматичное удаление ретинированного 18 зуба, ранее не функционировавшего. После удаления зуб помещен в чашку «Петри» со стерильным физиологическим раствором, смешанным с APRF гелем, с цель предотвращения гибели сосудисто-нервного пучка и высушивания твердых тканей зуба. Мембрану APRF разместили на дне лунки, удаленного второго моляра верхней челюсти (17 зуба), закрыв перфорационное отверстие и соустье с верхнечелюстной пазухой. 18 зуб разместили в лунке 17, заглубив его на 2 мм ниже окклюзионной поверхности стоящих рядом. Для оптимизации расположения корней аутотрансплантируемого 3го моляра, была проведена коррекция межкорневых перегородок лунки 17 зуба с использованием костных кусачек и остеотома. Наложены простые узловые и перекрестные швы на края лунки удаленного 18 зуба и аутотрансплантированного зуба. Аутотрансплантируемый третий моляр стабилизирован с помощью ортодонтической проволоки и фотополимеризующего жидкотекучего композита к соседнему зубу. Назначено антибактериальное и противовоспалительное лечение на 7 дней. Назначен антибактериальный назальный спрей «Полидекса», на 7 дней. Ротовые ванночки с антисептиком (хлоргекседин водный) на 10 дней. Рекомендовано обрабатывать слизистую оболочку в области зоны хирургии противовоспалительными и антибактериальными гелями для полости рта «Холисал», в течение 7 дней после хирургии. Пациенту рекомендована щадящая диета и ограничение приема жесткой и грубой пищи с исключением жевания на стороне оперативного вмешательства сроком до 10 дней. Контрольные осмотры
проводились через сутки и на 4-е сутки после оперативного вмешательства. Швы сняты на 10 сутки. Демонтаж шины, фиксирующей аутотрансплантарованый зуб, провели через 4 недели после оперативного вмешательства. Энододонтическое лечение аутотрансплатированного зуба не проводилось, т.к. зуб не демонстрирует признаков гибели сосудисто-нервного пучка. Рентгенодиагностические мероприятия проведены через 1,5 месяца и через 6 месяцев после хирургического лечения. Отмечается восстановление жевательной эффективности, нет ороантрального соустья, нет признаков воспаления верхнечелюстной пазухи. Предлагаемое изобретение позволяет:
Провести пластику (закрытие) перфорации (соустья) верхнечелюстного синуса (ороантрального сообщения) с использованием аутотрансплантации третьего моляра.
Тем самым создается возможность:
1) Закрыть сообщение между полостью рта и верхнечелюстной пазухой (ороантрального сообщения).
2) Провести профилактику и лечение одонтогенного перфоративного верхнечелюстного синусита.
3) Восстановить непрерывность зубного ряда.
4) Восстановить жевательную эффективность.
5) Избежать дорогостоящего восстановительного лечения с использованием дентальных имплантатов и масштабных костнопластических манипуляций.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРОФИЛАКТИКИ РЕЦИДИВОВ ОРОАНТРАЛЬНЫХ СООБЩЕНИЙ | 2012 |
|
RU2510246C1 |
| Способ лечения хронического одонтогенного верхнечелюстного синусита, осложненного наличием ороантрального сообщения | 2017 |
|
RU2649515C1 |
| Способ лечения хронического одонтогенного верхнечелюстного синусита, осложненного наличием ороантрального соустья | 2022 |
|
RU2790969C1 |
| СПОСОБ ЛЕЧЕНИЯ ХРОНИЧЕСКОГО ОДОНТОГЕННОГО ПЕРФОРАТИВНОГО ГАЙМОРИТА | 1992 |
|
RU2035894C1 |
| СПОСОБ ПРОФИЛАКТИКИ ПЕРФОРАЦИЙ ДНА ВЕРХНЕЧЕЛЮСТНОЙ ПАЗУХИ ПРИ УДАЛЕНИИ МОЛЯРОВ ВЕРХНЕЙ ЧЕЛЮСТИ | 2012 |
|
RU2508057C1 |
| СПОСОБ УСТРАНЕНИЯ ОРОАНТРАЛЬНОГО СООБЩЕНИЯ | 2012 |
|
RU2506913C2 |
| ЛЕЧЕБНЫЙ ЭЛИКСИР ДЛЯ ОРОШЕНИЯ СЛИЗИСТОЙ ОБОЛОЧКИ ВЕРХНЕЧЕЛЮСТНОГО СИНУСА ПРИ ПЛАСТИКЕ ОРОАНТРАЛЬНОГО СОУСТЬЯ | 2016 |
|
RU2679919C2 |
| СПОСОБ ОЦЕНКИ ПОТЕНЦИАЛЬНОГО РИСКА ВОЗНИКНОВЕНИЯ ОРОАНТРАЛЬНОГО СОУСТЬЯ ПРИ УДАЛЕНИИ ЗУБА ВЕРХНЕЙ ЧЕЛЮСТИ | 2023 |
|
RU2823852C1 |
| СПОСОБ УСТРАНЕНИЯ ОРОАНТРАЛЬНОГО СООБЩЕНИЯ ВЕРХНЕЧЕЛЮСТНОЙ ПАЗУХИ И ПОЛОСТИ РТА | 2010 |
|
RU2423939C1 |
| Способ пластики перфорации верхнечелюстного синуса | 2016 |
|
RU2649514C1 |
Изобретение относится к медицине, а именно к хирургической стоматологии и челюстно-лицевой хирургии, и может быть использовано при пластике соустья верхнечелюстной пазухи и полости рта, возникшего при удалении первого или второго моляра верхней челюсти. Проводят лучевую диагностику зоны предполагаемого хирургического вмешательства, определяя местоположение 3-го моляра верней челюсти, 1-го или 2-го моляра верхней челюсти, подлежащего удалению вследствие хронического одонтогенного процесса, распространяющегося на верхнечелюстной синус. Производят забор венозной крови пациента с целью получения плазмы, богатой тромбоцитами и фибрином в безвибрационной центрифуге - методика PRF или APRF. Затем под инфильтрационным обезболиванием производят атравматичное удаление 1-го или 2-го моляра челюсти - зуба, подлежащего удалению с разделением корней и отслаиванием слизисто-надкостничного лоскута. Проводят обработку зоны соустья лунки зуба и дна верхнечелюстной пазухи, для чего удаляют нежизнеспособные осколки костной ткани в лунке удаленного зуба, воспалительные грануляции, извлекают 3-й моляр и помещают его в чашку «Петри» со стерильным физиологическим раствором, смешанным с PRF или APRF гелем, с целью предотвращения гибели сосудисто-нервного пучка, волокон периодонтальной связки и высушивания твердых тканей зуба. Затем в лунке размещают третий моляр - зуб мудрости, заглубляя его на 1,5-2 мм ниже окклюзионной поверхности стоящих рядом зубов - зуб располагается вне окклюзионных контактов - после чего накладываются простые узловые и перекрестные швы на края лунки удаленных зубов. Аутотрансплантируемый третий моляр шинируют, то есть стабилизируют с помощью ортодонтической проволоки и фотополимеризующего жидкотекучего композита путем фиксации к соседним зубам. Проводят в постоперационном периоде антибактериальную и противовоспалительную терапию. При этом до проведения операции определяют степень прорезывания и архитектонику корней 3-го моляра верхней челюсти. Осуществляют аутотрансплантацию ранее не функционировавшего, находящего в состоянии незавершенного развития 3-го моляра, предварительно размещая полученную аутомембрану PRF или APRF на дне лунки удаленного 1-го или 2-го моляра верхней челюсти и осуществляя коррекцию межлуночковых – межкорневых - перегородок в зоне трансплантации в соответствии со строением аутотрансплантируемого3-го моляра. Способ, за счет закрытия перфорации ороантрального сообщения с использованием аутотрансплантации третьего моляра, позволяет провести профилактику и лечение одонтогенного перфоративного верхнечелюстного синусита, восстановить непрерывность зубного ряда и жевательную эффективность. 7 ил., 2 пр.
Способ пластики перфорации верхнечелюстного синуса с использованием аутотрансплантации третьего моляра, заключающийся в закрытии ороантрального сообщения использованием аутотрансплантата и проведении в постоперационном периоде антибактериальной и противовоспалительной терапии, включающий следующую последовательность действий: проводят лучевую диагностику зоны предполагаемого хирургического вмешательства, определяя местоположение 3-го моляра верней челюсти, 1-го или 2-го моляра верхней челюсти, подлежащего удалению вследствие хронического одонтогенного процесса, распространяющегося на верхнечелюстной синус, производят забор венозной крови пациента с целью получения плазмы, богатой тромбоцитами и фибрином в безвибрационной центрифуге - методика PRF или APRF, затем под инфильтрационным обезболиванием производят атравматичное удаление 1-го или 2-го моляра челюсти - зуба, подлежащего удалению с разделением корней и отслаиванием слизисто-надкостничного лоскута, проводят обработку зоны соустья лунки зуба и дна верхнечелюстной пазухи, для чего удаляют нежизнеспособные осколки костной ткани в лунке удаленного зуба, воспалительные грануляции, извлекают 3-й моляр и помещают его в чашку «Петри» со стерильным физиологическим раствором, смешанным с PRF или APRF гелем, с целью предотвращения гибели сосудисто-нервного пучка, волокон периодонтальной связки и высушивания твердых тканей зуба, затем в лунке размещают третий моляр - зуб мудрости, заглубляя его на 1,5-2 мм ниже окклюзионной поверхности стоящих рядом зубов - зуб располагается вне окклюзионных контактов - после чего накладываются простые узловые и перекрестные швы на края лунки удаленных зубов, аутотрансплантируемый третий моляр шинируют, то есть стабилизируют с помощью ортодонтической проволоки и фотополимеризующего жидкотекучего композита путем фиксации к соседним зубам, отличающийся тем, что определяют степень прорезывания и архитектонику корней 3-го моляра верхней челюсти, осуществляют аутотрансплантацию ранее не функционировавшего, находящего в состоянии незавершенного развития 3-го моляра, предварительно размещая полученную аутомембрану PRF или APRF на дне лунки удаленного 1-го или 2-го моляра верхней челюсти и осуществляя коррекцию межлуночковых – межкорневых - перегородок в зоне трансплантации в соответствии со строением аутотрансплантируемого 3-го моляра.
| СПОСОБ АУТОТРАНСПЛАНТАЦИИ ЗУБА С СОХРАНЕНИЕМ ЖИЗНЕСПОСОБНОСТИ ЕГО ПУЛЬПЫ | 2015 |
|
RU2605630C1 |
| СПОСОБ ЛЕЧЕНИЯ ПЕРФОРАЦИЙ СЛИЗИСТОЙ ОБОЛОЧКИ ВЕРХНЕЧЕЛЮСТНОГО СИНУСА ПРИ ОПЕРАЦИИ СИНУСЛИФТИНГА | 2018 |
|
RU2695768C1 |
| US 20100203473 A1, 12.08.2010 | |||
| US 2006287732 A1, 21.12.2006 | |||
| MOUNZER ASSAD et al., Evaluation of a New Surgical Technique for Closing Oroantral Fistula Using Auto-transplanted Upper Third Molar: A 1-Year Follow-Up Study, J | |||
| Maxillofac, Oral Surg, Jan-Mar 2018, 17(1):84-88 | |||
| MOUNZER ASSAD et | |||
Авторы
Даты
2023-01-18—Публикация
2021-11-01—Подача