Изобретение относится к медицине, а именно к хирургической стоматологии, и может быть использовано для восстановления целостности зубных рядов.
Аутотрансплантацией зуба называют удаление зуба из одной области и его реплантацию в другую область у одного и того же человека. Новое место может быть свежей лункой после удаления зуба, который невозможно реставрировать, или искусственно высверленная лунка на беззубом альвеолярном гребне. Это определение включает в себя хирургическую репозицию зуба в ту же самую лунку.
Основное преимущество данного способа - экономическая эффективность, реализуемая за счет возможности использования зуба, ранее не функционировавшего (обычно это - третий моляр, сверхкомплектные, ретинированные или дистопированные моляры, премоляры, резцы или клыки), путем переноса в функциональное положение для замещения утраченного зуба у одного и того же человека.
Основные недостатки способа - дополнительное хирургическое вмешательство, относительно низкая адаптивность в практике (например, несоответствие зуба и размера пространства), и, что более важно - низкая предсказуемость результата по сравнению с обычным ортопедическим лечением (имплантаты, мостовидные протезы, съемные протезы).
Неизбежно сравнение аутотрансплантации и имплантации (например, с помощью дентальных имплантатов) как методов лечения при замещении отсутствующих зубов, ряд авторов обоснованно считают реплантацию и аутотрансплантацию зубов альтернативой имплантации в современных экологических условиях [1].
Одно из основных преимуществ трансплантации над имплантацией - это возможность ее применения у пациентов до завершения пубертатного периода. Имплантаты не растут вместе с растущими пациентами и в результате оказываются в инфраокклюзии. Красота аутотрансплантированных зубов заключается в том, что они натуральны и могут прорезываться в гармонии с соседними зубами и растущими челюстями.
Существующие способы аутотрансплантации достаточно однотипны и включают несколько этапов: удаление зуба-донора, подготовка лунки-реципиента, удаление пульпы зуба-донора, установка зуба-донора в лунку-реципиент, фиксация (шинирование) зуба-донора к окружающим зубам (обычно - проволокой, пломбировочным материалом, полиамидными нитями).
Основные недостатки существующих способов - удаление пульпы из коронковой и корневой частей зуба-донора, что делает невозможным ее регенерацию и лишает ткани (дентин, эмаль, цемент) зуба-донора полноценной иннервации и кровоснабжения. Сроки службы таких зубов небольшие, поскольку только жизнеспособная пульпа дает гарантию максимально длительного функционирования зуба.
Вместе с тем, крайне важно не только сохранить пульпу аутотрансплантированного зуба, но и минимизировать воспалительную реакцию, чтобы донорский зуб обладал возможностью для регенерации пульпы и имел открытое апикальное отверстие, шириной более 1 мм.
Известен способ аутотрансплантации зуба, описанный в статье Ckyau Е. [2]. Сущность способа-прототипа заключается в том, что автор использует остеоиндуктивный потенциал клеток пародонтальной связки зуба (PDL), в результате приводящий к регенерации кости в промежутке между стенками лунки и трансплантированным зубом. По мнению автора, генетически клетки PDL могут дифференцироваться в фибробласты, цементобласты и остеобласты, что объясняет этот остеоиндуктивный феномен. Представляет интерес идея использовать в будущем такие полезные PDL клетки для улучшения разработанной автором методики аутотрансплантации. Новое прикрепление происходит примерно в течение 2 недель после аутотрансплантации между PDL соединительной тканью на поверхности донорского зуба и стенкой лунки реципиента. Положительный эффект автор подтверждает клиническими наблюдениями на рентгенограммах у детей и подростков.
Преимущества метода - автор использует потенциал собственных мезенхимальных клеток пародонтальной связки зуба, которые могут дифференцироваться в фибробласты, цементобласты и остеобласты, что обеспечивает остеоиндуктивный эффект аутотрансплантации и хорошее приживление.
Недостатки - отсутствуют объективные данные о сохранении жизнеспособности пульпы аутотрансплантированного зуба, которыми служат показатели электровозбудимости пульпы.
Известен способ посттравматической аутореплантации зубов, выбранный в качестве прототипа, направленный на повышение эффективности операции за счет сокращения сроков приживления зуба-донора и оптимизации процессов регенерации [3].
Способ осуществляют следующим образом. Удаленный зуб помещают в физиологический раствор. Лунку покрывают стерильным марлевым тампоном и больному предлагают сомкнуть челюсти. Далее приступают к обработке реплантата: пломбируют кариозные полости, если они не были запломбированы ранее, производят резекцию верхушки корня и расширяют каналы при помощи эндодонтического инструмента. Реплантант захватывают стерильным тампоном, смоченным физиологическим раствором. Орошение зуба и эндодонтического инструмента производят непрерывно через каждые 2-3 с. Расширенные каналы обрабатывают гипохлоридом натрия. Канал культи корня в области его окончания (4-5 мм) расширяют до границ цемента и он, таким образом, принимает вид конуса с вершиной, обращенной в сторону коронковой части зуба. Затем, при помощи каналонаполнителя, канал пломбируют цементом; лишь конусовидно расширенную часть заполняют амальгамой. Шейку зуба осторожно, чтобы не повредить надкостницу корня, очищают от обрывков слизистой оболочки, от зубных отложений, и подготовленный таким образом реплантат погружают в физиологический раствор, где он находится до помещения его в лунку.
Следующим этапом операции является обработка лунки реплантата: удаляют тампон, лунку промывают физиологическим раствором и вводят в нее в смеси Цефазолин натрия, Виферон и Дексаметазон в соотношении 1:1:0,1 в дозе 0,5-1 г, при этом лекарственную смесь размещают в лунке реплантируемого зуба.
Далее обработанный зуб помещают в лунку. Его покрывают двумя-тремя стерильными марлевыми тампонами и больному предлагают сомкнуть челюсти. Тампоны пациент удерживает 15-20 минут. Реплантированный зуб не выводят из контакта с зубами антагонистами, тем самым он не выключается из артикуляции.
Затем в проекции верхушки корня реплантируемого зуба делают дренажный канал круглого сечения диаметром 3-4 мм, проходящий от поверхности слизистой до дна лунки, в который устанавливают эластичный упругий дренаж в форме спирали. В целях закрепления реплантированного зуба в послеоперационном периоде применяют шинирование с помощью GlasSpan®. Шины можно снимать через 3-4 недели.
Преимущества метода - обеспечивается технический результат в виде надежной фиксации и приживления реплантированного зуба.
Недостатки: способ не предусматривает аутотрансплантации зуба, а направлен на его реплантацию, т.е. помещение обратно в его же лунку, пульпа зуба не сохраняется, в описании отсутствует методика стимулирования процесса регенерации.
Поставлена задача разработать способ аутотрансплантации зуба с сохранением жизнеспособности его пульпы.
Поставленная задача достигается за счет использования при аутотрансплантации тканеинженерной конструкции, состоящей из предварительно культивированных мезенхимальных клеток пульпы зуба-донора и матрицы-носителя для этих клеток - гидрогеля PuraMatrix/3DM.
Способ осуществляется следующим образом.
Под местной анестезией Sol. Ultracaini 4% с адреналином 1:100000 удаляют зуб-донор. Бором расширяют апикальное отверстие корня до 1 мм, через которое вводят пульпоэкстрактор на 3 мм длины корня и эвакуируют часть корневой пульпы зуба. Зуб-донор помещают до следующего этапа в стерильный физиологический раствор и хранят при температуре 4°С.
Следующим этапом является получение клеточной культуры из пульпы зуба-донора.
Полученный фрагмент пульпы зуба-донора отмывают раствором Хэнкса с цефазолином (1 г/л). Полученную клеточную суспензию центрифугируют в режиме 1,500×g, 10 минут и ресуспендируют в ростовой среде DMEM/F12, содержащей 15% эмбриональной телячьей сыворотки, селектированной для выращивания клеток в низкой плотности, 2 мМ глутамина. Суспензию клеток высевают на пластиковые чашки Петри с диаметром 100 мм. Плотность посева первичной клеточной суспензии составляет 15 миллионов мононуклеарных клеток на 1 см2. Через 1 сутки не прикрепившиеся клетки удаляют, ростовую среду заменяют, если ее рН менее 6,0 или более 8,0, на ростовую среду, рН которой лежит в пределах от 6,0 до 8,0, при этом элиминируют клетки, не относящиеся к популяции мезенхимальных стволовых клеток. Культуры инкубируют при 37°С в атмосфере 5% CO2. По достижении культурой 50% конфлуентности монослой трипсинизируют и пересевают на новые чашки с плотностью 10-30 клеток на 1 см в ростовой среде, дополнительно содержащей 10 мкг/мл трансферрина, 1 мкг/мл инсулина, 10 нг/мл фактора роста фибробластов - 2 и 8 ЕД/мл гепарина.
Через 3 дня отбирают плотные колонии мелких клеток (диаметром 7-10 мкм) с большим количеством митозов. Отобранные колонии рассевают в новые чашки с плотностью 20 клеток/см и выращивают до состояния преконфлуентности. Последующие пассажи (если планируется аутотрансплантация нескольких зубов) производят в том же режиме. Таким образом, продолжительность получения клеточной культуры из пульпы зуба-донора составляет до 5 суток.
В полученную таким образом культуру плюрипотентных мезенхимальных клеток по каплям добавляют гидрогель PuraMatrix/3DM до загустевания смеси.
Следующим этапом операции является формирование лунки-реципиента (если ее нет в челюсти), которую готовят по стандартной методике, аналогичной методу подготовки принимающего ложа для дентального имплантата: производят разрез слизистой оболочки, хирургическими сверлами необходимого диаметра просверливают кортикальную кость и формируют лунку-реципиент. После сверления лунку промывают физиологическим раствором и вводят в нее подготовленную тканеинженерную конструкцию на 2/3 объема лунки-реципиента.
Затем зуб-донор извлекают из стерильного физиологического раствора и помещают в лунку-реципиент.
Его покрывают двумя-тремя стерильными марлевыми тампонами и предлагают больному сомкнуть челюсти. Тампоны пациент удерживает 20-30 минут.
Аутотрансплантированный зуб не выводят из контакта с зубами антагонистами, тем самым он не выключается из артикуляции. В целях закрепления аутотрансплантированного зуба в послеоперационном периоде применяют шинирование с помощью композиционного пломбировочного материала. Шины снимают через 4 недели.
Послеоперационная терапия включает антибактериальные и десенсибилизирующие средства, например азитромицин и цетрин, которые рекомендуют принимать в течение 4-5 дней.
Контроль за жизнеспособностью пульпы аутотрансплантированного зуба осуществляется путем регистрации порога ее электровозбудимости. Значения электродиагностики (ЭОД) от 20 до 45 мкА в раннем послеоперационном периоде (3-30 суток) и от 6 до 15 мкА в позднем периоде (от 1 до 3 месяцев) являются подтверждением ее функциональной состоятельности.
Для объективной оценки эффективности разработанного метода авторами-заявителями проведено экспериментальное исследование на животных.
Цель эксперимента - оценить эффективность использования разработанной тканеинженерной конструкции в восстановительной клеточной терапии пульпы аутотрансплантированных зубов барана in vivo.
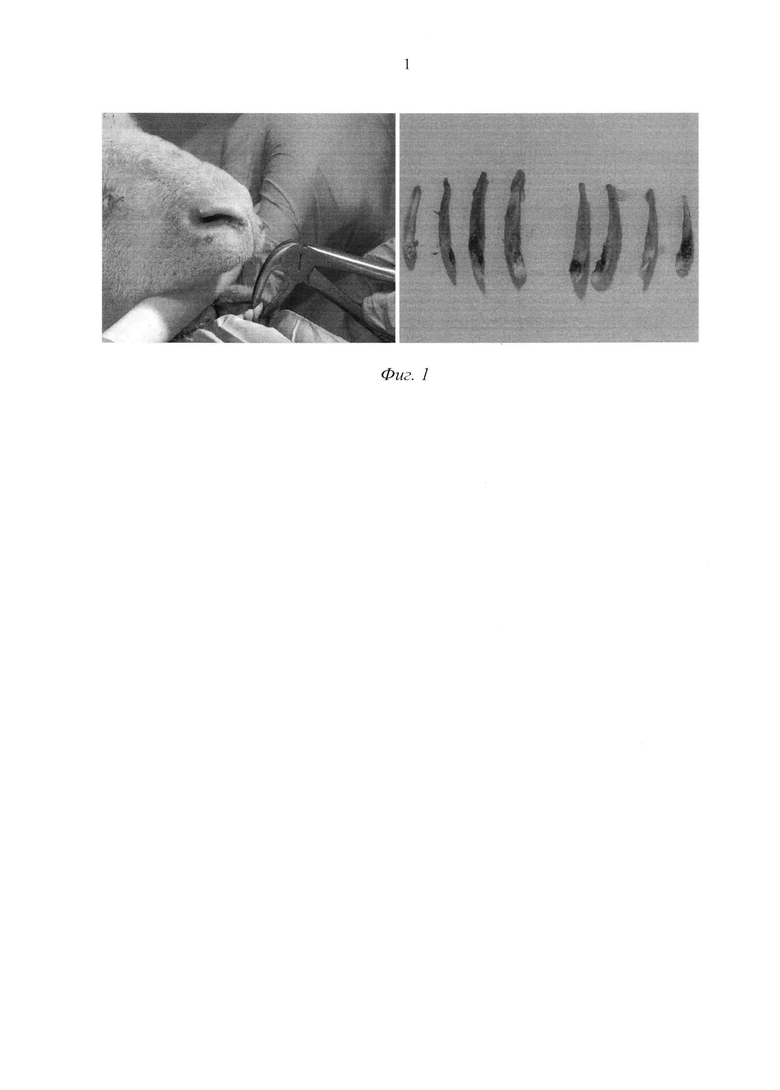
Материалы и методы экспериментального исследования. Объектом для исследования служили 14 взрослых баранов в возрасте от 3 до 5 лет. Животных разделили на 2 группы - основную и контрольную. В обеих группах животных оперировали под общим внутривенным наркозом (Zoletil 50) по одинаковой методике. Для аутотрансплантации использовали резцы (зацепы) нижней челюсти. Десневой край у зубов, подлежавших пересадке, отслаивали, зубы постепенно расшатывали с помощью прямого элеватора и удаляли щипцами (фиг. 1). После экстракции зубы помещали в стерильный физиологический раствор и хранили при температуре 4°С.
И в контрольной, и в основной группах каждый удаленный зуб пересаживали в освободившуюся лунку с противоположной стороны той же челюсти, т.е. меняли зубы местами. В контрольной группе трансплантировали зуб в лунку, заполненную сгустком крови.
В основной группе перед аутотрансплантацией принимающее ложе (лунку) на 2/3 заполняли индуктором регенерации, гидрогелем PuraMatrix/3DM с мезенхимальными клетками. Данная тканеинженерная конструкция представляет собой синтетический биодеградируемый матрикс-гель на основе олигопептидных фрагментов, формирующий нанонити и предварительно культивированные мезенхимальные клетки барана, обработанные 5-азацитидином. Готовый тканеинженерный продукт получали путем добавления геля к предварительно культивированным мезенхиальным клеткм in situ.
Все трансплантированные зубы в обеих группах шинировали между собой с помощью композитного пломбировочного материала.
Всего животным пересажено 112 зубов. Через 2-3 часа после операции животные становились активными, а через 6-12 часов начинали принимать пищу. В последующие 2-3 суток у них наблюдалась повышенная саливация. В период от 3 месяцев до 1 года вследствие рассасывания корней в контрольной и основной группах выпало 9 зубов (4 и 5 соответственно) - потеря обусловлена явным несоответствием трансплантируемого корня и воспринимающего ложа.
Через 3, 15 и 30 суток, 3, 6 и 12 месяцев от начала эксперимента под общим наркозом аутотрансплантированные зубы выпиливали блоком с окружающими мягкими тканями и альвеолярным отростком, рану ушивали. Операцию проводили без умерщвления животных, поскольку объем нанесенной операционной травмы не представлял критической угрозы для их жизни. Изъятые блоки с аутотрансплантированными зубами фиксировали в 10% нейтральном формалине, после чего проводили декальцинацию блоков в трилоне-Б. Далее материал заливали в гистологическую среду «Гистомикс» с использованием гистологического процессора замкнутого типа Tissue-Tek VIP™ 5 Jr и станции парафиновой заливки Tissue-Tek® ТЕС™ 5 фирмы Sakura (Япония). Из полученных блоков делали гистологические срезы толщиной 5-7 мкм и окрашивали гематоксилином и эозином, по Маллори красителями (Bio-Optica, Италия и Биовитрум, Россия) на автоматическом мультистейнере Prisma™. Для иммуногистохимических реакций использовали моноклональные антитела к β-галактозидазе (Diagnostic BioSystems, Нидерланды 1:25 - 1:50), моноклональные мышиные антитела к фактору Виллебранда (Diagnostic BioSystems, Нидерланды 1:25 - 1:50) и поликлональные кроличьи антитела к α-SMA (SpringBioScience, США). Негативным контролем служили реакции с заменой первых антител раствором для разведения (SpringBioScience, США).
Микроскопию срезов проводили на цифровом микроскопе со встроенным фотоаппаратом Olympus ВХ45.
С каждого препарата окрашенного позитивно на β-галактозидазу, фактор Виллебранда и a-SMA, выполняли по 10 цифровых снимков (в формате jpg, размером 3136×2352 пикселей в палитре 24 бит) случайно выбранных полей зрения при увеличении x100, x200, x400 и x1000. Морфометрические исследования проводили с использованием программы Видео-Тест Морфология 5.1 для Windows. Полученные цифровые данные были анализированы с применением статистического метода t-критерия Стьюдента в программе Primer of Biostatistics 4.03 для Windows. Достоверными считали различия при p<0,05.
Научно-исследовательская работа проведена в рамках Государственного задания Министерства здравоохранения Российской федерации совместно с Центральным НИИ овцеводства и козоводства РФ и Ставропольским государственным аграрным университетом.
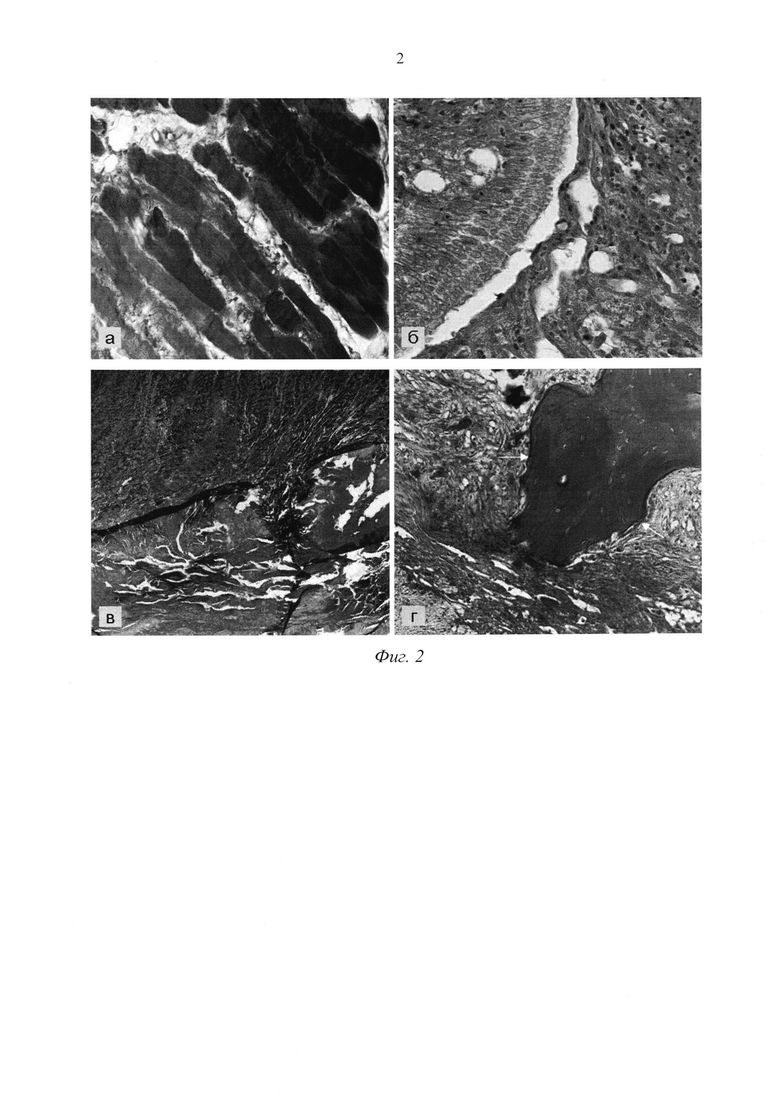
Результаты исследования. Дистрофические изменения пульпы в контрольной группе появляются к концу 3-х суток после аутотрансплантации зубов. Сетчатая дистрофия захватывает в первую очередь слой одонтобластов и, постепенно распространяясь на все слои пульпы, приводит ее к гибели уже к 15-м суткам (фиг. 2-а, б, в, г).
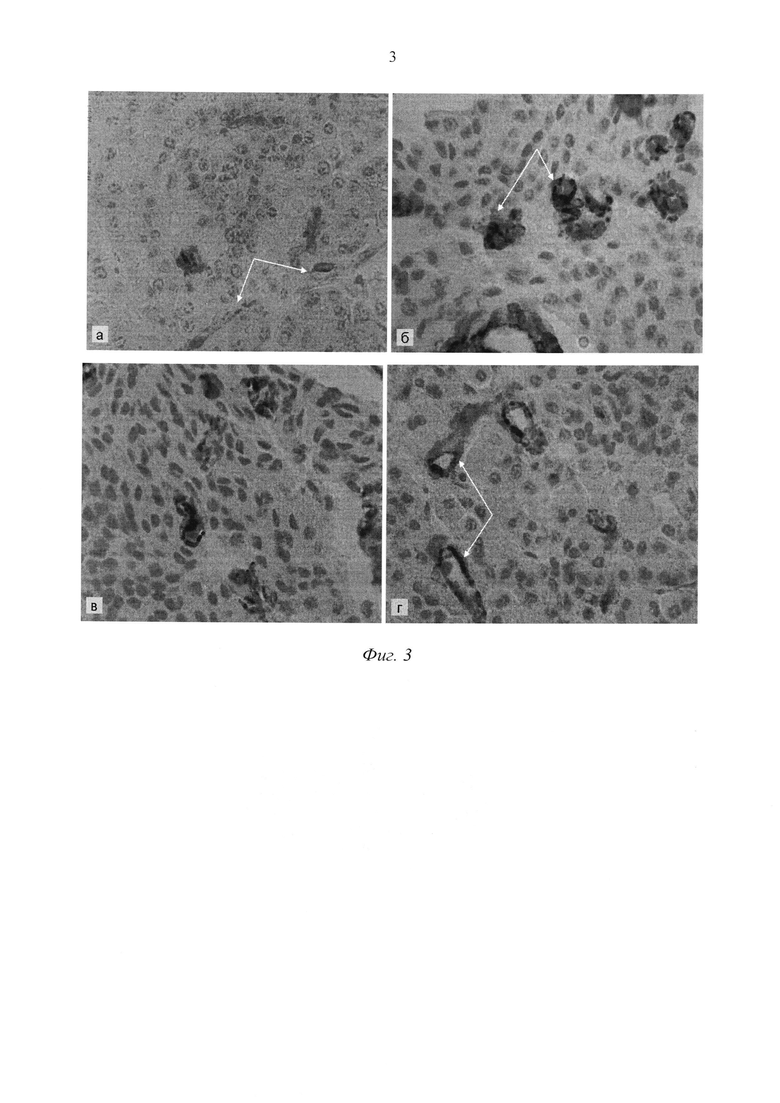
Иммуногистохимический метод контроля жизнедеятельности мезенхимальных клеток в основной группе показал, что после аутотрансплантации зуба с использованием тканеинженерной конструкции все прекультивированные клетки, равно как и трансплантируемые клетки, сохраняют свою жизнеспособность, а значит, и способность продуцировать факторы, ускоряющие процесс регенерации пульпы зуба и тканей пародонта. Данное явление выражалось в ускорении смены фаз регенераторного процесса: по сравнению с контрольной группой сокращались сроки периода клеточной инфильтрации, ускорялся темп неоангиогенеза и разрастания сосудистой сети пульпы (фиг. 3-а, б, в, г). На наш взгляд, данное явление связано с более высокой функциональной активностью мезенхимальных клеток в составе тканеинженерной конструкции в сочетании с материцей-носителем и индуктором регенерации, гидрогелем PuraMatrix/3DM, а также обусловлено создавшимися межклеточными взаимодействиями.
Полученные экспериментальные данные исследования позволяют рекомендовать разработанную тканеинженерную конструкцию в качестве носителя предварительно культивированных мезенхимальных клеток пульпы и гидрогеля PuraMatrix/3DM для эффективной доставки жизнеспособных клеток в патологический очаг, удержания их там и оптимизации условий их лечебного воздействия в местах повреждения тканей.
Таким образом, предложен новый способ лечения, характеризующийся тем, что, используя стандартные хирургические протоколы (удаление зуба-донора, формирование лунки-реципиента, шинирование зуба проволокой или композиционным пломбировочным материалом) и тканеинженерную конструкцию, состоящую из предварительно культивированных клеток пульпы зуба-донора и матрицы-носителя для этих клеток - гидрогеля PuraMatrix/3DM, получен технический результат, ранее не известный, имеющий высокий терапевтический эффект.
Хорошая совместимость указанных компонентов тканеинженерной конструкции обеспечивает синергизм их действия, приводящий к возникновению новых свойств и широкому спектру терапевтических эффектов: ускорении регенерации пульпы зуба-донора, приживления зуба-донора в лунке-реципиенте, восстановлению целостности зубного ряда.
Высокая эффективность разработанного способа аутотрансплантации зуба с сохранением жизнеспособности его пульпы позволяют эффективно его использовать ее при лечении различных патологических состояний, в том числе при наличии сверхкомплектных, ретинированных, дистопированных зубов, что подтверждено конкретными клиническими примерами.
Исследования проведены на базе кафедры стоматологии Ставропольского государственного медицинского университета и Ставропольской краевой стоматологической поликлиники.
Всем больным выполнялось рентгенологическое исследование до и после выполнения аутотрансплантации зуба с сохранением жизнеспособности его пульпы по вышеописанному способу.
Клинический пример 1.
Пациентка В., 17 лет, направлена из школьного стоматологического кабинета с кальцифицированным образованием в левой половине нижней челюсти. В анамнезе выявлены периодически повторяющиеся появления припухлости и болезненности в области нижней челюсти слева.
Объективно: слизистая оболочка полости рта нижней челюсти слева гиперемирована, отечна, в области 34-38 зубов определяются точечные кровоизлияния. Индекс гигиены (ИГ) (OHI-S) составил 2,5 балла (неудовлетворительная гигиена полости рта).
Рентгенологически: выявлен рентгеноконтрастный очаг поражения, расположенный в области от 35-38 зуба. Поверхность очага извитая, окружена рентгенопрозрачным ободом. 36 зуб смещен к нижней границе челюсти и располагается в нижнечелюстном канале. Рентгенологическая плотность образования составила 1500 ед по шкале Хаунсфилда. ЭОД 36, 37 зуба составляет 6-12 мкА, 38 зуба - 60 мкА.
Диагноз - одонтома нижней челюсти слева.
Лечение. Под инфильтрационной анестезией Sol. Ultracaini 4% с адреналином 1:100000 произведено хирургическое удаление одонтомы. Нижнечелюстной нерв сохранен без потери чувствительности. В ходе формирования доступа к одонтоме 36, 37, и 38 зубы удалены.
По показаниям ЭОД, проведенным до операции, принято решение произвести аутотрансплантацию 36 и 37 зуба с сохранением жизнеспособности пульпы по заявляемому способу.
Шаровидным бором расширены апикальные отверстия корней 36 и 37 зубов до 1 мм, куда введен пульпоэкстрактор на 3 мм длины корней и эвакуирована часть корневой пульпы. Зубы-доноры помещены до следующего этапа в стерильный физиологический раствор, где они хранятся при температуре 4°С.
Полученные фрагменты пульпы зубов-доноров отмыты раствором Хэнкса с цефазолином (1 г/л). Полученную клеточную суспензию центрифугировали в режиме 1,500×g, 10 минут и ресуспендировали в ростовой среде DMEM/F12, содержащей 15% эмбриональной телячьей сыворотки, селектированной для выращивания клеток в низкой плотности, 2 мМ глутамина. Суспензию клеток высеяна на пластиковые чашки Петри с диаметром 100 мм. Плотность посева первичной клеточной суспензии составила 15 миллионов мононуклеарных клеток на 1 см. Через 1 сутки не прикрепившиеся клетки удалены, ростовая среда заменена (поскольку ее рН была менее 6,0) на ростовую среду, рН которой составила 8,0, элиминированы клетки, не относящиеся к популяции мезенхимальных стволовых клеток. Культуры инкубированы при 37°С в атмосфере 5% СО2. По достижении культурой 50% конфлуентности монослой трипсинизирован и пересеян на новые чашки с плотностью 10-30 клеток на 1 см в ростовой среде, дополнительно содержащей 10 мкг/мл трансферрина, 1 мкг/мл инсулина, 10 нг/мл фактора роста фибробластов - 2 и 8 ЕД/мл гепарина.
Через 3 дня отобраны плотные колонии мелких клеток (диаметром 7-10 мкм) с большим количеством митозов. Отобранные колонии рассеяли в новые чашки с плотностью 20 клеток/см и выращивали до состояния преконфлуентности. Последующие пассажи (поскольку запланирована аутотрансплантация нескольких зубов) произведены в том же режиме. Таким образом, продолжительность получения клеточной культуры из пульпы зубов-доноров составила 5 суток. В полученную таким образом культуру плюрипотентных мезенхимальных клеток по каплям добавили гидрогель PuraMatrix/3DM до загустевания смеси.
Через 4 месяца после операции по удалению одонтомы произведено формирование 4 лунок-реципиентов (по числу корней зубов), которые подготовили по стандартной методике, аналогичной методу подготовки принимающего ложа для дентального имплантата: произвели разрез слизистой оболочки, хирургическими сверлами необходимого диаметра просверлили кортикальную кость и сформировали 4 лунки-реципиента. После сверления лунки промыты физиологическим раствором, в них введена подготовленная тканеинженерная конструкция на 2/3 их объема.
Зубы-доноры (36 и 37) извлечены из стерильного физиологического раствора и помещены в подготовленные лунки-реципиенты.
Аутотрансплантированные 36 и 37 зубы покрыты двумя стерильными марлевыми тампонами, которые удерживались пациенткой 30 минут.
Аутотрансплантированные зубы не выводили из контакта с зубами антагонистами, тем самым они не выключались из артикуляции. В целях закрепления аутотрансплантированных зубов в послеоперационном периоде использовали шинирование с помощью композиционного пломбировочного материала Филтек. Шины сняты через 4 недели после операции аутотрансплантации.
Послеоперационная терапия включала антибактериальные и десенсибилизирующие средства, азитромицин (по 500 мг 1 раз в сутки 5 суток) и цетрин (по 200 мг 2 раза в сутки 5 суток).
На контрольной рентгенограмме - полноценная интеграция корней аутотрансплантированных зубов-доноров в лунках-реципиентах. При повторном осмотре через 3, 7 и 30 суток больная жалоб не предъявляет. Результаты рентгенологического исследования, проведенные через 1 год, показали отсутствие признаков рассасывания костной ткани в области корней аутотрансплантированных зубов и отсутствие деструктивных изменений в окружающих периапикальных тканях.
Контроль за жизнеспособностью пульпы аутотрансплантированных зубов осуществляли на протяжении 1 года. Значения электродиагностики (ЭОД) 36 и 37 зубов через 3 суток после операции составили 20 и 22 мкА соответственно, через 1 месяц - 16 и 12 мкА соответственно, через 3 месяца - 6 и 8 мкА соответственно, через 1 год - 4 и 6 мкА соответственно.
Полученные данные являются подтверждением жизнеспособности и функциональной состоятельности пульпы аутотрансплантированных 36 и 37 зубов. Данный клинический пример продемонстрировал, что аутотрансплантированные зубы могут хорошо прижиться в искусственно просверленной полости лунки-реципиента во вторично регенерировавшейся кости после удаления патологического очага челюсти (одонтомы).
Клинический пример 2.
Пациент В., 14 лет, направлен на кафедру стоматологии с непрорезавшимся верхним правым боковым резцом и клыком (12 и 13 зубы).
На обзорной рентгенограмме выявлено, что расположенный горизонтально в теле альвеолярного отростка верхней челюсти 12 зуб блокировал прорезывание 13 зуба, который в свою очередь, смещенный лабиально, упирался в центральный резец слева - 11 зуб. Диагноз: ретенция и дистопия 12 и 13 зубов.
Лечение. Под инфильтрационной анестезией sol. Ultracaini 4% с адреналином 1:100000 12 зуб удален по частям (сохранить его целым не представлялось возможным), 13 зуб выведен от контакта с 11 зубом, извлечен из лунки и через 5 суток аутотрансплантирован по вышеописанной методике в позицию 12 зуба (интра-альвеолярная аутотрансплантация). Клык зафиксирован шиной из композиционного пломбировочного материала Филтек на 3 недели. В послеоперационном периоде 13 зуб занял вертикальное положение в функциональной окклюзии на месте 12 зуба.
На контрольной рентгенограмме - полноценная интеграция корня аутотрансплантированного 13 зуба. При повторных осмотрах через 3, 7 и 30 суток больной жалоб не предъявляет. Результаты рентгенологического исследования, проведенные через 1 год, указали на отсутствие признаков рассасывания костной ткани в области корня аутотрансплантированного клыка, отсутствие деструктивных изменений в окружающих периапикальных тканях, отсутствие признаков облитерации корневого канала, а также пульпарной камеры 13 зуба.
Контроль за жизнеспособностью пульпы аутотрансплантированного клыка осуществлялся на протяжении 2 лет. Значение ЭОД 13 зуба через 3 суток после операции составило 16 мкА, через 1 месяц - 12 мкА, через 3 месяца - 10 мкА, через 1 год - 6 мкА.
Всего таким образом трансплантировано 48 зубов человека. Аутотрансплантированные зубы не изменялись в цвете, сохраняли прежний блеск, видимые воспалительные явления мягких тканей вокруг аутотрансплантированных зубов, как правило, исчезали через 5-7 суток. В период от 3 месяцев до 1 года вследствие рассасывания корней выпало 2 (4,2%) из 48 аутотрансплантированных зубов - потери обусловлены явным несоответствием аутотрансплантируемого корня зуба-донора и воспринимающего ложа лунки-реципиента, эффективность заявляемого способа составила 95,8%.
Таким образом, полученные данные в экспериментальных условиях и в клинике свидетельствуют о высоком терапевтическом эффекте разработанного способа аутотрансплантации зуба с сохранением жизнеспособности его пульпы, что позволяет эффективно использовать его в стоматологической практике, например, при наличии сверхкомплектных, ретинированных, дистопированных зубов в ортодонтии и при хирургическом удалении опухолей челюстей.

| название | год | авторы | номер документа |
|---|---|---|---|
| МАТЕРИАЛ ДЛЯ ПЛОМБИРОВАНИЯ КОРНЕВЫХ КАНАЛОВ ЗУБОВ ПРИ ЛЕЧЕНИИ ДЕСТРУКТИВНЫХ ФОРМ ХРОНИЧЕСКОГО ПЕРИОДОНТИТА | 2015 |
|
RU2569762C1 |
| ПАСТА ДЛЯ НЕПРЯМОГО ПОКРЫТИЯ ПУЛЬПЫ ЗУБА ПРИ ЛЕЧЕНИИ ГЛУБОКОГО КАРИЕСА И ОСТРОГО ОЧАГОВОГО ПУЛЬПИТА | 2016 |
|
RU2623079C1 |
| ПАСТА ДЛЯ ВРЕМЕННОГО ПЛОМБИРОВАНИЯ ПРИ ЛЕЧЕНИИ ОСЛОЖНЕНИЙ КАРИЕСА ЗУБОВ | 2016 |
|
RU2616265C1 |
| СТОМАТОЛОГИЧЕСКИЙ МАТЕРИАЛ ДЛЯ ИЗОЛИРУЮЩЕЙ ПРОКЛАДКИ ПРИ ЛЕЧЕНИИ ГЛУБОКОГО КАРИЕСА И ОСТРОГО ОЧАГОВОГО ПУЛЬПИТА | 2016 |
|
RU2623863C1 |
| ПАСТА ДЛЯ ПЛОМБИРОВАНИЯ КОРНЕВЫХ КАНАЛОВ ЗУБОВ ПРИ ЛЕЧЕНИИ ПУЛЬПИТА | 2014 |
|
RU2546003C1 |
| КОМБИНИРОВАННАЯ ЛЕКАРСТВЕННАЯ ПАСТА ДЛЯ ЛЕЧЕНИЯ ГЛУБОКОГО КАРИЕСА ЗУБОВ | 2011 |
|
RU2452462C1 |
| СПОСОБ ВНУТРИРОТОВОГО ДОСТУПА К ВЕРХНЕЧЕЛЮСТНОМУ СИНУСУ ДЛЯ УДАЛЕНИЯ ПЛОМБИРОВОЧНОГО МАТЕРИАЛА | 2008 |
|
RU2369346C1 |
| КОМБИНИРОВАННАЯ ЛЕКАРСТВЕННАЯ ПАСТА ДЛЯ КОНСЕРВАТИВНОГО ЛЕЧЕНИЯ ОСТРОГО ОЧАГОВОГО ПУЛЬПИТА | 2011 |
|
RU2452461C1 |
| СПОСОБ УСКОРЕНИЯ РЕПАРАТИВНОЙ РЕГЕНЕРАЦИИ КОСТНОЙ ТКАНИ | 2020 |
|
RU2738085C1 |
| СПОСОБ УДАЛЕНИЯ И РЕПЛАНТАЦИИ ЗУБА ПРИ ЛЕЧЕНИИ ХРОНИЧЕСКОГО ПЕРИОДОНТИТА | 2007 |
|
RU2326611C1 |
Изобретение относится к медицине, а именно к хирургической стоматологии, и может быть использовано для восстановления целостности зубных рядов. Для этого способ аутотрансплантации зуба с сохранением жизнеспособности его пульпы включает удаление зуба-донора, формирование лунки-реципиента, аутотрансплантацию зуба-донора, покрытие его стерильными марлевыми тампонами, шинирование зуба композиционным пломбировочным материалом без выведения из контакта с зубами антагонистами. При этом до аутотрансплантации в лунку-реципиент на 2/3 ее объема вводят тканеинженерную конструкцию, состоящую из предварительно культивированных мезенхимальных клеток, полученных из пульпы зуба-донора, и гидрогеля PuraMatrix/3DM. Способ обеспечивает высокий терапевтический эффект аутотрансплантации зуба с сохранением жизнеспособности его пульпы, что позволяет эффективно использовать способ, например, при наличии сверхкомплектных, ретинированных, дистопированных зубов в ортодонтии и при хирургическом удалении опухолей челюстей. 2 пр., 3 ил.
Способ аутотрансплантации зуба с сохранением жизнеспособности его пульпы, включающий удаление зуба-донора, формирование лунки-реципиента, аутотрансплантацию зуба-донора, покрытие его стерильными марлевыми тампонами, которые удерживают 20-30 минут при сомкнутых челюстях пациента, шинирование зуба композиционным пломбировочным материалом без выведения из контакта с зубами антагонистами, отличающийся тем, что в лунку-реципиент на 2/3 ее объема вводят тканеинженерную конструкцию, состоящую из предварительно культивированных мезенхимальных клеток, полученных из пульпы зуба-донора, и гидрогеля PuraMatrix/3DM.
| US 20110002895 A1, 06.01.2011 | |||
| СПОСОБ СОЗДАНИЯ ЗУБА | 2010 |
|
RU2523559C2 |
| СПОСОБ ВОССТАНОВЛЕНИЯ КОСТИ АЛЬВЕОЛЯРНОГО ГРЕБНЯ ЧЕЛЮСТИ И ТКАНЕЙ ПАРОДОНТА С РЕДУЦИРОВАННЫМ РЕГЕНЕРАТОРНЫМ ПОТЕНЦИАЛОМ | 2006 |
|
RU2320285C2 |
| СПОСОБ ЛЕЧЕНИЯ ОСТРОГО ПАНКРЕАТИТА | 1993 |
|
RU2119769C1 |
| СКОГЛАНД А | |||
| Изменения в тканях незрелых собачьих зубов, аллотрансплантированные в хирургически приготовленные лунки | |||
| Сборник статей научно-практической конференции стоматологов Республики Башкортостан, 1996, C | |||
| Устройство для выпрямления многофазного тока | 1923 |
|
SU50A1 |
| NAKAHARA T Potential | |||
Авторы
Даты
2016-12-27—Публикация
2015-11-10—Подача