ОБЛАСТЬ ТЕХНИКИ ИЗОБРЕТЕНИЯ
Настоящее изобретение касается применения ингибиторов рецептора интерлейкина-4 для лечения и профилактики аллергических реакций и для повышения эффективности и (или) безопасности схем аллерген-специфической иммунотерапии.
УРОВЕНЬ ТЕХНИКИ
Аллергии и аллергические заболевания являются серьезными медицинскими состояниями, сопровождающимися осложнениями, которые по своей тяжести могут варьировать от не угрожающих жизни реакций, которые разрешаются со временем, до угрожающих жизни реакций, таких как анафилаксия. Аллергические реакции могут возникать в результате контакта с широким рядом веществ или воздействия широкого ряда веществ, например некоторых пищевых продуктов, яда насекомых, растительных материалов (например пыльца), химических веществ, лекарственных препаратов/лекарственных средств и перхоти животных. В настоящее время для лечения аллергии применяются такие методы как избегание контакта с аллергенами, фармакологическое лечение симптомов и профилактика с помощью аллерген-специфической иммунотерапии (АСИ). К сожалению, применяемые в настоящее время методы лечения часто недостаточно эффективны, дорогостоящи, непрактичны или несут существенный риск для пациента. Например, избегание контакта с аллергеном не всегда возможно и может отрицательно сказаться на качестве жизни пациента и лица, осуществляющего за ним уход. С другой стороны, иммунотерапевтические методы включают преднамеренное введение аллергена восприимчивым лицам и, поэтому, по своей сути, подвергают их риску возникновения нежелательных тяжелых аллергических реакций или анафилаксии. В связи с этим существует неудовлетворенная потребность в рассматриваемой области в новых терапевтических методах для лечения или профилактики аллергических реакций и повышения безопасности и (или) эффективности иммунотерапевтических схем.
КРАТКОЕ ОПИСАНИЕ СУЩНОСТИ НАСТОЯЩЕГО ИЗОБРЕТЕНИЯ
Согласно одному аспекту настоящего изобретения представлены способы лечения и профилактики и (или) уменьшения степени тяжести аллергической реакции у субъекта. Способы согласно этому аспекту настоящего изобретения включают введение нуждающемуся в этом субъекту фармацевтической композиции, содержащей антагонист рецептора интерлейкина-4 (ИЛ-4Р), в терапевтически эффективном количестве. Фармацевтическую композицию, содержащую антагонист ИЛ-4Р, можно вводить субъекту до, во время или после воздействия аллергена или появления симптомов аллергии.
Согласно другому аспекту настоящего изобретения представлены способы повышения эффективности и (или) безопасности схемы аллерген-специфической иммунотерапии (АСИ). Способы согласно этому аспекту настоящего изобретения включают введение нуждающемуся в этом субъекту фармацевтической композиции, содержащей антагонист ИЛ-4Р, в терапевтически эффективном количестве в комбинации со схемой АСИ. Согласно некоторым вариантам осуществления этого аспекта настоящего изобретения фармацевтическую композицию, содержащую антагонист ИЛ-4Р, вводят субъекту до начала схемы АСИ или во время схемы АСИ. Например, фармацевтическую композицию, содержащую антагонист ИЛ-4Р, можно вводить во время фазы увеличения дозы схемы АСИ и (или) во время поддерживающей фазы схемы АСИ.
Согласно другому аспекту настоящего изобретения, представлены способы снижения общих уровней IgE в сыворотке крови у субъекта, подвергнутого воздействию аллергена. Способы согласно этому аспекту настоящего изобретения включают введение субъекту фармацевтической композиции, содержащей антагонист ИЛ-4Р, в количестве, достаточном для снижения или полного устранения образования IgE либо для снижения или полного устранения уровней IgE в сыворотке крови у субъекта.
Согласно различным вариантам осуществления настоящего изобретения, фармацевтическую композицию, содержащую антагонист ИЛ-4Р, нуждающийся в этом субъект может получать перорально, подкожно, накожно или внутривенно.
Примерами антагонистов ИЛ-4Р, которые можно использовать в контексте способов настоящего изобретения, являются, например, низкомолекулярные химические ингибиторы ИЛ-4Р или его лигандов (ИЛ-4 и (или) ИЛ-13) или биологические вещества, воздействующие на ИЛ-4Р или его лиганды. Согласно некоторым вариантам осуществления настоящего изобретения, антагонист ИЛ-4Р может представлять собой антигенсвязывающий белок, который связывается с цепью ИЛ-4Рα и блокирует сигналы, опосредованные ИЛ-4, ИЛ-13 или и ИЛ-4, и ИЛ-13. Один из таких антигенсвязывающих белков, такой как дупилумаб, можно использовать в контексте способов настоящего изобретения в качестве антитела к ИЛ-4Рα.
Другие варианты осуществления настоящего изобретения станут ясны после ознакомления с последующим подробным описанием.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
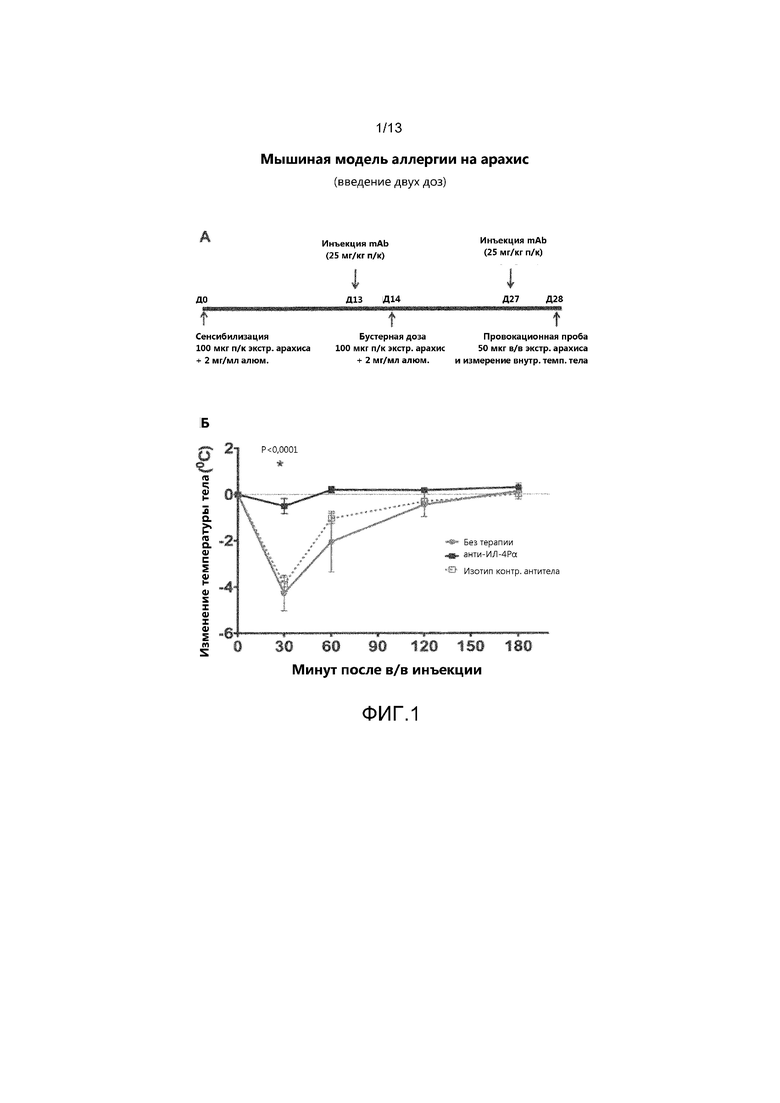
На фиг. 1, часть А, показана временная схема эксперимента с использованием мышиной модели с аллергией на арахис, в котором мыши получали две дозы антитела анти-ИЛ-4Рα. В части Б показана степень тяжести анафилаксии у экспериментальных мышей трех групп, которую определяли на основании постепенного снижения внутренней температуры тела после выполнения провокационной пробы с внутривенным введением экстракта арахиса. Значения для мышей, не получавших антитело, показаны серыми кружками; значения для мышей, получавших антитело анти-ИЛ-4Рα показаны черными квадратами; значения для мышей, получавших изотип контрольного антитела, показаны белыми квадратами.
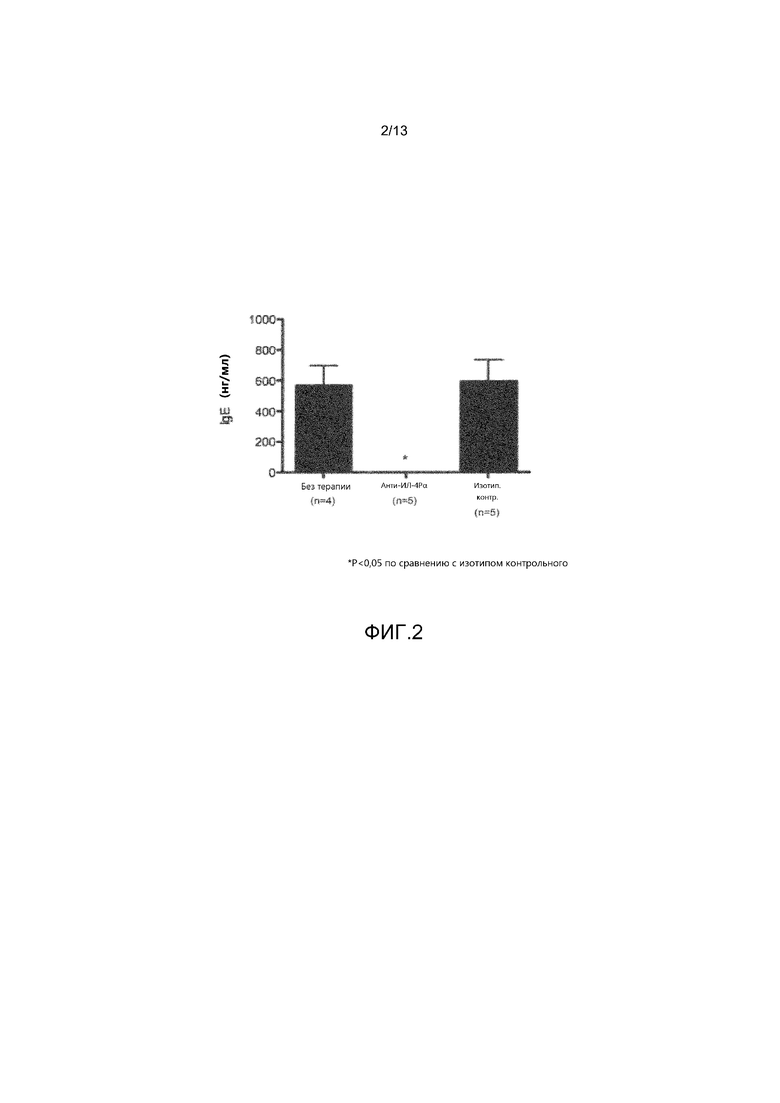
На фиг. 2 показаны уровни IgE у мышей трех групп, результаты для которых показаны на фиг. 1, после выполнения провокационной пробы с введением экстракта арахиса.
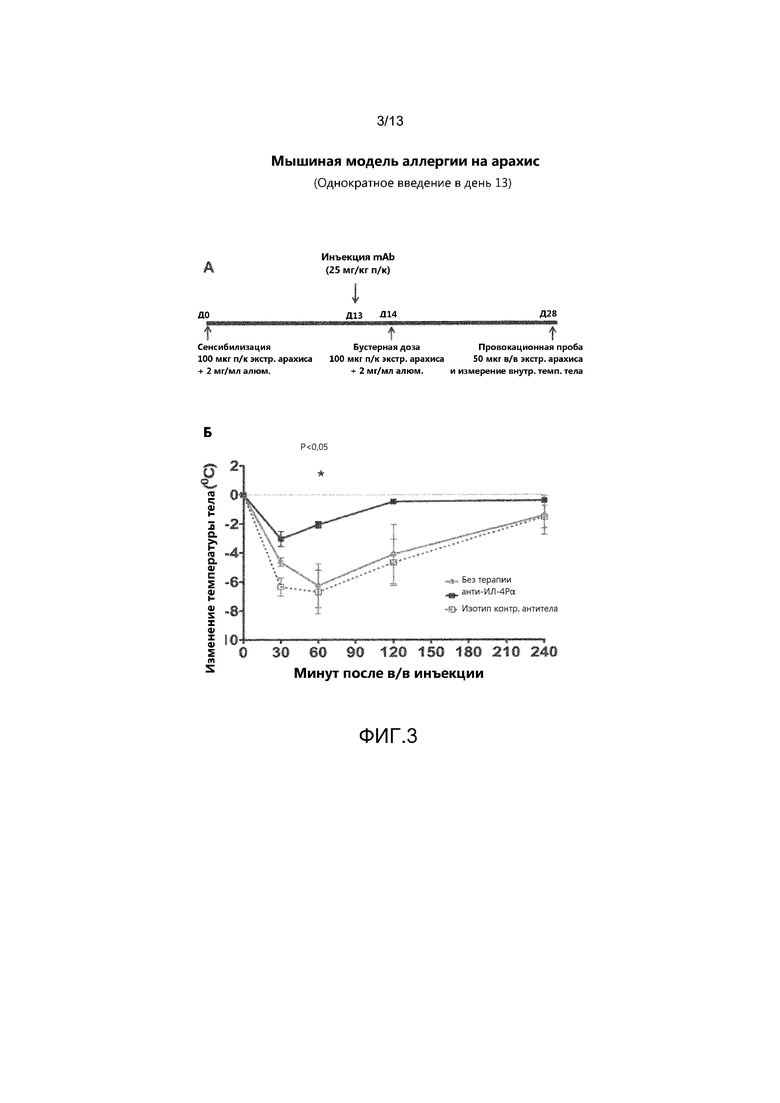
На фиг. 3, часть А, показана временная схема эксперимента с использованием мышиной модели с аллергией на арахис, в котором мыши получали одну дозу антитела анти-ИЛ-4Рα в день 13. В части Б показана степень тяжести анафилаксии у экспериментальных мышей трех групп, которую определяли на основании снижения внутренней температуры тела с течением времени после выполнения провокационной пробы с внутривенным введением экстракта арахиса. Значения для мышей, не получавших антитело, показаны серыми кружками; значения для мышей, получавших антитело анти-ИЛ-4Рα показаны черными квадратами; значения для мышей, получавших изотип контрольного антитела, показаны белыми квадратами.
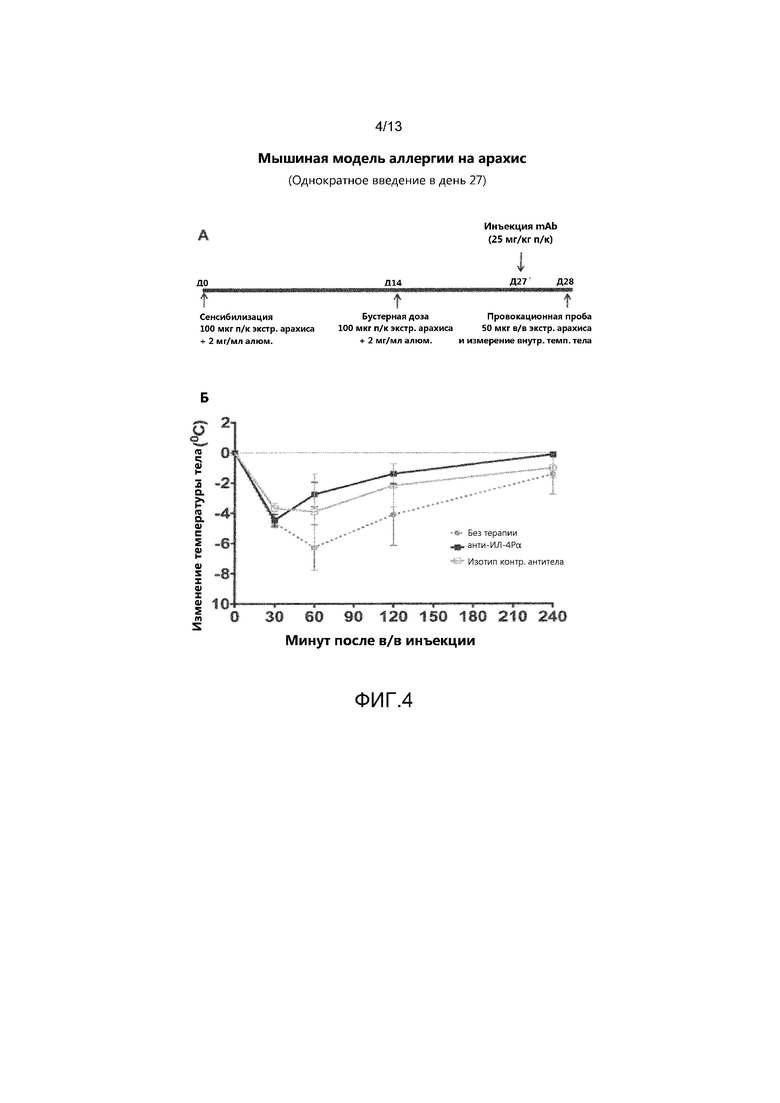
На фиг. 4, часть А, показана временная схема эксперимента с использованием мышиной модели с аллергией на арахис, в котором мыши получали одну дозу антитела анти-ИЛ-4Рα в день 27. В части Б показана степень тяжести анафилаксии у экспериментальных мышей трех групп, которую определяли на основании снижения внутренней температуры тела с течением времени после выполнения провокационной пробы с внутривенным введением экстракта арахиса. Значения для мышей, не получавших антитело, показаны серыми кружками; значения для мышей, получавших антитело анти-ИЛ-4Рα показаны черными квадратами; значения для мышей, получавших изотип контрольного антитела, показаны белыми квадратами.
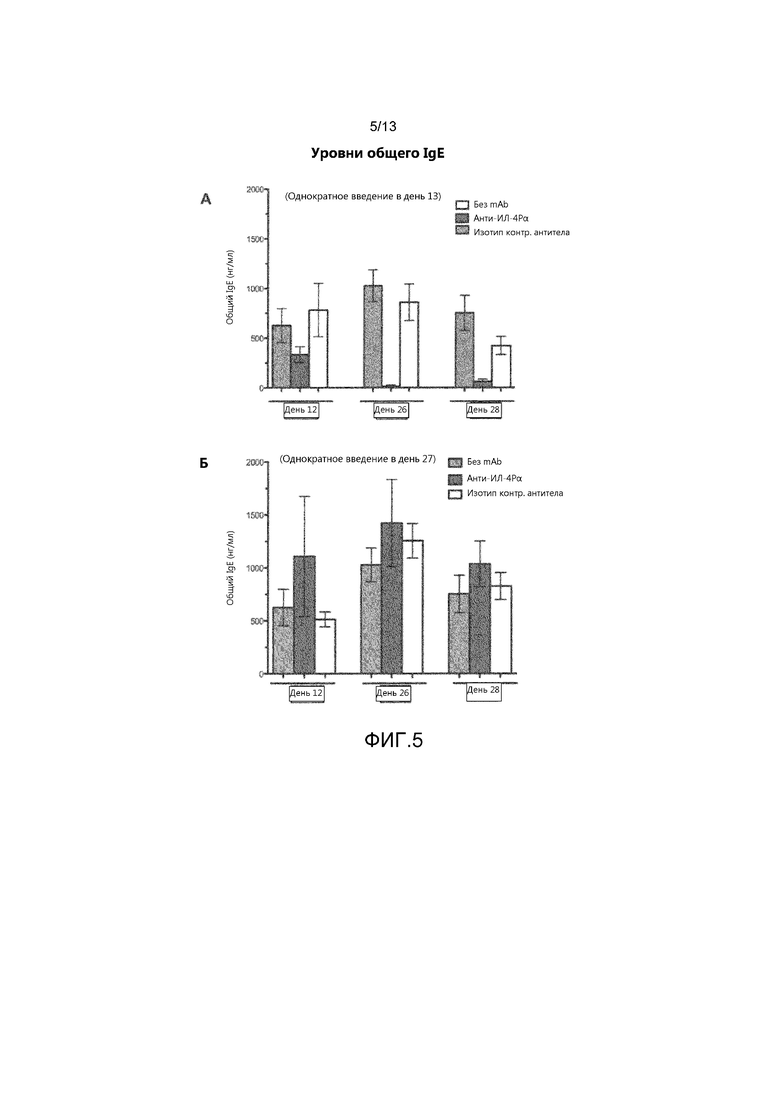
На фиг. 5 показаны уровни общего IgE у мышей трех групп, результаты для которых показаны на фиг. 3 и 4 (без введения mAb, введение анти-ИЛ-4Рα и введение изотипа контрольного антитела) в дни 12, 26 и 28 соответствующего эксперимента. В части А показаны результаты экспериментов, в которых животные получали одну дозу антитела в день 13; в части Б показаны результаты экспериментов, в которых животные получали одну дозу антитела в день 27.
На фиг. 6 показана временная схема эксперимента с использованием мышиной модели с применением специфической к арахису иммунотерапии, включавшей фазу формирования иммунного ответа при АСИ и провокационную пробу с введением экстракта арахиса. В указанные дни мыши получали пять инъекций антитела.
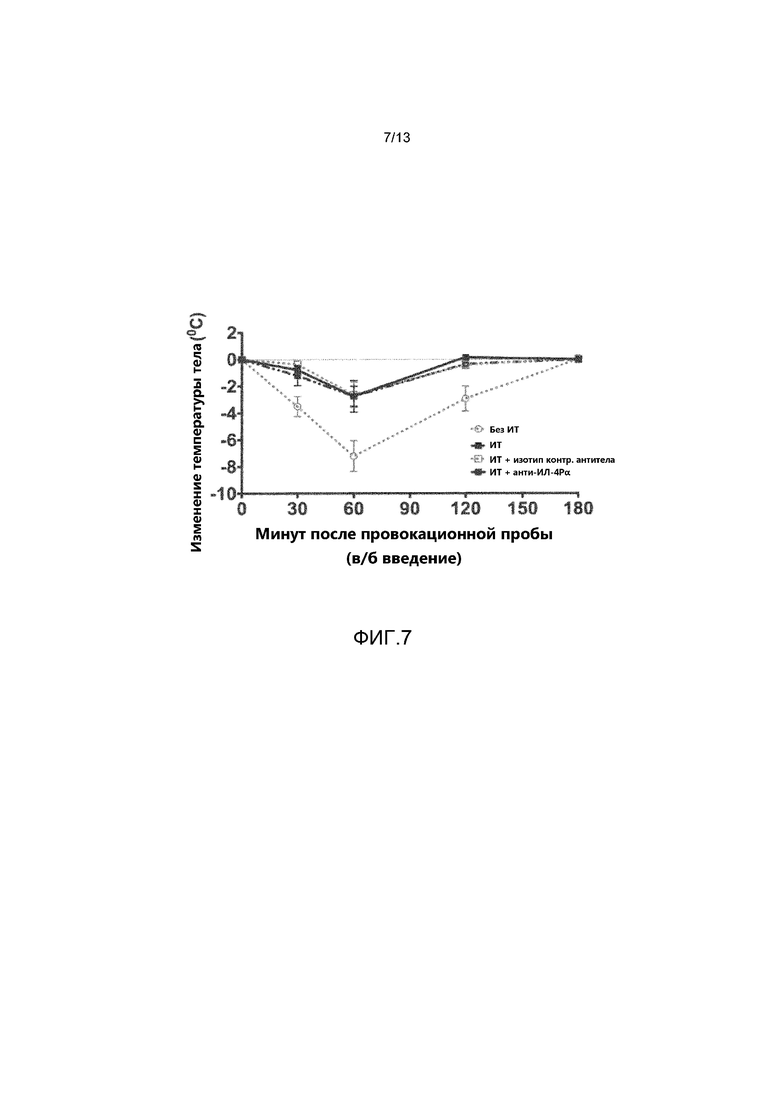
На фиг. 7 показана степень тяжести анафилаксии у экспериментальных мышей трех групп, получавших схема специфической к арахису иммунотерапии, схема которого показана на фиг. 6, а также у мышей контрольной группы, не получавших иммунотерапию. Степень тяжести анафилаксии определялись на основании снижения внутренней температуры тела с течением времени после выполнения провокационной пробы с введением экстракта арахиса. Значения для мышей, которым выполнили провокационную пробу с введением аллергена, но которые не получали иммунотерапию, показаны белыми кружками и штриховыми линиями («без ИТ»); значения для мышей, получавших иммунотерапию, но не получавших антитело, показаны черными квадратами и штриховой линией («ИТ»); значения для мышей, получавших иммунотерапию и изотип контрольного антитела, показаны белыми квадратами и штриховой линией («ИТ + изотип контрольного антитела»); значения для мышей, получавших иммунотерапию и антитело анти-ИЛ-4Рα, показаны черными квадратами и сплошной линией («ИТ + анти-ИЛ-4Рα»).
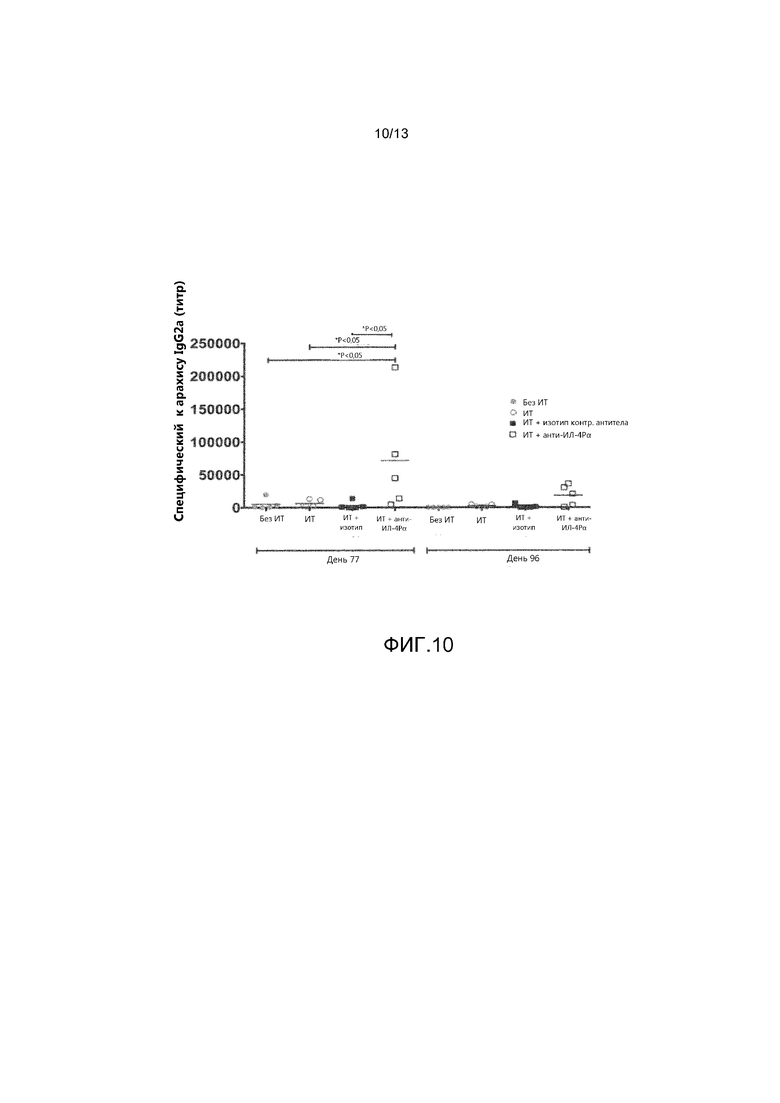
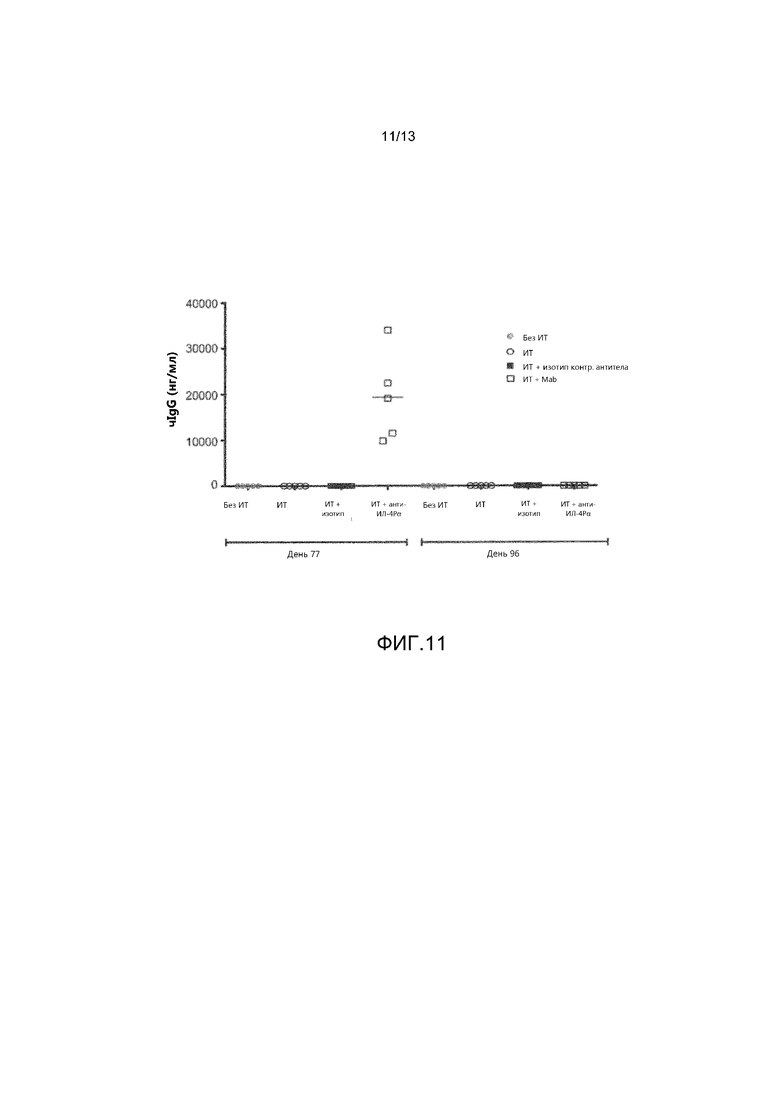
На фиг. 8, 9, 10 и 11 показаны уровни общего IgE (фиг. 8), уровни специфического для арахиса IgG1 (фиг. 9), уровни специфического для арахиса IgG2a (фиг. 10) и уровни hIgG (фиг. 11) у экспериментальных мышей трех групп, получавших специфическую к арахису схему иммунотерапии, показанную на фиг. 6, а также контрольной групп без иммунотерапии. Показаны различные уровни иммуноглобулина в дни 77 и 96. Значения для мышей, которым выполнили провокационную пробу с введением аллергена, но которые не получали иммунотерапию, показаны черными кружками («без ИТ»); значения для мышей, получавших иммунотерапию, но не получавших антитело, показаны белыми кружками («ИТ»); значения для мышей, получавших иммунотерапию и изотип контрольного антитела, показаны черными квадратами («ИТ + изотип контрольного антитела»); значения для мышей, получавших иммунотерапию и антитело анти-ИЛ-4Рα, показаны белыми квадратами («ИТ + анти-ИЛ-4Рα»). Каждый символ представляет уровень, измеренный у отдельной мыши.
На фиг. 12 показана временная схема эксперимента с использованием мышиной модели с применением специфической к арахису иммунотерапии, указана на фиг. 6, и в этом эксперименте в течение фазы формирования иммунного ответа мыши получали меньше доз экстракта арахиса (8 против 12). В указанные дни мыши получали пять инъекций антитела.
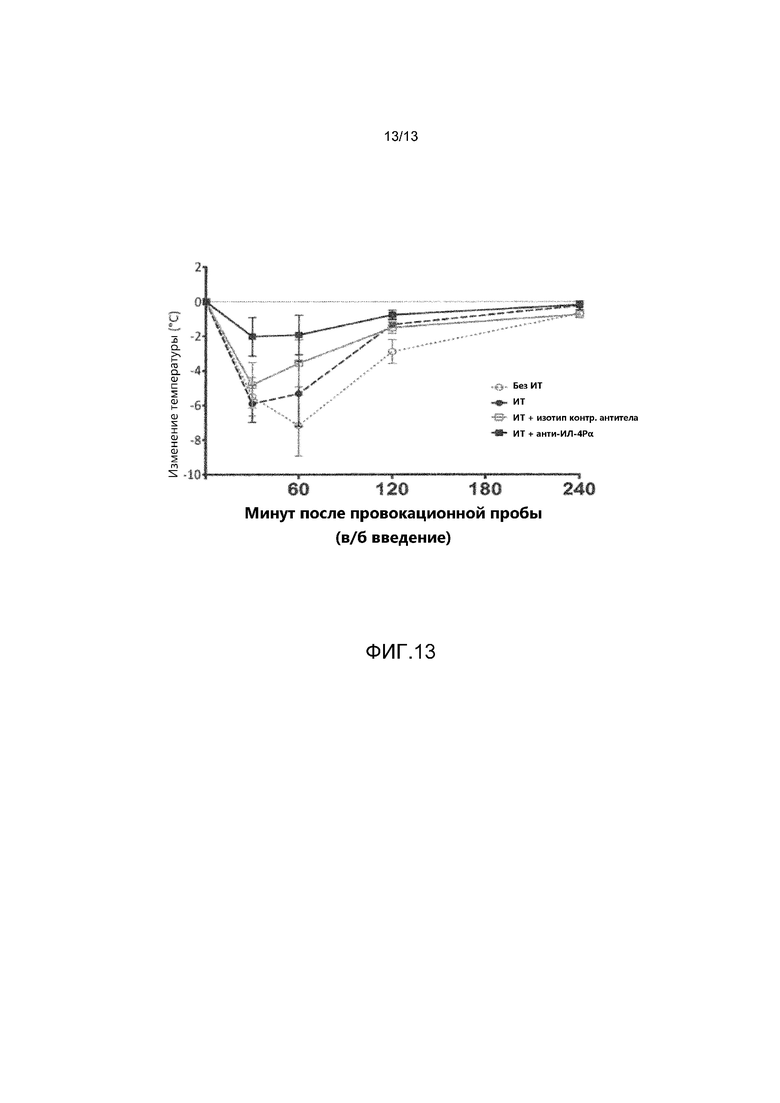
На фиг. 13 показана степень тяжести анафилаксии у экспериментальных мышей трех групп, получавших схему специфической к арахису иммунотерапии, показанную на фиг. 12, а также у мышей контрольной группы, не получавших иммунотерапию. Степень тяжести анафилаксии определялась на основании снижения внутренней температуры тела с течением времени после выполнения провокационной пробы с введением экстракта арахиса. Группы терапии соответствовали таковым, указанным на фиг. 6.
ПОДРОБНОЕ ОПИСАНИЕ
При интерпретации описания настоящего изобретения следует понимать, что его применение не ограничено описанными конкретными способами и экспериментальными условиями, поскольку эти способы и условия могу различаться. Следует также понимать и то, что терминология, используемая в этом документе, предназначена для описания только конкретных вариантов осуществления настоящего изобретения и не является ограничительной, поскольку объем настоящего изобретения будет ограничен только прилагаемой формулой изобретения.
Если не указано иное, все технические и научные термины, используемые в этом документе, имеют то же значение, что и значение, которое обычно понимается средним специалистом в рассматриваемой области, к которой принадлежит настоящее изобретение. В этом документе термин «приблизительно», в случае применения к конкретному указанному числовому значению, означает, что это значение может отличаться от указанного значения не более чем на 1%. Например, в этом документе выражение «приблизительно 100» включает значения 99 и 101 и все значения между ними (например, 99,1, 99,2, 99,3, 99,4 и т.д.).
Хотя любые способы и материалы, схожие со способами и материалами, описанными в этом документе, или эквивалентные им, могут применяться при реализации на практике настоящего изобретения, ниже рассматриваются предпочтительные способы и материалы. Все публикации, упомянутые в этом документе, полностью включены в данный документ посредством ссылок.
Способы лечения, профилактики или уменьшения степени тяжести аллергических реакций
Настоящее изобретение включает способы лечения и профилактики и (или) уменьшения степени тяжести аллергической реакции у субъекта. Способы согласно этому аспекту настоящего изобретения включают введение нуждающемуся в этом субъекту фармацевтической композиции, содержащей антагонист рецептора интерлейкина-4 (ИЛ-4Р), в терапевтически эффективном количестве. В этом документе термины «лечить», «лечение» и подобные им означают уменьшение степени тяжести симптомов, временное или постоянное устранение причины возникновения симптомов, либо профилактика или замедление возникновения симптомов аллергической реакции. В этом документе термин «нуждающийся в этом субъект» означает человека или животного, которые: (а) имеют предрасположенность к возникновению аллергических реакций при воздействии одного или более аллергенов; (б) ранее демонстрировали аллергический ответ или реакцию на один или более аллергенов; (в) имеют в анамнезе аллергические реакции; и (или) (г) демонстрируют признаки или симптомы аллергического ответа или анафилаксии.
Настоящее изобретение также включает способы снижения общих уровней IgE в сыворотке крови у субъекта, подвергнутого воздействию аллергена. Способы согласно этому аспекту настоящего изобретения включают введение субъекту фармацевтической композиции, содержащей антагонист рецептора интерлейкина-4 (ИЛ-4Р), в количестве, достаточном для снижения или полного устранения образования IgE либо для снижения или полного устранения уровней IgE в сыворотке крови у субъекта. В этом документе «снижение уровня IgE в сыворотке крови» означает, что измеренный уровень IgE в сыворотке крови у субъекта, подвергнутого воздействию аллергена и получившего лечение антагонистом ИЛ-4Р, по меньшей мере на 5%, 10%, 20%, 50%, 80% или 90% ниже, чем измеренный уровень IgE в сыворотке крови у этого же или аналогичного субъекта, который не получал лечение антагонистом ИЛ-4. Согласно некоторым вариантам осуществления настоящего изобретения, снижение уровня IgE в сыворотке крови означает, что в сыворотке крови субъекта аллерген-специфический IgE не определяется или определяется в незначительных количествах.
В этом документе фразы «аллергический ответ», «аллергическая реакция», «симптом аллергии» и подобные им означают один или более признаков или симптомов, выбранных из группы, включающей крапивницу (например аллергическую сыпь), ангионевротический отек, ринит, астму, рвоту, чихание, насморк, воспаление околоносовых пазух, слезотечение, свистящее дыхание, бронхоспазм, снижение максимальной скорости выдоха (ПСВ), нарушение функции желудочно-кишечного тракта, гиперемию кожи, отек губ, отек языка, снижение артериального давления, анафилаксию и органную дисфункцию/недостаточность. Фразы «аллергический ответ», «аллергическая реакция», «симптом аллергии» и т.д. также относятся к иммунологическим ответам и реакциями, таким как, например, повышение образования IgE и (или) повышение образования аллерген-специфического IgE.
Термин «аллерген», используемый в этом документе, означает любое вещество, химическую частицу или композицию, способную вызывать аллергический ответ у предрасположенного лица. Аллергены могут содержаться в или происходить из пищевых продуктов, таких как, например, молочные продукты (например коровье молоко), яйца, сельдерей, кунжут, пшеница, соя, рыба, морепродукты, сахара (например сахара, присутствующие в мясе, такие как альфа-галактоза), арахис, бобовые (например фасоль, горох, соя и др.) и орехи. Аллергены также могут содержаться в непищевых продуктах или происходить из непищевых продуктов, таких как, например, пыль (содержит продукты жизнедеятельности пылевого клеща), пыльца, яд насекомых (например яд пчел, ос, комаров, огненных муравьев и др.), грибковая плесень, мех животных, перхоть животных, шерсть, латекс, металлы (например никель), бытовые моющие средства, детергенты, лекарственные средства, косметика (например парфюмерия), лекарственные препараты (например пенициллин, сульфаниламиды, салицилаты и др.), терапевтические моноклональные антитела (например цетуксимаб), амброзия, трава и береза. Примерами пыльцевых аллергенов являются, например, пыльца деревьев, например пыльца березы, пыльца кедра, пыльца дуба, пыльца ольхи, пыльца граба, пыльца конского каштана, пыльца ивы, пыльца тополя, пыльца платана, пыльца липы, пыльца оливы, пыльца мексиканского можжевельника и пыльца Alstonia scholaris.
Способы настоящего изобретения включают введение субъекту фармацевтической композиции, содержащей антагонист ИЛ-4Р, до, после и (или) во время воздействия аллергена. Например, настоящее изобретение включает способы, заключающиеся в введении субъекту фармацевтической композиции, содержащей антагонист ИЛ-4Р, менее чем за 12 часов, менее чем за 10 часов, менее чем за 8 часов, менее чем за 6 часов, менее чем за 4 часа, менее чем за 2 часа, менее чем за 1 час или менее чем за 30 минут до воздействия аллергена. Согласно некоторым вариантам осуществления настоящего изобретения, фармацевтическую композицию, содержащую антагонист ИЛ-4Р, вводят субъекту за несколько дней или недель до воздействия аллергена (например от приблизительно 1 дня до приблизительно 2 недель до воздействия аллергена). Настоящее изобретение также включает способы, заключающиеся в введении субъекту фармацевтической композиции, содержащей антагонист ИЛ-4Р, менее чем за 12 часов, менее чем за 10 часов, менее чем за 8 часов, менее чем за 6 часов, менее чем за 4 часа, менее чем за 2 часа, менее чем за 1 час или менее чем за 30 минут после воздействия аллергена. В этом документе выражение «воздействие аллергена» означает любое случай, эпизод или происшествие, когда субъект глотает, вдыхает, касается или другим прямым или непрямым образом контактирует с аллергеном.
Настоящее изобретение также включает способы, заключающиеся в введении субъекту фармацевтической композиции, содержащей антагонист ИЛ-4Р, после возникновения у него одного или более симптомов аллергии. Например, настоящее изобретение включает способы, заключающиеся в введении субъекту фармацевтической композиции, содержащей антагонист ИЛ-4Р, сразу после, через 30 минут после, через 1 час после, через 2 часа после, через 4 часа после, через 6 часов после, через 8 часов после, через 10 часов после или через 12 часов после первого появления у него одного или более симптомов аллергии.
Настоящее изобретение также включает способы лечения, профилактики или уменьшения степени тяжести аллергической реакции, в которых аллергическую реакцию вызывает любой из вышеупомянутых аллергенов или классов аллергенов. Например, настоящее изобретение включает способы лечения, профилактики или уменьшения степени тяжести аллергической реакции, вызванной употреблением пищевого продукта или контактом с ним (например молоком, яйцами, пшеницей, соей, рыбой, морепродуктами, арахисом или орехами). Настоящее изобретение также включает способы лечения, профилактики или уменьшения степени тяжести аллергической реакции, вызванной непищевым аллергеном (например ядом насекомых, пылью, грибковой плесенью, перхотью животных, пыльцой, лекарственными средствами, амброзией, травами или березой).
Настоящее изобретение включает способы лечения, профилактики или уменьшения степени тяжести аллергической реакции, заключающиеся в введении нуждающемуся в этом субъекту фармацевтической композиции, содержащей антагонист ИЛ-4Р, в терапевтически эффективном количестве, причем фармацевтическую композицию вводят субъекту многократно, например в рамках конкретной схемы применения. Например, схема применения может включать многократное введение субъекту фармацевтической композиции с частотой приблизительно один раз в день, один раз в два дня, один раз в три дня, один раз в четыре дня, один раз в пять дней, один раз в шесть дней, один раз в неделю, один раз в две недели, один раз в три недели, один раз в четыре недели, один раз в месяц, один раз в два месяца, один раз в три месяца, один раз в четыре месяца или реже.
Способы настоящего изобретения, согласно некоторым вариантам осуществления настоящего изобретения, включают введение субъекту фармацевтической композиции, содержащей антагонист ИЛ-4Р, в терапевтически эффективном количестве в комбинации со вторым терапевтическим средством. Вторым терапевтическим средством может быть средство, выбранное из группы, включающей, например, стероиды, антигистаминные препараты, деконгестанты и анти- IgE препараты.
В этом документе фраза «в комбинации с» означает, что фармацевтическую композицию, содержащую антагонист ИЛ-4Р, вводят субъекту одновременно с вторым терапевтическим средством, непосредственно перед или непосредственно после применения второго терапевтического средства. Согласно некоторым вариантам осуществления настоящего изобретения, второе терапевтическое средство применяется совместно с антагонистом ИЛ-4Р. Согласно родственному варианту осуществления настоящего изобретения, настоящее изобретение включает способы, заключающиеся в введении фармацевтической композиции, содержащей антагонист ИЛ-4Р, в терапевтически эффективном количестве субъекту, получающему фоновую противоаллергическую терапию. Такая фоновая противоаллергическая терапия может включать курс применения, например, стероидов, антигистаминных препаратов, деконгестантов, анти- IgE препаратов., и пр. Антагонист ИЛ-4Р можно добавлять к фоновой противоаллергической терапии. Согласно некоторым вариантам осуществления настоящего изобретения, антагонист ИЛ-4Р добавляют к схеме «фоновой терапии с постепенным снижением дозы», при которой фоновая противоаллергическая терапия постепенно отменяется в течение периода времени (например со ступенчатым снижением дозы), в то время как антагонист ИЛ-4Р вводят субъекту в постоянной дозе либо в возрастающих дозах или в уменьшающихся дозах в течение периода времени.
Способы повышения эффективности и (или) безопасности аллерген-специфической иммунотерапии (АСИ)
Настоящее изобретение также включает способы повышения эффективности и (или) безопасности схемы аллерген-специфической иммунотерапии (АСИ). Способы согласно этому аспекту настоящего изобретения включают введение нуждающемуся в этом субъекту фармацевтической композиции, содержащей антагонист ИЛ-4Р, в терапевтически эффективном количестве непосредственно до введения или одновременно со схемой АСИ.
В этом документе выражения «аллерген-специфическая иммунотерапия», «специфическая иммунотерапия», «АСИ», «схема АСИ» и подобные им относятся к повторному введению аллергена субъекту в течение периода времени с целью лечения или профилактики аллергий и аллергических реакций или с целью снижения или устранения аллергических ответов. При типичной схеме АСИ субъекту с аллергией первоначально вводят небольшие количества аллергена с последующим введением аллергена в больших количествах. В некоторых случаях схема АСИ включает по меньшей мере две последовательные фазы: (1) фаза увеличения дозы и (2) поддерживающая фаза. В фазе увеличения дозы вводят возрастающие дозы аллергена до достижения эффективной и безопасной дозы. Дозу, установленную в конце фазы увеличения дозы, затем вводят субъекту в течение поддерживающей фазы. Длительность фазы увеличения дозы может составлять от нескольких недель до нескольких месяцев. Согласно некоторым вариантам осуществления настоящего изобретения, однако, фаза увеличения дозы имеет значительно меньшую длительность (например менее одной недели, менее 6 дней, менее 5 дней, менее 4 дней, менее 3 дней или менее 2 дней). Схемы АСИ, включающие фазу увеличения дозы длительностью менее 5 дней, иногда называют «срочной» иммунотерапией или «срочной АСИ». Поддерживающая фаза АСИ может длиться несколько недель, несколько месяцев, несколько лет или неопределенно долго.
Согласно этому аспекту настоящего изобретения, схема АСИ может включать введение пищевого аллергена, полученного из пищевого продукта, выбранного из группы, включающего молочные продукты, яйца, пшеницу, сою, рыбу, морепродукты, арахис и орехи. В качестве альтернативы, схема АСИ может включать введение непищевых аллергенов, выбранных из группы, включающей яд насекомых, пыль, грибковую плесень, перхоть животных, пыльцу, лекарственные средства, амброзию, траву или березу.
Согласно способам настоящего изобретения, антагонист ИЛ-4Р можно вводить субъекту на протяжении всего курса применения схемы АСИ или только в некоторые периоды курса применения схемы АСИ. Например, способы настоящего изобретения включают введение субъекту фармацевтической композиции, содержащей антагонист ИЛ-4Р, в терапевтически эффективном количестве с частотой приблизительно один раз в неделю, один раз в две недели, один раз в три недели, один раз в месяц, один раз в два месяца, один раз в четыре месяца, один раз в шесть месяцев или реже до начала или во время фазы увеличения дозы. Согласно некоторым вариантам осуществления настоящего изобретения, субъекту вводят фармацевтическую композицию, содержащую антагонист ИЛ-4Р, с частотой приблизительно один раз в неделю, один раз в две недели, один раз в три недели, один раз в месяц, один раз в два месяца, один раз в четыре месяца, один раз в шесть месяцев или реже во время или по окончании поддерживающей фазы.
Согласно настоящему изобретению, эффективность и (или) безопасность схемы АСИ «повышается», если у субъекта наблюдается один или более из следующих исходов или феноменов: (1) длительность фазы увеличения дозы уменьшается без ухудшения эффективности и безопасности; (2) длительность поддерживающей фазы уменьшается без ухудшения эффективности и безопасности; (3) количество доз аллергена, вводимых в течение фазы увеличения дозы или поддерживающей фазы, уменьшается без ухудшения эффективности и безопасности; (4) частота введения аллергена в течение фазы увеличения дозы или поддерживающей фазы уменьшается без ухудшения эффективности и безопасности; (5) доза аллергена, вводимая в течение фазы увеличения дозы или поддерживающей фазы, увеличивается без ухудшения эффективности и безопасности; (6) частота аллергических ответов или нежелательных побочных реакций, вызываемых схемой АСИ, снижается либо сводится к нулю; (7) применение или потребность в стандартных противоаллергических препаратах в течение фазы увеличения дозы или поддерживающей фазы (например стероидов, антигистаминных препаратов, деконгестантов, анти- IgE препаратов и т.д.) снижается или сводится к нулю; (8) уровень индуцированной аллергеном экспрессии IgE снижается; и (или) (9) частота аллергических реакций снижается или сводится к нулю. Эффективность схемы АСИ также считается «повышенной», согласно настоящему изобретению, если у субъекта наблюдается меньше тяжелых аллергических реакций и (или) они имеют меньшую степень тяжести после АСИ в комбинации с блокадой ИЛ-4Р по сравнению только с АСИ.
Настоящее изобретение также включает способы прекращения применения у субъекта схемы АСИ. Способы согласно этому аспекту настоящего изобретения включают введение субъекту одной или более доз фармацевтической композиции, содержащей антагонист ИЛ-4Р, и постепенное снижение частоты введения и (или) количества вводимого субъекту аллергена в течение применения схемы АСИ. Согласно некоторым вариантам осуществления настоящего изобретения, количество антагониста ИЛ-4Р увеличивают, тогда как количество вводимого аллергена в рамках схемы АСИ уменьшают. Предпочтительно, чтобы введение антагониста ИЛ-4Р позволило прекратить применение схемы АСИ с сохранением адекватной защиты от нежелательных аллергических реакций.
Антагонисты рецепторов интерлейкина-4
Способы настоящего изобретения включают введение нуждающемуся в этом субъекту терапевтической композиции, содержащей антагонист рецептора интерлейкина-4 (ИЛ-4Р). В этом документе «антагонистом ИЛ-4Р» (также упоминается в этом документе как «антагонист ИЛ-4Рα», «блокатор ИЛ-4Р», «блокатор ИЛ-4Рα» и др.) является любое средство, которое связывается или взаимодействует с ИЛ-4Рα или лигандом ИЛ-4Р и ингибирует или ослабляет нормальную биологическую сигнальную функцию, опосредованную рецептором ИЛ-4 типа 1 и (или) типа 2. Человеческий ИЛ-4Рα имеет аминокислотную последовательность со следующим идентификатором SEQ ID NO: 11. Рецептор ИЛ-4 типа 1 является димерным рецептором, имеющим цепь ИЛ-4Рα и цепь γc. Рецептор ИЛ-4 типа 2 является димерным рецептором, имеющим цепь ИЛ-4Рα и цепь ИЛ-13Рα1. Рецепторы ИЛ-4 типа 1 взаимодействуют с ИЛ-4 и стимулируются ИЛ-4, тогда как рецепторы ИЛ-4 типа 2 взаимодействуют как с ИЛ-4, так и ИЛ-13 и стимулируются ими. В связи с этими антагонисты ИЛ-4Р, которые могут использоваться для способов настоящего изобретения, могут блокировать сигналы, опосредованные ИЛ-4, сигналы, опосредованные ИЛ-13, и сигналы, опосредованные как ИЛ-4, так и ИЛ-13. Таким образом, антагонисты ИЛ-4Р настоящего изобретения могут препятствовать взаимодействию ИЛ-4 и (или) ИЛ-13 с рецепторами типа 1 или типа 2.
Примерами категорий антагонистов ИЛ-4Р, помимо прочего, являются низкомолекулярные антагонисты ИЛ-4Р, аптамеры к ИЛ-4Р, пептидные антагонисты ИЛ-4Р (например молекула типа «пептитело»), гибридные молекулы, содержащие фрагменты рецептора и антитела (например молекулы, полученные методом генной инженерии, содержащие лиганд-связывающий домен ИЛ-4Р) и антитела или антигенсвязывающие фрагменты антител, которые специфически связываются с человеческим ИЛ-4Рα. В этом документе к антагонистам ИЛ-4Р также относятся антигенсвязывающие белки, которые специфически связываются с ИЛ-4 и (или) ИЛ-13.
Антитела к ИЛ-4Рα и их антигенсвязывающие фрагменты
Согласно некоторым вариантам осуществления настоящего изобретения, антагонист ИЛ-4Р представляет собой антитело к ИЛ-4Рα или его антигенсвязывающий фрагмент. Термин «антитело», используемый в этом документе, относится к молекулам иммуноглобулинов, состоящим из четырех полипептидных цепей: двух тяжелых (H) цепей и двух легких (L) цепей, соединенных дисульфидными связями, а также к их мультимерам (например IgM). У типичного антитела каждая тяжелая цепь содержит вариабельную область (в этом документе используется сокращение HCVR или VH) и константную область. Константная область тяжелой цепи включает три домена: CH1, CH2 и CH3. Каждая легкая цепь состоит из вариабельной области (в этом документе используется сокращение LCVR или VL) и константной области. Константная область включает один домен (CL1). Области VH и VL в свою очередь включают гипервариабельные участки, называемые определяющими комплементарность участками (CDR), которые перемежаются с боле консервативными участками, называемыми каркасными (FR). Каждая область VH и VL включает три участка CDR и четыре участка FR, которые располагаются от N-конца до карбоксильного конца белковой цепи в следующем порядке: FR1, CDR1, FR2, CDR2, FR3, CDR3, FR4. Согласно различным вариантам осуществления настоящего изобретения, участки FR антитела к ИЛ-4Р (или его антигенсвязывающего фрагмента) могут иметь последовательность, идентичную герминативным последовательностям человека или могут иметь естественные или искусственные модификации. Аминокислотную консенсусную последовательность можно определить путем непосредственного сопоставления двух или более участков CDR.
Термин «антитело», используемый в этом документе, также включает антигенсвязывающие фрагменты или полные молекулы антител. Термины «антигенсвязывающая часть» антитела, «антигенсвязывающий фрагмент» антитела и им подобные, используемые в этом документе, включают любые естественные, получаемые ферментативным путем, синтетические или получаемые методом генной инженерии полипептиды или гликопротеины, которые специфически связываются с антигеном с образованием комплекса. Антигенсвязывающие фрагменты антитела можно получить, например, из полных молекул антител путем использования любых подходящих стандартных методик, например протеолитического расщепления или генной инженерии с применением рекомбинантных технологий с изменением и экспрессией ДНК, кодирующей вариабельные и, в некоторых случаях, константные домены антитела. Такая ДНК известна и (или) легко доступна из, например, коммерческих источников, библиотек ДНК (включая, например, библиотеки фаговых антител), либо ее можно синтезировать. ДНК можно секвенировать или изменять химически либо с помощью методик молекулярной биологии, например, для придания одному или более вариабельным и (или) константным доменам подходящей конфигурации, или для введения кодонов, создания цистеиновых остатков, модификации, добавления или удаления аминокислот и т. д.
Примерами антигенсвязывающих фрагментов, помимо прочего, являются: (i) фрагменты Fab; (ii) фрагменты F(ab')2; (iii) фрагменты Fd; (iv) фрагменты Fv; (v) одноцепочечные молекулы Fv (scFv); (vi) фрагменты dAb; и (vii) единицы минимального распознавания аминокислотных остатков, имитирующих гипервариабельные участки антитела (например отдельный определяющий комплементарность участок (CDR), такой как пептид CDR3), или пептиды c ограниченной конформационной свободой FR3-CDR3-FR4. Другие генно-инженерные молекулы, например домен-специфические антитела, антитела с одним доменом, антитела с удаленным доменом, химерные антитела, CDR-привитые антитела, диатела, триатела, тетратела, минитела, нанотела (например моновалентные нанотела, бивалентные нанотела и др.), иммунофармацевтические вещества на основе низкомолекулярного модульного белка (SMIP) и вариабельные акульи домены IgNAR, также входят в понятие «антигенсвязывающий фрагмент» в данном документе.
Антигенсвязывающий фрагмент антитела обычно включает по меньшей мере один вариабельный домен. Вариабельный домен может иметь любой размер или аминокислотную последовательность и обычно включает по меньшей мере один участок CDR, который прилежит к каркасному участку или находится в каркасном участке с одной или более последовательностями каркасного участка. В антигенсвязывающих фрагментах с доменом VH, связанным с доменом VL домены VH и VL могут располагаться относительно друг друга любым подходящим образом. Например, вариабельная область может быть димерной и содержать димеры VH-VH, VH-VL или VL-VL. В качестве альтернативы, антигенсвязывающий фрагмент антитела может содержать мономерный домен VH или VL.
Согласно некоторым вариантам осуществления настоящего изобретения, антигенсвязывающий фрагмент антитела может содержать по меньшей мере один вариабельный домен, ковалентно связанный по меньшей мере с одним константным доменом. Примерами конфигураций вариабельных и константных доменов, которые можно обнаружить в антигенсвязывающем фрагменте антитела в рамках настоящего изобретения, помимо прочего, являются: (i) VH-CH1; (ii) VH-CH2; (iii) VH-CH3; (iv) VH-CH1-CH2; (v) VH-CH1-CH2-CH3; (vi) VH-CH2-CH3; (vii) VH-CL; (viii) VL-CH1; (ix) VL-CH2; (x) VL-CH3; (xi) VL-CH1-CH2; (xii) VL-CH1-CH2-CH3; (xiii) VL-CH2-CH3; и (xiv) VL-CL. При любой конфигурации вариабельных и константных доменов, включая любую из представленных выше конфигураций, вариабельные и константные домены могу либо быть напрямую связаны друг с другом, либо связаны посредством полной или частичной шарнирной области либо посредством линкерной области. Шарнирная область может включать по меньшей мере 2 (например, 5, 10, 15, 20, 40, 60 или более) аминокислоты, что приводит к возникновению гибкой или полугибкой связи между прилежащими вариабельными и (или) константными доменами в молекуле, представляющей собой одиночный полипептид. Кроме того, антигенсвязывающий фрагмент антитела в рамках настоящего изобретения может включать гомодимер или гетеродимер (или другой мультимер) с любой из перечисленных вышей конфигураций вариабельных и константных доменов, связанных друг с другом нековалентной связью, и (или) с одним или более мономерными доменами VH или VL (например, дисульфидной(-ыми) связью(-ями)).
Термин «антитело», используемый в этом документе, также включает мультиспецифические (например биспецифические) антитела. Мультиспецифическое антитело или антигенсвязывающий фрагмент антитела обычно содержит по меньшей мере два разных вариабельных домена, причем каждый вариабельный домен способен специфически связываться с отдельным антигеном или с различными эпитопами этого же антигена. Любое мультиспецифическое антитело можно подготовить для использования в качестве антитела или антигенсвязывающего фрагмента антитела настоящего изобретения с помощью стандартных методик, доступных в рассматриваемой области. Например, настоящее изобретение включает способы, в которых используются биспецифические антитела, причем один фрагмент иммуноглобулина обладает специфичностью к ИЛ-4Рα или его фрагменту, а другой фрагмент иммуноглобулина обладает специфичностью ко второй терапевтической мишени или конъюгирован с терапевтическим веществом. Примерами биспецифических антител, которые можно использовать в контексте настоящего изобретения, являются, без ограничения, например биспецифические антитела на основе scFv или диатела, продукты слияния IgG и scFv, Ig с двойным вариабельным доменом (ДВД), антитела квадромы, антитела с укладкой типа «выступ в углублении», общие легкие цепи (например общие легкие цепи c укладкой типа «выступ в углублении»), антитела CrossMab, антитела CrossFab, антитела SEED, «лейциновая застежка», антитела Duobody, IgG1/IgG2, IgG с фрагментом Fab с двойным действием (DAF), и биспецифические антитела Mab2 (для получения информации о вышеперечисленных антитела см., например, Klein с соавт. 2012, mAbs 4:6, 1-11, а также упомянутые в другом месте этого документа источники). Биспецифические антитела также можно получить путем конъюгирования антитела с белком/нуклеиновой кислотой, например, когда синтетические аминокислоты с ортогональной химической реактивностью используют для получения сайт-специфического конъюгата антитела и олигонуклеотида, который затем самостоятельно трансформируется в мультимерный комплекс с заданной структурой, валентностью и геометрией. (См., например, Kazane с соавт., J. Am. Chem. Soc. [Epub: Dec. 4, 2012]).
Антитела, используемые для способов настоящего изобретения, могут быть человеческими антителами. Термин «человеческое антитело», используемый в этом документе, включает антитела с вариабельными и константными областями, полученными из герменативных последовательностей иммуноглобулина человека. Человеческие антитела, являющиеся предметом настоящего изобретения, могут, тем не менее, включать аминокислотные остатки, не кодируемые герминативными последовательностями иммуноглобулина человека (например мутации, возникшие вследствие случайного сайт-специфического мутагенеза in vitro, или соматические мутации, возникшие in vivo), например в участках CDR и, в частности, в участке CDR3. Однако термин «человеческое антитело», используемый в этом документе, не включает антитела, в которых последовательности CDR, полученные из герминативных последовательностей других видов млекопитающих, например мышей, были внесены в каркасную последовательность у человека.
Антитела, используемые для способов настоящего изобретения, могут быть рекомбинантными человеческими антителами. Термин «рекомбинантное человеческое антитело», используемый в этом документе, включает все человеческие антитела, приготовленные, экспрессированные, созданные или выделенные с помощью рекомбинантных методик, например антитела, экспрессированные с применением вектора рекомбинантной экспрессии, трансфицированного в клетку-хозяина (описано ниже), антитела, выделенные из библиотеки рекомбинантных комбинаторных антител человека (описано ниже), антитела, изолированные от животного (например мышей), являющегося трансгенным для генов иммуноглобулина человека (см., например, Taylor с соавт. (1992) Nucl. Acids Res. 20:6287-6295) или антитела, приготовленные, экспрессированные, созданные или выделенные любым другим способом, который включает сплайсинг гена иммуноглобулина человека до других последовательностей ДНК. Такие рекомбинантные человеческие антитела имеют вариабельные и константные области, полученные из герминативной последовательностей иммуноглобулина человека. Согласно некоторым вариантам осуществления настоящего изобретения, однако, такие рекомбинантные человеческие антитела подвержены мутагенезу in vitro (или, когда используется животное с трансгенностью в отношении последовательностей человеческого Ig, соматическому мутагенезу in vivo), и, таким образом, аминокислотные последовательности областей VH и VL рекомбинантных антител представляют собой последовательности, которые, хотя и получены из родственных для человека герминативных последовательностей VH и VL, могут отсутствовать в нормальных условиях в герминативном наборе антител человека in vivo.
Согласно некоторым вариантам осуществления настоящего изобретения, антитела, используемые для способов настоящего изобретения, специфически связываются с ИЛ-4Рα. Термин «специфически связывается» и подобные ему означают, что антитело или его антигенсвязывающий фрагмент образуют комплекс с антигеном, который относительно стабилен в физиологических условиях. Способы определения того, специфически ли связываются антитела с антигеном хорошо известны в рассматриваемой области и включают, например, равновесный диализ, поверхностный плазмонный резонанс, и тому подобные способы. Например, антитело, которое «специфически связывается» с ИЛ-4Рα, в контексте настоящего изобретения включает антитела, которые связываются с ИЛ-4Рα или его частью с KD менее приблизительно 1000 нМ, менее приблизительно 500 нМ, менее приблизительно 300 нМ, менее приблизительно 200 нМ, менее приблизительно 100 нМ, менее приблизительно 90 нМ, менее приблизительно 80 нМ, менее приблизительно 70 нМ, менее приблизительно 60 нМ, менее приблизительно 50 нМ, менее приблизительно 40 нМ, менее приблизительно 30 нМ, менее приблизительно 20 нМ, менее приблизительно 10 нМ, менее приблизительно 5 нМ, менее приблизительно 4 нМ, менее приблизительно 3 нМ, менее приблизительно 2 нМ, менее приблизительно 1 нМ или менее приблизительно 0,5 нМ, при определении с помощью метода поверхностного плазмонного резонанса. Выделенное антитело, которые специфически связывается с ИЛ-4Рα, может, однако, иметь перекрестную реактивность к другим антигенам, например молекулам ИЛ-4Рα других видов животных (не человека).
Согласно некоторым вариантам осуществления настоящего изобретения, антагонист ИЛ-4Р является антителом к ИЛ-4Рα или его антигенсвязывающим фрагментом и содержит вариабельную область тяжелой цепи (HCVR), вариабельную область легкой цепи (LCVR) и (или) определяющие комплементарность участки (CDR) с любой аминокислотной последовательностью антитела к ИЛ-4Р, указанной в патенте США № 7,608,693. Согласно некоторым вариантам осуществления настоящего изобретения, антитело к ИЛ-4Рα или его антигенсвязывающий фрагмент, который можно использовать в контексте способов настоящего изобретения, содержит определяющие комплементарность участки тяжелой цепи (HCDR) вариабельной области тяжелой цепи (HCVR) с аминокислотной последовательностью с идентификатором SEQ ID NO:1 и определяющие комплементарность участки легкой цепи (LCDR) вариабельной области легкой цепи (LCVR) с аминокислотной последовательностью с идентификатором SEQ ID NO:2. Согласно некоторым вариантам осуществления настоящего изобретения, антитело к ИЛ-4Рα или его антигенсвязывающий фрагмент содержит три HCDR (HCDR1, HCDR2 и HCDR3) и три LCDR (LCDR1, LCDR2 и LCDR3), причем HCDR1 имеет аминокислотную последовательность с идентификатором SEQ ID NO:3; HCDR2 имеет аминокислотную последовательность с идентификатором SEQ ID NO:4; HCDR3 имеет аминокислотную последовательность с идентификатором SEQ ID NO:5; LCDR1 имеет аминокислотную последовательность с идентификатором SEQ ID NO:6; LCDR2 имеет аминокислотную последовательность с идентификатором SEQ ID NO:7; и LCDR3 имеет аминокислотную последовательность с идентификатором SEQ ID NO:8. Согласно другим вариантам осуществления настоящего изобретения антитело к ИЛ-4Р или его антигенсвязывающий фрагмент содержит HCVR с аминокислотной последовательностью с идентификатором SEQ ID NO:1 и LCVR с аминокислотной последовательностью с идентификатором SEQ ID NO:2. Согласно некоторым вариантам осуществления настоящего изобретения, способы настоящего изобретения включают использование антитела к ИЛ-4Рα, известного в рассматриваемой области как дупилумаб, или его биоэквивалента.
К другим антителам к ИЛ-4Рα, которые можно использовать в контексте способов настоящего изобретения, относятся, например, антитело, известное в рассматриваемой области как AMG317 (Corren с соавт., 2010, Am J Respir Crit Care Med., 181(8):788-796), или любые антитела к ИЛ-4Рα, указанные в патенте США № 7,186,809, патенте США № 7,605,237, патенте США № 7,608,693 или патенте США № 8,092,804.
Антитела к ИЛ-4Рα, используемые в контексте способов настоящего изобретения, могут иметь pH-зависимые характеристики связывания. Например, антитело к ИЛ-4Рα, используемое для способов настоящего изобретения, может демонстрировать снижение связывания с ИЛ-4Рα при кислом pH по сравнению с нейтральным pH. В качестве альтернативы, антитело к ИЛ-4Рα настоящего изобретения может демонстрировать повышение связывания с его антигеном при кислом pH по сравнению с нейтральным pH. Выражение «кислый pH» охватывает значения pH менее 6,2, например приблизительно 6,0, 5,95, 5,9, 5,85, 5,8, 5,75, 5,7, 5,65, 5,6, 5,55, 5,5, 5,45, 5,4, 5,35, 5,3, 5,25, 5,2, 5,15, 5,1, 5,05, 5,0 или менее. В этом документе выражение «нейтральный pH» означает значение pH приблизительно от 7,0 до 7,4. Выражение «нейтральный pH» включает значения pH приблизительно 7,0, 7,05, 7,1, 7,15, 7,2, 7,25, 7,3, 7,35 и 7,4.
В некоторых случаях «снижение связывания с ИЛ-4Рα при кислом pH по сравнению с нейтральным pH» выражается в виде отношения значения KD связывания антитела с ИЛ-4Рα при кислом pH и отношения значения KD связывания антитела с ИЛ-4Рα при нейтральном pH (или наоборот). Например, антитело или его антигенсвязывающий фрагмент могут рассматриваться как демонстрирующие «снижение связывания с ИЛ-4Рα при кислом pH по сравнению с нейтральным pH» для целей настоящего изобретения, если отношение значений KD при кислом или нейтральном pH для антитела или его антигенсвязывающего фрагмента составляет приблизительно 3,0 или более. Согласно некоторым вариантам осуществления настоящего изобретения, отношение значений KD при кислом или нейтральном pH для антитела или его антигенсвязывающего фрагмента настоящего изобретения может составлять приблизительно 3,0, 3,5, 4,0, 4,5, 5,0, 5,5, 6,0, 6,5, 7,0, 7,5, 8,0, 8,5, 9,0, 9,5, 10,0, 10,5, 11,0, 11,5, 12,0, 12,5, 13,0, 13,5, 14,0, 14,5, 15,0, 20,0. 25,0, 30,0, 40,0, 50,0, 60,0, 70,0, 100,0 или более.
Антитела с pH-зависимыми характеристиками связывания можно получить, например, путем скрининга антител на предмет сниженного (или повышенного) связывания с конкретным антигеном при кислом pH по сравнению с нейтральным pH. Кроме того, модификация антигенсвязывающего домена на уровне аминокислот может дать антитела с pH-зависимыми характеристиками связывания. Например, путем замены одной или более аминокислот антигенсвязывающего фрагмента (например в пределах CDR) гистидиновым остатком, можно получить антитело со сниженным связыванием с антигеном при кислом pH по сравнению с нейтральным pH. В этом документе выражение «кислый pH» означает значение pH 6,0 или менее.
Фармацевтические композиции
Настоящее изобретение включает способы, заключающиеся в введении субъекту антагониста ИЛ-4Р, в которых антагонист ИЛ-4Р входит в состав фармацевтической композиции. В состав фармацевтических композиций, имеющих отношение к настоящему изобретению, входят подходящие носители, вспомогательные вещества и другие вещества, обеспечивающие надлежащие перенос, доставку и переносимость композиции, а также прочие ее свойства. Множество подходящих лекарственных форм можно найти в справочниках, известных всем химикам-фармацевтам: Remington's Pharmaceutical Sciences, Mack Publishing Company, Easton, PA, США. К этим лекарственным формам относятся: порошки, пасты, мази, желе, воски, масла, липиды, липидосодержащие везикулы (катионные или анионные) (например LIPOFECTIN™), конъюгаты ДНК, безводные абсорбционные пасты, эмульсия масла в воде и воды в масле, эмульсия карбовакса (твердый полиэтиленгликоль различной молекулярной массы), полутвердые гели и полутвердые смеси, содержащие карбовакс. См. также Powell с соавт. «Compendium of excipients for parenteral formulations» PDA (1998) J Pharm Sci Technol 52:238-311.
Известны и могут использоваться различные системы доставки фармацевтической композиции по настоящему изобретению, например препараты, инкапсулированные в липосомах, микрочастицы, микрокапсулы, рекомбинантные клетки, способные экспрессировать мутантные вирусы, опосредованный рецепторами эндоцитоз (см., например, Wu с соавт., 1987, J. Biol. Chem. 262:4429-4432). Способы введения включают, помимо прочего, внутрикожное, внутримышечное, внутрибрюшное, внутривенное, подкожное, интраназальное, эпидуральное и пероральное введение, а также другие способы. Настоящая композиция может быть доставлена в организм любым удобным способом, например путем инфузии или болюсной инъекции, либо за счет всасывания через эпителиальные и слизисто-кожные выстилки (например, слизистая оболочка полости рта, прямой кишки и кишечника); также ее можно вводить с другими биологически активными средствами.
Фармацевтическую композицию по настоящему изобретению можно вводить подкожно или внутривенно с помощью стандартных иглы и шприца. Кроме того, что касается подкожного введения, то фармацевтическую композицию по настоящему изобретению можно вводить с помощью устройства для доставки, представляющего собой шприц-ручку. Такое устройство для доставки, представляющее собой шприц-ручку, может быть предназначено для многократного или однократного пользования. Устройство для доставки, представляющее собой шприц-ручку многократного пользования, обычно имеет заменяемый картридж, содержащий фармацевтическую композицию. После введения фармацевтической композиции, содержащейся в картридже, пустой картридж можно выбросить и заменить на новый, содержащий фармацевтическую композицию. Устройство для доставки, представляющее собой шприц-ручку, затем можно использовать заново. Устройство для доставки, представляющее собой шприц-ручку однократного пользования, не имеет заменяемого картриджа. Скорее, устройство для доставки, представляющее собой шприц-ручку однократного пользования, поступает заполненным фармацевтической композицией, находящейся в емкости внутри устройства. После опорожнения емкости от фармацевтической композиции, устройство полностью выбрасывают.
В некоторых случаях фармацевтическую композицию можно вводить с помощью системы с контролируемым высвобождением лекарственного вещества. Согласно одному варианту осуществления настоящего изобретения, можно использовать помпу. Согласно другому варианту осуществления настоящего изобретения, можно использовать полимерные материалы; см. Medical Applications of Controlled Release, Langer and Wise (eds.), 1974, CRC Pres., Boca Raton, Florida, США. Согласно другому варианту осуществления настоящего изобретения, систему с контролируемой доставкой лекарственного вещества можно размещать вблизи целевого органа, что требует введения лишь части системной дозы (см., например, Goodson, 1984, in Medical Applications of Controlled Release, supra, vol. 2, pp. 115-138). Другие системы с контролируемой доставкой лекарственного вещества рассматриваются в обзорной статье Langer, 1990, Science 249:1527-1533.
К инъекционным препаратам могут относиться лекарственные формы для внутривенного, подкожного, внутрикожного и внутримышечного инъекционного введения, формы для внутривенного капельного введения и др. Эти инъекционные препараты можно готовить с помощью известных способов. Например, инъекционные препараты можно готовить путем растворения, суспендирования или эмульсифицирования антитела или его соли, описанной выше, в стерильной водной среде или масляной среде, обычно используемой для приготовления инъекционных препаратов. В качестве водных сред для приготовления инъекционных препаратов используются изотонический раствора хлорида натрия, изотонический раствор глюкозы и других вспомогательных веществ, например веществ, которые могут быть использованы в комбинации с подходящими солюбилизирующими веществами, например спиртом (например этиловым спиртом), полиспиртом (например пропиленгликолем, полиэтиленгликолем),), неионными сурфактантами (например, полисорбатом 80), аддуктом гидрогенизированного касторового масла HCO-50 (полиоксиэтилен (50 моль)) и др. В качестве масляной среды используются, например, кунжутное масло, соевое масло и др., которые можно использовать в комбинации с солюбилизирующим веществом, например бензилбензоатом, бензиловым спиртом и др. Приготовленный таким образом инъекционный препарат можно помещать в подходящую ампулу.
Предпочтительно, фармацевтические композиции для перорального или парентерального применения, рассмотренные выше, готовят в виде лекарственных форм с унифицированной дозой, соответствующей дозе действующих веществ. К таким лекарственным формам с унифицированной дозой относятся, например, таблетки, пилюли, капсулы, инъекционные лекарственные формы (раствор в ампулах), свечи и др.
Примеры фармацевтических композиций, содержащих антитело к ИЛ-4Р, которые можно использовать в контексте настоящего изобретения, указаны, например, в опубликованной патентной заявке для США № 2012/0097565.
Дозировка
Количество антагониста ИЛ-4Р (например, антитела к ИЛ-4Рα), вводимое субъекту согласно способам настоящего изобретения, обычно является терапевтически эффективным количеством. В этом документе фраза «терапевтически эффективное количество» означает количество антагониста ИЛ-4Р, вызывающие одно или более из нижеследующего: (а) уменьшение степени тяжести или длительности аллергической реакции; (б) уменьшение выраженности одного или более симптомов или признаков аллергической реакции; (в) профилактика или уменьшение выраженности анафилаксии; (г) снижение уровня IgE в сыворотке крови; (д) снижение частоты использования или необходимости использования стандартной противоаллергической терапии (например снижение частоты использования или отказ от использования антигистаминных препаратов, деконгестантов, интраназальных или ингаляционных стероидов, анти- IgE препаратов; и (е) снижение частоты аллергических ответов на аллерген-специфическую иммунотерапию (АСИ).
В случае антитела к ИЛ-4Рα, терапевтически эффективным количеством может быть количество от приблизительно 0,05 мг до приблизительно 600 мг, например приблизительно 0,05 мг, приблизительно 0,1 мг, приблизительно 1,0 мг, приблизительно 1,5 мг, приблизительно 2,0 мг, приблизительно 10 мг, приблизительно 20 мг, приблизительно 30 мг, приблизительно 40 мг, приблизительно 50 мг, приблизительно 60 мг, приблизительно 70 мг, приблизительно 80 мг, приблизительно 90 мг, приблизительно 100 мг, приблизительно 110 мг, приблизительно 120 мг, приблизительно 130 мг, приблизительно 140 мг, приблизительно 150 мг, приблизительно 160 мг, приблизительно 170 мг, приблизительно 180 мг, приблизительно 190 мг, приблизительно 200 мг, приблизительно 210 мг, приблизительно 220 мг, приблизительно 230 мг, приблизительно 240 мг, приблизительно 250 мг, приблизительно 260 мг, приблизительно 270 мг, приблизительно 280 мг, приблизительно 290 мг, приблизительно 300 мг, приблизительно 310 мг, приблизительно 320 мг, приблизительно 330 мг, приблизительно 340 мг, приблизительно 350 мг, приблизительно 360 мг, приблизительно 370 мг, приблизительно 380 мг, приблизительно 390 мг, приблизительно 400 мг, приблизительно 410 мг, приблизительно 420 мг, приблизительно 430 мг, приблизительно 440 мг, приблизительно 450 мг, приблизительно 460 мг, приблизительно 470 мг, приблизительно 480 мг, приблизительно 490 мг, приблизительно 500 мг, приблизительно 510 мг, приблизительно 520 мг, приблизительно 530 мг, приблизительно 540 мг, приблизительно 550 мг, приблизительно 560 мг, приблизительно 570 мг, приблизительно 580 мг, приблизительно 590 мг или приблизительно 600 мг антитела к ИЛ-4Р. Согласно некоторым вариантам осуществления настоящего изобретения, вводят 300 мг антитела к ИЛ-4Р.
Количество антагониста ИЛ-4Р, содержащееся в отдельной дозе, можно выражать в миллиграммах антитела на килограмм массы тела пациента (т. е. мг/кг). Например, антагонист ИЛ-4Р можно вводить пациенту в дозе приблизительно от 0,0001 до приблизительно 10 мг/кг массы тела.
ПРИМЕРЫ
Следующие примеры приведены с целью предоставления средним специалистам в рассматриваемой области полной информации и полного описания того, как надлежит выполнять и применять способы и композиции, являющиеся предметом настоящего изобретения, и не имеют своей целью ограничить ту область, которую изобретатели считают своим изобретением. Был приложены все усилия для обеспечения точности приведенных числовых значений (например количество, температура и т.д.), однако следует учитывать вероятность некоторых экспериментальных ошибок и отклонений. Если не указано иное, части — это части по массе, молекулярная масса — это средняя молекулярная масса, температура — это температура в градусах Цельсия и давление — это давление на уровне атмосферного давления или близкое к нему.
Пример 1. Блокада ИЛ-4Р предупреждает системную анафилаксию в мышиной модели с аллергией на арахис
В этом примере изучался эффект блокады ИЛ-4Рα на индуцированную арахисом анафилаксию у мышей. Схема протокола эксперимента представлена на фиг. 1А. Вкратце, по 5 мышей линии C57BL/6 в трех группах сенсибилизировали экстрактом сырого арахиса в дозе 100 мкг и квасцом (2 мг/мл) путем подкожного введения в день 0 с последующим введением бустерной дозы в день 14. В день 28 выполняли провокационную пробу с внутривенным введением экстракта арахиса в дозе 50 мкг. Мыши первой группы не получали терапию. Мыши второй группы получали подкожно противомышиное антитело к ИЛ-4Рα («анти-м-ИЛ-4Рα») в дозе 25 мг/кг в день 13 и день 27. Мыши третьей группы получали изотип контрольного антитела в день 13 и день 27. В этом примере противомышиным антителом к ИЛ-4Рα было антитело, содержащее HCVR с аминокислотной последовательностью с идентификатором SEQ ID NO:9, и LCVR с аминокислотной последовательностью с идентификатором SEQ ID NO:10.
Системная анафилаксия в этой модели проявлялась в виде снижения внутренней температуры тела. В связи с этим для оценки степени анафилаксии у этих экспериментальных животных измеряли внутреннюю температуру тела в течение 180 минут после выполнения провокационной пробы. Результаты показаны на фиг. 1Б. У мышей, не получавших терапию, и мышей, получавших изотип контрольного антитела, наблюдалось быстрое снижение внутренней температуры тела через 30 минут после выполнения провокационной пробы, что свидетельствует об анафилактической реакции. Внутренняя температура тела у контрольных мышей постепенно повышалась до исходного значения к 180-й минуте после выполнения провокационной пробы. В отличие от этого, у мышей, получавших анти-м-ИЛ-4Рα, наблюдалось только незначительное снижение внутренней температуры тела через 30 минут после выполнения провокационной пробы, и затем она возвращалась к норме на 60-й минуте. Различие в изменении внутренней температуры тела у мышей, получавших анти-м-ИЛ-4Рα, и контрольных мышей на 30-й минуте было статистически значимым (P<0,0001).
Также у мышей всех групп определяли терминальный уровень IgE (фиг. 2). Как показано на фиг., блокада ИЛ-4Рα существенно снижала уровни общего IgE до неопределяемых значений по сравнению с мышами, не получавшими лечения, и мышами, получавшими изотип контрольного антитела.
В рассматриваемых экспериментах животные получали две отдельные дозы антитела анти-м-ИЛ-4Рα (в день 13 и день 27). Затем на этой же мышиной модели с аллергией на арахис была проведена вторая серия экспериментов для оценки эффекта антитела после однократного введения в день 13 или день 27. Схема протокола эксперимента представлена на фиг. 3А (введение в день 13) и фиг. 4А (введение в день 27). Результаты показаны на фиг. 3Б и 4Б соответственно. У мышей, получавших однократного антитело анти-м-ИЛ-4Рα в день 13, наблюдалась значительно менее выраженная анафилаксия по сравнению с мышами, не получавшими терапию, и мышами, получавшими контрольное антитело (см. фиг. 3Б), однако защитный эффект не был настолько выраженным, как в эксперименте с введением двух доз (фиг. 1Б). Защитный эффект антитела анти-м-ИЛ-4Рα значительно ослаблялся у мышей, получавших одну дозу антитела в день 27 (см. фиг. 4Б).
В экспериментах с однократным введением антитела, уровни IgE определяли в образцах крови, взятых у животных в день 12, день 26 и день 28. Результаты показаны на фиг. 5А (введение в день 13) и фиг. 5Б (введение в день 27). Важно отметить, что эффект антитела анти-м-ИЛ-4Рα на системную анафилаксию коррелировал со степенью ингибирования образования IgE. Снижение уровней IgE не происходило сразу после введения антитела анти-м-ИЛ-4Рα, но наблюдалось приблизительно через 13 дней после его введения до того момента, когда уровни IgE полностью не определялись. Таким образом, этот пример подтверждает роль антагонизма ИЛ-4Р в предупреждении аллергических реакций.
Пример 2. Применение блокады ИЛ-4Р у животных с аллергией на арахис в сочетании со специфической иммунотерапией
Целью этого примера являлась оценка эффектов блокады ИЛ-4Рα в сочетании с аллерген-специфической иммунотерапией (АСИ). В этих экспериментах использовали модель мышей с аллергией на арахис, получавших специфическую иммунотерапию, разработанную частично на основе модели Kulis с соавт., J. Allergy Clin. Immunol. 127(1):81-88 (2011). Были проведены две серии экспериментов, описанных ниже.
Схема протокола эксперимента, использовавшегося для первой серии экспериментов, показана на фиг. 6. В этих экспериментах использовали четыре группы мышей. Мыши трех их этих четырех групп получали специфическую к арахису иммунотерапию, включавшую фазу сенсибилизации, фазу формирования иммунного ответа и фазу выполнения провокационной пробы. Фаза сенсибилизации включала внутрибрюшное введение экстракта арахиса в дозе 0,5 мг с 2 мг квасца в дни 0, 7 и 28. Фаза формирования иммунного ответа включала двенадцать отдельных введений различных доз экстракта арахиса без квасца в дни 49, 51, 53, 56, 58, 60, 63, 65, 67, 70, 72 и 74. Фаза выполнения провокационной пробы включала введение экстракта арахиса в дозе 1 мг в день 98.
В этих экспериментах использовались следующие группы терапии: животные группы А не получали ни иммунотерапию ни антитело («без ИТ»); животные группы Б получали иммунотерапию и не получали антитело («ИТ»); животные группы В получали иммунотерапию в сочетании с изотипом контрольного антитела в дни 36, 50, 57, 64 и 71 («ИТ+ изотип контрольного антитела»); и животные группы Г получали иммунотерапию в сочетании с антителом анти-м-ИЛ-4Рα (25 мг/кг подкожно) в дни 36, 50, 57, 64 и 71 («ИТ+ анти-м-ИЛ-4Рα»). В этих экспериментах использовали точно такое же антитело анти-м-ИЛ-4Рα, что и в примере 1 в этом документе.
Для оценки степени анафилаксии у этих экспериментальных животных измеряли внутреннюю температуру тела в течение 180 минут после выполнения провокационной пробы. Кроме того, в течение эксперимента (дни 35, 46, 77 и 98) у животных брали образцы крови для определения уровней иммуноглобулинов в сыворотке. Результаты по анафилаксии показаны на фиг. 7. Уровни общего IgE, IgG1, IgG2a и IgG в дни 77 и 96 показаны на фиг. 8, 9, 10 и 11 соответственно.
Результаты этих экспериментов показывают, что аллерген-специфическая иммунотерапия сама по себе защищает от индуцированной арахисом системной анафилаксии в этом модели (см. фиг. 7). Важно отметить, что введение антитела анти-м-ИЛ-4Рα не влияло на наблюдавшиеся положительные эффекты АСИ. Кроме того, у животных, получавших только ИТ и у животных, получавших ИТ в сочетании с изотипом контрольного антитела, наблюдалась тенденция к повышению уровня IgE, индуцированному АСИ. В отличие от этого, образование IgE блокировалось у животных, получавших анти-м-ИЛ-4Рα (см. фиг. 8). У животных, получавших иммунотерапию (с введением или без введения антитела), наблюдалась тенденция к увеличению титра обладающего специфичностью к арахису IgG1, однако статистическая значимость была достигнута у животных, получавших ИТ, только на день 77 (см. фиг. 9). Блокада ИЛ-4Рα также приводила к увеличению титра обладающего специфичностью к арахису IgG2a (см. фиг. 10). Результаты из этой серии экспериментов поддерживают использование блокады ИЛ-4Р в качестве средства для потенциального улучшения эффективности и безопасности аллерген-специфической иммунотерапии.
Затем была проведена вторая серия экспериментов для определения эффекта блокады ИЛ-4Р при применения схемы АСИ с введением меньшего числа доз аллергена в фазу формирования иммунного ответа. Схема протокола эксперимента, использовавшегося для второй серии экспериментов, показана на фиг. 12. Как и ранее, в этих экспериментов использовали четыре группы мышей. Мыши трех их четырех групп получали специфическую к арахису иммунотерапию, аналогичную терапии, которая использовалась в первой серии экспериментов, за исключением того, что животным вводили меньше доз аллергена в фазу формирования иммунного ответа. В частности, в фазу формирования иммунного ответа в этих экспериментах животным вводили экстракт арахиса без квасца в различных дозах только восемь (а не двенадцать) раз в дни 51 и 53 (0,1 мг), 58 и 60 (0,25 мг), 65 и 67 (0,5 мг) и 72 и 74 (0,5 мг).
И снова, использовались четыре группы терапии: «без ИТ», «только ИТ», «ИТ+ изотип контрольного антитела» и «ИТ + анти-м-ИЛ-4Рα». Антитело вводили в той же дозе, что и в первой серии экспериментов (25 мг/кг, подкожно), однако инъекции выполняли в дни 36, 49, 56, 63 и 70 (а не в дни 36, 50, 57, 64 и 71, как в первой серии экспериментов). Степени анафилаксии определяли путем измерения внутренней температуры тела в течение 240 минут после выполнения провокационной пробы. Результаты показаны на фиг. 13.
В этих экспериментах более редкое введение аллергена в фазу формирования иммунного ответа обеспечивало меньшую защиту от анафилаксии по сравнению с более частым введением, которое использовалось в первой серии экспериментов (8 доз против 12). В частности, наблюдалось существенное снижение внутренней температуры тела в группе «ИТ» и в группе «ИТ + изотип контрольного антитела» в течение первых 60 минут после выполнения провокационной пробы с аллергеном, которое было совсем немного менее выраженным, чем в группе мышей «без ИТ». В отличие от этого, у мышей, получавших только анти-м-ИЛ-4Рα, наблюдался только легкая анафилактическая реакция (т.е. незначительное снижение внутренней температуры тела). Фаза формирования иммунитета в этой модели может считаться аналогичной поддерживающей фазе при применении стандартных схем АСИ у человека. Таким образом, результаты этого эксперимента, свидетельствуют о том, что блокада ИЛ-4Р может существенно повысить безопасность и эффективность схем аллерген-специфической иммунотерапии за счет снижения дозы аллергена, вводимого в поддерживающую фазу. Более редкое введение аллергена также более удобно и может привести к улучшению соблюдения схем АСИ пациентом.
Применение настоящего изобретения не ограничивается конкретными вариантами осуществления настоящего изобретения, описанными в этом документе. Более того, различные модификации данного изобретения, помимо модификаций, описанных в этом документе, будут очевидны специалистам в рассматриваемой области, исходя из вышеупомянутого описания и сопровождающих текст фигур. Предполагается, что такие модификации попадают в сферу охвата прилагаемой формулы изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБЫ ЛЕЧЕНИЯ АЛЛЕРГИИ И ПОВЫШЕНИЯ ЭФФЕКТИВНОСТИ АЛЛЕРГЕН-СПЕЦИФИЧЕСКОЙ ИММУНОТЕРАПИИ ПУТЕМ ВВЕДЕНИЯ ИНГИБИТОРА ИЛ-4Р | 2014 |
|
RU2679920C2 |
| СПОСОБЫ ЛЕЧЕНИЯ ЭОЗИНОФИЛЬНОГО ЭЗОФАГИТА С ПОМОЩЬЮ ИНГИБИТОРА ИЛ-4Р | 2014 |
|
RU2679141C2 |
| СПОСОБЫ ПОВЫШЕНИЯ ЭФФЕКТИВНОСТИ ВАКЦИНЫ ПУТЕМ ВВЕДЕНИЯ АНТАГОНИСТА IL-4R | 2017 |
|
RU2753869C2 |
| СПОСОБЫ ЛЕЧЕНИЯ АЛЛЕРГИИ И УСИЛЕНИЯ АЛЛЕРГЕН-СПЕЦИФИЧЕСКОЙ ИММУНОТЕРАПИИ ПУТЕМ ВВЕДЕНИЯ АНТАГОНИСТА IL-4R | 2020 |
|
RU2833729C2 |
| СПОСОБЫ ЛЕЧЕНИЯ ИЛИ ПРЕДУПРЕЖДЕНИЯ АСТМЫ ПОСРЕДСТВОМ ВВЕДЕНИЯ АНТАГОНИСТА IL-4R | 2020 |
|
RU2832774C2 |
| СПОСОБЫ ПРЕДУПРЕЖДЕНИЯ ИЛИ ЛЕЧЕНИЯ АЛЛЕРГИИ ПОСРЕДСТВОМ ВВЕДЕНИЯ АНТАГОНИСТА IL-4R | 2017 |
|
RU2777328C2 |
| СПОСОБЫ ЛЕЧЕНИЯ ИЛИ ПРЕДУПРЕЖДЕНИЯ АСТМЫ ПУТЕМ ВВЕДЕНИЯ АНТАГОНИСТА IL-4R | 2018 |
|
RU2793745C2 |
| ЧЕЛОВЕЧЕСКИЕ АНТИТЕЛА К FEL D1 И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2013 |
|
RU2658491C2 |
| СПОСОБЫ ЛЕЧЕНИЯ ИЛИ ПРЕДОТВРАЩЕНИЯ АСТМЫ ПОСРЕДСТВОМ ВВЕДЕНИЯ АНТАГОНИСТА IL-4R | 2013 |
|
RU2690675C2 |
| СПОСОБЫ ЛЕЧЕНИЯ ИЛИ ПРЕДУПРЕЖДЕНИЯ АСТМЫ ПОСРЕДСТВОМ ВВЕДЕНИЯ АНТАГОНИСТА IL-4R | 2015 |
|
RU2713406C2 |




Изобретение касается способа лечения, профилактики или уменьшения степени тяжести аллергической реакции на аллерген. Способ включает введение терапевтически эффективного количества фармацевтической композиции, содержащей антагонист рецептора интерлейкина-4 (ИЛ-4Р), субъекту, имеющему аллергию на аллерген, где указанный антагонист ИЛ-4Р представляет собой антитело или его антигенсвязывающий фрагмент, который специфически связывается с ИЛ-4Р, где антитело или его антигенсвязывающий фрагмент содержит три HCDR (HCDR1, HCDR2 и HCDR3) и три LCDR (LCDR1, LCDR2 и LCDR3), причем HCDR1 содержит аминокислотную последовательность с идентификатором SEQ ID NO: 3; HCDR2 содержит аминокислотную последовательность с идентификатором SEQ ID NO: 4; HCDR3 содержит аминокислотную последовательность с идентификатором SEQ ID NO: 5; LCDR1 содержит аминокислотную последовательность с идентификатором SEQ ID NO: 6; LCDR2 содержит аминокислотную последовательность с идентификатором SEQ ID NO: 7; и LCDR3 содержит аминокислотную последовательность с идентификатором SEQ ID NO: 8; при этом способ включает многократное введение субъекту фармацевтической композиции до воздействия аллергена. Использование способа высокоэффективно для предотвращения или уменьшения тяжести аллергии и для снижения общего уровня IgE в сыворотке крови субъекта. 19 з.п. ф-лы, 2 пр., 13 ил.
1. Способ лечения, профилактики или уменьшения степени тяжести аллергической реакции на аллерген, включающий введение терапевтически эффективного количества фармацевтической композиции, содержащей антагонист рецептора интерлейкина-4 (ИЛ-4Р), субъекту, имеющему аллергию на аллерген, где указанный антагонист ИЛ-4Р представляет собой антитело или его антигенсвязывающий фрагмент, который специфически связывается с ИЛ-4Р, где антитело или его антигенсвязывающий фрагмент содержит три HCDR (HCDR1, HCDR2 и HCDR3) и три LCDR (LCDR1, LCDR2 и LCDR3), причем HCDR1 содержит аминокислотную последовательность с идентификатором SEQ ID NO: 3; HCDR2 содержит аминокислотную последовательность с идентификатором SEQ ID NO: 4; HCDR3 содержит аминокислотную последовательность с идентификатором SEQ ID NO: 5; LCDR1 содержит аминокислотную последовательность с идентификатором SEQ ID NO: 6; LCDR2 содержит аминокислотную последовательность с идентификатором SEQ ID NO: 7; и LCDR3 содержит аминокислотную последовательность с идентификатором SEQ ID NO: 8;
при этом способ включает многократное введение субъекту фармацевтической композиции до воздействия аллергена.
2. Способ по п. 1, где антитело или его антигенсвязывающий фрагмент содержит вариабельную область тяжелой цепи (HCVR), которая содержит аминокислотную последовательность с идентификатором SEQ ID NO: 1, и вариабельную область легкой цепи (LCVR), которая содержит аминокислотную последовательность с идентификатором SEQ ID NO: 2.
3. Способ по п. 1, где антагонистом ИЛ-4Р является дупилумаб или его биоэквивалент.
4. Способ по п. 1, где фармацевтическую композицию вводят субъекту по меньшей мере за две недели до воздействия аллергена.
5. Способ по п. 1, где способ включает введение фармацевтической композиции субъекту один раз каждую неделю или один раз каждые две недели.
6. Способ по п. 1, где фармацевтическая композиция содержит от 50 до 600 мг антагониста ИЛ-4Р.
7. Способ по п. 6, где фармацевтическая композиция содержит 300 мг антагониста ИЛ-4Р.
8. Способ по п. 1, где фармацевтическую композицию вводят подкожно.
9. Способ по п. 1, где аллергическая реакция включает один или более симптомов аллергии, выбранных из группы, состоящей из крапивницы, ангионевротического отека, ринита, астмы, рвоты, нарушения функции дыхания, отека губ, отека языка и снижения артериального давления.
10. Способ по п. 1, где аллергической реакцией является анафилаксия.
11. Способ по п. 1, где аллерген представляет собой пищевой аллерген.
12. Способ по п. 11, где пищевой аллерген выбран из группы, состоящей из молочных продуктов, яиц, пшеницы, сои, рыбы, морепродуктов, арахиса и орехов.
13. Способ по п. 12, где пищевой аллерген представляет собой арахис.
14. Способ по п. 12, где пищевой аллерген представляет собой молочный продукт, при этом молочный продукт представляет собой коровье молоко.
15. Способ по п. 1, где аллерген представляет собой непищевой аллерген.
16. Способ по п. 15, где непищевой аллерген выбран из группы, состоящей из пыли, пыльцы, яда насекомых, грибковой плесени, меха животных, перхоти животных, шерсти, латекса, металлов, бытовых моющих средств, детергентов, лекарственных средств, терапевтических моноклональных антител, амброзии, травы и березы.
17. Способ по п. 1, где фармацевтическую композицию вводят субъекту в комбинации со вторым терапевтическим средством, выбранным из группы, состоящей из стероидов, антигистаминных препаратов, деконгестантов и анти-IgE препаратов.
18. Способ по п. 1, где фармацевтическая композиция содержится в шприце.
19. Способ по п. 1, где фармацевтическая композиция содержится в устройстве для доставки, представляющем собой шприц-ручку.
20. Способ по п. 19, где устройство для доставки, представляющее собой шприц-ручку, является заполненным.
| "SANOFI AND REGENERON REPORT POSITIVE PROOF-OF-CONCEPT DATA FOR DUPILUMAB, AN IL-4R ALPHA ANTIBODY, IN ATOPIC DERMATITIS" | |||
| REGENERON, March 2, 2013, [онлайн], [найдено 26.07.2022] | |||
| Найдено из Интернет: https://investor.regeneron.com/news-releases/news-release-details/sanofi-and-regeneron-report-positive-proof-concept-data/ | |||
| Приспособление для суммирования отрезков прямых линий | 1923 |
|
SU2010A1 |
Авторы
Даты
2023-01-27—Публикация
2014-06-03—Подача