Предлагаемое изобретение относится к области органической химии, в частности, к способу получения бензимидазолов.
Бензимидазолы являются важным классом органических соединений в медицинской химии, обладающих широким спектром фармакологической активности. Производные бензимидазола применяются в качестве фармацевтических препаратов (дибазол, омепразол, мебендазол и др.) [C.S. Law, K.Y. Yeong // Chem. Med. Chem. 2021, 16(12), 1861-1877; R.S. Keri, A. Hiremathad, S. Budagumpi, B. M. Nagaraja // Chem Biol Drug Des 2014, 86(1), 19-65; K. Barot, S. Nikolova, I. Ivanov, M. Ghate // Mini-Rev. Med. Chem., 2013, 13(10), 1421-1447; N.R. Candeias, L.C. Branco, P. M.P. Gois, C.A.M. Afonso, A.F. Trindade // Chem. Rev. 2009, 109, 2703-2802]. Ряд бисбензимидазолов обладают выраженной противоопухолевой активностью [F.A. Tanious, D. Hamelberg, C. Bailly, A. Czarny, D.W. Boykin, W.D. Wilson // J. Am. Chem. Soc. 2004, 126, 143-153; J. Valdez, R. Cedillo, A.H. Campos, L. Yepez, F.H. Luis, G.N. Vazquez, A. Tapia, R. Cortes, M. Hernandez, R. Castillo // Bioorg. Med. Chem. Lett. 2002, 12, 2221 - 2224; T. Fekner, J. Gallucci, M.K. Chan // J. Am. Chem. Soc. 2004, 126, 223 - 236.].
Согласно литературным данным, основные методы получения бензимидазолов - реакция о-фенилендиамина с CO2/H2 и конденсация о-фенилендиамина с карбоновыми кислотами, с ортоэфирами, альдегидами и спиртами [D.W. Hein, R.J. Alheim, J.J. Leavitt // J. Am. Chem. Soc. 1957, 79, 427 - 429; Z. H. Zhang, J. J. Li, Y. Z. Gao, Y. H. Liu // J. Heterocycl. Chem. 2007, 44(6), 1509-1512; S. Shyshkanov, T. Nguyen, F. M. Ebrahim, K. Stylianou, P. Dyson // Angew. Chem. Int. Ed. 2019, 58(16), 5371-5375; J. Penieres-Carrillo, H. Ríos-Guerra, J. Pérez-Flores, B. Rodríguez-Molina, Á. Torres-Reyes, F. Barrera-Téllez, R. Luna-Mora // J. Heterocycl. Chem. 2019, 57(1), 436-455; K. Selvam, M. Annadhasan, R. Velmurugan, M. Swaminathan // Bull. Chem. Soc. Jpn. 2010, 83(7), 831-837].
Одним из наиболее привлекательных методов получения бензимидазолов является конденсация о-фенилендиамина с доступными спиртами.
Известен метод получения бензимидазолов, основанный на реакции о-фенилендиамина с алифатическими спиртами (этанол, н-пропанол, н-бутанол) в присутствии композитного катализатора Ag-TiO2/глина под воздействием «solarlight» (интенсивность солнечного света (1100©100 люкс, цифровой люксметр LTLutron LX10/A) и УФ-излучения в многоламповом фотохимическом реакторе Heber (модель HML-MP88), оснащенном 8 лампами (365 нм) [K. Selvam, M. Annadhasan, R. Velmurugan, M. Swaminathan // Bull. Chem. Soc. Jpn. 2010, 83(7), 831-837]. Все реакции проводили при мольном соотношении о-фенилендиамин : спирт = 1:2 в 25 мл ацетонитрила с использованием 200 мг катализатора Ag-TiO2/глина (5%) в условиях аэрации (скорость потока воздуха = 8,1 мл/с). Наряду с целевым бензимидазолами образуется 2,2'-диаминоазобензол.

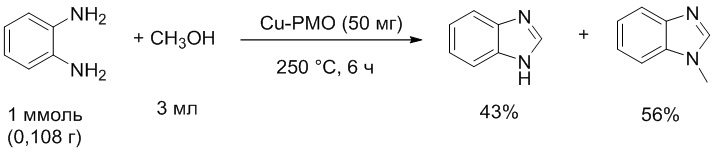
Осуществлен метод получения бензимидазолов реакцией о-фенилендиамина с метанолом, который находится в свехкритических условиях [Z. Sun, G. Bottari, K. Barta // Green Chem. 2015, 17(12), 5172-5181]. Продуктами реакции являются целевой бензимидазол и N-метилбензимидазол (1:1,3). Реакцию проводили в микрореакторе Swagelok из нержавеющей стали (10 мл). В реактор загружали 1 ммоль о-фенилендиамина (0,108 г) и 3 мл метанола (реагент и растворитель), добавляли 50 мг катализатора Cu-PMO (легированные медью пористые оксиды металлов). Реакцию проводили при температуре 250°С в течение 6 ч. После реакции катализатор отделяли от реакционного раствора центрифугированием и последующей декантацией, дополнительно промывали метанолом, затем ацетоном.
Известен метод синтеза 2-пропилбензимидазола из о-фенилендиамина и бутанола под действием катализатора Au-CeO2 [V.R. Ruiz, A. Cormaand, M. J. Sabater. // Tetrahedron. 2010, 66, 730-735]. В автоклав загружали 1 мл трифтортолуола, добавляли 1 ммоль (0,074 мл) спирта и катализатор (0,5 мол. %). Реакционную смесь нагревали при 90°С при непрерывном перемешивании в атмосфере кислорода (p(O2) = 0,5 МПа). Затем, после почти полного расходования исходного спирта, добавляли 1 ммоль (0,108 г) 1,2-фенилендиамина и нагревание продолжали до полного расходования диамина.

Предложен метод синтеза бензимидазолов реакцией о-фенилендиамина с метанолом и этанолом в присутствии родийсодержащего катализатора [S. Sharma, A. Sharma, P. Das // Adv. Synth. Catal. 2018, 361(1), 67-72]. Эксперименты проводились в автоклаве для гидротермального синтеза с тефлоновым покрытием, при температуре 130°C, в течение 48 ч. В автоклав загружали о-фенилендиамин, Rh@PS (полистирольная основа) (3 мол.%), 3 мл этанола, K2CO3 и 1,4-диоксан в качестве сорастворителя. Выход бензимидазола и 2-метилбензимидазола составил 97 и 98%, соответственно.

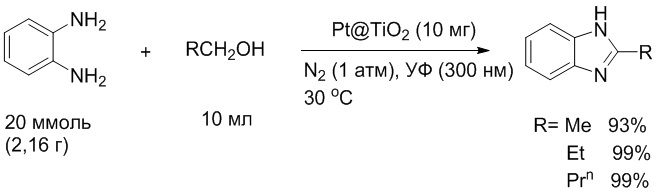
Известен метод синтеза производных бензимидазола взаимодействием о-фенилендиамина со спиртами (этанол, н-пропанол, н-бутанол) под действием платиносодержащего катализатора [Y. Shiraishi, Y. Sugano, S. Tanaka, T. Hirai // Angew. Chem. Int. Ed. 2010, 49(9), 1656-1660]. Реакцию проводили в стеклянной трубке из пирекса (20 см3). В трубку помещали 2,16 г (20 ммоль) о-фенилендиамина, 10 мл спирта и 10 мг катализатора. Затем пробирку продували N2 и подвергали фотооблучению ксеноновой лампой (2 кВт, UshioInc., интенсивность света 18,2 Вт⋅м2 при 300-400 нм) при перемешивании на магнитной мешалке при 30°С.
Недостатки методов
1. Применение дорогостоящих катализаторов (иридиевые, родиевые, платина-, золотосодержащие катализаторы, Ag-TiO2/глина);
2. Высокая температура реакции (до 250°С);
3. Длительность реакции (до 48 ч);
4. Низкий выход бензимидазолов и низкая селективность;
5. Применение токсичного растворителя ацетонитрила, который также входит в список прекурсоров;
6. Образование большого количества неорганических отходов из-за использования KOtBu, K2CO3;
7. Трудность масштабирования при применении УФ-облучения.
8. Необходимость поддержания высокой температуры и давления при использовании сверхкритического метанола.
Задачей предлагаемого изобретения является удешевление себестоимости конечного продукта за счет использования доступных и дешевых железосодержащих катализаторов - FeCl3⋅6H2O, Fe(acac)3.
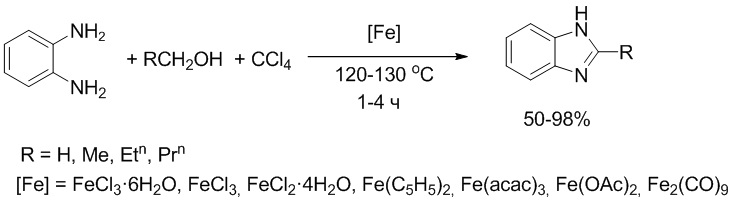
Сущность способа заключается во взаимодействии о-фенилендиамина со спиртами, а именно с метанолом, или этанолом, или н-пропанолом, или н-бутанолом под действием следующих железосодержащих катализаторов: FeCl3⋅6H2O, FeCl3, FeCl2⋅4H2O, Fe(C5H5)2, Fe(acac)3, Fe(OAc)2 и Fe2(CO)9. Продуктами конденсации о-фенилендиамина со спиртами являются 2-замещенные бензимидазолы, выходы которых составили 50-98%. Синтез проходит при мольном соотношении [катализатор]:[о-фенилендиамин]:[СCl4]:[спирт]= 1-2:100:1875-7500:1875-3750, при 120-130°С в течение 1-4 ч в среде CCl4. При 120°С и продолжительности реакции 3 ч и следующих соотношениях катализатора и реагентов [FeCl3⋅6H2O или Fe(acac)3]:[о-фенилендиамин]:[СCl4]:[спирт]= 1:100:7500:3750 выход 2-замещенных бензимидазолов достигает 97-98%. В отсутствие катализатора реакция не идет.
Существенные отличия предлагаемого способа от прототипа .
Для получения бензимидазолов из о-фенилендиамина и спиртов используют железосодержащий катализатор и реакцию проводят в среде ССl4, который является и реагентом, и растворителем.
Преимущества предлагаемого метода .
1. Высокий выход целевых продуктов.
2. Доступность и дешевизна катализатора.
3. Удешевление себестоимости и упрощение технологии в целом за счет уменьшения энерго- и трудозатрат.
Предлагаемый способ поясняется примерами:
ПРИМЕР 1. Реакции проводили в стеклянной ампуле (V=10 мл), помещенной в микроавтоклав из нержавеющей стали (V=17 мл) при регулируемом нагреве при перемешивании.
В ампулу загружали 0,005 ммоль катализатора (Fe(acac)3 (0,0018 г), 0,0005 моль о-фенилендиамина (0,054 г), 0,04 моль этанола (2,2 мл), 0,02 моль СCl4 (1,8 мл). Запаянную ампулу поместили в автоклав, автоклав герметично закрыли и нагревали при перемешивании при 120°С в течение 3 часов. После окончания реакции автоклав охлаждали до комнатной температуры, ампулу вскрывали, реакционную массу нейтрализовывали 10 мас.% NaHCO3 (перемешивание на магнитной мешалке в течение 15-20 мин), органический слой экстрагировали этилацетатом и отфильтровывали. Растворители отгоняли на роторном испарителе. Затем продукт выделяли колоночной хроматографией (SiO2, элюент - гексан-этилацетат (70:30)).
После отгона этилацетата на роторном испарителе конверсия исходного о-фенилендиамина составила 100%, выход 2-метилбензимидазола - 98%. Результаты приведены в таблице.
ПРИМЕР 2-4. Аналогично примеру 1, но вместо этанола использовали 0,04 моль следующих спиртов: метанол (1,6 мл), н-пропанол (3 мл), н-бутанол (3,7 мл).
ПРИМЕРЫ 5-10. Аналогично примеру 1, но в качестве катализаторов использовали 0,005 ммоль FeCl3 (0,0008 г), FeCl2⋅4H2O (0,0010 г), Fe(C5H5)2 (0,0009 г), Fe(OAc)2 (0,0008 г), Fe2(CO)9 (0,0018 г) и FeCl3⋅6H2O (0,0014 г).
ПРИМЕРЫ 11-13. Аналогично примеру 1, при разных соотношениях катализатора и реагентов и продолжительности реакции.
ПРИМЕРЫ 14, 15. Аналогично примеру 10, при разных соотношениях катализатора и реагентов и температуре реакции.
Строение полученных бензимидазолов доказано методами ЯМР-спектроскопии, масс-спектрометрии, HRMS, а также сравнением с известными образцами и литературными данными.
Бензимидазол.
Выход 97%, тв., т.пл. 170-171°С {т.пл. 171°С [W. Sun, X. Chen, Y. Hu, H. Geng, Y. Jiang, Y. Zhou, Y. Hu // Tetrahedron Lett. 2020, 61(43), 152442]}. Спектр ЯМР 1Н (CDCl3, δ, м.д.): 7.09 с (1H, NH); 7.66-7.70 м (2H, С4,7H), 7.26-7.31м (C5,6H). Спектр ЯМР 13С δ, м.д.: 140.57 (C2), 137.26 (C3a, 7a), 115.45 (C4,7), 123.10 (C5,6). Масс-спектр, m/z (Iотн (%)):118 (100) [М]+, 91(40), 64 (20).
HRMS (ESI-MS) m/z: [M+H]+ рассчитано для C7H6N2: 119.0610, найдено: 119.0604.
2-Метилбензимидазол.
Выход 98%, тв., т.пл. 176-177°С {т.пл. 176- 177°С [B. Raju, N. Theja, Dharma; J. Kumar // Synth. Commun. 2009, 39(1), 188]}. Спектр ЯМР 1Н (CDCl3, δ, м.д.): 2.68 с (3H, C8H3); 7.7 с (1H, NH); 7.57-7.59 м (2H, С4,7H), 7.25-7.27 м (C5,6H). Спектр ЯМР 13С δ, м.д.: 150.77 (C2), 137.66 (C3a, 7a), 114.4 (C4,7), 122.68 (C5,6), 14.65 (C8). Масс-спектр, m/z (Iотн (%)):132 (100) [М]+, 131 (75), 104 (10), 92 (10), 64 (15).
HRMS (ESI-MS) m/z: [M+H]+ рассчитано для C8H9N2: 133.0766, найдено: 133.0780.
2-Этилбензимидазол.
Выход 98%, тв., т.пл. 175-176°С {т.пл. 175°С [M. Zuo, W. Guo, Y. Pang, R. Guo, C. Hou, S. Sun, W. Chu // New J. Chem. 2020, 44(34), 14490-14495]}. Спектр ЯМР 1Н (CDCl3, δ, м.д.): 1.46 т (3H, C9H3, J 8 Гц), 3.05 к (2H, C8H2CH3, J 8 Гц), 8.2 с (1H, NH), 7.58-7.60 м (2H, С4,7H), 7.22-7.25 м (C5,6H). Спектр ЯМР 13С δ, м.д.: 156.63 (C2), 137.94 (C3a,7a), 114.5 (C4,7), 122.39 (C5,6), 22.41 (C8), 12.49 (С9). Масс-спектр, m/z (Iотн (%)): 146 (60) [М]+, 145 (100), 131 (20), 92 (10), 63(5).
HRMS (ESI-MS) m/z: [M+H]+ рассчитано для C10H12N2: 147.0922, найдено: 147.0923.
2-Пропилбензимидазол.
Выход 98%, тв., т.пл. 152-153°С {152-153°С [R. Seka, R. H. Muller // Monatsh. Chem. 2017, 97-105]}. Спектр ЯМР 1Н (CDCl3, δ, м.д.): 0.99 м (3H, C10H3), 1.86-1.99 м (2H, C9H2CH3), 3.00 т (2H, C8H2CH2CH3, J 8 Гц), 8.19 с (1H, NH), 7.56-7.62 м (2H, С4,7H), 7.20-7.28 м (C5,6H). Спектр ЯМР 13С δ, м.д.: 154.89 (C2), 137.33 (C3a, 7a), 114.46 (C4,7), 122.71 (C5,6), 30.76 (C8), 21.64 (С9), 13.92 (С10). Масс-спектр, m/z (Iотн (%)): 160 (30) [М] +, 132 (100), 118 (5), 104 (5), 77 (8).
HRMS (ESI-MS) m/z: [M+H]+ рассчитано для: C10H12N2: 161.1079 найдено: 161.1094.
Примеры, подтверждающие способ, приведены в таблице.
Синтез 2-замещенных бензимидазолов реакцией о-фенилендиамина со спиртами под действием железосодержащих катализаторов
п/п
[кат]:[о-фенилендиамин]:
[ROH]:[CCl4]
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ ХИНОЛИНОВ ИЗ АНИЛИНА, 1,2-ДИОЛОВ И ССl ПОД ДЕЙСТВИЕМ ЖЕЛЕЗОСОДЕРЖАЩИХ КАТАЛИЗАТОРОВ | 2015 |
|
RU2614251C2 |
| СПОСОБ ПОЛУЧЕНИЯ 2-ФЕНИЛ-3-АЛКИЛХИНОЛИНОВ | 2014 |
|
RU2565787C1 |
| СПОСОБ ПОЛУЧЕНИЯ АЛКИЛОВЫХ ЭФИРОВ ГИДРОКСИБЕНЗОЙНЫХ КИСЛОТ | 2017 |
|
RU2675496C1 |
| СПОСОБ ПОЛУЧЕНИЯ АЛКИЛОВЫХ ЭФИРОВ МЕТОКСИБЕНЗОЙНЫХ КИСЛОТ | 2016 |
|
RU2640206C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ ХИНОЛИНОВ ИЗ АНИЛИНА, 1,3-ДИОЛОВ И CCl4 ПОД ДЕЙСТВИЕМ ЖЕЛЕЗОСОДЕРЖАЩИХ КАТАЛИЗАТОРОВ | 2013 |
|
RU2561503C2 |
| СПОСОБ ПОЛУЧЕНИЯ МЕТИЛОВОГО ЭФИРА 2-БЕНЗО[b]ФУРАНКАРБОНОВОЙ КИСЛОТЫ | 2010 |
|
RU2455299C2 |
| СПОСОБ ПОЛУЧЕНИЯ ФЛУНАРИЗИНА | 2015 |
|
RU2600450C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1-ДИХЛОРМЕТИЛИЗОХИНОЛИНА | 2008 |
|
RU2402535C2 |
| СПОСОБ ПОЛУЧЕНИЯ МЕТИЛОВОГО ЭФИРА 5-АЦЕТИЛФУРАН-2-КАРБОНОВОЙ КИСЛОТЫ | 2008 |
|
RU2404173C2 |
| СПОСОБ ПОЛУЧЕНИЯ АЛКИЛОВЫХ ЭФИРОВ 4-БИФЕНИЛКАРБОНОВОЙ КИСЛОТЫ | 2016 |
|
RU2640205C1 |
Изобретение относится к области органической химии, а именно к способу получения бензимидазолов указанной формулы, где R = H, Me, Etn, Prn. Способ заключается во взаимодействии о-фенилендиамина с н-спиртами С1-С4 при использовании в качестве катализатора FeCl3⋅6H2O, или FeCl3, или FeCl2⋅4H2O, или Fe(C5H5)2, или Fe(acac)3, или Fe(OAc)2, или Fe2(CO)9 при мольном соотношении [катализатор]:[о-фенилендиамин]:[спирт]:[СCl4]=1-2:100:1875-7500:1875-3750 при температуре 120-130°С в течение 1-4 ч в среде CCl4. Предлагаемый способ позволяет получать бензимидазолы указанной формулы в более мягких условиях и с уменьшенным временем протекания реакции в присутствии доступного и недорогого железосодержащего катализатора с высоким выходом - 97-98%. 1 табл., 15 пр.
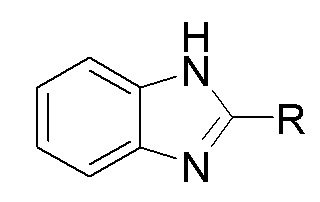
Способ получения бензимидазолов общей формулы
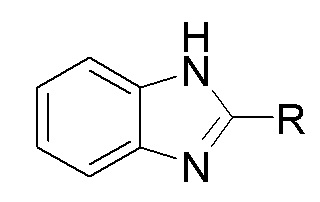 ,
,
где R = H, Me, Etn, Prn,
каталитической циклоконденсацией о-фенилендиамина с н-спиртами С1-С4, отличающийся тем, что в качестве катализатора используют FeCl3⋅6H2O, или FeCl3, или FeCl2⋅4H2O, или Fe(C5H5)2, или Fe(acac)3, или Fe(OAc)2, или Fe2(CO)9, реакцию проводят при мольном соотношении [катализатор]:[о-фенилендиамин]:[спирт]:[СCl4]=1-2:100:1875-7500:1875-3750, при температуре 120-130°С в течение 1-4 ч в среде CCl4.
| HIRAISHI Y | |||
| et al., One-Pot Synthesis of Benzimidazoles by Simultaneous Photocatalytic and Catalytic Reactions on Pt TiO2 Nanoparticles, ANGEWANDTE CHEMIE INTERNATIONAL EDITION, 2010, 49(9), pp | |||
| Регулирующее приспособление для ветряных двигателей со складными перьями или лопастями | 1924 |
|
SU1656A1 |
| WADA K | |||
| et al., Titania-supported iridium catalysts for dehydrogenative synthesis of benzimidazoles, CHINESE | |||
Авторы
Даты
2023-02-01—Публикация
2022-07-13—Подача