Изобретение относится к медицине и фармакологии и касается создания средств на основе высокомолекулярного полимера хитозана, с кровоостанавливающим и способствующим полимеризации фибрина действием в организме.
Наиболее часто в медицине в качестве гемостатических используются препараты викасола, дицинона, транексама, кальция, факторов свертывания. Однако, они имеют недостатки, главным из которых служит возможность передозировки. Также известны коагулянтные средства животного происхождения, представляющие собой коллаген (Manon-Jensen Т, Kjeld NG, Karsdal MA Collagen-mediated hemostasi // J Thromb Haemost. 2016 Mar;14(3):438-48. doi: 10.1111/jth.l3249. Epub 2016 Feb 17.).
Известен состав для борьбы с кровоточивостью, включающий водорастворимый хитозан, где разработаны композиции на основе различных форм хитозана, комплексносвязанного с ионами кальция, и исследование их кровоостанавливающих свойств в опытах in vitro и in vivo [Патент РФ №2545991, Кровоостанавливающий препарат, МПК А61K 31/715, А61K 31/115, опубликовано: 10.04.2015, Бюл. №10].
Однако, известный состав не достаточно эффективен для увеличения прокоагулянтной и фибринполимеризационной активностях, что не позволяет использовать его в медицинской практике для борьбы с кровоточивостью.
Техническим решением предлагаемого изобретения является увеличение прокоагулянтной и фибринполимеризационной активности
Поставленная задача решается в гемостатическом составе, включающем хитозан тем, что дополнительно содержит эпсилонаминокапроновую кислоту, причем хитозан и эпсилонаминокапроновая кислота взяты в весовых соотношениях 8,0-12,0: 1,0, соответственно.
В патентной и научно-технической литературе неизвестны технические решения аналогичные заявляемому, т.е. предложение соответствует критерию изобретения «новизна».
Заявленная композиция решает актуальную проблему - остановки и профилактики кровотечений животных, т.е. предложение «промышленно применимо».
Нами впервые показано, что сочетанное использование вышеуказанных отличительных признаков, взятых в определенных соотношениях компонентов, увеличивает прокоагулянтную и фибринполимеризационную активности, что приводит к достижению технического результата. Следовательно, изобретение соответствует критерию «изобретательский уровень».
Изобретение иллюстрируется на следующих примерах:
Пример 1. Смешиваем 8,0 г хитозана и 1,0 г эпсилонаминокапроновой кислоты, получая состав 1 при весовом соотношении компонентов, равном 8,0:1,0, соответственно.
Пример 2. Смешиваем 12,0 г хитозана и 1,0 г эпсилонаминокапроновой кислоты, получая состав 2 при весовом соотношении компонентов, равном 12,0:1,0, соответственно.
Пример 3. Смешиваем 10,0 г хитозана и 1,0 г эпсилонаминокапроновой кислоты, получая состав 3 при весовом соотношении компонентов, равном 10,0:1,0, соответственно.
Пример 4. Испытание составов 1-3, полученных в соответствии с примерами 1-3, проводят следующим образом.
К 1 г составов 1-3 добавляют 100 мл дистиллированной воды, перемешивают их в течение 10 мин при комнатной температуре, далее смесь оставляют в термостате при+37°С на 2 часа до применения.
Процедура опытов in vitro заключается в следующем: в предлагаемых составах 1-3 при добавлении к плазме крови была испытана фибринполимеризационная активность по методу Щербак И.Г. и др. (Щербак И.Г., Субботина Т.Ф., Фаенкова В.П. и др. Турбидиметрический анализ полимеризации фибрина в плазме крови // Вопр. мед. химии. 2001. №1. С.43-47.) и прокоагулянтная активность по тестам активированного частичного тромбопластинового времени (АЧТВ) и тромбинового времени (ТВ) по методам Баркаган З.С.и др. (Баркаган З.С., Момот А.П. Диагностика и контролируемая терапия нарушений гемостаза. М.: «Ньюдиамед», 2001. С.79-81.) в сравнении с контролем, которым были составы: прототип (состав 4), хитозан (состав 5) и эпсилон-аминокапроновая кислота (состав 6), причем к 0,3 г состава 4, 1 г состава 5 и 0,1 г состава 6 добавляли 100 мл дистиллированной воды, перемешивали их в течение 10 мин при комнатной температуре, далее оставляют на 2 часа до применения. Результаты испытаний представлены в таблице 1.
Пример 5. Испытание составов 1-3, полученных в соответствии с примерами 1-3, проводят следующим образом.
К 1 г составов 1-3 добавляют 100 мл физиологического раствора, перемешивают их в течение 5 мин при комнатной температуре, далее смесь оставляют в термостате при +38°С на 2 часа до применения.
Процедура опытов in vitro заключается в следующем: в предлагаемых составах 1-3 при добавлении к плазме крови была испытана фибринполимеризационная активность по методу Щербак И.Г. и др. (Щербак И.Г., Субботина Т.Ф., Фаенкова В.П. и др. Турбидиметрический анализ полимеризации фибрина в плазме крови // Вопр. мед. химии. 2001. №1. С.43-47.) и прокоагулянтная активность по тестам активированного частичного тромбопластинового времени (АЧТВ) и тромбинового времени (ТВ) по методам Баркаган З.С. и др. (Баркаган З.С, Момот А.П. Диагностика и контролируемая терапия нарушений гемостаза. М.: «Ньюдиамед», 2001. С.79-81.) в сравнении с контролем, которым были составы: прототип (состав 4), хитозан (состав 5) и эпсилон-аминокапроновая кислота (состав 6), причем к 0,3 г состава 4, 1 г состава 5 и 0,1 г состава 6 добавляли 100 мл физиологического раствора, перемешивали их в течение 10 мин при комнатной температуре, далее оставляют на 2 часа до применения. Результаты испытаний представлены в таблице 1.
Результаты испытаний представлены в таблице 2.
Таким образом, предлагаемое изобретение позволяет увеличить на 3-15% прокоагулянтные и на 4-30% фибринполимеризационные свойства целевого продукта.
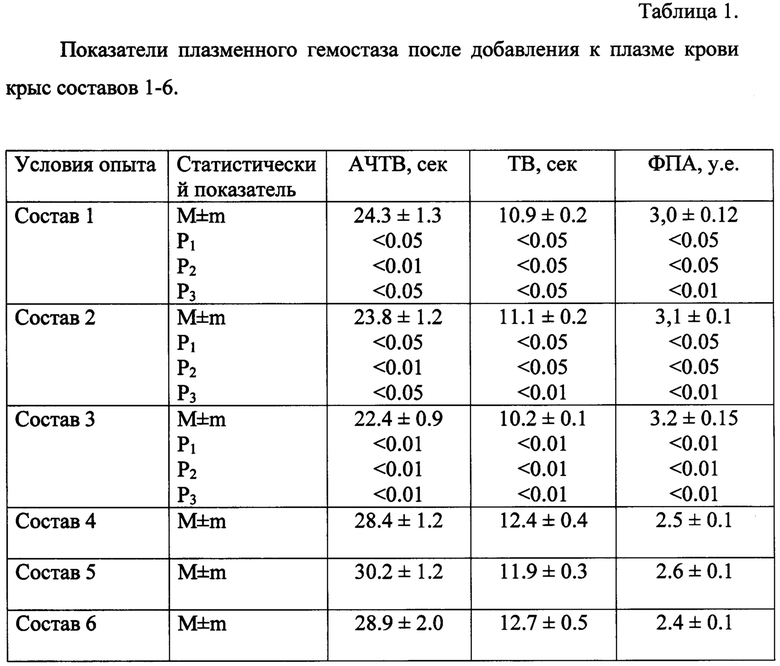
Примечания к таблице: АЧТВ - активированное частичное тромбопластиновое время, ТВ - тромбиновое время, ФПА - фибринполимеризационная активность.
Статистический показатель P1 рассчитан относительно состава 4, статистический показатель Р2 рассчитан относительно состава 5, статистический показатель Р3 рассчитан относительно состава 6
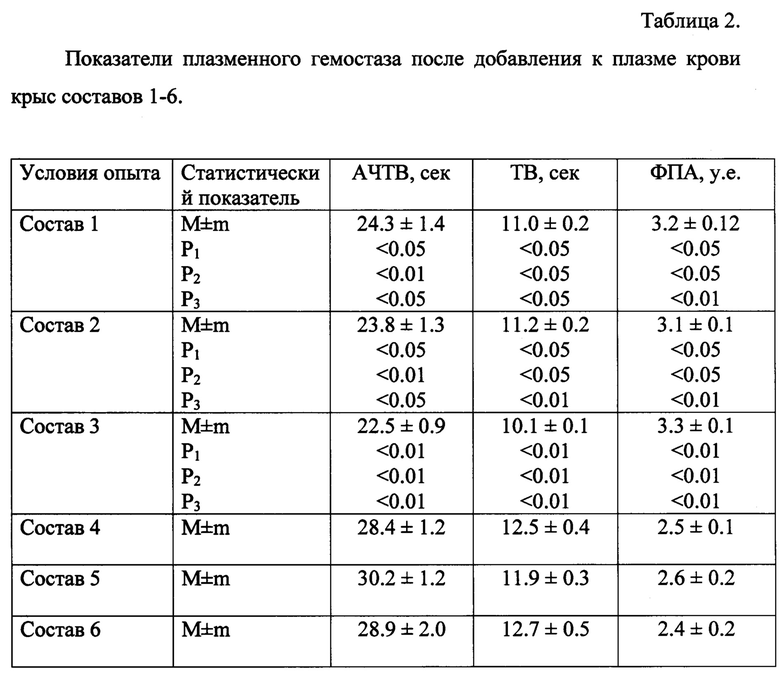
Примечания к таблице: АЧТВ - активированное частичное тромбопластиновое время, ТВ - тромбиновое время, ФПА - фибринполимеризационная активность.
Статистический показатель P1 рассчитан относительно состава 4, статистический показатель Р2 рассчитан относительно состава 5, статистический показатель Р3 рассчитан относительно состава 6.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ГЕМОСТАТИЧЕСКОГО СОСТАВА | 2021 |
|
RU2790831C2 |
| СПОСОБ ПОЛУЧЕНИЯ ГЕМОСТАТИЧЕСКОГО СОСТАВА | 2021 |
|
RU2781788C2 |
| Способ моделирования хронической токсической коагулопатии у экспериментальных животных | 2017 |
|
RU2661722C1 |
| СПОСОБ НОРМАЛИЗАЦИИ НАРУШЕНИЙ В КОАГУЛЯЦИОННОМ ЗВЕНЕ СИСТЕМЫ ГЕМОСТАЗА В ЭКСПЕРИМЕНТЕ | 2009 |
|
RU2391713C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ ХРОМ-ИНДУЦИРОВАННОЙ КОАГУЛОПАТИИ У КРЫС В ЭКСПЕРИМЕНТЕ | 2020 |
|
RU2743812C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ ХРОНИЧЕСКОЙ КОАГУЛОПАТИИ У ЖИВОТНЫХ В ЭКСПЕРИМЕНТЕ | 2020 |
|
RU2746831C1 |
| ПРИМЕНЕНИЕ ПОКАЗАТЕЛЕЙ КОАГУЛЯЦИОННОГО ГЕМОСТАЗА В КОМПЛЕКСНОЙ ДИСПАНСЕРИЗАЦИИ ВЫСОКОПРОДУКТИВНОГО КРУПНОГО РОГАТОГО СКОТА | 2022 |
|
RU2809362C1 |
| Способ профилактики хронической токсической коагулопатии у экспериментальных животных | 2018 |
|
RU2683723C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ПОКАЗАНИЙ К ТРАНСФУЗИИ КОРРЕКТОРОВ ПЛАЗМЕННО-КОАГУЛЯЦИОННОГО ГЕМОСТАЗА В КАРДИОХИРУРГИИ | 2014 |
|
RU2568581C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ФУНКЦИОНАЛЬНОГО СОСТОЯНИЯ СИСТЕМЫ ГЕМОСТАЗА ЛИЦ ПОЖИЛОГО И СТАРЧЕСКОГО ВОЗРАСТА | 2002 |
|
RU2263471C2 |
Настоящее изобретение относится к области медицины, а именно к гемостатическому составу, включающему хитозан, согласно изобретению дополнительно содержит эпсилонаминокапроновую кислоту, причем хитозан и эпсилонаминокапроновая кислота взяты в весовых соотношениях 8,0-12,0:1,0 соответственно. Настоящее изобретение обеспечивает увеличение прокоагулянтной и фибринполимеризационной активности. 2 табл., 5 пр.
Гемостатический состав, включающий хитозан, отличающийся тем, что дополнительно содержит эпсилонаминокапроновую кислоту, причем хитозан и эпсилонаминокапроновая кислота взяты в весовых соотношениях 8,0-12,0:1,0 соответственно.
| US 20200376157 A1, 03.12.2020 | |||
| Maksym V | |||
| Pogorielov, et al., Chitosan as a Hemostatic Agent: Current State / European Journal of Medicine | |||
| Series B, 2015, Vol.2, Is | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Dmitry Sonin et al., Biological Safety and Biodistribution of Chitosan Nanoparticles / Nanomaterials 2020, Vol.10, N.810, pp.1-23 | |||
| J F Hardy, et al., Natural and | |||
Авторы
Даты
2023-02-28—Публикация
2021-04-13—Подача