Изобретение относится к экспериментальной медицине, а именно к токсикологии и экологии, и может быть использовано для моделирования хронической коагулопатии, а также для экспериментальной разработки средств и методов профилактики и лечения нарушений системы гемостаза.
Молибден является важным биологически активным микроэлементом, необходимым для нормального осуществления процессов жизнедеятельности. Он играет важную роль в тканевом дыхании, является составной частью ферментов участвующих в регуляции процессов синтеза белка, входит в состав альдегидоксидазы, ксантиноксидазы и сульфита оксидазы, отвечающих за процессы метаболизма ДНК и РНК, установлено его влияние на углеводный обмен, вегетативную нервную систему, эндокринную функцию и другие процессы (Авцин А.П. и соавт. 1991). Вместе с тем, длительное поступление молибдена в организм в результате антропогенного загрязнения окружающей среды, может приводить к избыточному накоплению его в органах и тканях человека и полиорганным структурно-функциональным повреждениям (Реутова Н.В. Анализ заболеваемости населения в районе расположения вольфрамомолибденового комбината // Гигиена и санитария. 2007, (4), С. 13-15; Шерхов 3. X. и др. Морфофизиологические изменения органов и их систем у экспериментальных животных под действием молибдена /Воронеж: Науч. кн., 2012, С. 245). Показано, что поступивший в организм молибден накапливается преимущественно в почках и печени, обуславливая наиболее выраженное поражение этих органов (Брин В.Б. и соавт. Изменения мочеобразовательной функции почек под влиянием молибдата аммония у интактных крыс и в условиях экспериментальной гиперкальциемии, Нефрология, 2014, 18(5), С. 63-69). Показано, что молибденовая интоксикация сопровождается активацией перекисного окисления липидов, формированием окислительного стресса и повреждением мембранных структур (Брин В.Б. и соавт. 2012).
Данные многочисленных экспериментальных и клинических исследований позволяют считать, что при любых стрессорных воздействиях на организм одной из первых реагирует функциональная система свертывания крови (Киселёв В.И., Шахматов И.И. 2011), изменяя параметры своего функционирования, оказывает влияние на патогенез различных патологических процессов. Изменения системы гемостаза сопровождают патологию сердечно-сосудистой системы, гипертоническую болезнь, нарушения мозгового кровообращения, сахарный диабет, патологию печени и почек (Батырова А.С. и соавт. Современные представления о системе гемостаза при хронических заболеваниях печени // Клиническая лабораторная диагностика, 2015, (8), С. 40-47). Тромбин является физиологическим регулятором функциональной активности и жизнедеятельности клеток. Известна корреляция изменения гематологических показателей у работников тяжелой промышленности и стажа работы (Авцин А.П. Микроэлементозы человека: этиология, классификация, органопатология, М.: Медицина, 1991, С. 496). Однако, состояние свертывающей системы при молибденовой интоксикации не описано.
В доступной литературе встречаются лишь единичные работы, где описываются разнонаправленные и противоречивые изменения в системе гемостаза под влиянием различных соединений тяжелых металлов. Показано, что некоторые соединения тяжелых металлов способны к прокоагулянтной активности (Mutch N.J., Waters Е.K., Morrissey J.H. Immobilized transition metal ions stimulate contact activation and drive factor XII-mediated coagulation // J Thromb Haemost, 2012, 10(10), C. 2108-2115) в последовательности Ni2+>Cu2+>Co2+>Zn2+ вследствие активации внутреннего пути свертывания крови через фактор контакта. В работах других авторов напротив выявлялось снижение агрегационной активности тромбоцитов человека на фоне выраженной активации процессов перекисного окисления липидов под влиянием никеля (Chen C.Y., Lin Т.Н. Effects of nickel chloride on human platelets: enhancement of lipid peroxidation, inhibition of aggregation and interaction with ascorbic acid // Journal of Toxicology and Environmental Health Part A., 2001, (62)6, C. 431-438).
Актуальной является проблема создания удобной модели хронической коагулопатии, для разработки эффективных способов профилактики и лечения хронической интоксикации молибденом и его соединениями.
Известен способ моделирования хронической токсической коагулопатии у экспериментальных животных (Патент на изобретение RU 2661722 от 17.07.2017.) включающий ежедневное введение в желудок в течение двух месяцев хлорида никеля в дозе 5 мг/кг массы тела животного. Моделирование никелевой интоксикации у животных вызывает нарушения в системе клеточного и плазменного гемостаза. Недостатком данного способа является то, что с его помощью невозможно получить модель молибденовой коагулопатии, так как в прототипе не рассматривалось влияние молибдена на свертывающую систему крови. Известно, что разные металлы имеют преимущественные системы и органы «мишени» повреждающего воздействия.
Известен способ (Бышевский А.Ш. и соавт. Влияние комбинации витаминов-антиоксидантов на гемостаз при экспериментальной гипероксидации // Экспериментальная и клиническая фармакология, 2005, (68)3, С. 34-36) заключающийся в том, что ацетат свинца в дозе 0,5 мг/кг вводят крысам в течение 15 дней с пищей. Введение ацетата свинца вызывает снижение толерантности к тромбину, повышает уровень маркеров внутрисосудистого свертывания крови. Недостатком данного способа является сложность определения дозы свинца, поступающего в организм с пищей на единицу массы тела крыс.
Наиболее близким к предполагаемому изобретению является способ моделирования кадмиевой интоксикации у животных (Кухарчук О.Л. и соавт. Стан загального коагуляцiйного потенцiалу кровi i тканинного фiбринолiзу у бiлих щуpiв в нормi та при кадмiєвiй 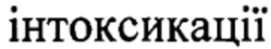 // Вюник про-блем
// Вюник про-блем 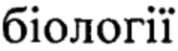 i медицини, 1999, (6), С. 130-136.), при котором животным ежедневно в течение двух недель через зонд в желудок вводят хлорид кадмия, в дозе 0,05 мг/кг массы тела.
i медицини, 1999, (6), С. 130-136.), при котором животным ежедневно в течение двух недель через зонд в желудок вводят хлорид кадмия, в дозе 0,05 мг/кг массы тела.
Моделирование кадмиевой интоксикации у животных в течение двух недель вызывает развитие синдрома диссеминированного внутрисосудистого свертывания крови. Нарушения в системе регуляции агрегатного состояния крови начинаются с токсического влияния на мембраны тромбоцитов, что приводит к увеличению их адгезивной и агрегационной активности, освобождению индукторов агрегации и вторичной активации коагуляционного гемостаза и снижению активности противосвертывающей системы крови.
Недостатком данного способа является:
- невозможность получения модели молибденовой коагулопатии, так как в прототипе не рассматривалось влияние молибдена на свертывающую систему крови. Химические соединения различных металлов имеют преимущественные системы и органы «мишени» воздействия на живой организм. Соли кадмия относится к токсическим веществам первого класса опасности, биологическая роль этого металла неизвестна. Молибден, напротив, является микроэлементом, необходимым для нормальной жизнедеятельности человека и животных. Входит в состав ферментов, участвует во многих внутриклеточных процессах (Авцин А.П. и соавт. 1991).
- влияние хлорида кадмия на организм в течение двух недель недостаточно для получения модели хронической коагулопатии. Длительный эксперимент -в течение двух месяцев является более приближенным к натуральным условиям (моделируя поступление металла в организм с пищей и водой из окружающей среды в условиях техногенного загрязнения окружающей среды), является более информативным, позволяя в разные сроки подробно в динамике изучить формирование нарушений звеньев системы гемостаза (через один и два месяца) в условиях токсического воздействия, что особенно важно в коагулологии.
Целью предполагаемого изобретения явилось создание модели хронической молибденовой коагулопатии.
Заявляемое изобретение направлено на решение задачи, заключающейся в создании способа моделирования хронической коагулопатии у экспериментальных животных.
Решение этой задачи позволяет:
- изучить более полно и в динамике патофизиологические механизмы развития коагулопатии при длительном воздействии молибдена,
- создать способ моделирования хронической коагулопатии у экспериментальных животных, повышающий воспроизводимость модели, удобный для проведения эксперимента на животных и экономически выгодный.
Для достижения этого технического результата заявляемый способ моделирования хронической коагулопатии у животных в эксперименте, включающий ежедневное один раз в сутки введение в желудок токсического вещества, отличающийся тем, что в качестве токсического вещества используют раствор парамолибдата аммония в течение 60 дней в дозе 50 мг/кг в пересчете на металл, где в единице раствора, равной 0,3 мл, содержится 5 мг молибдена. Данный способ отличается от прототипа использованием в качестве токсического вещества - парамолибдата аммония, длительностью и дозировкой введения металла.
Между отличительными признаками заявляемого изобретения и техническим результатом существует следующая причинно-следственная связь: длительное введение парамолибдата аммония в дозе 50 мг/кг приводит к развитию хронической молибденовой коагулопатии у экспериментальных животных, что является удобной и приближенной к натуральным условиям моделью.
По имеющимся у авторов сведениям совокупность существенных признаков, характеризующих сущность заявляемого изобретения не известна, что позволяет сделать вывод о соответствии изобретения критерию «новизна».
По мнению авторов, сущность заявляемого изобретения не следует для специалистов явным образом из известного уровня медицины, так как из него не выявляется вышеуказанная возможность получения способа моделирования хронической коагулопатии у экспериментальных животных. В научно-медицинской литературе нами не выявлено описание использования парамолибдата аммония для моделирования хронической молибденовой коагулопатии у экспериментальных животных. Следовательно, изобретение соответствует условию патентоспособности «изобретательский уровень», что позволяет сделать вывод о соответствии критерию «изобретательский уровень».
Совокупность существенных признаков, характеризующих сущность изобретения, в принципе может быть многократно использована в медицине с получением результата, заключающегося в легко воспроизводимом способе моделирования хронической коагулопатии у экспериментальных животных под влиянием молибдена, что позволяет сделать вывод о соответствии изобретения критерию «промышленная применимость».
Данный способ осуществляется следующим образом. Для получения токсического вещества парамолибдат аммония ((NH4)6Mo7O24• 4H2O) растворяют в дистиллированной воде таким образом, что в единице раствора, равной 0,3 мл, содержится 5 мг молибдена (в пересчете на металл). На каждые 100 г веса крысы вводят 0,3 мл токсического раствора, что не является чрезмерной водной нагрузкой на организм экспериментального животного. Раствор парамолибдата аммония вводят через атравматичный зонд в желудок в дозе 50 мг/кг, ежедневно 1 раз в сутки в течение 60 дней группе животных из 10 крыс.
Материалом для исследования являлась цельная кровь, а также богатая и бедная тромбоцитами плазма крови. Забор крови, стабилизация и получение образцов плазмы осуществлялись с учетом международных стандартов по клинической лабораторной диагностике для исследований в области гемостаза (Момот А.П. Патология гемостаза. Принципы и алгоритмы клинико-лабораторной диагностики, СПб.: Формат, 2006, 208 с.).
В пробах крови и плазмы определяют следующие показатели: АЧТВ -активированное частичное тромбопластиновое время по Caen et al. (1968); ПВ - протромбиновое время свертывания по Quick (1935); ТВ - тромбиновое время; ВПФМ - относительное время полимеризации фибрин-мономеров, Ф-ген - содержание фибриногена в плазме по Clauss (1961); АТ(III) - активность антитромбина III в плазме крови по В.А. Макарову и соавт. (2002); ВСЭЛ - время спонтанного эуглобулинового лизиса; РФМК - количество растворимых фибрин-мономерных комплексов (Елыкомов В.А., Момот А.П. Способ определения количества растворимого комплекса фибрин-мономера в плазме крови/ Авторское свидетельство 1371219, 1987, СССР); содержание D-димеров определяли на автоматическом анализаторе АС-4, с использование диагностических наборов «Helena» (Великобритания); количество тромбоцитов; агрегационную активность тромбоцитов (индуктор АДФ - 10,0 мкг/мл) (Баркаган, З.С., Момот А.П. Диагностика и контролируемая терапия нарушений гемостаза, М.: Ньюдиамед-АО, 2008, 292 с.). Коагулологические исследования были выполнены с применением наборов реагентов НПО «Ренам» и ООО фирмы «Технология-Стандарт», Россия на турбидиметрическом агрегометре АР-2110 и коагулометре CGL-2110 «Solar» (Беларусь).
Использование экспериментальных животных осуществляли в соответствии с Европейской конвенцией по охране позвоночных (1986) и правилами лабораторной практики в Российской Федерации (приказ МЗ РФ №708 от 23.08.2010).
Статистическую обработку полученных результатов проводили с использованием пакета программ "STATISTICA 10.0" (StatSoft) и Microsoft Excel 2016. Данные представлены в виде медианы (Me) и [25-75] процентили выборки. Для оценки статистической значимости различий в группах животных использовали непараметрический U-критерий Манна-Уитни. Различия считались достоверными при р<0,05.
Пример. Крысам-самцам линии Вистар в течение 2 месяцев ежедневно один раз в сутки через зонд в желудок вводили раствор парамолибдата аммония в дозе 50 мг/кг веса животного (10 крыс весом 200-300 гр). Контролем служили интактные животные (10 крыс) содержащиеся в стандартных условиях вивария. Состояние системы гемостаза оценивали через два месяца. В крови определяли показатели, характеризующие состояние сосудисто-тромбоцитарного звена гемостаза (количество тромбоцитов и их агрегационную активность), коагуляционного звена (АЧТВ, ПВ, ТВ, активность AT (III), (ВСЭЛ), содержание фибриногена) и уровня тромбинемии (РФМК, концентрацию D-димеров).
Через два месяца внутрижелудочного введения раствора парамолибдата аммония у экспериментальных животных выявляются нарушения механизмов свертывающей системы крови (Таблица 1).
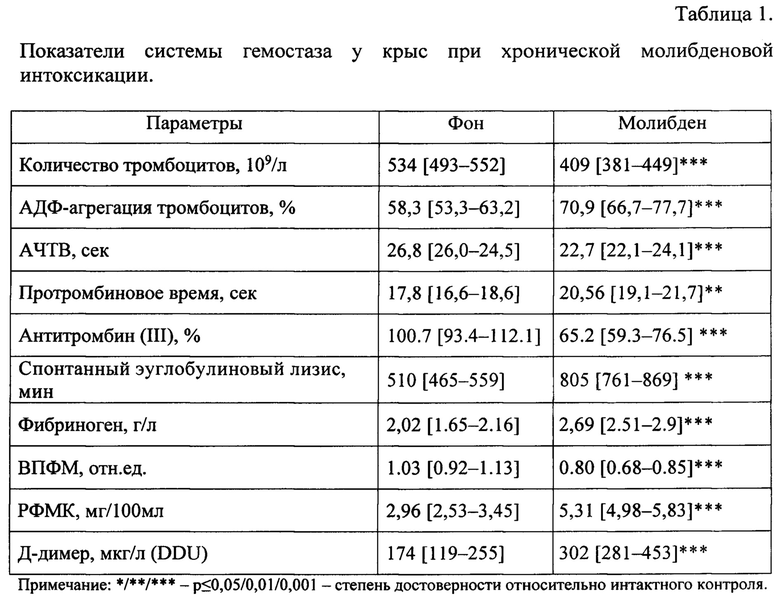
Наблюдается уменьшение количества тромбоцитов и увеличение их агрегационной функции, концентрация фибриногена возрастает достоверно выше контроля. Регистрируется укорочение АЧТВ и удлинение ПВ, тромбиновое время достоверно не меняется, однако выявляется укорочение более чувствительного маркера состояния конечного этапа гемокоагуляции - времени полимеризации фибрин мономеров (ВПФМ). Регистрируется уменьшение активности АТ(Ш) и замедление времени спонтанного эуглобулинового лизиса. Выявляется достоверное увеличение концентрации РФМК и Д-димеров (Полученные результаты отражены в таблице 1.).
Данные проведенных экспериментов демонстрируют развитие состояния тромботической готовности, определяемое Момотом А.П. и соавт. (А.П. Момот, Л.П. Цывкина, И.А. Тараненко Современные методы распознавания тромботической готовности, Барнаул, Изд-во Алт. ун-та, 2011, С. 138) как лабораторно выявляемую гиперкоагуляцию с возрастанием содержания в крови маркеров активации гемостаза, подавлением антикоагулянтной и фибринолитической активности. Гиперкоагуляционный синдром характеризуется состоянием повышенной готовности циркулирующей крови к свертыванию. При этом не выявляться тромбообразования в сосудистом русле, но может наблюдаться ряд клинических признаков предтромботического состояния в виде повышения вязкости крови, замедления венозного кровотока, преходящих и начальных признаков органной дисфункции.
Предлагаемый способ моделирования хронической коагулопатии у экспериментальных животных является эффективным, позволяет подробно изучить патофизиологические механизмы формирования коагулопатии при длительном воздействии молибдена на организм и может способствовать разработке и поиску средств для лечения и профилактики нарушений свертывающей системы крови.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРОФИЛАКТИКИ ХРОНИЧЕСКОЙ МОЛИБДЕНОВОЙ КОАГУЛОПАТИИ | 2020 |
|
RU2739690C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ ХРОНИЧЕСКОЙ ТОКСИЧЕСКОЙ КОАГУЛОПАТИИ У КРЫС | 2023 |
|
RU2800860C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ ХРОНИЧЕСКОЙ ТОКСИЧЕСКОЙ КОАГУЛОПАТИИ У КРЫС В ЭКСПЕРИМЕНТЕ | 2022 |
|
RU2785847C1 |
| Способ моделирования хронической токсической коагулопатии у экспериментальных животных | 2017 |
|
RU2661722C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ ХРОМ-ИНДУЦИРОВАННОЙ КОАГУЛОПАТИИ У КРЫС В ЭКСПЕРИМЕНТЕ | 2020 |
|
RU2743812C1 |
| СПОСОБ ПРОФИЛАКТИКИ ХРОНИЧЕСКОЙ СУЛЕМОВОЙ КОАГУЛОПАТИИ У КРЫС В ЭКСПЕРИМЕНТЕ | 2022 |
|
RU2788609C1 |
| СПОСОБ ПРОФИЛАКТИКИ ТОКСИЧЕСКОЙ КОАГУЛОПАТИИ У КРЫС | 2022 |
|
RU2794030C1 |
| СПОСОБ ПРОФИЛАКТИКИ ТОКСИЧЕСКОЙ КОАГУЛОПАТИИ У КРЫС | 2023 |
|
RU2829177C2 |
| Способ профилактики хронической свинцовой коагулопатии у экспериментальных животных | 2019 |
|
RU2706386C1 |
| Способ профилактики хронической токсической коагулопатии у экспериментальных животных | 2018 |
|
RU2683723C1 |
Изобретение относится к медицине, а именно к токсикологии и экологии, и касается моделирования хронической коагулопатии. Для этого экспериментальным животным в течение двух месяцев ежедневно один раз в сутки в желудок вводят раствор парамолибдата аммония в дозе 50 мг/кг в пересчете на металл, где в единице раствора, равной 0,3 мл, содержится 5 мг молибдена. Способ обеспечивает адекватное воспроизведение модели хронической коагулопатии у экспериментальных животных за счет оптимальной дозы и срока воздействия молибдена. 1 табл., 1 пр.
Способ моделирования хронической коагулопатии у животных в эксперименте, включающий ежедневное один раз в сутки введение в желудок токсического вещества, отличающийся тем, что в качестве токсического вещества используют раствор парамолибдата аммония в течение 60 дней в дозе 50 мг/кг в пересчете на металл, где в единице раствора, равной 0,3 мл, содержится 5 мг молибдена.
| Способ моделирования хронической токсической коагулопатии у экспериментальных животных | 2017 |
|
RU2661722C1 |
| СПОСОБ ПРОФИЛАКТИКИ ХРОНИЧЕСКОЙ ТОКСИЧЕСКОЙ КАРДИОПАТИИ У ЭКСПЕРИМЕНТАЛЬНЫХ ЖИВОТНЫХ | 2010 |
|
RU2424579C1 |
| US 201967768 A1, 06.06.2019, реферат | |||
| СИНЬКОВ С.В | |||
| и др | |||
| "Приобретенные коагулопатии: современные подходы к дифференциальной диагностике и интенсивной терапии с позиций доказательной медицины" | |||
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
| ANYANWU B.O | |||
| et al | |||
| "Heavy | |||
Авторы
Даты
2021-04-21—Публикация
2020-01-10—Подача