ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Изобретение относится к области фармацевтических композиций, содержащих изоксазолиновые соединения для применения у животных.
УРОВЕНЬ ТЕХНИКИ ИЗОБРЕТЕНИЯ
Изоксазолиновые соединения известны в данной области техники, и соединения из этого класса, как известно, обладают превосходной активностью против паразитарных инвазий животных.
Изоксазолиновые соединения и их применение в качестве противопаразитарных средств описаны, например, в заявке на патент США US 2007/0066617, и международных патентных заявках WO 2005/085216, WO 2007/079162, WO 2009/002809, WO 2009/024541, WO 2009/003075, WO 2010/070068 и WO 2010/079077.
Хотя различные пути введения являются известными, введение активных ингредиентов через системы снабжения питьевой водой интенсивно выращиваемым животным, таким как свиньи и птицы, является эффективным, поскольку оно делает возможным одновременное введение большому числу животных в течение определенного периода времени.
Многие свинофермы и птицефермы уже оснащены необходимыми устройствами для введения лекарств через системы питьевой воды.
Такие системы снабжения питьевой водой на фермах представляют собой комплексные системы резервуаров, дозирующих насосов, труб, витков, станочных поилок и ниппелей. Среднее помещение может содержать сотни метров труб с большим количеством витков и сотни индивидуальных чашек и/или ниппелей.
Вода в системе снабжения питьевой водой в свинарнике или птичнике подчиняется принципам ламинарного потока через трубы и витки и подвергается так называемым "касательным" силам, которые будут влиять на скорость потока. В такой сложной системе трубопроводов существуют значительные риски для сегрегации или осаждения лекарственного средства, конечно, когда речь идет о нерастворимых в воде соединениях.
Эффективность лекарственного средства через систему снабжения питьевой водой в целом во многом зависит от качества композиции (и ее стабильности в системе снабжения питьевой водой) и вкусовых качеств препарата.
Подходящая композиция должна обеспечить максимальную доступность активного ингредиента, минимальную или отсутствие сегрегации и осаждения активного вещества в системе снабжения питьевой водой, в насосах для лекарственного средства, в ниппелях, чашках и т.д., точное дозирование и равномерное распределение активного ингредиента в питьевой воде, и гарантированную стабильность активного ингредиента в самой композиции и после разбавления до целевой концентрации в лечебной питьевой воде.
Такие фармацевтические композиции отсутствуют в известном уровне техники.
Фармацевтическая композиция, которая была представлена в настоящем изобретении, удовлетворяет этим требованиям.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к применению фармацевтической композиции, содержащей изоксазолиновое соединение формулы (I),
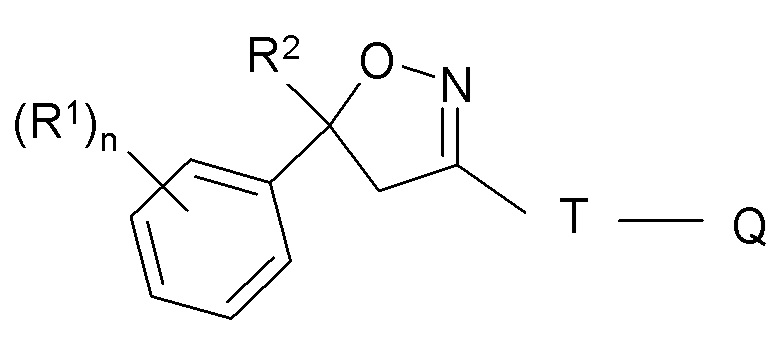 Формула (I),
Формула (I),
в которой
R1 = галоген, CF3, OCF3, CN,
N = целое число от 0 до 3, предпочтительно 1, 2 или 3,
R2 = С1-С3-галогеналкил, предпочтительно CF3 или CF2Cl,
Т=5- или 6-членное кольцо, которое необязательно замещено одним или несколькими радикалами Y,
Y = метил, галогенметил, галоген, CN, NO2, NH2-C=S, или два смежных радикала Y вместе образуют цепь, главным образом трех- или четырехчленную цепь;
Q = X-NR3R4 или 5-членное N-гетероарильное кольцо, которое необязательно замещено одним или несколькими радикалами;
Х = СН2, СН(СН3), СН(CN), CO, CS,
R3 = водород, метил, галогенэтил, галогенпропил, галогенбутил, метоксиметил, метоксиэтил, галогенметоксиметил, этоксиметил, галогенэтоксиметил, пропоксиметил, этиламинокарбонилметил, этиламинокарбонилэтил, диметоксиэтил, пропиниламинокарбонилметил, N-фенил-N-метил-амино, галогенэтиламинокарбонилметил, галогенэтиламинокарбонилэтил, тетрагидрофурил, метиламинокарбонилметил, (N,N-диметиламино)-карбонилметил, пропиламинокарбонилметил, циклопропиламинокарбонилметил, пропениламинокарбонилметил, галогенэтиламинокарбонилциклопропил,
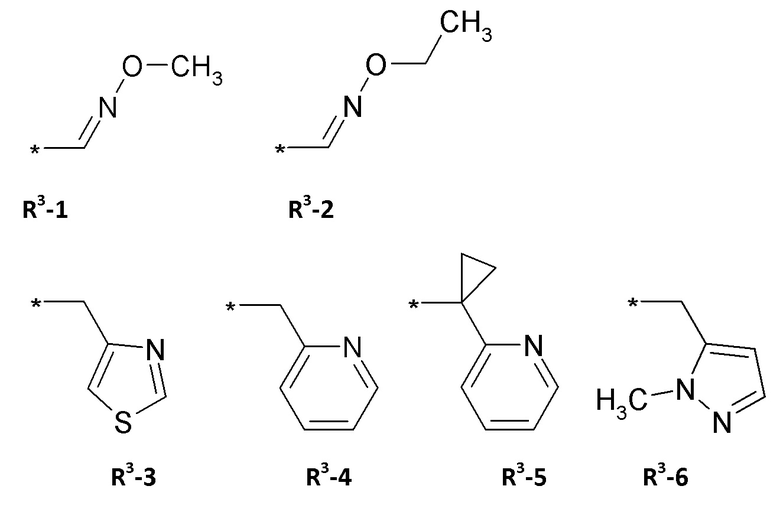
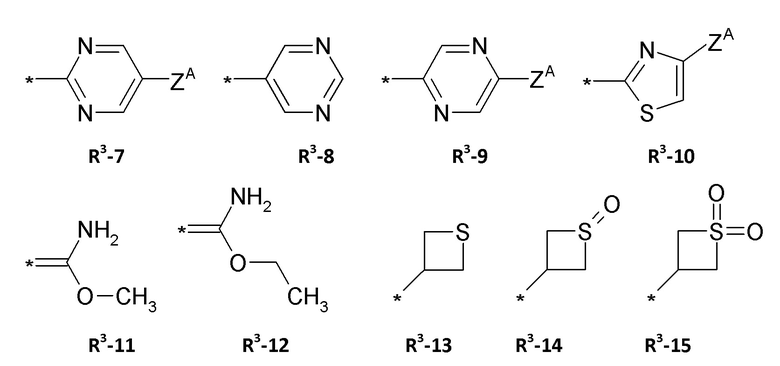 ,
,
где ZA = водород, галоген, циано, галогенметил (CF3);
R4 = водород, этил, метоксиметил, галогенметоксиметил, этоксиметил, галогенэтоксиметил, пропоксиметил, метилкарбонил, этилкарбонил, пропилкарбонил, циклопропилкарбонил, метоксикарбонил, метоксиметилкарбонил, аминокарбонил, этиламинокарбонилметил, этиламинокарбонилэтил, диметоксиэтил, пропиниламинокарбонилметил, галогенэтиламинокарбонилметил, цианометиламинокарбонилметил или галогенэтиламинокарбонилэтил;
или R3 и R4 вместе образуют заместитель, выбранный из группы, состоящей из:

или его соль, или его сольват и фармацевтически приемлемый носитель, содержащий моноэтиловый эфир диэтиленгликоля и полисорбатное поверхностно-активное вещество для получения лекарственного средства для введения через питьевую воду для профилактики или лечения паразитарных инвазий животных.
Другим аспектом настоящего изобретения является лечебная питьевая вода, содержащая фармацевтическую композицию, как описано выше, и воду.
Другим аспектом настоящего изобретения является способ получения лечебной питьевой воды для животных путем разбавления фармацевтической композиции, как описано выше, с помощью питьевой воды.
Другим аспектом настоящего изобретения является лечебная питьевая вода, как описано выше, для применения в лечении или профилактике паразитарных инвазий животных.
В частности, изобретение включает применение фармацевтической композиции, содержащей флураланер, афоксоланер, сароланер или лотиланер, или их соли, или их сольваты, и фармацевтически приемлемый носитель, содержащий моноэтиловый эфир диэтиленгликоля и полисорбатное поверхностно-активное вещество, для получения лекарственного средства для введения через питьевую воду для профилактики или лечения паразитарных инвазий животных.
Предпочтительно, флураланер, афоксоланер, сароланер или лотиланер присутствует в концентрации от 1,5 мг/мл до 100 мг/мл.
Соотношение моноэтилового эфира диэтиленгликоля и полисорбатного поверхностно-активного вещества составляет <50:50% масс./масс., предпочтительно 25/75% масс./масс.
Композиция согласно изобретению может дополнительно содержать этиллактат.
В одном из вариантов осуществления изобретения, полисорбатное поверхностно-активное вещество представляет собой полисорбат 80.
Далее, изобретение включает применение фармацевтической композиции, содержащей флураланер, афоксоланер, сароланер или лотиланер, или их соли, или их сольваты, и фармацевтически приемлемый носитель, содержащий моноэтиловый эфир диэтиленгликоля и полисорбатное поверхностно-активное вещество, для профилактики или лечения паразитарных инвазий у животных после введения животным через питьевую воду.
Предпочтительно, флураланер, афоксоланер, сароланер или лотиланер присутствует в концентрации от 1,5 мг/мл до 100 мг/мл.
Далее, соотношение моноэтилового эфира диэтиленгликоля и полисорбатного поверхностно-активного вещества может составлять <50:50% масс./масс., предпочтительно 25/75% масс./масс.
В одном из вариантов осуществления изобретения, композиция дополнительно содержит этиллактат.
Кроме того, полисорбатное поверхностно-активное вещество может представлять собой полисорбат 80.
Предпочтительно, животных выбирают из свиней и домашней птицы.
В одном из вариантов осуществления изобретения, животные представляют собой кур-несушек.
Далее, указанная паразитарная инвазия может представлять собой инвазию клещом.
Конкретнее, инвазия клещом представляет собой инвазию видом Dermanyssus или видом Ornithonyssus.
Далее, изобретение представляет собой лечебную питьевую воду, которая содержит смесь
фармацевтической композиции, содержащей флураланер, афоксоланер, сароланер или лотиланер, или его соль, или его сольват и фармацевтически приемлемый носитель, содержащий моноэтиловый эфир диэтиленгликоля и полисорбатное поверхностно-активное вещество, и
воды.
Предпочтительно, лечебная питьевая вода по изобретению содержит от 0,001 до 1 мг/мл флураланера, афоксоланера, сароланера или лотиланера.
Соотношение моноэтилового эфира диэтиленгликоля и полисорбатного поверхностно-активного вещества в указанной композиции составляет <50:50% масс./масс., предпочтительно 25/75% масс./масс.
Далее, изобретение относится к лечебной питьевой воде, в соответствии с вышеизложенным, где композиция дополнительно содержит этиллактат, а полисорбатное поверхностно-активное вещество представляет собой полисорбат 80.
Предпочтительно, животных, которым вводят лечебную питьевую воду по изобретению, выбирают из свиней и домашней птицы.
В одном из вариантов осуществления изобретения, животные представляют собой кур-несушек.
Указанная паразитарная инвазия может представлять собой инвазию клещом.
Конкретнее, инвазия клещом представляет собой инвазию видом Dermanyssus или видом Ornithonyssus.
Дополнительно, изобретение включает способ получения указанной лечебной питьевой воды, в котором фармацевтическую композицию разбавляют путем впрыскивания через систему дозирующего насоса в систему водоснабжения или путем смешивания с водой в резервуаре для лекарственных средств.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Было показано авторами изобретения, что фармацевтические композиции по настоящему изобретению, которые содержат изоксазолиновое соединение, как описано ниже, и фармацевтически приемлемый носитель, содержащий моноэтиловый эфир диэтиленгликоля и полисорбатное поверхностно-активное вещество, являются стабильными и эффективными в профилактике (предотвращении) и терапии (лечении) паразитарных инвазий животных.
Кроме того, было показано, что такие композиции могут быть использованы для приготовления лечебной воды, которая является достаточно стабильной и может быть равномерно распределена в системе, чтобы обеспечить введение эффективного количества изоксазолинового соединения животным через систему снабжения питьевой водой.
Изоксазолиновое соединение для применения в настоящем изобретении может быть описано формулой (I):
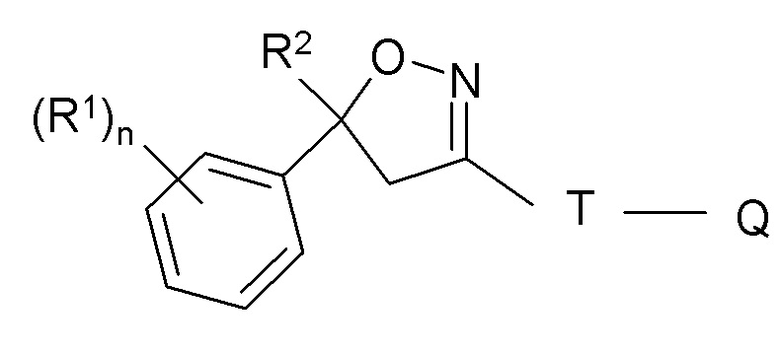 Формула (I),
Формула (I),
где
R1 = галоген, CF3, OCF3, CN,
n = целое число от 0 до 3, предпочтительно 1, 2 или 3,
R2 = С1-С3-галогеналкил, предпочтительно CF3 или CF2Cl,
Т = 5- или 6-членное кольцо, которое необязательно замещено одним или несколькими радикалами Y,
Y = метил, галогенметил, галоген, CN, NO2, NH2-C=S, два смежных радикала Y вместе образуют цепь СН-СН=СН-СН, N-СН=СН-СН, СН-N=CH-CH, СН-СН=N-СН или СН-СН=СН-N, HC=HC-СН, СН-СН=СН, СН=СН-N, N-СН=СН;
Q = X-NR3R4 или 5-членное N-гетероарильное кольцо, которое необязательно замещено одним или несколькими радикалами ZA, ZB ZD;
Х = СН2, СН(СН3), СН(CN), CO, CS,
R3 = водород, метил, галогенэтил, галогенпропил, галогенбутил, метоксиметил, метоксиэтил, галогенметоксиметил, этоксиметил, галогенэтоксиметил, пропоксиметил, этиламинокарбонилметил, этиламинокарбонилэтил, диметоксиэтил, пропиниламинокарбонилметил, N-фенил-N-метил-амино, галогенэтиламинокарбонилметил, галогенэтиламинокарбонилэтил, тетрагидрофурил, метиламинокарбонилметил, (N,N-диметиламино)-карбонилметил, пропиламинокарбонилметил, циклопропиламинокарбонилметил, пропениламинокарбонилметил, галогенэтиламинокарбонилциклопропил,
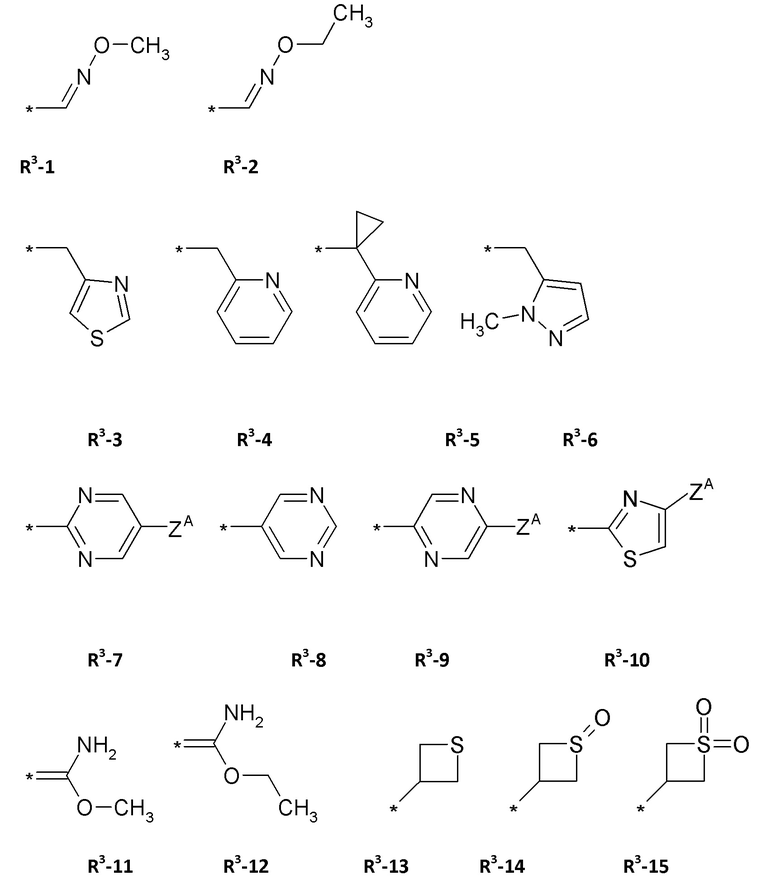
R4 = водород, этил, метоксиметил, галогенметоксиметил, этоксиметил, галогенэтоксиметил, пропоксиметил, метилкарбонил, этилкарбонил, пропилкарбонил, циклопропилкарбонил, метоксикарбонил, метоксиметилкарбонил, аминокарбонил, этиламинокарбонилметил, этиламинокарбонилэтил, диметоксиэтил, пропиниламинокарбонилметил, галогенэтиламинокарбонилметил, цианометиламинокарбонилметил или галогенэтиламинокарбонилэтил;
или
R3 и R4 вместе образуют заместитель, выбранный из группы, состоящей из:
 ,
,
где ZA = водород, галоген, циано, галогенметил (CF3).
В одном предпочтительном варианте осуществления в формуле (I) Т выбирают из
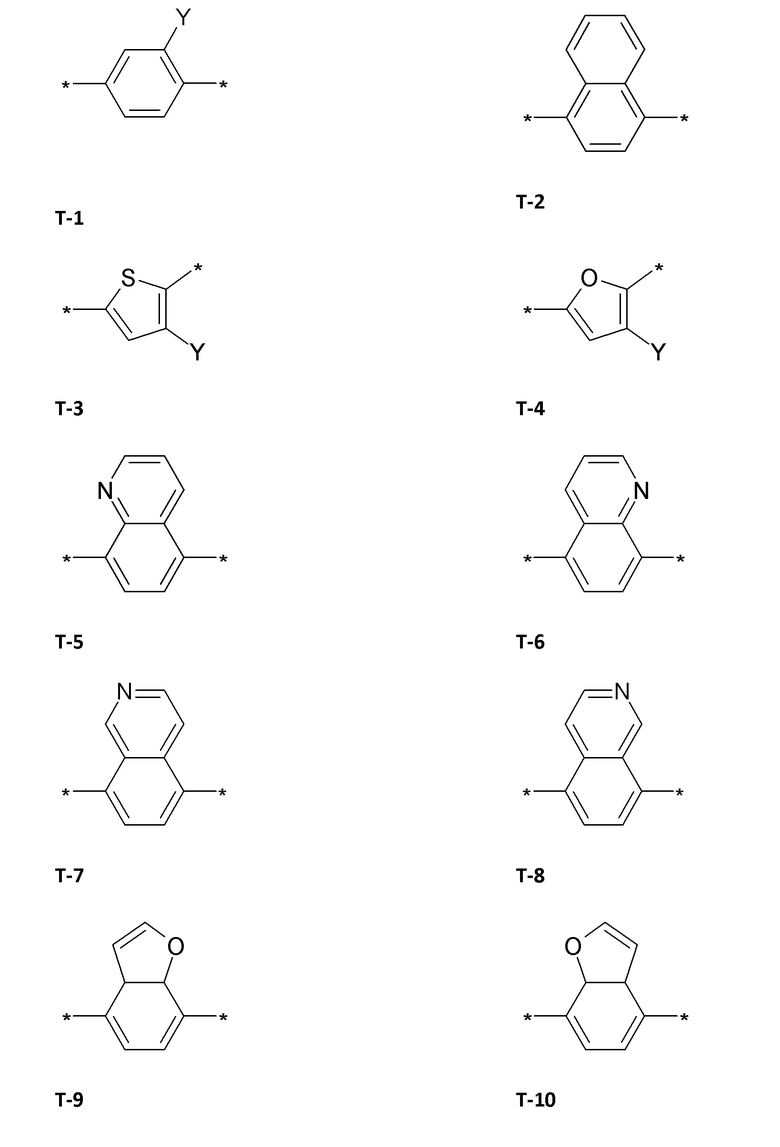
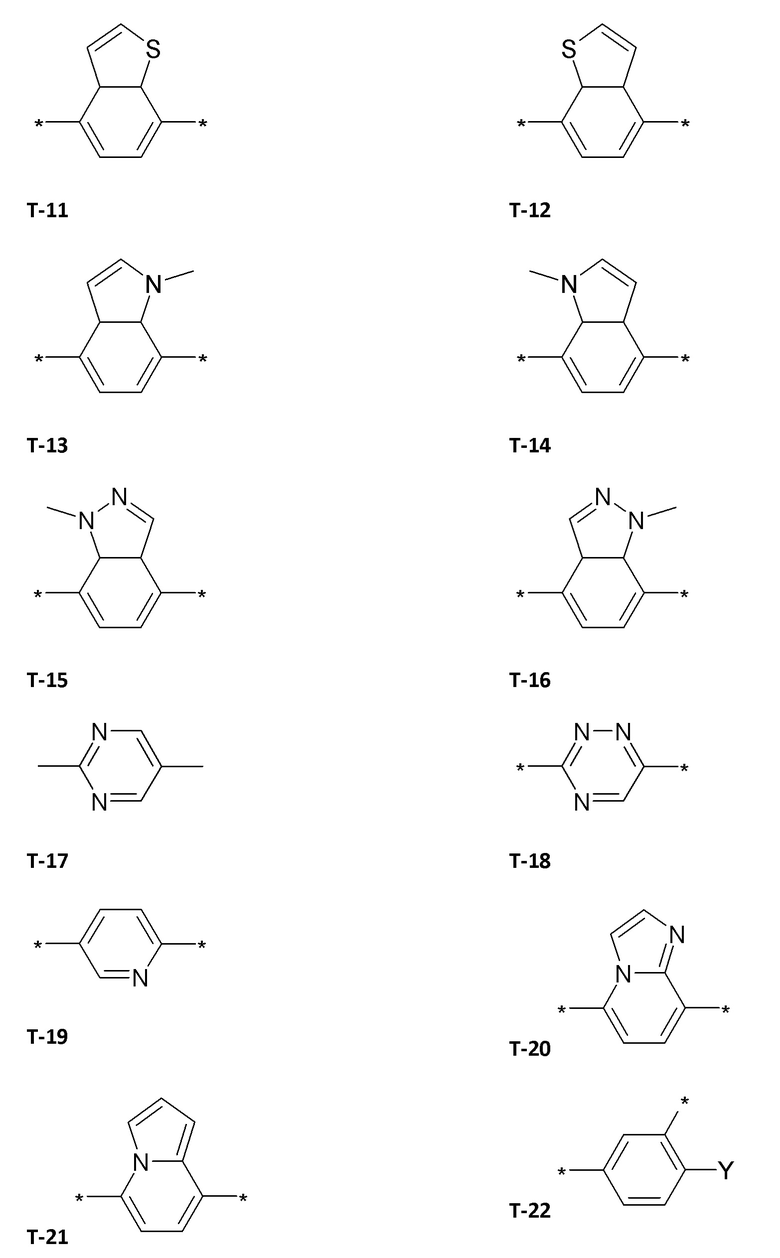 ,
,
где в Т-1, Т-3 и Т-4 радикал Y представляет собой водород, галоген, метил, галогенметил, этил, галогенэтил.
В предпочтительном варианте осуществления в формуле (I) Q выбирают из
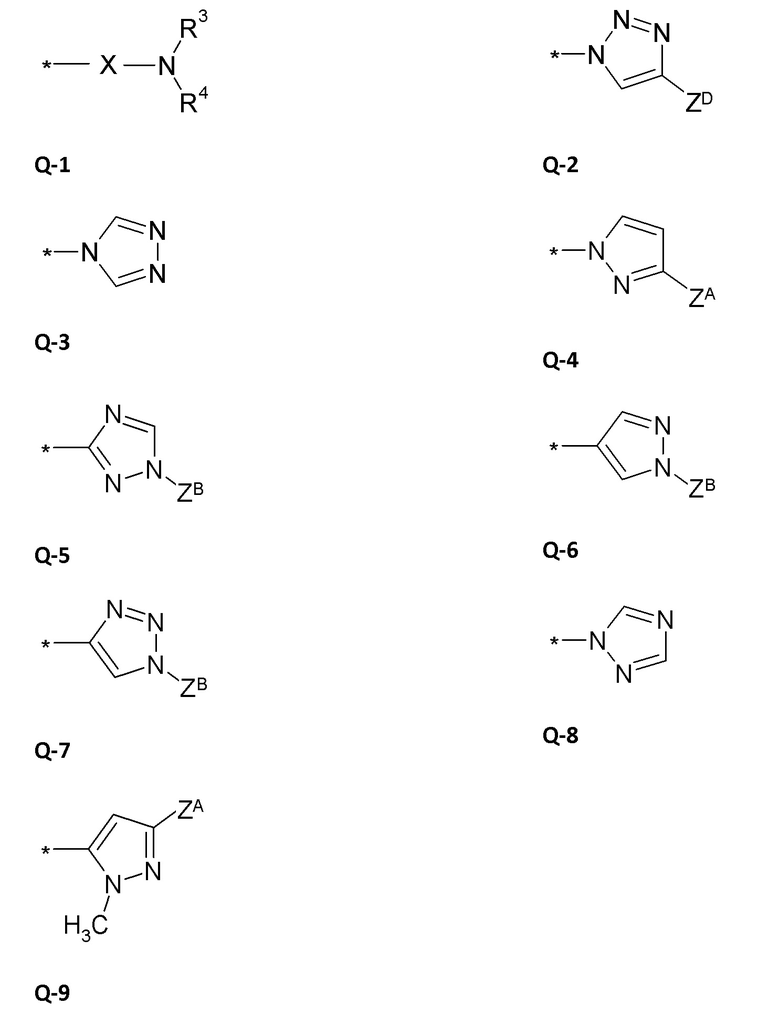 ,
,
где R3, R4, X и ZA имеют указанные выше значения.
ZB =
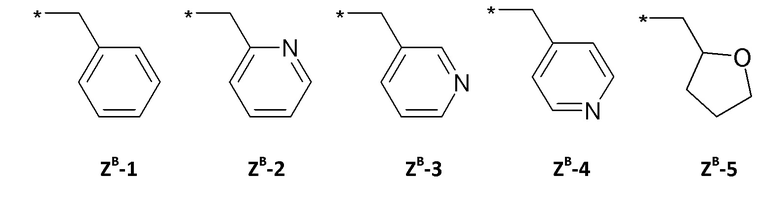
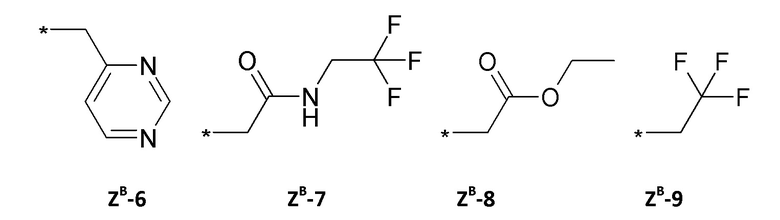
ZD =
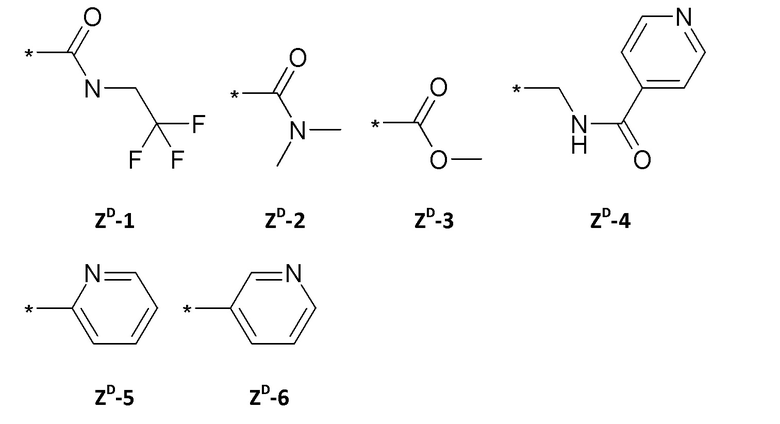
Предпочтительные изоксазолиновые соединения формулы (I) для применения по настоящему изобретению представляют собой:
Особенно предпочтительные изоксазолиновые соединения для применения по настоящему изобретению представляют собой
Более предпочтительное изоксазолиновое соединение для применения по настоящему изобретению имеет формулу (II),
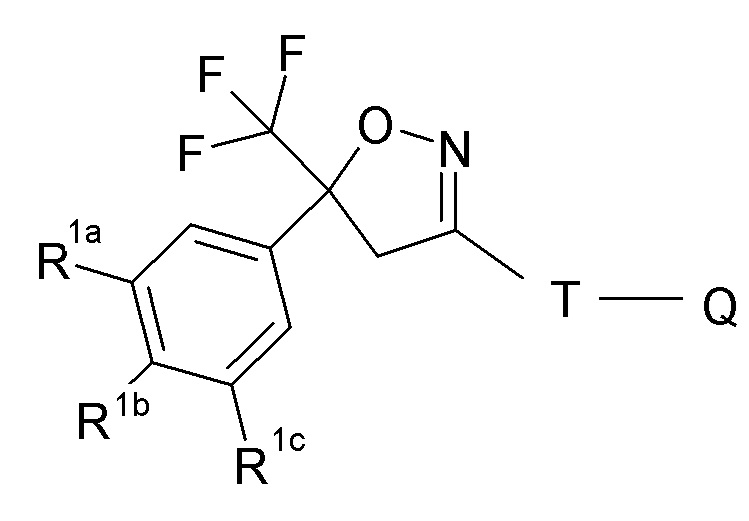 Формула II,
Формула II,
в которой
R1a, R1b, R1c независимо друг от друга представляют собой водород, Cl или CF3, предпочтительно R1a и R1c представляют собой Cl или CF3, и R1b представляет собой водород,
Т представляет собой
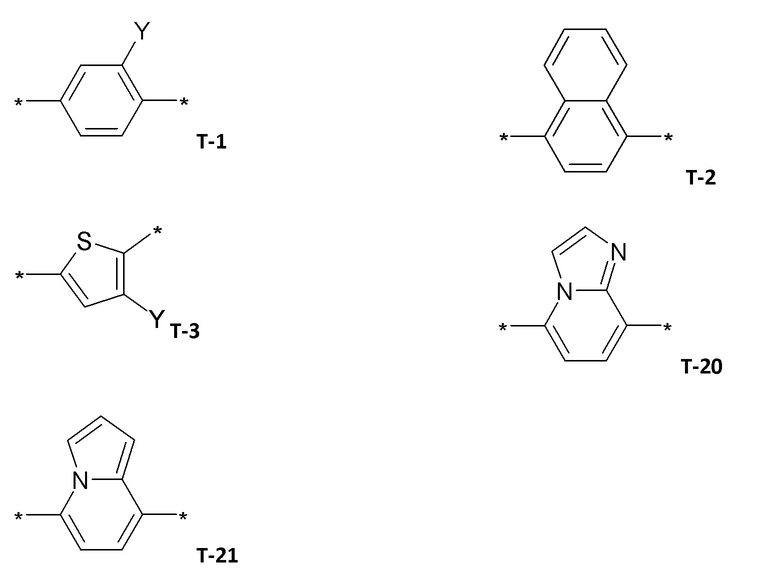 ,
,
где
Y представляет собой метил, бром, Cl, F, CN или C(S)NH2, и
Q является таким, как описано выше.
В другом предпочтительном варианте осуществления в формуле (II) R3 представляет собой Н, и R4 представляет собой -СН2-С(O)-NH-CH2-CF3, -СН2-С(O)-NH-СН2-СН3, -СН2-СН2-CF3 или -CH2-CF3.
В предпочтительном варианте осуществления изоксазолиновое соединение представляет собой 4-[5-(3,5-дихлофенил)-5-трифторметил-4,5-дигидроизоксазол-3-ил]-2-метил-N-[(2,2,2-трифтор-этилкарбамоил)-метил]-бензамид (CAS RN 864731-61-3 - флураланер USAN).
В другом варианте осуществления изоксазолиновое соединение представляет собой (Z)-4-[5-(3,5-дихлорфенил)-5-трифторметил-4,5-дигидроизоксазол-3-ил]-N-[(метоксиимино)метил]-2-метилбензамид (CAS RN 928789-76-8).
В другом варианте осуществления изоксазолиновое соединение представляет собой 4-[5-(3,5-дихлорфенил)-5-(трифторметил)-4H-изоксазол-3-ил]-2-метил-N-(тиетан-3-ил)бензамид (CAS RN 1164267-94-0), который был раскрыт в заявке WO 2009/0080250.
В другом предпочтительном варианте осуществления изобретения изоксазолиновое соединение представляет собой 4-[5-[3-хлор-5-(трифторметил)фенил]-4,5-дигидро-5-(трифторметил)-3-изоксазолил]-N-[2-оксо-2-[(2,2,2-трифторэтил)амино]этил]-1-нафталинкарбоксамид (CAS RN 1093861-60-9, USAN - афоксоланер), который был раскрыт в заявке WO 2007/079162.
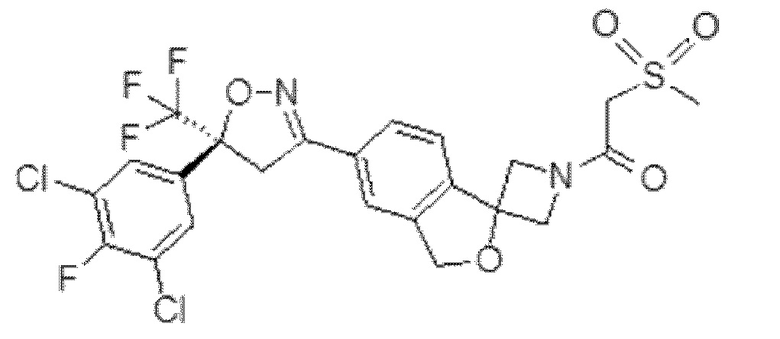
В другом варианте осуществления изоксазолиновое соединение представляет собой 1-[5'-[(5S)-5-(3,5-дихлор-4-фторфенил)-4,5-дигидро-5-(трифторметил)-3-изоксазолил]спиро[азетидин-3,1'(3'H)-изобензофуран]-1-ил]-2-(метилсульфонил)этанон - (Сароланер) (CAS RN 1398609-39-6).
В другом варианте осуществления изоксазолиновое соединение представляет собой 5-((5S)-4,5-дигидро-5-(3,4,5-трихлорфенил)-5-(трифторметил)-3-изоксазолил)-3-метил-N-(2-оксо-2-((2,2,2-трифторэтил)амино)этил)-2-тиофенкарбоксамид - (Лотиланер INN) (CAS RN 1369852-71-0).
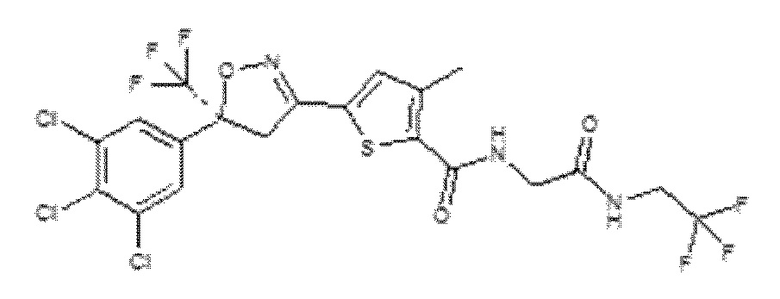
В другом варианте осуществления изоксазолиновое соединение представляет собой 5-[5-(3,5-дихлорфенил)-4,5-дигидро-5-(трифторметил)-3-изоксазолил]-3-метил-N-[2-оксо-2-[(2,2,2-трифторэтил)амино]этил]-2-тиофенкарбоксамид (CAS RN 1231754-09-8), который был раскрыт в заявке WO 2010/070068.
Способ (или применение) по настоящему изобретению включает применение рацемических смесей, например, равных количеств энантиомеров таких изоксазолиновых соединений, как описано выше. Кроме того, способ по настоящему изобретению включает в себя изоксазолиновые соединения, которые обогащены по сравнению с рацемической смесью энантиомером формулы 1. Также включены по существу чистые энантиомеры таких изоксазолиновых соединений.
При энантиомерном обогащении один энантиомер присутствует в большем количестве, чем другой, и степень обогащения может быть определена выражением энантиомерного избытка ("ee"), который определяется как (2х-l)-100%, где х представляет собой мольную долю доминантного энантиомера в смеси (например, ee 20% соответствует соотношению энантиомеров 60:40). Предпочтительно композиции для применения по настоящему изобретению имеют, по меньшей мере, 50% энантиомерный избыток; более предпочтительно, по меньшей мере, 75% энантиомерный избыток; еще более предпочтительно, по меньшей мере, 90% энантиомерный избыток; и наиболее предпочтительно, по меньшей мере, 94% энантиомерный избыток более активного изомера. Особо следует отметить энантиомерно чистые варианты осуществления более активного изомера.
Изоксазолиновые соединения, описанные выше, могут содержать дополнительные хиральные центры. Способ по данному изобретению включает рацемические смеси, а также обогащенные и по существу чистые стереоконфигурации при этих дополнительных хиральных центрах.
Ссылка на изоксазолиновое соединение в данном описании включает энантиомеры, соли и сольваты, а также N-оксиды, которые могут быть получены обычными способами.
Изоксазолиновое соединение, как описано выше, как правило, присутствует в композиции по настоящему изобретению в количестве от приблизительно 0,001 мг/мл до приблизительно 100 мг/мл.
Предпочтительная фармацевтическая композиция по настоящему изобретению представляет собой концентрированный раствор. Такой концентрированный раствор содержит от 1,5 мг/мл до 100 мг/мл изоксазолинового соединения, особенно флураланера.
Композиции согласно настоящему изобретению имеют особенно благоприятные свойства, такие как продолжительная стабильность после хранения и отсутствие осаждения изоксазолинового соединения после разбавления такой композиции в воде.
Фармацевтическая композиция по настоящему изобретению содержит фармацевтически приемлемый носитель, содержащий моноэтиловый эфир диэтиленгликоля и полисорбатное поверхностно-активное вещество.
Такой носитель должен быть по существу фармацевтически или ветеринарно чистым, и его компоненты должны быть нетоксичны в используемых количествах и должны быть совместимы с изоксазолиновыми соединениями.
Моноэтиловый эфир диэтиленгликоля используют в качестве растворителя, в таком носителе. Моноэтиловый эфир диэтиленгликоля или Транскутол (CAS № 31692-85-0) представляет собой соединение формулы (III)
R1--[O--(CH2)2]x--OR2 Формула (III),
где R1 = С2Н5, R2 = H и x = 2.
Продукты, содержащие моноэтиловый эфир диэтиленгликоля, являются, например, теми, которые известны и коммерчески доступны, например, под торговым наименованием Transcutol® от Gattefosse, (Сен-Приест, Франция), в частности, продукты Transcutol® V, P и HP.
Синонимичными названиями моноэтилового эфира диэтиленгликоля или Транскутола являются: 1-гидрокси-3,6-диоксаоктан, 2-(2'-этоксиэтокси)этанол, 2-(2-этоксиэтокси)этанол, 2-(2-этоксиэтилокси)этанол, 3,6-диокса-1-октанол, 3,6-диокса-1-октанол, 3,6-диоксаоктан-1-ол, этилдиэтиленгликоль, APV, карбитол, карбитол целлозольв, карбитол растворитель, DEGEE, DEGMEE, диэтиленгликоля этиловый эфир, диэтиленгликоля моноэтиловый эфир, дигликоля моноэтиловый эфир, диокситол, дованол, дованол 17, дованол DE, эктасолв DE, этанол, 2,2'-оксибис-, моноэтиловый эфир, этанол, 2-(2-этоксиэтокси)-, эфир моноэтиловый диэтиленгликоля, этокси дигликоль, этоксидигликоль, этилкарбитол, этил диэтиленгликоль, этилдиголь, этилдиэтиленгликоль, этилкарбитол.
Моноэтиловый эфир диэтиленгликоля как правило присутствует в композиции по изобретению в количестве от приблизительно 10% до приблизительно 75% по массе носителя.
В некоторых вариантах осуществления моноэтиловый эфир диэтиленгликоля присутствует в количестве от приблизительно 15% до приблизительно 60% по массе, от приблизительно 20% до приблизительно 55%, или от приблизительно 25% до приблизительно 50% по массе или приблизительно 12,5%, 25% или 37,5% по массе носителя.
В одном варианте осуществления композиция содержит, по меньшей мере, один дополнительный растворитель.
В одном варианте осуществления композиция дополнительно содержит этиллактат. Этиллактат, также известный как этиловый эфир молочной кислоты, представляет собой одноосновной сложный эфир, образованный молочной кислотой и этанолом.
В некоторых вариантах осуществления этиллактат присутствует в количестве от приблизительно 10% до приблизительно 50% по массе, или от приблизительно 10% до приблизительно 40% по массе или приблизительно 12,5%, 25% или 37,5% по массе носителя.
Предпочтительно соотношение моноэтилового эфира диэтиленгликоля и дополнительного растворителя, такого как этиллактат, составляет около 75%/25% масс./масс.
В одном из вариантов осуществления такой дополнительный растворитель представляет собой пирролидоновый растворитель, такой как 2-пиррол.
В некоторых вариантах осуществления 2-пиррол присутствует в количестве от приблизительно 10% до приблизительно 30% по массе, или приблизительно 12,5% или 25% по массе носителя.
Полисорбатные поверхностно-активные вещества показали благоприятные характеристики в композиции согласно настоящему изобретению. Как правило, может присутствовать одно или комбинация более чем одного полисорбатных поверхностно-активных веществ.
При контакте с водой полисорбатное поверхностно-активное вещество создает мицеллы вокруг изоксазолинового соединения, которое солюбилизируется в моноэтиловом эфире диэтиленгликоля, и сохраняет солюбилизираванное изоксазолиновое соединение в водной среде.
Полисорбатное поверхностно-активное вещество (сложный эфир сорбита, поли(окси-1,2-этандиил)производное, твин) представляет собой водорастворимый неионный поверхностно-активный агент, состоящий из сложных эфиров и эфиров алкоксикислот, полученных из шестиатомных спиртов, алкиленоксидов и жирных кислот добавлением полиоксиэтиленовых цепей к гидроксилу сорбита и гекситрол ангидридов (гекситаны и гексиды), полученных из сорбита, а затем частичной этерификацией с обычными жирными кислотами, такими как лауриновая, пальмитиновая, стеариновая и олеиновая кислоты.
В одном варианте осуществления полисорбатное поверхностно-активное вещество выбирают из одного или нескольких из Твин 20, Твин 40, Твин 60 и Твин 80, также известных в фармацевтической промышленности, как полисорбат 20, полисорбат 40, полисорбат 60 и полисорбат 80. Полисорбат 20 (полиоксиэтилированный монолаурат сорбитана) представляет собой сложный эфир лаурата, полисорбат 60 (полиоксиэтилированный моностеарат сорбитана) представляет собой смесь сложных эфиров стеарата и пальмитата; и полисорбат 80 (полиоксиэтилированный моноолеат сорбитана) представляет собой сложный эфир олеата.
Такие полисорбатные поверхностно-активные вещества являются коммерчески доступными и/или могут быть получены способами, известными в данной области техники.
В одном предпочтительном варианте осуществления полисорбатное поверхностно-активное вещество представляет собой полисорбат 80 (полиоксиэтилен моноолеат сорбитана, твин 80), имеющий химическое название полиоксиэтилен (20) моноолеат сорбитана, например, доступный от ICI Specialty Chemicals.
Полисорбатное поверхностно-активное вещество присутствует в композиции в количестве от приблизительно 5% до приблизительно 89% по массе носителя.
В некоторых вариантах осуществления настоящего изобретения концентрация полисорбатного поверхностно-активного вещества составляет от приблизительно 30% до приблизительно 80% по массе, от приблизительно 50% до приблизительно 75% по массе, или приблизительно 75% по массе носителя.
Соотношение моноэтилового эфира диэтиленгликоля и полисорбатного поверхностно-активного вещества составляет <50:50% масс./масс., предпочтительно 15/85, 20/80, 25/75, 30/70, 35/65, 40/60% масс./масс. В одном из вариантов осуществления соотношение составляет предпочтительно приблизительно 25/75% масс./масс. Было показано, что оно приводит к особенно стабильным фармацевтическим композициям.
Кроме того, носитель может содержать другие неактивные ингредиенты или эксципиенты, которые известны специалисту в данной области, например, как описано в источнике "Gennaro, Remington: The Science and Practice of Pharmacy" (20th Edition, 2000), включенном в настоящую заявку посредством ссылки.
Необязательно фармацевтическая композиция может также содержать противовспенивающий агент, такой как, например, 30% эмульсия симетикона USP, олеат натрия, каприлат натрия или их смеси.
Противовспенивающий агент присутствует в концентрации, достаточной для предотвращения образования пены, когда композицию по настоящему изобретению разбавляют водой. Эмульсия симетикона может присутствовать в концентрации от приблизительно 0,001% по массе до приблизительно 0,005% по массе носителя.
Необязательно фармацевтическая композиция может также содержать консервант. Консервант является консервантом, известным специалистам в данной области техники, и может представлять собой, например, бензиловый спирт, натриевую соль бутилпарабена, натриевую соль метилпарабена, натриевую соль пропилпарабена и их смеси. Он как правило присутствует в количестве от приблизительно 0,01% до приблизительно 3% по массе носителя.
Необязательно фармацевтическая композиция может также содержать антиоксидант. Антиоксидант представляет собой антиоксидант, известный специалистам в данной области техники, и может представлять собой, например, бутилированный гидроанизол, бутилированный гидротолуол, токоферол и его производное как α-токоферол полиэтиленгликоль сукцинат и их смеси. Он, как правило, присутствует в количестве от приблизительно 1% до приблизительно 10% по массе носителя.
Одним из аспектов настоящего изобретения является применение композиции согласно изобретению для получения лекарственного средства для профилактики или лечения паразитарной инвазии животного.
Под термином "лечащий" или "лечить" или "лечение" подразумевается применение или введение композиции по изобретению животному, которое имеет паразитарную инвазию для ликвидации паразита или уменьшения числа паразитов, заражающих животных.
Эффект композиции по настоящему изобретению может быть, например, овицидным, ларвицидным и/или представлять собой воздействие только на взрослых особей или их сочетание. Эффект может проявляться непосредственно, т.е. убивая паразитов либо сразу, либо после того, как прошло некоторое время, например, когда происходит линька, или разрушая их яйца, или косвенно, например, уменьшая количество откладываемых яиц и/или показатель выведения из яиц.
"Профилактика" или "предотвращение" означает, что новое заражение животных паразитами предотвращается путем убийства взрослых паразитов и любой стадии развития/личиночной стадии, которые способны заражать хозяина, перед заражением хозяина или непосредственно после заражения защищенного хозяина, или путем предотвращения возникновения потомства паразитов, например, уменьшая количество откладываемых яиц и/или показатель выведения из яиц.
Термин "эффективное количество" означает дозировку или количество изоксазолинового соединения, которое требуется, чтобы частично снизить или уменьшить численность паразитов на животном и/или в среде животного, например, доме/строении, и/или ингибировать развитие паразитарной инфекции на животном в целом или частично.
Эта величина легко определяется путем наблюдения или обнаружения численности паразитов либо на животном, либо в среде животного (например, с помощью ловушки) как до, так и после введения изоксазолинового соединения через питьевую воду таким животным, например, число паразитов снижается после первого введения на 5% до приблизительно 100%.
Следовательно, одним из аспектов настоящего изобретения является фармацевтическая композиция по настоящему изобретению, содержащая такую композицию для применения в профилактике или лечении паразитарных инвазий. Такие паразитарные инвазии могут представлять собой либо инвазии эктопаразитами, либо эндопаразитами.
В одном варианте осуществления паразитарная инвазия, которую предотвращают или лечат, представляет собой инвазию эктопаразитами. Конкретные примеры эктопаразитов включают, но не ограничиваются ими, блох (Ctenocephalides felis, вида Ctenocephalides и тому подобное), клещей (вида Rhipicephalus, вида Ixodes, вида Dermacentor, вида Amblyomma, вида Haemaphysalis, вида Boophilus и тому подобное) и клещей (вида Demodex, вида Sarcoptes, вида Otodectes, вида Cheyletiella, вида Dermanyssus, вида Ornithonyssus и тому подобное), вшей (вида Trichodectes, вида Felicola, вида Linognathus и тому подобное), комаров (вида Aedes, вида Culex, вида Anopheles и тому подобное) и мух (вида Hematobia, в том числе Haematobia irritans, вида Musca, вида Stomoxys, в том числе Stomoxys calcitrans, вида Dermatobia, вида Cochliomyia и тому подобное).
Главным образом, композиция согласно настоящему изобретению может быть введена всем видам животных, которые нуждаются в лечении или профилактике паразитарных инфекций, таким как свиньи, крупный рогатый скот, лошади, козы, овцы, собаки, кошки, птицы и рыбы.
В одном варианте осуществления животное представляет собой домашний скот, такой как свиньи, крупный рогатый скот, козы, овцы или домашние птицы.
В другом варианте осуществления животное представляет собой домашнее животное, такое как собаки, кошки или лошади. В другом варианте осуществления животное представляет собой домашнюю птицу или свинью.
Композицию по настоящему изобретению предпочтительно вводят посредством путей системного введения. "Системное введение" представляет собой введение на место, удаленное от места, где проживает, по меньшей мере, часть целевых паразитов.
При системном введении, по меньшей мере, часть соединения достигает целевого паразита через кровь животного-реципиента, другие биологические жидкости (лимфатическая жидкость) и/или ткани (например, кожа или жировая ткань).
Как правило, паразит глотает соединение вместе с кровью животного реципиента, другими жидкостями организма и/или тканями.
Системное введение может быть осуществлено в нескольких формах, например, пероральной, парентеральной или местной.
Фармацевтическая композиция может быть введена парентерально, например, посредством внутримышечной инъекции, внутривенной инъекции или подкожной инъекции.
В качестве альтернативы (или дополнительно) композиция по настоящему изобретению может быть системно введена местно с использованием трансдермального состава (т.е. состава, который проходит через кожу).
Такой трансдермальный состав может быть, например, в виде раствора для обработки, точечного нанесения, нанесения поливом или несения распылением. Особенно в случае состава для распыления фармацевтическая композиция может быть разбавлена водой с получением состава для распыления.
В качестве альтернативы фармацевтическую композицию можно вводить в виде ванны или раствора для обработки, например для овец или крупного рогатого скота. Для того чтобы приготовить такой состав для ванны или раствора для обработки фармацевтическую композицию разбавляют водой.
Фармацевтическая композиция по настоящему изобретению может быть разбавлена непосредственно с помощью воды, или предварительно разбавленный (мицеллярный) раствор, как описано ниже, разбавляют определенным объемом воды до эффективной (количества) концентрации изоксазолинового соединения в воде или пока не достигается требуемый путь введения.
Предварительно разбавленный (мицеллярный) раствор может быть получен из фармацевтической композиции, как описано выше (концентрированный раствор), путем смешивания с определенным объемом воды. Такой предварительно разбавленный раствор может быть дополнительно разведен в 1 до 5 раз. Такой предварительно разбавленный раствор содержит от 1 до 85% об./об. воды, главным образом, 1, 5, 10, 20, 30, 40, 50, 55, 60, 65, 70, 75, 80 или 85%. Такой раствор может быть введен животным в виде лечебной питьевой воды.
В некоторых вариантах осуществления композицию по настоящему изобретению системно вводят через пероральный путь в стандартной дозированной форме, такой как, например, раствор, суспензия (водная или неводная), эмульсия (типа масло-в-воде или вода-в-масле), эликсир, сироп или жидкая лекарственная форма для перорального введения.
Одной из предпочтительных форм введения пероральной стандартной дозированной формы является жидкая лекарственная форма для перорального введения, которую вводят, например, с помощью "шприца для вливания лекарства" через рот животных главным образом жвачным животным, например овцам, козам или крупному рогатому скоту, главным образом овцам.
В качестве альтернативы пероральное введение может быть осуществлено через корм животного-реципиента или питьевую воду, например, для корма она может быть тщательно диспергирована с обычным кормом животного-реципиента, использоваться в качестве подкормки или жидкости, которая добавляется к готовому корму.
В одном предпочтительном варианте осуществления композицию перорально вводят через питьевую воду. Следовательно, настоящее изобретение также относится к фармацевтической композиции, как описано в данном описании, для применения в профилактике или лечении инвазий паразитическими членистоногими животных.
В примерах показано (пример 5), что фармацевтическая композиция может быть использована для эффективной борьбы с инвазиями паразитическими членистоногими животных.
Пример 5 показывает, что введение через питьевую воду домашним птицам фармацевтической композиции по настоящему изобретению, содержащей изоксазолиновое соединение, как описано в данном описании, в данном случае флураланера, в результате привело к 99% подавлению красных птичьих клещей в течение, по меньшей мере, 15 дней. С помощью такого подавления паразитов жизненный цикл таких паразитических членистоногих может быть прерван, и установление новой значительной популяции в производственной единице может быть предотвращено в течение всего производственного цикла.
В одном из вариантов такими животными являются куры-несушки, которые производят яйца для потребления человеком. Такая фармацевтическая композиция также упоминается как "концентрированная фармацевтическая композиция" или как "концентрированный раствор".
Такие фармацевтические композиции могут быть получены методами, известными в данной области техники. Эти методы включают в себя, например, множество известных методов смешивания, растворения и эмульгирования.
В предпочтительном варианте осуществления фармацевтическая композиция предназначена для применения в получении лечебной питьевой воды для введения лекарственного средства животному через питьевую воду животного.
Таким образом, еще один вариант осуществления настоящего изобретения предоставляет лечебную питьевую воду, содержащую смесь фармацевтической композиции, как описано выше, и воды.
Лечебная питьевая вода, как правило, представляет собой питьевую воду, которая содержит фармацевтически активный ингредиент и воду.
Лечебную питьевую воду получают путем смешивания и разбавления количества (объема) фармацевтической композиции, как описано выше, с водой до концентрации изоксазолинового соединения, которая обеспечивает эффективное количество изоксазолинового соединения для некоторого количества животных, подвергнутых лечению, объемом питьевой воды, который в значительной степени соответствует объему, который будет потреблен такими животными в течение периода лечения.
Предварительно разбавленный (мицеллярный) раствор, который может быть использован в получении лечебной питьевой воды, как описано выше, может быть получен из фармацевтической композиции, как описано выше (концентрированного раствора), путем смешивания с определенным объемом питьевой воды.
Такой предварительно разбавленный раствор может быть дополнительно разведен в 1 до 5 раз для получения лечебной питьевой воды. Такой предварительное разбавленный раствор содержит от 1 до 85% об./об. воды, главным образом 1, 5, 10, 20, 30, 40, 50, 55, 60, 65, 70, 75, 80 или 85%.
Одним из аспектов настоящего изобретения является способ получения лечебной питьевой воды, в котором фармацевтическую композицию разбавляют путем впрыскивания через систему дозирующего насоса в систему водоснабжения или путем смешивания с водой в резервуаре для лекарственных средств.
Через лечебную питьевую воду фармацевтическая композиция, как описано выше, может быть доставлена целевому животному через выбранную систему снабжения питьевой водой путем смешивания и разбавления композиции с питьевой водой в центральной емкости для воды или в отдельном резервуаре для лекарственных средств и хранения.
В качестве альтернативы лечебная питьевая вода может быть получена путем впрыскивания композиции в соответствии с изобретением непрерывно в кольцевую систему для распределения питьевой воды с высоким или низким давлением с помощью дозирующего диспенсера или системы дозирующего насоса или системы дозатора лекарственных средств.
Системы дозирующего насоса задействуют насос, который передает отмеренные количества концентрата в водопроводные трубы при обычном разведении 1-5%.
В рамках систем дозирующих насосов, можно использовать электронные системы дозирующих насосов, такие как KONTI-DOS от Buerkert или механические дозирующие насосы, такие как дозирующие насосы с гидравлическим двигателем DOSATRON®, с гидравлическим приводом DOSMATIC®, пропорциональные медикаторы. Разнообразие полевых установок также касается самих систем водоснабжения: тупиковые системы или системы с замкнутым контуром различной длины с различными материалами труб (например, ПВХ, оцинкованное железо) и поилки, которые приспособлены для целевых животных, такие как колокольные поилки, ниппели.
В одном варианте осуществления фармацевтическая композиция может быть использована для лечения или профилактики паразитарных инвазий животных, особенно сельскохозяйственных животных (например, крупного рогатого скота, домашней птицы и свиней), с помощью изоксазолиновых соединений, например, флураланера, через системы питьевого водоснабжения.
Конечная концентрация изоксазолинового соединения в лечебной питьевой воде зависит от эффективного количества, массы тела животного, потребления животным воды и периода лечения. В общем случае эффективное количество на кг массы тела животных, подвергнутых лечению, обусловлено видом паразитической инфекции, подлежащей лечению, и является известным в данной области техники.
Медикатор использует, например, 10 мл фармацевтической композиции, как определено выше (концентрированной композиции), и далее разбавляет с помощью воды приблизительно в отношении 1:200, чтобы получить лечебную питьевую воду, имеющую концентрацию изоксазолинового соединения, например, флураланера, от 0,001 до приблизительно 1 мг/мл, особенно от приблизительно 0,05 до приблизительно 0,5 мг/мл.
В одном варианте осуществления лечебная вода имеет концентрацию от 0,002 до 0,2 мг/мл изоксазолинового соединения.
В одном конкретном варианте осуществления для конкретного изоксазолинового соединения флураланера концентрация в лечебной питьевой воде рассчитывается для обеспечения целевого количества флураланера на массу тела (МТ) домашней птицы, подвергаемой лечению, в интервале от приблизительно 0,1 мг до приблизительно 2 мг флураланера на килограмм массы тела в день.
Такое количество присутствует в объеме питьевой воды, обычно потребляемой домашней птицей, подвергаемой лечению, в период лечения от 2 до 24 ч, предпочтительно от 4-5 до 8 часов.
Фармацевтическую композицию можно сделать доступной в течение периода лечения для одного животного; или в то же время для группы животных или для всех животных в одном помещении (доме) или ферме через лечебную питьевую воду.
Введение фармацевтической композиции через лечебную питьевую воду, как определено ранее, является особенно полезным для домашней птицы и свиней. В случае домашней птицы особенно полезно для кур и индеек.
Введение фармацевтической композиции через лечебную питьевую воду, как определено ранее, является особенно полезным для типов кур, которых содержат в промышленном масштабе, например, куры-несушки, выращивание курочек или ремонтных цыплят, племенные несушки, и выращивание бройлерных курочек и племенных птиц.
Тем не менее, введение фармацевтической композиции через лечебную питьевую воду, как определено ранее, может быть также использовано и на других видах домашних птиц, таких как, например, индейки, гуси, утки, голуби, перепелки или фазаны.
Введение домашним птицам, которые содержатся для размножения или откладки яиц, которые содержатся дольше, чем приблизительно 8 недель, является предпочтительным. Сюда входят такие домашние птицы, которые в настоящее время (пока) не откладывают яйца (такие как, например, ремонтные цыплята). Особенно предпочтительным является введение курам-несушкам.
Термин "курица-несушка" или "несушка" является общим термином для взрослых самок кур, цыплят кур (Gallus Domesticus), которых в основном содержат для откладки яиц. Такие яйца обычно используются для потребления в качестве человеческой пищи.
Частота лечения с помощью фармацевтической композиции через лечебную питьевую воду зависит от паразита, от которого лечат или проводят профилактику (и от его биологического жизненного цикла) и производственного цикла животного-хозяина, подвергаемого лечению.
Фармацевтическую композицию по настоящему изобретению вводят через лечебную питьевую воду, по меньшей мере, один раз или два раза в производственный цикл животного-хозяина, подвергаемого лечению (например, период яйцекладки в случае кур-несушек).
Таким введением фармацевтической композиции через лечебную воду более высокая эффективность против паразитов может быть достигнута, так как на различные стадии жизненного цикла паразитов могут быть оказано влияние. По такой схеме введения популяция паразитов может быть уменьшена до уровня, который вызывает лишь минимальное повреждение животных и минимальные производственные потери.
Для некоторых паразитов, не на все стадии паразитов может быть оказано влияние путем однократного введения фармацевтической композиции через лечебную питьевую воду, потому что определенные стадии паразитов либо не питаются на животном, либо не в достаточной степени контролируются введением фармацевтической композиции через лечебную питьевую воду.
С введением второй дозы фармацевтической композиции через лечебную питьевую воду может быть оказано влияние на паразитов, которые развились (после жизненного цикла паразитов) из не восприимчивых стадий, или стадий паразитов, на которые трудно оказывать влияние, например, те, что созрели из ювенильных стадий паразитов (таких как яйца, нимфы или куколки) в течение этого периода.
Особенно предпочтительным является введение фармацевтической композиции через лечебную питьевую воду с интервалом приблизительно 7 дней или 14 дней (в зависимости от жизненного цикла паразита и производственного цикла животного-хозяина) один или два раза во время производственного цикла. Особенно предпочтительным является введение с интервалом 7 дней.
В одном варианте осуществления фармацевтическую композицию через лечебную питьевую воду вводят для лечения или профилактики инвазии клещом. Некоторые клещи мигрируют от птиц, грызунов, пищевого материала, растительного материала и домашней пыли и могут атаковать и раздражать животных и людей. Существуют различные категории клещей, включая северные куриные клещи (Ornithonyssus sylviarum), красные птичьи клещи (Dermanyssus gallinae), железницы (Demodex folliculorum), чесоточные клещи или клещи-возбудители зуда (вида Sarcoptes, вида Cheyletiella, вида Psorioptes).
В предпочтительном варианте осуществления инвазия клещом представляют собой инвазию клещом домашней птицы, особенно видом Dermanyssus (например, D. gallinae) и/или видом Ornithonyssus, особенно Ornithonyssus sylviarum.
В одном варианте осуществления введение фармацевтической композиции через обработанную питьевую воду в соответствии с изобретением контролирует стадии паразитических членистоногих, как описано выше, которые присутствуют в окружающей среде домашних птиц. Стадии паразитических членистоногих могут представлять собой все стадии жизненного цикла, которые известны специалистам в данной области, то есть как ювенильные стадии (развитие/личиночная стадия), так и стадии взрослого насекомого.
В одном варианте осуществления введение фармацевтической композиции через лечебную питьевую воду в соответствии с изобретением борется с членистоногими в среде домашних птиц, и особенно бройлерных цыплят, которые, как правило, не заражают животных непосредственно, но обеспечивают вред животным, такими как, например, чернотелки.
ПРИМЕРЫ
Пример 1
Приготовление концентрированного раствора
Композиции получали в соответствии со следующей процедурой:
Требуемое количество поверхностно-активного вещества и растворителя взвешивали в приспособленных контейнерах и эксципиенты выливали в технологический сосуд и взвешивали снова, чтобы ввести требуемые количества. Смесь перемешивали до полной гомогенизации. Активный ингредиент (изоксазолиновое соединение) добавляли к смеси поверхностно-активного вещества/растворителя при перемешивании дефлокулирующей лопастной мешалкой, и смесь перемешивали дефлокулирующей лопастной мешалкой до полного растворения активного ингредиента.
С помощью этого способа получали следующие композиции (концентрированные растворы), содержащие 1% масс./масс. Флураланера:
Стабильность концентрированного раствора в 10 мл стеклянных пробирках исследовали при 25°C/60% ОВ и 40°C/75% ОВ в течение 12 месяцев. Раствор был стабильным, по меньшей мере, 12 месяцев при 25°C/60% ОВ и 40°C/75% ОВ.
Пример 2
Получение предварительно разбавленного (мицеллярного) раствора
Предварительно разбавленные растворы готовили путем приготовления раствора 10% масс./масс. флураланера либо в Транскутоле V, либо в смеси Транскутола V/этиллактата в стеклянной пробирке емкостью 10 мл и добавления поверхностно-активного вещества и встряхивания. После этого очищенную воду добавляли к смеси растворителя/поверхностно-активного вещества и встряхивали.
Исследовали стабильность разбавленного раствора флураланера при 1 мкг/мл (Твин 80/Транскутол V 75/25 10мл-стеклянная пробирка). Растворы были стабильны в течение 2 дней при 25°C/60% ОВ и, по меньшей мере, 15 дней при температуре 2-8°C.
Следующие предварительно разбавленные растворы готовили и тестировали стабильность раствора (образование осадка). Наблюдали за предварительно разбавленными растворами при t=0, и одну аликвоту хранили в холодильнике при температуре 2-8°C и одну при 40°C/75% ОВ в течение 28 дней. Стабильность раствора (осадка) оценивали визуально в дни Д0, Д1, Д2, Д5, Д7, Д14, Д21 и Д28.
Исследованные составы приведены в таблице 1 ниже: TRV = Транскутол V, EL = Этиллактат
TRV= Транскутол V, EL= Этиллактат
Результаты:
Исследование стабильности разбавленных растворов флураланера в этиллактате/Транскутоле V /Твин 80/очищенной воде: Никакого осадка флураланера не наблюдали в разбавленных растворах в течение 5 дней после разбавления, за исключением разбавленных растворов EL/TRV-TW80'-W-40-20-40, который давал осадок на 5-й день, но не во время каких-либо других наблюдений в течение 28-дневного периода.
Исследование стабильности разбавленных растворов Транскутол V/твин 80/Очищенная вода: только один разбавленный раствор TRV-TW80-W-10-5-85 образовывал осадок на 5 день при 2-8°C и 40°C/75% ОВ.
Пример 3
Стабильность лечебной питьевой воды
Оценивали стабильность разбавленного раствора Флураланера при 1 мкг/мл, 2 мкг/мл, 10 мкг/мл и 20 мкг/мл (Твин 80/Транскутол V 75/25 в 25 м трубе (ПЭ-материал)). Растворы были стабильны в течение 4-х часов (симуляция лечения).
Пример 4
Технологическое исследование
Исследование проводили в коммерческом птичнике для приблизительно 36000 ремонтных цыплят с 4 батареями, каждый с 3 уровнями. 4 ПВХ тупиковых трубы для подвода воды (78 м длиной) поставляли воду для каждой батареи.
Питьевые ниппели (большие заглушки типа "винтовые ниппели" и "крышка", оснащенные "одноплечей" пластиковой капельной чашкой) устанавливали на водопроводных трубах. В этом производственном помещении оценивали поставку концентрированной композиции к питьевым ниппелям с использованием как системы дозирующего насоса, так и резервуара для лекарственных средств.
a) Дозирующий насос
Дозирующий насос и его контейнер для концентрированного раствора монтировали в водяной шланг, выходящий из трубы подачи воды и заканчивающийся в резервуаре с водой, в который отмеряли 105 л.
Дозирующий насос устанавливали на скорость впрыска 5%. Контейнер для концентрированного раствора заполняли в общей сложности на 8,8 л (175 × 0,05 [5%]).
После того, как контейнер был заполнен, расчетный объем 193 мл концентрированной композиции выливали в контейнер и затем перемешивали.
Дозирующий насос соединяли с водораспределительным патрубком и системой труб, заполненных лечебной водой.
b) Резервуар для лекарственных средств
Резервуар для лекарственных средств заполняли 175 л водопроводной воды.
Рассчитанный объем 193 мл концентрированной композиции выливали в емкость и затем перемешивали.
Резервуар для лекарственных средств соединяли с водораспределительным патрубком и системой труб, заполненных лечебной водой.
Ни одно животное не находилось в клетках. Поэтому водопроводные линии открывали через каждые 10 минут, чтобы имитировать непрерывный (периодический) поток питьевой воды. В каждом водоотводе 7,3 л лечебной воды оставляли стекать в тупиковую сторону трубы.
Образцы лечебной воды брали из 6 питьевых ниппелей: первый и последний питьевой ниппель в линии поилок, и от 4-х питьевых ниппелей, имеющих одинаковое расстояние, в заранее определенные моменты времени, с максимумом 4 ч, и анализировали на концентрацию флураланера.
Результаты:
В системе резервуара для лекарственных средств, концентрация Флураланера в ниппелях поилки - процент номинальной концентрации: 11,0 мкг/мл = 100%
В системе дозирующего насоса, концентрация Флураланера в ниппелях поилки - процент номинальной концентрации: 9,7 мкг/мл = 100%
Концентрация флураланера в питьевой воде остается постоянной в течение долгого времени и вдоль линии подачи питьевой воды, так как отклонение около 20%, как правило, является приемлемым при такой форме введения (до 4-х часов).
Пример 5
Исследование эффективности
Исследовали эффективность флураланера, который вводили перорально через лечебную питьевую воду, в борьбе с искусственно индуцированной инвазией красным птичьим клещом (Dermanyssus gallinae) кур-несушек. Группы A -D (n=6) лечили дозами по 2, 1 и 0,5 мг флураланера/кг массы тела единовременно или 1 мг флураланера/кг массы тела дробными дозами (по 0,5 мг/кг массы тела 2 раза).
Материалы и методы:
Потребление питьевой воды в каждой из групп измеряли за три дня до введения для расчета среднего суточного потребления воды. Лечебную воду готовили путем разбавления раствора флураланера (10 мг/мл), как показано в таблице ниже, до расчетной концентрации флураланера.
(%об./об.)
(мг/мл)
(моноэтиловый эфир диэтиленгликоля)
На Д0 (группа D дополнительно на Д7) куры в группах А-D получали флураланер через лечебную питьевую воду. Группа E получала неограниченно воду, не содержащую лекарственное средство.
Дозу для введения рассчитывали на основании средней массы тела каждой группы, подвергающейся лечению, полученной за один день до лечения (Д-1, Д 6). Концентрированный раствор флураланера разводили в питьевой воде для получения лечебной воды, готовой для потребления.
Лечебную питьевую воду готовили таким образом, что флураланер вводили в соответствии со следующим режимом дозирования:
Объем предложенной лечебной воды на группу на Д0 (группа D также на Д7) составлял примерно 50% от расчетного среднего ежедневного потребления воды, измеренного ранее в соответствующей группе, с тем, чтобы обеспечить потребление всей дозы.
После того, как вся лечебная вода потреблялась, другие 50% объема от среднего суточного потребления воды подавали в виде водопроводной воды в ту же поилку.
На 1-й день, 5-й день, 8-й день, 12 день, Д15, Д19 и Д22 четыре из шести кур в каждой группе заражали около 200 жизнеспособными клещами D. gallinae (некормленные нимфы и взрослые особи, которые голодали до заражения в течение 7 дней).
От каждой зараженной курицы приблизительно 25 налитых кровью клещей собирали и инкубировали в течение приблизительно 24 часов. Погибших, поврежденных и/или живых клещей подсчитывали визуально с помощью бинокуляра.
Клещей классифицировали как умерших, если не было определено никакого движения, или клещи лежали в дорсальном положении. Клещей классифицировали как поврежденных, если их движение было некоординированным.
Процент смертности клещей и подавления клещей рассчитывали для каждой группы, подвергнутой лечению, по сравнению с группой отрицательного контроля, не подвергнутой лечению.
Результаты:
Флураланер хорошо переносился курами.
% Смертности и % подавления красных клещей (Dermanyssus gallinae), оцененные приблизительно через 24 часа после заражения кур-несушек, получавших флураланер перорально через питьевую воду, приведены в таблицах 1 и 2. Быстрое начало действия продемонстрировали все вводимые дозы.
% Смертность D. gallinae оценивали через 24 часа после инвазии
Подавление D. gallinae оценивали через 24 часа после инвазии
На каждой оцениваемой временной точке, клещи, наблюдаемые у контрольной группы, не подвергнутой лечению, являлись жизнеспособными и показывали их нормальное поведение.
| название | год | авторы | номер документа |
|---|---|---|---|
| Изоксазолиновые композиции и их применение в провилактике или лечении паразитарных инвазий животных | 2014 |
|
RU2688919C1 |
| ПРИМЕНЕНИЕ ИЗОКСАЗОЛИНОВЫХ СОЕДИНЕНИЙ НА ДОМАШНЕЙ ПТИЦЕ | 2014 |
|
RU2796536C2 |
| ПРИМЕНЕНИЕ ИЗОКСАЗОЛИНОВЫХ СОЕДИНЕНИЙ НА ДОМАШНЕЙ ПТИЦЕ | 2014 |
|
RU2688167C1 |
| ТВЕРДЫЕ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ ДЛЯ ПЕРОРАЛЬНОГО ВВЕДЕНИЯ НА ОСНОВЕ ИЗОКСАЗОЛИНОВЫХ СОЕДИНЕНИЙ | 2013 |
|
RU2646483C2 |
| ТВЕРДЫЕ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ ДЛЯ ПЕРОРАЛЬНОГО ВВЕДЕНИЯ НА ОСНОВЕ ИЗОКСАЗОЛИНОВЫХ СОЕДИНЕНИЙ | 2013 |
|
RU2772279C2 |
| ПРИМЕНЕНИЕ ИЗОКСАЗОЛИНОВЫХ СОЕДИНЕНИЙ ДЛЯ ЛЕЧЕНИЯ ДЕМОДЕКОЗА | 2015 |
|
RU2709198C2 |
| ПРОТИВОПАРАЗИТАРНЫЕ КОМПОЗИЦИИ ДЛЯ ПРИМЕНЕНИЯ ПУТЕМ ОБЛИВАНИЯ | 2018 |
|
RU2802299C2 |
| ИНЪЕКЦИОННЫЕ ИЗОКСАЗОЛИНОВЫЕ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ И ИХ ПРИМЕНЕНИЕ | 2018 |
|
RU2799591C2 |
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ ДЛЯ ИНЪЕКЦИЙ И ИСПОЛЬЗОВАНИЕ ТАКОВЫХ | 2020 |
|
RU2829447C2 |
| ПРИМЕНЕНИЕ СОДЕРЖАЩИХ ИЗОКСАЗОЛИН СОЕДИНЕНИЙ В КАЧЕСТВЕ ПРОТИВОПАРАЗИТАРНЫХ СРЕДСТВ | 2014 |
|
RU2673723C1 |
Группа изобретений относится к области ветеринарии и направлена на лечение паразитарных инвазий животных. Предложено применение фармацевтической композиции, содержащей флураланер, афоксоланер, сароланер или лотиланер, или их соли, или их сольваты, и фармацевтически приемлемый носитель, содержащий моноэтиловый эфир диэтиленгликоля и полисорбатное поверхностно-активное вещество, для получения лекарственного средства для введения через питьевую воду для профилактики или лечения паразитарных инвазий животных. Также раскрывается применение фармацевтической композиции для профилактики или лечения паразитарных инвазий у животных после введения животным через питьевую воду, лечебная питьевая вода и способ получения лечебной питьевой воды. Группа изобретений обеспечивает эффективную профилактику и лечение паразитарных инвазий у животных. 4 н. и 32 з.п. ф-лы, 5 табл., 5 пр.
1. Применение фармацевтической композиции, содержащей флураланер, афоксоланер, сароланер или лотиланер, или их соли, или их сольваты, и фармацевтически приемлемый носитель, содержащий моноэтиловый эфир диэтиленгликоля и полисорбатное поверхностно-активное вещество, для получения лекарственного средства для введения через питьевую воду для профилактики или лечения паразитарных инвазий животных.
2. Применение по п.1, где флураланер, афоксоланер, сароланер или лотиланер присутствует в концентрации от 1,5 мг/мл до 100 мг/мл.
3. Применение по п.1 или 2, где соотношение моноэтилового эфира диэтиленгликоля и полисорбатного поверхностно-активного вещества составляет <50:50% масс./масс., предпочтительно 25/75% масс./масс.
4. Применение по п.1 или 2, где композиция дополнительно содержит этиллактат.
5. Применение по п.3, где композиция дополнительно содержит этиллактат.
6. Применение по п.1 или 2, где полисорбатное поверхностно-активное вещество представляет собой полисорбат 80.
7. Применение по п.3, где полисорбатное поверхностно-активное вещество представляет собой полисорбат 80.
8. Применение по п.4, где полисорбатное поверхностно-активное вещество представляет собой полисорбат 80.
9. Применение по п.5, где полисорбатное поверхностно-активное вещество представляет собой полисорбат 80.
10. Применение фармацевтической композиции, содержащей флураланер, афоксоланер, сароланер или лотиланер, или их соли, или их сольваты, и фармацевтически приемлемый носитель, содержащий моноэтиловый эфир диэтиленгликоля и полисорбатное поверхностно-активное вещество, для профилактики или лечения паразитарных инвазий у животных после введения животным через питьевую воду.
11. Применение по п.10, где флураланер, афоксоланер, сароланер или лотиланер присутствует в концентрации от 1,5 мг/мл до 100 мг/мл.
12. Применение по п.10 или 11, где соотношение моноэтилового эфира диэтиленгликоля и полисорбатного поверхностно-активного вещества составляет <50:50% масс./масс., предпочтительно 25/75% масс./масс.
13. Применение по п.10 или 11, где композиция дополнительно содержит этиллактат.
14. Применение по п.12, где композиция дополнительно содержит этиллактат.
15. Применение по п.10 или 11, где полисорбатное поверхностно-активное вещество представляет собой полисорбат 80.
16. Применение по п.12, где полисорбатное поверхностно-активное вещество представляет собой полисорбат 80.
17. Применение по п.13, где полисорбатное поверхностно-активное вещество представляет собой полисорбат 80.
18. Применение по п.14, где полисорбатное поверхностно-активное вещество представляет собой полисорбат 80.
19. Применение по любому из пп.10-18, где животных выбирают из свиней и домашней птицы.
20. Применение по п.19, где животные представляют собой кур-несушек.
21. Применение по любому из пп.10-20, где паразитарная инвазия представляет собой инвазию клещом.
22. Применение по п.21, где инвазия клещом представляет собой инвазию видом Dermanyssus или видом Ornithonyssus.
23. Лечебная питьевая вода для профилактики или лечения паразитарных инвазий у животных, содержащая смесь
фармацевтической композиции, содержащей флураланер, афоксоланер, сароланер или лотиланер, или его соль, или его сольват и фармацевтически приемлемый носитель, содержащий моноэтиловый эфир диэтиленгликоля и полисорбатное поверхностно-активное вещество, и
воды.
24. Лечебная питьевая вода по п.23, содержащая от 0,001 до 1 мг/мл флураланера, афоксоланера, сароланера или лотиланера.
25. Лечебная питьевая вода по п.23 или 24, где соотношение моноэтилового эфира диэтиленгликоля и полисорбатного поверхностно-активного вещества в композиции составляет <50:50% масс./масс., предпочтительно 25/75% масс./масс.
26. Лечебная питьевая вода по п.23 или 24, где композиция дополнительно содержит этиллактат.
27. Лечебная питьевая вода по п.25, где композиция дополнительно содержит этиллактат.
28. Лечебная питьевая вода по п.23 или 24, где полисорбатное поверхностно-активное вещество представляет собой полисорбат 80.
29. Лечебная питьевая вода по п.25, где полисорбатное поверхностно-активное вещество представляет собой полисорбат 80.
30. Лечебная питьевая вода по п.26, где полисорбатное поверхностно-активное вещество представляет собой полисорбат 80.
31. Лечебная питьевая вода по п.27, где полисорбатное поверхностно-активное вещество представляет собой полисорбат 80.
32. Лечебная питьевая вода по любому из пп.23-31, где животных выбирают из свиней и домашней птицы.
33. Лечебная питьевая вода по п.32, где животные представляют собой кур-несушек.
34. Лечебная питьевая вода по любому из пп.23-33, где паразитарная инвазия представляет собой инвазию клещом.
35. Лечебная питьевая вода по п.34, где инвазия клещом представляет собой инвазию видом Dermanyssus или видом Ornithonyssus.
36. Способ получения лечебной питьевой воды по любому из пп.23-31, в котором фармацевтическую композицию разбавляют путем впрыскивания через систему дозирующего насоса в систему водоснабжения или путем смешивания с водой в резервуаре для лекарственных средств.
| WO 2007053902 A1, 18.05.2007 | |||
| WO 2012089622 A3, 05.07.2012 | |||
| WO 2009024541 A3, 26.02.2009 | |||
| RU 2010102224 A, 10.08.2011 | |||
| US 20130065846, 14.03.2013. |
Авторы
Даты
2023-03-13—Публикация
2014-12-19—Подача