Изобретение относится к области биотехнологии, в частности к определению мутации S:N501Y SARS-CoV-2 с использованием полимеразной цепной реакции в режиме реального времени (ПЦР-РВ) и может применяться для идентификации геновариантов SARS-CoV-2 при эпидемиологических исследованиях.
Коронавирусная инфекция (COVID-19) это инфекционное заболевание, вызванное SARS-CoV-2. Вирус передается от человека к человеку воздушно-капельным путем. Изменения в структуре генома SARS-CoV-2 приводят к возникновению вариантов, которые ВОЗ обозначила как вызывающие интерес (VOIs, Variants of Interest), вызывающие озабоченность (VOCs, Variants of Concern) и линии VOC под мониторингом (VOC lineages under monitoring (VOC-LUM). Определение мутаций в геноме SARS-CoV-2 и их классификация на VOIs и VOCs и VOC-LUM является важным элементом молекулярно-генетического мониторинга штаммов новой коронавирусной инфекции. Мутации, детекция которых необходима, перечислены в докладах Технической консультативной группы по эволюции вируса SARS-CoV-2 (TAG-VE) ВОЗ [https://www.who.int/publications/rn on-sars-cov-2-virus-evolution-(tag-ve)].
Для определения геновариантов вируса и проведения молекулярно-генетического мониторинга SARS-CoV-2 используются методы полногеномного и фрагментного секвенирования, которые являются дорогостоящими и трудоемкими. С целью выявления SARS-CoV-2 Всемирной организацией здравоохранения предложено выделение РНК возбудителя с последующим проведением полимеразной цепной реакции с обратной транскрипцией (ОТ-ПЦР) [https://www.who.int/emergencies/diseases/novel-coronavirus-2019/technical-guidance/laboratory-guidance].
Известные протоколы исследования направлены на выявление специфических нуклеотидных последовательностей в генах и межгенных промежутках:
- ORF1ab, N [http://ivdc.chinacdc.cn/kyjz/202001/t20200121_211337.html];
- RdRP, Е, N [https://www.who.int/docs/default-source/coronaviruse/protocol-v2-1.pdf?sfvrsn=a9ef618c_2];
- ORF1b-nsp14, N [https://www.who.int/docs/default-source/coronaviruse/peiris-protocol-16-1-20.pdf?sfvrsn=af1aac73_4];
- S, N [https://www.who.int/docs/default-source/coronaviruse/method-niid-20200123-2.pdf?sfvrsn=fbf75320_7];
- N [https://www.who.int/docs/default-source/coronaviruse/conventional-rt-pcr-followed-by-sequencing-for-detection-of-ncov-rirl-nat-inst-health-t.pdf?sfvrsn=42271c6d_4];
- N [https://www.fda.gov/media/134922/download, https://www.who.int/docs/default-source/coronaviruse/uscdcrt-pcr-panel-primer-probes.pdf?sfvrsn=fa29cb4b_2];
- RdRP [https://www.who.int/docs/default-source/coronaviruse/real-time-rt-pcr-assays-for-the-detection-of-sars-cov-2-institut-pasteur-paris.pdf?sfvrsn=3662fcb6_2].
При этом, проведенный анализ полногеномных нуклеотидных последовательностей SARS-CoV-2 показал частое наличие мутаций (в особенности делеций) в геномах данного коронавируса. В связи с этим основным недостатком приведенных выше аналогов является риск получения ложно отрицательных результатов ОТ-ПЦР, обусловленных блокированием реакции при наличии мутаций в области амплифицируемого участка.
Из уровня техники известна комбинация праймера и зонда для обнаружения мутантных штаммов нового коронавируса, которая содержит праймеры с определенными нуклеотидными последовательностями и зонды с определенными нуклеотидными последовательностями. На основе комбинации праймера и зонда изобретение устанавливает способ обнаружения сайта мутации N501Y гена N и сайта мутации D614G гена N нового коронавируса на основе технологии ПЦР с наночастицами [Патент CN113278733, дата подачи 21.05.2021, дата публикации 20.08.2021]. Существенным недостатком данного решения является усложнение этапов пробоподготовки, кроме того, способ требует дополнительных затрат для обеспечения системы наночастицами.
Наборы, в которых предусмотрена мультиплексная ПЦР-РВ после проведения обратной транскрипции отличаются удобством для пользователя [1) The challenge of screening SARS-CoV-2 variants of concern with RT-qPCR: One variant can hide another. Jose Valter Joaquim Silva Junior, mgryd Merchioratto, Pablo Sebastian Britto de Oliveira, Thaisa Regina Rocha Lopes, Patricia Chaves Brites, Elehu Moura de Oliveira, Rudi Weiblen, Eduardo Furtado Flores, https://doi.org/10.1016/j.jviromet.2021.114248; 2) Rapid and simultaneous identification of three mutations by the Novaplex™ SARS-CoV-2 variants I assay kit. Wakaki Kami, Takeshi Kinjo, Wakako Arakaki, Hiroya Oki, Daisuke Motooka, Shota Nakamura, Jiro Fujita, https://doi.org/10.1016/i.icv.2021.104877; 3) Патент RU 2761025, 26.07.2021, 02.12.2021 4) Патент CN113817868, 08.07.2021, 21.12.2021; 5) Патент CN113215312, 28.04.2021, 06.08.2021; 6) Патент CN113005226, 07.02.2021, 22.06.2021; 7) Патент CN113278733, 21.05.2021, 20.08.2021]. Однако, использование данных наборов не предполагает быстрой возможности замены мишеней для детекции новых геновариантов, содержащих миссенс мутации или замены.
Детекция дополнительных специфичных для возникающих геновариантов мишеней, так же, как и исключение из анализа мишеней для циркулирующих геновариантов позволяет повысить эффективность лабораторного исследования в целом. В связи с этим существует потребность в разработке олигонуклеотидов для выявления мутации S:N501 Y как уникальной и значимой в эволюции вируса в биологических образцах с подтвержденным наличием РНК SARS-CoV-2. Разработка осуществляется за счет подбора праймеров и флуоресцентно-меченого зонда для проведения ПЦР-РВ.
Технический результат заявляемого изобретения направлен на выявление мутации S:N501Y в биологических образцах с подтвержденным наличием РНК SARS-CoV-2 с высокой степенью специфичности посредством олигонуклеотидов праймеров и флуоресцентно-меченого зонда, которые позволяют эффективно определять мутацию S:N501Y SARS-CoV-2 с использованием широко доступных методик и материалов.
Технический результат достигается за счет применения химически-синтезированных олигонуклеотидов для определения наличия мутации S:N501Y в биологическом образце с подтвержденным наличием РНК SARS-CoV-2, имеющих следующий олигонуклеотидный состав:
прямой праймер 501Ocv-F2 - SEQ ID NO: 1;
обратный праймер 1501cv-R - SEQ ID NO: 2;
флуоресцентный зонд 1501cv-Z - SEQ ID NO: 3.
Праймеры представляют собой последовательности олигонуклеотидов для амплификации фрагмента, содержащего мутацию S:N501Y в биологических образцах, с подтвержденным наличием РНК SARS-CoV-2. Флуоресцентно-меченый конформационно-блокированный зонд является олигонуклеотидом, содержащим флуорофор и гаситель флуоресценции, позволяющим детектировать амплифицированный фрагмент.
Заявляемые олигонуклеотиды разработаны на основе проведенного анализа последовательностей S-гена SARS-CoV-2, взятых из базы данных NCBI (https://www.ncbi.nlm.nih.gov/)), в результате которого выбран фрагмент для детекции мутации S:N501Y. К выбранному фрагменту были подобраны праймеры и зонд для амплификации 114 пар оснований: прямой праймер 501Ocv-F2 - SEQ ID NO: 1; обратный праймер 1501cv-R - SEQ ID NO: 2 и флуоресцентный зонд 1501cv-Z - SEQ ID NO: 3.
Заявляемое изобретение является результатом работы в рамках совершенствования молекулярно-генетического мониторинга вариантов вируса SARS-CoV-2, проведенной в ФБУН ЦНИИ Эпидемиологии Роспотребнадзора (Москва, Россия).
Для подбора целевых последовательностей - мест посадки олигонуклеотидов, используют фрагменты референсных геномов, взятые из базы данных NCBI (https://www.ncbi.nlm.nih.gov/), как SARS-CoV-2 дикого типа, так и тех геновариантов, в которых встречается мутация S:N501Y: Alpha (В.1.1.7), Beta (В.1.351), Gamma (P.1), Omicron (В.1.1.529), Mu (В.1.621), Theta (P.3), (В.1.640), (С.1.2). Для поиска консервативных участков последовательностей применяют современные алгоритмы in silico анализа нуклеотидных последовательностей и программы, находящиеся в открытом доступе, включая AlignX, SnapGene Viewer, MEGA, Unipro UGENE. Составляют перечень значимых мутаций, характерных для геновариантов. Затем подбирают олигонуклеотидные последовательности прямого и обратного праймеров, а также флуоресцентно-меченого зонда. Для детекции образцов, содержащих мутацию S:N501Y, используют канал для детекции флуорофора FAM. Упомянутые олигонуклеотидные последовательности приведены в Таблице 1.
Анализ заявляемых последовательностей с использованием ресурса Primer BLAST продемонстрировал, что прямой праймер 501Ocv-F2 (SEQ ID NO:l) и обратный праймер 1501cv-R (SEQ ID NO:2) амплифицируют участок, в котором располагается мутация S:N501Y со 100% специфичностью.
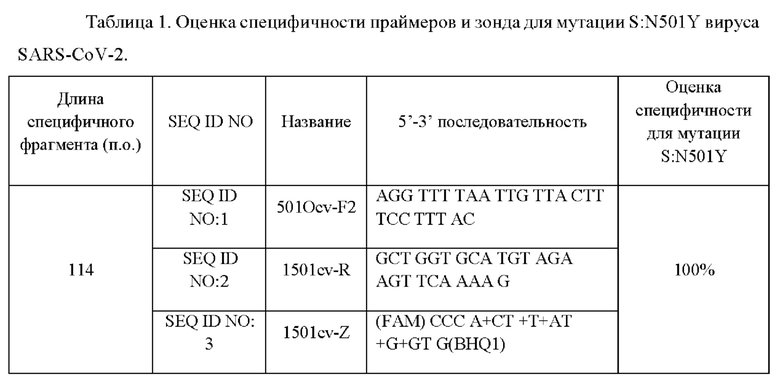
Где FAM - флуорофор, BHQ1 - гаситель флуоресценции, + перед нуклеотидом -модификация LNA.
В качестве биологического материала используются мазки/отделяемое носоглотки и ротоглотки, с подтвержденным наличием РНК SARS-CoV-2 (например, после проведения анализа на наборе реагентов АмплиСенс® COVID-19-FL).
Выделение РНК из биологического материала проводят в соответствии с МУ 1.3.2569-09 «Организация работ лабораторий, использующих методы амплификации нуклеиновых кислот при работе с материалом, содержащим микроорганизмы I-IV групп патогенности». Выделение РНК из биологического материала производят с помощью комплекта реагентов в соответствии с инструкцией производителя. Для выделения РНК может быть использован комплект реагентов «РИБО-преп» (ФБУН ЦНИИ Эпидемиологии Роспотребнадзора, Россия) или любой аналогичный набор для выделения РНК. Оптимальная концентрация РНК - 103 - 105 копий в 10 мкл. Реакцию обратной транскрипции (ОТ) проводят с помощью комплекта реагентов в соответствии с инструкцией производителя. Для проведения реакции ОТ может быть использован комплект реагентов «РЕВЕРТА-L» (ФБУН ЦНИИ Эпидемиологии Роспотребнадзора, Москва, Россия) или любой аналогичный набор. Готовый препарат кДНК может храниться при температуре от 2 до 8°С в течение недели, при температуре от минус 24 до минус 16°С в течение 6 мес.и при температуре не выше минус 68°С в течение года.
Полимеразная цепная реакция (ПЦР) - это эффективный способ получения in vitro большого числа копий специфических нуклеотидных последовательностей. Их амплификация осуществляется в ходе трехэтапного циклического процесса.
Процесс ПЦР-амплификации заключается в многократном повторении процессов денатурации, ренатурации и синтеза. Денатурация (95°С) - термическое воздействие на молекулу ДНК с целью получения одноцепочечной структуры. Ренатурация (55-60°С) - праймеры, добавленные в реакцию спариваются с разделенными цепями. Синтез (70-75°С) - синтез второй цепи ДНК. Каждый цикл длится 3-5 мин.
Анализ данных проводится на основе детекции амплификатором уровня флуоресцентного сигнала испускаемого интеркалирующим красителем. При увеличении числа копий анализируемого участка детектируется экспоненциальный рост флуоресцентного сигнала. В результате наблюдается S-образная кривая в случае наличия специфичного флуоресцентному зонду сигнала, или ее отсутствие, в случае неспецифичной для зонда последовательности. Анализ кривых позволяет судить об отсутствии или наличии мутации в исследуемых образцах.
ПЦР-РВ проводится с применением заявляемых, представленных в Таблице 1 олигонуклеотидов - праймеров и зонда, для детекции мутации S:N501Y SARS-CoV-2.
ПЦР-РВ проводят при следующих условиях:
Общий объем реакционной смеси - 25 мкл.
Компоненты ПЦР смешиваются следующим образом:
(а) 10 мкл смеси, содержащей:
- олигонуклеотидные праймеры SEQ ID NO: 1, SEQ ID NO: 2 - по 0,5 мМ;
- флуоресцентный зонд SEQ ID NO: 3-0,15 мМ;
- dNTPs - 0,44 мМ.
(b) реактив, содержащий рекомбинантный фермент Taq ДНК-полимеразу, например, 0,5 мкл «Полимераза TaqF» (ФБУН ЦНИИ Эпидемиологии Роспотребнадзора, Москва, Россия) или любой аналогичный коммерческий набор в соответствии с инструкцией производителя.
(c) ПЦР-буфер, содержащий MgCl2, например, 5,0 мкл ПЦР-буфера «ОТ-ПЦР-смесь-2 FEP/FRT» (ФБУН ЦНИИ Эпидемиологии Роспотребнадзора, Москва, Россия) или любого аналогичного коммерческого набора в соответствии с инструкцией производителя.
(d) полученная методом обратной транскрипции кДНК - 10 мкл. Амплификацию проводят на приборе с возможностью флуоресцентной детекции,
например, «Rotor-Gene Q» («Qiagen», Германия) или на любом другом приборе с 2-5 каналами детекции в соответствии с инструкцией производителя.
Амплификацию проводят по следующей программе: 1 цикл 95°С в течение 15 минут, 45 циклов при температуре 95°С - 10 секунд / 60°С - 20 секунд. Детекция флуоресценции проводится на этапе 60°С по каналу для флуорофора FAM.
Для анализа результатов задают пороговую линию, соответствующую величине 10% от среднего сигнала флуоресценции образца с наличием мутации S:N501Y. Образцы, для которых кривые флуоресценции пересекают пороговую линию, и, при этом кинетика накопления флуоресцентного сигнала является экспоненциальной, являются положительными, то есть содержат мутацию S:N501Y SARS-CoV-2.
Реализация заявляемого изобретения поясняется следующими примерами: Пример 1. Получение олигонуклеотидов для определения мутации S:N501Y SARS-CoV-2.
Для подбора последовательностей-мишеней - мест посадки олигонуклеотидов использованы фрагменты референсных геномов из базы данных NCBI (https://www.ncbi.nlm.nih.gov/) как SARS-CoV-2 дикого типа, так и тех геновариантов, в которых встречается мутация S:N501Y (Alpha (В.1.1.7), refseq MZ344997 (NCBI); Beta (B.1.1.351), refseq MW598419 (NCBI); Gamma (P.1), refseq MZ169911 (NCBI); Omicron (B.1.1.529), refseq OL672836 (NCBI) и другие). Для поиска мутаций использованы современные алгоритмы in silico анализа нуклеотидных последовательностей и программы, находящиеся в открытом доступе, включая AlignX, Unipro UGENE, олигокалькулятор (Oligo Calculators) Integrated DNA Technologies, Inc. (Oligo Analyzer (idtdna.com)). Был составлен перечень консервативных участков, характерных только мутации S:N501Y SARS-CoV-2, к которым подобраны олигонуклеотидные последовательности прямого 501Ocv-F2 и обратного 1501cv-R праймеров, а также флуоресцентный зонд 1501cv-Z.
Анализ упомянутых последовательностей с использованием ресурса Primer BLAST показал, что прямой 501Ocv-F2 и обратный 1501cv-R праймеры амлифицируют участок, в которой располагается мутация S:N501Y со 100% специфичностью.
Олигонуклеотиды для определения мутации S:N501Y SARS-CoV-2- прямой праймер 501Ocv-F2, обратный праймер 1501cv-R, флуоресцентный зонд 1501cv-Z, представлены уникальными последовательностями SEQ ID NO: 1, SEQ ID NO: 2 и SEQ ID NO: 3 соответственно.
Пример 2. Детекция мутации S:N501Y SARS-CoV-2 методом ПЦР-РВ.
Определение мутации S:N501Y SARS-CoV-2 проводят методом ПЦР-РВ при следующих условиях:
Общий объем реакционной смеси - 25 мкл.
Компоненты ПЦР смешиваются следующим образом:
(a) 10 мкл смеси, содержащей:
- олигонуклеотидные праймеры: SEQ ID NO: 1, SEQ ID NO: 2 по 0,5 мМ;
- флуоресцентный зонд: SEQ ID NO: 3-0,15 мМ;
- dNTPs - 0,44 мМ.
(b) 0,5 мкл реактива «Полимераза TaqF» (ФБУН ЦНИИ Эпидемиологии Роспотребнадзора, Россия), содержащего рекомбинантный фермент Taq ДНК-полимеразу.
(c) 5,0 мкл ПЦР-буфера «ОТ-ПЦР-смесь-2 FEP/FRT» (ФБУН ЦНИИ Эпидемиологии Роспотребнадзора, Россия), содержащего MgCl2.
(d) 10 мкл кДНК, полученной после реакции обратной транскрипции («РЕВЕРТА-L» ФБУН ЦНИИ Эпидемиологии Роспотребнадзора, Россия).
ПЦР-РВ проводили с флуоресцентной детекцией на приборе с 5 каналами детекции - «Rotor-Gene Q» («Qiagen», Германия).
Подготовленный описанным способом материал, содержащий уникальные олигонуклеотидные последовательности SEQ ID NO: 1-3, используют для определения мутации S:N501Y SARS-CoV-2 в образцах биологического материала.
Пример 3. Обнаружение мутации S:N501Y SARS-CoV-2 в образцах биологического материала.
Для определения мутации S:N501Y SARS-CoV-2 выбрано 96 образцов, с подтвержденным наличием РНК SARS-CoV-2.
Для исследования использовали клинический материал - мазки/отделяемое носоглотки и ротоглотки, содержащие РНК вируса SARS-CoV-2. Наличие РНК вируса SARS-CoV-2 подтверждено лабораторно с применением набора реагентов АмплиСенс® COVID-19-FL (ФБУН ЦНИИ Эпидемиологии Роспотребнадзора, Москва, Россия).
Выделение РНК из биологического материала проводили в соответствии с МУ 1.3.2569-09 «Организация работ лабораторий, использующих методы амплификации нуклеиновых кислот при работе с материалом, содержащим микроорганизмы I-IV групп патогенности». Выделение РНК осуществляли методом нуклеопреципитации с применением набора реагентов «РИБО-преп» (ФБУН ЦНИИ Эпидемиологии Роспотребнадзора, Москва, Россия) в соответствии с инструкцией к набору. Обратную транскрипцию проводили с применением набора реагентов «РЕВЕРТА-L» (ФБУН ЦНИИ Эпидемиологии Роспотребнадзора, Москва, Россия) в соответствии с инструкцией к набору.
ПЦР-РВ проводили в условиях, описанных в Примере 2, с использованием уникальных олигонуклеотидных последовательностей SEQ ID NO: 1-3.
Амплификацию проводили на приборе «ДТ-96» («ДНК-Технология», Россия) по следующей программе: 1 цикл 95°С в течение 15 минут, 45 циклов при температуре 95°С -10 секунд / 60°С - 20 секунд. Детекция флуоресценции проводилась на этапе 60°С по каналу для флуорофора FAM. Для анализа результатов задали пороговую линию, соответствующую величине 10% от среднего сигнала флуоресценции образца с наличием мутации S:N501Y. Для 94 образцов кривая флуоресценции пересекла пороговую линию и, при этом кинетика накопления флуоресцентного сигнала была экспоненциальной, что свидетельствует о том, что данные образцы содержат мутацию S:N501Y SARS-CoV-2.
Для данных 94 образцов наличие мутации S:N501Y SARS-CoV-2 подтверждено фрагментным секвенированием с использованием метода секвенирования по Сэнгеру. Фрагментное секвенирование выполнялось на генетическом анализаторе ABI 3500xL (Applied Biosystems, США), выравнивание и анализ полученных последовательностей выполнялось с помощью программы AlignX («Thermo Fisher Scientific)), США). Отсутствие мутации в 2 образцах без флуоресцентного сигнала также подтверждено фрагментным секвенированием.
Таким образом, из всей выборки выявлено 94 образца, содержащих мутацию S:N501Y SARS-CoV-2.
Пример 4. Обнаружение мутации S:N501Y SARS-CoV-2 в образцах биологического материала.
Для определения мутации S:N501Y SARS-CoV-2 выбрано 5 образцов, с подтвержденным наличием РНК SARS-CoV-2.
Для исследования использовали клинический материал - мазки/отделяемое носоглотки и ротоглотки, содержащие РНК SARS-CoV-2. Наличие РНК SARS-CoV-2 подтверждено лабораторно с применением набора реагентов АмплиСенс® COVTD-19-FL (ФБУН ЦНИИ Эпидемиологии Роспотребнадзора, Москва, Россия). Выделение РНК из биологического материала проводили в соответствии с МУ 1.3.2569-09 «Организация работ лабораторий, использующих методы амплификации нуклеиновых кислот при работе с материалом, содержащим микроорганизмы I-IV групп патогенности». Выделение РНК осуществляли методом нуклеопреципитации с применением набора реагентов «РИБО-преп» (ФБУН ЦНИИ Эпидемиологии Роспотребнадзора, Москва, Россия) в соответствии с инструкцией к набору. Обратную транскрипцию проводили с применением набора реагентов «РЕВЕРТА-L» (ФБУН ЦНИИ Эпидемиологии Роспотребнадзора, Москва, Россия) в соответствии с инструкцией к набору.
ПЦР-РВ проводили в условиях, описанных в Примере 2, с использованием уникальных олигонуклеотидных последовательностей SEQ ID NO: 1-3.
Амплификацию проводили на приборе «Rotor-Gene Q» («Qiagen», Германия) по следующей программе: 1 цикл 95°С в течение 15 минут, 45 циклов при температуре 95°С -10 секунд / 60°С - 20 секунд. Детекция флуоресценции проводилась на этапе 60°С по каналу для флуорофора FAM. Для анализа результатов задали пороговую линию, соответствующую величине 10% от среднего сигнала флуоресценции образца с наличием мутации S:N501Y. Для 4 образцов кривая флуоресценции пересекла пороговую линию и, при этом кинетика накопления флуоресцентного сигнала была экспоненциальной, что свидетельствует о том, что данные образцы содержат мутацию S:N501Y SARS-CoV-2.
Для данных 4 образцов наличие мутации S:N501Y SARS-CoV-2 подтверждено фрагментным секвенированием с использованием метода секвенирования по Сэнгеру. Фрагментное секвенирование выполнялось на генетическом анализаторе ABI 3500xL (Applied Biosystems, США), выравнивание и анализ полученных последовательностей выполнялось с помощью программы AlignX («Thermo Fisher Scientific)), США). Отсутствие мутации в 1 образце без флуоресцентного сигнала также подтверждено фрагментным секвенированием.
Таким образом, из всей выборки выявлено 4 образца, содержащих мутацию S:N501Y SARS-CoV-2.
Пример 5. Обнаружение мутации S:N501Y SARS-CoV-2 в образцах биологического материала.
Для определения мутации S:N501Y SARS-CoV-2 выбрано 15 образцов, с подтвержденным наличием РНК SARS-CoV-2.
Для исследования использовали клинический материал - мазки/отделяемое носоглотки и ротоглотки, содержащие РНК SARS-CoV-2. Наличие РНК SARS-CoV-2 подтверждено лабораторно с применением набора реагентов АмплиСенс® COVTD-19-FL (ФБУН ЦНИИ Эпидемиологии Роспотребнадзора, Москва, Россия). Выделение РНК из биологического материала проводили в соответствии с МУ 1.3.2569-09 «Организация работ лабораторий, использующих методы амплификации нуклеиновых кислот при работе с материалом, содержащим микроорганизмы I-IV групп патогенности». Выделение РНК осуществляли методом нуклеопреципитации с применением набора реагентов «РИБО-преп» (ФБУН ЦНИИ Эпидемиологии Роспотребнадзора, Москва, Россия) в соответствии с инструкцией к набору. Обратную транскрипцию проводили с применением набора реагентов «РЕВЕРТА-L» (ФБУН ЦНИИ Эпидемиологии Роспотребнадзора, Москва, Россия) в соответствии с инструкцией к набору.
ПЦР-РВ проводили в условиях, описанных в Примере 2, с использованием уникальных олигонуклеотидных последовательностей SEQ ID NO: 1-3.
Амплификацию проводили на приборе «Rotor-Gene Q» («Qiagen», Германия) по следующей программе: 1 цикл 95°С в течение 15 минут, 45 циклов при температуре 95°С -10 секунд / 60°С - 20 секунд. Детекция флуоресценции проводилась на этапе 60°С по каналу для флуорофора FAM. Для анализа результатов задали пороговую линию, соответствующую величине 10% от среднего сигнала флуоресценции образца с наличием мутации S:N501Y. Кривая флуоресценции не пересекла пороговую линию, что свидетельствовало о том, что в выборке отсутствуют образцы, содержащие мутацию S:N501Y SARS-CoV-2.
Наличие других мутаций SARS-CoV-2 в данных 15 образцах, а также отсутствие мутации S:N501Y подтверждено фрагментным секвенированием с использованием метода секвенирования по Сэнгеру. Фрагментное секвенирование выполнялось на генетическом анализаторе ABI 3500xL (Applied Biosystems, США), выравнивание и анализ полученных последовательностей выполнялось с помощью программы AlignX («Thermo Fisher Scientific)), США).
Заявляемое изобретение позволяет выявлять мутацию S:N501Y SARS-CoV-2 в биологических образцах с подтвержденным наличием РНК SARS-CoV-2. Синтезированные олигонуклеотиды SEQ ID NO NO: 1-3 не дают перекрестных реакций с другими протестированными образцами, амлифицируют заданный участок со 100% специфичностью и позволяют определять наличие или отсутствие в образцах биологического материала значимой мишени S:N501Y.
| название | год | авторы | номер документа |
|---|---|---|---|
| Олигонуклеотиды для определения мутации S:Ins214EPE SARS-CoV-2 | 2022 |
|
RU2795017C1 |
| Олигонуклеотиды для определения мутации S:delVYY143-145 SARS-CoV-2 | 2022 |
|
RU2795016C1 |
| Олигонуклеотиды для определения мутации S:L452R SARS-CoV-2 | 2022 |
|
RU2795018C1 |
| Олигонуклеотиды для определения мутации S:P681R SARS-CoV-2 | 2022 |
|
RU2795019C1 |
| Олигонуклеотиды для определения мутации S:delHV69-70 SARS-CoV-2 | 2022 |
|
RU2795014C1 |
| Способ выявления и количественного определения вируса SARS-COV-2 с помощью цифровой капельной ПЦР | 2024 |
|
RU2839700C1 |
| Способ генотипирования гена TLR8 по полиморфизму rs3764880 и набор олигонуклеотидных праймеров и зондов для его реализации | 2023 |
|
RU2805864C1 |
| Способ обнаружения РНК вируса SARS-CoV-2 в ультранизких концентрациях и специфические олигонуклеотиды для использования в способе | 2021 |
|
RU2764021C1 |
| Способ генотипирования гена TLR4 по полиморфизму rs4986790 и набор олигонуклеотидных праймеров и зондов для его реализации | 2023 |
|
RU2805862C1 |
| Способ обнаружения РНК вируса SARS-CoV-2 в ультранизких концентрациях и специфические олигонуклеотиды для использования в способе | 2021 |
|
RU2764022C1 |
Изобретение относится к области биотехнологии, к определению мутации S:N501Y SARS-CoV-2 методом полимеразной цепной реакции, проводимой в режиме реального времени. Описаны олигонуклеотиды для определения мутации S:N501Y SARS-CoV-2: прямой праймер 501Ocv-F2, обратный праймер 1501cv-R, флоуресцентный зонд 1501cv-Z, представленные уникальными последовательностями SEQ ID NO: 1-3 соответственно. При этом для создания прямого и обратного праймеров, флуоресцентного зонда используют фрагменты референсных геномов SARS-CoV-2 дикого типа, Alpha (В.1.1.7), Beta (В.1.351), Gamma (P.1), Omicron (B.1.1.529), Mu (В.1.621), Theta (Р.3), (В.1.640), (С.1.2). Синтезированные олигонуклеотиды SEQ ID NO NO: 1-3 не дают перекрестных реакций с другими протестированными образцами, амплифицируют заданный участок со 100% специфичностью и позволяют определять наличие или отсутствие в образцах биологического материала значимой мишени S:N501Y. 1 табл., 5 пр.
Набор праймеров и зонда определения мутации S:N501Y SARS-CoV-2, имеющий следующий состав:
прямой праймер 501Ocv-F2 - SEQ ID NO: 1;
обратный праймер 1501cv-R - SEQ ID NO: 2;
флуоресцентный зонд 1501cv-Z - SEQ ID NO: 3.
| Тест-система и способ для выявления РНК коронавируса SARS-COV-2, вируса-возбудителя коронавирусного заболевания 2019 COVID-19, методом полимеразной цепной реакции в режиме реального времени (Варианты) | 2020 |
|
RU2731390C1 |
| Тест-система на основе полимеразной цепной реакции с обратной транскрипцией для выявления SARS-CoV-2 линии Омикрон с определением субварианта BA.1 | 2022 |
|
RU2779025C1 |
| CN 111455114 A, 28.07.2020. | |||
Авторы
Даты
2023-03-14—Публикация
2022-10-06—Подача