Изобретение относится к медицине, а именно к экспериментальной хирургии, и может быть использовано для оптимизации восстановления костной ткани после оперативного лечения деструктивных поражений скелета туберкулезной этиологии.
Основой хирургического лечения костно-суставного туберкулеза является радикальная резекция деструктивных очагов в пределах здоровых тканей [1-3]. Большие пострезекционные полости, особенно, опорных (нижних) конечностей требуют пластического заполнения, для чего обычно используются имплантаты соответствующего размера [4, 5]. Цель костной пластики заключается в максимально полном восстановлении кости без формирования остаточной полости, заполненной рубцовой тканью [6].
Наиболее часто для костной пластики используют костные трансплантаты или небиологические резорбируемые материалы, которые в условиях послеоперационной адаптации подвергаются закономерным биологическим процессам, первой фазой которых является остеолизис -резорбция, которая в условиях исходного инфекционного процесса может быть достаточно выраженной или полной. При этом даже нормально текущий процесс адаптации имплантата в больших костных дефектах требует большего времени для восстановления и, следовательно, иммобилизации и ограничения осевой нагрузки на пораженный сегмент, что ухудшает условия реваскуляризации и остеогенеза, замедляя процессы остеорегенерации.
Одним из методов регуляции костеобразования после радикально-восстановительных операций может являться торможение активности остеокластов, обеспечивающих остеорезорбцию как один из начальных механизмов репаративной остеорегенерации. Указанным действием селективно обладают бисфосфонаты - препараты на основе пирофосфата, обладающие не только эффектом торможения дифференцировки остеокластов из предшественников, но и противовоспалительной активностью [7,8]. Бисфосфонаты используют при лечении как системных генетических заболеваний - первичный [9] и вторичный остеопороз [10], так и при очаговых поражениях костной ткани - кистах, метастазах литических опухолей, небактериальном остеомиелите [11-14]. В Российской Федерации наиболее часто у детей из бисфосфонатов применяется памидроновая кислота [15].
Памидроновая кислота (памидронат) - является препаратом, применяемым с первых недель жизни при несовершенном остеогенезе, ее эффективность и безопасность изучена в течение более чем 25 лет при данном заболевании, применение памидроната включено в соответствующие клинические рекомендации. Памидронат также используется для лечения небактериального остеомиелита у детей и купирования болевого синдрома при костных метастазах у взрослых и детей.
Задачей предлагаемого изобретения является разработка способа стимулирования остеорегенерации после оперативного лечения туберкулезного остита в эксперименте.
Задача реализуется тем, что кроликам на фоне противотуберкулезной терапии проводят резекцию деструктивных очагов в пределах здоровых тканей, заполняют операционный дефект пластическим материалом, затем после заживления операционной раны однократно вводят внутривенно раствор памидроновой кислоты из расчета 1 мг на кг массы животного.
Предлагаемый способ регуляции остеорегенерации после оперативного лечения туберкулезного остита в эксперименте является новым, ранее данные по стимулированию восстановления костной ткани после оперативного лечения деструктивных поражений скелета туберкулезной этиологии не публиковались.
Технический результат способа: выраженный остеолизис трансплантатов и более продолжительный индуцированный остеогенез. Способ поясняется графическим материалом, где: Фиг. 1. Динамика массы тела кроликов.
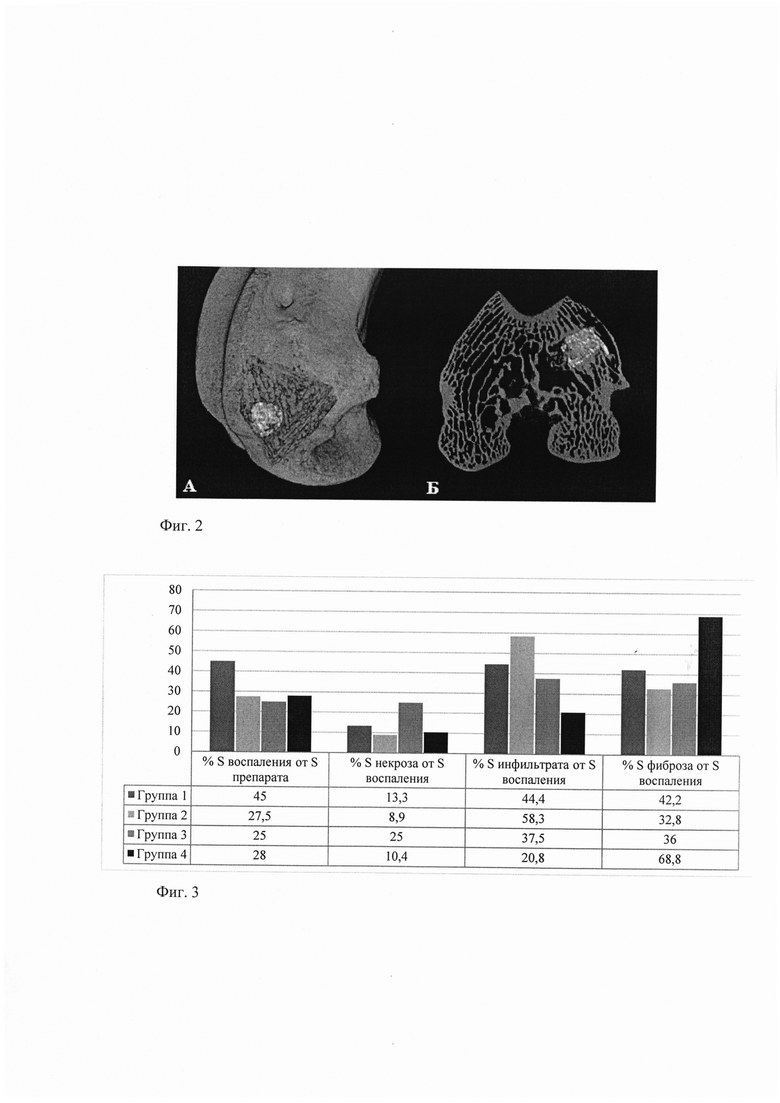
Фиг. 2. Зона имплантации образца группы №4, 6 месяцев наблюдения. А - реконструированное изображения, Б - КТ-срез. Визуализируется имплантат в медиальном мыщелке правой бедренной кости кролика неоднородной плотности, с включениями CaSo4, прорастающий костными балками.
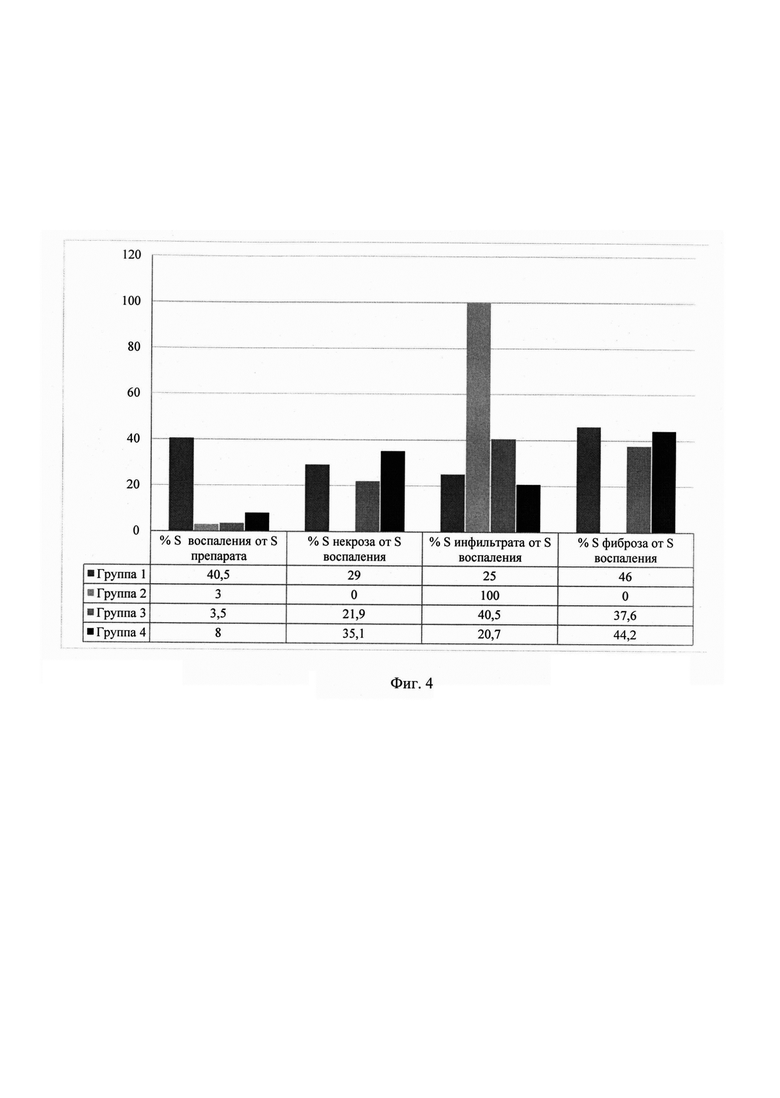
Фиг. 3. Характер и распространенность специфического воспаления, Me, 3 месяца наблюдения.
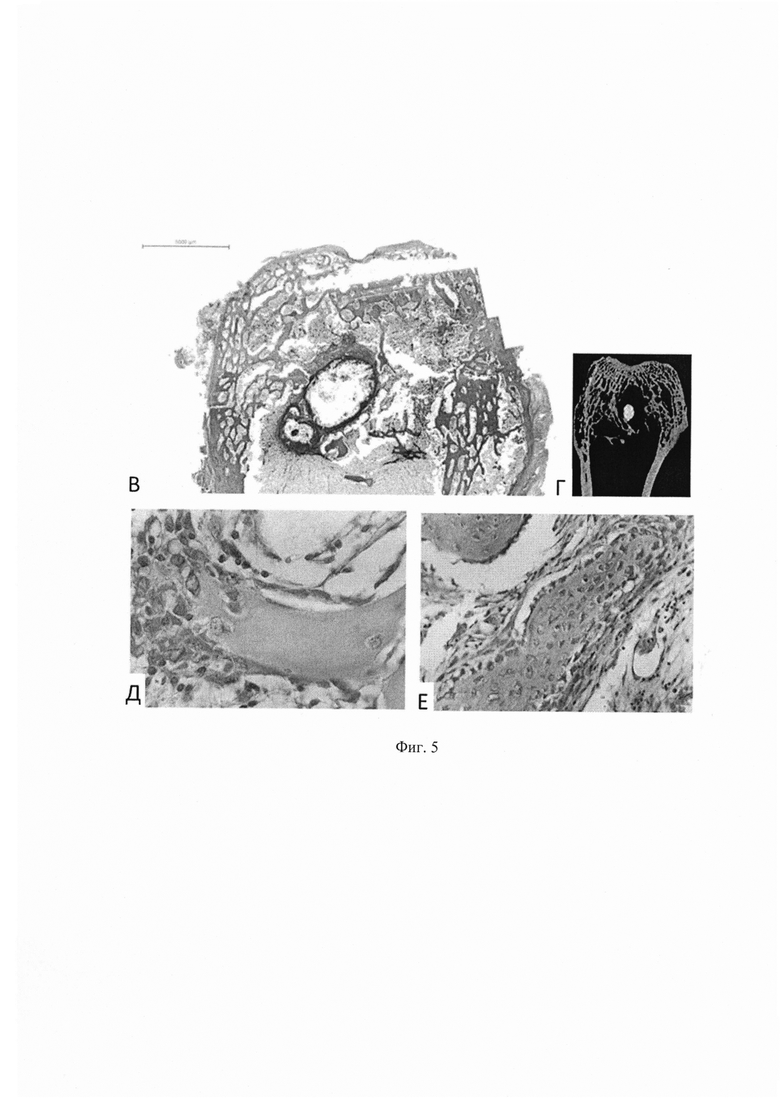
Фиг. 4. Характер и распространенность специфического воспаления, Me, 6 месяцев наблюдения.
Фиг. 5. Очаг неспецифического воспаления вокруг гранул имплантата с балками с активными остеобластами, гематоксилин-эозин (В
- препарат эпифиза, Г - КТ-изображение, Д, Е - препарат эпифиза, ув. 1000х).
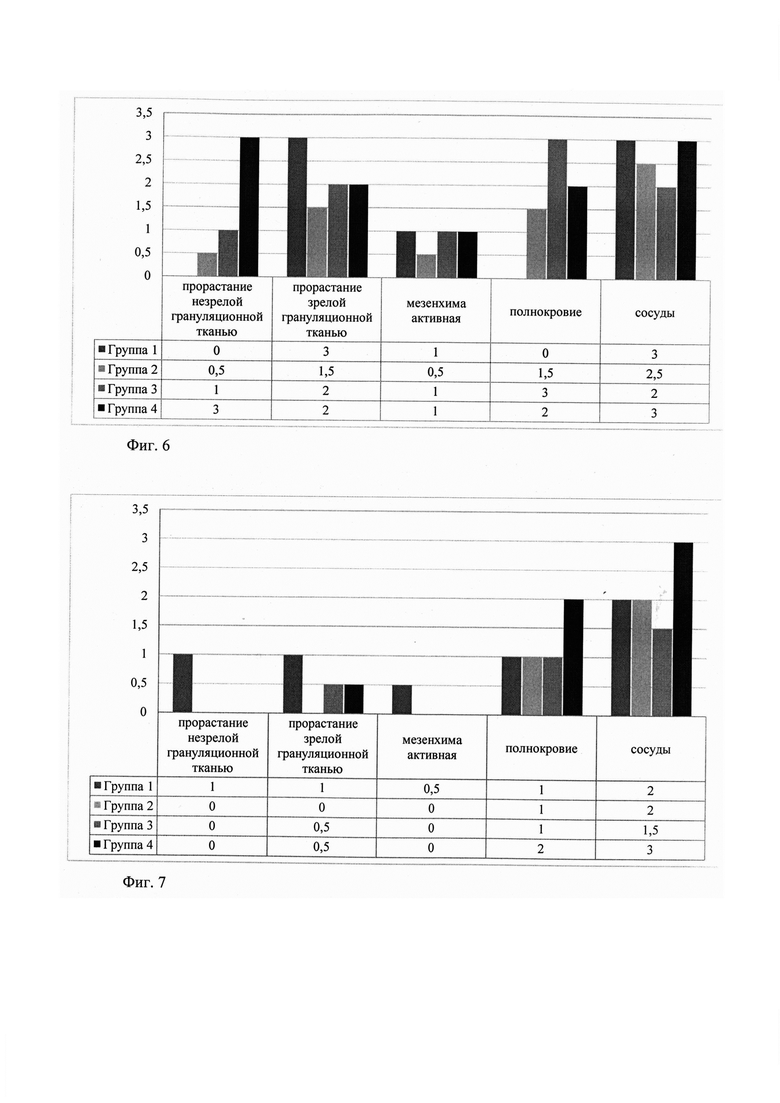
Фиг. 6. Паттерны регенеративного остеогенеза, баллы (0-3), Me, 3 месяца наблюдения.
Фиг. 7. Паттерны регенеративного остеогенеза, баллы (0 - 3), 6 месяцев наблюдения.
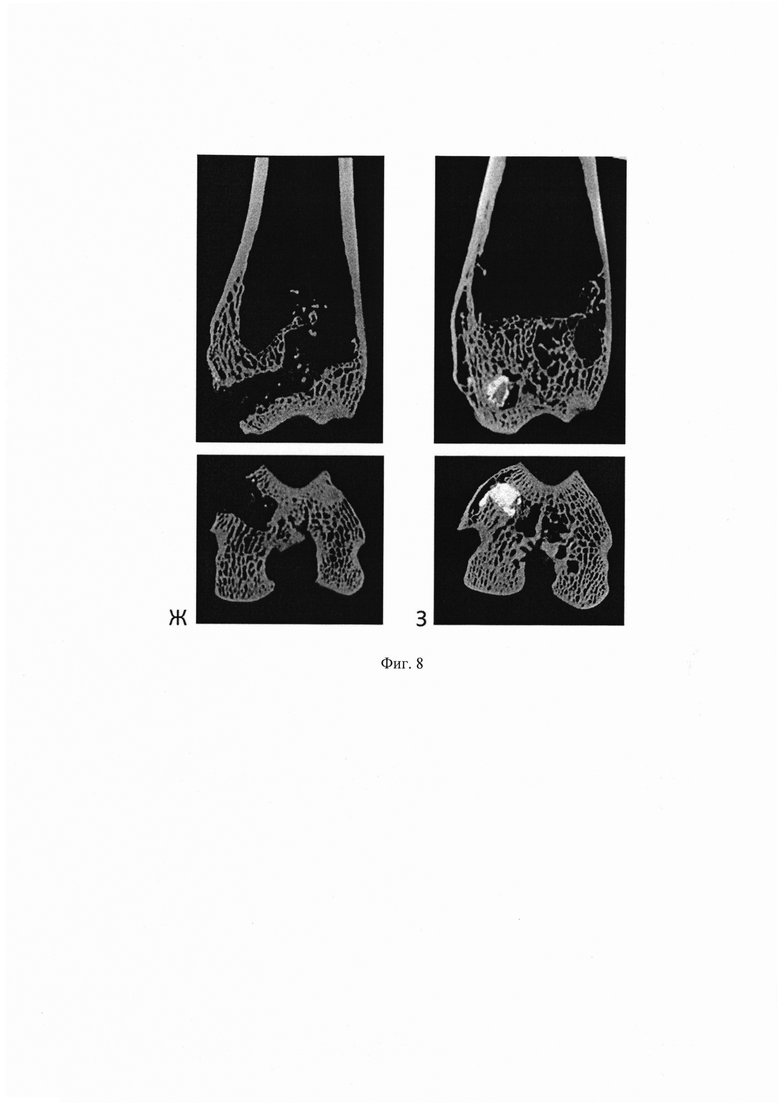
Фиг. 8. Пример бальной оценки КТ-признаков остеорегенерации и остеолизиса. Препарат Ж: визуализация имплантата в эпифизе - 0 баллов, прорастание имплантата костными балками - 0 баллов, структурность костных балок - 1 балл, структурность эпифизарной пластинки - 1 балл, формирование кортикальной замыкательной пластинки в месте трепанации - 0 баллов; костные полости - 2 балла, микросеквестры - 2 балла.
Препарат 3: визуализация имплантата в эпифизе - 2 балла, прорастание имплантата костными балками - 2 балла, структурность костных балок - 2 балла, структурность эпифизарной пластинки - 2 балла, формирование кортикальной замыкательной пластинки в месте трепанации - 2 балла; костные полости - 0 баллов, микросеквестры - 0 баллов.
Экспериментальные исследования проведены в федеральном государственном бюджетном учреждении «Санкт-Петербургский научно-исследовательский институт фтизиопульмонологии» Министерства здравоохранения Российской Федерации на 21 кролике-самце породы «Советская шиншилла». Создание модели туберкулезного остита в медиальном мыщелке правой бедренной кости кроликов выполнено согласно ранее разработанному и запатентованному методу [16] в модификации. В качестве инфекционного агента использован трехнедельный лекарственно-чувствительный референсный штамм Mycobacterium tuberculosis H37Rv. В ходе эксперимента, после моделирования костного очага специфического воспаления и подтверждения развития туберкулезного процесса, в т.ч. на основании положительных кожных проб с аллергеном туберкулезным рекомбинантным «Диаскинтест», животные были разделены на группы в зависимости от предпринятого хирургического и варианта последующего медикаментозного лечения:
группа 1 (контроль заражения, n=3) - кролики с моделированным туберкулезным оститом, не получавшие противотуберкулезную терапию (ПТТ) и не подвергавшиеся оперативному лечению;
группы 2-4 - кролики с моделированным туберкулезным оститом, которым после развития специфического очага туберкулезного остита назначалась противотуберкулезная терапия (ПТТ) в объеме изониазид 10 мг/кг, этамбутол и пиразинамид - по 20 мг/кг per os. Затем выполнялась некрэктомия полости деструкции с заполнением операционного дефекта гранулами пластического материала Osteoset®2DBM Pellets. Дальнейшее дифференцирование групп осуществлялось с учетом варианта лечения, в т.ч.:
… группа 2 (п=4 кролика) - ПТТ продолжалась до завершения эксперимента;
… группа 3 (п=7) - через 10 дней после операции однократно на фоне продолжающейся ПТТ вводилась памидроновая кислота в дозировке 1 мг/кг внутривенно медленно;
… группа 4 (п=7) - на 10 сутки после операции однократно введена памидроновая кислота с одновременной отменой дальнейшего проведения ПТТ.
Доза препарата для памидроната составила 1 мг/кг, препарат разводился раствором NaCL 0,9% до достижения концентрации менее 90 мг/250 мл, вводился внутривенно капельно медленно со скоростью инфузии не более 1 мг/мин. Максимальная доза препарата не должна превышать 90 мг.
Наблюдение за лабораторными животными осуществлялось на сроке 3 и 6 месяцев после хирургического лечения.
После эвтаназии, осуществленной в соответствии с требованиями, изложенным в Рекомендациях Европейской комиссии по эвтаназии и указанным в ГОСТ 33215-2014, всем животным для аутопсии проводили забор правой бедренной кости (зона операции); кроликам, выведенным из эксперимента через 6 месяцев, также проводили забор и левой (интактной) бедренной кости. Извлеченные образцы костей фиксировали в 10% растворе нейтрального забуференного формалина (рН 7,4).
Оценка состояния модельных животных проводилась на основании следующих критериев:
- потребления воды и продуктов питания;
- периодического (в начале исследования и перед выполнением основных этапов - заражение, операция, выведение) мониторинга динамики массы тела животных с использованием электронных весов модели AdventurerTM, точность взвешивания ±0,1 г.
- физической активности (хорошая/снижена);
- заживления операционной раны (первичным натяжением/ вторичным натяжением);
- осложнений операционной раны (абсцессы, гематомы -есть/нет); хромота (есть/нет).
… оценки эффективности модели туберкулезного остита (Диаскинтест, ГТПР-диагностика (положительный/отрицательный результат)).
В динамике в сыворотке крови оценивали наиболее часто используемые маркеры процессов остеогенеза: концентрации общей щелочной фосфатазы, альбумина, остеокальцина, β-Crosslaps, RANKL, склеростина. Забор крови осуществляли из краевой ушной вены в дебюте исследования, через 6 недель после заражения и в послеоперационном периоде - через 10 дней, 3 и 6 месяцев.
Количественной и качественная оценка в аутопсийном материале зоны имплантации, контралатерального мыщелка правой бедренной кости, а также медиального мыщелка левой бедренной кости (лучевые исследования проводились с использованием микротомографа Skyscan 1172 (Bruker) при размере пикселя 13 и 27 мкм) проводились по следующим параметрам:
- оптическую плотность костной ткани оценивали в единицах Хаунсфилда в программе-просмотрщике медицинских лучевых данных RadiAnt DICOM Viewer на площади 0,001 см2;
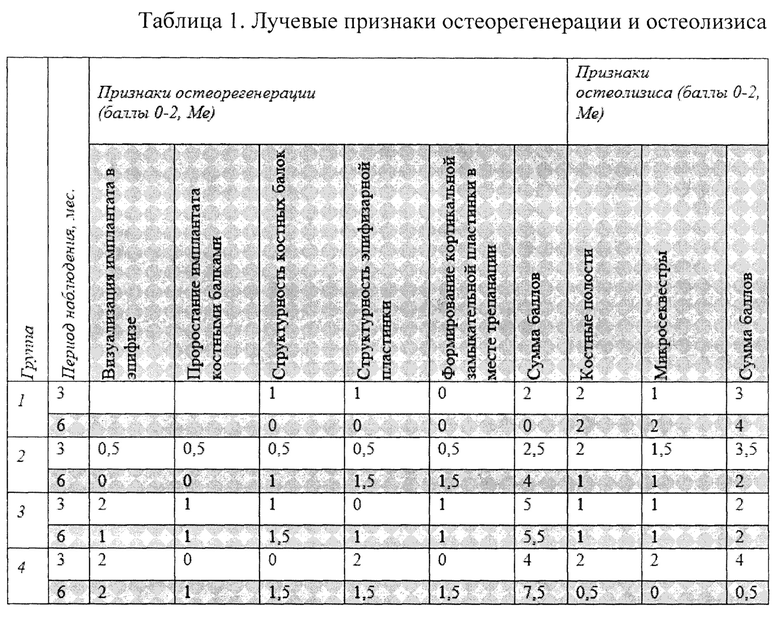
В соответствии с разработанной авторами условной качественно-количественной шкалой оценены пять признаков, характеризующих остеорегенерацию и два признака остеолизиса. Признаками остеорегнерации считали: сохранение визуализации и прорастание имплантата костными балками, восстановление структуры кортикальной замыкательной и эпифизарной пластинок, структурность костных балок; остеолизиса - наличие костных полостей и микросеквестров. В зависимости от выраженности признака присваиваются баллы от от 0 до 2, где 0 - признак отсутствует, 1 - умеренно выражен, 2 - ярко выражен:
1. Визуализация имплантата в эпифизе: не визуализируется - 0 баллов, визуализируются мелкие фрагменты имплантата до 0,5 см3 - 1 балл, визуализируются фрагменты имплантата более 0,5 см3 - 2 балла;
2. Прорастание имплантата костными балками: отсутствует - 0 балов, визуализируется частично - 1 балл, визуализируется на всем протяжении - 2 балла;
3. Структурность костных балок: костные балки бесструктурны на площади более 50% эпифиза - 0 баллов, структура костных балок сохранена на 50% - 90% площади эпифиза- 1 балл, структура костных балок сохранена более чем на 90% площади эпифиза;
4. Структурность эпифизарной пластинки: эпифизарная пластинка не визуализируется или визуализируется на площади менее 50% - 0 баллов, эпифизарная пластинка визуализируется на площади 50%-90% - 1 балл, эпифизарная пластинка визуализируется на площади более 90% - 2 балла;
5. Формирование кортикальной замыкательной пластинки в месте трепанации: отсутствует - 0 баллов, признаки формирования с наличием дефектов - 1 балл, полностью сформирована - 2 балла;
6. Костные полости: занимают более 20% площади эпифиза - 2 балла, занимают 10 - 20% площади эпифиза - 1 балл, отсутствуют или занимают до 10% - 0 баллов;
7. Микросеквестры: множественные - 2 балла; единичные (до 5 на срезе 1 мм) - 1 балл, отсутствуют - 0 баллов.
При сумме баллов признаков остеорегенерации от 7 до 10 констатируется выраженная регенерация костной ткани, при сумме баллов признаков остеолизиса от 2 до 4 - активный лизис костной ткани.
Стандартное гистологическое исследование микропрепаратов и морфологический анализ воспалительных и регенераторных процессов в тканях выполняли по изготовленным по стандартной методике и окрашенным гематоксилином и эозином и по методу Циля-Нельсена препаратам, а также по оцифрованным на сканере Pannoramic изображениям препаратов с использованием программ анализа изображений Orbit Image Analysis и Pannoramic Viewer.
Описательным методом оценивали:
- распространенность, степень/ выраженность/ стадию специфического инфильтрата (в баллах от 0 до 5);
- наличие КУМ (в баллах от 0 до 3);
- формирование очагов распада, явлений организации, фиброза, наличие перифокального воспаления (есть, нет);
- толщина фиброзной капсулы (в баллах от 0 до 3);
- дистрофические и регенераторные изменения костной ткани (есть, нет);
- структурность формирования костных балок в зоне образованной костной мозоли (есть, нет).
Морфометрическим методом в 10 полях зрения при увеличении х1000 выполняли оценку:
- количества и распределения клеток, характеризующих остеорегенерацию и ремодуляцию (остеобласты, остеокласты, остеоциты);
- зрелость костной ткани в очаге поражения (активность остеобластов и остеоцитов, зрелость грануляционной ткани,
фиброз, мезенхима, вновь образованные балочные структуры, секвестры) - в баллах от 0 до 3. Морфометрический анализ в программе Orbit Image Analysis и Pannoramic Viewer оценивал:
- параметры площадей костной ткани (% от площади кости);
- параметры площадей специфического воспаления с разделением на зоны некроза, инфильтрата и фиброза (% от площади кости и % от площади всего воспаления);
- толщину костных балок (мкм) в эпифизарной части дистальных участков бедренных костей.
Полученные данные подвергали статистической обработке методами вариационной статистики при помощи программ Microsoft Exel и STATISTICA 10 с определением показателей среднего значения (М), доверительного интервала (р), различия считали достоверными при р<0,07. Для сравнения выборок использовали непараметрические критерии Краскела-Уоллиса и Манна-Уитни для независимых выборок. Корреляционный анализ выполнен с помощью коэффициента корреляции Пирсона.
Эффективность способа иллюстрируют следующие результаты:
не зарегистрированы летальные исходы, нежелательные реакции на введение ПТТ и БФ. Заживление операционной раны происходило первичным натяжением. Все животные, кроме одного из группы контроля (генерализация туберкулезной инфекции) к моменту выведения находились в удовлетворительном состоянии;
прирост массы тела отмечен у всех кроликов в пределах от 4,8 до 15,3% за весь период наблюдения (Фиг. 1). При этом, в группах 3 и 4, получавших памидроновую кислоту, отмечены максимальные весовые прибавки, составившие в группе 3+15,3% за весь период наблюдения и +10,6% от момента хирургического лечения до окончания эксперимента (р=0,04); в группе 4 -+7,7% и +10,6%, за аналогичные периоды.
отличительными лучевыми признаками групп 3 и 4 является сохранение изображения имплантата в 85,7-100% случаев даже при наличии костных полостей, а также его прорастание костными балками (Фиг. 2) (для сравнения - в группе 2 имплантат на сроке наблюдения 3 мес.определяется лишь в 50% случаев, на сроке 6 мес. - ни в одном препарате не просматривается);
нарастание суммы баллов признаков, характерных для остеорегенерации, в динамике отмечается среди всех получавших лечение группах (2-4). На сроке 3 месяца их минимальные значения определяются в группе 2 (2,5 баллов), максимальные - в группе 3. При этом на сроке 6 месяцев в группе 4 имеются максимальные значения паттернов остеорегенерации (7,5 баллов) и минимальные - остеолизиса (0,5 балла) (табл. 1);
проявления специфического воспаления максимально отмечаются в группах 2-4 на 3 месяце наблюдения и занимают от 10% до 50% площади эпифиза, в т.ч. КУМ обнаружены в большинстве очагов (Фиг. 3). На фоне ПТТ, БФ и их комбинации к 6 мес.отмечена значительная положительная динамика в виде нивелирования специфического воспаления в 50-75% случаев (Фиг. 4).
Характерной гистологической особенностью групп 3 и 4 является:
обнаружение стромальных тяжей, представленных фибробласто-фиброцитоподобными клетками, коллагеновыми структурами, которые отходят лучами от зон остаточного воспаления (вокруг гранул имплантата); увеличенное количество полнокровных сосудов в этих зонах. На костных балках увеличено количество активных остеобластов (Фиг. 5);
наличие признаков активного ремоделирования костной ткани в зоне воспаления, имеющей больше грануляционной ткани, активной мезенхимы и полнокровных сосудов на сроке 3 месяца (Фиг. 6). На сроке 6 месяцев наибольшее количество грануляционной ткани и полнокровных сосудов отмечено в группе 4 (Фиг. 7);
при оценке соотношений плотности имплантата, количества остеокластов в зоне воспаления и средним на препарат определяется сильная отрицательная корреляция (коэффициент Пирсона - 1) на сроке 3 месяца между группами 2, 3 и 4, и на сроке 6 месяцев - между группами 2 и 4.
Таким образом, комплексный анализ результатов морфометрического исследования позволяет сделать вывод о наличии в препаратах групп 3 и 4 (животные, получавшие памидроновую кислоту) как менее выраженного остеолизиса трансплантатов, так и более продолжительного индуцированного остеогенеза.
Источники информации:
1. Фтизиатрия: национальное руководство / под ред. М.И. Перельмана. - Москва: ГЭОТАР-Медиа, 2007. - 512 р.
2. Хирургическое лечение костно-суставного туберкулеза / под ред. Ю.Н. Левашева, А.Ю. Мушкин. - Санкт-Петербург, 2008.
3. Внелегочный туберкулез: руководство для врачей / под ред. Н.А. Браженко. - Санкт-Петербург: СпецЛит, 2013. - 395 с.
4. Сердобинцев М.С., Кафтырев А.С., Луцкая О.Л., Лобач В.Ю. Пластика костных дефектов в хирургии туберкулеза костей и суставов (экспериментальное исследование) // Сборник научных трудов по итогам международной научно-практической конференции. - Новосибирск, 2015. - С. 162-164.
5. Байдарбеков М.У., Нурахметов А.А., Оспанов К.Т., Кожаков А.С. Эволюция клеточных технологий в лечении нарушений репаративной регенерации костной ткани длинных трубчатых костей (обзор литературы) // Вестник Казахского Национального медицинского университета. - 2021. - №3.- С. 360-366.
6. Алаторцев А.В. Ортопедические последствия туберкулезных оститов у детей: возможность прогноза и эффективность хирургического лечения: дис …канд. мед. наук. - Санкт-Петербург, 2006.
7. Петухова В.В., Мушкин А.Ю., Костик М.М. Применение бисфосфонатов при костной патологии у детей (систематический обзор) // Медицинский альянс.- 2021. - Т. 9, №3. - С. 59-70.
8. Antoniazzi F., Mottes М., Fraschini P., Brunelli P.C., Tat L. Osteogenesis imperfecta: practical treatment guidelines // Paediatric Drugs. - 2000. - Vol. 2, №6. - P. 465-488.
9. Lindahl K., Kindmark A., Rubin C.-J., Malmgren В., Grigelioniene G., Soderhall S., Ljunggren O., Astrom E. Decreased fracture rate, pharmacogenetics and BMD response in 79 Swedish children with osteogenesis imperfecta types I, III and IV treated with Pamidronate // Bone. - 2016. - Vol. 87. - P. 11-18.
10. Кенис B.M., Сапоговский A.B., Прокопенко Т.Н., Бергалиев А.Н., Иванов С.В., Киселева Т.И. Динамика среднесрочных показателей остеоденситометрии у пациентов с детским церебральным параличом и SpinaBifida, получавших терапию ибандроновой кислотой // Ортопедия, травматология и восстановительная хирургия детского возраста. - 2020. - Vol. 8, №2. - С. 129-136.
11. Biggin A., Zheng L., Briody J.N., Соогеу С.Р., Munns C.F. The long-term effects of switching from active intravenous bisphosphonate treatment to low-dose maintenance therapy in children with osteogenesis imperfecta // Hormone Research in Paediatrics. - 2015. - Vol. 83, №3. - P. 183-189.
12. Cornelis F., Trachetet M.E., Amoretti N., Verdier D., Fournier C., Pillet O., Gille O., Hauger O. Bisphosphonate therapy for unresectable symptomatic benign bone tumors: A long-term prospective study of tolerance and efficacy // Bone. - 2014. - Vol..58. - P. 11-16.
13. McQuade M., Houghton K. Use of bisphosphonates in a case of perthes disease // Orthopaedic. Nursing. - 2005. - Vol..24, №6. - P. 393-398.
14. Schnabel A., Range U., Hahn G., Berner R., Hedrich C.M. Treatment response and longterm outcomes in children with chronic nonbacterial osteomyelitis // The Journal of Rheumatology. - 2017. - Vol. 44, №7. - P. 1058-1065.
15. The peculiarities and treatment outcomes of the spinal form of chronic non-bacterial osteomyelitis in children: a retrospective cohort study / M.M. Kostik, O.L. Kopchak, A.S. Maletin, A.Y. Mushkin // Rheumatology International. - 2020. - Vol.40, №1. - P. 97-105.
16. Патент №2421823 С1 Российская Федерация, МПК G09B 23/28. Способ моделирования туберкулезного остита различной степени тяжести: №2009140048/14: заявл. 29.10.2009: опубл. 20.06.2011 / Васильева С.Н., Кафтырев А.С., Виноградова Т.Н. [и др.]; заявитель СПб НИИФ.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ МОДЕЛИРОВАНИЯ ТУБЕРКУЛЕЗНОГО ОСТИТА РАЗЛИЧНОЙ СТЕПЕНИ ТЯЖЕСТИ | 2009 |
|
RU2421823C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ ТУБЕРКУЛЕЗНОГО ОМАРТРИТА | 2003 |
|
RU2265891C2 |
| Способ диагностики остеомиелита у детей | 2016 |
|
RU2651091C1 |
| СПОСОБ СОЗДАНИЯ МОДЕЛИ СЕГМЕНТАРНОГО ОСТЕОНЕКРОЗА МЫЩЕЛКОВ, СОСТАВЛЯЮЩИХ КОЛЕННЫЙ СУСТАВ У ЖИВОТНЫХ | 2004 |
|
RU2269824C2 |
| БИОЛОГИЧЕСКИ АКТИВНОЕ СРЕДСТВО, ОБЛАДАЮЩЕЕ ЛОКАЛЬНЫМ ПРОТИВОВОСПАЛИТЕЛЬНЫМ ДЕЙСТВИЕМ ПРИ АДЪЮВАНТНОМ АРТРИТЕ | 2021 |
|
RU2771567C1 |
| СПОСОБ ВЫБОРА ТАКТИКИ ЛЕЧЕНИЯ ОСТРОГО ГЕМАТОГЕННОГО ОСТЕОМИЕЛИТА У НОВОРОЖДЕННЫХ | 2008 |
|
RU2378990C1 |
| СПОСОБ ЛЕЧЕНИЯ БОЛЕЗНИ ОСГУДА-ШЛАТТЕРА | 2015 |
|
RU2599202C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ СТЕПЕНИ ЗАМЕЩЕНИЯ ОПЕРАЦИОННОЙ ПОЛОСТИ ПРИ ТУБЕРКУЛЕЗНЫХ ОСТИТАХ У ДЕТЕЙ МЛАДШЕГО ВОЗРАСТА | 2007 |
|
RU2374991C2 |
| КОМПОЗИЦИЯ - ОСТЕОИНДУКТОР И ОСТЕОКОНДУКТОР, ПРИ ЛЕЧЕНИИ КОСТНОЙ ПАТОЛОГИИ В СТОМАТОЛОГИИ И ЧЕЛЮСТНО-ЛИЦЕВОЙ ХИРУРГИИ, И СПОСОБ ПОЛУЧЕНИЯ КОМПОЗИЦИИ - ОСТЕОИНДУКТОРА И ОСТЕОКОНДУКТОРА, ПРИ ЛЕЧЕНИИ КОСТНОЙ ПАТОЛОГИИ В СТОМАТОЛОГИИ И ЧЕЛЮСТНО-ЛИЦЕВОЙ ХИРУРГИИ | 2008 |
|
RU2383564C1 |
| БИОСОВМЕСТИМАЯ КОМПОЗИЦИЯ ДЛЯ ВОСПОЛНЕНИЯ (ЛЕЧЕНИЯ) ЧАСТИЧНЫХ И ПОЛНЫХ ДЕФЕКТОВ ХРЯЩЕВОЙ И КОСТНОЙ ТКАНИ И СПОСОБ ПОЛУЧЕНИЯ БИОСОВМЕСТИМОЙ КОМПОЗИЦИИ ДЛЯ ВОСПОЛНЕНИЯ (ЛЕЧЕНИЯ) ЧАСТИЧНЫХ И ПОЛНЫХ ДЕФЕКТОВ ХРЯЩЕВОЙ И КОСТНОЙ ТКАНИ | 2008 |
|
RU2385727C1 |

Изобретение относится к медицине, а именно к экспериментальной хирургии, и может быть использовано для оптимизации восстановления костной ткани после оперативного лечения деструктивных поражений скелета туберкулезной этиологии. Кроликам после радикально-восстановительного хирургического вмешательства после заживления операционной раны однократно вводят памидроновую кислоту в дозе 1 мг/кг внутривенно. Способ обеспечивает торможение лизиса имплантата, более продолжительный индуцированный остеогенез и неоангиогенез в зоне костной резекции за счет введения памидроновой кислоты. 8 ил., 1 табл.
Способ стимулирования остеорегенерации после оперативного лечения туберкулезного остита в эксперименте, отличающийся тем, что кроликам на фоне противотуберкулезной химиотерапии проводят резекцию деструктивных очагов в пределах здоровых тканей, заполняют операционный дефект пластическим материалом, затем после заживления операционной раны однократно вводят внутривенно раствор памидроновой кислоты из расчета 1 мг на кг массы животного.
| RU 2776787 C1, 26.07.2022 | |||
| ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ОСТЕОНЕКРОЗА И ДЛЯ ЛЕЧЕНИЯ ПАЦИЕНТОВ С РИСКОМ РАЗВИТИЯ ОСТЕОНЕКРОЗА | 2001 |
|
RU2284821C2 |
| Способ моделирования асептического аминобисфосфонатного остеонекроза нижней челюсти у лабораторных белых крыс | 2016 |
|
RU2653627C1 |
| СПОСОБ ЛЕЧЕНИЯ КОСТНЫХ НАРУШЕНИЙ | 2002 |
|
RU2294203C2 |
| Петухова В.В., Мушкин А.Ю., Костик М.М | |||
| Способ регенерирования сульфо-кислот, употребленных при гидролизе жиров | 1924 |
|
SU2021A1 |
| - Т | |||
| Разборный с внутренней печью кипятильник | 1922 |
|
SU9A1 |
| - С | |||
| Устройство для охлаждения водою паров жидкостей, кипящих выше воды, в применении к разделению смесей жидкостей при перегонке с дефлегматором | 1915 |
|
SU59A1 |
| Antoniazzi F., Mottes М., Fraschini P., Brunelli P.C., Tat L | |||
Авторы
Даты
2023-03-22—Публикация
2022-12-22—Подача