Изобретение относится к области аналитической химии, а именно к способам сорбционного концентрирования и разделения неполярных веществ, таких как фосфатидилхолин и α-токоферол, для последующего их определения в растительных образцах, фармацевтических препаратах. Способ сорбционного концентрирования и разделения неполярных веществ включает сорбционное извлечение фосфолипидов и токоферолов пропусканием их смеси через наноструктурированный мезопористый кремнезем, синтезированный с добавками фосфатидилхолина.
Синтез мезопористых материалов проведен темплатным методом, предполагающим, что упорядоченная структура кремнезема сформирована на поверхности гексагональных цилиндрических мицелл бромида цетилтриметиламмония (CTABr). Особенностью используемого в работе кремнезема является то, что в раствор CTABr добавляется фосфотидилхолин, влияющий на структуру и размер мицелл. Молекулы фосфолипидов с дифильной структурой, обладая сходными с бромидом цетилтриметиламмония физико-химическими свойствами способны влиять на мицеллообразование темплата. Использование молекул аналита (фосфатидилхолина) в качестве добавок к темплату способствует улучшению сорбционных характеристик, получаемых мезопористых материалов. Добавки фосфатидилхолина на этапе формирования золя кремниевой кислоты приводят к увеличению селективности кремнезема по отношению к одному из сорбатов. В качестве источника кремния использован тетраэтоксисилан (TEOS).
Разделение близких по свойствам неполярных веществ α-токоферола и фосфатидилхолина осуществлено в динамических условиях на хроматографической колонке, заполненной синтезированным кремнеземом с молекулярными отпечатками фосфолипида. Хроматографическую колонку заполняют мезопористым сорбентом, предварительно фракционированным до размера частиц 0.1-0.25 мм. Молекулярный импринтинг приводит к увеличению эффективности хроматографического разделения фосфатидилхолина и α-токоферола. Аналоги изобретения.
Известен способ [Garcira-Martirnez J., Brugarolas P., Domirnguez-Domirnguez S. Ordered circular mesoporosity induced by phospholipids / J. Garcira-Martirnez, P. Brugarolas, S. Domirnguez-Domirnguez // Microporous and Mesoporous Materials - 2007 - №100. - P. 63-69] синтеза мезопористых материалов в присутствии лецитина. В этом исследовании бромид цетилтриметиламмония (CTABr) и L-α-фосфатидилхолин (лецитин) были использованы в качестве темплата. Было показано, что для небольших концентраций лецитина, полученные материалы с охраняют характеристику гексагональной упорядоченности пор МСМ-41, о чем свидетельствуют результаты рентгеновской дифракции электронов и микроскопии. Поры синтезированных материалов при этом не прямые и параллельные как у МСМ-41, а круговые и концентрические. Однако в данной работе не были изучены сорбционные свойства материала и возможность его использования для выделения и разделения веществ.
В работе [  El Haskouri J.,
El Haskouri J.,
 Solid-phase extraction of phospholipids using mesoporous silica nanoparticles: application to human milk samples /
Solid-phase extraction of phospholipids using mesoporous silica nanoparticles: application to human milk samples /  E.F.
E.F.  // Analytical and Bioanalytical Chemistry. - 2018. - №410. - V. 20. - P. 4847-4854] были получены материалы мезопористого кремнезема с бимодальными системами пор, кремнезем МСМ-41. Данные материалы применялись как сорбенты в твердофазной экстракции для выделения фосфолипидов. В указанной работе отсутствуют данные о сорбции фосфолипида в динамических условиях на хроматографических колонках. Не рассматривается возможность использования кремнезема для хроматографического разделения близких по физико-химическим свойствам веществ, в том числе неполярных органических веществ. Не рассматривается эффект добавок одного из сорбатов на стадии синтеза материала на селективность кремнезема при сорбции веществ в условиях фронтальной хроматографии.
// Analytical and Bioanalytical Chemistry. - 2018. - №410. - V. 20. - P. 4847-4854] были получены материалы мезопористого кремнезема с бимодальными системами пор, кремнезем МСМ-41. Данные материалы применялись как сорбенты в твердофазной экстракции для выделения фосфолипидов. В указанной работе отсутствуют данные о сорбции фосфолипида в динамических условиях на хроматографических колонках. Не рассматривается возможность использования кремнезема для хроматографического разделения близких по физико-химическим свойствам веществ, в том числе неполярных органических веществ. Не рассматривается эффект добавок одного из сорбатов на стадии синтеза материала на селективность кремнезема при сорбции веществ в условиях фронтальной хроматографии.
В работе [Динамика сорбции фосфатидилхолина мезопористыми композитами на основе МСМ-41/ Л.А. Синяева, Н.А. Беланова, С.И. Карпов, В.Ф. Селеменев F. Roessner, // Журнал физической химии. - 2016. - Т. 90. - №11. - С. 1701-11709] изучены сорбционные свойства мезопористых композитов на основе МСМ-41 при сорбции фосфатидилхолина из гексановых растворов. Показано, что структурированные мезопористые материалы обладают высокой адсорбционной емкостью по отношению к исследуемому фосфолипиду. В данной работе изучена сорбция веществ в динамических условиях (при фронтальной хромато графии). Однако при этом не проводилось сорбционно-хроматографическое разделение биологически активных веществ (α-токоферола, фосфатидилхолина) мезопористыми сорбентами, синтезированными в присутствии гелевого компонента. Не рассмотрена конкурентная сорбция близких по физико-химическим свойствам веществ. Не выявлялся эффект влияния молекулярного импринтинга фосфолипида на эффективность хроматографического разделения α-токоферола и фосфатидилхолина.
Из работы [Сафонова Е.Ф. Выделение и изучение фосфолипидов масла семян амаранта. / Автореферат дисс.на соиск. уч. степ.канд. хим. наук. - М., 2004 г.], взятого за прототип, известен способ разделения фосфолипидного комплекса (ФЛК). В работе методом переменных концентраций были установлены сорбционные емкости некоторых ионогенных и неионогенных сорбентов по отношению к фосфатидилхолину (ФХ). Показано, что наибольшей сорбционной емкостью обладают сорбенты КРС-2П, АВ-17-2П и неионогенный сорбент Стиросорб. Хроматографирование проводили в следующих условиях: колонки стеклянные 15×0.9 см, длина сорбционного слоя 10 см, температура 20°С, хлороформно-этанольный (1:10) раствор ФЛК с концентрацией 3 г/л объемом 0.1 л; скорость пропускания 0.5 мл/мин. Однако в данной работе не приведены данные о сорбционном концентрировании фосфатидилхолина, не рассматривается разделение фосфатидилхолина с другими неполярными веществами другого класса, в том числе токоферолами, не рассматривались мезопористые материалы и мезопористые материалы с молекулярными отпечатками типа МСМ-41 как сорбенты для сорбционного извлечения и разделения фосфолипидов.
Изобретение обеспечивает хроматографическое разделение близких по свойствам "а-токоферола и фосфатидилхолина на синтезированных с молекулярными отпечатками фосфатидилхолина мезопористых материалах типа МСМ-41.
Задачей данного изобретения является разработка способа сорбционного концентрирования фосфатидилхолина и хроматографического разделения фосфатидилхолина и α-токоферола из гексановых растворов сорбционно-хроматографическим методом на материале типа МСМ-41, синтезированным в присутствии фосфатидилхолина.
Технический результат заключается в разработке способа разделения фосфатидилхолина и α-токоферола мезопористым сорбентом, обеспечивающего повышение эффективности хроматографического разделения фосфатидилхолина и α-токоферола из гексановых растворов на кремнеземе, синтезированном темплатным методом в присутствии фосфатидилхолина в 20-30 раз по сравнению с классическим силикагелем и в 1,3 раза с мезопористым материалом, синтезированном без добавки фосфатидилхолина.
Различие в селективности мезопористого материала, определяет возможность хроматографического разделения близких по природе веществ (α-токоферола и фосфатидилхолина). Возрастание сродства к фосфолипиду и увеличение эффективности колонки, заполненной упорядоченным кремнеземом при разделении рассматриваемых сорбатов (фиг. 6) обеспечивается молекулярным импринтингом фосфолипида с меньшим размыванием сорбционного фронта на кривой сорбции.
Технический результат достигается тем, что в способе разделения фосфатидилхолина и α-токоферола мезопористым сорбентом, включающем пропускание бинарного раствора сорбатов через хроматографическую колонку, заполненную сорбентом, согласно изобретению, хроматографическую колонку заполняют мезопористым сорбентом MkPh, синтезированным в присутствии фосфатидилхолина, при мольном соотношении компонентов 132.06H2O:1.33NH3:1.0TEOS:0.11CTABr:0.011 фосфатидилхолин; для разделения фосфатидилхолина и α-токоферола сорбент фракционируют до размера частиц 0.1-0.25 мм; высота слоя сорбента составляет 3 см; диаметр колонки равен 0.5 см; через хроматографическую колонку пропускают гексановый бинарный раствор фосфатидилхолина и α-токоферола с концентрациями 2.0⋅10-3 моль/дм3, скорость пропускания раствора 0.5 см3/мин; разделение ведут при 25°С, раствор пропускают до того момента, когда концентрация элюата будет равна концентрации исходного раствора.
Решение задачи достигается синтезом наноструктурированного кремнезема с молекулярными отпечатками фосфатидилхолина, что обеспечивает дифференциацию скоростей массопереноса сорбатов и определяет возможность их хроматографического разделения, а именно более ранний проскок менее сорбируемого компонента (α-токоферола) и более поздний выход фосфатидилхолина.
На фиг. 1 представлена схема синтеза мезопористых материалов.
На фиг. 2 приведены изотермы низкотемпературной адсорбции/десорбции азота (77 К) мезопористых материалов: 1 - ММС-1; 2-MkPh.
На фиг. 3 в таблице 1 приведены значения поверхностных и объемных характеристик мезопористых материалов ММС-1 и MkPh, определенных методом адсорбции/десорбции азота.
На фиг. 4 приведены рентгеновские дифрактограммы образцов мезопористых материалов: 1 - ММС-1; 2 - MkPh. На дифрактограмме мезопористых материалов ММС-1, MkPh присутствует интенсивный пик с рефлексом 2.0 (100) и два максимума меньшей интенсивности при 3.8 (110), 4.4 (200), характеризующие гексагональную структуру мезопор материалов.
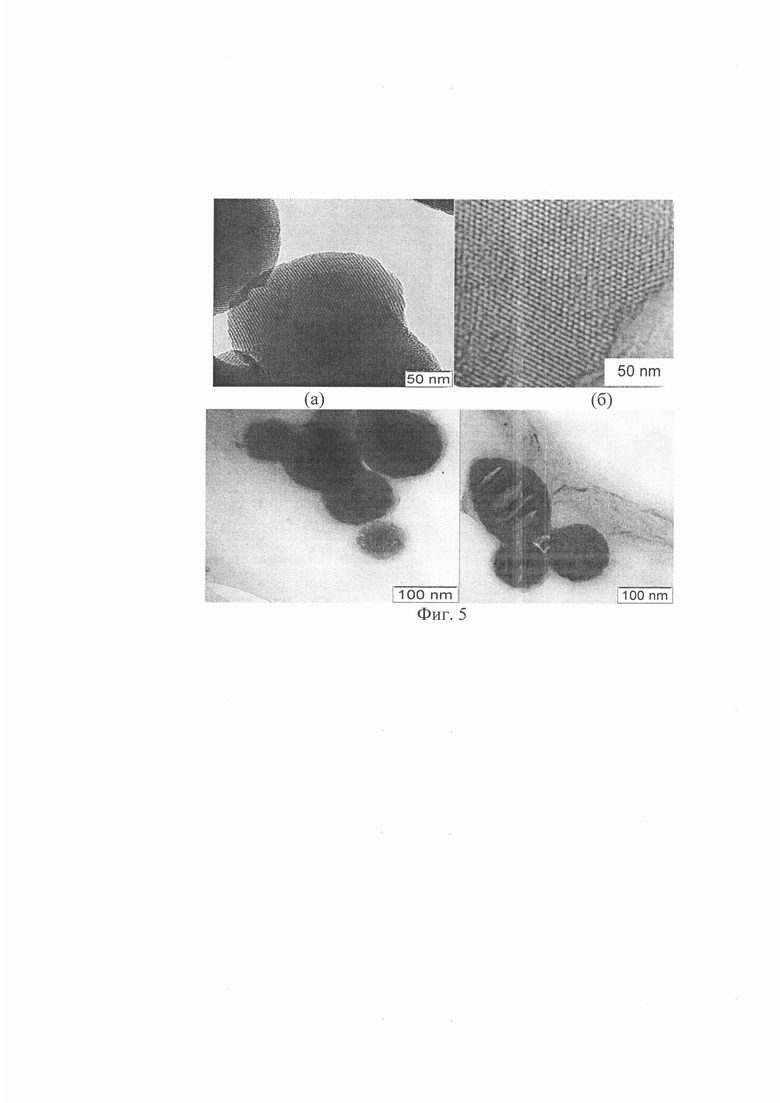
На фиг. 5 приведены микрофотографии просвечивающей электронной микроскопии (ПЭМ) высокого разрешения упорядоченного мезопористого материала MkPh в продольном (а) и поперечном (б) сечениях.
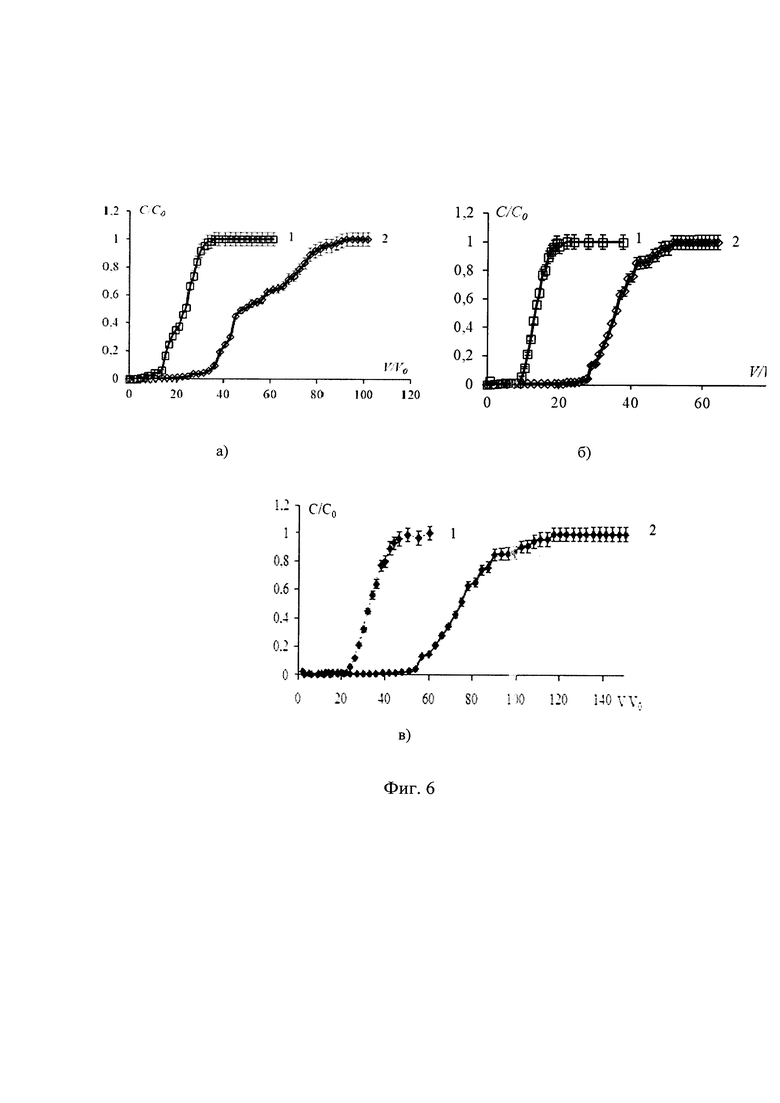
На фиг. 6 приведены выходные кривые сорбции фосфатидилхолина и α-токоферола из гексановых растворов (скорость пропускания раствора U=0.5 см3/мин, масса сорбента m=0.35 г, С0, С - исходная и равновесная концентрация фосфатидилхолина и α-токоферола, соответственно, моль/дм3, V0, V - объем сорбента и элюата, соответственно, см3, где а - силикагель, б - мезопористый материал ММС-1, в - мезопористый материал, синтезированный в присутствии целевого компонента - фосфатидилхолина - MkPh).
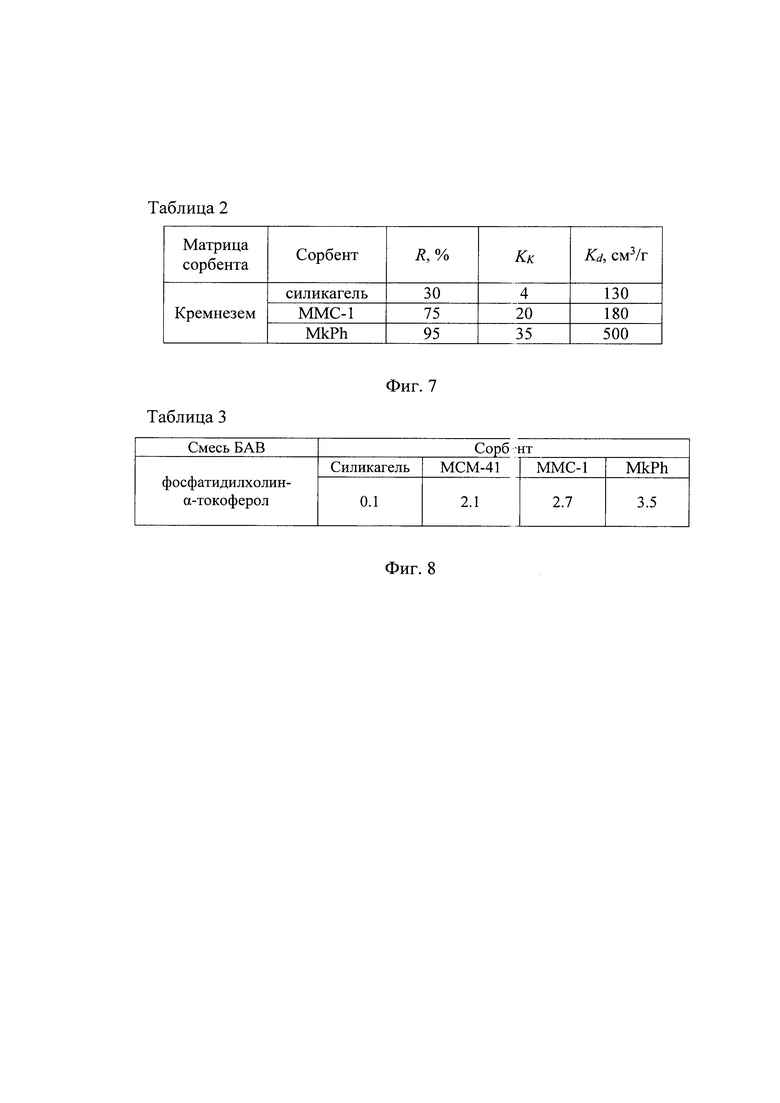
На фиг. 7 приведена таблица 2 значений с епени извлечения R (%), коэффициента концентрирования KK и коэффициента распределения Kd (см3/г) фосфатидилхолина на мезопористых сорбентах ММС-1 и MkPh.
На фиг. 8 приведена таблица 3 значений разрешения хроматографических зон (Rs) бинарных смесей фосфатидилхолина и α-токоферола из гексановых растворов при их сорбции различными сорбентами.
Синтез мезоструктурированного материала ММС-1 (аналог МСМ-41) проводился согласно способу, описанному в патенте РФ 2287485 (опубл. 20.11.2006) в спиртово-аммиачной реакционной среде при мольном соотношении компонентов: 1.0TEOS:0.2CTABr:21.0NH3:50.0C2H5OH:475.0H2O. При подготовке реакционной смеси навеску CTABr растворяли в водно-спиртовом растворе при рН=12.5 (регулировалось добавлением аммиака). По окончании гомогенизации в раствор бромида цетилтриметиламмония (CTABr) вносили тетраэтоксисилан (TEOS) - (C2H5O)4Si. Осаждение и первичная конденсация продукта проводились при интенсивном перемешивании в течение 2 ч при T=298 K. Конденсированный продукт вместе с маточным раствором помещали в пропиленовую емкость для проведения дальнейшей гидротермальной обработки при температуре 393 K при непрерывном вращении автоклава. После гидротермальной обработки осадок отфильтровывался, сушился в комнатных условиях при температуре T=295±2 K. Удаление темплата проводилось термостатированием при температуре 823 K в течение 6 часов.
Синтез мезопористых материалов в присутствии целевого компонента - фосфатидилхолина (MkPh) проводили согласно [  H. М.,
H. М., I., El Haskouri J.,
I., El Haskouri J.,  P.,
P.,  E.F., Herrero-
E.F., Herrero- J.M. Solid-phase extraction of phospholipids using mesoporous silica nanoparticles: application to human milk samples / H.M.
J.M. Solid-phase extraction of phospholipids using mesoporous silica nanoparticles: application to human milk samples / H.M.  I. Ten-
I. Ten- J. El Haskouri, P.
J. El Haskouri, P.  E.F.
E.F.  J. Manuel Herrero-
J. Manuel Herrero- // Analytical and Bioanalytical Chemistry. - 2018. - №410. - V. 20. - P. 4847-4854]. 0.3 г фосфатидилхолина (95% L-α-phosphatidylcholine, «Sigma-Aldrich»)) смешивали с раствором, содержащем 4.77 г аммиака (33 мас. %),
// Analytical and Bioanalytical Chemistry. - 2018. - №410. - V. 20. - P. 4847-4854]. 0.3 г фосфатидилхолина (95% L-α-phosphatidylcholine, «Sigma-Aldrich»)) смешивали с раствором, содержащем 4.77 г аммиака (33 мас. %),
1.39 г CTABr и 80 мл деионизированной воды. В полученную реакционную смесь добавляли 7.0 г TEOS. Смесь выдерживали при температуре 25°С. Мольное соотношении компонентов смеси для синтеза: 132.06Н2О:1.33NH4OH:1.0TEOS:0.11CTABr:0.011 фосфатидилхолин. Твердые вещества отфильтровывали через 24 часа через бумажный фильтр «синяя лента», промывали дистиллированной водой до отсутствия в промывных водах CTABr и сушили на воздухе до постоянной массы. Конечный материал прокаливали при температуре 823 K в течение 1 часа. Схема синтеза мезопористых материалов представлена на фиг. 1.
Для оценки изменения текстурных характеристик мезопористых сорбентов был использован метод низкотемпературной адсорбции/десорбции азота. Экспериментальные кривые низкотемпературной адсорбции/десорбции азота для мезопористых сорбентов (1 - ММС-1, 2 -MkPh) относятся к IV-ому типу (по классификации IUPAC). Вид изотерм для синтезированных образцов мезопористых материалов ММС-1, MkPh (фиг. 2) указывает на получение упорядоченных материалов с объемными характеристиками, обуславливающими высокую сорбционную способность. Данные материалы имеют упорядоченную структуру, аналогичную МСМ-41. Для мезопористого материала MkPh наблюдается гистерезис и капиллярная конденсация возникает при более высоких значениях относительных давлений р/р0=0.75. В таблице 1 приведены значения поверхностных и объемных характеристик мезопористых материалов ММС-1 и MkPh, определенных методом адсорбции/десорбции азота.
Для подтверждения сохранения высокоупорядоченной гексагональной структуры мезопор синтезированные образцы в присутствии целевого компонента - фосфатидилхолина (MkPh) анализировали методом рентгеноструктурного анализа (фиг. 4).
Анализ синтезированных мезопористых материалов (ММС-1, MkPh), проведенный с использованием просвечивающей электронной микроскопии (ПЭМ) высокого разрешения (фиг. 5) подтверждает сделанные предположения о получении высокоупорядоченного наноструктурированного материала. Результаты ПЭМ показывают, что система пор и каналов синтезированного сорбента в присутствии целевого компонента MkPh состоит из параллельных трубок, имеющих гексагональное строение.
Пример 1
Силикагелем заполняют колонки. Диаметр колонки d=0.5 см. Высота слоя сорбента 3.0 см. Через колонку пропускают гексановый бинарный раствор α-токоферола (С0=2.0⋅10-3 моль/дм3) и фосфатидилхолина (С0=2.0⋅10-3 моль/дм3). Скорость пропускания раствора 0.5 см3/мин, масса сорбента m=0.35 г, t=25°С, V/V0=110. Выходные кривые сорбции представлены на фиг. 6а (1 - α-токоферол, 2 - фосфатидилхолин).
Пример 2
Мезопористый ММС-1 получают по методике, описанной выше. Сорбентом заполняют колонки. Диаметр колонки d=0.5 см. Высота слоя сорбента 3.0 см. Через колонку пропускают гексановый бинарный раствор α-токоферола (С0=2.0⋅10-3 моль/дм3) и фосфатидилхолина (С0=2.0⋅10-3 моль/дм3). Выходные кривые сорбции представлены на фиг. 6б (1 - α-токоферол, 2 - фосфатидилхолин). Скорость пропускания раствора 0.5 см3/мин, масса сорбента m=0.35 г, t=25°C, V/V0=70.
Пример 3
Мезопористый кремнезем с молекулярными отпечатками фосфатидилхолина (MkPh) получают по методике, описанной выше. Мезопористым сорбентом заполняют колонки. Диаметр колонки d=0.5 см. Высота слоя сорбента 3.0 см. Через колонку пропускают гексановый бинарный раствор α-токоферола (С0=2.0⋅10-3 моль/дм3) и фосфатидилхолина (С0=2.0⋅10-3 моль/дм3). Выходные кривые сорбции представлены на фиг.6 (1 - α-токоферол, 2 - фосфатидилхолин). Скорость пропускания раствора 0.5 см3/мин, масса сорбента m=0.35 г, t=25°С, V/V0=130.
Изобретение обеспечивает повышение коэффициентов концентрирования (Кк) при сорбционном концентрировании фосфатидилхолина и α-токоферола и хроматографическом разделении их смеси (фиг. 7).
При выборе условий сорбционно-хроматографического процесса предполагается оптимизация коэффициента концентрирования Кк, влияющего на данный процесс:
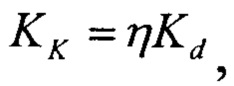
где η - доля полной емкости сорбента, использованная к моменту окончания концентрирования.
Применение упорядоченных материалов типа МСМ-41 позволяет значительно повысить коэффициенты концентрирования (Кк) по сравнению с традиционными кремнеземами. На мезопористых композитах на основе МСМ-41 (ММС-1, MkPh) достигается 20-50 кратное концентрирование фосфатидилхолина по сравнению с исходной концентрацией С0 фосфолипида в растворе.
Для количественного описания разделения компонентов рассчитано разрешение хроматографических зон (фиг. 8) с применением выражения, характеризующего разрешение хроматографических зон:
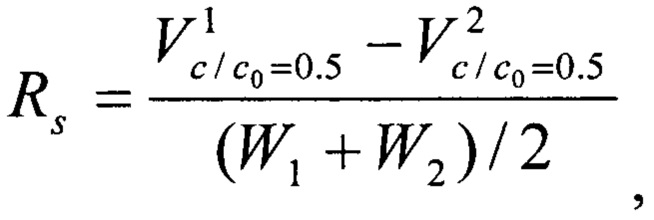
где  и
и 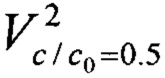 - объем раствора, пропущенного до с/с0=0.5 наиболее и менее сорбируемого компонента соответственно, дм3;
- объем раствора, пропущенного до с/с0=0.5 наиболее и менее сорбируемого компонента соответственно, дм3;
W1 и W2 - ширина хроматографической зоны (ширина пика у основания при переходе к дифференциальной зависимости), дм3.
Изучение сорбции биологически активных веществ в динамических условиях мезопористыми материалами типа МСМ-41 показало их преимущество по сравнению с традиционными неупорядоченными кремнеземами. На мезопористых материалах типа МСМ-41 (ММС-1, MkPh) благодаря меньшему размыванию фронта сорбции достигается удовлетворительное разрешение хроматографических зон (фиг. 8).
При использовании исследуемых мезоструктурированных сорбентов при хроматографическом разделении α-токоферола и фосфатидилхолина наблюдается увеличение разрешения в ряду силикагель <МСМ-41<ММС-1<MkPh, что свидетельствует о применимости наноструктурированных кремнеземов МСМ-41, ММС-1 и MkPh в процессах сорбционного концентрирования фосфолипидов и фитостеролов.
Мезопористые материалы эффективны в процессах хроматографического разделения смесей, содержащих молекулы фосфатидилхолина и α-токоферола. Синтетические мезопористые кремнеземы ММС-1 и MkPh позволяют достигать высокого разрешения зон разделяемых компонентов (RS>1.5), что обеспечивает выделение фосфатидилхолина в чистом виде. Использование синтезированных мезопористых сорбентов с молекулярными отпечатками фосфолипида при разделении фосфатидилхолина и α-токоферола позволяет увеличивать разрешение хроматографических зон сорбатов.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ КОНЦЕНТРИРОВАНИЯ И РАЗДЕЛЕНИЯ ФЛАВОНОИДОВ | 2016 |
|
RU2646805C1 |
| СПОСОБ ФРАКЦИОНИРОВАНИЯ КОМПЛЕКСА БИОФЛАВОНОИДОВ ОБЛЕПИХОВОГО ШРОТА | 2020 |
|
RU2759297C1 |
| Способ оценки избирательности активных центров сорбента при сорбционной очистке сточных и технологических вод | 2018 |
|
RU2691141C1 |
| Сорбент для извлечения ионов переходных металлов из растворов и хроматографии | 1987 |
|
SU1437776A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ПАРОВ АЛКИЛФТОРФОСФОНАТОВ В ВОЗДУХЕ | 2006 |
|
RU2308716C1 |
| МОНОЛИТНЫЕ КОМПОЗИТНЫЕ СОРБЕНТЫ ДЛЯ ИЗВЛЕЧЕНИЯ РТУТИ ИЗ ВОДНЫХ СРЕД | 2022 |
|
RU2794732C1 |
| СПОСОБ ПОЛУЧЕНИЯ МЕЗОПОРИСТОГО КОМПОЗИТНОГО СОРБЕНТА | 2015 |
|
RU2593768C1 |
| СПОСОБ ОТДЕЛЕНИЯ ПЛАТИНЫ (II, IV) И ПАЛЛАДИЯ (II) ОТ СЕРЕБРА (I), ЖЕЛЕЗА (III) И МЕДИ (II) В СОЛЯНОКИСЛЫХ РАСТВОРАХ | 2019 |
|
RU2694855C1 |
| СПОСОБ ВЫДЕЛЕНИЯ НИКОТИНОВОЙ КИСЛОТЫ ИЗ ВОДНОГО РАСТВОРА | 2015 |
|
RU2613981C1 |
| Сорбент для извлечения ионов ртути из растворов | 1985 |
|
SU1318286A1 |


Изобретение относится к области аналитической химии, а именно к способам сорбционного концентрирования и разделения неполярных веществ, таких как фосфатидилхолин и α-токоферол, для последующего их определения в растительных образцах, фармацевтических препаратах. Предложен способ разделения фосфатидилхолина и α-токоферола мезопористым сорбентом, включающий пропускание бинарного раствора сорбатов через хроматографическую колонку, заполненную сорбентом, характеризующийся тем, что хроматографическую колонку заполняют мезопористым сорбентом MkPh, синтезированным в присутствии фосфатидилхолина, при мольном соотношении компонентов 132.06H2O:1.33NH3:1.0TEOS:0.11CTABr:0.011 фосфатидилхолин, для разделения фосфатидилхолина и α-токоферола сорбент фракционируют до размера частиц 0,1-0,25 мм, высота слоя сорбента составляет 3 см, диаметр колонки равен 0,5 см, через хроматографическую колонку пропускают гексановый бинарный раствор фосфатидилхолина и α-токоферола с концентрациями 2,0⋅10-3 моль/дм3, скорость пропускания раствора 0,5 см3/мин, разделение ведут при 25°С, раствор пропускают до того момента, когда концентрация элюата будет равна концентрации исходного раствора. Изобретение обеспечивает способ разделения фосфатидилхолина и α-токоферола мезопористым сорбентом, характеризующийся повышением эффективности хроматографического разделения фосфатидилхолина и α-токоферола из гексановых растворов на кремнеземе, синтезированном темплатным методом в присутствии фосфатидилхолина в 20-30 раз по сравнению с классическим силикагелем и в 1,3 раза с мезопористым материалом, синтезированным без добавки фосфатидилхолина. 8 ил., 3 пр.
Способ разделения фосфатидилхолина и α-токоферола мезопористым сорбентом, включающий пропускание бинарного раствора сорбатов через хроматографическую колонку, заполненную сорбентом, отличающийся тем, что хроматографическую колонку заполняют мезопористым сорбентом MkPh, синтезированным в присутствии фосфатидилхолина, при мольном соотношении компонентов 132.06H2O:1.33NH3:1.0TEOS:0.11CTABr:0.011 фосфатидилхолин; для разделения фосфатидилхолина и α-токоферола сорбент фракционируют до размера частиц 0,1-0,25 мм; высота слоя сорбента составляет 3 см; диаметр колонки равен 0,5 см; через хроматографическую колонку пропускают гексановый бинарный раствор фосфатидилхолина и α-токоферола с концентрациями 2,0⋅10-3 моль/дм3; скорость пропускания раствора 0,5 см3/мин; разделение ведут при 25°С; раствор пропускают до того момента, когда концентрация элюата будет равна концентрации исходного раствора.
| САФОНОВА Е | |||
| Ф | |||
| Выделение и изучение фосфолипидов масла семян амаранта | |||
| Автореферат на соискание ученой степени кандидата химических наук, 2004, С.1-28 | |||
| СИНЯЕВА Л | |||
| А | |||
| и др | |||
| Механический грохот | 1922 |
|
SU41A1 |
| Журнал Физической Химии, 2016, Т.90, No.11, С.1701-1709 | |||
| Martinez Perez-Cejuela H | |||
| et al | |||
Авторы
Даты
2023-03-28—Публикация
2022-08-01—Подача