Изобретение относится к химии высокомолекулярных соединений, а именно к получению полимерных сорбционных материалов, которые могут найти применение в технологиях водоподготовки и экологии, в частности в качестве эффективных сорбентов для доочистки поверхностных и питьевых вод от загрязнений ртутью, а также для аналитического концентрирования ртути в задачах экологического мониторинга.
Ртуть является одним из наиболее токсичных загрязнителей водных ресурсов, использующихся для получения воды питьевого качества. За последние несколько десятилетий разработаны технологии удаления ртути из воды химическим осаждением, ионным обменом, мембранной фильтрацией, электролитическими методами, обратным осмосом, экстракцией растворителем и адсорбцией. С точки зрения соотношения эффективность/стоимость, простоты оборудования и применимости в различных масштабах адсорбция остаётся одним из наиболее привлекательных методов извлечения ионов ртути. Несмотря на то, что некоторые из известных сорбентов имеют высокую сорбционную ёмкость по ионам ртути, медленная кинетика сорбции и недостаточная эффективность извлечения при низком и очень низком содержании ртути в очищаемой воде существенно ограничивают возможности их применения как в водоочистке, так и при аналитическом концентрировании для целей экологического мониторинга.
К настоящему времени получены сорбенты для извлечения ртути на основе наночастиц, в том числе магнитных, ион-импринтированных полимеров, мезопористых неорганических материалов, углеродных нанотрубок, оксидов графена и др. Наноразмерные материалы привлекают большое внимание благодаря развитой поверхности и широкому спектру перспективных химических, физических и биологических свойств. Известно, что введение в состав сорбентов серосодержащих функциональных групп или наполнителей позволяет значительно улучшить эффективность сорбционного извлечения ртути в силу химического сродства между серой и ртутью и образования малорастворимых соединений.
Известен композитный сорбент ртути, получаемый реакцией диатомитового исходного материала с гамма-меркаптопропилтриметоксисиланом в растворе хлороформа [з. US №20100276372, опубл. 04.11.2010]. Способ изготовления композита включает стадию формирования подложки из порошков коммерческого или природного диатомита из скелетов диатомовых водорослей с размером частиц 1-1000 мкм. Затем добавляют гамма-меркаптопропилтриметоксисилан в соотношении (по массе) к диатомиту 0,1-1 и хлороформ в соотношении к диатомиту 1-2. Реакцию проводят в герметичном химически стойком сосуде, таком как стекло, тефлон или сосуд из нержавеющей стали при перемешивании при комнатной температуре в течение 24-96 часов. После перемешивания в течение 4 дней при комнатной температуре на магнитной мешалке суспензию промывают хлороформом и фильтруют через воронку Бюхнера с фильтровальной бумагой. Затем отделяют твёрдое вещество от жидкости, сушат на воздухе и диспергируют с получением гранул.
Сорбцию ртути проводят в статическом режиме, добавляя требуемое количество адсорбента из диатомита с гранулометрическим составом 5-82 мкм к 50-100 мл раствора ртути определённой концентрации. После реакции раствор тщательно фильтруют, а фильтрат собирают для измерения концентрации ртути. Максимальная рассчитанная ёмкость составила 428 мг Hg/г адсорбента.
Недостатками известного сорбента является использование для получения сорбента ограничено доступных и токсичных реагентов, помимо этого после извлечения ртути в статическом режиме требуется проведение нескольких стадий фильтрации, так как сорбент имеет широкий гранулометрический состав.
Описан способ получения сорбента на основе активированных углей для извлечения ртути из сточных вод химических предприятий [пат. RU №2753230, опубл. 12.08.2021, бюл. 23]. Сорбент получают в две стадии. На первой стадии гранулированный активированный уголь пропитывают раствором сульфата марганца(II) с концентрацией 0,25-7,5 мас. %. После обработки раствором MnSO4 активированный уголь вылёживают и доводят до воздушно-сухого состояния. На второй стадии полученный модифицированный полупродукт помещают в 5% избыток раствора сульфида натрия с концентрацией 10% на 1 час. После обработки образец отделяют от жидкости и сушат. Таким способом получают образцы с содержанием 0,5-15 мас. % MnS. Исследование эффективности полученных образцов проводили в статических условиях при следующих параметрах процесса очистки: масса образца 2,5 г, объём очищаемого раствора 50 см3, время контакта 1 час, скорость перемешивания 100-120 об/мин, концентрация ртути в растворе 1,2-123,7 мг/дм3. По истечении времени контакта сорбент отделяли от очищаемого раствора, в котором анализировали остаточное содержание ртути. Эффективность извлечения ртути для сорбента 0,5 мас. % MnS - 76,2-99,4%, для сорбента 15 мас. % MnS - 93,0-99,8%. Ресурс работы 1 кг сорбента (~2 дм3) составил более 106 дм3 очищаемой воды при концентрации раствора 24 мг/дм3 и менее. Максимальная равновесная ёмкость сорбента 2,3 мг/г.
К основным недостаткам предложенного способа очистки от ртути можно отнести невысокую сорбционную ёмкость материала, а также его низкую механическую прочность.
В [пат. RU №2441699, опубл. 10.02.2012, бюл. 4] описан мелкодисперсный поглотитель ртути. Для его получения смешивают в присутствии воды соединение железа, меди или никеля, способное образовывать сульфид металла, с материалом носителя из оксида алюминия с размером гранул 2,8-4,75 мм, первым связующим из кальций-алюминатного цемента и вторым связующим из аттапульгитовой глины. Смесь измельчают до размера зёрен 1,0-2,0 мм, сушат и сульфидируют в 1,0% H2S в азоте при скорости потока 42 л/ч. После стадии сульфидирования H2S выдувают из реактора, получая сульфид железа, меди или никеля. Сорбцию ртути из ртутьсодержащего потока проводили путём контактирования с известным поглотителем.
Недостатками являются невысокая механическая прочность, так как основные компоненты неустойчивы к истиранию, кроме того, использование сероводорода для получения материала требует повышенных мер безопасности.
Известен способ извлечения ртути с использованием композитного адсорбента с высокой эффективностью удаления метилртути (MeHg+) на основе аэрогеля поливинилового спирта (ПВС) с включением частиц дисульфида молибдена по форме напоминающих наноцветки (MoS2NF) [Chong-Bo Ma et al. «Investigation of an eco-friendly aerogel as a substrate for the immobilization of MoS2 nanoflowers for removal of mercury species from aqueous solutions» // Journal of Colloid and Interface Science, 2018, V.525, рр. 251-259].
Для получения композита тетратиомолибдат аммония (NH4)2MoS4 и триоктилфосфин растворяют в диметилформамиде. Высушенный аэрогель ПВС погружают в этот раствор, быстро пропитывают, переносят в автоклав с тефлоновым покрытием и нагревают при 200°С в течение 24 ч для проведения сольвотермической реакции. Затем аэрогели разрезают на гранулы размером 5×5 мм и погружают в деионизированную воду на трое суток для удаления примесей. Сорбенты хранят в деионизированной воде до дальнейшего использования. Максимальный коэффициент распределения при очистке от ртути составил 9,71⋅107 мл/г. Кроме того, адсорбент работал в широком диапазоне рН и мог эффективно очищать как загрязнённую озёрную, так и морскую воду.
Недостатками предложенного сорбента является использование токсичных реагентов, высокого давления и температуры для его получения, значительное падение эффективности сорбента при отклонении от оптимальных характеристик полимерной матрицы и условий сольвотермального синтеза.
Описаны высокоэффективные тиокраун-полимеры для извлечения ртути из жидкостей [пат. US №6402960, опубл. 11.06.2002]. Получение тиокраун-полимеров включает на первом этапе синтез тиокраун-эфиров, с одной или несколькими серосодержащими боковыми группами. Преимущественно тиокраун-эфир содержит 3-6 атомов серы в цикле. Конверсия гидроксиалкильных боковых групп в аминогруппы позволяет иммобилизировать молекулы тиокраун-эфиров на полимерной подложке. В конкретном способе осуществления изобретения используют ациклический предшественник тиокраун-эфира 2,3-димеркапто-1-пропанол, содержащий боковой фрагмент, который после реакции циклизации химически модифицируют реакционноспособной группой, например, аминогруппой для закрепления тиокраун-эфира на диоксиде кремния или сополимерах полистирола, полиэтилена, полиметиметакрилата. Способность тиокраун-полимеров к экстракции ртути тестировали в водных растворах при различных концентрациях Hg2+, значениях pH и времени реакции. Эффективность извлечения ионов ртути составила 95-99%.
Недостатком известного сорбента является сложный синтез тиокраун-полимера с использованием дорогостоящих и зачастую высокотоксичных реактивов. Помимо этого, недостаточная степень извлечения ртути не позволяет использовать известные тиокраун-полимеры для извлечения ртути из питьевой воды.
Известен композитный материал для сорбции ионов ртути на основе гидрогелей графен/дисульфид молибдена, получаемых гидротермальным методом [Yu-Ting Zhuang et al. «Three-dimensional molybdenum disulfide/graphene hydrogel with tunable heterointerfaces for high selective Hg(II) scavenging» // Journal of Colloid and Interface Science, 2018, V.514, рр. 715-722]. Для его приготовления 0,0165 г (NH4)6Mo7O24⋅4H2O и 0,0350 г CH4N2S диспергируют в 10 мл растворителя с содержанием графена 1 мг/мл. После перемешивания в течение 10 мин к вышеуказанной дисперсии добавляют 5 мг D-глюкозы и затем непрерывно перемешивают ещё в течение 30 мин. Смесь прекурсоров переносят в автоклав из нержавеющей стали с тефлоновым покрытием объёмом 25 мл и нагревают при 180°С в течение 8 часов. Полученные гидрогели промывают деионизированной водой до нейтральной реакции. Синтезированные гидрогели обладают высокой адсорбционной ёмкостью (340 мг/г), хорошей стабильностью, а также селективностью к ионам Hg(II), благодаря пористой структуре, большой удельной поверхности и высокому сродству ртути к сере. Гидрогель с 70 мас. % MoS2 в динамическом режиме сорбции показал высокую селективность в отношении ионов Hg(II) со значением коэффициента распределения 7,49×106 мл/г даже в присутствии других мешающих ионов.
К основному недостатку аналога можно отнести склонность наночастиц сульфида молибдена к агрегации с резкой потерей сорбционной ёмкости. Помимо этого, заполнение крупными гранулами гидрогеля сорбционной колонки не исключает возможность образования каналов между частицами сорбента, по которым содержащий ртуть раствор будет проходить без очистки.
В работе [Baimenov A. Zh. et al. «Efficient removal of mercury(II) from water by use of cryogels and comparison to commercial adsorbents under environmentally relevant conditions» // Journal of Hazardous Materials, 2020, V. 399, №15, Р. 123056] показана эффективность макропористых криогелей для удаления ртути в статическом режиме из модельных растворов Hg(NO3)2 и HgCl2. Криогели двух типов, содержащие карбокси- и сульфогруппы, синтезировали методом радикальной полимеризации. Для первого раствора рассчитанные количества метакриловой кислоты или 2-акриламидо-2-метил-1-пропансульфоновой кислоты растворяли в дегазированной сверхчистой воде при интенсивном перемешивании с последующим добавлением 5М раствора NaOH для нейтрализации кислоты. Для второго раствора в дегазированной сверхчистой воде при непрерывном перемешивании растворяли мономеры диметилакриламида и алиламина и подкисляли концентрированной H3PO4 для перехода аллиламина в фосфатную соль. Затем, после смешения двух растворов, проводили дегазацию раствора продувкой азота в течение 30 минут, добавляли по каплям тетраметилэтилендиамин и охлаждали до 2-4°C в течение 30 минут в атмосфере азота с последующим добавлением при перемешивании 5 мас. % персульфата аммония. Наконец, 2 мл смеси загружали в пластиковые шприцы диаметром 1 см, которые сразу же закупоривали во избежание попадания кислорода воздуха в раствор и предотвращения ингибирования радикальной полимеризации. Шприцы погружали в охлаждаемую этанолом криованну с программным управлением и выдерживали при -12°С в течение 24 часов. Полученные монолитные криогели оттаивали в теплой воде при температуре 23-25°С и промывали сначала 1% этанолом, а затем 2 л чистой воды. Воду удаляли из криогелей с помощью лиофильной сушки при -53°C и 0,4 мбар в течение 48 часов.
Извлечение ртути из модельных растворов проводили в пластиковых пробирках, содержащих 0,08 г криогелей и 100 мл раствора HgCl2 или Hg(NO3)2 с концентрацией Hg2+100 мг/л, при встряхивании со скоростью 120 об/мин. Криогели показали эффективное извлечение ртути при сорбционной емкости 260 мг/г из раствора HgCl2 и 620 мг/г из раствора Hg(NO3)2.
Недостатком указанных криогелей является сложный синтез за счёт использования большого количества реактивов, необходимость обеспечения инертной атмосферы, применение дорогостоящего оборудования для лиофилизации криогелей.
Использование криогелей в форме монолитных материалов в динамических условиях потенциально позволяет повысить эффективность сорбции посредством улучшения массопереноса за счёт обеспечения прохождения раствора через весь объём сорбента. Открытая пористая структура криогелей с толщиной полимерных стенок в несколько микрон обеспечивает высокую скорость внутренней диффузии адсорбата в полимерную фазу монолитного криогеля, что позволяет избежать роста сопротивления на колонке при увеличении скорости потока жидкости, как это происходит для гранулированных материалов с размером гранул в диапазоне микрометров.
Наиболее близким по совокупности признаков к заявляемым композитным сорбентам является монолитный криогель на основе полиэтиленимина [пат. RU №2741002, опубл. 22.01.2021, бюл. 3]. Его получают путём сшивки полиэтиленимина (ПЭИ) в 5% растворе (рН 11) с диглицидиловым эфиром 1,4-бутандиола (ДГЭ-1,4-БД) при молярном соотношении 4:1. А именно, после добавления сшивающего агента при интенсивном перемешивании раствор ПЭИ помещают в сорбционную колонку, герметизируют и замораживают при температуре -20°С. После оттаивания через 7 дней выдержки в замороженном виде, криогель промывают при скорости потока 100 колоночных объёмов в час (к.о./ч) водой для получения формы свободного основания (криогель ПЭИ).
Недостаток прототипа заключён в том, что для известного сорбента предложено применение для извлечения органических загрязнителей и ряда ионов тяжёлых металлов, но для извлечения Hg(II) его не использовали.
В связи с изложенным, была поставлена задача получить высокоэффективный монолитный сорбент на ионы ртути, позволяющий проводить доочистку воды.
Техническим результатом заявляемого изобретения является ряд высокоёмких композитных сорбентов ионов Hg(II) на основе полиэтиленимина с частицами сульфидов переходных металлов, которые повышают эффективность извлечения ионов ртути.
Указанный технический результат достигают монолитными композитными криогелями для извлечения ионов ртути на основе сшитого полиэтиленимина с частицами сульфидов переходных металлов Zn, Cu, Ni, Co, которые формируют в объёме криогеля последовательным пропусканием раствора соли одного из указанных переходных металлов, а затем раствора Na2S.
Композитные сорбенты получают формированием in situ наночастиц сульфидов цинка, меди, никеля и кобальта в криогеле ПЭИ. Последний получают путём сшивки молекул ПЭИ в 5% растворе (рН 10-11) с ДГЭ-1,4-БД при молярном соотношении ДГЭ-1,4-БД:ПЭИ 1:4. Для этого раствор ПЭИ после добавления сшивающего агента при интенсивном перемешивании помещают в сорбционную колонку, запаивают парафильмом, помещают в морозильную камеру при температуре -20°С и выдерживают в течение 7 дней. После оттаивания криогель промывают водой с помощью перистальтического насоса при скорости потока до 100 колоночных объёмов (к.о.)/ч. Затем через криогель ПЭИ пропускают раствор соли переходного металла из ряда Zn(II), Cu(II), Ni(II), Co(II) до достижения максимальной динамической сорбционной ёмкости, о чём судят по проскоку на выходной кривой при анализе концентрации ионов металлов на выходе из колонки с помощью атомно-абсорбционного пламенно-эмиссионного спектрометра. Насыщенный ионами металла-прекурсора криогель ПЭИ промывают водой и пропускают через него раствор сульфида натрия из расчёта, что мольное отношение введённых в колонку ионов S2- к иону переходного металла-прекурсора в криогеле выше 1,5.
Сорбцию ионов Hg(II) на монолитных композитных криогелях исследовали в статическом и динамическом режимах. Для использования в статическом режиме полученный криогель с частицами сульфидов металлов извлекали из колонки, нарезали в форме дисков толщиной 3-4 мм и погружали при соотношении сорбент:раствор = 1:1000 в раствор 0,5 мМ NaCl с концентрацией Hg(II) 0,5-500 мг/л. Извлечение ртути проводили при температуре +23°С, рН 4,5, время контакта 72 часа, скорость перемешивания 220 об/мин. Остаточную концентрацию ртути в растворе определяли с помощью атомно-абсорбционного пламенно-эмиссионного спектрометра. Степень извлечения (R) ртути рассчитывали по формуле:

где C0 и C - исходная и остаточная концентрации ртути в растворе соответственно (мг/л).
Сорбцию в динамическом режиме исследовали из растворов с содержанием ртути от 0,4 мкг/л до 200 мг/л и скорости потока от 38 до 250 к.о./ч. Концентрацию ртути в растворе после выхода из сорбционной колонки определяли методом атомно-абсорбционной спектрометрии холодного пара с использованием ртутно-гидридной приставки. Если концентрация ртути была менее 0,006 мг/л определение проводили методом масс-спектрометрии с индуктивно связанной плазмой. Раствор, содержащий 50 мкг/л индия, использовали в качестве внутреннего стандарта. Построение калибровочной кривой проводили с использованием стандартного раствора с концентрацией ртути 0,5 мкг/л (стандарт 2A-Hg). Предел обнаружения ртути составил 0,046 мкг/л, стандартное отклонение <10%.
Коэффициент очистки (КО) рассчитывали по формуле:

где C0 и C - исходная и остаточная концентрации Hg(II) в растворе соответственно (мг/л).
Полную динамическую сорбционную ёмкость (ПДСЕ) рассчитывали интегрированием выходных кривых сорбции ионов ртути по уравнению:
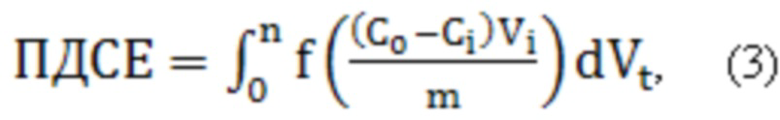
где C0 - начальная концентрация Hg(II) (мг/л), Ci - концентрация Hg(II) в i-й порции выходного раствора (мг/л), Vi - объём i-й порции выходного раствора (мл), m - масса сухого монолитного сорбента в сорбционной колонке (г), Vt - объём раствора, прошедшего через колонку до проскока 100% от исходной концентрации ртути (мл).
Изобретение проиллюстрировано следующим графиком:
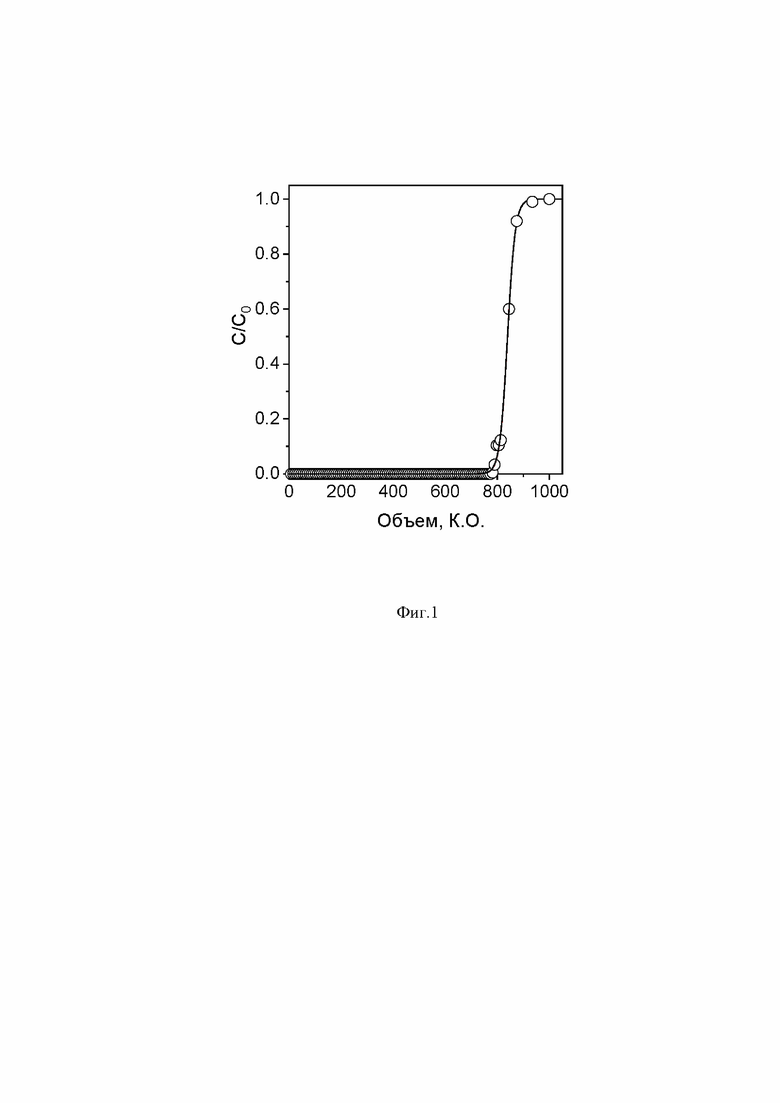
Фиг. 1. Выходная кривая сорбции ионов Hg(II) на монолитном криогеле ПЭИ/ZnS (высота слоя - 6 см, диаметр - 0,48 см) при скорости потока 38 к.о./ч из 0,5 мМ раствора NaCl с исходным содержанием ртути (С0) 200 мг/л, рН 4,5.
Заявляемое изобретение реализовано в следующих примерах.
Пример 1.
Монолитный криогель ПЭИ получали как описано выше. А именно, после добавления сшивающего агента при интенсивном перемешивании 1 мл раствора ПЭИ помещали в сорбционную колонку с внутренним диаметром 4,8 мм, герметизировали и замораживали при температуре -20°С, после чего промывали деионизированной водой. Затем криогель ПЭИ насыщали ионами Cu(II), путём пропускания через него раствора Cu(NO3)2 с концентрацией Cu(II) 100 мг/л со скоростью потока 120 к.о./ч. При полном насыщении криогель содержал 120 мг/г Cu(II). После промывки криогеля, содержащего ионы Cu(II), водой с применением перистальтического насоса пропускали 50 мл 0,01М раствора Na2S со скоростью потока 8 к.о./ч в циклическом режиме в течение 18 часов. По окончании процесса композит промывали 150 мл воды и запечатывали парафильмом для хранения в набухшем состоянии до использования. Сорбцию ионов ртути в статических условиях на композите ПЭИ/CuS проводили из раствора с концентрацией Hg(II) 48 мг/л в условиях, описанных в общей части. Степень извлечения ртути составила 95,7%, остаточная концентрация Hg(II) в растворе 2,04 мг/л.
Пример 2.
Монолитный криогель ПЭИ получали как описано в примере 1. Затем криогель ПЭИ насыщали ионами Ni(II), путём пропускания через него раствора Ni(NO3)2 с концентрацией Ni(II) 100 мг/л со скоростью потока 40 к.о./ч. При полном насыщении криогель содержал 82 мг/г Ni(II). После промывки криогеля, содержащего ионы Ni(II), водой с применением перистальтического насоса пропускали 40 мл 0,01М раствора Na2S со скоростью потока 8 к.о./ч в циклическом режиме в течение 18 часов. По окончании процесса композит промывали 150 мл воды и запечатывали парафильмом для хранения в набухшем состоянии до использования. Сорбцию ионов ртути в статических условиях на композите ПЭИ/NiS проводили из раствора с концентрацией Hg(II) 57 мг/л в условиях, описанных в общей части. Степень извлечения ртути составила 99,6%, остаточная концентрация Hg(II) в растворе 0,228 мг/л.
Пример 3
Монолитный криогель ПЭИ получали как описано в примере 1. Затем криогель ПЭИ насыщали ионами Co(II), путём пропускания через него раствора Со(NO3)2 с концентрацией Co(II) 50 мг/л со скоростью потока 20 к.о./ч. При полном насыщении криогель содержал 34 мг/г Co(II). После промывки криогеля, содержащего ионы Co(II), водой с применением перистальтического насоса пропускали 40 мл 0,01М раствора Na2S со скоростью потока 8 к.о./ч в циклическом режиме в течение 18 часов. По окончании процесса композит промывали 150 мл воды и запечатывали парафильмом для хранения в набухшем состоянии до использования. Сорбцию ионов ртути в статических условиях на композите ПЭИ/CoS проводили из раствора с концентрацией Hg(II) 57 мг/л в условиях, описанных в общей части. Степень извлечения ртути составила 99,6%, остаточная концентрация Hg(II) в растворе 0,228 мг/л.
Пример 4
Монолитный криогель ПЭИ получали как описано в примере 1. Затем криогель ПЭИ насыщали ионами Zn(II), путём пропускания через него раствора Zn(NO3)2 с концентрацией Zn(II) 100 мг/л со скоростью потока 40 к.о./ч. При полном насыщении криогель содержал 114 мг/г Zn(II). После промывки криогеля, содержащего ионы Zn(II), водой с применением перистальтического насоса пропускали 50 мл 0,01М раствора Na2S со скоростью потока 8 к.о./ч в циклическом режиме в течение 18 часов. По окончании процесса композит промывали 150 мл воды и запечатывали парафильмом для хранения в набухшем состоянии до использования. Сорбцию ионов в статических условиях в растворах с разным содержанием ртути проводили на композите ПЭИ/ZnS в условиях, описанных в общей части. Эффективность очистки воды монолитным композитным сорбентом приведена в следующей таблице.
Пример 5.
Монолитный композитный криогель ПЭИ, содержащий наночастицы сульфида цинка (ПЭИ/ZnS), получали как описано в примере 4. Для исследования сорбции ртути через колонку с композитным криогелем пропускали раствор 0,5 мМ NaCl с содержанием Hg(II) 200 мг/л (рН=4,5) при скорости потока 38 к.о./ч. Выходная кривая сорбции представлена на Фиг. 1. Концентрация Hg(II) на выходе после сорбции на криогеле ПЭИ/ZnS из раствора с содержанием ртути 200 мг/л до точки проскока составила 0,9 мкг/л, коэффициент очистки (КО) >105. Рассчитанное из выходной кривой значение полной динамической сорбционной ёмкости (ПДСЕ) составило - 6,08 ммоль/г.
Пример 6.
Монолитный композитный криогель ПЭИ/ZnS получали как описано в примере 4. Эффективность извлечения ртути в динамическом режиме на монолитном криогеле ПЭИ/ZnS исследовали при скорости потока 38 к.о./ч и 250 к.о./ч из раствора 0,5 мМ NaCl с содержанием Hg(II) 9,8 мг/л (рН=4,5). Остаточные концентрации ртути в растворе и эффективность очистки приведены в следующей таблице в сравнении с эффективностью криогелей без частиц сульфида металла.
| название | год | авторы | номер документа |
|---|---|---|---|
| МОНОЛИТНЫЕ СОРБЦИОННЫЕ МАТЕРИАЛЫ НА ОСНОВЕ ПОЛИЭТИЛЕНИМИНА ДЛЯ ИЗВЛЕЧЕНИЯ ИОНОВ ТЯЖЁЛЫХ МЕТАЛЛОВ И ОРГАНИЧЕСКИХ ЗАГРЯЗНИТЕЛЕЙ | 2020 |
|
RU2741002C1 |
| СПОСОБ ПОЛУЧЕНИЯ СОРБЕНТА РЕДКОЗЕМЕЛЬНЫХ МЕТАЛЛОВ | 2014 |
|
RU2579133C1 |
| НАПОЛНЕННЫЙ ЧАСТИЦАМИ СОРБЕНТА МАКРОПОРИСТЫЙ ПОЛИМЕРНЫЙ МАТЕРИАЛ, КОМПОЗИЦИЯ ДЛЯ ЕГО ПОЛУЧЕНИЯ И СПОСОБ ПОЛУЧЕНИЯ | 2015 |
|
RU2601605C1 |
| Сорбент для извлечения ионов ртути из растворов | 1985 |
|
SU1318286A1 |
| СПОСОБ ПОЛУЧЕНИЯ СЕРОСОДЕРЖАЩИХ СОРБЕНТОВ ДЛЯ ОЧИСТКИ СТОЧНЫХ ВОД ОТ ТЯЖЕЛЫХ МЕТАЛЛОВ | 2010 |
|
RU2475299C2 |
| СОРБЦИОННЫЙ МАТЕРИАЛ ДЛЯ СЕЛЕКТИВНОГО ИЗВЛЕЧЕНИЯ РАДИОНУКЛИДОВ СТРОНЦИЯ ИЗ РАСТВОРОВ С ВЫСОКИМ СОДЕРЖАНИЕМ СОЛЕЙ ЖЕСТКОСТИ, СПОСОБ ЕГО ПОЛУЧЕНИЯ, ЕГО ПРИМЕНЕНИЕ И СПОСОБ ИЗВЛЕЧЕНИЯ РАДИОНУКЛИДОВ СТРОНЦИЯ ИЗ РАСТВОРОВ С ВЫСОКИМ СОДЕРЖАНИЕМ СОЛЕЙ ЖЕСТКОСТИ | 2016 |
|
RU2620259C1 |
| Способ получения волокнистых сорбентов для извлечения цезия | 2023 |
|
RU2828608C1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ ЗОЛОТА ИЗ ЦИАНИДНЫХ РАСТВОРОВ C ПРИСУТСТВУЮЩЕЙ В НИХ РАСТВОРЕННОЙ РТУТЬЮ | 2011 |
|
RU2460814C1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ РТУТИ (II) ИЗ КИСЛЫХ РАСТВОРОВ | 1999 |
|
RU2161593C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИМЕР-НЕОРГАНИЧЕСКИХ КОМПОЗИТНЫХ СОРБЕНТОВ | 2012 |
|
RU2527217C1 |
Изобретение относится к химии высокомолекулярных соединений, а именно к получению полимерных сорбционных материалов, которые могут найти применение в технологиях водоподготовки и экологии, в частности в качестве эффективных сорбентов для доочистки поверхностных и питьевых вод от загрязнений ртутью, а также для аналитического концентрирования ртути в задачах экологического мониторинга. Представлен монолитный композитный криогель на основе сшитого полиэтиленимина для извлечения ионов ртути из воды, который содержит частицы сульфидов металлов, выбранных из ряда Cu, Ni, Co. Изобретение обеспечивает ряд высокоёмких композитных сорбентов ионов Hg(II) на основе полиэтиленимина с частицами сульфидов переходных металлов, которые повышают эффективность извлечения ионов ртути. 1 ил., 6 пр., 2 табл.
Монолитный композитный криогель на основе сшитого полиэтиленимина для извлечения ионов ртути из воды, который содержит частицы сульфидов металлов, выбранных из ряда Cu, Ni, Co.
| МАЛАХОВА И | |||
| А | |||
| и др | |||
| Супермакропористые композитные материалы для извлечения ионов Hg(II) и Cs(I) | |||
| Материалы V Всероссийской научной конференции "Актуальные проблемы теории и практики гетерогенных катализаторов и адсорбентов", 30 июня-2 июля 2021, С.506 | |||
| МОНОЛИТНЫЕ СОРБЦИОННЫЕ МАТЕРИАЛЫ НА ОСНОВЕ ПОЛИЭТИЛЕНИМИНА ДЛЯ ИЗВЛЕЧЕНИЯ ИОНОВ ТЯЖЁЛЫХ МЕТАЛЛОВ И ОРГАНИЧЕСКИХ ЗАГРЯЗНИТЕЛЕЙ | 2020 |
|
RU2741002C1 |
| PRIVAR Y | |||
| et al | |||
| Polyethyleneimine cryogels for metal ions | |||
Авторы
Даты
2023-04-24—Публикация
2022-08-02—Подача