Изобретение относится к антибактериальным средствам на основе серебряных солей метил (2Z)-4-арил-2-{4-[(4,6-диметилпиримидин-2-ил)сульфамоил]фениламино}-4-оксобут-2-еноатов формулы (I, II):
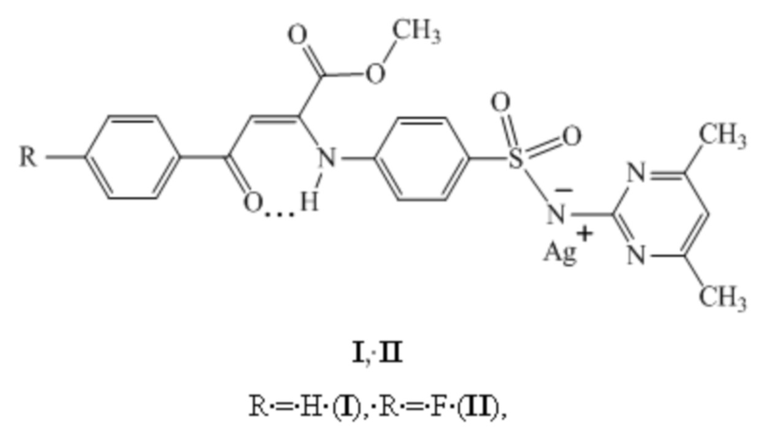
что позволяет предположить возможность их применения в медицине в качестве антибактериальных лекарственных средств.
Ближайшими аналогами по структуре и действию заявляемым соединениям являются метил (2Z)-4-арил-2-{4-[(4,6-диметилпиримидин-2-ил)сульфамоил]фениламино}-4-оксобут-2-еноаты (Iа, IIа) (Синтез и биологическая активность соединений, полученных на основе взаимодействия метиловых эфиров ароилпировиноградных кислот с сульфадимидином / В.Л. Гейн, О.В. Бобровская, М.В. Дмитриев, Р.Р. Махмудов, В.Д. Белоногова // Журнал общей химии. - 2018. - Т. 88, вып. 6. - С. 914-921) формулы:
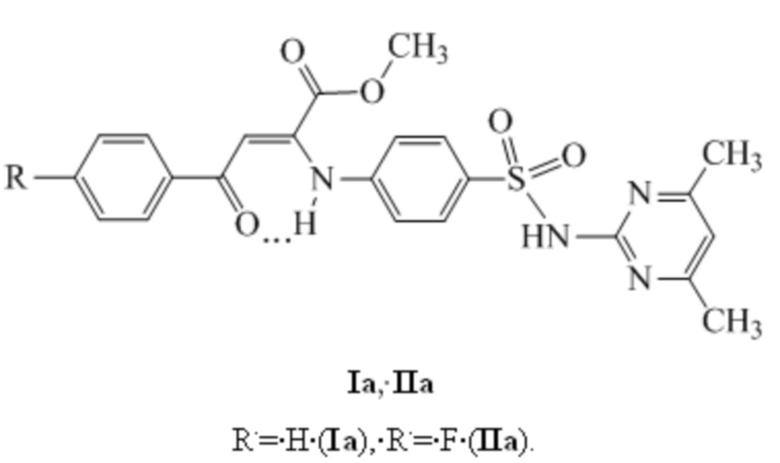
Структурные аналоги (Iа, IIа) обладают низкой антибактериальной активностью (таблица 1).
В медицинской практике широко используется диоксидин в качестве антибактериального лекарственного средства, аналогичного по фармакологическому действию заявляемым соединениям (I, II), которое выбрано нами в качестве эталона сравнения (Машковский М.Д. Лекарственные средства. - 16-е изд., перераб., испр. и доп. - М.: Новая волна, 2012. - С. 848).
Задачей изобретения является поиск новых соединений с высоким антибактериальным действием и низкой токсичностью в ряду метил (2Z)-4-арил-2-{4-[(4,6-диметилпиримидин-2-ил)сульфамоил]фениламино}-4-оксобут-2-еноатов.
Поставленная задача решается применением серебряных солей метил (2Z)-4-арил-2-{4-[(4,6-диметилпиримидин-2-ил)сульфамоил]фениламино}-4-оксобут-2-еноатов (I, II), которые обладают высокой антибактериальной активностью и низкой токсичностью.
Соединения (I, II) синтезируют взаимодействием метил (2Z)-4-арил-2-{4-[(4,6-диметилпиримидин-2-ил)сульфамоил]фениламино}-4-оксобут-2-еноатов (Iа, IIа) c серебра нитратом в смеси этанол-ДМФА в соотношении 2:1 по методике (Синтез и противомикробная активность метил 4-арил-2-{4-[(4,6-диметилпиримидин-2-ил)сульфамоил]фениламино}-4-оксобут-2-еноатов и их серебряных солей / В.Л. Гейн, О.В. Бобровская, Е.А. Машкина, В.В. Новикова, Р.Р. Махмудов, А.Н. Янкин, С.Е. Данилов, Е.А. Хволис, В.Д. Белоногова, Д.К. Гуляев // Журнал общей химии. - 2020. - Т. 90, № 5. - С. 723-729) по следующей схеме:
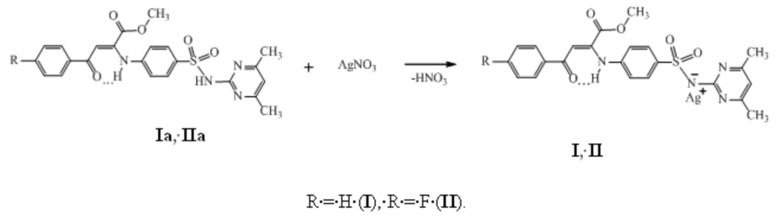
Синтез исходных метил (2Z)-4-арил-2-{4-[(4,6-диметилпиримидин-2-ил)сульфамоил]фениламино}-4-оксобут-2-еноатов (Iа, IIа) осуществлён cогласно ранее описанной методики (Синтез и биологическая активность соединений, полученных на основе взаимодействия метиловых эфиров ароилпировиноградных кислот с сульфадимидином / В.Л. Гейн, О.В. Бобровская, М.В. Дмитриев, Р.Р. Махмудов, В.Д. Белоногова // Журнал общей химии. - 2018. - Т. 88, вып. 6. - С. 914-921).
Изобретение иллюстрируется следующими примерами.
Пример 1. Получение соединения (I)
К горячему раствору 2.33 г (0.005 моль) метил (2Z)-2-{4-[(4,6-диметилпиримидин-2-ил)сульфамоил]фениламино}-4-оксо-4-фенилбут-2-еноата (Iа) в 30-35 мл смеси этанол-ДМФА (2:1) приливали горячий раствор 0.85 г (0.005 моль) серебра нитрата в 42.5 мл этанола (2%-ный раствор). Выпавший осадок отфильтровывали, промывали на фильтре от следов серебра нитрата этанолом и водой, сушили, снова промывали этанолом и сушили. Выход 2.32 г (81%). Т. пл. 284-286°С. Найдено, %: C 48.03; Н 3.74; N 9.84; S 5.53. С23H21AgN4O5S. Вычислено, %: C 48.18; Н 3.69; N 9.77; S 5.59. ИК спектр (ИК-Фурье спектрометр IRAffinity-1 Shimadzu (Япония), в таблетках с KBr, ν, см-1): 3350 (NН), 1738 (СОсл.эф), 1616 (СОкет.), 1376, 1142 (SО2). Спектр ЯМР 1Н (Bruker Avance III HD (400 МГц), рабочая частота 400 МГц, DMSО-d6, ТМS, δ, м.д.): 2.36 с (6H, 2CH3), 3.76 с (3H, СООСН3), 6.57 с (1H, C5H), 6.66 с (1Н, С3Н=), 6.71-8.01 м (9Н, CHAr), 11.74 с (1Н, NН). Масс-спектр (Bruker micrOTOF, HRMS-ESI, m/z): 489.1217 [M-Ag+Na]+.
Соединение (I) - жёлтое кристаллическое вещество, растворимое при нагревании в диметилформамиде, диметилсульфоксиде, ледяной уксусной кислоте и нерастворимое в этиловом спирте, изопропаноле, воде.
Пример 2. Получение соединения (II)
К горячему раствору 2.42 г (0.005 моль) метил (2Z)-2-{4-[(4,6-диметилпиримидин-2-ил)сульфамоил]фениламино}-4-оксо-4-(4-фторфенил)бут-2-еноата (IIа) в 30-35 мл смеси этанол-ДМФА (2:1) приливали горячий раствор 0.85 г (0.005 моль) серебра нитрата в 42.5 мл этанола (2%-ный раствор). Выпавший осадок отфильтровывали, промывали на фильтре от следов серебра нитрата этанолом и водой, сушили, снова промывали этанолом и сушили. Выход 2,34 г (79%). Т. пл. 286-288°С. Найдено, %: C 46.83; Н 3.35; N 9.39; S 5.46. С23H20AgFN4O5S. Вычислено, %: C 46.71; Н 3.41; N 9.47; S 5.42. ИК спектр (ИК-Фурье спектрометр IRAffinity-1 Shimadzu (Япония), в таблетках с KBr, ν, см-1): 3351 (NН), 1736 (СОсл.эф), 1623 (СОкет.), 1375, 1140 (SО2). Спектр ЯМР 1Н (Bruker Avance III HD (400 МГц), рабочая частота 400 МГц, DMSО-d6, ТМS, δ, м.д.): 2.35 с (6H, 2CH3), 3.75 с (3H, СООСН3), 6.53 с (1H, C5H), 6.66 с (1Н, С3Н=), 6.55-8.08 м (8Н, CHAr), 11.71 с (1Н, NН). Масс-спектр (Bruker micrOTOF, HRMS-ESI, m/z): 591.0252 [M]+.
Соединение (II) - жёлтое с коричневатым оттенком кристаллическое вещество, растворимое при нагревании в диметилформамиде, диметилсульфоксиде, ледяной уксусной кислоте и нерастворимое в этиловом спирте, изопропаноле, воде.
Пример 3. Исследование антибактериальной активности и острой токсичности соединений (I, II)
Острую токсичность (ЛД50, мг/кг) соединений (I, II) изучали на белых мышах (самках) массой 16-18 г при однократном внутрибрюшинном введении (Руководство по проведению доклинических исследований лекарственных средств / под ред. А.Н. Миронова, Н.Д. Бунятян, А.Н. Васильева, О.Л. Верстаковой, М.В. Журавлевой, В.К. Лепахина, Н.В. Коробова, В.А. Меркулова, С.Н. Орехова, И.В. Сакаевой, Д.Б. Утешева, А.Н. Яворского. - Ч. 1. - М.: Гриф и К, 2012. - 944 с.). За животными вели наблюдение в течение 10 суток, фиксируя поведение, интенсивность и характер двигательной активности, наличие судорог, координацию движений, тонус скелетной мускулатуры, реакции на тактильные, звуковые и световые раздражители, частоту и глубину дыхательных движений, ритм сердечных сокращений, состояние волосяного и кожного покрова, окраску видимых слизистых оболочек, потребление воды и пищи, изменение массы тела.
Рассчитывали острую токсичность, соблюдая рекомендации государственного фармакологического комитета по изучению общетоксического действия биологически активных веществ (Методические рекомендации по изучению общетоксического действия фармакологических средств. Утв. 25. 12. 97 / Вестн. фармакоп. комитета. - 1998. - №1. - С. 27-32).
Установлено, что ЛД50 для соединения (I) составляет >1000 мг/кг, для соединения (II) >1100 мг/кг (таблица 1). Следовательно, заявляемые соединения (I, II) менее токсичны, чем эталон сравнения диоксидин, ЛД50 которого 750 мг/кг (U.S. National Library of Medicine [Электронный ресурс]. - Режим доступа: https://chem.nlm.nih.gov/chemidplus/name/dioxydine) в 1,33 раза (соединение I), и, соответственно, в 1,47 раза (соединение II).
Согласно классификации токсичности препаратов соединения (I, II) относятся к классу практически нетоксичных веществ (Сидоров, К.К. О классификации токсичности ядов при парентеральных способах введения / К.К. Сидоров // Токсикология новых промышленных химических веществ. - 1973. - Вып. 13. - С. 47-51; Березовская, И.В. Классификация химических веществ по параметрам острой токсичности при парентеральных способах введения / И.В. Березовская // Химико-фармацевтический журнал. - 2003. - Т. 37, № 3. - С. 32-34).
Антибактериальную активность заявляемых соединений (I, II) определяли пробирочным методом двукратных серийных разведений в жидкой питательной среде (Руководство по проведению доклинических исследований лекарственных средств / под ред. А.Н. Миронова, Н.Д. Бунятян, А.Н. Васильева, О.Л. Верстаковой, М.В. Журавлевой, В.К. Лепахина, Н.В. Коробова, В.А. Меркулова, С.Н. Орехова, И.В. Сакаевой, Д.Б. Утешева, А.Н. Яворского. - М.: Гриф и К, 2012. - Ч. 1. - 944 с).
Скрининг антибактериальной активности осуществляли в отношении типовых штаммов Staphylococcus aureus ATCC 6538-P, Escherichia coli ATCC 25922. Исследуемые соединения массой 0,05 г растворяли в 5 мл ДМСО, получая основной раствор вещества в концентрации 104 мкг/мл. Данный раствор служил основой для рабочего раствора, имеющего концентрацию 2×103 мкг/мл, который последовательно разводили двукратно в жидкой питательной среде в ряду из 10 пробирок. Концентрация исследуемых соединений в первой пробирке ряда разведений в питательной среде составляла 1000,0 мкг/мл. Для определения антибактериальной активности использовали питательный бульон (ФБУН ГНЦ ПМБ, г. Оболенск) и типовые суточные культуры, выращенные на питательном агаре. Концентрация микробных клеток в опыте составила 2-5×105 КОЕ/мл. В качестве положительного контроля использовали питательную среду с внесенной исследуемой культурой. В качестве отрицательного контроля использовали интактную питательную среду. Посевы инкубировали в термостате при температуре 35±2°С. Оценку роста бактерий проводили визуально через 18-24 ч инкубирования. В качестве значения МПК (минимальной подавляющей концентрации) принимали наименьшую концентрацию соединения, при которой отсутствует видимый рост тест-организма.
Полученные результаты заявляемых соединений (I, II) по антибактериальной активности сравнивали с экспериментальными данными диоксидина (таблица 1). Кроме того, антибактериальную активность заявляемых соединений (I, II) сравнивали с активностью аналогов по структуре (Iа, IIа). Результаты испытаний антибактериальной активности и острой токсичности представлены в таблице 1.
Антибактериальная активность и острая токсичность соединений (I, II)
ЛД50, мг/кг, (в/б)
МПК, мкг/мл
25922
(1% раствор)
*U.S. National Library of Medicine [Электронный ресурс]. - Режим доступа: https://chem.nlm.nih.gov/chemidplus/name/dioxydine.
Как видно из таблицы 1, структурные аналоги (Iа, IIа) обладают низкой антибактериальной активностью. Введение ионов серебра в структуру метил (2Z)-4-арил-2-{4-[(4,6-диметилпиримидин-2-ил)сульфамоил]фениламино}-4-оксобут-2-еноатов с образованием серебряных солей метил (2Z)-4-арил-2-{4-[(4,6-диметилпиримидин-2-ил)сульфамоил]фениламино}-4-оксобут-2-еноатов (I, II) приводит к резкому усилению биологического действия в отношении изучаемых штаммов микроорганизмов. Заявляемые соединения (I, II) по антибактериальной активности превосходят эффект эталона сравнения диоксидина в отношении Staphylococcus aureus ATCC 6538-P ~ в 62,5-125 раз (МПК 62,5/1,0 и 62,5/0,5), Escherichia coli ATCC 25922 ~ в 125-250 раз (МПК 31,2/0,25 и 31,2/0,125 ), а также менее токсичны, чем диоксидин.
Таким образом, серебряные соли метил (2Z)-4-арил-2-{4-[(4,6-диметилпиримидин-2-ил)сульфамоил]фениламино}-4-оксобут-2-еноатов (I, II) проявляют высокую антибактериальную активность, которая превышает действие эталона сравнения диоксидина и структурных аналогов (Iа, IIа), а также являются практически нетоксичными, и могут найти применение в медицине в качестве потенциальных лекарственных средств.
Изобретение относится к применению серебряных солей метил (2Z)-4-арил-2-{4-[(4,6-диметилпиримидин-2-ил)сульфамоил]фениламино}-4-оксобут-2-еноатов формулы I, II в качестве антибактериальных лекарственных средств. Указанные соли обладают низкой токсичностью и могут найти применение в медицине. 1 табл., 3 пр.
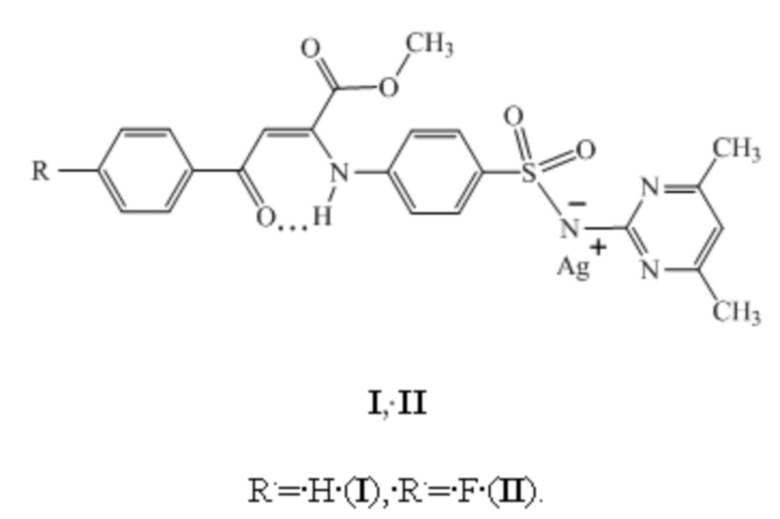
Применение серебряных солей метил (2Z)-4-арил-2-{4-[(4,6-диметилпиримидин-2-ил)сульфамоил]фениламино}-4-оксобут-2-еноатов формулы (I, II)
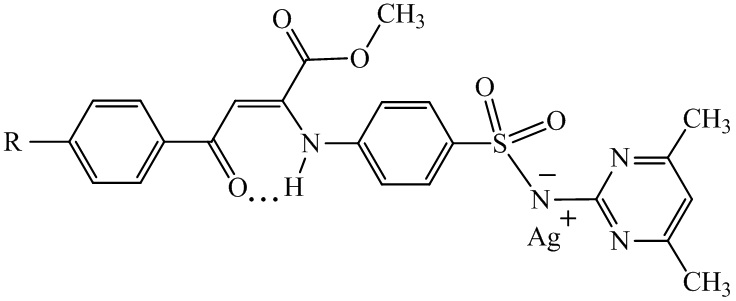
I, II
R = H (I), R = F (II)
в качестве средств, обладающих антибактериальной активностью.
| Гейн В.Л | |||
| и др., Синтез и противомикробная активность метил-4-арил-2-(4-[(4,6-диметилпиримидин-2-ил)сульфамоил] фениламино)-4-оксобут-2-еноатов и их серебряных солей | |||
| ЖУРНАЛ ОБЩЕЙ ХИМИИ, 2020, том 90, 5, с | |||
| ГРОМКО - ГОВОРЯЩИЙ ТЕЛЕФОН | 1920 |
|
SU723A1 |
| Gein V.L | |||
| et al., Synthesis and biological activity of compounds obtained by reacting methyl aroylpyruvates with sulfadimidine | |||
Авторы
Даты
2023-03-31—Публикация
2022-07-08—Подача