ОБЛАСТЬ ТЕХНИКИ
[001] Настоящее изобретение относится к соединениям, селективно разрушающим андрогенные рецепторы (SARD), на основе пиррола, пиразола, имидазола, триазола и морфолина, включающим гетероциклические анилидные кольца, и их синтетическим предшественникам, R-изомерам и негидроксилированным и/или нехиральным пропанамидам и фармацевтическим композициям и способам их применения при лечении рака предстательной железы, распространенного рака предстательной железы, устойчивого к кастрации рака предстательной железы, тройного негативного рака молочной железы, других видов рака, при которых происходит экспрессия андрогенных рецепторов, андрогенной алопеции или других гиперандрогенных кожных заболеваний, болезни Кеннеди, бокового амиотрофического склероза (БАС), аневризмы брюшной аорты (ААА) и фибромы матки, а также к способам уменьшения уровня полноразмерных андрогенных рецепторов (AR-FL), включая патогенные или устойчивые мутации, сплайсированные формы AR (AR-SV) и патогенные полиглутаминовые (polyQ) полиморфные формы AR, у субъекта.
УРОВЕНЬ ТЕХНИКИ
[002] Рак предстательной железы (PCa) является одним из наиболее часто диагностируемых некожных видов рака у мужчин в США и второй по распространенности причиной смерти от рака, включая более 200000 новых случаев и более 30000 смертей за год в США. Ежегодный прирост глобального рынка средств терапии PCa составляет 15-20%.
[003] Андрогенная депривационная терапия (АДТ) является стандартом лечения распространенного PCa. Пациентам с распространенным раком предстательной железы проводят АДТ с применением рилизинг-фактора лютеинизирующего гормона (РФЛГ), антагонистов РФЛГ или путем двусторонней орхиэктомии. Несмотря на первоначальный ответ на АДТ, заболевание неизбежно прогрессирует, и рак приобретает форму устойчивого к кастрации рака предстательной железы (CRPC). До 30% пациентов с раком предстательной железы, которым проводят первичное лечение посредством лучевой терапии или хирургии, подвержены развитию метастатического заболевания в течение 10 лет после первичного лечения. Ежегодно примерно у 50000 пациентов развивается метастатическое заболевание, которое называют метастатическим CRPC (mCRPC).
[004] Медианная выживаемость пациентов с CRPC составляет 12-18 месяцев. Даже после приобретения устойчивости к кастрации дальнейший рост CRPC по-прежнему зависит от сигнального пути андрогенного рецептора (AR). Основной причиной повторного появления CRPC является реактивация AR посредством альтернативных механизмов, таких как: 1) интракринный синтез андрогенов, 2) сплайсированные формы AR (AR-SV), например, в которых отсутствует лиганд-связывающий домен (LBD), 3) мутации AR-LBD, которые могут иметь устойчивость к антагонистам AR (т.е. мутанты, которые не восприимчивы к ингибированию антагонистами AR, а в некоторых случаях антагонисты AR действуют как агонисты AR, имеющих указанные мутации LBD), и 4) амплификации гена AR в опухоли. Ключевое препятствие для успешного излечения CRPC заключается в том, что ингибиторы сигнальной системы AR, такие как энзалутамид, бикалутамид и абиратерон, действующие на LBD, не могут эффективно подавлять рост, опосредованный зависящими от N-терминального домена (NTD) AR-SV с конститутивной активностью, такими как AR-V7, который является наиболее распространенной формой AR-SV. В недавних прорывных клинических исследованиях энзалутамида и абиратерона у пациентов с CRPC было продемонстрировано, что только 13,9% пациентов с положительным статусом AR-V7 из 202 пациентов, начавших лечение энзалутамидом (Xtandi) или абиратерона ацетатом (Zytiga), имели ответ ПСА хотя бы на один из способов лечения (Antonarakis ES, Lu C, Luber B, et al. J. Clin. Oncol. 2017, April 6. doi: 10.1200 / JCO.2016.70.1961), что указывает на потребность в антагонистах AR следующего поколения, которые направленно действуют на AR-SV. Кроме того, значительное число пациентов с CRPC становятся невосприимчивыми к абиратерону или энзалутамиду, что дополнительно подчеркивает потребность в антагонистах AR следующего поколения.
[005] Имеющиеся данные демонстрируют, что рост CRPC зависит от конститутивно активных AR, включая AR-SV, в которых отсутствует LBD, такие как AR-V7, и поэтому традиционные антагонисты не могут его подавлять. Ингибирование и разрушение AR посредством связывания с доменом, отличным от AR LBD, являются альтернативными стратегиями для борьбы с CRPC.
[006] Молекулы, разрушающие AR, предотвращают любую самопроизвольную активацию AR посредством факторов роста или сигнальных путей или неконтролируемую лиганд-зависимую активацию. Кроме того, молекулы, которые ингибируют конститутивную активацию AR-SV, крайне важны для обеспечения продолжительного благоприятного действия у пациентов с CRPC.
[007] В настоящее время известно только несколько хемотипов, которые разрушают AR, включая SARD ARN-509, AZD-3514 и ASC-J9. Тем не менее, указанные молекулы разрушают AR не напрямую в концентрациях, значительно превышающих коэффициент связывания, и они не могут разрушать AR-SV, которые в последние годы стали основной причиной повторного появления CRPC, устойчивого к лечению.
[008] В настоящем изобретении описаны новые антагонисты AR с уникальной фармакологией, которые прочно (с высокой активностью и эффективностью) и селективно связывают AR (в некоторых случаях лучше, чем известные антагонисты; связывают LBD и/или NTD), действуют как антагонисты AR и разрушают полноразмерные AR (AR-FL) и AR-SV. Соединения, селективно разрушающие андрогенные рецепторы (SARD), обладают двойной функцией разрушения и ингибирования AR-SV и этим отличаются от любых доступных средств терапии CRPC. Указанные новые соединения, селективно разрушающие андрогенные рецепторы (SARD), подавляют рост клеток и опухолей PCa, пролиферация которых зависит от AR-FL и AR-SV.
[009] Развитие SARD в качестве новых терапевтических средств для лечения CRPC, которые не поддаются лечению любыми другими антагонистами, является перспективным. Указанное уникальное свойство разрушения AR-SV имеет чрезвычайно важные последствия для здоровья при раке предстательной железы. На момент подачи заявки была описана только одна серия синтетических молекул (EPI-001, EPI-506 и т.д.) и некоторые натуральные продукты, выделенные из морских организмов, такие как синкотамиды и простой глицериновый эфир нафтетенон B, которые связываются с AR-NTD и подавляют функцию AR и рост клеток PCa, но при этом имеют пониженную аффинность и не могут разрушать рецептор. SARD, описанные в настоящем документе, также связывают AR-NTD и ингибируют активность AR, опосредованную NTD (например, не зависящую от лиганда).
[0010] Положительная корреляция между AR и PCa и отсутствие надежного антагониста AR подчеркивают необходимость в молекулах, которые ингибируют функцию AR посредством новых или альтернативных механизмов и/или участков связывания и которые могут проявлять антагонистическую активность в измененной клеточной среде.
[0011] Хотя традиционные антиандрогены, такие как энзалутамид, бикалутамид и флутамид, и андрогенная депривационная терапия (АДТ) были одобрены для использования при раке предстательной железы, существуют веские доказательства того, что антиандрогены также можно применять при различных других гормонозависимых и гормононезависимых раковых заболеваниях. Например, антиандрогены исследовали при раке молочной железы (энзалутамид; Breast Cancer Res. (2014) 16(1): R7), немелкоклеточном раке легких (кшРНКи AR), почечно-клеточной карциноме (ASC-J9), злокачественных образованиях, связанных с частичным синдромом нечувствительности к андрогенам (PAIS), таких как гонадальные опухоли и семинома, распространенном раке поджелудочной железы (World J. Gastroenterology 20(29), 9229), раке яичников, фаллопиевых труб или брюшной полости, рака слюнных желез (Head and Neck (2016) 38, 724-731; АДТ исследовали при экспрессирующих AR появившихся повторно/метастатических раковых заболеваниях слюнных желез, было подтверждено благоприятное действие на конечные показатели выживаемости без прогрессирования и общей выживаемости), раке мочевого пузыря (Oncotarget 6(30), 29860-29876); Int J. Endocrinol (2015), ID статьи 384860), раке поджелудочной железы, лимфоме (включая мантийноклеточную) и печеночноклеточной карциноме. Использование более высокоактивного антиандрогена, такого как SARD, при указанных раковых заболеваниях может более эффективно излечивать прогрессирование этих и других видов рака. Лечение с применением SARD может оказывать благоприятное действие и при других раковых заболеваниях, таких как рак молочной железы (например, тройной негативный рак молочной железы (ТНРМЖ)), рак яичек, раковые заболевания, связанные с частичным синдромом нечувствительности к андрогенам (PAIS), такие как гонадальные опухоли и семинома, рак матки, рак яичников, рак фаллопиевых труб или брюшной полости, рак слюнных желез, рак мочевого пузыря, урогенитальный рак, рак мозга, рак кожи, лимфома, мантийноклеточная лимфома, рак печени, печеночноклеточная карцинома, рак почки, почечноклеточная карцинома, остеосаркома, рак поджелудочной железы, рак эндометрия, рак легкого, немелкоклеточный рак легкого (НМРЛ), рак желудка, рак толстой кишки, перианальная аденома или рак центральной нервной системы.
[0012] Тройной негативный рак молочной железы (ТНРМЖ) представляет собой тип рака молочной железы, при котором отсутствует экспрессия рецептора эстрогена (ER), рецептора прогестерона (PR) и рецепторной киназы HER2. Таким образом, при ТНРМЖ отсутствуют гормональные и киназные терапевтические мишени, на которые воздействуют при лечении других типов первичных раковых заболеваний молочной железы. Соответственно, химиотерапия часто является начальным способом фармакотерапии ТНРМЖ. Интересно, что при ТНРМЖ сохраняется экспрессия AR, это позволяет проводить направленную гормональную терапию в качестве альтернативы химиотерапии. При ER-положительном раке молочной железы AR является индикатором положительного прогноза, так как считается, что активация AR ограничивает и/или сдерживает эффекты ER в тканях и опухолях молочной железы. Тем не менее, в отсутствие ER, AR фактически может поддерживать рост раковых опухолей молочной железы. Хотя роль AR при ТНРМЖ выяснена не в полной мере, существуют доказательства того, что некоторые формы ТНРМЖ могут поддерживаться посредством андрогеннезависимой активации AR-SV, в которых отсутствует LBD, или андрогензависимой активации полноразмерных AR. Таким образом, энзалутамид и другие традиционные антагонисты AR, действующие на LBD, не обладают активностью антагониста в отношении AR-SV при указанных ТНРМЖ. Тем не менее, SARD согласно настоящему изобретению, которые могут разрушать AR-SV (см. таблицу 1 и пример 5) через участок связывания в NTD AR (см. пример 9), могут действовать как антагонисты AR, включая AR-SV, что наблюдали в ксенотрансплантатах, выделенных у пациента с ТНРМЖ, и обеспечивать противоопухолевое действие, как показано в примере 8.
[0013] Традиционные антиандрогены, такие как бикалутамид и флутамид, были одобрены для использования при раке предстательной железы. В последующих исследованиях была продемонстрирована возможность применения антиандрогенов (например, флутамида, спиронолактона, ципротерона ацетата, финастерида и хлормадинона ацетата) при андрогензависимых дерматологических состояниях, таких как андрогенная алопеция (облысение по мужскому типу), обыкновенные угри и гирсутизм (например, избыточный рост волос на лице у женщин). Препубертатная кастрация предотвращает выработку кожного сала и андрогенную алопецию, но ее эффект можно обращать вспять при использовании тестостерона, что предполагает его зависимость от андрогена.
[0014] Ген AR имеет полиморфизм повторов глутамина (polyQ) в экзоне 1, сокращение которого может способствовать трансактивации AR (т.е. гиперандрогении). Было обнаружено, что укороченные полиморфные формы polyQ чаще встречаются у людей с алопецией, гирсутизмом и акне. Использование классических антиандрогенов для этих целей нежелательно, так как они неэффективны введении через кожу, а их долгосрочное системное введение повышает риск нежелательных сексуальных эффектов, таких как гинекомастия и импотенция. Кроме того, аналогично CPRC, обсуждаемому выше, подавление активности только лигандзависимых AR может быть недостаточным, так как AR могут активироваться различными клеточными факторами, отличными от эндогенных андрогенов тестостерона (T) и дигидротестостерона (ДГТ), такими как избыточная экспрессия факторов роста, киназ, коактиваторов и/или случайная активация другими гормонами (например, эстрогенами или глюкокортикоидами). Следовательно, блокирование связывания T и ДГТ с AR при использовании классического антиандрогена может оказаться недостаточным для достижения желаемой эффективности.
[0015] Новой концепцией является местное нанесение SARD для локального разрушения AR в пораженных участках кожи или других тканей в отсутствие проявления системного антиандрогенного действия. Для указанного применения предпочтительными являются SARD, которые не проникают через кожу или быстро подвергаются метаболизму.
[0016] Подтверждением этого подхода является тот факт, что заживление кожной раны замедляется при использовании андрогенов. Кастрация мышей ускоряет заживление кожных ран и при этом уменьшает воспаление в ранах. Отрицательная корреляция между уровнем андрогенов и заживлением и воспалением кожи, отчасти объясняет еще один механизм, при котором высокий уровень эндогенных андрогенов усугубляет гиперандрогенные дерматологические состояния. Кроме того, она обосновывает целесообразность лечения ран, таких как диабетические язвы или даже травмы, или кожные нарушения с компонентом воспаления, такие как акне или псориаз, с применением местного SARD.
[0017] Андрогенная алопеция возникает у ~50% белых мужчин среднего возраста и примерно у 90%, достигших 80-летия. Миноксидил (местный сосудорасширяющий агент) и финастерид (системный ингибитор 5-альфа-редуктазы типа II) одобрены FDA при алопеции, но для достижения терапевтического эффекта требуется 4-12 месяцев лечения, при этом в большинстве случаев происходит только остановка выпадения волос, а слабое или умеренное восстановление роста волос наблюдается только в 30-60% случаев. Так как доступные в настоящее время способы лечения имеют замедленную и ограниченную эффективность, которая может сильно различаться для каждого индивидуума, и вызывают нежелательные сексуальные побочные эффекты, важно найти новый подход к лечению андрогенной алопеции и других гиперандрогенных дерматологических заболеваний.
[0018] Боковой амиотрофический склероз (БАС) является смертельным нейродегенеративным заболеванием, характеризующимся селективной утратой верхних и нижних моторных нейронов и атрофией скелетных мышц. Эпидемиологические и экспериментальные данные позволяют предположить участие андрогенов в патогенезе БАС (“Anabolic/androgenic steroid nandrolone exacerbates gene expression modifications induced by mutant SOD1 in muscles of mice models of amyotrophic lateral sclerosis.”Galbiati M, Onesto E, Zito A, Crippa V, Rusmini P, Mariotti R, Bentivoglio M, Bendotti C, Poletti A. Pharmacol. Res. 2012, 65(2), 221-230), но механизм, посредством которого андрогены модифицируют фенотип БАС, неизвестен. В модели БАС у трансгенных животных было продемонстрировано увеличение выживаемости после хирургической кастрации (т.е. андрогенной абляции). Лечение этих кастрированных животных агонистом андрогенов нандролона деканоатом ухудшило проявления болезни. Кастрация снижает уровень AR, что может являться причиной продления выживаемости. Положительное действие на выживаемость обращается вспять при введении агониста андрогенов (“Androgens affect muscle, motor neuron, and survival in a mouse model of SOD1-related amyotrophic lateral sclerosis.”Aggarwal T, Polanco MJ, Scaramuzzino C, Rocchi A, Milioto C, Emionite L, Ognio E, Sambataro F, Galbiati M, Poletti A, Pennuto M. Neurobiol. Aging. 2014 35(8), 1929-1938). Важно отметить, что стимуляция нандролона деканоатом ускоряла рекрутинг эндогенных андрогенных рецепторов в биохимические комплексы, которые были нерастворимы в додецилсульфате натрия, этот факт соответствует агрегации белка. В целом, эти результаты проливают свет на роль андрогенов в качестве модификаторов патогенеза БАС, действующих посредством нарушения регуляции гомеостаза андрогенных рецепторов. Антиандрогены должны блокировать действие нандролона ундеканоата или эндогенных андрогенов и уменьшать токсичность, вызванную агрегацией AR. Кроме того, антиандроген, который может блокировать действие LBD-зависимых агонистов AR и одновременно уменьшать уровень белка AR, такой как SARD согласно настоящему изобретению, может являться средством для терапии БАС. Рилузол является доступным лекарственным средством для лечения БАС, тем не менее, он имеет только краткосрочное действие. Существует острая необходимость в лекарственных средствах, которые продлевают выживаемость пациентов с БАС.
[0019] Действие андрогенного рецептора способствует пролиферации клеток матки. Гиперандрогенность короткоцепочечного polyQ AR связывают с ростом лейомиомы или фибромы матки. (Hsieh YY, Chang CC, Tsai FJ, Lin CC, Yeh LS, Peng CT. J. Assist. Reprod. Genet. 2004, 21(12), 453-457). В отдельном исследовании бразильских женщин было показано, что AR с более короткими и длинными аллелями с повторами [CAG](n) встречались в этом исследовании исключительно в группе женщин с лейомиомой (Rosa FE, Canevari Rde A, Ambrosio EP, Ramos Cirilo PD, Pontes A, Rainho CA, Rogatto SR. Clin. Chem. Lab. Med. 2008, 46(6), 814-823). Аналогично, у индийских женщин, наличие длинных форм polyQ AR было связано с эндометриозом и лейомиомой и могло быть отнесено к показателям высокого риска заболевания. SARD можно применять у женщин с фибромой матки, в частности у тех, у кого происходит экспрессия аллелей с более короткими и длинными повторами [CAG](n), для лечения существующей фибромы матки, предупреждения усугубления фибромы и/или уменьшения онкогенности, связанной с фибромой.
[0020] Аневризма брюшной аорты (ААА) представляет собой увеличенную область в нижней части аорты, основного кровеносного сосуда, который поставляет кровь в организм. Аорта, схожая по толщине с садовым шлангом, проходит от сердца через центр грудной клетки и брюшной полости. Поскольку аорта является основным поставщиком крови в организме, разрыв аневризмы брюшной аорты может вызвать опасное для жизни кровотечение. В зависимости от размера и скорости роста аневризмы брюшной аорты лечение может варьироваться от выжидательного наблюдения до экстренной операции. После обнаружения аневризмы брюшной аорты врачи проводят ее тщательное исследование, чтобы можно было запланировать операцию, если это необходимо. Экстренная операция на разрыве аневризмы брюшной аорты может быть рискованной. Блокада AR (фармакологическая или генетическая) уменьшает ААА. Дэвис (Davis) с соавторами (Davis JP, Salmon M, Pope NH, Lu G, Su G, Meher A, Ailawadi G, Upchurch GR Jr. J Vasc Surg (2016) 63(6):1602-1612) показали, что флутамид (50 мг/кг) или кетоконазол (150 мг/кг) уменьшали AAA, индуцированную эластазой поджелудочной железы свиней (0,35 Ед/мл), на 84,2% и 91,5% по сравнению с носителем (121%). Кроме того, у мышей AR -/- было показано уменьшение роста AAA (64,4%) по сравнению с мышами дикого типа (в обоих случаях вводили эластазу). Соответственно, введение SARD пациенту, страдающему от AAA, может способствовать обращению вспять, излечению или задержке прогрессирования AAA до того момента, при котором потребуется операция.
[0021] X-сцепленная спинально-бульбарная мышечная атрофия (SBMA-также известная как болезнь Кеннеди) представляет собой мышечную атрофию, которая возникает из-за дефекта гена андрогенных рецепторов на X-хромосоме. Слабость проксимальных мышц конечностей и мышц ротовой полости приводит к физическим ограничениям, включая в некоторых случаях необходимость использования инвалидной коляски. Мутация приводит к встраиванию длинной полиглутаминовой цепи в N-терминальный домен андрогенного рецептора (polyQ AR). Связывание и активация этого удлиненного polyQ AR эндогенными андрогенами (тестостероном и ДГТ) приводят к развертыванию и ядерной транслокации мутантного андрогенного рецептора. Индуцированная андрогенами токсичность и андрогензависимое накопление в ядре белка polyQ AR вероятно являются ключевыми факторами патогенеза. Таким образом, ингибирование активированного андрогеном polyQ AR может являться одним из способов терапии (A. Baniahmad. Inhibition of the androgen receptor by antiandrogens in spinobulbar muscle atrophy. J. Mol. Neurosci. 2016 58(3), 343-347). Эти стадии требуются для патогенеза и приводят к частичной потере функции трансактивации (т.е. к нечувствительности к андрогенам) и слабоизученной нейромышечной дегенерации. Обоснование использования антиандрогенов приведено в отчете, согласно которому антиандроген флутамид обеспечивает защиту самцов мышей от андрогензависимой токсичности в трех моделях спинально-бульбарной мышечной атрофии (Renier KJ, Troxell-Smith SM, Johansen JA, Katsuno M, Adachi H, Sobue G, Chua JP, Sun Kim H, Lieberman AP, Breedlove SM, Jordan CL. Endocrinology 2014, 155(7), 2624-2634). В настоящее время отсутствуют способы лечения, модифицирующие заболевание, имеются только способы, направленные на симптомы. Попытки направленного воздействия на polyQ AR, который является медиатором токсичности первого порядка, при болезни Кеннеди посредством изменения клеточного строения для ускорения его разрушения, т.е. при использовании SARD, являются перспективными для терапевтического вмешательства. Агенты, селективно разрушающие андрогенные рецепторы, такие как те, что описаны в настоящем документе, связывают и разрушают все исследуемые андрогенные рецепторы (полноразмерные, сплайсированные формы, мутанты, устойчивые к антиандрогенам, и т.д.), таким образом, можно ожидать разрушение и полиморфных форм polyQ AR, это указывает на то, что они являются многообещающими средствами для лечения SBMA.
[0022] В настоящем документе описаны, помимо прочего, соединения, селективно разрушающие андрогенные рецепторы (SARD), на основе пиррола, пиразола, триазола, имидазола и морфолина, которые могут связывать LBD и/или в качестве альтернативы домен связывания и разрушения (BDD), расположенный в NTD, действовать как антагонисты AR и разрушать AR, блокируя тем самым лигандзависимую и лиганднезависимую активность AR. Этот новый механизм обеспечивает улучшенную эффективность при системном (например, при раке предстательной железы) или местном введении (например, при дерматологических заболеваниях).
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0023] Один из вариантов реализации включает соединение, селективно разрушающее андрогенные рецепторы (SARD), представленное структурой формулы I:
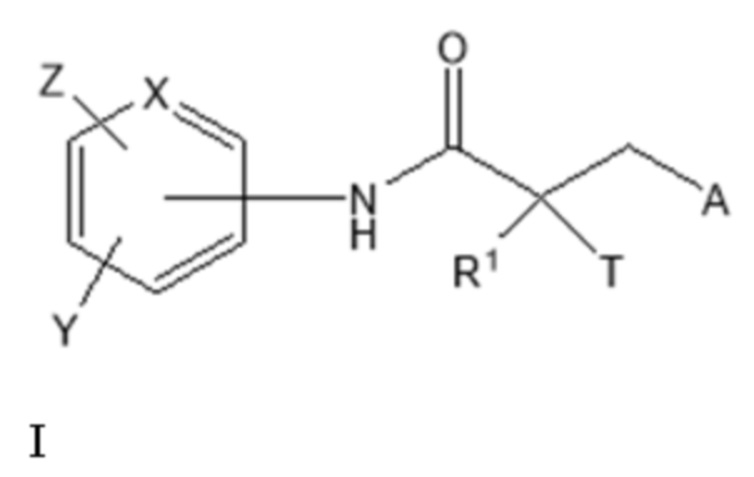
где
T представляет собой H, OH, OR, OCOR, CH3, -NHCOCH3 или NHCOR;
R1 представляет собой H, CH3, CH2F, CHF2, CF3, CH2CH3 или CF2CF3;
или T и R1 образуют 3-8-членное карбоциклическое или гетероциклическое кольцо;
Y представляет собой H, CF3, F, I, Br, Cl, CN или C(R)3;
Z представляет собой H, NO2, CN, галогенид, COOH, COR, NHCOR, CONHR,
или Y и Z образуют 5-8-членное конденсированное кольцо;
X представляет собой CH или N;
R представляет собой H, алкил, алкенил, галогеналкил, спирт, CH2CH2OH, CF3, CH2Cl, CH2CH2Cl, арил, F, Cl, Br, I или OH;
A представляет собой R2 или R3;
R2 представляет собой пяти- или шестичленное насыщенное или ненасыщенное кольцо, содержащее по меньшей мере один атом азота и 0, 1 или 2 двойные связи, необязательно замещенное по меньшей мере одним из Q1, Q2, Q3 или Q4, каждый из которых независимо выбран из водорода, кето, замещенного или незамещенного линейного или разветвленного алкила, замещенного или незамещенного циклоалкила, замещенного или незамещенного гетероциклоалкила, галогеналкила, CF3, замещенного или незамещенного арила, замещенного или незамещенного фенила, F, Cl, Br, I, CN, NO2, гидроксила, алкокси, OR, арилалкила, NCS, малеимида, NHCOOR, N(R)2, NHCOR, CONHR, COOR или COR;
R3 представляет собой NHR2, галогенид, N3, OR4, CF3, COR4, COCl, COOCOR4, COOR4, OCOR4, OCONHR4, NHCOOR4, NHCONHR4, OCOOR4, CN, CONH2, CONH(R4), CON(R4)2, SR4, SO2R4, SOR4, SO3H, SO2NH2, SO2NH(R4), SO2N(R4)2, NH2, NH(R4), N(R4)2, CO(N-гетероцикл), C(O)(C1-C10)алкил, NO2, цианат, изоцианат, тиоцианат, изотиоцианат, мезилат, тозилат, трифлат, PO(OH)2 или OPO(OH)2; и
R4 представляет собой H, алкил, галогеналкил, циклоалкил, арил или гетероарил, причем указанные алкильные, галогеналкильные, циклоалкильные, арильные или гетероарильные группы необязательно замещены;
или его оптический изомер, изомер, фармацевтически приемлемую соль, фармацевтический продукт, полиморф, гидрат или любую их комбинацию;
где если A представляет собой Br или I, R1 представляет собой CH3, и T представляет собой OH, то X представляет собой N, или анилиновое кольцо образует конденсированное гетероциклическое кольцо.
[0024] В другом варианте реализации настоящее изобретение относится к соединению SARD, представленному структурой формулы IA:
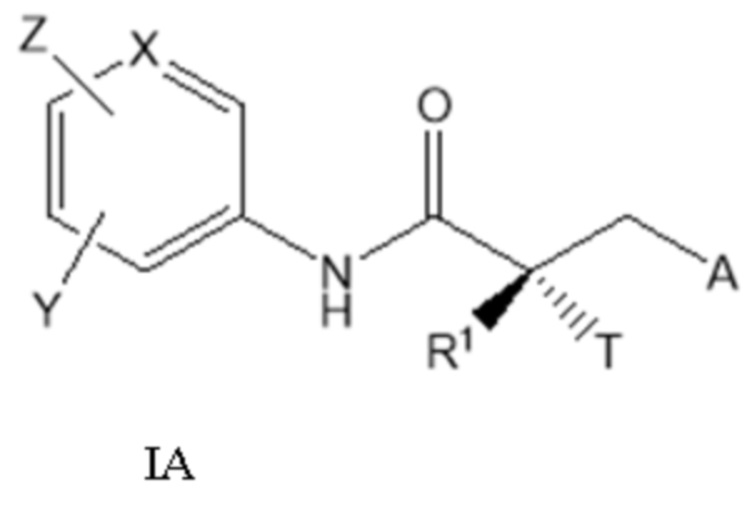
где
T представляет собой H, OH, OR, OCOR, CH3, -NHCOCH3 или NHCOR;
R1 представляет собой H, CH3, CH2F, CHF2, CF3, CH2CH3 или CF2CF3;
или T и R1 образуют 3-8-членное карбоциклическое или гетероциклическое кольцо;
Y представляет собой H, CF3, F, I, Br, Cl, CN или C(R)3;
Z представляет собой H, NO2, CN, галогенид, COOH, COR, NHCOR, CONHR,
или Y и Z образуют 5-8-членное конденсированное кольцо;
X представляет собой CH или N;
R представляет собой H, алкил, алкенил, галогеналкил, спирт, CH2CH2OH, CF3, CH2Cl, CH2CH2Cl, арил, F, Cl, Br, I или OH;
A представляет собой R2 или R3;
R2 представляет собой пяти- или шестичленное насыщенное или ненасыщенное кольцо, содержащее по меньшей мере один атом азота и 0, 1 или 2 двойные связи, необязательно замещенное по меньшей мере одним из Q1, Q2, Q3 или Q4, каждый из которых независимо выбран из водорода, кето, замещенного или незамещенного линейного или разветвленного алкила, замещенного или незамещенного циклоалкила, замещенного или незамещенного гетероциклоалкила, галогеналкила, CF3, замещенного или незамещенного арила, замещенного или незамещенного фенила, F, Cl, Br, I, CN, NO2, гидроксила, алкокси, OR, арилалкила, NCS, малеимида, NHCOOR, N(R)2, NHCOR, CONHR, COOR или COR;
R3 представляет собой, NHR2, галогенид, N3, OR4, CF3, COR4, COCl, COOCOR4, COOR4, OCOR4, OCONHR4, NHCOOR4, NHCONHR4, OCOOR4, CN, CONH2, CONH(R4), CON(R4)2, SR4, SO2R4, SOR4 SO3H, SO2NH2, SO2NH(R4), SO2N(R4)2, NH2, NH(R4), N(R4)2, CO(N-гетероцикл), C(O)(C1-C10)алкил, NO2, цианат, изоцианат, тиоцианат, изотиоцианат, мезилат, тозилат, трифлат, PO(OH)2 или OPO(OH)2; и
R4 представляет собой H, алкил, галогеналкил, циклоалкил, арил или гетероарил, причем указанные алкильные, галогеналкильные, циклоалкильные, арильные или гетероарильные группы необязательно замещены;
или его изомер, фармацевтически приемлемую соль, фармацевтический продукт, полиморф, гидрат или любую их комбинацию;
где если A представляет собой Br или I, R1 представляет собой CH3, и T представляет собой OH, то X представляет собой N, или анилиновое кольцо образует конденсированное гетероциклическое кольцо.
[0025] В другом варианте реализации настоящее изобретение относится к соединению SARD, представленному структурой формулы IB:
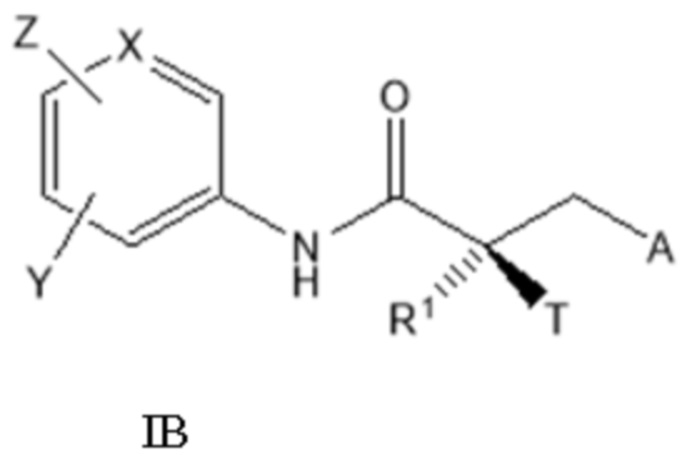
где
T представляет собой H, OH, OR, OCOR, CH3, -NHCOCH3 или NHCOR;
R1 представляет собой H, CH3, CH2F, CHF2, CF3, CH2CH3 или CF2CF3;
или T и R1 образуют 3-8-членное карбоциклическое или гетероциклическое кольцо;
Y представляет собой H, CF3, F, I, Br, Cl, CN или C(R)3;
Z представляет собой H, NO2, CN, галогенид, COOH, COR, NHCOR, CONHR,
или Y и Z образуют 5-8-членное конденсированное кольцо;
X представляет собой CH или N;
R представляет собой H, алкил, алкенил, галогеналкил, спирт, CH2CH2OH, CF3, CH2Cl, CH2CH2Cl, арил, F, Cl, Br, I или OH;
A представляет собой R2 или R3;
R2 представляет собой пяти- или шестичленное насыщенное или ненасыщенное кольцо, содержащее по меньшей мере один атом азота и 0, 1 или 2 двойные связи, необязательно замещенное по меньшей мере одним из Q1, Q2, Q3 или Q4, каждый из которых независимо выбран из водорода, кето, замещенного или незамещенного линейного или разветвленного алкила, замещенного или незамещенного циклоалкила, замещенного или незамещенного гетероциклоалкила, галогеналкила, CF3, замещенного или незамещенного арила, замещенного или незамещенного фенила, F, Cl, Br, I, CN, NO2, гидроксила, алкокси, OR, арилалкила, NCS, малеимида, NHCOOR, N(R)2, NHCOR, CONHR, COOR или COR;
R3 представляет собой NHR2, галогенид, N3, OR4, CF3, COR4, COCl, COOCOR4, COOR4, OCOR4, OCONHR4, NHCOOR4, NHCONHR4, OCOOR4, CN, CONH2, CONH(R4), CON(R4)2, SR4, SO2R4, SOR4 SO3H, SO2NH2, SO2NH(R4), SO2N(R4)2, NH2, NH(R4), N(R4)2, CO(N-гетероцикл), NO2, цианат, изоцианат, тиоцианат, изотиоцианат, мезилат, тозилат, трифлат, PO(OH)2 или OPO(OH)2; и
R4 представляет собой H, алкил, галогеналкил, циклоалкил, арил или гетероарил, причем указанные алкильные, галогеналкильные, циклоалкильные, арильные или гетероарильные группы необязательно замещены;
или его изомер, фармацевтически приемлемую соль, фармацевтический продукт, полиморф, гидрат или любую их комбинацию;
где если A представляет собой Br или I, R1 представляет собой CH3, и T представляет собой OH, то X представляет собой N, или анилиновое кольцо образует конденсированное гетероциклическое кольцо.
[0026] Изобретение включает соединение SARD, представленное структурой формулы II:
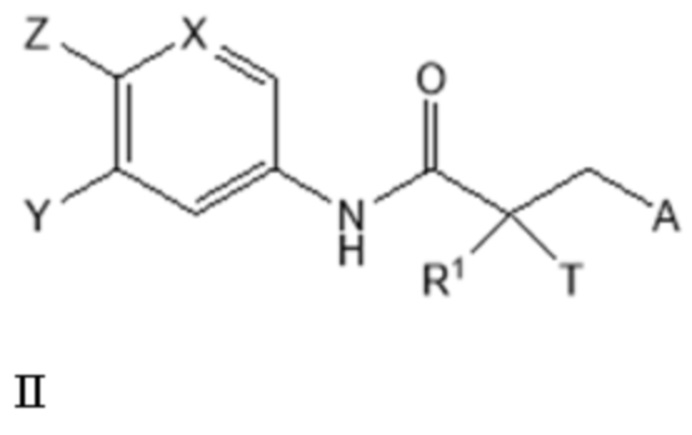
где
T представляет собой H, OH, OR, OCOR, CH3, -NHCOCH3 или NHCOR;
R1 представляет собой H, CH3, CH2F, CHF2, CF3, CH2CH3 или CF2CF3;
или T и R1 образуют 3-8-членное карбоциклическое или гетероциклическое кольцо;
Y представляет собой H, CF3, F, I, Br, Cl, CN или C(R)3;
Z представляет собой H, NO2, CN, галогенид, COOH, COR, NHCOR, CONHR,
или Y и Z образуют 5-8- членное конденсированное кольцо;
X представляет собой CH или N;
R представляет собой H, алкил, алкенил, галогеналкил, спирт, CH2CH2OH, CF3, CH2Cl, CH2CH2Cl, арил, F, Cl, Br, I или OH;
A представляет собой R2 или R3;
R2 представляет собой пиррольное, пирролиновое, пирролидиновое, пиразольное, пиразолиновое, пиразолидиновое, триазольное, имидазольное, имидазолиновое, имидазолидиновое или морфолиновое кольцо, причем указанное кольцо необязательно замещено по меньшей мере одним из Q1, Q2, Q3 или Q4, каждый из которых независимо выбран из водорода, кето, замещенного или незамещенного линейного или разветвленного алкила, замещенного или незамещенного циклоалкила, замещенного или незамещенного гетероциклоалкила, галогеналкила, CF3, замещенного или незамещенного арила, замещенного или незамещенного фенила, F, Cl, Br, I, CN, NO2, гидроксила, алкокси, OR, арилалкила, NCS, малеимида, NHCOOR, N(R)2, NHCOR, CONHR, COOR или COR;
R3 представляет собой NHR2, галогенид, N3, OR4, CF3, COR4, COCl, COOCOR4, COOR4, OCOR4, OCONHR4, NHCOOR4, NHCONHR4, OCOOR4, CN, CONH2, CONH(R4), CON(R4)2, SR4, SO2R4, SOR4 SO3H, SO2NH2, SO2NH(R4), SO2N(R4)2, NH2, NH(R4), N(R4)2, CO(N-гетероцикл), NO2, цианат, изоцианат, тиоцианат, изотиоцианат, мезилат, тозилат, трифлат, PO(OH)2 или OPO(OH)2; и
R4 представляет собой H, алкил, галогеналкил, циклоалкил, арил или гетероарил, причем указанные алкильные, галогеналкильные, циклоалкильные, арильные или гетероарильные группы необязательно замещены;
или его оптический изомер, изомер, фармацевтически приемлемую соль, фармацевтический продукт, полиморф, гидрат или любую их комбинацию;
где если A представляет собой Br или I, R1 представляет собой CH3, и T представляет собой OH, то X представляет собой N, или анилиновое кольцо образует конденсированное гетероциклическое кольцо.
[0027] В другом варианте реализации настоящее изобретение относится к соединению SARD, представленному структурой формулы IIA:
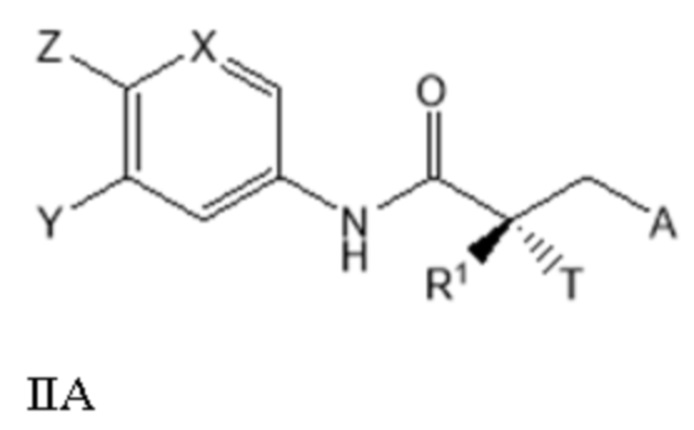
где
T представляет собой H, OH, OR, OCOR, CH3, -NHCOCH3 или NHCOR;
R1 представляет собой H, CH3, CH2F, CHF2, CF3, CH2CH3 или CF2CF3;
или T и R1 образуют 3-8-членное карбоциклическое или гетероциклическое кольцо;
Y представляет собой H, CF3, F, I, Br, Cl, CN или C(R)3;
Z представляет собой H, NO2, CN, галогенид, COOH, COR, NHCOR, CONHR,
или Y и Z образуют 5-8-членное конденсированное кольцо;
X представляет собой CH или N;
R представляет собой H, алкил, алкенил, галогеналкил, спирт, CH2CH2OH, CF3, CH2Cl, CH2CH2Cl, арил, F, Cl, Br, I или OH;
A представляет собой R2 или R3;
R2 представляет собой пиррольное, пирролиновое, пирролидиновое, пиразольное, пиразолиновое, пиразолидиновое, триазольное, имидазольное, имидазолиновое, имидазолидиновое или морфолиновое кольцо, причем указанное кольцо необязательно замещено по меньшей мере одним из Q1, Q2, Q3 или Q4, каждый из которых независимо выбран из водорода, кето, замещенного или незамещенного линейного или разветвленного алкила, замещенного или незамещенного циклоалкила, замещенного или незамещенного гетероциклоалкила, галогеналкила, CF3, замещенного или незамещенного арила, замещенного или незамещенного фенила, F, Cl, Br, I, CN, NO2, гидроксила, алкокси, OR, арилалкила, NCS, малеимида, NHCOOR, N(R)2, NHCOR, CONHR, COOR или COR;
R3 представляет собой NHR2, галогенид, N3, OR4, CF3, COR4, COCl, COOCOR4, COOR4, OCOR4, OCONHR4, NHCOOR4, NHCONHR4, OCOOR4, CN, CONH2, CONH(R4), CON(R4)2, SR4, SO2R4, SOR4 SO3H, SO2NH2, SO2NH(R4), SO2N(R4)2, NH2, NH(R4), N(R4)2, CO(N-гетероцикл), NO2, цианат, изоцианат, тиоцианат, изотиоцианат, мезилат, тозилат, трифлат, PO(OH)2 или OPO(OH)2; и
R4 представляет собой H, алкил, галогеналкил, циклоалкил, арил или гетероарил, причем указанные алкильные, галогеналкильные, циклоалкильные, арильные или гетероарильные группы необязательно замещены;
или его изомер, фармацевтически приемлемую соль, фармацевтический продукт, полиморф, гидрат или любую их комбинацию;
где если A представляет собой Br или I, R1 представляет собой CH3, и T представляет собой OH, то X представляет собой N, или анилиновое кольцо образует конденсированное гетероциклическое кольцо.
[0028] В другом варианте реализации настоящее изобретение относится к соединению SARD, представленному структурой формулы IIB:
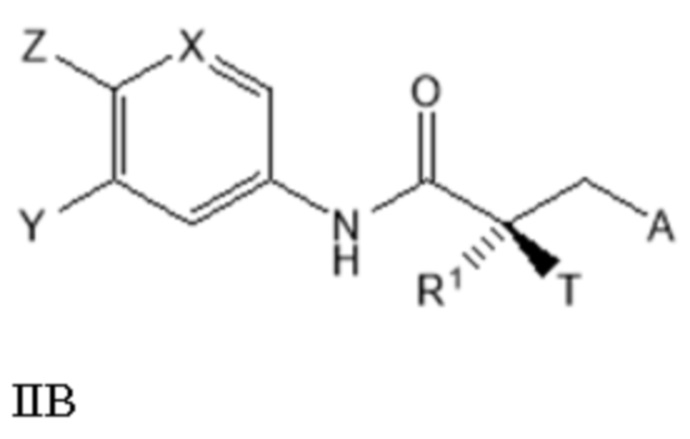
где
T представляет собой H, OH, OR, OCOR, CH3, -NHCOCH3 или NHCOR;
R1 представляет собой H, CH3, CH2F, CHF2, CF3, CH2CH3 или CF2CF3;
или T и R1 образуют 3-8-членное карбоциклическое или гетероциклическое кольцо;
Y представляет собой H, CF3, F, I, Br, Cl, CN или C(R)3;
Z представляет собой H, NO2, CN, галогенид, COOH, COR, NHCOR, CONHR,
или Y и Z образуют 5-8-членное конденсированное кольцо;
X представляет собой CH или N;
R представляет собой H, алкил, алкенил, галогеналкил, спирт, CH2CH2OH, CF3, CH2Cl, CH2CH2Cl, арил, F, Cl, Br, I или OH;
A представляет собой R2 или R3;
R2 представляет собой пиррольное, пирролиновое, пирролидиновое, пиразольное, пиразолиновое, пиразолидиновое, триазольное, имидазольное, имидазолиновое, имидазолидиновое или морфолиновое кольцо, причем указанное кольцо необязательно замещено по меньшей мере одним из Q1, Q2, Q3 или Q4, каждый из которых независимо выбран из водорода, кето, замещенного или незамещенного линейного или разветвленного алкила, замещенного или незамещенного циклоалкила, замещенного или незамещенного гетероциклоалкила, галогеналкила, CF3, замещенного или незамещенного арила, замещенного или незамещенного фенила, F, Cl, Br, I, CN, NO2, гидроксила, алкокси, OR, арилалкила, NCS, малеимида, NHCOOR, N(R)2, NHCOR, CONHR, COOR или COR;
R3 представляет собой NHR2, галогенид, N3, OR4, CF3, COR4, COCl, COOCOR4, COOR4, OCOR4, OCONHR4, NHCOOR4, NHCONHR4, OCOOR4, CN, CONH2, CONH(R4), CON(R4)2, SR4, SO2R4, SOR4 SO3H, SO2NH2, SO2NH(R4), SO2N(R4)2, NH2, NH(R4), N(R4)2, CO(N-гетероцикл), NO2, цианат, изоцианат, тиоцианат, изотиоцианат, мезилат, тозилат, трифлат, PO(OH)2 или OPO(OH)2; и
R4 представляет собой H, алкил, галогеналкил, циклоалкил, арил или гетероарил, причем указанные алкильные, галогеналкильные, циклоалкильные, арильные или гетероарильные группы необязательно замещены;
или его изомер, фармацевтически приемлемую соль, фармацевтический продукт, полиморф, гидрат или любую их комбинацию;
где если A представляет собой Br или I, R1 представляет собой CH3, и T представляет собой OH, то X представляет собой N, или анилиновое кольцо образует конденсированное гетероциклическое кольцо.
[0029] В другом варианте реализации изобретение относится к соединению, селективно разрушающему андрогенные рецепторы, представленному структурой формулы VII:
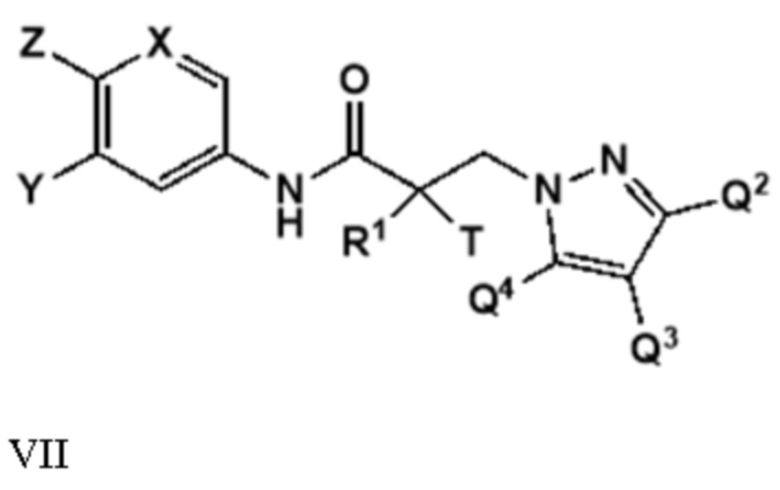
где
X представляет собой CH или N;
Y представляет собой H, CF3, F, I, Br, Cl, CN или C(R)3;
Z представляет собой H, NO2, CN, галогенид, COOH, COR, NHCOR, CONHR,
или Y и Z образуют 5-8-членное конденсированное кольцо;
R1 представляет собой H, CH3, CH2F, CHF2, CF3, CH2CH3 или CF2CF3;
T представляет собой H, OH, OR, OCOR, CH3, -NHCOCH3 или NHCOR;
или T и R1 образуют 3-8-членное карбоциклическое или гетероциклическое кольцо;
R представляет собой H, алкил, алкенил, галогеналкил, спирт, CH2CH2OH, CF3, CH2Cl, CH2CH2Cl, арил, F, Cl, Br, I или OH; и
каждый из Q2, Q3 или Q4 независимо выбран из водорода, кето, замещенного или незамещенного линейного или разветвленного алкила, замещенного или незамещенного циклоалкила, замещенного или незамещенного гетероциклоалкила, галогеналкила, CF3, замещенного или незамещенного арила, замещенного или незамещенного фенила, F, Cl, Br, I, CN, NO2, гидроксила, алкокси, OR, арилалкила, NCS, малеимида, NHCOOR, N(R)2, NHCOR, CONHR, COOR или COR; или его оптический изомер, изомер, фармацевтически приемлемую соль, фармацевтический продукт, полиморф, гидрат или любую их комбинацию.
[0030] В другом варианте реализации изобретение включает соединение, селективно разрушающее андрогенные рецепторы, представленное структурой формулы VIIA:
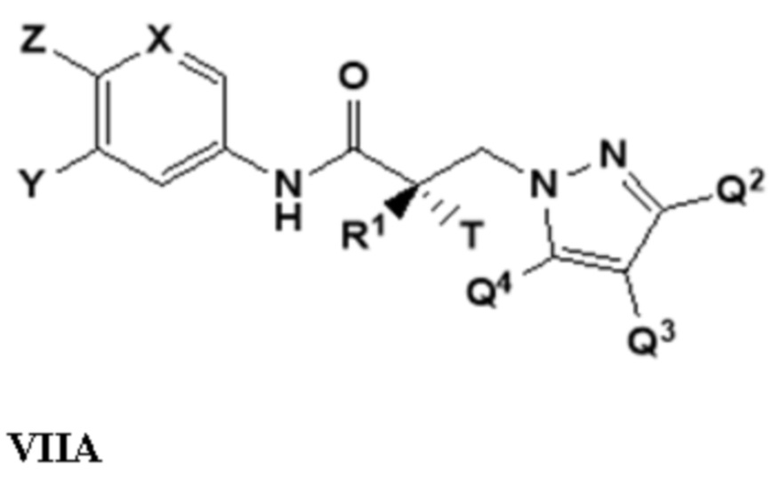
где
X представляет собой CH или N;
Y представляет собой H, CF3, F, I, Br, Cl, CN или C(R)3;
Z представляет собой H, NO2, CN, галогенид, COOH, COR, NHCOR, CONHR,
или Y и Z образуют 5-8-членное конденсированное кольцо;
R1 представляет собой H, CH3, CH2F, CHF2, CF3, CH2CH3 или CF2CF3;
T представляет собой H, OH, OR, OCOR, CH3, -NHCOCH3 или NHCOR;
или T и R1 образуют 3-8-членное карбоциклическое или гетероциклическое кольцо;
R представляет собой H, алкил, алкенил, галогеналкил, спирт, CH2CH2OH, CF3, CH2Cl, CH2CH2Cl, арил, F, Cl, Br, I или OH; и
каждый из Q2, Q3 или Q4 независимо выбран из водорода, кето, замещенного или незамещенного линейного или разветвленного алкила, замещенного или незамещенного циклоалкила, замещенного или незамещенного гетероциклоалкила, галогеналкила, CF3, замещенного или незамещенного арила, замещенного или незамещенного фенила, F, Cl, Br, I, CN, NO2, гидроксила, алкокси, OR, арилалкила, NCS, малеимида, NHCOOR, N(R)2, NHCOR, CONHR, COOR или COR; или его изомер, фармацевтически приемлемую соль, фармацевтический продукт, полиморф, гидрат или любую их комбинацию.
[0031] В другом варианте реализации изобретение включает соединение, селективно разрушающее андрогенные рецепторы, представленное структурой формулы VIIB:
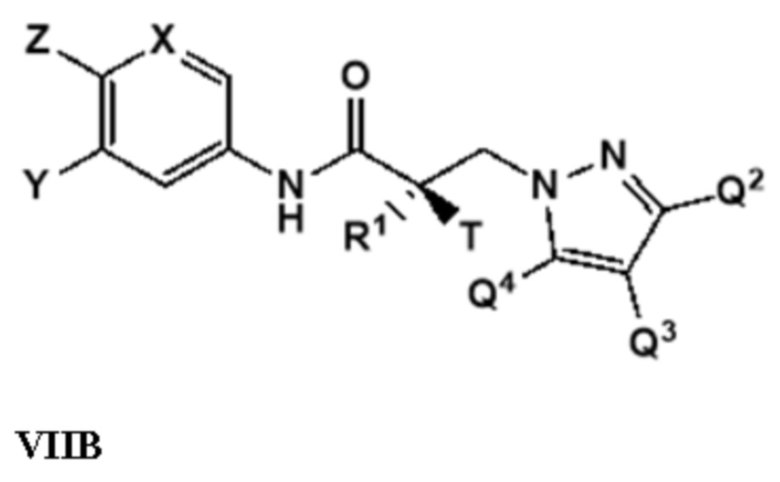
где
X представляет собой CH или N;
Y представляет собой H, CF3, F, I, Br, Cl, CN или C(R)3;
Z представляет собой H, NO2, CN, галогенид, COOH, COR, NHCOR, CONHR,
или Y и Z образуют 5-8-членное конденсированное кольцо;
R1 представляет собой H, CH3, CH2F, CHF2, CF3, CH2CH3 или CF2CF3;
T представляет собой H, OH, OR, OCOR, CH3, -NHCOCH3 или NHCOR;
или T и R1 образуют 3-8-членное карбоциклическое или гетероциклическое кольцо;
R представляет собой H, алкил, алкенил, галогеналкил, спирт, CH2CH2OH, CF3, CH2Cl, CH2CH2Cl, арил, F, Cl, Br, I или OH;
и
каждый из Q2, Q3 или Q4 независимо выбран из водорода, кето, замещенного или незамещенного линейного или разветвленного алкила, замещенного или незамещенного циклоалкила, замещенного или незамещенного гетероциклоалкила, галогеналкила, CF3, замещенного или незамещенного арила, замещенного или незамещенного фенила, F, Cl, Br, I, CN, NO2, гидроксила, алкокси, OR, арилалкила, NCS, малеимида, NHCOOR, N(R)2, NHCOR, CONHR, COOR или COR; или его изомер, фармацевтически приемлемую соль, фармацевтический продукт, полиморф, гидрат или любую их комбинацию.
Еще один вариант реализации изобретения включает соединение SARD, представленное структурой любого из следующих соединений:
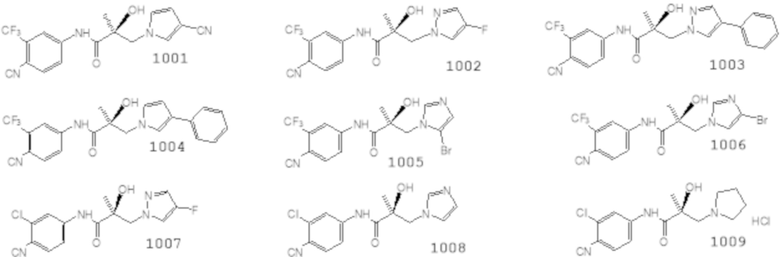
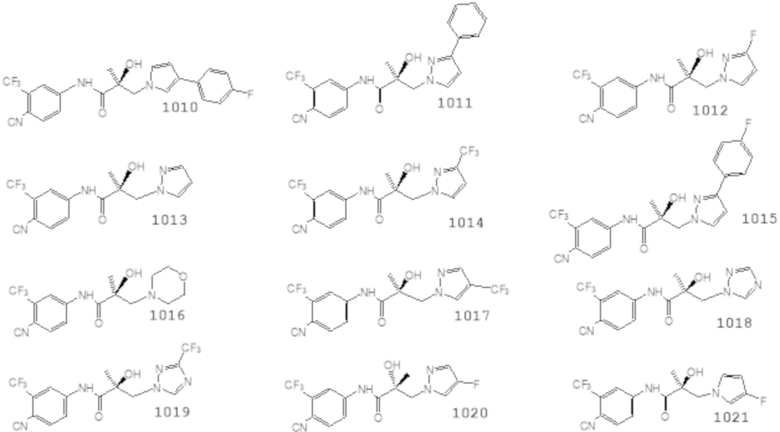
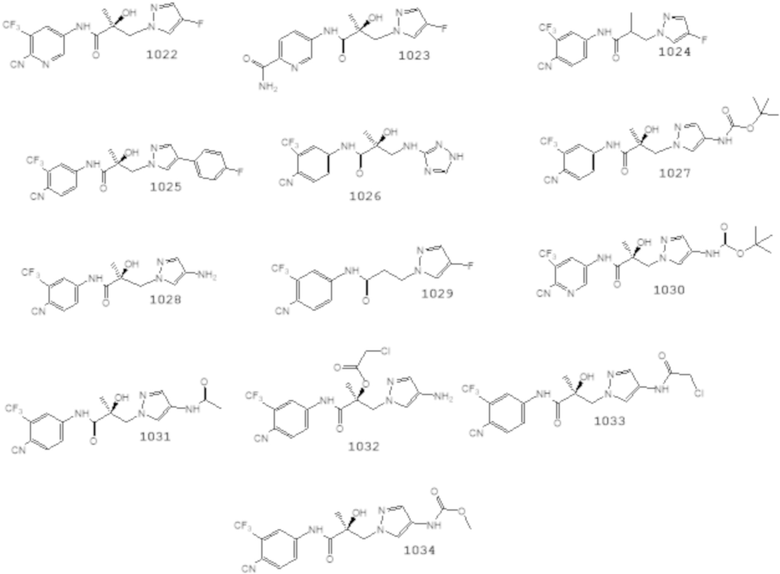
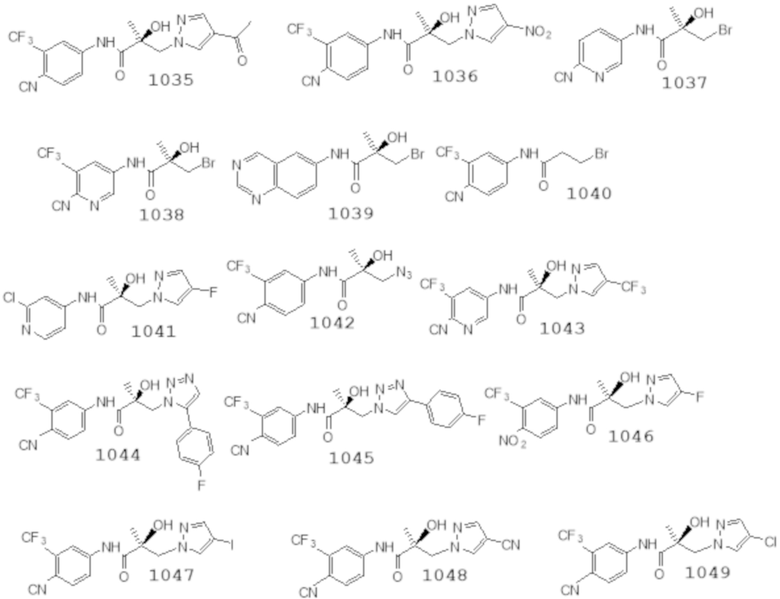 .
.
[0032] Один из вариантов реализации изобретения включает соединение SARD, обладающее по меньшей мере одним из следующих свойств: связывает AR через альтернативный домен связывания и разрушения (BDD), например, в NTD; связывает AR через лиганд-связывающий домен (LBD) AR; имеет разрушающую активность в отношении сплайсированной формы AR (AR-SV); имеет разрушающую активность в отношении полноразмерного AR (AR-FL), включая его патогенные мутации; имеет ингибирующую активность в отношении AR-SV (т.е. активность антагониста AR-SV); имеет ингибирующую активность в отношении AR-FL (т.е. активность антагониста AR-FL), включая его патогенные мутации; обладает двойной функцией разрушения AR-SV и ингибирования AR-SV; и/или двойной функцией разрушения AR-FL и ингибирования AR-FL.
[0033] Другой вариант реализации изобретения включает фармацевтические композиции, содержащие соединение SARD согласно настоящему изобретению или его изомер, фармацевтически приемлемую соль, фармацевтический продукт, полиморф, гидрат или любую их комбинацию и фармацевтически приемлемый носитель. Фармацевтическая композиция может быть предназначена для местного применения. Местная фармацевтическая композиция может представлять собой раствор, лосьон, бальзам, крем, мазь, липосому, состав для распыления, гель, пену, шариковый стик, очищающее жидкое или брусковое мыло, эмульсию, мусс, аэрозоль или шампунь.
[0034] Изобретение включает способ лечения рака предстательной железы (PCa) или продления выживаемости субъекта мужского пола, нуждающегося в лечении, включающий введение субъекту терапевтически эффективного количества соединения формулы I -VII, IA-ID, IIA, IIB, VIIA или VIIB или любого из соединений 1001-1049. Рак предстательной железы включает, но не ограничивается ими, распространенный рак предстательной железы, устойчивый к кастрации рак предстательной железы (CRPC), метастатический CRPC (mCRPC), неметастатический CRPC (nmCRPC), nmCRPC высокого риска или любую их комбинацию. Другой вариант реализации изобретения включает способ, дополнительно включающий проведение андрогенной депривационной терапии. В качестве альтернативы способ может излечивать рак предстательной железы или другой вид рака, устойчивый к способу лечения с использованием известного(-ых) антагониста(-ов) андрогенных рецепторов или АДТ. В другом варианте реализации способ может излечивать устойчивый к энзалутамиду рак предстательной железы. В другом варианте реализации способ может излечивать устойчивый к абиратерону рак предстательной железы. Еще один вариант реализации изобретения включает способ лечения рака предстательной железы или другого вида рака, устойчивого к антагонисту AR, с применением соединения SARD согласно настоящему изобретению, где антагонист(-ы) андрогенных рецепторов представляет(-ют) собой по меньшей мере одно из энзалутамида, бикалутамида, абиратерона, ARN-509, ODM-201, EPI-001, EPI-506, AZD-3514, галетерона, ASC-J9, флутамида, гидроксифлутамида, нилутамида, ципротерона ацетата, кетоконазола или спиронолактона.
[0035] Еще один вариант реализации изобретения включает способ лечения рака предстательной железы или других раковых заболеваний с применением соединения SARD согласно настоящему изобретению, где другие раковые заболевания выбраны из рака молочной железы, такого как тройной негативный рак молочной железы (ТНРМЖ), рака яичек, раковых заболеваний, связанных с частичным синдромом нечувствительности к андрогенам (PAIS), таких как гонадальные опухоли и семинома, рака матки, рака яичников, рака фаллопиевых труб или брюшной полости, рака слюнных желез, рака мочевого пузыря, урогенитального рака, рака мозга, рака кожи, лимфомы, мантийноклеточной лимфомы, рака печени, печеночноклеточной карциномы, рака почки, почечноклеточной карциномы, остеосаркомы, рака поджелудочной железы, рака эндометрия, рака легкого, немелкоклеточного рака легкого (НМРЛ), рака желудка, рака толстой кишки, перианальной аденомы или рака центральной нервной системы. В другом варианте реализации рак молочной железы представляет собой тройной негативный рак молочной железы (ТНРМЖ).
[0036] Изобретение включает способ уменьшения уровня сплайсированных форм AR у субъекта, включающий введение субъекту терапевтически эффективного количества соединения согласно настоящему изобретению или его изомера, фармацевтически приемлемой соли, фармацевтического продукта, полиморфа, гидрата или любой их комбинации. Способ дополнительно может включать уменьшение уровня полноразмерного AR у субъекта.
[0037] Другой вариант реализации изобретения включает способ лечения болезни Кеннеди у субъекта, включающий введение субъекту соединения формулы I -VII, IA-ID, IIA, IIB, VIIA или VIIB или соединения другой формулы согласно настоящему изобретению.
[0038] Еще один вариант реализации изобретения включает способ: (a) лечения акне у субъекта, например, обыкновенных угрей; (b) уменьшения выработки кожного сала у субъекта, например, для лечения себореи, себорейного дерматита или акне; (c) лечения гирсутизма у субъекта, например, избыточного роста волос на лице у женщин; (d) лечения алопеции у субъекта, например, андрогенной алопеции, гнездной алопеции, алопеции, вызванной химиотерапией, алопеции, вызванной лучевой терапией, алопеции, вызванной рубцеванием, или алопеции, вызванной стрессом; (e) лечения гормонального состояния у женщин, например, преждевременного полового созревания, раннего полового созревания, дисменореи, аменореи, синдрома многокамерной матки, эндометриоза, гистеромиомы, аномального маточного кровотечения, раннего менархе, фиброкистозной болезни молочной железы, фибромы матки, кисты яичников, синдрома поликистозных яичников, преэклампсии, эклампсии беременных, преждевременных родов, предменструального синдрома или вагинальной сухости; (f) лечения половой перверсии, гиперсексуальности или парафилии у субъекта; (g) лечения андрогенного психоза у субъекта; (h) лечения вирилизации у субъекта; (i) лечения полного или частичного синдрома нечувствительности к андрогенам у субъекта; (j) увеличения или модуляции овуляции у животного; (k) лечения рака у субъекта; или любую их комбинацию, путем введения соединения согласно настоящему изобретению или содержащей его фармацевтической композиции.
[0039] Один из вариантов реализации изобретения включает способы уменьшения уровня полиглутаминовых полиморфов (polyQ) AR у субъекта, включающие введение соединения согласно настоящему изобретению. Способ может подавлять, разрушать функцию полиглутаминовых (polyQ) полиморфов AR (polyQ-AR) или обеспечивать оба указанных действия. PolyQ-AR может представлять собой короткоцепочечный полиморф polyQ или длинноцепочечный полиморф polyQ. Если polyQ-AR представляет собой короткоцепочечный полиморф polyQ, то способ дополнительно излечивает кожное заболевание. Если polyQ-AR представляет собой длинноцепочечный полиморф polyQ, то способ дополнительно излечивает болезнь Кеннеди.
[0040] Другой вариант реализации изобретения включает способы лечения бокового амиотрофического склероза (БАС) у субъекта путем введения терапевтически эффективного количества соединения согласно настоящему изобретению или его изомера, фармацевтически приемлемой соли, фармацевтического продукта, полиморфа, гидрата или любой их комбинации; или содержащей его фармацевтической композиции.
[0041] Другой вариант реализации изобретения включает способы лечения аневризмы брюшной аорты (AAA) у субъекта путем введения терапевтически эффективного количества соединения согласно настоящему изобретению или его изомера, фармацевтически приемлемой соли, фармацевтического продукта, полиморфа, гидрата или любой их комбинации; или содержащей его фармацевтической композиции.
[0042] Еще один вариант реализации изобретения включает способы лечения фибромы матки у субъекта путем введения терапевтически эффективного количества соединения согласно настоящему изобретению или его изомера, фармацевтически приемлемой соли, фармацевтического продукта, полиморфа, гидрата или любой их комбинации; или содержащей его фармацевтической композиции.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0043] Объект, рассматриваемый в качестве изобретения, конкретным образом описан и явным образом заявлен в заключительной части описания. Тем не менее, изобретение в частях, касающихся его устройства и способа реализации, а также его задачи, отличительные признаки и преимущества, станут более понятны после изучения последующего подробного описания совместно с прилагаемыми чертежами.
[0044] Фигуры 1A-1C: Результат трансактивации для 1002 был описан на основе измерения излучения, испускаемого люциферазой, и выражен как интенсивность в относительных световых единицах (ОСЕ). На фигуре 1A приведен график зависимости результатов в ОСЕ, отложенных по оси y, от концентрации SARD, отложенной по оси x, где значения для антагониста обозначены жирными точками. По жирным точкам была построена кривая. На фигуре 1B проиллюстрирован вестерн-блот исследования разрушения андрогенных рецепторов с использованием клеток AD1, результаты приведены в таблице 1 в столбце Активность SARD: ингибирование полноразмерного AR, %. На фигуре 1C проиллюстрирован вестерн-блот исследования разрушения сплайсированной формы андрогенных рецепторов с использованием клеток D567es. Перорально активное соединение 1002, селективно разрушающее андрогенные рецепторы, полностью разрушает полноразмерный AR (не показано) и сплайсированную форм AR (показано) в концентрации 1 мкМ. В указанном эксперименте эндогенный ARSV разрушается in vitro в клетках v567es. (Результаты для клеток 22RV1 указаны в таблице 1 в столбце ‘Активность SARD: ингибирование S.V. %’.)
[0045] Фигура 2A и фигура 2B: Результаты трансактивации для 11 (индол) и 1002 (пиразол согласно настоящему изобретению) были описаны на основании измерения излучения, испускаемого люциферазой, и выражены как интенсивность в относительных световых единицах (ОСЕ). На фигуре 2A приведен график зависимости результатов в ОСЕ, отложенных по оси y, от концентрации SARD, отложенной по оси x, где значения для антагониста приведены для 11 и 1002. Соединение 11 обозначено жирными точками и сплошной линией, а 1002 обозначено пустыми точками и пунктирной линией. По жирным и пустым точкам были построены кривые для 1002 и 11, соответственно. На фигуре 2B проиллюстрирован вестерн-блот исследования разрушения AR с использованием клеток AD1 (полноразмерный AR) и исследования сплайсированной формы с использованием клеток 22RV1 для 11, 11R (R-изомер 11), 1002 и 1020 (R-изомер 1002). Результаты указаны в таблице 1 в столбцах ‘Активность SARD: Ингибирование полноразмерного AR, %’ и ‘Активность SARD: Ингибирование S.V. %’, соответственно. Вкратце, R-изомер индольных и пиразольных SARD сохранял активность SARD в отличие от LBD-зависимых ингибиторов.
[0046] Фигура 3А и фигура 3В: Результат трансактивации для 1003 был описан на основе измерения излучения, испускаемого люциферазой, и выражен как интенсивность в относительных световых единицах (ОСЕ). На фигуре 3A приведен график зависимости результатов в ОСЕ, отложенных по оси y, от концентрации SARD, отложенной по оси x, где значения для агониста обозначены жирными точками, и значения для антагониста обозначены пустыми точками. По пустым точкам была построена кривая. На фигуре 3B проиллюстрирован вестерн-блот исследования разрушения полноразмерных андрогенных рецепторов, результаты приведены в таблице 1 в столбце Активность SARD: ингибирование полноразмерного AR, %.
[0047] Фигура 4А и фигура 4В: Результат трансактивации для 1004 был описан на основе измерения излучения, испускаемого люциферазой, и выражен как интенсивность в относительных световых единицах (ОСЕ). На фигуре 4A приведен график зависимости результатов в ОСЕ, отложенных по оси y, от концентрации SARD, отложенной по оси x, где значения для агониста обозначены жирными точками, и значения для антагониста обозначены пустыми точками. По пустым точкам была построена кривая. На фигуре 4B проиллюстрирован вестерн-блот исследования разрушения полноразмерных андрогенных рецепторов, результаты приведены в таблице 1 в столбце Активность SARD: ингибирование полноразмерного AR, %. Числа под вестерн-блотом обозначают отношение AR к актину в каждой полосе.
[0048] Фигура 5А и фигура 5В: Результаты трансактивации для 1005 были описан на основе измерения излучения, испускаемого люциферазой, и выражены как интенсивность в относительных световых единицах (ОСЕ). На фигуре 5A приведен график зависимости результатов в ОСЕ, отложенных по оси y, от концентрации SARD, отложенной по оси x, где значения для агониста обозначены жирными точками, и значения для антагониста обозначены пустыми точками. По пустым точкам была построена кривая. На фигуре 5B проиллюстрирован вестерн-блот исследования разрушения полноразмерных андрогенных рецепторов, результаты приведены в таблице 1 в столбце Активность SARD: ингибирование полноразмерного AR, %.
[0049] Фигура 6А и фигура 6В: Результат трансактивации для 1006 был описан на основе измерения излучения, испускаемого люциферазой, и выражен как интенсивность в относительных световых единицах (ОСЕ). На фигуре 6A приведен график зависимости результатов в ОСЕ, отложенных по оси y, от концентрации SARD, отложенной по оси x, где значения для агониста обозначены жирными точками, и значения для антагониста обозначены пустыми точками. По пустым точкам была построена кривая. На фигуре 6B проиллюстрирован вестерн-блот исследования разрушения полноразмерных андрогенных рецепторов, результаты приведены в таблице 1 в столбце Активность SARD: ингибирование полноразмерного AR, %.
[0050] Фигура 7: Вестерн-блот исследования разрушения полноразмерных андрогенных рецепторов показан для соединения 17, результаты приведены в таблице 1 в столбце Активность SARD: ингибирование полноразмерного AR, %.
[0051] Фигура 8: Результат трансактивации для 1011 был описан на основе измерения излучения, испускаемого люциферазой, и выражен как интенсивность в относительных световых единицах (ОСЕ). На фигуре 8 приведен график зависимости результатов в ОСЕ, отложенных по оси y, от концентрации SARD, отложенной по оси x, где значения для антагониста обозначены жирными точками. По жирным точкам была построена кривая.
[0052] Фигура 9: Результат трансактивации для 1010 был описан на основе измерения излучения, испускаемого люциферазой, и выражен как интенсивность в относительных световых единицах (ОСЕ). На фигуре 9 приведен график зависимости результатов в ОСЕ, отложенных по оси y, от концентрации SARD, отложенной по оси x, где значения для антагониста обозначены жирными точками. По жирным точкам была построена кривая.
[0053] Фигура 10: Результат трансактивации для 1009 был описан на основе измерения излучения, испускаемого люциферазой, и выражен как интенсивность в относительных световых единицах (ОСЕ). На фигуре 10 приведен график зависимости результатов в ОСЕ, отложенных по оси y, от концентрации SARD, отложенной по оси x, где значения для антагониста обозначены жирными точками. По жирным точкам была построена кривая.
[0054] Фигура 11: Результат трансактивации для 1008 был описан на основе измерения излучения, испускаемого люциферазой, и выражен как интенсивность в относительных световых единицах (ОСЕ). На фигуре 11 приведен график зависимости результатов в ОСЕ, отложенных по оси y, от концентрации SARD, отложенной по оси x, где значения для антагониста обозначены жирными точками. По жирным точкам была построена кривая.
[0055] Фигура 12: Результат трансактивации для 1007 был описан на основе измерения излучения, испускаемого люциферазой, и выражен как интенсивность в относительных световых единицах (ОСЕ). На фигуре 12 приведен график зависимости результатов в ОСЕ, отложенных по оси y, от концентрации SARD, отложенной по оси x, где значения для антагониста обозначены жирными точками. По жирным точкам была построена кривая.
[0056] Фигуры 13A-13C: Результат трансактивации для 1001 был описан на основе измерения излучения, испускаемого люциферазой, и выражен как интенсивность в относительных световых единицах (ОСЕ). На фигуре 13A приведен график зависимости результатов в ОСЕ, отложенных по оси y, от концентрации SARD, отложенной по оси x, где значения для антагониста обозначены жирными точками. По жирным точкам была построена кривая. На фигуре 13B проиллюстрирован вестерн-блот исследования разрушения полноразмерных андрогенных рецепторов, результаты приведены в таблице 1 в столбце Активность SARD: ингибирование полноразмерного AR, %. На фигуре 13C проиллюстрирован вестерн-блот исследования разрушения сплайсированной формы андрогенных рецепторов с использованием клеток 22RV1, результаты приведены в таблице 1 в столбце Активность SARD: ингибирование S.V., %.
[0057] Фигура 14: На фигуре 14 проиллюстрированы данные I фазы и фаз I и II в виде таблицы с исходными данными для определения метаболической стабильности 1002 в микросомах печени мышей (MLM) и значений T1/2 (период полувыведения в минутах) и CLint (клиренс в мкл/мин/мг белка), вычисленных по приведенным данным.
[0058] Фигура 15A и фигура 15B: На фигуре 15A приведены данные I фазы в виде таблицы с исходными данными и графически изображенные данные одного эксперимента с использованием 1002 в микросомах печени мышей (MLM). На фигуре 15B приведены данные I и II фазы в виде таблицы с исходными данными и графически изображенные данные одного эксперимента с использованием 1002 в микросомах печени мышей (MLM). Значение T1/2 составляло 224 мин. CLint составлял 3,12 мкл/мин/мг.
[0059] Фигура 16A и фигура 16B: На фигуре 16A приведены данные I фазы для микросом печени человека (HLM). На фигуре 16B приведены данные I и II фазы в виде таблицы с исходными данными и графически изображенные данные одного эксперимента с использованием 1002 в микросомах печени человека (HLM). В указанном эксперименте вычисленное значение T1/2 было бесконечным, и CLint составлял 0. Это позволяет предположить повышенную стабильность 1002 в HLM по сравнению с MLM.
[0060] Фигура 17: На фигуре 17 приведены данные I фазы в виде таблицы с исходными данными и графически изображенные данные одного эксперимента с использованием 1001 в микросомах печени мышей (MLM). Значение T1/2 составляло 23,5 мин, и CLint составлял 29,5 л/мин/мг. Результаты указывают на относительно плохую стабильность 1001, но при этом она все равно лучше по сравнению с 11.
[0061] Фигура 18A и фигура 18B: Способ Хершбергера (мыши): Самцам мышей (с массой тела 20-25 граммов; n = 5-7/группа), которых исследовали без операции (фигура 18A) или кастрировали (фигура 18B), проводили лечение, как указано на фигурах, в течение 13 дней. Лечение кастрированных мышей начинали через 3 дня после кастрации. Мышей умерщвляли на 14 день после начала лечения, удаляли семенные железы и взвешивали. Указывали измеренную массу семенных желез или нормированную по массе тела.
[0062] Фигура 19A и фигура 19B: Способ Хершбергера (крысы): На фигуре 19A указана масса органов у интактных крыс линии Спраг-Доули с массой тела 165-180 граммов, которым ежедневно перорально вводили носитель, 40 мг/кг 1002, 60 мг/кг 1002 или 20 мг/кг энзалутамида. После 13 дней лечения крыс умерщвляли и измеряли массу предстательной железы, семенных желез и мышцы, поднимающей задний проход. На фигуре 19B эти же данные приведены в виде уменьшения в % по сравнению с носителем. На нижнем правом графике приведено сравнение массы органов в % у интактных и кастрированных крыс, которым вводили носитель.
[0063] Фигура 20A и фигура 20B: Разрушение полноразмерных и сплайсированных (AR-v567ES) андрогенных рецепторов (in vitro) для 1010, 1012, 1014, 1015, 1016, 1017, 1019 и 1022: На фигуре 20A проиллюстрирован вестерн-блот для каждого соединения в исследовании разрушения полноразмерных андрогенных рецепторов. Результаты приведены в таблице 1 в столбце Активность SARD: Ингибирование полноразмерного AR, %. На фигуре 20B проиллюстрирован вестерн-блот исследования разрушения сплайсированной формы андрогенных рецепторов с использованием D567es.
[0064] Фигура 21A и фигура 21B: Противоопухолевая эффективность 1002 в ксенотрансплантате тройного негативного рака молочной железы (ТНРМЖ), выделенном у пациента (PDX), показана для тройного негативного рака молочной железы HBrt 1071 (фигура 21A) и тройного негативного рака молочной железы HBrt 1361 (фигура 21B).
[0065] Фигура 22: изображено связывание 1002 с участком AF-1 N-терминального домена (NTD) андрогенного рецептора. В экспериментах 1D и waterLogsy ЯМР продемонстрировано, что полоса 1002 уширяется в присутствии пептида, полученного из участка AF-1 NTD. Кроме того, в экспериментах релаксации и waterLogsy продемонстрировано, что скорость вращения в растворе 1002 замедляется при добавлении AF-1, это явным образом указывает на то, что связывание 1002 с участком AF-1 является предпочтительным способом взаимодействия с белком.
[0066] Фигура 23: показаны результаты исследования роста клеток MR49F LNCaP, устойчивых к энзалутамиду (LNCaP-EnzR), при использовании 1002 и 1014. 1002 и 1014 подавляют рост клеток LNCaP-EnzR в нижнем микромолярном диапазоне.
[0067] Фигура 24: изображены уровни 11, 34, 36, 96, 103, 1002, 1010, 1012 и 1014 в сыворотке и опухоли в эксперименте с использованием ксенотрансплантата 22RV1.
[0068] Фигура 25: изображено уменьшение массы семенных желез (изменение в % ) у животных, которым вводили 34, 36, 1002, 1010, 1012 и 1014 в исследовании Хершбергера.
[0069] Фигура 26: изображено подавление роста опухоли в ксенотрансплантатах, устойчивых к LNCaP-энзалутамиду (LNCaP-EnzR), которые обрабатывали путем перорального введения 60 мг/кг 1014. Показаны результаты двух различных экспериментов (эксперимент 1 и эксперимент 2).
[0070] Фигуры 27A-27D: изображены результаты исследований флуоресценции в стационарном состоянии, которые демонстрируют взаимодействие SARD 1002, 1010 и 36 (индол) и N-терминальных фрагментов AR, таких как AR-NTD (аминокислоты 1-559) и AR-AF1 (аминокислоты 141-486). На фигуре 27A показано изменение сигнала флуоресценции AR-NTD и AR-AF1 в присутствии мочевины (денатурирующий агент), TMAO (стабилизатор укладки белка) и буфера, но не SARD. На фигурах 27B-27D показаны изменения флуоресценции AR-NTD и AR-AF1, связанные с титрованием 1002 (фигура 27B), 1010 (фигура 27C) и 36 (фигура 27D), соответственно.
Фигуры 28A-28D: изображено разрушение полноразмерных и/или сплайсированных (22RV1) андрогенных рецепторов (in vitro) при использовании 1024 (фигура 28A), 1029 (фигура 28B), 1037 и 1041 (фигура 28C) и 1044-1045 (фигура 28D). На фигурах 28A, 28C и 28D проиллюстрирован вестерн-блот исследований разрушения полноразмерных андрогенных рецепторов. Результаты приведены в таблице 1 в столбце Активность SARD: Ингибирование полноразмерного AR, %. На фигуре 28B проиллюстрирован вестерн-блот исследования разрушения сплайсированных форм андрогенных рецепторов при использовании клеток 22RV1, результаты которого приведены в таблице 1 в столбце с заголовком ‘Активность SARD: ингибирование S.V. %".
[0071] Следует понимать, что для простоты и ясности иллюстрации элементы, показанные на фигурах, необязательно изображены в масштабе. Например, размеры некоторых элементов могут быть увеличены по сравнению с другими элементами для ясности. Кроме того, если это уместно, номера позиций могут повторяться на фигурах при обозначении соответствующих или аналогичных элементов.
ПОДРОБНОЕ ОПИСАНИЕ НАСТОЯЩЕГО ИЗОБРЕТЕНИЯ
[0072] В последующем подробном описании приведены разнообразные конкретные детали, которые помогают в полной мере понять изобретение. Тем не менее, специалистам в данной области техники будет понятно, что настоящее изобретение может быть реализовано и без этих конкретных деталей. В других случаях хорошо известные способы, процедуры и компоненты не были описаны подробно, чтобы не вносить неясность в настоящее изобретение.
[0073] Андрогены действуют в клетках путем связывания AR, члена суперсемейства стероидных рецепторов факторов транскрипции. Так как рост и поддержание рака предстательной железы (PCa) в значительной степени контролируются андрогенами в кровотоке, то лечение PCa в значительной степени основано на способах терапии, направленно действующих на AR. Лечение антагонистами AR, такими как энзалутамид, бикалутамид или гидроксифлутамид, для нарушения активации рецепторов, успешно использовалось в прошлом для уменьшения роста PCa. Все доступные в настоящее время антагонисты AR обеспечивают конкурентное связывание AR и рекрутинг корепрессоров, таких как NCoR и SMRT, для подавления транскрипции целевых генов. Тем не менее, изменение внутриклеточной сигнальной системы, мутации AR и повышенная экспрессия коактиваторов приводят к нарушению функции антагонистов или даже к превращению антагонистов в агонисты. В исследованиях было продемонстрировано, что мутации W741 и T877 в AR превращают бикалутамид и гидроксифлутамид, соответственно, в агонисты. Аналогичным образом, при увеличенном уровне внутриклеточных цитокинов происходит рекрутинг коактиваторов вместо корепрессоров к AR-восприимчивым промоторам, что впоследствии обеспечивает превращение бикалутамида в агонист. Аналогично, мутации, связанные с устойчивостью к энзалутамиду, включают F876, H874, T877 и двойные мутации T877/S888, T877/D890, F876/T877 (т.е. в клетках MR49) и H874/T877 (Genome Biol. (2016) 17:10 (doi: 10.1186/s13059-015-0864-1)). Мутации устойчивости к абиратерону включают мутации L702H, которые приводят к активации AR глюкокортикоидами, такими как преднизон, это вызывает устойчивость к абиратерону, так как абиратерон, как правило, назначают в комбинации с преднизоном. При развитии устойчивости к энзалутамиду пациент часто невосприимчив также к абиратерону, и наоборот; или продолжительность ответа является очень небольшой. Эта ситуация подчеркивает необходимость эффективной антиадрогенной терапии для предотвращения реактивации AR при распространенных формах рака предстательной железы.
[0074] Несмотря на первоначальный ответ на андрогенную депривационную терапию (АДТ) прогрессирование PCa неизбежно, и рак приобретает форму устойчивого к кастрации рака предстательной железы (CRPC). Основной причиной повторного появления устойчивого к кастрации рака предстательной железы (CRPC) является реактивация андрогенных рецепторов (AR) посредством альтернативных механизмов, таких как:
(a) интракринный синтез андрогенов;
(b) экспрессия сплайсированных форм AR (AR-SV), например, в которых отсутствует лиганд-связывающий домен (LBD);
(c) мутации AR-LBD, которые могут приводить к устойчивости к антагонистам;
(d) повышенная восприимчивость AR к низкому уровню андрогенов, например, из-за амплификации гена AR или мутации AR;
(e) амплификация гена AR в опухоли; и
(f) повышенная экспрессия коактиваторов и/или измененная внутриклеточная сигнальная трансдукция.
[0075] Изобретение включает новые соединения, селективно разрушающие андрогенные рецепторы (SARD), описанные формулой I, которые подавляют рост клеток и опухолей рака предстательной железы (PCa), пролиферация которых зависит от полноразмерных AR (AR-FL), включая патогенные и устойчивые мутации и рецептор дикого типа, и/или сплайсированных форм AR (AR-SV).
[0076] При использовании в настоящем описании, если отсутствуют иные определения, соединение, «селективно разрушающее андрогенные рецепторы» (SARD), представляет собой антагонист андрогенных рецепторов, который может подавлять рост клеток и опухолей PCa, пролиферация которых зависит от полноразмерных AR (AR-FL) и/или сплайсированных форм AR (AR-SV). Соединение SARD не может связываться с лигандсвязывающим доменом (LBD). В качестве альтернативы, соединение, «селективно разрушающее андрогенные рецепторы» (SARD), представляет собой антагонист андрогенных рецепторов, который может вызывать разрушение различных патогенных мутантных форм AR и AR дикого типа и тем самым может проявлять антиадрогенные свойства в разнообразных патогенных измененных клеточных средах, сопровождающих болезненные состояния, подразумеваемые в настоящем изобретении. В одном варианте реализации SARD является активным при пероральном введении. В другом варианте реализации SARD наносят местно в область действия.
[0077] Соединение SARD может связывать N-терминальный домен (NTD) AR; альтернативный домен связывания и разрушения (BDD) AR; одновременно лигандсвязывающий домен (LBD) AR и альтернативный домен связывания и разрушения (BDD); или одновременно N-терминальный домен (NTD) и лигандсвязывающий домен (LBD) AR. В одном из вариантов реализации BDD может быть расположен в NTD. В одном из вариантов реализации BDD расположен в участке AF-1 NTD. В качестве альтернативы соединение SARD может: подавлять рост, опосредованный зависимым от N-терминального домена (NTD) AR-SV с конститутивной активностью; или ингибировать AR посредством связывания с доменом, отличным от AR LBD. Кроме того, соединение SARD может быть сильным (т.е. высокоактивным и крайне эффективным) селективным антагонистом андрогенных рецепторов, который имеет активность антагониста AR, превышающую другие известные антагонисты AR (например, энзалутамид, бикалутамид и абиратерон).
[0078] Соединение SARD может представлять собой селективный агонист андрогенных рецепторов, который направленно действует на AR-SV, которые не поддаются ингибированию традиционными антагонистами. Соединение SARD может проявлять любой из следующих видов активности, включая, но не ограничиваясь ими: активность разрушения AR-SV; активность разрушения AR-FL; ингибирующую активность в отношении AR-SV (т.е. антагониста AR-SV); ингибирующую активность в отношении AR-FL (т.е. антагониста AR-FL); подавление конститутивной активации AR-SV; или подавление конститутивной активации AR-FL. В качестве альтернативы соединение SARD может обладать двойной функцией разрушения AR-SV и ингибирования AR-SV и/или двойной функцией разрушения AR-FL и ингибирования AR-FL; или в качестве альтернативы обладает всеми четырьмя указанными видами активности.
[0079] Соединение SARD также может разрушать AR-FL и AR-SV. Соединение SARD может разрушать AR посредством связывания с доменом, отличным от AR LBD. Соединение SARD может обладать двойной функцией разрушения и ингибирования AR-SV, которая отличает его от любых доступных средств терапии CRPC. Соединение SARD может подавлять реактивацию AR посредством альтернативных механизмов, таких как: интракринный синтез андрогенов, экспрессия AR-SV, в которых отсутствует лигандсвязывающий домен (LBD), и мутации AR-LBD, которые могут приводить к устойчивости к антагонистам, или подавлять повторно активированные андрогенные рецепторы, присутствующие в патогенной измененной клеточной среде.
[0080] Примеры сплайсированных форм AR включают, но не ограничиваются ими, AR-V7 и ARv567es (или AR-V12; S. Sun, et al. Castration resistance in human prostate cancer is conferred by a frequently occurring androgen receptor splice variant. J Clin Invest. (2010) 120(8), 2715-2730). Неограничивающими примерами мутаций AR, придающих устойчивость к антиандрогенам, являются: мутации W741L, T877A и F876L (J. D. Joseph et al. A clinically relevant androgen receptor mutation confers resistance to second-generation antiandrogens enzalutamide and ARN-509. Cancer Discov. (2013) 3(9), 1020-1029). В данной области техники известно множество других мутаций LBD, придающих устойчивость, и постоянно открываются новые. AR-V7 представляет собой сплайсированную форму AR, в которой отсутствует LBD (A. H. Bryce & E. S. Antonarakis. Androgen receptor splice variant 7 in castration-resistant prostate cancer: Clinical considerations. Int J Urol. (2016 Jun 3) 23(8), 646-53. doi: 10.1111/iju.13134). Он является конститутивно активным и, как было продемонстрировано, является причиной агрессивности PCa и устойчивости к эндокринной терапии.
[0081] Изобретение включает новые соединения, селективно разрушающие андрогенные рецепторы (SARD), формулы I -VII, IA-ID, IIA, IIB, VIIA или VIIB, которые связывают AR через альтернативный домен связывания и разрушения (BDD), например, NTD или AF-1. SARD могут дополнительно связывать лигандсвязывающий домен (LBD) AR.
[0082] Соединения SARD можно применять для лечения CRPC, который не может быть излечен любым другим антагонистом. Соединения SARD могут излечивать CRPC путем разрушения AR-SV. Соединения SARD могут сохранять активность антагониста в отношении мутантов AR, которые обычно превращают антагонисты AR в агонисты. Например, соединения SARD сохраняют активность антагониста в отношении мутантов AR W741L, T877A и F876L (J. D. Joseph et al. A clinically relevant androgen receptor mutation confers resistance to second-generation antiandrogens enzalutamide and ARN-509. Cancer Discov. (2013) 3(9), 1020-1029). В качестве альтернативы соединения SARD обладают активностью антагониста в измененной клеточной среде, в которой агенты, действующие на LBD, теряют эффективность, или в которой NTD-зависимая активность AR является конститутивной.
Соединения, селективно разрушающие андрогенные рецепторы (SARD)
[0083] Изобретение включает соединения, селективно разрушающие андрогенные рецепторы (SARD), представленные структурой формулы I:
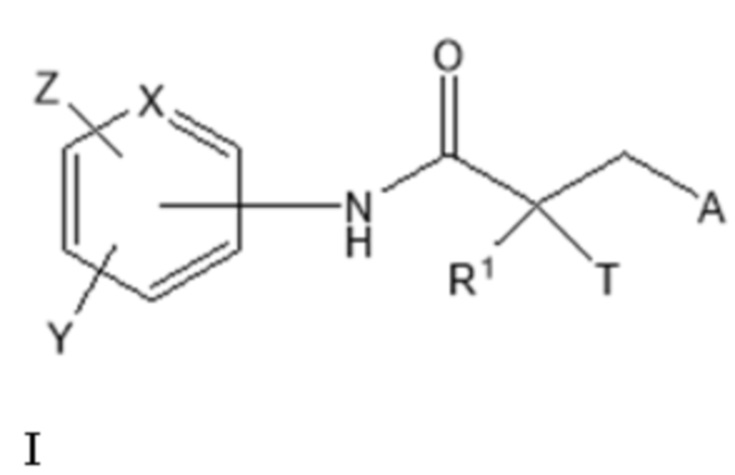
где
T представляет собой H, OH, OR, OCOR, CH3, -NHCOCH3 или NHCOR;
R1 представляет собой H, CH3, CH2F, CHF2, CF3, CH2CH3 или CF2CF3;
или T и R1 образуют 3-8-членное карбоциклическое или гетероциклическое кольцо;
Y представляет собой H, CF3, F, I, Br, Cl, CN или C(R)3;
Z представляет собой H, NO2, CN, галогенид, COOH, COR, NHCOR, CONHR,
или Y и Z образуют 5-8-членное конденсированное кольцо;
X представляет собой CH или N;
R представляет собой H, алкил, алкенил, галогеналкил, спирт, CH2CH2OH, CF3, CH2Cl, CH2CH2Cl, арил, F, Cl, Br, I или OH;
A представляет собой R2 или R3;
R2 представляет собой пяти- или шестичленное насыщенное или ненасыщенное кольцо, содержащее по меньшей мере один атом азота и 0, 1 или 2 двойные связи, необязательно замещенное по меньшей мере одним из Q1, Q2, Q3 или Q4, каждый из которых независимо выбран из водорода, кето, замещенного или незамещенного линейного или разветвленного алкила, замещенного или незамещенного циклоалкила, замещенного или незамещенного гетероциклоалкила, галогеналкила, CF3, замещенного или незамещенного арила, замещенного или незамещенного фенила, F, Cl, Br, I, CN, NO2, гидроксила, алкокси, OR, арилалкила, NCS, малеимида, NHCOOR, N(R)2, NHCOR, CONHR, COOR или COR;
R3 представляет собой NHR2, галогенид, N3, OR4, CF3, COR4, COCl, COOCOR4, COOR4, OCOR4, OCONHR4, NHCOOR4, NHCONHR4, OCOOR4, CN, CONH2, CONH(R4), CON(R4)2, SR4, SO2R4, SOR4 SO3H, SO2NH2, SO2NH(R4), SO2N(R4)2, NH2, NH(R4), N(R4)2, CO(N-гетероцикл), NO2, цианат, изоцианат, тиоцианат, изотиоцианат, мезилат, тозилат, трифлат, PO(OH)2 или OPO(OH)2; и
R4 представляет собой H, алкил, галогеналкил, циклоалкил, арил или гетероарил, причем указанные алкильные, галогеналкильные, циклоалкильные, арильные или гетероарильные группы необязательно замещены;
или его оптический изомер, изомер, фармацевтически приемлемую соль, фармацевтический продукт, полиморф, гидрат или любую их комбинацию;
где если A представляет собой Br или I, R1 представляет собой CH3, и T представляет собой OH, то X представляет собой N, или анилиновое кольцо образует конденсированное гетероциклическое кольцо.
[0084] В различных вариантах реализации соединение SARD формулы I содержит хиральный атом углерода. В других вариантах реализации соединение SARD формулы I представляет собой рацемическую смесь. В других вариантах реализации соединение SARD формулы I представляет собой (S)-изомер. В других вариантах реализации соединение SARD формулы I представляет собой (R)-изомер.
[0085] Изобретение включает соединения, селективно разрушающие андрогенные рецепторы (SARD), представленные структурой формулы IA:
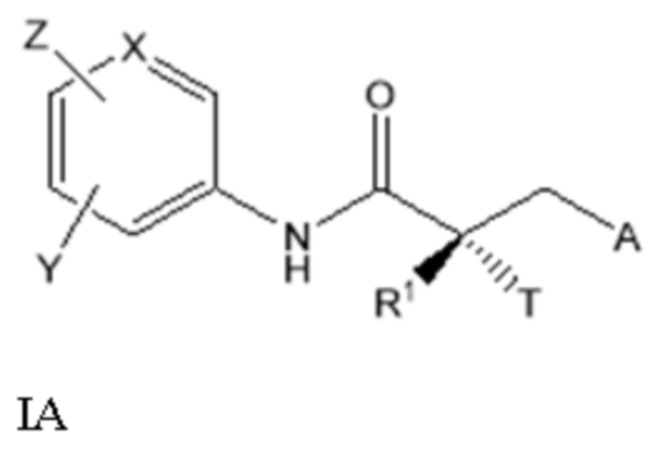
где
T представляет собой H, OH, OR, OCOR, CH3, -NHCOCH3 или NHCOR;
R1 представляет собой H, CH3, CH2F, CHF2, CF3, CH2CH3 или CF2CF3;
или T и R1 образуют 3-8-членное карбоциклическое или гетероциклическое кольцо;
Y представляет собой H, CF3, F, I, Br, Cl, CN или C(R)3;
Z представляет собой H, NO2, CN, галогенид, COOH, COR, NHCOR, CONHR,
или Y и Z образуют 5-8-членное конденсированное кольцо;
X представляет собой CH или N;
R представляет собой H, алкил, алкенил, галогеналкил, спирт, CH2CH2OH, CF3, CH2Cl, CH2CH2Cl, арил, F, Cl, Br, I или OH;
A представляет собой R2 или R3;
R2 представляет собой пяти- или шестичленное насыщенное или ненасыщенное кольцо, содержащее по меньшей мере один атом азота и 0, 1 или 2 двойные связи, необязательно замещенное по меньшей мере одним из Q1, Q2, Q3 или Q4, каждый из которых независимо выбран из водорода, кето, замещенного или незамещенного линейного или разветвленного алкила, замещенного или незамещенного циклоалкила, замещенного или незамещенного гетероциклоалкила, галогеналкила, CF3, замещенного или незамещенного арила, замещенного или незамещенного фенила, F, Cl, Br, I, CN, NO2, гидроксила, алкокси, OR, арилалкила, NCS, малеимида, NHCOOR, N(R)2, NHCOR, CONHR, COOR или COR;
R3 представляет собой NHR2, галогенид, N3, OR4, CF3, COR4, COCl, COOCOR4, COOR4, OCOR4, OCONHR4, NHCOOR4, NHCONHR4, OCOOR4, CN, CONH2, CONH(R4), CON(R4)2, SR4, SO2R4, SOR4 SO3H, SO2NH2, SO2NH(R4), SO2N(R4)2, NH2, NH(R4), N(R4)2, CO(N-гетероцикл), NO2, цианат, изоцианат, тиоцианат, изотиоцианат, мезилат, тозилат, трифлат, PO(OH)2 или OPO(OH)2; и
R4 представляет собой H, алкил, галогеналкил, циклоалкил, арил или гетероарил, причем указанные алкильные, галогеналкильные, циклоалкильные, арильные или гетероарильные группы необязательно замещены;
или их изомеры, фармацевтически приемлемые соли, фармацевтические продукты, полиморфы, гидраты или любые их комбинации;
где если A представляет собой Br или I, R1 представляет собой CH3, и T представляет собой OH, то X представляет собой N, или анилиновое кольцо образует конденсированное гетероциклическое кольцо.
[0086] Изобретение включает соединения, селективно разрушающие андрогенные рецепторы (SARD), представленные структурой формулы IB:
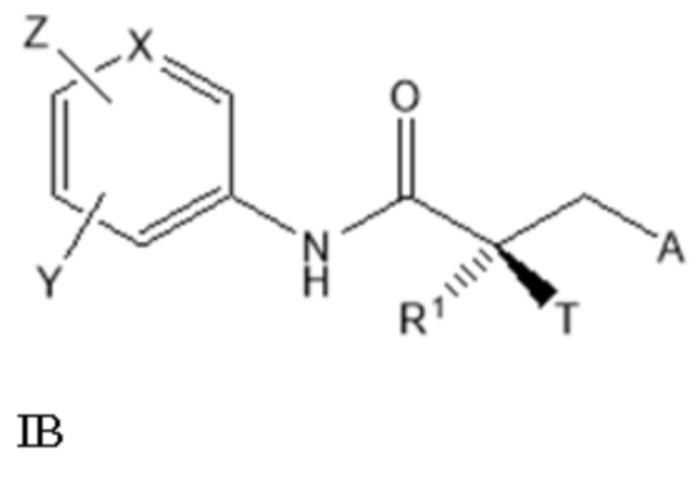
где
T представляет собой H, OH, OR, OCOR, CH3, -NHCOCH3 или NHCOR;
R1 представляет собой H, CH3, CH2F, CHF2, CF3, CH2CH3 или CF2CF3;
или T и R1 образуют 3-8-членное карбоциклическое или гетероциклическое кольцо;
Y представляет собой H, CF3, F, I, Br, Cl, CN или C(R)3;
Z представляет собой H, NO2, CN, галогенид, COOH, COR, NHCOR, CONHR,
или Y и Z образуют 5-8-членное конденсированное кольцо;
X представляет собой CH или N;
R представляет собой H, алкил, алкенил, галогеналкил, спирт, CH2CH2OH, CF3, CH2Cl, CH2CH2Cl, арил, F, Cl, Br, I или OH;
A представляет собой R2 или R3;
R2 представляет собой пяти- или шестичленное насыщенное или ненасыщенное кольцо, содержащее по меньшей мере один атом азота и 0, 1 или 2 двойные связи, необязательно замещенное по меньшей мере одним из Q1, Q2, Q3 или Q4, каждый из которых независимо выбран из водорода, кето, замещенного или незамещенного линейного или разветвленного алкила, замещенного или незамещенного циклоалкила, замещенного или незамещенного гетероциклоалкила, галогеналкила, CF3, замещенного или незамещенного арила, замещенного или незамещенного фенила, F, Cl, Br, I, CN, NO2, гидроксила, алкокси, OR, арилалкила, NCS, малеимида, NHCOOR, N(R)2, NHCOR, CONHR, COOR или COR;
R3 представляет собой NHR2, галогенид, N3, OR4, CF3, COR4, COCl, COOCOR4, COOR4, OCOR4, OCONHR4, NHCOOR4, NHCONHR4, OCOOR4, CN, CONH2, CONH(R4), CON(R4)2, SR4, SO2R4, SOR4 SO3H, SO2NH2, SO2NH(R4), SO2N(R4)2, NH2, NH(R4), N(R4)2, CO(N-гетероцикл), NO2, цианат, изоцианат, тиоцианат, изотиоцианат, мезилат, тозилат, трифлат, PO(OH)2 или OPO(OH)2; и
R4 представляет собой H, алкил, галогеналкил, циклоалкил, арил или гетероарил, причем указанные алкильные, галогеналкильные, циклоалкильные, арильные или гетероарильные группы необязательно замещены;
или их изомеры, фармацевтически приемлемые соли, фармацевтические продукты, полиморфы, гидраты или любые их комбинации;
где если A представляет собой Br или I, R1 представляет собой CH3, и T представляет собой OH, то X представляет собой N, или анилиновое кольцо образует конденсированное гетероциклическое кольцо.
[0087] Изобретение включает соединения, селективно разрушающие андрогенные рецепторы (SARD), представленные структурой формулы IC:
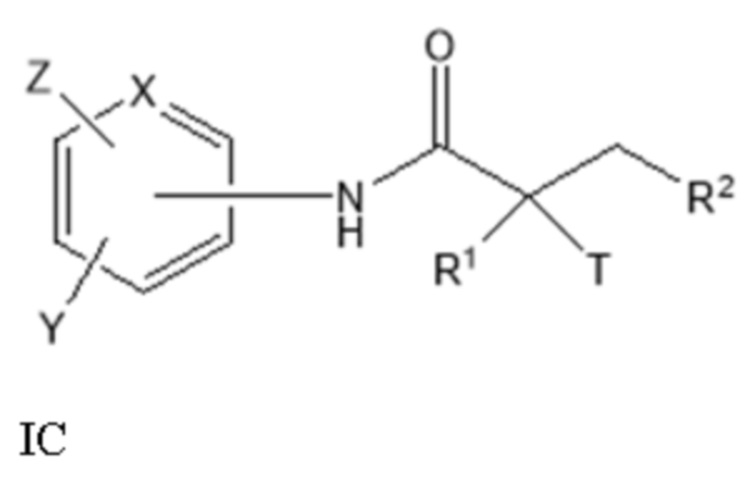
где
T представляет собой H, OH, OR, OCOR, CH3, -NHCOCH3 или NHCOR;
R1 представляет собой H, CH3, CH2F, CHF2, CF3, CH2CH3 или CF2CF3;
или T и R1 образуют 3-8-членное карбоциклическое или гетероциклическое кольцо;
Y представляет собой H, CF3, F, I, Br, Cl, CN или C(R)3;
Z представляет собой H, NO2, CN, галогенид, COOH, COR, NHCOR, CONHR,
или Y и Z образуют 5-8-членное конденсированное кольцо;
X представляет собой CH или N;
R представляет собой H, алкил, алкенил, галогеналкил, спирт, CH2CH2OH, CF3, CH2Cl, CH2CH2Cl, арил, F, Cl, Br, I или OH;
R2 представляет собой пяти- или шестичленное насыщенное или ненасыщенное кольцо, содержащее по меньшей мере один атом азота и 0, 1 или 2 двойные связи, необязательно замещенное по меньшей мере одним из Q1, Q2, Q3 или Q4, каждый из которых независимо выбран из водорода, кето, замещенного или незамещенного линейного или разветвленного алкила, замещенного или незамещенного циклоалкила, замещенного или незамещенного гетероциклоалкила, галогеналкила, CF3, замещенного или незамещенного арила, замещенного или незамещенного фенила, F, Cl, Br, I, CN, NO2, гидроксила, алкокси, OR, арилалкила, NCS, малеимида, NHCOOR, N(R)2, NHCOR, CONHR, COOR или COR;
или их оптические изомеры, изомеры, фармацевтически приемлемые соли, фармацевтические продукты, полиморфы, гидраты или любые их комбинации.
[0088] Изобретение включает соединения, селективно разрушающие андрогенные рецепторы (SARD), представленные структурой формулы ID:
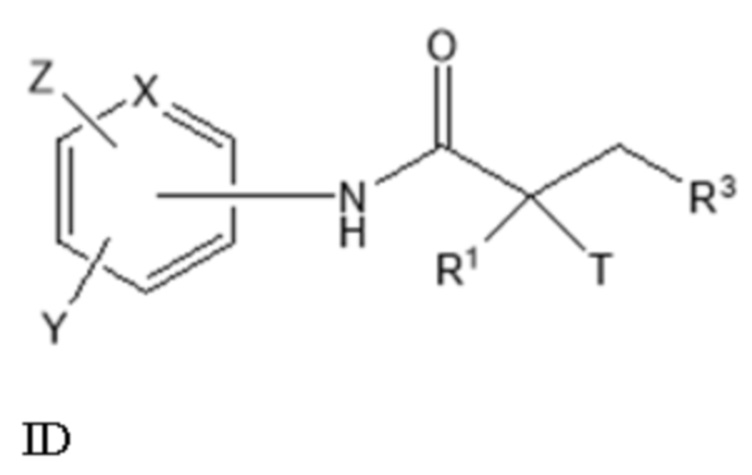
где
T представляет собой H, OH, OR, OCOR, CH3, -NHCOCH3 или NHCOR;
R1 представляет собой H, CH3, CH2F, CHF2, CF3, CH2CH3 или CF2CF3;
или T и R1 образуют 3-8-членное карбоциклическое или гетероциклическое кольцо;
Y представляет собой H, CF3, F, I, Br, Cl, CN или C(R)3;
Z представляет собой H, NO2, CN, галогенид, COOH, COR, NHCOR, CONHR,
или Y и Z образуют 5-8-членное конденсированное кольцо;
X представляет собой CH или N;
R представляет собой H, алкил, алкенил, галогеналкил, спирт, CH2CH2OH, CF3, CH2Cl, CH2CH2Cl, арил, F, Cl, Br, I или OH;
R3 представляет собой NHR2, галогенид, N3, OR4, CF3, COR4, COCl, COOCOR4, COOR4, OCOR4, OCONHR4, NHCOOR4, NHCONHR4, OCOOR4, CN, CONH2, CONH(R4), CON(R4)2, SR4, SO2R4, SOR4 SO3H, SO2NH2, SO2NH(R4), SO2N(R4)2, NH2, NH(R4), N(R4)2, CO(N-гетероцикл), NO2, цианат, изоцианат, тиоцианат, изотиоцианат, мезилат, тозилат, трифлат, PO(OH)2 или OPO(OH)2; и
R4 представляет собой H, алкил, галогеналкил, циклоалкил, арил или гетероарил, причем указанные алкильные, галогеналкильные, циклоалкильные, арильные или гетероарильные группы необязательно замещены;
или их оптические изомеры, изомеры, фармацевтически приемлемые соли, фармацевтические продукты, полиморфы, гидраты или любые их комбинации;
где если R3 представляет собой Br или I, R1 представляет собой CH3, и T представляет собой OH, то X представляет собой N, или анилиновое кольцо образует конденсированное гетероциклическое кольцо.
[0089] Изобретение включает соединение SARD, представленное структурой формулы II:
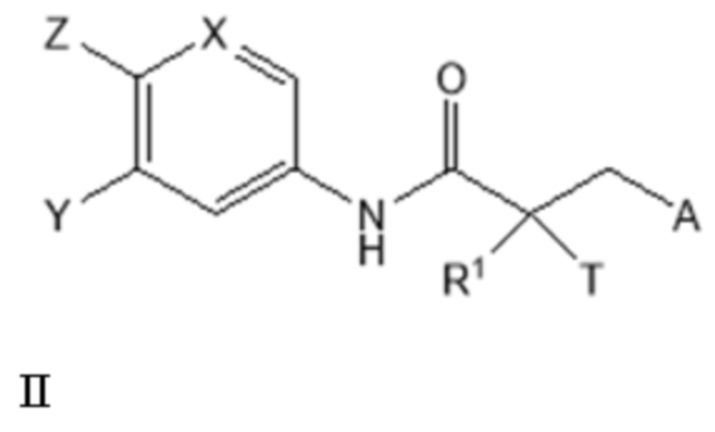
где
T представляет собой H, OH, OR, OCOR, CH3, -NHCOCH3 или NHCOR;
R1 представляет собой H, CH3, CH2F, CHF2, CF3, CH2CH3 или CF2CF3;
или T и R1 образуют 3-8-членное карбоциклическое или гетероциклическое кольцо;
Y представляет собой H, CF3, F, I, Br, Cl, CN или C(R)3;
Z представляет собой H, NO2, CN, галогенид, COOH, COR, NHCOR, CONHR,
или Y и Z образуют 5-8-членное конденсированное кольцо;
X представляет собой CH или N;
R представляет собой H, алкил, алкенил, галогеналкил, спирт, CH2CH2OH, CF3, CH2Cl, CH2CH2Cl, арил, F, Cl, Br, I или OH;
A представляет собой R2 или R3;
R2 представляет собой пиррольное, пирролиновое, пирролидиновое, пиразольное, пиразолиновое, пиразолидиновое, триазольное, имидазольное, имидазолиновое, имидазолидиновое или морфолиновое кольцо, причем указанное кольцо необязательно замещено по меньшей мере одним из Q1, Q2, Q3 или Q4, каждый из которых независимо выбран из водорода, кето, замещенного или незамещенного линейного или разветвленного алкила, замещенного или незамещенного циклоалкила, замещенного или незамещенного гетероциклоалкила, галогеналкила, CF3, замещенного или незамещенного арила, замещенного или незамещенного фенила, F, Cl, Br, I, CN, NO2, гидроксила, алкокси, OR, арилалкила, NCS, малеимида, NHCOOR, N(R)2, NHCOR, CONHR, COOR или COR;
R3 представляет собой NHR2, галогенид, N3, OR4, CF3, COR4, COCl, COOCOR4, COOR4, OCOR4, OCONHR4, NHCOOR4, NHCONHR4, OCOOR4, CN, CONH2, CONH(R4), CON(R4)2, SR4, SO2R4, SOR4 SO3H, SO2NH2, SO2NH(R4), SO2N(R4)2, NH2, NH(R4), N(R4)2, CO(N-гетероцикл), NO2, цианат, изоцианат, тиоцианат, изотиоцианат, мезилат, тозилат, трифлат, PO(OH)2 или OPO(OH)2; и
R4 представляет собой H, алкил, галогеналкил, циклоалкил, арил или гетероарил, причем указанные алкильные, галогеналкильные, циклоалкильные, арильные или гетероарильные группы необязательно замещены;
или его оптический изомер, изомер, фармацевтически приемлемую соль, фармацевтический продукт, полиморф, гидрат или любую их комбинацию;
где если A представляет собой Br или I, R1 представляет собой CH3, и T представляет собой OH, то X представляет собой N, или анилиновое кольцо образует конденсированное гетероциклическое кольцо.
[0090] В различных вариантах реализации соединение SARD формулы II содержит хиральный атом углерода. В других вариантах реализации соединение SARD формулы II представляет собой рацемическую смесь. В других вариантах реализации соединение SARD формулы II представляет собой (S)-изомер. В других вариантах реализации соединение SARD формулы II представляет собой (R)-изомер.
[0091] Изобретение включает соединение SARD, представленное структурой формулы IIA:
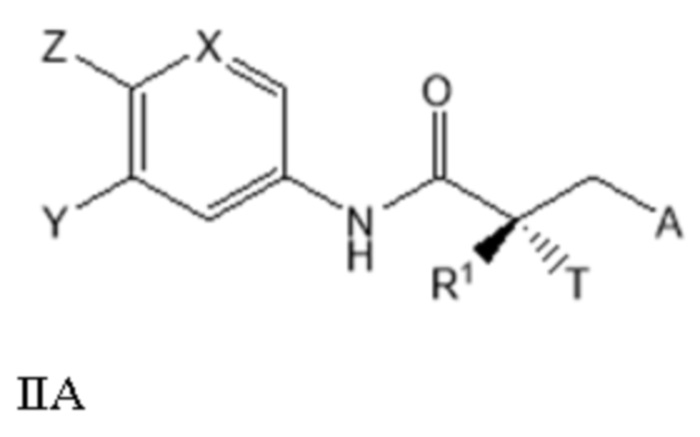
где
T представляет собой H, OH, OR, OCOR, CH3, -NHCOCH3 или NHCOR;
R1 представляет собой H, CH3, CH2F, CHF2, CF3, CH2CH3 или CF2CF3;
или T и R1 образуют 3-8-членное карбоциклическое или гетероциклическое кольцо;
Y представляет собой H, CF3, F, I, Br, Cl, CN или C(R)3;
Z представляет собой H, NO2, CN, галогенид, COOH, COR, NHCOR, CONHR,
или Y и Z образуют 5-8-членное конденсированное кольцо;
X представляет собой CH или N;
R представляет собой H, алкил, алкенил, галогеналкил, спирт, CH2CH2OH, CF3, CH2Cl, CH2CH2Cl, арил, F, Cl, Br, I или OH;
A представляет собой R2 или R3;
R2 представляет собой пиррольное, пирролиновое, пирролидиновое, пиразольное, пиразолиновое, пиразолидиновое, триазольное, имидазольное, имидазолиновое, имидазолидиновое или морфолиновое кольцо, причем указанное кольцо необязательно замещено по меньшей мере одним из Q1, Q2, Q3 или Q4, каждый из которых независимо выбран из водорода, кето, замещенного или незамещенного линейного или разветвленного алкила, замещенного или незамещенного циклоалкила, замещенного или незамещенного гетероциклоалкила, галогеналкила, CF3, замещенного или незамещенного арила, замещенного или незамещенного фенила, F, Cl, Br, I, CN, NO2, гидроксила, алкокси, OR, арилалкила, NCS, малеимида, NHCOOR, N(R)2, NHCOR, CONHR, COOR или COR;
R3 представляет собой NHR2, галогенид, N3, OR4, CF3, COR4, COCl, COOCOR4, COOR4, OCOR4, OCONHR4, NHCOOR4, NHCONHR4, OCOOR4, CN, CONH2, CONH(R4), CON(R4)2, SR4, SO2R4, SOR4 SO3H, SO2NH2, SO2NH(R4), SO2N(R4)2, NH2, NH(R4), N(R4)2, CO(N-гетероцикл), NO2, цианат, изоцианат, тиоцианат, изотиоцианат, мезилат, тозилат, трифлат, PO(OH)2 или OPO(OH)2; и
R4 представляет собой H, алкил, галогеналкил, циклоалкил, арил или гетероарил, причем указанные алкильные, галогеналкильные, циклоалкильные, арильные или гетероарильные группы необязательно замещены;
или его изомер, фармацевтически приемлемую соль, фармацевтический продукт, полиморф, гидрат или любую их комбинацию;
где если A представляет собой Br или I, R1 представляет собой CH3, и T представляет собой OH, то X представляет собой N, или анилиновое кольцо образует конденсированное гетероциклическое кольцо.
[0092] Изобретение включает соединение SARD, представленное структурой формулы IIB:
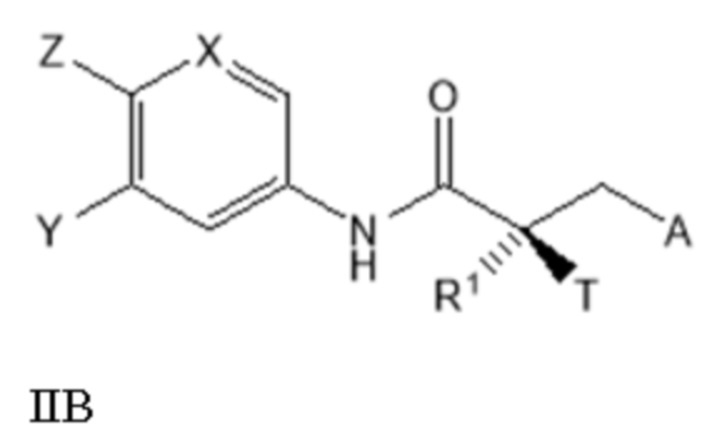
где
R1 представляет собой H, CH3, CH2F, CHF2, CF3, CH2CH3 или CF2CF3;
или T и R1 образуют 3-8-членное карбоциклическое или гетероциклическое кольцо;
T представляет собой H, OH, OR, OCOR, CH3, -NHCOCH3 или NHCOR;
Y представляет собой H, CF3, F, I, Br, Cl, CN или C(R)3;
Z представляет собой H, NO2, CN, галогенид, COOH, COR, NHCOR, CONHR,
или Y и Z образуют 5-8-членное конденсированное кольцо;
X представляет собой CH или N;
R представляет собой H, алкил, алкенил, галогеналкил, спирт, CH2CH2OH, CF3, CH2Cl, CH2CH2Cl, арил, F, Cl, Br, I или OH;
A представляет собой R2 или R3;
R2 представляет собой пиррольное, пирролиновое, пирролидиновое, пиразольное, пиразолиновое, пиразолидиновое, триазольное, имидазольное, имидазолиновое, имидазолидиновое или морфолиновое кольцо, причем указанное кольцо необязательно замещено по меньшей мере одним из Q1, Q2, Q3 или Q4, каждый из которых независимо выбран из водорода, кето, замещенного или незамещенного линейного или разветвленного алкила, замещенного или незамещенного циклоалкила, замещенного или незамещенного гетероциклоалкила, галогеналкила, CF3, замещенного или незамещенного арила, замещенного или незамещенного фенила, F, Cl, Br, I, CN, NO2, гидроксила, алкокси, OR, арилалкила, NCS, малеимида, NHCOOR, N(R)2, NHCOR, CONHR, COOR или COR;
R3 представляет собой NHR2, галогенид, N3, OR4, CF3, COR4, COCl, COOCOR4, COOR4, OCOR4, OCONHR4, NHCOOR4, NHCONHR4, OCOOR4, CN, CONH2, CONH(R4), CON(R4)2, SR4, SO2R4, SOR4 SO3H, SO2NH2, SO2NH(R4), SO2N(R4)2, NH2, NH(R4), N(R4)2, CO(N-гетероцикл), NO2, цианат, изоцианат, тиоцианат, изотиоцианат, мезилат, тозилат, трифлат, PO(OH)2 или OPO(OH)2; и
R4 представляет собой H, алкил, галогеналкил, циклоалкил, арил или гетероарил, причем указанные алкильные, галогеналкильные, циклоалкильные, арильные или гетероарильные группы необязательно замещены;
или его изомер, фармацевтически приемлемую соль, фармацевтический продукт, полиморф, гидрат или любую их комбинацию;
где если A представляет собой Br или I, R1 представляет собой CH3, и T представляет собой OH, то X представляет собой N, или анилиновое кольцо образует конденсированное гетероциклическое кольцо.
[0093] Изобретение включает соединение SARD, представленное структурой формулы III:
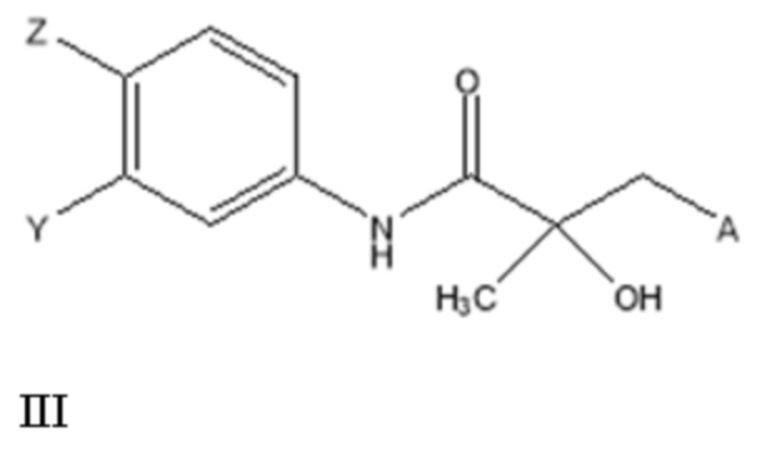
где
Y представляет собой H, CF3, F, I, Br, Cl, CN или C(R)3;
Z представляет собой H, NO2, CN, галогенид, COOH, COR, NHCOR, CONHR,
или Y и Z образуют 5-8-членное конденсированное кольцо;
R представляет собой H, алкил, алкенил, галогеналкил, спирт, CH2CH2OH, CF3, CH2Cl, CH2CH2Cl, арил, F, Cl, Br, I или OH;
A представляет собой R2 или R3;
R2 представляет собой пиррольное, пирролиновое, пирролидиновое, пиразольное, пиразолиновое, пиразолидиновое, триазольное, имидазольное, имидазолиновое, имидазолидиновое или морфолиновое кольцо, причем указанное кольцо необязательно замещено по меньшей мере одним из Q1, Q2, Q3 или Q4, каждый из которых независимо выбран из водорода, кето, замещенного или незамещенного линейного или разветвленного алкила, замещенного или незамещенного циклоалкила, замещенного или незамещенного гетероциклоалкила, галогеналкила, CF3, замещенного или незамещенного арила, замещенного или незамещенного фенила, F, Cl, Br, I, CN, NO2, гидроксила, алкокси, OR, арилалкила, NCS, малеимида, NHCOOR, N(R)2, NHCOR, CONHR, COOR или COR;
R3 представляет собой NHR2, галогенид, N3, OR4, CF3, COR4, COCl, COOCOR4, COOR4, OCOR4, OCONHR4, NHCOOR4, NHCONHR4, OCOOR4, CN, CONH2, CONH(R4), CON(R4)2, SR4, SO2R4, SOR4 SO3H, SO2NH2, SO2NH(R4), SO2N(R4)2, NH2, NH(R4), N(R4)2, CO(N-гетероцикл), NO2, цианат, изоцианат, тиоцианат, изотиоцианат, мезилат, тозилат, трифлат, PO(OH)2 или OPO(OH)2; и
R4 представляет собой H, алкил, галогеналкил, циклоалкил, арил или гетероарил, причем указанные алкильные, галогеналкильные, циклоалкильные, арильные или гетероарильные группы необязательно замещены;
или его оптический изомер, изомер, фармацевтически приемлемую соль, фармацевтический продукт, полиморф, гидрат или любую их комбинацию;
где если A представляет собой Br или I, то анилиновое кольцо образует конденсированное гетероциклическое кольцо.
[0094] В различных вариантах реализации соединение SARD формулы III содержит хиральный атом углерода. В других вариантах реализации соединение SARD формулы III представляет собой рацемическую смесь. В других вариантах реализации соединение SARD формулы III представляет собой (S)-изомер. В других вариантах реализации соединение SARD формулы III представляет собой (R)-изомер.
[0095] Изобретение включает соединение, селективно разрушающее андрогенные рецепторы, представленное структурой формулы IV:
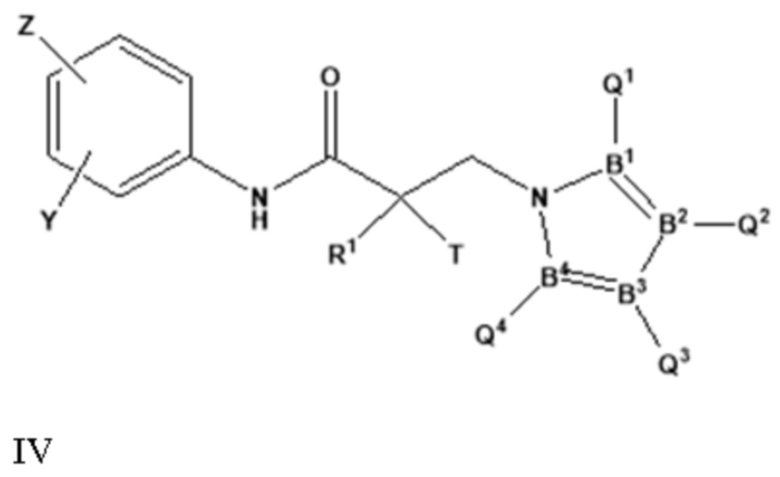
где
каждый B1, B2, B3 и B4 независимо представляет собой углерод или азот;
Y представляет собой H, CF3, F, I, Br, Cl, CN или C(R)3;
Z представляет собой H, NO2, CN, галогенид, COOH, COR, NHCOR, CONHR,
или Y и Z образуют 5-8-членное конденсированное кольцо;
R1 представляет собой H, CH3, CH2F, CHF2, CF3, CH2CH3 или CF2CF3;
T представляет собой H, OH, OR, OCOR, CH3, -NHCOCH3 или NHCOR;
или T и R1 образуют 3-8-членное карбоциклическое или гетероциклическое кольцо;
R представляет собой H, алкил, алкенил, галогеналкил, спирт, CH2CH2OH, CF3, CH2Cl, CH2CH2Cl, арил, F, Cl, Br, I или OH; и
каждый Q1, Q2, Q3 или Q4 независимо выбран из водорода, кето, замещенного или незамещенного линейного или разветвленного алкила, замещенного или незамещенного циклоалкила, замещенного или незамещенного гетероциклоалкила, галогеналкила, CF3, замещенного или незамещенного арила, замещенного или незамещенного фенила, F, Cl, Br, I, CN, NO2, гидроксила, алкокси, OR, арилалкила, NCS, малеимида, NHCOOR, N(R)2, NHCOR, CONHR, COOR или COR; где если B1, B2, B3 или B4 представляет собой азот, то Q1, Q2, Q3 или Q4, соответственно, отсутствует; или его оптический изомер, изомер, фармацевтически приемлемую соль, фармацевтический продукт, полиморф, гидрат или любую их комбинацию.
[0096] В различных вариантах реализации соединение SARD формулы IV содержит хиральный атом углерода. В других вариантах реализации соединение SARD формулы IV представляет собой рацемическую смесь. В других вариантах реализации соединение SARD формулы IV представляет собой (S)-изомер. В других вариантах реализации соединение SARD формулы IV представляет собой (R)-изомер.
[0097] Изобретение включает соединение, селективно разрушающее андрогенные рецепторы, представленное структурой формулы V:
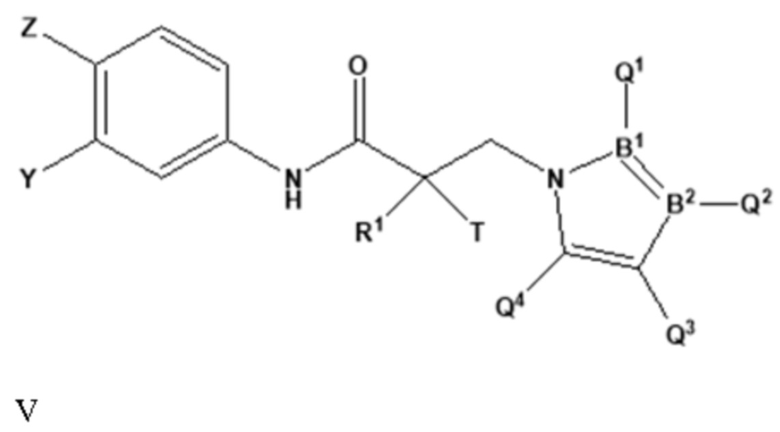
где
каждый B1 и B2 независимо представляет собой углерод или азот;
Y представляет собой H, CF3, F, I, Br, Cl, CN или C(R)3;
Z представляет собой H, NO2, CN, галогенид, COOH, COR, NHCOR, CONHR,
или Y и Z образуют 5-8- членное конденсированное кольцо;
R1 представляет собой H, CH3, CH2F, CHF2, CF3, CH2CH3 или CF2CF3;
T представляет собой H, OH, OR, OCOR, CH3, -NHCOCH3 или NHCOR;
или T и R1 образуют 3-8-членное карбоциклическое или гетероциклическое кольцо;
R представляет собой H, алкил, алкенил, галогеналкил, спирт, CH2CH2OH, CF3, CH2Cl, CH2CH2Cl, арил, F, Cl, Br, I или OH; и
каждый Q1, Q2, Q3 или Q4 независимо выбран из водорода, кето, замещенного или незамещенного линейного или разветвленного алкила, замещенного или незамещенного циклоалкила, замещенного или незамещенного гетероциклоалкила, галогеналкила, CF3, замещенного или незамещенного арила, замещенного или незамещенного фенила, F, Cl, Br, I, CN, NO2, гидроксила, алкокси, OR, арилалкила, NCS, малеимида, NHCOOR, N(R)2, NHCOR, CONHR, COOR или COR; где если B1 или B2 представляет собой азот, то Q1 или Q2, соответственно, отсутствует; или его оптический изомер, изомер, фармацевтически приемлемую соль, фармацевтический продукт, полиморф, гидрат или любую их комбинацию.
[0098] В различных вариантах реализации соединение SARD формулы V содержит хиральный атом углерода. В других вариантах реализации соединение SARD формулы V представляет собой рацемическую смесь. В других вариантах реализации соединение SARD формулы V представляет собой (S)-изомер. В других вариантах реализации соединение SARD формулы V представляет собой (R)-изомер.
[0099] Изобретение включает соединение, селективно разрушающее андрогенные рецепторы, представленное структурой формулы VI:
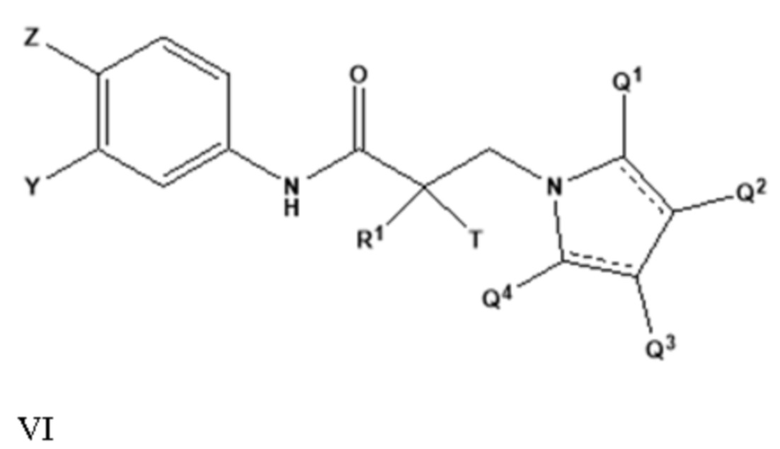
где
 представляет собой простую или двойную связь;
представляет собой простую или двойную связь;
Y представляет собой H, CF3, F, I, Br, Cl, CN или C(R)3;
Z представляет собой H, NO2, CN, галогенид, COOH, COR, NHCOR, CONHR,
или Y и Z образуют 5-8-членное конденсированное кольцо;
R1 представляет собой H, CH3, CH2F, CHF2, CF3, CH2CH3 или CF2CF3;
T представляет собой H, OH, OR, OCOR, CH3, -NHCOCH3 или NHCOR;
или T и R1 образуют 3-8-членное карбоциклическое или гетероциклическое кольцо;
R представляет собой H, алкил, алкенил, галогеналкил, спирт, CH2CH2OH, CF3, CH2Cl, CH2CH2Cl, арил, F, Cl, Br, I или OH; и
каждый из Q1, Q2, Q3 или Q4 независимо выбран из водорода, кето, замещенного или незамещенного линейного или разветвленного алкила, замещенного или незамещенного циклоалкила, замещенного или незамещенного гетероциклоалкила, галогеналкила, CF3, замещенного или незамещенного арила, замещенного или незамещенного фенила, F, Cl, Br, I, CN, NO2, гидроксила, алкокси, OR, арилалкила, NCS, малеимида, NHCOOR, N(R)2, NHCOR, CONHR, COOR или COR; или его оптический изомер, изомер, фармацевтически приемлемую соль, фармацевтический продукт, полиморф, гидрат или любую их комбинацию.
[00100] В различных вариантах реализации соединение SARD формулы VI содержит хиральный атом углерода. В других вариантах реализации соединение SARD формулы VI представляет собой рацемическую смесь. В других вариантах реализации соединение SARD формулы VI представляет собой (S)-изомер. В других вариантах реализации соединение SARD формулы VI представляет собой (R)-изомер.
[00101] Изобретение включает соединение, селективно разрушающее андрогенные рецепторы, представленное структурой формулы VII:
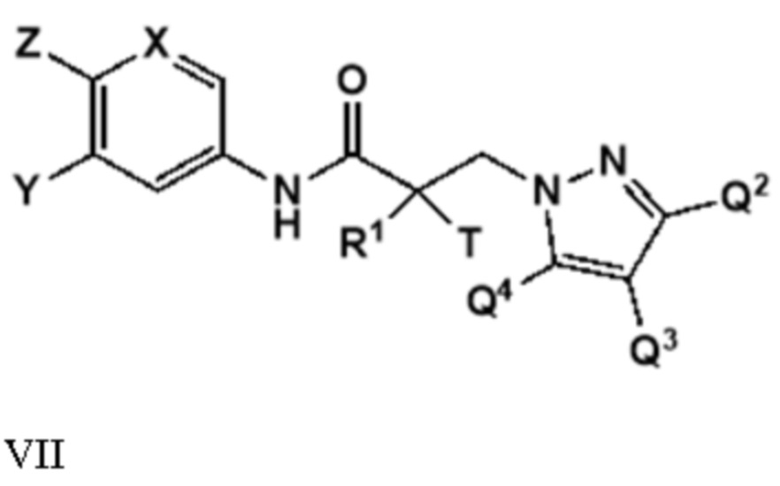
где
X представляет собой CH или N;
Y представляет собой H, CF3, F, I, Br, Cl, CN или C(R)3;
Z представляет собой H, NO2, CN, галогенид, COOH, COR, NHCOR, CONHR,
или Y и Z образуют 5-8-членное конденсированное кольцо;
R1 представляет собой H, CH3, CH2F, CHF2, CF3, CH2CH3 или CF2CF3;
T представляет собой H, OH, OR, OCOR, CH3, -NHCOCH3 или NHCOR;
или T и R1 образуют 3-8-членное карбоциклическое или гетероциклическое кольцо;
R представляет собой H, алкил, алкенил, галогеналкил, спирт, CH2CH2OH, CF3, CH2Cl, CH2CH2Cl, арил, F, Cl, Br, I или OH; и
каждый из Q2, Q3 или Q4 независимо выбран из водорода, кето, замещенного или незамещенного линейного или разветвленного алкила, замещенного или незамещенного циклоалкила, замещенного или незамещенного гетероциклоалкила, галогеналкила, CF3, замещенного или незамещенного арила, замещенного или незамещенного фенила, F, Cl, Br, I, CN, NO2, гидроксила, алкокси, OR, арилалкила, NCS, малеимида, NHCOOR, N(R)2, NHCOR, CONHR, COOR или COR; или его оптический изомер, изомер, фармацевтически приемлемую соль, фармацевтический продукт, полиморф, гидрат или любую их комбинацию.
[00102] В различных вариантах реализации соединение SARD формулы VII содержит хиральный атом углерода. В других вариантах реализации соединение SARD формулы VII представляет собой рацемическую смесь. В других вариантах реализации соединение SARD формулы VII представляет собой (S)-изомер. В других вариантах реализации соединение SARD формулы VII представляет собой (R)-изомер.
[00103] Изобретение включает соединение, селективно разрушающее андрогенные рецепторы, представленное структурой формулы VIIA:
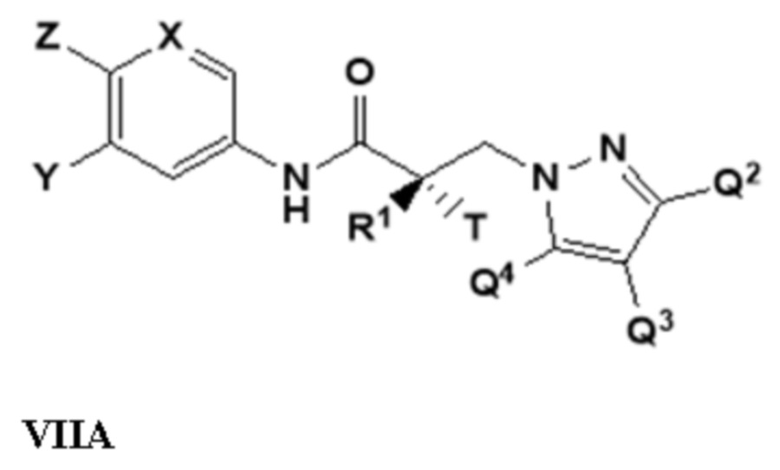
где
X представляет собой CH или N;
Y представляет собой H, CF3, F, I, Br, Cl, CN или C(R)3;
Z представляет собой H, NO2, CN, галогенид, COOH, COR, NHCOR, CONHR,
или Y и Z образуют 5-8-членное конденсированное кольцо;
R1 представляет собой H, CH3, CH2F, CHF2, CF3, CH2CH3 или CF2CF3;
T представляет собой H, OH, OR, OCOR, CH3, -NHCOCH3 или NHCOR;
или T и R1 образуют 3-8-членное карбоциклическое или гетероциклическое кольцо;
R представляет собой H, алкил, алкенил, галогеналкил, спирт, CH2CH2OH, CF3, CH2Cl, CH2CH2Cl, арил, F, Cl, Br, I или OH; и
каждый из Q2, Q3 или Q4 независимо выбран из водорода, кето, замещенного или незамещенного линейного или разветвленного алкила, замещенного или незамещенного циклоалкила, замещенного или незамещенного гетероциклоалкила, галогеналкила, CF3, замещенного или незамещенного арила, замещенного или незамещенного фенила, F, Cl, Br, I, CN, NO2, гидроксила, алкокси, OR, арилалкила, NCS, малеимида, NHCOOR, N(R)2, NHCOR, CONHR, COOR или COR; или его изомер, фармацевтически приемлемую соль, фармацевтический продукт, полиморф, гидрат или любую их комбинацию.
[00104] Изобретение включает соединение, селективно разрушающее андрогенные рецепторы, представленное структурой формулы VIIB:
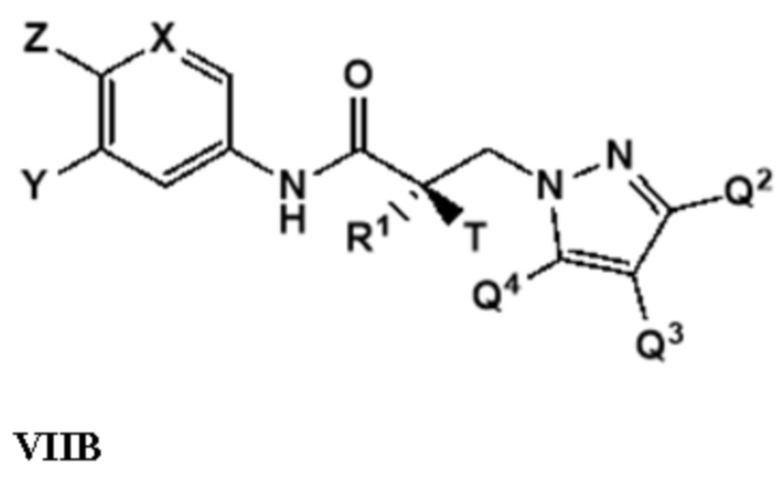
где
X представляет собой CH или N;
Y представляет собой H, CF3, F, I, Br, Cl, CN или C(R)3;
Z представляет собой H, NO2, CN, галогенид, COOH, COR, NHCOR, CONHR,
или Y и Z образуют 5-8- членное конденсированное кольцо;
R1 представляет собой H, CH3, CH2F, CHF2, CF3, CH2CH3 или CF2CF3;
T представляет собой H, OH, OR, OCOR, CH3, -NHCOCH3 или NHCOR;
или T и R1 образуют 3-8-членное карбоциклическое или гетероциклическое кольцо;
R представляет собой H, алкил, алкенил, галогеналкил, спирт, CH2CH2OH, CF3, CH2Cl, CH2CH2Cl, арил, F, Cl, Br, I или OH; и
каждый из Q2, Q3 или Q4 независимо выбран из водорода, кето, замещенного или незамещенного линейного или разветвленного алкила, замещенного или незамещенного циклоалкила, замещенного или незамещенного гетероциклоалкила, галогеналкила, CF3, замещенного или незамещенного арила, замещенного или незамещенного фенила, F, Cl, Br, I, CN, NO2, гидроксила, алкокси, OR, арилалкила, NCS, малеимида, NHCOOR, N(R)2, NHCOR, CONHR, COOR или COR; или его изомер, фармацевтически приемлемую соль, фармацевтический продукт, полиморф, гидрат или любую их комбинацию.
[00105] В одном из вариантов реализации A в формуле I-III, IA, IB, IIA и IIB, и R2 в формуле IC представляет собой пяти- или шестичленное насыщенное или ненасыщенное кольцо, содержащее по меньшей мере один атом азота. В другом варианте реализации A представляет собой замещенное или незамещенное пиррольное, пирролиновое, пирролидиновое, пиразольное, пиразолиновое, пиразолидиновое, имидазольное, имидазолиновое, имидазолидиновое, триазольное, тетразольное, пиридиновое, морфолиновое или другое гетероциклическое кольцо. Каждое из них представляет собой отдельный вариант реализации настоящего изобретения. В другом варианте реализации A представляет собой пяти- или шестичленное гетероциклическое кольцо. В другом варианте реализации атом азота в пяти- или шестичленном насыщенном или ненасыщенном кольце присоединен к основной структуре молекулы. В другом варианте реализации атом углерода в пяти- или шестичленном насыщенном или ненасыщенном кольце присоединен к основной структуре молекулы.
[00106] В одном из вариантов реализации A в формуле I-III, IA, IB, IIA и IIB, и R3 в формуле ID представляют собой NHR2, галогенид, N3, OR4, CF3, COR4, COCl, COOCOR4, COOR4, OCOR4, OCONHR4, NHCOOR4, NHCONHR4, OCOOR4, CN, CONH2, CONH(R4), CON(R4)2, SR4, SO2R4, SOR4 SO3H, SO2NH2, SO2NH(R4), SO2N(R4)2, NH2, NH(R4), N(R4)2, CO(N-гетероцикл), NO2, цианат, изоцианат, тиоцианат, изотиоцианат, мезилат, тозилат, трифлат, PO(OH)2 или OPO(OH)2; где R4 представляет собой H, алкил, галогеналкил, циклоалкил, арил или гетероарил, причем указанные алкильные, галогеналкильные, циклоалкильные, арильные или гетероарильные группы необязательно замещены.
[00107] В одном из вариантов реализации A в формуле I-III, IA, IB, IIA и IIB, и R3 в формуле ID представляют собой NHR2. В одном из вариантов реализации A в формуле I-III, IA, IB, IIA и IIB, и R3 в формуле ID представляют собой галогенид. В одном из вариантов реализации A в формуле I-III, IA, IB, IIA и IIB, и R3 в формуле ID представляют собой F. В одном из вариантов реализации A в формуле I-III, IA, IB, IIA и IIB, и R3 в формуле ID представляют собой Br. В одном из вариантов реализации A в формуле I-III, IA, IB, IIA и IIB, и R3 в формуле ID представляют собой Cl. В одном из вариантов реализации A в формуле I-III, IA, IB, IIA и IIB, и R3 в формуле ID представляют собой I. В одном из вариантов реализации A в формуле I-III, IA, IB, IIA и IIB, и R3 в формуле ID представляют собой N3. В одном из вариантов реализации A в формуле I-III, IA, IB, IIA и IIB, и R3 в формуле ID представляют собой OR4. В одном из вариантов реализации A в формуле I-III, IA, IB, IIA и IIB, и R3 в формуле ID представляют собой CF3. В одном из вариантов реализации A в формуле I-III, IA, IB, IIA и IIB, и R3 в формуле ID представляют собой COR4. В одном из вариантов реализации A в формуле I-III, IA, IB, IIA и IIB, и R3 в формуле ID представляют собой COCl. В одном из вариантов реализации A в формуле I-III, IA, IB, IIA и IIB, и R3 в формуле ID представляют собой COOCOR4. В одном из вариантов реализации A в формуле I-III, IA, IB, IIA и IIB, и R3 в формуле ID представляют собой COOR4. В одном из вариантов реализации A в формуле I-III, IA, IB, IIA и IIB, и R3 в формуле ID представляют собой OCOR4. В одном из вариантов реализации A в формуле I-III, IA, IB, IIA и IIB, и R3 в формуле ID представляют собой OCONHR4. В одном из вариантов реализации A в формуле I-III, IA, IB, IIA и IIB, и R3 в формуле ID представляют собой NHCOOR4. В одном из вариантов реализации A в формуле I-III, IA, IB, IIA и IIB, и R3 в формуле ID представляют собой NHCONHR4. В одном из вариантов реализации A в формуле I-III, IA, IB, IIA и IIB, и R3 в формуле ID представляют собой OCOOR4. В одном из вариантов реализации A в формуле I-III, IA, IB, IIA и IIB, и R3 в формуле ID представляют собой CN. В одном из вариантов реализации A в формуле I-III, IA, IB, IIA и IIB, и R3 в формуле ID представляют собой CON(R4)2. В одном из вариантов реализации A в формуле I-III, IA, IB, IIA и IIB, и R3 в формуле ID представляют собой SR4. В одном из вариантов реализации A в формуле I-III, IA, IB, IIA и IIB, и R3 в формуле ID представляют собой SO2R4. В одном из вариантов реализации A в формуле I-III, IA, IB, IIA и IIB, и R3 в формуле ID представляют собой SOR4. В одном из вариантов реализации A в формуле I-III, IA, IB, IIA и IIB, и R3 в формуле ID представляют собой SO3H. В одном из вариантов реализации A в формуле I-III, IA, IB, IIA и IIB, и R3 в формуле ID представляют собой SO2NH2. В одном из вариантов реализации A в формуле I-III, IA, IB, IIA и IIB, и R3 в формуле ID представляют собой SO2NH(R4). В одном из вариантов реализации A в формуле I-III, IA, IB, IIA и IIB, и R3 в формуле ID представляют собой SO2N(R4)2. В одном из вариантов реализации A в формуле I-III, IA, IB, IIA и IIB, и R3 в формуле ID представляют собой NH2. В одном из вариантов реализации A в формуле I-III, IA, IB, IIA и IIB, и R3 в формуле ID представляют собой NH(R4). В одном из вариантов реализации A в формуле I-III, IA, IB, IIA и IIB, и R3 в формуле ID представляют собой N(R4)2. В одном из вариантов реализации A в формуле I-III, IA, IB, IIA и IIB, и R3 в формуле ID представляют собой CONH2. В одном из вариантов реализации A в формуле I-III, IA, IB, IIA и IIB, и R3 в формуле ID представляют собой CONH(R4). В одном из вариантов реализации A в формуле I-III, IA, IB, IIA и IIB, и R3 в формуле ID представляют собой СО(N-гетероцикл). В одном из вариантов реализации A в формуле I-III, IA, IB, IIA и IIB, и R3 в формуле ID представляют собой NO2. В одном из вариантов реализации A в формуле I-III, IA, IB, IIA и IIB, и R3 в формуле ID представляют собой цианат. В одном из вариантов реализации A в формуле I-III, IA, IB, IIA и IIB, и R3 в формуле ID представляют собой изоцианат. В одном из вариантов реализации A в формуле I-III, IA, IB, IIA и IIB, и R3 в формуле ID представляют собой тиоцианат. В одном из вариантов реализации A в формуле I-III, IA, IB, IIA и IIB, и R3 в формуле ID представляют собой изотиоцианат. В одном из вариантов реализации A в формуле I-III, IA, IB, IIA и IIB, и R3 в формуле ID представляют собой мезилат. В одном из вариантов реализации A в формуле I-III, IA, IB, IIA и IIB, и R3 в формуле ID представляют собой тозилат. В одном из вариантов реализации A в формуле I-III, IA, IB, IIA и IIB, и R3 в формуле ID представляют собой трифлат. В одном из вариантов реализации A в формуле I-III, IA, IB, IIA и IIB, и R3 в формуле ID представляют собой PO(OH)2. В одном из вариантов реализации A в формуле I-III, IA, IB, IIA и IIB, и R3 в формуле ID представляют собой OPO(OH)2.
[00108] В одном из вариантов реализации R4 представляет собой H, алкил, галогеналкил, циклоалкил, арил или гетероарил, причем указанные алкильные, галогеналкильные, циклоалкильные, арильные или гетероарильные группы необязательно замещены. Каждый из них представляет собой отдельный вариант реализации настоящего изобретения. В другом варианте реализации R4 представляет собой H. В других вариантах реализации R4 представляет собой алкил. В других вариантах реализации алкил представляет собой метил, этил, пропил, изопропил, бутил, трет-бутил, пентил, неопентил, изопентил, гексил или гептил, каждый из которых представляет собой отдельный вариант реализации настоящего изобретения. В других вариантах реализации R4 представляет собой галогеналкил. В другом варианте реализации галогеналкил представляет собой CF3, CF2CF3, йодметил, бромметил, бромэтил, бромпропил, каждый из которых представляет собой отдельный вариант реализации изобретения. В других вариантах реализации R4 представляет собой циклоалкил. В других вариантах реализации циклоалкил представляет собой циклобутил, циклопентил, циклогексил. В различных вариантах реализации алкил, галогеналкил, циклоалкил, арил или гетероарил в R4 дополнительно замещены одной или более группами, выбранными из: галогенида, CN, CO2H, OH, SH, NH2, NO2, CO2-(C1-C6 алкила) или O-(C1-C6 алкила); каждый из которых представляет собой отдельный вариант реализации настоящего изобретения.
[00109] В конкретном варианте реализации формул I - VI, IA-IC, IIA или IIB Q1 представляет собой водород. В конкретном варианте реализации формул I - VI, IA-IC, IIA или IIB Q1 представляет собой CN. В конкретном варианте реализации формул I - VI, IA-IC, IIA или IIB Q1 представляет собой F. В конкретном варианте реализации формул I - VI, IA-IC, IIA или IIB Q1 представляет собой NCS. В конкретном варианте реализации формул I - VI, IA-IC, IIA или IIB Q1 представляет собой малеимид. В конкретном варианте реализации формул I - VI, IA-IC, IIA или IIB Q1 представляет собой NHCOOR. В конкретном варианте реализации формул I - VI, IA-IC, IIA или IIB Q1 представляет собой N(R)2. В конкретном варианте реализации формул I - VI, IA-IC, IIA или IIB Q1 представляет собой CONHR. В конкретном варианте реализации формул I - VI, IA-IC, IIA или IIB Q1 представляет собой NHCOR. В конкретном варианте реализации формул I - VI, IA-IC, IIA или IIB Q1 представляет собой Cl. В конкретном варианте реализации формул I - VI, IA-IC, IIA или IIB Q1 представляет собой Br. В конкретном варианте реализации формул I - VI, IA-IC, IIA или IIB Q1 представляет собой I. В конкретном варианте реализации формул I - VI, IA-IC, IIA или IIB Q1 представляет собой NO2. В конкретном варианте реализации формул I - VI, IA-IC, IIA или IIB Q1 представляет собой фенил. В конкретном варианте реализации формул I - VI, IA-IC, IIA или IIB Q1 представляет собой 4-фторфенил. В конкретном варианте реализации формул I - VI, IA-IC, IIA или IIB Q1 представляет собой CF3. В конкретном варианте реализации формул I - VI, IA-IC, IIA или IIB Q1 представляет собой замещенный или незамещенный алкил. В конкретном варианте реализации формул I - VI, IA-IC, IIA или IIB Q1 представляет собой замещенный или незамещенный циклоалкил. В конкретном варианте реализации формул I - VI, IA-IC, IIA или IIB Q1 представляет собой замещенный или незамещенный гетероциклоалкил. В конкретном варианте реализации формул I - VI, IA-IC, IIA или IIB Q1 представляет собой галогеналкил. В конкретном варианте реализации формул I - VI, IA-IC, IIA или IIB Q1 представляет собой замещенный или незамещенный арил. В конкретном варианте реализации формул I - VI, IA-IC, IIA или IIB Q1 представляет собой гидроксил. В конкретном варианте реализации формул I - VI, IA-IC, IIA или IIB Q1 представляет собой алкокси. В конкретном варианте реализации формул I - VI, IA-IC, IIA или IIB Q1 представляет собой OR. В конкретном варианте реализации формул I - VI, IA-IC, IIA или IIB Q1 представляет собой арилалкил. В конкретном варианте реализации формул I - VI, IA-IC, IIA или IIB Q1 представляет собой амин. В конкретном варианте реализации формул I - VI, IA-IC, IIA или IIB Q1 представляет собой амид. В конкретном варианте реализации формул I - VI, IA-IC, IIA и IIB Q1 представляет собой COOR. В конкретном варианте реализации формул I - VI, IA-IC, IIA или IIB Q1 представляет собой COR. В конкретном варианте реализации формул I - VI, IA-IC, IIA или IIB Q1 представляет собой кето.
[00110] В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q2 представляет собой CN. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q2 представляет собой водород. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q2 представляет собой кето. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q2 представляет собой NCS. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q2 представляет собой малеимид. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q2 представляет собой NHCOOR. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q2 представляет собой N(R)2. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q2 представляет собой CONHR. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q2 представляет собой NHCOR. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q2 представляет собой F. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q2 представляет собой Cl. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q2 представляет собой Br. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q2 представляет собой I. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q2 представляет собой NO2. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q2 представляет собой фенил. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q2 представляет собой 4-фторфенил. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q2 представляет собой CF3. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q2 представляет собой замещенный или незамещенный алкил. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q2 представляет собой замещенный или незамещенный циклоалкил. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q2 представляет собой замещенный или незамещенный гетероциклоалкил. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q2 представляет собой галогеналкил. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q2 представляет собой замещенный или незамещенный арил. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q2 представляет собой гидроксил. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q2 представляет собой алкокси. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q2 представляет собой OR. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q2 представляет собой арилалкил. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q2 представляет собой амин. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q2 представляет собой амид. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q2 представляет собой COOR. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q2 представляет собой COR.
[00111] В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q3 представляет собой CN. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q3 представляет собой F. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q3 представляет собой NCS. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q3 представляет собой малеимид. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q3 представляет собой NHCOOR. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q3 представляет собой N(R)2. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q3 представляет собой CONHR. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q3 представляет собой NHCOR. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q3 представляет собой водород. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q3 представляет собой кето. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q3 представляет собой Cl. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q3 представляет собой Br. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q3 представляет собой I. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q3 представляет собой NO2. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q3 представляет собой фенил. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q3 представляет собой 4-фторфенил. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q3 представляет собой CF3. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q3 представляет собой замещенный или незамещенный алкил. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q3 представляет собой замещенный или незамещенный циклоалкил. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q3 представляет собой замещенный или незамещенный гетероциклоалкил. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q3 представляет собой галогеналкил. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q3 представляет собой замещенный или незамещенный арил. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q3 представляет собой гидроксил. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q3 представляет собой алкокси. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q3 представляет собой OR. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q3 представляет собой арилалкил. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q3 представляет собой амин. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q3 представляет собой амид. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q3 представляет собой COOR. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q3 представляет собой COR.
[00112] В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q4 представляет собой CN. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q4 представляет собой F. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q4 представляет собой NCS. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q4 представляет собой малеимид. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q4 представляет собой NHCOOR. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q4 представляет собой N(R)2. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q4 представляет собой CONHR. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q4 представляет собой NHCOR. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q4 представляет собой водород. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q4 представляет собой кето. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q4 представляет собой Cl. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q4 представляет собой Br. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q4 представляет собой I. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q4 представляет собой NO2. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q4 представляет собой фенил. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q4 представляет собой 4-фторфенил. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q4 представляет собой CF3. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q4 представляет собой замещенный или незамещенный алкил. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q4 представляет собой замещенный или незамещенный циклоалкил. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q4 представляет собой замещенный или незамещенный гетероциклоалкил. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q4 представляет собой галогеналкил. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q4 представляет собой замещенный или незамещенный арил. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q4 представляет собой гидроксил. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q4 представляет собой алкокси. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q4 представляет собой OR. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q4 представляет собой арилалкил. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q4 представляет собой амин. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q4 представляет собой амид. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q4 представляет собой COOR. В конкретном варианте реализации формул I -VII, IA-IC, IIA, IIB, VIIA или VIIB Q4 представляет собой COR. В конкретном варианте реализации формул I, IA, IB, IC, ID, II, IIA, IIB, VII, VIIA или VIIB X представляет собой CH. В конкретном варианте реализации формул I, IA, IB, IC, ID, II, IIA, IIB, VII, VIIA или VIIB X представляет собой N.
[00113] В некоторых вариантах реализации, если A или R3 представляет собой Br или I, R1 представляет собой CH3, и T представляет собой OH, то X представляет собой N или анилиновое кольцо образует конденсированное гетероциклическое кольцо.
[00114] В конкретном варианте реализации формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB Y представляет собой H. В конкретном варианте реализации формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB Y представляет собой CF3. В конкретном варианте реализации формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB Y представляет собой F. В конкретном варианте реализации формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB Y представляет собой I. В конкретном варианте реализации формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB Y представляет собой Br. В конкретном варианте реализации формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB Y представляет собой Cl. В конкретном варианте реализации формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB Y представляет собой CN. В конкретном варианте реализации формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB Y представляет собой C(R)3.
[00115] В конкретном варианте реализации формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB Z представляет собой H. В конкретном варианте реализации формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB Z представляет собой NO2. В конкретном варианте реализации формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB Z представляет собой CN. В конкретном варианте реализации формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB Z представляет собой галогенид. В конкретном варианте реализации формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB Z представляет собой F. В конкретном варианте реализации формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB Z представляет собой Cl. В конкретном варианте реализации формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB Z представляет собой Br. В конкретном варианте реализации формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB Z представляет собой I. В конкретном варианте реализации формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB Z представляет собой COOH. В конкретном варианте реализации формул I -VII, IA, IB, I IC, ID, IA, IIB, VIIA или VIIB Z представляет собой COR. В конкретном варианте реализации формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB Z представляет собой NHCOR. В конкретном варианте реализации формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB Z представляет собой CONHR.
[00116] В конкретном варианте реализации формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB Y и Z образуют кольцо, конденсированное с фенилом. В других вариантах реализации кольцо, конденсированное с фенилом, представляет собой 5-8-членное кольцо. В других вариантах реализации кольцо, конденсированное с фенилом, представляет собой 5- или 6-членное кольцо. В других вариантах реализации кольцо является карбоциклическим или гетероциклическим. В других вариантах реализации Y и Z совместно с фенилом образуют нафтил, хинолинил, бензимидазолил, индазолил, индолил, изоиндолил, инденил или хиназолинил. В конкретном варианте реализации Y и Z совместно с фенилом образуют хиназолин-6-ильную систему колец.
[00117] В конкретном варианте реализации формул I, II, IV, V, VI, VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB R1 представляет собой H. В конкретном варианте реализации формул I, II, IV, V, VI, VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB R1 представляет собой CH3. В конкретном варианте реализации формул I, II, IV, V, VI, VII, IA, IB, IIA, IIB, IC, ID, VIIA или VIIB R1 представляет собой CH2F. В конкретном варианте реализации формул I, II, IV, V, VI, VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB R1 представляет собой CHF2. В конкретном варианте реализации формул I, II, IV, V, VI, VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB R1 представляет собой CF3. В конкретном варианте реализации формул I, II, IV, V, VI, VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB R1 представляет собой CH2CH3. В конкретном варианте реализации формул I, II, IV, V, VI, VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB R1 представляет собой CF2CF3.
[00118] В конкретном варианте реализации формул I, II, IV, V, VI, VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB T представляет собой H. В конкретном варианте реализации формул I, II, IV, V, VI, VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB T представляет собой OH. В конкретном варианте реализации формул I, II, IV, V, VI, VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB T представляет собой OR. В конкретном варианте реализации формул I, II, IV, V, VI, VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB T представляет собой OCOR. В конкретном варианте реализации формул I, II, IV, V, VI, VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB T представляет собой CH3. В конкретном варианте реализации формул I, II, IV, V, VI, VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB T представляет собой -NHCOCH3. В конкретном варианте реализации формул I, II, IV, V, VI, VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB T представляет собой NHCOR.
[00119] В конкретном варианте реализации формул I, II, IV, V, VI, VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB T совместно с R1 образуют 3-8-членное карбоциклическое или гетероциклическое кольцо. В других вариантах реализации T совместно с R1 образуют 3-, 4-, 5-, 6-, 7- или 8-членное карбоциклическое или гетероциклическое кольцо. Каждое из них представляет собой отдельный вариант реализации настоящего изобретения. В некоторых вариантах реализации T совместно с R1 образуют карбоциклическое кольцо, такое как циклопропил, циклобутил, циклопентил, циклогексил и т.д. В некоторых вариантах реализации T совместно с R1 образуют гетероциклическое кольцо, такое как пиперидин, пиридин, фуран, тиофен, пиррол, пиразол, пиримидин и т.д.
[00120] В конкретном варианте реализации формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB R представляет собой H. В конкретном варианте реализации формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB R представляет собой алкил. В конкретном варианте реализации формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB R представляет собой алкенил. В конкретном варианте реализации формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB R представляет собой галогеналкил. В конкретном варианте реализации формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB R представляет собой спирт. В конкретном варианте реализации формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB R представляет собой CH2CH2OH. В конкретном варианте реализации формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB R представляет собой CF3. В конкретном варианте реализации формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB R представляет собой CH2Cl. В конкретном варианте реализации формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB R представляет собой CH2CH2Cl. В конкретном варианте реализации формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB R представляет собой арил. В конкретном варианте реализации формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB R представляет собой F. В конкретном варианте реализации формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB R представляет собой Cl. В конкретном варианте реализации формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB R представляет собой Br. В конкретном варианте реализации формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB R представляет собой I. В конкретном варианте реализации формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB R представляет собой OH.
[00121] В конкретном варианте реализации формулы IV Q1 представляет собой H, CN, CF3, фенил, 4-фторфенил, F, Br, Cl, I, COMe, NHCOOMe, NHCOMe или NHCOOC(CH3)3.
[00122] В конкретном варианте реализации формулы V Q1 представляет собой H, CN, CF3, фенил, 4-фторфенил, F, Br, Cl, I, COMe, NHCOOMe, NHCOMe или NHCOOC(CH3)3.
[00123] В конкретном варианте реализации формулы VI Q1 представляет собой H, CN, CF3, фенил, 4-фторфенил, F, Br, Cl, I, COMe, NHCOOMe, NHCOMe или NHCOOC(CH3)3.
[00124] В конкретном варианте реализации формулы IV Q2 представляет собой H, CN, CF3, фенил, 4-фторфенил, F, Br, Cl, I, COMe, NHCOOMe, NHCOMe или NHCOOC(CH3)3.
[00125] В конкретном варианте реализации формулы V Q2 представляет собой H, CN, CF3, фенил, 4-фторфенил, F, Br, Cl, I, COMe, NHCOOMe, NHCOMe или NHCOOC(CH3)3.
[00126] В конкретном варианте реализации формулы VI Q2 представляет собой H, CN, CF3, фенил, 4-фторфенил, F, Br, Cl, I, COMe, NHCOOMe, NHCOMe или NHCOOC(CH3)3.
[00127] В конкретном варианте реализации формулы VII Q2 представляет собой H, CN, CF3, фенил, 4-фторфенил, F, Br, Cl, I, COMe, NHCOOMe, NHCOMe или NHCOOC(CH3)3.
[00128] В конкретном варианте реализации формулы VIIA Q2 представляет собой H, CN, CF3, фенил, 4-фторфенил, F, Br, Cl, I, COMe, NHCOOMe, NHCOMe или NHCOOC(CH3)3.
[00129] В конкретном варианте реализации формулы VIIB Q2 представляет собой H, CN, CF3, фенил, 4-фторфенил, F, Br, Cl, I, COMe, NHCOOMe, NHCOMe или NHCOOC(CH3)3.
[00130] В конкретном варианте реализации формулы IV Q3 представляет собой H, CN, CF3, фенил, 4-фторфенил, F, Br, Cl, I, COMe, NHCOOMe, NHCOMe или NHCOOC(CH3)3.
[00131] В конкретном варианте реализации формулы V Q3 представляет собой H, CN, CF3, фенил, 4-фторфенил, F, Br, Cl, I, COMe, NHCOOMe, NHCOMe или NHCOOC(CH3)3.
[00132] В конкретном варианте реализации формулы VI Q3 представляет собой H, CN, CF3, фенил, 4-фторфенил, F, Br, Cl, I, COMe, NHCOOMe, NHCOMe или NHCOOC(CH3)3.
[00133] В конкретном варианте реализации формулы VII Q3 представляет собой H, CN, CF3, фенил, 4-фторфенил, F, Br, Cl, I, COMe, NHCOOMe, NHCOMe или NHCOOC(CH3)3.
[00134] В конкретном варианте реализации формулы IV Q4 представляет собой H, CN, CF3, фенил, 4-фторфенил, F, Br, Cl, I, COMe, NHCOOMe, NHCOMe или NHCOOC(CH3)3.
[00135] В конкретном варианте реализации формулы V Q4 представляет собой H, CN, CF3, фенил, 4-фторфенил, F, Br, Cl, I, COMe, NHCOOMe, NHCOMe или NHCOOC(CH3)3.
[00136] В конкретном варианте реализации формулы VI Q4 представляет собой H, CN, CF3, фенил, 4-фторфенил, F, Br, Cl, I, COMe, NHCOOMe, NHCOMe или NHCOOC(CH3)3.
[00137] В конкретном варианте реализации формулы VII Q4 представляет собой H, CN, CF3, фенил, 4-фторфенил, F, Br, Cl, I, COMe, NHCOOMe, NHCOMe или NHCOOC(CH3)3.
[00138] В конкретном варианте реализации формулы VIIA Q4 представляет собой H, CN, CF3, фенил, 4-фторфенил, F, Br, Cl, I, COMe, NHCOOMe, NHCOMe или NHCOOC(CH3)3.
[00139] В конкретном варианте реализации формулы VIIB Q4 представляет собой H, CN, CF3, фенил, 4-фторфенил, F, Br, Cl, I, COMe, NHCOOMe, NHCOMe или NHCOOC(CH3)3.
[00140] Изобретение включает соединение, селективно разрушающее андрогенные рецепторы (SARD), выбранное из любой из следующих структур:




[00141] При использовании в настоящем описании термин «гетероцикл» или «гетероциклическое кольцо» относится к кольцевой структуре, содержащей помимо атомов углерода по меньшей мере один атом серы, кислорода, азота или любую их комбинацию в составе кольца. Гетероцикл может представлять собой 3-12-членное кольцо; 4-8-членное кольцо; 5-7-членное кольцо; или 6-членное кольцо. Предпочтительно гетероцикл представляет собой 5-6-членное кольцо. Типичные примеры гетероциклов включают, но не ограничиваются ими, пиперидин, пиридин, фуран, тиофен, пиррол, пирролидин, пиразол, пиразин, пиперазин или пиримидин. Примеры C5-C8 гетероциклических колец включают пиран, дигидропиран, тетрагидропиран, дигидропиррол, тетрагидропиррол, пиразин, дигидропиразин, тетрагидропиразин, пиримидин, дигидропиримидин, тетрагидропиримидон, пиразол, дигидропиразол, тетрагидропиразол, триазол, тетразол, пиперидин, пиперазин, пиридин, дигидропиридин, тетрагидропиридин, морфолин, тиоморфолин, фуран, дигидрофуран, тетрагидрофуран, тиофен, дигидротиофен, тетрагидротиофен, тиазол, имидазол, изоксазол и т.д. Гетероциклическое кольцо может быть конденсировано с другим насыщенным или ненасыщенным циклоалкильным или насыщенным или ненасыщенным гетероциклическим кольцом. Если гетероциклическое кольцо является замещенным, то заместители включают по меньшей мере одно из галогена, галогеналкила, гидроксила, алкокси, карбонила, амидо, алкиламидо, диалкиламидо, циано, нитро, CO2H, амино, алкиламино, диалкиламино, карбоксила, тиола или тиоалкила.
[00142] Термин «анилиновая система колец» относится к общему для всех соединений кольцу, изображенному слева на структурах, приведенных в настоящем документе, замещенному X, Y и/или Z.
[00143] Термин «циклоалкил» относится к неароматическому моноциклическому или полициклическому кольцу, содержащему атомы углерода и водорода. Циклоалкильная группа может содержать одну или более углерод-углеродных двойных связей в кольце, если кольцо в результате их наличия не становится ароматическим. Примеры циклоалкильных групп включают, но не ограничиваются ими, (C3-C7) циклоалкильные группы, такие как циклопропил, циклобутил, циклопентил, циклогексил и циклогептил и насыщенные циклические и бициклические терпены, и (C3-C7) циклоалкенильные группы, такие как циклопропенил, циклобутенил, циклопентенил, циклогексенил и циклогептенил и ненасыщенные циклические и бициклические терпены. Примеры C5-C8 карбоциклов включают циклопентановое, циклопентеновое, циклогексановое и циклогексеновое кольца. Циклоалкильная группа может быть незамещенной или замещенной по меньшей мере одним заместителем. Предпочтительно циклоалкильная группа представляет собой моноциклическое кольцо или бициклическое кольцо.
[00144] Термин «алкил» относится к насыщенному алифатическому углеводороду, включая линейные и разветвленные углеводороды. Как правило, алкильная группа содержит 1-12 атомов углерода, 1-7 атомов углерода, 1-6 атомов углерода или 1-4 атомов углерода. Разветвленный алкил представляет собой алкил, замещенный алкильными боковыми цепями, содержащими от 1 до 5 атомов углерода. Разветвленный алкил может содержать алкил, замещенный C1-C5 галогеналкилом. Кроме того, алкильная группа может быть замещена по меньшей мере одним из галогена, галогеналкила, гидроксила, алкоксикарбонила, амидо, алкиламидо, диалкиламидо, нитро, CN, амино, алкиламино, диалкиламино, карбоксила, тио или тиоалкила.
[00145] «Арилалкильная» группа относится к алкилу, связанному с арилом, где алкил и арил такие, как определено в настоящем описании. Примером арилалкильной группы является бензильная группа.
[00146] «Алкенильная» группа относится к ненасыщенному углеводороду, включая линейные и разветвленные углеводороды, содержащему одну или более двойных связей. Алкенильная группа может содержать 2-12 атомов углерода, предпочтительно алкенильная группа содержит 2-6 атомов углерода или 2-4 атомов углерода. Примеры алкенильных групп включают, но не ограничиваются ими, этенил, пропенил, бутенил, циклогексенил и т.д. Алкенильная группа может быть замещена по меньшей мере одним галогеном, гидрокси, алкоксикарбонилом, амидо, алкиламидо, диалкиламидо, нитро, амино, алкиламино, диалкиламино, карбоксилом, тио или тиоалкилом.
[00147] При использовании в настоящем описании термин «арильная» группа относится к ароматической группе, содержащей по меньшей мере одну карбоциклическую ароматическую группу или гетероциклическую ароматическую группу, которая может быть незамещенной или замещенной. Заместители, если они присутствуют, включают, но не ограничиваются ими, по меньшей мере один галоген, галогеналкил, гидрокси, алкоксикарбонил, амидо, алкиламидо, диалкиламидо, нитро, амино, алкиламино, диалкиламино, карбокси или тио или тиоалкил. Неограничивающими примерами арильных колец являются фенил, нафтил, пиранил, пирролил, пиразинил, пиримидинил, пиразолил, пиридинил, фуранил, тиофенил, тиазолил, имидазолил, изоксазолил и т.д. Арильная группа может представлять собой 4-12-членное кольцо, предпочтительно арильная группа представляет собой 4-8-членное кольцо. Также арильная группа может представлять собой 6- или 5-членное кольцо.
[00148] Термин «гетероарил» относится к ароматической группе, содержащей по меньшей мере одно гетероциклическое ароматическое кольцо. В одном из вариантов реализации гетероарил содержит по меньшей мере один гетероатом, такой как сера, кислород, азот, кремний, фосфор, или любую их комбинацию в составе кольца. В другом варианте реализации гетероарил может быть незамещенным или замещен одной или более группами, выбранными из галогена, арила, гетероарила, циано, галогеналкила, гидрокси, алкоксикарбонила, амидо, алкиламидо, диалкиламидо, нитро, амино, алкиламино, диалкиламино, карбокси или тио или тиоалкила. Неограничивающими примерами гетероарильных колец являются пиранил, пирролил, пиразинил, пиримидинил, пиразолил, пиридинил, фуранил, тиофенил, тиазолил, индолил, имидазолил, изоксазолил и т.д. В одном из вариантов реализации гетероарильная группа представляет собой 5-12-членное кольцо. В одном из вариантов реализации гетероарильная группа представляет собой пятичленное кольцо. В одном из вариантов реализации гетероарильная группа представляет собой шестичленное кольцо. В другом варианте реализации гетероарильная группа представляет собой 5-8-членное кольцо. В другом варианте реализации гетероарильная группа содержит 1-4 конденсированных колец. В одном из вариантов реализации гетероарильная группа представляет собой 1,2,3-триазол. В одном из вариантов реализации гетероарил представляет собой пиридил. В одном из вариантов реализации гетероарил представляет собой бипиридил. В одном из вариантов реализации гетероарил представляет собой терпиридил.
[00149] При использовании в настоящем описании термин «галогеналкильная» группа относится к алкильной группе, замещенной одним или более атомами галогенов, например, F, Cl, Br или I.
[00150] «Гидроксильная» группа относится к ОН-группе. Специалистам в данной области техники будет понятно, что если T, Q1, Q2, Q3 или Q4 в соединениях согласно настоящему изобретению представляет собой OR, то R не является OH.
[00151] Термин «галоген» или «галоген-» или «галогенид» относится к галогену: F, Cl, Br или I.
[00152] В одном из вариантов реализации в настоящем изобретении предложены соединения и/или их применение и/или их производные, оптические изомеры, изомеры, метаболиты, фармацевтически приемлемые соли, фармацевтические продукты, гидраты, N-оксиды, пролекарства, полиморфы, кристаллы или их комбинации.
[00153] В одном из вариантов реализации в способах согласно настоящему изобретению применяют «фармацевтически приемлемые соли» соединений, которые могут быть получены при взаимодействии соединения согласно настоящему изобретению с кислотой или основанием.
[00154] Соединения согласно настоящему изобретению можно превращать в фармацевтически приемлемые соли. Фармацевтически приемлемую соль можно получать путем взаимодействия соединения с кислотой или основанием.
[00155] Подходящие фармацевтически приемлемые соли аминов можно получать из неорганической кислоты или из органической кислоты. Примеры неорганических солей аминов включают, но не ограничиваются ими, бисульфаты, бораты, бромиды, хлориды, гемисульфаты, гидроброматы, гидрохлораты, 2-гидроксиэтилсульфонаты (гидроксиэтансульфонаты), йодаты, йодиды, изотионаты, нитраты, персульфаты, фосфаты, сульфаты, сульфаматы, сульфанилаты, сульфокислоты (алкилсульфонаты, арилсульфонаты, галогензамещенные алкилсульфонаты, галогензамещенные арилсульфонаты), сульфонаты или тиоцианаты.
[00156] Примеры органических солей аминов могут быть выбраны из алифатических, циклоалифатических, ароматических, аралифатических, гетероциклических, карбоновых и сульфоновых классов органических кислот, примерами которых являются ацетаты, аргинины, аспартаты, аскорбаты, адипаты, антранилаты, альгенаты, алкилкарбоксилаты, замещенные алкилкарбоксилаты, альгинаты, бензолсульфонаты, бензоаты, бисульфаты, бутираты, бикарбонаты, битартраты, карбоксилаты, цитраты, камфораты, камфорсульфонаты, циклогексилсульфаматы, циклопентанпропионаты, эдетаты кальция, камзилаты, карбонаты, клавуланаты, циннаматы, дикарбоксилаты, диглюконаты, додецилсульфонаты, дигидрохлориды, деканоаты, энантаты, этансульфонаты, эдетаты, эдизилаты, эстолаты, эзилаты, фумараты, формиаты, фториды, галактуронаты, глюконаты, глутаматы, гликоляты, глюкораты, глюкогептаноаты, глицерофосфаты, глюцептаты, гликолиларсанилаты, глутараты, глутаматы, гептаноаты, гексаноаты, гидроксималеаты, гидроксикарбоновые кислоты, гексилрезорцинаты, гидроксибензоаты, гидроксинафтоаты, гидрофтораты, лактаты, лактобионаты, лаураты, малаты, малеаты, метиленбис(бета-оксинафтоат), малонаты, манделаты, мезилаты, метансульфонаты, метилбромиды, метилнитраты, метилсульфонаты, малеаты монокалия, мукаты, монокарбоксилаты, нитраты, нафталинсульфонаты, 2-нафталинсульфонаты, никотинаты, нафзилаты, N-метилглюкамины, оксалаты, октаноаты, олеаты, памоаты, фенилацетаты, пикраты, фенилбензоаты, пивалаты, пропионаты, фталаты, пектинаты, фенилпропионаты, пальмитаты, пантотенаты, полигалактураты, пируваты, хинаты, салицилаты, сукцинаты, стеараты, сульфанилаты, субацетаты, тартраты, теофиллинацетаты, п-толуолсульфонаты (тозилаты), трифторацетаты, терефталаты, таннаты, теоклаты, тригалогенацетаты, триэтиодиды, трикарбоксилаты, ундеканоаты и валераты. Примеры неорганических солей карбоновых кислот или фенолов могут быть выбраны из аммония щелочных металлов и щелочноземельных металлов. Щелочные металлы включают, но не ограничиваются ими, литий, натрий, калий или цезий. Щелочно-земельные металлы включают, но не ограничиваются ими, кальций, магний, алюминий; цинк, барий, холины или четвертичный аммоний. Примеры органических солей карбоновых кислот или фенолов могут быть выбраны из аргинина, органических аминов, включая алифатические органические амины, алициклические органические амины, ароматические органические амины, бензатины, трет-бутиламины, бенэтамины (N-бензилфенэтиламин), дициклогексиламины, диметиламины, диэтаноламины, этаноламины, этилендиамины, гидрабамины, имидазолы, лизины, метиламины, мегламины, N-метил-D-глюкамины, N,N'-дибензилэтилендиамины, никотинамиды, органические амины, орнитины, пиридины, пиколины, пиперазины, прокаин, трис(гидроксиметил)метиламины, триэтиламины, триэтаноламины, триметиламины, трометамины и мочевины.
[00157] В различных вариантах реализации фармацевтически приемлемые соли соединений согласно настоящему изобретению включают: соль HCl, соль щавелевой кислоты, соль L-(+)-винной кислоты, соль HBr и соль янтарной кислоты. Каждая из них представляет собой отдельный вариант реализации настоящего изобретения.
[00158] Соли могут быть получены традиционными способами, такими как взаимодействие продукта в виде свободного основания или свободной кислоты с одним или более эквивалентами соответствующей(-его) кислоты или основания в растворителе или среде, в котором-(ой) соль не растворяется, или в растворителе, таком как вода, который удаляют в вакууме или путем лиофилизации, или путем замены иона существующей соли на другой ион в подходящей ионообменной смоле.
[00159] В способах согласно настоящему изобретению можно применять незаряженное соединение или фармацевтически приемлемую соль соединения. В частности, в способах применяют фармацевтически приемлемые соли соединений формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB. Фармацевтически приемлемая соль может представлять собой соль амина или соль фенола соединений формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB.
[00160] В одном из вариантов реализации в способах согласно настоящему изобретению применяют свободное основание, свободную кислоту, незаряженные или не включенные в комплекс соединения формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB и/или их изомеры, фармацевтические продукты, гидраты, полиморфы или их комбинации.
[00161] В одном из вариантов реализации в способах согласно настоящему изобретению применяют оптический изомер соединения формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB. В одном из вариантов реализации в способах согласно настоящему изобретению применяют изомер соединения формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB. В одном из вариантов реализации в способах согласно настоящему изобретению применяют фармацевтический продукт соединения формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB. В одном из вариантов реализации в способах согласно настоящему изобретению применяют гидрат соединения формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB. В одном из вариантов реализации в способах согласно настоящему изобретению применяют полиморф соединения формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB. В одном из вариантов реализации в способах согласно настоящему изобретению применяют метаболит соединения формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB. В другом варианте реализации в способах согласно настоящему изобретению применяют композицию, содержащую соединение формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB, такое как описано в настоящем документе, или в другом варианте реализации комбинацию изомера, метаболита, фармацевтического продукта, гидрата, полиморфа соединения формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB.
[00162] При использовании в настоящем описании термин «изомер» включает, но не ограничивается ими, оптические изомеры, структурные изомеры или конформационные изомеры.
[00163] Термин «изомер» включает оптические изомеры соединения SARD. Специалистам в данной области техники будет понятно, что SARD согласно настоящему изобретению содержат по меньшей мере один хиральный центр. Соответственно, соединения могут существовать в виде оптически активных (таких как (R)-изомер или (S)-изомер) или рацемических форм. Оптически активные соединения могут существовать в виде энантиомерно обогащенных смесей. Некоторые соединения также могут проявлять полиморфизм. Следует понимать, что настоящее изобретение включает любые рацемические, оптически активные, полиморфные или стереоизомерные формы или их смеси. Таким образом, изобретение может включать соединения SARD в виде чистых (R)-изомеров или чистых (S)-изомеров. В данной области техники известны способы получения оптически активных форм, например, путем разделения рацемической формы способами перекристаллизации, синтеза из оптически активных исходных веществ, хирального синтеза или хроматографического разделения с применением хиральной неподвижной фазы.
[00164] Соединения согласно настоящему изобретению могут представлять собой гидраты соединений. При использовании в настоящем описании термин «гидрат» включает, но не ограничивается ими, полугидрат, моногидрат, дигидрат или тригидрат. Изобретение также включает применение N-оксидов аминозаместителей соединений, описанных в настоящем документе.
[00165] В настоящем изобретении в других вариантах реализации предложено применение метаболитов соединений, таких как описано в настоящем документе. В одном из вариантов реализации «метаболит» обозначает любое вещество, образующееся из другого вещества в результате метаболизма или метаболического процесса.
[00166] В одном из вариантов реализации соединения согласно настоящему изобретению получают согласно примеру 1.
Биологическая активность агентов, селективно разрушающих андрогенные рецепторы
[00167] Способ лечения рака предстательной железы (PCa) или увеличения выживаемости субъекта мужского пола, страдающего от рака предстательной железы, включает введение субъекту терапевтически эффективного количества соединения или его фармацевтически приемлемой соли, представленного соединением формулы I:
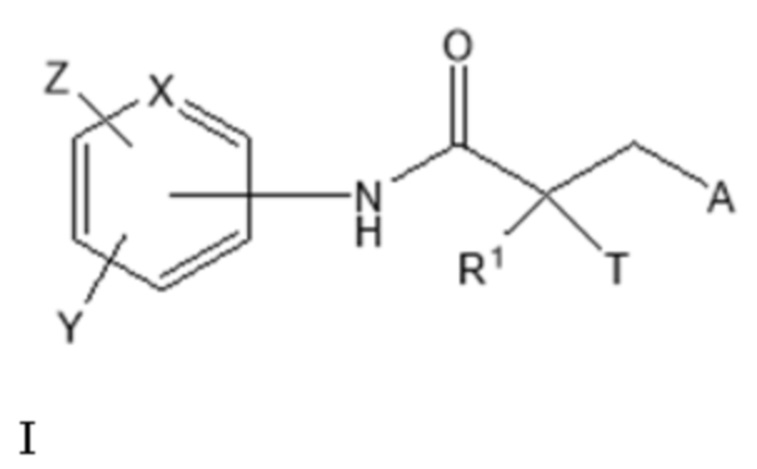
где
T представляет собой H, OH, OR, OCOR, CH3, -NHCOCH3 или NHCOR;
R1 представляет собой H, CH3, CH2F, CHF2, CF3, CH2CH3 или CF2CF3;
или T и R1 образуют 3-8-членное карбоциклическое или гетероциклическое кольцо;
Y представляет собой H, CF3, F, I, Br, Cl, CN или C(R)3;
Z представляет собой H, NO2, CN, галогенид, COOH, COR, NHCOR, CONHR, или Y и Z образуют 5-8-членное кольцо;
X представляет собой CH или N;
R представляет собой H, алкил, алкенил, галогеналкил, спирт, CH2CH2OH, CF3, CH2Cl, CH2CH2Cl, арил, F, Cl, Br, I или OH;
A представляет собой R2 или R3;
R2 представляет собой пятичленное насыщенное или ненасыщенное кольцо, содержащее по меньшей мере один атом азота и 0, 1 или 2 двойные связи, необязательно замещенное по меньшей мере одним из Q1, Q2, Q3 или Q4, каждый из которых независимо выбран из водорода, кето, замещенного или незамещенного линейного или разветвленного алкила, замещенного или незамещенного циклоалкила, замещенного или незамещенного гетероциклоалкила, галогеналкила, CF3, замещенного или незамещенного арила, замещенного или незамещенного фенила, F, Cl, Br, I, CN, NO2, гидроксила, алкокси, OR, бензила, NCS, малеимида, NHCOOR, N(R)2, NHCOR, CONHR, COOR или COR;
R3 представляет собой NHR2, галогенид, N3, OR4, CF3, COR4, COCl, COOCOR4, COOR4, OCOR4, OCONHR4, NHCOOR4, NHCONHR4, OCOOR4, CN, CONH2, CONH(R4), CON(R4)2, SR4, SO2R4, SOR4 SO3H, SO2NH2, SO2NH(R4), SO2N(R4)2, NH2, NH(R4), N(R4)2, CO(N-гетероцикл), C(O)(C1-C10)алкил, NO2, цианат, изоцианат, тиоцианат, изотиоцианат, мезилат, тозилат, трифлат, PO(OH)2 или OPO(OH)2; и
R4 представляет собой H, алкил, галогеналкил, циклоалкил, арил или гетероарил, причем указанные алкильные, галогеналкильные, циклоалкильные, арильные или гетероарильные группы необязательно замещены;
или его оптического изомера, изомера, фармацевтически приемлемой соли, фармацевтического продукта, полиморфа, гидрата или любой их комбинации.
[00168] В другом варианте реализации, если A представляет собой Br или I, R1 представляет собой CH3, и T представляет собой OH, то X представляет собой N, или анилиновое кольцо образует конденсированное гетероциклическое кольцо.
[00169] Способ лечения рака предстательной железы (PCa) или увеличения выживаемости субъекта мужского пола, страдающего от рака предстательной железы, включает введение субъекту терапевтически эффективного количества соединения или его фармацевтически приемлемой соли или изомера, представленного соединением формул I -VII, IA-ID, IIA, IIB, VIIA или VIIB.
[00170] Рак предстательной железы может представлять собой распространенный рак предстательной железы, не поддающийся лечению рак предстательной железы, устойчивый к кастрации рак предстательной железы (CRPC), метастатический CRPC (mCRPC), неметастатический CRPC (nmCRPC), nmCRPC высокого риска или любую их комбинацию.
[00171] Пролиферация рака предстательной железы может зависеть от AR-FL и/или AR-SV. Рак предстательной железы или другой вид рака может быть устойчивым к лечению другим антагонистом андрогенных рецепторов. Рак предстательной железы или другой вид рака может быть устойчивым к лечению энзалутамидом, бикалутамидом, абиратероном, ARN-509, ODM-201, EPI-001, EPI-506, AZD-3514, галатероном, ASC-J9, флутамидом, гидроксифлутамидом, нилутамидом, ципротерона ацетатом, кетоконазолом, спиронолактоном или любой их комбинацией. Способ также может уменьшать уровень AR, AR-FL, AR-FL с мутациями AR-LBD, придающими устойчивость к антиандрогенам, AR-SV, генетически амплифицированных AR или любой их комбинации.
[00172] В одном из вариантов реализации в настоящем изобретении предложен способ лечения устойчивого к энзалутамиду рака предстательной железы, включающий введение субъекту терапевтически эффективного количества соединения согласно настоящему изобретению или его оптического изомера, изомера, фармацевтически приемлемой соли, фармацевтического продукта, полиморфа, гидрата или любой их комбинации.
[00173] В одном из вариантов реализации в настоящем изобретении предложен способ лечения устойчивого к абиратерону рака предстательной железы, включающий введение субъекту терапевтически эффективного количества соединения согласно настоящему изобретению или его оптического изомера, изомера, фармацевтически приемлемой соли, фармацевтического продукта, полиморфа, гидрата или любой их комбинации.
[00174] В одном из вариантов реализации в настоящем изобретении предложен способ лечения тройного негативного рака молочной железы (ТНРМЖ), включающий введение субъекту терапевтически эффективного количества соединения согласно настоящему изобретению или его оптического изомера, изомера, фармацевтически приемлемой соли, фармацевтического продукта, полиморфа, гидрата или любой их комбинации.
[00175] Способ может дополнительно включать вторую терапию, такую как андрогенная депривационная терапия (АДТ) или агонист или антагонист РФЛГ. Агонисты РФЛГ включают, но не ограничиваются ими, леупролида ацетат.
[00176] Изобретение включает способ лечения или подавления прогрессирования рака предстательной железы (PCa) или увеличения выживаемости субъекта мужского пола, страдающего от рака предстательной железы, включающий введение субъекту терапевтически эффективного количества соединения SARD или его фармацевтически приемлемой соли, где соединение представляет собой по меньшей мере одно из соединений 1001-1049.
[00177] Изобретение включает способ лечения или подавления прогрессирования не поддающегося лечению рака предстательной железы (PCa) или увеличения выживаемости субъекта мужского пола, страдающего от не поддающегося лечению рака предстательной железы, включающий введение субъекту терапевтически эффективного количества соединения SARD или его фармацевтически приемлемой соли, где соединение представляет собой соединение формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB, или соединение представляет собой по меньшей мере одно из соединений 1001-1049.
[00178] Изобретение включает способ лечения или увеличения выживаемости субъекта мужского пола, страдающего от устойчивого к кастрации рака предстательной железы (CRPC), включающий введение субъекту терапевтически эффективного количества SARD, где соединение представляет собой соединение формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB или по меньшей мере одно из соединений 1001-1049.
[00179] Способ может дополнительно включать проведение андрогенной депривационной терапии субъекту.
[00180] Изобретение включает способ лечения или подавления прогрессирования устойчивого к энзалутамиду рака предстательной железы (PCa) или увеличения выживаемости субъекта мужского пола, страдающего от устойчивого к энзалутамиду рака предстательной железы, включающий введение субъекту терапевтически эффективного количества соединения SARD или его фармацевтически приемлемой соли, где соединение представляет собой соединение формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB, или соединение представляет собой по меньшей мере одно из соединений 1001-1049.
[00181] Способ может дополнительно включать проведение андрогенной депривационной терапии субъекту.
[00182] Изобретение включает способ лечения или подавления прогрессирования тройного негативного рака молочной железы (ТНРМЖ) или увеличения выживаемости субъекта женского пола, страдающего от тройного негативного рака молочной железы, включающий введение субъекту терапевтически эффективного количества соединения SARD или его фармацевтически приемлемой соли, где соединение представляет собой соединение формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB, или соединение представляет собой по меньшей мере одно из соединений 1001-1049.
[00183] При использовании в настоящем описании термин «увеличение выживаемости» относится к продлению периода выживаемости субъекта. Таким образом, в этом контексте соединения согласно настоящему изобретению можно применять для увеличения выживаемости мужчин с распространенным раком предстательной железы, не поддающимся лечению раком предстательной железы, устойчивым к кастрации раком предстательной железы (CRPC); метастатическим CRPC (mCRPC); неметастатическим CRPC (nmCRPC); или nmCRPC высокого риска; или женщин с ТНРМЖ.
[00184] В качестве альтернативы при использовании в настоящем описании термины «увеличивать», «увеличение» или «увеличенный», которые можно использовать взаимозаменяемо, относятся к постепенно растущему объекту (например, по размеру, количеству, числу или интенсивности), где, например, объект представляет собой глобулин, связывающий половые гормоны (ГСПГ), или простатспецифический антиген (ПСА).
[00185] Соединения и композиции согласно настоящему изобретению можно применять для увеличения выживаемости без метастазов (MFS) у субъекта, страдающего от неметастатического рака предстательной железы. Неметастатический рак предстательной железы может представлять собой неметастатический распространенный рак предстательной железы, неметастатический CRPC (nmCRPC) или nmCRPC высого риска.
[00186] Соединения SARD, описанные в настоящем документе, можно применять для обеспечения двойного действия. Например, соединения SARD могут излечивать рак предстательной железы и предотвращать метастазы. Рак предстательной железы может представлять собой не поддающийся лечению рак предстательной железы; распространенный рак предстательной железы; устойчивый к кастрации рак предстательной железы (CRPC); метастатический CRPC (mCRPC); неметастатический CRPC (nmCRPC); или nmCRPC высокого риска.
[00187] Соединения SARD, описанные в настоящем документе, можно применять для обеспечения двойного действия. Например, соединения SARD могут излечивать ТНРМЖ и предотвращать метастазы.
[00188] Мужчины с распространенным раком предстательной железы, которые имеют высокий риск прогрессирования устойчивого к кастрации рака предстательной железы (CRPC), представляют собой мужчин, которым проводят АДТ, у которых общая концентрация тестостерона в сыворотке составляет более 20 нг/дл, или мужчин с распространенным раком предстательной железы, у которых на момент начала АДТ (1) имеется подтвержденный рак предстательной железы с показателем Глисона 4 или 5, (2) имеется метастатический рак предстательной железы, (3) время удвоения ПСА составляет <3 месяцев, (4) уровень ПСА составляет ≥20 нг/мл, или (5) уровень ПСА восстанавливается за <3 года после проведения радикальной местной терапии (радикальной простатэктомии или лучевой терапии).
[00189] Нормальный уровень простатспецифического антигена (ПСА) зависит от нескольких факторов, таких как возраст субъекта мужского пола и размер предстательной железы, помимо прочего. Уровень ПСА в диапазоне 2,5-10 нг/мл считается «пограничным», а уровень выше 10 нг/мл считается «высоким». Изменение уровня или «скорость изменения уровня ПСА» более 0,75/год считается высоким. Уровень ПСА может увеличиваться несмотря на текущее проведение АДТ или историю проведения АДТ, хирургической кастрации или на лечение антиандрогенами и/или агонистом РФЛГ.
[00190] Мужчины с высоким риском неметастатического устойчивого к кастрации рака предстательной железы (nmCRPC высокого риска) могут включать субъектов с коротким периодом удвоения ПСА, у которых ожидаемая продолжительность выживаемости без прогрессирования составляет примерно 18 месяцев или менее (Miller K, Moul JW, Gleave M, et al. 2013. “Phase III, randomized, placebo-controlled study of once-daily oral zibotentan (ZD4054) in patients with non-metastatic castration-resistant prostate cancer,” Prostate Canc Prost Dis. Feb; 16:187-192). Относительно быстрое прогрессирование заболевания подчеркивает важность новых способов терапии для указанных индивидуумов.
[00191] При помощи способов согласно настоящему изобретению можно лечить субъектов с уровнем ПСА более 8 нг/мл, где субъект страдает от nmCRPC высокого риска. Популяция пациентов включает субъектов, страдающих от nmCRPC, где уровень ПСА удваивается менее чем за 8 месяцев или менее чем за 10 месяцев. При помощи способа также можно лечить популяции пациентов, где общий уровень тестостерона в сыворотке составляет более 20 нг/мл у субъекта, страдающего от nmCRPC высокого риска. В одном случае уровень свободного тестостерона в сыворотке превышает уровень, наблюдаемый после проведения орхиэктомии у субъекта мужского пола, страдающего от nmCRPC высокого риска.
[00192] Фармацевтические композиции согласно настоящему изобретению могут дополнительно содержать по меньшей мере один агонист или антагонист РФЛГ, антиандроген, лекарственное средство, действующее на рецептор запрограммированной гибели 1 (анти-PD-1), или лекарственное средство анти-PD-L1. Агонисты РФЛГ включают, но не ограничиваются ими, леупролида ацетат (Lupron®) (патенты США №5480656; 5575987; 5631020; 5643607; 5716640; 5814342; 6036976, содержание которых включено в настоящую заявку посредством ссылок) или госерелина ацетат (Zoladex®) (патенты США №7118552; 7220247; 7500964, содержание которых включено в настоящую заявку посредством ссылок). Антагонисты РФЛГ включают, но не ограничиваются ими, дегареликс или абареликс. Антиандрогены включают, но не ограничиваются ими, бикалутамид, флутамид, финастерид, дутастерид, энзалутамид, нилутамид, хлормадинон, абиратерон или любую их комбинацию. Лекарственные средства, действующие на PD-1, включают, но не ограничиваются ими, AMP-224, ниволумаб, пембролизумаб, пидилизумаб и AMP-554. Лекарственные средства, действующие на PD-L1, включают, но не ограничиваются ими, BMS-936559, атезолизумаб, дурвалумаб, авелумаб и MPDL3280A. Лекарственные средства, действующие на CTLA-4, включают, но не ограничиваются ими, ипилимумаб и тремелимумаб.
[00193] Лечение рака предстательной железы, распространенного рака предстательной железы, CRPC, mCRPC и/или nmCRPC может приводить к клинически значимому улучшению симптомов, функций и/или выживаемости, связанных с раком предстательной железы. Клинически значимое улучшение может быть определено по увеличению радиографической выживаемости без прогрессирования (rPFS), если рак является метастатическим, или по увеличению выживаемости без метастазов (MFS), если рак является неметастатическим, помимо прочего.
[00194] Изобретение включает способы уменьшения уровня простатспецифического антигена (ПСА) в сыворотке у субъекта мужского пола, страдающего от рака предстательной железы, распространенного рака предстательной железы, метастатического рака предстательной железы или устойчивого к кастрации рака предстательной железы (CRPC), включающие введение терапевтически эффективного количества SARD, где соединение представлено структурой формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB.
[00195] Изобретение включает способ вторичной гормональной терапии, который уменьшает уровень ПСА в сыворотке у субъекта мужского пола, страдающего от устойчивого к кастрации рака предстательной железы (CRPC), включающий введение терапевтически эффективного количества соединения формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB, который уменьшает уровень ПСА в сыворотке у субъекта мужского пола, страдающего от устойчивого к кастрации рака предстательной железы.
[00196] Изобретение включает способ уменьшения уровня AR, полноразмерного AR (AR-FL), AR-FL с мутациями AR-LBD, придающими устойчивость к антиандрогенам, сплайсированной формы AR (AR-SV) и/или амплификации гена AR в опухоли у субъекта, нуждающегося в этом, включающий введение терапевтически эффективного количества соединения формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB для уменьшения уровня AR, полноразмерного AR (AR-FL), AR-FL с мутациями AR-LBD, придающими устойчивость к антиандрогенам, или другими мутациями AR, сплайсированной формы AR (AR-SV) и/или амплификации гена AR в опухоли.
[00197] Способ может увеличивать радиографическую выживаемость без прогрессирования (rPFS) или выживаемость без метастазов (MFS).
[00198] У субъектов может иметься неметастатический рак; была неэффективно проведена андрогенная депривационная терапия (АДТ), проведена орхиэктомия, или имеется высокий или повышенный уровень простатспецифических антигенов (ПСА); субъекты могут представлять собой пациента с раком предстательной железы, распространенным раком предстательной железы, не поддающимся лечению раком предстательной железы, пациента с CRPC, пациента с метастатическим устойчивым к кастрации раком предстательной железы (mCRPC) или пациента с неметастатическим устойчивым к кастрации раком предстательной железы (nmCRPC). У указанных субъектов не поддающийся лечению рак может представлять собой устойчивый к энзалутамиду рак предстательной железы. У указанных субъектов nmCRPC может представлять собой nmCRPC высокого риска. Кроме того, субъекту может проводиться андрогенная депривационная терапия (АДТ) при кастрационном уровне общего T или в его отсутствие.
[00199] При использовании в настоящем описании фраза «субъект, страдающий от устойчивого к кастрации рака предстательной железы» относится к субъекту, имеющему по меньшей мере одну из следующих характеристик: предшествующее проведение андрогенной депривационной терапии (АДТ); наличие ответа на АДТ и текущий уровень ПСА в сыворотке > 2 нг/мл или >2 нг/мл и увеличение на 25% по сравнению с минимальным значением, достигнутым во время АДТ; субъект, у которого несмотря на проведение андрогенной депривационной терапии диагностировано увеличение уровня ПСА в сыворотке; кастрационный уровень общего тестостерона в сыворотке (<50 нг/дл) или кастрационный общего тестостерона в сыворотке (<20 нг/дл). У субъекта может повышаться уровень ПСА в сыворотке во время двух последовательных измерений, проводимых с интервалом по меньшей мере 2 недели; может быть проведено эффективное лечение путем АДТ; или ранее подтвержден ответ уровня ПСА в сыворотке после начала АДТ.
[00200] При использовании в настоящем описании термин «увеличение уровня ПСА в сыворотке» относится к увеличению на 25% или более уровня ПСА в сыворотке и абсолютному увеличению на 2 нг/мл или более относительно минимального значения; или к уровню ПСА в сыворотке >2 нг/мл или >2 нг/мл и увеличению на 25% по сравнению с началом андрогенной депривационной терапии (АДТ). Термин «минимальное значение» относится к наименьшему уровню ПСА у пациента, которому проводят АДТ.
[00201] Термин «ответ уровня ПСА в сыворотке» относится по меньшей мере к одному из следующего: уменьшению по меньшей мере на 90% по сравнению с уровнем ПСА в сыворотке до начала АДТ; обеспечению не поддающегося обнаружению уровня ПСА в сыворотке <10 нг/мл (<0,2 нг/мл) в любой момент времени; уменьшению уровня ПСА в сыворотке по меньшей мере на 50% относительно исходного уровня; уменьшению уровня ПСА в сыворотке по меньшей мере на 90% относительно исходного уровня; уменьшению уровня ПСА в сыворотке по меньшей мере на 30% относительно исходного уровня; или уменьшению уровня ПСА в сыворотке по меньшей мере на 10% относительно исходного уровня.
[00202] Способы согласно настоящему изобретению включают комбинированное проведение АДТ и введение соединения согласно настоящему изобретению. Формы проведения АДТ включают использование агониста РФЛГ. Агонисты РФЛГ включают, но не ограничиваются ими, леупролида ацетат (Lupron®) (патенты США №5480656; 5575987; 5631020; 5643607; 5716640; 5814342; 6036976, содержание которых включено в настоящую заявку посредством ссылок) или госерелина ацетат (Zoladex®) (патенты США №7118552; 7220247; 7500964, содержание которых включено в настоящую заявку посредством ссылок). Формы проведения АДТ включают, но не ограничиваются ими, использование антагонистов РФЛГ, антиандрогенов с обратимым действием или двустороннюю орхиэктомию. Антагонисты РФЛГ включают, но не ограничиваются ими, дегареликс и абареликс. Антиандрогены включают, но не ограничиваются ими, бикалутамид, флутамид, финастерид, дутастерид, энзалутамид, EPI-001, EPI-506, ARN-509, ODM-201, нилутамид, хлормадинон, абиратерон или любую их комбинацию.
[00203] Способы согласно настоящему изобретению включают введение по меньшей мере одного соединения согласно настоящему изобретению и ингибитора лиазы (например, абиратерона).
[00204] Термин «распространенный рак предстательной железы» относится к метастатическому раку, изначально возникшему в предстательной железе и широко метастазировавшему за пределы предстательной железы, например, в окружающие ткани, включая семенные железы, тазовые лимфатические узлы или кости, или в другие части организма. Патологии рака предстательной железы оцениваются по шкале Глисона от 1 до 5 в порядке увеличения злокачественности. Пациенты со значительным риском прогрессирующего заболевания и/или смерти от рака предстательной железы должны быть проверены по этой шкале, и у любого пациента, у которого рак развился за пределы капсулы предстательной железы и имеет степень тяжести не менее IIB, в явной форме проявляется «распространенное» заболевание. «Распространенный рак предстательной железы» может относиться к местно-распространенному раку предстательной железы. Аналогично, «распространенный рак молочной железы» относится к метастатическому раку, изначально возникшему в молочной железе и широко метастазировавшему за пределы молочной железы в окружающие ткани или другие части организма, такие как печень, мозг, легкие или кости.
[00205] Термин «не поддающийся лечению» может относиться к раковым заболеваниям, которые не отвечают на лечение. Например, рак предстательной железы или молочной железы может быть устойчивым в начале лечения или может приобретать устойчивость во время лечения. «Не поддающийся лечению рак» также может быть назван в настоящем документе «устойчивым раком».
[00206] Термин «устойчивый к кастрации рак предстательной железы» (CPRC) относится к распространенному раку предстательной железы, который усугубляется или прогрессирует при проведении пациенту АДТ или других способов терапии для уменьшения уровня тестостерона, или к раку предстательной железы, который рассматривают как не восприимчивый к действию гормонов, не зависящий от действия гормонов, не зависящий от андрогенов или устойчивый к химической или хирургической кастрации. CRPC может возникать в результате активации AR путем интракринного синтеза андрогенов; экспрессии сплайсированных форм AR (AR-SV), в которых отсутствует лигандсвязывающий домен (LBD); или экспрессии AR-LBD или других мутаций AR, которые могут приобретать устойчивость к антагонистам. Устойчивый к кастрации рак предстательной железы (CRPC) представляет собой распространенный рак предстательной железы, который развился, несмотря на проведение АДТ и/или хирургическую кастрацию. Устойчивый к кастрации рак предстательной железы определен как рак предстательной железы, который прогрессирует или усугубляется или отрицательно влияет на здоровье пациента, несмотря на предшествующее проведение хирургической кастрации, текущее лечение агонистами гонадотропин-высвобождающего гормона (например, леупролидом) или его антагонистами (например, дегареликсом или абареликсом), антиандрогенами (например, бикалутамидом, флутамидом, энзалутамидом, кетоконазолом, аминоглутетамидом), химиотерапевтическими агентами (например, доцетакселом, паклитакселом, кабазитакселом, адриамицином, митоксантроном, эстрамустином, циклофосфамидом), ингибиторами киназ (иматинибом (Gleevec®) или гефитинибом (Iressa®), кабозантинибом (Cometriq™, также известным как XL184)) или при помощи других способов терапии рака предстательной железы (например, вакцины (сипулейцел-T (Provenge®), GVAX и т.д), травяных препаратов (PC-SPES) и ингибиторов лиазы (абиратерон)), что подтверждается увеличенным или повышенным уровнем простатспецифического антигена (ПСА) в сыворотке, метастазами, метастазами в кости, болью, поражением лимфатических узлов, увеличением размера или уровня маркеров роста опухоли в сыворотке, ухудшением диагностических прогностических маркеров или состояния пациента.
[00207] Устойчивый к кастрации рак предстательной железы может быть определен как рак предстательной железы, не зависящий от воздействия гормонов. У мужчин с устойчивым к кастрации раком предстательной железы опухолевые клетки могут расти в отсутствие андрогенов (гормонов, которые способствуют развитию и поддержанию половой функции у мужчин).
[00208] На ранних стадиях для роста раковых заболеваний предстательной железы требуются андрогены, но распространенные формы рака предстательной железы не зависят от андрогенов или не зависят от воздействия гормонов.
[00209] Термин «андрогенная депривационная терапия» (АДТ) может включать орхиэктомию; введение аналогов рилизинг-фактора лютеинизирующего гормона (РФЛГ); введение антагонистов рилизинг-фактора лютеинизирующего гормона (РФЛГ); введение ингибиторов 5α-редуктазы; введение антиандрогенов; введение ингибиторов биосинтеза тестостерона; введение эстрогенов; или введение ингибиторов 17α-гидроксилазы/C17,20-лиазы (CYP17A1). Лекарственные средства, действующие на РФЛГ, уменьшают количество тестостерона, вырабатываемого в яичках. Примеры аналогов РФЛГ, доступных в США, включают леупролид (Lupron®, Viadur®, Eligard®), госерелин (Zoladex®), трипторелин (Trelstar®) и гистрелин (Vantas®). Антиандрогены блокируют способность организма использовать любые андрогены. Примеры антиандрогенных препаратов включают энзалутамид (Xtandi®), флутамид (Eulexin®), бикалутамид (Casodex®) и нилутамид (Nilandron®). Антагонисты рилизинг-фактора лютеинизирующего гормона (РФЛГ) включают абареликс (Plenaxis®) или дегареликс (Firmagon®) (который одобрен FDA в 2008 году для использования при лечении распространенного рака предстательной железы). Ингибиторы 5α-редуктазы блокируют способность организма превращать тестостерон в более активный андроген, 5α-дигидротестостерон (ДГТ), и включают лекарственные средства, такие как финастерид (Proscar®) и дутастерид (Avodart®). Ингибиторы биосинтеза тестостерона включают лекарственные средства, такие как кетоконазол (Nizoral®). Эстрогены включают диэтилстилбестрол или 17α-эстрадиол. Ингибиторы 17α-гидроксилазы/C17,20-лиазы (CYP17A1) включают абиратерон (Zytiga®).
[00210] Изобретение включает способ лечения устойчивого к антиандрогенам рака предстательной железы. Антиандроген может включать, но не ограничивается ими, бикалутамид, гидроксифлутамид, флутамид, энзалутамид или абиратерон.
Лечение тройного негативного рака молочной железы (ТНРМЖ)
[00211] Тройной негативный рак молочной железы (ТНРМЖ) представляет собой тип рака молочной железы, при котором отсутствует экспрессия рецептора эстрогена (ER), рецептора прогестерона (PR) и рецепторной киназы HER2. Таким образом, при ТНРМЖ отсутствуют гормональные и киназные терапевтические мишени, на которые воздействуют при лечении других типов первичных раковых заболеваний молочной железы. Соответственно, химиотерапия часто является начальным способом фармакотерапии ТНРМЖ. Интересно, что при ТНРМЖ сохраняется экспрессия AR, это позволяет проводить направленную гормональную терапию в качестве альтернативы химиотерапии. При ER-положительном раке молочной железы AR является индикатором положительного прогноза, так как считается, что активация AR ограничивает и/или сдерживает эффекты ER в тканях и опухолях молочной железы. Тем не менее, в отсутствие ER, AR фактически может поддерживать рост раковых опухолей молочной железы. Хотя роль AR при ТНРМЖ выяснена не в полной мере, существуют доказательства того, что некоторые формы ТНРМЖ могут поддерживаться посредством андрогеннезависимой активации AR-SV, в которых отсутствует LBD, или андрогензависимой активации полноразмерных AR. Таким образом, энзалутамид и другие традиционные антагонисты AR, действующие на LBD, не обладают активностью антагониста в отношении AR-SV при указанных ТНРМЖ. Тем не менее, SARD согласно настоящему изобретению, которые могут разрушать AR-SV (см. таблицу 1 и пример 5) через участок связывания в NTD AR (см. пример 9), могут действовать как антагонисты AR при указанных формах ТНРМЖ и обеспечивать противоопухолевое действие, как показано в примере 8.
[00212] Лечение болезни Кеннеди
[00213] Мышечная атрофия (МА) характеризуется истощением или ослаблением мышц и уменьшением мышечной массы. Например, постполиомиелитная MA представляет собой мышечное истощение, которое происходит в рамках постполиомиелитного синдрома (ППС). Атрофия включает слабость, мышечную усталость и боль. Другим типом МА является Х-сцепленная спинально-бульбарная мышечная атрофия (SBMA--также известная как болезнь Кеннеди). Эта болезнь возникает из-за дефекта в гене андрогенных рецепторов на X-хромосоме, поражает только мужчин и проявляется в позднем подростковом или взрослом возрасте. Слабость проксимальных мышц конечностей и мышц ротовой полости приводит к физическим ограничениям, включая в некоторых случаях необходимость использования инвалидной коляски. Мутация приводит увеличению полиглутаминовой цепи в N-терминальном домене андрогенного рецептора (polyQ AR).
[00214] Связывание и активация polyQ AR эндогенными андрогенами (тестостероном и ДГТ) приводят к развертыванию и ядерной транслокации мутантного андрогенного рецептора. Индуцированная андрогенами токсичность и андрогензависимое накопление в ядре белка polyQ AR вероятно являются ключевыми факторами патогенеза. Таким образом, ингибирование активированного андрогеном polyQ AR может являться одним из способов терапии (A. Baniahmad. Inhibition of the androgen receptor by antiandrogens in spinobulbar muscle atrophy. J. Mol. Neurosci. 2016 58(3), 343-347). Эти стадии требуются для патогенеза и приводят к частичной потере функции трансактивации (т.е. к нечувствительности к андрогенам) и слабоизученной нейромышечной дегенерации. Проведение периферической антисмысловой терапии polyQ AR обеспечивает избавление от заболевания в моделях SBMA у мышей (Cell Reports 7, 774-784, May 8, 2014). Дополнительные обоснования использования антиандрогенов приведены в отчете, согласно которому антиандроген флутамид обеспечивает защиту самцов мышей от андрогензависимой токсичности в трех моделях спинально-бульбарной мышечной атрофии (Renier KJ, Troxell-Smith SM, Johansen JA, Katsuno M, Adachi H, Sobue G, Chua JP, Sun Kim H, Lieberman AP, Breedlove SM, Jordan CL. Endocrinology 2014, 155(7), 2624-2634). Эти стадии требуются для патогенеза и приводят к частичной потере функции трансактивации (т.е. к нечувствительности к андрогенам) и слабоизученной нейромышечной дегенерации. В настоящее время отсутствуют способы лечения, модифицирующие заболевание, имеются только способы, направленные на симптомы. Попытки направленного воздействия на polyQ AR, который является медиатором токсичности первого порядка, посредством изменения клеточного строения для ускорения его разрушения являются перспективными для терапевтического вмешательства.
[00215] Агенты, селективно разрушающие андрогенные рецепторы, такие как описано в настоящем документе, связывают, ингибируют трансактивацию и разрушают все андрогенные рецепторы, исследованные на момент подачи заявки (полноразмерные, сплайсированные формы, мутанты, устойчивые к антиандрогенам, и т.д.), это указывает на то, что они являются многообещающими средствами для лечения заболеваний, патогенез которых зависит от андрогенов, таких как SBMA.
[00216] Изобретение включает способы лечения болезни Кеннеди, включающие введение терапевтически эффективного количества соединения формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB.
[00217] При использовании в настоящем описании термин «состояния, связанные с андрогенными рецепторами» или «заболевания или нарушения, восприимчивые к андрогенами» или «заболевания или нарушения, зависящие от андрогенов» представляют собой состояния, заболевания или нарушения, которые модулируются активностью андрогенных рецепторов, или патогенез которых зависит от этой активности. Андрогенные рецепторы экспрессируются в большинстве тканей организма, тем не менее, их избыточная экспрессия происходит, помимо прочего, в предстательной железе и коже. АДТ многие годы является основным способом лечения рака предстательной железы, и SARD также могут быть эффективными при лечении различных форм рака предстательной железы, доброкачественной гипертрофии предстательной железы, простатомегалии и других заболеваний предстательной железы.
[00218] Изобретение включает способы лечения доброкачественной гипертрофии предстательной железы, включающие введение терапевтически эффективного количества по меньшей мере одного соединения формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB.
[00219] Изобретение включает способы лечения простатомегалии, включающие введение терапевтически эффективного количества по меньшей мере одного соединения формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB.
[00220] Изобретение включает способы лечения гиперпролиферативных нарушений и заболеваний предстательной железы, включающие введение терапевтически эффективного количества соединения формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB.
[00221] Влияние AR на коже проявляется в половом диморфизме и дерматологических проблемах, связанных с половым созреванием, в подростковом и раннем взрослом возрасте. Гиперандрогения в период полового созревания стимулирует рост терминальных волос, выработку кожного сала и делает подростков мужского пола предрасположенными к акне, обыкновенным угрям, себорее, избыточной выработке кожного сала, гнойному гидрадениту, гирсутизму, гипертрихозу, чрезмерной волосатости, андрогенной алопеции, облысению по мужскому типу и другим дерматологическим заболеваниям. Хотя антиандрогены теоретически должны предупреждать обсуждаемые гиперандрогенные дерматологические заболевания, их действие ограничено токсичностью, сексуальными побочными эффектами и отсутствием эффективности при местном применении. SARD согласно настоящему изобретению с высокой активностью подавляют лигандзависимую и лиганднезависимую активацию AR и (в некоторых случаях) имеют короткий биологический период полувыведения из сыворотки, это позволяет предположить, что местные составы SARD согласно настоящему изобретению можно наносить на участки, пораженные акне, себорейным дерматитом и/или гирсутизмом в отсутствие риска системных побочных эффектов.
[00222] Изобретение включает способы лечения акне, обыкновенных угрей, себореи, себорейного дерматита, гнойного гидраденита, гирсутизма, гипертрихоза, чрезмерной волосатости и алопеции, включающие введение терапевтически эффективного количества соединения формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB или любого из соединений 1001-1049.
[00223] Соединения и/или композиции, описанные в настоящем документе, можно применять для лечения выпадения волос, алопеции, андрогенной алопеции, гнездной алопеции, алопеции, вызванной химиотерапией, алопеции, вызванной лучевой терапией, алопеции, вызванной рубцеванием, или алопеции, вызванной стрессом. Как правило, «выпадение волос» или «алопеция» относится к облысению, наиболее распространенным видом которого является облысение по мужскому типу. Облысение обычно начинается с локального выпадения волос на волосистой части головы и иногда прогрессирует до полного облысения и даже выпадения волос на теле. Выпадение волос поражает как мужчин, так и женщин.
[00224] Изобретение включает способы лечения андрогенной алопеции, включающие введение терапевтически эффективного количества соединения формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB или любого из соединений 1001-1049.
[00225] SARD согласно настоящему изобретению также можно применять в лечении гормональных состояний у женщин, у которых может иметься гиперандрогенный патогенез, такой как преждевременное половое созревание, раннее половое созревание, дисменорея, аменорея, синдром многокамерной матки, эндометриоз, гистеромиома, аномальное маточное кровотечение, раннее менархе, фиброкистозная болезнь молочной железы, фиброма матки, киста яичников, синдром поликистозных яичников, преэклампсия, эклампсия беременных, преждевременные роды, предменструальный синдром и/или вагинальная сухость.
[00226] Изобретение включает способы лечения преждевременного полового созревания, раннего полового созревания, дисменореи или аменореи, синдрома многокамерной матки, эндометриоза, гистеромиомы, аномального маточного кровотечения, гиперандрогенных заболеваний (таких как синдром поликистозных яичников (СПКЯ)), фиброкистозной болезни молочной железы, фибромы матки, кисты яичников, синдрома поликистозных яичников, преэклампсии, эклампсии беременных, преждевременных родов, предменструального синдрома или вагинальной сухости, включающие введение терапевтически эффективного количества соединения формул I -VII, IA-ID, IIA, IIB, VIIA или VIIB или любого из соединений 1001-1049.
[00227] SARD согласно настоящему изобретению также можно применять в лечении половой перверсии, гиперсексуальности, парафилии, андрогенного психоза, вирилизации, синдрома нечувствительности к андрогенам (AIS) (такого как полный AIS (CAIS) и частичный AIS (PAIS)) и для улучшения овуляции у животных.
[00228] Изобретение включает способы лечения половой перверсии, гиперсексуальности, парафилии, андрогенного психоза, вирилизации, синдрома нечувствительности к андрогенам, увеличения или модуляции или улучшения овуляции, включающие введение терапевтически эффективного количества соединения формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB или любого из соединений 1001-1049.
[00229] SARD согласно настоящему изобретению также можно применять для лечения гормонозависимых раковых заболеваний, таких как рак предстательной железы, рак молочной железы, рак яичек, рак яичников, печеночноклеточная карцинома, урогенитальный рак и т.д. В другом варианте реализации рак молочной железы представляет собой тройной негативный рак молочной железы. Кроме того, местное или системное введение SARD может подходить для лечения заболеваний-предшественников гормонозависимых форм рака, таких как простатическая интраэпителиальная неоплазия (ПИН) и атипическая мелкоацинарная пролиферация (АМАП).
[00230] Изобретение включает способы лечения рака молочной железы, рака яичек, рака матки, рака яичников, урогенитального рака, заболеваний-предшественников рака предстательной железы или солидных опухолей, связанных с AR или экспрессирующих AR, включающие введение терапевтически эффективного количества соединения формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB. Заболевание-предшественник рака предстательной железы может представлять собой простатическую интраэпителиальную неоплазию (ПИН) или атипическую мелкоацинарную пролиферацию (ASAP). Опухоль может представлять собой печеночноклеточную карциному (HCC) или рак мочевого пузыря. Уровень тестостерона в сыворотке может быть положительно связан с развитием HCC. С учетом эпидемиологических, экспериментальных наблюдений и особенно того факта, что мужчины имеют значительно более высокий риск рака мочевого пузыря по сравнению с женщинами, полагают, что андрогены и/или AR также могут участвовать в инициировании рака мочевого пузыря.
[00231] Несмотря на то, что традиционные антиандрогены, такие как энзалутамид, бикалутамид и флутамид, и средства андрогенной депривационной терапии (АДТ), такие как леупролид, были одобрены для использования при раке предстательной железы, существуют веские доказательства того, что антиандрогены также можно применять при различных других гормонозависимых и гормононезависимых формах рака. Например, антиандрогены успешно прошли испытания при раке молочной железы (энзалутамид; Breast Cancer Res (2014) 16(1): R7), немелкоклеточном раке легкого (кшРНКи AR), почечноклеточной карциноме (ASC-J9), злокачественных образованиях, связанных с частичной потерей чувствительности к андрогенам, таких как гонадальные опухоли и семинома, распространенном раке поджелудочной железы (World J Gastroenterology 20(29):9229), раке яичников, фаллопиевых труб или брюшной полости, раке слюнных желез (Head and Neck (2016) 38: 724-731; АДТ исследовали при возникших повторно/метастатических раковых заболеваниях слюнных желез, при которых происходит экспрессия AR, было подтверждено, что она благоприятно влияет на конечные измеряемые показатели выживаемости без прогрессирования и общей выживаемости), раке мочевого пузыря (Oncotarget 6 (30): 29860-29876); Int J Endocrinol (2015), ID статьи 384860), раке поджелудочной железы, лимфоме (включая мантийноклеточную) и печеночноклеточной карциноме. Использование более высокоактивного антиандрогена, такого как SARD, при указанных раковых заболеваниях может излечивать прогрессирование этих и других видов рака. Лечение с применением SARD также может оказывать благоприятное действие и при других раковых заболеваниях, таких как рак яичек, рак матки, рак яичников, урогенитальный рак, рак молочной железы, рак мозга, рак кожи, лимфома, рак печени, рак почки, остеосаркома, рак поджелудочной железы, рак эндометрия, рак легкого, немелкоклеточный рак легкого (НМРЛ), рак толстой кишки, перианальная аденома или рак центральной нервной системы.
[00232] SARD согласно настоящему изобретению также можно применять для лечения других раковых заболеваний, при которых задействован AR, таких как рак молочной железы, мозга, кожи, яичников, мочевого пузыря, лимфома, рак печени, почки, поджелудочной железы, эндометрия, легкого (например, НМРЛ), толстой кишки, перианальная аденома, рак ЦНС, меланома, гиперкальцемия при злокачественных образованиях и метастатических заболеваниях костей и т.д.
[00233] Таким образом, изобретение включает способы лечения гиперкальцемии при злокачественных образованиях, метастатических заболеваний кости, рака мозга, рака кожи, рака мочевого пузыря, лимфомы, рака печени, рака почки, остеосаркомы, рака поджелудочной железы, рака эндометрия, рака легкого, рака центральной нервной системы, рака желудка, рака толстой кишки, меланомы, бокового амиотрофического склероза (БАС) и/или фибромы матки, включающие введение терапевтически эффективного количества соединения формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB или любого из соединений 1001-1049. Рак легкого может представлять собой немелкоклеточный рак легкого (НМРЛ).
[00234] SARD согласно настоящему изобретению также можно применять для лечения гормононезависимых раковых заболеваний. Гормононезависимые формы рака включают заболевания печени, протоков слюнных желез и т.д.
[00235] В другом варианте реализации SARD согласно настоящему изобретению применяют для лечения рака желудка. В другом варианте реализации SARD согласно настоящему изобретению применяют для лечения карциномы протоков слюнных желез. В другом варианте реализации SARD согласно настоящему изобретению применяют для лечения рака мочевого пузыря. В другом варианте реализации SARD согласно настоящему изобретению применяют для лечения рака пищевода. В другом варианте реализации SARD согласно настоящему изобретению применяют для лечения рака поджелудочной железы. В другом варианте реализации SARD согласно настоящему изобретению применяют для лечения рака толстой кишки. В другом варианте реализации SARD согласно настоящему изобретению применяют для лечения немелкоклеточного рака легкого. В другом варианте реализации SARD согласно настоящему изобретению применяют для лечения почечноклеточной карциномы.
[00236] AR влияет на инициирование рака при печеночноклеточной карциноме (HCC). Таким образом, направленное действие на AR может представлять собой подходящий способ лечения пациентов с HCC на ранней стадии. Существуют подтверждения того, что на поздних стадиях HCC метастазы подавляются под действием андрогенов. В другом варианте реализации SARD согласно настоящему изобретению применяют для лечения печеночноклеточной карциномы (HCC).
[00237] Локати (Locati et al.) с соавторами в Head & Neck, 2016, 724-731, продемонстрировали применение андрогенной депривационной терапии (АДТ) при повторно возникающих/метастатических раковых заболеваниях слюнных желез, при которых происходит экспрессия AR, и подтвердили улучшение конечных измеряемых показателей выживаемости без прогрессирования и общей выживаемости при проведении АДТ. В другом варианте реализации SARD согласно настоящему изобретению применяют для лечения рака слюнных желез.
[00238] Кавахара (Kawahara et al.) с соавторами в Oncotarget, 2015, Vol 6 (30), 29860-29876, продемонстрировали, что совместное ингибирование ELK1 и инактивацию AR можно применять в качестве терапевтического подхода при лечении рака мочевого пузыря. МакБет (McBeth et al.) с соавторами Int J Endocrinology, 2015, Vol 2015, ID статьи 384860, предположили возможность применения антиандрогенной терапии и глюкокортикоидов в качестве способа лечения рака мочевого пузыря, так как считается, что эта форма рака имеет воспалительную этиологию. В другом варианте реализации SARD согласно настоящему изобретению применяют для лечения рака мочевого пузыря необязательно в комбинации с глюкокортикоидами.
Аневризма брюшной аорты (AAA)
[00239] Аневризма брюшной аорты (ААА) представляет собой увеличенную область в нижней части аорты, основного кровеносного сосуда, который поставляет кровь в организм. Аорта, схожая по толщине с садовым шлангом, проходит от сердца через центр грудной клетки и брюшной полости. Поскольку аорта является основным поставщиком крови в организме, разрыв аневризмы брюшной аорты может вызвать опасное для жизни кровотечение. В зависимости от размера и скорости роста аневризмы брюшной аорты лечение может варьироваться от выжидательного наблюдения до экстренной операции. После обнаружения аневризмы брюшной аорты врачи проводят ее тщательное исследование, чтобы можно было запланировать операцию, если это необходимо. Экстренная операция на разрыве аневризмы брюшной аорты может быть рискованной. Блокада AR (фармакологическая или генетическая) уменьшает ААА. Дэвис (Davis) с соавторами (Davis JP, Salmon M, Pope NH, Lu G, Su G, Meher A, Ailawadi G, Upchurch GR Jr. J Vasc Surg (2016) 63(6):1602-1612) показали, что флутамид (50 мг/кг) или кетоконазол (150 мг/кг) уменьшали AAA, индуцированную эластазой поджелудочной железы свиней (0,35 Ед/мл), на 84,2% и 91,5% по сравнению с носителем (121%). Кроме того, у мышей AR -/- было показано уменьшение роста AAA (64,4%) по сравнению с мышами дикого типа (в обоих случаях вводили эластазу). Соответственно, введение SARD пациенту, страдающему от AAA, может способствовать обращению вспять, излечению или задержке прогрессирования AAA до того момента, при котором требуется операция.
Лечение ран
[00240] Обычно раны и/или язвы проявляются на коже или на слизистой поверхности или в результате омертвения органа. Рана может возникать в результате дефекта или поражения мягкой ткани или вызывающего его состояния. Термин «рана» обозначает физическое повреждение с нарушением целостности тканевых структур, нарывами, поражениями, некрозом и/или язвообразованием. Термин «нарыв» относится к любому поражению кожи или слизистых мембран, и термин «язва» относится к местному дефекту или формированию полости на поверхности органа или ткани, которые возникают в результате отслаивания некротической ткани. «Поражение» в общем случае включает любой дефект ткани. «Некроз» относится к гибели ткани, вызванной инфекцией, повреждением, воспалением или омертвением. Все указанные термины включены в термин «рана», который обозначает любую рану на любой конкретной стадии процесса заживления, включая стадию перед началом заживления или даже перед специальным нанесением раны, таким как хирургический разрез (для профилактического лечения).
[00241] Примерами ран, которые могут быть излечены согласно настоящему изобретению, являются асептические раны, ушибленные раны, резаные раны, рваные раны, непроникающие раны (т.е. раны, при которых кожный покров не нарушается, но имеется повреждение нижележащих структур), открытые раны, проникающие раны, прободные раны, колотые раны, септические раны, подкожные раны и т.д. Примеры нарывов включают, но не ограничиваются ими, пролежни, нарывы в полости рта, хромовые язвы, герпес, намины и т.д. Примеры язв включают, но не ограничиваются ими, пептическую язву, язву двенадцатиперстной кишки, язву желудка, подагрическую язву, диабетическую язву, гипертензионную ишемическую язву, циркуляторную язву, варикозную язву (венозную язву), подъязычную язву, язву подслизистого слоя, симптоматическую язву, трофическую язву, тропическую язву, венерическую язву, например, вызванную гонореей (включая уретрит, эндоцервицит и проктит). Состояния, связанные с ранами или нарывами, которые могут быть эффективно излечены согласно настоящему изобретению, включают, но не ограничиваются ими, ожоги, карбункулы, столбняк, газовую гангрену, скарлатину, рожу, сикоз обыкновенный, фолликулит, контагиозное импетиго, буллезное импетиго и т.д. Следует понимать, что определения терминов «рана» и «язва» или «рана» и «нарыв» могут перекрываться, кроме того, термины часто используют произвольно.
[00242] Виды ран, поддающихся лечению согласно настоящему изобретению, также включают: i) обычные раны, такие как, например, хирургические, травматические, инфекционные, ишемические, термические, химические и буллезные раны; ii) раны полости рта, такие как, например, постэкстракционные раны, эндодонтические раны, в частности, связанные с лечением кист, гнойников, язв и поражений бактериального, вирусного или аутоиммунного происхождения, механические, химические, термические, инфекционные и лихеноидные раны; герпетические язвы, афтозный стоматит, острый некротический язвенный гингивит и синдром жжения полости рта являются конкретными примерами; и iii) раны на коже, такие как, например, новообразования, ожоги (например, химические, термические), поражения (бактериальные, вирусные, аутоиммунные), укусы и хирургические разрезы. Другим способом классификации ран является площадь некроза ткани, где выделяют раны: i) с незначительным некрозом ткани (из-за хирургических разрезов, незначительных ссадин и мелких укусов) или ii) со значительным некрозом ткани. Последняя группа включает ишемические язвы, намины, фистулы, рваные раны, тяжелые укусы, термические ожоги и раны донорского участка (в мягких и твердых тканях) и омертвение. Другие раны включают ишемические язвы, намины, фистулы, тяжелые укусы, термические ожоги или раны донорского участка.
[00243] Ишемические язвы и намины представляют собой раны, который, как правило, заживляются очень медленно, и в указанных случаях, в частности, улучшенное и ускоренное заживление является крайне важным для пациента. Кроме того, затраты на лечение пациентов, страдающих от указанных ран, значительно понижаются при улучшении и ускорении заживления.
[00244] Раны донорского участка представляют собой раны, которые, например, возникают при удалении твердых тканей из одной части организма в другую часть организма, например, при трансплантации. Раны, возникающие при указанных операциях, крайне болезненны, и улучшенное их заживление, таким образом, является наиболее ценным вариантом.
[00245] В одном случае рана, которая требует лечения, выбрана из группы, состоящей из асептических ран, омертвения, ушибленных ран, резаных ран, рваных ран, непроникающих ран, открытых ран, проникающих ран, прободных ран, колотых ран, септических ран и подкожных ран.
[00246] Изобретение включает способы лечения субъекта, страдающего от раны, включающие введение субъекту терапевтически эффективного количества соединения формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB, его фармацевтически приемлемой соли или содержащей его фармацевтической композиции.
[00247] Изобретение включает способы лечения субъекта, страдающего от ожога, включающие введение субъекту терапевтически эффективного количества соединения формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB, его фармацевтически приемлемой соли или содержащей его фармацевтической композиции.
[00248] Термин «кожа» используется в очень широком смысле и включает эпидермальный слой кожи и в тех случаях, когда поверхность кожи повреждена в большей или меньшей степени, также дермальный слой кожи. Помимо рогового слоя эпидермальный слой кожи представляет собой внешний (эпителиальный) слой, а более глубокий слой соединительной ткани кожи называют дермой.
[00249] Поскольку кожа является наиболее открытой частью тела, она особенно подвержена различным видам повреждений, таким как, например, разрывы, порезы, ссадины, ожоги и обморожения или травмы, возникающие в результате различных заболеваний. Кроме того, крупные участки кожи часто разрушаются во время несчастных случаев. Тем не менее, вследствие важной защитной и физиологической функции кожи целостность кожи важна для хорошего самочувствия индивидуума, и любое повреждение или разрыв представляет угрозу, которая должна быть устранена организмом для защиты и продолжения существования.
[00250] Помимо кожи повреждения также могут возникать во всех видах тканей (т.е. в мягких и твердых тканях). Травмы мягких тканей, включая слизистые мембраны и/или кожу, особенно подходят для реализации настоящего изобретения.
[00251] Исцеление раны на коже или слизистой мембране протекает в несколько стадий, которые приводят к восстановлению или регенерации кожи или слизистой мембраны. В последние годы регенерацию и восстановление относят к двум различным типам исцеления. Регенерация может быть определена как биологический процесс, при котором полностью возобновляются архитектура и функция утраченной ткани. Восстановление, с другой стороны, представляет собой биологический процесс, при котором целостность разрушенной ткани восстанавливается посредством новых тканей, которые по структуре и функции не являются копиями утраченной ткани.
[00252] Заживление большинства ран происходит посредством восстановления, это обозначает образование новой ткани, которая структурно и химически отличается от исходной ткани (рубцовая ткань). На ранней стадии восстановления ткани одним из процессов, который происходит практически во всех случаях, является образование промежуточной соединительной ткани в поврежденной области ткани. Этот процесс начинается с образования новой внеклеточной коллагеновой матрицы под действием фибробластов. Указанная новая внеклеточная коллагеновая матрица является основой для соединительной ткани во время конечного процесса заживления. Результатом заживления в большинстве тканей является образование рубца, содержащего соединительную ткань. В тканях, которые обладают регенеративными свойствами, таких как, например, кожа и кость, конечное заживление включает регенерацию исходной ткани. Указанная регенерированная ткань также часто имеет некоторые характеристики рубцов, например, утолщение на месте заживления перелома кости.
[00253] В обычных условиях в организме обеспечены механизмы заживления поврежденной кожи или слизистой для восстановления целостности кожного барьера или слизистой. Процесс восстановления даже незначительных разрывов или ран может протекать в течение периода времени от нескольких часов и дней до нескольких недель. Тем не менее, при язвообразовании заживление может протекать очень медленно, и рана может сохраняться в течение продолжительного периода времени, т.е. несколько месяцев или даже лет.
[00254] Ожоги связаны с пониженным уровнем тестостерона, а гипогонадизм связан с задержкой заживления ран. Изобретение включает способы лечения субъекта, страдающего от раны или ожога, путем введения по меньшей мере одного соединения SARD согласно настоящему изобретению. SARD может ускорять устранение ожога или раны, участвует в процессе заживления ожога или раны или излечивает вторичное осложнение после ожога или раны.
[00255] Для лечения ожогов или ран можно дополнительно применять по меньшей мере один фактор роста, такой как эпидермальный фактор роста (EGF), трансформирующий ростовой фактор-α (TGF-α), фактор роста тромбоцитов (PDGF), факторы роста фибробластов (FGF), включая кислотный фактор роста фибробластов (α-FGF) и основный фактор роста фибробластов (β-FGF), трансформирующий ростовой фактор-β (TGF-β) и инсулиноподобные факторы роста (IGF-1 и IGF-2), или любую их комбинацию, которые ускоряют заживление ран.
[00256] Заживление ран может быть измерено разными способами, известными в данной области техники, включая, но не ограничиваясь ими, прочность растяжения, содержание гидроксипролина или коллагена, экспрессию проколлагена или реэпителизация. Например, SARD, такой как описано в настоящем документе, можно вводить перорально или местно в дозировке примерно 0,1-100 мг в день. Терапевтическую эффективность измеряют как эффективность улучшения заживления ран по сравнению с ситуацией, когда соединение SARD не используют. Улучшенное заживление ран может быть измерено известными способами, например, по уменьшению времени заживления, увеличению плотности коллагена, увеличению уровня гидроксипролина, уменьшению осложнений, увеличению прочности растяжения и увеличению насыщенности рубцовой ткани клетками.
[00257] Следует понимать, что термин «уменьшение патогенеза» включает уменьшение повреждения ткани или повреждения органа, связанного с конкретным заболеванием, нарушением или состоянием. Термин может включать уменьшение частоты появления или тяжести заболевания, нарушения или состояния, связанного с изучаемым состоянием, или уменьшение количества заболеваний, нарушений или состояний, связанных с указанным состоянием, или связанных с ним симптомов.
Фармацевтические композиции
[00258] Соединения согласно настоящему изобретению можно применять в фармацевтических композициях. При использовании в настоящем описании «фармацевтическая композиция» обозначает соединение или фармацевтически приемлемую соль активного агента совместно с фармацевтически приемлемым носителем или разбавителем. «Терапевтически эффективное количество» при использовании в настоящем описании относится к такому количеству, которое обеспечивает терапевтический эффект при данном показании и режиме введения.
[00259] При использовании в настоящем описании термин «введение» относится к приведению субъекта в контакт с соединением согласно настоящему изобретению. При использовании в настоящем описании введение можно проводить in vitro, т.е. в пробирке для исследования, или in vivo, т.е. в клетки или ткани живых организмов, например, человека. Субъекты могут представлять собой субъекта мужского пола или субъекта женского пола или субъектов обоих полов.
[00260] Доступны разнообразные справочные материалы, в которых описаны способы получения различных композиций или составов, подходящих для введения соединения согласно настоящему изобретению. Примеры способов получения составов и препаратов можно найти в Handbook of Pharmaceutical Excipients, American Pharmaceutical Association (текущее издание); Pharmaceutical Dosage Forms: Tablets (Lieberman, Lachman and Schwartz, редакторы) текущее издание, опубликованной в Marcel Dekker, Inc., а также в Remington's Pharmaceutical Sciences (Arthur Osol, редактор), 1553-1593 (текущее издание).
[00261] Способ введения и лекарственная форма тесно связаны с терапевтическим количеством соединений или композиций, которые являются желательными и эффективными для данного лечебного применения.
[00262] Фармацевтические композиции согласно настоящему изобретению можно вводить субъекту любым способом, известным специалистам в данной области техники. Указанные способы включают, но не ограничиваются ими, пероральное, парентеральное, внутрисосудистое, околоопухолевое, чресслизистое, чрескожное, внутримышечное, интраназальное, внутривенное, внутрикожное, подкожное, подъязычное, интраперитонеальное, интравентрикулярное, интракраниальное, внутривагинальное, ингаляционное, ректальное или внутриопухолевое введение. Указанные способы включают любые средства, которые могут доставлять композицию в ткань (например, иглу или катетер). В качестве альтернативы для нанесения на поверхности кожи, глаз или слизистой может требоваться местное введение. Другим способом введения является введение путем распыления или введение состава в виде аэрозоля. Фармацевтические композиции можно вводить местно на поверхности тела, и, таким образом, их получают в форме, подходящей для местного введения. Подходящие местные составы включают гели, мази, кремы, лосьоны, капли и т.д. Для местного применения композиции получают и наносят в виде растворов, суспензий или эмульсий в физиологически приемлемом разбавителе совместно с фармацевтическим носителем или без него.
[00263] Подходящие лекарственные формы включают, но не ограничиваются ими, формы для перорального, ректального, подъязычного, чресслизистого, интраназального, глазного, подкожного, внутримышечного, внутривенного, чрескожного, интраспинального, интратекального, внутрисуставного, внутриартериального, субарахноидального, бронхиального, лимфатического и внутриматочного введения и другие лекарственные формы для системной доставки активных ингредиентов. В зависимости от показания предпочтительными являются составы, подходящие для перорального или местного введения.
[00264] Местное введение: Соединения формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB можно вводить местно. При использовании в настоящем описании «местное введение» относится к нанесению соединений формул I -VII, IA-ID, IIA, IIB, VIIA или VIIB (и необязательно носителя) непосредственно на кожу и/или волосы. Местная композиция может иметь форму растворов, лосьонов, бальзамов, кремов, мазей, липосом, составов для распыления, гелей, пен, шариковых стиков и любого другого состава, обычно используемого в дерматологии.
[00265] Местное введение используют при показаниях, связанных с кожей, таких как гирсутизм, алопеция, акне и избыточная выработка кожного сала. Доза может быть различной, но согласно основным рекомендациям соединение содержится в дерматологически приемлемом носителе в количестве от примерно 0,01 до 50% (масс./масс.) и чаще от примерно 0,1 до 10% (масс./масс.). Как правило, дерматологический препарат наносят на пораженный участок от 1 до 4 раз в день. «Дерматологически приемлемый» относится к носителю, который можно наносить на кожу или волосы и который обеспечивает диффузию лекарственного средства к месту действия. Более конкретно, «место действия» относится к участку, на котором желательно ингибирование андрогенных рецепторов или разрушение андрогенных рецепторов.
[00266] Соединения формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB можно применять местно для облегчения алопеции, в частности, андрогенной алопеции. Андрогены оказывают выраженное влияние как на рост, так и на выпадение волос. На большинстве участков тела, таких как подбородок и лобковая кожа, андрогены стимулируют рост волос за счет продления фазы роста цикла развития волоса (анаген) и увеличения размера фолликул. Для роста волос на волосистой части головы андрогены не требуются, но андрогены, что парадоксально, необходимы для облысения волосистой частиц головы у индивидуумов, генетически предрасположенных к этом (андрогенная алопеция), в этом случае происходит постепенное сокращение фазы анагена и уменьшение размера волосяных фолликулов. Андрогенная алопеция также распространена у женщин, где она обычно проявляется в виде диффузного выпадения волос, но не по типу, наблюдаемому у мужчин.
[00267] Несмотря на то, что соединения формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB, как правило, применяют для облегчения андрогенной алопеции, соединения можно применять для облегчения любого типа алопеции. Примеры неандрогенной алопеции включают, но не ограничиваются ими, гнездную алопецию, алопецию, вызванную лучевой терапией или химиотерапией, алопецию, вызванную рубцеванием, или алопецию, вызванную стрессом.
[00268] Соединения формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB можно наносить местно на волосистую часть головы и волосы для предупреждения или лечения облысения. Кроме того, соединение формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB можно наносить местно для индуцирования или ускорения роста или повторного роста волос на волосистой части головы.
[00269] Изобретение также включает местное введение соединения формулы I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB для лечения или предупреждения роста волос в участках, где указанный рост волос нежелателен. Один из указанных способов применения предназначен для облегчения гирсутизма. Гирсутизм представляет собой избыточный рост волос на участках, на которых волосы, как правило, отсутствуют (например, на лице у женщин). Указанный неприемлемый рост волос, как правило, встречается у женщин и часто наблюдается в период менопаузы. Местное введение соединений формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB позволяет облегчать это состояние и приводит к уменьшению или устранению указанного неприемлемого или нежелательного роста волос.
[00270] Соединения формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB также можно наносить местно для уменьшения выработки кожного сала. Кожное сало состоит из триглицеридов, сложных эфиров восков, жирных кислот, сложных эфиров стерола и сквалена. Кожное сало вырабатывается в ацинарных клетках сальных желез и накапливается при старении этих клеток. После созревания происходит лизис ацинарных клеток, в результате чего кожное сало высвобождается через люминальную поверхность протоков и, таким образом, может осаждаться на поверхности кожи.
[00271] У некоторых индивидуумов избыточное количество кожного сала секретируется на коже. Это может иметь ряд неблагоприятных последствий. Это может усугублять акне, так как кожное сало является основным источником питания Propionbacterium acnes, возбудителя акне. В результате кожа может приобретать жирный внешний вид, что, как правило, считается косметически непривлекательным.
[00272] Образование кожного сала регулируется факторами роста и различными гормонами, включая андрогены. Клеточный и молекулярный механизм, посредством которого андрогены влияют на сальные железы, до конца не выяснен. Тем не менее, в клинической практике подтверждено, что андрогены влияют на выработку кожного сала. Выработка кожного сала значительно увеличивается в период полового созревания, когда уровень андрогенов является максимальным. Соединения формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB подавляют секрецию кожного сала и тем самым уменьшают количество кожного сала на поверхности кожи. Соединения формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB можно применять для лечения различных кожных заболеваний. таких как акне или себорейный дерматит.
[00273] Помимо лечения заболеваний, связанных с избыточной выработкой кожного сала соединения формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB также можно применять для обеспечения косметического эффекта. Некоторые потребители считают, что они страдают от избыточной активности сальных желез. Они считают, что их кожа является жирной и поэтому непривлекательной. Эти индивидуумы могут применять соединения формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB для уменьшения количества кожного сала на коже. Уменьшение секреции кожного сала может понижать жирность кожи у индивидуумов, пораженных указанными состояниями.
[00274] Для лечения указанных местных показаний изобретение включает косметические или фармацевтические композиции (такие как дерматологические композиции), содержащие по меньшей мере одно соединение формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB. Указанные дерматологические композиции содержат от 0,001% до 10% (масс./масс.) соединения(-ий) в смеси с дерматологически приемлемым носителем, более предпочтительно от 0,1 до 5% (масс./масс.) соединений. Указанные композиции, как правило, наносят от 1 до 4 раз в день. Для обсуждения способов получения указанных составов читатель может обратиться к Remington’s Pharmaceutical Science, 17 издание, Mark Publishing Co., Easton, PA.
[00275] Композиции согласно настоящему изобретению также могут включать твердые препараты, такие как жидкие или брусковые мыла. Указанные композиции получают согласно способам, известным в данной области техники.
[00276] Составы, такие как водные, спиртовые или водно-спиртовые растворы или кремы, гели, эмульсии или муссы или композиции в виде аэрозоля с газом-вытеснителем, можно применять для лечения показаний, возникающих в тех местах, где растут волосы. Таким образом, композиция также может представлять собой композицию для ухода за волосами. Указанные композиции для ухода за волосами включают, но не ограничиваются ими, шампунь, лосьон для укладки волос, лосьон для укрепления волос, крем или гель для укладки волос, окрашивающую композицию или лосьон или гель для предупреждения выпадения волос. Количества различных компонентов дерматологических композиций соответствуют тем, что традиционно используют в рассматриваемых областях техники.
[00277] Медицинские и косметические агенты, содержащие соединения формул I -VII, IA, IB, IC, ID, IIA, IIB, VIIA или VIIB, как правило, упаковывают для розничной реализации (т.е. изготавливают изделие). Указанные изделия имеют этикетки и упаковки, на которых содержатся инструкции для пациента по применению продукта. Указанные инструкции включают состояние, подвергающееся лечению, продолжительность лечения, режим введения и т.д.
[00278] Было показано, что антиандрогены, такие как финастерид или флутамид, до некоторой степени уменьшают уровень андрогенов или блокируют действие андрогенов на коже, но имеют нежелательные системные эффекты. Альтернативным подходом является местное нанесение соединения, селективно разрушающего андрогенные рецепторы (SARD), на пораженные участки. Указанное соединение SARD обеспечивает высокоактивное, но местное ингибирование активности AR и местное разрушение AR, не поступает в системный кровоток субъекта и быстро метаболизируется до поступления в кровь, что ограничивает системное воздействие.
[00279] Для получения указанных фармацевтических лекарственных форм активный ингредиент можно смешивать с фармацевтическим носителем согласно традиционным способам получения фармацевтических препаратов. Носитель может иметь разнообразные формы в зависимости от формы препарата, необходимой для введения.
[00280] При использовании в настоящем описании «фармацевтически приемлемые носители или разбавители» хорошо известны специалистам в данной области техники. Носитель или разбавитель может представлять собой твердый носитель или разбавитель в случае твердых составов, жидкий носитель или разбавитель в случае жидких составов или их смеси.
[00281] Твердые носители/разбавители включают, но не ограничиваются ими, камедь, крахмал (например, кукурузный крахмал, прежелатинизированный крахмал), сахар (например, лактозу, маннит, сахарозу, декстрозу), целлюлозный материал (например, микрокристаллическую целлюлозу), акрилат (например, полиметакрилат), карбонат кальция, оксид магния, тальк или их смеси.
[00282] Пероральное и парентеральное введение: Для получения композиций в пероральной лекарственной форме можно применять любые традиционные фармацевтические среды. Таким образом, в случае жидких пероральных препаратов, таких как суспензии, эликсиры и растворы, подходящие носители и добавки включают воду, гликоли, масла, спирты, вкусоароматические добавки, консерванты, красители и т.д. В случае твердых пероральных препаратов, таких как порошки, капсулы и таблетки, подходящие носители и добавки включают крахмалы, сахара, разбавители, гранулирующие агенты, смазывающие вещества, связывающие вещества, разрыхлители и т.д. Благодаря простоте введения таблетки и капсулы представляют собой наиболее эффективные пероральные стандартные лекарственные формы. При желании, на таблетки можно наносить сахарное покрытие или кишечнорастворимое покрытие стандартными способами.
[00283] В случае парентеральных составов носитель, как правило, содержит стерильную воду, но при этом могут быть включены и другие ингредиенты, такие как те, что способствуют растворению или консервации. Также можно получать инъекционные растворы, в этом случае можно применять подходящие стабилизаторы.
[00284] Для некоторых применений предпочтительно можно применять активный агент в «векторизованной» форме, полученной, например, путем инкапсулирования активного агента в липосому или другую инкапсулирующую среду, или фиксации активного агента, например, путем образования ковалентных связей, хелатообразования или образования координационных связей в виде ассоциатов с подходящей биомолекулой, например, выбранной из белков, липопротеинов, гликопротеинов и полисахаридов.
[00285] В способах лечения с применением составов, подходящих для перорального введения, можно применять отдельные стандартные формы, такие как капсулы, крахмальные капсулы, таблетки или пастилки, каждая из которых содержит предварительно определенное количество активного ингредиента. Необязательно можно применять суспензию в водной жидкости или неводной жидкости, такую как сироп, эликсир, эмульсия или жидкий состав с одноразовой дозой.
[00286] Таблетку можно получать путем прессования или литья или влажного гранулирования необязательно совместно с одним или более вспомогательными ингредиентами. Прессованные таблетки можно получать путем прессования в подходящем устройстве, где активное соединение, которое имеет свободнотекучую форму, такую как порошок или гранулы, необязательно смешивают, например, со связывающим веществом, разрыхлителем, смазывающим веществом, инертным разбавителем, поверхностно-активным веществом или высвобождающим агентом. Формованные таблетки, состоящие из смеси порошкового активного соединения с подходящим носителем, можно получать путем литья в подходящем устройстве.
[00287] Сироп можно получать путем добавления активного соединения в концентрированный водный раствор сахара, например, сахарозы, в который также может(-гут) быть добавлен(-ы) любой(-ые) вспомогательный(-е) ингредиент(-ы). Указанный(-е) вспомогательный(-е) ингредиент(-ы) может(-гут) включать вкусоароматические добавки, подходящие консерванты, агенты, замедляющие кристаллизацию сахара, и агенты, увеличивающие растворимость любых других ингредиентов, таких как полигидроксилированный спирт, например, глицерин или сорбит.
[00288] Составы, подходящие для парентерального введения, могут содержать стерильный водный препарат активного соединения, который предпочтительно является изотоническим с кровью потребителя (например, физиологический солевой раствор). Указанные составы могут включать суспендирующие агенты и загустители и липосомы или другие микродисперсные системы, которые предназначены для направленной доставки соединения к компонентам крови или одному или более органам. Составы могут содержаться в форме с однократной или многоразовой дозировкой.
[00289] Парентеральное введение может включать любую подходящую форму системной доставки. Введение, например, может представлять собой внутривенное, внутриартериальное, интратекальное, внутримышечное, подкожное, внутримышечное, внутрибрюшное (например, интраперитонеальное) и т.д. введение и может осуществляться с применением инфузионных помп (внешних или имплантируемых) или любых других средств, подходящих для желаемого режима введения.
[00290] Составы для интраназального или иного чресслизистого распыления (например, ингаляционные формы) могут содержать очищенные водные растворы активных соединений совместно с консервантами и изотоническими агентами. Указанные составы предпочтительно доводят до значения pH и изотоничности, совместимых с введением через интраназальные или другие слизистые мембраны. В качестве альтернативы они могут иметь форму мелкодисперсных твердых порошков, суспендированных в газовом носителе. Указанные составы можно доставлять при помощи любых подходящих средств или способов, например, с использованием небулайзера, распылителя, дозирующего ингалятора и т.д.
[00291] Составы для ректального введения могут иметь форму суппозиториев с подходящим носителем, таким как масло какао, гидрогенизированные жиры или гидрогенизированные жирные карбоновые кислоты.
[00292] Чрескожные составы можно получать путем введения активного агента в тиксотропный или желатиновый носитель, такой как целлюлозная среда, например, метилцеллюлоза или гидроксиэтилцеллюлоза, после чего полученный состав упаковывают в устройство для чрескожного введения, предназначенное для надежного удерживания в контакте с кожей носителя.
[00293] Помимо вышеуказанных ингредиентов составы согласно настоящему изобретению могут дополнительно включать один или более ингредиентов, выбранных из разбавителей, буферов, вкусоароматических добавок, связывающих веществ, разрыхлителей, поверхностно-активных веществ, загустителей, смазывающих веществ, консервантов (включая антиоксиданты) и т.д.
[00294] Составы могут иметь немедленное высвобождение, замедленное высвобождение, отсроченное высвобождение или любой другой профиль высвобождения, известный специалистам в данной области техники.
[00295] Можно ожидать, что в случае введения млекопитающим и в частности человеку лечащий врач может определять фактическую дозировку и продолжительность лечения, которые более всего подходят для индивидуума, и могут изменять ее в зависимости от возраста, массы тела, генетических факторов и/или ответа конкретного индивидуума.
[00296] Способы согласно настоящему изобретению включают введение соединения в терапевтически эффективном количестве. Терапевтически эффективное количество может включать различные дозировки.
[00297] В одном из вариантов реализации соединение согласно настоящему изобретению вводят в дозировке 1-3000 мг в день. В дополнительных вариантах реализации соединение согласно настоящему изобретению вводят в дозе 1-10 мг в день, 3-26 мг в день, 3-60 мг в день, 3-16 мг в день, 3-30 мг в день, 10-26 мг в день, 15-60 мг, 50-100 мг в день, 50-200 мг в день, 100-250 мг в день, 125-300 мг в день, 20-50 мг в день, 5-50 мг в день, 200-500 мг в день, 125-500 мг в день, 500-1000 мг в день, 200-1000 мг в день, 1000-2000 мг в день, 1000-3000 мг в день, 125-3000 мг в день, 2000-3000 мг в день, 300-1500 мг в день или 100-1000 мг в день. В одном из вариантов реализации соединение согласно настоящему изобретению вводят в дозировке 25 мг в день. В одном из вариантов реализации соединение согласно настоящему изобретению вводят в дозировке 40 мг в день. В одном из вариантов реализации соединение согласно настоящему изобретению вводят в дозировке 50 мг в день. В одном из вариантов реализации соединение согласно настоящему изобретению вводят в дозировке 67,5 мг в день. В одном из вариантов реализации соединение согласно настоящему изобретению вводят в дозировке 75 мг в день. В одном из вариантов реализации соединение согласно настоящему изобретению вводят в дозировке 80 мг в день. В одном из вариантов реализации соединение согласно настоящему изобретению вводят в дозировке 100 мг в день. В одном из вариантов реализации соединение согласно настоящему изобретению вводят в дозировке 125 мг в день. В одном из вариантов реализации соединение согласно настоящему изобретению вводят в дозировке 250 мг в день. В одном из вариантов реализации соединение согласно настоящему изобретению вводят в дозировке 300 мг в день. В одном из вариантов реализации соединение согласно настоящему изобретению вводят в дозировке 500 мг в день. В одном из вариантов реализации соединение согласно настоящему изобретению вводят в дозировке 600 мг в день. В одном из вариантов реализации соединение согласно настоящему изобретению вводят в дозировке 1000 мг в день. В одном из вариантов реализации соединение согласно настоящему изобретению вводят в дозировке 1500 мг в день. В одном из вариантов реализации соединение согласно настоящему изобретению вводят в дозировке 2000 мг в день. В одном из вариантов реализации соединение согласно настоящему изобретению вводят в дозировке 2500 мг в день. В одном из вариантов реализации соединение согласно настоящему изобретению вводят в дозировке 3000 мг в день.
[00298] Способы могут включать введение соединения в различных дозировках. Например, соединение можно вводить в дозировке 3 мг, 10 мг, 30 мг, 40 мг, 50 мг, 80 мг, 100 мг, 120 мг, 125 мг, 200 мг, 250 мг, 300 мг, 450 мг, 500 мг, 600 мг, 900 мг, 1000 мг, 1500 мг, 2000 мг, 2500 мг или 3000 мг.
[00299] В качестве альтернативы соединение можно вводить в дозировке 0,1 мг/кг/день. Соединение можно вводить в дозировке от 0,2 до 30 мг/кг/день или 0,2 мг/кг/день, 0,3 мг/кг/день, 1 мг/кг/ день, 3 мг/кг/день, 5 мг/кг/день, 10 мг/кг/день, 20 мг/кг/день, 30 мг/кг/день, 50 мг/кг/день или 100 мг/кг/день.
[00300] Фармацевтическая композиция может представлять собой твердую лекарственную форму, раствор или чрескожный пластырь. Твердые лекарственные формы включают, но не ограничиваются ими, таблетки и капсулы.
[00301] Следующие примеры приведены для более полной иллюстрации предпочтительных вариантов реализации изобретения. Тем не менее, их не следует рассматривать как ограничивающие каким-либо образом широкий объем изобретения.
ПРИМЕРЫ
ПРИМЕР 1
Синтез SARD
Синтез промежуточных соединений 9-10
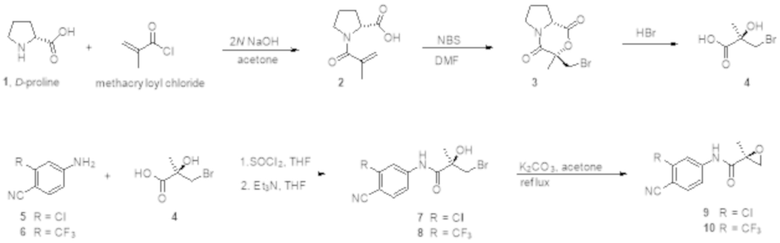 Схема 1. Синтез промежуточных соединений 9-10.
Схема 1. Синтез промежуточных соединений 9-10.
(2 R )-1-метакрилоилпирролидин-2-карбоновая кислота ( 2 )
[00302] D-пролин (1, 14,93 г, 0,13 моль) растворяли в 71 мл 2н. NaOH и охлаждали на ледяной бане. Полученный щелочной раствор разбавляли ацетоном (71 мл). В водный раствор D-пролина одновременно добавляли раствор метакрилоилхлорида (13,56 г, 0,13 моль) в ацетоне (71 мл) и 2н. раствор NaOH (71 мл) в течение 40 минут на ледяной бане. Во время добавления метакрилоилхлорида поддерживали температуру 10-11°C. После перемешивания (3 часа (ч), комнатная температура (КТ)) выпаривали смесь в вакууме при температуре 35-45°C для удаления ацетона. Полученный раствор промывали диэтиловым эфиром и подкисляли до рН 2 концентрированной HCl. Кислую смесь насыщали NaCl и экстрагировали EtOAc (100 мл x3). Объединенные экстракты сушили над Na2SO4, фильтровали через Celite® и выпаривали в вакууме с получением неочищенного продукта в виде бесцветного маслянистого вещества. Перекристаллизация маслянистого вещества из диэтилового эфира и гексанов приводила к получению 16,2 г (68%) целевого соединения в виде бесцветных кристаллов: Тпл 102,1-103,4°C (справ. Тпл 102,5-103,5°C); на ЯМР-спектре полученного соединения было продемонстрировано наличие двух ротамеров титульного соединения.
[00303] 1H ЯМР (300 МГц, ДМСО-d6) δ 5,28 (s) и 5,15 (s) для первого ротамера, 5,15 (s) и 5,03 (s) для второго ротамера (всего 2H для обоих ротамеров, CH2 винила), 4,48-4,44 для первого ротамера, 4,24-4,20 (m) для второго ротамера (всего 1H для обоих ротамеров, CH при хиральном центре), 3,57-3,38 (m, 2H, CH2), 2,27-2,12 (1H, CH), 1,97-1,72 (m, 6H, CH2, CH, Me); 13C ЯМР (75 МГц, ДМСО-d6) δ для основного ротамера 173,3, 169,1, 140,9, 116,4, 58,3, 48,7, 28,9, 24,7, 19,5: для незначительного ротамера 174,0, 170,0, 141,6, 115,2, 60,3, 45,9, 31,0, 22,3, 19,7; ИКС (KBr) 3437 (OH), 1737 (C=O), 1647 (CO, COOH), 1584, 1508, 1459, 1369, 1348, 1178 см-1; [α]D26 +80,8° (c = 1, MeOH); анализ, Расчет для C9H13NO3: C 59,00, H 7,15, N 7,65. Эксперимент: C 59,13, H 7,19, N 7,61.
(3 R ,8a R )-3-бромметил-3-метилтетрагидропирроло[2,1- c ][1,4]оксазин-1,4-дион ( 3 )
[00304] В перемешиваемый раствор (метилакрилоил)пирролидина (16,1 г, 88 ммоль) в 70 мл ДМФ по каплям добавляли раствор NBS (23,5 г, 0,132 ммоль) в 100 мл ДМФ в атмосфере аргона при КТ и перемешивали полученную смесь в течение 3 дней. Удаляли растворитель в вакууме, осаждалось желтое твердое вещество. Твердое вещество суспендировали в воде, перемешивали в течение ночи при КТ, фильтровали и сушили с получением 18,6 г (81%) (уменьшение массы после сушки ~ 34%) титульного соединения в виде желтого твердого вещества: Тпл 158,1-160,3°C;
[00305] 1H ЯМР (300 МГц, ДМСО-d6) δ 4,69 (dd, J = 9,6 Гц, J = 6,7 Гц, 1H, CH при хиральном центре), 4,02 (d, J = 11,4 Гц, 1H, CHHa), 3,86 (d, J = 11,4 Гц, 1H, CHHb), 3,53-3,24 (m, 4H, CH2), 2,30-2,20 (m, 1H, CH), 2,04-1,72 (m, 3H, CH2 и CH), 1,56 (s, 2H, Me); 13C ЯМР (75 МГц, ДМСО-d6) δ 167,3, 163,1, 83,9, 57,2, 45,4, 37,8, 29,0, 22,9, 21,6; ИКС (KBr) 3474, 1745 (C=O), 1687 (C=O), 1448, 1377, 1360, 1308, 1227, 1159, 1062 см-1; [α]D26 +124,5° (c = 1,3, хлороформ); анализ расчет для C9H12BrNO3: C 41,24, H 4,61, N 5,34. Эксперимент: C 41,46, H 4,64, N 5,32.
(2 R )-3-бром-2-гидрокси-2-метилпропановая кислота ( 4 )
[00306] Смесь бромлактона (18,5 г, 71 ммоль) в 300 мл 24% HBr грели при температуре обратной конденсации в течение 1 часа. Полученный раствор разбавляли солевым раствором (200 мл) и экстрагировали этилацетатом (100 мл x4). Объединенные экстракты промывали насыщенным NaHCO3 (100 мл x4). Водный раствор подкисляли концентрированной HCl до pH = 1, после чего экстрагировали этилацетатом (100 мл x4). Объединенный органический раствор сушили над Na2SO4, фильтровали через Celite® и выпаривали в вакууме досуха. Перекристаллизация из толуола приводила к получению 10,2 г (86%) целевого соединения в виде бесцветных кристаллов: Тпл 110,3-113,8°C;
[00307] 1H ЯМР (300 МГц, ДМСО-d6) δ 3,63 (d, J = 10,1 Гц, 1H, CHHa), 3,52 (d, J = 10,1 Гц, 1H, CHHb), 1,35 (s, 3H, Me); ИКС (KBr) 3434 (OH), 3300-2500 (COOH), 1730 (C=O), 1449, 1421, 1380, 1292, 1193, 1085 см-1; [α]D26 +10,5° (c = 2,6, MeOH); анализ, расчет для C4H7BrO3: C 26,25, H 3,86. Эксперимент: C 26,28, H 3,75.
(2 R )-3-бром- N -[4-циано-3-(трифторметил)фенил]-2-гидрокси-2-метилпропанамид ( 8)
[00308] В охлажденный раствор (менее 4°C) (R)-3-бром-2-гидрокси-2-метилпропановой кислоты (4, 51,13 г, 0,28 моль) в 300 мл ТГФ по каплям добавляли тионилхлорид (46,02 г, 0,39 моль) в атмосфере аргона. Полученную смесь перемешивали в течение 3 ч в тех же условиях. В смесь добавляли Et3N (39,14 г, 0,39 моль) и перемешивали в течение 20 минут в тех же условиях. Через 20 минут добавляли 5-амино-2-цианобензотрифторид (6, 40,0 г, 0,21 моль), 400 мл ТГФ и затем оставляли смесь перемешиваться на ночь при КТ. Удаляли растворитель при пониженном давлении с получением твердого вещества, которое обрабатывали 300 мл H2O и экстрагировали EtOAc (2 ×400 мл). Объединенные органические экстракты промывали насыщенным раствором NaHCO3 (2 × 300 мл) и солевым раствором (300 мл). Органический слой сушили над MgSO4 и концентрировали при пониженном давлении с получением твердого вещества, которое очищали путем колоночной хроматографии с использованием CH2Cl2/EtOAc (80:20) с получением твердого вещества. Полученное твердое вещество перекристаллизовывали из смеси CH2Cl2/гексан с получением 55,8 г (73,9%) (2R)-3-бром-N-[4-циано-3-(трифторметил)фенил]-2-гидрокси-2-метилпропанамида в виде светло-желтого твердого вещества.
1H ЯМР (CDCl3/TMS) δ 1,66 (s, 3H, CH3), 3,11 (s, 1H, OH), 3,63 (d, J = 10,8 Гц, 1H, CH2), 4,05 (d, J = 10,8 Гц, 1H, CH2), 7,85 (d, J = 8,4 Гц, 1H, ArH), 7,99 (dd, J = 2,1, 8,4 Гц, 1H, ArH), 8,12 (d, J = 2,1 Гц, 1H, ArH), 9,04 (шир.s, 1H, NH). МС (ИЭР ) 349,0 [M - H] -; Тпл 124-126°C.
(2 R )-3-бром- N -(4-циано-3-хлорфенил)-2-гидрокси-2-метилпропанамид ( 7 )
[00309] В атмосфере аргона в охлажденный раствор (менее 4°C) (R)-3-бром-2-гидрокси-2-метилпропановой кислоты (4, 24,3 г, 0,133 моль) в 300 мл ТГФ по каплям добавляли тионилхлорид (15 мл, 0,20 моль) на бане лед-вода. Полученную смесь перемешивали в течение 3 ч в тех же условиях. В смесь добавляли Et3N (35 мл, 0,245 моль) и перемешивали в течение 20 минут в тех же условиях. Через 20 минут добавляли раствор 4-амино-2-хлорбензонитрила (5, 15,6 г, 0,10 моль) в 100 мл ТГФ и затем оставляли смесь перемешиваться на ночь при КТ. Удаляли растворитель при пониженном давлении с получением твердого вещества, которое обрабатывали 300 мл H2O и экстрагировали EtOAc (2 × 150 мл). Объединенные органические экстракты промывали насыщенным раствором NaHCO3 (2 × 150 мл) и солевым раствором (300 мл). Органический слой сушили над MgSO4 и концентрировали при пониженном давлении с получением твердого вещества, которое очищали путем колоночной флэш-хроматографии с использованием CH2Cl2/EtOAc (80:20) с получением твердого вещества. Полученное твердое вещество перекристаллизовывали из смеси CH2Cl2/гексан с получением 31,8 г (73%) (2R)-3-бром-N-(4-циано-3-хлорфенил)-2-гидрокси-2-метилпропанамида (7) в виде светло-желтого твердого вещества.
1H ЯМР (CDCl3, 400 МГц) δ 1,7 (s, 3H, CH3), 3,0 (s, 1H, OH), 3,7 (d, 1H, CH), 4,0 (d, 1H, CH), 7,5 (d, 1H, ArH), 7,7 (d, 1H, ArH), 8,0 (s, 1H, ArH), 8,8 (s, 1H, NH). МС: 342 (M + 23); Тпл 129°C.
( S )- N -(3-хлор-4-цианофенил)-2-метилоксиран-2-карбоксамид ( 9 )
[00310] Смесь 3-бром-N-(4-циано-3-хлорфенил)-2-гидрокси-2-метилпропанамида (7, 0,84 ммоль) и карбоната калия (1,68 ммоль) в 10 мл ацетона нагревали до температуры обратной конденсации в течение 30 минут. После завершения конверсии исходного бромида 7 в целевой эпоксид 9, которую отслеживали путем ТСХ, выпаривали растворитель при пониженном давлении с получением желтоватого остатка, который выливали в 10 мл безводного EtOAc. Раствор фильтровали через подложку с Celite® для удаления остатков K2CO3 и конденсировали при пониженном давлении с получением эпоксида 9 в виде светло-желтоватого твердого вещества.
[00311] 1H ЯМР (CDCl3, 400 МГц) δ 8,41 (шир.s, NH), 8,02 (d, J = 2,0 Гц, 1H, ArH), 7,91 (dd, J = 2,0, 8,4 Гц, 1H, ArH), 7,79 (d, J = 2,0 Гц, 1H, ArH), 3,01 (s, 2H), 1,69 (s, 3H). МС (ИЭР) m/z 235,0 [M - H] -.
Соединения с 5-членными кольцами
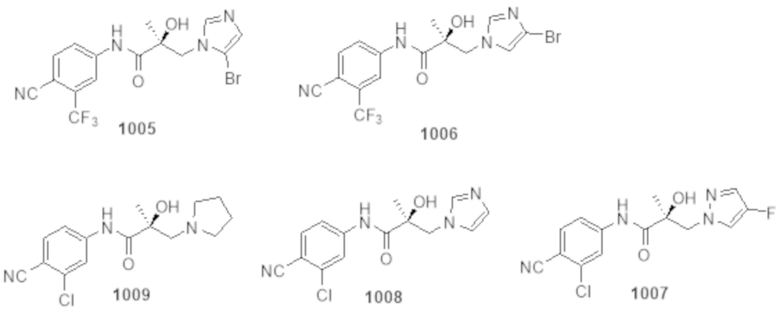
[00312] Соединения с пятичленными кольцами согласно настоящему изобретению получали при помощи следующих общих способов синтеза (способ А и способ B), где m = 0. Переменные X и Y определены таким образом, чтобы можно было получать целевое соединение.
[00313] Способ A:
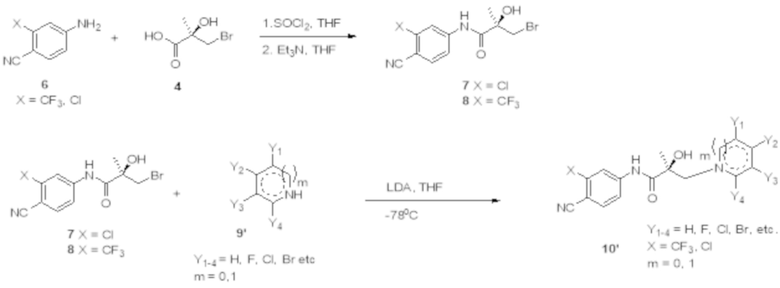
[00314] Получение раствора диизопропиламида лития (LDA) в ТГФ: В перемешиваемый раствор свежеперегнанного диизопропиламина (0,14 мл, 1,2 ммоль) в 5 мл безводного ТГФ добавляли раствор н-бутиллития (0,53 мл, 1,32 ммоль, 2,5 M раствор в гексане) при -78°C в атмосфере аргона. Полученный раствор LDA или коммерческий 2,0 M LDA медленно нагревали до 0°C и перемешивали в течение 10 минут, после чего снова охлаждали до -78°C. В раствор LDA по каплям добавляли раствор 9’ (1,0 ммоль) в 5 мл ТГФ в течение 20 минут. По каплям добавляли соединение 7 или 8 в ТГФ через капельную воронку в атмосфере аргона при -78°C. Реакционную смесь перемешивали при указанной температуре в течение 30 минут и гасили реакцию путем добавления нас. NH4Cl. Раствор концентрировали при пониженном давлении и диспергировали в избытке EtOAc и сушили над Na2SO4. Концентрировали раствор и перекристаллизовывали полученное твердое вещество из смеси EtOAc/гексан или ДХМ/гексан с получением указанного соединения 10’. Концентрировали маточный раствор и очищали путем колоночной флэш-хроматографии (EtOAc/гексан) с получением второй партии 10’.
[00315] Способ B:
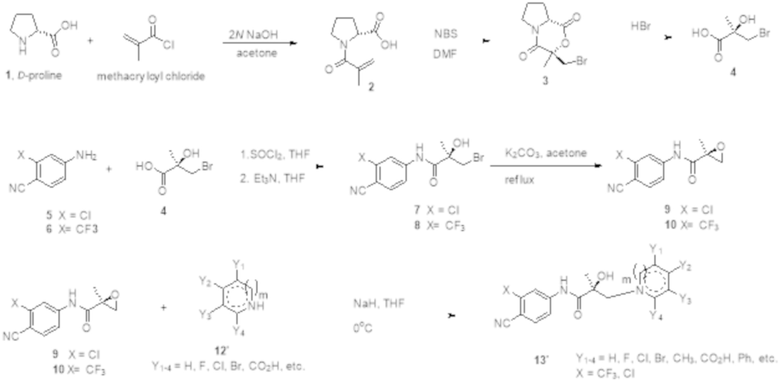
[00316] Стадии вплоть до синтеза оксиранов 9 и 10 являются такими же, что описано выше на схеме 1. 60% дисперсию NaH в минеральном масле (228 мг, 5,7 ммоль) в 20 мл безводного ТГФ добавляли в 100 мл высушенную двухгорлую круглодонную колбу, оборудованную капельной воронкой. В раствор добавляли соединение общей структуры 12’ (2,84 ммоль) в атмосфере аргона на ледяной бане и перемешивали полученный раствор в течение 30 минут на бане лед-вода. В колбу через капельную воронку добавляли эпоксид 9 или 10 (2,84 ммоль в ТГФ) в атмосфере аргона на бане лед-вода и перемешивали в течение ночи при КТ. После добавления 1 мл H2O концентрировали реакционную смесь при пониженном давлении и затем диспергировали в 50 мл EtOAc, промывали 50 мл (×2) воды, солевым раствором, сушили над безводным MgSO4 и выпаривали досуха. Смесь очищали путем колоночной флэш-хроматографии с использованием смеси EtOAc/гексан в качестве элюента и затем перекристаллизовывали конденсированные соединения в смеси EtOAc/гексан с получением продукта общей структуры 13’.
[00317] Пример способа синтеза 1001:
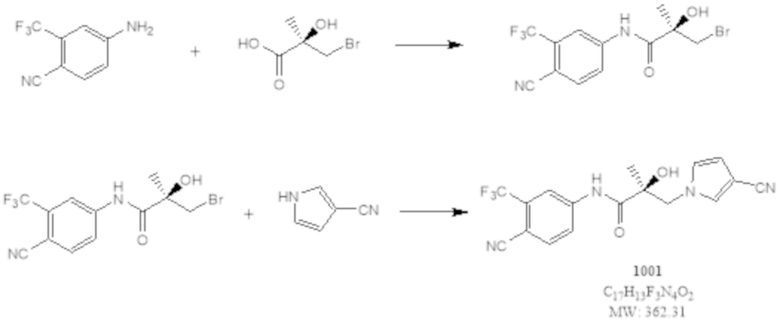
( S )-3-(3-циано-1 H -пиррол-1-ил)- N -(4-циано-3-(трифторметил)фенил)-2-гидрокси-2-метилпропанамид (C17H13F3N4O2) ( 1001 )
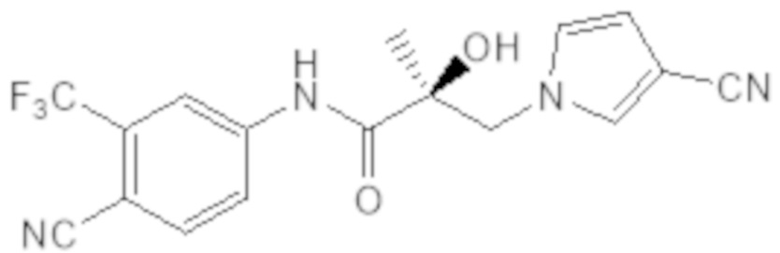
[00318] В раствор 1H-пиррол-3-карбонитрила (0,10 г, 0,00108 моль) в безводном ТГФ (10 мл), который охлаждали на бане лед-вода, в атмосфере аргона добавляли гидрид натрия (60% дисперсия в масле, 0,090 г, 0,00217 моль). После завершения добавления полученную смесь перемешивали в течение 3 часов. В полученный выше раствор добавляли (R)-3-бром-N-(4-циано-3-(трифторметил)фенил)-2-гидрокси-2-метилпропанамид (8, 0,38 г, 0,00108 моль) и полученную реакционную смесь оставляли перемешиваться на ночь при КТ в атмосфере аргона. Реакцию гасили водой и экстрагировали смесь этилацетатом. Органический слой промывали солевым раствором, сушили MgSO4, фильтровали и концентрировали в вакууме. Продукт очищали на колонке с силикагелем с использованием этилацетата и гексанов (1:1) в качестве элюента с получением 0,26 г титульного соединения в виде розоватого твердого вещества.
[00319] Соединение 1001 было охарактеризовано следующим образом: 1H ЯМР (400 МГц, ДМСО-d6) δ 10,44 (s, 1H, NH), 8,44 (s, 1H, ArH), 8,24 (d, J = 8,8 Гц, 1H, ArH), 8,10 (d, J = 8,8 Гц, 1H, ArH), 7,49 (s, 1H, пиррол-H), 6,38 (t, J = 2,0 Гц, 1H, пиррол-H), 6,41-6,40 (m, 2H, OH и пиррол-H), 4,30 (d, J = 14,0 Гц, 1H, CH), 4,14 (d, J = 14,0 Гц, 1H, CH), 1,34 (s, 3H, CH3); (ИЭР, положительные ионы): 363,1079 [M+H]+.
( S )- N -(4-циано-3-(трифторметил)фенил)-3-(4-фтор-1 H -пиразол-1-ил)-2-гидрокси-2-метилпропанамид (C15H12F4N4O2) ( 1002 )
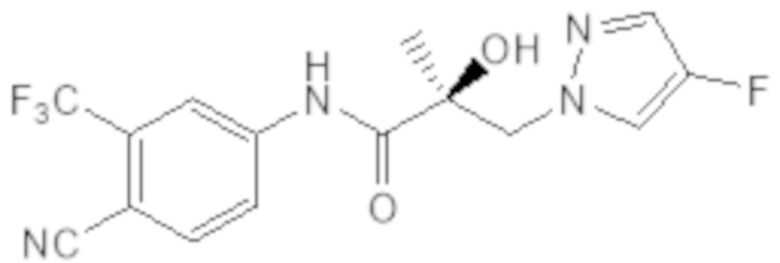
[00320] В раствор 4-фторпиразола (0,10 г, 0,00116 моль) в безводном ТГФ (10 мл), который охлаждали на бане лед-вода, в атмосфере аргона добавляли гидрид натрия (60% дисперсия в масле, 0,12 г, 0,00291 моль). После завершения добавления полученную смесь перемешивали в течение 3 часов. В полученный выше раствор добавляли (R)-3-бром-N-(4-циано-3-(трифторметил)фенил)-2-гидрокси-2-метилпропанамид (8) (0,41 г, 0,00116 моль) и полученную реакционную смесь оставляли перемешиваться на ночь при КТ в атмосфере аргона. Реакцию гасили водой и экстрагировали смесь этилацетатом. Органический слой промывали солевым раствором, сушили MgSO4, фильтровали и концентрировали в вакууме. Продукт очищали на колонке с силикагелем с использованием этилацетата и гексанов (1:1) в качестве элюента с получением 0,13 г титульного соединения в виде белого твердого вещества.
[00321] Соединение 1002 было охарактеризовано следующим образом: 1H ЯМР (400 МГц, ДМСО-d6) δ 10,39 (s, 1H, NH), 8,47 (d, J = 1,6 Гц, 1H, ArH), 8,24 (dd, J = 8,4 Гц, J = 2,0 Гц, 1H, ArH), 8,10 (d, J = 8,4 Гц, 1H, ArH), 7,73 (d, J = 4,4 Гц, 1H, пиразол-H), 7,41 (d, J = 4,4 Гц, 1H, пиразол-H), 6,31 (s, 1H, OH), 4,38 (d, J = 14,0 Гц, 1H, CH), 4,21 (d, J = 14,0 Гц, 1H, CH), 1,34 (s, 3H, CH3); масс-спектр (ИЭР, положительные ионы): 357,0966 [M+H]+; Тпл 109-111°C.
[00322] Гидрохлорид (S)-N-(4-циано-3-(трифторметил)фенил)-3-(4-фтор-1H-пиразол-1-ил)-2-гидрокси-2-метилпропанамида (C15H13ClF4N4O2) (1002-HCl)
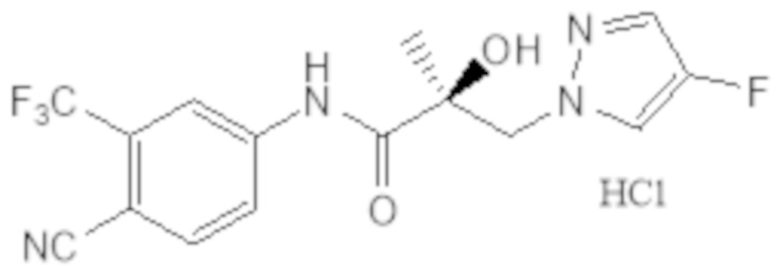
[00323] В раствор (S)-N-(4-циано-3-(трифторметил)фенил)-3-(4-фтор-1H-пиразол-1-ил)-2-гидрокси-2-метилпропанамида (0,100 г, 0,2807 ммоль) в 3 мл метанола добавляли хлороводород (2 M HCl в диэтиловом эфире, 0,15 мл, 0,2947 моль). После завершения добавления полученную смесь перемешивали в течение 1-2 часов при КТ. Удаляли растворитель в вакууме и сушили с получением 0,11 г (99%) титульного соединения в виде белой пены.
[00324] Оксалат (S)-N-(4-циано-3-(трифторметил)фенил)-3-(4-фтор-1H-пиразол-1-ил)-2-гидрокси-2-метилпропанамида (C17H14F4N4O6) (соль щавелевой кислоты 1002)
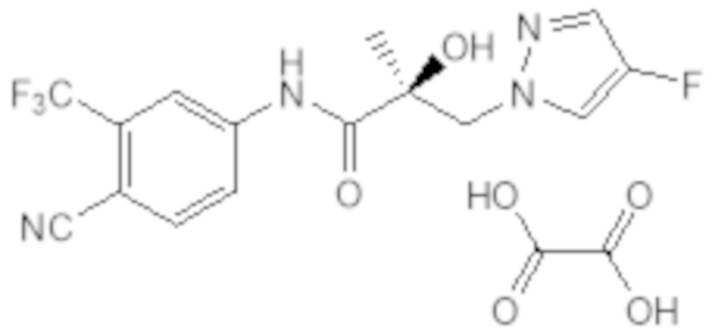
[00325] В раствор (S)-N-(4-циано-3-(трифторметил)фенил)-3-(4-фтор-1H-пиразол-1-ил)-2-гидрокси-2-метилпропанамида (0,050 г, 0,14034 ммоль) в 2 мл метанола добавляли щавелевую кислоту (0,0177 г, 0,14034 моль). После завершения добавления полученную смесь перемешивали в течение 1-2 часов при КТ. В полученный выше раствор добавляли диэтиловый эфир, отфильтровывали твердое вещество и сушили в вакууме с получением 0,058 г (92%) титульного соединения в виде белого твердого вещества.
[00326] Соединение 1002-оксалат было охарактеризовано следующим образом: 1H ЯМР (400 МГц, ДМСО-d6) δ 14,02 (шир.s, 2H), 10,38 (s, 1H, NH), 8,46 (s, 1H, ArH), 8,24 (d, J = 8,4 Гц, 1H, ArH), 8,10 (d, J = 8,4 Гц, 1H, ArH), 7,73 (d, J = 4,8 Гц, 1H, пиразол-H), 7,41 (d, J = 4,0 Гц, 1H, пиразол-H), 6,30 (s, 1H, OH), 4,38 (d, J = 14,0 Гц, 1H, CH), 4,31 (s, 2H), 4,21 (d, J = 14,0 Гц, 1H, CH), 2,42 (s, 4H), 1,34 (s, 3H, CH3).
[00327] 2,3-дигидроксисукцинат (S)-N-(4-циано-3-(трифторметил)фенил)-3-(4-фтор-1H-пиразол-1-ил)-2-гидрокси-2-метилпропанамида (C19H18F4N4O8) (соль винной кислоты 1002)
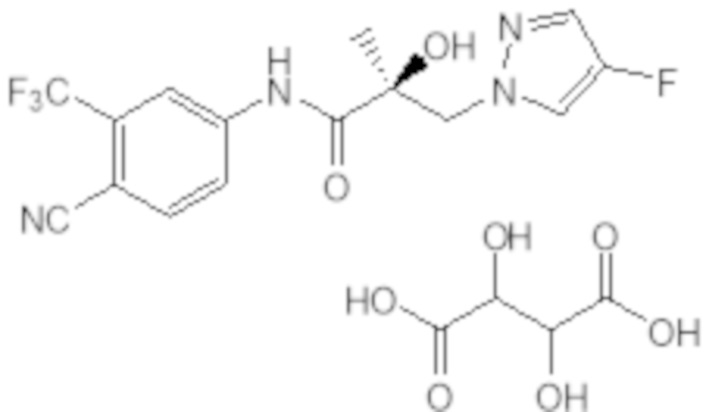
В раствор (S)-N-(4-циано-3-(трифторметил)фенил)-3-(4-фтор-1H-пиразол-1-ил)-2-гидрокси-2-метилпропанамида (0,050 г, 0,14034 ммоль) в 2 мл метанола добавляли L-(+)-винную кислоту (0,021 г, 0,14034 моль). После завершения добавления полученную смесь перемешивали в течение 1-2 часов при КТ. В полученный выше раствор добавляли диэтиловый эфир, отфильтровывали твердое вещество и сушили в вакууме с получением 0,067 г (94%) титульного соединения в виде белого твердого вещества.
Соединение 1002-соль винной кислоты было охарактеризовано следующим образом: 1H ЯМР (400 МГц, ДМСО-d6) δ 12,69 (s, 2H), 10,38 (s, 1H, NH), 8,46 (s, 1H, ArH), 8,24 (d, J = 8,4 Гц, 1H, ArH), 8,10 (d, J = 8,4 Гц, 1H, ArH), 7,73 (d, J = 4,4 Гц, 1H, пиразол-H), 7,41 (d, J = 4,0 Гц, 1H, пиразол-H), 6,30 (s, 1H, OH), 5,08 (s, 2H, OH), 4,38 (d, J = 14,0 Гц, 1H, CH), 4,31 (s, 2H), 4,21 (d, J = 14,0 Гц, 1H, CH), 2,42 (s, 4H), 1,34 (s, 3H, CH3).
Гидробромид ( S )- N -(4-циано-3-(трифторметил)фенил)-3-(4-фтор-1 H -пиразол-1-ил)-2-гидрокси-2-метилпропанамида (C15H13BrF4N4O2) ( 1002-HBr )
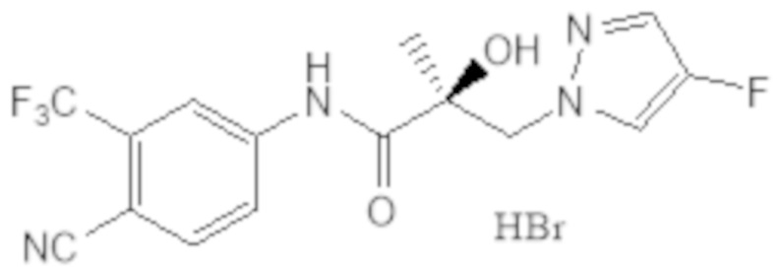
В раствор (S)-N-(4-циано-3-(трифторметил)фенил)-3-(4-фтор-1H-пиразол-1-ил)-2-гидрокси-2-метилпропанамида (0,050 г, 0,1403 ммоль) в 2 мл метанола добавляли бромоводород (48% (масс./масс.) водный раствор, 0,0159 мл, 0,1403 моль). После завершения добавления полученную смесь перемешивали в течение 1-2 часов при КТ. Удаляли растворитель в вакууме и сушили с получением 0,061 г (99%) титульного соединения в виде желтоватой пены.
Сукцинат ( S )- N -(4-циано-3-(трифторметил)фенил)-3-(4-фтор-1 H -пиразол-1-ил)-2-гидрокси-2-метилпропанамида ( соль янтарной кислоты 1002 ) (C19H18F4N4O6)
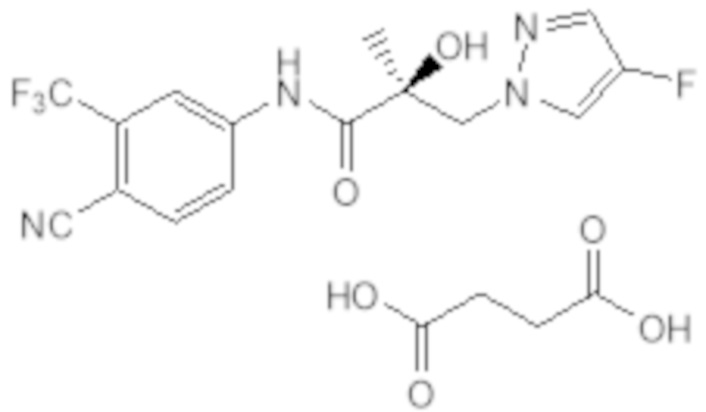
В раствор (S)-N-(4-циано-3-(трифторметил)фенил)-3-(4-фтор-1H-пиразол-1-ил)-2-гидрокси-2-метилпропанамида (0,050 г, 0,14034 ммоль) в 2 мл метанола добавляли янтарную кислоту (0,0166 г, 0,14034 моль). После завершения добавления полученную смесь перемешивали в течение 1-2 часов при КТ. В полученный выше раствор добавляли диэтиловый эфир, отфильтровывали твердое вещество и сушили в вакууме с получением 0,063 г (95%) титульного соединения в виде белого твердого вещества.
Соединение 1002-соль винной кислоты было охарактеризовано следующим образом: 1H ЯМР (400 МГц, ДМСО-d6) δ 12,14 (s, 2H), 10,39 (s, 1H, NH), 8,46 (s, 1H, ArH), 8,24 (d, J = 8,8 Гц, 1H, ArH), 8,10 (d, J = 8,8 Гц, 1H, ArH), 7,73 (d, J = 4,4 Гц, 1H, пиразол-H), 7,41 (d, J = 4,4 Гц, 1H, пиразол-H), 6,30 (s, 1H, OH), 4,39 (d, J = 14,0 Гц, 1H, CH), 4,21 (d, J = 14,0 Гц, 1H, CH), 2,42 (s, 4H), 1,34 (s, 3H, CH3).
( S )- N -(4-циано-3-(трифторметил)фенил)-2-гидрокси-2-метил-3-(4-фенил-1 H -пиразол-1-ил)пропанамид (C21H17F3N4O2) ( 1003 )
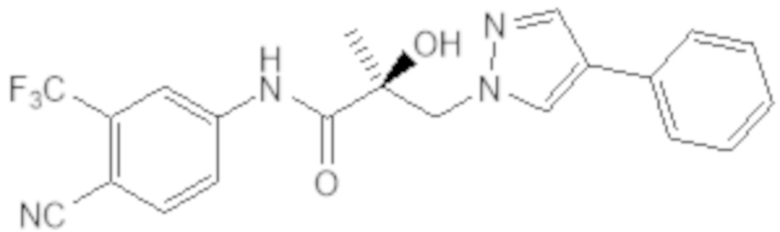
[00328] В раствор 4-фенилпиразола (0,50 г, 0,003468 моль) в безводном ТГФ (10 мл), который охлаждали на бане лед-вода, в атмосфере аргона добавляли гидрид натрия (60% дисперсия в масле (0,35 г, 0,00867 моль)). После завершения добавления полученную смесь перемешивали в течение 3 часов. В полученный выше раствор добавляли (R)-3-бром-N-(4-циано-3-(трифторметил)фенил)-2-гидрокси-2-метилпропанамид (8, 1,22 г, 0,003468 моль) и полученную реакционную смесь оставляли перемешиваться на ночь при КТ в атмосфере аргона. Реакцию гасили водой и экстрагировали смесь этилацетатом. Органический слой промывали солевым раствором, сушили MgSO4, фильтровали и концентрировали в вакууме. Продукт очищали на колонке с силикагелем с использованием этилацетата и гексанов (1:2) в качестве элюента с получением 0,90 г титульного соединения в виде белых игольчатых кристаллов.
[00329] Соединение 1003 было охарактеризовано следующим образом: 1H ЯМР (400 МГц, ДМСО-d6) δ 10,40 (s, 1H, NH), 8,46 (d, J = 2,0 Гц, 1H, ArH), 8,24 (dd, J = 8,4 Гц, J = 2,0 Гц, 1H, ArH), 8,09 (d, J = 8,4 Гц, 1H, ArH), 8,05 (s, 1H, пиразол-H), 7,82 (s, 1H, пиразол-H), 7,52-7,45 (m, 2H, ArH), 7,35-7,31 (m, 2H, ArH), 7,20-7,16 (m, 1H, ArH), 6,33 (s, 1H, OH), 4,50 (d, J = 14,0 Гц, 1H, CH), 4,30 (d, J = 14,0 Гц, 1H, CH), 1,40 (s, 3H, CH3); масс-спектр (ИЭР, положительные ионы): 415,1455 [M+H]+.
( S )- N -(4-циано-3-(трифторметил)фенил)-2-гидрокси-2-метил-3-(3-фенил-1 H -пиррол-1-ил)пропанамид (C22H18F3N3O2) ( 1004 )
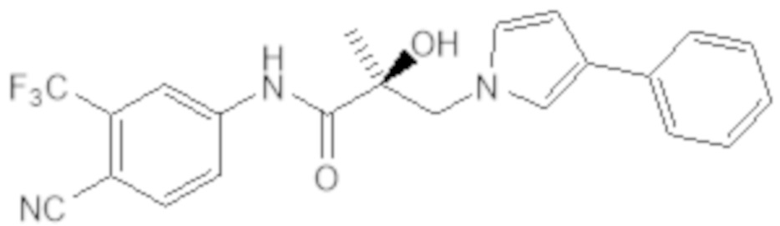
[00330] В раствор 4-фенилпиррола (0,50 г, 0,00349 моль) в безводном ТГФ (10 мл), который охлаждали на бане лед-вода, в атмосфере аргона добавляли гидрид натрия (60% дисперсия в масле, 0,35 г, 0,00873 моль). После завершения добавления полученную смесь перемешивали в течение 3 часов. В полученный выше раствор добавляли (R)-3-бром-N-(4-циано-3-(трифторметил)фенил)-2-гидрокси-2-метилпропанамид (8, 1,23 г, 0,00349 моль) и полученную реакционную смесь оставляли перемешиваться на ночь при КТ в атмосфере аргона. Реакцию гасили водой и экстрагировали смесь этилацетатом. Органический слой промывали солевым раствором, сушили MgSO4, фильтровали и концентрировали в вакууме. Продукт очищали на колонке с силикагелем с использованием этилацетата и гексанов (1:2) в качестве элюента с получением 0,90 г титульного соединения в виде розового твердого вещества.
[00331] Соединение 1004 было охарактеризовано следующим образом: 1H ЯМР (400 МГц, ДМСО-d6) δ 10,41 (s, 1H, NH), 8,24 (d, J = 1,6 Гц, 1H, ArH), 8,17 (dd, J = 8,4 Гц, J = 2,0 Гц, 1H, ArH), 8,07 (d, J = 8,4 Гц, 1H, ArH), 7,38-7,33 (m, 4H, ArH), 7,28-7,24 (m, 1H, ArH), 6,96 (t, J = 3,0 Гц, 1H, пиррол-H), 6,28 (s, 1H, OH), 6,07 (t, J = 3,5 Гц, 1H, пиррол-H), 6,03 (m, 1H, пиррол-H), 4,30-4,22 (m, 2H, CH2), 1,01 (s, 3H, CH3); масс-спектр (ИЭР, положительные ионы): 414,1432 [M+H]+.
Бром-1 H -имидазол-1-ил)- N -(4-циано-3-(трифторметил)фенил)-2-гидрокси-2-метилпропанамиды ( 1005 и 1006 )
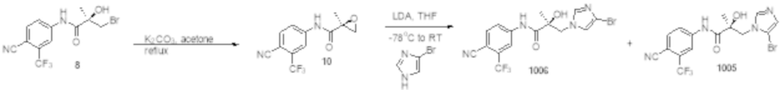
[00332] В раствор 4-бром-1H-имидазола (1,0 ммоль, 2 ммоль) в 5 мл безводного ТГФ медленно добавляли раствор диизопропиламида лития (2,0 M) в смеси ТГФ/гептан/этилбензол (1 мл) при -78°C и нагревали до 0°C, перемешивали в течение 10 минут и снова охлаждали до -78°C. В раствор по каплям добавляли раствор (S)-N-(4-циано-3-(трифторметил)фенил)-2-метилоксиран-2-карбоксамида (10, 1 ммоль), полученного из 8 (1 ммоль), и перемешивали реакционную смесь в течение ночи. После гашения путем добавления нас. NH4Cl концентрировали раствор при пониженном давлении и диспергировали в избытке EtOAc и сушили над Na2SO4. Концентрировали раствор и очищали путем колоночной флэш-хроматографии (EtOAc/гексан) с получением целевых продуктов с общим выходом 69% (37% 1005 и 32% 1006) в виде белых твердых веществ.
[00333] Соединения были охарактеризованы следующим образом:
( S )-3-(5-бром-1 H -имидазол-1-ил)- N -(4-циано-3-(трифторметил)фенил)-2-гидрокси-2-метилпропанамид (C15H12BrF3N4O2) ( 1005 )
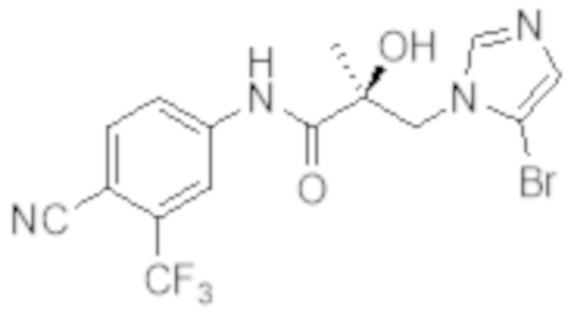
[00334] Способ A (с использованием бромамида 8 и 4-бром-1H-имидазола вместо соединения общей структуры 9’) приводил к получению белого твердого вещества; 1H ЯМР (ацетон-d6, 400 МГц) δ 9,93 (шир.s, 1H, NH), 8,44 (d, J = 2,0 Гц, 1H), 8,26 (dd, J = 8,6, 2,0 Гц, 1H), 8,03 (d, J = 8,6 Гц, 1H), 7,47 (s, 1H), 7,11 (s, 1H), 5,83 (s, 1H, OH), 4,50 (d, J = 14,0 Гц, 1H), 4,23 (d, J = 14,0 Гц, 1H), 1,55 (s, 3H); 19F ЯМР (ацетон-d6, 400 МГц) δ 114,69; МС (ИЭР): 415,0 [M - H]-; ЖХМС (ИЭР) m/z, расчет для C15H11N4O2F3Br: 415,0088. Эксперимент: 415,0017 [М - Н]-.
( S )-3-(4-бром-1 H -имидазол-1-ил)- N -(4-циано-3-(трифторметил)фенил)-2-гидрокси-2-метилпропанамид (C15H12BrF3N4O2) ( 1006 )
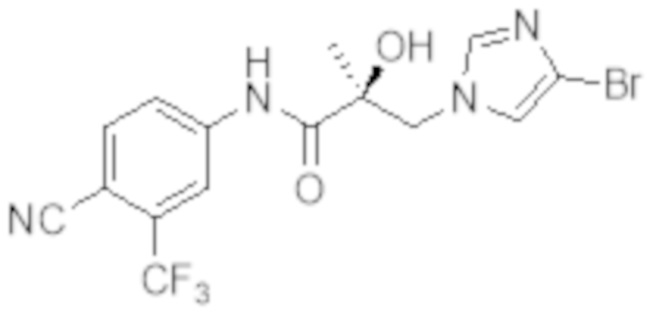
[00335] Способ A (с использованием бромамида 8 и 4-бром-1H-имидазола вместо соединения общей структуры 9’) приводил к получению белого твердого вещества; 1H ЯМР (CDCl3, 400 МГц) δ 9,48 (шир.s, 1H, NH), 8,15 (s, 1H), 7,97 (d, J = 8,6 Гц, 1H), 7,83 (d, J = 8,6 Гц, 1H), 7,71 (s, 1H), 6,75 (s, 1H), 4,53 (d, J = 14,4 Гц, 1H), 4,09 (d, J = 14,4 Гц, 1H), 2,84 (s, 1H, OH), 1,45 (s, 3H); 19F ЯМР (CDCl3, 400 МГц) δ -62,19; МС (ИЭР): 415,0 [M - H]-.
( S )- N -(3-хлор-4-цианофенил)-2-гидрокси-3-(1 H -имидазол-1-ил)-2-метилпропанамид (C14H13ClN4O2) ( 1008 )
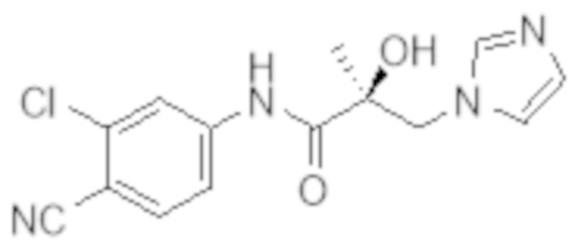
[00336] Способ A (с использованием бромамида 7 и 1H-имидазола вместо соединения общей структуры 9’) приводил к получению желтоватого твердого вещества. Выход 53%; 1H ЯМР (ДМСО-d6, 400 МГц) δ 10,24 (шир.s, 1H, NH), 8,19 (s, 1H), 7,90 (m, 2H), 7,53 (s, 1H), 7,05 (s, 1H), 6,83 (s, 1H), 6,40 (шир.s, 1H, OH), 4,31 (d, J = 14,4 Гц, 1H), 4,11 (d, J = 14,4 Гц, 1H), 1,34 (s, 3H); ЖХМС (ИЭР) m/z, расчет для C14H14ClN4O2: 305,0805. Эксперимент: 305,0809 [М + Н]+.
( S )- N -(3-хлор-4-цианофенил)-2-гидрокси-2-метил-3-(пирролидин-1-ил)пропанамид (C15H18ClN3O2) ( 1009 )
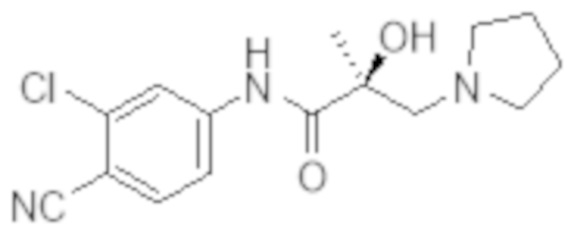
[00337] Способ A (с использованием бромамида 7 и пирролидина вместо соединения общей структуры 9’) обеспечивал выход 89%; 1H ЯМР (CDCl3, 400 МГц) δ 9,41 (шир.s, 1H, NH), 7,98 (d, J = 2,0 Гц, 1H), 7,62 (d, J = 8,8 Гц, 1H), 7,51 (dd, J = 8,8, 2,0 Гц, 1H), 5,20 (s, 1H), 3,15 (d, J = 12,4 Гц, 1H), 2,72 (d, J = 12,4 Гц, 1H), 2,64-2,58 (m, 4H), 1,76 (m, 4H), 1,41 (s, 3H); 13C ЯМР (CDCl3, 100 МГц) δ 175,6 (-NHCO-), 142,5, 137,9, 134,6, 119,9, 117,3, 116,1, 108,0, 72,9, 62,3, 54,6 (2C), 25,5, 24,0; ЖХМС (ИЭР) m/z, расчет для C15H19ClN3O2: 308,1166. Эксперимент: 308,1173 [М + Н]+.
Получение соли HCl ( S )- N -(3-хлор-4-цианофенил)-2-гидрокси-2-метил-3-(пирролидин-1-ил)пропанамида
[00338] В раствор 1009 в EtOH (20 мл) по каплям добавляли ацетилхлорид (1 мл) при 0°C и дополнительно перемешивали при КТ в течение ночи и удаляли растворитель с получением целевой соли 1009.
( S )- N -(3-хлор-4-цианофенил)-3-(4-фтор-1 H -пиразол-1-ил)-2-гидрокси-2-метилпропанамид (C14H12ClFN4O2) ( 1007 )
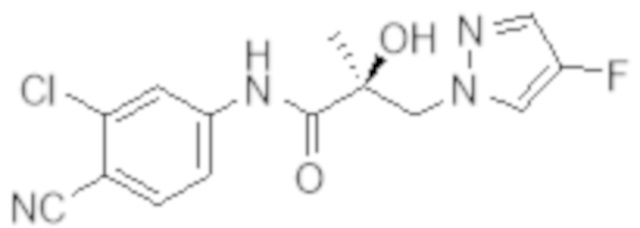
[00339] Способ B (с использованием оксирана 9 и 4-фтор-1H-пиразола вместо соединения общей структуры 12’) приводил к получению желтоватого твердого вещества; выход 72%; 1H ЯМР (CDCl3, 400 МГц) δ 8,97 (шир.s, 1H, NH), 7,88 (d, J = 2,0 Гц, 1H), 7,60 (d, J = 8,4 Гц, 1H), 7,45 (dd, J = 8,4, 2,0 Гц, 1H), 7,36 (d, J = 4,0 Гц, 1H), 7,35 (d, J = 4,4 Гц, 1H), 5,86 (шир.s, 1H, OH), 4,54 (d, J = 14,0 Гц, 1H), 4,15 (d, J = 14,0 Гц, 1H), 1,46 (s, 3H); 19F ЯМР (CDCl3, 400 МГц) δ -176,47; ЖХМС (ИЭР ) m/z, расчет для C14H13ClFN4O2: 323,0711. Эксперимент: 323,0710 [М + Н]+.
( S )- N -(4-циано-3-(трифторметил)фенил)-3-(3-(4-фторфенил)-1 H -пиррол-1-ил)-2-гидрокси-2-метилпропанамид (C22H17F4N3O2) ( 1010 )
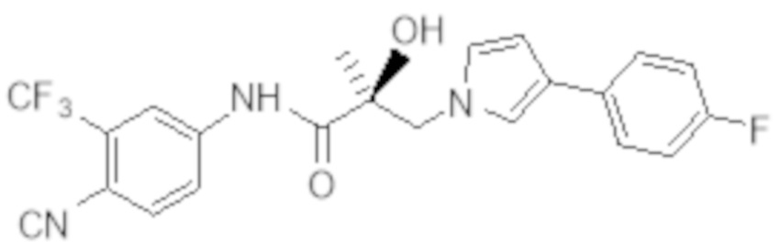
[00340] В раствор 3-(4-фторфенил)пиррола (0,50 г, 0,003102 моль) в безводном ТГФ (10 мл), который охлаждали на бане лед-вода, в атмосфере аргона добавляли гидрид натрия (60% дисперсия в масле, 0,37 г, 0,009306 моль). После завершения добавления полученную смесь перемешивали в течение 3 часов. В полученный выше раствор добавляли (R)-3-бром-N-(4-циано-3-(трифторметил)фенил)-2-гидрокси-2-метилпропанамид (8) (1,09 г, 0,003102 моль) и полученную реакционную смесь оставляли перемешиваться на ночь при КТ в атмосфере аргона. Реакцию гасили водой и экстрагировали смесь этилацетатом. Органический слой промывали солевым раствором, сушили MgSO4, фильтровали и концентрировали в вакууме. Продукт очищали на колонке с силикагелем с использованием этилацетата и гексанов (от 1:2 до 1:1) в качестве элюента с получением 0,60 г (45%) соединения в виде желтоватого твердого вещества.
[00341] Соединение 1010 было охарактеризовано следующим образом: 1H ЯМР (400 МГц, ДМСО-d6) δ 10,40 (s, 1H, NH), 8,42 (d, J = 2,0 Гц, 1H, ArH), 8,24 (dd, J = 8,8 Гц, J = 2,0 Гц, 1H, ArH), 8,07 (d, J = 8,8 Гц, 1H, ArH), 7,43-7,38 (m, 2H, ArH), 7,11-7,05 (m, 3H, ArH), 6,73 (t, J = 2,0 Гц, 1H, пиррол-H), 6,33 (s, 1H, OH), 4,24 (d, J = 14,0 Гц, 1H, CH), 4,05 (d, J = 14,0 Гц, 1H, CH), 1,37 (s, 3H, CH3); масс-спектр (ИЭР, положительные ионы): 432,1352 [M+H]+; Тпл 187-189°C.
( S )- N -(4-циано-3-(трифторметил)фенил)-2-гидрокси-2-метил-3-(3-фенил-1 H -пиразол-1-ил)пропанамид (C21H17F3N4O2) ( 1011 )
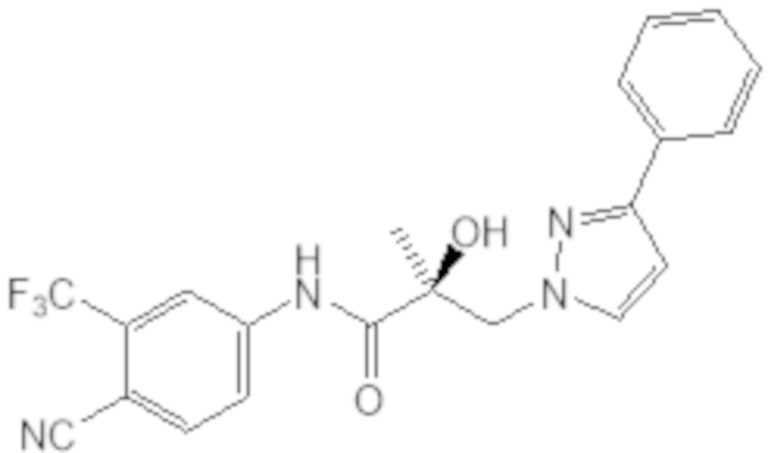
[00342] В раствор 3-фенилпиразола (0,50 г, 0,003468 моль) в безводном ТГФ (10 мл), который охлаждали на бане лед-вода, в атмосфере аргона добавляли гидрид натрия (60% дисперсия в масле, 0,35 г, 0,00867 моль). После завершения добавления полученную смесь перемешивали в течение 3 часов. В полученный выше раствор добавляли (R)-3-бром-N-(4-циано-3-(трифторметил)фенил)-2-гидрокси-2-метилпропанамид (8, 1,22 г, 0,003468 моль) и полученную реакционную смесь оставляли перемешиваться на ночь при КТ в атмосфере аргона. Реакцию гасили водой и экстрагировали смесь этилацетатом. Органический слой промывали солевым раствором, сушили MgSO4, фильтровали и концентрировали в вакууме. Продукт очищали на колонке с силикагелем с использованием этилацетата и гексанов (от 1:3 до 1:2) в качестве элюента с получением 0,60 г титульного соединения в виде белых игольчатых кристаллов.
[00343] Соединение 1011 было охарактеризовано следующим образом: 1H ЯМР (400 МГц, ДМСО-d6) δ 10,33 (s, 1H, NH), 8,48 (d, J = 2,0 Гц, 1H, ArH), 8,22 (dd, J = 8,2 Гц, J = 2,0 Гц, 1H, ArH), 8,05 (d, J = 8,2 Гц, 1H, ArH), 7,69 (d, J = 2,0 Гц, 1H, ArH), 7,60-7,57 (m, 2H, ArH), 7,28-7,21 (m, 3H, ArH), 6,66 (d, J = 3,0 Гц, 1H, ArH), 6,31 (s, 1H, OH), 4,52 (d, J = 14,6 Гц, 1H, CH), 4,32 (d, J = 14,6 Гц, 1H, CH), 1,43 (s, 3H, CH3).
( S )- N -(4-циано-3-(трифторметил)фенил)-3-(3-фтор-1 H -пиразол-1-ил)-2-гидрокси-2-метилпропанамид (C15H12F4N4O2) ( 1012 )
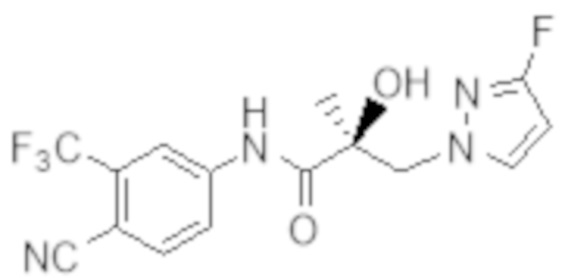
[00344] В раствор 3-фторпиразола (0,20 г, 0,00232 моль) в безводном ТГФ (10 мл), который охлаждали на бане лед-вода, в атмосфере аргона добавляли гидрид натрия (60% дисперсия в масле, 0,24 г, 0,00582 моль). После завершения добавления полученную смесь перемешивали в течение 3 часов. В полученный выше раствор добавляли (R)-3-бром-N-(4-циано-3-(трифторметил)фенил)-2-гидрокси-2-метилпропанамид (8, 0,82 г, 0,00232 моль) и полученную реакционную смесь оставляли перемешиваться на ночь при КТ в атмосфере аргона. Реакцию гасили водой и экстрагировали смесь этилацетатом. Органический слой промывали солевым раствором, сушили MgSO4, фильтровали и концентрировали в вакууме. Продукт очищали на колонке с силикагелем с использованием этилацетата и гексанов (2:1) в качестве элюента с получением 0,36 г соединения в виде белых игольчатых кристаллов.
[00345] Соединение 1012 было охарактеризовано следующим образом: 1H ЯМР (400 МГц, ДМСО-d6) δ 10,39 (s, 1H, NH), 8,47 (d, J = 2,0 Гц, 1H, ArH), 8,24 (dd, J = 8,8 Гц, J = 2,0 Гц, 1H, ArH), 8,11 (d, J = 8,8 Гц, 1H, ArH), 7,55 (t, J = 3,0 Гц, 1H, пиразол-H), 6,29 (s, 1H, OH), 5,93-5,91 (m, 1H, пиразол-H), 4,34 (d, J = 13,6 Гц, 1H, CH), 4,15 (d, J = 13,6 Гц, 1H, CH), 1,36 (s, 3H, CH3); масс-спектр (ИЭР, положительные ионы): 357,0966 [M+H]+.
( S )- N -(4-циано-3-(трифторметил)фенил)-2-гидрокси-2-метил-3-(1 H -пиразол-1-ил)пропанамид (C15H13F3N4O2) ( 1013 )
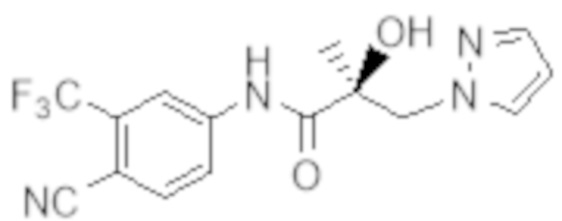
[00346] В раствор 1H-пиразола (0,20 г, 0,002938 моль) в безводном ТГФ (10 мл), который охлаждали на бане лед-вода, в атмосфере аргона добавляли гидрид натрия (60% дисперсия в масле, 0,29 г, 0,007344 моль). После завершения добавления полученную смесь перемешивали в течение 3 часов. В полученный выше раствор добавляли (R)-3-бром-N-(4-циано-3-(трифторметил)фенил)-2-гидрокси-2-метилпропанамид (8, 1,03 г, 0,002938 моль) и полученную реакционную смесь оставляли перемешиваться на ночь при КТ в атмосфере аргона. Реакцию гасили водой и экстрагировали смесь этилацетатом. Органический слой промывали солевым раствором, сушили MgSO4, фильтровали и концентрировали в вакууме. Продукт очищали на колонке с силикагелем с использованием этилацетата и гексанов (2:1) в качестве элюента с получением 0,52 г соединения в виде белого твердого вещества.
[00347] Соединение 1013 было охарактеризовано следующим образом: 1H ЯМР (400 МГц, ДМСО-d6) δ 10,39 (s, 1H, NH), 8,48 (d, J = 2,0 Гц, 1H, ArH), 8,22 (dd, J = 8,2 Гц, J = 2,0 Гц, 1H, ArH), 8,08 (d, J = 8,2 Гц, 1H, ArH), 7,66-7,65 (m, 1H, пиразол-H), 7,39-7,38 (m, 1H, пиразол-H), 6,28 (s, 1H, OH), 6,25-6,23 (m, 1H, пиразол-H), 4,50 (d, J = 13,6 Гц, 1H, CH), 4,29 (d, J = 13,6 Гц, 1H, CH), 1,35 (s, 3H, CH3); масс-спектр (ИЭР, положительные ионы): 339,1105 [M+H]+.
( S )- N -(4-циано-3-(трифторметил)фенил)-2-гидрокси-2-метил-3-(3-(трифторметил)-1 H -пиразол-1-ил)пропанамид (C16H12F6N4O2) ( 1014 )
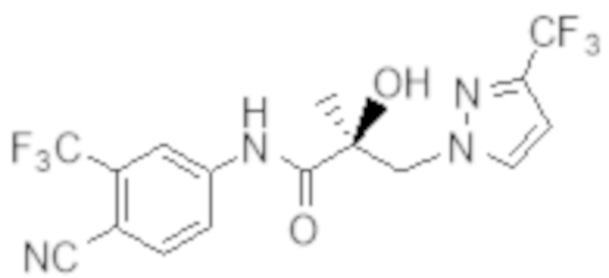
В раствор 3-(трифторметил)пиразола (0,20 г, 0,00147 моль) в безводном ТГФ (10 мл), который охлаждали на бане лед-вода, в атмосфере аргона добавляли гидрид натрия (60% дисперсия в масле, 0,15 г, 0,003674 моль). После завершения добавления полученную смесь перемешивали в течение 3 часов. В полученный выше раствор добавляли (R)-3-бром-N-(4-циано-3-(трифторметил)фенил)-2-гидрокси-2-метилпропанамид (8) (0,516 г, 0,00147 моль) и полученную реакционную смесь оставляли перемешиваться на ночь при КТ в атмосфере аргона. Реакцию гасили водой и экстрагировали смесь этилацетатом. Органический слой промывали солевым раствором, сушили MgSO4, фильтровали и концентрировали в вакууме. Продукт очищали на колонке с силикагелем с использованием этилацетата и гексанов (2:1) в качестве элюента с получением титульного соединения (103 мг, 70%) в виде белого твердого вещества.
Соединение 1014 было охарактеризовано следующим образом: 1H ЯМР (400 МГц, ДМСО-d6) δ 10,31 (шир.s, 1H, NH), 8,42 (d, J = 2,0 Гц, 1H, ArH), 8,19 (dd, J = 8,8, 2,0 Гц, 1H, ArH), 8,09 (d, J = 8,8 Гц, 1H, ArH), 7,83 (d, J = 1,2 Гц, 1H, ArH), 6,67 (d, J = 2,0 Гц, 1H, ArH), 6,41 (шир.s, OH), 4,56 (d, J = 14,0 Гц, 1H, CHH), 4,37 (d, J = 14,0 Гц, 1H, CHH), 1,41 (s, 3H, CH3); 19F ЯМР (CDCl3, развязка) δ -60,44, -61,25; МСВР (ИЭР) m/z, расчет для C16H12F6N4O2: 407,0943 [M + H]+; эксперимент: 407,0943 [M + H]+; Тпл 153-155°C.
( S )- N -(4-циано-3-(трифторметил)фенил)-3-(3-(4-фторфенил)-1 H -пиразол-1-ил)-2-гидрокси-2-метилпропанамид (C21H16F4N4O2) ( 1015 )
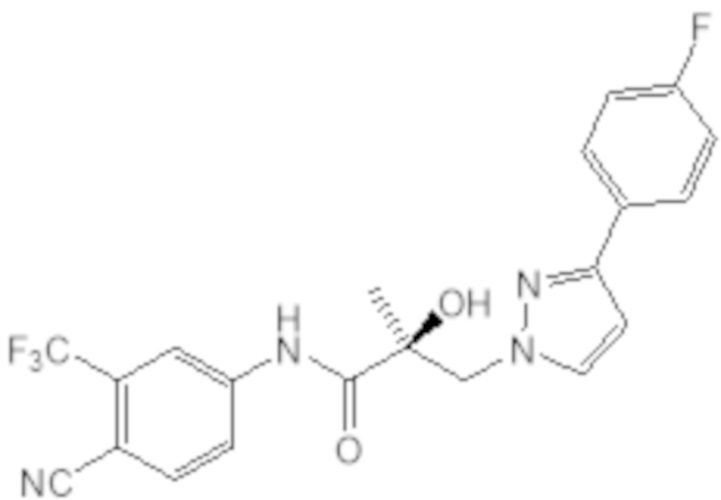
[00348] В раствор 3-(4-фторфенил)пиразола (0,30 г, 0,00185 моль) в безводном ТГФ (10 мл), который охлаждали на бане лед-вода, в атмосфере аргона добавляли гидрид натрия (60% дисперсия в масле, 0,22 г, 0,00555 моль). После завершения добавления полученную смесь перемешивали в течение 3 часов. В полученный выше раствор добавляли (R)-3-бром-N-(4-циано-3-(трифторметил)фенил)-2-гидрокси-2-метилпропанамид (8) (0,65 г, 0,00185 моль) и полученную реакционную смесь оставляли перемешиваться на ночь при КТ в атмосфере аргона. Реакцию гасили водой и экстрагировали смесь этилацетатом. Органический слой промывали солевым раствором, сушили MgSO4, фильтровали и концентрировали в вакууме. Продукт очищали на колонке с силикагелем с использованием этилацетата и гексанов (2:1) в качестве элюента с получением 0,32 г (40%) титульного соединения в виде розоватого твердого вещества.
[00349] Соединение 1015 было охарактеризовано следующим образом: 1H ЯМР (400 МГц, ДМСО-d6) δ 10,30 (s, 1H, NH), 8,41 (d, J = 2,0 Гц, 1H, ArH), 8,21 (dd, J = 8,2 Гц, J = 2,0 Гц, 1H, ArH), 8,05 (d, J = 8,2 Гц, 1H, ArH), 7,68 (d, J = 2,0 Гц, 1H, ArH), 7,64-7,59 (m, 2H, ArH), 7,11-7,05 (m, 2H, ArH), 6,65 (d, J = 3,0 Гц, 1H, ArH), 6,31 (s, 1H, OH), 4,50 (d, J = 13,6 Гц, 1H, CH), 4,30 (d, J = 13,6 Гц, 1H, CH), 1,42 (s, 3H, CH3); масс-спектр (ИЭР, положительные ионы): 433,1312 [M+H]+.
( S )- N -(4-циано-3-(трифторметил)фенил)-2-гидрокси-2-метил-3-морфолинопропанамид (C16H18F3N3O3) ( 1016 )
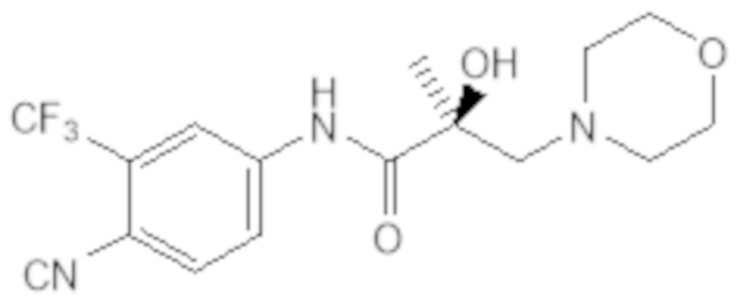
[00350] В атмосфере аргона в раствор 0,09 мл морфолина (0,67 ммоль) в ТГФ (10 мл) медленно добавляли 1,0 мл бис(триметилсилил)амида лития в ТГФ (1 ммоль, Aldrich, 1 M раствор в ТГФ) при -78°C и перемешивали в течение 30 минут при указанной температуре. В раствор по каплям добавляли раствор 8 (234 мг, 0,67 ммоль) в 5 ил ТГФ. Реакционную смесь перемешивали при указанной температуре в течение 30 минут, затем перемешивали в течение ночи при КТ и гасили реакцию путем добавления нас. раствора NH4Cl. Концентрировали смесь при пониженном давлении, диспергировали в избытке EtOAc, сушили над Na2SO4, концентрировали и очищали путем колоночной флэш-хроматографии (EtOAc/гексан) с получением целевого соединения (209 мг, выход 88%) в виде белого твердого вещества.
Соединение 1016 было охарактеризовано следующим образом: 1H ЯМР (CDCl3, 400 МГц) δ 9,36 (шир.s, 1H, NH), 8,08 (d, J = 1,6 Гц, 1H), 7,94 (dd, J = 8,4, 1,6 Гц, 1H), 7,80 (d, J = 8,4 Гц, 1H), 3,68 (m, 4H), 3,28 (d, J = 13,2 Гц, 1H), 2,55 (m, 4H), 2,42 (d, J = 13,2 Гц, 1H), 1,50 (шир.s, 1H, OH), 1,42 (s, 3H); 19F ЯМР (ацетон-d6, 400 МГц) δ -62,20; ЖХМС (ИЭР ) m/z, расчет для C16H19F3N3O3: 358,1379. Эксперимент: 358,1383 [М + Н]+.
(S)-N-(4-циано-3-(трифторметил)фенил)-2-гидрокси-2-метил-3-(4-(трифторметил)-1H-пиразол-1-ил)пропанамид (C16H12F6N4O2) (1017)
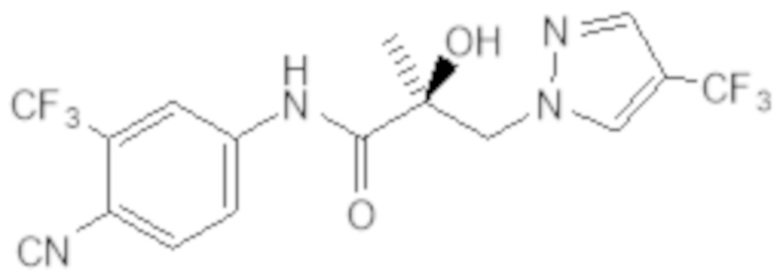
[00351] В раствор 4-(трифторметил)пиразола (0,20 г, 0,00147 моль) в безводном ТГФ (10 мл), который охлаждали на бане лед-вода, в атмосфере аргона добавляли гидрид натрия (60% дисперсия в масле, 0,18 г, 0,004409 моль). После завершения добавления полученную смесь перемешивали в течение 3 часов. В полученный выше раствор добавляли (R)-3-бром-N-(4-циано-3-(трифторметил)фенил)-2-гидрокси-2-метилпропанамид (8) (0,516 г, 0,00147 моль) и полученную реакционную смесь оставляли перемешиваться на ночь при КТ в атмосфере аргона. Реакцию гасили водой и экстрагировали смесь этилацетатом. Органический слой промывали солевым раствором, сушили MgSO4, фильтровали и концентрировали в вакууме. Продукт очищали на колонке с силикагелем с использованием ДХМ и этилацетата (19:1) в качестве элюента с получением 0,30 г (50%) титульного соединения в виде белой пены.
[00352] Соединение 1017 было охарактеризовано следующим образом: 1H ЯМР (400 МГц, ДМСО-d6) δ 10,38 (s, 1H, NH), 8,45 (d, J = 2,0 Гц, 1H, ArH), 8,25-8,22 (m, 2H, ArH и пиразол-H), 8,11 (d, J = 8,2 Гц, 1H, ArH), 7,82 (s, 1H, пиразол-H), 6,39 (s, 1H, OH), 4,55 (d, J = 14,0 Гц, 1H, CH), 4,37 (d, J = 14,0 Гц, 1H, CH), 1,40 (s, 3H, CH3); масс-спектр (ИЭР, положительные ионы): 407,0945 [M+H]+.
Триазолы 1018 и 1019:
( S )- N -(4-циано-3-(трифторметил)фенил)-2-гидрокси-2-метил-3-(1 H -1,2,4-триазол-1-ил)пропанамид (C14H12F3N5O2) ( 1018 )

[00353] В сухой продутой азотом 50 мл круглодонной колбе эпоксид (10, 270 мг, 1 ммоль), 1,2,4-триазол (69 мг, 1 ммоль) и K2CO3 (268 мг, 2 ммоль) диспергировали в 10 мл 2-бутанона (метилэтилкетон (МЭК)). Смесь нагревали до температуры обратной конденсации в течение 12 часов. Полученную смесь охлаждали до КТ. Понижали объем смеси при пониженном давлении, выливали в воду и экстрагировали этилацетатом (3 раза). Органический слой сушили над MgSO4, концентрировали и очищали путем колоночной флэш-хроматографии (этилацетат/гексан, 2:3 (об./об.)) на силикагеле с получением целевого продукта (143 мг, выход 43%). Соединение 1018 было охарактеризовано следующим образом: 1H ЯМР (CDCl3, 400 МГц) δ 9,10 (шир.s, 1H, NH), 8,15 (s, 1H), 8,02 (d, J = 2,0 Гц, 1H), 7,88 (dd, J = 8,4, 2,0 Гц, 1H), 7,78 (d, J = 8,4 Гц, 1H), 5,70 (шир.s, 1H, OH), 4,79 (d, J = 14,0 Гц, 1H), 4,35 (d, J = 14,0 Гц, 1H), 1,53 (s, 3H); 19F ЯМР (CDCl3, 400 МГц) δ -62,22; МСВР (ИЭР) m/z, расчет для C14H12F3N5O2 точная масса: 340,1021 [M + H]+. Эксперимент: 340,1067 [M + H]+.
[00354]
(S)-N-(4-циано-3-(трифторметил)фенил)-2-гидрокси-2-метил-3-(3-(трифторметил)-1H-1,2,4-триазол-1-ил)пропанамид (C15H11F6N5O2) (1019)
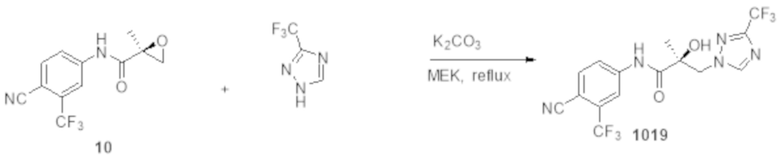
[00355] В сухой продутой азотом 50 мл круглодонной колбе эпоксид (10, 270 мг, 1 ммоль), 3-(трифторметил)-1H-1,2,4-триазол (137 мг, 1 ммоль) и K2CO3 (268 мг, 2 ммоль) диспергировали в 10 мл 2-бутанона (метилэтилкетон или МЭК). Смесь нагревали до температуры обратной конденсации в течение 12 часов. Полученную смесь охлаждали до КТ. Понижали объем смеси при пониженном давлении, выливали в воду и экстрагировали этилацетатом (3 раза). Органический слой сушили над MgSO4, концентрировали и очищали путем колоночной флэш-хроматографии (этилацетат/гексан, 2:3 (об./об.)) на силикагеле с получением целевого продукта (213 мг, выход 53%).
[00356] Соединение 1019 было охарактеризовано следующим образом: 1H ЯМР (ацетон-d6, 400 МГц) δ 9,88 (шир.s, 1H, NH), 9,44 (s, 1H), 8,44 (s, 1H), 8,25 (d, J = 8,4 Гц, 1H), 8,04 (d, J = 8,4 Гц, 1H), 4,82 (d, J = 14,4 Гц, 1H), 4,61 (d, J = 14,4 Гц, 1H), 2,88 (шир.s, 1H, OH), 1,61 (s, 3H); 19F ЯМР (CDCl3, 400 МГц) δ -62,26, -65,25; МСВР (ИЭР) m/z, расчет для C15H11F6N5O2 точная масса: 408,0895 [M + H]+. Эксперимент: 408,0898 [M + H]+.
(R)-N-(4-циано-3-(трифторметил)фенил)-3-(4-фтор-1H-пиразол-1-ил)-2-гидрокси-2-метилпропанамид (C15H12F4N4O2) (1020)
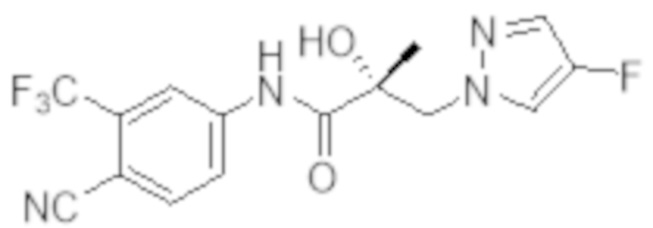
[00357] В раствор 4-фтор-1H-пиразола (0,1 г, 1,16 моль) в безводном ТГФ (10 мл), который охлаждали на ледяной бане, в атмосфере аргона добавляли гидрид натрия (60% дисперсия в минеральном масле, 0,12 г, 2,91 моль). После завершения добавления полученную смесь перемешивали в течение 3 часов. В полученный выше раствор добавляли (S)-3-бром-N-(4-циано-3-(трифторметил)фенил)-2-гидрокси-2-метилпропанамид (S-изомер 8 (8S)*; 0,41 г, 1,16 ммоль) и полученную реакционную смесь оставляли перемешиваться на ночь при КТ в атмосфере аргона. Реакцию гасили водой и экстрагировали смесь этилацетатом. Органический слой промывали солевым раствором, сушили безводным MgSO4, фильтровали и концентрировали при пониженном давлении. Смесь очищали путем колоночной флэш-хроматографии с использованием этилацетата и гексанов (2/3 (об./об.)) в качестве элюента с получением титульного соединения (127 мг, 71%) в виде белого твердого вещества.
[00358] Соединение 1020 было охарактеризовано следующим образом: 1H ЯМР (400 МГц, CDCl3) δ 9,07 (шир.s, 1H, NH), 8,01 (d, J = 2,0 Гц, 1H), 7,95 (dd, J = 8,4, 2,0 Гц, 1H), 7,78 (d, J = 8,4 Гц, 1H), 7,38 (d, J = 4,0 Гц, 1H), 7,34 (d, J = 4,4 Гц, 1H), 5,92 (s, OH), 4,54 (d, J = 14,0 Гц, 1H), 4,16 (d, J = 14,4 Гц, 1H), 1,47 (s, 3H); 19F ЯМР (CDCl3, развязка) δ -62,23, -176,47; МСВР (ИЭР) m/z, расчет для C15H12F4N4O2: 357,0975 [M + H]+; эксперимент: 357,0984 [M + H]+; [α]D24 +126,7 (c = 1,0, MeOH) (сравнение с S-изомером: [α]D24 -136,0° (c = 0,5, MeOH)).
*: 8S синтезировали из L-пролина при помощи того же способа, что и при получении 8 (т.е. R-изомера), описанного на схеме 1.
( S )- N- (4-циано-3-(трифторметил)фенил)-3-(3-фтор-1 H -пиррол-1-ил)-2-гидрокси-2-метилпропанамид (C16H13F4N3O2) (1021 )
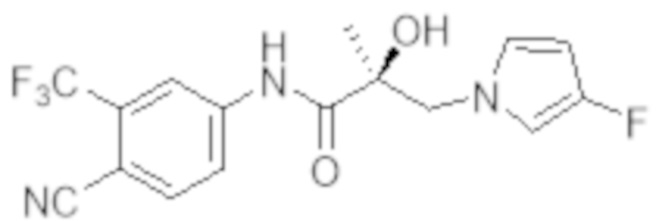
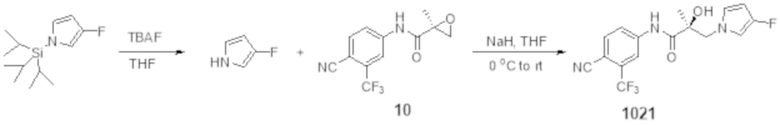
[00359] В раствор 3-фтор-1-(триизопропилсилил)-1H-пиррола (1,21 г, 5 ммоль) в 20 мл безводного ТГФ добавляли фторид н-тетрабутиламмония в тетрагидрофуране (7,5 мл, 7,5 ммоль; 1M) при КТ в атмосфере аргона. Перемешивали раствор в течение 1 часа. Без обработки охлаждали колбу до 0°C на бане лед-вода. В раствор добавляли 60% NaH в минеральном масле (133 мг, 3,33 ммоль). Реакционную смесь перемешивали в течение 30 минут и добавляли эпоксид 10 (450 мг, 1,67 ммоль) в безводном ТГФ через капельную воронку в атмосфере аргона на бане лед-вода и перемешивали в течение ночи при КТ. После гашения 1 мл H2O концентрировали реакционную смесь при пониженном давлении и затем диспергировали в 50 мл EtOAc, промывали водой, выпаривали, сушили над безводным MgSO4 и выпаривали досуха. Смесь очищали путем колоночной флэш-хроматографии с использованием смеси EtOAc/гексан = 1/1 в качестве элюента и затем конденсированные соединения перекристаллизовывали в смеси EtOAc/гексан с получением целевого продукта 1021 (181 мг, 31%) в виде белого твердого вещества.
[00360] Соединение 1021 было охарактеризовано следующим образом: 1H ЯМР (400 МГц, CDCl3) δ 8,91 (шир.s, 1H, NH), 8,03 (d, J = 2,0 Гц, 1H), 7,90 (dd, J = 8,4, 2,0 Гц, 1H), 7,81 (d, J = 8,4 Гц, 1H), 6,47 (m, 1H), 6,41 (m, 1H), 5,91 (dd, J = 2,8, 2,0 Гц, 1H), 4,36 (d, J = 14,4 Гц, 1H), 3,98 (d, J = 14,4 Гц, 1H), 1,54 (s, 3H); 19F ЯМР (CDCl3, развязка) δ -62,18, -164,26; МСВР (ИЭР) m/z, расчет для C16H14F4N3O2: 356,1022 [M + H]+, эксперимент: 356,1021 [M + H]+; 378,0839 [H + Na]+.
( S )- N -(6-циано-5-(трифторметил)пиридин-3-ил)-3-(4-фтор-1 H -пиразол-1-ил)-2-гидрокси-2-метилпропанамид (C14H11F4N5O2) ( 1022 )
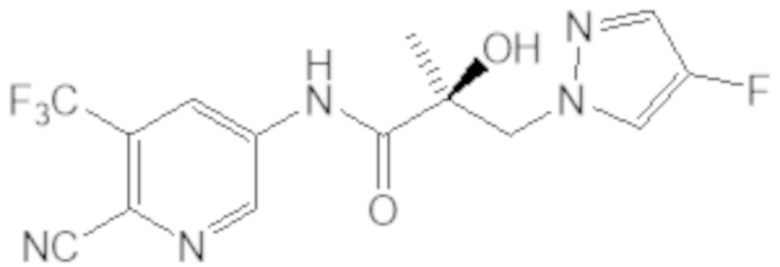
( R )-3-бром- N -(6-циано-5-(трифторметил)пиридин-3-ил)-2-гидрокси-2-метилпропанамид
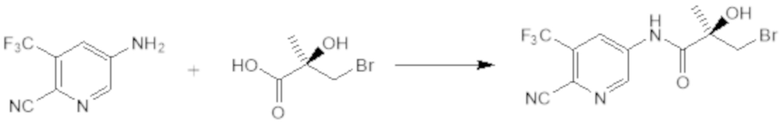
[00361] Проводили взаимодействие (R)-3-бром-2-гидрокси-2-метилпропановой кислоты (4, 1,03 г, 0,005625 моль) с тионилхлоридом (0,80 г, 0,006751 моль), триметиламином (0,74 г, 0,007313 моль) и 5-амино-3-(трифторметил)пиколинонитрилом (1,00 г, 0,005344 моль) с получением титульного соединения. Продукт очищали на колонке с силикагелем с использованием гексанов и этилацетата (2:1) в качестве элюента с получением 1,70 г (90%) титульного соединения в виде желтоватого твердого вещества.
[00362] 1H ЯМР (400 МГц, ДМСО-d6) δ 10,82 (s, 1H, NH), 9,41 (d, J = 2,0 Гц, 1H, ArH), 8,90 (d, J = 2,0 Гц, 1H, ArH), 6,51 (s, 1H, OH), 3,84 (d, J = 10,4 Гц, 1H, CH), 3,61 (d, J = 10,4 Гц, 1H, CH), 1,50 (s, 3H, CH3); масс-спектр (ИЭР, положительные ионы): 351,9915 [M+H]+.
( S )- N -(6-циано-5-(трифторметил)пиридин-3-ил)-3-(4-фтор-1 H -пиразол-1-ил)-2-гидрокси-2-метилпропанамид
[00363] В раствор 4-фторпиразола (0,20 г, 0,0023237 моль) в безводном ТГФ (5 мл), который охлаждали на бане лед-вода, в атмосфере аргона добавляли гидрид натрия (60% дисперсия в масле, 0,28 г, 0,0069711 моль). После завершения добавления полученную смесь перемешивали в течение 3 часов. В полученный выше раствор добавляли (R)-3-бром-N-(6-циано-5-(трифторметил)пиридин-3-ил)-2-гидрокси-2-метилпропанамид (0,82 г, 0,0023237 моль) и полученную реакционную смесь оставляли перемешиваться на ночь при КТ в атмосфере аргона. Реакцию гасили водой и экстрагировали смесь этилацетатом. Органический слой промывали солевым раствором, сушили MgSO4, фильтровали и концентрировали в вакууме. Продукт очищали на колонке с силикагелем с использованием гексанов и этилацетата (1:1) в качестве элюента с получением 0,50 г (60,2%) титульного соединения в виде белого твердого вещества.
[00364] Соединение 1022 было охарактеризовано следующим образом: 1H ЯМР (400 МГц, ДМСО-d6) δ 10,64 (s, 1H, NH), 9,32 (d, J = 2,0 Гц, 1H, ArH), 8,82 (d, J = 2,0 Гц, 1H, ArH), 7,75 (d, J = 4,8 Гц, 1H, пиразол-H), 7,40 (d, J = 4,0 Гц, 1H, пиразол-H), 6,41 (s, 1H, OH), 4,39 (d, J = 14,0 Гц, 1H, CH), 4,22 (d, J = 14,0 Гц, 1H, CH), 1,36 (s, 3H, CH3); (ИЭР, положительные ионы): 358,0939 [M+H]+, 380,0749 [M+Na]+.
( S )-5-(3-(4-фтор-1 H -пиразол-1-ил)-2-гидрокси-2-метилпропанамидо)пиколинамид (C13H14FN5O3) ( 1023 )
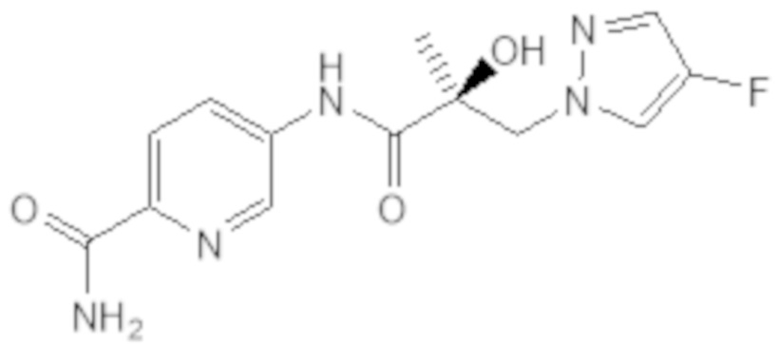
( R )-3-бром- N -(6-цианопиридин-3-ил)-2-гидрокси-2-метилпропанамид
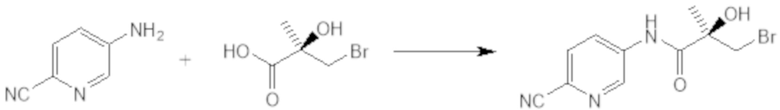
[00365] Проводили взаимодействие (R)-3-бром-2-гидрокси-2-метилпропановой кислоты (4, 3,24 г, 0,017674 моль) с тионилхлоридом (2,53 г, 0,021208 моль), триметиламином (2,33 г, 0,022976 моль) и 5-аминопиколинонитрилом (2,00 г, 0,01679 моль) с получением титульного соединения. Продукт очищали на колонке с силикагелем с использованием дихлорметана (ДХМ) и метанола (19:1) в качестве элюента с получением 4,40 г (92%) титульного соединения в виде желтоватого твердого вещества.
[00366] 1H ЯМР (400 Мгц, ДМСО-d6) δ 10,42 (s, 1H, NH), 9,12 (d, J = 2,4 Гц, 1H, ArH), 8,44 (dd, J = 8,8 Гц, J = 2,4 Гц, 1H, ArH), 8,00 (d, J = 8,8 Гц, 1H, ArH), 6,40 (s, 1H, OH), 3,83 (d, J = 10,4 Гц, 1H, CH), 3,59 (d, J = 10,4 Гц, 1H, CH), 1,49 (s, 3H, CH3); масс-спектр (ИЭР, положительные ионы): 284,0042 [M+H]+.
( S )-5-(3-(4-фтор-1 H -пиразол-1-ил)-2-гидрокси-2-метилпропанамидо)пиколинамид
[00367] В раствор 4-фторпиразола (0,20 г, 0,0023237 моль) в безводном ТГФ (5 мл), который охлаждали на бане лед-вода, в атмосфере аргона добавляли гидрид натрия (60% дисперсия в масле, 0,28 г, 0,0069711 моль). После завершения добавления полученную смесь перемешивали в течение 3 часов. В полученный выше раствор добавляли (R)-3-бром-N-(6-цианопиридин-3-ил)-2-гидрокси-2-метилпропанамид (0,66 г, 0,0023237 моль) и полученную реакционную смесь оставляли перемешиваться на ночь при КТ в атмосфере аргона. Реакцию гасили водой и экстрагировали смесь этилацетатом. Органический слой промывали солевым раствором, сушили MgSO4, фильтровали и концентрировали в вакууме. Продукт очищали на колонке с силикагелем с использованием ДХМ и метанола (9:1) в качестве элюента с получением 0,10 г (15%) титульного соединения в виде белого твердого вещества.
[00368] Соединение 1023 было охарактеризовано следующим образом: 1H ЯМР (400 МГц, ДМСО-d6) δ 10,08 (s, 1H, NH), 8,89 (d, J = 2,4 Гц, 1H, ArH), 8,30 (dd, J = 8,2 Гц, J = 2,4 Гц, 1H, ArH), 8,01 (s, 1H, NH), 7,98 (d, J = 8,2 Гц, 1H, ArH), 7,73 (d, J = 4,4 Гц, 1H, пиразол-H), 7,51 (s, 1H, NH), 7,42 (d, J = 4,0 Гц, 1H, пиразол-H), 6,24 (s, 1H, OH), 4,38 (d, J = 14,0 Гц, 1H, CH), 4,42 (d, J = 14,0 Гц, 1H, CH), 1,34 (s, 3H, CH3); масс-спектр (ИЭР, положительные ионы): 308,1177 [M+H]+, 330,0987 [M+Na]+.
N -(4-циано-3-(трифторметил)фенил)-3-(4-фтор-1 H -пиразол-1-ил)-2-метилпропанамид (C15H12F4N4O) ( 1024 )
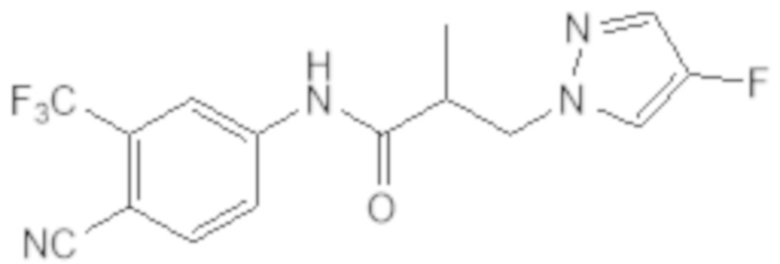
3-бром- N -(4-циано-3-(трифторметил)фенил)-2-метилпропанамид
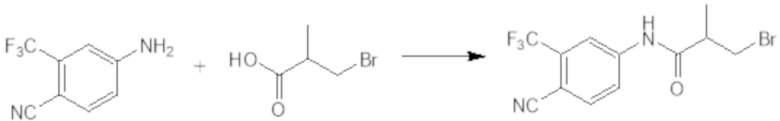
[00369] Проводили взаимодействие 3-бром-2-метилпропановой кислоты (2,00 г, 0,011976 моль) с тионилхлоридом (1,71 г, 0,014371 моль), триметиламином (1,58 г, 0,015569 моль) и 4-амино-2-(трифторметил)бензонитрилом (2,12 г, 0,011377 моль) с получением титульного соединения. Продукт очищали на колонке с силикагелем с использованием гексанов и этилацетата (2:1) в качестве элюента с получением 3,50 г (91%) титульного соединения в виде желтого или светло-коричневого твердого вещества.
[00370] 1H ЯМР (400 МГц, ДМСО-d6) δ 10,85 (s, 1H, NH), 8,30 (s, 1H, ArH), 8,12 (d, J = 8,2 Гц, 1H, ArH), 8,03 (d, J = 8,2 Гц, 1H, ArH), 3,72-3,67 (m, 1H, CH), 3,63-3,59 (m, 1H, CH), 3,03-2,97 (m, 1H, CH), 1,24 (d, J = 6,8 Гц, 3H, CH3); масс-спектр (ИЭР, отрицательные ионы): 334,85 [M-H]-.
N -(4-циано-3-(трифторметил)фенил)-3-(4-фтор-1 H -пиразол-1-ил)-2-метилпропанамид
[00371] В раствор 4-фторпиразола (0,20 г, 0,0023237 моль) в безводном ТГФ (5 мл), который охлаждали на бане лед-вода, в атмосфере аргона добавляли гидрид натрия (60% дисперсия в масле, 0,28 г, 0,0069711 моль). После завершения добавления полученную смесь перемешивали в течение 3 часов. В полученный выше раствор добавляли 3-бром-N-(4-циано-3-(трифторметил)фенил)-2-метилпропанамид (0,78 г, 0,0023237 моль) и полученную реакционную смесь оставляли перемешиваться на ночь при КТ в атмосфере аргона. Реакцию гасили водой и экстрагировали смесь этилацетатом. Органический слой промывали солевым раствором, сушили MgSO4, фильтровали и концентрировали в вакууме. Продукт очищали на колонке с силикагелем с использованием гексанов и этилацетата (1:1) в качестве элюента с получением 0,050 г титульного соединения в виде желтоватого твердого вещества.
[00372] Соединение 1024 было охарактеризовано следующим образом: 1H ЯМР (400 МГц, ДМСО-d6) δ 10,77 (s, 1H, NH), 8,25 (s, 1H, ArH), 8,10 (d, J = 8,2 Hz, 1H, ArH), 7,96 (d, J = 8,2 Гц, 1H, ArH), 7,85 (d, J = 4,4 Гц, 1H, пиразол-H), 7,47 (d, J = 4,4 Гц, 1H, пиразол-H), 4,35-4,30 (m, 1H, CH), 4,12-4,07 (m, 1H, CH), 3,12-3,10 (m, 1H, CH), 1,22 (d, J = 6,8 Гц, 3H, CH3).
[00373] (S)-N-(4-циано-3-(трифторметил)фенил)-3-(4-(4-фторфенил)-1H-пиразол-1-ил)-2-гидрокси-2-метилпропанамид (C21H16F4N4O2) (1025)
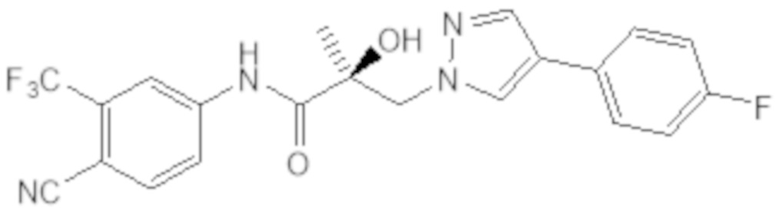
[00374] В раствор 4-(4-фторфенил)-1H-пиразола (0,20 г, 0,0012334 моль) в безводном ТГФ (10 мл), который охлаждали на бане лед-вода, в атмосфере аргона добавляли гидрид натрия (60% дисперсия в масле, 0,15 г, 0,0037001 моль). После завершения добавления полученную смесь перемешивали в течение 3 часов. В полученный выше раствор добавляли (R)-3-бром-N-(4-циано-3-(трифторметил)фенил)-2-гидрокси-2-метилпропанамид (0,43 г, 0,0012334 моль) и полученную реакционную смесь оставляли перемешиваться на ночь при КТ в атмосфере аргона. Реакцию гасили водой и экстрагировали смесь этилацетатом. Органический слой промывали солевым раствором, сушили MgSO4, фильтровали и концентрировали в вакууме. Продукт очищали на колонке с силикагелем с использованием ДХМ и этилацетата (19:1) в качестве элюента с получением 0,33 г (62%) титульного соединения в виде белого твердого вещества.
[00375] Соединение 1025 было охарактеризовано следующим образом: 1H ЯМР (400 МГц, ДМСО-d6) δ 10,29 (s, 1H, NH), 8,41 (s, 1H, ArH), 8,21 (d, J = 8,8 Гц, 1H, ArH), 8,05 (d, J = 8,8 Гц, 1H, ArH), 7,68 (s, 1H, пиразол-H), 7,61 (t, J = 6,4 Гц, 2H, ArH), 7,08 (t, J = 8,4 Гц, 2H, ArH), 6,65 (s, 1H, пиразол-H), 6,30 (s, 1H, OH), 4,51 (d, J = 14,0 Гц, 1H, CH), 4,31 (d, J = 14,0 Гц, 1H, CH), 1,42 (s, 3H, CH3); масс-спектр (ИЭР, отрицательные ионы): 431,12 [M-H]-.
( S )-3-((1 H -1,2,4-триазол-3-ил)амино)- N -(4-циано-3-(трифторметил)фенил)-2-гидрокси-2-метилпропанамид (C14H13F3N6O2) ( 1026 )
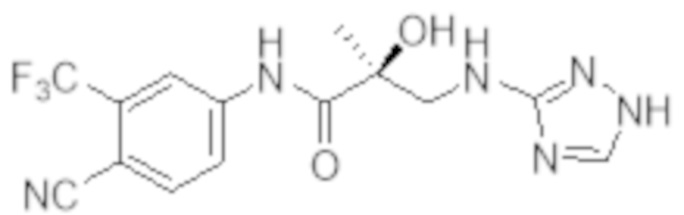

[00376] В атмосфере аргона 100 мл круглодонную колбу охлаждали до 0°C на бане лед-вода. В колбу добавляли 60% NaH в минеральном масле (265 мг, 6,6 ммоль) на бане лед-вода и вливали безводный ТГФ (20 мл) при указанной температуре. В колбу добавляли 3-амино-1,2,4-триазол (164 мг, 2 ммоль) при указанной температуре и перемешивали реакционную смесь в течение 30 минут. Затем через капельную воронку добавляли полученный раствор (R)-3-бром-N-(4-циано-3-(трифторметил)фенил)-2-гидрокси-2-метилпропанамида (8, 702 мг, 2 ммоль) в безводном ТГФ (10 мл) в атмосфере аргона на бане лед-вода и перемешивали в течение ночи при КТ. После гашения 1 мл H2O концентрировали реакционную смесь при пониженном давлении и затем диспергировали в 50 мл EtOAc, промывали водой, выпаривали, сушили над безводным MgSO4 и выпаривали досуха. Смесь очищали путем колоночной флэш-хроматографии с использованием смеси EtOAc/гексан (2:1 (об./об.)) в качестве элюента с получением целевого продукта в виде коричневого твердого вещества.
[00377] Соединение 1026 было охарактеризовано следующим образом: 1H ЯМР (CDCl3, 400 МГц) δ 9,10 (шир.s, 1H, C(O)NH), 8,01 (m, 1H, ArH), 7,87 и 7,81 (dd, J = 8,4, 2,0 Гц, 1H, ArH), 7,78 (d, J = 8,4 Hz, 1H, ArH), 7,72 и 7,51 (s, 1H, ArH), 5,90 и 5,65 (шир.s, 1H, NH), 4,74 (шир.s, 1H, NH), 4,56 и 4,55 (d, J = 14,4 и 13,6 Гц, 1H, CH2), 4,24 (шир.s, 1H, OH), 4,07 и 3,97 (d, J = 13,6 и 14,4 Гц, 1H, CH2), 1,56 и 1,48 (s, 3H, CH3); 19F ЯМР (ацетон-d6, 400 МГц) δ -62,24; МС (ИЭР) m/z 353,03 [M - H]-; 355,10 [M + H]+; МСВР (ИЭР) m/z, расчет для C14H13F3N6O2: 355,1130 [M + H]+, эксперимент: 355,1128 [M + H]+.
Трет -бутил-( S )-(1-(3-((4-циано-3-(трифторметил)фенил)амино)-2-гидрокси-2-метил-3-оксопропил)-1 H -пиразол-4-ил)карбамат (C20H22F3N5O4) ( 1027 )
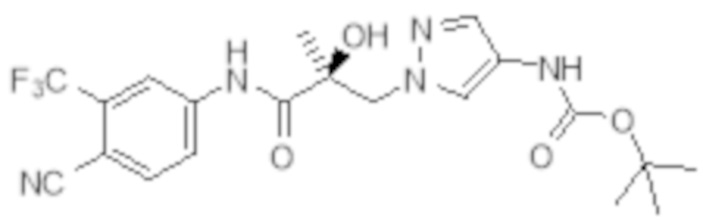
Трет -бутил-1 H -пиразол-4-илкарбамат ( 1027a )
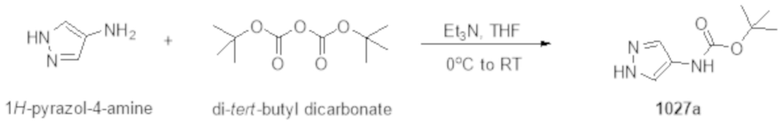
[00378] В атмосфере аргона в раствор 1H-пиразол-4-амина (2 г, 28,9 ммоль) и ди-трет-бутилдикарбоната (6,3 г, 28,9 ммоль) в 100 мл безводного ТГФ добавляли триэтиламин (1,68 мл, 12 ммоль) при 0°C. После перемешивания в течение 30 минут температуру повышали до КТ и перемешивали смесь в течение 2 часов. Реакционную смесь при пониженном давлении и затем диспергировали в 50 мл EtOAc, промывали водой, выпаривали, сушили над безводным MgSO4 и выпаривали досуха. Смесь очищали путем колоночной флэш-хроматографии с использованием смеси EtOAc/гексан в отношении 1:1 (об./об.) в качестве элюента и затем конденсированные соединения перекристаллизовывали с использованием смеси EtOAc/гексан (1:1 (об./об.)) с получением целевого продукта. 1H ЯМР (CDCl3, 400 МГц) δ 7,63 (s, 2H, ArH), 6,29 (шир.s, 1H, NH), 1,51 (s, 9H, C(CH3)3); МС (ИЭР) m/z 182,1 [M - H]-.
( S )- трет -бутил-(1-(3-((4-циано-3-(трифторметил)фенил)амино)-2-гидрокси-2-метил-3-оксопропил)-1 H -пиразол-4-ил)карбамат
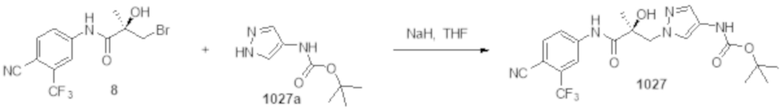
[00379] В атмосфере аргона 100 мл круглодонную колбу охлаждали до 0°C на бане лед-вода. В колбу добавляли 60% NaH в минеральном масле (160 мг, 4 ммоль) на бане лед-вода и вливали безводный ТГФ (20 мл) при указанной температуре. В колбу добавляли трет-бутил-1H-пиразол-4-илкарбамат (1027a, 366 мг, 2 ммоль) при указанной температуре и перемешивали реакционную смесь в течение 30 минут, затем через капельную воронку добавляли полученный раствор (R)-3-бром-N-(4-циано-3-(трифторметил)фенил)-2-гидрокси-2-метилпропанамида (8, 702 мг, 2 ммоль) в безводном ТГФ в атмосфере аргона на бане лед-вода и перемешивали в течение ночи при КТ. После гашения 1 мл H2O концентрировали реакционную смесь при пониженном давлении и затем диспергировали в 50 мл EtOAc, промывали водой, выпаривали, сушили над безводным MgSO4 и выпаривали досуха. Смесь очищали путем колоночной флэш-хроматографии с использованием смеси EtOAc/гексан (2:1 (об./об.)) в качестве элюента с получением целевого продукта (563 мг, 62%) в виде желтоватого твердого вещества.
[00380] Соединение 1027 было охарактеризовано следующим образом: 1H ЯМР (CDCl3, 400 МГц) δ 9,13 (шир.s, 1H, C(O)NH), 8,01 (d, 1H, J = 8,4 Гц, ArH), 7,85 (dd, J = 8,4, 1,6 Гц, 1H, ArH), 7,76 (d, J = 8,4 Гц, 1H, ArH), 7,63 (s, 1H, ArH), 7,43 (s, 1H, ArH), 6,21 (шир.s, 1H, C(O)NH), 6,17 (шир.s, 1H, OH), 4,54 (d, J = 14,0 Гц, 1H, CH2), 4,17 (d, J = 14,0 Гц, 1H, CH2), 1,47 (s, 9H, C(CH3)3), 1,45 (s, 3H, CH3); 19F ЯМР (ацетон-d6, 400 МГц) δ -62,10; МС (ИЭР) m/z 452,11 [M - H]-; 454,06 [M + H]+.
( S )-3-(4-амино-1 H -пиразол-1-ил)- N -(4-циано-3-(трифторметил)фенил)-2-гидрокси-2-метилпропанамид (C15H14F3N5O2) ( 1028 )
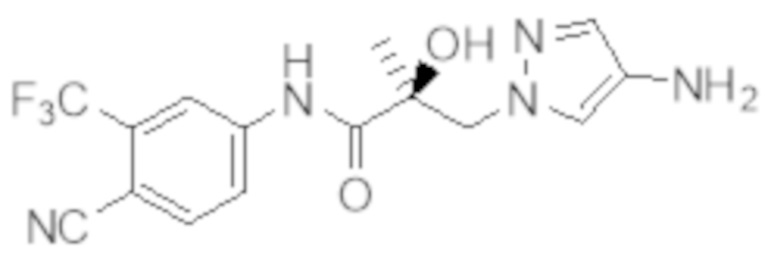
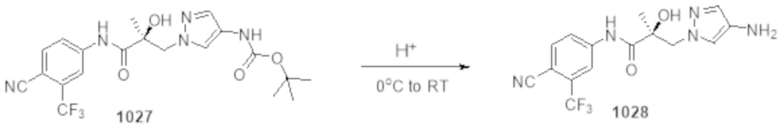
[00381] В атмосфере аргона 100 мл круглодонную колбу охлаждали до 0°C на бане лед-вода. В раствор 1027 (815 мг, 1,80 ммоль) в безводном EtOH (20 мл) по каплям добавляли 5 мл ацетилхлорида на бане лед-вода. Реакционную смесь перемешивали в течение 30 минут при указанной температуре. Концентрировали растворитель при пониженном давлении и затем диспергировали смесь в 50 мл EtOAc, промывали водой, выпаривали, сушили над безводным MgSO4 и выпаривали досуха. Смесь очищали путем колоночной флэш-хроматографии с использованием смесей EtOAc/гексан (в отношениях от 3:1 до 6:1 (об./об.)) в качестве элюента с получением целевого продукта (583 мг, 92%) в виде коричневого твердого вещества.
[00382] Соединение 1028 было охарактеризовано следующим образом: 1H ЯМР (ацетон-d6, 400 МГц) δ 10,07 (шир.s, 1H, C(O)NH), 8,50 (s, 1H, ArH), 8,46 (s, 1H, ArH), 8,26 (d, J = 8,0 Гц, 1H, ArH), 8,01 (d, J = 8,0 Гц, 1H, ArH), 7,83 (s, 1H, ArH), 4,73 (d, J = 14,0 Гц, 1H, CH2), 4,53 (d, J = 14,0 Гц, 1H, CH2), 2,95 (шир.s, 1H, OH), 1,51 (s, 3H, CH3); 19F ЯМР (ацетон-d6, 400 МГц) δ 114,77; МС (ИЭР) m/z 351,98 [M - H]-; 354,08 [M + H]+.
N -(4-циано-3-(трифторметил)фенил)-3-(4-фтор-1 H -пиразол-1-ил)пропанамид (C14H10F4N4O) ( 1029 )
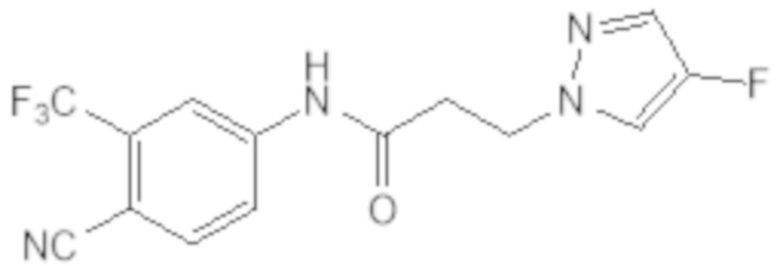
3-бром- N -(4-циано-3-(трифторметил)фенил)пропанамид (C11H8BrF3N2O)
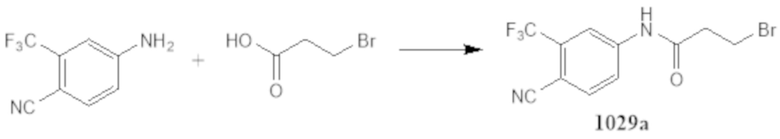
[00383] Проводили взаимодействие 3-бромпропановой кислоты (2,00 г, 0,0130745 моль) с тионилхлоридом (1,87 г, 0,0156894 моль), триметиламином (1,72 г, 0,0169968 моль) и 4-амино-2-(трифторметил)бензонитрилом (2,31 г, 0,0124207 моль) с получением титульного соединения. Продукт очищали на колонке с силикагелем с использованием ДХМ и метанола (19:1) в качестве элюента с получением 2,31 г (55%) титульного соединения в виде желтоватого твердого вещества. 1H ЯМР (400 МГц, ДМСО-d6) δ 10,85 (s, 1H, NH), 8,28 (d, J = 2,4 Гц, 1H, ArH), 8,12 (dd, J = 8,8 Гц, J = 2,4 Гц, 1H, ArH), 7,99 (d, J = 8,8 Гц, 1H, ArH), 3,76 (t, J = 6,0 Гц, 2H, CH2), 3,06 (t, J = 6,0 Гц, 2H, CH2).
N -(4-циано-3-(трифторметил)фенил)-3-(4-фтор-1 H -пиразол-1-ил)пропанамид (C14H10F4N4O)
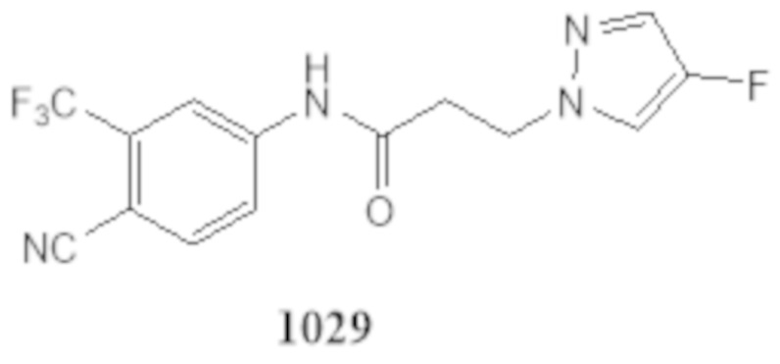
[00384] В раствор 4-фторпиразола (0,20 г, 0,0023237 моль) в безводном ТГФ (5 мл), который охлаждали на бане лед-вода, в атмосфере аргона добавляли гидрид натрия (60% дисперсия в масле, 0,28 г, 0,0069711 моль). После завершения добавления полученную смесь перемешивали в течение 3 часов. В полученный выше раствор добавляли 3-бром-N-(4-циано-3-(трифторметил)фенил)пропанамид (1029a, 0,75 г, 0,0023237 моль) и полученную реакционную смесь оставляли перемешиваться на ночь при КТ в атмосфере аргона. Реакцию гасили водой и экстрагировали смесь этилацетатом. Органический слой промывали солевым раствором, сушили MgSO4, фильтровали и концентрировали в вакууме. Продукт очищали на колонке с силикагелем с использованием ДХМ и метанола (19:1) в качестве элюента с получением 0,75 мг (10%) титульного соединения в виде белого твердого вещества.
[00385] Соединение 1029 было охарактеризовано следующим образом: 1H ЯМР (400 МГц, ДМСО-d6) δ 10,81 (s, 1H, NH), 8,25 (d, J = 2,4 Гц, 1H, ArH), 8,10 (dd, J = 8,8 Гц, J = 2,4 Гц, 1H, ArH), 7,95 (d, J = 8,8 Гц, 1H, ArH), 7,88 (s, 1H, пиразол-H), 7,46 (s, 1H, пиразол-H), 4,35 (t, J = 6,0 Гц, 2H, CH2), 2,79 (t, J = 6,0 Гц, 2H, CH2); масс-спектр (ИЭР, отрицательные ионы): 325,03 [M-H]-.
( S )- трет -бутил-(1-(3-((6-циано-5-(трифторметил)пиридин-3-ил)амино)-2-гидрокси-2-метил-3-оксопропил)-1 H -пиразол-4-ил)карбамат (C19H21F3N6O4) ( 1030 )
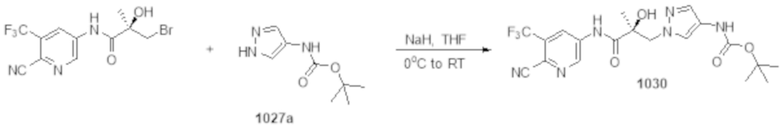
[00386] В атмосфере аргона 50 мл круглодонную колбу охлаждали до 0°C на бане лед-вода. В колбу добавляли 60% NaH в минеральном масле (160 мг, 4 ммоль) на бане лед-вода и вливали безводный ТГФ (10 мл) при указанной температуре. В колбу добавляли трет-бутил-1H-пиразол-4-илкарбамат (1027a, 183 мг, 1 ммоль) при указанной температуре и перемешивали реакционную смесь в течение 30 минут. Затем через капельную воронку добавляли полученный раствор (R)-3-бром-N-(6-циано-5-(трифторметил)пиридин-3-ил)-2-гидрокси-2-метилпропанамида (352 мг, 1 ммоль) в безводном ТГФ в атмосфере аргона на бане лед-вода и перемешивали в течение ночи при КТ. После гашения 1 мл H2O концентрировали реакционную смесь при пониженном давлении и затем диспергировали в 30 мл EtOAc, промывали водой, выпаривали, сушили над безводным MgSO4 и выпаривали досуха. Смесь очищали путем колоночной флэш-хроматографии с использованием смеси EtOAc/гексан в качестве элюента с получением целевого продукта (273 мг, 60%) в виде желтоватого твердого вещества.
[00387] Соединение 1030 было охарактеризовано следующим образом: 1H ЯМР (CDCl3, 400 МГц) δ 9,28 (шир.s, 1H, C(O)NH), 8,80 (s, 1H, ArH), 8,67 (s, 1H, ArH), 7,63 (шир.s, 1H, C(O)NH), 7,43 (s, 1H, ArH), 6,29 (шир.s, 1H, OH), 6,21 (s, 1H, ArH), 4,55 (d, J = 14,0 Гц, 1H, CH2), 4,18 (d, J = 14,0 Гц, 1H, CH2), 1,51 (s, 3H, CH3) 1,47 (s, 9H, C(CH3)3); 19F ЯМР (CDCl3, 400 МГц) δ -62,11; МС (ИЭР) m/z 453,16 [M - H]-; 477,16 [M + Na]+.
( S )-3-(4-ацетамидо-1 H -пиразол-1-ил)- N -(4-циано-3-(трифторметил)фенил)-2-гидрокси-2-метилпропанамид (C17H16F3N5O3) ( 1031 )

[00388] В атмосфере аргона в раствор 1028 (150 мг, 0,43 ммоль) и триэтиламина (0,09 мл, 0,64 ммоль) в 10 мл безводного ДХМ добавляли ацетилхлорид (AcCl, 0,038 мл, 0,53 ммоль) на бане лед-вода. После перемешивания в течение 30 минут температуру повышали до КТ и перемешивали смесь в течение 2 часов. Реакционную смесь при пониженном давлении и затем диспергировали в 10 мл EtOAc, промывали водой, выпаривали, сушили над безводным MgSO4 и выпаривали досуха. Смесь очищали путем колоночной флэш-хроматографии с использованием смеси ацетон/гексан (1/2, (об./об.)) в качестве элюента с получением 1031 (150 мг, 89%) в виде белого твердого вещества.
[00389] Соединение 1031 было охарактеризовано следующим образом: 1H ЯМР (CDCl3, 400 МГц) δ 9,08 (шир.s, 1H, C(O)NH), 7,92 (шир.s, 1H, C(O)NH), 7,82-7,80 (m, 2H, ArH), 7,69 (d, J = 8,4 Гц, 1H, ArH), 7,44 (s, 1H, ArH), 7,15 (s, 1H, ArH), 6,10 (шир.s, 1H, OH), 4,49 (d, J = 13,6 Гц, 1H, CH2), 4,13 (d, J = 13,6 Гц, 1H, CH2), 2,04 (s, 3H, NH(CO)CH3), 1,39 (s, 3H, CH3); 19F ЯМР (CDCl3, 400 МГц) δ -62,20; МС (ИЭР) m/z 394,06 [M - H]-; 396,11 [M + H]+.
( S )-3-(4-амино-1 H -пиразол-1-ил)-1-((4-циано-3-(трифторметил)фенил)амино)-2-метил-1-оксопропан-2-ил-2-хлорацетат (C17H15ClF3N5O3) ( 1032 ); и
( S )-3-(4-(2-хлорацетамидо)-1 H -пиразол-1-ил)- N -(4-циано-3-(трифторметил)фенил)-2-гидрокси-2-метилпропанамид (C17H15ClF3N5O3) ( 1033 )
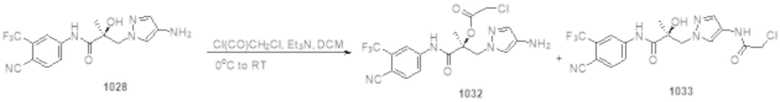
[00390] В атмосфере аргона в раствор 1028 (263 мг, 0,75 ммоль) и триэтиламина (0,16 мл, 1,12 ммоль) в 50 мл безводного ДХМ добавляли хлорацетилхлорид (0,074 мл, 0,94 ммоль) на бане лед-вода. После перемешивания в течение 30 минут температуру повышали до КТ и перемешивали смесь в течение 2 часов. Реакционную смесь при пониженном давлении и затем диспергировали в 30 мл EtOAc, промывали водой, выпаривали, сушили над безводным MgSO4 и выпаривали досуха. Смесь очищали путем колоночной флэш-хроматографии с использованием смеси EtOAc/гексан (3/1 (об./об.)) в качестве элюента с получением 1032 (105 мг, 33%) и 1033 (117 мг, 36%) в виде желтоватых твердых веществ. Общий выход 70%.
Соединение 1032 было охарактеризовано следующим образом: 1H ЯМР (CDCl3, 400 МГц) δ 9,22 (шир.s, NH2), 8,10 (шир.s, 1H, C(O)NH), 7,93 (d, J = 1,8 Гц, 1H, ArH), 7,86 (d, J = 1,8 Гц, 1H, ArH), 7,79 (d, J = 8,4 Гц, 1H, ArH), 5,16 (d, J = 14,8 Гц, 1H, CH2), 4,62 (d, J = 14,8 Гц, 1H, CH2), 4,11 (s, 2H, CH2Cl), 1,77 (s, 3H, CH3); 19F ЯМР (CDCl3, 400 МГц) δ 114,77; МС (ИЭР) m/z 428,03 [M - H]-; 452,02 [M + Na]+.
[00391] Соединение 1033 было охарактеризовано следующим образом: 1H ЯМР (CDCl3, 400 МГц) δ 9,12 (шир.s, 1H, C(O)NH), 8,12 (шир.s, 1H, C(O)NH), 7,99 (d, J = 1,6 Гц, 1H, ArH), 7,92 (s, 1H, ArH), 7,87 (dd, J = 8,8, 1,6 Гц, 1H, ArH), 7,76 (d, J = 8,8 Гц, 1H, ArH), 7,61 (s, 1H, ArH), 6,11 (шир.s, 1H, OH), 4,60 (d, J = 13,6 Гц, 1H, CH2), 4,22 (d, J = 13,6 Гц, 1H, CH2), 4,17 (s, 2H, CH2Cl), 1,47 (s, 3H, CH3); 19F ЯМР (CDCl3, 400 МГц) δ -62,19; МС (ИЭР) m/z 428,00 [M - H]-; 452,01 [M + Na]+.
( S )-метил-(1-(3-((4-циано-3-(трифторметил)фенил)амино)-2-гидрокси-2-метил-3-оксопропил)-1 H -пиразол-4-ил)карбамат (C17H16F3N5O4) ( 1034 )
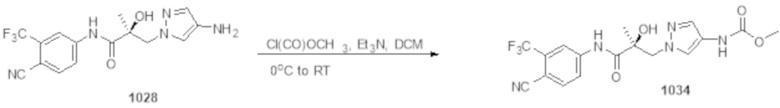
[00392] В атмосфере аргона в раствор 1028 (170 мг, 0,48 ммоль) и триэтиламина (0,16 мл, 1,15 ммоль) в 10 мл безводного ДХМ добавляли метилкарбонохлоридат (0,04 мл, 0,58 ммоль) на бане лед-вода. После перемешивания в течение 30 минут температуру повышали до КТ и перемешивали смесь в течение 2 часов. Реакционную смесь при пониженном давлении и затем диспергировали в 10 мл EtOAc, промывали водой, выпаривали, сушили над безводным MgSO4 и выпаривали досуха. Смесь очищали путем колоночной флэш-хроматографии с использованием смеси EtOAc/гексан (2/1, (об./об.)) в качестве элюента с получением 1034 (141 мг, 71%) в виде белого твердого вещества.
[00393] Соединение 1034 было охарактеризовано следующим образом: 1H ЯМР (CDCl3, 400 МГц) δ 9,07 (шир.s, 1H, C(O)NH), 7,91 (s, 1H, ArH), 7,79 (d, J = 7,2 Гц, 1H, ArH), 7,69 (d, J = 7,2 Гц, 1H, ArH), 7,57 (s, 1H, ArH), 7,40 (s, 1H, ArH), 6,33 (шир.s, 1H, NH), 6,08 (шир.s, 1H, OH), 4,50 (d, J = 13,6 Гц, 1H, CH2), 4,12 (d, J = 13,6 Гц, 1H, CH2), 3,67 (s, 3H, NH(CO)OCH3), 1,39 (s, 3H, CH3); 19F ЯМР (CDCl3, 400 МГц) δ -62,21; МС (ИЭР) m/z 410,30 [M - H]-; 413,21 [M + H]+.
( S )-3-(4-ацетил-1 H -пиразол-1-ил)- N -(4-циано-3-(трифторметил)фенил)-2-гидрокси-2-метилпропанамид (C17H15F3N4O3) ( 1035 )
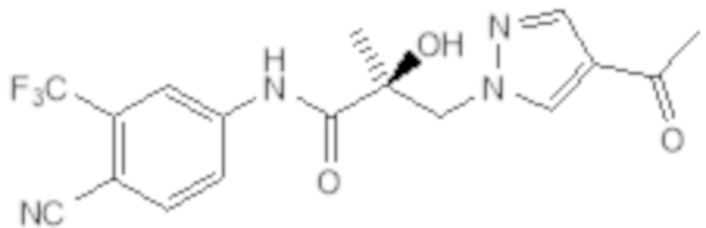
[00394] В раствор 1-(1H-пиразол-4-ил)этанона (0,10 г, 0,000908 моль) в безводном ТГФ (5 мл), который охлаждали на бане лед-вода, в атмосфере аргона добавляли гидрид натрия (60% дисперсия в масле, 0,11 г, 0,002725 моль). После завершения добавления полученную смесь перемешивали в течение 3 часов. В полученный выше раствор добавляли (R)-3-бром-N-(4-циано-3-(трифторметил)фенил)-2-гидрокси-2-метилпропанамид (8, 0,32 г, 0,000908 моль) и полученную реакционную смесь оставляли перемешиваться на ночь при КТ в атмосфере аргона. Реакцию гасили водой и экстрагировали смесь этилацетатом. Органический слой промывали солевым раствором, сушили MgSO4, фильтровали и концентрировали в вакууме. Продукт очищали на колонке с силикагелем с использованием ДХМ и этилацетата (19:1) в качестве элюента с получением 70 мг (20%) титульного соединения в виде желтоватого твердого вещества.
[00395] Соединение 1035 было охарактеризовано следующим образом: 1H ЯМР (400 МГц, ДМСО-d6) δ 10,37 (s, 1H, NH), 8,45 (d, J = 1,2 Гц, 1H, ArH), 8,25 (s, 1H, пиразол-H), 8,23 (d, J = 8,2 Гц, J = 1,2 Гц, 1H, ArH), 8,10 (d, J = 8,2 Гц, 1H, ArH), 7,86 (s, 1H, пиразол-H), 6,37 (s, 1H, OH), 4,50 (d, J = 14,0 Гц, 1H, CH), 4,33 (d, J = 14,0 Гц, 1H, CH), 2,34 (s, 3H, CH3), 1,39 (s, 3H, CH3); масс-спектр (ИЭР, отрицательные ионы): 379,14 [M-H]-; (ИЭР, положительные ионы): 413,18 [M+Na]+.
( S )- N -(4-циано-3-(трифторметил)фенил)-2-гидрокси-2-метил-3-(4-нитро-1 H -пиразол-1-ил)пропанамид (C15H12F3N5O4) ( 1036 )
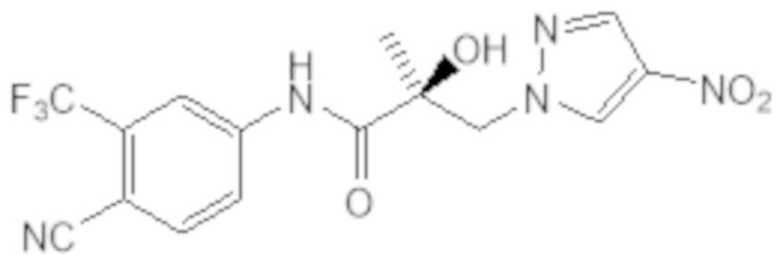
[00396] В раствор 4-нитро-1H-пиразола (0,10 г, 0,0008844 моль) в безводном ТГФ (5 мл), который охлаждали на бане лед-вода, в атмосфере аргона добавляли гидрид натрия (60% дисперсия в масле, 0,106 г, 0,002653 моль). После завершения добавления полученную смесь перемешивали в течение 3 часов. В полученный выше раствор добавляли (R)-3-бром-N-(4-циано-3-(трифторметил)фенил)-2-гидрокси-2-метилпропанамид (8, 0,31 г, 0,0008844 моль) и полученную реакционную смесь оставляли перемешиваться на ночь при КТ в атмосфере аргона. Реакцию гасили водой и экстрагировали смесь этилацетатом. Органический слой промывали солевым раствором, сушили MgSO4, фильтровали и концентрировали в вакууме. Продукт очищали на колонке с силикагелем с использованием гексанов и этилацетата (1:1) в качестве элюента с получением 0,15 г (44%) титульного соединения в виде беловатого твердого вещества.
[00397] Соединение 1036 было охарактеризовано следующим образом: 1H ЯМР (400 МГц, ДМСО-d6) δ 10,36 (s, 1H, NH), 8,69 (s, 1H, пиразол-H), 8,45 (d, J = 1,2 Гц, 1H, ArH), 8,23 (d, J = 8,8 Гц, J = 1,2 Гц, 1H, ArH), 8,19 (s, 1H, пиразол-H), 8,11 (d, J = 8,8 Гц, 1H, ArH), 6,47 (s, 1H, OH), 4,56 (d, J = 14,0 Гц, 1H, CH), 4,38 (d, J = 14,0 Гц, 1H, CH), 1,41 (s, 3H, CH3); масс-спектр (ИЭР, отрицательные ионы): 382,13 [M-H]-.
( R )-3-бром- N -(6-цианопиридин-3-ил)-2-гидрокси-2-метилпропанамид (C10H10BrN3O2) ( 1037 )
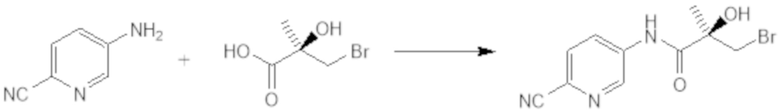
[00398] Проводили взаимодействие (R)-3-бром-2-гидрокси-2-метилпропановой кислоты (4, 3,24 г, 0,017674 моль) с тионилхлоридом (2,53 г, 0,021208 моль), триметиламином (2,33 г, 0,022976 моль) и 5-аминопиколинонитрилом (2,00 г, 0,01679 моль) с получением титульного соединения. Продукт очищали на колонке с силикагелем с использованием ДХМ и метанола (19:1) в качестве элюента с получением 4,40 г (92%) титульного соединения в виде желтоватого твердого вещества.
[00399] Соединение 1037 было охарактеризовано следующим образом: 1H ЯМР (400 МГц, ДМСО-d6) δ 10,42 (s, 1H, NH), 9,12 (d, J = 2,4 Гц, 1H, ArH), 8,44 (dd, J = 8,8 Гц, J = 2,4 Гц, 1H, ArH), 8,00 (d, J = 8,8 Гц, 1H, ArH), 6,40 (s, 1H, OH), 3,83 (d, J = 10,4 Гц, 1H, CH), 3,59 (d, J = 10,4 Гц, 1H, CH), 1,49 (s, 3H, CH3); масс-спектр (ИЭР, положительные ионы): 284,0042 [M+H]+.
( R )-3-бром- N -(6-циано-5-(трифторметил)пиридин-3-ил)-2-гидрокси-2-метилпропанамид (C11H9BrF3N3O2) ( 1038 )
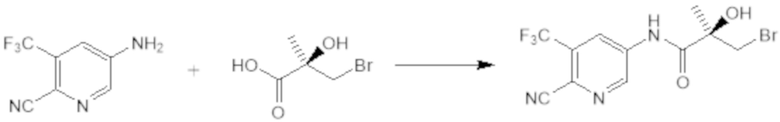
[00400] Проводили взаимодействие (R)-3-бром-2-гидрокси-2-метилпропановой кислоты (4, 1,03 г, 0,005625 моль) с тионилхлоридом (0,80 г, 0,006751 моль), триметиламином (0,74 г, 0,007313 моль) и 5-амино-3-(трифторметил)пиколинонитрилом (1,00 г, 0,005344 моль) с получением титульного соединения. Продукт очищали на колонке с силикагелем с использованием гексанов и этилацетата (2:1) в качестве элюента с получением 1,70 г (90%) титульного соединения в виде желтоватого твердого вещества.
[00401] Соединение 1038 было охарактеризовано следующим образом: 1H ЯМР (400 МГц, ДМСО-d6) δ 10,82 (s, 1H, NH), 9,41 (d, J = 2,0 Гц, 1H, ArH), 8,90 (d, J = 2,0 Гц, 1H, ArH), 6,51 (s, 1H, OH), 3,84 (d, J = 10,4 Гц, 1H, CH), 3,61 (d, J = 10,4 Гц, 1H, CH), 1,50 (s, 3H, CH3); масс-спектр (ИЭР, положительные ионы): 351,9915 [M+H]+.
( R )-3-бром-2-гидрокси-2-метил- N -(хиназолин-6-ил)пропанамид (C12H12BrN3O2) ( 1039 )
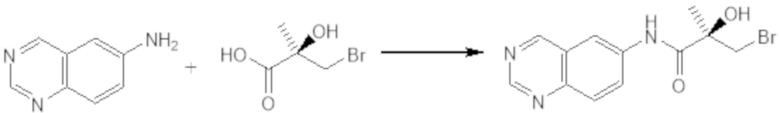
[00402] Проводили взаимодействие (R)-3-бром-2-гидрокси-2-метилпропановой кислоты (2,65 г, 0,014503 моль) с тионилхлоридом (2,07 г, 0,017404 моль), триметиламином (1,91 г, 0,018854 моль) и хиназолин-6-амином (2,00 г, 0,013778 моль) с получением титульного соединения. Продукт очищали на колонке с силикагелем с использованием гексанов и этилацетата (от 3:1 до 2:1) в качестве элюента с получением 0,71 г титульного соединения в виде желтоватого твердого вещества.
[00403] Соединение 1039 было охарактеризовано следующий образом: масс-спектр (ИЭР, положительные ионы) 309,98 [M+H]+.
3-бром- N -(4-циано-3-(трифторметил)фенил)пропанамид (C11H8BrF3N2O) ( 1040 )
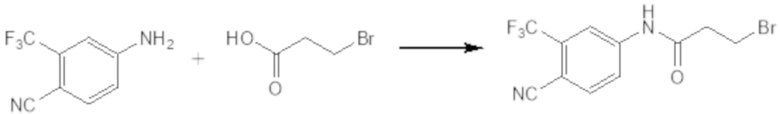
[00404] Проводили взаимодействие 3-бромпропановой кислоты (2,00 г, 0,0130745 моль) с тионилхлоридом (1,87 г, 0,0156894 моль), триметиламином (1,72 г, 0,0169968 моль) и 4-амино-2-(трифторметил)бензонитрилом (2,31 г, 0,0124207 моль) с получением титульного соединения. Продукт очищали на колонке с силикагелем с использованием ДХМ и метанола (19:1) в качестве элюента с получением 2,31 г (55%) титульного соединения в виде желтоватого твердого вещества.
[00405] Соединение 1040 было охарактеризовано следующим образом: 1H ЯМР (400 МГц, ДМСО-d6) δ 10,85 (s, 1H, NH), 8,28 (d, J = 2,4 Гц, 1H, ArH), 8,12 (dd, J = 8,8 Гц, J = 2,4 Гц, 1H, ArH), 7,99 (d, J = 8,8 Гц, 1H, ArH), 3,76 (t, J = 6,0 Гц, 2H, CH2), 3,06 (t, J = 6,0 Гц, 2H, CH2).
( S )- N -(2-хлорпиридин-4-ил)-3-(4-фтор-1 H -пиразол-1-ил)-2-гидрокси-2-метилпропанамид (C12H12ClFN4O2) ( 1041 )
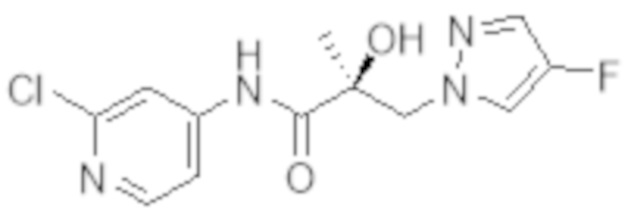
( R )-3-бром- N -(2-хлорпиридин-4-ил)-2-гидрокси-2-метилпропанамид
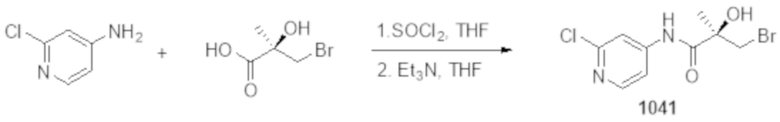
[00406] В охлажденный раствор (менее 4°C) (R)-3-бром-2-гидрокси-2-метилпропановой кислоты (4, 18,3 г, 0,100 моль) в 100 мл ТГФ по каплям добавляли тионилхлорид (11,2 мл, 0,154 моль) в атмосфере аргона. Полученную смесь перемешивали в течение 3 ч в тех же условиях. В смесь добавляли Et3N (25,7 мл, 0,185 моль) и перемешивали в течение 20 минут в тех же условиях. Через 20 минут добавляли 2-хлорпиридин-4-амин (9,89 г, 0,077 моль), 100 мл ТГФ и затем оставляли смесь перемешиваться на ночь при КТ. Удаляли растворитель при пониженном давлении с получением твердого вещества, которое обрабатывали 100 мл H2O и экстрагировали EtOAc (2 × 50 мл). Объединенные органические экстракты промывали насыщенным раствором NaHCO3 (2 × 100 мл) и солевым раствором (100 мл). Органический слой сушили над MgSO4 и концентрировали при пониженном давлении с получением твердого вещества, которое растворяли и очищали путем колоночной хроматографии с использованием CH2Cl2/EtOAc (80:20) с получением твердого вещества. Полученное твердое вещество перекристаллизовывали из смеси CH2Cl2/гексан с получением 12,6 г (43%) (R)-3-бром-N-(2-хлорпиридин-4-ил)-2-гидрокси-2-метилпропанамида в виде светло-желтого твердого вещества. 1H ЯМР (400 МГц, CDCl3) δ 9,06 (шир.s, 1H, NH), 8,31 (d, J = 5,6 Гц, 1H), 7,77 (d, J = 0,8 Гц, 1H), 7,45 (dd, J = 5,6, 0,8 Гц, 1H), 4,81 (шир.s, 1H, OH), 3,97 (d, J = 10,6 Гц, 1H), 3,60 (d, J = 10,6 Гц, 1H), 1,64 (s, 3H); МС (ИЭР) m/z 295,28 [M + H] +.
( S )- N -(2-хлорпиридин-4-ил)-3-(4-фтор-1 H -пиразол-1-ил)-2-гидрокси-2-метилпропанамид (C12H12ClFN4O2)
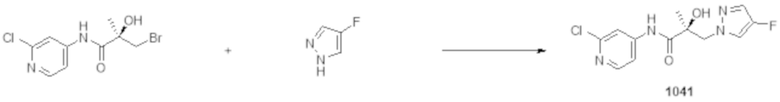
[00407] В сухой продутой азотом 100 мл круглодонной колбе, оборудованной капельной воронкой, в атмосфере аргона в 10 мл безводного растворителя ТГФ добавляли 60% дисперсию NaH в минеральном масле (96 мг, 2,4 ммоль) на бане лед-вода. Добавляли 4-фтор-1H-пиразол (103 мг, 1,2 ммоль) и перемешивали раствор в течение 30 минут на бане лед-вода. В колбу через капельную воронку добавляли раствор (R)-3-бром-N-(2-хлорпиридин-4-ил)-2-гидрокси-2-метилпропанамида (293 мг, 1,0 ммоль) в 5 мл безводного ТГФ в атмосфере аргона на бане лед-вода и перемешивали в течение ночи при КТ. После добавления 1 мл H2O концентрировали реакционную смесь при пониженном давлении и затем диспергировали в 50 мл EtOAc, промывали 50 мл (×2) воды, выпаривали, сушили над безводным MgSO4 и выпаривали досуха. Смесь очищали путем колоночной флэш-хроматографии с использованием смеси EtOAc/гексан в отношении 1:2 в качестве элюента с получением титульного соединения (55%) в виде белого твердого вещества.
[00408] Соединение 1041 было охарактеризовано следующим образом: 1H ЯМР (400 МГц, CDCl3) δ 8,90 (шир.s, 1H, NH), 8,26 (d, J = 5,6 Гц, 1H), 7,63 (s, 1H), 7,75 (d, J = 4,2 Гц, 1H), 7,33 (d, J = 4,2 Гц, 1H), 7,31 (dd, J = 5,6, 1,2 Гц, 1H), 5,88 (s, 1H, OH), 4,53 (d, J = 13,6 Гц, 1H), 4,14 (d, J = 13,6 Гц, 1H), 1,45 (s, 3H); 19F ЯМР (CDCl3, развязка) δ -176,47; МС (ИЭР) m/z 298,98 [M + H] +; 296,96 [M - H]-.
( S )-3-азидо- N -(4-циано-3-(трифторметил)фенил)-2-гидрокси-2-метилпропанамид (C12H10F3N5O2) ( 1042 )
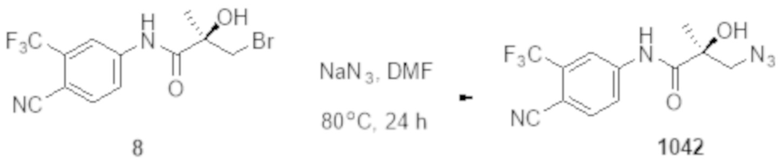
[00409] Раствор 8 (351 мг, 1 ммоль) в ДМФ (10 мл) обрабатывали NaN3 (325 мг, 5 ммоль) в атмосфере аргона при 80°C в течение 24 часов. Затем охлаждали реакционную смесь и экстрагировали CH2Cl2 (3 × 20 мл). Объединенные органические слои промывали H2O (3 × 20 мл) и солевым раствором, сушили и выпаривали с получением неочищенного маслянистого вещества, которое очищали путем хроматографии на силикагеле (EtOAc/н-гексан= 1:2 (об./об.)) с получением титульного соединения в виде желтого твердого вещества (224 мг, 72%).
Соединение 1042 было охарактеризовано следующим образом: 1H ЯМР (400 МГц, CDCl3) δ 9,00 (шир.s, 1H, NH), 8,08 (s, 1H), 7,95 (d, J = 8,4 Гц, 1H), 7,81 (d, J = 8,4 Гц, 1H), 3,92 (d, J = 12,4 Гц, 1H), 3,50 (d, J = 12,4 Гц, 1H), 2,96 (s, 1H, OH), 1,54 (s, 3H); 19F ЯМР (CDCl3, развязка) δ -62,21; МС (ИЭР) m/z 314,03 [M + H] +; 312,18 [M - H] -.
( S )- N -(6-циано-5-(трифторметил)пиридин-3-ил)-2-гидрокси-2-метил-3-(4-(трифторметил)-1 H -пиразол-1-ил)пропанамид (C15H11F6N5O2) ( 1043 )
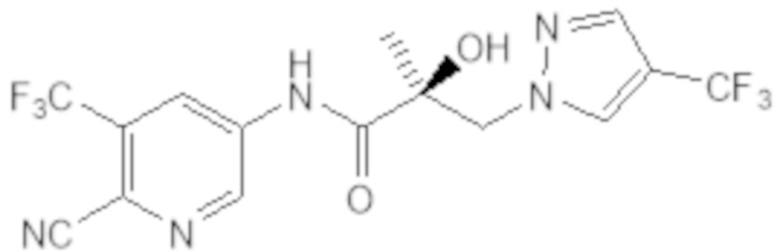
[00410] В раствор 4-(трифторметил)пиразола (0,10 г, 0,0007349 моль) в безводном ТГФ (5 мл), который охлаждали на бане лед-вода, в атмосфере аргона добавляли гидрид натрия (60% дисперсия в масле, 0,09 г, 0,002025 моль). После завершения добавления полученную смесь перемешивали в течение 3 часов. В полученный выше раствор добавляли (R)-3-бром-N-(6-циано-5-(трифторметил)пиридин-3-ил)-2-гидрокси-2-метилпропанамид (0,26 г, 0,0007349 моль) и полученную реакционную смесь оставляли перемешиваться на ночь при КТ в атмосфере аргона. Реакцию гасили водой и экстрагировали смесь этилацетатом. Органический слой промывали солевым раствором, сушили MgSO4, фильтровали и концентрировали в вакууме. Продукт очищали на колонке с силикагелем с использованием ДХМ и этилацетата (19:1) в качестве элюента с получением 0,18 г (60%) титульного соединения в виде белого твердого вещества.
Соединение 1043 было охарактеризовано следующим образом: 1H ЯМР (400 МГц, ДМСО-d6) δ 10,63 (s, 1H, NH), 9,31 (s, 1H, ArH), 8,80 (s, 1H, ArH), 8,32 (s, 1H, пиразол-H), 7,81 (s, 1H, пиразол-H), 6,48 (s, 1H, OH), 4,55 (d, J = 14,0 Гц, 1H, CH), 4,37 (d, J = 14,0 Гц, 1H, CH), 1,42 (s, 3H, CH3); масс-спектр (ИЭР, отрицательные ионы): 406,08 [M-H]-; (ИЭР, положительные ионы): [M+H]+, 430,13 [M+Na]+.
( S )- N -(4-циано-3-(трифторметил)фенил)-3-(5-(4-фторфенил)-1 H -1,2,3-триазол-1-ил)-2-гидрокси-2-метилпропанамид (C20H15F4N5O2) ( 1044 )
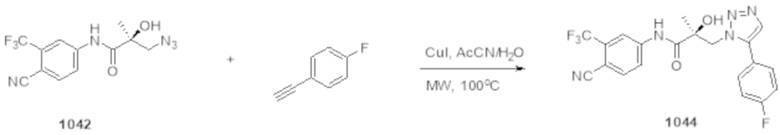
[00411] Смесь 1042 (57 мг, 0,18 ммоль), 1-этинил-4-фторбензола (0,015 мл, 0,18 ммоль)и йодида меди (11 мг, 0,055 ммоль) в AcCN/H2O (1/0,5 мл) помещали в сосуд с крышкой. Реакционный сосуд помещали в реакционный блок в микроволновом реакторе. Дважды проводили программируемый цикл, включавший микроволновое (МВ) облучение в течение 30 минут (300 Вт) при 100°C и 25-минутный перерыв (охлаждение вентилятором), так как исходные вещества присутствовали на ТСХ после проведения первого цикла (общее время облучения, 60 минут). Смесь переносили в круглодонную колбу для концентрирования при пониженном давлении и выливали в EtOAc, затем промывали водой и сушили над MgSO4, концентрировали и очищали путем хроматографии на силикагеле (EtOAc/гексан = 2:1) с получением титульного соединения в виде желтого твердого вещества (69,8 мг, 90%).
[00412] Соединение 1044 было охарактеризовано следующим образом: 1H ЯМР (400 МГц, ацетон-d6) δ 9,00 (шир.s, 1H, NH), 8,44 (s, 1H), 8,30 (s, 1H), 8,25 (d, J = 8,4 Гц, 1H), 8,02 (d, J = 8,4 Гц, 1H), 7,89 (dd, J = 8,0, 2,4 Гц, 2H), 7,20 (d, J = 8,8 Гц, 2H), 5,67 (s, 1H, OH), 4,92 (d, J = 14,0 Гц, 1H), 4,72 (d, J = 14,0 Гц, 1H), 1,60 (s, 3H); 19F ЯМР (ацетон-d6, развязка) δ 114,68, 61,64; МС (ИЭР) m/z 432,11 [M - H] - 434,08 [M + H] +. Различия в структуре 1044 по сравнению с его изомером 1045 (см. ниже) определяли способами 2D ЯМР NOESY и COSY.
( S )- N -(4-циано-3-(трифторметил)фенил)-3-(4-(4-фторфенил)-1 H -1,2,3-триазол-1-ил)-2-гидрокси-2-метилпропанамид (C20H15F4N5O2) ( 1045 )
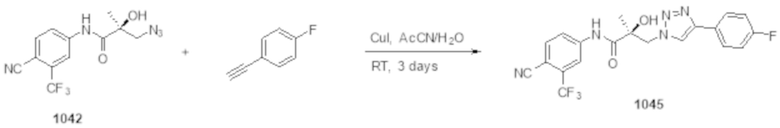
[00413] В суспензию йодида меди (I) (11 мг, 0,055 ммоль) в смеси ацетонитрил (7 мл)/вода (3 мл) добавляли 1042 (57 мг, 0,182 ммоль) при КТ и затем добавляли 1-этинил-4-фторбензол (0,015 мл, 0,182 ммоль). Полученную реакционную смесь перемешивали при КТ в течение 3 дней. Выпаривали смесь при пониженном давлении, выливали в смесь вода:солевой раствор (1:1, (об./об.)) и затем экстрагировали этилацетатом. Затем промывали объединенные органические экстракты солевым раствором, сушили над сульфатом натрия, фильтровали и упаривали. Проводили очистку путем хроматографии (оксид кремния, 60% этилацетат в гексане) с получением желтого твердого вещества (51,3 мг, 65%).
[00414] Соединение 1045 было охарактеризовано следующим образом: 1H ЯМР (400 МГц, CDCl3) δ 9,07 (шир.s, 1H, NH), 7,82-7,80 (m, 1H), 7,79 (s, 1H), 7,76-7,74 (m, 2H), 7,72 (dd, J = 8,2, 2,8 Гц, 2H), 7,10 (t, J = 8,8 Гц, 2H), 5,15 (шир.s, 1H, OH), 4,96 (d, J = 14,0 Гц, 1H), 4,61 (d, J = 14,0 Гц, 1H), 1,62 (s, 3H); 19F ЯМР (CDCl3, развязка) δ -62,24, -112,36; МС (ИЭР) m/z 432,17 [M - H] - 434,09 [M + H]+. Различия в структуре 1045 по сравнению с его изомером 1044 (см. выше) определяли способами 2D ЯМР NOESY и COSY. Например, на спектре 1045 имеется кросс-пик NOE для метиленового протона и триазольного протона, который указывает на то, что эти протоны расположены на расстоянии ~4,5 Å друг от друга, это выполняется для 1045, но не 1044. Этот кросс-пик не наблюдали для 1044.
( S )-3-(4-фтор-1 H -пиразол-1-ил)-2-гидрокси-2-метил- N -(4-нитро-3-(трифторметил)фенил)-пропанамид (C14H12F4N4O4) ( 1046 )

[00415] В сухую продутую азотом 100 мл круглодонную колбу, оборудованную капельной воронкой, содержащую 4-фтор-1H-пиразол (691 мг, 8,03 ммоль), в атмосфере аргона добавляли 60% дисперсию NaH в минеральном масле (674 мг, 16,9 ммоль) а 60 мл безводного растворителя ТГФ на бане лед-вода. Смесь перемешивали в течение 30 минут на бане лед-вода. В колбу через капельную воронку добавляли раствор (R)-3-бром-2-гидрокси-2-метил-N-(4-нитро-3-(трифторметил)фенил)пропанамида (2,98 г, 8,03 ммоль) в 10 мл безводного ТГФ в атмосфере аргона на бане лед-вода и перемешивали в течение ночи при КТ. После добавления 1 мл H2O концентрировали реакционную смесь при пониженном давлении и затем диспергировали в 50 мл EtOAc, промывали 50 мл (x2) воды, выпаривали, сушили над безводным MgSO4 и выпаривали досуха. Смесь очищали путем колоночной флэш-хроматографии с использованием смеси EtOAc/гексан в отношении 1:2 в качестве элюента с получением титульного соединения (2,01 г, 67%) в виде желтого твердого вещества.
[00416] Соединение 1046 было охарактеризовано следующим образом: 1H ЯМР (400 МГц, CDCl3) δ 9,14 (шир.s, 1H, NH), 8,01 (s, 1H), 7,97-7,91 (m, 2H), 7,38 (d, J = 3,6 Гц, 1H), 7,35 (d, J = 4,4 Гц, 1H), 5,95 (s, 1H, OH), 4,56 (d, J = 14,0 Гц, 1H), 4,17 (d, J = 14,0 Гц, 1H), 1,48 (s, 3H); 19F ЯМР (CDCl3, развязка) δ -60,13, -176,47; МС (ИЭР) m/z 375,08 [M - H] -; 377,22 [M + H] +; 399,04 [M + Na] +.
( S )- N -(4-циано-3-(трифторметил)фенил)-2-гидрокси-3-(4-йод-1 H -пиразол-1-ил)-2-метилпропанамид (C15H12F3IN4O2) ( 1047 )
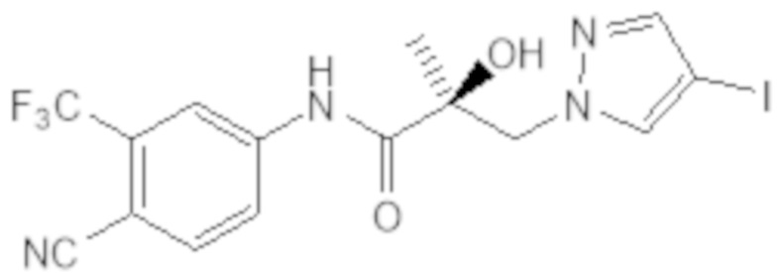
[00417] В раствор 4-йод-1H-пиразола (0,20 г, 0,001031 моль) в безводном ТГФ (5 мл), который охлаждали на бане лед-вода, в атмосфере аргона добавляли гидрид натрия (60% дисперсия в масле, 0,124 г, 0,003093 моль). После завершения добавления полученную смесь перемешивали в течение 3 часов. В полученный выше раствор добавляли (R)-3-бром-N-(4-циано-3-(трифторметил)фенил)-2-гидрокси-2-метилпропанамид (8, 0,36 г, 0,001031 моль) и полученную реакционную смесь оставляли перемешиваться на ночь при КТ в атмосфере аргона. Реакцию гасили водой и экстрагировали смесь этилацетатом. Органический слой промывали солевым раствором, сушили MgSO4, фильтровали и концентрировали в вакууме. Продукт очищали на колонке с силикагелем с использованием ДХМ и этилацетата (19:1) в качестве элюента с получением 0,25 г (52%) титульного соединения в виде беловатого твердого вещества.
Соединение 1047 было охарактеризовано следующим образом: 1H ЯМР (400 МГц, ДМСО-d6) δ 10,36 (s, 1H, NH), 8,45 (s, 1H, ArH), 8,23 (d, J = 8,8 Гц, J = 1,2 Гц, 1H, ArH), 8,10 (d, J = 8,8 Гц, 1H, ArH), 7,78 (s, 1H, пиразол-H), 7,46 (s, 1H, пиразол-H), 6,31 (s, 1H, OH), 4,48 (d, J = 14,0 Гц, 1H, CH), 4,31 (d, J = 14,0 Гц, 1H, CH), 1,35 (s, 3H, CH3); масс-спектр (ИЭР, отрицательные ионы): 463,18 [M-H]-; (ИЭР, положительные ионы): 486,96 [M+Na]+.
( S )-3-(4-циано-1 H -пиразол-1-ил)- N -(4-циано-3-(трифторметил)фенил)-2-гидрокси-2-метилпропанамид (C16H12F3N5O2) ( 1048 )
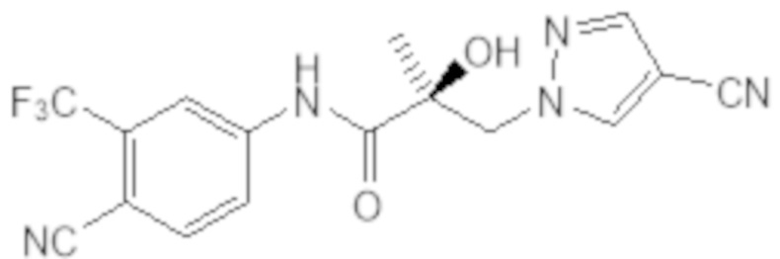
[00418] В раствор 1H-пиразол-4-карбонитрила (0,10 г, 0,001074 моль) в безводном ТГФ (5 мл), который охлаждали на бане лед-вода, в атмосфере аргона добавляли гидрид натрия (60% дисперсия в масле, 0,11 г, 0,003223 моль). После завершения добавления полученную смесь перемешивали в течение 3 часов. В полученный выше раствор добавляли (R)-3-бром-N-(4-циано-3-(трифторметил)фенил)-2-гидрокси-2-метилпропанамид (8, 0,377 г, 0,001074 моль) и полученную реакционную смесь оставляли перемешиваться на ночь при КТ в атмосфере аргона. Реакцию гасили водой и экстрагировали смесь этилацетатом. Органический слой промывали солевым раствором, сушили MgSO4, фильтровали и концентрировали в вакууме. Продукт очищали на колонке с силикагелем с использованием гексана и этилацетата (от 1:1 до 1:2) в качестве элюента с получением 0,18 г (46%) титульного соединения в виде белого твердого вещества.
Соединение 1048 было охарактеризовано следующим образом: 1H ЯМР (400 МГц, ДМСО-d6) δ 10,35 (s, 1H, NH), 8,45 (d, J = 1,2 Гц, 1H, ArH), 8,43 (s, 1H, пиразол-H), 8,22 (d, J = 8,8 Гц, J = 1,2 Гц, 1H, ArH), 8,10 (d, J = 8,8 Гц, 1H, ArH), 7,98 (s, 1H, пиразол-H), 6,41 (s, 1H, OH), 4,45 (d, J = 14,0 Гц, 1H, CH), 4,36 (d, J = 14,0 Гц, 1H, CH), 1,38 (s, 3H, CH3); масс-спектр (ИЭР, отрицательные ионы): 362,11 [M-H]-; (ИЭР, положительные ионы): 386,07 [M+Na]+.
( S )-3-(4-хлор-1 H -пиразол-1-ил)- N -(4-циано-3-(трифторметил)фенил)-2-гидрокси-2-метилпропанамид (C15H12ClF3N4O2) ( 1049 )
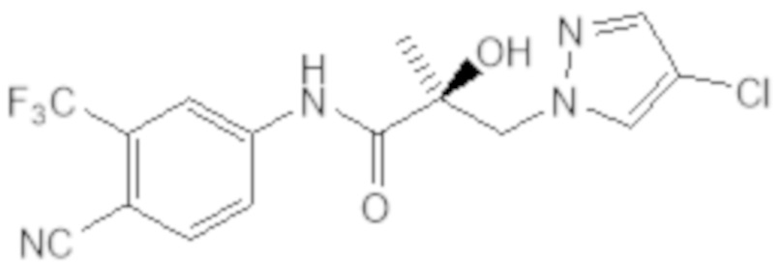
[00419] В раствор 4-хлор-1H-пиразола (0,15 г, 0,001463 моль) в безводном ТГФ (5 мл), который охлаждали на бане лед-вода, в атмосфере аргона добавляли гидрид натрия (60% дисперсия в масле, 0,18 г, 0,004389 моль). После завершения добавления полученную смесь перемешивали в течение 3 часов. В полученный выше раствор добавляли (R)-3-бром-N-(4-циано-3-(трифторметил)фенил)-2-гидрокси-2-метилпропанамид (8, 0,51 г, 0,001463 моль) и полученную реакционную смесь оставляли перемешиваться на ночь при КТ в атмосфере аргона. Реакцию гасили водой и экстрагировали смесь этилацетатом. Органический слой промывали солевым раствором, сушили MgSO4, фильтровали и концентрировали в вакууме. Продукт очищали на колонке с силикагелем с использованием дихлорметана и этилацетата (19:1) в качестве элюента с получением 0,30 г (55%) титульного соединения в виде белого твердого вещества.
[00420] Соединение 1049 было охарактеризовано следующим образом: 1H ЯМР (400 МГц, ДМСО-d6) δ 10,38 (s, 1H, NH), 8,46 (s, 1H, ArH), 8,23 (d, J = 8,6 Гц, J = 1,2 Гц, 1H, ArH), 8,10 (d, J = 8,6 Гц, 1H, ArH), 7,83 (s, 1H, пиразол-H), 7,47 (s, 1H, пиразол-H), 6,34 (s, 1H, OH), 4,45 (d, J = 14,0 Гц, 1H, CH), 4,27 (d, J = 14,0 Гц, 1H, CH), 1,36 (s, 3H, CH3); масс-спектр (ИЭР, отрицательные ионы): 371,68 [M-H]-.
ПРИМЕР 2
Коэффициент распределения в системе октанол-вода (Log P)
[00421] Log P представляет собой логарифмированное значение коэффициента распределения в системе октанол-вода, который часто используют на ранних стадиях разработки лекарственных средств для приблизительной оценки способности конкретной молекулы проникать через биологические мембраны. Log P вычисляли при помощи ChemDraw Ultra версии 12.0.2.1016 (Perkin-Elmer, Waltham, Massachusetts 02451). Вычисленные значения Log P приведены в таблице 1 в столбце с заголовком ‘Log P (от -0,4 до +5,6)’. Правило пяти Липинского представляет собой набор критериев, позволяющих предсказывать пероральную биодоступность. Один из указанных критериев пероральной биодоступности заключается в том, что Log P должен находиться между значениями, указанными в заголовке столбца (в диапазоне от -0,4 (относительно гидрофильный) до +5,6 (относительно липофильный)), или, что используется чаще, должен составлять <5. Одной из задач при разработке SARD являлось улучшение растворимости в воде. Моноциклические матрицы согласно настоящему изобретению, такие как пиразолы, пирролы и т.д., имеют повышенную растворимость в воде по сравнению с полученными ранее аналогами. Например, можно провести сравнение значений Log P для SARD, полученных на основе других матриц, например, алкиламиновой 17, индолиновой 100 и индольной 11, с моноциклическими системами согласно настоящему изобретению (1001-1049).
[00422]
(от -0,4 до +5,6)
T1/2 (мин) и CLint (мкл/мин/мг)
(ДГТ = 1 нМ
ингибирование, %, при
1,10 мкМ
ингибирование, %, при 10 мкМ
(агонист)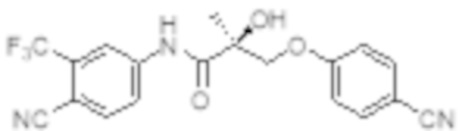
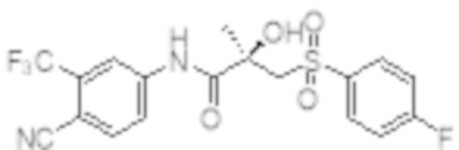
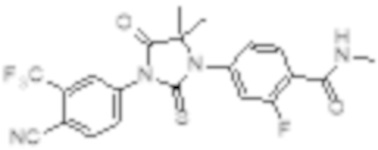
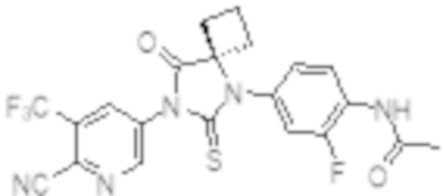
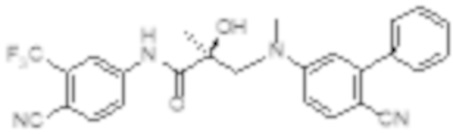
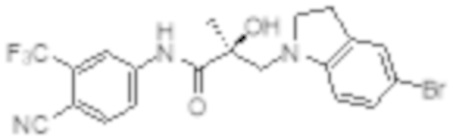
10,38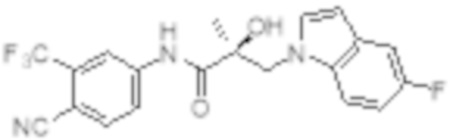
56,14
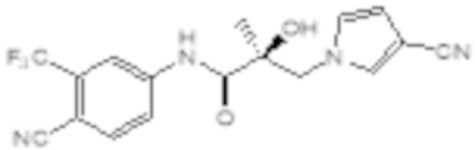
29,5
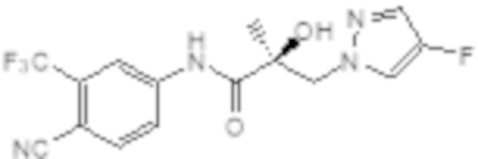
0,89
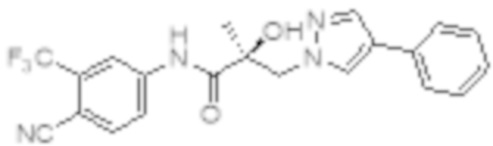
14,31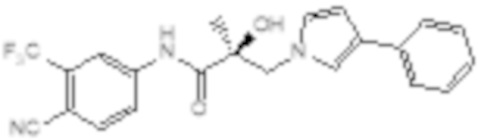
175,2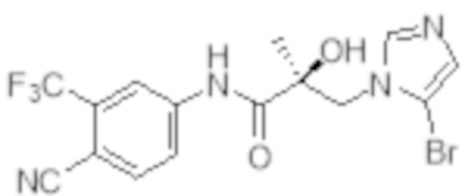
41,58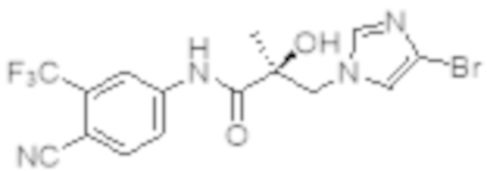
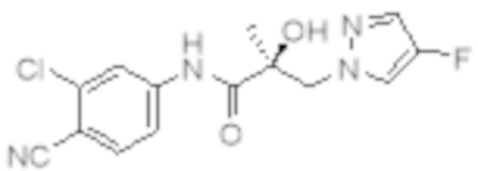
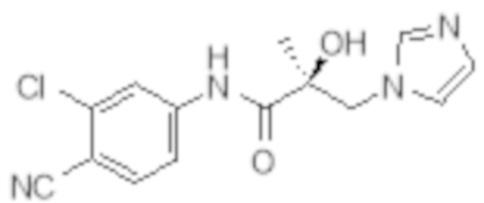
28,16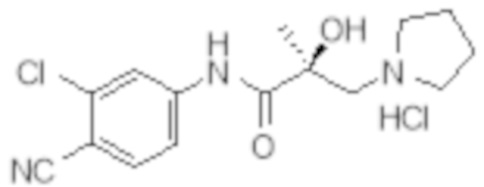
(для свободного амина)
(для своб. амина)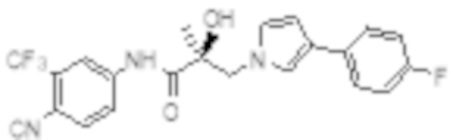
38,66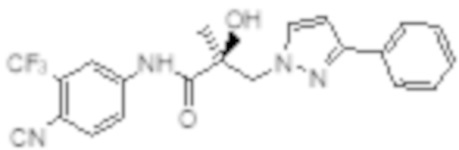
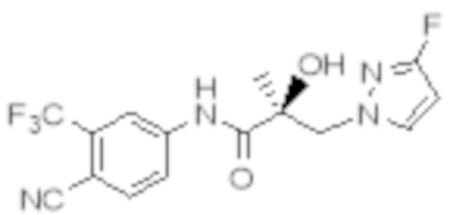
1,02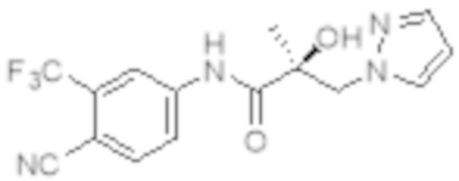
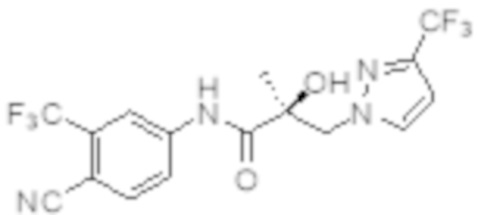
(сравнимо с 11 в том же эксп.)
(сравнимо с 11 в том же эксп.)
0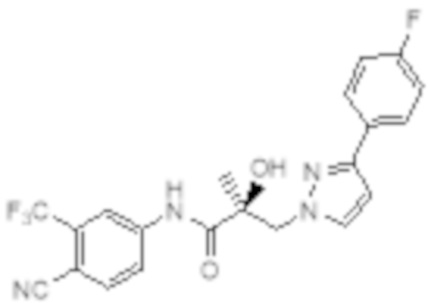
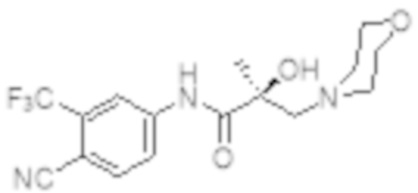
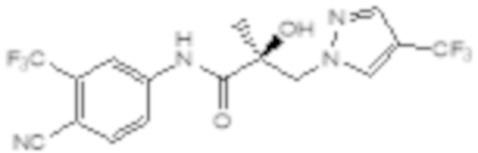
0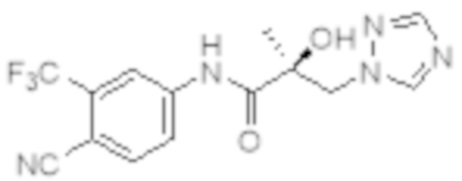
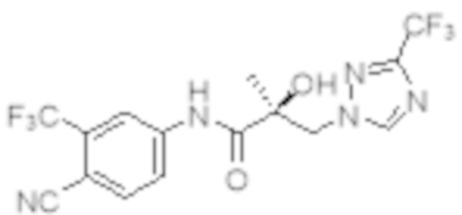
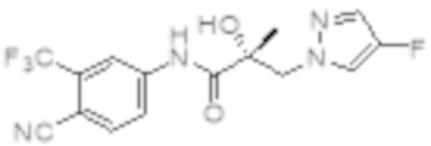
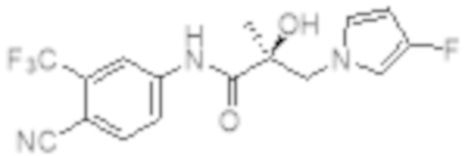
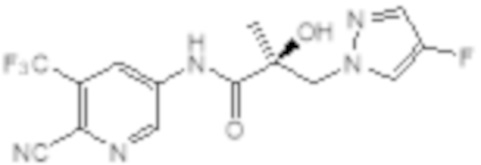
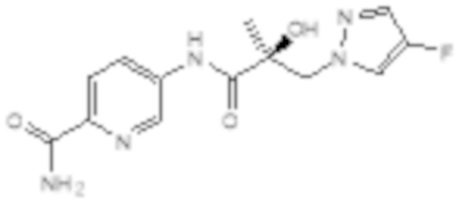
0
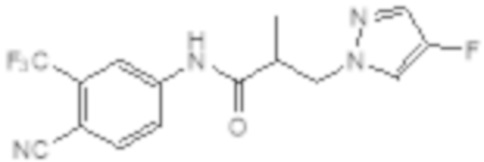
0
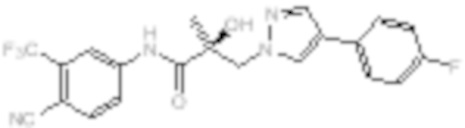
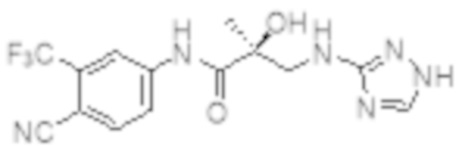
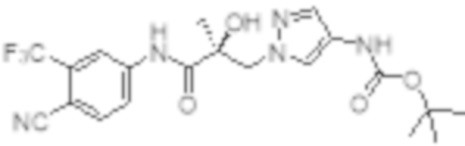
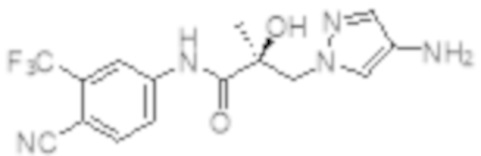
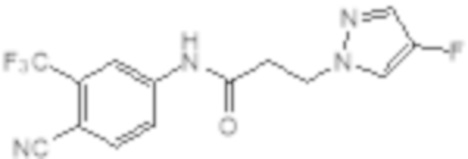
связывает
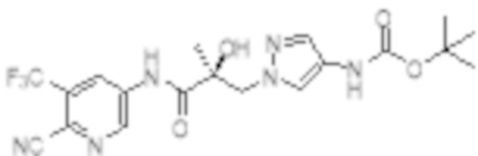
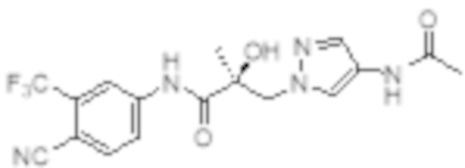
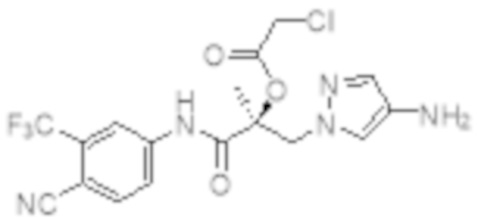
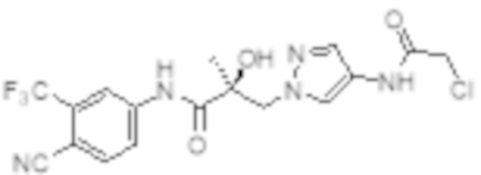
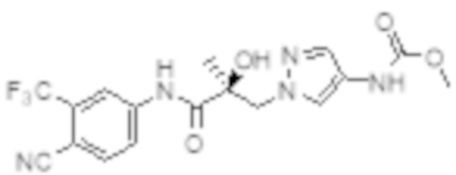
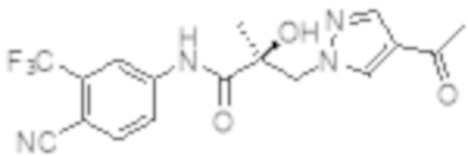
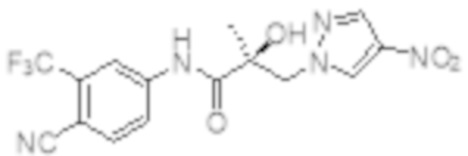
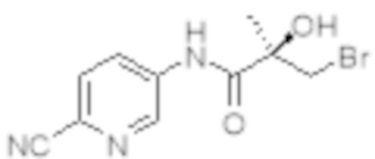
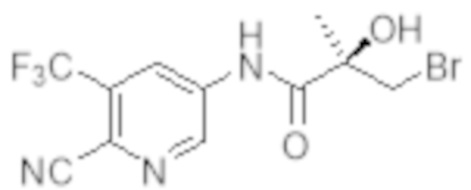
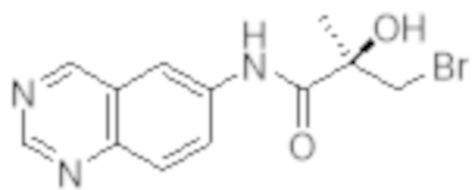
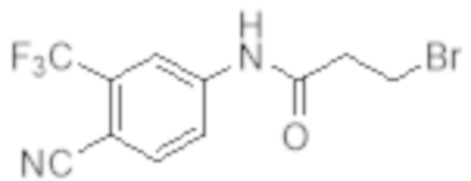
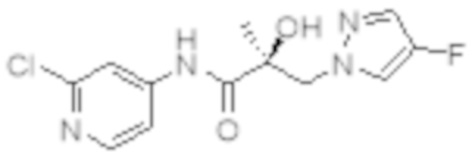
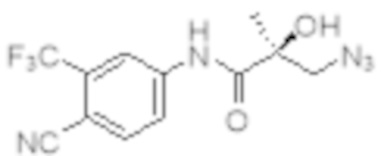
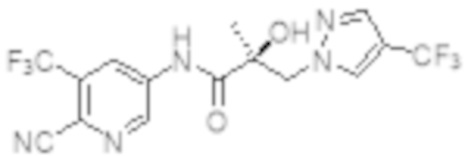
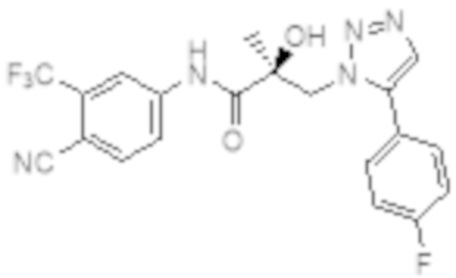
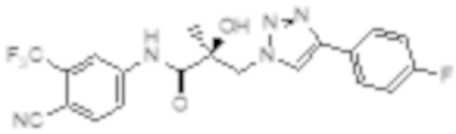
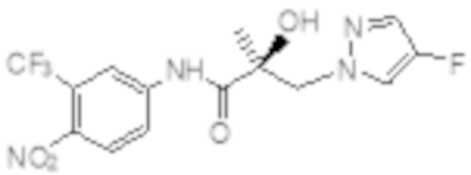
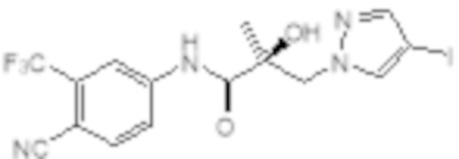
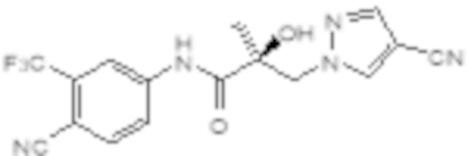
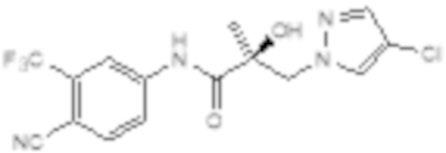
(мин)
(мин)
11
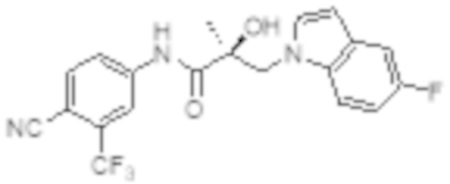
1001
1002
1004

ПРИМЕР 3
Исследование трансактивации
[00423] Способы: Клетки HEK-293 трансфицировали указанными рецепторами и GRE-LUC и люциферазой CMV-renilla. Клетки обрабатывали через 24 часа после трансфекции, и исследование люциферазы проводили через 48 часов после трансфекции. Соединения SARD не ингибировали трансактивацию рецепторов, отличных от AR, в концентрации менее 10 мкМ. Экспериментальный способ описан ниже.
[00424] AR человека клонировали в основной вектор CMV и использовали в исследовании трансактивации. Клетки HEK-293 помещали в количестве 120000 клеток на лунку в 24-луночный планшет в ДМЭ + 5% csFBS. Клетки трансфицировали с использованием липофектамина (Invitrogen, Carlsbad, CA), 0,25 мкг GRE-LUC, 0,01 мкг CMV-LUC (люцифераза renilla) и 25 нг AR. Клетки обрабатывали через 24 часа после трансфекции, и исследование люциферазы проводили через 48 часов после трансфекции. Результаты трансактивации определяли на основании измеренных значений испускания излучения люциферазой и выражали в относительных световых единицах (ОСЕ). Исследование проводили в режиме антагониста (IC50) с использованием известного агониста R1881 в концентрации EC50 0,1 нМ и SARD согласно настоящему изобретению в увеличивающихся концентрациях. Данные для режима агониста выражали на качественном уровне, например, как частичный агонист или примерное значение EC50 энобосарма, для некоторых соединений в таблице 1. Данные для антагонистов приведены как значения IC50 (нМ), полученные по четырехпараметровой логистической кривой, и указаны в таблице 1 в столбце с заголовком ‘IC50’.
[00425] Результаты: Типовые графики показаны на фигурах 1A (1002), 2A (11 и 1002), 3A (1003), 4A (1004), 5A (1005), 6A (1006), 8-12 (1007-1011) и 13A (1001), где на графиках показана зависимость результатов в ОСЕ, отложенных по оси y, от концентрации SARD, отложенной по оси x (нМ). На указанных фигурах данные для режима антагониста показаны при помощи построения кривой, при этом данные для режима агониста (если они присутствуют) указаны без построения кривой. Наблюдали только слабый или частичный агонизм. В исследования фармакодинамики in vivo продемонстрирован высокоактивный и крайне эффективный антагонизм в андроген-зависимых тканях (см. примеры 7 и 10 в настоящем документе). На фигуре 2 приведено прямое сравнение антагонизма 11 (жирные точки) и 1002 (пустые точки). Другие значения IC50, указанные в таблице 1, вычисляли таким же образом.
[00426] 1002 представлял собой высокоактивный антагонист (199,36 нМ; таблица 1 и фигура 1A) и обеспечивал ингибирование, сравнимое с 11 (85,1 нМ; фигура 2), которое представляет собой исключительно активный индольный SARD, который не имеет пероральной биодоступности. Несмотря на 2-кратное увеличение IC50 (таблица 1) и отсутствие связывания с AR-LBD (см. пример 4 и таблицу 1), 1002 имел значительно более выраженную активность разрушения AR in vitro (см. пример 5 и таблицу 1). Кроме того, в отличие от 11, 1002 имело высокую стабильность in vitro в микросомах печени мышей (таблица 1) и человека (таблица 2), что отражалось в улучшении фармакодинамики in vivo (см. пример 7 в настоящем документе) у мышей и крыс. Исходя только из структурных различий, увеличение активности SARD in vitro и метаболической стабильности являлись неожиданными результатами. Аналогично, значительное улучшение эффективности in vivo не могло быть предсказано (т.е. оказалось неожиданным) с учетом исключительно структурных различий. Для 1012, 1014 и 1017 также была продемонстрирована улучшенная метаболическая стабильность in vitro, это позволяет предположить, что пиразольный фрагмент может являться одной из причин неожиданной стабильности 1002.
[00427] Как будет обсуждаться ниже, для 1002 и 1014 также была продемонстрирована значительная противоопухолевая активность в исследованиях ксенотрансплантатов in vivo (см. примеры 8 и 10), это позволяет предположить, что биодоступность указанных соединений является достаточной для предполагаемых способов применения.
[00428] Для 1004 (пиррол) и 1006 (имидазол) было продемонстрировано высокоактивное ингибирование (178,77 нМ и 148,94 нМ; таблица 1; фигуры 4A и 6A), но низкая активность SARD, при этом для 1005 и 1016 было продемонстрировано слабое ингибирование, но высокая активность SARD, это позволяет предположить, что ингибирование in vitro слабо коррелирует с активностью SARD. Тем не менее, 1010 (пиррол), 1012 (пиразол) и 1014 (пиразол) обеспечивали высокоактивное ингибирование и разрушение. В целом, связывание LBD или LBD-зависимое ингибирование и активность SARD in vitro, вероятно, не зависят друг от друга, но при этом имеется весьма приемлемая взаимосвязь структуры и активности. Значения для других соединений согласно настоящему изобретению приведены в таблицах 1 и 2.
[00429] Высокоактивное ингибирование трансактивации также наблюдали для 1020 (192 нМ), 1022 (92 нМ) и 1024 (464 нМ). 1020 представляет собой R-изомер пиразола 1002 и подобно 1002 не связывает LBD, но при этом имеет высокую активность SARD. Аналогично, индольный SARD 11 и R-изомер 11 имеют сравнимую активность SARD (таблица 1 и фигура 2B) в отношении AR-FL (LNCaP) и AR-SV (22RV1). Это резко отличается от пропанамидных SARM, таких как энобосарм, R-изомеры которых, как правило, имеют в 100 раз более низкую активность связывания LBD и агониста (данные не показаны). Это является дополнительным подтверждением того, что активность SARD не опосредуется LBD, что будет более подробно обсуждаться ниже в примере 9. В примере 9 продемонстрирован новый участок связывания в N-терминальном домене (NTD), который определяет различия взаимосвязи структуры и активности традиционных антагонистов AR, которые связывают LBD, и SARD согласно настоящему изобретению, которые действуют через NTD. Сохранение активности SARD для противоположных изомеров (в отличие от SARM) позволяет предположить, что для участка связывания NTD стереоспецифичность лигандов не важна. Кроме того, для участка связывания NTD, вероятно, не требуется наличие хиральной гидроксильной группы, которая является консервативной для связывающих LBD (агонистов и) антагонистов. Например, 1024 представляет собой нехиральный рацемат пропанамида, в котором отсутствует гидроксил, но которое при этом сохраняет активность SARD (таблица 1: 60% разрушение AR-FL) и способность ингибировать AR (таблица 1: IC50 = 464 нМ), несмотря на отсутствие связывания LBD (таблица 1: Ki: не связывает). Кроме того, в 1029 хиральный центр заменен на метиленовую группу, но при этом сохраняется некоторая активность SARD (таблица 1: 35% разрушение AR-FL) и антагонизм в отношении AR (таблица 1: IC50 = 2124 нМ). 1032, в котором гидроксильная группа защищена путем ацилирования, не связывает LBD, но является антагонистом AR. Другим возможным различием между SAR является A-кольцо, которое является консервативным для агентов, связывающих LBD, в которых оно содержит 4-циано- или нитро- и 3-трифторметильные или 3-хлор-заместители. Тем не менее, замена CF3 в 1002 на Cl в 1007 приводила к уменьшению активности SARD. Кроме того, 1022 содержит новое пиридиновое A-кольцо и не связывает LBD, но сохраняет высокоактивное ингибирование трансактивации (92 нМ) и активность SARD (таблица 1). Аналогично, активность SARD отсутствует у 1037 и 1041, которые содержат пиридиновые A-кольца (таблица 1 и фигура 28C), и 1043 является высокоактивным пиридиновым антагонистом, но имеет низкую активность SARD (таблица 1). Также, 1037 представляет собой 3-бромпропанамид (т.е. в нем отсутствует гетероциклическое B-кольцо), который слабо связывает LBD (4547 нМ), но является высокоактивным антагонистом (350,5 нМ) и сохраняет активность SARD, это демонстрирует, что наличие B-кольца в SARD согласно настоящему изобретению является необязательным (таблица 1). Указанные наблюдения подтверждают, что активность SARD может быть оптимизирована в отсутствие данных связывания LBD, и объясняют разрушение сплайсированных форм AR, в которых отсутствует LBD.
ПРИМЕР 4
Исследование аффинности к лиганд-связывающему домену (LBD) андрогенных рецепторов человека (hAR)
[00430] Способы: hAR-LBD (633-919) клонировали в pGex4t.1. Получали крупную серию AR-LBD, меченного GST, и очищали на колонке GST. Рекомбинантный AR-LBD объединяли с [3H]миболероном (PerkinElmer, Waltham, MA) в буфере A (10 мМ Tris, pH 7,4, 1,5 мМ ЭДТА динатрия, 0,25 M сахароза, 10 мМ молибдат натрия, 1 мМ ФМСФ) для определения равновесной константы диссоциации (Kd) [3H]миболерона. Белок инкубировали совместно с увеличивающимися концентрациями [3H]миболерона в присутствии немеченного миболерона в высокой концентрации или без него при 4°C в течение 18 часов для определения общего и неспецифического связывания. Затем величину неспецифического связывания вычитали из общего связывания для определения специфического связывания и использовали нелинейную регрессию кривой связывания лиганда с одним участком насыщения для определения Kd миболерона.
[00431] SARD или ДГТ в увеличивающихся концентрациях (диапазон: от 10-12 до 10-4 M) инкубировали с [3H]миболероном и AR-LBD в условиях, описанных выше. После инкубации связанный с лигандом комплекс AR-LBD выделяли с использованием гидроксиапатита BiogelHT, промывали и анализировали в сцинтилляционном счетчике после добавления сцинтилляционного коктейля.
[00432] Результаты: Результаты этого исследования приведены в виде значений Ki (нМ) в таблице 1 в столбце с заголовком ‘Связывание wt AR (Ki (левый столбец))’. Как обсуждалось выше и как видно из таблицы 1, корреляция между аффинностью к AR-LBD и активностью SARD является очень слабой. Например, для 1002, 1005, 1015, 1019, 1020 и 1022 наблюдается активность SARD in vitro, но отсутствует аффинность связывания LBD (таблица 1).
ПРИМЕР 5
Исследования in vitro для определения активности SARD
[00433] Разрушение андрогенных рецепторов LNCaP или AD1 (полноразмерный AR): Проводили исследование действия соединений согласно настоящему изобретению на экспрессию полноразмерного белка AR. Способы: Клетки LNCaP или AD1, экспрессирующие полноразмерный AR, помещали в количестве 750000-1000000 клеток/лунка в 6-луночный планшет в питательную среду (RPMI + 10% ЭБС). Через двадцать четыре часа среду заменяли на RPMI + 1% csFBS, не содержащую феноловый красный, и выдерживали в указанной среде в течение 2 дней. Среду снова заменяли на RPMI + 1% csFBS, не содержащую феноловый красный, и обрабатывали клетки SARD (от 1 нМ до 10 мМ) в комбинации с 0,1 нМ R1881. Через 24 часа после обработки клетки промывали холодным ФБР и собирали. Белок экстрагировали солевым лизисным буфером с использованием трех циклов замораживания-оттаивания. Проводили оценку концентрации белка и пять микрограммов общего белка помещали в ДСН-ПААГ, фракционировали и переносили на мембрану ПВДФ. В мембрану вводили зонды антитела к AR N-20 (SantaCruz Biotechnology, Inc., Dallas, Texas 75220) и антитела к актину (Sigma-Aldrich, St. Louis, MO).
[00434] Результаты: Разрушение клеток LNCaP или AD1 описано в таблице 1 в столбце с заголовком ‘Полноразмерный, ингибирование, %, при 1, 10 мкМ’. Результаты указанного исследования приведены на фигурах 1B (1002), 2B (11, 11R, 1002, 1020), 3B-6B (1003-1006), 7 (17), 13B (1001), 20A (1010, 1012, 1014, 1015, 1017, 1019 и 1022), 28A (1024 и 1029), 28C (1037 и 1041), 28D (1044 и 1045) в виде изображений пленок вестерн-блоттинга (пленки, проявленные при помощи хемилюминесценции).
[00435] Разрушение андрогенных рецепторов 22RV1 или D567es (сплайсированная форма (S.V.) AR): Эффект обработки SARD на уровень AR измеряли в устойчивых к действию андрогенов раковых клетках предстательной железы 22RV-1 или D567es. Способы: Клетки 22RV1 или D567es, экспрессирующие сплайсированные формы AR (AR-SV), помещали в количестве 750000-1000000 клеток/лунка в 6-луночный планшет в питательную среду (RPMI + 10% ЭБС). Через двадцать четыре часа после размещения клеток заменяли среду и проводили обработку. Через 24-30 часов после обработки клетки промывали холодным ФБР и собирали. Белок экстрагировали солевым лизисным буфером с использованием трех циклов замораживания-оттаивания. Проводили оценку концентрации белка и пять микрограммов общего белка помещали в ДСН-ПААГ, фракционировали и переносили на мембрану ПВДФ. В мембрану вводили зонды антитела к AR N-20 (Santa Cruz Biotechnology, Inc., Dallas, Texas 75220) и антитела к актину (Sigma-Aldrich, St. Louis, MO).
[00436] Результаты: Разрушение клеток 22RV1 или D567es описано в таблице 1 в столбце под заголовком “S.V. ингибирование, %, при 10 мкМ.” Результаты этого исследования для клеток D567es приведены на фигурах 1C (1002) и 20B (1010, 1012, 1014-1017, 1019 и 1022) и для клеток 22RV1 на фигурах 2B (11, 11R), 13C (1001) и 28B (1024 и 1029) в виде изображений пленок вестерн-блоттинга (пленки, проявленные при помощи хемилюминесценции).
ПРИМЕР 6
Исследования метаболизма в микросомах печени мышей (DMPK (MLM))
[00437] Определение метаболической стабильности (in vitro CLint) исследуемых соединений: метаболизм I фазы: Исследование проводили в конечном объеме 0,5 мл в двух повторностях (n=2). Исследуемое соединение (1 мМ) предварительно инкубировали в течение 10 минут при 37°C в 100 мМ Tris-HCl, pH 7,5, содержащем 0,5 мг/мл микросомального белка печени. После предварительной инкубации инициировали реакцию путем добавления 1 мМ НАДФН (который предварительно инкубировали при 37°C). Инкубацию проводили в трех повторностях в течение различных периодов времени (0, 5, 10, 15, 30 и 60 минут). Отбирали 100 мл аликвоты и гасили реакцию 100 мл внутреннего стандарта, содержащего ацетонитрил. Образцы перемешивали на вортексе и центрифугировали при 4000 об./мин в течение 10 минут. Надосадочную жидкость переносили в 96-луночные планшеты и передавали для анализа ЖХ-МС/МС. В качестве контроля проводили инкубацию образцов в отсутствие НАДФН. По значению %PCR (% оставшегося исходного соединения) вычисляли скорость израсходования соединения (коэффициент наклона) и in vitro CLint (мкл/мин/мг белка).
[00438] Результаты: На фигуре 14 приведены данные I фазы в виде таблицы с исходными данными одного эксперимента с использованием MLM для соединения 1002, а также вычисленные с их помощью значения T1/2 (полувыведение) и CLint (клиренс). На фигурах 15A и 16A приведены данные I фазы в виде таблицы с исходными данными и графически изображенные данные одного эксперимента с использованием 1002 в микросомах печени мышей (MLM) и микросомах печени человека (HLM), соответственно. Аналогично, на фигуре 17 приведены данные MLM для 1001, и с их помощью вычисляли значения T1/2 (полувыведение) и CLint (клиренс), приведенные в таблицах 1 и 2.
[00439] Метаболическая стабильность в I и II фазах метаболического пути
[00440] В настоящем анализе исследуемое соединение инкубировали совместно с микросомами печени и определяли израсходование лекарственного средства путем исследовательской ЖХ-МС/МС. Для симуляции II фазы метаболического пути (глюкуронирование) в исследовании использовали UDPGA и аламетицин. По значению %PCR (% оставшегося исходного соединения) вычисляли скорость израсходования соединения (коэффициент наклона на графике зависимости концентрации от времени) и in vitro CLint (мкл/мин/мг белка). Результаты этого исследования, в котором использовали микросомы печени мышей (MLM), приведены в таблице 1 в столбце с заголовком “DMPK (MLM) T1/2 (мин) и CLint (мкл/мин/мг)”. Первое значение представляет собой вычисленный период полувыведения (T1/2) исследуемого соединения в MLM, выраженный в минутах, и 2е значение представляет собой характеристический CL (CLint) исследуемого соединения MLM, выраженный в мл/мин/мг белка.
[00441] Результаты: На фигуре 14 приведены данные I и II фазы в виде таблицы с исходными данными одного эксперимента, а также вычисленные с их помощью значения T1/2 (полувыведение) и CLint (клиренс). На фигурах 15B (микросомы печени мышей (MLM)) и 16B (микросомы печени человека (HLM)) приведены данные I и II фазы для 1002 в виде таблицы с исходными данными для отдельных экспериментов и графически изображенные данные. Полученные данные продемонстрировали, что 1002 является стабильным в MLM и крайне стабильным в HLM. Анализ ЖХ-МС/МС проводили, как описано ниже.
[00442] Метаболическая стабильность 1002 и других пиразолов согласно настоящему изобретению была неожиданной с учетом известных SARD (100, 17 и 11, см. таблицу 1). См. также примеры 8 и 10 для сравнения пиразолов с известными ранее матрицами SARD и изучения неожиданных результатов метаболической стабильности, фармакодинамики in vivo, концентрации в сыворотке и опухоли in vivo и противоопухолевой эффективности in vivo при распространенном раке предстательной железы (пример 10) и тройном негативном раке молочной железы (пример 8). Кроме того, по данным MLM для 1024 (таблица 1), соединения, не содержащего гидроксигруппу, и 1023, соединения, содержащего пиридиновое A-кольцо (не содержащего карбонитрил), было показано отсутствие метаболизма после инкубации совместно с MLM в течение 60 минут. Это демонстрирует метаболическую стабильность SARD согласно настоящему изобретению, включая те, что содержат пиразольные B-кольца, но в которых отсутствует гидроксильная группа, и/или содержат альтернативные A-кольца.
Анализ ЖХ-МС/МС:
[00443] Анализ исследуемых соединений проводили на системе ЖХ-МС/МС, состоящей из хроматографа ВЭЖХ Agilent 1100 HPLC и масс-спектрометра MDS/Sciex 4000 Q-Trap™. Разделение проводили на аналитической колонке C18 (Alltima™, 2,1 X 100 мм, 3 мкм), защищенной системой защитных картриджей C18 (SecurityGuard™ ULTRA картриджи СВЭЖХ для колонок с внутр.диам. 4,6 мм, Phenomenex). Подвижная фаза состояла из канала A (95% ацетонитрил + 5% вода + 0,1% муравьиная кислота) и канала C (95% вода + 5% ацетонитрил + 0,1% муравьиная кислота), доставку проводили с расходом 0,4 мл/мин. Объемное отношение ацетонитрила к воде было оптимизировано для каждого анализируемого соединения. Проводили многократное сканирование для отслеживания реакции с использованием газа завесы, газа камеры соударений, распылительного газа и вспомогательного газа, оптимизированных для каждого соединения, и источника нагрева при 550°C. Молекулярные ионы получали путем приложения напряжения ионного распыления -4200 В (режим отрицательных ионов). Потенциал декластеризации, потенциал ввода, энергия соударения, масса ионов продукта и потенциал на выходе из ячейки были оптимизированы для каждого соединения.
ПРИМЕР 7
Антагонизм in vivo, продемонстрированный соединением SARD 1002
[00444] Способ Хершбергера: Самцам мышей (масса тела 20-25 граммов; n=5-7/группа), которых исследовали без операции или кастрировали, проводили лечение, как указано на фигурах, в течение 13 дней. Лечение кастрированных мышей начинали через 3 дня после кастрации. Мышей умерщвляли на 14 день после начала лечения, удаляли семенные железы и взвешивали. Указывали измеренную массу семенных желез или нормированную по массе тела.
[00445] Результаты: 1002 значительно уменьшало массу семенных желез при ежедневном пероральном введении 40 мг/кг дозы мышам, которым не проводили операцию (фигура 18A), и 100 мг/кг дозы кастрированным мышам (фигура 18B). Уменьшение массы семенных желез, которое является показателем антагонизма в отношении андрогенных рецепторов (AR), было более выраженным по сравнению с 20 мг/кг/день дозой энзалутамида. 1002 было эффективным даже у кастрированных мышей, это указывает на то, что 1002 с высокой активностью ингибировало любую остаточную активность AR в целевых тканях с AR у кастрированных мышей, и является хорошим показателем возможности использования SARD согласно настоящему изобретению при лечении пациентов с раком предстательной железы, которым проводили АДТ. Это позволяет предположить, что даже несмотря на наличие слабого частичного агонизма в отношении AR в экспериментах трансактивации in vitro, основным механизмом действия in vivo является антагонизм в отношении AR. Кроме того, активность in vivo для дозы 40 мг/кг (40 mpk) 1002 значительно превышала активность SARD, которые авторы ранее исследовали в своей лаборатории и in vivo действие которых проявлялось только в дозе 100 мг/кг или более, несмотря на сравнимую активность ингибирования транскрипции in vitro. Это позволяет предположить, что неожиданная метаболическая стабильность 1002 определила его клинически значимую пероральную биодоступность.
[00446] Эксперименты Хершбергера повторяли на крысах, так как известно, что крысы являются более восприимчивыми при моделировании андрогенной и анаболической активности агонистов и антагонистов AR. Крысам линии Спраг-Доули (с массой тела 165-180 г) перорально вводили носитель, 40 mpk 1002, 60 mpk 1002 или 20 mpk энзалутамида. После 13 дней лечения крыс умерщвляли и измеряли массу предстательной железы, семенных желез и мышцы, поднимающей задний проход. 1002 в дозе 40 мг/кг действовало как антагонист в отношении массы семенных желез, предстательной железы и мышцы, поднимающей задний проход, примерно в той же степени, что и 20 мг/кг энзалутамида, а 60 мг/кг доза 1002 еще больше уменьшала массу каждой из указанных тканей практически до уровня кастрированных животных (фигура 19A). На фигуре 19А показано уменьшение абсолютной массы органов у крыс, которым не проводили операцию, а на фигуре 19B приведены данные для тех же органов в виде уменьшения в % по сравнению с контрольной группой, в которой вводили носитель. На нижнем правом графике на фигуре 19B показано влияние кастрации на массу семенных желез и предстательной железы. 1002 в дозе 60 мг/кг уменьшало массу предстательной железы и семенных желез на ~70% по сравнению с уменьшением на 90% и 85%, соответственно, обеспечиваемым после кастрации (не показано). 1002 является первым SARD с достаточной биодоступностью, чтобы обеспечивать более выраженный антагонизм в отношении AR in vivo по сравнению с энзалутамидом, несмотря на то, что оно имеет более низкую активность в отношении трансактивации in vitro (IC50) и не связывает LBD (Ki). 1002 обладает высокой разрушительной активностью SARD in vitro. Соответственно, неожиданно более выраженный антагонизм in vivo 1002 по сравнению с энзалутамидом (в IND энзалутамида указано, что 100 mpk и 30 mpk дозы имеют сравнимую эффективность in vivo, таким образом 20 mpk доза предположительно имела эффективность, близкую к Emax, и незначительную растворимость) не может быть объяснен в рамках традиционного ингибирования AR через LBD, но, напротив, позволяет предположить, что антагонизм в отношении AR может быть связан с высокоактивным разрушением AR, которое является уникальным свойством соединений согласно настоящему изобретению.
[00447] См. также пример 9 для изучения многочисленных биофизических доказательств, подтверждающих, что 1002 и другие SARD согласно настоящему изобретению связывают NTD. См. также пример 10, в котором получены неожиданные результаты для 1014 в исследовании Хершбергера и в других исследованиях in vivo.
ПРИМЕР 8
Противоопухолевая активность in vivo, продемонстрированная соединением SARD 1002 в ксенотрансплантатах (PDX), выделенных у пациентов с тройным негативным раком молочной железы (ТНРМЖ)
[00448] Сбор образцов у пациентов и получение PDX: Образцы у пациентов с раком молочной железы собирали с согласия пациента в соответствии с протоколом, одобренным экспертным советом организации (ЭСО) Научного центра здоровья при университете Теннесси (UTHSC). Вкратце, образцы собирали сразу после проведения хирургии в среду RPMI, содержащую смесь пенициллин:стрептомицин и фунгизон (Thermo Fischer Scientific), и отправляли в лабораторию, поместив в лед. Ткани тщательно измельчали и обрабатывали коллагеназой в течение 2 часов. Переваренные ткани промывали бессывороточной средой и имплантировали подкожно в виде 1 мм3 фрагментов самкам мышей Nod Scid Gamma (NSG). Два указанных PDX, собранных у пациентов с тройным негативным раком (ТНРМЖ), HBrT-1071 и HBrT-1361, которые были охарактеризованы как ТНРМЖ в момент сбора, имплантировали мышам после овариэктомии. Все исследования животных проводили в соответствии с протоколами, одобренными Комиссией по уходу за животными и их использованию (ACUC) UTHSC. Самок мышей NSG (возрастом 6-8 недель), которых приобретали в JAX labs (Bar Harbor, ME), размещали по пять животных в клетке, предоставляли свободный доступ к воде и коммерческому корму для грызунов (корм для грызунов Harlan Teklad 22/5 - 8640). HBrT-1071 и HBrT-1361 имплантировали (1 мм3) под жировую прослойку молочной железы путем хирургии с изофлурановой анестезией. После того, как размер опухоли достигал 100-200 мм3, животных случайным образом распределяли по группам и вводили носитель (полиэтиленгликоль-300:ДМСО в отношении 85:15) или 1002 (60 мг/кг/день п.о.). Размеры опухоли измеряли три раза в неделю при помощи штангенциркуля и вычисляли объем опухоли по формуле длина*ширина*ширина*0,5236. В конце экспериментов животных умерщвляли, опухоли взвешивали и собирали для дальнейшей обработки. Собирали кровь, отделяли сыворотку и хранили при -80°C.
[00449] Результаты: Соединение SARD 1002 подавляло рост опухоли в двух различных моделях PDX ТНРМЖ (фигуры 21A и 21B), тогда как энзалутамид неэффективно подавлял рост опухоли (фигура 21A). 1002 значительно подавляло рост PDX ТНРМЖ HBrt 1071, подавление роста опухоли в процентах составляло 65%. Аналогично, 1002 уменьшало массу опухоли более чем на 50% (фигура 21A). В противоположность этому, опухоли, собранные у животных, которым вводили энзалутамид, по размеру не отличались от опухолей у животных, которым вводили носитель, при этом, вероятно, имелась тенденция к ускорению роста опухоли. 1002 значительно подавляло рост PDX ТНРМЖ HBrt-1361, где подавление роста опухоли в процентах составляло ~50%, и уменьшало массу опухоли более чем на 40% (фигура 21B). Кроме того, при анализе AR, которые присутствовали в указанных опухолях, был показан высокий уровень сплайсированных форм AR (фигура 21A, полоса 1071). Этот факт объясняет, почему 1002, которое представляет собой SARD, связывающий NTD (см. пример 9 ниже для биофизического подтверждения связывания NTD), могло подавлять рост опухоли, и при этом LBD-зависимый антагонист AR энзалутамид был неэффективным. Это позволяет предположить, что SARD могут подавлять формы рака, зависимые от сплайсированной формы AR, такие как ТНРМЖ и распространенный рак предстательной железы (см. пример 10), например, формы, при которых происходит экспрессия AR-V7 или других AR, в которых отсутствует LBD. Кроме того, это подтверждает, что благодаря неожиданной пероральной биодоступности 1002 и других SARD согласно настоящему изобретению, например, 1014 и 1010, их уровни в сыворотке и опухоли (см. также пример 10) после перорального введения были достаточными для лечения распространенных и устойчивых AR-зависимых форм рака.
ПРИМЕР 9
SARD связывают участок AF-1 в N-терминальном домене (NTD) андрогенных рецепторов
[00450] Ядерный магнитный резонанс (ЯМР): AF-1 и различные фрагменты AF-1 клонировали в векторы pGex4t.1 и pGex6p.1. Для очистки белков инициировали рост крупномасштабной бульонной культуры Луриа при помощи 1 мМ изопропил-β-D-1-тиогалактопиранозида (IPTG), когда ОП достигала 0,6, и инкубировали при 25°C в течение 6 часов. Собирали клетки и проводили лизис в лизисном буфере (50 мМ Tris pH 7,5, 25-250 мМ NaCl, ДНКазе, ингибиторы протеазы, глицерин, ЭГТА, DTT и сахароза). Лизаты белков очищали с использованием зерен глутатион-сефарозы путем инкубации в течение ночи при 4°C при осторожном перемешивании и элюировали очищенный белок буфером для элюирования (лизисный буфер без ДНКазы), содержащим 50 мМ восстановленного глутатиона. Очищенные белки концентрировали с использованием концентраторов белков Amicon или GE. В тех случаях, когда требовалось расщепление GST, использовали PreScission Protease (GE Life Sciences). Белки дополнительно очищали путем FPLC (GE AKTA FPLC) с использованием гель-фильтрационных (Superdex75 10/300 GL) и ионообменных (HiPrep Q FF 16/10) колонок. Соединения, отдельно или в комбинации с очищенным белком, вводили к 1H ЯМР спектрометр (Bruker 400) в общем объеме 500 мкл, где 5 мМ белок и 200-500 мМ низкомолекулярный препарат (полученный в дейтерированном ДМСО (ДМСО-d6)) вводили в 20 мМ фосфатный буфер, полученный в 100% дейтерированной воде.
[00451] Данные ЯМР собирали на спектрометре a Bruker AVANCEIII 400 МГц (Bruker BioSpin Co. Billerica, MA USA), оборудованном ЯМР-зондом BBO 5 мм, при помощи программного обеспечения TopSpin 3.0. Эксперименты 1H протонного ЯМР и разностного ЯМР с переносом насыщения (STD) проводили при помощи стандартных импульсных последовательностей, доступных в библиотеке TopSpin. Ширину спектра устанавливали на 16 ppm, центрировали по пику H2O. Использовали 32K комплексных экспериментальных точек во временной области (TD), получали 256 сканов для 1H протонного ЯМР и 1024 скана для приближения STD. Для STD сигналы в режиме активного и подавленного резонанса собирали в режиме чередования. Частоту облучения в режимах активного и подавленного резонанса устанавливали на 0,8 ppm и -20 ppm, соответственно. Проводили STD в образце, содержащем только соединение-лиганд, с использованием схожих настроек, чтобы выделить сигналы STD, соответствующие белку в образце комплекса белок-соединение. Данные собирали при комнатной температуре. Химические сдвиги указывали с использованием пика H2O при 4,70 ppm для сравнения.
[00452] Результаты: 1H ЯМР использовали для скрининга высокой производительности для обнаружения связывания небольших молекул массой менее 500 Да с крупным белками с массой более 5 кДа. Использование одномерного ЯМР для наблюдения изменения ширины линий или уширение линий в качестве высокоскоростного способа выявления связывания молекул с белками и последующее использование спектроскопии, основанной на анализе воды-лиганда (WaterLOGSY), или разностного ЯМР с переносом насыщения (STD) в качестве подтверждающих методик являются более простым по сравнению с другими биофизическими способами. Указанные эксперименты основаны на том факте, что наблюдаемые параметры ЯМР, такие как ширина линий и ЯЭО, значительно различаются для небольших молекул и крупных молекул. Уменьшение времени вращательной корреляции при связывании низкомолекулярного лиганда с тяжелой молекулярной мишенью приводит к аномальному результату ЯМР для тяжелой молекулы, характеризующемуся уширением и ослаблением пиков лиганда на 1H ЯМР и отрицательными пиками ЯЭО в анализе waterLOGSY по сравнению со свободным состоянием. В отсутствие аффинности результаты ЯМР для небольших молекул (острые пики на 1H ЯМР и положительные значения ЯЭО) получают даже в присутствии белковой мишени. Это различие является основанием для проведения экспериментов по скринингу путем ЯМР.
[00453] С учетом указанных принципов 1H ЯМР использовали для подтверждения связывания 1002 с участком AF-1. 1002 (500 мМ) растворяли в дейтерированном ДМСО (ДМСО-d6) и инкубировали отдельно или в смеси с 5 мМ AF-1 и определяли связывание молекул с белком путем ЯМР. Для 1002, исследуемого отдельно, наблюдали острые пики, это указывает на то, что лиганд содержится в свободном состоянии, при этом для 1002 в комбинации с AF-1 получали широкие диффузные и более низкие пики лиганда, что указывает на аффинность 1002 к AF-1 (фигура 22). Для дополнительного подтверждения результатов 1D ЯМР был проведен анализ WaterLOGSY с использованием только 1002 или его комбинации с AF-1. Для 1002, исследуемого отдельно, получали уплощенный положительный сигнал, при этом для 1002 в комбинации с AF-1 получали отрицательный сигнал, что свидетельствует о связывании с белком (фигура 22). Полученные результаты подтверждают, что 1002 связывает AF-1 в NTD AR, и объясняют, каким образом молекула, которая не связывает LBD AR (таблица 1), может ингибировать AR in vitro и in vivo.
[00454] Флуоресценция в стационарном состоянии: Рекомбинантные меченные гистидином AR-NTD (аминокислоты 1-559) и AR-AF1 (аминокислоты 141-486) очищали, как описано выше. Спектр флуоресценции в стационарном состоянии для белков (1 мкМ), исследуемых отдельно или после титрования 1002 в увеличивающихся концентрациях (1 мкМ, 2 мкМ, 5 мкМ, 10 мкМ, 25 мкМ и 50 мкМ), получали после возбуждения при 278 нм на спектрофотометре Shimadzu Fluorescence. Белки предварительно инкубировали во льду в течение 30 минут совместно с 1002. Результаты показаны для трех независимых экспериментов (n-3) после измерения в двух повторностях.
[00455] Результаты: Для пиразольного SARD 1002 было показано значительное увеличение сигнала флуоресценции в области, в которой наблюдается испускание тирозина (фигура 27B, 307 нм). Обычно сигнал тирозина не наблюдается из-за переноса энергии на триптофановые остатки в свернутых/частично свернутых полипептидах. Увеличение сигнала тирозина схоже с наблюдаемым для несвернутого/денатурированного AR-NTD или AR-AF1, например, при добавлении мочевины (фигура 27A). Тем не менее, соответствующее «красное смещение (увеличение длины волны) сигнала триптофана не наблюдается (см. для сравнения фигуры 27A и 27B, в мочевине λmax изменяется от 344 нм до 347 нм). 1002 может обеспечивать развертывание рецепторных полипептидов (что приводит к испусканию тирозина), но защищает триптофановые остатки.
[00456] Для пиррольного SARD 1010 наблюдалось некоторое гашение, но его зависимость от концентрации была слабой. Тем не менее, более удивительным являлся устойчивый и значительный «синий сдвиг» (в сторону более коротких длин волн), который соответствовал свернутой форме AR-NTD/AF (т.е. спектр TMAO на фигуре 27C, изменение λmax от 344 нм до 340 нм). На основании имеющихся данных можно предположить, что 1010 может стабилизировать структуру полипептидов AR. Данные для индольного SARD 36 (фигура 27D) были схожими с теми, что наблюдали для 1002, но изменения флуоресценции были выражены слабее. В каждом случае наблюдалось взаимодействие между SARD и AR-1 или NTD. Хотя изменение флуоресцентной поляризации (FP) не было идентичным, полученные схожие результаты для различных матриц SARD позволяют предположить, что взаимодействие с N-концом андрогенного рецептора является общим отличительным признаком SARD согласно настоящему изобретению. Кроме того, 1002 не взаимодействует с LBD, но при этом сохраняет выраженный антагонизм в отношении AR и высокую активность SARD.
ПРИМЕР 10
Метаболическая стабильность пиразолов, таких как 1014 и 1002, раскрывает терапевтический потенциал SARD in vivo
Характеристики in vitro :
[00457] Трансактивация (IC50): Как отмечалось в таблице 1, согласно способу, описанному в примере 3, 1014 представляет собой высокоактивный ингибитор AR, имеющий значение IC50 205 нМ, схожее с 1002 (199 нМ).
[00458] Связывание LBD (Ki): Как отмечалось в таблице 1, согласно способу, описанному в примере 4, 1014 связывает LBD AR с Ki 512 нМ, тогда как 1002 не связывает LBD.
Активность SARD : Как отмечалось в таблице 1, согласно способам, описанным в примере 5, 1014 и 1002 могут с высокой активностью разрушать полноразмерные и сплайсированные формы андрогенных рецепторов.
[00459] Исследование клеток MR49F LNCaP, устойчивых к энзалутамиду (LNCaP-EnzR): Клетки помещали в количестве 10000 клеток/лунка в среду RPMI + 1% csFBS, не содержащую феноловый красный, в 96-луночный планшет. Клетки обрабатывали в среде дозой SARD, вызывающей ответ. По завершении трех дней заменяли среду и проводили повторную обработку клеток. По завершении 6 дней измеряли количество живых клеток в исследовании Cell-Titer-Glo (Promega).
[00460] Результаты: Для 1002 и 1014 продемонстрировано сравнимое подавление роста устойчивой к энзалутамиду формы клеточной линии LNCaP (LNCaP-EnzR), в которой имеется двойная мутация F876L/T877A, которая и придает устойчивость к энзалутамиду. 1002 и 1014 оба имели значения IC50 ~3 мкМ и обеспечивали практически полное подавление при 10 мкМ (фигура 23), это позволяет предположить, что оба SARD могут обеспечивать благоприятное действие у пациентов с раком предстательной железы, устойчивым к энзалутамиду, при обеспечении указанного уровня в опухоли. (см. таблицу 4 ниже)
Исследование метаболизма в микросомах печени:
[00461] Материалы: Микросомы приобретали в Xenotech, LLC. Растворы ‘A’ и ‘B’ (кат. №451220 и 451200, соответственно) для растворения системы регенерации НАДФН (NRS) получали в Corning Life Sciences. Верапамил, генистеин, UDPGA, аламетицин и хлорид магния приобретали в Sigma-Aldrich. Сахаролактон получали в Santa Cruz Biotechnology.
Способ: фаза I
[00462] Готовили маточные растворы исследуемого соединения в 10 мМ концентрации в ДМСО. Их разбавляли до концентрации 50 мкМ в 50% смеси ацетонитрил (ACN)/H2O для получения рабочего маточного раствора 100X. Использовали микросомы печени с конечной концентрацией белка 1,0 мг/мл. Для каждого временного интервала (0, 5, 10, 30 и 60 минут) использовали лунки в двух повторностях. Реакции проводили при 37°C на встряхиваемой водяной бане, конечную концентрацию растворителя поддерживали на постоянном уровне 0,5%. Для каждого временного интервала удаляли 100 мкл реакционной смеси и добавляли в лунку с образцом, содержащую 100 мкл ледяного 100% ACN (совместно с внутренним стандартом), для остановки реакции. Конечный объем каждой реакционной смеси составлял 200 мкл, включая: 66 мкл 0,2 M буфера KPO4, (pH 7,4); 50 мкл раствора NRS; и 10 мкл микросом (20 мг/мл маточный раствор).
[00463] NRS представляет собой раствор глюкоза-6-фосфат-дегидрогеназы, НАДФ+, MgCl2 и глюкоза-6-фосфата, полученный согласно инструкциям производителя. В 5,0 мл маточного раствора NRS содержится 3,8 мл H2O, 1,0 мл раствора “A” и 0,2 мл раствора “B”. Реакции в лунках с положительным контролем (верапамил, 0,5 мкМ) останавливали холодным ацетонитрилом, содержащим внутренний стандарт.
Фазы I и II
[00464] Реакции проводили в таких же условиях, что описано выше. В каждую реакцию также включали дополнительные кофакторы. Добавляли UDPGA в конечной концентрации 5,0 мМ. В каждую реакционную смесь добавляли сахаролактон (ингибитор β-глюкуронидазы) и аламетицин (порообразующий пептид) в конечной концентрации 5,0 мМ и 50 мкг/мл, соответственно. В 200 мкл микросомальной реакционной смеси содержалось 65 мкл 0,2 M KPO4 (pH 7,4), 50 мкл смеси NRS, 66 мкл UDPGA (15 мМ маточный раствор); 5,0 мкл сахаролактона (200 мМ маточный раствор); 0,5 мкл аламетицина (20 мг/мл); 0,6 мкл MgCl2 (1 М маточный раствор) и 10 мкл микросом (20 мг/мл маточный раствор). Реакцию в лунках с положительным контролем (генистеин, 2,0 мкМ) останавливали ледяным ацетонитрилом, содержащим внутренний стандарт.
[00465] Образцы центрифугировали при 3000 об./мин в течение 10 минут для удаления клеточного дебриса и осажденного белка. Затем примерно 150 мкл надосадочной жидкости переносили в новый блок для образца для проведения анализа.
Анализ данных
[00466] Для определения периода полувыведения и клиренса проводили подстановку данных при помощи GraphPad Prism в уравнение нелинейной регрессии, предполагая однофазное экспоненциальное уменьшение уровня.
[00467] Результаты: Проводили сравнение 1014 с другими соединениями, включая 1002, в исследованиях метаболизма в микросомах печени. Интересно отметить, что период полувыведения 1002 составлял примерно 1 час in vitro, при этом 1014 имело бесконечный период полувыведения в том же исследовании, т.е. после инкубации в течение 120 минут более 50% соединения сохранялось в реакционной смеси (таблица 3). Как видно в таблице 3, для пиразолов 1002, 1014 и 1022 (см. также таблицу 1 для 1023 и 1024) было продемонстрировано значительное улучшение метаболической стабильности in vitro по сравнению с соединениями на основе индола (11, 34, 36) и индолина (103) (и пиррола 1010) (таблица 3), но при этом сохранение активности SARD (таблица 1). Это позволило предположить значительную биодоступность in vivo для 1002 и 1014.
(S)-N-(4-циано-3-(трифторметил)фенил)-2-гидрокси-2-метил-3-(4-(трифторметил)-1Н-индазол-1-ил)пропанамид
(S)-N-(3-хлор-4-цианофенил)-3-(4-фтор-1Н-индол-1-ил)-2-гидрокси-2-метилпропанамид
(S)-N-(3-хлор-4-цианофенил)-3-(5-фтор-6-фенил-1Н-индол-1-ил)-2-гидрокси-2-метилпропанамид
(S)-N-(4-циано-3-(трифторметил)фенил)-3-(5-фтор-1Н-индол-1-ил)-2-гидрокси-2-метилпропанамид
(S)-N-(3-хлор-4-цианофенил)-3-(4-фториндолин-1-ил)-2-гидрокси-2-метилпропанамид
[00468] Характеристики in vivo:
[00469] Концентрации 1014 в сыворотке и опухоли в эксперименте с использованием ксенотрансплантата: Бестимусных мышей с подкожно имплантированными клетками 22RV1 случайным образом распределяли по группам, когда размер опухоли достигал от 100 до 200 мм3. Мышам вводили носитель (20:80 вода:ПЭГ-400) или 60 мг/кг/день 1014 (или указанные дозы других SARD) в носителе в течение 21 дня. После завершения 21 дня мышей умерщвляли и собирали кровь и опухоли для дальнейшего анализа. При измерении концентрации лекарственного средства у животных, которым вводили 1014, было продемонстрировано значительное накопление лекарственного средства в сыворотке (20,1 мкМ) и опухоли (35,6 мкМ) (таблица 4 и фигура 24) по сравнению с другими молекулами, исследуемыми параллельно в том же эксперименте. Указанные уровни 1014 in vivo, даже с учетом имеющих схожую структуру пиразолов 1002 и 1012, были неожиданными. Кроме того, указанные уровни помогают объяснить эффективность в ксенотрансплантатах LNCaP-EnzR (см. фигуру 26 и ее описание ниже). Несмотря на то, что опухоли 22RV1 не были восприимчивы к SARD в данном конкретном эксперименте, вероятно из-за не зависящего от андрогенов роста, полученный результат позволяет предположить, что андроген-зависимые опухоли, например, LNCaP-EnzR, могут быть восприимчивыми. Другой вывод из полученных данных заключается в том, что концентрация в опухоли превышала концентрацию в сыворотке, это позволяет предположить накопление лекарственного средства в опухоли. Результаты показаны в таблице 4 и на фигуре 24.
[00470] Исследование Хершбергера: Самцов мышей C57BL/6 (возрастом 6-8 недель), которым не проводили кастрацию, случайным образом распределяли с учетом массы тела и вводили различные соединения, указанные на фигуре 25, в течение 14 дней. После завершения 14 дней мышей умерщвляли и взвешивали семенные железы. Для 1014 было продемонстрировано наилучшее уменьшение массы семенных желез по сравнению с другими соединениями, за ним следовало 1002, это позволяет предположить, что указанные вводимые перорально SARD присутствовали в количестве, которое было достаточным для проявления антагонизма в отношении AR в андроген-зависимых тканях у некастрированных животных. Индолы 34 и 36, пиррол 1010 и пиразол 1012 не проявляли выраженного антагонизма в отношении AR in vivo в указанном исследовании.
[00471] Ксенотрансплантат LNCaP, устойчивый к энзалутамиду (LNCaP-EnzR): Клетки MR49F LNCaP-EnzR в RPMI + 10% ЭБС смешивали с матригелем (BD Biosciences) (1:1) и вводили подкожную инъекцию мышам NOD SCID Gamma (NSG) (100 мкл). После того, как размер опухоли достигал 100-200 мм3, животных случайным образом распределяли по группам и вводили носитель (20:80 вода:ПЭГ-300) или 1014 (60 мг/кг/день) в носителе. Объем опухоли измеряли два раза в неделю. После завершения исследования умерщвляли животных, выделяли опухоли, взвешивали и хранили для дальнейшего анализа. Эксперимент проводили дважды с двумя различными партиями клеток, и результаты показаны на фигуре 26. Результаты: В двух отдельных экспериментах 1014 с высокой активностью подавляло рост опухоли и уменьшало объем опухоли примерно на 60-70% по сравнению с животными, которым вводили носитель. Полученный результаты позволяют предположить, что 1014 и другие SARD согласно настоящему изобретению при пероральном введении были терапевтически эффективными при устойчивых к энзалутамиду (т.е. распространенных и не поддающихся лечению) формах рака предстательной железы.
[00472] Вывод: Все полученные результаты указывают на то, что 1014 обладает неожиданными свойствами, связанными с его медленным метаболизмом и накоплением в опухоли. Несмотря на то, что 1014 имеет схожую структуру с 1002 и отличается только наличием заместителя CF3 в третьем положении пиразольного кольца (по сравнению с 4-фтор-заместителем в 1002), оно имеет исключительную устойчивость к метаболизму в микросомах печени и, таким образом, в значительных количествах накапливается в сыворотке, андроген-зависимых органах и опухолях, что является неожиданным на фоне других исследуемых SARD и данных, известных из уровня техники. Это обеспечило неожиданную эффективность in vivo после перорального введения, такую как фармакодинамика (в исследовании Хершбергера было продемонстрировано наиболее эффективное действие на массу семенных желез, наблюдаемое для исследуемых SARD) и подавление роста ксенотрансплантатов опухолей (ксенотрансплантат LNCaP-EnzR), которая была невозможной для описанных ранее матриц SARD, таких как 11, 100 и 17, или других SARD, известных из уровня техники.
[00473] Несмотря на то, что определенные отличительные признаки изобретения были проиллюстрированы и описаны в настоящем документе, множество модификаций, замен, изменений и эквивалентов могут быть предложены специалистами в данной области техники. Таким образом, следует понимать, что прилагаемая формула изобретения включает все указанные модификации и изменения, не выходящие за рамки истинной сущности изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| СЕЛЕКТИВНЫЕ ЛИГАНДЫ-РАЗРУШИТЕЛИ АНДРОГЕННЫХ РЕЦЕПТОРОВ (SARD) И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2016 |
|
RU2689988C2 |
| СЕЛЕКТИВНЫЕ ЛИГАНДЫ-РАЗРУШИТЕЛИ АНДРОГЕННЫХ РЕЦЕПТОВ (SARD) И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2016 |
|
RU2724103C2 |
| СПОСОБЫ ЛЕЧЕНИЯ УРОЛОГИЧЕСКИХ НАРУШЕНИЙ С ПРИМЕНЕНИЕМ СЕЛЕКТИВНЫХ МОДУЛЯТОРОВ АНДРОГЕНОВЫХ РЕЦЕПТОРОВ | 2015 |
|
RU2691652C2 |
| СПОСОБ ЛЕЧЕНИЯ АНДРОГЕН-РЕЦЕПТОР(AR)-ПОЛОЖИТЕЛЬНЫХ ФОРМ РАКА МОЛОЧНОЙ ЖЕЛЕЗЫ С ИСПОЛЬЗОВАНИЕМ СЕЛЕКТИВНЫХ МОДУЛЯТОРОВ АНДРОГЕННЫХ РЕЦЕПТОРОВ (SARM) | 2013 |
|
RU2717835C2 |
| СПОСОБ ЛЕЧЕНИЯ АНДРОГЕН-РЕЦЕПТОРА(AR)-ПОЛОЖИТЕЛЬНЫХ ФОРМ РАКА МОЛОЧНОЙ ЖЕЛЕЗЫ С ИСПОЛЬЗОВАНИЕМ СЕЛЕКТИВНЫХ МОДУЛЯТОРОВ АНДРОГЕННЫХ РЕЦЕПТОРОВ(SARM) | 2013 |
|
RU2648959C2 |
| γ-ДИКЕТОНЫ В КАЧЕСТВЕ АКТИВАТОРОВ WNT/β-КАТЕНИНОВОГО СИГНАЛЬНОГО ПУТИ | 2014 |
|
RU2680716C2 |
| ЛИГАНДЫ РЕЦЕПТОРОВ ЭСТРОГЕНОВ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2010 |
|
RU2543339C2 |
| СОЕДИНЕНИЯ SARM И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2011 |
|
RU2571421C2 |
| МОДУЛЯТОРЫ АНДРОГЕНОВОГО РЕЦЕПТОРА И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2797622C2 |
| НОВЫЕ НИТРОФЕНИЛИПРИТНЫЕ И НИТРОФЕНИЛАЗИРИДИНОВЫЕ СПИРТЫ И ИХ СООТВЕТСТВУЮЩИЕ ФОСФАТЫ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ НАЦЕЛЕННЫХ ЦИТОТОКСИЧЕСКИХ СРЕДСТВ | 2004 |
|
RU2372324C2 |
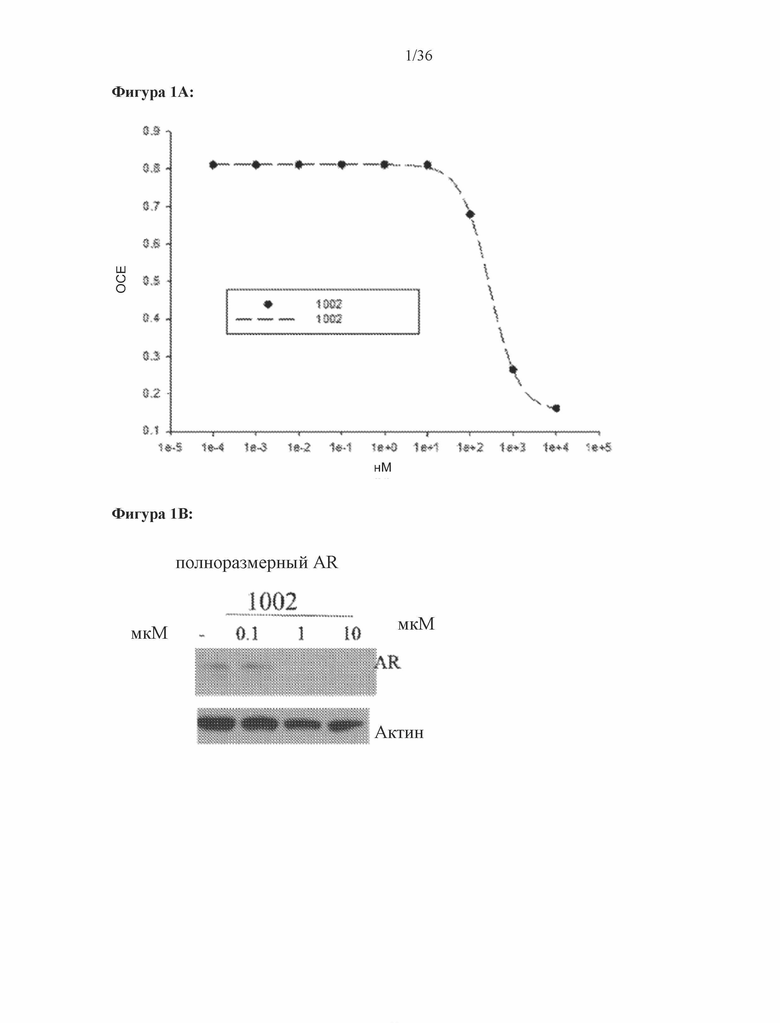
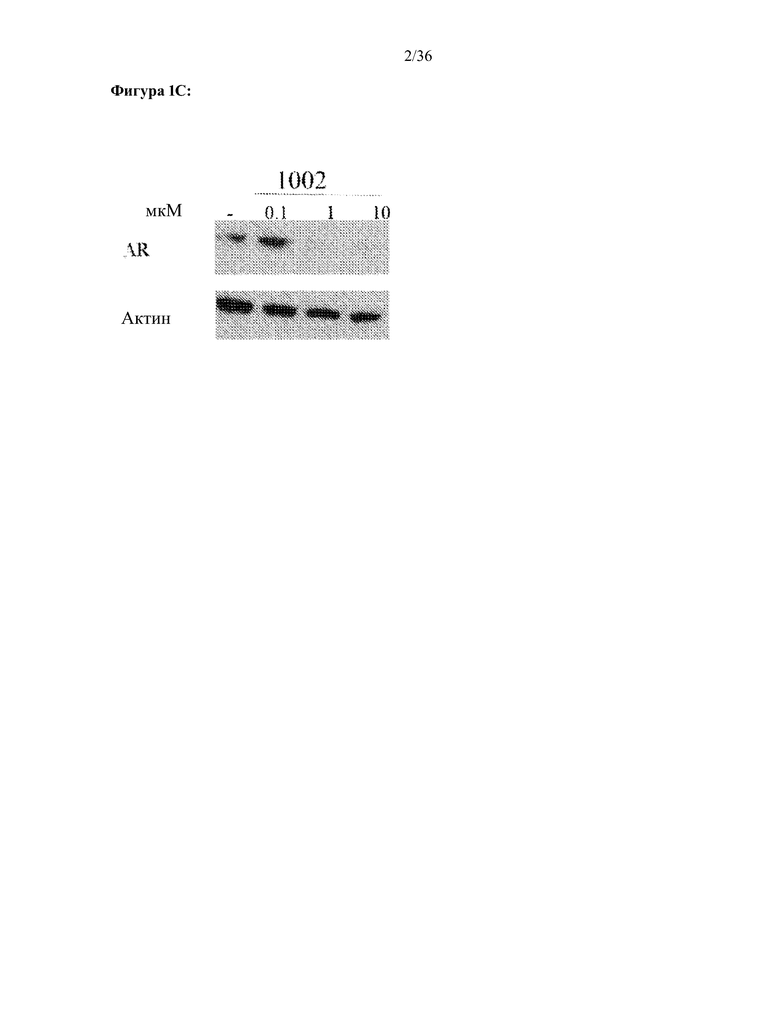
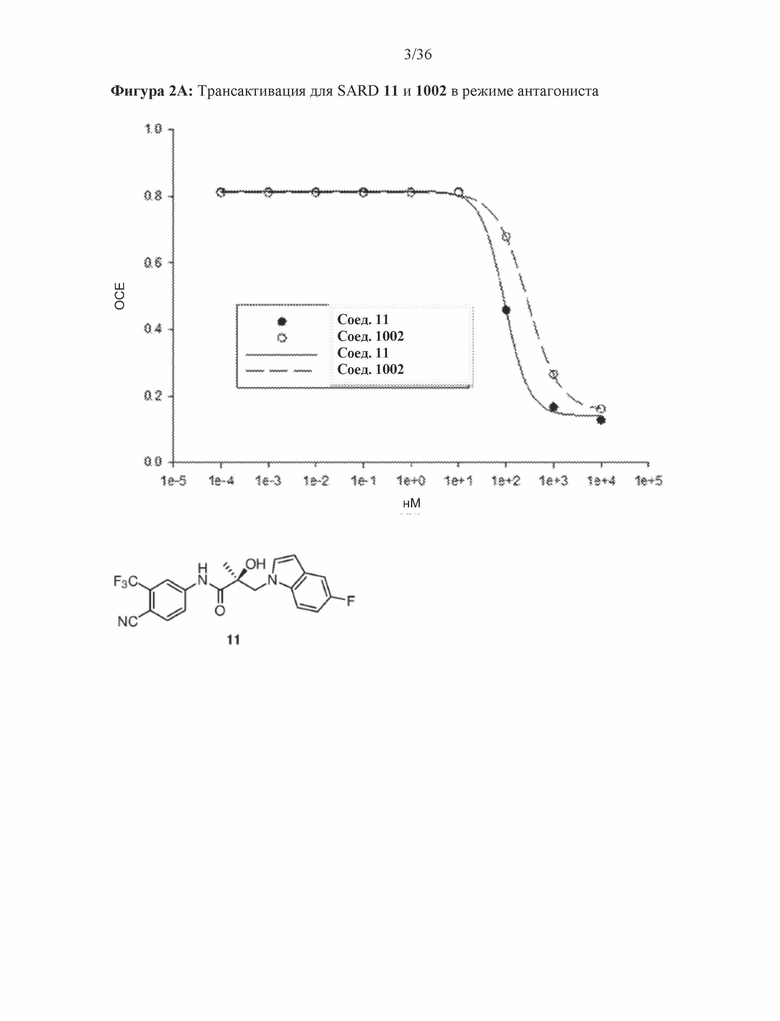
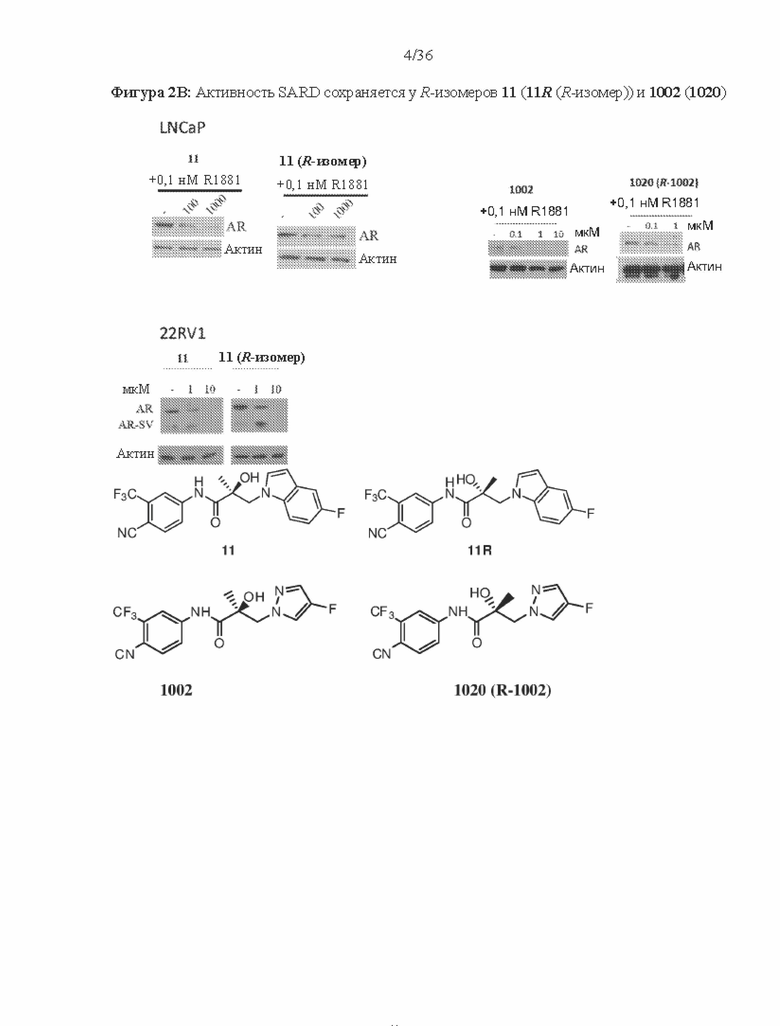
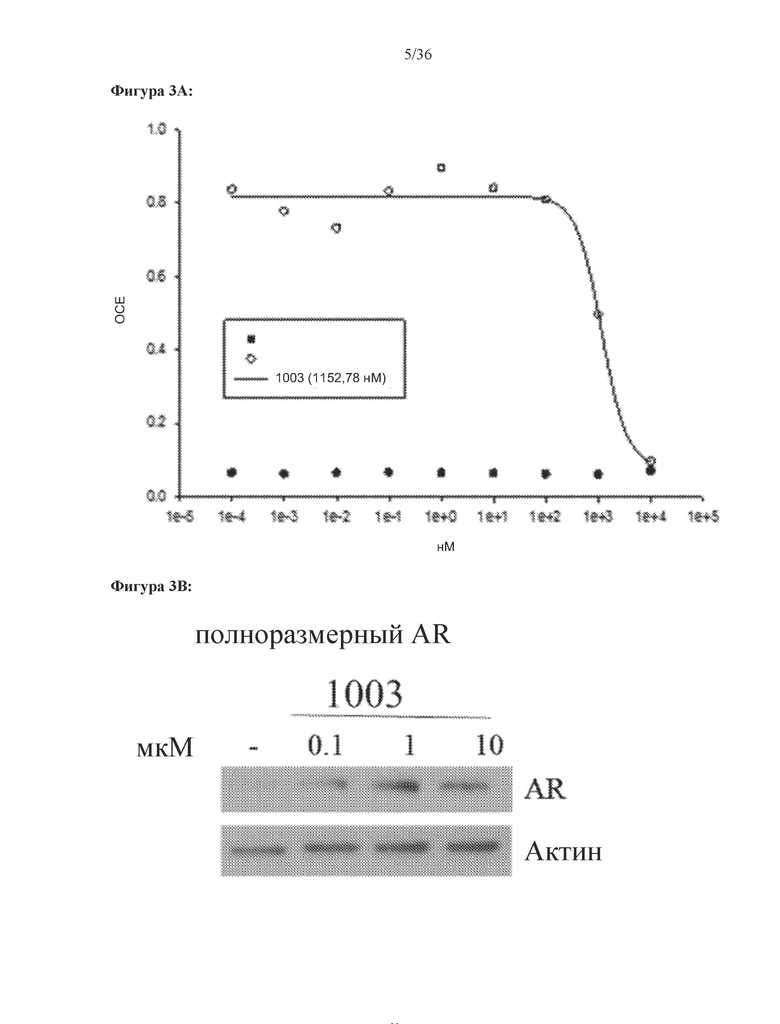
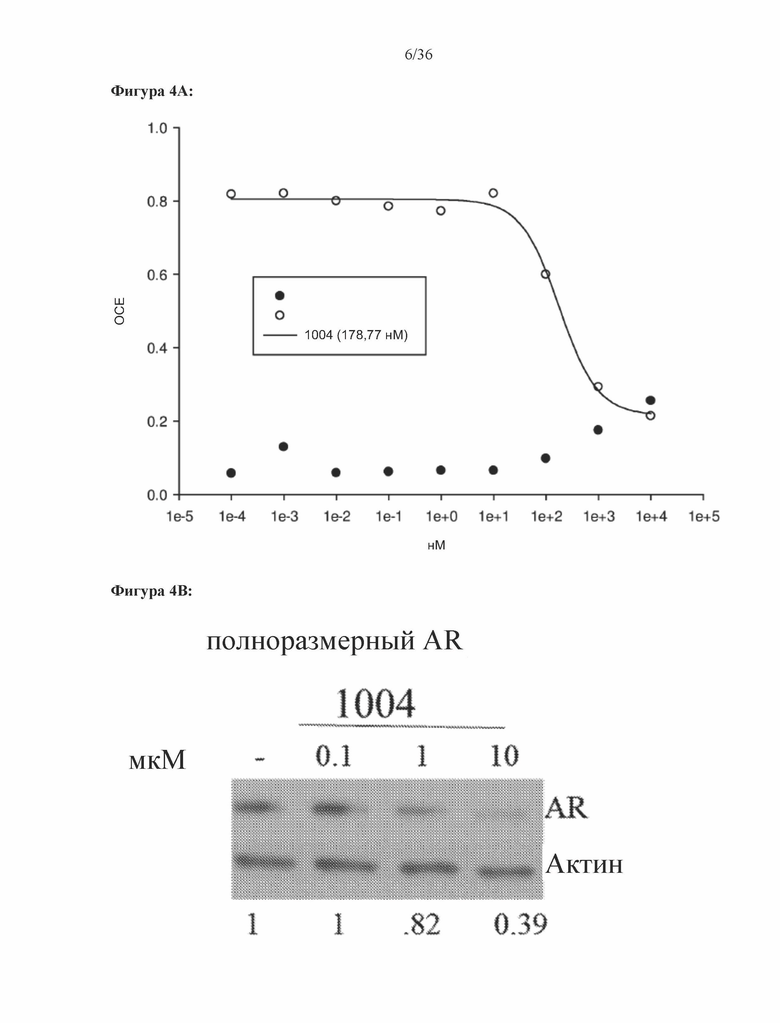
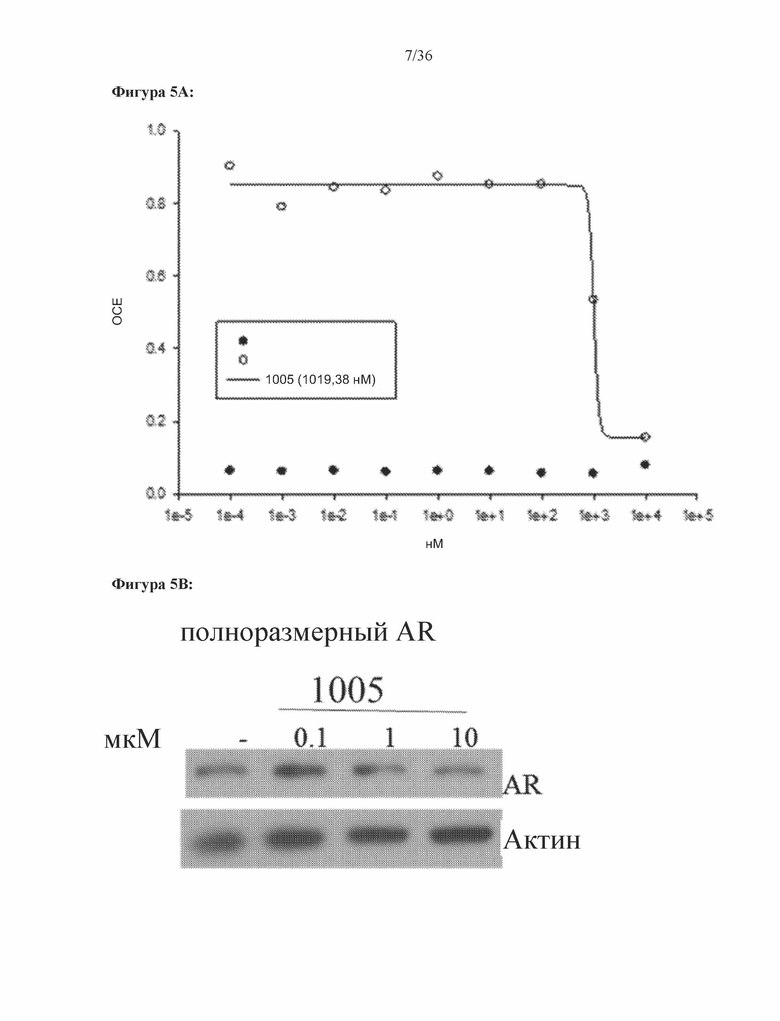
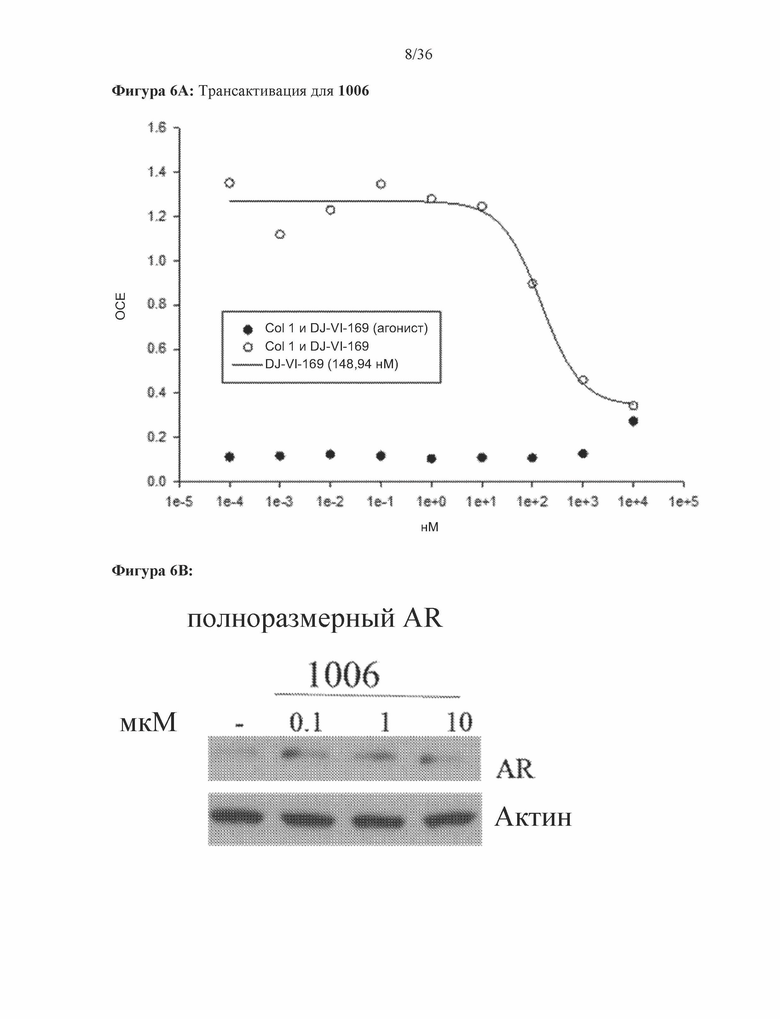
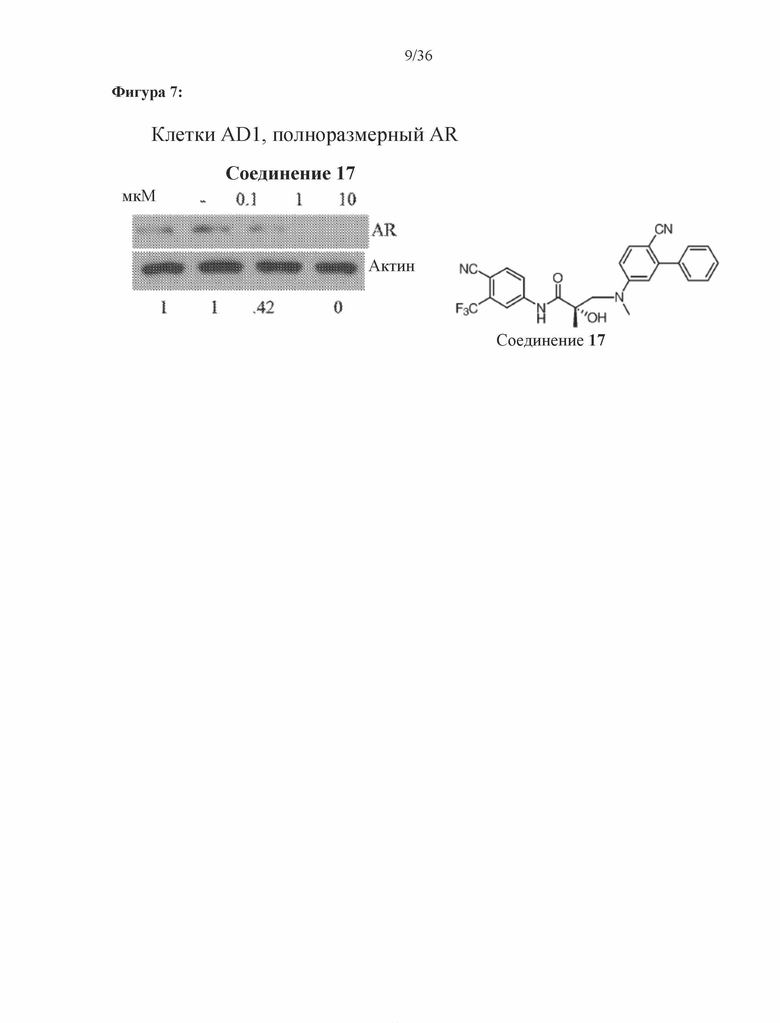
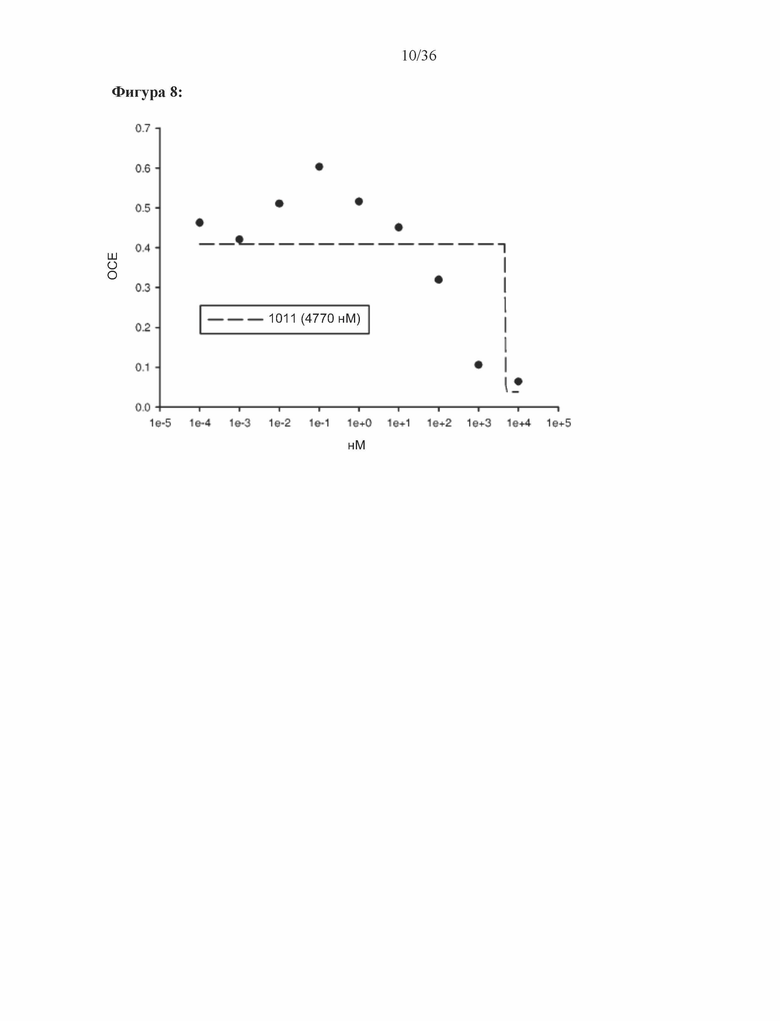
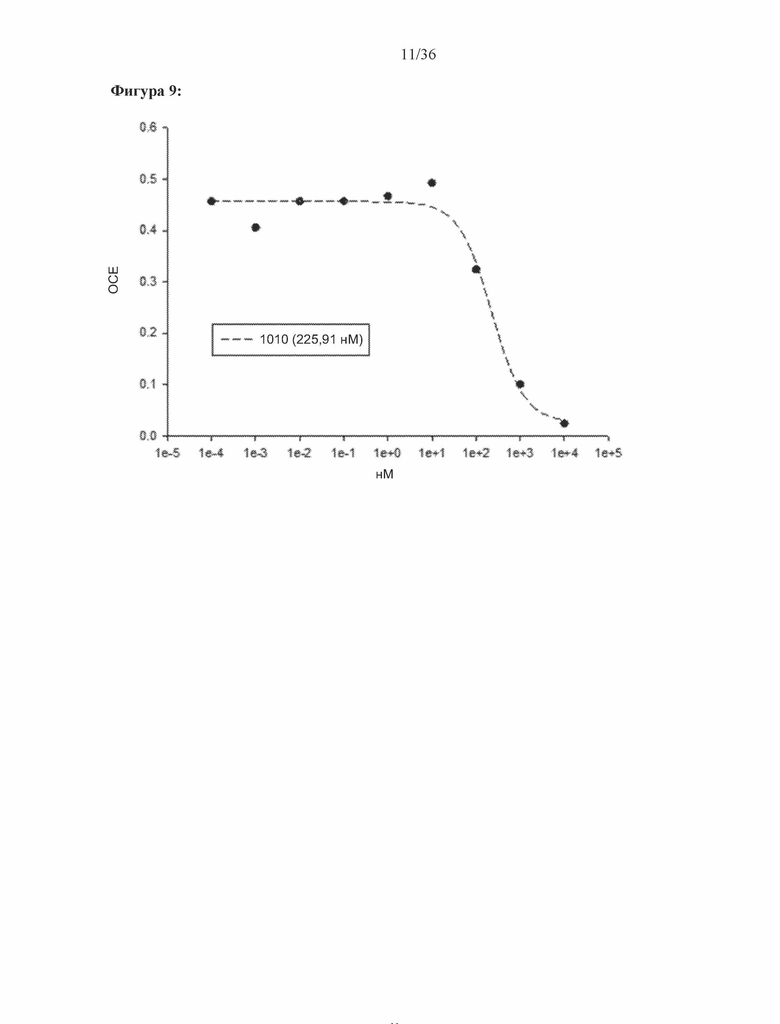
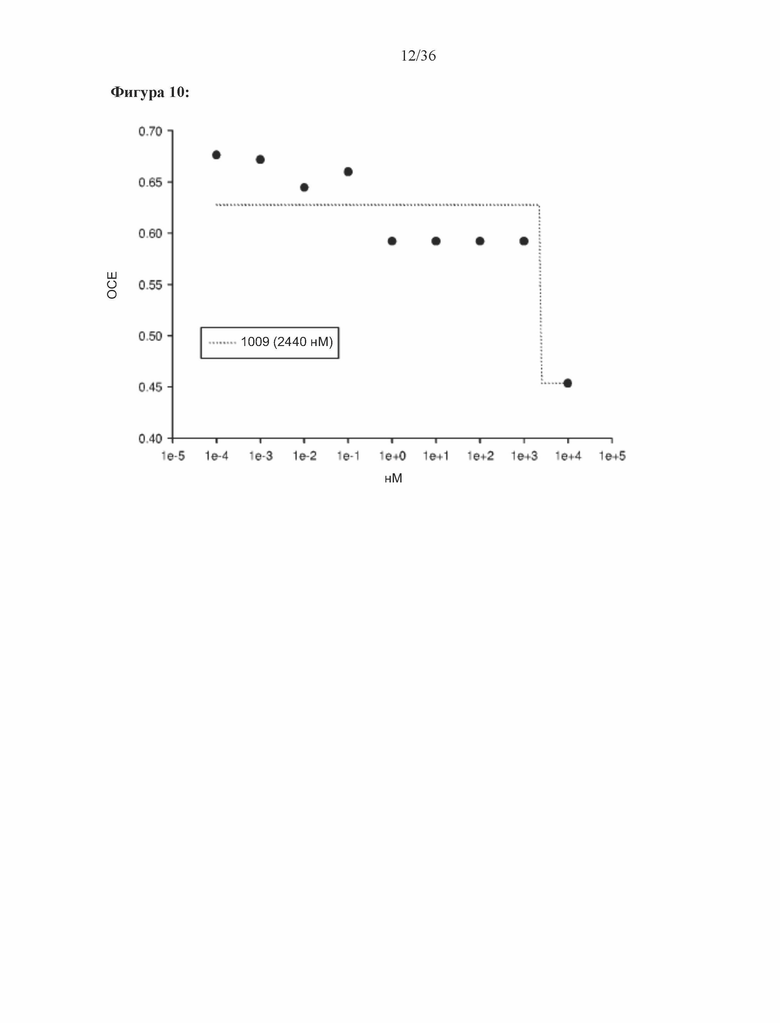

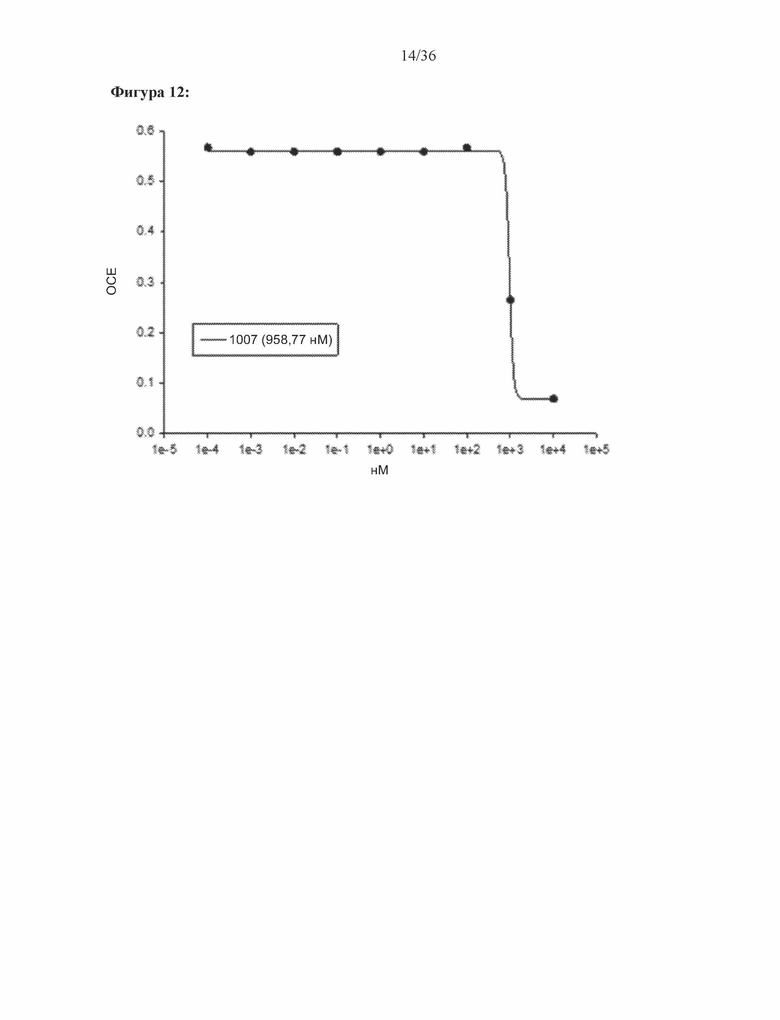
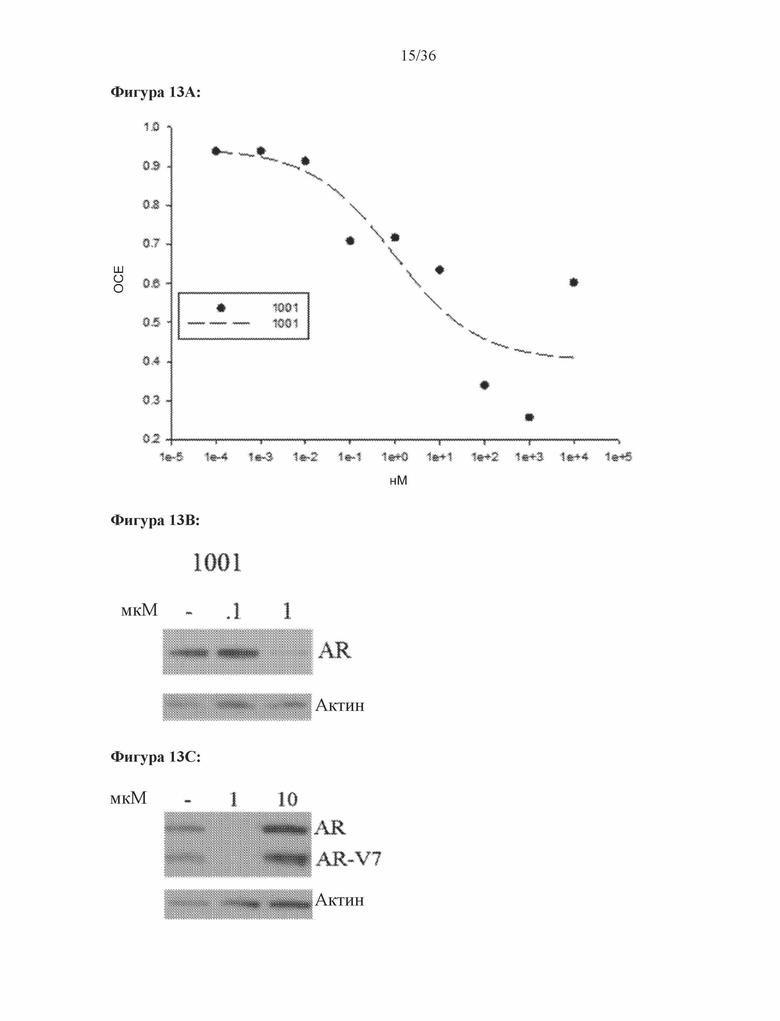
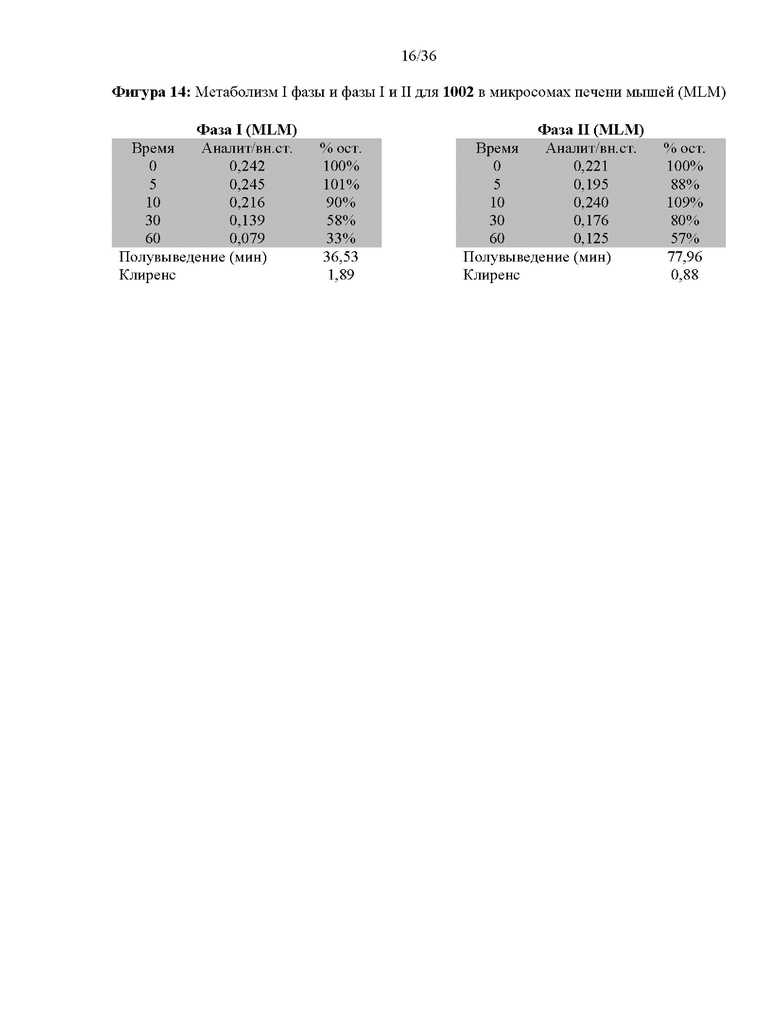
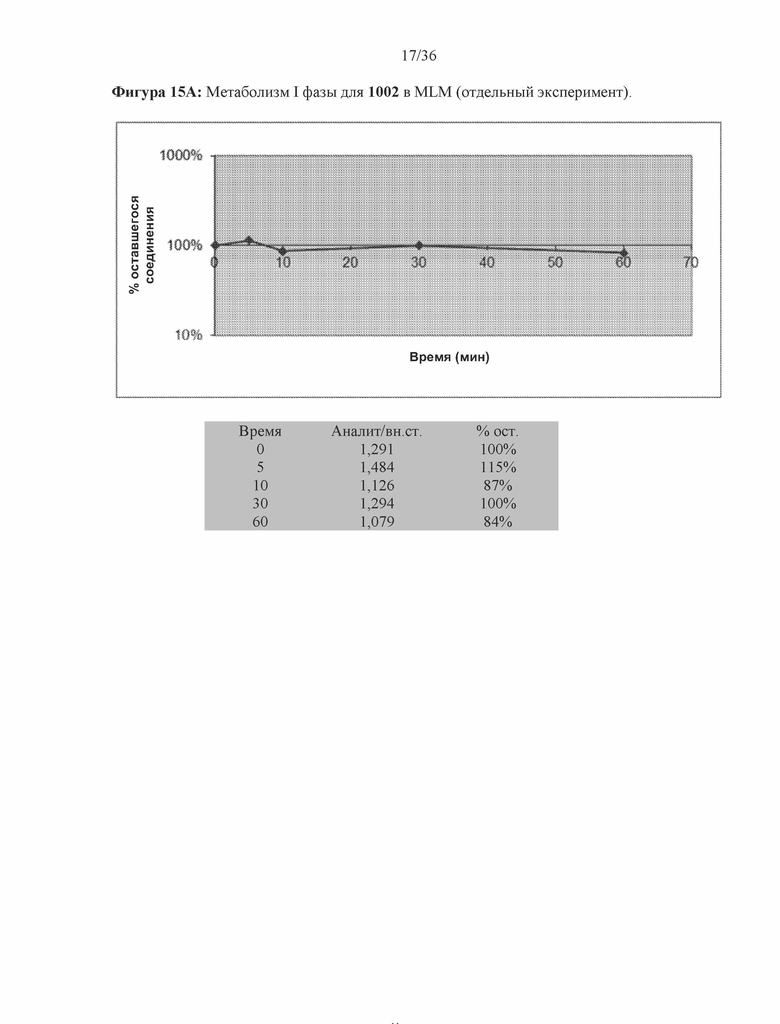
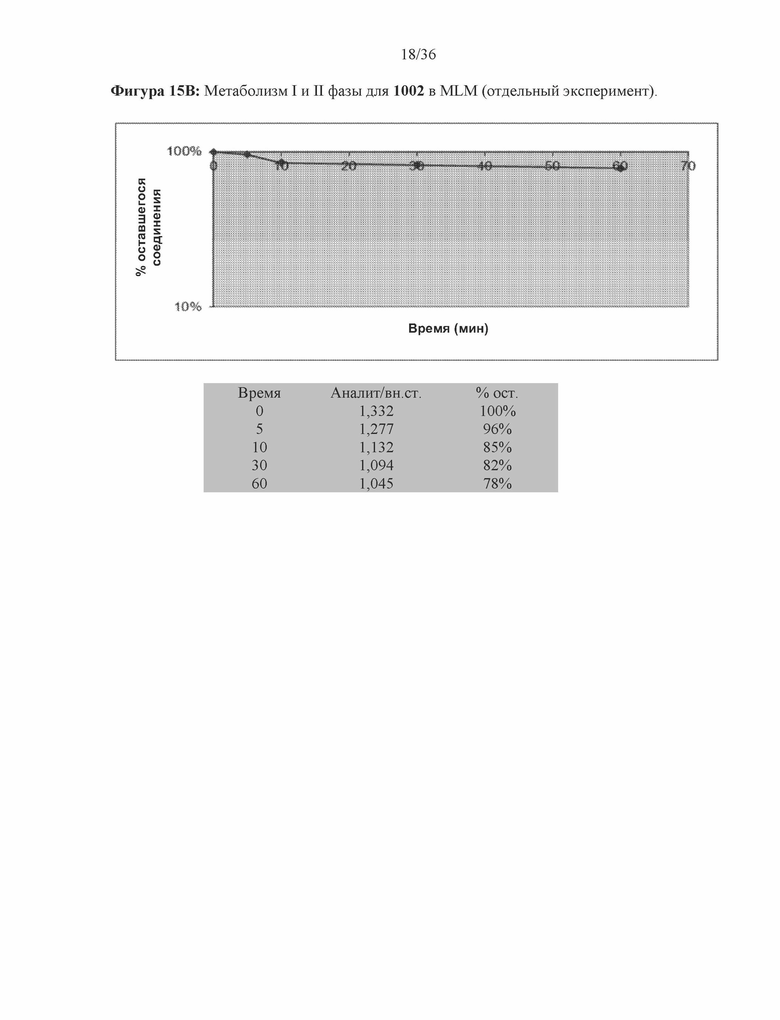
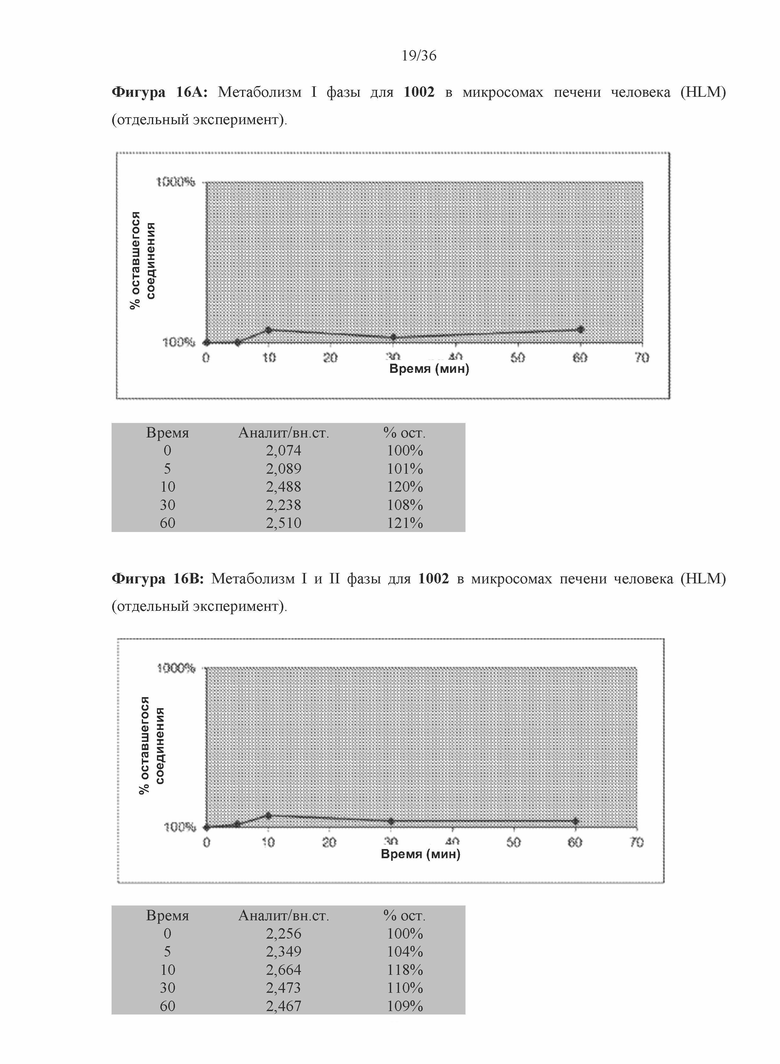
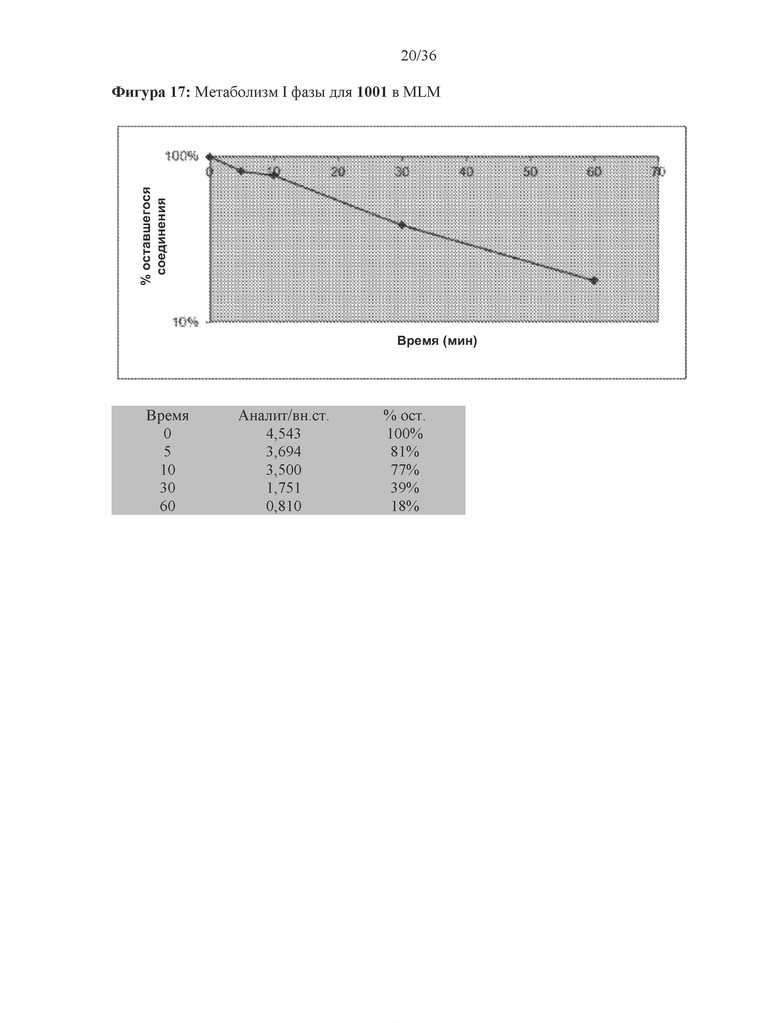
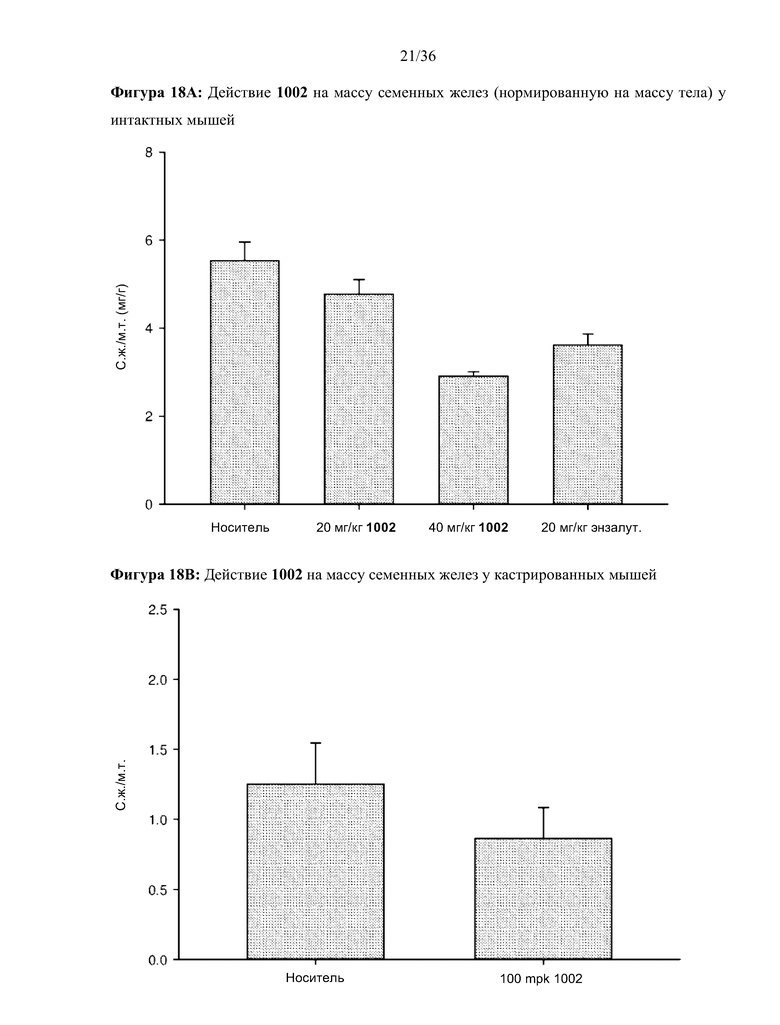
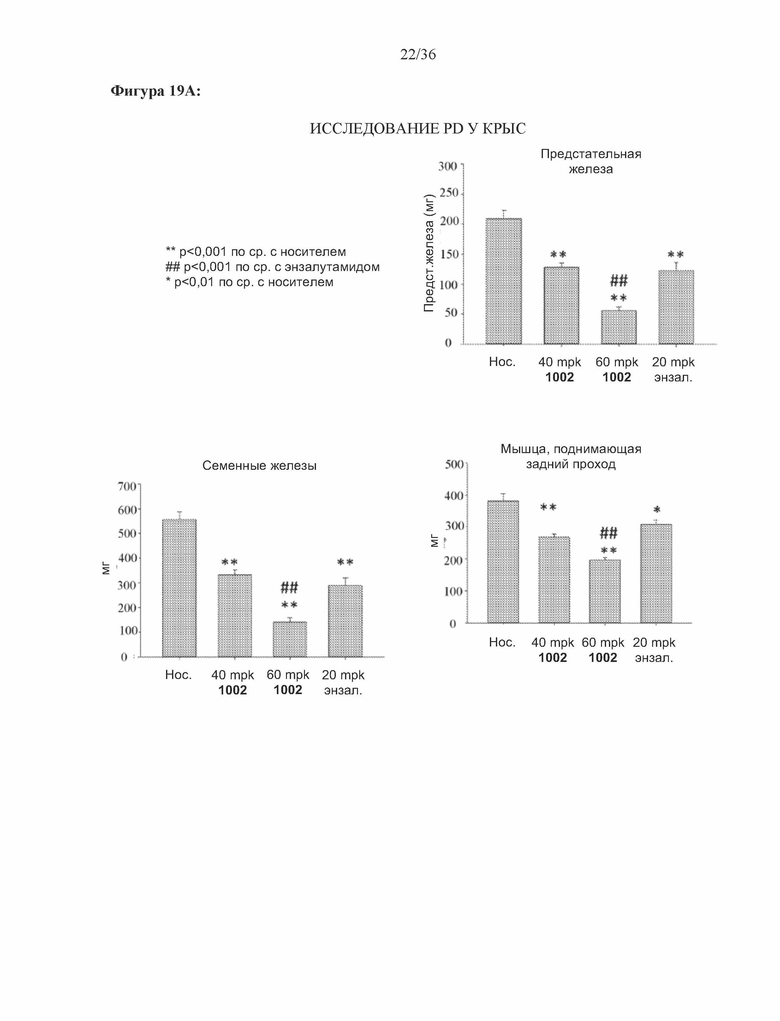
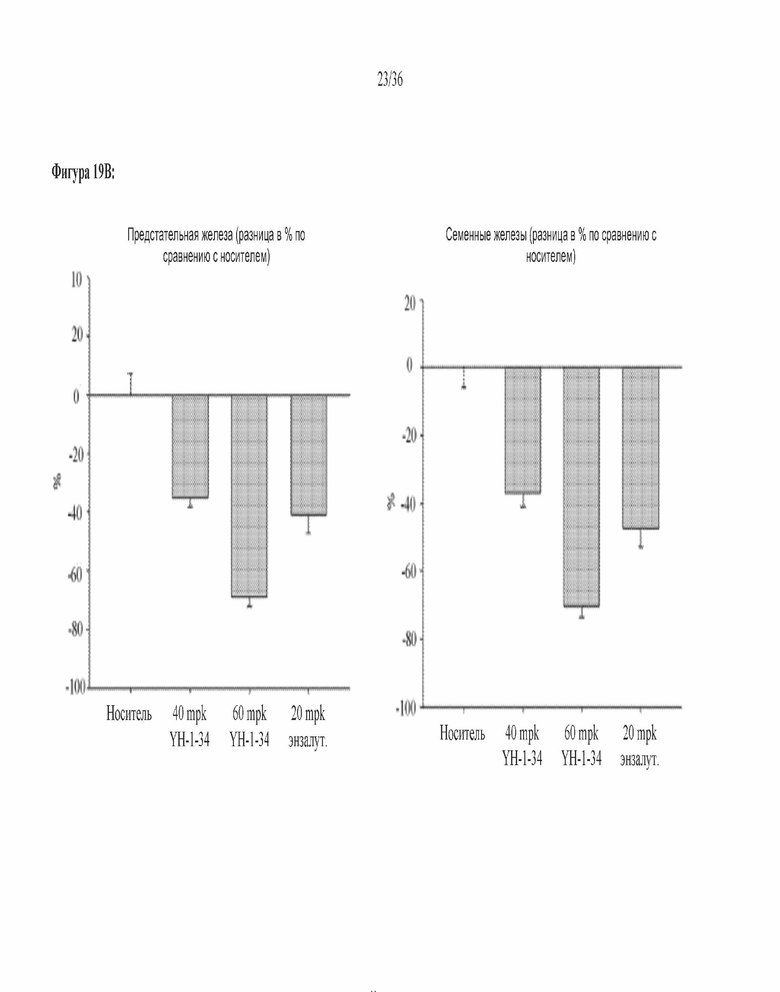
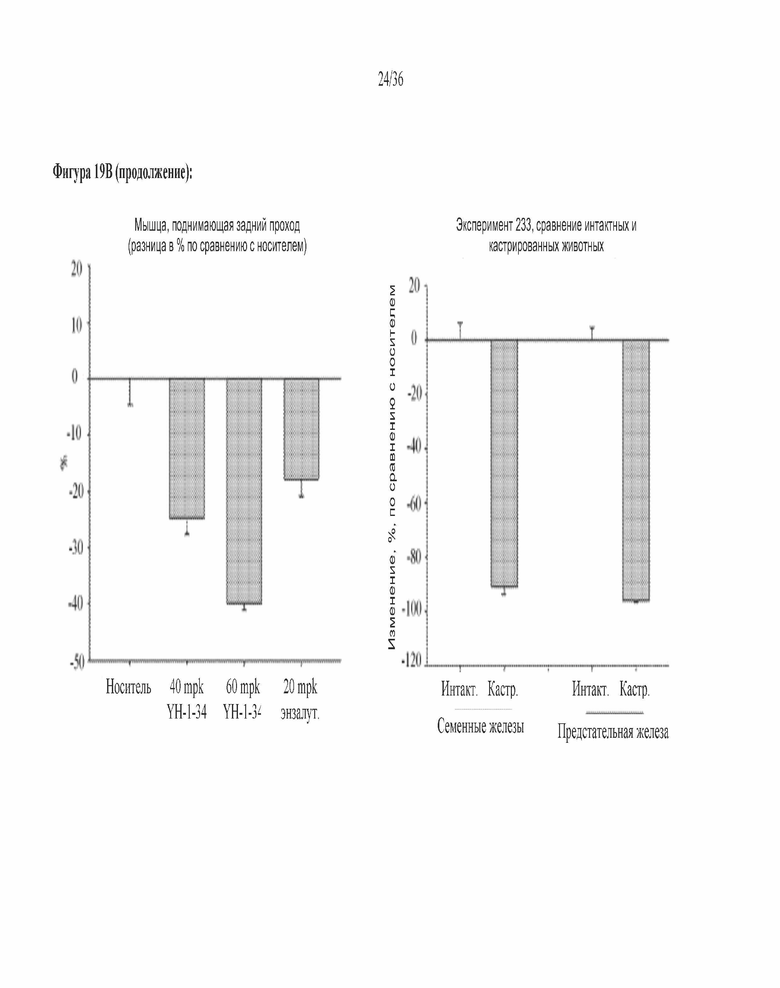
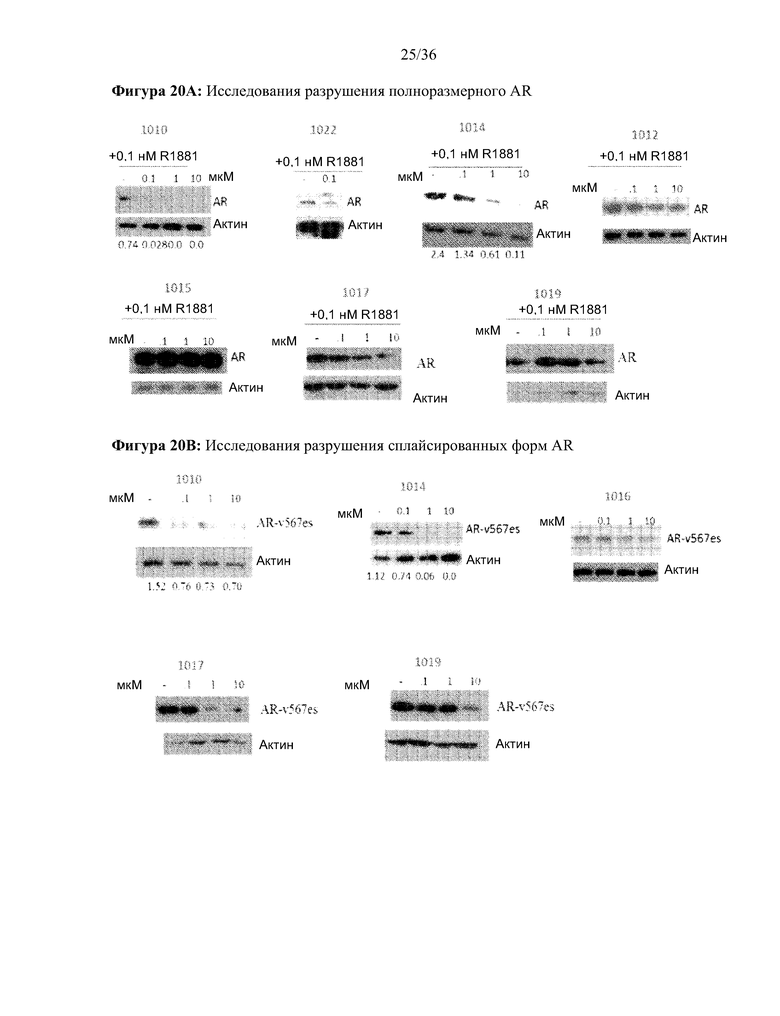
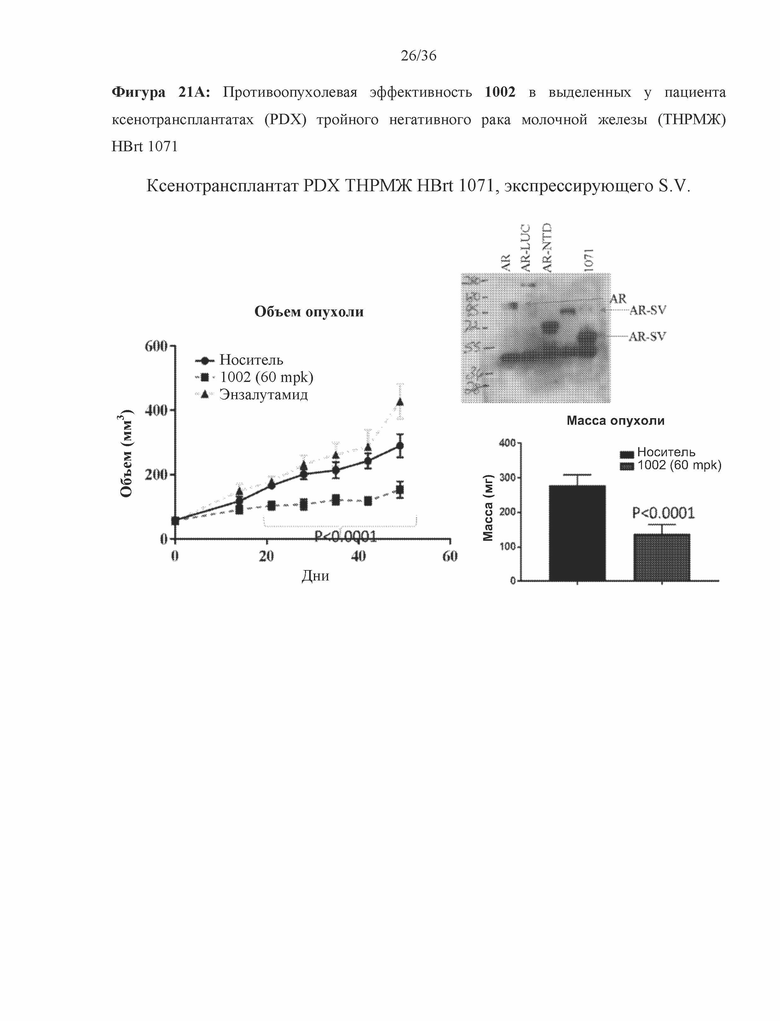
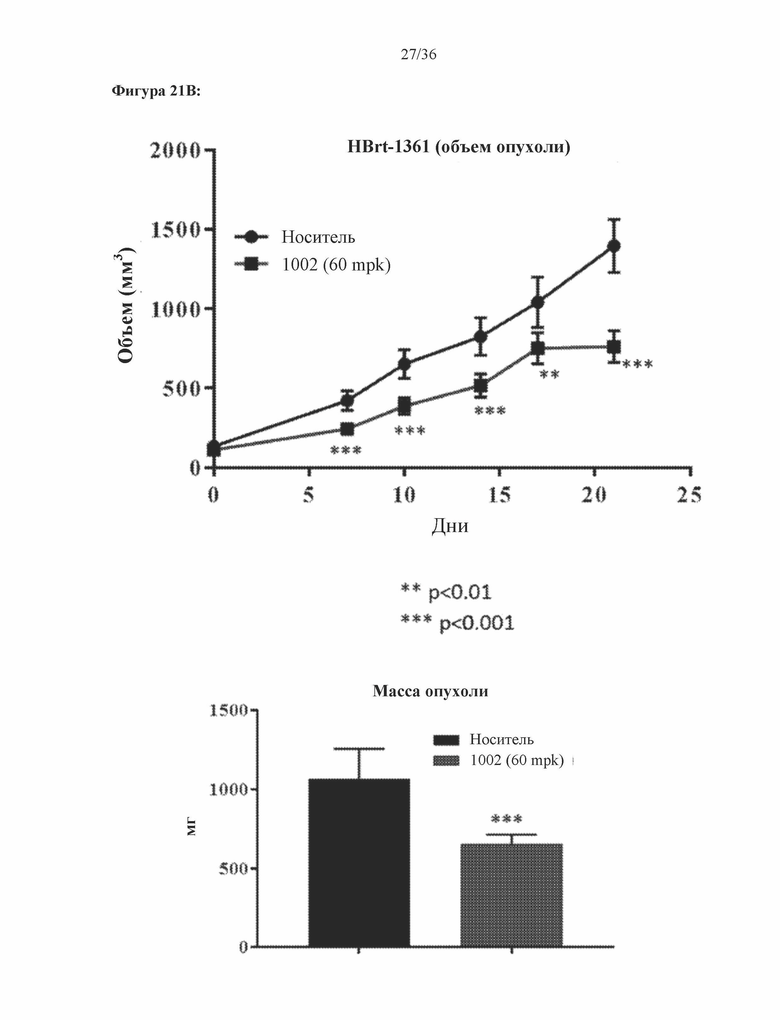
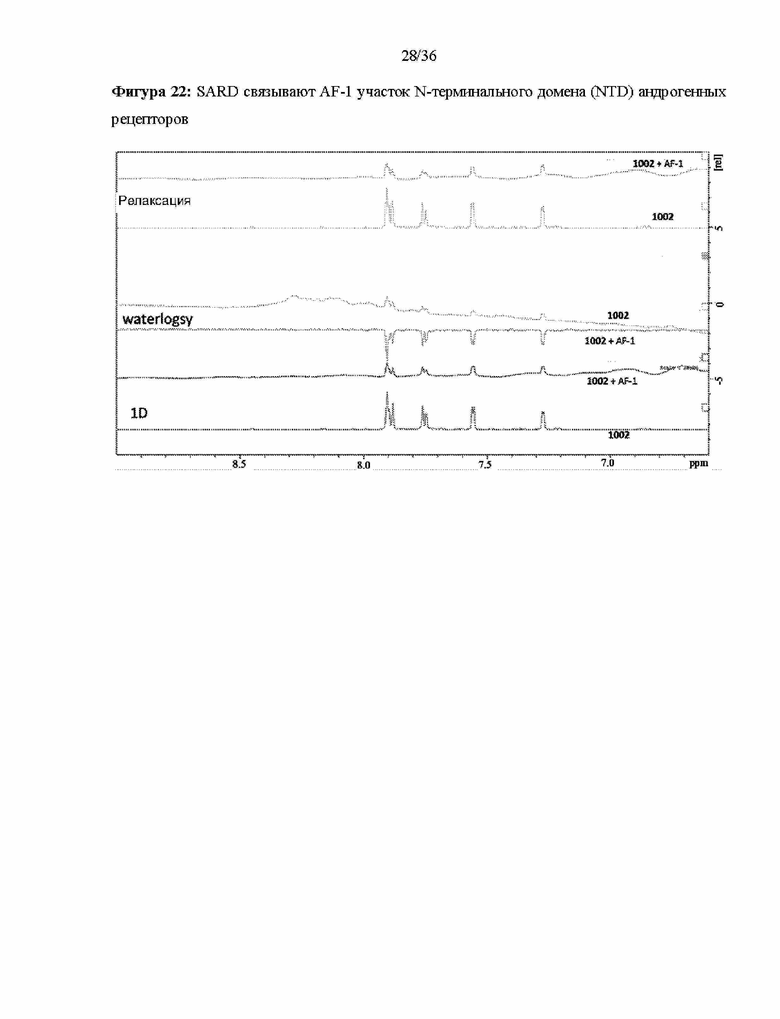
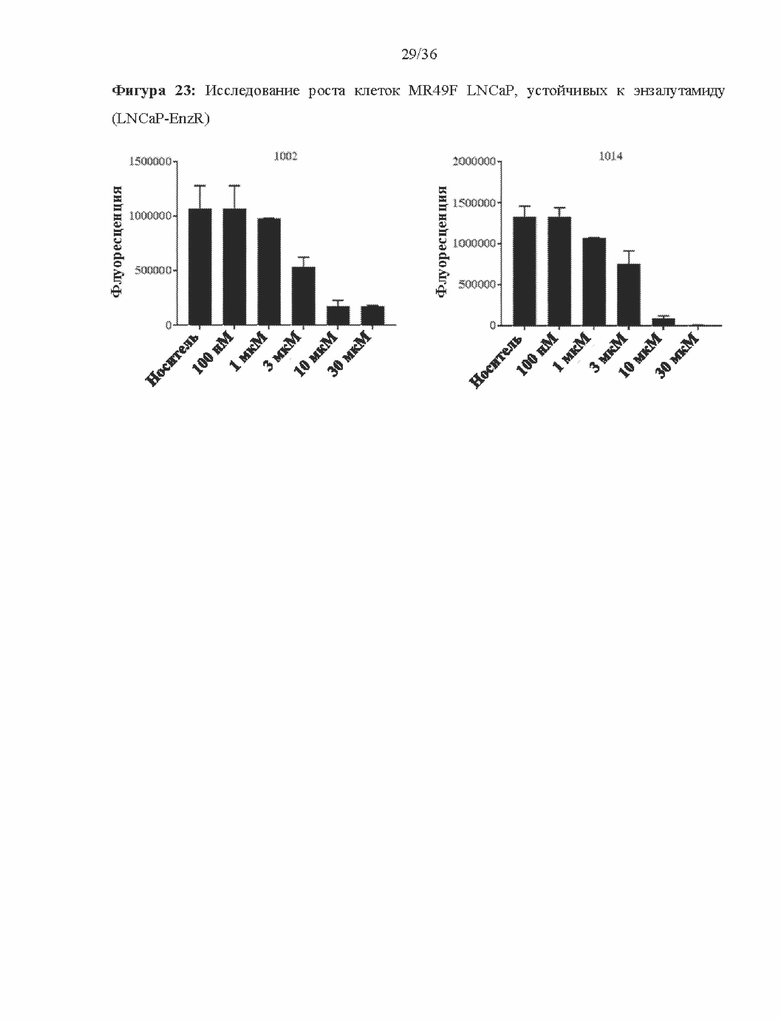
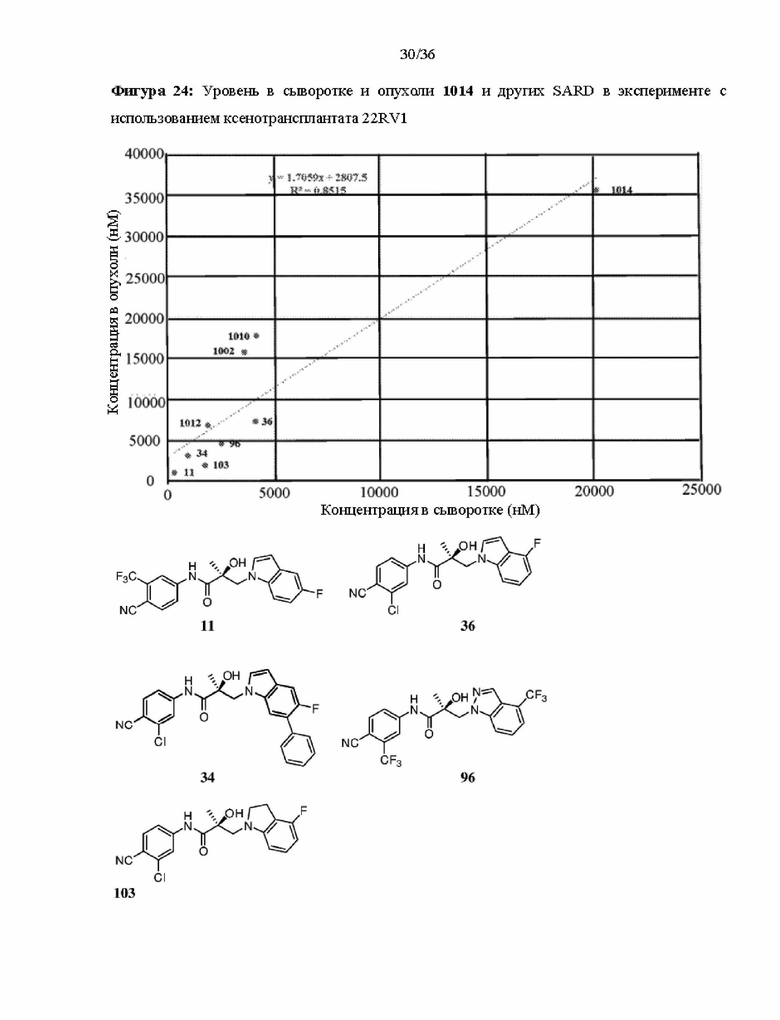
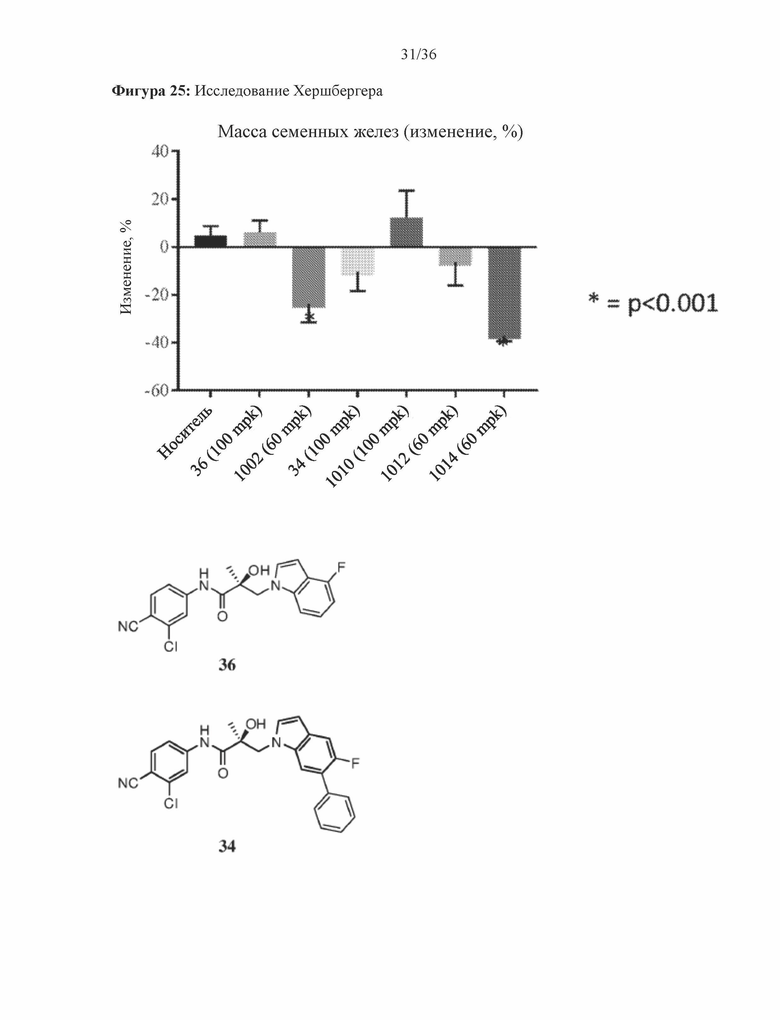
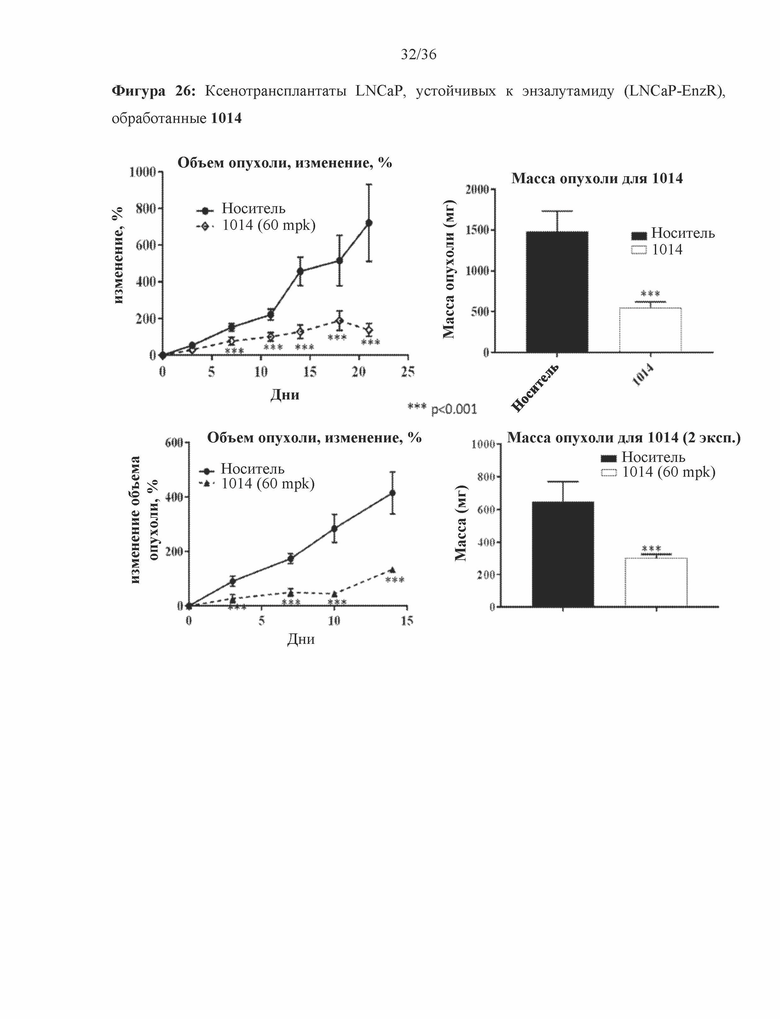
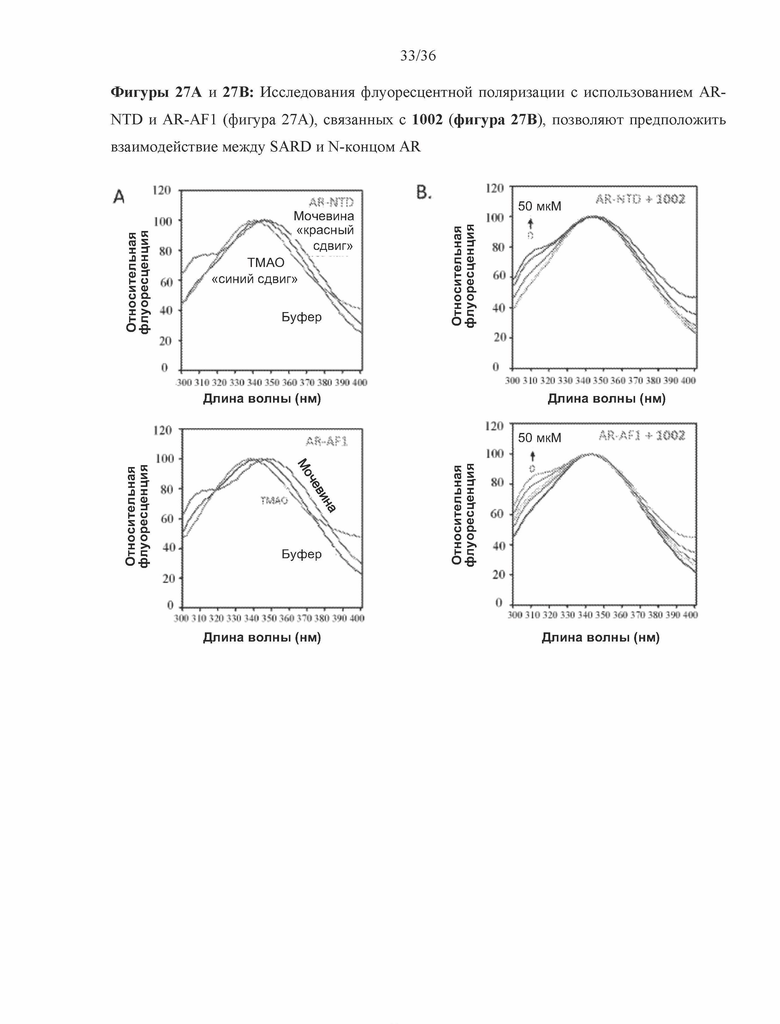
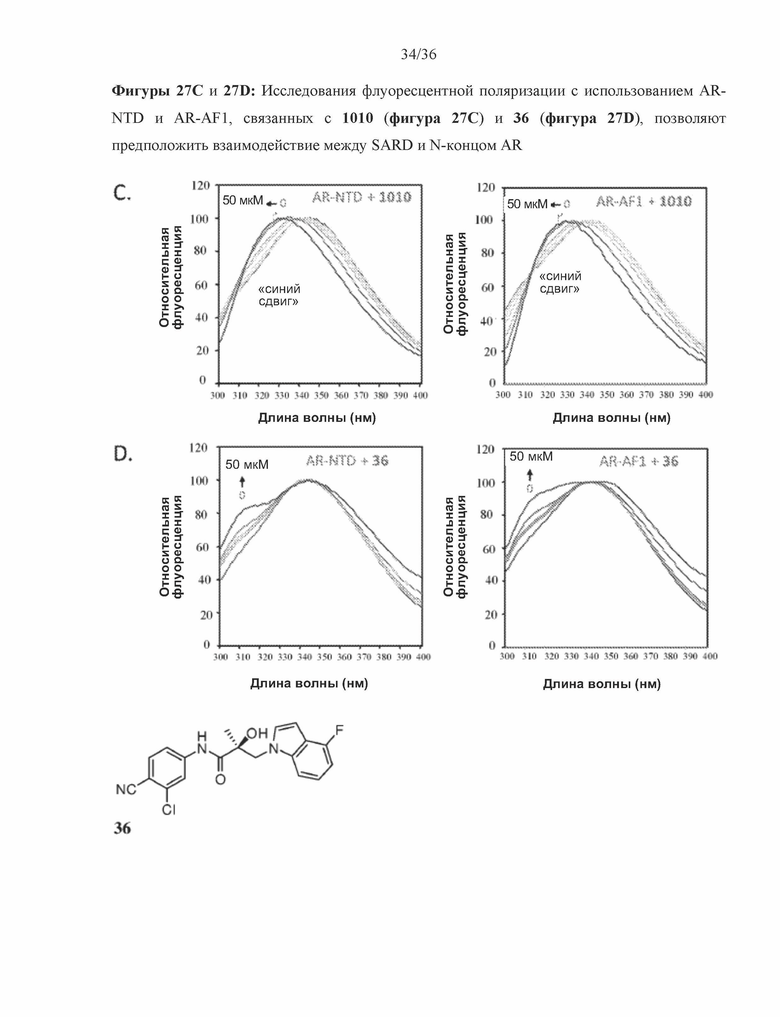
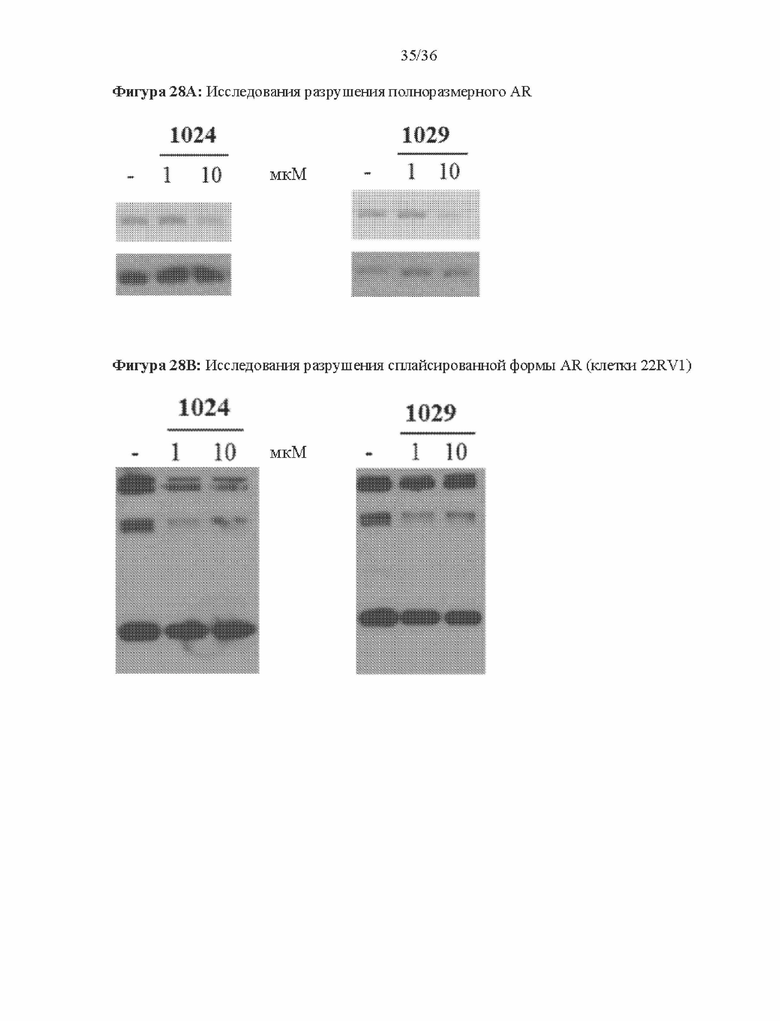
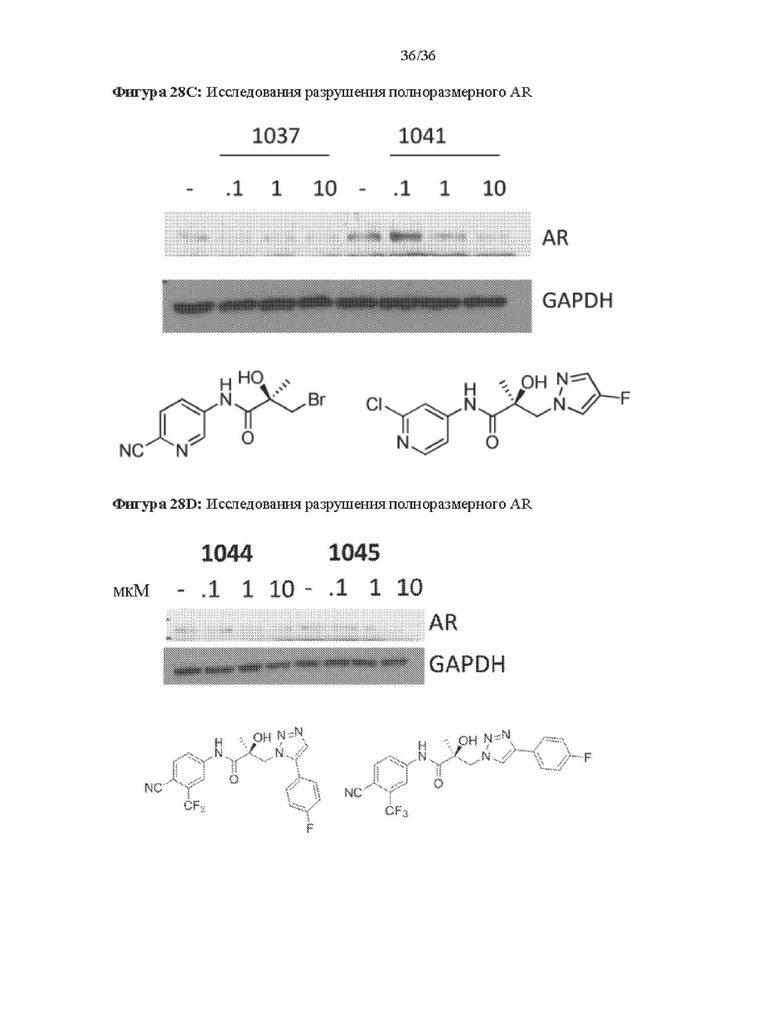
Изобретение относится к соединению, представленному структурой формулы I, где T представляет собой OH; R1 представляет собой CH3; Y представляет собой H, CF3, F, I, Br, Cl или CN; Z представляет собой H, NO2, CN, галогенид, COOH, COR, NHCOR или CONHR; X представляет собой CH или N; R представляет собой H, С1-С6 алкил или CH2Cl; A представляет собой R2; R2 представляет собой пиразольное, имидазольное или триазольное кольцо, незамещенное или замещенное по меньшей мере одним из Q1, Q2, Q3 или Q4, каждый из которых независимо выбран из водорода, линейного или разветвленного С1-С6 алкила, С1-С6 галогеналкила, фенила, F, Cl, Br, I, CN, NO2, OR, бензила, NHCOOR, N(R)2, NHCOR, CONHR, COOR или COR; где указанный фенил не замещен или замещен галогеном; или его оптический изомер или фармацевтически приемлемая соль. Изобретение относится к фармацевтической композиции, обладающей активностью селективного разрушения андрогенных рецепторов (SARD), содержащей терапевтически эффективное количество соединения SARD по изобретению или его оптический изомер или фармацевтически приемлемую соль и фармацевтически приемлемый носитель. Технический результат - соединениям, селективно разрушающие андрогенные рецепторы (SARD), на основе пиразола, имидазола, триазола для применения при лечении рака предстательной железы, рака предстательной железы, устойчивого к энзалутамиду и абиратренону, рака, чувствительного к андрогенным рецепторам (AR). 6 н. и 17 з.п. ф-лы, 4 табл., 49 ил., 10 пр.
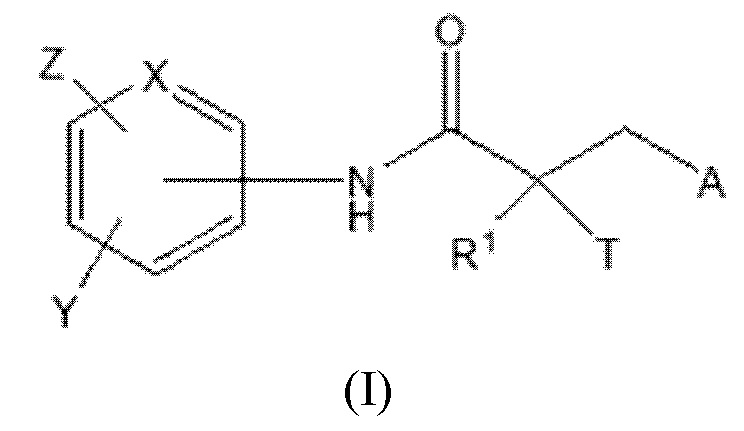
1. Соединение, селективно разрушающее андрогенные рецепторы (SARD), представленное структурой формулы I:
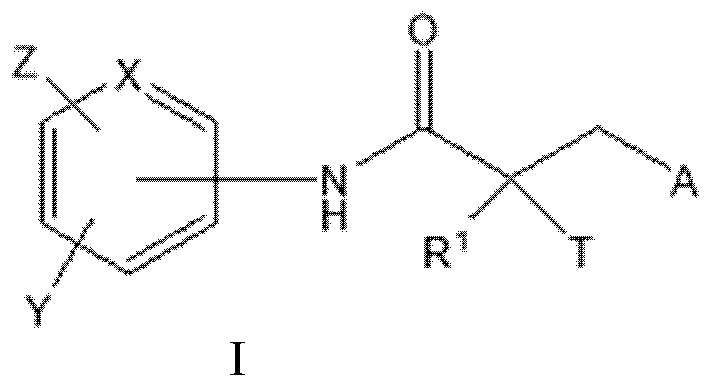
где
T представляет собой OH;
R1 представляет собой CH3;
Y представляет собой H, CF3, F, I, Br, Cl или CN;
Z представляет собой H, NO2, CN, галогенид, COOH, COR, NHCOR или CONHR;
X представляет собой CH или N;
R представляет собой H, С1-С6 алкил или CH2Cl;
A представляет собой R2;
R2 представляет собой пиразольное, имидазольное или триазольное кольцо, незамещенное или замещенное по меньшей мере одним из Q1, Q2, Q3 или Q4, каждый из которых независимо выбран из водорода, линейного или разветвленного С1-С6 алкила, С1-С6 галогеналкила, фенила, F, Cl, Br, I, CN, NO2, OR, бензила, NHCOOR, N(R)2, NHCOR, CONHR, COOR или COR; где указанный фенил не замещен или замещен галогеном;
или его оптический изомер или фармацевтически приемлемая соль.
2. Соединение, селективно разрушающее андрогенные рецепторы (SARD), по п.1, представленной структурой формулы IA:
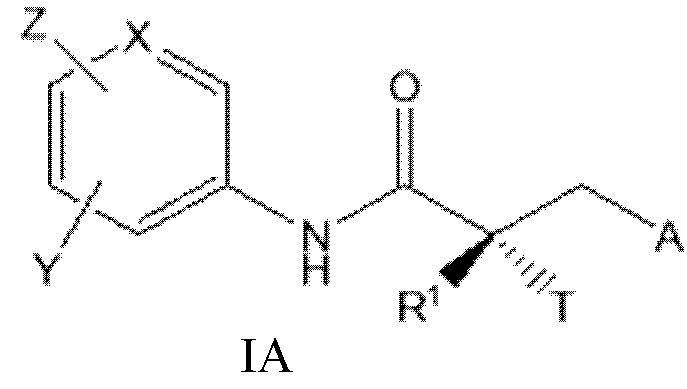
или его оптический изомер или фармацевтически приемлемая соль.
3. Соединение, селективно разрушающее андрогенные рецепторы (SARD), по п.1, представленной структурой формулы IB:
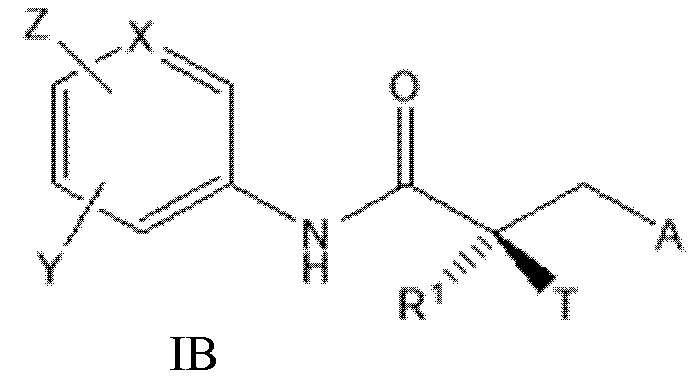
или его оптический изомер или фармацевтически приемлемая соль.
4. Соединение SARD по п.1, представленное структурой формулы II:
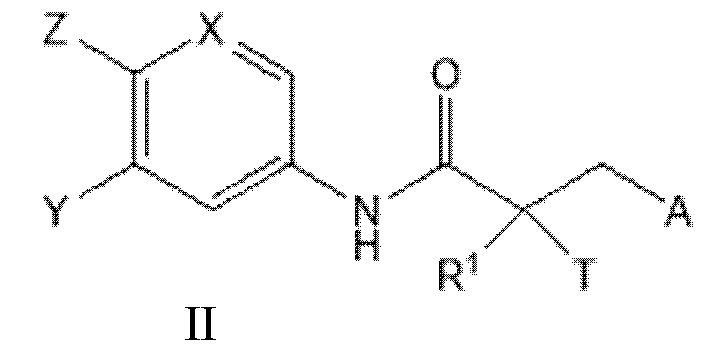
где
T представляет собой OH;
R1 представляет собой CH3;
Y представляет собой H, CF3, F, I, Br, Cl или CN;
Z представляет собой H, NO2, CN, галогенид, COOH, COR, NHCOR или CONHR;
X представляет собой CH или N;
R представляет собой H, С1-С6 алкил или CH2Cl;
A представляет собой R2;
R2 представляет собой пиразольное, триазольное или имидазольное кольцо, причем указанное кольцо не замещено или замещено по меньшей мере одним из Q1, Q2, Q3 или Q4, каждый из которых независимо выбран из водорода, линейного или разветвленного С1-С6 алкила, С1-С6 галогеналкила, фенила, F, Cl, Br, I, CN, NO2, OR, бензила, NHCOOR, N(R)2, NHCOR, CONHR, COOR или COR; где указанный фенил не замещен или замещен галогеном;
или его оптический изомер или фармацевтически приемлемая соль.
5. Соединение SARD по п.4, представленное структурой формулы IIA:
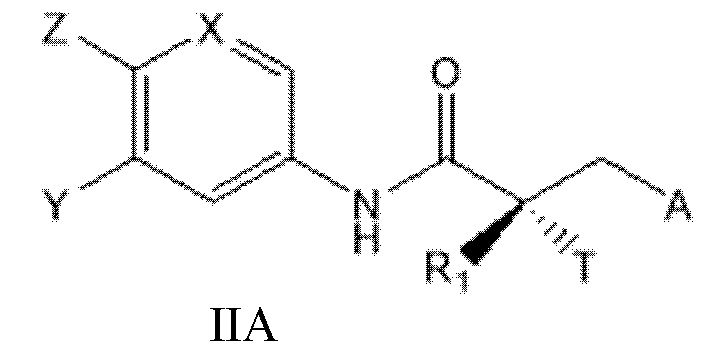
или его оптический изомер или фармацевтически приемлемая соль.
6. Соединение SARD по п.4, представленное структурой формулы IIB:
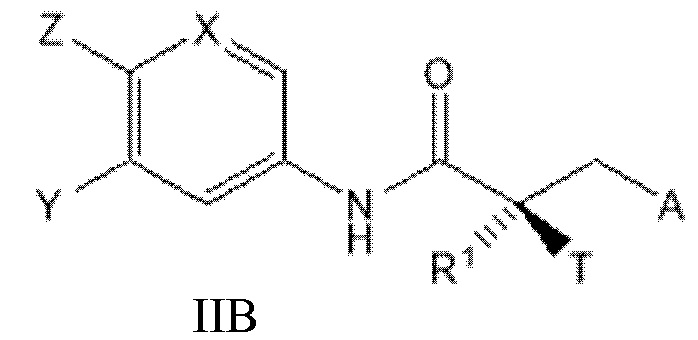
или его оптический изомер или фармацевтически приемлемая соль.
7. Соединение SARD по п.1, представленное структурой формулы VII:
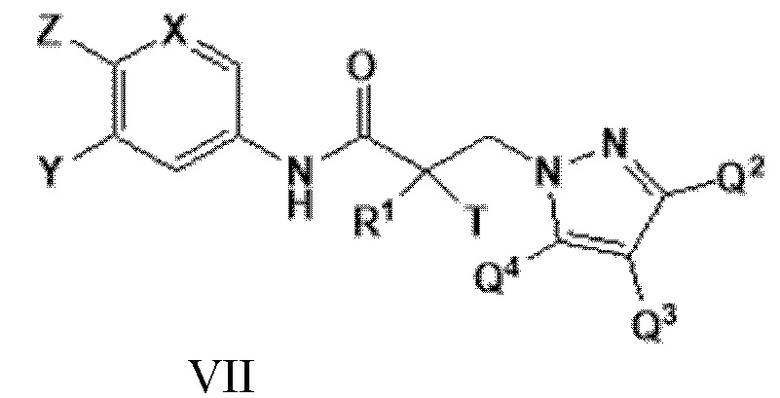
где
X представляет собой CH или N;
Y представляет собой H, CF3, F, I, Br, Cl или CN;
Z представляет собой H, NO2, CN, галогенид, COOH, COR, NHCOR или CONHR;
R1 представляет собой CH3;
T представляет собой OH;
R представляет собой H или С1-С6 алкил; и
каждый из Q2, Q3 или Q4 независимо выбран из водорода, линейного или разветвленного С1-С6 алкила, С1-С6 галогеналкила, фенила, F, Cl, Br, I, CN, NO2, OR, бензила, NHCOOR, N(R)2, NHCOR, CONHR, COOR или COR, где указанный фенил незамещен или замещен галогеном; или его оптический изомер или фармацевтически приемлемая соль.
8. Соединение SARD по п.7, представленное структурой формулы VIIA:
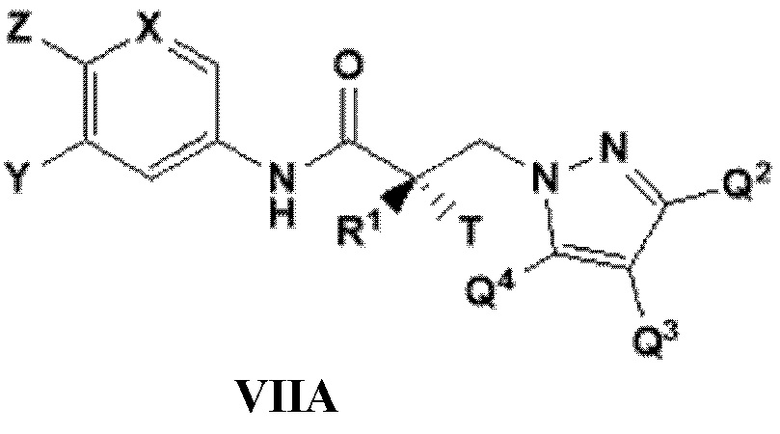
или его оптический изомер или фармацевтически приемлемая соль.
9. Соединение SARD по п.7, представленное структурой формулы VIIB:
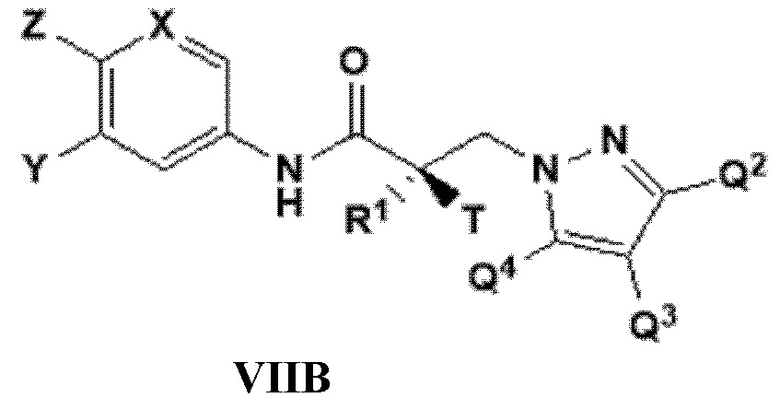
или его оптический изомер или фармацевтически приемлемая соль.
10. Соединение SARD по любому из пп. 1-9, отличающееся тем, что Q1, Q2, Q3 или Q4 представляет собой водород, CN, NO2, CF3, F, Cl, Br, I, NHCOOR, N(R)2, NHCOR, COR или фенил, не замещенный или замещенный галогеном.
11. Соединение SARD по п.1, представленное структурой любого из следующих соединений:
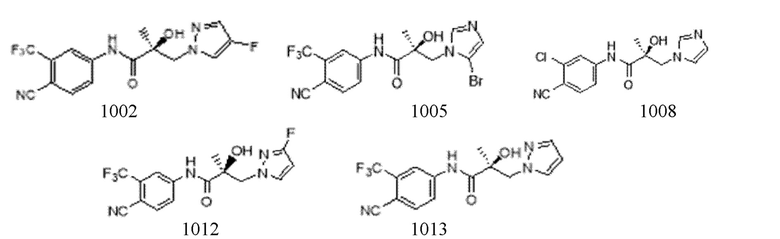
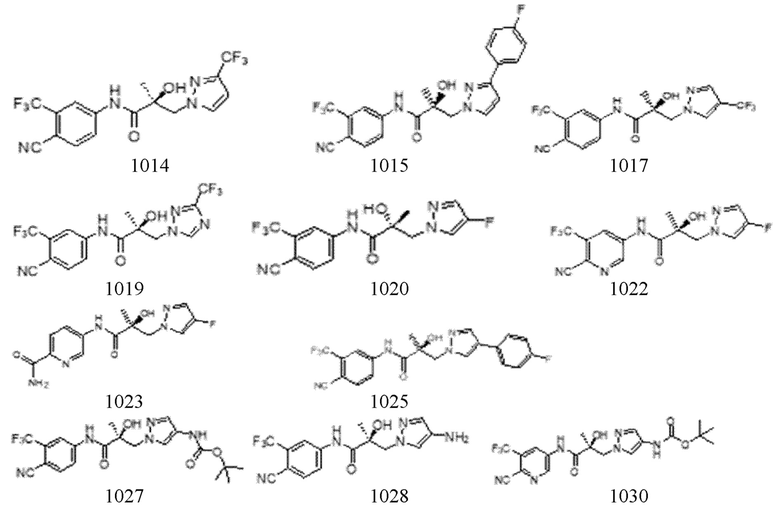
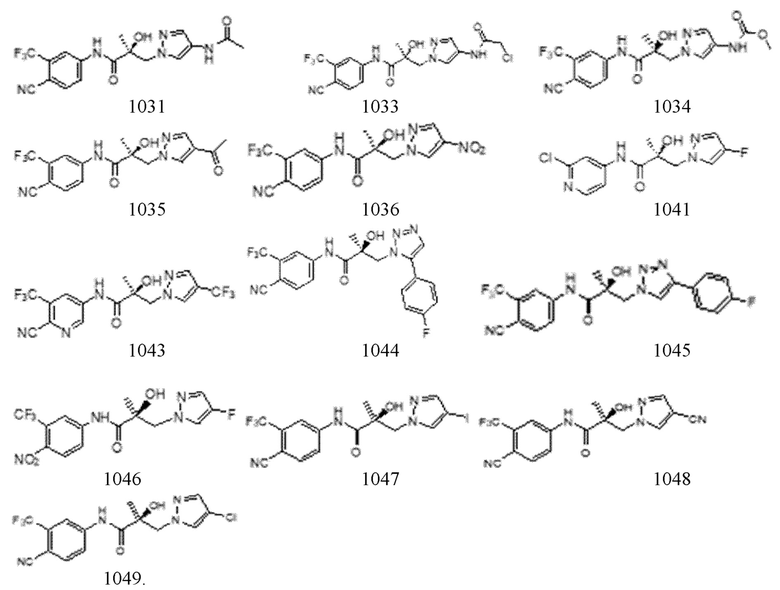
12. Соединение SARD по п.1, представляющее собой соединение 1002
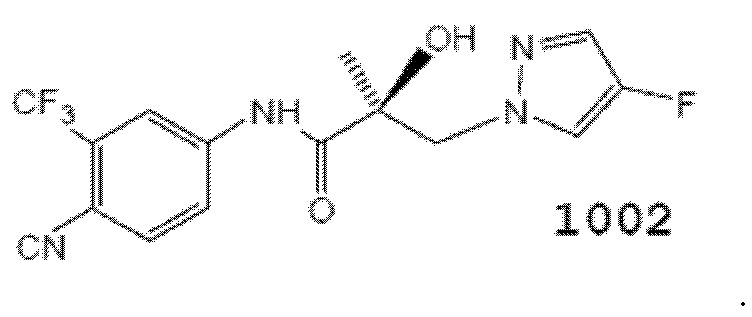
13. Фармацевтическая композиция, обладающая активностью селективного разрушения андрогенных рецепторов (SARD), содержащая терапевтически эффективное количество соединения SARD по любому из пп. 1-12 или его оптический изомер или фармацевтически приемлемую соль и фармацевтически приемлемый носитель.
14. Способ лечения рака предстательной железы (PCa) или увеличения выживаемости субъекта мужского пола, страдающего от рака предстательной железы, включающий введение субъекту терапевтически эффективного количества соединения по любому из пп. 1-12 или его оптического изомера или фармацевтически приемлемой соли.
15. Способ по п.14, отличающийся тем, что указанный рак предстательной железы представляет собой по меньшей мере одно из распространенного рака предстательной железы, не поддающегося лечению рака предстательной железы, устойчивого к кастрации рака предстательной железы (CRPC), метастатического CRPC (mCRPC), неметастатического CRPC (nmCRPC) или nmCRPC высокого риска.
16. Способ по пп. 14 или 15, дополнительно включающий проведение андрогенной депривационной терапии (АДТ).
17. Способ по любому из пп. 14-16, отличающийся тем, что указанный рак предстательной железы устойчив к лечению антагонистом(-ами) андрогенных рецепторов.
18. Способ по п.17, отличающийся тем, что указанный антагонист андрогенных рецепторов представляет собой по меньшей мере одно из энзалутамида, бикалутамида, абиратерона, ARN-509, ODM-201, EPI-001, EPI-506, AZD-3514, галетерона, ASC-J9, флутамида, гидроксифлутамида, нилутамида, ципротерона ацетата, кетоконазола или спиронолактона.
19. Способ лечения устойчивого к энзалутамиду рака предстательной железы у субъекта, включающий введение субъекту терапевтически эффективного количества соединения по любому из пп. 1-12 или его оптического изомера или фармацевтически приемлемой соли.
20. Способ лечения устойчивого к абиратерону рака предстательной железы, включающий введение субъекту терапевтически эффективного количества соединения по любому из пп. 1-12 или его оптического изомера или фармацевтически приемлемой соли.
21. Способ лечения рака, чувствительного к андрогенным рецепторам (AR) у субъекта, включающий введение субъекту терапевтически эффективного количества фармацевтической композиции по п.13.
22. Способ по п.21, отличающийся тем, что указанный рак представляет собой по меньшей мере одно из рака молочной железы, рака яичек, раковых заболеваний, связанных с частичным синдромом нечувствительности к андрогенам (PAIS), таких как гонадальные опухоли и семинома, рака матки, рака яичников, рака фаллопиевых труб или брюшной полости, рака слюнных желез, рака мочевого пузыря, урогенитального рака, рака мозга, рака кожи, лимфомы, мантийноклеточной лимфомы, рака печени, печеночноклеточной карциномы, рака почки, почечноклеточной карциномы, остеосаркомы, рака поджелудочной железы, рака эндометрия, рака легкого, немелкоклеточного рака легкого (НМРЛ), рака желудка, рака толстой кишки, перианальной аденомы или рака центральной нервной системы.
23. Способ по п.22, отличающийся тем, что указанный рак молочной железы представляет собой тройной негативный рак молочной железы.
| СПОСОБ ПРОИЗВОДСТВА ВЕРМИШЕЛИ БЫСТРОГО ПРИГОТОВЛЕНИЯ И УПАКОВКА ВЕРМИШЕЛИ БЫСТРОГО ПРИГОТОВЛЕНИЯ | 1999 |
|
RU2159049C1 |
| US 20100331418 A1, 30.12.2010 | |||
| WO 2003074473 A2, 12.09.2003 | |||
| WO 2008044033 A1, 17.04.2008 | |||
| EP 253503 A2, 20.01.1988 | |||
| Местное применение антиандрогена от выпадения волос и других гиперандрогенных состояний | 2000 |
|
RU2225390C2 |
| WO 2013064681 A1, 10.05.2013 | |||
| US 20070265290 A1, 15.11.2007 | |||
| WO 2008137038 A1, 13.11.2008 | |||
| Mohler, M | |||
| L., Coss, C | |||
| C., Duke, C | |||
| B., Patil, S | |||
| A., Miller, D | |||
| D., & Dalton, J | |||
| T | |||
Авторы
Даты
2023-05-03—Публикация
2017-06-12—Подача