Изобретение относится к соединениям из класса производных изатина, обладающих противоопухолевой активностью в отношении опухолевых клеток.
Настоящее изобретение относится к производным гидразина, соединенными с двумя остатками N-замещенных изатина посредством азометиновой связи к их фармацевтически приемлемым солям, которые могут быть использованы в качестве противораковых препаратов. Настоящее изобретение также относится к фармацевтическим средствам, содержащим указанные соединения. Изобретение может быть использовано в медицине, фармацевтической промышленности, биохимии и биологических исследованиях по оценке пролиферативной активности и выживаемости опухолевых клеток.
Химические вещества на основе изатина используются в фармацевтической промышленности (Hua Guo et.al. Med / Chem. 2020; 20(16):1499-1503 [1]; [2] Hany S Ibrahim et.al. Eur. J. Med. Chem. 2016 Jan 27;108:415-422 [2]; Yani Hou et.al. Eur. J. Med. Chem. 2016 Jan 27; 108: 415-422 [3]).
Ядро изатина встроено в различные бис-изатиновые соединения. Известны комбинации бис-изатинов, обладающие биологической активностью по отношению к различным типам мишеней внутри клеток. Например, сунитиниб (ингибитор тирозинкиназы и ингибитор VEGF-рецепторов), интеданиб ингибитор сразу 3-х ростовых факторов (VEGFR, PDGFR и FGFR) (Chengyuan Liang et.al. Europen Journal of Medicinal Chemistry. 74, 2014, 742-750 [4]).
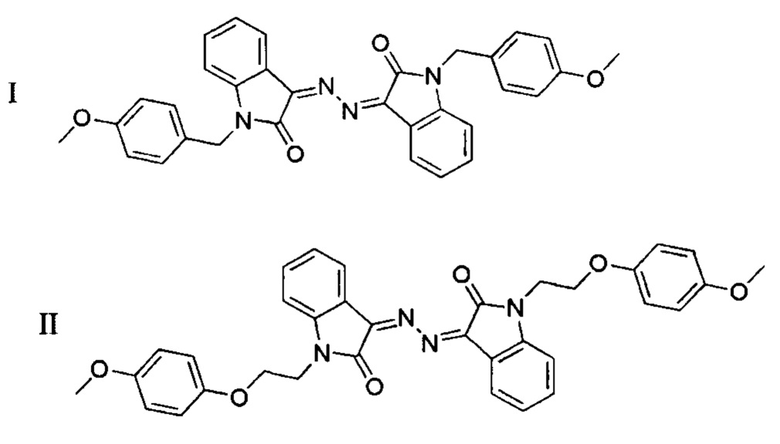
Известны производные бис-изатина и изатина, содержащие гидразидный фрагмент, которые проявляют анти-пролиферативный эффект в отношении различных раковых клеточных линий, описанные в работе [2], их структура:
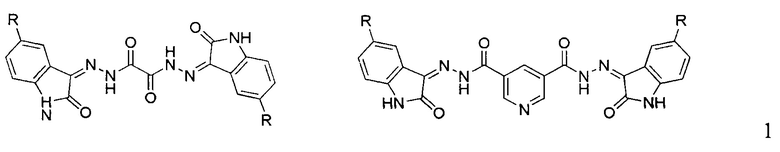
Заявляемые соединения по структуре отличаются от них тем, что они содержат лишь один остаток гидразина.
В качестве аналога и прототипа рассмотрены более близкие по структуре соединения изатина.
Известны производные бис-изатина (N,N'-гидразино-бис-изатина), описанные в патенте US 20120252860 А1, которые обладают противопухолевой активностью в отношении раковых клеток [5]. Один из приведенных в указанном патенте препаратов представляет собой производное, в котором оба остатка изатина имеют заместитель (фенил) у атома азота - 3,3'-(гидразин-1,2-диилиден)бис(1-фенилиндолин-2-он) (структура 2). Показатель IC50 (концентрация, которая приводит к гибели 50% клеток, оцененная по снижению метаболической активности) этого соединения равен 25,56±2,39 миллимоля. Наиболее активный из описанных в упоминаемом патенте препаратов, содержащий один заместитель у атома азота изатинового остатка, имеет показатель IC50 равный 6.79 миллимоля, (структура 1). Оценка жизнеспособности клеток была выполнена по изменению метаболической активности, что не всегда коррелирует с гибелью клеток
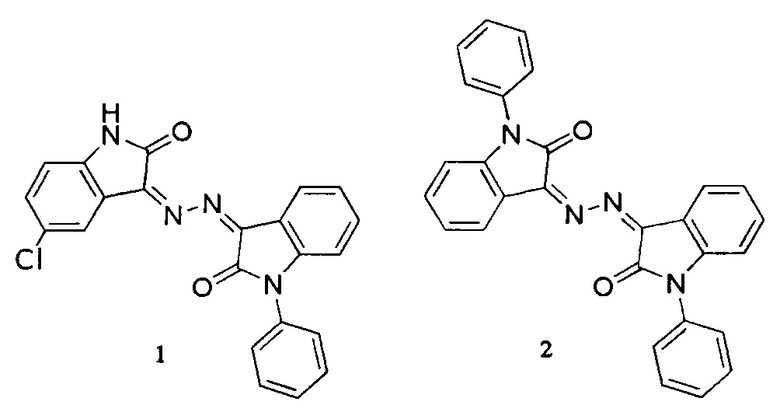
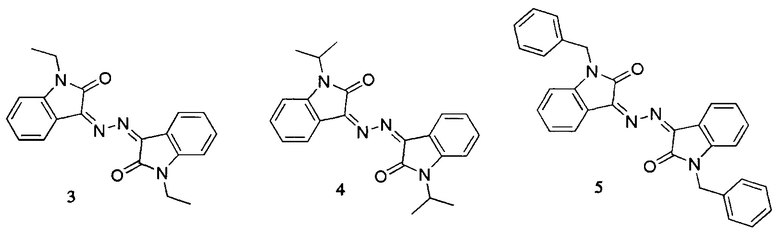
В качестве прототипа рассмотрены производные бис-изатина (N,N'-гидразино-бис-изатина), имеющие алкильные заместители у атомов азота изатинового остатка, опубликованные в статье: (Chengyuan Liang et.al. Eur. J. Med. Chem. 74, 2014, 742-750) [4]. Препараты, содержащие заместители у атома азота изатиновых остатков: этил (структура 3), изо-пропил (структура 4) или бензил (структура 5), проявляют противопухолевую активность только в диапазоне концентраций 35-100 мкМ и выше. Препарат, проявивший наибольшую активность (IC50 около 4.2 мкМ) по отношению к раковым клеткам человека, не содержит заместителей у атомов азота изатиновых остатков, что отличает его от соединений в заявляемом изобретении.
Таким образом, хотя рассмотренные в аналоге и прототипе производные N,N'-гидразино-бис-изатина и показывают определенную (невысокую) противопухолевую активность, но жизнеспособность опухолевых клеток оценивалась только по изменению их метаболической активности, что не всегда коррелирует с гибелью клетки. Поэтому такая оценка недостаточно корректна поскольку она завышает количество погибших клеток, включая в их число клетки с замедленным метаболизмом.
Технический эффект заявляемого изобретения - расширение класса производных N,N'-гидразино-бис-изатиновых соединений, обладающих более высокой противопухолевой активностью по сравнению с препаратами из этой группы соединений, повышение точности оценки противопухолевой активности соединений, воздействующих на опухолевые клетки, путем определения их пролиферативной активности на опухолевых и неопухолевых клеточных линиях человека с последующим морфологическим и проточно-цитометрическим анализом прогрессии клеток по фазам клеточного цикла и оценкой апоптотической гибели клеток.
Технический эффект достигается тем, что синтезированы новые производные из класса N,N'-гидразино-бис-изатина, содержащие заместители у атома азота изатиновых остатков, обладающие высокой противопухолевой активностью, следующей структуры:
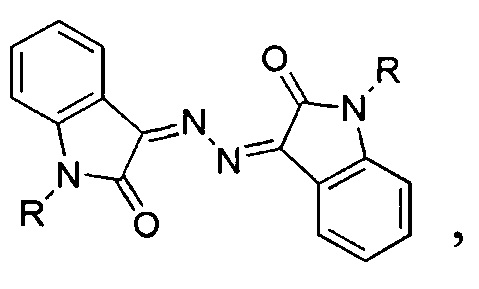
где R - это 4-метоксибензил Препарат I
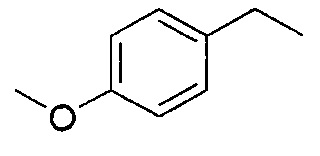
или
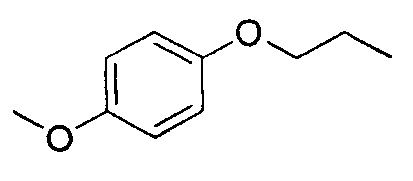
Препарат II
R - это 2-(4-метоксифенокси)-этил
и структуры соединений имеют вид:
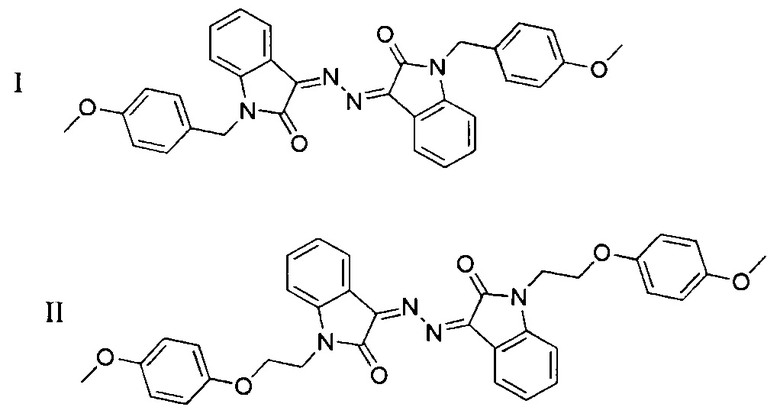
препарат I: 3,3'-(гидразин-1,2-диилиден)бис(1-(4-метоксибензил)индолин-2-он,
препарат II: 3,3'-(гидразин-1,2-диилиден)бис(1-(2-(4-метоксифенокси)этил)-индолин-2-он.
Экспериментальным путем обнаружено, что заявляемые препараты, содержащие заместители у атомов азота изатиновых остатков, показали более высокую противопухолевую активность, чем прототип и аналог, а также широко используемый в медицинской практике противоопухолевый препарат доксорубицин, не относящийся к изатинам. Это подтверждено исследованиями их антипролиферативной активности на опухолевых и неопухолевых клеточных линий человека, а также морфологическим и проточно-цитометрическим анализами прогрессии клеток по фазам клеточного цикла и оценкой апоптотической гибели клеток. Установлено, что созданные вещества в микромолярных концентрациях селективно ингибируют пролиферацию опухолевых клеток путем блокирования клеток в G1/S и G2/M фазах клеточного цикла и индукции апоптотической гибели клеток.
Синтез заявляемых соединений
Спектры ЯМР 1Н и 13С в дейтерированном диметилсульфоксиде (DMSO-d6) были записаны на спектрометре Spinsolve 60 Carbon (Magritek) с рабочей частотой 60 МГц 15 МГц для 1Н и 13С, соответственно. Химические сдвиги приведены в м.д. В качестве внутреннего стандарта использовался пик растворителя (2.50 и 39.4 для 1Н и 13С, соответственно). Индивидуальность синтезированных соединений доказана методом тонкослойной хроматографии на пластинках Merck Kieselgel 60 F254.
Получение препарата I:
3,3'-(гидразин-1,2-диилиден)бис(1-(4-метоксибензил)индолин-2-он.
Стадия 1. Получение 1-(4-метоксибензил)индолин-2,3-диона
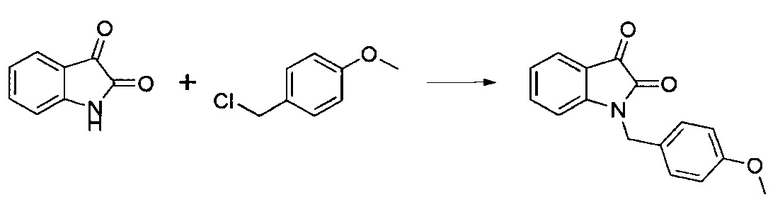
К нагретому до 70-80°С 0.1-2.0 молярному раствору изатина (1.47 г, 10 ммол) в диметилформамиде прибавляют 1 эквивалента безводного тонко растертого карбоната калия (1.38 г, 10 ммоль) и йодида калия (50 мг) и при перемешивании постепенно прибавляют 4-метоксибензил хлорид (1.64 г, 1.05 ммоль). Реакционную смесь перемешивают при 70°С 10-15 часов (контроль с помощью ТСХ). Смесь охлаждают и при перемешивании выливают в десятикратный объем холодной воды, что сопровождается выделением оранжевого осадка, который отфильтровывают, промывают на фильтре водой, затем этанолом. Сырой продукт очищают перекристаллизацией из этанола, метанола или 2-пропанола. Выход 1.95 г (73%). т.пл. 178-184°С. 1Н-ЯМР (60 МГц, DMSO-d6) δ (мд): 7.75-7.54 (м, 4Н), 7.48 (м, 1Н), 7.37-7.11 (м, 5Н), 6.82 (м, 2Н), 5.17 (2Н, s), 3.74 (3Н, s). 13С-ЯМР (15 МГц, DMSO-d6) δ (мд): 184.2, 160.1, 158.8, 148.5, 134.4, 133.7, 130.3, 127.8(2С) 124.7, 122.3, 117.7, 114.4 (2С), 55.6, 47.3.
Стадия 2. Получение 3,3'-(гидразин-1,2-диилиден)бис(1-(4-метоксибензил)индолин-2-она (препарат I)
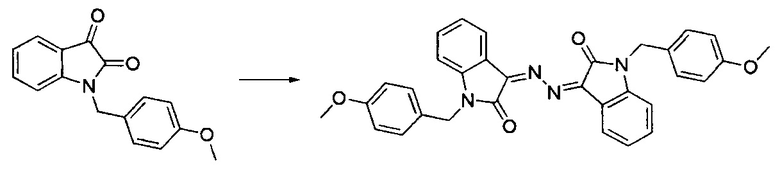
К суспензии 1-(4-метоксибензил)индолин-2,3-диона (5.34 г, 20.0 ммоль) в этаноле (100 мл), содержащем уксусную кислоту (0.03 г, 0.5 моль), прибавили гидразин-гидрат (0,525 г, 10.5 ммоль), и реакционную смесь кипятили с обратным холодильником. Через 30 минут кипячения исходные реагенты растворились, реакционная смесь потемнела, и из нее начал выпадать осадок. Реакционную смесь охладили, осадок отфильтровали и промыли этанолом. Сырой продукт растворили при нагревании в минимальном количестве диметилформамида и высадили изопропиловым спиртом. Осадок отфильтровали и промыли этанолом. Выход продукта в виде блестящих темно-бордовых кристаллов с т.пл. выше 219°С 4,25 г (79%). 1Н-ЯМР (60 МГц, DMSO-d6) δ (мд): 7.76-7.11 (м, 4Н), 6.97-6.63 (м, 4Н), 4.96 (с, 2Н), 3.74 (с, 3Н). 13С-ЯМР (15 МГц, DMSO-d6) δ (мд): 163.1, 158.9, 147.8, 137.2, 134.0, 131.6, 129.7, 127.4(2С) 124.7, 121.2, 117.4, 114.6 (2С), 55.6, 47.1.
Получение препарата II: 3,3'-(гидразин-1,2-диилиден)бис(1-(2-(4-метоксифенокси)этил)-индолин-2-она.
Стадия 1. Получение 1-(2-(4-метоксифенокси)этил)индолин-2,3-диона
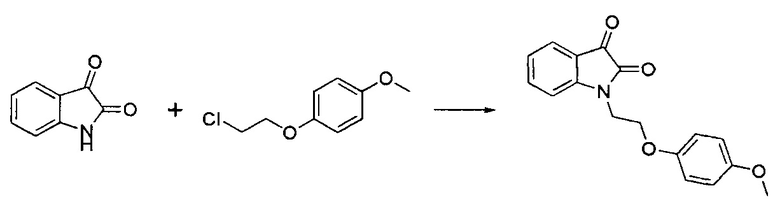
К суспензии изатина (1.47 г, 10.0 ммоль), безводного тонко растертого карбоната калия (1.38 г, 10.0 ммоль) и йодида калия (50 мг) в диметилформамиде (10 мл) прибавляют 1-(2-хлороэтокси)-4-метоксибензола (1.87 г, 10.0 ммоль) и реакционную смесь перемешивают 10-15 часов при 70°С до завершения реакции (контроль с помощью ТСХ). Смесь охлаждают и при перемешивании выливают в десятикратный объем холодной воды, что приводит выделением оранжевого осадка, который отфильтровывают, промывают на фильтре водой, затем этанолом. Сырой продукт очищают перекристаллизацией из этанола, метанола или 2-пропанола. 1,6 г (61%). Т. пл. 115-120°С, выход 2.26 г (76%). 1Н-ЯМР (60 МГц, DMSO-d6) δ (мд): 8.01-7.32 (м, 4Н), 6.84-6.66 (м, 4Н), 4.20 (м, 2Н), 3.72 (с, 3Н), 3.38 (м, 2Н). 13С-ЯМР (15 МГц, DMSO-d6) δ (мд): 180.1, 161.1, 151.2, 149.5, 148.0, 134.6, 130.4, 124.7, 121.9, 117.8, 115.2 (2С), 114.8(2С), 65.8, 55.6, 39.5.
Стадия 2. Получение 3,3'-(гидразин-1,2-диилиден)бис(1-(2-(4-метоксифенокси)этил)-индолин-2-она (препарат II).
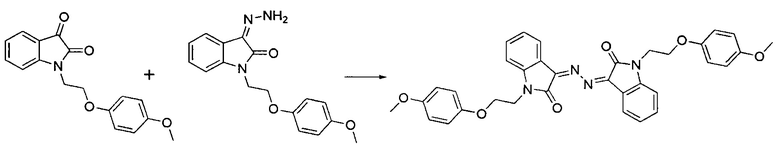
1-(2-(4-метоксифенокси)этил)индолин-2,3-дион (2.97 г, 10.0 ммоль) и 3-гидразоно-1-(2-(4-метоксифенокси)этил)индолин-2-он (3.11 г, 10.0 ммоль) в смеси этанола (100 мл) и уксусной кислоты (15 мл) кипятили с обратным холодильником. Через 30 минут кипячения исходные реагенты растворились, реакционная смесь потемнела, и из нее стал выпадать осадок продукта. Реакционную смесь охладили, осадок отфильтровали и промыли этанолом. Сырой продукт растворили при нагревании в минимальном количестве диметилформамида и высадили изо-пропиловым спиртом. Осадок отфильтровали и промыли этанолом.
Выход продукта в виде блестящих темно-бордовых кристаллов с т.пл. выше 219°С 4,84 г (76%). 1Н-ЯМР (60 МГц, DMSO-d6) δ (мд): 7.71-7.02 (м, 4Н), 6.84-6.66 (м, 4Н), 4.20 (м, 2Н), 3.71 (с, 3Н), 3.37 (м, 2Н). 13С-ЯМР (15 МГц, DMSO-d6) δ (мд): 163.1, 152.3, 149.6, 147.5, 137.6, 131.2, 129.3, 124.5, 121.6, 117.5, 115.3 (2), 114.9 (2), 65.9, 55.7, 39.5.
Доказательство противопухолевой активности заявляемых соединений.
Объекты исследования: работа выполнена на клетках карциномы шейки матки (линия HeLa G63), и на эндотелиоцитах (линия ECV 304) человека. Клетки культивировали в среде Игла с добавлением 10% эмбриональной сыворотки и гентамицина (50 мкг/мл) («БиолоТ»). Для обработки клеток готовили 1 миллимолярные растворы (ммоль/л), препаратов I и II в DMSO, из которых затем готовили растворы исследуемых концентраций (от 10 до 0.3 мкМ) в питательной среде. Цитомерический анализ состава клеточной популяции проводили на цитометре, созданном в отделе молекулярной и радиационной биофизики Петербургского института ядерной физики им. Б.П. Константинова. Морфологический анализ проводили на инвертированном микроскопе «EVOS". Исследования противопухолевой активности препаратов I и II в концентрациях от 0.3 до 10 мкМ проводили через 24 и 48 часов после обработки опухолевых клеток каждым из этих препаратов. Клетки, выращенные в 24-х луночных планшетах, отмывали от инкубационной среды, заливали раствором Версена и после отслоения клеток от поверхности планшета добавляли 0.1% раствор бромистого этидия, ресуспендировали и суспензию анализировали на проточном цитометре (Freid J., et.al. The Journal of Histochemistry and Cytochemistry. 1978; 26(11): 921-933) ([6].
По такой же схеме была исследована противопухолевая активность доксорубицина. Доксорубицин (Sigma, США) добавляли в питательную среду в концентрации 3.45 мкМ. Доксорубицин - один из наиболее часто назначаемых цитостатических препаратов был использован в качестве стандартного соединения. Низкие дозы доксорубицина индуцируют блок G2/M, высокие блокируют в S-фазе и индуцируют апоптоз (Biochem. Biophys. Res. Commun. 2005 v. 334, p. 1014-1021) [7]).
Противопухолевая активность определена по результатам цитометрического анализа пролиферативной активности (погрессия по стадиям клеточного циула) и апоптотической гибель клеток (популяция суб-G1 с содержанием ДНК <2с, образующаяся при фрагментации ядер в процессе апоптоза, что регистрируется и при морфологическом анализе клеточной популяции). Этот метод оценки клеточной выживаемости является более корректным, нежели метод изменения метаболической активности, используемый авторами в аналоге, поскольку мы регистрируем уже разрушение клеточного ядра, а снижение метаболической активности может происходить и при временной остановке пролиферации не всегда приводит к гибели клетки.
Результаты представлены в таблице I.

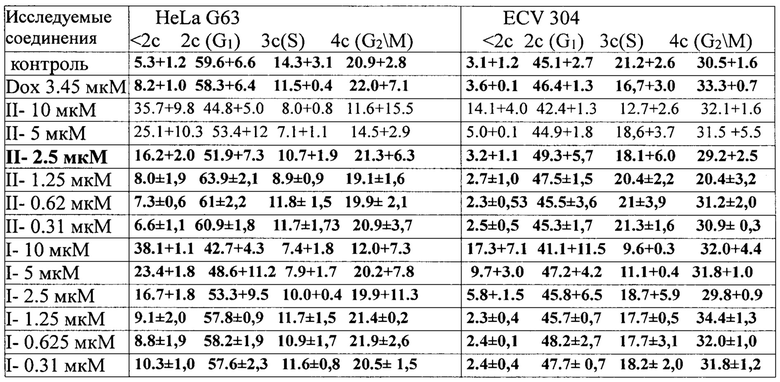
Каждая точка представляет среднее арифметическое значение 3-5 повторов (%) ± стандартное отклонение (М±σ).
48-ми часовая обработка клеток HeLa G63 этими агентами существенно влияла на перераспределение клеток по содержанию ДНК (по фазам клеточного цикла) по сравнению с необработанным контролем. Видно, что дозо-зависимое увеличение доли клеток с содержанием ДНК меньше диплоидного (суб-G1-популяция) свидетельствующее об апоптотической гибели клеток (Biochem. Biophys. Res. Commun. 2005 v. 334, p.1014-1021 [8]). При концентрациях 1.25 мкМ и 2.5 мкМ доля этой популяции увеличивается втрое, при концентрации 5 мкМ - в 5 раз, а при концентрации 10 мкМ почти в 10 раз. В остальных фазах клеточного цикла G1, S и G2/M регистрировали дозо-зависимое снижение доли клеток по отношению к необработанному контролю. В меньшей степени снижалась доля клеток в фазе G1, в большей в S- и G2/М-фазах, что может свидетельствовать о блокировании клеточной пролиферации в точках перехода клеток из G1- в S-фазу. При концентрациях от 1.25 мкМ до 0.3 мкМ эффективность препаратов I и II и существенно не менялась. Можно предположить появление порога насыщения эффекта.
Аналогичная обработка клеток ECV 304 исследуемыми агентами также носит дозо-зависимый характер, при этом эффективность препарата II в индукции апоптоза (доля клеток с содержанием ДНК меньше 2 с) ниже, чем препарата I. Препарат II при концентрациях 2.5 и 5 мкМ незначительно влияет на изменение доли клеток в G1-фазе, S- и G2/М-фазах и только при концентрации 10 мкМ в 2.5 раза увеличивалась доля клеток <2с (суб G1-популяция). Доля клеток в G1-фазе менялась несущественно, но при этом снижалась доля клеток в S-фазе и увеличивалась доля клеток G2/М-фазе. Можно предположить, что в данной клеточной линии этот агент блокирует пролиферацию в G2/М-фазах. Обработка клеток ECV 304 препаратом I выявила ту же закономерность, что и при обработке препаратом II, но эффекты были более выраженными. Так, при обработке клеток препаратом I доля апоптотических клеток увеличивалась вдвое, при концентрации 2.5 мкМ, втрое при 5 мкМ и в 5 раз при 10 мкМ. При 5 и 10 мкМ концентрациях снижалась доля клеток в S-фазе и увеличивалась доля клеток в G2/M-фазах. При концентрациях препарата II от 2.5 мкМ и меньше, а для препарата I - от 1.25 мкМ и меньше эффект 48-ми часовой обработки не регистрировался на ECV 304 клетках.
Для пояснения сущности изобретения представлены также следующие графические материалы.
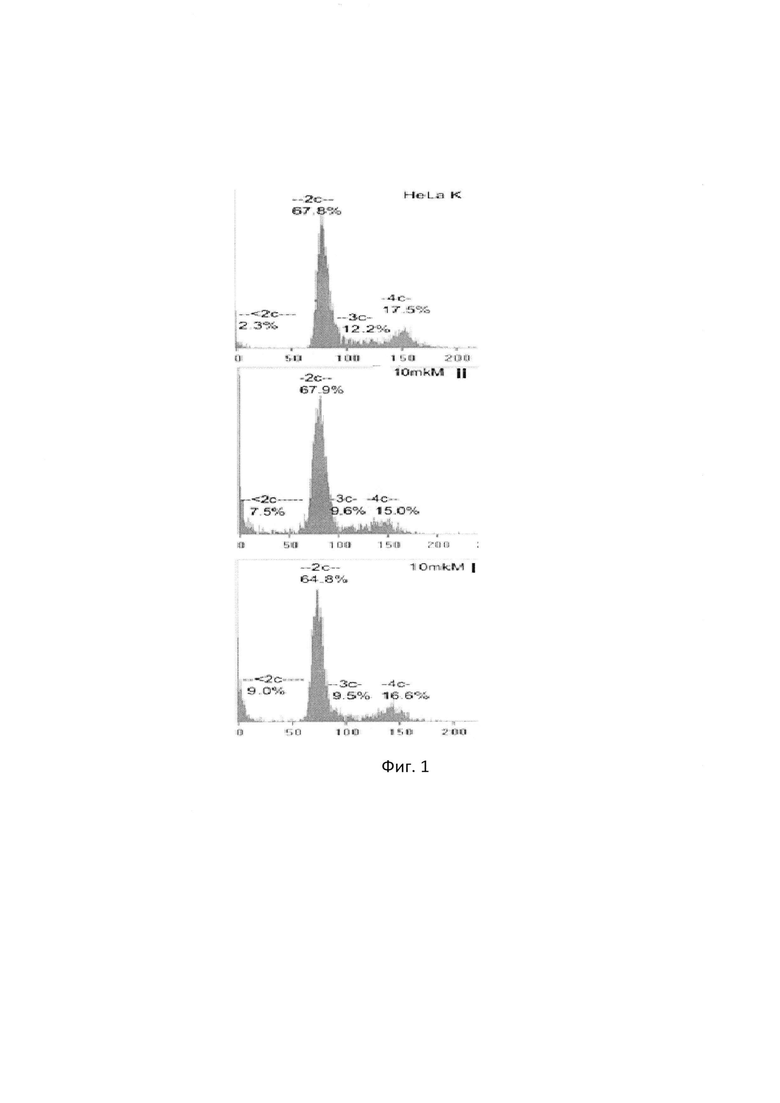
На фиг. 1 представлены результаты концентраций препаратов I и II цитометрического анализа влияния 10 мкМ на прогрессию по циклу (пролиферативная активность) и апоптотическую гибель (цитотоксичность) HeLa G63 через 24 ч после обработки.
Из гистограмм видно, что препараты I и II в данной концентрации несущественно влияют на прогрессию клеток по циклу, не меняют уровень клеток, находящихся в G1- и G2/М-фазах, и лишь немного снижают уровень клеток в S-фазе. При этом незначительно увеличивается доля клеток с содержанием ДНК <2с. 24-х часовая инкубация клеток обоими препаратами в концентрациях меньше 10 мкМ была неэффективной (поэтому данные не приводятся).
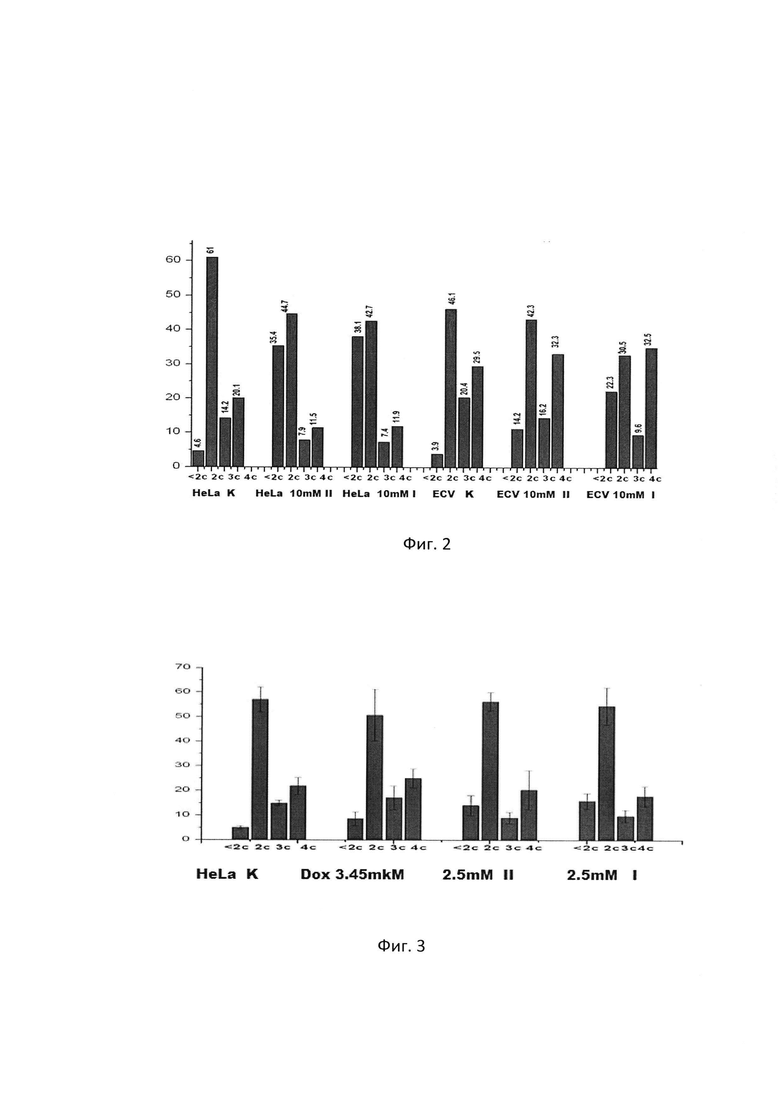
На фиг. 2 представлено распределение клеток HeLa G63 и ECV 304 по фазам клеточного цикла после 48-ми часовой обработки их 10 мкМ либо препаратом I, либо препаратом II.
Из диаграмм видна большая цитотоксичность (доля клеток с содержанием ДНК <2с) этих препаратов в отношении опухолевых клеток HeLa, G63. и заявляемые препараты показывают практически равную эффективность в отношении этих опухолевых клеток HeLa, G63 (в 5 раз возрастала доля клеток с содержанием ДНК <2с по сравнению с контролем). На клетках ECV 304 цитотоксичность этих препаратов почти вдвое ниже, и наблюдается различие в эффективности препарата II (в 3.5 раза) и препарата I (в 5раз), которое регистрировалось и при более низких концентрациях (см. таблица 1).
Кроме того, при концентрациях меньше, чем 2.5 мкМ регистрируется селективность действия синтезированных производных изатина в отношении опухолевых клеток. Оба препарата в данной концентрации проявляют антипролиферативный эффект, но опухолевые клетки HeLa G63 они блокируют при переходе из G1- в S-фазу, а на неопухолевые клетки ECV 304 аккумулируют в G2/М-фазе. Очевидно, что оба препарата в одной и той же концентрации в разных типах клеток включает различные чек-поинты.
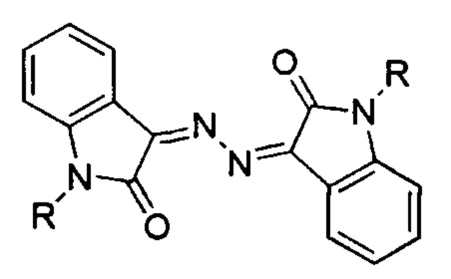
Результаты сравнительных исследований антипролиферативной эффективности синтезированных соединений бис-изатинов с противоопухолевым агентом доксорубицином представлены на фигуре 3 в виде распределения клеток HeLa G63 по фазам клеточного цикл после 48-ми часовой обработки 3.4 мкМ доксорубицином и 2.5 мкм препаратом II или препаратом I. Как видно из диаграмм (фигура 3), выбранная доза (3.4 мкМ) доксорубицина увеличивает долю <2с клеток вдвое по сравнению с контролем и немного увеличивает долю клеток в G2/М-фазе, а препараты II и I в меньшей концентрации (2.5 мкМ) увеличивают долю <2с клеток вдвое больше, чем доксорубицин, и втрое больше, чем в контроле, и снижают долю клеток в S-фазе. Из литературных данных известно, что низкие дозы доксорубицина индуцируют блок в G2/М-фазе, а высокие блокируют в S-фазе индуцируют апоптоз. [7].
Из таблицы 1 видно, что препараты II и I в концентрациях от 1.25 мкМ до 0.3 мкМ, а доксорубицин в концентрации 3.4 мкМ в 1.6 раза увеличивали долю апоптотически гибнущих клеток. Иными словами, противоопухолевая активность препаратов II и I была почти на порядок выше широко используемого противоопухолевого препарата.
Данные, представленных в таблице 1 и на фигуре 1-3, доказывают следующее:
1. противоопухолевая активность заявляемых препаратов проявляет дозо-зависимое ингибирование роста и пролиферации клеток линии HeLa G63 и ECV 304 в диапозона доз от 5 до 10 мкМ.
2- при концентрациях от 2.5 мкМ и ниже (1.25; 0.6; и 0.3 мкМ) оба препарата проявляли селективную цитотоксичность в отношении опухолевых клеток.
3- блокирование пролиферации опухолевых клеток (HeLa G63) регистрировалось при переходе клеток из G1- в S-фазу, а не опухолевых (ECV 304) в G2/M фазах.
Вывод: Заявляемые соединения обладают высокой противопухолевой активностью, величина которой определена надежными методами, что является важной предпосылкой для использования заявляемых веществ в медицине, фармацевтической промышленности, биохимии и биологических исследованиях.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ радиосенсибилизации опухолевых клеток | 2019 |
|
RU2723393C1 |
| Композиция, ингибирующая рост и выживаемость опухолевых клеток | 2019 |
|
RU2707554C1 |
| Способ обработки опухолевых клеток | 2016 |
|
RU2632429C1 |
| Фторсодержащие бензилированные изатины | 2023 |
|
RU2816105C1 |
| Фторсодержащие бензилированные изатины, обладающие противоопухолевой активностью | 2022 |
|
RU2802016C1 |
| Бромсодержащие пространственно-затрудненные фенолы, обладающие противоопухолевой активностью | 2023 |
|
RU2822270C1 |
| ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ДОБРОКАЧЕСТВЕННЫХ И ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕВЫХ ЗАБОЛЕВАНИЙ, СОДЕРЖАЩЕЕ ПРОИЗВОДНОЕ ДИСОРАЗОЛА | 2003 |
|
RU2322236C2 |
| Способ оценки суммарного показателя анеуплоидии и пролиферативной активности опухолевых клеток немелкоклеточного рака легкого и рака яичников с использованием специфического красителя ДНК нового поколения DRAQ7 | 2016 |
|
RU2639251C1 |
| N,N'-(АЛКАНДИИЛ)БИС[ЛАБДА-7(9),13,14-ТРИЕН-4-КАРБОКСАМИДЫ], ОБЛАДАЮЩИЕ ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ | 2017 |
|
RU2654201C1 |
| Новые пространственно-затрудненные фенолы, содержащие бензофуроксановые фрагменты, обладающие противоопухолевой активностью | 2022 |
|
RU2796810C1 |
Изобретение относится к производным N,N'-гидразино-бис-изатина указанной ниже формулы, обладающим высокой противоопухолевой активностью. В формуле R представляет собой 4-метоксибензил (препарат I) или 2-(4-метоксифенокси)-этил (препарат II). Препарат I представляет собой 3,3'-(гидразин-1,2-диилиден)бис(1-(4-метоксибензил)индолин-2-он), препарат II представляет собой 3,3'-(гидразин-1,2-диилиден)бис(1-(2-(4-метоксифенокси)этил)-индолин-2-он). 3 ил., 1 табл., 3 пр.
 ,
,
Производные N,N'-гидразино-бис-изатина, обладающие высокой противоопухолевой активностью, следующей структуры:
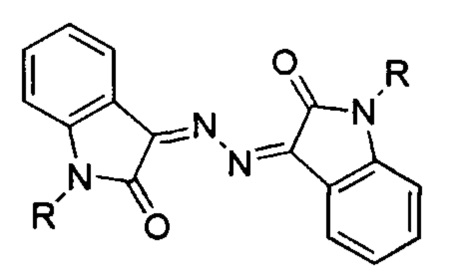 ,
,
где R - это 4-метоксибензил 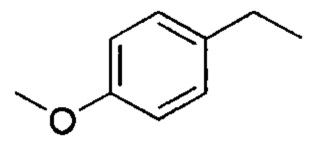 препарат I
препарат I
или R - это 2-(4-метоксифенокси)-этил 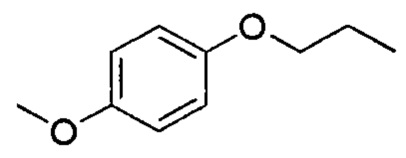 препарат II,
препарат II,
и структуры соединений имеют вид
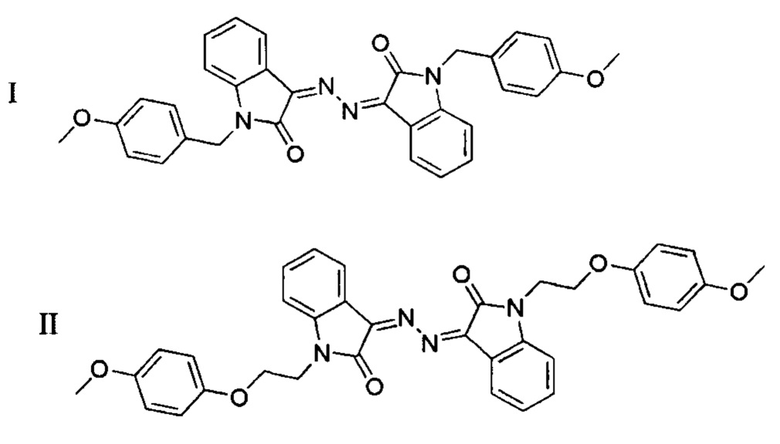
препарат I: 3,3'-(гидразин-1,2-диилиден)бис(1-(4-метоксибензил)индолин-2-он),
препарат II: 3,3'-(гидразин-1,2-диилиден)бис(1-(2-(4-метоксифенокси)этил)-индолин-2-он).
| CHENGYUAN LIANG ET AL, Synthesis, in vitro and in vivo antitumor activity of symmetrical bis-Schiff base derivatives of isatin, EUROPEAN JOURNAL OF MEDICINAL CHEMISTRY, 2014, 74, pp | |||
| КОЛЕНЧАТЫЙ ВАЛ С ДИФФЕРЕНЦИАЛЬНОЙ ПЕРЕДАЧЕЙ | 1923 |
|
SU742A1 |
| US 2012252860 A1, 04.10.2012 | |||
| GUPTA A | |||
| K | |||
| ET AL, Systematic Review on Cytotoxic and Anticancer Potential of N-Substituted | |||
Авторы
Даты
2023-05-25—Публикация
2023-02-10—Подача