Изобретение относится к ядерной медицине, а именно к: технологиям лучевой терапии быстрыми нейтронами, средствам дистанционной короткофокусной лучевой терапии, средствам формирования терапевтического пучка стандартных апертур различных размеров, в частности к биологической защите для проведения дистанционной терапии 14 МэВ нейтронами.
Известно средство для дистанционной терапии быстрыми нейтронами (Зырянов Б.Н., Мусабаева Л.И., Летов В.Н., Лисин В.А. Дистанционная нейтронная терапия. Томск, 1991). В качестве источника быстрых нейтронов с энергией 6,5 МэВ, образующихся по ядерной реакции 9Be(d,n)10B, используют стационарный циклотрон У-12 Интенсивность потока нейтронов на выходе коллиматора составляет 6,5⋅109 н/стерадиан⋅мкА⋅с. Радиационная защита толщиной 85 см выполнена из железа и борированного полиэтилена. При этом мощность дозы на поверхности тела пациента равна 15 сГр/мин.
Недостатком технического решения является низкая эффективность радиационной защиты при небольшой толщине.
Известно средство нейтронной терапии на стационарном генераторе "НГ-12И". В качестве источника быстрых нейтронов с энергией 14 МэВ с выходом из мишени 1,5⋅1012 н/с используют ядерную реакцию 3T(d,n)4He (Важенин А.В., Рыковский Г.Н. Уральский центр нейтронной терапии: история создания, методология, результаты работы. М.: Издательство РАМН, 2008). В зависимости от локализации заболевания пациента размещают на кресле или на медицинском столе при горизонтальном или вертикальном расположении канала нейтронов, соответственно. Радиационная защита толщиной 65 см выполнена из железа и борированного полиэтилена. Мощность дозы для РИП равным 86 см составляет 9 сГр/мин.
Недостатком технического решения является низкая эффективность радиационной защиты при небольшой толщине.
Известно средство для дистанционной терапии быстрыми нейтронами (Verbeke JM, Leung KN, Vujic J. Development of a sealed-accelerator-tube neutron generator. Appl Radiat Isot 1998 May- Jun; 49(5-6):723-725). В качестве источника нейтронов используют ядерную реакцию 3T(d,n)4He с выходом нейтронов 5⋅1012 н/с и энергией 14 МэВ. Нейтронная головка состоит из источника нейтронов, нейтронного канала и радиационной защиты, изготовленной из железа, свинца и борированного полиэтилена. Мощность дозы на расстоянии 100 см от источника нейтронов до пациента составляет более 15 сГр/мин.
Недостатком технического решения является низкая эффективность радиационной защиты при небольшой толщине.
Известно устройство для дистанционной терапии быстрыми нейтронами на исследовательском ядерном реакторе FRM I (Wagner FM, Kneschaurek P, Kastenmuller at. el. A The Munich Fission Neutron Therapy Facility MEDAPP at the research reactor FRM II. Strahlenther Onkol. 2008 Dec; 184(12):643-6). В помещении ядерного реактора устанавливают фильтр, который выводит из пучка нейтроны малых энергий и его спектр становится жестче. Пациента располагают на кресле в медицинском блоке. Его перемещение на второе - противоположное поле облучения осуществляют вращением кресла. К настоящему времени исследовательский ядерный реактор FRM I выведен из эксплуатации. Метод дистанционной терапии быстрыми нейтронами с такими же характеристиками пучка нейтронов перенесен на другой исследовательский реактор FRM II, на котором к настоящему времени прошли курс лечения более 100 пациентов.
Известно устройство для терапии на основе генератора быстрых нейтронов с энергией 14 МэВ на вакуумных трубках с использованием ядерной реакции 3T(d,n)4He с выходом 5⋅1012 н./с. (Verbeke JM, Leung KN, Vujic J. Development of a sealed-accelerator-tube neutron generator. Appl Radiat Isot 1998 May-Jun; 49(5-6):723-725). Устройство содержит источник нейтронов, испускаемых мишенью, окруженный радиационной защитой. В защите расположен нейтронный канал (коллиматор). Мишень расположена вблизи торца коллиматора. Система формирования радиационного поля в этой установке выполнена из железа, борированного полиэтилена и свинца. Сменные коллиматоры в форме усеченных пирамид из специальной стали формируют поля квадратного или прямоугольного сечения размерами 8×8, 10×10, 12×12, 13×13 и 15,5×10 см2. Мощность дозы (кермы) для РИП=100 см составляет >15 сГр/мин и 20 сГр/мин для РИП=85 см. Половинная доза расположена на глубине 10,8 см. Качество радиационной защиты Н, определяемое как расстояние от края нейтронного канала на поверхности защиты со стороны пациента, на котором керма уменьшается с 80% до 20%, составляет 2,5 см. Для измерения дозы во время терапевтического сеанса используется измерительная система с детектором на основе тканеэквивалентной ионизационной камеры, которая расположена в центре пучка нейтронов внутри нейтронного канала. Такой же детектор используют для исследования дозовых распределений в водном фантоме с клиновидным фильтром при планировании нейтронной терапии злокачественных новообразований сложной геометрической формы.
Недостатком технического решения является существование реакций взаимодействия железа с нейтроном: 56Fe(n,p)56Mn, 54Fe(n,γ)55Fe с периодом полураспада 2,74 года, которые приводят к накоплению активности сменных коллиматоров из любой специальной стали.
Самым близким (прототипом) к заявленному техническому решению является устройство для проведения дистанционной терапии 14 МэВ нейтронами (RU 2442620 С2), которое включает генератор нейтронов, расположенный вплотную к биологической защите на одной оси со встроенным в нее нейтронным каналом.
Недостатком технического решения является относительно высокий уровень дозы в тени защиты, так как защиты выполнены однородными из одного материала или составными, из частей в виде усеченных конусов, вставленных один в другой, из металлов, или гидридов металлов, или металлоподобных веществ, или пористых материалов, содержащих легкие ядра, или водородосодержащих соединений.
Техническим результатом является снижение радиационной нагрузки на органы пациента до 3 раз, снижение радиационной нагрузки на персонал до 10 раз, сокращение фракции лечения до 22,5 - 25 минут (180-200 сГр).
Технический результат решается тем, что, также как и в известном устройстве (RU 2442620), имеется корпус конусной формы со встроенным нейтронным каналом на одной оси с нейтронным генератором, пентаборид вольфрама W2B5 в своем составе.
Особенностью технического решения является то, что стенка корпуса биологической защиты имеет толщину 5 мм с высотой корпуса 30 см, причем корпус заполнен механической смесью зерен пентаборида вольфрама W2B5, полученной из молотой шихты WO3, восстановленной алюмотермическим методом, с фракцией зерен от 30 микрон до 3 миллиметров, с долей пентаборида 0.8 без уплотнения, а также полиэтиленом и водородсодержащим материалом в виде порошка тяжелых гидридов: TaH0.8, HfH4.45, La-Ce H3, а встроенный нейтронный канал содержит вложенные аппликаторы, формы кругового конуса, причем стенки канала, аппликаторы и корпус устройства, спаянные оловом, выполнены из листов 5 мм из композита вольфрама W-Cu-Ni.
Изобретение поясняется подробным описанием, примерами исполнения защиты и иллюстрациями, на которых изображено:
Фиг. 1 - фотоиллюстрация устройства для нейтронной терапии генератором НГ-14: 1 - генератор нейтронов; 2 - поворотный механизм; 3 - биологическая защита.
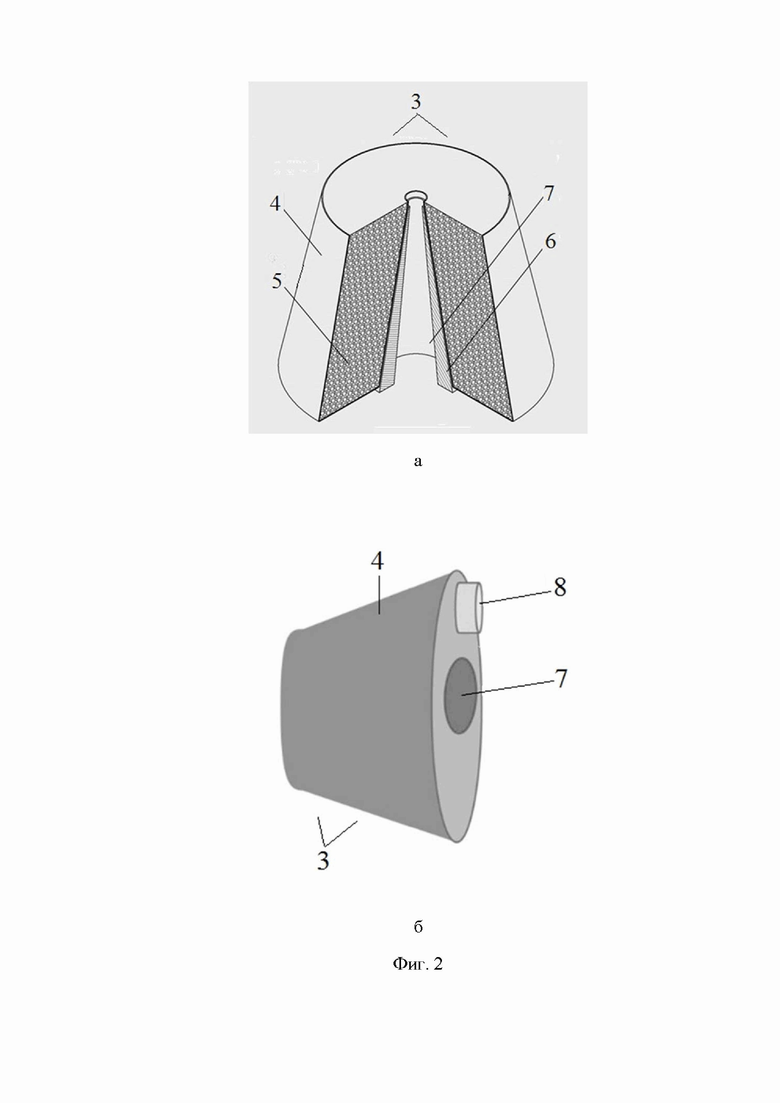
Фиг. 2 - схема биологической защиты - 3: а) вид прямой проекции с разрезом: 4 - корпус биологической защиты, 5 - механическая смесь зерен пентаборида вольфрама W2B5, заполненная водородсодержащим материалом в виде порошка тяжелых гидридов - металлов, интерметаллических соединений или в виде жидкости - расплава полиэтилена, 6 - аппликатор канала, 7 - нейтронный канал; б) вид сбоку: 4 - корпус биологической защиты, 7 - нейтронный канал, 8 - сегмент функциональной защиты.
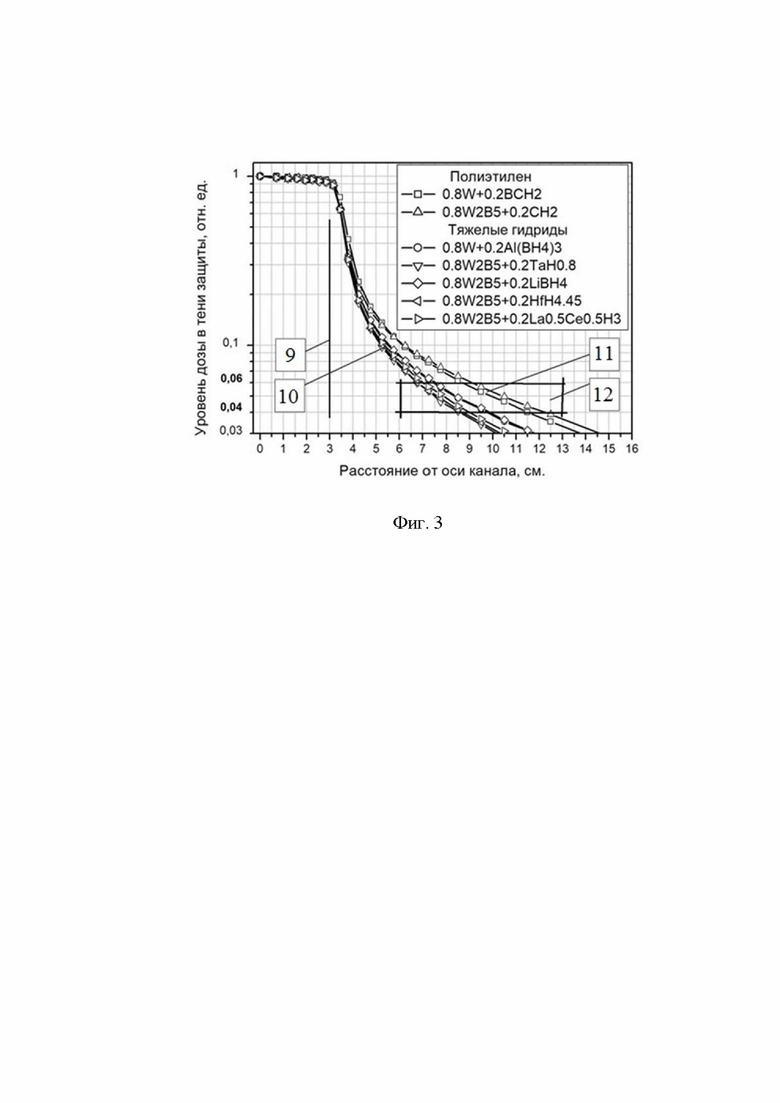
Фиг. 3 - Диаграмма распределения доз нейтронов в тени защиты и средние массовые доли материалов: 9 - экстраполированная граница края нейтронного канала, 10 - распределения с меньшим уровнем дозы, 11 - распределения с большим уровнем дозы, 12 - Уровень дозы нейтронов в тени защиты не превышает 4-6%.
Пример осуществления изобретения
Биологическая защита 3 с поворотным механизмом 2 примыкает к нейтронному генератору 1 (Фиг. 1). Биологическая защита 3 (Фиг. 1, Фиг. 2 а, б) содержит тонкостенный (5 мм) корпус 4 высотой 30 см (определяется клиническим условием по мощности дозы при выходе генератора ~1011н/сек - не менее 8 сГр/мин на объект) с нейтронным каналом 7, с вкладышами аппликаторами 6 конусной формы на одной оси с нейтронным генератором 1, причем внутренность корпуса 4 заполнена механической смесью пентаборида вольфрама W2B5 5 (Фиг 2 а), полученной из молотой шихты WO3, восстановленной до пентаборида алюмотермическим методом, с фракцией зерен от 30 микрон до 3 миллиметров, с долей пентаборида равной 0.8 без уплотнения, а также полиэтиленом и водородсодержащим материалом в виде порошка тяжелых гидридов: TaH0.8, HfH4.45, La-Ce H3, а встроенный нейтронный канал содержит вложенные аппликаторы, формы кругового конуса, причем стенки канала 7, аппликаторы 6 и корпус 4 устройства, спаянные оловом, выполнены из листов 5 мм из композита вольфрама W-Cu-Ni.
Вблизи выходного отверстия нейтронного канала 7 с обратной стороны корпуса 4 имеется функциональная (теневая), защита 8 в виде сегмента пластичной формы, состоящего из механической смеси пентаборида вольфрама W2B5 и пластичного водородосодержащего наполнителя в виде пластилина (например, марки «Луч»). Функциональная защита 8 имеет толщину и диаметр 10 см и закреплена на корпусе со стороны очага поражения, являясь теневой защитой критических органов. Вложенный аппликатор 6 (Фиг. 2а), выполнен в виде кругового конуса нейтронного канала, для изменения формы и размеров нейтронных полей.
Пример исполнения
Биологическая защита выполнена с водородсодержащим материалом в виде порошка тяжелых и легких гидридов: CH2 (полиэтилен), BCH2 (борированный полиэтилен, 30% массовых по 10B), TaH0.8, HfH4.45, La-CeH3, Al(BH4)3, Li(BH4).
Результаты оценок (методом Монте-Карло) распределений дозы в тени защиты по радиусу канала в примерах 1-2 представлены на диаграмме (Фиг. 3). Распределения с меньшим уровнем дозы 10 (Фиг. 3) соответствуют заполнению защиты тяжелым гидридом, с большим 11 (Фиг. 3) - легким гидридом. При этом уменьшение критических лучевых нагрузок соответствуют величине полного макросечения рассеяния 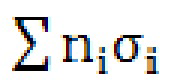 среды с пентаборидом ~1/3 1/см - уменьшаются как
среды с пентаборидом ~1/3 1/см - уменьшаются как 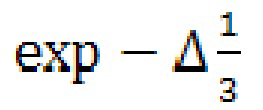 на расстоянии Δ (толщина сегмента). Уровень дозы нейтронов в тени защиты не превышает 4-6%, 12 (Фиг. 3) на расстоянии 6-13 см от оси канала или 3-10 см от экстраполированной границы края канала 9 (Фиг. 3), что обеспечивает достижение технического результата в любом из приведенных примеров исполнения защиты и позволяет использовать дальние поля нейтронов (10-30 см от обреза защиты до очага поражения), примерно с четырехкратным увеличением времени экспозиции, не превышая критических лучевых нагрузок ближайших органов (5-15 см от очага поражения) при толщине биологической защиты 30 см. Согласно оценки скорости активации 186W вложенных аппликаторов 6 (Фиг. 2 а) методом Монте-Карло, в гетерогенной модели реальной засыпки зерна пентаборида 5 (Фиг. 2 а), через неделю работы генератора, радиационные нагрузки на персонал не превышают суточной дозы во вредных условиях по группе А.
на расстоянии Δ (толщина сегмента). Уровень дозы нейтронов в тени защиты не превышает 4-6%, 12 (Фиг. 3) на расстоянии 6-13 см от оси канала или 3-10 см от экстраполированной границы края канала 9 (Фиг. 3), что обеспечивает достижение технического результата в любом из приведенных примеров исполнения защиты и позволяет использовать дальние поля нейтронов (10-30 см от обреза защиты до очага поражения), примерно с четырехкратным увеличением времени экспозиции, не превышая критических лучевых нагрузок ближайших органов (5-15 см от очага поражения) при толщине биологической защиты 30 см. Согласно оценки скорости активации 186W вложенных аппликаторов 6 (Фиг. 2 а) методом Монте-Карло, в гетерогенной модели реальной засыпки зерна пентаборида 5 (Фиг. 2 а), через неделю работы генератора, радиационные нагрузки на персонал не превышают суточной дозы во вредных условиях по группе А.
Принцип действия устройства
Генератор нейтронов (НГ-24МТ) подключают к блоку управления. На корпусе генератора устанавливают детектор флюенса для отпуска дозы. В соседнем помещении размещают приборы, контролирующие длительность сеанса терапии. На начальном этапе проводят исследования доз в фантоме - по глубине и по радиусу пучка нейтронов. После расчетно-экспериментального анализа данных дозиметрии приступают к нейтронной терапии.
Для проведения нейтронной терапии изготавливают функциональную защиту в виде пластичного сегмента, для этого смешивают механическую смесь пентаборида вольфрама W2B5 (зерно молотой шихты WO3) и пластичный водородосодержащий наполнитель - пластилин марки «Луч». Пластичный сегмент имеет диаметр и толщину 10 см. Функциональную защиту закрепляют на корпусе (например, пластырем) с обратной стороны корпуса биологической защиты, со стороны очага поражения, вблизи выходного отверстия нейтронного канала и проводят нейтронную терапию.
Клинические примеры
Пример 1
Пациент С., 65 лет, поступил с диагнозом: рак гортани Т2N0M0.
Пациенту назначена дистанционная лучевая терапия СОД 66 Гр: суммарная очаговая доза 66*100/10 (ОБЭ нейтронов) / (180, 200) сГр = (36, 32) фракций по (180, 200) сГр, по (180, 200) / 8 сГр/мин.
Для проведения нейтронной терапии изготовили функциональную защиту в виде пластичного сегмента: смешали механическую смесь пентаборида вольфрама W2B5 и пластичный водородосодержащий наполнитель - пластилин, марки «Луч». Сегмент толщиной 10 см, диаметром 10 см. Функциональную защиту установили с обратной стороны корпуса биологической защиты, вблизи выходного отверстия нейтронного канала. Так как критический орган - зрительный нерв, то пластичный сегмент был закреплен со стороны головы. Нейтронную терапию проводили 22,5 мин на фракцию.
Пример 2
Пациент З., 72 лет, поступил с диагнозом: рак гортани Т2N0M0, II ст.
Пациенту назначена дистанционная лучевая терапия СОД 66 Гр: суммарная очаговая доза 66*100/10 (ОБЭ нейтронов) / (180, 200) сГр = (36, 32) фракций по (180, 200) сГр, по (180, 200) / 8 сГр/мин (клиническое условие).
Для проведения нейтронной терапии изготовили функциональную защиту в виде пластичного сегмента: смешали механическую смесь пентаборида вольфрама W2B5 и пластичный водородосодержащий наполнитель - пластилин, марки «Луч». Сегмент изготовили толщиной 10 см, диаметром 10 см. Функциональную защиту установили с обратной стороны корпуса биологической защиты, вблизи выходного отверстия нейтронного канала. Пластичный сегмент был закреплен со стороны головы. Нейтронную терапию проводили 25 мин на фракцию.
Пример 3
Пациент Ш., 69 лет, поступил с диагнозом: рак гортани Т2N0M0, II ст.
Пациенту назначена дистанционная лучевая терапия СОД 66 Гр: суммарная очаговая доза 66*100/10 (ОБЭ нейтронов) / (180, 200) сГр = (36, 32) фракций по (180, 200) сГр, по (180, 200) / 8 сГр/мин (клиническое условие).
Для проведения нейтронной терапии изготовили функциональную защиту в виде пластичного сегмента: смешали механическую смесь пентаборида вольфрама W2B5 и пластичный водородосодержащий наполнитель - пластилин, марки «Луч». Сегмент изготовили толщиной 10 см, диаметром 10 см. Функциональную защиту установили с обратной стороны корпуса биологической защиты, вблизи выходного отверстия нейтронного канала. Пластичный сегмент был закреплен со стороны головы. Нейтронную терапию проводили 24 мин на фракцию.
Предложенное изобретение промышленно применимо, экономически выгодно и за счет использования биологической и функциональной защиты с механической смесью пентаборида позволяет:
- снизить радиационную нагрузку на органы пациента до 3 раз;
- снизить радиационные нагрузки на персонал до 10 раз;
- сократить фракцию лечения до 22,5 - 25 минут (180-200 сГр).
| название | год | авторы | номер документа |
|---|---|---|---|
| УСТРОЙСТВО ДЛЯ ЛУЧЕВОЙ ТЕРАПИИ БЫСТРЫМИ НЕЙТРОНАМИ | 2009 |
|
RU2442620C2 |
| АППАРАТ ДЛЯ ДИСТАНЦИОННОЙ НЕЙТРОННОЙ ТЕРАПИИ | 2013 |
|
RU2526244C1 |
| Устройство для дистанционной нейтронной терапии | 1990 |
|
SU1762945A1 |
| СПОСОБ ФОРМИРОВАНИЯ ПОГЛОЩЕННОЙ ДОЗЫ ИЗЛУЧЕНИЯ ПРИ НЕЙТРОННОЙ ТЕРАПИИ | 2000 |
|
RU2191610C2 |
| СПОСОБ НЕЙТРОН-ЗАХВАТНОЙ ТЕРАПИИ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 1998 |
|
RU2141860C1 |
| ТРАНСФОРМАТОР ГАММА-НЕЙТРОННОГО ИЗЛУЧЕНИЯ | 2014 |
|
RU2559198C1 |
| Композиционный материал на основе сверхвысокомолекулярного полиэтилена для комбинированной радио и радиационной защиты, наполненный пентаборидом дивольфрама и техническим углеродом | 2016 |
|
RU2632932C1 |
| Облучатель для нейтронно-захватной терапии | 2015 |
|
RU2691322C2 |
| Облучатель для нейтронно-захватной терапии | 2015 |
|
RU2695255C2 |
| УСТРОЙСТВО ДЛЯ ТЕРАПИИ ОНКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ | 2009 |
|
RU2424832C1 |

Изобретение относится к медицинской технике, а именно к: технологиям лучевой терапии быстрыми нейтронами. Стенка корпуса биологической защиты имеет толщину 5 мм с высотой корпуса 30 см, причем корпус заполнен механической смесью зерен пентаборида вольфрама W2B5, полученной из молотой шихты WO3, восстановленной алюмотермическим методом, с фракцией зерен от 30 микрон до 3 миллиметров, с долей пентаборида 0.8 без уплотнения, полиэтилена и водородсодержащего материала в виде порошка тяжелых гидридов: TaH0.8, HfH4.45, La-Ce H3. Встроенный нейтронный канал содержит вложенные аппликаторы, формы кругового конуса, причем стенки канала, аппликаторы и корпус устройства, спаянные оловом, выполнены из тонких листов 5 мм из композита вольфрама W-Cu-Ni. Предложенное изобретение промышленно применимо, экономически выгодно и за счет использования биологической и функциональной защиты с механической смесью смесью пентаборида позволяет: снизить радиационную нагрузку на органы пациента до 3 раз; снизить радиационные нагрузки на персонал до 10 раз; сократить фракцию лечения до 22,5 - 25 минут (180-200 сГр). 3 ил., 3 пр.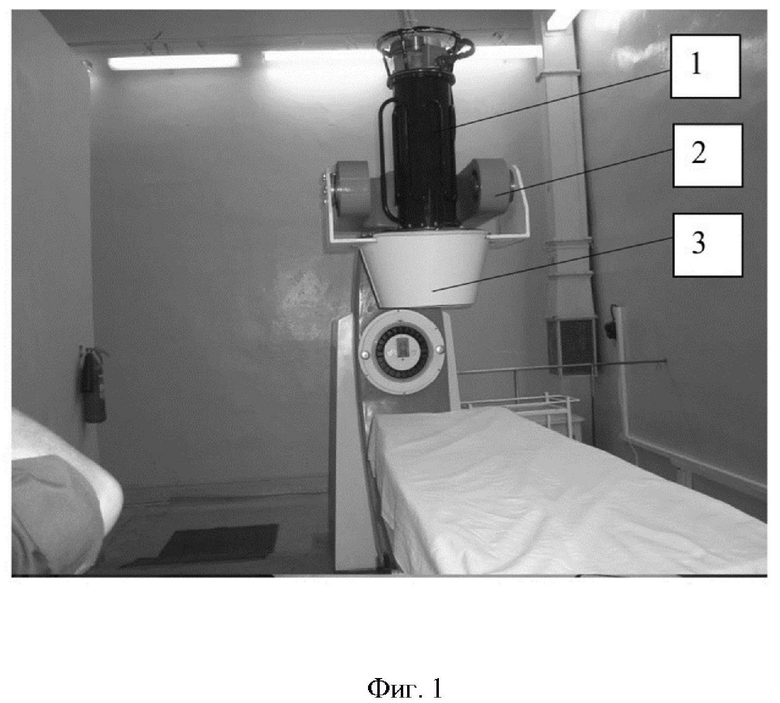
Биологическая защита к нейтронному генератору для проведения дистанционной терапии 14 МэВ нейтронами, включающая корпус конусной формы со встроенным нейтронным каналом на одной оси с нейтронным генератором, пентаборид вольфрама W2B5 в своем составе, отличающаяся тем, что стенка корпуса биологической защиты имеет толщину 5 мм с высотой корпуса 30 см, причем корпус заполнен механической смесью зерен пентаборида вольфрама W2B5, полученной из молотой шихты WO3, восстановленной алюмотермическим методом, с фракцией зерен от 30 микрон до 3 миллиметров, с долей пентаборида 0.8 без уплотнения, а также полиэтиленом и водородсодержащим материалом в виде порошка тяжелых гидридов: TaH0.8, HfH4.45, La-Ce H3, а встроенный нейтронный канал содержит вложенные аппликаторы, формы кругового конуса, причем стенки канала, аппликаторы и корпус устройства, спаянные оловом, выполнены из листов 5 мм из композита вольфрама W-Cu-Ni.
| УСТРОЙСТВО ДЛЯ ЛУЧЕВОЙ ТЕРАПИИ БЫСТРЫМИ НЕЙТРОНАМИ | 2009 |
|
RU2442620C2 |
| WO 2018232435 A1, 27.12.2018 | |||
| РАДИАЦИОННО-СТОЙКАЯ КАМЕРА | 2010 |
|
RU2546126C2 |
| Композиционный материал на основе сверхвысокомолекулярного полиэтилена для комбинированной радио и радиационной защиты, наполненный пентаборидом дивольфрама и техническим углеродом | 2016 |
|
RU2632932C1 |
| УМНОЖИТЕЛЬ НЕЙТРОНОВ | 2018 |
|
RU2689399C1 |
Авторы
Даты
2023-05-29—Публикация
2022-11-16—Подача