ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
[1] Настоящее изобретение испрашивает приоритет согласно предварительной заявке на патент США №62/429041, поданной 1 декабря 2016 года и имеющей название: TETRAHYDRONAPHTHALENE AND TETRAHYDROISOQUINOLINE DERIVATIVES AS ESTROGEN RECEPTOR DEGRADERS, и согласно предварительной заявке на патент США №62/540049, поданной 1 августа 2017 года и имеющей название: TETRAHYDRONAPHTHALENE AND TETRAHYDROISOQUINOLINE DERIVATIVES AS ESTROGEN RECEPTOR DEGRADERS, содержание которых включено в данный документ посредством ссылки во всей своей полноте для всех целей.
ВКЛЮЧЕНИЕ ПОСРЕДСТВОМ ССЫЛКИ
[2] Заявка на патент США с регистрационным №15/230354, поданная 5 августа 2016 года; и заявка на патент США №15/206497, поданная 11 июля 2016; и заявка на патент США №15/209648, поданная 13 июля 2016 года; и заявка на патент США с регистрационным №15/730728, поданная 11 октября 2017 года; и заявка на патент США с регистрационным №14/686640, поданная 14 апреля 2015 года, опубликованная как публикация заявки на патент США №2015/0291562; и заявка на патент США с регистрационным №14/792414, поданная 6 июля 2015 года, опубликованная как публикация заявки на патент США №2016/0058872; и заявка на патент США с регистрационным №14/371956, поданная 11 июля 2014 года, опубликованная как публикация заявки на патент США №2014/0356322; и заявка на патент с регистрационным №62/395228, поданная 15 сентября 2016 года под названием «INDOLE DERIVATIVES AS ESTROGEN RECEPTOR DEGRADERS»; и заявка на патент США с регистрационным №15/074820, поданная 18 марта 2016 года, опубликованная как публикация заявки на патент США №2016/0272639; и предварительная заявка на патент США с регистрационным №62/452972, поданная 31 января 2017 года; и предварительная заявка на патент США с регистрационным №62/429041, поданная 1 декабря 2016 года; и международная заявка на патент № PCT/US2016/023258, поданная 18 марта 2016 года, опубликованная как публикация международной заявки на патент № WO2016/149668, все из которых включены в данный документ посредством ссылки во всей своей полноте. Кроме того, все источники, упомянутые в данном документе, включены в данный документ посредством ссылки во всей своей полноте.
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
[3] Настоящее изобретение относится к соединениям, композициям и лекарственным препаратам, содержащим соединения, и к способам их получения. Настоящее изобретение также относится к применению соединений, композиций и лекарственных препаратов, например, в качестве ингибиторов активности эстрогенового рецептора, в том числе для разрушения эстрогенового рецептора, для лечения заболеваний и состояний, опосредованных эстрогеновым рецептором, например, для лечения рака молочной железы.
УРОВЕНЬ ТЕХНИКИ
[4] Эстрогеновый рецептор (ER) является представителем семейства ядерных гормональных рецепторов и функционирует как лиганд-активируемый фактор транскрипции, вовлеченный в повышение и снижение экспрессии генов. Естественный гормон для эстрогенового рецептора представляет собой 17-бета-эстрадиол (Е2) и родственные метаболиты. Связывание эстрадиола с эстрогеновым рецептором вызывает димеризацию рецептора, и димер, в свою очередь, связывается с эстрогеновыми ответными элементами (ERE) на ДНК. Комплекс ER-ДНК привлекает другие факторы транскрипции, ответственные за транскрипцию ДНК ниже от ERE в mRNA, которая, в конце концов, транслируется в белок. Альтернативно взаимодействие ER с ДНК может быть опосредованным через посредничество других факторов транскрипции, в частности fos и jun. Поскольку экспрессия большого числа генов регулируется эстрогеновым рецептором, и поскольку эстрогеновый рецептор экспрессируется во множестве типов клеток, модуляция эстрогенового рецептора посредством связывания либо с естественными гормонами, либо с синтетическими лигандами ER может иметь значительные эффекты на физиологию и патофизиологию организма.
[5] Для ряда заболеваний их этиология и/или патология опосредована ER. В совокупности такие заболевания называются эстрогензависимыми заболеваниями. Эстрогены являются критически важными для полового развития женщин. Кроме того, эстрогены выполняют важную функцию в поддержании костной плотности, регуляции уровней липидов в крови и, по-видимому, обладают нейропротекторными эффектами. Следовательно, сниженное продуцирование эстрогена у женщин после менопаузы ассоциировано с рядом заболеваний, таких как остеопороз, атеросклероз, депрессия и когнитивные расстройства. В свою очередь, некоторые типы пролиферативных заболеваний, такие как рак молочной железы и матки и эндометриоз, индуцированы эстрогенами и, следовательно, антиэстрогены (т.е. антагонисты эстрогена) обладают применимостью в предупреждении и лечении таких типов нарушений.
[6] Существуют две различные формы эстрогенового рецептора, обычно называемые α и β, каждая из которых кодируется отдельным геном (соответственно ESR1 и ESR2). Оба ER широко экспрессируются в различных типах ткани, но существуют некоторые существенные отличия в их паттернах экспрессии. ERα встречается в эндометрии, раковых клетках молочной железы, клетках стромы яичника и гипоталамусе. У мужчин белок ERα встречается в эпителии отводящих протоков. Экспрессия белка ERβ была подтверждена в почках, головном мозге, костях, сердце, легких, слизистой оболочке кишечника, предстательной железе и эндотелиальных клетках. Следовательно, разработка селективных лигандов, таким образом, может обеспечить сохранение положительных аспектов эстрогена.
[7] Рак молочной железы является наиболее распространенным злокачественным новообразованием, затрагивающим женщин, и частота возникновения заболевания увеличивается во всем мире. В частности, эстрогены действуют как эндокринные факторы роста для по меньшей мере одной трети случаев рака молочной железы, и лишение опухоли данного стимула является общепризнанной терапией для заболевания на поздней стадии у женщин до менопаузы, этого достигают путем прекращения функции яичников посредством хирургического вмешательства, лучевой терапии или медицинскими способами и у женщин после менопаузы - путем применения ингибиторов ароматазы.
[8] Альтернативный подход к выводу эстрогена заключается в антагонизировании эстрогена с помощью антиэстрогенов. Они представляют собой лекарственные средства, которые связываются с эстрогеновыми рецепторами (ER), присутствующими в эстрогенчувствительной ткани, и конкурируют за них. Традиционные нестероидные антиэстрогены, такие как тамоксифен, эффективно конкурируют за связывание с ER, но их эффективность зачастую ограничена частичным агонизмом, который они демонстрируют, что приводит к неполной блокировке опосредованной эстрогеном активности. Специфичный или «чистый» антиэстроген с высокой аффинностью к ER и без какого-либо агонистического эффекта может обладать преимуществами в лечении эстрогензависимого заболевания по сравнению с традиционными нестероидными антиэстрогенами. Фулвестрант является первым из нового класса эффективных чистых антиэстрогенов и характеризуется полным отсутствием активности частичного агониста, эстроген-подобной активности, ассоциированных с доступными в настоящее время антиэстрогенами, такими как тамоксифен.
[9] В связи с этим существует необходимость в других подходах антагонизирования рецептора ER. Один подход будет заключаться в разработке селективных супрессоров или разрушителей ER, которые уменьшают уровень экспрессии ER либо на уровне транскрипции, либо на уровне белка.
[10] Большинство низкомолекулярных лекарственных средств связывают ферменты или рецепторы в плотных и четко определенных карманах. С другой стороны, общеизвестно, что осуществить нацеливание белок-белковых взаимодействий с применением малых молекул является сложным из-за их большой поверхности контакта и вовлечения мелких бороздок или плоских поверхностей соприкосновения. Е3-убиквитинлигазы (из которых сотни известны у людей) придают субстратную специфичность для убиквитинирования и, следовательно, являются более привлекательными терапевтическими мишенями, чем обычные ингибиторы протеасом из-за их специфичности в отношении определенных белковых субстратов. Разработка лигандов для Е3-лигаз оказалась сложной, частично из-за того факта, что они должны нарушать белок-белковые взаимодействия. Однако недавние разработки позволили получить специфические лиганды, которые связываются с такими лигазами. Например, с момента открытия нутлинов, первых низкомолекулярных ингибиторов E3-лигазы, сообщалось о дополнительных соединениях, которые нацеливаются на E3-лигазы, однако данная область остается недостаточно развитой. Например, с момента открытия нутлинов, первых низкомолекулярных ингибиторов гомолога 2 double minute мыши (MDM2), являющегося E3-лигазой, сообщалось о дополнительных соединениях, которые нацеливаются на E3-лигазы MDM2 (т.е. double minute 2 человека или HDM2) (J. Di, et al. Current Cancer Drug Targets (2011), 11(8), 987-994).
[11] Ген-супрессор опухоли р53 выполняет важную функцию в прекращении роста клеток и апоптозе в ответ на повреждение ДНК или стресс (A. Vazquez, et al. Nat. Rev. Drug. Dis. (2008), 7, 979-982), и инактивация р53 была предложена как один из основных путей выживания опухолевых клеток (А.J. Levine, et al. Nature (2000), 408, 307-310). У приблизительно 50% пациентов, у которых имеется рак, была обнаружена мутация р53 (М. Hollstein, et al. Science (1991), 233, 49-53), тогда как у пациентов с р53 дикого типа зачастую обнаруживают супрессию р53 с помощью MDM2 посредством белок-белкового взаимодействия р53 и MDM2 (Р. Chene, et al. Nat. Rev. Cancer (2003), 3, 102-109). В нормальных клеточных условиях без онкогенного сигнала стресса MDM2 поддерживает р53 при низких концентрациях. В ответ на повреждение ДНК или клеточный стресс уровень р53 увеличивается, и это также вызывает увеличение уровня MDM2 вследствие отрицательной обратной связи от ауторегуляторной системы p53/MDM2. Другими словами, р53 регулирует MDM2 на уровне транскрипции, и MDM2 регулирует р53 на уровне его активности (А.J. Levine, et al. Genes Dev. (1993) 7, 1126-1132).
[12] Несколько механизмов могут объяснить супрессию р53 с помощью MDM2. Сначала MDM2 связывается с N-концевым доменом р53 и блокирует экспрессию р53-чувствительных генов (J. Momand, et al. Cell (1992), 69, 1237-1245). Затем MDM2 перемещает р53 от ядра в цитоплазму для способствования протеолитическому разрушению (J. Roth, et al. EMBO J. (1998), 17, 554-564). Наконец, MDM2 осуществляет собственную E3-лигазную активность, заключающуюся в конъюгировании убиквитина с р53 для его разрушения с помощью протеасомной убиквитин-зависимой системы 26s (UPS) (Y. Haupt, et al. Nature (1997) 387, 296-299). В связи с этим, поскольку MDM2 функционирует в качестве E3-лигазы, рекрутирование MDM2 к обуславливающему заболевание белку и осуществление его убиквитинирования и разрушения является очень интересным подходом для разработки лекарственных средств.
[13] Одна E3-лигаза с многообещающим терапевтическим потенциалом представляет собой онкосупрессор болезни Гиппеля-Линдау (VHL), субъединицу, осуществляющую распознавание субстрата, E3-лигазного комплекса VCB, который также состоит из элонгинов В и С, Cul2 и Rbx1. Основной субстрат VHL представляет собой фактор, индуцируемый гипоксией 1α (HIF-1α), фактор транскрипции, повышающий экспрессию генов, такой как проангиогенный фактор роста VEGF, и цитокин эритропоэтин, индуцирующий образование эритроцитов в ответ на низкие уровни кислорода. Были получены первые низкомолекулярные лиганды белка Гиппеля-Линдау (VHL), связывающиеся с субъединицей, осуществляющей распознавание субстрата, E3-лигазы, и получили кристаллические структуры, подтверждающие, что соединение имитирует механизм связывания фактора транскрипции HIF-1α, главного субстрата VHL.
[14] Цереблон представляет собой белок, который у людей кодируется геном CRBN. Ортологи CRBN являются высококонсервативными среди организмов, начиная от растений и заканчивая людьми, что подчеркивает его физиологическое значение. Цереблон входит в состав E3-убиквитинлигазного комплекса со связывающимся с поврежденной ДНК белком 1 (DDB1), куллином-4А (CUL4A) и регулятором куллинов 1 (ROC1). Данный комплекс осуществляет убиквитинирование ряда других белков. С помощью механизма, который еще полностью не выяснен, убиквитинирование целевых белков с помощью цереблона приводит к повышенным уровням фактора роста фибробластов 8 (FGF8) и фактора роста фибробластов 10 (FGF10). FGF8, в свою очередь, регулирует ряд процессов развития, таких как образование конечностей и слухового пузырька. Конечный результат состоит в том, что данный комплекс убиквитинлигазы является важным для роста конечностей у эмбрионов. В отсутствие цереблона DDB1 образует комплекс с DDB2, который функционирует как белок, связывающийся с поврежденной ДНК.
[15] Ингибиторы белков апоптоза (IAP) представляют собой семейство белков, вовлеченных в подавление апоптоза, т.е. гибель клеток. Семейство IAP человека включает 8 представителей, и многочисленные другие организмы содержат гомологи IAP. IAP содержат специфичный в отношении E3-лигазы домен и повторяющиеся домены бакуловирусного IAP (BIR), которые распознают субстраты и способствуют их убиквитинированию. IAP способствуют убиквитинированию и могут непосредственно связывать и ингибировать каспазы. Каспазы представляют собой протеазы (например, каспаза-3, каспаза-7 и каспаза-9), которые обеспечивают осуществление апоптоза. В связи с этим посредством связывания каспаз IAP предотвращают гибель клеток. Однако проапоптический стимул может привести к высвобождению митохондриальных белков DIABLO (также известных как второй митохондриальный активатор каспаз или SMAC) и HTRA2 (также известный как Omi). Связывание DIABLO и HTRA2, по-видимому, блокирует активность IAP.
[16] SMAC взаимодействует по сути со всеми известными IAP, в том числе с XIAP, c-IAP1, C-IAP2, NIL-IAP, Bruce и сурвивином. Первые четыре аминокислоты (AVPI) зрелого SMAC связываются с частью IAP, которая, как полагают, является ключевой для блокирования антиапоптических эффектов IAP.
[17] Бифункциональные соединения, такие как соединения, описанные в публикациях заявок на патент США №№2015-0291562 и 2014-0356322 (включенные в данный документ посредством ссылки), действуют таким образом, чтобы обеспечить рекрутинг эндогенных белков к E3-убиквитинлигазе для разрушения. В частности, в публикациях описаны бифункциональные или химерные соединения, осуществляющие целенаправленное воздействие посредством протеолиза (PROTAC), которые находят применение в качестве модуляторов направленного убиквитинирования разнообразных полипептидов и других белков, которые затем разрушаются и/или другим образом ингибируются с помощью бифункциональных соединений.
[18] В настоящем изобретении определены соединения, способные подавлять функцию эстрогенового рецептора, в том числе соединения, которые разрушают эстрогеновый рецептор.
КРАТКОЕ ОПИСАНИЕ
[19] В настоящем изобретении описаны бифункциональные соединения, функция которых состоит в привлечении эндогенных белков к E3-убиквитинлигазе для разрушения, и способы их применения. В частности, настоящее изобретение предусматривает бифункциональные или химерные соединения, осуществляющие целенаправленное воздействие посредством протеолиза (PROTAC), которые находят применение в качестве модуляторов направленного убиквитинирования разнообразных полипептидов и других белков, которые затем разрушаются и/или другим образом ингибируются с помощью бифункциональных соединений, описанных в данном документе. Преимущество соединений, представленных в данном документе, состоит в том, что возможен широкий спектр фармакологических активностей, согласующийся с разрушением/ингибированием целевых полипептидов из практически любого класса или семейства белков. Кроме того, в описании представлены способы применения эффективного количества соединений, описанных в данном документе, для лечения или облегчения болезненного состояния, такого как рак, например, рак молочной железы.
[20] В связи с этим, в одном аспекте настоящего изобретения предусмотрены бифункциональные соединения или соединения PROTAC, которые содержат фрагмент, связывающий E3-убиквитинлигазу (т.е. лиганд для E3-убиквитинлигазы или группа «ULM»), и фрагмент, который связывает целевой белок (т.е. лиганд, нацеливающийся на белок/полипептид, или группа «РТМ») так, что целевой белок/полипептид размещают в непосредственной близости от убиквитинлигазы для осуществления разрушения (и ингибирования) данного белка. В предпочтительном варианте осуществления ULM (модулятор убиквитинлигазы) может представлять собой фрагмент, связывающийся с белком Гиппеля-Линдау (VHL) E3-убиквитинлигазного комплекса (VLM), или фрагмент, связывающийся с цереблоном E3-убиквитинлигазного комплекса (CLM), или фрагмент, связывающий E3-убиквитинлигазу, представляющую собой гомолог 2 double minute мыши (MDM2) (MLM), или фрагмент, связывающийся с IAP E3-убиквитинлигазного комплекса (т.е. «ILM»). Например, структура бифункционального соединения может быть изображена как:

[21] Соответствующие положения фрагментов РТМ и ULM (например, VLM, CLM, MLM, ILM или их комбинации), а также их число, как проиллюстрировано в данном документе, представлено только в качестве примера и не предназначено для ограничения соединений каким-либо образом. Специалисту в данной области техники будет понятно, что бифункциональные соединения, описанные в данном документе, могут быть синтезированы так, что число и положение соответствующих функциональных фрагментов могут варьировать по необходимости.
[22] В определенных вариантах осуществления бифункциональное соединение дополнительно содержит химический линкер («L»). В данном примере структура бифункционального соединения может быть изображена как:

где РТМ представляет собой фрагмент, нацеливающийся на белок/полипептид, L представляет собой линкер, например, связь или химическую группу, связывающий РТМ с ULM, и ULM представляет собой фрагмент, связывающийся с IAP E3-убиквитинлигазного комплекса (ILM), или фрагмент, связывающийся с белком Гиппеля-Линдау (VHL) E3-убиквитинлигазного комплекса (VLM), или фрагмент, связывающийся с цереблоном E3-убиквитинлигазного комплекса (CLM), или фрагмент, связывающий E3-убиквитинлигазу, представляющую собой гомолог 2 double minute мыши (MDM2) (MLM).
[23] Например, структура бифункционального соединения может быть изображена как:
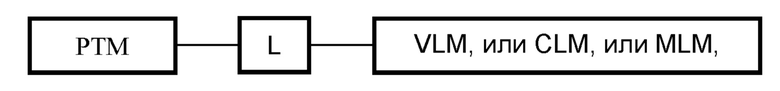
где РТМ представляет собой фрагмент, нацеливающийся на белок/полипептид; «L» представляет собой линкер (например, связь или химическую линкерную группу), связывающий РТМ и по меньшей мере одно из VLM, CLM, MLM, ILM или их комбинацию; VLM представляет собой фрагмент, связывающийся с белком Гиппеля-Линдау E3-убиквитинлигазного комплекса, который связывается с VHL E3-лигазного комплекса; CLM представляет собой фрагмент, связывающийся с цереблоном E3-убиквитинлигазного комплекса, который связывается с цереблоном; MLM представляет собой фрагмент, связывающий E3-убиквитинлигазу MDM2; и ILM представляет собой фрагмент, связывающийся с IAP, который связывается с IAP.
[24] В одном аспекте настоящее изобретение предусматривает соединение формулы (I) или (II),
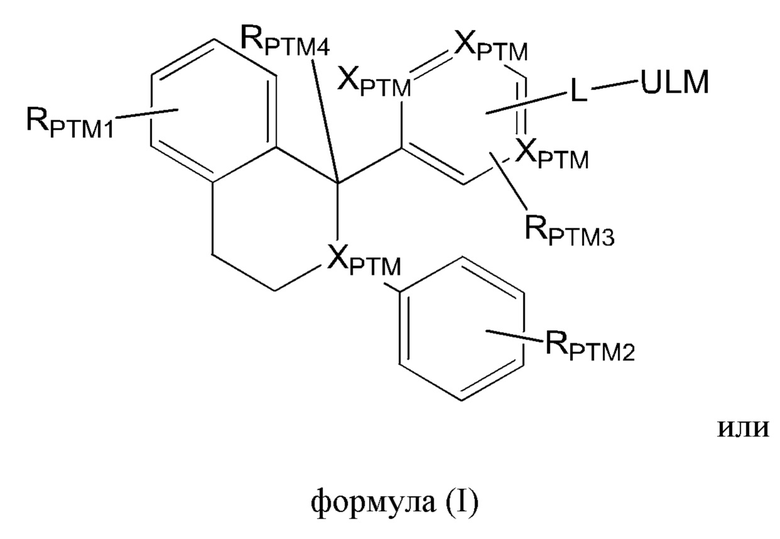
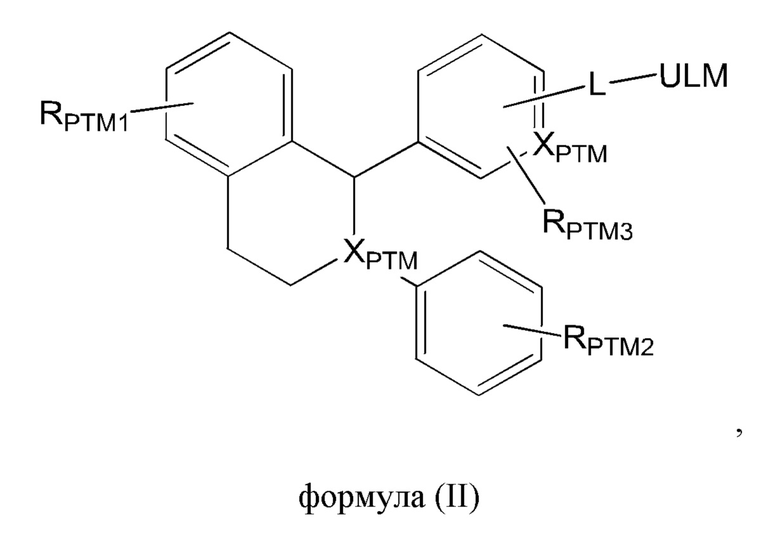
где
каждый XPTM независимо представляет собой СН, N;
ULM представляет собой ULM, представляющий собой ILM, или VLM, или CLM, или MLM;
L представляет собой связь или линкерный фрагмент, связывающий тетрагидронафталиновый или тетрагидроизохинолиновый фрагмент и по меньшей мере одно из VLM, CLM, ILM, VLM или их комбинацию;
каждый RPTM1 независимо представляет собой ОН, галоген, алкокси (например, метокси или этокси), O(CO)RPTM, при этом замещение может предусматривать моно-, ди- или тризамещение, и rptm представляет собой алкильную или циклоалкильную группу с 1-6 атомами углерода или арильные группы;
каждый RPTM2 независимо представляет собой Н, галоген, CN, CF3, линейный или разветвленный алкил, алкокси (например, метокси или этокси), при этом замещение может предусматривать моно- или дизамещение;
каждый PPTM3 независимо представляет собой Н, галоген, при этом замещение может предусматривать моно- или дизамещение; и
RPTM4 представляет собой Н, алкил, метил, этил.
[25] В некоторых предпочтительных вариантах осуществления ILM представляет собой тетрапептидный фрагмент AVPI. В связи с этим в определенных дополнительных вариантах осуществления ILM бифункционального соединения содержит аминокислоты аланин (А), валин (V), пролин (Р) и изолейцин (I) или их неприродные миметики соответственно. В дополнительных вариантах осуществления аминокислоты в тетрапептидном фрагменте AVPI соединены друг с другом посредством амидных связей (т.е. -C(O)NH- или -NHC(O)-).
[26] В определенных вариантах осуществления соединения, описанные в данном документе, содержат несколько независимо выбранных ULM, несколько РТМ, несколько химических линкеров или их комбинацию.
[27] В определенных вариантах осуществления ILM содержит химические фрагменты, такие как фрагменты, описанные в данном документе.
[28] В дополнительных вариантах осуществления VLM может представлять собой гидроксипролин или его производное. Кроме того, другие рассматриваемые VLM включены в публикацию заявки на патент США №2014/03022523, которая, как указано выше, включена в данный документ во всей своей полноте.
[29] В одном варианте осуществления CLM содержит химическую группу, полученную из имида, тиоимида, амида или тиоамида. В конкретном варианте осуществления химическая группа представляет собой фталимидную группу или ее аналог или производное. В определенном варианте осуществления CLM представляет собой талидомид, леналидомид, помалидомид, их аналоги, их изостеры или их производные. Другие рассматриваемые CLM описаны в публикации заявки на патент США №2015/0291562, которая включена в данный документ во всей своей полноте.
[30] В определенных вариантах осуществления MLM может представлять собой нутлин или его производное. Кроме того, другие рассматриваемые MLM включены в заявку на патент США №15/206497, поданную 11 июля 2016 года, которая, как указано выше, включена в данный документ во всей своей полноте. В определенных дополнительных вариантах осуществления MLM бифункционального соединения содержит химические фрагменты, такие как замещенные имидазолины, замещенные спироиндолиноны, замещенные пирролидины, замещенные пиперидиноны, замещенные морфолиноны, замещенные пирролопиримидины, замещенные имидазолопиридины, замещенный тиазолоимидазолин, замещенные пирролопирролидиноны и замещенные изохинолиноны.
[31] В дополнительных вариантах осуществления MLM предусматривает основные структуры, указанные выше, со смежными бис-арильными замещениями, расположенными в виде цис- или транс-конфигураций.
[32] В определенных вариантах осуществления «L» представляет собой связь. В дополнительных вариантах осуществления линкер «L» представляет собой соединяющую молекулу с линейной структурой с числом отличных от водорода атомов в диапазоне от 1 до 20. Соединяющая молекула «L» может содержать без ограничения функциональные группы, такие как эфирная, амидная, алкановая, алкеновая, алкиновая группы, кетогруппа, гидроксильная группа, группа карбоновой кислоты, тиоэфирная, сульфоксидная и сульфоновая группы. Линкер может содержать ароматические, гетероароматические, циклические, бициклические и трициклические фрагменты. Замещение галогеном, таким как Cl, F, Br и I, может быть включено в линкер. В случае замещения фтором, могут быть включены один или множество атомов фтора.
[33] В определенных вариантах осуществления VLM представляет собой производное транс-3-гидроксипролина, где как азот, так и карбоновая кислота в транс-3-гидроксипролине функционализированы как амиды.
[34] В одном варианте осуществления CLM содержит химическую группу, полученную из имида, тиоимида, амида или тиоамида. В конкретных вариантах осуществления химическая группа представляет собой фталимидогруппу или ее аналог или производное. В определенных вариантах осуществления CLM представляет собой талидомид, леналидомид, помалидомид, их аналоги, их изостеры или их производные. Другие рассматриваемые CLM описаны в публикации заявки на патент США US 2015/-0291562, которая включена в данный документ во всей своей полноте. В некоторых вариантах осуществления CLM представляет собой производное пиперидин-2,6-диона, где пиперидин-2,6-дион может быть замещен в 3-положении, и при этом 3-замещение может предусматривать замещение бициклическими гетероароматическими соединениями с соединением в виде связи С-N или связи С-С. Примеры CLM могут представлять собой без ограничения помалидомид, леналидомид и талидомид и их производные.
[35] В определенных вариантах осуществления «L» представляет собой связь. В дополнительных вариантах осуществления линкер «L» представляет собой соединяющую молекулу с линейной структурой с числом отличных от водорода атомов в диапазоне от 1 до 20. Соединяющая молекула «L» может содержать без ограничения функциональные группы, такие как эфирная, амидная, алкановая, алкеновая, алкиновая группы, кетогруппа, гидроксильная группа, группа карбоновой кислоты, тиоэфирная, сульфоксидная и сульфоновая группы. Линкер может содержать ароматические, гетероароматические, циклические, бициклические и трициклические фрагменты. Замещение галогеном, таким как Cl, F, Br и I, может быть включено в линкер. В случае замещения фтором, могут быть включены один или множество атомов фтора.
[36] В дополнительном аспекте в описании представлены терапевтические композиции, содержащие эффективное количество соединения, описанного в данном документе, или его солевой формы и фармацевтически приемлемый носитель. Терапевтические композиции модулируют разрушение и/или ингибирование белка у пациента или субъекта, например, у животного, как, например, у человека, и могут применяться для лечения или облегчения болезненных состояний или состояний, модулирование которых обеспечивается посредством разрушения и/или ингибирования белка. В определенных вариантах осуществления терапевтические композиции, описанные в данном документе, можно применять для обеспечения разрушения белков, представляющих интерес, для лечения или облегчения заболевания, например рака. В определенных дополнительных вариантах осуществления заболевание представляет собой по меньшей мере одно из рака молочной железы, рака матки, рака яичников, рака предстательной железы, рака эндометрия, эндометриоза или их комбинации. В еще одном аспекте настоящее изобретение предусматривает способ обеспечения убиквитинирования/разрушения целевого белка в клетке. В определенных вариантах осуществления способ включает введение бифункционального соединения, описанного в данном документе, содержащего ILM и РТМ, РТМ и VLM или РТМ и CLM, или РТМ и MLM, предпочтительно соединенных с помощью линкерного фрагмента, описанного далее в данном документе, где VLM/ILM/CLM/MLM связаны с РТМ посредством линкера для нацеливания на белок, который связывается с РТМ для разрушения. Подобным образом, при этом РТМ (например, тетрагидронафталиновый или тетрагидроизохинолиновый фрагмент) связан с по меньшей мере одним из VLM, CLM, MLM, ILM или их комбинацией с помощью линкера для нацеливания на белок или полипептид для разрушения. Разрушение целевого белка будет происходить при размещении целевого белка в непосредственной близости от E3-убиквитинлигазы, что, таким образом, приводит к разрушению целевого белка/подавлению его эффектов и контролю уровней белка. Контроль уровней белка, предоставляемый настоящим изобретением, обеспечивает лечение болезненного состояния или состояния, модулируемых за счет целевого белка путем снижения уровня данного белка в клетках пациента.
[37] В еще одном аспекте в описании представлены способы лечения или облегчения заболевания, нарушения или их симптома у субъекта или пациента, например, у животного, такого как человек, включающие введение субъекту, нуждающемуся в этом, композиции, содержащей эффективное количество, например терапевтически эффективное количество, соединения, описанного в данном документе, или его солевой формы и фармацевтически приемлемый носитель, при этом композиция является эффективной для лечения или облегчения заболевания или нарушения или их симптома у субъекта.
[38] В другом аспекте в описании предусмотрены способы идентификации эффектов разрушения белков, представляющих интерес, в биологической системе с применением соединений в соответствии с настоящим изобретением.
[39] Предшествующие общие области применения приведены только в качестве примера и не предназначены для ограничения объема настоящего изобретения и прилагаемой формулы изобретения. Дополнительные объекты и преимущества, ассоциированные с композициями, способами и процессами по настоящему изобретению будут понятны специалисту в данной области техники в свете данных формулы изобретения, описания и примеров. Например, различные аспекты и варианты осуществления настоящего изобретения можно применять в многочисленных комбинациях, все из которых явным образом предусмотрены настоящим описанием. Такие дополнительные аспекты и варианты осуществления явным образом включены в объем настоящего изобретения. Публикации и другие материалы, применяемые в данном документе для освещения уровня техники настоящего изобретения и, в конкретных случаях, для предоставления дополнительных подробностей в отношении его реализации, включены посредством ссылки.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
[40] Сопутствующие графические материалы, которые включены в описание и образуют его часть, иллюстрируют несколько вариантов осуществления настоящего изобретения и вместе с описанием служат для объяснения идей настоящего изобретения. Графические материалы предназначены только для иллюстрации варианта осуществления настоящего изобретения и не должны толковаться как ограничивающие настоящее изобретение. Дополнительные объекты, признаки и преимущества настоящего изобретения станут очевидными из следующего подробного описания, рассматриваемого совместно с сопутствующими фигурами, показывающими иллюстративные варианты осуществления настоящего изобретения, в которых:
[41] Фигура 1. Иллюстрация основного принципа функционирования PROTAC. (А) Иллюстративные PROTAC содержат фрагмент, нацеливающийся на белок (РТМ; заштрихованный прямоугольник темного цвета), фрагмент, связывающий убиквитинлигазу (ULM; заштрихованный треугольник светлого цвета), и необязательно линкерный фрагмент (L; черная линия), связывающий или присоединяющий РТМ к ULM. (В) Проиллюстрировано функциональное применение PROTAC, описанных в данном документе. Вкратце, ULM распознает и связывается со специфичной E3-убиквитинлигазой, и РТМ связывается и рекрутирует целевой белок, приводя его в непосредственную близость от E3-убиквитинлигазы. Как правило, E3-убиквитинлигаза образует комплекс с Е2-убиквитинконъюгирующим белком и либо отдельно, либо с помощью белка Е2 катализирует присоединение убиквитина {темные круги) к лизину на целевом белке посредством изопептидной связи. На полиубиквитинированный белок (крайний справа) затем целенаправленно воздействуют с разрушением с помощью протеосомального механизма клетки.
[42] Фигура 2. Разрушение ERα в клетках MCF7 с помощью иллюстративных соединений по настоящему изобретению: пример 1 и пример 62. Клетки MCF7 обрабатывали соединениями в 7 концентрациях (100 нМ, 30 нМ, 10 нМ, 3 нМ, 1 нМ, 0,3 нМ и 0,1 нМ) в присутствии 10% FBS. Клетки инкубировали в течение 48 часов перед лизисом. Лизат анализировали посредством иммуноблоттинга. D: DMSO.
[43] Фигура 3. Разрушение ERα в клетках MCF7 с помощью иллюстративных соединений по настоящему изобретению: пример 341, пример 510, пример 511 и пример 515. Клетки MCF7 обрабатывали соединениями в 5 концентрациях (100 нМ, 33 нМ, 11 нМ, 3,7 нМ и 1,2 нМ) или фулвестрантом при 100 нМ в присутствии 10% FBS. Клетки инкубировали в течение 72 часов перед лизисом. Лизат анализировали посредством иммуноблоттинга. F: фулвестрант.
[44] Фигура 4. Разрушение ERα в клетках T47D с помощью иллюстративных соединений по настоящему изобретению: примеры 1 и 62. Клетки T47D обрабатывали соединениями в 7 концентрациях (100 нМ, 30 нМ, 10 нМ, 3 нМ, 1 нМ, 0,3 нМ и 0,1 нМ) или с помощью DMSO в присутствии 10% FBS. Клетки инкубировали в течение 72 часов перед лизисом. Лизат анализировали посредством иммуноблоттинга. D: DMSO.
[45] Фигура 5. Таблица 1. Активность, способы синтеза и определение характеристик иллюстративных PROTAC, целенаправленно воздействующих на ER.
[46] Фигура 6. Таблица 2. Активность, способы синтеза и определение характеристик иллюстративных PROTAC, целенаправленно воздействующих на ER.
[47] Фигура 7. Таблица 3. Активность в отношении разрушения ERα, химическое название и данные ЯМР для иллюстративных PROTAC, целенаправленно воздействующих на ER. Диапазоны DC50 касательно разрушения: DC50 < 5 нМ (А); 5 нМ < DC50 < 50 нМ (В); DC50 > 50 нМ (С); диапазоны Dmax касательно разрушения: Dmax > 75% (А); 50% < Dmax < 75 (В); Dmax < 50% (С).
ПОДРОБНОЕ ОПИСАНИЕ
[48] Следующее подробное описание представлено для оказания специалисту в данной области техники поддержки в отношении практического применения настоящего изобретения. Специалисты в данной области техники могут осуществлять модификации и изменения в вариантах осуществления, описанных в данном документе, без отступления от сущности или объема настоящего изобретения. Все публикации, заявки на патенты, патенты, фигуры и другие источники, упомянутые в данном документе, явным образом включены посредством ссылки во всей своей полноте.
[49] В настоящем изобретении описаны композиции и способы, которые относятся к удивительному и неожиданному открытию того, что белок E3-убиквитинлигазного комплекса (например, ингибиторы белков апоптоза (IAP), белок Гиппеля-Линдау (VHL) E3-убиквитинлигазного комплекса, цереблон E3-убиквитинлигазного комплекса или E3-убиквитинлигаза, представляющая собой гомолог 2 double minute мыши (MDM2)) убиквитинирует целевой белок как только его и целевой белок размещает в непосредственной близости друг от друга бифункциональная или химерная конструкция, которая связывает белок E3-убиквитинлигазного комплекса и целевой белок. Соответственно, настоящее изобретение предусматривает такие соединения и композиции, содержащие фрагмент, связывающий E3-убиквитинлигазу («ULM»), связанный с фрагментом, связывающим белок-мишень («РТМ»), что обеспечивает убиквитинирование выбранного целевого белка (например, эстрогенового рецептора [ER]) с обеспечением разрушения целевого белка протеасомой (см. фигуры 1А и 1В). Настоящее изобретение также предусматривает библиотеку композиций и ее применение.
[50] В определенных аспектах настоящее изобретение предусматривает соединения, которые содержат лиганд, например низкомолекулярный лиганд (т.е. с молекулярной массой менее 2000, 1000, 500 или 200 дальтон), который способен связываться с E3-убиквитинлигазой, такой как IAP, VHL, MDM2 или цереблон, и фрагмент, который способен связываться с целевым белком таким образом, что целевой белок (такой как ER) размещается в непосредственной близости от E3-убиквитинлигазы с осуществлением разрушения (и/или ингибирования) данного белка. Низкомолекулярный может означать, в дополнение к вышеуказанному, что молекула не является пептидилом, т.е. обычно не считается пептидом, например, содержит менее 4, 3 или 2 аминокислот. В соответствии с настоящим описанием молекула РТМ, ULM или PROTAC может быть низкомолекулярной.
[51] Если не указано иное, все технические и научные термины, применяемые в данном документе, имеют то же значение, обычно понятное специалисту в данной области техники, к которой относится настоящее изобретение. Терминология, применяемая в описании, предназначена только для описания конкретных вариантов осуществления и не предполагается как ограничивающая настоящее изобретение.
[52] Если представлен диапазон значений, подразумевается, что каждое промежуточное значение с точностью до десятой доли единицы нижнего предела, если из контекста явно не следует иное (как, например, в случае группы, содержащей определенное количество атомов углерода, в случае которой представлено количество каждого атома углерода, который попадает в диапазон), между верхним и нижним пределом данного диапазона и любое другое указанное или промежуточное значение в данном указанном диапазоне охватываются настоящим изобретением. Верхние и нижние пределы таких меньших диапазонов, которые могут быть независимо включены в меньшие диапазоны, также охватываются настоящим изобретением, с учетом любого конкретно исключенного предела в указанном диапазоне. Если указанный диапазон включает один или оба предела, диапазоны, исключающие оба из этих включенных пределов, также включены в настоящее изобретение.
[53] Для описания настоящего изобретения применяют следующие термины. В случаях, если термин конкретно не определен в данном документе, то такой термин имеет значение, общепризнанное средними специалистами в данной области техники, при использовании такого термина в контексте его применения в описании настоящего изобретения.
[54] Формы единственного числа, используемые в данном документе и в прилагаемой формуле изобретения, используются в данном документе для обозначения одного или более одного (т.е. по меньшей мере одного) грамматических объектов данной формы единственного числа, если в контексте явно не указано иное. В качестве примера «элемент» означает один элемент или более одного элемента.
[55] Фразу «и/или», используемую в данном документе в описании и в формуле изобретения, следует понимать как означающую «один или оба» из элементов, объединенных таким образом, т.е. элементы, которые в одних случаях присутствуют совместно, а в других случаях присутствуют раздельно. Несколько элементов, перечисленных с помощью «и/или», должны толковаться одинаково, т.е. «один или более» из элементов, объединенных таким образом. Могут необязательно присутствовать другие элементы, отличные от элементов, конкретно определенных выражением «и/или», независимо от того, связаны ли они или не связаны с данными конкретно определенными элементами. Таким образом, в качестве неограничивающего примера ссылка на «А и/или В», в случае применения совместно с открытой формулировкой, такой как «содержащий», может относиться в одном варианте осуществления только к А (необязательно включая элементы, отличные от В); в другом варианте осуществления только к В (необязательно включая элементы, отличные от А); в еще одном варианте осуществления как к А, так и к В (необязательно включая другие элементы) и т.д.
[56] Как используется в данном документе в описании и в формуле изобретения, термин «или» следует понимать как имеющий такое же значение, как «и/или», как определено выше. Например, при разделении объектов в списке «или» или «и/или» следует понимать как включающие, т.е. включение по меньшей мере одного, но также включение более одного из числа или списка элементов и необязательно дополнительных не включенных в список объектов. Только термины, четко указывающие на противоположное, такие как «только один из» или «точно один из», или, если применяется в формуле изобретения, «состоящий из», будут относиться к включению точно одного элемента из числа или списка элементов. В целом, термин «или», используемый в данном документе, следует понимать только как указывающий на исключающие альтернативы (т.е. «один или другой, но не оба»), если ему предшествуют термины исключительности, такие как «либо», «один из», «только один из» или «точно один из».
[57] В формуле изобретения, а также в вышеприведенном описании все переходные фразы, такие как «содержащий», «включающий», «несущий», «имеющий», «вмещающий», «предусматривающий», «удерживающий», «состоящий из» и т.п., следует понимать как открытые, т.е. означающие включающий без ограничения. Только переходные фразы «состоящий из» и «по сути состоящий из» должны быть закрытыми или полузакрытыми переходными фразами соответственно, как изложено в разделе 2111.03 руководства по процедурам патентной экспертизы патентного ведомства США.
[58] Используемую в данном документе в описании и в формуле изобретения фразу «по меньшей мере один» по отношению к списку одного или более элементов следует понимать как означающую по меньшей мере один элемент, выбранный из любого одного или более элементов в списке элементов, но не обязательно включающую по меньшей мере один из абсолютно всех элементов, конкретно перечисленных в списке элементов, и не исключающую любые комбинации элементов из списка элементов. Данное определение также допускает то, что необязательно могут присутствовать элементы, отличные от элементов, конкретно идентифицированных в списке элементов, к которым относится фраза «по меньшей мере один», независимо от того, связаны ли они или не связаны с данными конкретно определенными элементами. Таким образом, в качестве неограничивающего примера «по меньшей мере один из А и В» (или эквивалентно «по меньшей мере один из А или В», или эквивалентно «по меньшей мере один из А и/или В») может относиться в одном варианте осуществления к по меньшей мере одному, необязательно включая более одного. А, без присутствия В (и необязательно включая элементы, отличные от В); в другом варианте осуществления к по меньшей мере одному, необязательно включая более одного. В, без присутствия А (и необязательно включая элементы, отличные от А); в еще одном варианте осуществления к по меньшей мере одному, необязательно включая более одного, А и по меньшей мере одному, необязательно включая более одного, В (и необязательно включая другие элементы) и т.д.
[59] Также следует понимать, что в определенных способах, описанных в данном документе, которые включают более одной стадии или действия, порядок стадий или действий способа не обязательно ограничен порядком, в котором изложены стадии или действия способа, если в контексте не указано иное.
[60] Термины «совместное введение» и «осуществление совместного введения» или «комбинированная терапия» относятся как к одновременному введению (введению двух или более терапевтических средств в одно и то же время), так и к разделенному во времени введению (введение одного или более терапевтических средств в момент времени, отличный от момента введения дополнительного терапевтического средства или средств), при условии, что терапевтические средства присутствуют у пациента до некоторой степени, предпочтительно в эффективных количествах, в одно и то же время. В определенных предпочтительных аспектах одно или более соединений по настоящему изобретению, описанных в данном документе, вводят совместно в комбинации с по меньшей мере одним дополнительным биологически активным средством, в том числе, в частности, противораковым средством. В особенно предпочтительных аспектах совместное введение соединений приводит к синергетической активности и/или терапии, в том числе противораковой активности.
[61] Термин «соединение», используемый в данном документе, если не указано иное, относится к любому конкретному химическому соединению, раскрытому в данном документе, и включает его таутомеры, региоизомеры, геометрические изомеры и, в применимых случаях, стереоизомеры, включая оптические изомеры (энантиомеры) и другие стереоизомеры (диастереомеры), а также его фармацевтически приемлемые соли и производные, в том числе пролекарство и/или их дейтерированные формы, в случае применимости в соответствующем контексте. Рассматриваемые дейтерированные малые молекулы представляют собой молекулы, в которых один или более атомов водорода, содержащихся в молекуле лекарственного средства, были заменены дейтерием.
[62] При его использовании в соответствующем контексте термин «соединение» обычно относится к одному соединению, но он также может включать другие соединения, такие как стереоизомеры, региоизомеры и/или оптические изомеры (включая рацемические смеси), а также конкретные энантиомеры или энантиомерно обогащенные смеси раскрытых соединений. В соответствующем контексте данный термин также относится к формам пролекарства соединений, которые были модифицированы для облегчения введения и доставки соединений к месту осуществления активности. Следует отметить, что при описании соединений по настоящему изобретению среди прочего описаны многочисленные заместители и переменные, связанные с ними. Средние специалисты в данной области техники поймут, что молекулы, которые описаны в данном документе, представляют собой устойчивые соединения, как в общем описано в данном документе. Если показана связь, как двойная связь, так и одинарная связь представлены или понимаются в контексте показанного соединения и широко известных правил взаимодействия валентности.
[63] Термин «убиквитинлигаза» относится к семейству белков, которые облегчают перенос убиквитина к специфичному субстратному белку, осуществляя нацеливание субстратного белка для разрушения. Например, IAP является белком E3-убиквитинлигазного комплекса, который в отдельности или в комбинации с Е2-убиквитинконъюгирующим ферментом обуславливает присоединение убиквитина к лизину на целевом белке и затем осуществляет нацеливание специфичных белковых субстратов для разрушения с помощью протеасомы. Таким образом, E3-убиквитинлигаза в отдельности или в комплексе с Е2-убиквитинконъюгирующим ферментом является ответственной за перенос убиквитина к целевым белкам. В целом, убиквитинлигаза вовлечена в полиубиквитинирование так, что второй убиквитин присоединяется к первому, третий присоединяется ко второму и т.д. С помощью полиубиквитинирования белки метятся для разрушения с помощью протеасомы. Однако существуют некоторые явления убиквитинирования, которые ограничены моноубиквитинированием, при котором к молекуле субстрата убиквитинлигазой добавляется только один убиквитин. Моноубиквитинированные белки не являются целевыми для протеасомы для разрушения, но вместо этого их расположение в клетке или функция могут быть изменены, например, посредством связывания других белков, которые содержат домены, которые могут связывать убиквитин. Дополнительно усложняет задачу то, что Е3 может осуществлять целенаправленное воздействие на различные лизины на убиквитине с образованием цепей. Наиболее распространенный лизин представляет собой Lys48 в цепи убиквитина. Данный лизин используется для образования полиубиквитина, который распознается протеасомой.
[64] Термин «пациент» или «субъект» используется по всему настоящему описанию для описания животного, предпочтительно человека или домашнего животного, которым предоставляется лечение, в том числе профилактическое лечение, с помощью композиций в соответствии с настоящим изобретением. Для лечения тех инфекций, состояний или болезненных состояний, которые являются специфическими для конкретного животного, как, например, для пациента-человека, термин пациент относится к данному конкретному животному, в том числе домашнему животному, такому как собака или кошка, или сельскохозяйственному животному, такому как лошадь, корова, овца и т.д. В целом, в настоящем изобретении термин пациент относится к пациенту-человеку, если иное не указано или не подразумевается из контекста применения данного термина.
[65] Термин «эффективный» используется для описания количества соединения, композиции или компонента, которые при применении в контексте их предполагаемого применения оказывают предполагаемый результат. Термин «эффективный» включает все другие термины эффективного количества или эффективной концентрации, которые иным образом описаны или используются в настоящей заявке.
[66] Соединения и композиции
[67] В одном аспекте в описании представлены соединения, содержащие фрагмент, связывающий E3-убиквитинлигазу («ULM»), то есть фрагмент, связывающийся с IAP E3-убиквитинлигазного комплекса («ILM»), фрагмент, связывающийся с цереблоном E3-убиквитинлигазного комплекса («CLM»), фрагмент, связывающийся с белком Гиппеля-Линдау (VHL) E3-убиквитинлигазного комплекса (VLM), и/или фрагмент, связывающий E3-убиквитинлигазу, представляющую собой гомолог 2 double minute мыши (MDM2) (MLM). В иллюстративном варианте осуществления ULM связан с фрагментом, связывающим целевой белок (РТМ), с помощью химического линкера (L) в соответствии со структурой:
где L представляет собой связь или химическую линкерную группу, ULM представляет собой фрагмент, связывающий E3-убиквитинлигазу, и РТМ представляет собой фрагмент, связывающий целевой белок. Число и/или относительные положения фрагментов в соединениях, проиллюстрированных в данном документе, представлены только в качестве примера. Специалисту в данной области техники будет понятно, что соединения, описанные в данном документе, можно синтезировать с любым необходимым числом и/или относительным положением соответствующих функциональных фрагментов.
[68] Термины ULM, ILM, VLM, MLM и CLM применяют в их включительном смысле, если в контексте не указано иное. Например, термин ULM включает все ULM, в том числе таковые, которые связывают IAP (т.е. ILM), MDM2 (т.е. MLM), цереблон (т.е. CLM) и VHL (т.е. VLM). Кроме того, термин ILM включает все возможные фрагменты, связывающиеся с IAP E3-убиквитинлигазного комплекса, термин MLM включает все возможные фрагменты, связывающие E3-убиквитинлигазу MDM2, термин VLM включает все возможные фрагменты, связывающиеся с VHL, и термин CLM включает все фрагменты, связывающиеся с цереблоном.
[69] В другом аспекте настоящее изобретение предусматривает бифункциональные или мультифункциональные соединения (например, PROTAC), пригодные для регулирования активности белка посредством индуцирования разрушения целевого белка. В определенных вариантах осуществления соединение содержит ILM, или VLM, или CLM, или MLM, связанные, например связанные ковалентно, непосредственно или опосредованно, с фрагментом, который связывает целевой белок (т.е. фрагментом, нацеливающимся на белок, или «РТМ»). В определенных вариантах осуществления ILM/VLM/CLM/MLM и РТМ соединены или связаны с помощью химического линкера (L). ILM связывает IAP E3-убиквитинлигазного комплекса, VLM связывает VHL, CLM связывает цереблон E3-убиквитинлигазного комплекса, и MLM связывает E3-убиквитинлигазу MDM2, и РТМ распознает целевой белок, и при этом взаимодействие соответствующих фрагментов с их мишенями способствует разрушению целевого белка путем размещения целевого белка в непосредственной близости от белка убиквитинлигазного комплекса. Иллюстративное бифункциональное соединение может быть изображено как:
[70] В определенных вариантах осуществления бифункциональное соединение дополнительно содержит химический линкер («L»). Например, бифункциональное соединение может быть изображено как:
где РТМ представляет собой фрагмент, нацеливающийся на белок/полипептид, L представляет собой химический линкер, ILM представляет собой фрагмент, связывающийся с IAP E3-убиквитинлигазного комплекса, CLM представляет собой фрагмент, связывающийся с цереблоном E3-убиквитинлигазного комплекса, VLM представляет собой фрагмент, связывающийся с VHL, и MLM представляет собой фрагмент, связывающий E3-убиквитинлигазу MDM2.
[71] В определенных вариантах осуществления ULM (например, ILM, CLM, VLM или MLM) демонстрирует активность или связывается с E3-убиквитинлигазой (например, IAP E3-убиквитинлигазного комплекса, цереблоном E3-убиквитинлигазного комплекса, VHL или E3-убиквитинлигазой MDM2) с IC50, составляющей менее приблизительно 200 мкМ. IC50 можно определить в соответствии с любым способом, известным из уровня техники, например, с помощью анализа поляризации флуоресценции.
[72] В определенных дополнительных вариантах осуществления бифункциональные соединения, описанные в данном документе, демонстрируют активность с IC50, составляющей менее приблизительно 100, 50, 10, 1, 0,5, 0,1, 0,05, 0,01, 0,005, 0,001 мМ, или менее приблизительно 100, 50, 10, 1, 0,5, 0,1, 0,05, 0,01, 0,005, 0,001 мкМ, или менее приблизительно 100, 50, 10, 1, 0,5, 0,1, 0,05, 0,01, 0,005, 0,001 нМ, или менее приблизительно 100, 50, 10, 1, 0,5, 0,1, 0,05, 0,01, 0,005, 0,001 пМ.
[73] В определенных вариантах осуществления соединения, описанные в данном документе, содержат множество РТМ (нацеливающихся на одинаковые или различные белки-мишени), множество ULM, один или более ULM (т.е. фрагментов, которые специфически связываются с множеством/различными E3-убиквитинлигазами, например, VHL, IAP, цереблоном и/или MDM2) или их комбинацию. В любом из аспектов или вариантов осуществления, описанных в данном документе, РТМ и ULM (например, ILM, VLM, CLM и/или MLM) могут быть непосредственно связаны или связаны с помощью одного или более химических линкеров или их комбинации. В дополнительных вариантах осуществления если соединение содержит множество ULM, ULM могут относиться к одной и той же E3-убиквитинлигазе, или каждый соответствующий ULM может специфически связываться с отличной E3-убиквитинлигазой. В еще одних дополнительных вариантах осуществления, если соединение содержит множество РТМ, РТМ могут связываться с одним и тем же целевым белком или каждый соответствующий РТМ может специфически связываться с отличным целевым белком.
[74] В определенных вариантах осуществления, если соединение содержит множество ULM, ULM являются идентичными. В дополнительных вариантах осуществления в соединении, содержащем ряд ULM (например, ULM, ULM' и т.д.), по меньшей мере один РТМ непосредственно связан с ULM или связан с помощью химического линкера (L) или как одного, так и другого. В определенных дополнительных вариантах осуществления соединение, содержащее ряд ULM, дополнительно содержит множество РТМ. В еще одних дополнительных вариантах осуществления РТМ являются одинаковыми или необязательно различными. В еще одних дополнительных вариантах осуществления, если РТМ являются различными, соответствующие РТМ могут связывать один и тот же белок-мишень или специфически связываться с различными белками-мишенями.
[75] В определенных вариантах осуществления соединение может содержать ряд ULM и/или ряд ULM'. В дополнительных вариантах осуществления соединение, содержащее по меньшей мере два различных ULM, ряд ULM и/или ряд ULM', дополнительно содержит по меньшей мере один РТМ, непосредственно связанный с ULM или ULM' или связанный с помощью химического линкера или как одного, так и другого. В любом из вариантов осуществления, описанных в данном документе, соединение, содержащее по меньшей мере два различных ULM, может дополнительно содержать несколько РТМ. В еще одних дополнительных вариантах осуществления РТМ являются одинаковыми или необязательно различными. В еще одних дополнительных вариантах осуществления, если РТМ являются различными, соответствующие РТМ могут связывать один и тот же белок-мишень или специфически связываться с различными белками-мишенями. В еще одних дополнительных вариантах осуществления РТМ сам по себе представляет собой ULM (или ULM'), такой как ILM, VLM, CLM, MLM, ILM', VLM', CLM' и/или MLM'.
[76] В дополнительных вариантах осуществления в описании представлены соединения, описанные в данном документе, в том числе их энантиомеры, диастереомеры, сольваты и полиморфы, в том числе их фармацевтически приемлемые солевые формы, например, солевые формы присоединения кислоты и основания.
[77] В одном аспекте настоящее изобретение предусматривает соединение формулы (I) или (II),
 где
где
каждый XPTM независимо представляет собой СН, N;
ULM представляет собой ULM, представляющий собой ILM, или VLM, или CLM, или MLM;
L представляет собой связь или линкерный фрагмент, связывающий тетрагидронафталиновый или тетрагидроизохинолиновый фрагмент и по меньшей мере одно из VLM, CLM, ILM, VLM или их комбинацию;
каждый RPTM1 независимо представляет собой ОН, галоген, алкокси (например, метокси или этокси), O(CO)RPTM, при этом замещение может предусматривать моно-, ди- или тризамещение, и RPTM представляет собой алкильную или циклоалкильную группу с 1-6 атомами углерода или арильные группы;
каждый RPTM2 независимо представляет собой Н, галоген, CN, CF3, линейный или разветвленный алкил, алкокси (например, метокси или этокси), при этом замещение может предусматривать моно- или дизамещение;
каждый RPTM3 независимо представляет собой Н, галоген, при этом замещение может предусматривать моно- или дизамещение; и
RPTM4 представляет собой Н, алкил, метил, этил.
[78] Целевой белок (например, эстрогеновый рецептор) включает олигопептиды и полипептидные последовательности достаточной длины для того, чтобы они могли связываться с группой РТМ в соответствии с настоящим изобретением. Группы РТМ в соответствии с настоящим изобретением включают, например, любой фрагмент, который специфически связывается с эстрогеновым рецептором (связывается с целевым белком). В композициях, описанных ниже, проиллюстрированы некоторые из представителей низкомолекулярных фрагментов, связывающих целевой белок. Такие низкомолекулярные фрагменты, связывающие целевой белок, также включают фармацевтически приемлемые соли, энантиомеры, сольваты и полиморфы таких композиций, а также другие малые молекулы, которые могут нацеливаться на белок, представляющий интерес. Такие связывающие фрагменты соединены с фрагментом, связывающим убиквитинлигазу, предпочтительно с помощью линкера с целью размещения целевого белка (с которым связан фрагмент, нацеливающийся на белок) в непосредственной близости от убиквитинлигазы для убиквитинирования и разрушения.
[79] Настоящее изобретение может применяться для лечения ряда болезненных состояний и/или состояний, в том числе любого болезненного состояния и/или состояния, при котором нарушена регуляция белков, и при котором пациент получит пользу от разрушения и/или ингибирования белков.
[80] В дополнительном аспекте в описании представлены терапевтические композиции, содержащие эффективное количество соединения, описанного в данном документе, или его солевой формы и фармацевтически приемлемый носитель, добавку или вспомогательное вещество и необязательно дополнительное биологически активное средство. Терапевтические композиции модулируют разрушение и/или ингибирование белка у пациента или субъекта, например, у животного, такого как человека, и могут применяться для лечения или облегчения болезненных состояний или состояний, модулирование которых обеспечивается посредством разрушения/ингибирования белка. В определенных вариантах осуществления терапевтические композиции, описанные в данном документе, можно применять для обеспечения разрушения белков, представляющих интерес, для лечения или облегчения заболевания, например рака. В определенных дополнительных вариантах осуществления заболевание представляет собой по меньшей мере одно из рака молочной железы, рака матки, рака яичников, рака предстательной железы, рака эндометрия, эндометриоза или их комбинации.
[81] В альтернативных аспектах настоящее изобретение относится к способу лечения болезненного состояния или облегчения симптомов заболевания или состояния у субъекта, нуждающегося в этом, путем разрушения белка или полипептида, за счет которых модулируется болезненное состояние или состояние, включающему введение указанному пациенту или субъекту эффективного количества, например терапевтически эффективного количества, по меньшей мере одного соединения, описанного в данном документе выше, необязательно в комбинации с фармацевтически приемлемым носителем, добавкой или вспомогательным веществом и необязательно дополнительным биологически активным средством, при этом композиция является эффективной в лечении или облегчении заболевания или нарушения или их симптома у субъекта. Способ в соответствии с настоящим изобретением можно применять для лечения большого количества болезненных состояний или состояний, в том числе рака и/или эндометриоза, посредством введения эффективных количеств по меньшей мере одного соединения, описанного в данном документе. Болезненное состояние или состояние может представлять собой заболевание, вызванное микробным организмом или другим экзогенным организмом, таким как вирус, бактерия, гриб, простейшие или другой микроорганизм, или может представлять собой болезненное состояние, которое вызвано сверхэкспрессией белка, что приводит к болезненному состоянию и/или состоянию.
[82] В другом аспекте в описании предусмотрены способы идентификации эффектов разрушения белков, представляющих интерес, в биологической системе с применением соединений в соответствии с настоящим изобретением.
[83] Термин «целевой белок» используется в данном документе для описания белка или полипептида, которые представляют собой мишень для связывания с соединением в соответствии с настоящим изобретением и разрушения посредством убиквитинлигазы. Такие низкомолекулярные фрагменты, связывающие целевой белок, также включают фармацевтически приемлемые соли, энантиомеры, сольваты и полиморфы таких композиций, а также другие малые молекулы, которые могут нацеливаться на белок, представляющий интерес, такой как эстрогеновый рецептор. Данные связывающие фрагменты соединены с по меньшей мере одной группой ULM (например, VLM и/или CLM) с помощью по меньшей мере одной линкерной группы L.
[84] Термин «фрагмент, нацеливающийся на белок» или РТМ используется для описания малой молекулы, которая связывается с целевым белком или другим белком или полипептидом, представляющим интерес, и обеспечивает размещение/присутствие данного белка или полипептида в непосредственной близости от убиквитинлигазы таким образом, что может происходить разрушение белка или полипептида посредством убиквитинлигазы. Неограничивающие примеры низкомолекулярных фрагментов, связывающих целевой белок, включают селективные модуляторы эстрогенового рецептора, среди многочисленных других. В композициях, описанных ниже, проиллюстрированы некоторые из представителей низкомолекулярных целевых белков.
[85] В соединениях и композициях, описанных в данном документе, проиллюстрированы некоторые представители данных типов низкомолекулярных фрагментов, связывающих целевой белок. Такие низкомолекулярные фрагменты, связывающие целевой белок, также включают фармацевтически приемлемые соли, энантиомеры, сольваты и полиморфы таких композиций, а также другие малые молекулы, которые могут нацеливаться на белок, представляющий интерес. Источники, цитируемые в данном документе ниже, включены в данный документ посредством ссылки во всей своей полноте.
[86] Иллюстративные ILM
[87] Тетрапептидные фрагменты AVPI
[88] В любом из соединений, описанных в данном документе, ILM может содержать тетрапептидный фрагмент аланин-валин-пролин-изолейцин (AVPI) или его неприродный миметик. В определенных вариантах осуществления ILM выбран из группы, состоящей из химических структур, представленных с помощью формул (I), (II), (III), (IV) и (V),

где
R1 для формул (I), (II), (III), (IV) и (V) выбран из Н или алкила;
R2 для формул (I), (II), (III), (IV) и (V) выбран из Н или алкила;
R3 для формул (I), (II), (III), (IV) и (V) выбран из Н, алкила, циклоалкила и гетероциклоалкила;
R5 и R6 для формул (I), (II), (III), (IV) и (V) независимо выбраны из Н, алкила, циклоалкила, гетероциклоалкила, или более предпочтительно R5 и R6, взятые вместе для формул (I), (II), (III), (IV) и (V), образуют пирролидиновое или пиперидиновое кольцо, дополнительно необязательно конденсированное с 1-2 циклоалкильными, гетероциклоалкильными, арильными или гетероарильными кольцами, каждое из которых затем может быть дополнительно конденсировано с другим циклоалкильным, гетероциклоалкильным, арильным или гетероарильным кольцом;
R3 и R5 для формул (I), (II), (III), (IV) и (V), взятые вместе могут образовывать 5-8-членное кольцо, дополнительно необязательно конденсированное с 1-2 циклоалкильными, гетероциклоалкильными, арильными или гетероарильными кольцами;
R7 для формул (I), (II), (III), (IV) и (V) выбран из циклоалкила, циклоалкилалкила, гетероциклоалкила, гетероциклоалкилалкила, арила, арилалкила, гетероарила или гетероарилалкила, каждый из которых дополнительно необязательно замещен 1-3 заместителями, выбранными из галогена, алкила, галогеналкила, гидроксила, алкокси, циано, (гетеро)циклоалкила или (гетеро)арила, или R7 представляет собой -C(O)NH-R4; и
R4 выбран из алкила, циклоалкила, гетероциклоалкила, циклоалкилалкила, гетероциклоалкилалкила, арила, арилалкила, гетероарила, гетероарилалкила, дополнительно необязательно замещенных 1-3 заместителями, описанными выше.
[89] Как показано выше, Р1, Р2, Р3 и Р4 в формуле (II) соответствуют А, V, Р и I соответственно тетрапептидного фрагмента AVPI или его неприродного миметика. Аналогично каждая из формул (I) и (III) - (V) содержит части, соответствующие А, V, Р и I тетрапептидного фрагмента AVPI или его неприродного миметика.
[90] В любом из соединений, описанных в данном документе, ILM может характеризоваться структурой формулы (VI), которая представляет собой производное антагонистов IAP, описанное в публ. WO №2008/014236, или соответствующим ей неприродным миметиком,

где
R1 в формуле (VI) независимо выбран из Н, C1-C4-алкила, C1-C4-алкенила, C1-C4-алкинила или C3-C10-циклоалкила, которые являются незамещенными или замещенными;
R2 в формуле (VI) независимо выбран из Н, C1-C4-алкила, C1-C4-алкенила, C1-C4-алкинила или C3-C10-циклоалкила, которые являются незамещенными или замещенными;
R3 в формуле (VI) независимо выбран из Н, -CF3, -С2Н5, C1-C4-алкила, C1-C4-алкенила, C1-C4-алкинила, -CH2-Z, или любые R2 и R3 вместе образуют гетероциклическое кольцо;
каждый Z в формуле (VI) независимо выбран из Н, -ОН, F, Cl, -СН3, -CF3, -CH2Cl, -CH2F или -CH2OH;
R4 в формуле (VI) независимо выбран из C1-C16-алкила с прямой или разветвленной цепью, C1-C16-алкенила, C1-C16-алкинила, C3-C10-циклоалкила, -(СН2)0-6-Z1, -(СН2)0-6-арила и -(CH2)0-6-het, где алкил, циклоалкил и фенил являются незамещенными или замещенными;
R5 в формуле (VI) независимо выбран из Н, C1-10-алкила, арила, фенила, С3-7-циклоалкила, -(СН2)1-6-С3-7-циклоалкила, -C1-10-алкиларила, -(СН2)0-6-С3-7-циклоалкила-(СН2)0-6-фенила, -(СН2)0-4-СН[(СН2)1-4-фенил]2, инданила, -C(O)-C1-10-алкила, -С(O)-(СН2)1-6-С3-7-циклоалкила, -С(O)-(СН2)0-6-фенила, -(СН2)0-6-С(O)-фенила, -(CH2)0-6-het, -C(O)-(CH2)1-6-het, или R5 выбран из остатка аминокислоты, при этом алкильные, циклоалкильные, фенильные и арильные заместители являются незамещенными или замещенными;
Z1 в формуле (VI) независимо выбран из -N(R10)-C(O)-C1-10-алкила, -N(R10)-С(O)-(СН2)0-6-С3-7-циклоалкила, -N(R10)-С(O)-(СН2)0-6-фенила, -N(R10)-C(O)(CH2)1-6-het, -C(O)-N(R11)(R12), -С(O)-O-С1-10-алкила, -С(O)-O-(СН2)1-6-С3-7-циклоалкила, -С(O)-O-(СН2)0-6-фенила, -C(O)-O-(CH2)1-6-het, -O-С(O)-С1-10-алкила, -O-С(O)-(СН2)1-6-С3-7-циклоалкила, -O-С(O)-(СН2)0-6-фенила, -O-C(O)-(CH2)1-6-het, где алкил, циклоалкил и фенил являются незамещенными или замещенными;
het в формуле (VI) независимо выбран из 5-7-членного гетероциклического кольца, содержащего от 1 до 4 гетероатомов, выбранных из N, О и S, или 8-12-членной конденсированной кольцевой системы, содержащей по меньшей мере одно 5-7-членное гетероциклическое кольцо, содержащее 1, 2 или 3 гетероатома, выбранные из N, О и S, при этом гетероциклическое кольцо или конденсированная кольцевая система являются незамещенными или замещенными по атому углерода или азота;
R10 в формуле (VI) выбран из Н, -СН3, -CF3, -CH2OH или -CH2Cl;
R11 и R12 в формуле (VI) независимо выбраны из Н, C1-4-алкила, С3-7-циклоалкила, -(СН2)1-6-С3-7-циклоалкила, (СН2)0-6-фенила, где алкил, циклоалкил и фенил являются незамещенными или замещенными; или R11 и R12 вместе с атомом азота образуют het, и
U в формуле (VI) независимо является таким, как показано на формуле (VII),
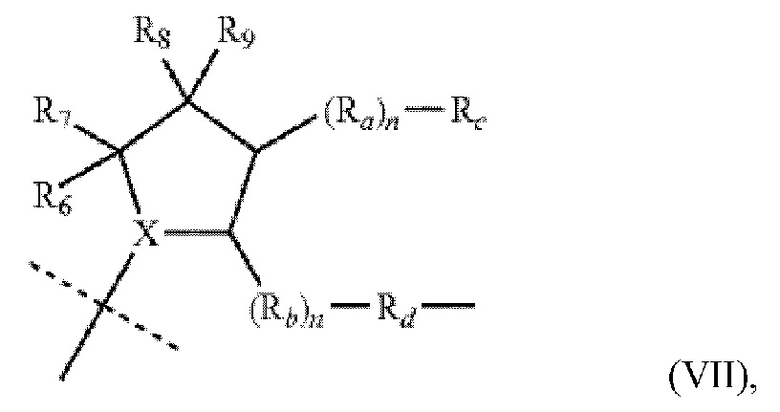
где
каждый n в формуле (VII) независимо выбран из 0-5;
Х в формуле (VII) выбран из группы, состоящей из -СН и N;
Ra и Rb в формуле (VII) независимо выбраны из группы, состоящей из атомов O, S или N или С0-8-алкила, где один или более атомов углерода в алкильной цепи необязательно заменены гетероатомом, выбранным из O, S или N, и при этом каждый алкил независимо является либо незамещенным, либо замещенным;
Rd в формуле (VII) выбран из группы, состоящей из Re-Q-(Rf)p(Rg)q и Ar1-D-Ar2;
Rc в формуле (VII) выбран из группы, состоящей из Н, или любые Rc и Rd вместе образуют циклоалкил или het; при этом если Rc и Rd образуют циклоалкил или het, R5 присоединен к образованному кольцу при атоме С или N;
р и q в формуле (VII) независимо выбраны из 0 или 1;
Re в формуле (VII) выбран из группы, состоящей из C1-8-алкила и алкилидена, и при этом каждый Re является либо незамещенным, либо замещенным;
Q выбран из группы, состоящей из N, О, S, S(O) и S(O)2;
Ar1 и Ar2 в формуле (VII) независимо выбраны из группы, состоящей из замещенного или незамещенного арила и het;
Rf и Rg в формуле (VII) независимо выбраны из Н, -C1-10-алкила, C1-10-алкиларила, -ОН, -О-С1-10-алкила, -(СН2)0-6-С3-7-циклоалкила, -O-(СН2)0-6-арила, фенила, арила, фенил-фенила, -(CH2)1-6-het, -O-(CH2)1-6-het, -OR13, -C(O)-R13, -C(O)-N(R13)(R14), -N(R13)(R14), -S-R13, -S(O)-R13, -S(O)2-R13, -S(O)2-NR13R14, -NR13-S(O)2-R14, -S-Ct-10-алкила, арил-С1-4-алкила или het-C1-4-алкила, где алкил, циклоалкил, het и арил являются незамещенными или замещенными, -SO2-C1-2-алкила, -SO2-C1-2-алкилфенила, -O-C1-4-алкила, или любые Rg и Rf вместе образуют кольцо, выбранное из het или арила;
D в формуле (VII) выбран из группы, состоящей из -СО-, -С(O)-С1-7-алкилена или арилена, -CF2-, -O-, -S(O)r, где r составляет 0-2, 1,3-диоксалана или C1-7-алкил-ОН; где алкил, алкилен или арилилен являются незамещенными или замещенными одним или более атомами галогена, ОН, -O-C1-6-алкилом, -S-C1-6-алкилом или -CF3; или каждый D независимо выбран из N(Rh);
Rh выбран из группы, состоящей из Н, незамещенного или замещенного C1-7-алкила, арила, незамещенного или замещенного -O-(С1-7-циклоалкил), -C(O)-C1-10-алкила, -С(O)-С0-10-алкиларила, -С-О-С01-10-алкила, -С-O-С0-10-алкиларила, -SO2-C1-10-алкила или -SO2-(С0-10-алкиларил);
R6, R7, R8 и R9 в формуле (VII) независимо выбраны из группы, состоящей из Н, -C1-10-алкила, -C1-10-алкокси, арил-C1-10-алкокси, -ОН, -О-C1-10-алкила, -(СН2)0-6-C3-7-циклоалкила, -O-(СН2)0-6-арила, фенила, -(CH2)1-6-het, -O-(CH2)1-6-het, -OR13, -C(O)-R13, -C(O)-N(R13)(R14), -N(R13)(R14), -S-R13, -S(O)-R13, -S(O)2-R13, -S(O)2-NR13R14 или -NR13-S(O)2-R14; где каждый алкил, циклоалкил и арил является незамещенным или замещенным; и любые R6, R7, R8 и R9 вместе необязательно образуют кольцевую систему;
R13 и R14 в формуле (VII) независимо выбраны из группы, состоящей из Н, C1-10-алкила, -(СН2)0-6-С3-7-циклоалкила, -(СН2)0-6-(СН)0-1-(арил)1-2, -С(O)-С1-10-алкила, -С(O)-(СН2)1-6-С3-7-циклоалкила, -С(O)-O-(СН2)0-6-арила, -С(O)-(СН2)0-6-O-флуоренила, -C(O)-NH-(CH2)0-6-арила, -С(O)-(СН2)0-6-арила, -C(O)-(CH2)0-6-het, -C(S)-C1-10-алкила, -С(S)-(СН2)1-6-С3-7-циклоалкила, -С(S)-O-(СН2)0-6-арила, -С(S)-(СН2)0-6-O-флуоренила, -C(S)-NH-(CH2)0-6-арила, -С(S)-(СН2)0-6-арила или -C(S)-(CH2)1-6-het, где каждый алкил, циклоалкил и арил является незамещенным или замещенным, или любые R13 и R14 вместе с атомом азота образуют het;
при этом алкильные заместители в R13 и R14 в формуле (VII) являются незамещенными или замещенными, и если они замещены, то они замещены одним или более заместителями, выбранными из C1-10-алкила, галогена, ОН, -O-C1-6-алкила, -S-C1-6-алкила и -CF3; и замещенный фенил или арил в R13 и R14 замещены одним или более заместителями, выбранными из галогена, гидроксила, C1-4-алкила, C1-4-алкокси, нитро, -CN, -O-С(O)-С1-4-алкила и -С(O)-O-С1-4-арила; или его фармацевтически приемлемая соль или гидрат.
[91] В определенных вариантах осуществления соединение дополнительно содержит независимо выбранный второй ILM, присоединенный к ILM формулы (VI) или его неприродному миметику с помощью по меньшей мере одной дополнительной независимо выбранной линкерной группы. В одном варианте осуществления второй ILM представляет собой производное формулы (VI) или его неприродный миметик. В определенном варианте осуществления по меньшей мере одна дополнительная независимо выбранная линкерная группа предусматривает две дополнительные независимо выбранные линкерные группы, химически соединяющие ILM и второй ILM. В одном варианте осуществления по меньшей мере одна дополнительная линкерная группа для ILM формулы (VI) или его неприродного миметика химически соединяет группы, выбранные из R4 и R5. Например, ILM формулы (VI) и второй ILM формулы (VI) или их неприродный миметик могут быть соединены, как показано ниже.

[92] В определенных вариантах осуществления ILM, по меньшей мере одна дополнительная независимо выбранная линкерная группа L и второй ILM характеризуются структурой, выбранной из группы, состоящей из:

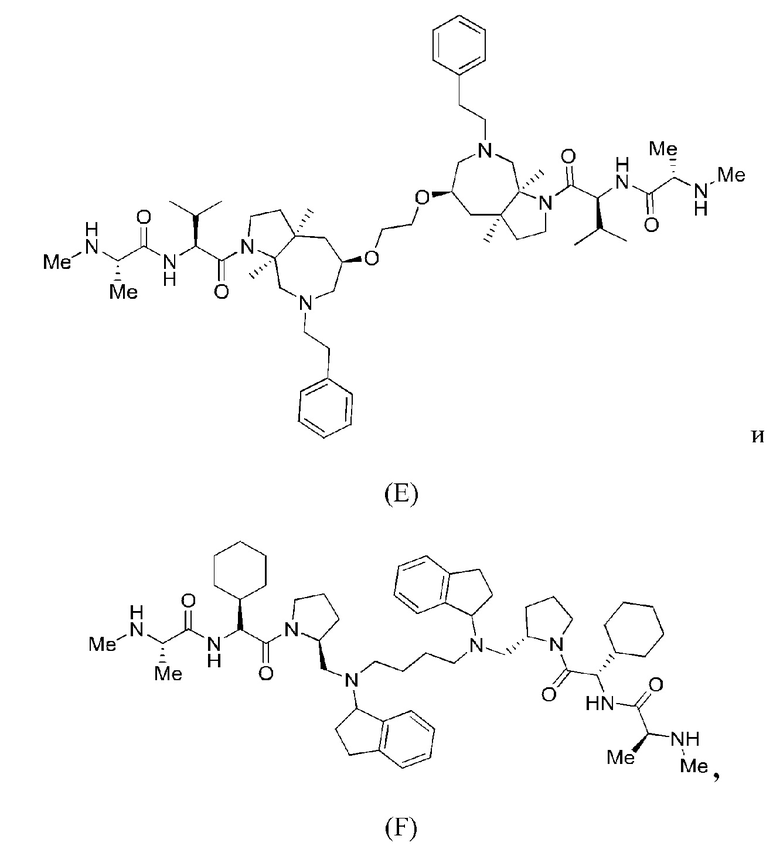
которые являются производными антагонистов IAP, описанных в публ. WO №2008/014236.
[93] В любом из соединений, описанных в данном документе, ILM может характеризоваться структурой формулы (VIII), которая основана на структуре лигандов IAP, описанных в Ndubaku, С., et al. Antagonism of c-IAP and XIAP proteins is required for efficient induction of cell death by small-molecule IAP antagonists, ACS Chem. Biol., 557-566, 4 (7) (2009), или соответствующим ей неприродным миметиком,

где каждый из А1 и А2 в формуле (VIII) независимо выбран из необязательно замещенных моноциклических конденсированных колец, арилов и гетероарилов; и
R в формуле (VIII) выбран из Н или Me.
[94] В конкретном варианте осуществления линкерная группа L присоединена к А1 в формуле (VIII). В другом варианте осуществления линкерная группа L присоединена к А2 в формуле (VIII).
[95] В конкретном варианте осуществления ILM выбран из группы, состоящей из

[96] В любом из соединений, описанных в данном документе, ILM может характеризоваться структурой формулы (IX), которая получена из хемотипов, на которые сделана перекрестная ссылка в Mannhold, R., et al. IAP antagonists: promising candidates for cancer therapy. Drug Discov. Today, 15 (5-6), 210-9 (2010), или соответствующим ей неприродным миметиком,

где R1 выбран из алкила, циклоалкила и гетероциклоалкила и наиболее предпочтительно из изопропила, трет-бутила, циклогексила и тетрагидропиранила, и R2 в формуле (IX) выбран из -OPh или Н.
[97] В любом из соединений, описанных в данном документе, ILM может характеризоваться структурой формулы (X), которая получена из хемотипов, на которые сделана перекрестная ссылка в Mannhold, R., et al. IAP antagonists: promising candidates for cancer therapy. Drug Discov. Today, 15 (5-6), 210-9 (2010), или соответствующим ей неприродным миметиком,

где
R1 в формуле (X) выбран из Н, -CH2OH, --CH2CH2OH, --CH2NH2, -CH2CH2NH2;
Х в формуле (X) выбран из S или СН2;
R2 в формуле (X) выбран из

R3 и R4 в формуле (X) независимо выбраны из Н или Me.
[98] В любом из соединений, описанных в данном документе, ILM может характеризоваться структурой формулы (XI), которая получена из хемотипов, на которые сделана перекрестная ссылка в Mannhold, R., et al. IAP antagonists: promising candidates for cancer therapy. Drug Discov. Today, 15 (5-6), 210-9 (2010), или соответствующим ей неприродным миметиком,

где R1 в формуле (XI) выбран из Н или Me, и R2 в формуле (XI) выбран из Н или
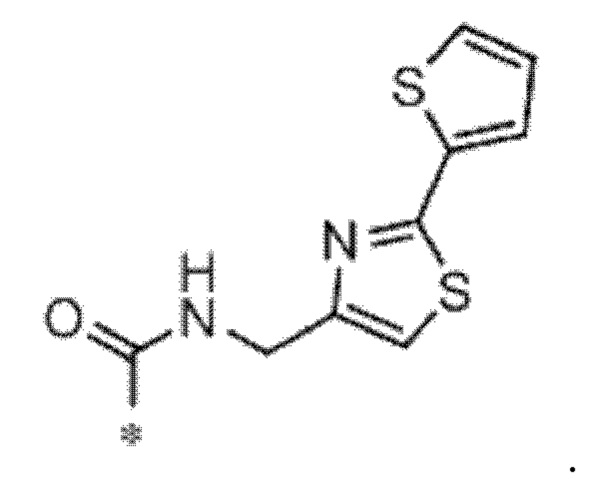
[99] В любом из соединений, описанных в данном документе, ILM может характеризоваться структурой формулы (XII), которая получена из хемотипов, на которые сделана перекрестная ссылка в Mannhold, R., et al. IAP antagonists: promising candidates for cancer therapy. Drug Discov. Today, 15 (5-6), 210-9 (2010), или соответствующим ей неприродным миметиком,

где
R1 в формуле (XII) выбран из

R2 в формуле (XII) выбран из

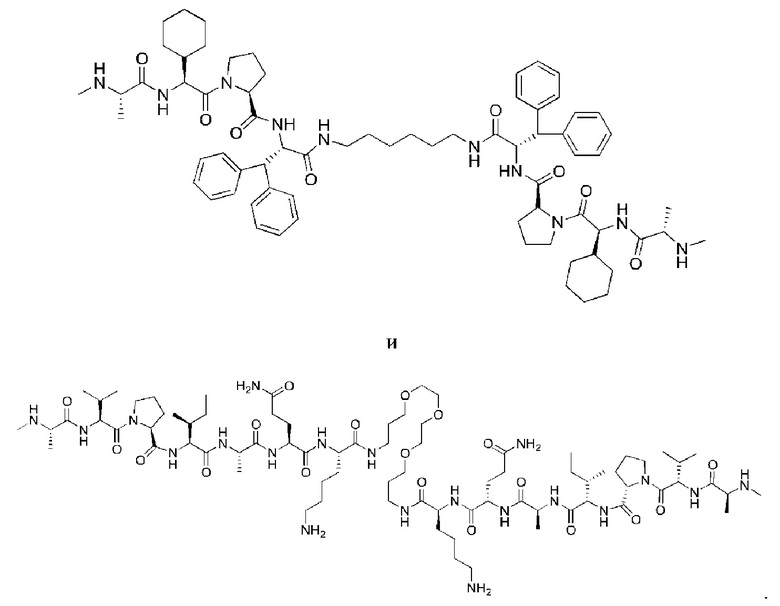
[100] В любом из соединений, описанных в данном документе, фрагмент, связывающийся с IAP E3-убиквитинлигазного комплекса, выбран из группы, состоящей из:


[101] В любом из соединений, описанных в данном документе, ILM может характеризоваться структурой формулы (XIII), которая основана на структуре лигандов IAP, кратко представленных в Flygare, J.A., et al. Small-molecule pan-IAP antagonists: a patent review, Expert Opin. Ther. Pat., 20 (2), 251-67 (2010), или соответствующим ей неприродным миметиком,
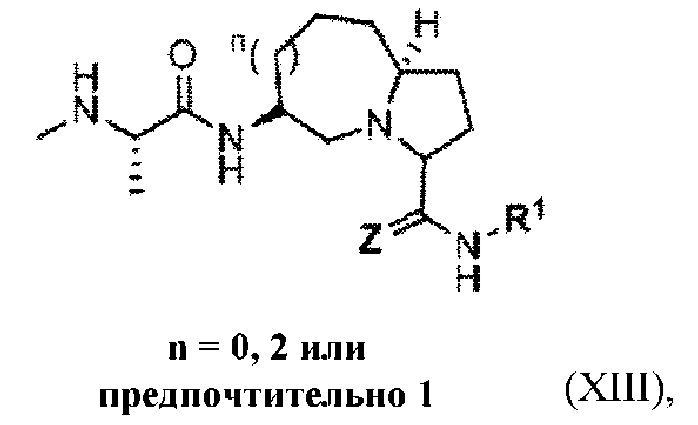
где
Z в формуле (XIII) отсутствует или представляет собой О;
R1 в формуле (XIII) выбран из
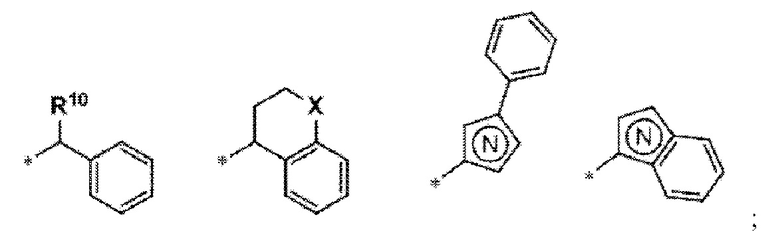
R10 в  выбран из Н, алкила или арила;
выбран из Н, алкила или арила;
X выбран из СН2 и О; и
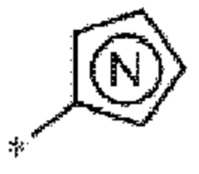 представляет собой содержащий азот гетероарил.
представляет собой содержащий азот гетероарил.
[102] В любом из соединений, описанных в данном документе, ILM может характеризоваться структурой формулы (XIV), которая основана на структуре лигандов IAP, кратко представленных в Flygare, J.A., et al. Small-molecule pan-IAP antagonists: a patent review, Expert Opin. Ther. Pat., 20 (2), 251-67 (2010), или соответствующим ей неприродным миметиком,

где
Z в формуле (XIV) отсутствует или представляет собой О;
R3 и R4 в формуле (XIV) независимо выбраны из Н или Me;
R1 в формуле (XIV) выбран из

R10 в  выбран из Н, алкила или арила;
выбран из Н, алкила или арила;
X в  выбран из СН2 и О; и
выбран из СН2 и О; и
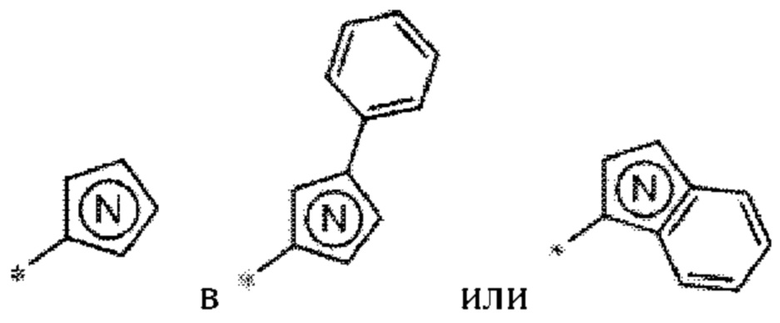 представляет собой содержащий азот гетероарил.
представляет собой содержащий азот гетероарил.
[103] В любом из соединений, описанных в данном документе, ILM выбран из группы, состоящей из

которые представляют собой производные лигандов, раскрытых в публ. патента США №2008/0269140 и в патенте США №7244851.
[104] В любом из соединений, описанных в данном документе, ILM может характеризоваться структурой формулы (XV), которая представляет собой производное лиганда IAP, описанное в публ. WO №2008/128171, или соответствующим ей неприродным миметиком,
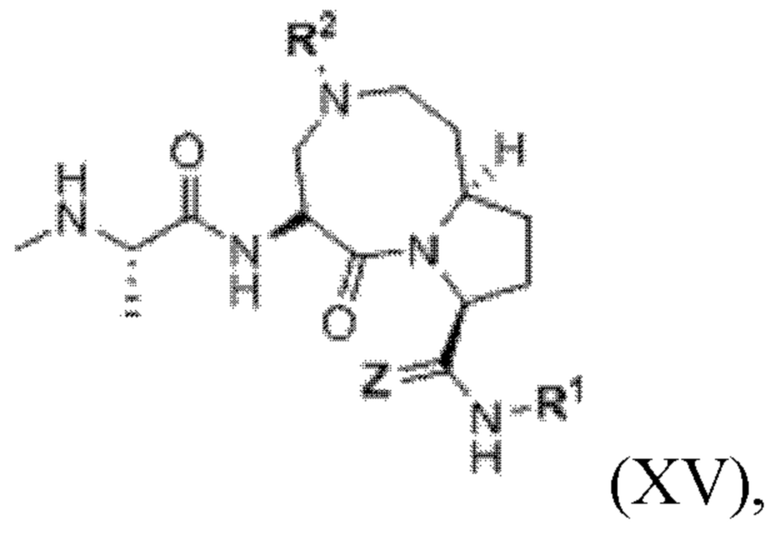
где
Z в формуле (XV) отсутствует или представляет собой О;
R1 в формуле (XV) выбран из

R10 в  выбран из Н, алкила или арила;
выбран из Н, алкила или арила;
X в  выбран из СН2 и О; и
выбран из СН2 и О; и
 представляет собой содержащий азот гетероарил; и
представляет собой содержащий азот гетероарил; и
R2 в формуле (XV) выбран из Н, алкила или ацила.
[105] В конкретном варианте осуществления ILM характеризуется следующей структурой:
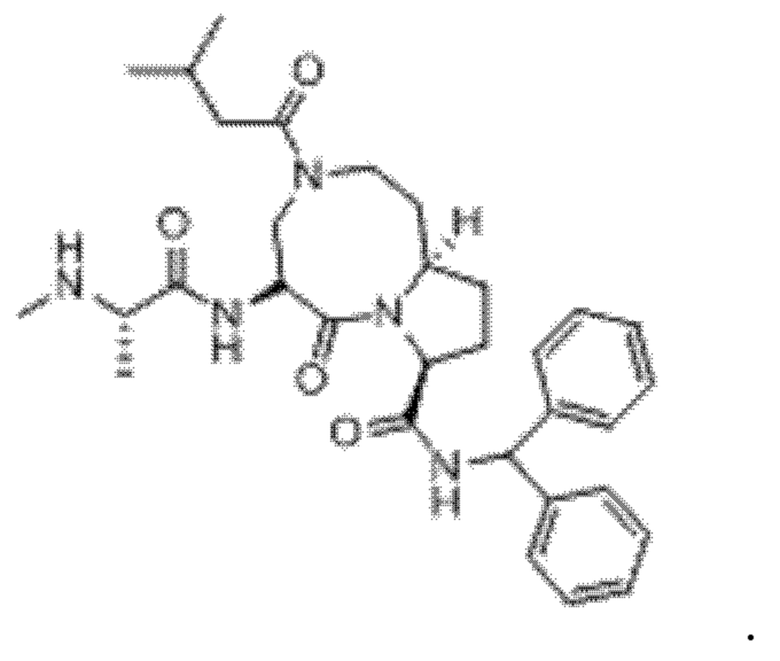
[106] В любом из соединений, описанных в данном документе, ILM может характеризоваться структурой формулы (XVI), которая основана на структуре лиганда IAP, описанного в публ. WO №2006/069063, или соответствующим ей неприродным миметиком,

где
R2 в формуле (XVI) выбран из алкила, циклоалкила и гетероциклоалкила; более предпочтительно из изопропила, трет-бутила, циклогексила и тетрагидропиранила, наиболее предпочтительно из циклогексила;
 в формуле (XVI) представляет собой 5- или 6-членный содержащий азот гетероарил; более предпочтительно, 5-членный содержащий азот гетероарил и наиболее предпочтительно тиазол; и
в формуле (XVI) представляет собой 5- или 6-членный содержащий азот гетероарил; более предпочтительно, 5-членный содержащий азот гетероарил и наиболее предпочтительно тиазол; и
Ar в формуле (XVI) представляет собой арил или гетероарил.
[107] В любом из соединений, описанных в данном документе, ILM может характеризоваться структурой формулы (XVII), которая основана на структуре лигандов IAP, описанных в Cohen, F. et al., Antogonists of inhibitors of apoptosis proteins based on thiazole amide isosteres, Bioorg. Med. Chem. Lett., 20(7), 2229-33 (2010), или соответствующим ей неприродным миметиком,

где
R1 в формуле (XVII) выбран из группы, состоящей из галогена (например, фтора), циано, 
X в формуле (XVII) выбран из группы, состоящей из О или СН2.
[108] В любом из соединений, описанных в данном документе, ILM может характеризоваться структурой формулы (XVIII), которая основана на структуре лигандов IAP, описанных в Cohen, F. et al., Antogonists of inhibitors of apoptosis proteins based on thiazole amide isosteres, Bioorg. Med. Chem. Lett., 20(7), 2229-33 (2010), или соответствующим ей неприродным миметиком,

где R в формуле (XVIII) выбран из алкила, арила, гетероарила, арилалкила, гетероарилалкила или галогена (в различных положениях замещения).
[109] В любом из соединений, описанных в данном документе, ILM может характеризоваться структурой формулы (XIX), которая основана на структуре лигандов IAP, описанных в Cohen, F. et al., Antogonists of inhibitors of apoptosis proteins based on thiazole amide isosteres, Bioorg. Med. Chem. Lett., 20(7), 2229-33 (2010), или соответствующим ей неприродным миметиком,

где  представляет собой 6-членный содержащий азот гетероарил.
представляет собой 6-членный содержащий азот гетероарил.
[110] В определенном варианте осуществления ILM согласно композиции выбран из группы, состоящей из

[111] В определенных вариантах осуществления ILM согласно композиции выбран из группы, состоящей из:
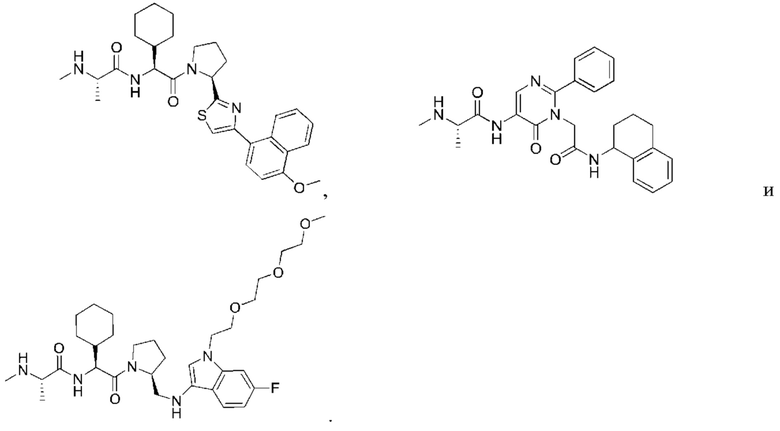
[112] В любом из соединений, описанных в данном документе, ILM может характеризоваться структурой формулы (XX), которая основана на структуре лигандов IAP, описанных в публ. WO №2007/101347, или соответствующим ей неприродным миметиком,

где X в формуле (XX) выбран из CH2, О, NH или S.
[113] В любом из соединений, описанных в данном документе, ILM может характеризоваться структурой формулы (XXI), которая основана на структуре лигандов IAP, описанных в патенте США №7345081 и патенте США №7419975, или соответствующим ей неприродным миметиком,

где
R2 в формуле (XXI) выбран из 
R5 в формуле (XXI) выбран из 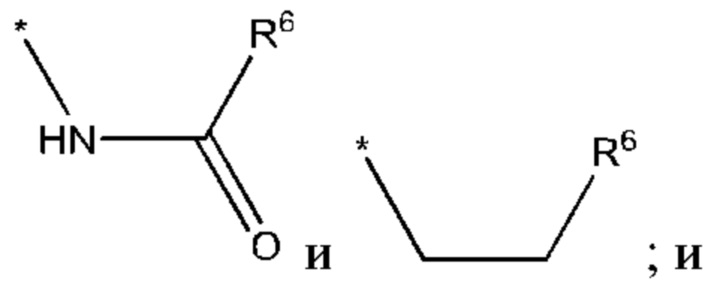
W в формуле (XXI) выбран из СН или N; и
R6 в  независимо представляет собой моно- или бициклический конденсированный арил или гетероарил.
независимо представляет собой моно- или бициклический конденсированный арил или гетероарил.
[114] В определенных вариантах осуществления ILM в соединении выбран из группы, состоящей из

[115] В определенных вариантах осуществления ILM в соединении выбран из группы, состоящей из


которые описаны в публ. WO №2009/060292, патенте США №7517906, публ. WO №2008/134679, публ. WO №2007/130626 и публ. WO №2008/128121.
[116] В любом из соединений, описанных в данном документе, ILM может характеризоваться структурой формулы (XXII) или (XXIII), которая получена из структуры лигандов IAP, описанных в публ. WO №2015/006524 и Perez HL, Discovery of potent heterodimeric antagonists of inhibitor of apoptosis proteins (IAPs) with sustained antitumor activity. J. Med. Chem. 58(3), 1556-62 (2015), или соответствующим ей неприродным миметиком,

где
R1 в формуле (XXII) или (XXIII) представляет собой необязательно замещенный алкил, необязательно замещенный циклоалкил, необязательно замещенный циклоалкилалкил, необязательно замещенный гетероциклил, необязательно замещенный арилалкил или необязательно замещенный арил;
R2 в формуле (XXII) или (XXIII) представляет собой необязательно замещенный алкил, необязательно замещенный циклоалкил, необязательно замещенный циклоалкилалкил, необязательно замещенный гетероциклил, необязательно замещенный арилалкил или необязательно замещенный арил;
или альтернативно R1 и R2 в формуле (XXII) или (XXIII) независимо представляют собой необязательно замещенный тиоалкил, где заместители, присоединенные к атому S тиоалкила, представляют собой необязательно замещенный алкил, необязательно замещенный разветвленный алкил, необязательно замещенный гетероциклил, -(CH2)vCOR20, -CH2CHR21COR22 или -CH2R23;
где
v представляет собой целое число 1-3;
R20 и R22 в -(CH2)vCOR20 и -CH2R23 независимо выбраны из ОН, NR24R25 или OR26;
R21 в -CH2CHR21COR2 выбран из группы, состоящей из NR24R25;
R23 в -CH2R23 выбран из необязательно замещенного арила или необязательно замещенного гетероциклила, где необязательные заместители включают алкил и галоген;
R24 в NR24R25 выбран из водорода или необязательно замещенного алкила;
R25 в NR24R25 выбран из водорода, необязательно замещенного алкила, необязательно замещенного разветвленного алкила, необязательно замещенного арилалкила, необязательно замещенного гетероциклила, -СН2(OCH2CH2O)mCH3 или полиаминной цепи, такой как спермин или спермидин;
R26 в OR26 выбран из необязательно замещенного алкила, где необязательные заместители представляют собой ОН, галоген или NH2; и
m представляет собой целое число 1-8;
R3 и R4 в формуле (XXII) или (XXIII) независимо выбраны из необязательно замещенного алкила, необязательно замещенного циклоалкила, необязательно замещенного арила, необязательно замещенного арилалкила, необязательно замещенного арилалкокси, необязательно замещенного гетероарила, необязательно замещенного гетероциклила, необязательно замещенного гетероарилалкила или необязательно замещенного гетероциклоалкила, где заместители представляют собой алкил, галоген или ОН;
R5, R6, R7 и R8 в формуле (XXII) или (XXIII) независимо выбраны из водорода, необязательно замещенного алкила или необязательно замещенного циклоалкила; и
X выбран из связи или химической линкерной группы, и/или его фармацевтически приемлемая соль, таутомер или стереоизомер.
[117] В определенных вариантах осуществления X представляет собой связь или выбран из группы, состоящей из

где «*» представляет собой точку присоединения РТМ, L или ULM, например ILM.
[118] В любом из соединений, описанных в данном документе, ILM может характеризоваться структурой формулы (XXIV) или (XXVI), которая получена из структуры лигандов IAP, описанных в публ. WO №2015/006524 и Perez HL, Discovery of potent heterodimeric antagonists of inhibitor of apoptosis proteins (IAPs) with sustained antitumor activity. J. Med. Chem. 58(3), 1556-62 (2015), или соответствующим ей неприродным миметиком, и химический линкер к линкерной группе L, как показано,

где
R1 в формуле (XXIV), (XXV) или (XXVI) выбран из необязательно замещенного алкила, необязательно замещенного циклоалкила, необязательно замещенного циклоалкилалкила, необязательно замещенного гетер оциклила, необязательно замещенного арилалкила или необязательно замещенного арила;
R2 в формуле (XXIV), (XXV) или (XXVI) выбран из необязательно замещенного алкила, необязательно замещенного циклоалкила, необязательно замещенного циклоалкилалкила, необязательно замещенного гетероциклила, необязательно замещенного арилалкила или необязательно замещенного арила;
или альтернативно
R1 и R2 в формуле (XXIV), (XXV) или (XXVI) независимо выбраны из необязательно замещенного тиоалкила, где заместители, присоединенные к атому S тиоалкила, представляют собой необязательно замещенный алкил, необязательно замещенный разветвленный алкил, необязательно замещенный гетероциклил, -(CH2)vCOR20, -CH2CHR21COR22 или -CH2R23,
где
v представляет собой целое число 1-3;
R20 и R22 в -(CH2)vCOR20 и -CH2R23 независимо выбраны из ОН, NR24R25 или OR26;
R21 в -CH2CHR21COR2 выбран из NR24R25;
R23 в -CH2R23 выбран из необязательно замещенного арила или необязательно замещенного гетероциклила, где необязательные заместители включают алкил и галоген;
R24 в NR24R25 выбран из водорода или необязательно замещенного алкила;
R25 в NR24R25 выбран из водорода, необязательно замещенного алкила, необязательно замещенного разветвленного алкила, необязательно замещенного арилалкила, необязательно замещенного гетероциклила, -СН2(OCH2CH2O)mCH3 или полиаминной цепи, такой как спермин или спермидин;
R26 в OR26 выбран из необязательно замещенного алкила, где необязательные заместители представляют собой ОН, галоген или NH2; и
m представляет собой целое число 1-8;
R3 и R4 в формуле (XXIV), (XXV) или (XXVI) независимо представляют собой необязательно замещенный алкил, необязательно замещенный циклоалкил, необязательно замещенный арил, необязательно замещенный арилалкил, необязательно замещенный арилалкокси, необязательно замещенный гетероарил, необязательно замещенный гетероциклил, необязательно замещенный гетероарилалкил или необязательно замещенный гетероциклоалкил, где заместители представляют собой алкил, галоген или ОН;
R5, R6, R7 и R8 в формуле (XXIV), (XXV) или (XXVI) независимо представляют собой водород, необязательно замещенный алкил или необязательно замещенный циклоалкил; и/или его фармацевтически приемлемая соль, таутомер или стереоизомер.
[119] В конкретном варианте осуществления в ILM в соответствии с формулами (XXII)-(XXVI),
R7 и R8 выбраны из Н или Me;
R5 и R6 выбраны из группы, включающей

R3 и R4 выбраны из группы, включающей

[120] В любом из соединений, описанных в данном документе, ILM может характеризоваться структурой формулы (XXVII) или (XXVII), которая получена из структуры лигандов IAP, описанных в публ. WO №2014/055461 и Kim, KS, Discovery of tetrahydroisoquinoline-based bivalent heterodimeric IAP antagonists. Bioorg. Med. Chem. Lett. 24(21), 5022-9 (2014), или соответствующим ей неприродным миметиком,

где
R35 представляет собой 1-2 заместителя, выбранные из алкила, галогена, алкокси, циано и галогеналкокси;
R1 в формуле (XXVII) и (XXVIII) выбран из Н или необязательно замещенного алкила, необязательно замещенного циклоалкила, необязательно замещенного циклоалкилалкила, необязательно замещенного гетероциклила, необязательно замещенного арилалкила или необязательно замещенного арила;
R2 в формуле (XXVII) и (XXVIII) выбран из Н или необязательно замещенного алкила, необязательно замещенного циклоалкила, необязательно замещенного циклоалкилалкила, необязательно замещенного гетероциклила, необязательно замещенного арилалкила или необязательно замещенного арила;
или альтернативно
R1 и R2 в формуле (XXVII) и (XXVIII) независимо выбраны из необязательно замещенного тиоалкила -CR60R61SR70, где R60 и R61 выбраны из Н или метила, и R70 выбран из необязательно замещенного алкила, необязательно замещенного разветвленного алкила, необязательно замещенного гетероциклила, -(CH2)vCOR20, -CH2CHR21COR22 или -CH2R23,
где
v представляет собой целое число 1-3;
R20 и R22 в -(CH2)vCOR20 и -CH2CHR21COR22 независимо выбраны из ОН, NR24R25 или OR26;
R21 в -CH2CHR21COR22 выбран из NR24R25;
R23 в -CH2R23 выбран из необязательно замещенного арила или необязательно замещенного гетероциклила, где необязательные заместители включают алкил и галоген;
R24 в NR24R25 выбран из водорода или необязательно замещенного алкила;
R25 в NR24R25 выбран из водорода, необязательно замещенного алкила, необязательно замещенного разветвленного алкила, необязательно замещенного арилалкила, необязательно замещенного гетероциклила, -СН2СН2(ОСН2СН2)mCH3 или полиаминной цепи -[CH2CH2(CH2)δNH]ψCH2CH2(CH2)ϖNH2, такой как спермин или спермидин;
где δ=0-2, ψ=1-3, ϖ=0-2;
R26 в OR26 представляет собой необязательно замещенный алкил, где необязательные заместители представляют собой ОН, галоген или NH2; и
m представляет собой целое число 1-8,
R3 и R4 в формуле (XXVII) и (XXVIII) независимо выбраны из необязательно замещенного алкила, необязательно замещенного циклоалкила, необязательно замещенного арила, необязательно замещенного арилалкила, необязательно замещенного арилалкокси, необязательно замещенного гетероарила, необязательно замещенного гетероциклила, необязательно замещенного гетероарилалкила или необязательно замещенного гетероциклоалкила, где заместители представляют собой алкил, галоген или ОН;
R5, R6, R7 и R8 в формуле (XXVII) и (XXVIII) независимо выбраны из водорода, необязательно замещенного алкила или необязательно замещенного циклоалкила;
R31 в формулах (XXVII) и (XXVIII) выбран из алкила, арила, арилалкила, гетероарила или гетероарилалкила, необязательно дополнительно замещенных, предпочтительно выбранных из группы, состоящей из

X в формулах (XXVII) и (XXVIII) выбран из -(CR81R82)m-, необязательно замещенных гетероарила или гетероциклила,

Z в формулах (XXVII) выбран из С=O, -О-, -NR, -CONH-, -NHCO- или может отсутствовать;
R81 и R82 в -(CR81R82)m- независимо выбраны из водорода, галогена, алкила или циклоалкила, или R81 и R82 могут быть взяты вместе с образованием карбоциклического кольца;
R10 и R11 в  независимо выбраны из водорода, галогена или алкила;
независимо выбраны из водорода, галогена или алкила;
R12, R13, R14, R15 и R16 в 
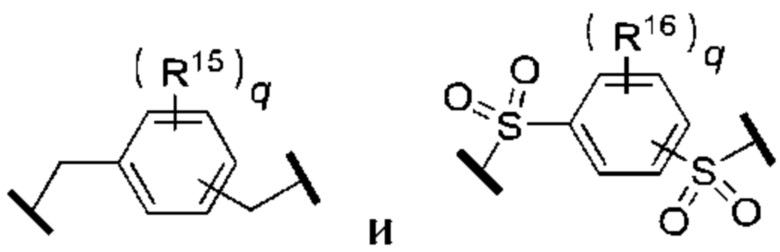 независимо выбраны из водорода, галогена или необязательно замещенного алкила или OR17;
независимо выбраны из водорода, галогена или необязательно замещенного алкила или OR17;
R17 выбран из водорода, необязательно замещенного алкила или необязательно замещенного циклоалкила;
m и n в -(CR21R22)m- и  независимо равняются 0, 1, 2, 3 или 4;
независимо равняются 0, 1, 2, 3 или 4;
о и р в  независимо равняются 0, 1, 2 или 3;
независимо равняются 0, 1, 2 или 3;
q и t в  независимо равняются 0, 1, 2, 3 или 4;
независимо равняются 0, 1, 2, 3 или 4;
r в  равняется 0 или 1;
равняется 0 или 1;
и/или его фармацевтически приемлемая соль, таутомер или стереоизомер.
[121] В любом из соединений, описанных в данном документе, ILM может характеризоваться структурой формулы (XXIX), (XXX), (XXXI) или (XXXII), которая получена из структуры лигандов IAP, описанных в публ. WO №2014/055461 и Kim, KS, Discovery of tetrahydroisoquinoline-based bivalent heterodimeric IAP antagonists. Bioorg. Med. Chem. Lett. 24(21), 5022-9 (2014), или соответствующим ей неприродным миметиком, и химический линкер к линкерной группе L, как показано,

где
R2 в формулах (XXIX)-(XXXII) выбран из Н, необязательно замещенного алкила, необязательно замещенного циклоалкила, необязательно замещенного циклоалкилалкила, необязательно замещенного гетероциклила, необязательно замещенного арилалкила или необязательно замещенного арила;
или альтернативно
R1 и R2 в формуле (XXVII) и (XXVIII) независимо выбраны из Н, необязательно замещенного тиоалкила -CR60R61SR70, где R60 и R61 выбраны из Н или метила, и R70 представляет собой необязательно замещенный алкил, необязательно замещенный разветвленный алкил, необязательно замещенный гетероциклил, -(CH2)vCOR20, -CH2CHR21COR22 или -CH2R23;
где
v представляет собой целое число 1-3;
R20 и R22 в -(CH2)vCOR20 и -CH2CHR21COR22 независимо выбраны из ОН, NR24R25 или OR26;
R21 в -CH2CHR21COR22 выбран из NR24R25;
R23 в -CH2R23 выбран из необязательно замещенного арила или необязательно замещенного гетероциклила, где необязательные заместители включают алкил и галоген;
R24 в NR24R25 выбран из водорода или необязательно замещенного алкила;
R25 в NR24R25 выбран из водорода, необязательно замещенного алкила, необязательно замещенного разветвленного алкила, необязательно замещенного арилалкила, необязательно замещенного гетероциклила, -СН2СН2(ОСН2СН2)mCH3 или полиаминной цепи -[CH2CH2(CH2)δNH]ψCH2CH2(CH2)ϖrNH2, такой как спермин или спермидин,
где δ=0-2, ψ=1-3, ϖ=0-2;
R26 в OR26 представляет собой необязательно замещенный алкил, где необязательные заместители представляет собой ОН, галоген или NH2;
m представляет собой целое число 1-8;
R6 и R8 в формуле (XXIX)-(XXXII) независимо выбраны из водорода, необязательно замещенного алкила или необязательно замещенного циклоалкила; и
R31 в формулах (XXIX)-(XXXII) выбран из алкила, арила, арилалкила, гетероарила или гетероарилалкила, необязательно дополнительно замещенных, предпочтительно выбранных из группы, состоящей из

[122] В определенных вариантах осуществления ILM в соединении представляет собой

[123] В любом из соединений, описанных в данном документе, ILM может характеризоваться структурой формулы (XXXIII), которая получена из структуры лигандов IAP, описанных в публ. WO №2014/074658 и публ. WO №2013/071035, или соответствующим ей неприродным миметиком,

где
R2 в формуле (XXXIII) выбран из Н, необязательно замещенного алкила, необязательно замещенного циклоалкила, необязательно замещенного циклоалкилалкила, необязательно замещенного гетероциклила, необязательно замещенного арилалкила или необязательно замещенного арила;
R6 и R8 в формуле (XXXIII) независимо выбраны из водорода, необязательно замещенного алкила или необязательно замещенного циклоалкила;
R32 в формуле (XXXIII) выбран из (С1-С4алкилен)-R33, где R33 выбран из водорода, арила, гетероарила или циклоалкила, необязательно дополнительно замещенных;
X в формуле (XXXIII) выбран из

Z и Z' в формуле (XXXIII) независимо выбраны из

 где каждый
где каждый  представляет собой точку присоединения к соединению, и Z и Z' не могут одновременно представлять собой
представляет собой точку присоединения к соединению, и Z и Z' не могут одновременно представлять собой  в каком-либо приведенном соединении;
в каком-либо приведенном соединении;
Y в формуле (XXXIII) выбран из

 где Z и Z' в формуле (XXXIII) являются одинаковыми, и Z представляет собой
где Z и Z' в формуле (XXXIII) являются одинаковыми, и Z представляет собой  где каждый
где каждый  представляет собой точку присоединения к соединению, X выбран из
представляет собой точку присоединения к соединению, X выбран из

Y в формуле (XXXIII) независимо выбран из


где
 представляет собой точку присоединения к части -С=O соединения;
представляет собой точку присоединения к части -С=O соединения;
 представляет собой точку присоединения к части -NH соединения;
представляет собой точку присоединения к части -NH соединения;
 представляет собой первую точку присоединения к Z;
представляет собой первую точку присоединения к Z;
 представляет собой вторую точку присоединения к Z;
представляет собой вторую точку присоединения к Z;
m представляет собой целое число 0-3;
n представляет собой целое число от 1-3;
р представляет собой целое число 0-4; и
А представляет собой -C(O)R3;
R3 в -C(O)R3 выбран из ОН, NHCN, NHSO2R10, NHOR11 или N(R12)(R13);
R10 и F11 в NHSO2R10 и NHOR11 независимо выбраны из водорода, необязательно замещенного -С1-С4алкила, циклоалкила, арила, гетероарила, гетероциклила или гетероциклоалкила;
R12 и R13 в N(R12)(R13) независимо выбраны из водорода, -С1-С4алкила, -(С1-С4)алкилен)-NH-(С1-С4алкил) и -(С1-С4алкилен)-O-(С1-С4гидроксиалкил), или R12 и R13 взяты вместе с атомом азота, с которым они обычно связаны, с образованием насыщенного гетероциклила, необязательно содержащего один дополнительный гетероатом, выбранный из N, О и S, и при этом насыщенный гетероцикл необязательно замещен метилом.
[124] В любом из соединений, описанных в данном документе, ILM может характеризоваться структурой формулы (XXXIV) или (XXXV), которая получена из структуры лигандов IAP, описанных в публ. WO №2014/047024, или соответствующим ей неприродным миметиком,

где
X в формуле (XXXIV) или (XXXV) отсутствует или выбран из группы, состоящей из -(CR10R11)m-, необязательно замещенного гетероарила или необязательно замещенного гетероциклила,

Y и Z в формуле (XXXIV) или (XXXV) независимо выбраны из С=O, -O-, -NR9-, -CONH-, -NHCO- или могут отсутствовать;
R1 и R2 в формуле (XXXIV) или (XXXV) независимо выбраны из необязательно замещенного алкила, необязательно замещенного циклоалкила, необязательно замещенного циклоалкилалкила, необязательно замещенного арилалкила, необязательно замещенного арила, или
R1 и R2 в формуле (XXXIV) или (XXXV) независимо выбраны из необязательно замещенного тиоалкила, где заместители, присоединенные к атому S тиоалкила, представляют собой необязательно замещенный алкил, необязательно замещенный разветвленный алкил, необязательно замещенный гетероциклил, -(CH2)vCOR20, -CH2CHR21COR22 или -CH2R23; где
v представляет собой целое число 1-3;
R20 и R22 в -(CH2)vCOR20 и -CH2CHR21COR22 независимо выбраны из ОН, NR24R25 или OR26;
R21 в -CH2CHR21COR22 выбран из NR24R25;
R23 в -CH2R23 выбран из необязательно замещенного арила или необязательно замещенного гетероциклила, где необязательные заместители включают алкил и галоген;
R24 в NR24R25 выбран из водорода или необязательно замещенного алкила;
R25 в NR24R25 выбран из водорода, необязательно замещенного алкила, необязательно замещенного разветвленного алкила, необязательно замещенного арилалкила, необязательно замещенного гетероциклила, -СН2(ОСН2СН20)mCH3 или полиаминной цепи;
R26 представляет собой необязательно замещенный алкил, где необязательные заместители представляют собой ОН, галоген или NH2;
m в -(CR10R11)m- представляет собой целое число 1-8;
R3 и R4 в формуле (XXXIV) или (XXXV) независимо выбраны из необязательно замещенного алкила, необязательно замещенного циклоалкила, необязательно замещенного арила, необязательно замещенного арилалкила, необязательно замещенного арилалкокси, необязательно замещенного гетероарила, необязательно замещенного гетероциклила, необязательно замещенного гетероарилалкила или необязательно замещенного гетероциклоалкила, где заместители представляют собой алкил, галоген или ОН;
R5, R6, R7 и R8 в формуле (XXXIV) или (XXXV) независимо выбраны из водорода, необязательно замещенного алкила или необязательно замещенного циклоалкила; и
R10 и R11 в -(CR10R11)m- независимо выбраны из водорода, галогена или необязательно замещенного алкила;
R12 и R13 в 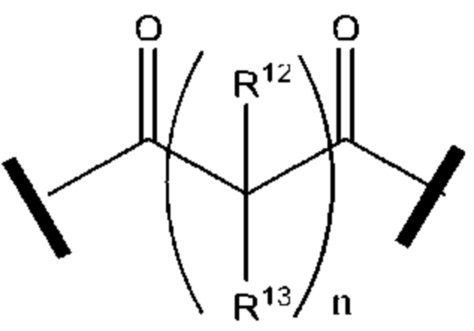 независимо выбраны из водорода, галогена или необязательно замещенного алкила, или R12 и R13 могут быть взяты вместе с образованием карбоциклического кольца;
независимо выбраны из водорода, галогена или необязательно замещенного алкила, или R12 и R13 могут быть взяты вместе с образованием карбоциклического кольца;
R14, R15, R16, R17 и R18 в 
 независимо выбраны из водорода, галогена, необязательно замещенного алкила или OR19;
независимо выбраны из водорода, галогена, необязательно замещенного алкила или OR19;
R19 в OR19 выбран из водорода, необязательно замещенного алкила или необязательно замещенного циклоалкила;
m и n в -(CR10R11)m- независимо равняются 0, 1, 2, 3 или 4;
о и р в -(CR10R11)m- независимо равняются 0, 1, 2 или 3;
q в -(CR10R11)m- равняется 0, 1, 2, 3 или 4; r равняется 0 или 1;
t в -(CR10R11)m- равняется 1, 2 или 3; и/или его фармацевтически приемлемая соль, таутомер или стереоизомер.
[125] В любом из соединений, описанных в данном документе, ILM может характеризоваться структурой формулы (XXXVI), которая получена из структуры лигандов IAP, описанных в публ. WO №2014/025759, или соответствующим ей неприродным миметиком,

где
А в формуле (XXXVI) выбран из  где пунктирная линия представляет собой необязательную двойную связь;
где пунктирная линия представляет собой необязательную двойную связь;
X в формуле (XXXVI) выбран из -(CR21R22)m-, 
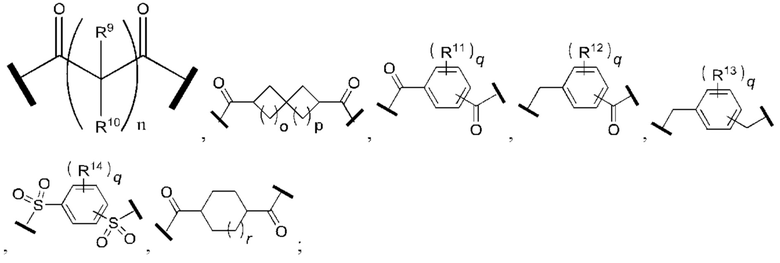
Y и Z в формуле (XXXVI) независимо выбраны из -0-, -NR6- или отсутствуют;
V в формуле (XXXVI) выбран из -N- или -СН-;
W в формуле (XXXVI) выбран из -СН- или -N-;
R1 в формуле (XXXVI) выбран из необязательно замещенного алкила, необязательно замещенного циклоалкила, необязательно замещенного циклоалкилалкила, необязательно замещенного арилалкила или необязательно замещенного арила;
R3 и R4 в формуле (XXXVI) независимо выбраны из необязательно замещенного алкила, необязательно замещенного циклоалкила, необязательно замещенного арила, необязательно замещенного гетероарила, необязательно замещенного гетероциклила, необязательно замещенного арилалкила, необязательно замещенного гетероарилалкила или необязательно замещенного гетероциклоалкила;
R5, R6, R7 и R8 в формуле (XXIV), (XXV) или (XXVI) независимо выбраны из водорода, необязательно замещенного алкила или необязательно замещенного циклоалкила или предпочтительно метила;
R9 и R10 в  независимо выбраны из водорода, галогена или необязательно замещенного алкила, или R9 и R10 могут быть взяты вместе с образованием кольца;
независимо выбраны из водорода, галогена или необязательно замещенного алкила, или R9 и R10 могут быть взяты вместе с образованием кольца;
R11, R12, R13 и R14 в 
 независимо выбраны из водорода, галогена, необязательно замещенного алкила или OR15;
независимо выбраны из водорода, галогена, необязательно замещенного алкила или OR15;
R15 в OR15 выбран из водорода, необязательно замещенного алкила или необязательно замещенного циклоалкила;
m и n в -(CR21R22)m- и  независимо выбраны из 0, 1, 2, 3 или 4;
независимо выбраны из 0, 1, 2, 3 или 4;
о и р в  и независимо выбраны из 0, 1, 2 или 3;
и независимо выбраны из 0, 1, 2 или 3;
q в 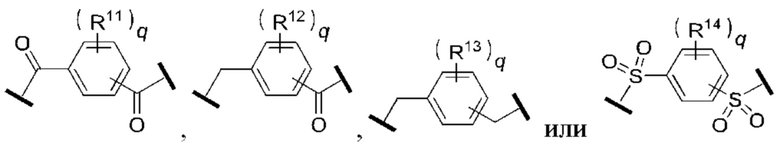 выбран из 0, 1, 2, 3 или 4;
выбран из 0, 1, 2, 3 или 4;
r в  выбран из 0 или 1, и/или или его фармацевтически приемлемая соль, таутомер или стереоизомер.
выбран из 0 или 1, и/или или его фармацевтически приемлемая соль, таутомер или стереоизомер.
[126] В любом из соединений, описанных в данном документе, ILM может характеризоваться структурой формулы (XXXVII) или (XXXVIII), которая получена из структуры лигандов IAP, описанных в публ. WO №2014/011712, или соответствующим ей неприродным миметиком,
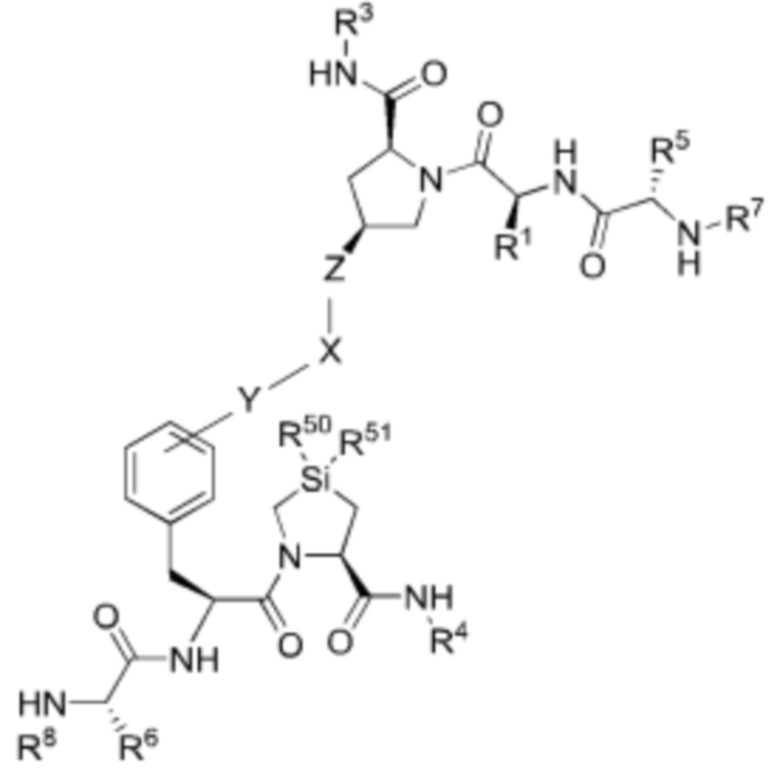

где
X в формулах (XXXVII) и (XXXVIII) представляет собой -(CR16R17)m-,
 или отсутствует;
или отсутствует;
Y и Z в формуле (XXXVII) и (XXXVIII) независимо выбраны из -0-, С=0, NR6 или отсутствуют;
R1 и R2 в формуле (XXXVII) и (XXXVIII) выбраны из необязательно замещенного алкила, необязательно замещенного циклоалкила, необязательно замещенного алкиларила или необязательно замещенного арила;
R3 и R4 в формуле (XXXVII) и (XXXVIII) независимо выбраны из необязательно замещенного алкила, необязательно замещенного циклоалкила, необязательно замещенного циклоалкилалкила, необязательно замещенного арилалкила или необязательно замещенного арила;
R5 и R6 в формуле (XXXVII) и (XXXVIII) независимо выбраны из необязательно замещенного алкила или необязательно замещенного циклоалкила;
R7 и R8 в формуле (XXXVII) и (XXXVIII) независимо выбраны из водорода, необязательно замещенного алкила или необязательно замещенного циклоалкила или предпочтительно метила;
R9 и R10 в  независимо выбраны из водорода, необязательно замещенного алкила, или R9 и R10 могут быть взяты вместе с образованием кольца;
независимо выбраны из водорода, необязательно замещенного алкила, или R9 и R10 могут быть взяты вместе с образованием кольца;
R11-R14 в
 независимо выбраны из водорода, галогена, необязательно замещенного алкила или
независимо выбраны из водорода, галогена, необязательно замещенного алкила или
OR15;
R15 в OR15 выбран из водорода, необязательно замещенного алкила или необязательно замещенного циклоалкила;
R16 и R17 в -(CR16R17)m- независимо выбраны из водорода, галогена или необязательно замещенного алкила;
R50 и R51 в формуле (XXXVII) и (XXXVIII) независимо выбраны из необязательно замещенного алкила, или R50 и R51 взяты вместе с образованием кольца;
m и n в -(CR16R17)m- и 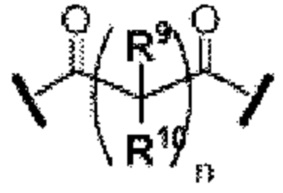 независимо представляют собой целое число 0-4;
независимо представляют собой целое число 0-4;
о и р в  независимо представляют собой целое число 0-3;
независимо представляют собой целое число 0-3;
q в  представляет собой целое число 0-4; и
представляет собой целое число 0-4; и
r в 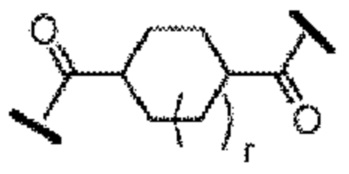 представляет собой целое число 0-1;
представляет собой целое число 0-1;
или его фармацевтически приемлемая соль, таутомер или стереоизомер.
[127] В одном варианте осуществления R1 и R2 в ILM формулы (XXXVII) или (XXXVIII) представляют собой трет-бутил, и R3 и R4 в ILM формулы (XXXVII) или (XXXVIII) представляют собой тетрагидронафталин.
[128] В любом из соединений, описанных в данном документе, ILM может характеризоваться структурой формулы (XXXIX) или (XL), которая получена из структуры лигандов IAP, описанных в публ. WO №2013/071039, или соответствующим ей неприродным миметиком,

где
R43 и R44 в формулах (XXXIX) и (XL) независимо выбраны из водорода, алкила, арила, арилалкила, гетероарила, гетероарилалкила, циклоалкила, циклоалкилалкила, дополнительно необязательно замещенных, и
R6 и R8 в формуле (XXXIX) и (XL) независимо выбраны из водорода, необязательно замещенного алкила или необязательно замещенного циклоалкила;
каждый X в формулах (XXXIX) и (XL) независимо выбран из

каждый Z в формулах (XXXIX) и (XL) выбран из  где каждый
где каждый  представляет собой точку присоединения к соединению; и
представляет собой точку присоединения к соединению; и
каждый Y выбран из


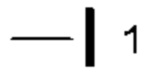 представляет собой точку присоединения к части -С=O соединения;
представляет собой точку присоединения к части -С=O соединения;
 представляет собой точку присоединения к аминочасти соединения;
представляет собой точку присоединения к аминочасти соединения;
 представляет собой первую точку присоединения к Z;
представляет собой первую точку присоединения к Z;
 представляет собой вторую точку присоединения к Z; и
представляет собой вторую точку присоединения к Z; и
А выбран из -C(O)R3 или
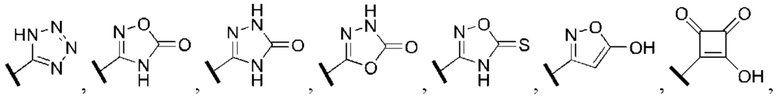
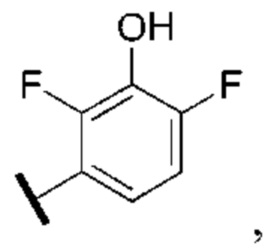 или таутомерная форма любого из вышеуказанных, где:
или таутомерная форма любого из вышеуказанных, где:
R3 в -C(O)R3 выбран из ОН, NHCN, NHS02R10, NHOR11 или N(R12)(R13);
R10 и R11 в NHS02R10 и NHOR11 независимо выбраны из -С1-С4алкила, циклоалкила, арила, гетероарила или гетероциклоалкила, любой из которых необязательно замещен, и водорода;
каждый из R12 и R13 в N(R12)(R13) независимо выбран из водорода, -С1-С4алкила, -(С1-С4алкилен)-NH-(С1-С4алкил), бензила, -(С1-С4алкилен)-С(O)ОН,
-(С1-С4алкилен)-С(O)СН3, -СН(бензил)-СООН, -С1-С4алкокси и
-(С1-С4алкилен)-O-(С1-С4гидроксиалкил); или R12 и R13 в N(R12)(R13) взяты вместе с атомом азота, с которым они совместно связаны, с образованием насыщенного гетероциклила, необязательно содержащего один дополнительный гетероатом, выбранный из N, О и S, и при этом насыщенный гетероцикл необязательно замещен метилом.
[129] В любом из соединений, описанных в данном документе, ILM может характеризоваться структурой формулы (XLI), которая получена из структуры лигандов IAP, описанных в публ. WO №2013/071039, или соответствующим ей неприродным миметиком,
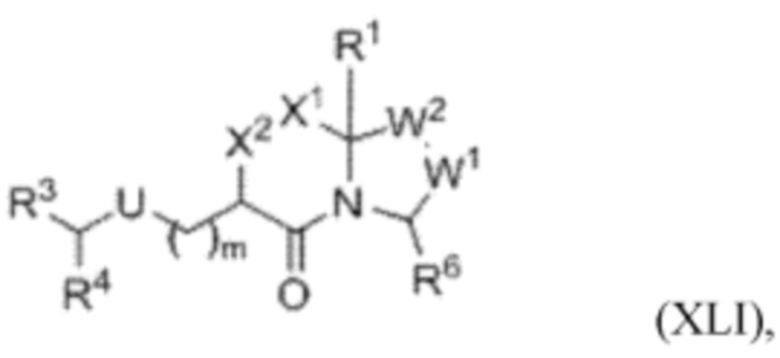
где
W1 в формуле (XLI) выбран из О, S, N-RA или C(R8a)(R8b);
W2 в формуле (XLI) выбран из О, S, N-RA или C(R8c)(R8d); при условии, что W1 и W2 одновременно не представляют собой О или одновременно не представляют собой S;
R1 в формуле (XLI) выбран из Н, C1-С6алкила, С3-С6циклоалкила, -C1-С6алкил-(замещенный или незамещенный С3-С6циклоалкил), замещенного или незамещенного арила, замещенного или незамещенного гетероарила, -С1-С6алкил-(замещенный или незамещенный арил) или -С1-С6алкил-(замещенный или незамещенный гетероарил);
если X1 выбран из О, N-RA, S, S(O) или S(O)2, то X2 представляет собой C(R2aR2b);
или
X1 в формуле (XLI) выбран из CR2cR2d, и X2 представляет собой CR2aR2b, и R2c и R2a вместе образуют связь;
или
X1 и X2 в формуле (XLI) независимо выбраны из С и N и являются членами конденсированного замещенного или незамещенного насыщенного или частично насыщенного 3-10-членного циклоалкильного кольца, конденсированного замещенного или незамещенного насыщенного или частично насыщенного 3-10-членного гетероциклоалкильного кольца, конденсированного замещенного или незамещенного 5-10-членного арильного кольца или конденсированного замещенного или незамещенного 5-10-членного гетероарильного кольца;
или
X1 в формуле (XLI) выбран из CH2, и X2 представляет собой С=O, C=C(RC)2 или C=NRC; где каждый Rc независимо выбран из Н, -CN, -ОН, алкокси, замещенного или незамещенного C1-С6алкила, замещенного или незамещенного С3-С6циклоалкила, замещенного или незамещенного С2-С5гетероциклоалкила, замещенного или незамещенного арила, замещенного или незамещенного гетероарила, -C1-С6алкил-(замещенный или незамещенный С3-С6циклоалкил), -С1-С6алкил-(замещенный или незамещенный С2-С5гетероциклоалкил), -С1-С6алкил-(замещенный или незамещенный арил) или -С1-С6алкил-(замещенный или незамещенный гетероарил);
RA в N-RA выбран из Н, C1-С6алкила, -С(=O)С1-С2алкила, замещенного или незамещенного арила или замещенного или незамещенного гетероарила;
R2a, R2b, R2c, R2d в CR2cR2d и CR2aR2b независимо выбраны из Н, замещенного или незамещенного С1-С6алкила, замещенного или незамещенного C1-С6гетероалкила, замещенного или незамещенного С3-С6циклоалкила, замещенного или незамещенного С2-С5гетероциклоалкила, замещенного или незамещенного арила, замещенного или незамещенного гетероарила, -С1-С6алкил-(замещенный или незамещенный С3-С6циклоалкил), -С1-С6алкил-(замещенный или незамещенный С2-С5гетероциклоалкил), -С1-С6алкил-(замещенный или незамещенный арил), -C1-С6алкил-(замещенный или незамещенный гетероарил) и -C(=O)RB;
RB в -C(=O)RB выбран из замещенного или незамещенного C1-С6алкила, замещенного или незамещенного С3-С6циклоалкила, замещенного или незамещенного С2-С5гетероциклоалкила, замещенного или незамещенного арила, замещенного или незамещенного гетероарила, -С1-С6алкил-(замещенный или незамещенный С3-С6циклоалкил), -С1-С6алкил-(замещенный или незамещенный С2-С5гетероциклоалкил), -С1-С6алкил-(замещенный или незамещенный арил), -C1-С6алкил-(замещенный или незамещенный гетероарил) или -NRDRE;
RD и RE в NRDRE независимо выбраны из Н, замещенного или незамещенного C1-С6алкила, замещенного или незамещенного С3-С6циклоалкила, замещенного или незамещенного С2-С5гетероциклоалкила, замещенного или незамещенного арила, замещенного или незамещенного гетероарила, -С1-С6алкил-(замещенный или незамещенный С3-С6циклоалкил), -С1-С6алкил-(замещенный или незамещенный С2-С5гетероциклоалкил), -С1-С6алкил-(замещенный или незамещенный арил) или -C1-С6алкил-(замещенный или незамещенный гетероарил);
m в формуле (XLI) выбран из 0, 1 или 2;
-U- в формуле (XLI) выбран из -NHC(=O)-, -C(=O)NH-, -NHS(=O)2-, -S(=O)2NH-, -NHC(=O)NH-, -NH(C=O)O-, -O(C=O)NH- или -NHS(=O)2NH-;
R3 в формуле (XLI) выбран из C1-С3алкила или C1-С3фторалкила;
R4 в формуле (XLI) выбран из -NHR5, -N(R5)2, -N+(R5)3 или -OR5;
каждый R5 в -NHR5, -N(R5)2, -N+(R5)3 и -OR5 независимо выбран из Н, C1-С3алкила, C1-С3галогеналкила, C1-С3гетероалкила и -С1-С3алкил-(С3-С5циклоалкил);
или
R3 и R5 в формуле (XLI) вместе с атомами, к которым они присоединены, образуют замещенное или незамещенное 5-7-членное кольцо;
или
R3 в формуле (XLI) связан с атомом азота в U с образованием замещенного или незамещенного 5-7-членного кольца;
R6 в формуле (XLI) выбран из -NHC(=O)R7, -C(=O)NHR7, -NHS(=O)2R7, -S(=O)2NHR7; -NHC(=O)NHR7, -NHS(=O)2NHR7, -(C1-С3алкил)-NHC(=O)R7, -(C1-С3алкил)-C(=O)NHR7, -(C1-С3алкил)-NHS(=O)2R7, -(C1-С3алкил)-S(=O)2NHR7; -(C1-С3алкил)-NHC(=O)NHR7, -(C1-С3алкил)-NHS(=O)2NHR7, замещенного или незамещенного С2-С10гетероциклоалкила или замещенного или незамещенного гетероарила;
каждый R7 в -NHC(=O)R7, -C(=O)NHR7, -NHS(=O)2R7, -S(=O)2NHR7; -NHC(=O)NHR7, -NHS(=O)2NHR7, -(C1-С3алкил)-NHC(=O)R7, -(C1-С3алкил)-C(=O)NHR7, -(C1-С3алкил)-NHS(=O)2R7, -(C1-С3алкил)-S(=O)2NHR7; -(C1-С3алкил)-NHC(=O)NHR7, -(C1-С3алкил)-NHS(=O)2NHR7 независимо выбран из C1-С6алкила, C1-С6галогеналкила, C1-С6гетероалкила, замещенного или незамещенного С3-С10циклоалкила, замещенного или незамещенного С2-С10гетероциклоалкила, замещенного или незамещенного арила, замещенного или незамещенного гетероарила, -С1-С6алкил-(замещенный или незамещенный С3-С10циклоалкил), -C1-С6алкил-(замещенный или незамещенный С2-С10 гетероциклоалкил), -С1-С6алкил-(замещенный или незамещенный арил), -С1-С6алкил-(замещенный или незамещенный гетероарил), -(СН2)р-СН(замещенный или незамещенный арил)2, -(СН2)р-СН(замещенный или незамещенный гетероарил)2, -(СН2)Р-СН(замещенный или незамещенный арил)(замещенный или незамещенный гетероарил), -(замещенный или незамещенный арил)-(замещенный или незамещенный арил), -(замещенный или незамещенный арил)-(замещенный или незамещенный гетероарил), -(замещенный или незамещенный гетероарил)-(замещенный или незамещенный арил) или -(замещенный или незамещенный гетероарил)-(замещенный или незамещенный гетероарил);
р в R7 выбран из 0, 1 или 2;
R8a, R8b, R8c и R8d в C(R8a)(R8b) и C(R8c)(R8d) независимо выбраны из Н, C1-С6алкила, C1-С6фторалкила, C1-С6алкокси, C1-С6гетероалкила и замещенного или незамещенного арила;
или
R8a и R8d определены выше, и R8b и R8c вместе образуют связь; или
R8a и R8d определены выше, и R8b и R8c вместе с атомами, к которым они присоединены, образуют замещенное или незамещенное конденсированное 5-7-членное насыщенное или частично насыщенное карбоциклическое кольцо или гетероциклическое кольцо, содержащее 1-3 гетероатома, выбранные из S, О и N, замещенное или незамещенное конденсированное 5-10-членное арильное кольцо или замещенное или незамещенное конденсированное 5-10-членное гетероарильное кольцо, содержащее 1-3 гетероатома, выбранные из S, О и N;
или
R8c и R8d определены выше, и R8a и R8b вместе с атомами, к которым они присоединены, образуют замещенный или незамещенный насыщенный или частично насыщенный 3-7-членный спироцикл или гетероспироцикл, содержащий 1-3 гетероатома, выбранные из S, О и N;
или
R8a и R8b определены выше, и R8c и R8d вместе с атомами, к которым они присоединены, образуют замещенный или незамещенный насыщенный или частично насыщенный 3-7-членный спироцикл или гетероспироцикл, содержащий 1-3 гетероатома, выбранные из S, О и N;
где каждый замещенный алкил, гетероалкил, конденсированное кольцо, спироцикл, гетероспироцикл, циклоалкил, гетероциклоалкил, арил или гетероарил замещен 1-3 R9; и
каждый R9 в R8a, R8b, R8c и R8d независимо выбран из галогена, -ОН, -SH, (С=O), CN, С1-С4алкила, С1-С4фторалкила, С1-С4алкокси, С1-С1фторалкокси, -NH2, -NH(C1-С4алкил), -NH(С1-С4алкил)2, -С(=O)ОН, -C(=0)NH2, -С(=O)С1-С3алкила, -S(=O)2CH3, -NH(C1-С4алкил)-OH, -NH(С1-С4алкил)-O-(С-С4алкил), -O(C1-С4алкил)-NH2; -O(C1-С4алкил)-NH-(С1-С4алкил) и -O(С1-С4алкил)-N-(С1-С4алкил)2, или два R9 вместе с атомами, к которым они присоединены, образуют метилендиокси- или этилендиокси-кольцо, замещенное или незамещенное галогеном, -ОН или C1-С3алкилом.
[130] В любом из соединений, описанных в данном документе, ILM может характеризоваться структурой формулы (XLII), которая получена из структуры лигандов IAP, описанных в публ. WO №2013/071039, или соответствующим ей неприродным миметиком,

где
W1 в формуле (XLII) представляет собой О, S, N-RA или C(R8a)(R8b);
W2 в формуле (XLII) представляет собой О, S, N-RA или C(R8c)(R8d); при условии, что W1 и W2 одновременно не представляют собой О или одновременно не представляют собой S;
R1 в формуле (XLII) выбран из Н, C1-С6алкила, С3-С6циклоалкила, -C1-С6алкил-(замещенный или незамещенный С3-С6циклоалкил), замещенного или незамещенного арила, замещенного или незамещенного гетероарила, -С1-С6алкил-(замещенный или незамещенный арил) или -С1-С6алкил-(замещенный или незамещенный гетероарил);
если X1 в формуле (XLII) представляет собой N-RA, то X2 представляет собой С=O или CR2cR2d, и X3 представляет собой CR2aR2b;
или
если X1 в формуле (XLII) выбран из S, S(O) или S(O)2, то X2 представляет собой CR2cR2d, и X3 представляет собой CR2aR2b;
или
если X1 в формуле (XLII) представляет собой О, то X2 представляет собой CR2cR2d и N-RA и X3 представляет собой CR2aR2b;
или
если X1 в формуле (XLII) представляет собой СН3, то X2 выбран из О, N-RA, S, S(O) или S(O)2, и X3 представляет собой CR2aR2b;
если X1 в формуле (XLII) представляет собой CR2eR2f, то и Х2 представляет собой CR2cR2d, и R2e и R2c вместе образуют связь, и X3 в формуле (VLII) представляет собой CR2aR2b;
или
X1 и X3 в формуле (XLII) одновременно представляет собой CH2, и X2 в формуле (XLII) представляет собой С=0, C=C(RC)2 или C=NRC; где каждый RC независимо выбран из Н, -CN, -ОН, алкокси, замещенного или незамещенного С1-С6алкила, замещенного или незамещенного С3-С6циклоалкила, замещенного или незамещенного С2-С5гетероциклоалкила, замещенного или незамещенного арила, замещенного или незамещенного гетероарила, -С1-С6алкил-(замещенный или незамещенный С3-С6циклоалкил), -С1-С6алкил-(замещенный или незамещенный С2-С5гетероциклоалкил), -С1-С6алкил-(замещенный или незамещенный арил) или -C1-С6алкил-(замещенный или незамещенный гетероарил);
или
X1 и X2 в формуле (XLII) независимо выбраны из С и N и являются членами конденсированного замещенного или незамещенного насыщенного или частично насыщенного 3-10-членного циклоалкильного кольца, конденсированного замещенного или незамещенного насыщенного или частично насыщенного 3-10-членного гетероциклоалкильного кольца, конденсированного замещенного или незамещенного 5-10-членного арильного кольца или конденсированного замещенного или незамещенного 5-10-членного гетероарильного кольца, и X3 представляет собой CR2aR2b;
или
X2 и X3 в формуле (XLII) независимо выбраны из С и N и являются членами конденсированного замещенного или незамещенного насыщенного или частично насыщенного 3-10-членного циклоалкильного кольца, конденсированного замещенного или незамещенного насыщенного или частично насыщенного 3-10-членного гетероциклоалкильного кольца, конденсированного замещенного или незамещенного 5-10-членного арильного кольца или конденсированного замещенного или незамещенного 5-10-членного гетероарильного кольца, и X1 в формуле (VLII) представляет собой CR2eR2f;
RA в N-RA выбран из Н, C1-С6алкила, -С(=O)С1-С2алкила, замещенного или незамещенного арила или замещенного или незамещенного гетероарила;
R2a, R2b, R2c, R2d, R2e и R2f в CR2cR2d, CR2aR2b и CR2eR2f независимо выбраны из H, замещенного или незамещенного С1-С6алкила, замещенного или незамещенного C1-С6гетероалкила, замещенного или незамещенного С3-С6циклоалкила, замещенного или незамещенного С2-С5гетероциклоалкила, замещенного или незамещенного арила, замещенного или незамещенного гетероарила, -С1-С6алкил-(замещенный или незамещенный С3-С6циклоалкил), -С1-С6алкил-(замещенный или незамещенный С2-С5 гетероциклоалкил), -С1-С6алкил-(замещенный или незамещенный арил), -C1-С6алкил-(замещенный или незамещенный гетероарил) и -C(=O)RB;
RB в -C(=O)RB выбран из замещенного или незамещенного C1-С6алкила, замещенного или незамещенного С3-С6циклоалкила, замещенного или незамещенного С2-С5гетероциклоалкила, замещенного или незамещенного арила, замещенного или незамещенного гетероарила, -С1-С6алкил-(замещенный или незамещенный С3-С6циклоалкил), -С1-С6алкил-(замещенный или незамещенный С2-С5гетероциклоалкил), -С1-С6алкил-(замещенный или незамещенный арил), -C1-С6алкил-(замещенный или незамещенный гетероарил) или -NRDRE;
RD и RE в NRDRE независимо выбраны из Н, замещенного или незамещенного C1-С6алкила, замещенного или незамещенного С3-С6циклоалкила, замещенного или незамещенного С2-С5гетероциклоалкила, замещенного или незамещенного арила, замещенного или незамещенного гетероарила, -С1-С6алкил-(замещенный или незамещенный С3-С6циклоалкил), -С1-С6алкил-(замещенный или незамещенный С2-С5 гетероциклоалкил), -С1-С6алкил-(замещенный или незамещенный арил) или -C1-С6алкил-(замещенный или незамещенный гетероарил);
m в формуле (XLII) выбран из 0, 1 или 2;
-U- в формуле (XLII) выбран из -NHC(=O)-, -C(=O)NH-, -NHS(=O)2-, -S(=O)2NH-, -NHC(=O)NH-, -NH(C=O)O-, -O(C=O)NH- или -NHS(=O)2NH-;
R3 в формуле (XLII) выбран из C1-С3алкила или C1-С3фторалкила;
R4 в формуле (XLII) выбран из -NHR5, -N(R5)2, -N+(R5)3 или -OR5;
каждый R5 в -NHR5, -N(R5)2, -N+(R5)3 и -OR5 независимо выбран из Н, C1-С3алкила, C1-С3галогеналкила, C1-С3гетероалкила и -С1-Сзалкил-(С3-С5циклоалкил);
или
R3 и R5 в формуле (XLII) вместе с атомами, к которым они присоединены, образуют замещенное или незамещенное 5-7-членное кольцо;
или
R3 в формуле (XLII) связан с атомом азота в U с образованием замещенного или незамещенного 5-7-членного кольца;
R6 в формуле (XLII) выбран из -NHC(=O)R7, -C(=O)NHR7, -NHS(=O)2R7, -S(=O)2NHR7; -NHC(=O)NHR7, -NHS(=O)2NHR7, -(C1-С3алкил)-NHC(=O)R7, -(C1-С3алкил)-C(=O)NHR7, -(C1-С3алкил)-NHS(=O)2R7, -(C1-С3алкил)-S(=O)2NHR7; -(C1-С3алкил)-NHC(=O)NHR7, -(C1-С3алкил)-NHS(=O)2NHR7, замещенного или незамещенного С2-С10гетероциклоалкила или замещенного или незамещенного гетероарила;
каждый R7 в -NHC(=O)R7, -C(=O)NHR7, -NHS(=O)2R7, -S(=O)2NHR7; -NHC(=O)NHR7, -NHS(=O)2NHR7, -(C1-С3алкил)-NHC(=O)R7, -(C1-С3алкил)-C(=O)NHR7, -(C1-С3алкил)-NHS(=O)2R7, -(C1-С3алкил)-S(=O)2NHR7; -(C1-С3алкил)-NHC(=O)NHR7, -(C1-С3алкил)-NHS(=O)2NHR7 независимо выбран из C1-С6алкила, C1-С6галогеналкила, C1-С6гетероалкила, замещенного или незамещенного С3-С10циклоалкила, замещенного или незамещенного С2-С10гетероциклоалкила, замещенного или незамещенного арила, замещенного или незамещенного гетероарила, -С1-С6алкил-(замещенный или незамещенный С3-С10циклоалкил), -C1-С6алкил-(замещенный или незамещенный С2-С10 гетероциклоалкил), -С1-С6алкил-(замещенный или незамещенный арил), -С1-С6алкил-(замещенный или незамещенный гетероарил), -(СН2)р-СН(замещенный или незамещенный арил)2, -(СН2)p-СН(замещенный или незамещенный гетероарил)2, -(СН2)Р-СН(замещенный или незамещенный арил)(замещенный или незамещенный гетероарил), -(замещенный или незамещенный арил)-(замещенный или незамещенный арил), -(замещенный или незамещенный арил)-(замещенный или незамещенный гетероарил), -(замещенный или незамещенный гетероарил)-(замещенный или незамещенный арил) или -(замещенный или незамещенный гетероарил)-(замещенный или незамещенный гетероарил);
р в R7 выбран из 0, 1 или 2;
R8a, R8b, R8c и R8d в C(R8a)(R8b) и C(R8c)(R8d) независимо выбраны из Н, C1-С6алкила, C1-С6фторалкила, C1-С6алкокси, C1-С6гетероалкила и замещенного или незамещенного арила;
или
R8a и R8d определены выше, и R8b и R8c вместе образуют связь; или
R8a и R8d определены выше, и R8b и R8c вместе с атомами, к которым они присоединены, образуют замещенное или незамещенное конденсированное 5-7-членное насыщенное или частично насыщенное карбоциклическое кольцо или гетероциклическое кольцо, содержащее 1-3 гетероатома, выбранные из S, О и N, замещенное или незамещенное конденсированное 5-10-членное арильное кольцо или замещенное или незамещенное конденсированное 5-10-членное гетероарильное кольцо, содержащее 1-3 гетероатома, выбранные из S, О и N;
или
R8c и R8d определены выше, и R8a и R8b вместе с атомами, к которым они присоединены, образуют замещенный или незамещенный насыщенный или частично насыщенный 3-7-членный спироцикл или гетероспироцикл, содержащий 1-3 гетероатома, выбранные из S, О и N;
или
R8a и R8b определены выше, и R8c и R8d вместе с атомами, к которым они присоединены, образуют замещенный или незамещенный насыщенный или частично насыщенный 3-7-членный спироцикл или гетероспироцикл, содержащий 1-3 гетероатома, выбранные из S, О и N;
где каждый замещенный алкил, гетероалкил, конденсированное кольцо, спироцикл, гетероспироцикл, циклоалкил, гетероциклоалкил, арил или гетероарил замещен 1-3 R9; и
каждый R9 в R8a, R8b, R8c и R8d независимо выбран из галогена, -ОН, -SH, (С=O), CN, С1-С4алкила, С1-С4фторалкила, С1-С4алкокси, С1-С4фторалкокси, -NH2, -NH(C1-С4алкил), -NH(С1-С4алкил)2, -С(=O)ОН, -C(=O)NH2, -С(=O)С1-С3алкила, -S(=O)2CH3, -NH(C1-С4алкил)-OH, -NH(С1-С4алкил)-O-(С-С4алкил), -O(C1-С4алкил)-NH2; -O(C1-С4алкил)-NH-(С1-С4алкил) и -O(С1-С4алкил)-N-(С1-С4алкил)2, или два R9 вместе с атомами, к которым они присоединены, образуют метилендиокси- или этилендиокси-кольцо, замещенное или незамещенное галогеном, -ОН или C1-С3алкилом.
[131] В любом из соединений, описанных в данном документе, ILM может характеризоваться структурой формулы (XLIII), которая получена из структуры лигандов IAP, описанных в публ. WO №2013/071039, или соответствующим ей неприродным миметиком,

где
W1 в формуле (XLIII) выбран из О, S, N-RA или C(R8a)(R8b);
W2 в формуле (XLIII) выбран из О, S, N-RA или C(R8c)(R8d); при условии, что W1 и W2 одновременно не представляют собой О или одновременно не представляют собой S;
R1 в формуле (XLIII) выбран из Н, C1-С6алкила, С3-С6циклоалкила, -C1-С6алкил-(замещенный или незамещенный С3-С6циклоалкил), замещенного или незамещенного арила, замещенного или незамещенного гетероарила, -С1-С6алкил-(замещенный или незамещенный арил) или -С1-С6алкил-(замещенный или незамещенный гетероарил);
если X1 в формуле (XLIII) выбран из N-RA, S, S(O) или S(O)2, то X2 в формуле (XLIII) представляет собой CR2cR2d, и X3 в формуле (XLIII) представляет собой CR2aR2b;
или
если X1 в формуле (XLIII) представляет собой О, то X2 в формуле (XLIII) выбран из О, N-RA, S, S(O) или S(O)2, и X3 в формуле (XLIII) представляет собой CR2aR2b.
или
если X1 в формуле (XLIII) представляет собой CR2eR2f, то и X2 в формуле (XLIII) представляет собой CR2cR2d, и R2e и R2c вместе образуют связь, и X3 в формуле (XLIII) представляет собой CR2aR2b;
или
X1 и X2 в формуле (XLIII) независимо выбраны из С и N и являются членами конденсированного замещенного или незамещенного насыщенного или частично насыщенного 3-10-членного циклоалкильного кольца, конденсированного замещенного или незамещенного насыщенного или частично насыщенного 3-10-членного гетероциклоалкильного кольца, конденсированного замещенного или незамещенного 5-10-членного арильного кольца или конденсированного замещенного или незамещенного 5-10-членного гетероарильного кольца, и X3 в формуле (XLIII) представляет собой CR2aR2b;
или
X2 и X3 в формуле (XLIII) независимо выбраны из С и N и являются членами конденсированного замещенного или незамещенного насыщенного или частично насыщенного 3-10-членного циклоалкильного кольца, конденсированного замещенного или незамещенного насыщенного или частично насыщенного 3-10-членного гетероциклоалкильного кольца, конденсированного замещенного или незамещенного 5-10-членного арильного кольца или конденсированного замещенного или незамещенного 5-10-членного гетероарильного кольца, и X1 в формуле (VLII) представляет собой CR2eR2f;
RA в N-RA представляет собой Н, C1-С6алкил, -С(=O)С1-С2алкил, замещенный или незамещенный арил или замещенный или незамещенный гетероарил;
R2a, R2b, R2c, R2d, R2e и R2f в CR2cR2d, CR2aR2b и CR2eR2f независимо выбраны из H, замещенного или незамещенного C1-С6алкила, замещенного или незамещенного C1-С6гетероалкила, замещенного или незамещенного С3-С6циклоалкила, замещенного или незамещенного С2-С5гетероциклоалкила, замещенного или незамещенного арила, замещенного или незамещенного гетероарила, -С1-С6алкил-(замещенный или незамещенный С3-С6циклоалкил), -С1-С6алкил-(замещенный или незамещенный С2-С5гетероциклоалкил), -С1-С6алкил-(замещенный или незамещенный арил), -C1-С6алкил-(замещенный или незамещенный гетероарил) и -C(=O)RB;
RB в -C(=O)RB представляет собой замещенный или незамещенный C1-С6алкил, замещенный или незамещенный С3-С6циклоалкил, замещенный или незамещенный С2-С5 гетероциклоалкил, замещенный или незамещенный арил, замещенный или незамещенный гетероарил, -С1-С6алкил-(замещенный или незамещенный С3-С6циклоалкил), -С1-С6алкил-(замещенный или незамещенный С2-С5 гетероциклоалкил), -С1-С6алкил-(замещенный или незамещенный арил), -C1-С6алкил-(замещенный или незамещенный гетероарил), или -NRDRE;
RD и RE в NRDRE независимо выбраны из Н, замещенного или незамещенного C1-С6алкила, замещенного или незамещенного С3-С6циклоалкила, замещенного или незамещенного С2-С5гетероциклоалкила, замещенного или незамещенного арила, замещенного или незамещенного гетероарила, -С1-С6алкил-(замещенный или незамещенный С3-С6циклоалкил), -С1-С6алкил-(замещенный или незамещенный С2-С5 гетероциклоалкил), -С1-С6алкил-(замещенный или незамещенный арил) или -C1-С6алкил-(замещенный или незамещенный гетероарил);
m в формуле (XLIII) равняется 0, 1 или 2;
-U- в формуле (XLIII) представляет собой -NHC(=O)-, -C(=O)NH-, -NHS(=O)2-, -S(=O)2NH-, -NHC(=O)NH-, -NH(C=O)O-, -O(C=O)NH- или -NHS(=O)2NH-;
R3 в формуле (XLIII) представляет собой C1-С3алкил или C1-С3фторалкил;
R4 в формуле (XLIII) представляет собой -NHR5, -N(R5)2, -N+(R5)3 или -OR5;
каждый R5 в -NHR5, -N(R5)2, -N+(R5)3 и -OR5 независимо выбран из Н, C1-С3алкила, C1-С3галогеналкила, C1-С3гетероалкила и -С1-С3алкил-(С3-С5циклоалкил);
или
R3 и R5 в формуле (XLIII) вместе с атомами, к которым они присоединены, образуют замещенное или незамещенное 5-7-членное кольцо;
или
R3 в формуле (XLIII) связан с атомом азота в U с образованием замещенного или незамещенного 5-7-членного кольца;
R6 в формуле (XLIII) выбран из -NHC(=O)R7, -C(=O)NHR7, -NHS(=O)2R7, -S(=O)2NHR7; -NHC(=O)NHR7, -NHS(=O)2NHR7, -(C1-С3алкил)-NHC(=O)R7, -(C1-С3алкил)-С(=O)NHR7, -(Cl-С3алкил)-NHS(=O)2R7, -(C1-С3алкил)-S(=O)2NHR7; -(C1-С3алкил)-NHC(=O)NHR7, -(C1-С3алкил)-NHS(=O)2NHR7, замещенного или незамещенного С2-С10гетероциклоалкила или замещенного или незамещенного гетероарила;
каждый R7 в -NHC(=O)R7, -C(=O)NHR7, -NHS(=O)2R7, -S(=O)2NHR7; -NHC(=O)NHR7, -NHS(=O)2NHR7, -(C1-С3алкил)-NHC(=O)R7, -(C1-С3алкил)-C(=O)NHR7, -(C1-С3алкил)-NHS(=O)2R7, -(C1-С3алкил)-S(=O)2NHR7; -(C1-С3алкил)-NHC(=O)NHR7, -(C1-С3алкил)-NHS(=O)2NHR7 независимо выбран из C1-С6алкила, C1-С6галогеналкила, C1-С6гетероалкила, замещенного или незамещенного С3-С10циклоалкила, замещенного или незамещенного С2-С10гетероциклоалкила, замещенного или незамещенного арила, замещенного или незамещенного гетероарила, -С1-С6алкил-(замещенный или незамещенный С3-С10циклоалкил), -C1-С6алкил-(замещенный или незамещенный С2-С10гетероциклоалкил), -С1-С6алкил-(замещенный или незамещенный арил), -С1-С6алкил-(замещенный или незамещенный гетероарил), -(СН2)р-СН(замещенный или незамещенный арил)2, -(СН2)р-СН(замещенный или незамещенный гетероарил)2, -(СН2)Р-СН(замещенный или незамещенный арил)(замещенный или незамещенный гетероарил), -(замещенный или незамещенный арил)-(замещенный или незамещенный арил), -(замещенный или незамещенный арил)-(замещенный или незамещенный гетероарил), -(замещенный или незамещенный гетероарил)-(замещенный или незамещенный арил) или -(замещенный или незамещенный гетероарил)-(замещенный или незамещенный гетероарил);
р в R7 равняется 0, 1 или 2;
R8a, R8b, R8c и R8d в C(R8a)(R8b) и C(R8c)(R8d) независимо выбраны из Н, C1-С6алкила, C1-С6фторалкила, C1-С6алкокси, C1-С6гетероалкила и замещенного или незамещенного арила;
или
R8a и R8d определены выше, и R8b и R8c вместе образуют связь;
или
R8a и R8d определены выше, и R8b и R8c вместе с атомами, к которым они присоединены, образуют замещенное или незамещенное конденсированное 5-7-членное насыщенное или частично насыщенное карбоциклическое кольцо или гетероциклическое кольцо, содержащее 1-3 гетероатома, выбранные из S, О и N, замещенное или незамещенное конденсированное 5-10-членное арильное кольцо или замещенное или незамещенное конденсированное 5-10-членное гетероарильное кольцо, содержащее 1-3 гетероатома, выбранные из S, О и N;
или
R8c и R8d определены выше, и R8a и R8b вместе с атомами, к которым они присоединены, образуют замещенный или незамещенный насыщенный или частично насыщенный 3-7-членный спироцикл или гетероспироцикл, содержащий 1-3 гетероатома, выбранные из S, О и N;
или
R8a и R8b определены выше, и R8c и R8d вместе с атомами, к которым они присоединены, образуют замещенный или незамещенный насыщенный или частично насыщенный 3-7-членный спироцикл или гетероспироцикл, содержащий 1-3 гетероатома, выбранные из S, О и N;
где каждый замещенный алкил, гетероалкил, конденсированное кольцо, спироцикл, гетероспироцикл, циклоалкил, гетероциклоалкил, арил или гетероарил замещен 1-3 R9; и
каждый R9 в R8a, R8b, R8c и R8d независимо выбран из галогена, -ОН, -SH, (С=O), CN, С1-С4алкила, С1-С4фторалкила, С1-С4алкокси, С1-С4фторалкокси, -NH2, -NH(C1-С4алкил), -NH(С1-С4алкил)2, -С(=O)ОН, -C(=0)NH2, -С(=O)С1-С3алкила, -S(=O)2CH3, -NH(C1-С4алкил)-OH, -NH(С1-С4алкил)-O-(С-С4алкил), -O(C1-С4алкил)-NH2; -O(C1-С4алкил)-NH-(С1-С4алкил) и -O(С1-С4алкил)-N-(С1-С4алкил)2, или два R9 вместе с атомами, к которым они присоединены, образуют метилендиокси- или этилендиокси-кольцо, замещенное или незамещенное галогеном, -ОН или C1-С3алкилом.
[132] В любом из соединений, описанных в данном документе, ILM может характеризоваться структурой формулы (XLIV), которая получена из структуры лигандов IAP, описанных в публ. WO №2013/071039, или соответствующим ей неприродным миметиком,

где
W1 в формуле (XLIV) выбран из О, S, N-RA или C(R8a)(R8b);
W2 в формуле (XLIV) выбран из О, S, N-RA или C(R8c)(R8d); при условии, что W1 и W2 одновременно не представляют собой О или одновременно не представляют собой S;
W3 в формуле (XLIV) выбран из О, S, N-RA или C(R8e)(R8f), при условии, что кольцо, содержащее W1, W2 и W3, не содержит двух смежных атомов кислорода или атомов серы;
R1 в формуле (XLIV) выбран из Н, C1-С6алкила, С3-С6циклоалкила, -C1-С6алкил-(замещенный или незамещенный С3-С6циклоалкил), замещенного или незамещенного арила, замещенного или незамещенного гетероарила, -C1-С6алкил-(замещенный или незамещенный арил) или -С1-С6алкил-(замещенный или незамещенный гетероарил);
если X1 в формуле (XLIV) представляет собой О, то X2 в формуле (XLIV) выбран из CR2cR2d и N-RA, и X3 в формуле (XLIV) представляет собой CR2aR2b;
или
если X1 в формуле (XLIV) представляет собой CH2, то X2 в формуле (XLIV) выбран из О, N-RA, S, S(O) или S(O)2, и X3 в формуле (XLIV) представляет собой CR2aR2b.
или
если X1 в формуле (XLIV) представляет собой CR2eR2f, то и X2 в формуле (XLIV) представляет собой CR2cR2d, и R2e и R2c вместе образуют связь, и X3 в формуле (VLIV) представляет собой CR2aR2b;
или
X1 и X3 в формуле (XLIV) одновременно представляет собой CH2, и X2 в формуле (XLII) представляет собой С=0, C=C(RC)2 или C=NRC; где каждый RC независимо выбран из Н, -CN, -ОН, алкокси, замещенного или незамещенного C1-С6алкила, замещенного или незамещенного С3-С6циклоалкила, замещенного или незамещенного С2-С5гетероциклоалкила, замещенного или незамещенного арила, замещенного или незамещенного гетероарила, -С1-С6алкил-(замещенный или незамещенный С3-С6циклоалкил), -С1-С6алкил-(замещенный или незамещенный С2-С5гетероциклоалкил), -С1-С6алкил-(замещенный или незамещенный арил), или -C1-С6алкил-(замещенный или незамещенный гетероарил);
или
X1 и X2 в формуле (XLIV) независимо выбраны из С и N и являются членами конденсированного замещенного или незамещенного насыщенного или частично насыщенного 3-10-членного циклоалкильного кольца, конденсированного замещенного или незамещенного насыщенного или частично насыщенного 3-10-членного гетероциклоалкильного кольца, конденсированного замещенного или незамещенного 5-10-членного арильного кольца или конденсированного замещенного или незамещенного 5-10-членного гетероарильного кольца, и X3 в формуле (XLIV) представляет собой CR2aR2b;
или
X2 и X3 в формуле (XLIV) независимо выбраны из С и N и являются членами конденсированного замещенного или незамещенного насыщенного или частично насыщенного 3-10-членного циклоалкильного кольца, конденсированного замещенного или незамещенного насыщенного или частично насыщенного 3-10-членного гетероциклоалкильного кольца, конденсированного замещенного или незамещенного 5-10-членного арильного кольца или конденсированного замещенного или незамещенного 5-10-членного гетероарильного кольца, и X1 в формуле (VLIV) представляет собой CR2eR2f;
RA в N-RA выбран из Н, C1-С6алкила, -С(=O)С1-С2алкила, замещенного или незамещенного арила или замещенного или незамещенного гетероарила;
R2a, R2b, R2c, R2d, R2e и R2f в CR2cR2d, CR2aR2b и CR2eR2f независимо выбраны из H, замещенного или незамещенного C1-С6алкила, замещенного или незамещенного C1-С6гетероалкила, замещенного или незамещенного С3-С6циклоалкила, замещенного или незамещенного С2-С5гетероциклоалкила, замещенного или незамещенного арила, замещенного или незамещенного гетероарила, -С1-С6алкил-(замещенный или незамещенный С3-С6циклоалкил), -С1-С6алкил-(замещенный или незамещенный С2-С5 гетероциклоалкил), -С1-С6алкил-(замещенный или незамещенный арил), -C1-С6алкил-(замещенный или незамещенный гетероарил) и -C(=O)RB;
RB в -C(=O)RB выбран из замещенного или незамещенного C1-С6алкила, замещенного или незамещенного С3-С6циклоалкила, замещенного или незамещенного С2-С5гетероциклоалкила, замещенного или незамещенного арила, замещенного или незамещенного гетероарила, -С1-С6алкил-(замещенный или незамещенный С3-С6циклоалкил), -С1-С6алкил-(замещенный или незамещенный С2-С5гетероциклоалкил), -С1-С6алкил-(замещенный или незамещенный арил), -C1-С6алкил-(замещенный или незамещенный гетероарил) или -NRDRE;
RD и RE в NRDRE независимо выбраны из Н, замещенного или незамещенного C1-С6алкила, замещенного или незамещенного С3-С6циклоалкила, замещенного или незамещенного С2-С5гетероциклоалкила, замещенного или незамещенного арила, замещенного или незамещенного гетероарила, -С1-С6алкил-(замещенный или незамещенный С3-С6циклоалкил), -С1-С6алкил-(замещенный или незамещенный С2-С5 гетероциклоалкил), -С1-С6алкил-(замещенный или незамещенный арил) или -C1-С6алкил-(замещенный или незамещенный гетероарил);
m в формуле (XLIV) выбран из 0, 1 или 2;
-U- в формуле (XLIV) выбран из -NHC(=O)-, -C(=O)NH-, -NHS(=O)2-, -S(=O)2NH-, -NHC(=O)NH-, -NH(C=O)O-, -O(C=O)NH- или -NHS(=O)2NH-;
R3 в формуле (XLIV) выбран из C1-С3алкила или C1-С3фторалкила;
R4 в формуле (XLIV) выбран из -NHR5, -N(R5)2, -N+(R5)3 или -OR5;
каждый R5 в -NHR5, -N(R5)2, -N+(R5)3 и -OR5 независимо выбран из Н, C1-С3алкила, C1-С3галогеналкила, C1-С3гетероалкила и -С1-С3алкил-(С3-С5циклоалкил);
или
R3 и R5 в формуле (XLIV) вместе с атомами, к которым они присоединены, образуют замещенное или незамещенное 5-7-членное кольцо;
или
R3 в формуле (XLIII) связан с атомом азота в U с образованием замещенного или незамещенного 5-7-членного кольца;
R6 в формуле (XLIII) выбран из -NHC(=O)R7, -C(=O)NHR7, -NHS(=O)2R7, -S(=O)2NHR7; -NHC(=O)NHR7, -NHS(=O)2NHR7, -(C1-С3алкил)-NHC(=O)R7, -(C1-С3алкил)-C(=O)NHR7, -(C1-С3алкил)-NHS(=O)2R7, -(C1-С3алкил)-S(=O)2NHR7; -(C1-С3алкил)-NHC(=O)NHR7, -(C1-С3алкил)-NHS(=O)2NHR7, замещенного или незамещенного С2-С10гетероциклоалкила или замещенного или незамещенного гетероарила;
каждый R7 в -NHC(=O)R7, -C(=O)NHR7, -NHS(=O)2R7, -S(=O)2NHR7; -NHC(=O)NHR7, -NHS(=O)2NHR7, -(C1-С3алкил)-NHC(=O)R7, -(C1-С3алкил)-C(=O)NHR7, -(C1-С3алкил)-NHS(=O)2R7, -(C1-С3алкил)-S(=O)2NHR7; -(C1-С3алкил)-NHC(=O)NHR7, -(C1-С3алкил)-NHS(=O)2NHR7 независимо выбран из C1-С6алкила, C1-С6галогеналкила, C1-С6гетероалкила, замещенного или незамещенного С3-С10циклоалкила, замещенного или незамещенного С2-С10гетероциклоалкила, замещенного или незамещенного арила, замещенного или незамещенного гетероарила, -С1-С6алкил-(замещенный или незамещенный С3-С10циклоалкил), -C1-С6алкил-(замещенный или незамещенный С2-С10гетероциклоалкил), -С1-С6алкил-(замещенный или незамещенный арил), -С1-С6алкил-(замещенный или незамещенный гетероарил), -(СН2)р-СН(замещенный или незамещенный арил)2, -(СН2)p-СН(замещенный или незамещенный гетероарил)2, -(СН2)P-СН(замещенный или незамещенный арил)(замещенный или незамещенный гетероарил), -(замещенный или незамещенный арил)-(замещенный или незамещенный арил), -(замещенный или незамещенный арил)-(замещенный или незамещенный гетероарил), -(замещенный или незамещенный гетероарил)-(замещенный или незамещенный арил) или -(замещенный или незамещенный гетероарил)-(замещенный или незамещенный гетероарил);
р в R7 выбран из 0, 1 или 2;
R8a, R8b, R8c, R8d, R8e и R8f в C(R8a)(R8b), C(R8c)(R8d) и C(R8e)(R8f) независимо выбраны из H, C1-С6алкила, C1-С6фторалкила, C1-С6алкокси, C1-С6гетероалкила и замещенного или незамещенного арила;
или
R8a, R8d, R8e и R8f в C(R8a)(R8b), C(R8c)(R8d) и C(R8e)(R8f) определены выше, и R8b и R8c вместе образуют связь;
или
R8a, R8b, R8d и R8f в C(R8a)(R8b), C(R8c)(R8d) и C(R8e)(R8f) определены выше, и R8c и R8e вместе образуют связь;
или
R8a, R8d, R8e и R8f в C(R8a)(R8b), C(R8c)(R8d) и C(R8e)(R8f) определены выше, и R8b и R8c вместе с атомами, к которым они присоединены, образуют замещенное или незамещенное конденсированное 5-7-членное насыщенное или частично насыщенное карбоциклическое кольцо или гетероциклическое кольцо, содержащее 1-3 гетероатома, выбранные из S, О и N, замещенное или незамещенное конденсированное 5-10-членное арильное кольцо или замещенное или незамещенное конденсированное 5-10-членное гетероарильное кольцо, содержащее от 1 до 3 гетероатомов, выбранных из S, О и N;
или
R8a, R8b, R8d и R8f в C(R8a)(R8b), C(R8c)(R8d) и C(R8e)(R8f) определены выше, и R8c и R8e вместе с атомами, к которым они присоединены, образуют замещенное или незамещенное конденсированное 5-7-членное насыщенное или частично насыщенное карбоциклическое кольцо или гетероциклическое кольцо, содержащее 1-3 гетероатома, выбранные из S, О и N, замещенное или незамещенное конденсированное 5-10-членное арильное кольцо или замещенное или незамещенное конденсированное 5-10-членное гетероарильное кольцо, содержащее от 1 до 3 гетероатомов, выбранных из S, О и N;
или
R8c, R8d, R8e и R8f в C(R8c)(R8d) и C(R8e)(R8f) определены выше, и R8a и R8b вместе с атомами, к которым они присоединены, образуют замещенный или незамещенный насыщенный или частично насыщенный 3-7-членный спироцикл или гетероспироцикл, содержащий от 1 до 3 гетероатомов, выбранных из S, О и N;
или
R8a, R8b, R8e и R8f в C(R8a)(R8b) и C(R8e)(R8f) определены выше, и R8c и R8d вместе с атомами, к которым они присоединены, образуют замещенный или незамещенный насыщенный или частично насыщенный 3-7-членный спироцикл или гетероспироцикл, содержащий от 1 до 3 гетероатомов, выбранных из S, О и N;
или
R8a, R8b, R8c и R8d в C(R8a)(R8b) и C(R8c)(R8d) определены выше, и R8e и R8f вместе с атомами, к которым они присоединены, образуют замещенный или незамещенный насыщенный или частично насыщенный 3-7-членный спироцикл или гетероспироцикл, содержащий от 1 до 3 гетероатомов, выбранных из S, О и N;
или
где каждый замещенный алкил, гетероалкил, конденсированное кольцо, спироцикл, гетероспироцикл, циклоалкил, гетероциклоалкил, арил или гетероарил замещен 1-3 R9; и
каждый R9 в R8a, R8b, R8c, R8d, R8e и R8f независимо выбран из галогена, -ОН, -SH, (С=O), CN, С1-С4алкила, С1-С4фторалкила, С1-С4алкокси, С1-С4фторалкокси, -NH2, -NH(C1-С4алкил), -NH(C1-С4алкил)2, -С(=O)ОН, -C(=0)NH2, -С(=O)С1-С3алкила, -S(=O)2CH3, -NH(С1-С4алкил)-ОН, -NH(С1-С4алкил)-O-(С-С4алкил), -O(С1-С4алкил)-NH2; -O(С1-С4алкил)-NH-(С1-С4алкил) и -O(С1-С4алкил)-N-(С1-С4алкил)2, или два R9 вместе с атомами, к которым они присоединены, образуют метилендиокси- или этилендиокси-кольцо замещенное или незамещенное галогеном, -ОН или C1-С3алкилом.
[133] В любом из соединений, описанных в данном документе, ILM может характеризоваться структурой формулы (XLV), (XLVI) или (XLVII), которая получена из структуры лигандов IAP, описанных in Vamos, М., et al., Expedient synthesis of highly potent antagonists of inhibitor of apoptosis proteins (IAPs) with unique selectivity for ML-IAP, ACS Chem. Biol., 8(4), 725-32 (2013), или соответствующим ей неприродным миметиком,
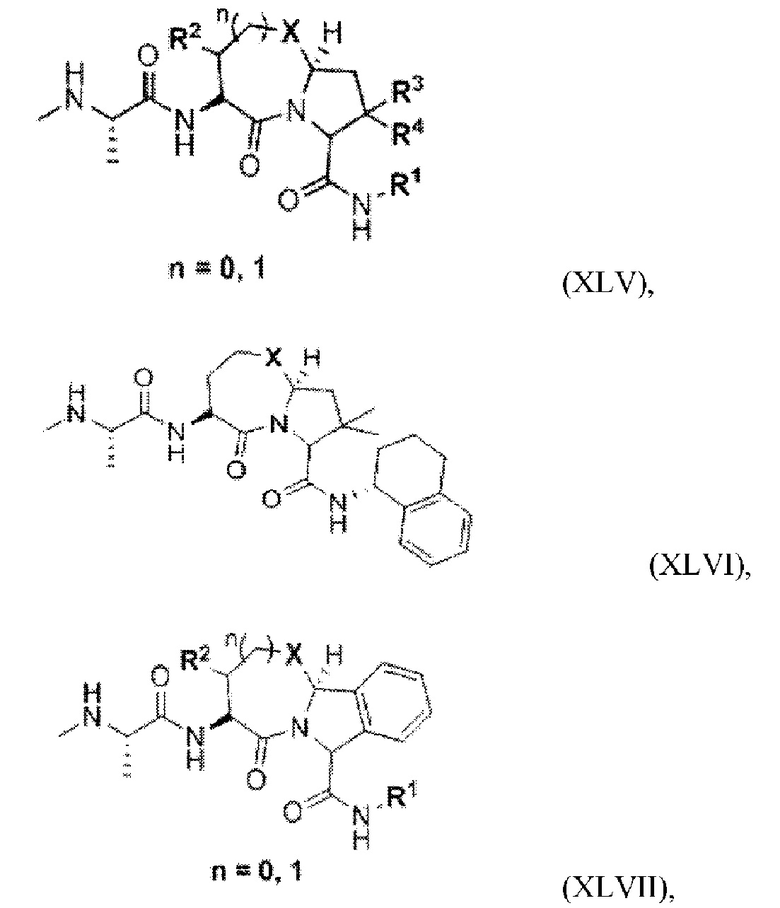
где
R2, R3 и R4 в формуле (XLV) независимо выбраны из Н или Me;
X в формуле (XLV) независимо выбран из О или S; и
R1 в формуле (XLV) выбран из

[134] В конкретном варианте осуществления ILM характеризуется структурой в соответствии с формулой (XLVIII),

где R3 и R4 в формуле (XLVIII) независимо выбраны из Н или ME;
 представляет собой 5-членный гетероцикл, выбранный из
представляет собой 5-членный гетероцикл, выбранный из
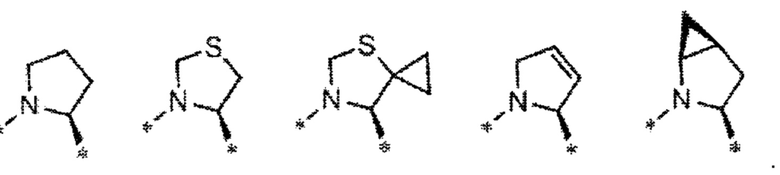
[135] В конкретном варианте осуществления  в формуле (XLVIII) представляет собой
в формуле (XLVIII) представляет собой 
[136] В конкретном варианте осуществления ILM характеризуется структурой и присоединен к линкерной группе L, как показано ниже

[137] В конкретном варианте осуществления ILM характеризуется структурой в соответствии с формулой (XLIX), (L) или (LI),

где
R3 в формуле (XLIX), (L) или (LI) независимо выбран из Н или ME;
 представляет собой 5-членный гетероцикл, выбранный из
представляет собой 5-членный гетероцикл, выбранный из
 и
и
L в формуле (XLIX), (L) или (LI) выбран из

[138] В конкретном варианте осуществления L в формуле (XLIX), (L) или (LI) представляет собой

[139] В конкретном варианте осуществления ILM характеризуется структурой в соответствии с формулой (LII),

[140] В конкретном варианте осуществления ILM в соответствии с формулой (LII) химически соединен с линкерной группой L в области, обозначенной  и как показано ниже.
и как показано ниже.
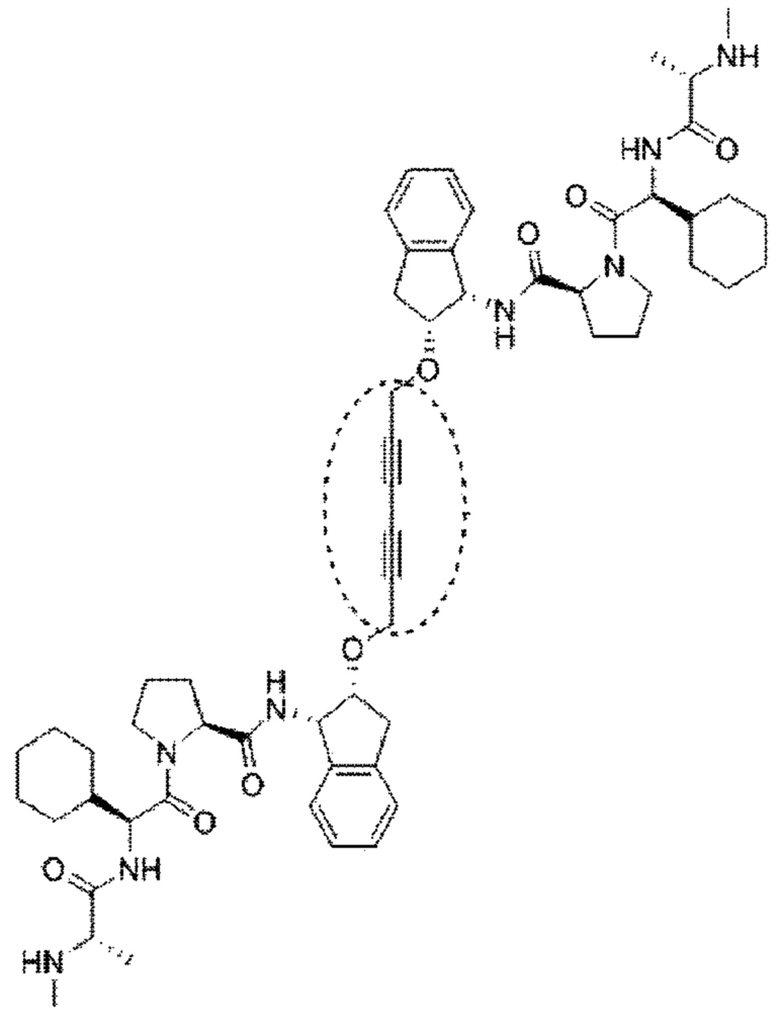
[141] В любом из соединений, описанных в данном документе, ILM может характеризоваться структурой формулы (LIII) или (LIV), которая основана на структуре лигандов IAP, описанных в Hennessy, EJ, et al., Discovery of aminopiperidine-based Smac mimetics as IAP antagonists, Bioorg. Med. Chem. Lett., 22(4), 1960-4 (2012), или соответствующим ей неприродным миметиком,

где
R1 в формулах (LIII) и (LIV) выбран из

R2 в формулах (LIII) и (LIV) выбран из Н или Me;
R3 в формулах (LIII) и (LIV) выбран из

X выбран из Н, галогена, метила, метокси, гидрокси, нитро или трифторметила.
[142] В любом из соединений, описанных в данном документе, ILM может характеризоваться структурой и быть химически соединенным с линкером, как показано в формуле (LV) или (LVI), или соответствующим ей неприродным миметиком,

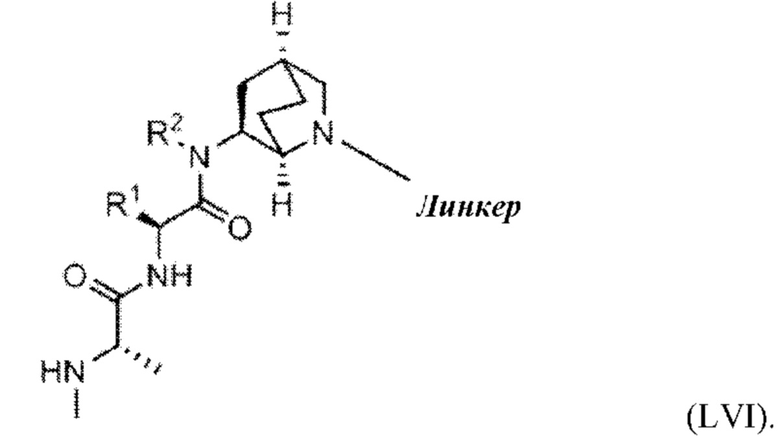
[143] В любом из соединений, описанных в данном документе, ILM может характеризоваться структурой формулы (LVII), которая основана на структуре лигандов IAP, описанных в Cohen, F, et al., Orally bioavailable antagonists of inhibitor of apoptosis proteins based on an azabicyclooctane scaffold, J. Med. Chem., 52(6), 1723-30 (2009), или соответствующим ей неприродным миметиком,
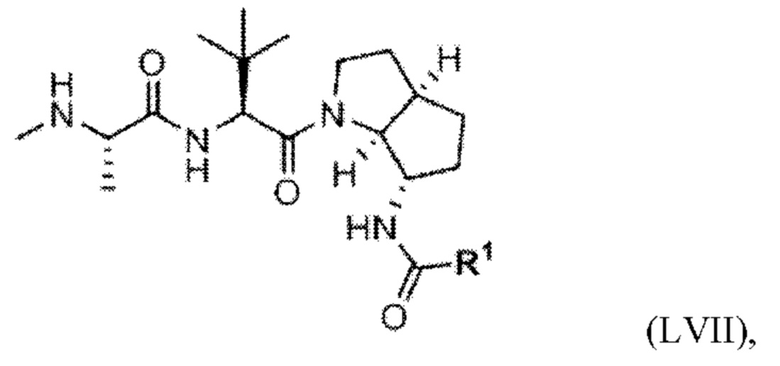
где
R1 в формуле (LVII) выбран из

X в 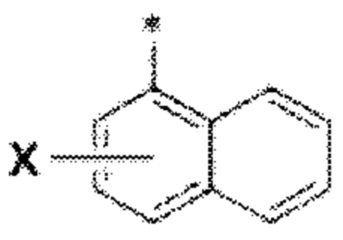 выбран из Н, фтора, метила или метокси.
выбран из Н, фтора, метила или метокси.
[144] В конкретном варианте осуществления ILM представлен следующей структурой:

[145] В конкретном варианте осуществления ILM выбран из группы, состоящей из следующего, и при этом показана химическая связь между ILM и линкерной группой L,

[146] В любом из соединений, описанных в данном документе, ILM выбран из группы, состоящей из представленных ниже структур, которые основаны на структуре лигандов IAP, описанных в Asano, М, et al., Design, sterioselective synthesis, and biological evaluation of novel tri-cyclic compounds as inhibitor of apoptosis proteins (IAP) antagonists, Bioorg. Med. Chem., 21(18): 5725-37 (2013), или соответствующих им неприродных миметиков,

[147] В конкретном варианте осуществления ILM выбран из группы, состоящей из следующего, и при этом показана химическая связь между ILM и линкерной группой L,

[148] В любом из соединений, описанных в данном документе, ILM может характеризоваться структурой формулы (LVIII), которая основана на структуре лигандов IAP, описанных в Asano, М, et al., Design, sterioselective synthesis, and biological evaluation of novel tri-cyclic compounds as inhibitor of apoptosis proteins (IAP) antagonists, Bioorg. Med. Chem., 21(18): 5725-37 (2013), или соответствующим ей неприродным миметиком,

где X в формуле (LVIII) представляет собой один или два заместителя, независимо выбранных из Н, галогена или циано.
[149] В любом из соединений, описанных в данном документе, ILM может характеризоваться структурой и быть химически соединенным с линкерной группой L, как показано в формуле (LIX) или (LX), или соответствующим ей неприродным миметиком,

где X в формуле (LIX) и (LX) представляет собой один или два заместителя, независимо выбранные из Н, галогена или циано, и; и L в формулах (LIX) и (LX) представляет собой линкерную группу, описанную в данном документе.
[150] В любом из соединений, описанных в данном документе, ILM может характеризоваться структурой формулы (LXI), которая основана на структуре лигандов IAP, описанных в Ardecky, RJ, et al., Design, sysnthesis and evaluation of inhibitor of apoptosis (IAP) antagonists that are highly selective for the BIR2 domain of XIAP, Bioorg. Med. Chem., 23(14): 4253-7 (2013), или соответствующим ей неприродным миметиком,

где
 в формуле (LXI) представляет собой природную или неприродную аминокислоту; и
в формуле (LXI) представляет собой природную или неприродную аминокислоту; и
R2 в формуле (LXI) выбран из 
[151] В любом из соединений, описанных в данном документе, ILM может характеризоваться структурой и быть химически соединенным с линкерной группой L, как показано в формуле (LXII) или (LLXIII), или соответствующим ей неприродным миметиком,


 в формуле (LXI) представляет собой природную или неприродную аминокислоту; и
в формуле (LXI) представляет собой природную или неприродную аминокислоту; и
L в формуле (LXI) представляет собой линкерную группу, описанную в данном документе.
[152] В любом из соединений, описанных в данном документе, ILM может характеризоваться структурой, выбранной из группы, состоящей из следующего, которая основана на структуре лигандов IAP, описанных в Wang, J, et al., Discovery of novel second mitochondrial-derived activator of caspase mimetics as selective inhibitor or apoptosis protein inhibitors, J. Pharmacol. Exp. Ther., 349(2): 319-29 (2014), или соответствующим ей неприродным миметиком,

[153] В любом из соединений, описанных в данном документе, ILM характеризуется структурой в соответствии с формулой (LXIX), которая основана на структуре лигандов IAP, описанных в Hird, AW, et al., Structure-based design and synthesis of tricyclic IAP (Inhibitors of Apoptosis Proteins) inhibitors, Bioorg. Med. Chem. Lett., 24(7): 1820-4 (2014), или соответствующим ей неприродным миметиком,
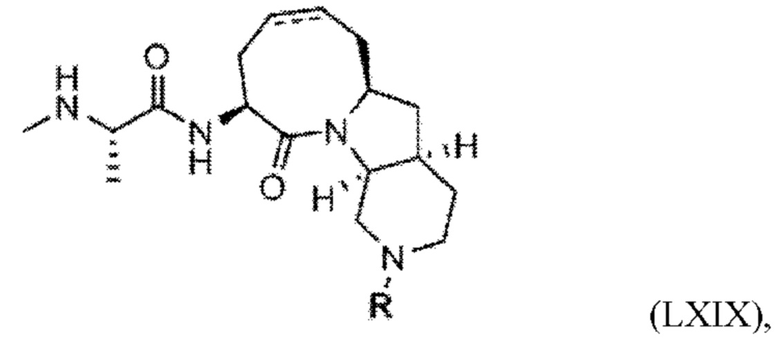
где R в формуле LIX выбран из группы, состоящей из
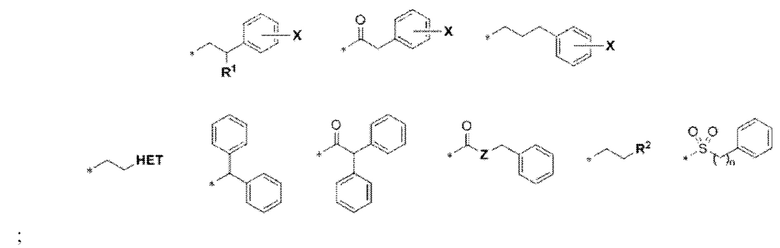
R1 в 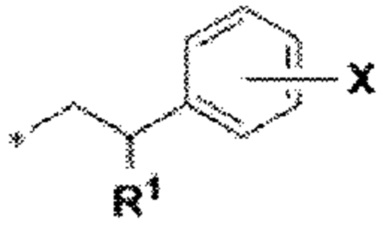 выбран из Н или Me;
выбран из Н или Me;

R2 в выбран из алкила или циклоалкила;
X в 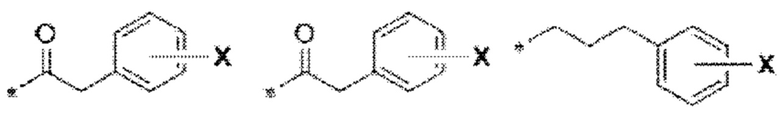 представляет собой 1-2 заместителя, независимо выбранные из галогена, гидрокси, метокси, нитро и трифторметила;
представляет собой 1-2 заместителя, независимо выбранные из галогена, гидрокси, метокси, нитро и трифторметила;
Z в 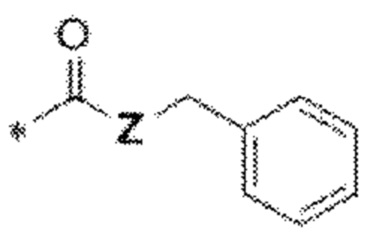 представляет собой О или NH;
представляет собой О или NH;
НЕТ в  представляет собой моно- или конденсированный бициклический гетероарил; и
представляет собой моно- или конденсированный бициклический гетероарил; и
 в формуле (LIX) представляет собой необязательную двойную связь.
в формуле (LIX) представляет собой необязательную двойную связь.
[154] В конкретном варианте осуществления ILM в соединении характеризуется химической структурой, представленной

[155] В конкретном варианте осуществления ILM в соединении характеризуется химической структурой, выбранной из группы, состоящей из
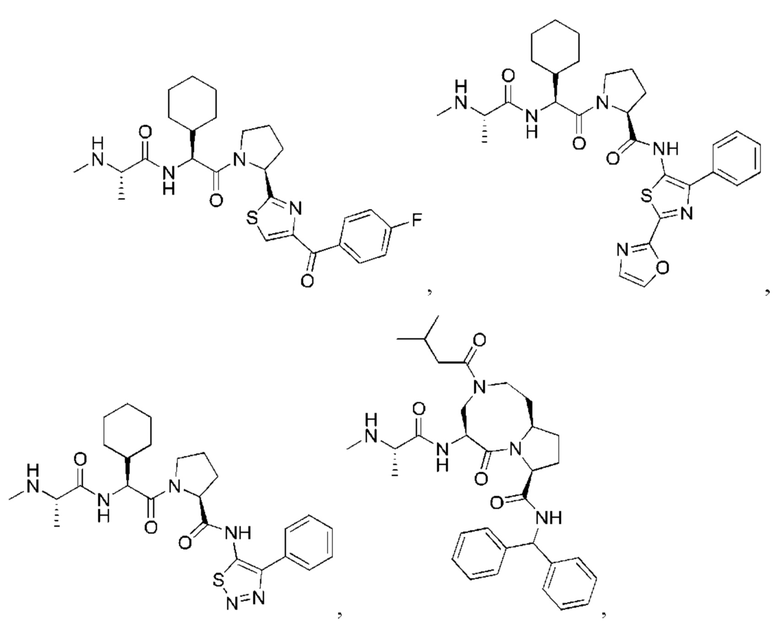
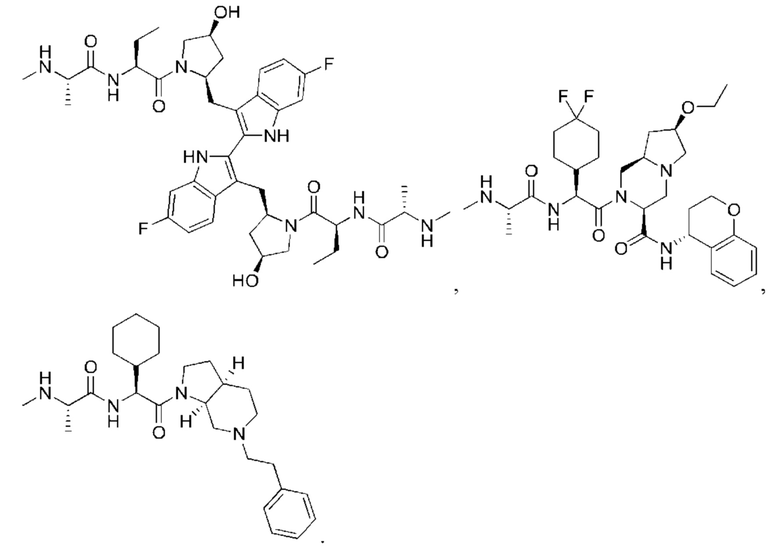
[156] Термин «независимо» используется в данном документе для указания того, что переменная, которая применяется независимо, варьируется независимо от применения к применению.
[157] Под термином «алкил» в его соответствующем контексте следует понимать линейный, разветвленный или циклический полностью насыщенный углеводородный радикал или алкильную группу, предпочтительно C1-С10, более предпочтительно C1-С6, в качестве альтернативы C1-С3алкильную группу, которая может быть необязательно замещена. Примеры алкильных групп представляют собой, среди прочих, метил, этил, н-бутил, втор-бутил, н-гексил, н-гептил, н-октил, н-нонил, н-децил, изопропил, 2-метилпропил, циклопропил, циклопропилметил, пиклобутил, циклопентил, циклопентилэтил, пиклогексилэтил и циклогексил. В определенных вариантах осуществления алкильная группа имеет на конце галогенсодержащую группу (At, Br, Cl, F или I). В некоторых предпочтительных вариантах осуществления соединения в соответствии с настоящим изобретении могут применяться для ковалентного связывания с ферментами дегалогеназами. Данные соединения, как правило, содержат боковую цепь (зачастую соединенную с помощью полиэтиленгликолевой группы), которая заканчивается алкильной группой, которая содержит заместитель, представляющий собой атом галогена (зачастую хлор или бром), на своем дальнем конце, которая обеспечивает ковалентное связывание соединения, содержащего такой фрагмент, с белком.
[158] Термин «алкенил» относится к линейным, разветвленным или циклическим углеводородным радикалам С2-С10 (предпочтительно С2-С6), содержащим по меньшей мере одну связь С=С.
[159] Термин «алкинил» относится к линейным, разветвленным или циклическим углеводородным радикалам С2-С10 (предпочтительно С2-С6), содержащим по меньшей мере одну связь С≡С.
[160] Термин «алкилен», если применяется, относится к группе -(СН2)n- (n представляет собой целое число, как правило, 0-6), которая может быть необязательно замещена. Если группа замещена, то алкиленовая группа предпочтительно замещена по одной или более метиленовым группам C1-С6алкильной группой (в том числе циклопропильной группой или трет-бутильной группой), но также может быть замещена одной или более галогенсодержащими группами, предпочтительно 1-3 галогенсодержащими группами, или одной или двумя гидроксильными группами, группами O-(С1-С6алкил) или аминокислотными боковыми цепями, как далее раскрыто в данном документе. В определенных вариантах осуществления алкиленовая группа может быть замещена уретаном или алкоксигруппой (или другой группой), которая дополнительно замещена полиэтиленгликолевой цепью (от 1 до 10, предпочтительно от 1 до 6, зачастую от 1 до 4 этиленгликолевых звеньев), которая замещена (предпочтительно, но не исключительно на дальнем конце полиэтиленгликолевой цепи) алкильной цепью, замещенной одной галогенсодержащей группой, предпочтительно хлорсодержащей группой. В других дополнительных вариантах осуществления алкиленовая (зачастую, метиленовая) группа может быть замещена группой в виде аминокислотной боковой цепи, такой как группа в виде боковой цепи, представляющей собой природную или неприродную аминокислоту, например, аланин, β-аланин, аргинин, аспарагин, аспарагиновая кислота, пистеин, цистин, глутаминовая кислота, глутамин, глицин, фенилаланин, гистидин, изолейцин, лизин, лейцин, метионин, пролин, серии, треонин, валин, триптофан или тирозин.
[161] Под термином «незамещенный» следует понимать замещенный только атомами водорода. Диапазон атомов углерода, который включает С0, означает, что углерод отсутствует и заменен на Н. Таким образом, диапазон атомов углерода, который представляет собой С0-С6, предусматривает 1, 2, 3, 4, 5 и 6 атомов углерода, а в случае С0 вместо углерода находится Н.
[162] Термин «замещенный» или «необязательно замещенный» будет означать независимо (т.е. если встречается более одного заместителя, каждый заместитель является независимым относительно другого заместителя) один или более заместителей (независимо не более пяти заместителей, предпочтительно не более трех заместителей, зачастую 1 или 2 заместителя на фрагменте в соединении в соответствии с настоящим изобретением и может включать заместители, которые сами могут быть дополнительно замещены) в положении атома углерода (или азота) в любом месте в молекуле в соответствующем контексте, и под заместителями подразумеваются гидроксил, тиол, карбоксил, циано (C≡N), нитро (NO2), галоген (предпочтительно 1, 2 или 3 атома галогена, особенно на алкиле, особенно в метальной группе, как, например, трифторметил), алкильная группа (предпочтительно C1-С10, более предпочтительно C1-С6), арил (особенно фенил и замещенный фенил, например, бензил или бензоил), алкоксигруппа (предпочтительно C1-С6алкил или арил, в том числе фенил и замещенный фенил), простой тиоэфир (C1-С6алкил или арил), ацил (предпочтительно C1-С6ацил), сложный эфир или сложный тиоэфир (предпочтительно C1-С6алкил или арил), в том числе сложный алкиленовый эфир (так, что присоединение происходит по алкиленовой группе, а не по сложноэфирной функциональной группе, которая предпочтительно замещена C1-С6алкильной или арильной группой), предпочтительно C1-С6алкил или арил, галоген (предпочтительно F или Cl), амин (в том числе пяти- или шестичленный циклический алкиленамин, в том числе дополнительно C1-С6алкиламин или C1-С6диалкиламин, при этом алкильные группы могут быть замещены одной или двумя гидроксильными группами) или необязательно замещенная группа -N(С0-С6алкил)С(O)(O-С1-С6алкил) (которая может быть необязательно замещена полиэтиленгликолевой цепью, к которой дополнительно присоединена алкильная группа, содержащая один атом галогена, предпочтительно заместитель, представляющий собой атом хлора), гидразин, амидо, предпочтительно замещенный одной или двумя C1-С6алкильными группами (в том числе карбоксамид, который необязательно замещен одной или двумя C1-С6алкильными группами), алканол (предпочтительно C1-С6алкил или арил) или алкановая кислота (предпочтительно C1-С6алкил или арил). Заместители в соответствии с настоящим изобретением могут включать, например, группы -SiR1R2R3, где каждый из R1 и R2 описан далее в данном документе, и R3 представляет собой Н или C1-С6алкильную группу, предпочтительно R1, R2, R3 в данном контексте представляют собой C1-С3алкильную группу (в том числе изопропиловую или трет-бутиловую группу). Каждая из вышеописанных групп может быть непосредственно связана с замещенным фрагментом, или альтернативно заместитель может быть соединен с замещенным фрагментом (предпочтительно в случае арильного или гетероарильного фрагмента) посредством необязательно замещенной группы -(СН2)m- или альтернативно необязательно замещенных групп -(ОСН2)m-, -(ОСН2СН2)m- или -(CH2CH2O)m-, которые могут быть замещены любым одним или более из вышеописанных заместителей. Алкиленовые группы -(СН2)m-, или группы -(СН2)n-, или другие цепи, такие как этиленгликолевые цепи, определенные выше, могут быть замещены в любом месте на цепи. Предпочтительные заместители на алкиленовых группах включают галоген или C1-С6алкильные (предпочтительно C1-С3) группы, которые могут быть необязательно замещены одной или двумя гидроксильными группами, одной или двумя эфирными группами (группами O-C1-С6), не более чем тремя галогенсодержащими группами (предпочтительно F), или боковую цепь в виде аминокислоты, как далее описано в данном документе, и необязательно замещенный амид (предпочтительно карбоксамид, замещенный, как описано выше) или уретановые группы (зачастую с одним или двумя заместителями, представляющими собой С0-С6алкил, при этом группа(-ы) может(-гут) быть дополнительно замещена(-ы)). В определенных вариантах осуществления алкиленовая группа (зачастую одна метиленовая группа) замещена одной или двумя необязательно замещенными C1-С6алкильными группами, предпочтительно C1-С4алкильной группой, чаще всего метильной или О-метильной группами или боковой цепью аминокислоты, как далее описано в данном документе. В настоящем изобретении фрагмент в молекуле может быть необязательно замещен не более чем пятью заместителями, предпочтительно не более чем тремя заместителями. Чаще всего в настоящем изобретении фрагменты, которые являются замещенными, замещены одним или двумя заместителями.
[163] Под термином «замещенный» (каждый заместитель является независимым от любого другого заместителя) в контексте его применения также следует понимать C1-С6алкил, C1-С6алкокси, галоген, амидо, карбоксамидо, сульфон, в том числе сульфонамид, кето, карбокси, сложный C1-С6эфир (сложный оксиэфир или сложный карбонильный эфир), C1-С6кето, уретан -O-C(O)-NR1R2 или -N(R1)-C(O)-O-R1, нитро, циано и амин (в том числе, в частности, C1-С6алкилен-NR1R2, моно- или дизамещенные C1-С6алкилом амины, которые могут быть необязательно замещены одной или двумя гидроксильными группами). Каждая из данных групп содержит, если не указано иное, в соответствующем контексте от 1 до 6 атомов углерода. В определенных вариантах осуществления предпочтительные заместители будут включать, например, -NH-, -NHC(O)-, -О-, =O, -(CH2)m- (в данном контексте m и n равняются 1, 2, 3, 4, 5 или 6), -S-, -S(O)-, SO2- или -NH-C(O)-NH-, -(СН2)nOH, -(CH2)nSH, -(СН2)nCOOH, C1-С6алкил, -(СН2)nO-(С1-С6алкил), -(CH2)nC(O)-(C1-С6алкил), -(СН2)nOC(O)-(С1-С6алкил), -(СН2)nC(O)O-(С1-С6алкил), -(CH2)nNHC(O)-R1, -(CH2)nC(O)-NR1R2, -(ОСН2)nOH, -(CH2O)nCOOH, C1-С6алкил, -(OCH2)nO-(C1-С6алкил), -(CH2O)nC(O)-(С1-С6алкил), -(OCH2)nNHC(O)-R1, -(CH2O)nC(O)-NR1R2, -S(O)2-RS, -S(O)-RS (RS представляет собой C1-С6алкил или группу -(CH2)m-NR1R2), NO2, CN или галоген (F, Cl, Br, I, предпочтительно F или Cl), в зависимости от контекста применения заместителя. Каждый из R1 и R2 в соответствующем контексте представляет собой Н или C1-С6алкильную группу (которая может быть необязательно замещена одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами, предпочтительно фтором). В химическом контексте определенного соединения и применяемого заместителя под термином «замещенный» также следует понимать необязательно замещенную арильную или гетероарильную группу или необязательно замещенную гетероциклическую группу, описанные далее в данном документе. Алкиленовые группы также могут быть замещены, как далее раскрыто в данном документе, предпочтительно необязательно замещенными C1-С6алкильными группами (метил, этил, или гидроксиметил, или гидроксиэтил являются предпочтительными, обеспечивая таким образом хиральный центр), группой, представляющей собой боковую цепь аминокислоты, как далее описано в данном документе, амидогруппой, как описано выше в данном документе, или уретановой группой, группой O-C(O)-NR1R2, где R1 и R2 являются такими, как описано далее в данном документе, хотя в качестве заместителей также можно применять многочисленные другие группы. Различные необязательно замещенные фрагменты могут быть замещены 3 или более заместителями, предпочтительно не более чем 3 заместителями и предпочтительно 1 или 2 заместителями. Следует отметить, что в случаях, где в соединении в конкретном положении молекулы необходимо замещение (в основном, из-за валентности), но замещение не указано, то данный заместитель толкуют или понимают как Н, если контекст замещения не предполагает иного.
[164] Термин «арил» или «ароматический» в соответствующем контексте относится к замещенному (как далее описано в данном документе) или незамещенному одновалентному ароматическому радикалу, имеющему одно кольцо (например, бензол, фенил, бензил) или конденсированные кольца (например, нафтил, антраценил, фенантренил и т.д.), и он может быть связан с соединением в соответствии с настоящим изобретением в любом доступном устойчивом положении на кольце(-ах), или в ином случае как указано в представленной химической структуре. Другие примеры арильных групп в соответствующем контексте могут включать, среди прочих, гетероциклические ароматические кольцевые системы, «гетероарильные» группы, содержащие один или более атомов азота, кислорода или серы в кольце (моноциклическом), такие как имидазол, фурил, пиррол, фуранил, тиен, тиазол, пиридин, пиримидин, пиразин, триазол, оксазол, или конденсированные кольцевые системы, такие как индол, хинолин, индолизин, азаиндолизин, бензофуразан и т.д., которые могут быть необязательно замещены, как описано выше. В число гетероарильных групп, которые могут быть упомянуты, включены, среди прочих, азотсодержащие гетероарильные группы, такие как пиррол, пиридин, пиридон, пиридазин, пиримидин, пиразин, пиразол, имидазол, триазол, триазин, тетразол, индол, изоиндол, индолизин, азаиндолизин, пурин, индазол, хинолин, дигидрохинолин, тетрагидрохинолин, изохинолин, дигидроизохинолин, тетрагидроизохинолин, хинолизин, фталазин, нафтиридин, хиноксалин, хиназолин, циннолин, птеридин, имидазопиридин, имидазотриазин, пиразинопиридазин, акридин, фенантридин, карбазол, карбазолин, пиримидин, фенантролин, фенацен, оксадиазол, бензимидазол, пирролопиридин, пирролопиримидин и пиридопиримидин; серосодержащие ароматические гетероциклы, такие как тиофен и бензотиофен; кислородсодержащие ароматические гетероциклы, такие как фуран, пиран, циклопентапиран, бензофуран и изобензофуран; а также ароматические гетероциклы, содержащие 2 или более гетероатомов, выбранных из азота, серы и кислорода, такие как тиазол, тиадизол, изотиазол, бензоксазол, бензотиазол, бензотиадиазол, фенотиазин, изоксазол, фуразан, феноксазин, пиразолоксазол, имидазотиазол, тиенофуран, фуропиррол, пиридоксазин, фуропиридин, фуропиримидин, тиенопиримидин и оксазол, все из которых могут быть необязательно замещены.
[165] Термин «замещенный арил» относится к ароматической карбоциклической группе, состоящей из по меньшей мере одного ароматического кольца или нескольких конденсированных колец, по меньшей мере одно из которых является ароматическим, где кольцо(-а) является(являются) замещенным(-и) одним или более заместителями. Например, арильная группа может содержать заместитель(-ли), выбранный(-ые) из -(СН2)nOH, -(СН2)n-O-(С1-С6)алкила, -(CH2)n-O-(CH2)n-(C1-С6)алкила, -(СН2)n-С(O)(С0-С6)алкила, -(СН2)n-С(O)O(С0-С6)алкила, -(СН2)n-ОС(O)(С0-С6)алкила, амина, моно- или ди-(С1-С6алкил)амина, где алкильная группа на амине необязательно замещена 1 или 2 гидроксильными группами или не более чем тремя галогенсодержащими группами (предпочтительно F, Cl), ОН, СООН, C1-С6алкила, предпочтительно СН3, CF3, ОМе, OCF3, NO2 или группы CN (замещение каждой из которых может происходить в орто-, мета- и/или пара-положениях фенильного кольца, предпочтительно пара-), необязательно замещенной фенильной группы (фенильная группа как таковая предпочтительно соединена с группой РТМ, в том числе с группой ULM, с помощью линкерной группы) и/или из по меньшей мере одного из F, Cl, ОН, СООН, СН3, CF3, ОМе, OCF3, NO2 или группы CN (в орто-, мета-и/или пара-положениях фенильного кольца, предпочтительно пара-), нафтильной группы, которая может быть необязательно замещена, необязательно замещенного гетероарила, предпочтительно необязательно замещенного изоксазола, в том числе метилзамещенного изоксазола, необязательно замещенного оксазола, в том числе метилзамещенного оксазола, необязательно замещенного тиазола, в том числе метилзамещенного тиазола, необязательно замещенного изотиазола, в том числе метилзамещенного изотиазола, необязательно замещенного пиррола, в том числе метилзамещенного пиррола, необязательно замещенного имидазола, в том числе метилимидазола, необязательно замещенного бензимидазола или метоксибензилимидазола, необязательно замещенного оксимидазола или метилоксимидазола, необязательно замещенной диазольной группы, в том числе метилдиазольной группы, необязательно замещенной триазольной группы, в том числе метилзамещенной триазольной группы, необязательно замещенной пиридиновой группы, в том числе галоген- (предпочтительно, F) или метилзамещенной пиридиновой группы или оксапиридиновой группы (где пиридиновая группа соединена с фенильной группой с помощью атома кислорода), необязательно замещенного фурана, необязательно замещенного бензофурана, необязательно замещенного дигидробензофурана, необязательно замещенного индола, индолизина или азаиндолизина (2, 3, или 4-азаиндолизина), необязательно замещенного хинолина и их комбинаций.
[166] «Карбоксил» обозначает группу --C(O)OR, где R представляет собой водород, алкил, замещенный алкил, арил, замещенный арил, гетероарил или замещенный гетероарил, при этом такие типичные заместители имеют значения, которые идентичны определениям соответствующих групп, определенных в данном документе.
[167] Термин «гетероарил» или «гетарил» может означать без ограничения необязательно замещенный хинолин (который может быть присоединен к фармакофору или замещен по любому атому углерода в хинолиновом кольце), необязательно замещенный индол (в том числе дигидроиндол), необязательно замещенный индолизин, необязательно замещенный азаиндолизин (2, 3 или 4-азаиндолизин), необязательно замещенный бензимидазол, бензодиазол, бензоксофуран, необязательно замещенный имидазол, необязательно замещенный изоксазол, необязательно замещенный оксазол (предпочтительно метилзамещенный), необязательно замещенный диазол, необязательно замещенный триазол, тетразол, необязательно замещенный бензофуран, необязательно замещенный тиофен, необязательно замещенный тиазол (предпочтительно метил- и/или тиолзамещенный), необязательно замещенный изотиазол, необязательно замещенный триазол (предпочтительно 1,2,3-триазол, замещенный метильной группой, триизопропилсилильной группой, необязательно замещенной -(CH2)m-O-C1-С6алкильной группой или необязательно замещенной -(СН2)m-С(O)-O-С1-С6алкильной группой), необязательно замещенный пиридин (2-, 3 или 4-пиридин) или группу в соответствии с химической структурой:
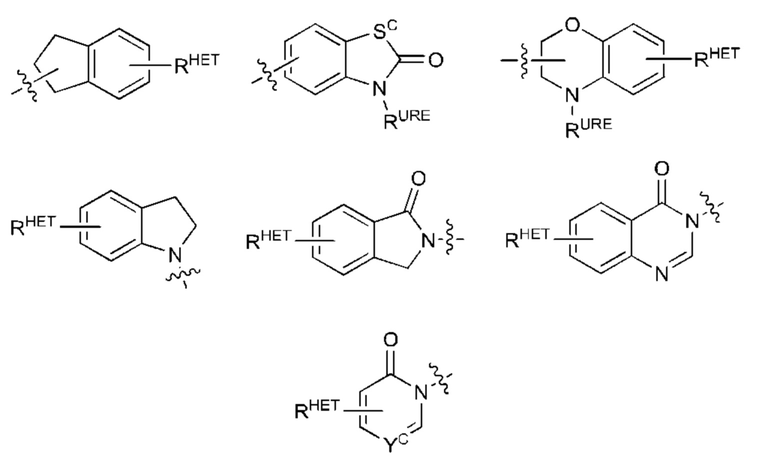
где
Sc представляет собой CHRSS, NRURE или О;
RHET представляет собой Н, CN, NO2, галоген (предпочтительно Cl или F), необязательно замещенный C1-С6алкил (предпочтительно замещенный одной или двумя гидроксильными группами или не более чем тремя галогене о держащими группами (например, CF3), необязательно замещенный O(С1-С6алкил) (предпочтительно замещенный одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами) или необязательно замещенную ацетиленовую группу -C≡C-Ra, где Ra представляет собой Н или C1-С6алкильную группу (предпочтительно C1-С3алкил);
RSS представляет собой Н, CN, NO2, галоген (предпочтительно F или Cl), необязательно замещенный C1-С6алкил (предпочтительно замещенный одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами), необязательно замещенный O-(С1-С6алкил) (предпочтительно замещенный одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами) или необязательно замещенный -С(O)(С1-С6алкил) (предпочтительно замещенный одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами);
RURE представляет собой Н, C1-С6алкил (предпочтительно Н или C1-С3алкил) или -С(O)(С1-С6алкил), каждая группа из которых необязательно замещена одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами, предпочтительно фтором, или необязательно замещенный гетероцикл, например, пиперидин, морфолин, пирролидин, тетрагидрофуран, тетрагидротиофен, пиперидин, пиперазин, каждый из которых необязательно замещен, и
YC представляет собой N или C-RYC, где RYC представляет собой Н, ОН, CN, NO2, галоген (предпочтительно Cl или F), необязательно замещенный C1-С6алкил (предпочтительно замещенный одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами (например, CF3), необязательно замещенный O(С1-С6алкил) (предпочтительно замещенный одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами) или необязательно замещенную ацетиленовую группу -C≡C-Ra, где Ra представляет собой Н или C1-С6алкильную группу (предпочтительно C1-С3алкил);
[168] Термины «аралкил» и «гетероарилалкил» относятся к группам, которые содержат как арил или, соответственно, гетероарил, а также алкил и/или гетероалкил и/или карбоциклические и/или гетероциклоалкильные кольцевые системы в соответствии с представленными выше определениями.
[169] Термин «арилалкил», применяемый в данном документе, относится к арильной группе, определенной выше, присоединенной к алкильной группе, определенной выше. Арилалкильная группа присоединена к исходному фрагменту посредством алкильной группы, где алкильная группа содержит от одного до шести атомов углерода. Арильная группа в арилалкильной группе может быть замещена, как определено выше.
[170] Термин «гетероцикл» относится к циклической группе, которая содержит по меньшей мере один гетероатом, например, N, О или S, и может быть ароматической (гетероарил) или неароматической. Таким образом, гетероарильные фрагменты включены в определение гетероцикла, в зависимости от контекста их применения. Иллюстративные гетероарильные группы описаны выше в данном документе.
[171] Иллюстративные гетероциклические группы включают, среди прочих, азетидинил, бензимидазолил, 1,4-бензодиоксанил, 1,3-бензодиоксолил, бензоксазолил, бензотиазолил, бензотиенил, дигидроимидазолил, дигидропиранил, дигидрофуранил, диоксанил, диоксоланил, этиленмочевину, 1,3-диоксолан, 1,3-диоксан, 1,4-диоксан, фурил, гомопиперидинил, имидазолил, имидазолинил, имидазолидинил, индолинил, индолил, изохинолинил, изотиазолидинил, изотиазолил, изоксазолидинил, изоксазолил, морфолинил, нафтиридинил, оксазолидинил, оксазолил, пиридон, 2-пирролидон. пиридин, пиперазинил, N-метилпиперазинил, пиперидинил, фталимид, сукцинимид, пиразинил, пиразолинил, пиридил, пиримидинил, пирролидинил, пирролинил, пирролил, хинолинил, тетрагидрофуранил, тетрагидропиранил, тетрагидрохинолин, тиазолидинил, тиазолил, тиенил, тетрагидротиофен, оксан, оксетанил, оксатиоланил, тиан.
[172] Гетероциклические группы могут быть необязательно замещены членом, выбранным из группы, состоящей из алкокси, замещенного алкокси, циклоалкила, замещенного циклоалкила, циклоалкенила, замещенного циклоалкенила, ацила, ациламино, ацилокси, амино, замещенного амино, аминоацила, аминоацилокси, оксиаминоацила, азидо, циано, галогена, гидроксила, кето, тиокето, карбокси, карбоксиалкила, тиоарилокси, тиогетероарилокси, тиогетероциклоокси, тиола, тиоалкокси, замещенного тиоалкокси, арила, арилокси, гетероарила, гетероарилокси, гетероциклической группы, гетероциклоокси, гидроксиамино, алкоксиамино, нитро, -SO-алкила, -SO-замещенного алкила, -SO-арила, -SO-гетероарила, -SO2-алкила, -SO2-замещенного алкила, -SO2-арила, оксо (=O) и -SO2-гетероарила. Такие гетероциклические группы могут иметь одно кольцо или множество конденсированных колец. Примеры содержащих азот гетероциклов и гетероарилов включают без ограничения пиррол, имидазол, пиразол, пиридин, пиразин, пиримидин, пиридазин, индолизин, изоиндол, индол, индазол, пурин, хинолизин, изохинолин, хинолин, фталазин, нафтилпиридин, хиноксалин, хиназолин, циннолин, птеридин, карбазол, карболин, фенантридин, акридин, фенантролин, изотиазол, феназин, изоксазол, феноксазин, фенотиазин, имидазолидин, имидазолин, пиперидин, пиперазин, индолин, морфолино, пиперидинил, тетрагидрофуранил и т.п., а также содержащие N-алкоксиазот гетероциклы. Термин «гетероциклическая группа» также включает бициклические группы, в которых любое из гетероциклических колец конденсировано с бензольным кольцом или циклогексановым кольцом или другим гетероциклическим кольцом (например, индол ил, хинолил, изохинолил, тетрагидрохинолил и т.п.).
[173] Термин «циклоалкил» может означать без ограничения одновалентные группы, полученные из моноциклических или полициклических алкильных групп или циклоалканов, определенных в данном документе, например, насыщенные моноциклические углеводородные группы, содержащие от трех до двадцати атомов углерода в кольце, в том числе без ограничения циклопропил, циклобутил, циклопентил, циклогексил, циклогептил и т.п. Термин «замещенный циклоалкил» может означать без ограничения моноциклическую или полициклическую алкильную группу и предусматривает замещение одним или более заместителями, например, амино, галогеном, алкилом, замещенным алкилом, карбилокси, карбилмеркапто, арилом, нитро, меркапто или сульфо, при этом такие типичные группы-заместители имеют значения, которые идентичны определениям соответствующих групп, определенных в данном обозначении.
[174] «Гетероциклоалкил» относится к моноциклической или полициклической алкильной группе, в которой по меньшей мере один атом углерода в кольце его циклической структуры заменен гетероатомом, выбранным из группы, состоящей из N, О, S или Р. «Замещенный гетероциклоалкил» относится к моноциклической или полициклической алкильной группе, в которой по меньшей мере один атом углерода в кольце его циклической структуры заменен гетероатомом, выбранным из группы, состоящей из N, О, S или Р, и при этом группа содержит один или более заместителей, выбранных из группы, состоящей из галогена, алкила, замещенного алкила, карбилокси, карбилмеркапто, арила, нитро, меркапто или сульфо, при этом такие типичные группы-заместители имеют значения, которые идентичны определениям соответствующих групп, определенных в данном документе.
[175] Под термином «углеводородный радикал» следует понимать соединение, которое содержит атомы углерода и водорода и которое может быть полностью насыщенным, частично ненасыщенным или ароматическим, и он включает арильные группы, алкильные группы, алкенильные группы и алкинильные группы.
[176] Термин «независимо» используется в данном документе для указания того, что переменная, которая применяется независимо, варьируется независимо от применения к применению.
[177] Термин «низший алкил» относится к метилу, этилу или пропилу.
[178] Термин «низший алкокси» относится к метокси, этокси или пропокси.
[179] В любом из вариантов осуществления, описанных в данном документе, W, X, Y, Z, G, G', R, R', R'', Q1-Q4, А и Rn могут быть независимо ковалентно связаны с линкером и/или линкером, к которому присоединены одна или более групп РТМ, ULM, ILM или ILM'.
[180] Иллюстративные MLM
[181] В определенных дополнительных вариантах осуществления MLM бифункционального соединения содержит химические фрагменты, такие как замещенные имидазолины, замещенные спироиндолиноны, замещенные пирролидины, замещенные пиперидиноны, замещенные морфолиноны, замещенные пирролопиримидины, замещенные имидазолопиридины, замещенный тиазолоимидазолин, замещенные пирролопирролидиноны и замещенные изохинолиноны.
[182] В дополнительных вариантах осуществления MLM предусматривает основные структуры, указанные выше, со смежными бис-арильными замещениями, расположенными в виде цис- или транс-конфигураций.
[183] В еще одних дополнительных вариантах осуществления MLM содержит часть структурных признаков как в RG7112, RG7388, SAR405838, AMG-232, АМ-7209, DS-5272, МK-8242 и NVP-CGM-097 и их аналоги или производные.
[184] В определенных предпочтительных вариантах осуществления MLM представляет собой производное замещенного имидазолина, представленного с помощью формулы (А-1), или тиазолоимидазолина, представленного с помощью формулы (А-2), или спироиндолинона, представленного с помощью формулы (А-3), или пироллидина, представленного с помощью формулы (А-4), или пиперидинона/морфолинона, представленного с помощью формулы (А-5), или изохинолинона, представленного с помощью формулы (А-6), или пироллопиримидина/имидазолопиридина, представленного с помощью формулы (А-7), или пирролопирролидинона/имидазолопирролидинона, представленного с помощью формулы (А-8).

где в приведенных выше формуле (А-1) - формуле (А-8)
X в формуле (A-1) - формуле (А-8) выбран из группы, состоящей из углерода, кислорода, серы, сульфоксида, сульфона и N-Ra;
Ra независимо представляет собой Н или алкильную группу с количеством атомов углерода 1-6;
Y и Z в формуле (А-1) - формуле (А-8) независимо представляют собой углерод или азот;
А, А' и А'' в формуле (А-1) - формуле (А-8) независимо выбраны из С, N, О или S, также могут представлять собой один или два атома, образующие конденсированное бициклическое кольцо или 6,5- и 5,5-конденсированную ароматическую бициклическую группу;
R1, R2 в формуле (А-1) - формуле (А-8) независимо выбраны из группы, состоящей из арильной или гетероарильной группы, при этом гетероарильная группа содержит один или два гетероатома, независимо выбранные из серы или азота, при этом арильная или гетероарильная группа может быть моноциклической или бициклической или незамещенной или замещенной одним - тремя заместителями, независимо выбранными из группы, состоящей из
галогена, -CN, С1-С6алкильной группы, С3-С6циклоалкила, -ОН, алкокси с 1-6 атомами углерода, фторзамещенного алкокси с 1-6 атомами углерода, сульфоксида с 1-6 атомами углерода, сульфона с 1-6 атомами углерода, кетона с 2-6 атомами углерода, амидов с 2-6 атомами углерода и диалкиламина с 2-6 атомами углерода;
R3, R4 в формуле (А-1) - формуле (А-8) независимо выбраны из группы, состоящей из Н, метила и С1-С6алкила;
R5 в формуле (А-1) - формуле (А-8) выбран из группы, состоящей из арильной или гетероарильной группы, при этом гетероарильная группа содержит один или два гетероатома, независимо выбранные из серы или азота, при этом арильная или гетероарильная группа может быть моноциклической или бициклической или незамещенной или замещенной одним - тремя заместителями, независимо выбранными из группы, состоящей из
галогена, -CN, С1-С6алкильной группы, С3-С6циклоалкила, -ОН, алкокси с 1-6 атомами углерода, фторзамещенного алкокси с 1-6 атомами углерода, сульфоксида с 1-6 атомами углерода, сульфона с 1-6 атомами углерода, кетона с 2-6 атомами углерода, амидов с 2-6 атомами углерода, диалкиламина с 2-6 атомами углерода, алкилового эфира (С2-С6), алкилкетона (С3-С6), морфолинила, сложного алкилового эфира (С3-С6), алкилцианида (С3-С6);
R6 в формуле (А-1) - формуле (А-8) представляет собой Н или -C(=O)Rb, где
Rb формуле (А-1) - формуле (А-8) выбран из группы, состоящей из алкила, циклоалкила, моно-, ди- или тризамещенного арила или гетероарила, 4-морфолинила, 1-(3-оксопиперазунил), 1-пиперидинила, 4-N-Rc-морфолинила, 4-Rc-1-пиперидинила и 3-Rc-1-пиперидинила, где
Rc в формуле (А-1) - формуле (А-8) выбран из группы, состоящей из алкила, фторзамещенного алкила, цианоалкила, гидроксилзамещенного алкила, циклоалкила, алкоксиалкила, амидалкила, алкилсульфона, алкилсульфоксида, алкиламида, арила, гетероарила, моно-, бис- и тризамещенного арила или гетероарила, CH2CH2Rd и CH2CH2CH2Rd, где
Rd в формуле (А-1) - формуле (А-8) выбран из группы, состоящей из алкокси, алкилсульфона, алкилсульфоксида, N-замещенного карбоксамида, -NHC(O)-алкила, -NH-SO2-алкила, арила, замещенного арила, гетероарила, замещенного гетероарила;
R7 в формуле (А-1) - формуле (А-8) выбран из группы, состоящей из Н, С1-С6алкила, циклического алкила, фторзамещенного алкила, цианозамещенного алкила, 5- или 6-членного гетероарила или арила, замещенного 5- или 6-членного гетероарила или арила;
R8 в формуле (А-1) - формуле (А-8) выбран из группы, состоящей из -Re-C(O)-Rf, -Re-алкокси, -Re-арила, -Re-гетероарила и -Re-C(O)-Rf-C(O)-Rg, где:
Re в формуле (А-1) - формуле (А-8) представляет собой алкилен с 1-6 атомами углерода или связь;
Rf в формуле (А-1) - формуле (А-8) представляет собой замещенный 4-7-членный гетероцикл;
Rg в формуле (A-1) - формуле (A-8) выбран из группы, состоящей из арила, гетероарила, замещенного арила или гетероарила и 4-7-членного гетероцикла;
R9 в формуле (А-1) - формуле (А-8) выбран из группы, состоящей из моно-, бис- или тризамещения заместителями в конденсированном бициклическом ароматическом кольце в формуле (А-3), где заместители независимо выбраны из группы, состоящей из галогена, алкена, алкина, алкила, незамещенного или замещенного Cl или F;
R10 в формуле (А-1) - формуле (А-8) выбран из группы, состоящей из арильной или гетероарильной группы, где гетероарильная группа может содержать один или два гетероатома, такие как сера или азот, при этом арильная или гетероарильная группа могут быть моноциклическими или бициклическими, арильная или гетероарильная группа могут быть незамещенными или замещенными одним - тремя заместителями, в том числе галогеном, F, Cl, -CN, алкеном, алкином, С1-С6алкильной группой, С1-С6циклоалкилом, -ОН, алкокси с 1-6 атомами углерода, фторзамещенным алкокси с 1-6 атомами углерода, сульфоксидом с 1-6 атомами углерода, сульфоном с 1-6 атомами углерода, кетоном с 2-6 атомами углерода;
R11 в формуле (А-1) - формуле (А-8) представляет собой -C(O)-N(Rh)(Ri), где Rh и Ri выбраны из группы, состоящей из следующих групп:
Н, С1-С6алкила, алкоксизамещенного алкила, сульфонзамещенного алкила, арила, гетероарила, моно-, бис- или тризамещенного арила или гетероарила, алкилкарбоновой кислоты, гетероарилкарбоновой кислоты, алкилкарбоновой кислоты, фторзамещенной алкилкарбоновой кислоты, арилзамещенного циклоалкила, гетероарилзамещенного циклоалкила; где
Rh и Ri в формуле (А-1) - формуле (А-8) независимо выбраны из группы, состоящей из Н, при этом они соединены с образованием кольца, 4-гидроксициклогегексана; моно- и дигидроксизамещенного алкила (С3-С6); 3-гидроксициклобутана; фенил-4-карбоновой кислоты и замещенной фенил-4-карбоновой кислоты;
R12 и R13 в формуле (А-1) - формуле (А-8) независимо выбраны из Н, низшего алкила (С1-С6), низшего алкенила (С2-С6), низшего алкинила (С2-С6), циклоалкила (4-, 5- и 6-членное кольцо), замещенного циклоалкила, циклоалкенила, замещенного циклоалкенила, 5- и 6-членного арила и гетероарила, R12 и R13 могут быть соединены с образованием 5- и 6-членного кольца с замещением в кольце или без него;
R14 в формуле (А-1) - формуле (А-8) выбран из группы, состоящей из алкила, замещенного алкила, алкенила, замещенного алкенила, арила, замещенного арила, гетероарила, замещенного гетероарила, гетероцикла, замещенного гетероцикла, циклоалкила, замещенного циклоалкила, циклоалкенила и замещенного циклоалкенила;
R15 в формуле (А-1) - формуле (А-8) представляет собой CN;
R16 в формуле (А-1) - формуле (А-8) выбран из группы, состоящей из С1-6алкила, С1-6циклоалкила, С2-6алкенила, С1-6алкила или С3-6циклоалкила с одним или несколькими атомами водорода, замененными фтором, алкила или циклоалкила с одной группой CH2, замененной S(=O), -S или -S(=O)2, алкила или циклоалкила с концевой группой СН3, замененной S(=O)2N(алкил)(алкил), -С(=O)N(алкил)(алкил), -N(алкил)S(=O)2(алкил), -С(=O)2(алкил), -О(алкил), С1-6алкила или алкилциклоалкила с атомом водорода, замененным гидроксильной группой, 3-7-членного циклоалкила или гетероциклоалкила, необязательно содержащих группу -(С=0)-, или 5-6-членной арильной или гетероарильной группы, при этом гетероциклоалкильная или гетероарильная группа может содержать от одного до трех гетероатомов, независимо выбранных из О, N или S, и при этом циклоалкильная, гетероциклоалкильная, арильная или гетероарильная группа может быть незамещенной или замещенной одним - тремя заместителями, независимо выбранными из галогена, С1-6алкильных групп, гидроксилированного С1-6алкила, С1-6алкилсодержащего тиоэфира, простого эфира, сульфона, сульфоксида, фторзамещенного простого эфира или цианогруппы;
R17 в формуле (А-1) - формуле (А-8) выбран из группы, состоящей из (CH2)nC(O)NRkR1, где Rk и R1 независимо выбраны из Н, С1-6алкила, гидроксилированного С1-6алкила, С1-6алкоксиалкила, С1-6алкила с одним или несколькими атомами водорода, замененными фтором, С1-6алкила с одним атомом углерода, замененным S(O), S(O)(O), С1-6алкоксиалкила с одним или несколькими атомами водорода, замененными фтором, С1-6алкила с атомом водорода, замененным цианогруппой, 5- и 6-членного арила или гетероарила, алкиларила с алкильной группой, содержащей 1-6 атомов углерода, и алкилгетероарила с алкильной группой, содержащей 1-6 атомов углерода, где арильная или гетероарильная группа могут быть дополнительно замещены;
R18 в формуле (А-1) - формуле (А-8) выбран из группы, состоящей из замещенного арила, гетероарила, алкила, циклоалкила, при этом замещение предпочтительно предусматривает -N(С1-4алкил)(циклоалкил), -N(C1-4алкил)алкилциклоалкил и -N(C1-4алкил)[(алкил)-(гетероцикл-замещенный)-циклоалкил];
R19 в формуле (А-1) - формуле (А-8) выбран из группы, состоящей из арила, гетероарила, бициклического гетероарила, и при этом такие арильные или гетероарильные группы могут быть замещены галогеном, С1-6алкилом, С1-6циклоалкилом, CF3, F, CN, алкином, алкилсульфоном, при этом замещение атомом галогена может предусматривать моно-, бис- или тризамещение;
R20 и R21 в формуле (А-1) - формуле (А-8) независимо выбраны из С1-6алкила, С1-6циклоалкила, С1-6алкокси, гидроксилированного С1-6алкокси и фторзамещенного С1-6алкокси, при этом R20 и R21 дополнительно могут быть соединены с образованием 5-, 6- и 7-членного циклического или гетероциклического кольца, которое может быть дополнительно замещено;
R22 в формуле (А-1) - формуле (А-8) выбран из группы, состоящей из Н, С1-6алкила, С1-6циклоалкила, карбоновой кислоты, сложного эфира карбоновой кислоты, амида, обратного амида, сульфонамида, обратного сульфонамида, N-ацилмочевины, содержащего азот 5-членного гетероцикла, при этом 5-членные гетероциклы могут быть дополнительно замещены С1-6алкилом, алкокси, фторзамещенным алкилом, CN и алкилсульфоном;
R23 в формуле (А-1) - формуле (А-8) выбран из арила, гетероарила, -О-арила, -О-гетероарила, -О-алкила, -О-алкилциклоалкила, -NH-алкила, -NH-алкилциклоалкила, -N(Н)-арила, -N(Н)-гетероарила, -N(алкил)-арила, -N(алкил)-гетероарила, при этом арильные или гетероарильные группы могут быть замещены галогеном, С1-6алкилом, гидроксилированным С1-6алкилом, циклоалкилом, фторзамещенным С1-6алкилом, CN, алкокси, алкилсульфоном, амидом и сульфонамидом;
R24 в формуле (А-1) - формуле (А-8) выбран из группы, состоящей из -СН2-(С1-6алкил), -СН2-циклоалкила, -СН2-арила, СН2-гетероарила, где алкил, циклоалкил, арил и гетероарил могут быть замещены галогеном, алкокси, гидроксилированным алкилом, цианозамещенным алкилом, циклоалкилом и замещенным циклоалкилом;
R25 в формуле (А-1) - формуле (А-8) выбран из группы, состоящей из С1-6алкила, С1-6алкилциклоалкила, алкоксизамещенного алкила, гидроксилированного алкила, арила, гетероарила, замещенного арила или гетероарила, 5-, 6- и 7-членных содержащих азот насыщенных гетероциклов, 5,6-конденсированных и 6,6-конденсированных содержащих азот насыщенных гетероциклов, и при этом такие насыщенные гетероциклы могут быть замещены С1-6алкилом, фторзамещенным С1-6алкилом, алкокси, арилом и гетероарильной группой;
R26 в формуле (А-1) - формуле (А-8) выбран из группы, состоящей из С1-6алкила, С3-6циклоалкила, при этом алкил или циклоалкил могут быть замещены -ОН, алкокси, фторзамещенным алкокси, фторзамещенным алкилом, -NH2, -NH-алкилом, NH-С(O)алкилом, -NH-S(O)2-алкилом и -S(O)2-алкилом;
R27 в формуле (А-1) - формуле (А-8) выбран из группы, состоящей из арила, гетероарила, бициклического гетероарила, где арильные или гетероарильные группы могут быть замещены С1-6алкилом, алкокси, NH2, NH-алкилом, галогеном или -CN, и при этом замещение может независимо предусматривать моно-, бис- и тризамещение;
R28 в формуле (А-1) - формуле (А-8) выбран из группы, состоящей из арила, 5- и 6-членного гетероарила, бициклического гетероарила, циклоалкила, насыщенного гетероцикла, такого как пиперидин, пиперидинон, тетрагидропиран, N-ацилпиперидин, где циклоалкил, насыщенный гетероцикл, арил или гетероарил могут быть дополнительно замещены -ОН, алкокси, при этом моно-, бис- или тризамещение предусматривает замещение галогеном, -CN, алкилсульфоном и фторзамещенными алкильными группами; и
R1'' в формуле (А-1) - формуле (А-8) выбран из группы, состоящей из алкила, арилзамещенного алкила, алкоксизамещенного алкила, циклоалкила, арилзамещенного циклоалкила и алкоксизамещенного циклоалкила.
[185] В определенных вариантах осуществления гетероциклы в Rf и Rg в формуле (А-1) - формуле (А-8) представляют собой замещенный пирролидин, замещенный пиперидин, замещенный пиперазин.
[186] Более конкретно, неограничивающие примеры MLM включают показанные ниже MLM, а также «гибридные» молекулы MLM, которые образуются в результате комбинации 1 или более различных признаков, показанных в молекулах ниже.
[187] С применением MLM в формуле А-1 - А-8 следующие PROTAC могут быть получены с обеспечением нацеливания на конкретный белок для разрушения, где «L» представляет собой соединяющую молекулу (т.е. линкерную группу), и «РТМ» представляет собой лиганд, связывающийся с целевым белком.
[188] В определенных вариантах осуществления в описании представлена бифункциональная молекула, характеризующаяся структурой, выбранной из группы, состоящей из
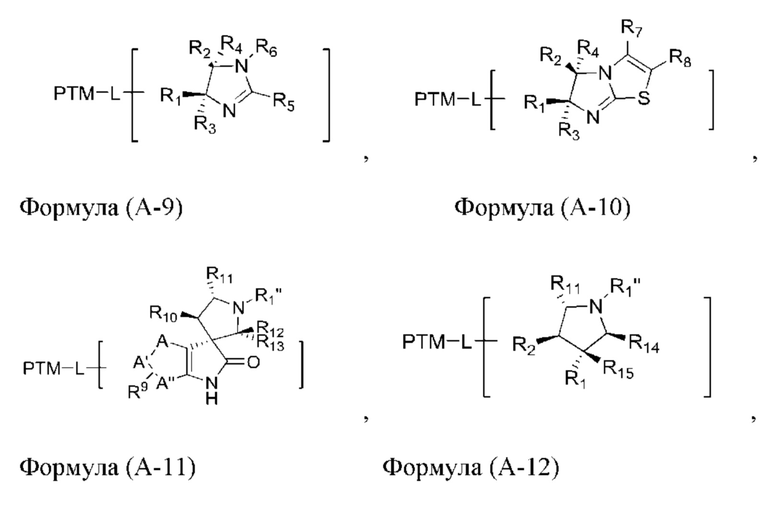

где X, Ra, Y, Z, A, A', A'', R1, R2, R3, R4, R5, R6, Rb, Rc, Rd, R7, Re, Rf, Rg, R9, R10, R11, R12, R13, R14, R15, R16, R17, Rk, Rl, R18, R19, R20, R21, R22, R23, R24, R25, R26, R27, R28 и R1'' определены в данном документе в отношении формул (А-1) - (А-8).
[189] В определенных вариантах осуществления в описании представлены бифункциональные или химерные молекулы со структурой PTM-L-MLM, где РТМ представляет собой фрагмент, связывающий белок-мишень, связанный с MLM с помощью L, где L представляет собой связь (т.е. отсутствует) или химический линкер. В определенных вариантах осуществления MLM характеризуется структурой, выбранной из группы, состоящей из А-1-1, А-1-2, А-1-3 и А-1-4:

где
R1' и R2' в формулах А-1-1 - А-1-4 (т.е. А-1-1, А-1-2, А-1-3 и А-1-4) независимо выбраны из группы, состоящей из F, Cl, Br, I, ацетилена, CN, CF3 и NO2;
R3' выбран из группы, состоящей из -ОСН3, -ОСН2СН3, -OCH2CH2F, -ОСН2СН2ОСН3 и -ОСН(СН3)2;
R4' в формулах А-1-1 - А-1-4 выбран из группы, состоящей из Н, галогена, -СН3, -CF3, -ОСН3, -С(СН3)3, -СН(СН3)2, -циклопропила, -CN, -С(СН3)2ОН, -С(СН3)2OCH2CH3, -С(СН3)2СН2ОН, -С(СН3)2CH2OCH2CH3, -С(СН3)2СН2ОСН2СН2ОН, -С(СН3)2CH2OCH2CH3, -C(CH3)2CN, -C(CH3)2C(O)CH3, -C(CH3)2C(O)NHCH3, -C(CH3)2C(O)N(CH3)2, -SCH3, -SCH2CH3, -S(O)2CH3, -S(O2)CH2CH3, -NHC(CH3)3, -N(СН3)2, пирролидинила и 4-морфолинила;
R5' в формулах А-1-1 - А-1-4 выбран из группы, состоящей из галогена, -циклопропила, -S(O)2CH3, -S(O)2CH2CH3, 1-пирролидинила, -NH2, -N(CH3)2 и -NHC(CH3)3; и
R6' в формулах А-1-1 - А-1-4 выбран из структур, представленных ниже, где точка соединения с линкером указана как «*».
Помимо R6' как точки присоединения линкера R4' также может служить как положение присоединения линкера. В случае, если R4' является местом соединения линкера, линкер будет соединен с концевым атомом групп R4', показанных выше.
[190] В определенных вариантах осуществления положение соединения линкера в формулах А-1-1 - А-1-4 находится на по меньшей мере одном из R4' или R6' или как на одном, так и на другом.
[191] В определенных вариантах осуществления R6' в формулах А-1-1 - А-1-4 независимо выбран из группы, состоящей из Н,

 где «*» указывает точку присоединения линкера.
где «*» указывает точку присоединения линкера.
[192] В определенных вариантах осуществления линкер в формуле А-4-1 - А-4-6 присоединен к по меньшей мере одному из R1', R2', R3', R4', R5', R6' или их комбинации.
[193] В определенных вариантах осуществления в описании представлены бифункциональные или химерные молекулы со структурой PTM-L-MLM, где РТМ представляет собой фрагмент, связывающий белок-мишень, связанный с MLM с помощью L, где L представляет собой связь (т.е. отсутствует) или химический линкер. В определенных вариантах осуществления MLM характеризуется структурой, выбранной из группы, состоящей из А-4-1, А-4-2, А-4-3, А-4-4, А-4-5 и А-4-6:
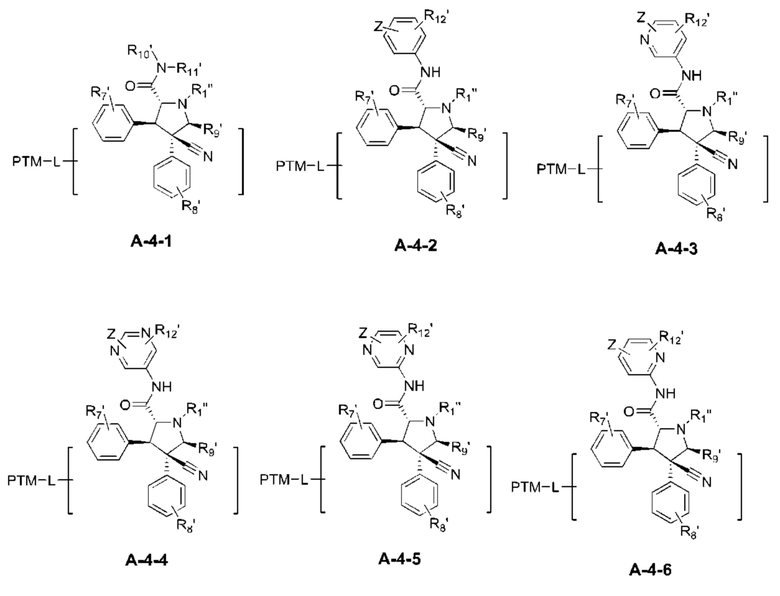
где
R7' в формуле А-4-1 - А-4-6 (т.е. А-4-1, А-4-2, А-4-3, А-4-4, А-4-5 и А-4-6) представляет собой член, выбранный из группы, состоящей из галогена, моно- и ди- или тризамещенного галогена;
R8' в формуле А-4-1 - А-4-6 выбран из группы, состоящей из Н, -F, -Cl, -Br, -I, -CN, -NO2, этиленила, циклопропила, метила, этила, изопропила, винила, метокси, этокси, изопропокси, -ОН, другого С1-6алкила, других С1-6алкенила и С1-6алкинила, моно-, ди- или тризамещенных;
R9' в формуле А-4-1 - А-4-6 выбран из группы, состоящей из алкила, замещенного алкила, алкенила, замещенного алкенила, алкинила, замещенного алкинила, арила, замещенного арила, гетероарила, замещенного гетероарила, циклоалкила, замещенного циклоалкила, алкенила и замещенного циклоалкенила;
Z в формуле А-4-1 - А-4-6 выбран из группы, состоящей из Н, -ОСН3, -ОСН2СН3 и галогена;
каждый из R10' и R11' в формуле А-4-1 - А-4-6 независимо выбран из группы, состоящей из Н, (CH2)n-R', (CH2)n-NR'R'', (CH2)n-NR'COR'', (CH2)n-NR'SO2R'', (CH2)n-COOH, (CH2)n-COOR', (CH)n-CONR'R'', (CH2)n-OR', (CH2)n-SR', (CH2)n-SOR', (CH2)n-CH(OH)-R', (CH2)n-COR', (CH2)n-SO2R', (CH2)n-SONR'R'', (CH2)n-SO2NR'R'', (CH2CH2O)m-(CH2)n-R', (CH2CH2O)m-(CH2)n-OH, (CH2CH2O)m-(CH2)n-OR', (CH2CH2O)m-(CH2)n-NR'R'', (CH2CH2O)m-(CH2)n-NR'COR'', (CH2CH2O)m(CH2)n-NR'SO2R'', (CH2CH2O)m(CH2)n-COOH, (CH2CH2O)m(CH2)n-COOR', (CH2CH2O)m-(CH2)n-CONR'R'', (CH2CH2O)m-(CH2)n-SO2R', (CH2CH2O)m-(CH2)n-COR', (CH2CH2O)m-(CH2)n-SONR'R'', (CH2CH2O)m-(CH2)n-SO2NR'R'', (CH2)p-(CH2CH2O)m-(CH2)nR', (CH2)p-(CH2CH2O)m-(CH2)n-OH, (CH2)p-(CH2CH2O)m-(CH2)n-OR', (CH2)p-(CH2CH2O)m-(CH2)n-NR'R'', (CH2)p-(CH2CH2O)m-(CH2)n-NR'COR'', (CH2)p-(CH2CH2O)m-(CH2)n-NR'SO2R'', (CH2)p-(CH2CH2O)m-(CH2)n-COOH, (CH2)p-(CH2CH2O)m-(CH2)n-COOR', (CH2)p-(CH2CH2O)m-(CH2)n-CONR'R'', (CH2)p-(CH2CH2O)m-(CH2)n-SO2R', (CH2)p-(CH2CH2O)m-(CH2)n-COR', (CH2)p-(CH2CH2O)m-(CH2)n-SONR'R'', (CH2)p-(CH2CH2O)m-(CH2)n-SO2NR'R'', арил-(СН2)n-СООН и гетероарилалкил-СО-алкил-NR'R''m, где алкил может быть замещен с помощью OR', а также гетероарил-(СН2)n-гетероцикла, где гетероцикл может необязательно быть замещен алкилом, гидроксилом, COOR' и COR'; где R' и R'' выбраны из Н, алкила, алкила, замещенного галогеном, гидроксила, NH2, NH(алкил), N(алкил)2, оксо, карбокси, циклоалкила и гетероарила;
m, n и р независимо составляют 0-6;
R12' в формуле А-4-1 - А-4-6 выбран из группы, состоящей из -О-(алкил), -О-(алкил)-алкокси, -С(O)-(алкил), -С(ОН)-алкилалкокси, -С(O)-NH-(алкил), -C(O)-N-(алкил)2, -S(O)-(алкил), S(O)2-(алкил), -С(O)-(циклический амин) и -О-арил-(алкил), -О-арил-(алкокси);
R1'' в формуле А-4-1 - А-4-6 выбран из группы, состоящей из алкила, арилзамещенного алкила, алкоксизамещенного алкила, циклоалкила, арилзамещенного циклоалкила и алкоксизамещенного циклоалкила.
[194] В любом из аспектов или вариантов осуществления, описанных в данном документе, алкил, алкокси или т.п. могут представлять собой низший алкил или низший алкокси.
[195] В определенных вариантах осуществления положение линкерного соединения в формуле А-4-1 - А-4-6 находится на по меньшей мере одном из Z, R8', R9', R10', R11'', R12'' или R1''.
[196] Способ, применяемый для разработки химерных молекул, представленных в А-1-1 - А-1-4, А-4-1 - А-4-6 можно применять по отношению к MLM с формулой А-2, А-3, А-5, А-6, А-7 и А-8, где гидрофильная область в MLM может быть соединена с линкером «L», который будет присоединен к «РТМ», лиганду, нацеливающемуся на белок, с конструированием PROTAC.
[197] Иллюстративные фрагменты, связывающие MDM2, включают без ограничения следующие:
[198] 1. Ингибиторы HDM2/MDM2, идентифицированные в Vassilev, et al., In vivo activation of the p53 pathway by small-molecule antagonists of MDM2, SCIENCE vol: 303, pag: 844-848 (2004) и Schneekloth, et al., Targeted intracellular protein degradation induced by a small molecule: En route to chemical proteomics, Bioorg. Med. Chem. Lett. 18 (2008) 5904-5908, в том числе (или дополнительно) соединения нутлин-3, нутлин-2 и нутлин-1 (дериватизированный), описанные ниже, а также все их производные и аналоги:

(дериватизированный, где линкерная группа L или группа -(L-MLM) присоединены, например, при метоксигруппе или гидроксильной группе);

(дериватизированный, где линкерная группа L или группа -(L-MLM) присоединены, например, при метоксигруппе или гидроксильной группе);

(дериватизированный, где линкерная группа L или группа -(L-MLM) присоединены, например, посредством метоксигруппы или гидроксильной группы); и
[199] 2. Транс-4-йод-4'-боранил-халькон
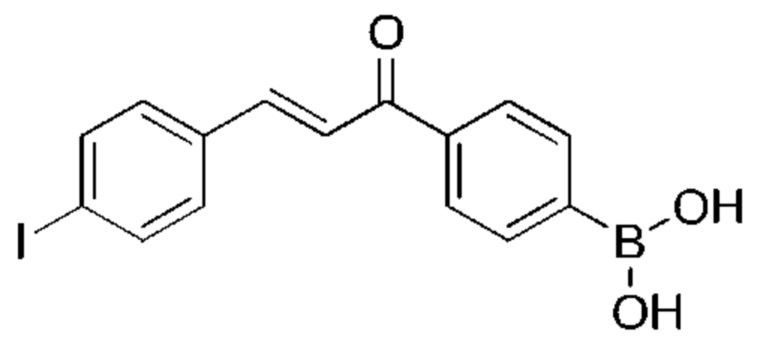
[200] (дериватизированный, где линкерная группа L или линкерная группа L или группа -(L-MLM) присоединены, например, посредством гидроксигруппы).
[201] Иллюстративные CLM
[202] Неоимидные соединения
[203] В одном аспекте в описании представлены соединения, пригодные для связывания и/или ингибирования цереблона. В определенных вариантах осуществления соединение выбрано из группы, состоящей из химических структур:
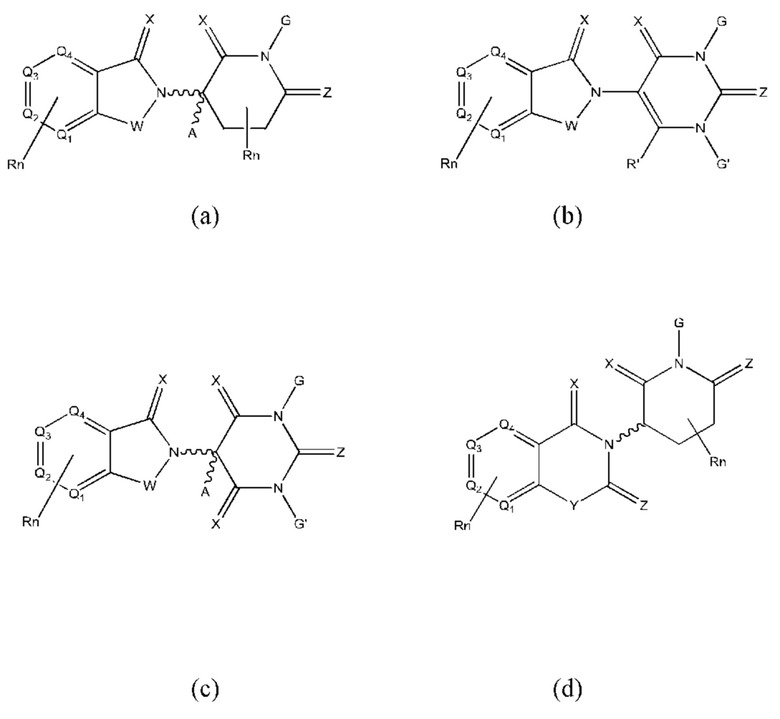

где
W в формулах (а) - (f) независимо выбран из группы, состоящей из CH2, CHR, С=O, SO2, NH и N-алкила;
X в формулах (а) - (f) независимо выбран из группы, состоящей из О, S и H2;
Y в формулах (а) - (f) независимо выбран из группы, состоящей из CH2, -C=CR', NH, N-алкила, N-арила, N-гетероарила, N-циклоалкила, N-гетероциклила, О и S;
Z в формулах (а) - (f) независимо выбран из группы, состоящей из О и S или H2, за исключением того, что X и Z одновременно не могут представлять собой H2;
G и G' в формулах (а) - (f) независимо выбраны из группы, состоящей из Н, алкила (линейного, разветвленного, необязательно замещенного), ОН, R'OCOOR, R'OCONRR'', CH2-гетероциклила, необязательно замещенного с помощью R' и бензила, необязательно замещенного с помощью R';
Q1-Q4 в формулах (а) - (f) представляет собой атом углерода С, замещенный группой, независимо выбранной из R, R', N или N-оксида;
А в формулах (а) - (f) независимо выбран из группы, состоящей из Н, алкила (линейного, разветвленного, необязательно замещенного), циклоалкила, Cl и F;
R в формулах (а) - (f) предусматривает без ограничения -CONR'R'', -OR', -NR'R'', -SR', -SO2R', -SO2NR'R'', -CR'R''-, -CR'NR'R''-, (-CR'O)nR'', -арил, -гетероарил, -алкил (линейный, разветвленный, необязательно замещенный), -циклоалкил, -гетероциклил, -P(O)(OR')R'', -P(O)R'R'', -OP(O)(OR')R'', -OP(O)R'R'', -Cl, -F, -Br, -I, -CF3, -CN, -NR'SO2NR'R'', -NR'CONR'R'', -CONR'COR'', -NR'C(=N-CN)NR'R'', -C(=N-CN)NR'R'', -NR'C(=N-CN)R'', -NR'C(=C-NO2)NR'R'', -SO2NR'COR'', -NO2, -CO2R', -C(C=N-OR')R'', -CR'=CR'R'', -CCR', -S(C=O)(C=N-R')R'', -SF5 и -OCF3;
R' и R'' в формулах (a) - (f) независимо выбраны из связи, Н, алкила, циклоалкила, арила, гетероарила, гетероциклической группы, -C(=O)R, гетероциклила, каждый из которых необязательно замещен;
n в формулах (а) - (f) представляет собой целое число 1-10 (например, 1-4);
 в формулах (а) - (f) представляет собой связь, которая может обеспечивать стереоспецифическую конфигурацию ((R) или (S)) или не обеспечивать стереоспецифическую конфигурацию; и
в формулах (а) - (f) представляет собой связь, которая может обеспечивать стереоспецифическую конфигурацию ((R) или (S)) или не обеспечивать стереоспецифическую конфигурацию; и
Rn в формулах (а) - (f) содержит 1-4 независимых функциональных групп или атомов.
[204] Иллюстративные CLM
[205] В любом из соединений, описанных в данном документе, CLM предусматривает химическую структуру, выбранную из группы:


где
W в формулах (а) - (f) независимо выбран из группы, состоящей из CH2, CHR, С=O, SO2, NH и N-алкила;
X в формулах (а) - (f) независимо выбран из группы, состоящей из О, S и Н2;
Y в формулах (а) - (f) независимо выбран из группы, состоящей из CH2, -C=CR', NH, N-алкила, N-арила, N-гетероарила, N-циклоалкила, N-гетероциклила, О и S;
Z в формулах (а) - (f) независимо выбран из группы, состоящей из О и S или Н2, за исключением того, что X и Z одновременно не могут представлять собой Н2;
G и G' в формулах (а) - (f) независимо выбраны из группы, состоящей из Н, алкила (линейного, разветвленного), ОН, R'OCOOR, R'OCONRR'', CH2-гетероциклила, необязательно замещенного R' и бензила, необязательно замещенного R';
Q1-Q4 в формулах (а) - (f) представляет собой атом углерода С, замещенный группой, независимо выбранной из R, R', N или N-оксида;
А в формулах (а) - (f) независимо выбран из группы, состоящей из Н, алкила (линейного, разветвленного, необязательно замещенного), циклоалкила, Cl и F;
R в формулах (а) - (f) предусматривает без ограничения -CONR'R'', -OR', -NR'R'', -SR', -SO2R', -SO2NR'R'', -CR'R''-, -CR'NR'R''-, -арил, -гетероарил, -алкил, -циклоалкил, -гетероциклил, -P(O)(OR')R'', -P(O)R'R'', -OP(O)(OR')R'', -OP(O)R'R'', -Cl, -F, -Br, -I, -CF3, -CN, -NR'SO2NR'R'', -NR'CONR'R'', -CONR'COR'', -NR'C(=N-CN)NR'R'', -C(=N-CN)NR'R'', -NR'C(=N-CN)R'', -NR'C(=C-NO2)NR'R'', SO2NR'COR'', -NO2, -CO2R', -C(C=N-OR')R'', -CR'=CR'R'', -CCR', -S(C=O)(C=N-R')R'',-SF5 и -OCF3;
R' и R'' в формулах (a) - (f) независимо выбраны из связи, Н, алкила, циклоалкила, арила, гетероарила, гетероциклической группы, -C(=O)R, гетероциклила, каждый из которых необязательно замещен;
n в формулах (а) - (f) представляет собой целое число 1-10 (например, 1-4);
 в формулах (а) - (f) представляет собой связь, которая может обеспечивать стереоспецифическую конфигурацию ((R) или (S)) или не обеспечивать стереоспецифическую конфигурацию; и
в формулах (а) - (f) представляет собой связь, которая может обеспечивать стереоспецифическую конфигурацию ((R) или (S)) или не обеспечивать стереоспецифическую конфигурацию; и
Rn в формулах (а) - (f) предусматривает 1-4 независимых функциональных групп или атомов, и при этом необязательно одна(один) из них модифицирована(модифицирован) так, чтобы ковалентно связываться с РТМ, химической линкерной группой (L), ULM, CLM (или CLM') или их комбинацией.
[206] В определенных вариантах осуществления, описанных в данном документе, CLM или ULM предусматривает химическую структуру, выбранную из группы:
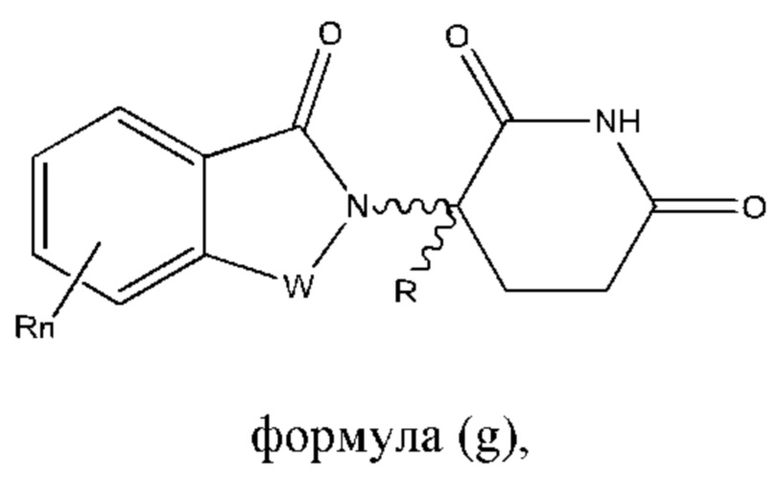
где
W в формуле (g) независимо выбран из группы, состоящей из CH2, С=O, NH и N-алкила;
R в формуле (g) независимо выбран из Н, метила, алкила (например, С1-С6алкила (линейного, разветвленного, необязательно замещенного));
 в формуле (g) представляет собой связь, которая может обеспечивать стереоспецифическую конфигурацию ((R) или (S)) или не обеспечивать стереоспецифическую конфигурацию; и
в формуле (g) представляет собой связь, которая может обеспечивать стереоспецифическую конфигурацию ((R) или (S)) или не обеспечивать стереоспецифическую конфигурацию; и
Rn в формуле (g) предусматривает 1-4 независимо выбранных функциональных групп или атомов, и при этом необязательно одна(один) из них модифицирована(модифицирован) так, чтобы ковалентно связываться с РТМ, химической линкерной группой (L), ULM, CLM (или CLM') или их комбинацией.
[207] В любом из вариантов осуществления, описанных в данном документе, W, X, Y, Z, G, G', R, R', R'', Q1-Q4, А и Rn в формулах (a) - (g) могут быть независимо ковалентно связаны с линкером и/или линкером, к которому присоединены одна или более групп РТМ, ULM, CLM или CLM'.
[208] Более конкретно, неограничивающие примеры CLM включают показанные ниже CLM, а также «гибридные» молекулы CLM, которые образуются в результате комбинации 1 или более различных признаков, показанных в молекулах ниже.


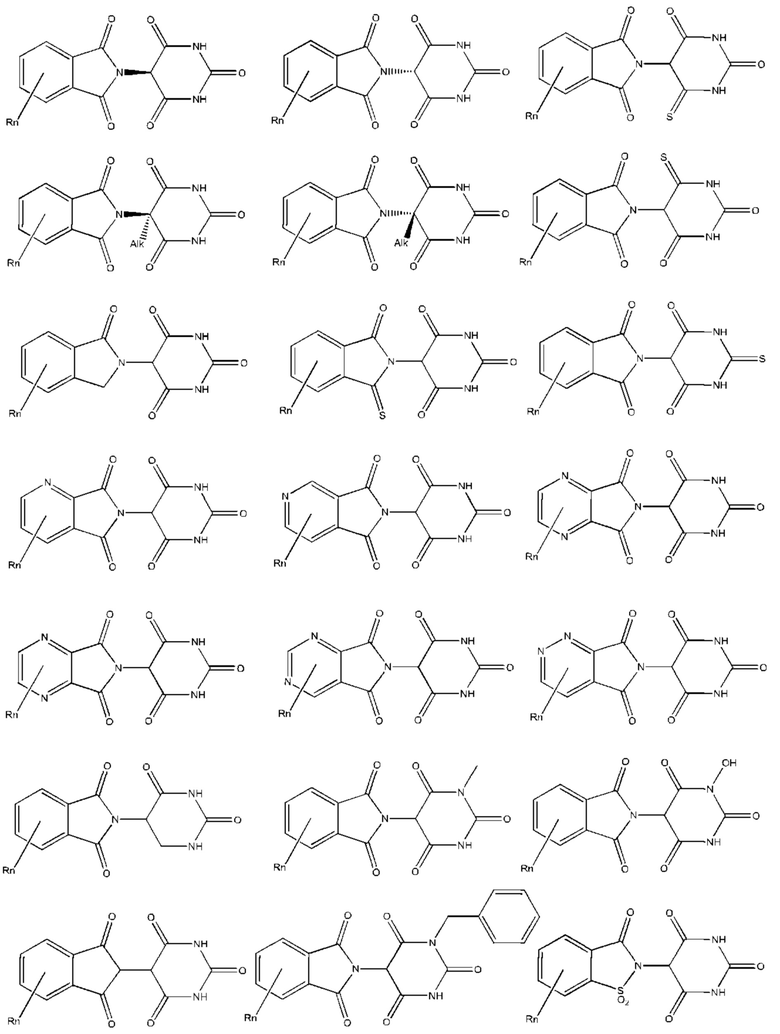

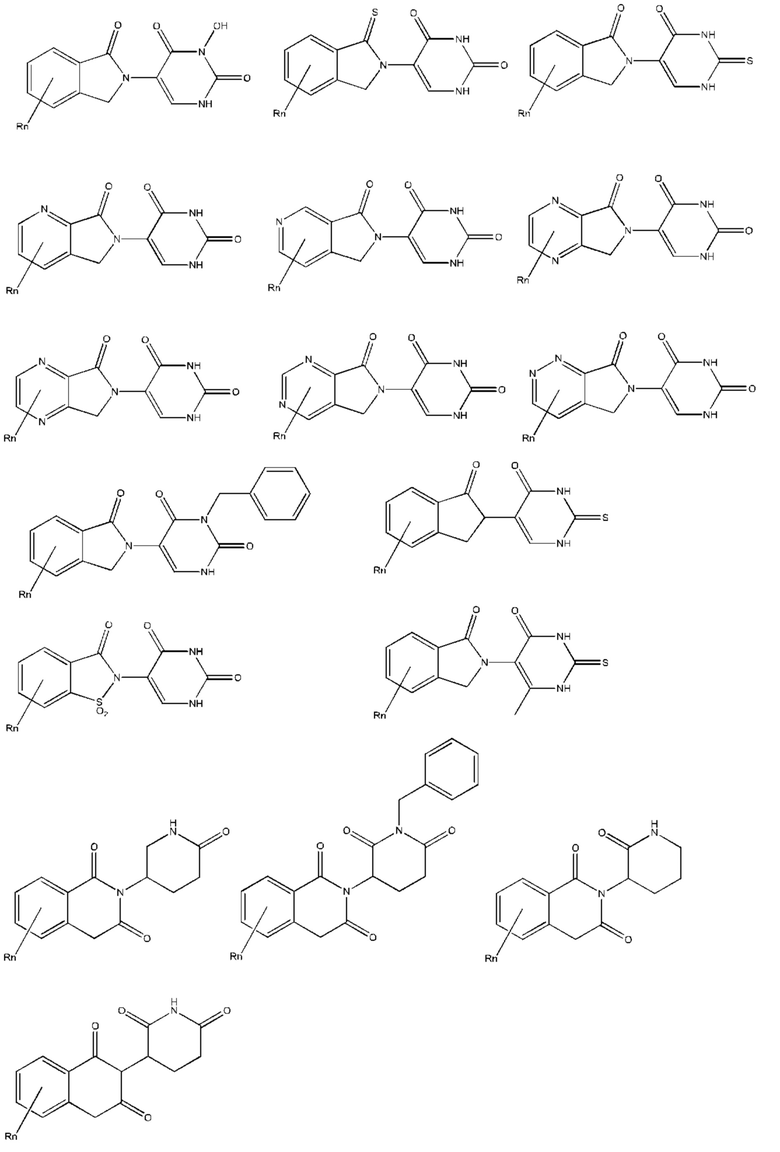

[209] В любом из соединений, описанных в данном документе, CLM предусматривает химическую структуру, выбранную из группы:



где
W в формулах (h) - (ad) независимо выбран из CH2, CHR, С=O, SO2, NH и N-алкила;
Q1, Q2, Q3, Q4, Q5 в формулах (h) - (ас) независимо представляют собой атом углерода С, замещенный группой, независимо выбранной из R', N или N-оксида;
R1 в формулах (h) - (ad) выбран из Н, CN, С1-С3-алкила;
R2 в формулах (h) - (ad) выбран из группы, состоящей из Н, CN, С1-С3-алкила, CHF2, CF3, СНО;
R3 в формулах (h) - (ad) выбран из Н, алкила, замещенного алкила, алкокси, замещенного алкокси;
R4 в формулах (h) - (ad) выбран из Н, алкила, замещенного алкила;
R5 в формулах (h) - (ad) представляет собой Н или низший алкил;
X в формулах (h) - (ad) представляет собой С, СН или N;
R' в формулах (h) - (ad) выбран из Н, галогена, алкила, замещенного алкила, алкокси, замещенного алкокси;
R в формулах (h) - (ad) представляет собой Н, ОН, низший алкил, низший алкокси, циано, галогенированный низший алкокси или галогенированный низший алкил;
 в формулах (h) - (ad) представляет собой одинарную или двойную связь; и
в формулах (h) - (ad) представляет собой одинарную или двойную связь; и
CLM ковалентно связан с РТМ, химической линкерной группой (L), ULM, CLM (или CLM') или их комбинацией.
[210] В любом аспекте или варианте осуществления, описанных в данном документе, CLM или CLM' ковалентно связаны с РТМ, химической линкерной группой (L), ULM, CLM, CLM' или их комбинацией с помощью R-группы (такой как R, R1, R2, R3, R4 или R'), W, X или Q-группы (такой как Q1, Q2, Q3, Q4 или Q5) из формул (h) - (ad).
[211] В любом из вариантов осуществления, описанных в данном документе, CLM или CLM' ковалентно связаны с РТМ, химической линкерной группой (L), ULM, CLM, CLM' или их комбинацией с помощью W, X, R, R1, R2, R3, R4, R5, R', Q1, Q2, Q3, Q4 и Q5 из формул (h) - (ad).
[212] В любом из вариантов осуществления, описанных в данном документе, W, X, R1, R2, R3, R4, R', Q1, Q2, Q3, Q4 и Q5 из формул (h) - (ad) могут быть независимо ковалентно связаны с линкером и/или линкером, к которому присоединены одна или более групп РТМ, ULM, ULM', CLM или CLM'.
[213] Более конкретно, неограничивающие примеры CLM включают показанные ниже CLM, а также «гибридные» молекулы или соединения, которые образуются в результате комбинирования 1 или более признаков следующих соединений:


где
W в формулах (ае) - (ар) независимо выбран из группы, состоящей из CH2, CHR, С=O, SO2, NH и N-алкила;
R1 в формулах (ае) - (ар) выбран из группы, состоящей из Н, CN, С1-С3-алкила;
R3 в формулах (ае) - (ар) выбран из Н, алкила, замещенного алкила, алкокси, замещенного алкокси;
R в формулах (ае) - (ар) представляет собой Н;
 представляет собой одинарную или двойную связь; и
представляет собой одинарную или двойную связь; и
Rn в формулах (ае) - (ар) предусматривает функциональную группу или атом.
[214] В любом из вариантов осуществления, описанных в данном документе, W, R1, R2, Q1, Q2, Q3, Q4 и Rn в формулах (ае) - (ар) могут быть независимо ковалентно связаны с линкером и/или линкером, к которому присоединены одна или более групп РТМ, ULM, ULM', CLM или CLM'.
[215] В любом из вариантов осуществления, описанных в данном документе, R1, R2, Q1, Q2, Q3, Q4 и Rn в формулах (ае) - (ар) могут быть независимо ковалентно связаны с линкером и/или линкером, к которому присоединены одна или более групп РТМ, ULM, ULM', CLM или CLM'.
[216] В любом из вариантов осуществления, описанных в данном документе, Q1, Q2, Q3, Q4 и Rn в формулах (ае) - (ар) могут быть независимо ковалентно связаны с линкером и/или линкером, к которому присоединены одна или более групп РТМ, ULM, ULM', CLM или CLM'.
[217] В любом аспекте или варианте осуществления, описанных в данном документе, Rn в формулах (ае) - (ар) модифицирован так, чтобы ковалентно связываться с линкерной группой (L), РТМ, ULM, вторым CLM, имеющим такую же химическую структуру, как CLM, CLM', вторым линкером или любым их множеством или комбинацией.
[218] В любом аспекте или варианте осуществления, описанных в данном документе, CLM выбран из:

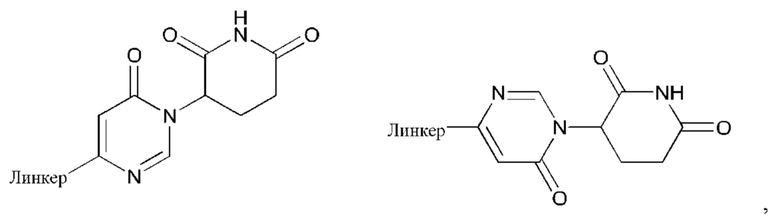
где R' представляет собой галоген, и R1 описан выше в отношении формул (h) - (ab) или (ас) - (an).
[219] В определенных случаях CLM может представлять собой имиды, которые связываются с цереблоном Е3-лигазного комплекса. Такие имиды и точка присоединения линкера могут быть представлены без ограничения следующими структурами:
 , где
, где
R' представляет собой галоген.
[220] Иллюстративные VLM
[221] В определенных вариантах осуществления соединений, описанных в данном документе, ULM представляет собой VLM и имеет химическую структуру, выбранную из группы ULM-a:
 где
где
пунктирная линия указывает на присоединение по меньшей мере одного РТМ, другого ULM, или VLM, или MLM, или ILM, или CLM (т.е. ULM', или VLM', или CLM', или ILM', или MLM') или химического линкерного фрагмента, связывающего по меньшей мере один РТМ, ULM', или VLM', или CLM', или ILM', или MLM' с другим концом линкера;
каждый из X1, X2 в формуле ULM-a независимо выбран из группы, состоящей из связи, О, NRY3, CRY3RY4, С=O, C=S, SO и SO2;
каждый из RY3, RY4 в формуле ULM-a независимо выбран из группы, состоящей из Н, линейного или разветвленного C1-6алкила, необязательно замещенного 1 или более атомами галогена, необязательно замещенного C1-6алкоксила (например, необязательно замещенного 0-3 группами RP);
RP в формуле ULM-a представляет собой 0, 1, 2 или 3 группы, при этом каждая независимо выбрана из группы, состоящей из Н, галогена, -ОН, C1-3алкила, С=O;
W3 в формуле ULM-a выбран из группы, состоящей из необязательно замещенного -T-N(R1aR1b)X3, -T-N(R1aR1b), -Т-арила, необязательно замещенного -Т-гетероарила, необязательно замещенного -Т-гетероцикла, необязательно замещенного -NR1-Т-арила, необязательно замещенного -NR1-Т-гетероарила или необязательно замещенного -NR1-Т-гетероцикла;
X3 в формуле ULM-a представляет собой С=O, R1, R1a, R1b;
каждый из R1, R1a, R1b независимо выбран из группы, состоящей из Н, линейной или разветвленной C1-С6алкильной группы, необязательно замещенной 1 или более атомами галогена или группами -ОН, RY3C=O, RY3C=S, RY3SO, RY3SO2, N(RY3RY4)C=O, N(RY3RY4)C=S, N(RY3RY4)SO и N(RY3RY4)SO2;
T в формуле ULM-a ковалентно связан с X1;
W4 в формуле ULM-a представляет собой необязательно замещенный -NR1-T-арил, необязательно замещенную -NR1-T-гетероарильную группу или необязательно замещенный -NR1-T-гетероцикл, где -NR1 ковалентно связан с X2, и R1 представляет собой Н или СН3, предпочтительно Н.
[222] В любом из вариантов осуществления, описанных в данном документе, Т выбран из группы, состоящей из необязательно замещенного алкила, группы -(СН2)n-, где каждая из метиленовых групп необязательно замещена одним или двумя заместителями, выбранными из группы, состоящей из галогена, метила, линейной или разветвленной C1-С6алкильной группы, необязательно замещенной 1 или более атомами галогена или группами -ОН, или необязательно замещенной аминокислотной боковой цепи; и n составляет 0-6, зачастую 0, 1, 2 или 3, предпочтительно 0 или 1.
[223] В определенных вариантах осуществления W4 в формуле ULM-a представляет собой 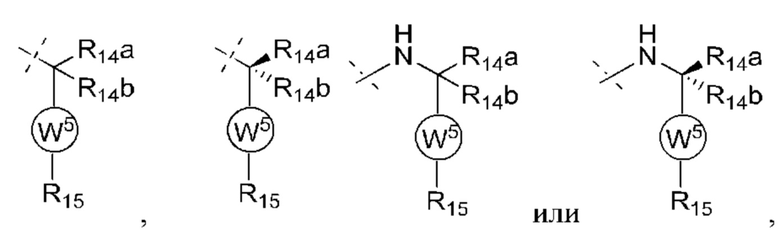 где каждый из R14a, R14b независимо выбран из группы, состоящей из Н, галогеналкила или необязательно замещенного алкила.
где каждый из R14a, R14b независимо выбран из группы, состоящей из Н, галогеналкила или необязательно замещенного алкила.
[224] В любом из вариантов осуществления W5 в формуле ULM-a выбран из группы, состоящей из фенила или 5-10-членного гетероарила,
R15 в формуле ULM-a выбран из группы, состоящей из Н, галогена, CN, ОН, NO2, N R14aR14b, OR14a, CONR14aR14b, NR14aCOR14b, SO2NR14aR14b, NR14a SO2R14b, необязательно замещенного алкила, необязательно замещенного галогеналкила, необязательно замещенного галогеналкокси; арила, гетероарила, циклоалкила или циклогетероалкила.
[225] В дополнительных вариантах осуществления заместители W4 для применения в настоящем изобретении также включают конкретно (и без ограничения конкретным раскрытым соединением) заместители W4, которые обнаружены в определенных соединениях, раскрытых в данном документе. Каждый из таких заместителей W4 может применяться совместно с любым количеством заместителей W3, которые также раскрыты в данном документе.
[226] В определенных дополнительных вариантах осуществления ULM-a необязательно замещен 0-3 группами RP в пирролидиновом фрагменте. Каждая RP независимо представляет собой Н, галоген, -ОН, C1-3-алкил, С=O.
[227] В любом из вариантов осуществления, описанных в данном документе, W3, W4 в формуле ULM-a могут быть независимо ковалентно связаны с линкером, к которому присоединены одна или более групп РТМ.
и где пунктирная линия указывает на участок присоединения по меньшей мере одного РТМ, другого ULM (ULM') или химического линкерного фрагмента, связывающего по меньшей мере один РТМ, или ULM', или оба из них, к ULM.
[228] В определенных вариантах осуществления ULM представляет собой VHL и представлен структурой:

где
W3 в формуле ULM-b выбран из группы, состоящей из необязательно замещенного арила, необязательно замещенного гетероарила, или 
R9 и R10 в формуле ULM-b независимо представляют собой водород, необязательно замещенный алкил, необязательно замещенный циклоалкил, необязательно замещенный гидроксиалкил, необязательно замещенный гетероарил или галогеналкил, или R9, R10 и атом углерода, к которому они присоединены, образуют необязательно замещенный циклоалкил;
R11 в формуле ULM-b выбран из группы, состоящей из необязательно замещенной гетероциклической группы, необязательно замещенного алкокси, необязательно замещенного гетероарила, необязательно замещенного арила, 

R12 в формуле ULM-b выбран из группы, состоящей из Н или необязательно замещенного алкила;
R13 в формуле ULM-b выбран из группы, состоящей из Н, необязательно замещенного алкила, необязательно замещенного алкилкарбонила, необязательно замещенного (циклоалкил)алкилкарбонила, необязательно замещенного аралкилкарбонила, необязательно замещенного арилкарбонила, необязательно замещенного (гетероциклил)карбонила или необязательно замещенного аралкила;
каждый из R14a, R14b в формуле ULM-b независимо выбран из группы, состоящей из Н, галогеналкила или необязательно замещенного алкила;
W5 в формуле ULM-b выбран из группы, состоящей из фенила или 5-10-членного гетероарила,
R15 в формуле ULM-b выбран из группы, состоящей из Н, галогена, CN, ОН, NO2, N R14aR14b, OR14a, CONR14aR14b, NR14aCOR14b, SO2NR14aR14b, NR14a SO2R14b, необязательно замещенного алкила, необязательно замещенного галогеналкила, необязательно замещенного галогеналкокси; арила, гетероарила, циклоалкила или циклогетероалкила (каждый необязательно замещен);
R16 в формуле ULM-b независимо выбран из группы, состоящей из галогена, необязательно замещенного алкила, необязательно замещенного галогеналкила, гидрокси или необязательно замещенного галогеналкокси;
ο в формуле ULM-b равняется 0, 1, 2, 3 или 4;
R18 в формуле ULM-b независимо выбран из группы, состоящей из Н, галогена, необязательно замещенного алкокси, циано, необязательно замещенного алкила, галогеналкила, галогеналкокси или линкера; и
р в формуле ULM-b равняется 0, 1, 2, 3 или 4, и при этом пунктирная линия указывает на участок присоединения по меньшей мере одного РТМ, другого ULM (ULM') или химического линкерного фрагмента, связывающего по меньшей мере один РТМ, или ULM', или оба из них, к ULM.
[229] В определенных вариантах осуществления R15 в формуле ULM-b представляет собой 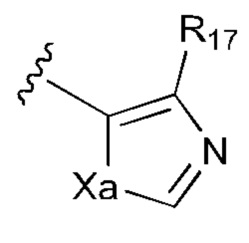 , где R17 представляет собой Н, галоген, необязательно замещенный С3-6циклоалкил, необязательно замещенный C1-6алкил, необязательно замещенный C1-6алкенил и C1-6галогеналкил; и Ха представляет собой S или О.
, где R17 представляет собой Н, галоген, необязательно замещенный С3-6циклоалкил, необязательно замещенный C1-6алкил, необязательно замещенный C1-6алкенил и C1-6галогеналкил; и Ха представляет собой S или О.
[230] В определенных вариантах осуществления R17 в формуле ULM-b выбран из группы, состоящей из метила, этила, изопропила и циклопропила.
[231] В определенных дополнительных вариантах осуществления R15 в формуле ULM-b выбран из группы, состоящей из
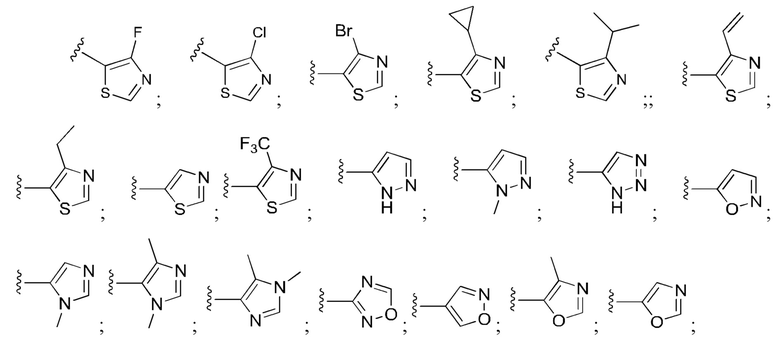
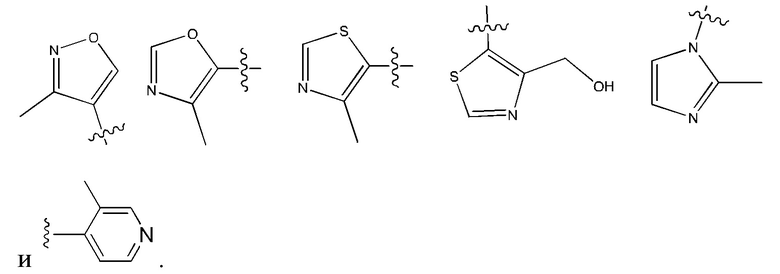
[232] В определенных вариантах осуществления, R11 в формуле ULM-b выбран из группы, состоящей из

[233] В определенных вариантах осуществления ULM имеет химическую структуру, выбранную из группы, состоящей из

где
R1 в формулах ULM-c, ULM-d и ULM-e представляет собой Н, этил, изопропил, трет-бутил, втор-бутил, циклопропил, циклобутил, циклопентил или циклогексил; необязательно замещенный алкил, необязательно замещенный гидроксиалкил, необязательно замещенный гетероарил или галогеналкил;
R14a в формулах ULM-c, ULM-d и ULM-e представляет собой Н, галогеналкил, необязательно замещенный алкил, метил, фторметил, гидроксиметил, этил, изопропил или циклопропил;
R15 в формулах ULM-c, ULM-d и ULM-e выбран из группы, состоящей из Н, галогена, CN, ОН, NO2, необязательно замещенного гетероарила, необязательно замещенного арила; необязательно замещенного алкила, необязательно замещенного галогеналкила, необязательно замещенного галогеналкокси, циклоалкила или циклогетероалкила;
X в формулах ULM-c, ULM-d и ULM-e представляет собой С или С=O;
R3 в формулах ULM-c, ULM-d и ULM-e отсутствует или представляет собой необязательно замещенный 5- или 6-членный гетероарил; и
где пунктирная линия указывает на участок присоединения по меньшей мере одного РТМ, другого ULM (ULM') или химического линкерного фрагмента, связывающего по меньшей мере один РТМ, или ULM', или оба из них, к ULM.
[234] В определенных вариантах осуществления ULM предусматривает группу в соответствии с химической структурой:

ULM-f
где
R14a в формуле ULM-f представляет собой Н, галогеналкил, необязательно замещенный алкил, метил, фторметил, гидроксиметил, этил, изопропил или циклопропил;
R9 в формуле ULM-f представляет собой Н;
R10 в формуле ULM-f представляет собой Н, этил, изопропил, трет-бутил, втор-бутил, циклопропил, циклобутил, циклопентил или циклогексил;
R11 в формуле ULM-f представляет собой 
 или необязательно замещенный гетероарил;
или необязательно замещенный гетероарил;
р в формуле ULM-f представляет собой 0, 1, 2, 3 или 4;
каждый R18 в формуле ULM-f независимо представляет собой галоген, необязательно замещенный алкокси, циано, необязательно замещенный алкил, галогеналкил, галогеналкокси или линкер;
R12 в формуле ULM-f представляет собой Н, С=O;
R13 в формуле ULM-f представляет собой Н, необязательно замещенный алкил, необязательно замещенный алкилкарбонил, необязательно замещенный (циклоалкил)алкилкарбонил, необязательно замещенный аралкилкарбонил, необязательно замещенный арилкарбонил, необязательно замещенный (гетероциклил)карбонил или необязательно замещенный аралкил,
R15 в формуле ULM-f выбран из группы, состоящей из Н, галогена, Cl, CN, ОН, NO2, необязательно замещенного гетероарила, необязательно замещенного арила;


где пунктирная линия в формуле ULM-f указывает на участок присоединения по меньшей мере одного РТМ, другого ULM (ULM') или химического линкерного фрагмента, связывающего по меньшей мере один РТМ, или ULM', или оба из них, к ULM.
[235] В определенных вариантах осуществления ULM выбран из следующих структур:





где n равняется 0 или 1.
[236] В определенных вариантах осуществления ULM выбран из следующих структур:

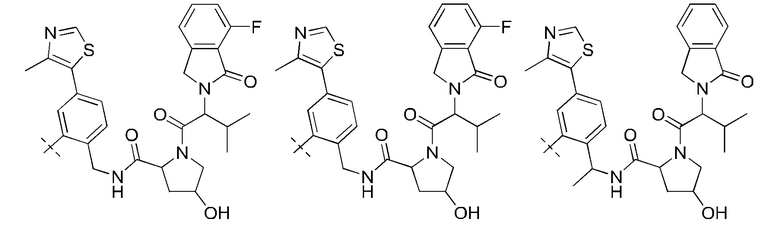










где фенильное кольцо в ULM-a1-ULM-a15, ULM-b1-ULM-b12, ULM-c1-ULM-c15 и ULM-d1-ULM-d9 необязательно замещено группами, представляющими собой атом фтора, низший алкил и алкокси, и при этом пунктирная линия указывает на участок присоединения по меньшей мере одного РТМ, другого ULM (ULM') или химического линкерного фрагмента, связывающего по меньшей мере один РТМ, или ULM', или оба из них, к ULM-a.
[237] В одном варианте осуществления фенильное кольцо в ULM-a1-ULM-а15, ULM-b1-ULM-b12, ULM-c1-ULM-c15 и ULM-d1-ULM-d9 может быть функционализировано как сложный эфир, чтобы сделать его частью пролекарства.
[238] В определенных вариантах осуществления гидроксильная группа на пирролидиновом кольце в ULM-a1-ULM-a15, ULM-b1-ULM-b12, ULM-c1-ULM-c15 и ULM-d1-ULM-d9 соответственно содержит связанный сложноэфирной связью фрагмент пролекарства.
[239] В любом из аспектов или вариантов осуществления, описанных в данном документе, каждый из ULM и ULM' в случае его присутствия независимо представляет собой группу в соответствии с химической структурой:
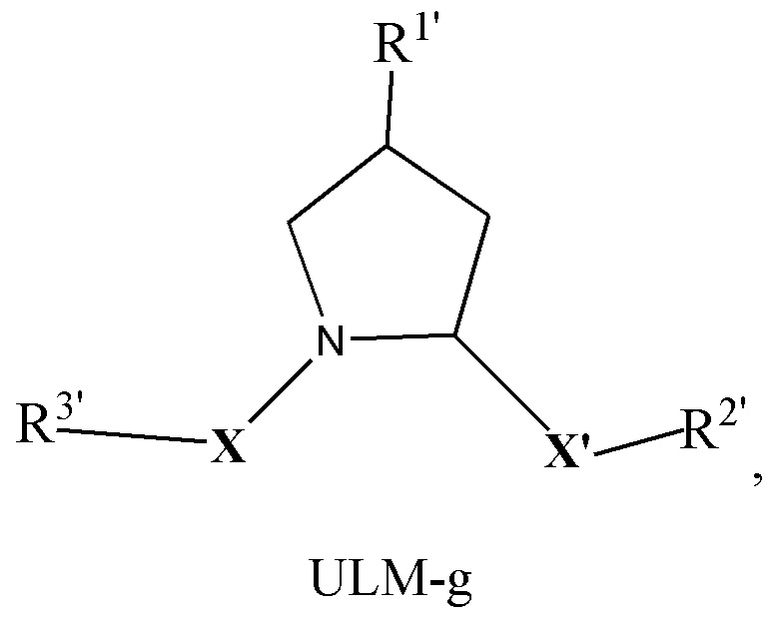
где
R1' в ULM-g представляет собой необязательно замещенную C1-С6алкильную группу, необязательно замещенную -(СН2)nOH, необязательно замещенную -(CH2)nSH, необязательно замещенную (СН2)n-O-(С1-С6)алкильную группу, необязательно замещенную (СН2)n-WCOCW-(С0-С6)алкильную группу, содержащую эпоксидный фрагмент WCOCW, где каждый W независимо представляет собой Н или C1-С3алкильную группу, необязательно замещенную -(СН2)nCOOH, необязательно замещенную -(СН2)nC(O)-(С1-С6алкил), необязательно замещенную -(CH2)nNHC(O)-R1, необязательно замещенную -(CH2)nC(O)-NR1R2, необязательно замещенную -(CH2)nOC(O)-NR1R2, -(CH2O)nH, необязательно замещенную -(CH2)nOC(O)-(C1-С6алкил), необязательно замещенную -(СН2)nC(O)-O-(С1-С6алкил), необязательно замещенную -(CH2O)nCOOH, необязательно замещенную -(ОСН2)nO-(С1-С6алкил), необязательно замещенную -(CH2O)nC(O)-(С1-С6алкил), необязательно замещенную -(OCH2)nNHC(O)-R1, необязательно замещенную -(CH2O)nC(O)-NR1R2, -(CH2CH2O)nH, необязательно замещенную -(CH2CH2O)nCOOH, необязательно замещенную -(ОСН2СН2)nO-(С1-С6алкил), необязательно замещенную -(CH2CH2O)nC(O)-(C1-С6алкил), необязательно замещенную -(OCH2CH2)nNHC(O)-R1, необязательно замещенную -(CH2CH2O)nC(O)-NR1R2, необязательно замещенную -SO2RS, необязательно замещенную S(O)RS, NO2, CN или галоген (F, Cl, Br, I, предпочтительно F или Cl);
каждый из R1 и R2 в ULM-g независимо представляет собой Н или C1-С6алкильную группу, которая может быть необязательно замещена одной или двумя гидроксильными группами или не более чем тремя галогене о держащими группами (предпочтительно фтором);
RS в ULM-g представляет собой C1-С6алкильную группу, необязательно замещенную арильную, гетероарильную или гетероциклическую группу или группу -(CH2)mNR1R2;
каждый из X и X' в ULM-g независимо представляет собой С=O, C=S, -S(O), S(O)2, (предпочтительно как X, так и X' представляют собой С=O);
R2' в ULM-g представляет собой необязательно замещенную -(СН2)n-(C=O)u(NR1)v(SO2)wалкильную группу, необязательно замещенную группу -(СН2)n-(C=O)u(NR1)v(SO2)wNR1NR2N, необязательно замещенный -(CH2)n-(C=O)u(NR1)v(SO2)w-арил, необязательно замещенный -(CH2)n-(C=O)u(NR1)v(SO2)w-гетероарил, необязательно замещенный -(CH2)n-(C=O)vNR1(SO2)w-гетероцикл, необязательно замещенный -NR1-(CH2)n-C(O)u(NR1)v(SO2)w-алкил, необязательно замещенную -NR1-(CH2)n-C(O)u(NR1)v(SO2)w-NR1NR2N, необязательно замещенную -NR1-(CH2)n-C(O)u(NR1)v(SO2)w-NR1C(O)R1N, необязательно замещенный -NR1-(CH2)n-(C=O)u(NR1)v(SO2)w-арил, необязательно замещенный -NR1-(CH2)n-(C=O)u(NR1)v(SO2)w-гетероарил или необязательно замещенный -NR1-(CH2)n-(C=O)vNR1(SO2)w-гетероцикл, необязательно замещенную -XR2'-алкильную группу; необязательно замещенную -XR2'-арильную группу; необязательно замещенную -XR2'-гетероарильную группу; необязательно замещенную -XR2'-гетероциклическую группу; необязательно замещенный;
R3' в ULM-g представляет собой необязательно замещенный алкил, необязательно замещенный -(CH2)n-(O)u(NR1)v(SO2)w-алкил, необязательно замещенный -(CH2)n-C(O)u(NR1)v(SO2)w-NR1NR2N, необязательно замещенный -(CH2)n-C(O)u(NR1)v(SO2)w-NR1C(O)R1N, необязательно замещенный -(CH2)n-C(O)u(NR1)v(SO2)w-C(O)NR1R2, необязательно замещенный -(CH2)n-C(O)u(NR1)v(SO2)w-арил, необязательно замещенный -(CH2)n-C(O)u(NR1)v(SO2)w-гетероарил, необязательно замещенный -(CH2)n-C(O)u(NR1)v(SO2)w-гетероцикл, необязательно замещенный -NR1-(CH2)n-C(O)u(NR1)v(SO2)w-алкил, необязательно замещенный -NR1-(CH2)n-C(O)u(NR1)v(SO2)w-NR1NR2N, необязательно замещенный -NR1-(CH2)n-C(O)u(NR1)v(SO2)w-NR1C(O)R1N, необязательно замещенный -NR1(CH2)n-C(O)u(NR1)v(SO2)w-арил, необязательно замещенный -NR1-(CH2)n-C(O)u(NR1)v(SO2)w-гетероарил, необязательно замещенный -NR1-(CH2)n-C(O)u(NR1)v(SO2)w-гетероцикл, необязательно замещенный -O-(CH2)n-(C=O)u(NR1)v(SO2)w-алкил, необязательно замещенный -O-(CH2)n-(C=O)u(NR1)v(SO2)w-NR1NR2N, необязательно замещенный -О-(CH2)n-(C=O)u(NR1)v(SO2)w-NR1C(O)R1N, необязательно замещенный -O-(СН2)n-(C=O)u(NR1)v(SO2)w-арил, необязательно замещенный -O-(CH2)n-(C=O)u(NR1)v(SO2)w-гетероарил или необязательно замещенный -O-(CH2)n-(C=O)u(NR1)v(SO2)w-гетероцикл; -(CH2)n-(V)n'-(CH2)n-(V)n'-алкильную группу, необязательно замещенную -(СН2)n-(V)n'-(СН2)n-(V)n'-арильную группу, необязательно замещенную -(CH2)n-(V)n'-(CH2)n-(V)n'-гетероарильную группу, необязательно замещенную -(CH2)n-(V)n'-(CH2)n-(V)n'-гетероциклическую группу, необязательно замещенную -(CH2)n-N(R1')(C=O)m'-(V)n'-алкильную группу, необязательно замещенную -(CH2)n-N(R1')(C=O)m'-(V)n'-арильную группу, необязательно замещенную -(CH2)n-N(R1')(C=O)m'-(V)n'-гетероарильную группу, необязательно замещенную -(CH2)n-N(R1')(C=O)m'-(V)n'-гетероциклическую группу, необязательно замещенную -XR3'-алкильную группу; необязательно замещенную -XR3'-арильную группу; необязательно замещенную -XR3'-гетероарильную группу; необязательно замещенную -XR3'-гетероциклическую группу; необязательно замещенные;
каждый из R1N и R2N в ULM-g независимо представляет собой Н, C1-С6алкил, который необязательно замещен одной или двумя гидроксильными группами и не более чем тремя галогенсодержащими группами, или необязательно замещенную -(СН2)n-арильную, -(CH2)n-гетероарильную или -(CH2)n-гетероциклическую группу;
V в ULM-g представляет собой О, S или NR1;
R1 в ULM-g является таким же, как указано выше;
каждый из R1 и R1' в ULM-g независимо представляет собой Н или C1-С3алкильную группу;
каждый из XR2' и XR3' в ULM-g независимо представляет собой необязательно замещенную -(СН2)n-, -(CH2)n-CH(Xv)=CH(Xv)- (цис или транс), -(СН2)n-СН≡СН-, -(CH2CH2O)n-или С3-С6циклоалкильную группу, где Xv представляет собой Н, галоген или C1-С3алкильную группу, которая необязательно замещена;
каждый m в ULM-g независимо равняется 0, 1, 2, 3, 4, 5, 6;
каждый m' в ULM-g независимо равняется 0 или 1;
каждый n в ULM-g независимо равняется 0, 1, 2, 3, 4, 5, 6;
каждый n' в ULM-g независимо равняется 0 или 1;
каждый u в ULM-g независимо равняется 0 или 1;
каждый v в ULM-g независимо равняется 0 или 1;
каждый w в ULM-g независимо равняется 0 или 1; и
любой один или более из R1', R2', R3', X и X' в ULM-g необязательно модифицированы так, чтобы ковалентно связываться с группой РТМ посредством линкерной группы, если РТМ не представляет собой ULM', или если РТМ представляет собой ULM', то любой один или более из R1', R2', R3', X и X' в каждом из ULM и ULM' необязательно модифицированы так, чтобы ковалентно связываться друг с другом непосредственно или посредством линкерной группы, или ее фармацевтически приемлемую соль, стереоизомер, сольват или полиморф.
[240] В любом из аспектов или вариантов осуществления, описанных в данном документе, каждый из ULM и ULM' в случае его присутствия независимо представляет собой группу в соответствии с химической структурой:

где
каждый из R1', R2 и R3' в ULM-h является таким же, как указано выше, и X представляет собой группу С=O, C=S, -S(O) или группу S(O)2, более предпочтительно группу С=O, и
любой один или более из R1', R2' и R3' в ULM-h необязательно модифицированы так, чтобы связываться с линкерной группой, с которой дополнительно ковалентно связана группа РТМ, если РТМ не представляет собой ULM', или если РТМ представляет собой ULM', то любой один или более из R1', R2', R3' в каждом из ULM и ULM' необязательно модифицированы так, чтобы ковалентно связываться друг с другом непосредственно или посредством линкерной группы, или
ее фармацевтически приемлемую соль, энантиомер, диастереомер, сольват или полиморф.
[241] В любом из аспектов или вариантов осуществления, описанных в данном документе, каждый из ULM и ULM' в случае его присутствия независимо соответствует химической структуре:
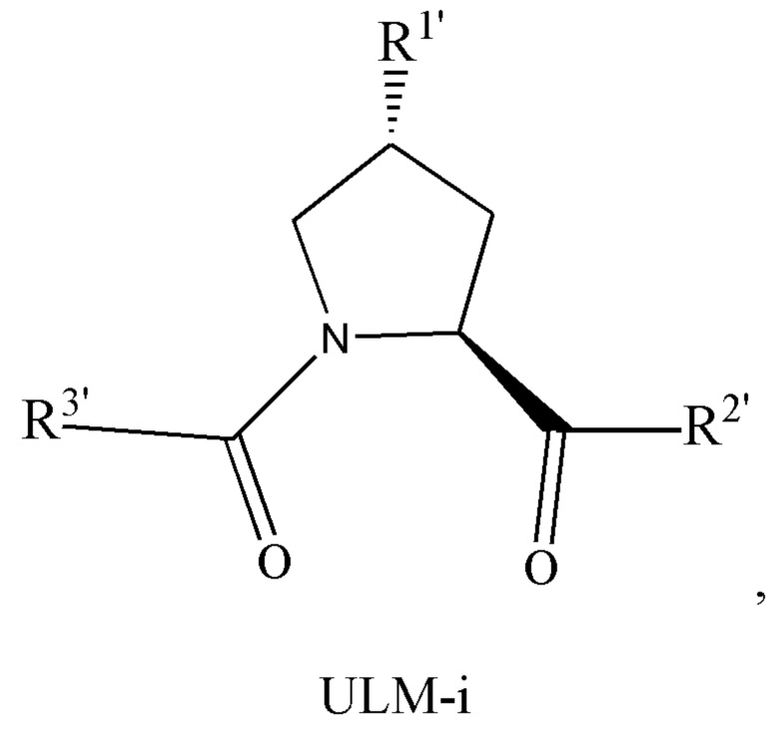
где
любой один или более из R1', R2' и R3' в ULM-I необязательно модифицированы так, чтобы связываться с линкерной группой, с которой дополнительно ковалентно связана группа РТМ, если РТМ не представляет собой ULM', или если РТМ представляет собой ULM', то любой один или более из R1', R2', R3' в каждом из ULM и ULM' необязательно модифицированы так, чтобы ковалентно связываться друг с другом непосредственно или посредством линкерной группы, или
ее фармацевтически приемлемой соли, энантиомеру, диастереомеру, сольвату или полиморфу.
[242] В дополнительных предпочтительных аспектах настоящего изобретения R1' в ULM-g-ULM-i предпочтительно представляет собой гидроксильную группу или группу, которая может быть метаболизирована до гидроксильной или карбоксильной группы, вследствие чего соединение представляет собой форму пролекарства активного соединения. Иллюстративные предпочтительные группы R1' включают, например, -(СН2)nOH, (СН2)n-O-(С1-С6)алкильную группу, -(СН2)nCOOH, -(CH2O)nH, необязательно замещенную -(СН2)nOC(O)-(С1-С6алкил) или необязательно замещенную -(СН2)nC(O)-O-(С1-С6алкил), где n равняется 0 или 1. Если R1' представляет собой или содержит группу карбоновой кислоты, гидроксильную группу или аминогруппу, то гидроксильная группа, группа карбоновой кислоты или аминогруппа (каждая из которых может быть необязательно замещена) могут быть дополнительно химически модифицированы для обеспечения ковалентной связи с линкерной группой, с которой связана группа РТМ (в том числе группа ULM');
[243] X и X' в случае ее присутствия в ULM-g и ULM-h предпочтительно представляют собой группу С=O, C=S, -S(O) или группу S(O)2, более предпочтительно группу С=O;
[244] R2' в ULM-g-ULM-i предпочтительно представляет собой необязательно замещенный -NR1-Т-арильную, необязательно замещенную -NR1-T-гетероарильную группу или необязательно замещенный -NR1-Т-гетероцикл, где R1 представляет собой Н или СН3, предпочтительно Н, и Т представляет собой необязательно замещенную группу -(СН2)n, где каждая из метиленовых групп может быть необязательно замещена одним или двумя заместителями, предпочтительно выбранными из галогена, боковой цепи аминокислоты, как далее описано в данном документе, или C1-С3алкильной группой, предпочтительно одной или двумя метальными группами, которые могут быть необязательно замещены; и n равняется 0-6, зачастую 0, 1, 2 или 3, предпочтительно 0 или 1. В качестве альтернативы, Т может также представлять собой группу -(CH2O)n-, группу -(OCH2)n, группу -(CH2CH2O)n-, группу -(OCH2CH2)n-, все группы из которых необязательно замещены.
[245] Предпочтительные арильные группы для R2' в ULM-g-ULM-i включают необязательно замещенные фенильные или нафтильные группы, предпочтительно фенильные группы, где фенильная или нафтильная группа необязательно соединены с РТМ (в том числе группой ULM') посредством линкерной группы и/или необязательно замещены галогеном (предпочтительно F или Cl), амином, моноалкил- или диалкиламином (предпочтительно диметиламином), F, Cl, ОН, СООН, C1-С6алкилом, предпочтительно СН3, CF3, ОМе, OCF3, NO2 или группой CN (замещение каждой из которых может быть в орто-, мета- и/или пара- положениях фенильного кольца, предпочтительно пара-), необязательно замещенную фенильную группу (фенильная группа как таковая необязательно соединена с группой РТМ, в том числе группой ULM' посредством линкерной группы), и/или при этом она необязательно замещена по меньшей мере одним из F, Cl, ОН, СООН, СН3, CF3, ОМе, OCF3, NO2 или группы CN (в орто-, мета- и/или пара- положениях фенильного кольца, предпочтительно пара-), нафтильную группу, которая может быть необязательно замещена, необязательно замещенный гетероарил, предпочтительно необязательно замещенный изоксазол, в том числе метилзамещенный изоксазол, необязательно замещенный оксазол, в том числе метилзамещенный оксазол, необязательно замещенный тиазол, в том числе метилзамещенный тиазол, необязательно замещенный изотиазол, в том числе метилзамещенный изотиазол, необязательно замещенный пиррол, в том числе метилзамещенный пиррол, необязательно замещенный имидазол, в том числе метилимидазол, необязательно замещенный бензимидазол или метоксибензилимидазол, необязательно замещенный оксимидазол или метилоксимидазол, необязательно замещенную диазольную группу, в том числе метилдиазольную группу, необязательно замещенную триазольную группу, в том числе метилзамещенную триазольную группу, необязательно замещенную пиридиновую группу, в том числе галоген- (предпочтительно F) или метилзамещенную пиридиновую группу или оксапиридиновую группу (где пиридиновая группа соединена с фенильной группой с помощью атома кислорода), необязательно замещенный фуран, необязательно замещенный бензофуран, необязательно замещенный дигидробензофуран, необязательно замещенный индол, индолизин или азаиндолизин (2, 3 или 4-азаиндолизин), необязательно замещенный хинолин, необязательно замещенную группу в соответствии с химической структурой:



где
Sc в ULM-g-ULM-i представляет собой CHRSS, NRURE или О;
RHET в ULM-g-ULM-i представляет собой Н, CN, NO2, галоген (предпочтительно Cl или F), необязательно замещенный C1-С6алкил (предпочтительно замещенный одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами (например, CF3), необязательно замещенный O(С1-С6алкил) (предпочтительно замещенный одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами) или необязательно замещенную ацетиленовую группу -C≡C-Ra, где Ra представляет собой Н или C1-С6алкильную группу (предпочтительно C1-С3алкил);
RSS в ULM-g-ULM-i представляет собой Н, CN, NO2, галоген (предпочтительно F или Cl), необязательно замещенный C1-С6алкил (предпочтительно замещенный одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами), необязательно замещенный O-(C1-С6алкил) (предпочтительно замещенный одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами) или необязательно замещенный -С(O)(С1-С6алкил) (предпочтительно замещенный одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами);
RURE в ULM-g-ULM-i представляет собой H, C1-С6алкил (предпочтительно Н или C1-С3алкил) или -С(O)(С1-С6алкил), каждая группа из которых необязательно замещена одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами, предпочтительно фтором, или необязательно замещенную фенильную группу, необязательно замещенный гетероарил или необязательно замещенный гетероцикл, предпочтительно, например, пиперидин, морфолин, пирролидин, тетрагидрофуран);
RPRO в ULM-g-ULM-i представляет собой Н, необязательно замещенный C1-С6алкил или необязательно замещенный арил (фенил или нафтил), гетероарильную или гетероциклическую группу, выбранную из группы, состоящей из оксазола, изоксазола, тиазола, изотиазола, имидазола, диазола, оксимидазола, пиррола, пирролидина, фурана, дигидрофурана, тетрагидрофурана, тиена, дигидротиена, тетрагидротиена, пиридина, пиперидина, пиперазина, морфолина, хинолина (при этом каждый предпочтительно замещен C1-С3алкильной группой, предпочтительно метальной группой или галогенсодержащей группой, предпочтительно F или Cl), бензофурана, индола, индолизина, азаиндолизина;
каждый из RPRO1 и RPRO2 в ULM-g-ULM-i независимо представляет собой Н, необязательно замещенную C1-С3алкильную группу или вместе образуют кетогруппу, и
каждый n в ULM-g-ULM-i независимо равняется 0, 1, 2, 3, 4, 5 или 6 (предпочтительно 0 или 1), или представляет собой необязательно замещенный гетероцикл, предпочтительно тетрагидрофуран, тетрагидротиен, пиперидин, пиперазин или морфолин (каждая группа из которых, если замещена, предпочтительно замещена метилом или галогеном (F, Br, Cl)), каждая группа из которых может быть необязательно присоединена к группе РТМ (в том числе группе ULM') посредством линкерной группы.
[246] В определенных предпочтительных аспектах  в ULM-g-ULM-i представляет собой группу
в ULM-g-ULM-i представляет собой группу

где RPRO и n в ULM-g-ULM-i являются такими же, как указано выше.
[247] Предпочтительные гетероарильные группы для R2 в ULM-g-ULM-i включают необязательно замещенный хинолин (который может быть присоединен к фармакофору или замещен при любом атоме углерода в хинолиновом кольце), необязательно замещенный индол, необязательно замещенный индолизин, необязательно замещенный азаиндолизин, необязательно замещенный бензофуран, в том числе необязательно замещенный бензофуран, необязательно замещенный изоксазол, необязательно замещенный тиазол, необязательно замещенный изотиазол, необязательно замещенный тиофен, необязательно замещенный пиридин (2-, 3 или 4-пиридин), необязательно замещенный имидазол, необязательно замещенный пиррол, необязательно замещенный диазол, необязательно замещенный триазол, тетразол, необязательно замещенный оксимидазол или группу в соответствии с химической структурой:



где
Sc в ULM-g-ULM-i представляет собой CHRSS, NRURE или О;
RHET в ULM-g-ULM-i представляет собой Н, CN, NO2, галоген (предпочтительно Cl или F), необязательно замещенный C1-С6алкил (предпочтительно замещенный одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами (например, CF3)), необязательно замещенный O(С1-С6алкил) (предпочтительно замещенный одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами) или необязательно замещенную ацетиленовую группу -C≡C-Ra, где Ra в ULM-g-ULM-i представляет собой Н или C1-С6алкильную группу (предпочтительно C1-С3алкил);
RSS в ULM-g-ULM-i представляет собой Н, CN, NO2, галоген (предпочтительно F или Cl), необязательно замещенный C1-С6алкил (предпочтительно замещенный одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами), необязательно замещенный O-(C1-С6алкил) (предпочтительно замещенный одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами) или необязательно замещенный -С(O)(С1-С6алкил) (предпочтительно замещенный одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами);
RURE в ULM-g-ULM-i представляет собой Н, C1-С6алкил (предпочтительно Н или C1-С3алкил) или -С(O)(С1-С6алкил), каждая группа из которых необязательно замещена одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами, предпочтительно фтором, или необязательно замещенный гетероцикл, например, пиперидин, морфолин, пирролидин, тетрагидрофуран, тетрагидротиофен, пиперидин, пиперазин, каждый из которых необязательно замещен, и
YC в ULM-g-ULM-i представляет собой N или C-RYC, где RYC представляет собой Н, ОН, CN, NO2, галоген (предпочтительно Cl или F), необязательно замещенный C1-С6алкил (предпочтительно замещенный одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами (например, CF3)), необязательно замещенный O(С1-С6алкил) (предпочтительно замещенный одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами) или необязательно замещенную ацетиленовую группу -C≡C-Ra, где Ra представляет собой Н или C1-С6алкильную группу (предпочтительно C1-С3алкил), каждая группа из которых может быть необязательно соединена с группой РТМ (в том числе группой ULM') посредством линкерной группы.
[248] Предпочтительные гетероциклические группы для R2' в ULM-g-ULM-i включают тетрагидрофуран, тетрагидротиен, тетрагидрохинолин, пиперидин, пиперазин, пирролидин, морфолин, океан или тиан, каждая группа из которых может быть необязательно замещена, или группу в соответствии с химической структурой:

предпочтительно группу 
где
RPRO в ULM-g-ULM-i представляет собой Н, необязательно замещенный C1-С6алкил или необязательно замещенную арильную, гетероарильную или гетероциклическую группу;
каждый из RPRO1 и RPRO2 в ULM-g-ULM-i независимо представляет собой Н, необязательно замещенную C1-С3алкильную группу или вместе образуют кетогруппу; и
каждый n в ULM-g-ULM-i независимо равняется 0, 1, 2, 3, 4, 5 или 6 (зачастую 0 или 1), каждая группа из которых может быть необязательно соединена с группой РТМ (в том числе группой ULM') посредством линкерной группы.
[249] Предпочтительные заместители R2' в ULM-g-ULM-i также включают конкретно (и без ограничения конкретным раскрытым соединением) заместители R2', которые обнаружены в определенных соединениях, раскрытых в данном документе (которые включают конкретные соединения, которые раскрыты в настоящем описании и прилагаемых к нему графических материалах). Каждый из таких заместителей R2' может применяться совместно с любым количеством заместителей R3', которые также раскрыты в данном документе.
[250] R3 в ULM-g-ULM-i предпочтительно представляет собой необязательно замещенный -Т-арил, необязательно замещенный -Т-гетероарил, необязательно замещенный -Т-гетероцикл, необязательно замещенный -NR1-Т-арил, необязательно замещенный -NR1-Т-гетероарил или необязательно замещенный -NR1-Т-гетероцикл, где R1 представляет собой Н или C1-С3алкильную группу, предпочтительно Н или СН3, Т представляет собой необязательно замещенную группу -(СН2)n, где каждая из метиленовых групп может быть необязательно замещена одним или двумя заместителями, предпочтительно выбранными из галогена, C1-С3алкильной группы или боковой цепи аминокислоты, как далее описано в данном документе, предпочтительно метила, который может быть необязательно замещен; и n равняется 0-6, зачастую 0, 1, 2 или 3, предпочтительно 0 или 1. В качестве альтернативы, Т может также представлять собой группу -(CH2O)n-, группу -(ОСН2)n-, группу -(CH2CH2O)n-, группу -(OCH2CH2)n-, каждая группа из которых необязательно замещена.
[251] Предпочтительные арильные группы для R3 в ULM-g-ULM-i включают необязательно замещенные фенильные или нафтильные группы, предпочтительно фенильные группы, где фенильная или нафтильная группа необязательно соединены с группой РТМ (в том числе группой ULM') посредством линкерной группы и/или необязательно замещены галогеном (предпочтительно F или Cl), амином, моноалкил- или диалкиламином (предпочтительно диметиламином), амидогруппой (предпочтительно группой -(CH2)m-NR1C(O)R2, где m, R1 и R2 являются такими же, как указано выше), галогеном (зачастую F или Cl), ОН, СН3, CF3, ОМе, OCF3, NO2, CN или группой S(O)2RS (RS представляет собой C1-С6алкильную группу, необязательно замещенную арильную, гетероарильную или гетероциклическую группу или группу -(CH2)mNR1R2), замещение каждой из которых может быть в орто-, мета- и/или пара-положениях фенильного кольца, предпочтительно пара-, или арил (предпочтительно фенил), гетероарил или гетероцикл. Предпочтительно указанная замещающая фенильная группа представляет собой необязательно замещенную фенильную группу (т.е. замещающая фенильная группа сама по себе предпочтительно замещена по меньшей мере одним из F, Cl, ОН, SH, СООН, СН3, CF3, ОМе, OCF3, NO2, CN или линкерной группой, к которой присоединена группа РТМ (в том числе группа ULM'), где замещение происходит в орто-, мета- и/или пара-положениях фенильного кольца, предпочтительно пара-), нафтильную группу, которая может быть необязательно замещена, в том числе как описано выше, необязательно замещенный гетероарил, предпочтительно необязательно замещенный изоксазол, в том числе метилзамещенный изоксазол, необязательно замещенный оксазол, в том числе метилзамещенный оксазол, необязательно замещенный тиазол, в том числе метилзамещенный тиазол, необязательно замещенный пиррол, в том числе метилзамещенный пиррол, необязательно замещенный имидазол, в том числе метилимидазол, бензилимидазол или метоксибензилимидазол, оксимидазол или метилоксимидазол, необязательно замещенную диазольную группу, в том числе метилдиазольную группу, необязательно замещенную триазольную группу, в том числе метилзамещенную триазольную группу, пиридиновую группу, в том числе галоген- (предпочтительно F) или метилзамещенную пиридиновую группу или оксапиридиновую группу (где пиридиновая группа соединена с фенильной группой с помощью атома кислорода), или необязательно замещенный гетероцикл (тетрагидрофуран, тетрагидротиофен, пирролидин, пиперидин, морфолин, пиперазин, тетрагидрохинолин, океан или тиан). Каждая из арильной, гетероарильной или гетероциклической групп может быть необязательно соединена с группой РТМ (в том числе группой ULM') с помощью линкерной группы.
[252] Предпочтительные гетероарильные группы для R3 в ULM-g-ULM-i включают необязательно замещенный хинолин (который может быть присоединен к фармакофору или замещен при любом атоме углерода в хинолиновом кольце), необязательно замещенный индол (в том числе дигидроиндол), необязательно замещенный индолизин, необязательно замещенный азаиндолизин (2, 3 или 4-азаиндолизин), необязательно замещенный бензимидазол, бензодиазол, бензоксофуран, необязательно замещенный имидазол, необязательно замещенный изоксазол, необязательно замещенный оксазол (предпочтительно метилзамещенный), необязательно замещенный диазол, необязательно замещенный триазол, тетразол, необязательно замещенный бензофуран, необязательно замещенный тиофен, необязательно замещенный тиазол (предпочтительно метил- и/или тиолзамещенный), необязательно замещенный изотиазол, необязательно замещенный триазол (предпочтительно 1,2,3-триазол, замещенный метильной группой, триизопропилсилильной группой, необязательно замещенной -(CH2)m-O-C1-С6алкильной группой или необязательно замещенной -(СН2)m-С(O)-O-С1-С6алкильной группой), необязательно замещенный пиридин (2-, 3 или 4-пиридин) или группу в соответствии с химической структурой:



где
Sc в ULM-g-ULM-i представляет собой CHRSS, NRURE или О;
RHET в ULM-g-ULM-i представляет собой Н, CN, NO2, галоген (предпочтительно Cl или F), необязательно замещенный C1-С6алкил (предпочтительно замещенный одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами (например, CF3), необязательно замещенный O(С1-С6алкил) (предпочтительно замещенный одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами) или необязательно замещенную ацетиленовую группу -C≡C-Ra, где Ra представляет собой Н или C1-С6алкильную группу (предпочтительно C1-С3алкил);
RSS в ULM-g-ULM-i представляет собой Н, CN, NO2, галоген (предпочтительно F или Cl), необязательно замещенный C1-С6алкил (предпочтительно замещенный одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами), необязательно замещенный O-(C1-С6алкил) (предпочтительно замещенный одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами) или необязательно замещенный -С(O)(С1-С6алкил) (предпочтительно замещенный одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами);
RURE в ULM-g-ULM-i представляет собой Н, C1-С6алкил (предпочтительно Н или C1-С3алкил) или -С(O)(С1-С6алкил), каждая группа из которых необязательно замещена одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами, предпочтительно фтором, или необязательно замещенный гетероцикл, например, пиперидин, морфолин, пирролидин, тетрагидрофуран, тетрагидротиофен, пиперидин, пиперазин, каждый из которых необязательно замещен, и
YC в ULM-g-ULM-i представляет собой N или C-RYC, где RYC представляет собой Н, ОН, CN, NO2, галоген (предпочтительно Cl или F), необязательно замещенный C1-С6алкил (предпочтительно замещенный одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами (например, CF3)), необязательно замещенный O(С1-С6алкил) (предпочтительно замещенный одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами) или необязательно замещенную ацетиленовую группу -C≡C-Ra, где Ra представляет собой Н или C1-С6алкильную группу (предпочтительно C1-С3алкил). Каждая из указанных гетероарильных групп может быть необязательно соединена с группой РТМ (в том числе группой ULM') посредством линкерной группы.
[253] Предпочтительные гетероциклические группы для R3 в ULM-g-ULM-i включают тетрагидрохинолин, пиперидин, пиперазин, пирролидин, морфолин, тетрагидрофуран, тетрагидротиофен, океан и тиан, каждая группа из которых может быть необязательно замещена, или группу в соответствии с химической структурой:
 или
или 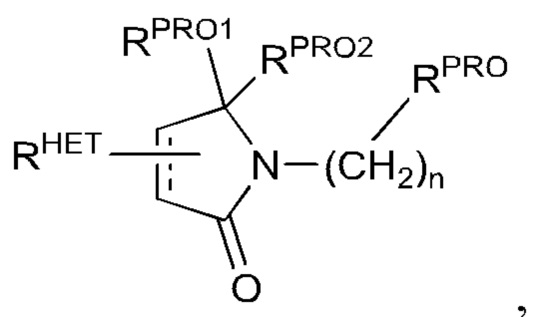 предпочтительно группу
предпочтительно группу 
где
RPRO в ULM-g-ULM-i представляет собой Н, необязательно замещенный C1-С6алкил или необязательно замещенный арил (фенил или нафтил), гетероарильную или гетероциклическую группу, выбранную из группы, состоящей из оксазола, изоксазола, тиазола, изотиазола, имидазола, диазола, оксимидазола, пиррола, пирролидина, фурана, дигидрофурана, тетрагидрофурана, тиена, дигидротиена, тетрагидротиена, пиридина, пиперидина, пиперазина, морфолина, хинолина (при этом каждый предпочтительно замещен C1-С3алкильной группой, предпочтительно метальной группой или галогенсодержащей группой, предпочтительно F или Cl), бензофурана, индола, индолизина, азаиндолизина;
каждый из RPRO1 и RPRO2 в ULM-g-ULM-i независимо представляет собой Н, необязательно замещенную C1-С3алкильную группу или вместе образуют кетогруппу, и
каждый n в ULM-g-ULM-i равняется 0, 1, 2, 3, 4, 5 или 6 (предпочтительно 0 или 1), где каждая из указанных гетероциклических групп может быть необязательно соединена с группой РТМ (в том числе группой ULM') посредством линкерной группы.
[254] Предпочтительные заместители R3' в ULM-g-ULM-i также включают конкретно (и без ограничения конкретным раскрытым соединением) заместители R3', которые обнаружены в определенных соединениях, раскрытых в данном документе (которые включают конкретные соединения, которые раскрыты в настоящем описании и прилагаемых к нему графических материалах). Каждый из таких заместителей R3' может применяться совместно с любым количеством заместителей R2', которые также раскрыты в данном документе.
[255] В определенных альтернативных предпочтительных вариантах осуществления R2' в ULM-g-ULM-i представляет собой необязательно замещенную -NR1-XR2'-алкильную группу, -NR1-XR2'-арильную группу; необязательно замещенный -NR1- XR2'-НЕТ, необязательно замещенный -NR1-XR2'-арил-НЕТ или необязательно замещенный -NR1-XR2'-НЕТ-арил,
где
R1 в ULM-g-ULM-i представляет собой H или C1-С3алкильную группу (предпочтительно Н);
XR2' в ULM-g-ULM-i представляет собой необязательно замещенную -(СН2)n-, -(CH2)n-CH(Xv)=CH(Xv)- (цис или транс), -(СН2)n-СН≡СН-, -(CH2CH2O)n- или С3-С6циклоалкильную группу; и
Xv в ULM-g-ULM-i представляет собой Н, галоген или C1-С3алкильную группу, которая необязательно замещена одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами;
алкил в ULM-g-ULM-i представляет собой необязательно замещенную С1-С10алкильную (предпочтительно C1-С6алкильную) группу (в определенных предпочтительных вариантах осуществления алкильная группа содержит на конце галогенсодержащую группу, зачастую Cl или Br);
арил в ULM-g-ULM-i представляет собой необязательно замещенную фенильную или нафтильную группу (предпочтительно фенильную группу); и
НЕТ в ULM-g-ULM-i представляет собой необязательно замещенный оксазол, изоксазол, тиазол, изотиазол, имидазол, диазол, оксимидазол, пиррол, пирролидин, фуран, дигидрофуран, тетрагидрофуран, тиен, дигидротиен, тетрагидротиен, пиридин, пиперидин, пиперазин, морфолин, бензофуран, индол, индолизин, азаиндолизин, хинолин (при этом если замещен, то каждый предпочтительно замещен C1-С3алкильной группой, предпочтительно метильной группой или галогенсодержащей группой, предпочтительно F или Cl) или группу в соответствии с химической структурой:
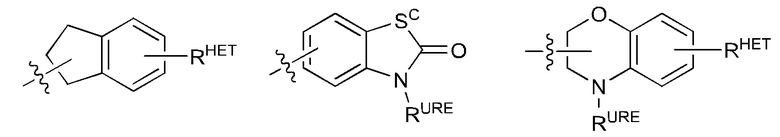


Sc в ULM-g-ULM-i представляет собой CHRSS, NRURE или О;
RHET в ULM-g-ULM-i представляет собой H, CN, NO2, галоген (предпочтительно Cl или F), необязательно замещенный C1-С6алкил (предпочтительно замещенный одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами (например, CF3), необязательно замещенный O(С1-С6алкил) (предпочтительно замещенный одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами) или необязательно замещенную ацетиленовую группу -C≡C-Ra, где Ra представляет собой Н или C1-С6алкильную группу (предпочтительно C1-С3алкил);
RSS в ULM-g-ULM-i представляет собой Н, CN, NO2, галоген (предпочтительно F или Cl), необязательно замещенный C1-С6алкил (предпочтительно замещенный одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами), необязательно замещенный O-(C1-С6алкил) (предпочтительно замещенный одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами) или необязательно замещенный -С(O)(С1-С6алкил) (предпочтительно замещенный одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами);
RURE в ULM-g-ULM-i представляет собой Н, C1-С6алкил (предпочтительно Н или C1-С3алкил) или -С(O)(С1-С6алкил), каждая группа из которых необязательно замещена одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами, предпочтительно фтором, или необязательно замещенный гетероцикл, например, пиперидин, морфолин, пирролидин, тетрагидрофуран, тетрагидротиофен, пиперидин, пиперазин, каждый из которых необязательно замещен;
YC в ULM-g-ULM-i представляет собой N или C-RYC, где RYC представляет собой Н, ОН, CN, NO2, галоген (предпочтительно Cl или F), необязательно замещенный C1-С6алкил (предпочтительно замещенный одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами (например, CF3), необязательно замещенный O(С1-С6алкил) (предпочтительно замещенный одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами) или необязательно замещенную ацетиленовую группу -C≡C-Ra, где Ra представляет собой Н или C1-С6алкильную группу (предпочтительно C1-С3алкил);
RPRO в ULM-g-ULM-i представляет собой Н, необязательно замещенный C1-С6алкил или необязательно замещенный арил (фенил или нафтил), гетероарильную или гетероциклическую группу, выбранную из группы, состоящей из оксазола, изоксазола, тиазола, изотиазола, имидазола, диазола, оксимидазола, пиррола, пирролидина, фурана, дигидрофурана, тетрагидрофурана, тиена, дигидротиена, тетрагидротиена, пиридина, пиперидина, пиперазина, морфолина, хинолина (при этом каждый предпочтительно замещен C1-С3алкильной группой, предпочтительно метальной группой или галогенсодержащей группой, предпочтительно F или Cl), бензофурана, индола, индолизина, азаиндолизина;
каждый из RPRO1 и RPRO2 в ULM-g-ULM-i независимо представляет собой Н, необязательно замещенную C1-С3алкильную группу или вместе образуют кетогруппу, и
каждый n в ULM-g-ULM-i независимо равняется 0, 1, 2, 3, 4, 5 или 6 (предпочтительно 0 или 1).
[256] Каждая из указанных групп может быть необязательно соединена с группой РТМ (в том числе группой ULM') посредством линкерной группы.
[257] В определенных альтернативных предпочтительных вариантах осуществления настоящего изобретения R3' в ULM-g-ULM-i представляет собой необязательно замещенную группу -(CH2)n-(V)n'-(CH2)n-(V)n'-RS3', необязательно замещенную группу -(CH2)n-N(R1')(C=O)m'-(V)n'-RS3', необязательно замещенную -XR3'-алкильную группу, необязательно замещенную -XR3' -арильную группу; необязательно замещенную группу -XR3'-НЕТ, необязательно замещенную группу -XR3'-арил-НЕТ или необязательно замещенную -XR3' -НЕТ-арильную группу,
где
RS3' представляет собой необязательно замещенную алкильную группу (C1-C10, предпочтительно C1-С6алкил), необязательно замещенную арильную группу или группу НЕТ;
R1' представляет собой Н или C1-С3алкильную группу (предпочтительно Н);
V представляет собой О, S или NR1';
XR3' представляет собой -(СН2)n-, -(CH2CH2O)n-, -(CH2)n-CH(Xv)=CH(Xv)- (цис или транс), -(СН2)n-СН≡СН- или С3-С6циклоалкильную группу, все из которых необязательно замещены;
Xv представляет собой Н, галоген или C1-С3алкильную группу, которая необязательно замещена одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами;
алкил представляет собой необязательно замещенную C1-С10алкильную (предпочтительно C1-С6алкильную) группу (в определенных предпочтительных вариантах осуществления алкильная группа содержит на конце галогенсодержащую группу, зачастую Cl или Br);
арил представляет собой необязательно замещенную фенильную или нафтильную группу (предпочтительно фенильную группу); и
НЕТ представляет собой необязательно замещенный оксазол, изоксазол, тиазол, изотиазол, имидазол, диазол, оксимидазол, пиррол, пирролидин, фуран, дигидрофуран, тетрагидрофуран, тиен, дигидротиен, тетрагидротиен, пиридин, пиперидин, пиперазин, морфолин, бензофуран, индол, индолизин, азаиндолизин, хинолин (при этом если замещен, то каждый предпочтительно замещен C1-С3алкильной группой, предпочтительно метильной группой или галогенсодержащей группой, предпочтительно F или Cl) или группу в соответствии с химической структурой:



Sc в ULM-g-ULM-i представляет собой CHRSS, NRURE или О;
RHET в ULM-g-ULM-i представляет собой Н, CN, NO2, галоген (предпочтительно Cl или F), необязательно замещенный C1-С6алкил (предпочтительно замещенный одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами (например, CF3), необязательно замещенный O(С1-С6алкил) (предпочтительно замещенный одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами) или необязательно замещенную ацетиленовую группу -C≡C-Ra, где Ra представляет собой Н или C1-С6алкильную группу (предпочтительно C1-С3алкил);
RSS в ULM-g-ULM-i представляет собой Н, CN, NO2, галоген (предпочтительно F или Cl), необязательно замещенный C1-С6алкил (предпочтительно замещенный одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами), необязательно замещенный O-(C1-С6алкил) (предпочтительно замещенный одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами) или необязательно замещенный -С(O)(С1-С6алкил) (предпочтительно замещенный одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами);
RURE в ULM-g-ULM-i представляет собой H, C1-С6алкил (предпочтительно Н или C1-С3алкил) или -С(O)(С0-С6алкил), каждая группа из которых необязательно замещена одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами, предпочтительно фтором, или необязательно замещенный гетероцикл, например, пиперидин, морфолин, пирролидин, тетрагидрофуран, тетрагидротиофен, пиперидин, пиперазин, каждый из которых необязательно замещен;
YC в ULM-g-ULM-i представляет собой N или C-RYC, где RYC представляет собой Н, ОН, CN, NO2, галоген (предпочтительно Cl или F), необязательно замещенный C1-С6алкил (предпочтительно замещенный одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами (например, CF3), необязательно замещенный O(С1-С6алкил) (предпочтительно замещенный одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами) или необязательно замещенную ацетиленовую группу -C≡C-Ra, где Ra представляет собой Н или C1-С6алкильную группу (предпочтительно C1-С3алкил);
RPRO в ULM-g-ULM-i представляет собой Н, необязательно замещенный C1-С6алкил или необязательно замещенный арил (фенил или нафтил), гетероарильную или гетероциклическую группу, выбранную из группы, состоящей из оксазола, изоксазола, тиазола, изотиазола, имидазола, диазола, оксимидазола, пиррола, пирролидина, фурана, дигидрофурана, тетрагидрофурана, тиена, дигидротиена, тетрагидротиена, пиридина, пиперидина, пиперазина, морфолина, хинолина (при этом каждый предпочтительно замещен C1-С3алкильной группой, предпочтительно метальной группой или галогенсодержащей группой, предпочтительно F или Cl), бензофурана, индола, индолизина, азаиндолизина;
каждый из RPRO1 и RPRO2 в ULM-g-ULM-i независимо представляет собой Н, необязательно замещенную C1-С3алкильную группу или вместе образуют кетогруппу;
каждый n в ULM-g-ULM-i независимо равняется 0, 1, 2, 3, 4, 5 или 6 (предпочтительно 0 или 1);
каждый m' в ULM-g-ULM-i равняется 0 или 1; и
каждый n' в ULM-g-ULM-i равняется 0 или 1;
где каждое из указанных соединений, предпочтительно при алкильных, арильных или Het-группах, необязательно соединено с группой РТМ (в том числе группой ULM') посредством линкерной группы.
[258] В альтернативных вариантах осуществления R3' в ULM-g-ULM-i представляет собой -(СН2)n-арил, -(CH2CH2O)n-арил, -(CH2)n-HET или -(CH2CH2O)n-НЕТ,
где
указанный арил в ULM-g-ULM-i представляет собой фенил, который необязательно замещен одним или двумя заместителями, где указанный(-ые) заместитель(-ли) предпочтительно выбран(-ы) из -(СН2)nOH, C1-С6алкила, который сам по себе дополнительно необязательно замещен CN, галогеном (не более чем тремя галогенсодержащими группами), ОН, -(СН2)nO(С1-С6)алкилом, амином, моно- или ди-(C1-С6алкил)амином, где алкильная группа на амине необязательно замещена 1 или 2 гидроксильными группами или не более чем тремя галогенсодержащими группами (предпочтительно F, Cl), или
указанная арильная группа в ULM-g-ULM-i замещена -(СН2)nOH, -(СН2)n-O-(С1-С6)алкилом, -(СН2)n-O-(СН2)n-(С1-С6)алкилом, -(СН2)n-С(O)(С0-С6)алкилом, (СН2)n-С(O)O(С0-С6)алкилом, -(СН2)n-ОС(O)(С0-С6)алкилом, амином, моно- или ди-(С1-С6алкил)амином, где алкильная группа на амине необязательно замещена 1 или 2 гидроксильными группами или не более чем тремя галогенсодержащими группами (предпочтительно F, Cl), CN, NO2, необязательно замещенной -(CH2)n-(V)m'-CH2)n-(V)m'-(С1-С6)алкильной группой, группой-(V)m'-(CH2CH2O)n-RPEG, где V представляет собой О, S или NR1', R1' представляет собой Н или C1-С3алкильную группу (предпочтительно Н), и RPEG представляет собой Н или C1-С6алкильную группу, которая необязательно замещена (в том числе необязательно замещена карбоксильной группой), или
указанная арильная группа в ULM-g-ULM-i необязательно замещена гетероциклом, в том числе гетероарилом, выбранным из группы, состоящей из оксазола, изоксазола, тиазола, изотиазола, имидазола, диазола, оксимидазола, пиррола, пирролидина, фурана, дигидрофурана, тетрагидрофурана, тиена, дигидротиена, тетрагидротиена, пиридина, пиперидина, пиперазина, морфолина, хинолина, бензофурана, индола, индолизина, азаиндолизина (при этом если замещен, то каждый предпочтительно замещен C1-С3алкильной группой, предпочтительно метальной группой или галогенсодержащей группой, предпочтительно F или Cl) или группой в соответствии с химической структурой:


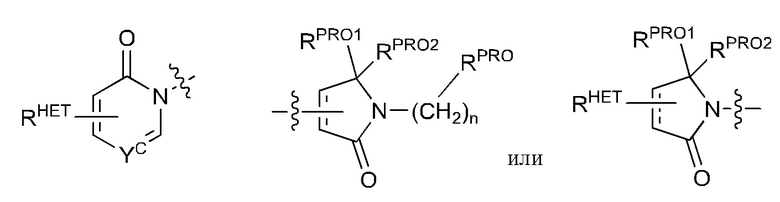
Sc в ULM-g-ULM-i представляет собой CHRSS, NRURE или О;
RHET в ULM-g-ULM-i представляет собой Н, CN, NO2, галоген (предпочтительно Cl или F), необязательно замещенный C1-С6алкил (предпочтительно замещенный одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами (например, CF3), необязательно замещенный O(С1-С6алкил) (предпочтительно замещенный одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами) или необязательно замещенную ацетиленовую группу -C≡C-Ra, где Ra представляет собой Н или C1-С6алкильную группу (предпочтительно C1-С3алкил);
RSS в ULM-g-ULM-i представляет собой Н, CN, NO2, галоген (предпочтительно F или Cl), необязательно замещенный C1-С6алкил (предпочтительно замещенный одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами), необязательно замещенный O-(C1-С6алкил) (предпочтительно замещенный одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами) или необязательно замещенный -С(O)(С1-С6алкил) (предпочтительно замещенный одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами);
RURE в ULM-g-ULM-i представляет собой Н, C1-С6алкил (предпочтительно Н или C1-С3алкил) или -С(O)(С0-С6алкил), каждая группа из которых необязательно замещена одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами, предпочтительно фтором, или необязательно замещенный гетероцикл, например, пиперидин, морфолин, пирролидин, тетрагидрофуран, тетрагидротиофен, пиперидин, пиперазин, каждый из которых необязательно замещен;
YC в ULM-g-ULM-i представляет собой N или C-RYC, где RYC представляет собой Н, ОН, CN, NO2, галоген (предпочтительно Cl или F), необязательно замещенный C1-С6алкил (предпочтительно замещенный одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами (например, CF3), необязательно замещенный O(С1-С6алкил) (предпочтительно замещенный одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами) или необязательно замещенную ацетиленовую группу -C≡C-Ra, где Ra представляет собой Н или C1-С6алкильную группу (предпочтительно C1-С3алкил);
RPRO в ULM-g-ULM-i представляет собой Н, необязательно замещенный C1-С6алкил или необязательно замещенный арил (фенил или нафтил), гетероарильную или гетероциклическую группу, выбранную из группы, состоящей из оксазола, изоксазола, тиазола, изотиазола, имидазола, диазола, оксимидазола, пиррола, пирролидина, фурана, дигидрофурана, тетрагидрофурана, тиена, дигидротиена, тетрагидротиена, пиридина, пиперидина, пиперазина, морфолина, хинолина (при этом каждый предпочтительно замещен C1-С3алкильной группой, предпочтительно метальной группой или галогенсодержащей группой, предпочтительно F или Cl), бензофурана, индола, индолизина, азаиндолизина;
каждый из RPRO1 и RPRO2 в ULM-g-ULM-i независимо представляет собой Н, необязательно замещенную C1-С3алкильную группу или вместе образуют кетогруппу;
НЕТ в ULM-g-ULM-i предпочтительно представляет собой оксазол, изоксазол, тиазол, изотиазол, имидазол, диазол, оксимидазол, пиррол, пирролидин, фуран, дигидрофуран, тетрагидрофуран, тиен, дигидротиен, тетрагидротиен, пиридин, пиперидин, пиперазин, морфолин, хинолин (при этом каждый предпочтительно замещен C1-С3алкильной группой, предпочтительно метильной группой или галогенсодержащей группой, предпочтительно F или Cl), бензофуран, индол, индолизин, азаиндолизин или группу в соответствии с химической структурой:

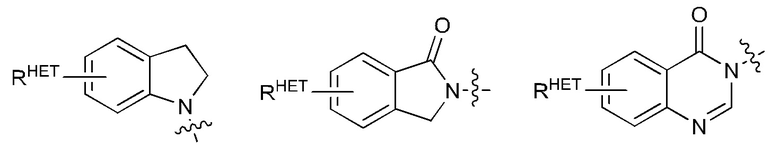

Sc в ULM-g-ULM-i представляет собой CHRSS, NRURE или О;
RHET в ULM-g-ULM-i представляет собой Н, CN, NO2, галоген (предпочтительно Cl или F), необязательно замещенный C1-С6алкил (предпочтительно замещенный одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами (например, CF3), необязательно замещенный O(С1-С6алкил) (предпочтительно замещенный одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами) или необязательно замещенную ацетиленовую группу -C≡C-Ra, где Ra представляет собой Н или C1-С6алкильную группу (предпочтительно C1-С3алкил);
RSS в ULM-g-ULM-i представляет собой Н, CN, NO2, галоген (предпочтительно F или Cl), необязательно замещенный C1-С6алкил (предпочтительно замещенный одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами), необязательно замещенный O-(C1-С6алкил) (предпочтительно замещенный одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами) или необязательно замещенный -С(O)(С1-С6алкил) (предпочтительно замещенный одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами);
RURE в ULM-g-ULM-i представляет собой Н, C1-С6алкил (предпочтительно Н или C1-С3алкил) или -С(O)(С0-С6алкил), каждая группа из которых необязательно замещена одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами, предпочтительно фтором, или необязательно замещенный гетероцикл, например, пиперидин, морфолин, пирролидин, тетрагидрофуран, тетрагидротиофен, пиперидин, пиперазин, каждый из которых необязательно замещен;
YC в ULM-g-ULM-i представляет собой N или C-RYC, где RYC представляет собой Н, ОН, CN, NO2, галоген (предпочтительно Cl или F), необязательно замещенный C1-С6алкил (предпочтительно замещенный одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами (например, CF3), необязательно замещенный O(С1-С6алкил) (предпочтительно замещенный одной или двумя гидроксильными группами или не более чем тремя галогенсодержащими группами) или необязательно замещенную ацетиленовую группу -C≡C-Ra, где Ra представляет собой Н или C1-С6алкильную группу (предпочтительно C1-С3алкил);
RPRO в ULM-g-ULM-i представляет собой Н, необязательно замещенный C1-С6алкил или необязательно замещенную арильную, гетероарильную или гетероциклическую группу;
каждый из RPRO1 и RPRO2 в ULM-g-ULM-i независимо представляет собой Н, необязательно замещенную C1-С3алкильную группу или вместе образуют кетогруппу;
каждый m' в ULM-g-ULM-i независимо равняется 0 или 1; и
каждый n в ULM-g-ULM-i независимо равняется 0, 1, 2, 3, 4, 5 или 6 (предпочтительно 0 или 1),
где каждое из указанных соединений, предпочтительно при указанных арильных или НЕТ-группах, необязательно соединено с группой РТМ (в том числе группой ULM') с помощью линкерной группы.
[259] В еще одних дополнительных вариантах осуществления предпочтительные соединения включают соединения в соответствии с химической структурой:

где
R1' в ULM-i представляет собой ОН или группу, которая метаболизируется у пациента или субъекта до ОН;
R2' в ULM-i представляет собой -NH-CH2-арил-НЕТ (предпочтительно фенил, соединенный непосредственно с метилзамещенным тиазолом);
R3' в ULM-i представляет собой группу -CHRCR3'-NH-C(O)-R3P1 или группу -CHRCR3'-R3P2;
RCR3' в ULM-i представляет собой С1-С4алкильную группу, предпочтительно метил, изопропил или трет-бутил;
R3P1 в ULM-i представляет собой C1-С3алкил (предпочтительно метил), необязательно замещенную оксетановую группу (предпочтительно метилзамещенную группу -(СН2)nOCH3, где n равняется 1 или 2 (предпочтительно 2), или группу  (этилэфирная группа предпочтительно замещена при фенильном фрагменте в мета-положении), морфолиновую группу (соединенную с карбонилом во 2 или 3 положении;
(этилэфирная группа предпочтительно замещена при фенильном фрагменте в мета-положении), морфолиновую группу (соединенную с карбонилом во 2 или 3 положении;
R3P2 в ULM-i представляет собой группу 
арил в ULM-i представляет собой фенил;
НЕТ в ULM-i представляет собой необязательно замещенный тиазол или изотиазол; и
RHET в ULM-i представляет собой Н или галогенсодержащую группу (предпочтительно Н);
или их фармацевтически приемлемую соль, стереоизомер, сольват или полиморф, где каждое из указанных соединений необязательно соединено с группой РТМ (в том числе группой ULM') посредством линкерной группы.
[260] В определенных аспектах бифункциональные соединения содержат фрагмент, связывающий Е3-убиквитинлигазу (ULM), где ULM представляет собой группу в соответствии с химической структурой:

где
каждый из R5 и R6 в ULM-j независимо представляет собой ОН, SH или необязательно замещенный алкил, или R5, R6 и атом углерода, к которому они присоединены, образуют карбонил;
R7 в ULM-j представляет собой Н или необязательно замещенный алкил;
Е в ULM-j представляет собой связь, С=O или C=S;
G в ULM-j представляет собой связь, необязательно замещенный алкил, -СООН или C=J;
J в ULM-j представляет собой О или N-R8;
R8 в ULM-j представляет собой Н, CN, необязательно замещенный алкил или необязательно замещенный алкокси;
М в ULM-j представляет собой необязательно замещенный арил, необязательно замещенный гетероарил, необязательно замещенную гетероциклическую группу или 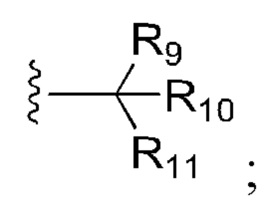
каждый из R9 и R10 в ULM-j независимо представляет собой Н; необязательно замещенный алкил, необязательно замещенный циклоалкил, необязательно замещенный гидроксиалкил, необязательно замещенный тиоалкил, ULM, соединенный с помощью дисульфидной связи, необязательно замещенный гетероарил или галогеналкил; или R9, R10 и атом углерода, к которому они присоединены, образуют необязательно замещенный циклоалкил;
R11 в ULM-j представляет собой необязательно замещенную гетероциклическую группу, необязательно замещенный алкокси, необязательно замещенный гетероарил, необязательно замещенный арил или 
R12 в ULM-j представляет собой Н или необязательно замещенный алкил;
R13 в ULM-j представляет собой Н, необязательно замещенный алкил, необязательно замещенный алкилкарбонил, необязательно замещенный (циклоалкил)алкилкарбонил, необязательно замещенный аралкилкарбонил, необязательно замещенный арилкарбонил, необязательно замещенный (гетероциклил)карбонил или необязательно замещенный аралкил; необязательно замещенный (оксоалкил)карбамат,
каждый R14 в ULM-j независимо представляет собой Н, галогеналкил, необязательно замещенный циклоалкил, необязательно замещенный алкил или необязательно замещенный гетероциклоалкил;
R15 в ULM-j представляет собой Н, необязательно замещенный гетероарил, галогеналкил, необязательно замещенный арил, необязательно замещенный алкокси или необязательно замещенный гетероциклил;
каждый R16 в ULM-j независимо представляет собой галоген, необязательно замещенный алкил, необязательно замещенный галогеналкил, CN или необязательно замещенный галогеналкокси;
каждый R25 в ULM-j независимо представляет собой Н или необязательно замещенный алкил; или обе группы R25 могут быть взяты вместе с образованием оксо- или необязательно замещенной циклоалкильной группы;
R23 в ULM-j представляет собой Н или ОН;
Z1, Z2, Z3 и Z4 в ULM-j независимо представляют собой С или N; и
о в ULM-j равняется 0, 1, 2, 3 или 4, или ее фармацевтически приемлемую соль, стереоизомер, сольват или полиморф.
[261] В определенных вариантах осуществления, где G в ULM-j представляет собой C=J, J представляет собой О, R7 представляет собой Н, каждый R14 представляет собой Н, и о равняется 0.
[262] В определенных вариантах осуществления, где G в ULM-j представляет собой C=J, J представляет собой О, R7 представляет собой Н, каждый R14 представляет собой Н, R15 представляет собой необязательно замещенный гетероарил, и о равняется 0. В других случаях Е представляет собой С=O, и М представляет собой 
[263] В определенных вариантах осуществления, где Е в ULM-j представляет собой С=O, R11 представляет собой необязательно замещенную гетероциклическую группу или  и М представляет собой
и М представляет собой 
[264] В определенных вариантах осуществления, где Е в ULM-j представляет собой С=O, М представляет собой  и R11 представляет собой
и R11 представляет собой  или
или  , каждый R18 независимо представляет собой галоген, необязательно замещенный алкокси, циано, необязательно замещенный алкил, галогеналкил или галогеналкокси; и р равняется 0, 1, 2, 3 или 4.
, каждый R18 независимо представляет собой галоген, необязательно замещенный алкокси, циано, необязательно замещенный алкил, галогеналкил или галогеналкокси; и р равняется 0, 1, 2, 3 или 4.
[265] В определенных вариантах осуществления каждый из ULM и ULM' в случае его присутствия независимо представляет собой группу в соответствии с химической структурой:

где
G в ULM-k представляет собой C=J, J представляет собой О;
R7 в ULM-k представляет собой Н;
каждый R14 в ULM-k представляет собой Н;
о в ULM-k равняется 0;
R15 в ULM-k представляет собой 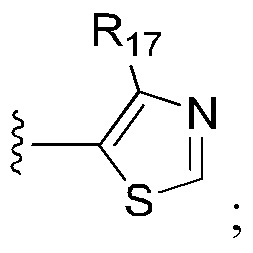 и
и
R17 в ULM-k представляет собой Н, галоген, необязательно замещенный циклоалкил, необязательно замещенный алкил, необязательно замещенный алкенил и галогеналкил.
[266] В других случаях R17 в ULM-k представляет собой алкил (например, метил) или циклоалкил (например, циклопропил).
[267] В других вариантах осуществления каждый из ULM и ULM' в случае его присутствия независимо представляет собой группу в соответствии с химической структурой:
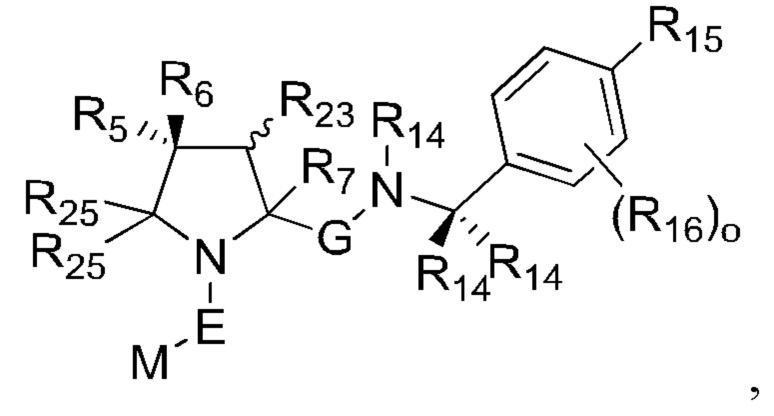
где
G в ULM-k представляет собой C=J, J представляет собой О;
R7 в ULM-k представляет собой Н;
каждый R14 в ULM-k представляет собой Н;
о в ULM-k равняется 0; и
R15 в ULM-k выбран из группы, состоящей из:



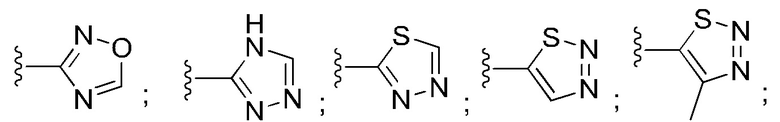
 где R30 в ULM-k представляет собой Н или необязательно замещенный алкил.
где R30 в ULM-k представляет собой Н или необязательно замещенный алкил.
[268] В других вариантах осуществления каждый из ULM и ULM' в случае его присутствия независимо представляет собой группу в соответствии с химической структурой:

где
Е в ULM-k представляет собой С=O;
М в ULM-k представляет собой 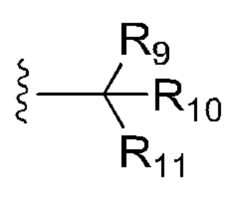 ; и
; и
R11 в ULM-k выбран из группы, состоящей из:





[269] В еще одних вариантах осуществления соединение имеет химическую структуру:

где Е в ULM-k представляет собой С=O;
R11 в ULM-k представляет собой  и
и
М в ULM-k представляет собой 
q в ULM-k равняется 1 или 2;
R20 в ULM-k представляет собой Н, необязательно замещенный алкил, необязательно замещенный циклоалкил, необязательно замещенный арил или 
R21 в ULM-k представляет собой Н или необязательно замещенный алкил; и
R22 в ULM-k представляет собой Н, необязательно замещенный алкил, необязательно замещенный алкокси или галогеналкил.
[270] В любом варианте осуществления, описанном в данном документе, R11 в ULM-j или ULM-k выбран из группы, состоящей из:
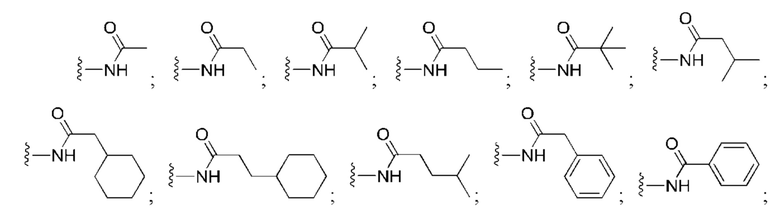
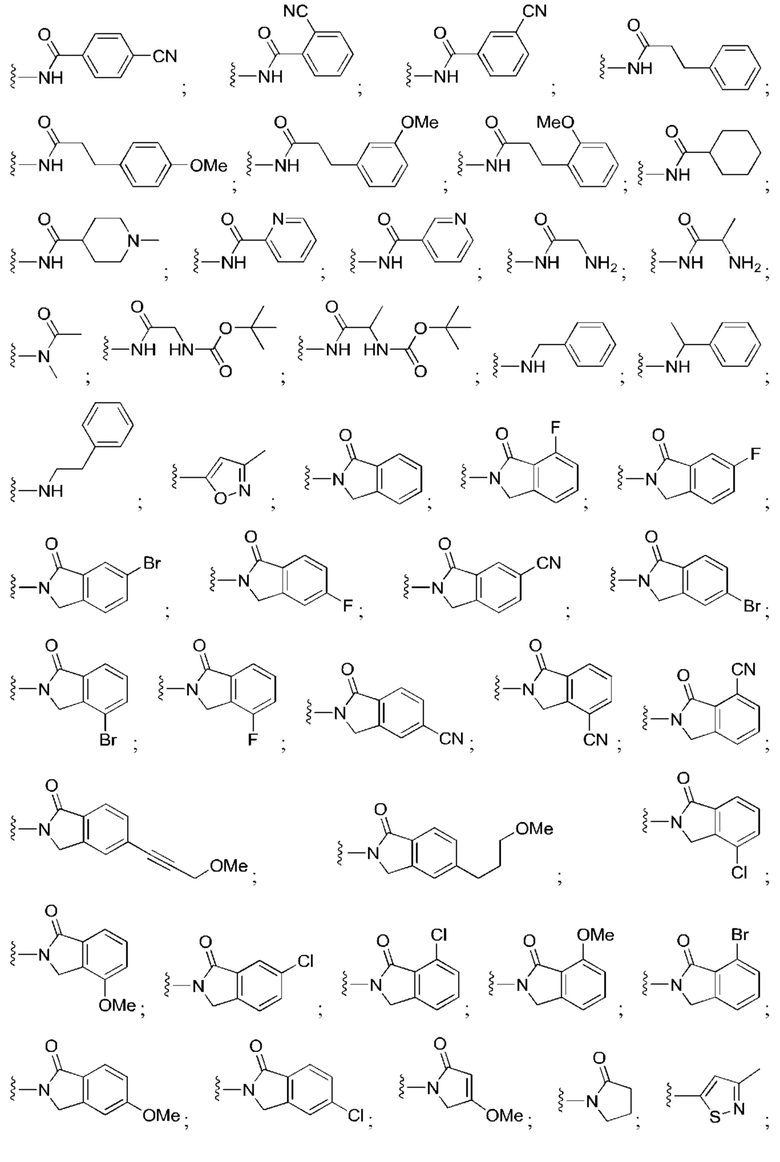

[271] В определенных вариантах осуществления R11 в ULM-j или ULM-k выбран из группы, состоящей из:

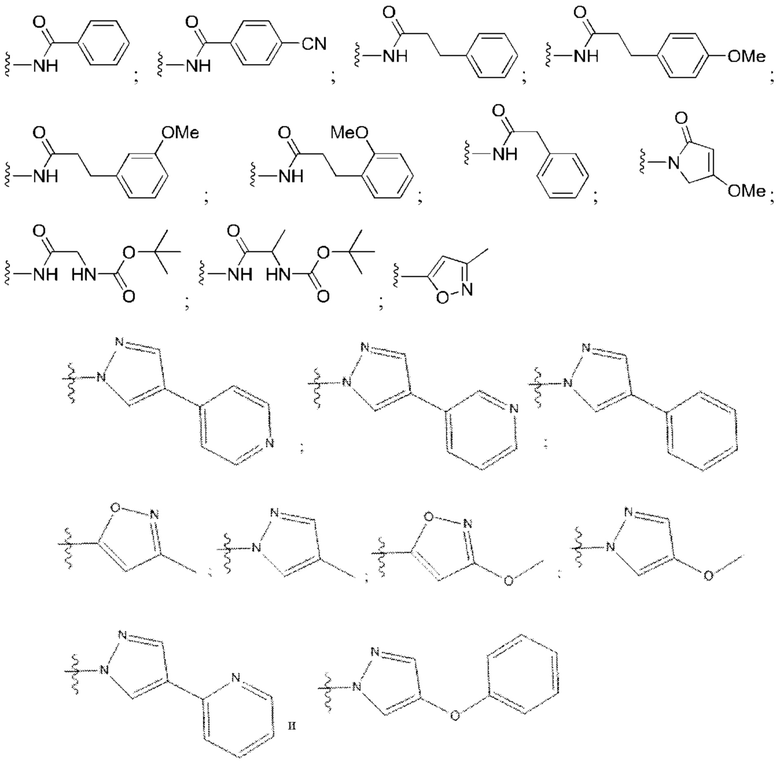
[272] В определенных вариантах осуществления ULM (или ULM' в случае его присутствия) представляет собой группу в соответствии с химической структурой:


где
X в ULM-l представляет собой О или S;
Y в ULM-l представляет собой Н, метил или этил;
R17 в ULM-l представляет собой Н, метил, этил, гидроксиметил или циклопропил;
М в ULM-l представляет собой необязательно замещенный арил, необязательно замещенный гетероарил или 
R9 в ulm-l представляет собой Н;
R10 в ULM-l представляет собой Н, необязательно замещенный алкил, необязательно замещенный галогеналкил, необязательно замещенный гетероарил, необязательно замещенный арил, необязательно замещенный гидроксиалкил, необязательно замещенный тиоалкил или циклоалкил;
R11 в ULM-l представляет собой необязательно замещенную гетероароматическую группу, необязательно замещенную гетероциклическую группу, необязательно замещенный арил или 
R12 в ULM-l представляет собой Н или необязательно замещенный алкил; и
R13 в ULM-l представляет собой Н, необязательно замещенный алкил, необязательно замещенный алкилкарбонил, необязательно замещенный (циклоалкил)алкилкарбонил, необязательно замещенный аралкилкарбонил, необязательно замещенный арилкарбонил, необязательно замещенный (гетероциклил)карбонил или необязательно замещенный аралкил; необязательно замещенный (оксоалкил)карбамат.
[273] В некоторых вариантах осуществления каждый из ULM и ULM' в случае его присутствия независимо представляет собой группу в соответствии с химической структурой:

где
Y в ULM-m представляет собой Н, метил или этил;
R9 в ULM-m представляет собой Н;
R10 представляет собой изопропил, трет-бутил, втор-бутил, циклопентил или циклогексил;
R11 в ULM-m представляет собой необязательно замещенный амид, необязательно замещенный изоиндолинон, необязательно замещенный изооксазол, необязательно замещенные гетероциклы.
[274] В других предпочтительных вариантах осуществления настоящего изобретения каждый из ULM и ULM' в случае его присутствия независимо представляет собой группу в соответствии с химической структурой:

где
R17 в ULM-n представляет собой метил, этил или циклопропил; и
R9, R10 и R11 в ULM-n определены выше. В других случаях R9 представляет собой Н; и
R10 в ULM-n представляет собой Н, алкил или циклоалкил (предпочтительно изопропил, трет-бутил, втор-бутил, циклопентил или циклогексил).
[275] В любом из аспектов или вариантов осуществления, описанных в данном документе, ULM (или ULM' в случае его присутствия), как описано в данном документе, может представлять собой его фармацевтически приемлемую соль, энантиомер, диастереомер, сольват или полиморф. Кроме того, в любом из аспектов или вариантов осуществления, описанных в данном документе, ULM (или ULM' в случае его присутствия), как описано в данном документе, может быть связан с РТМ непосредственно с помощью связи или химического линкера.
[276] В определенных аспектах настоящего изобретения фрагмент ULM выбран из группы, состоящей из




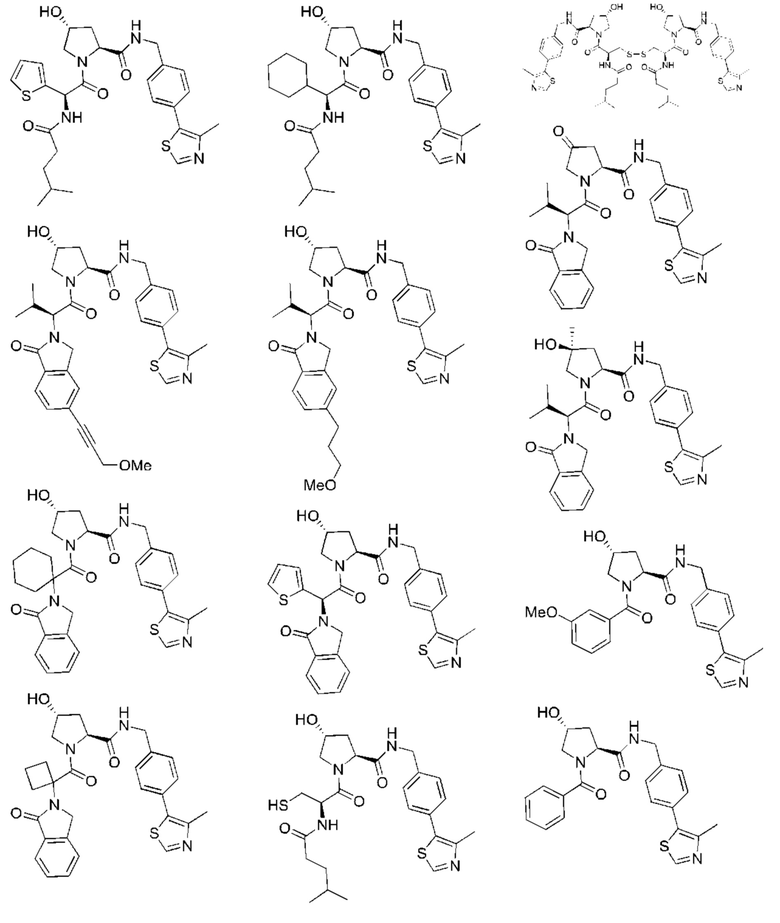
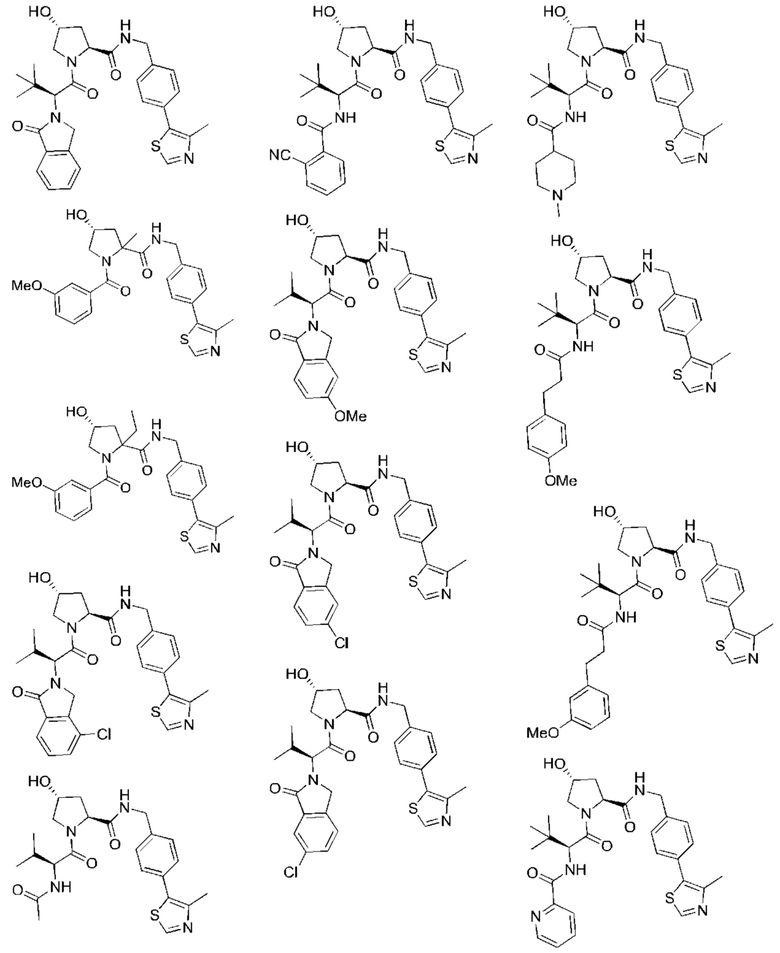




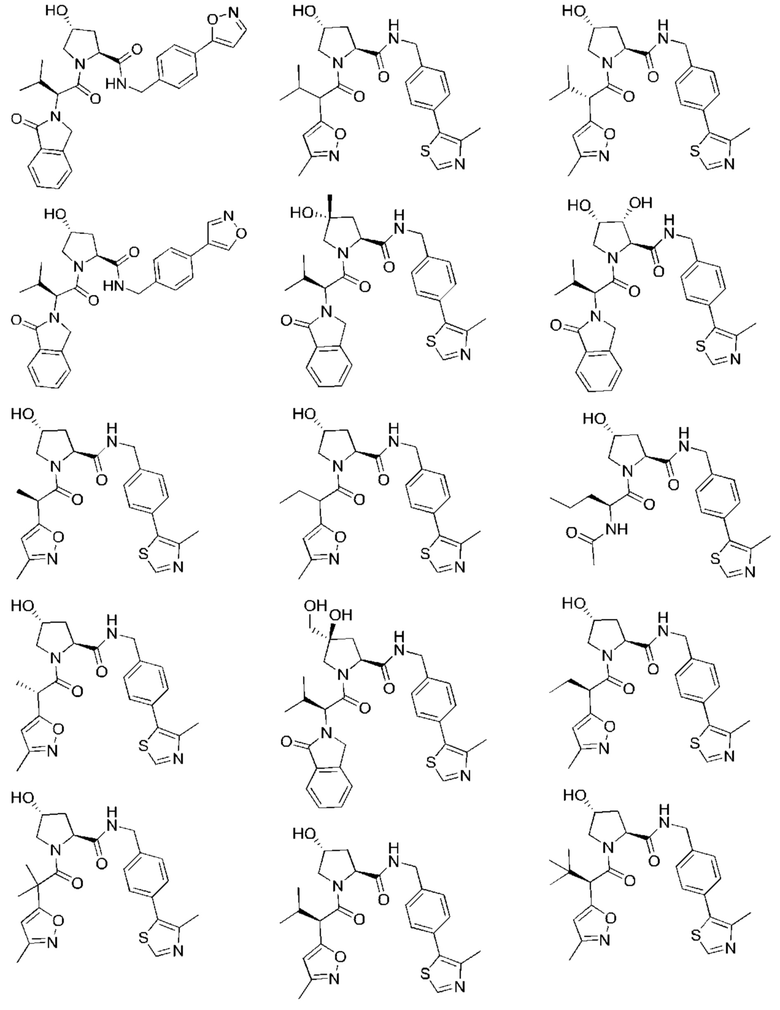

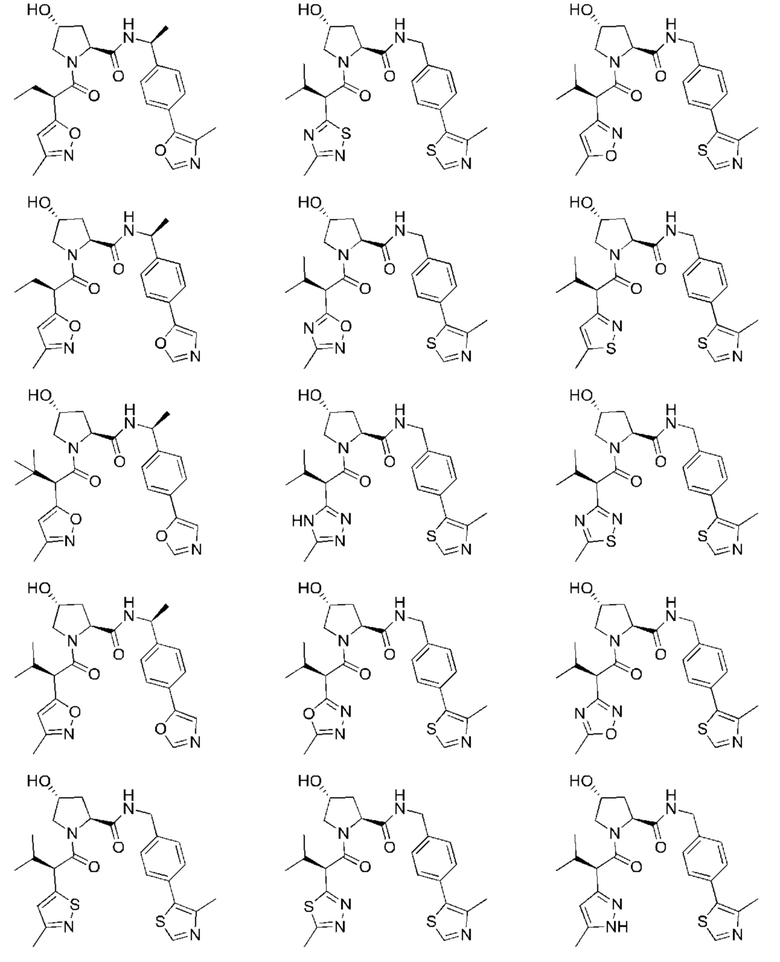

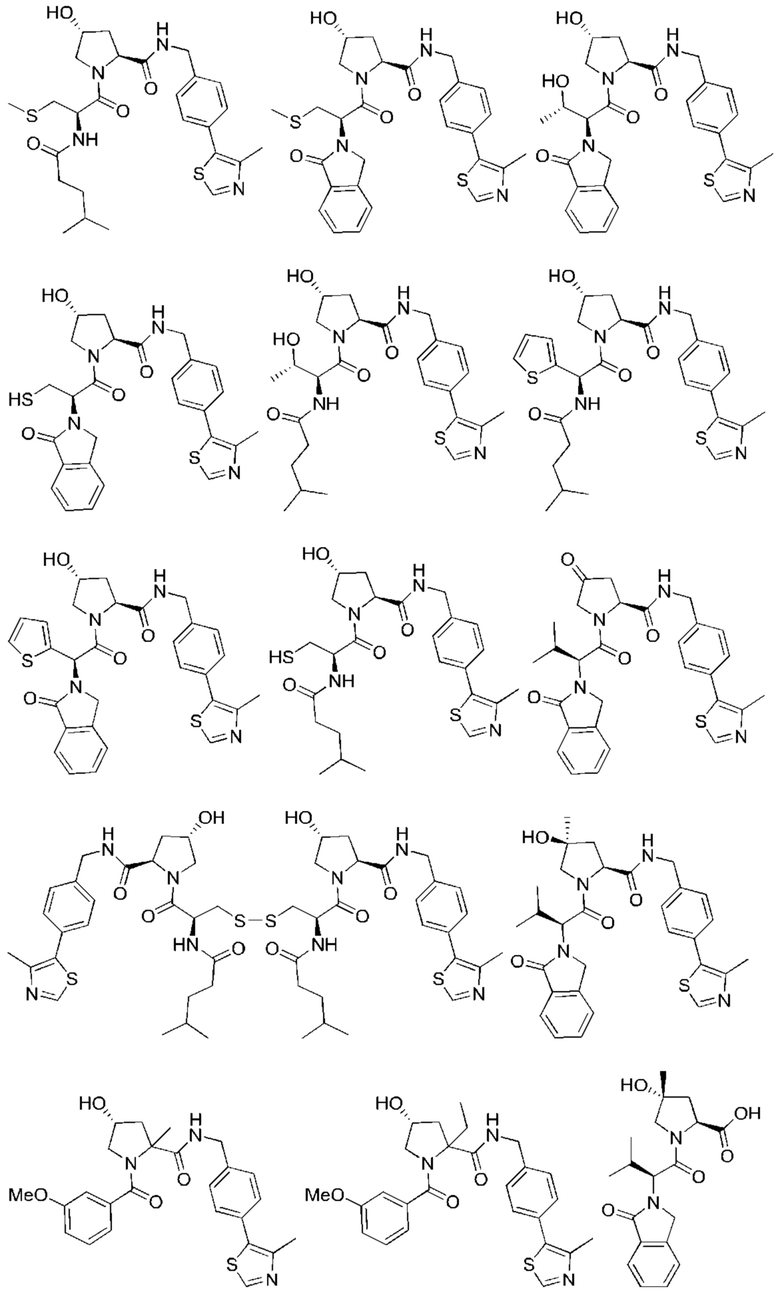
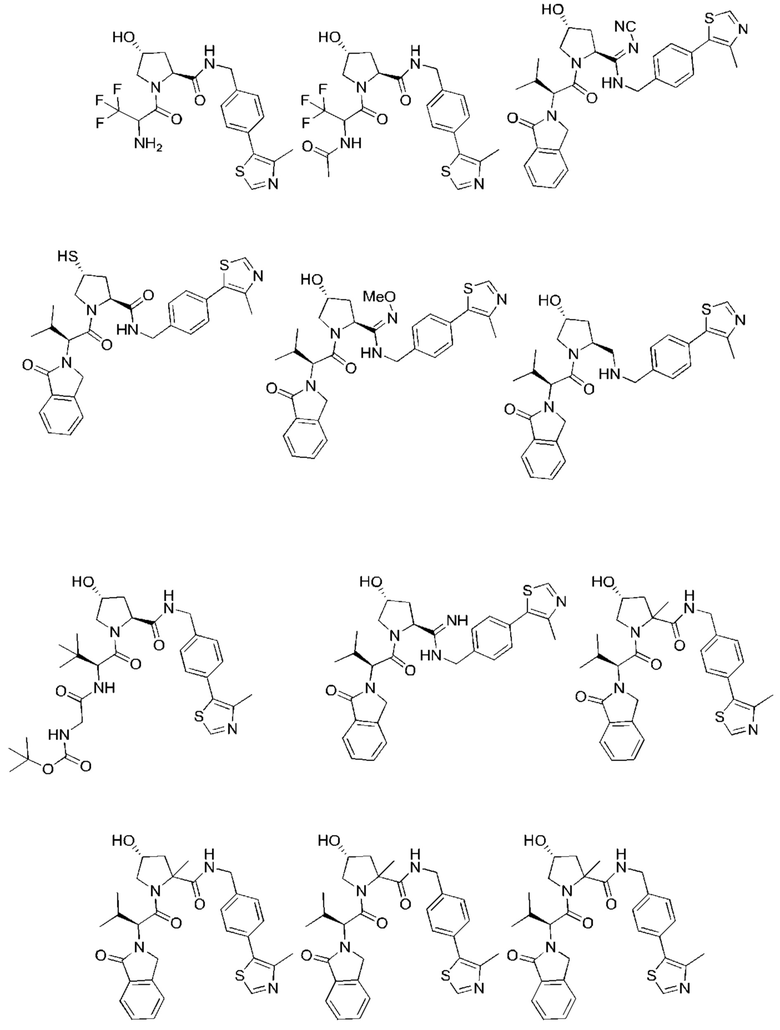





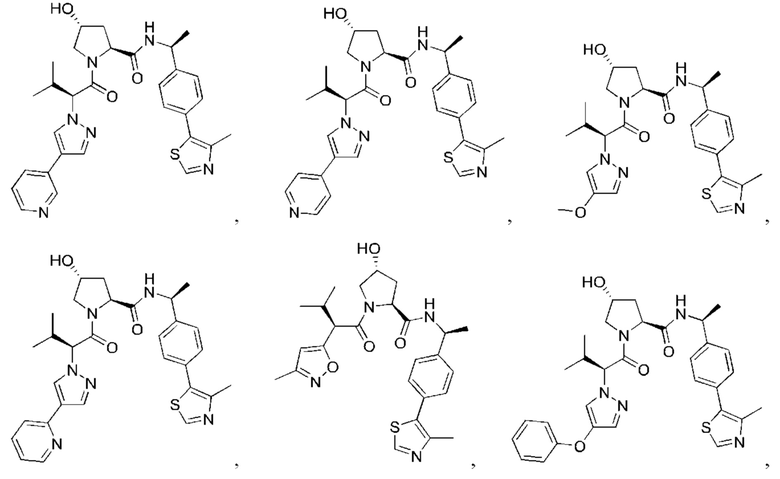
 где VLM может быть соединен с РТМ посредством линкера, описанного в данном документе, в любом подходящем положении, в том числе, например, при ариле, гетероариле, фениле или фениле индольной группы, необязательно с помощью любой подходящей функциональной группы, такой как амин, сложный эфир, эфир, алкил или алкокси.
где VLM может быть соединен с РТМ посредством линкера, описанного в данном документе, в любом подходящем положении, в том числе, например, при ариле, гетероариле, фениле или фениле индольной группы, необязательно с помощью любой подходящей функциональной группы, такой как амин, сложный эфир, эфир, алкил или алкокси.
Иллюстративные линкеры
[277] В определенных вариантах осуществления соединения, описанные в данном документе, включают один или более РТМ, химически соединенные или связанные с одним или более ULM (например, по меньшей мере одним из CLM, VLM, MLM, ILM или их комбинации) посредством химического линкера (L). В определенных вариантах осуществления линкерная группа L представляет собой группу, содержащую одно или более ковалентно связанных структурных звеньев (например, -ALl…(AL)q- или -(AL)q-), где Al представляет собой группу, связанную с РТМ, и Aq представляет собой группу, связанную с ULM.
[278] В определенных вариантах осуществления линкерная группа L представляет собой -(AL)q-:
(AL)q представляет собой группу, которая соединена с по меньшей мере одним из ULM (таким как CLM, VLM, ILM, MLM, CLM', VLM', ILM' и/или MLM'), фрагментом РТМ или их комбинацией; и
q в линкере представляет собой целое число, которое больше или равняется 1;
каждый AL независимо выбран из группы, состоящей из связи, CRL1RL2, О, S, SO, SO2, NRL3, SO2NRL3, SONRL3, CONRL3, NRL3CONRL4, NRL3SO2NRL4, CO, CRL1=CRL2, C=C, SiRL1RL2, P(O)RL1, P(O)ORL1, NRL3C(=NCN)NRL4, NRL3C(=NCN), NRL3C(=CNO2)NRL4, С3-11циклоалкила, необязательно замещенного 0-6 группами RL1 и/или RL2, С5-13спироциклоалкила, необязательно замещенного 0-9 группами RL1 и/или RL2, С3-11гетероциклила, необязательно замещенного 0-6 группами RL1 и/или RL2, С5-13спирогетероциклоалкила, необязательно замещенного 0-8 группами RL1 и/или RL2, арила, необязательно замещенного 0-6 группами RL1 и/или RL2, гетероарила, необязательно замещенного 0-6 группами RL1 и/или RL2, где каждый из RL1 или RL2 независимо необязательно связан с другими группами с образованием циклоалкильного и/или гетероциклильного фрагмента, необязательно замещенного 0-4 группами RL5; и
каждая из RL1, RL2, RL3, RL4 и RL5 независимо представляет собой Н, галоген, С1-8алкил, ОС1-8алкил, SC1-8алкил, NHC1-8алкил, N(С1-8алкил)2, С3-11циклоалкил, арил, гетероарил, С3-11гетероциклил, ОС1-8циклоалкил, SC1-8циклоалкил, NHC1-8циклоалкил, N(С1-8циклоалкил)2, N(С1-8циклоалкил)(С1-8алкил), ОН, NH2, SH, SO2C1-8алкил, Р(O)(ОС1-8алкил)(С1-8алкил), Р(O)(ОС1-8алкил)2, СС-С1-8алкил, CCH, CH=CH(C1-8алкил), С(С1-8алкил)=СН(С1-8алкил), С(С1-8алкил)=С(С1-8алкил)2, Si(OH)3, Si(C1-8алкил)3, Si(ОН)(С1-8алкил)2, СОС1-8алкил, СО2Н, галоген, CN, CF3, CHF2, CH2F, NO2, SF5, SO2NHC1-8алкил, SO2N(C1-8алкил)2, SONHC1-8алкил, SON(C1-8алкил)2, CONHC1-8алкил, CON(С1-8алкил)2, N(С1-8алкил)CONH(С1-8алкил), N(С1-8алкил)CON(С1-8алкил)2, NHCONH(C1-8алкил), NHCON(C1-8алкил)2, NHCONH2, N(C1-8алкил)SO2NH(C1-8алкил), N(C1-8алкил)SO2N(C1-8алкил)2, NHSO2NH(C1-8алкил), NHSO2N(C1-8алкил)2, NHSO2NH2.
[279] В определенных вариантах осуществления q в линкере представляет собой целое число, которое больше или равняется 0. В определенных вариантах осуществления q представляет собой целое число, которое больше или равняется 1.
[280] Например, в определенных вариантах осуществления, если q в линкере равняется более 2, (AL)q представляет собой группу, которая соединена с ULM, и Al и (AL)q соединены посредством структурных звеньев линкера (L).
[281] Например, в определенных вариантах осуществления, если q в линкере равняется 2, (AL)q представляет собой группу, которая соединена с ALl и с ULM.
[282] Например, в определенных вариантах осуществления, если q в линкере равняется 1, структура линкерной группы L предусматривает -ALl-, и ALl представляет собой группу, которая соединена с фрагментом ULM и фрагментом РТМ.
[283] В определенных вариантах осуществления линкер (L) предусматривает группу, представленную общей структурой, выбранной из группы, состоящей из
-NR(CH2)n-(низший алкил)-, -NR(CH2)n-(низший алкоксил)-, -NR(CH2)n-(низший алкоксил)-ОСН2-, -NR(CH2)n-(низший алкоксил)-(низший алкил)-ОСН2-, -NR(CH2)n-(циклоалкил)-(низший алкил)-ОСН2-, -NR(CH2)n-(гетероциклоалкил), -NR(CH2CH2O)n-(низший алкил)-O-СН2-, -NR(CH2CH2O)n-(гетероциклоалкил)-O-СН2-, -NR(CH2CH2O)n-арил-O-CH2-, -NR(CH2CH2O)n-(гетероарил)-O-СН2-, -NR(CH2CH2O)n-(циклоалкил)-O-(гетероарил)-O-СН2-, -NR(CH2CH2O)n-(циклоалкил)-O-арил-O-CH2-, -NR(CH2CH2O)n-(низший алкил)-NH-арил-O-СН2-, -NR(CH2CH2O)n-(низший алкил)-O-арил-CH2, -NR(CH2CH2O)n-циклоалкил-O-арил-, -NR(CH2CH2O)n-циклоалкил-O-(гетероарил)-, -NR(CH2CH2)n-(циклоалкил-O-(гетероцикл)-CH2, -NR(CH2CH2)n-(гетероцикл)-(гетероцикл)-СН2, -N(R1R2)-(гетероцикл)-CH2; где
n в линкере может равняться 0-10;
R в линкере может представлять собой Н, низший алкил;
R1 и R2 в линкере могут образовывать кольцо с соединяющим N.
[284] В определенных вариантах осуществления линкер (L) предусматривает группу, представленную общей структурой, выбранной из группы, состоящей из
-N(R)-(CH2)m-O(CH2)n-O(CH2)o-O(CH2)p-O(CH2)q-O(CH2)r-OCH2-,
-O-(CH2)m-O(CH2)n-O(CH2)o-O(CH2)p-O(CH2)q-O(CH2)r-OCH2-,
-O-(CH2)m-O(CH2)n-O(CH2)o-O(CH2)p-O(CH2)q-O(CH2)r-O-;
-N(R)-(CH2)m-O(CH2)n-O(CH2)o-O(CH2)p-O(CH2)q-O(CH2)r-O-;
-(CH2)m-O(CH2)n-O(CH2)o-O(CH2)p-O(CH2)q-O(CH2)r-O-;
-(CH2)m-O(CH2)n-O(CH2)o-O(CH2)p-O(CH2)q-O(CH2)r-OCH2-;


 где
где
m, n, o, р, q и r в линкере независимо равняются 0, 1, 2, 3, 4, 5, 6;
если число равняется нулю, то связь N-O или O-O отсутствует;
R в линкере представляет собой Н, метил и этил;
X в линкере представляет собой Н и F;

где m в линкере может равняться 2, 3, 4, 5;




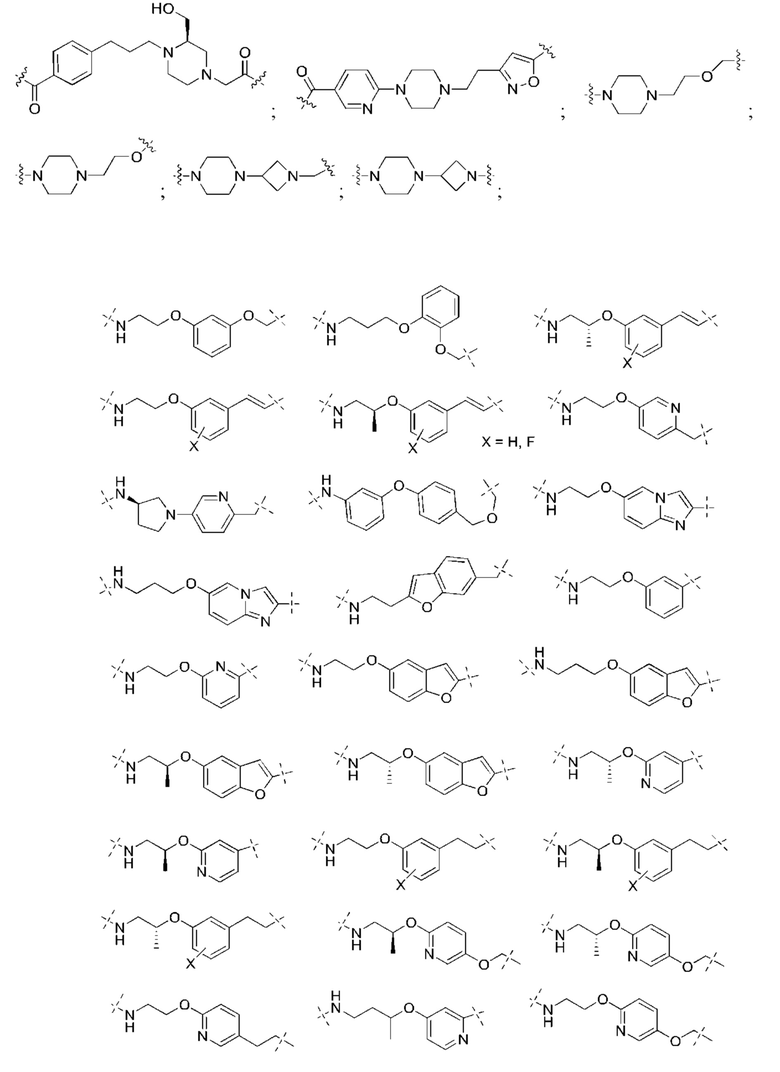
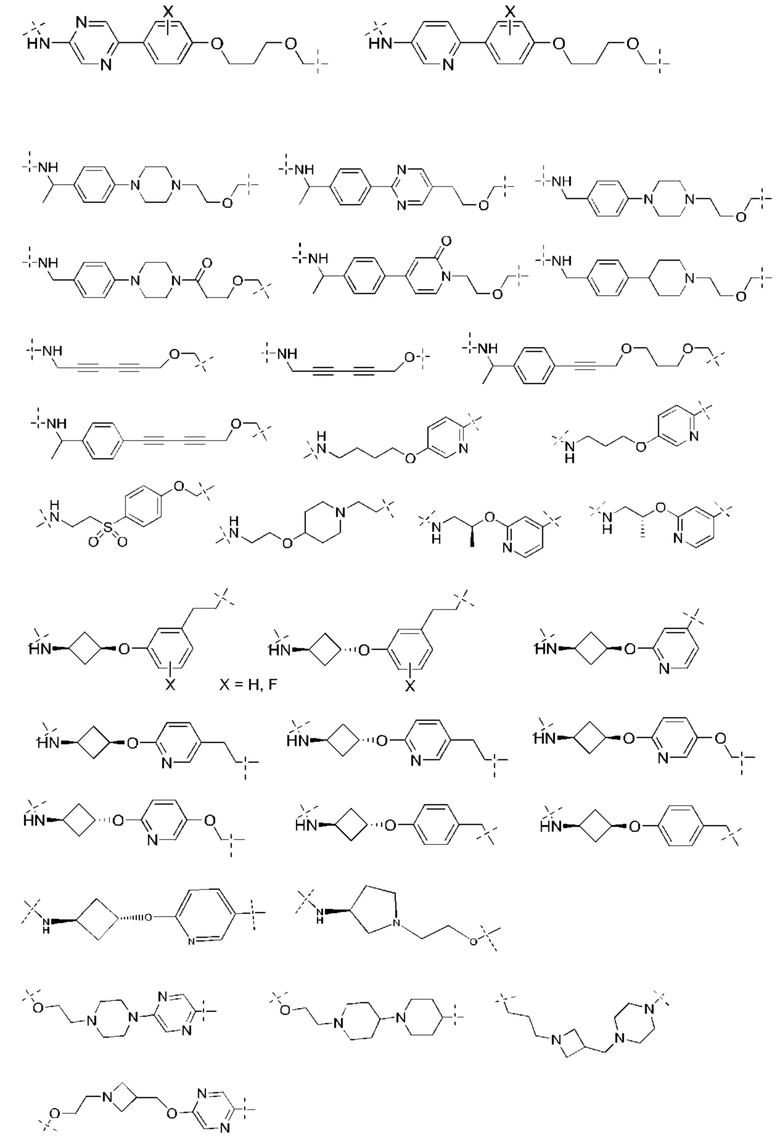


где каждый n и m в линкере может независимо равняться 0, 1, 2, 3, 4, 5, 6.
[285] В любом аспекте или варианте осуществления, описанных в данном документе, линкер (L) выбран из группы, состоящей из:
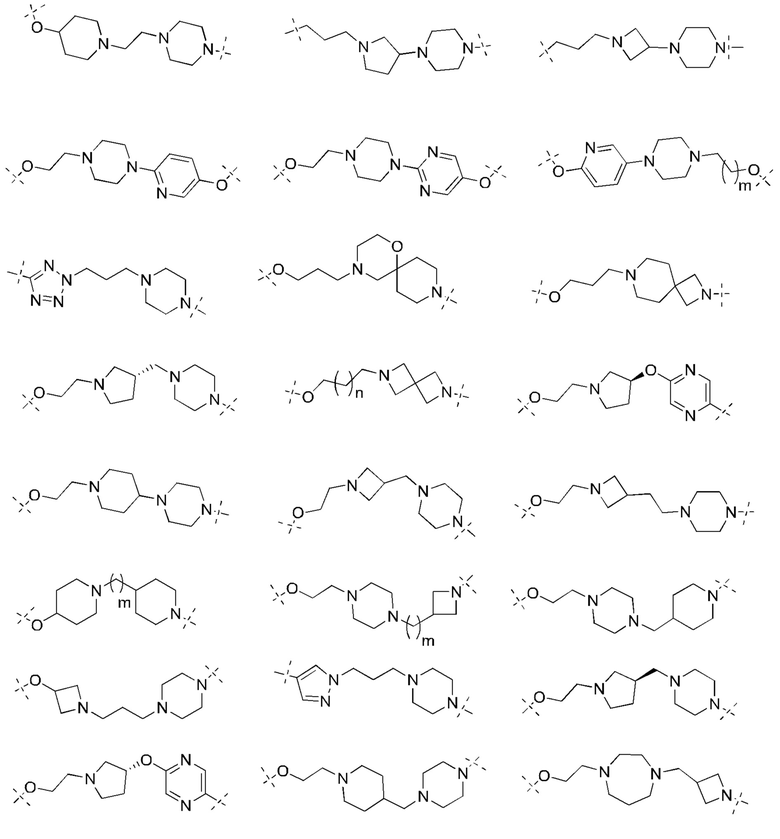
m = 1, 2; n = 0, 1
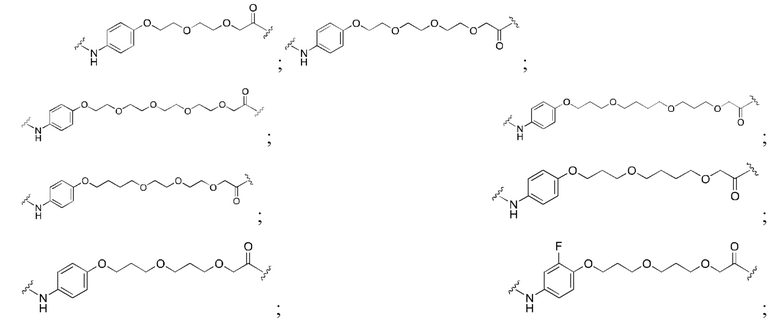


[286] В любом аспекте или варианте осуществления, описанных в данном документе, линкер (L) выбран из группы, состоящей из:

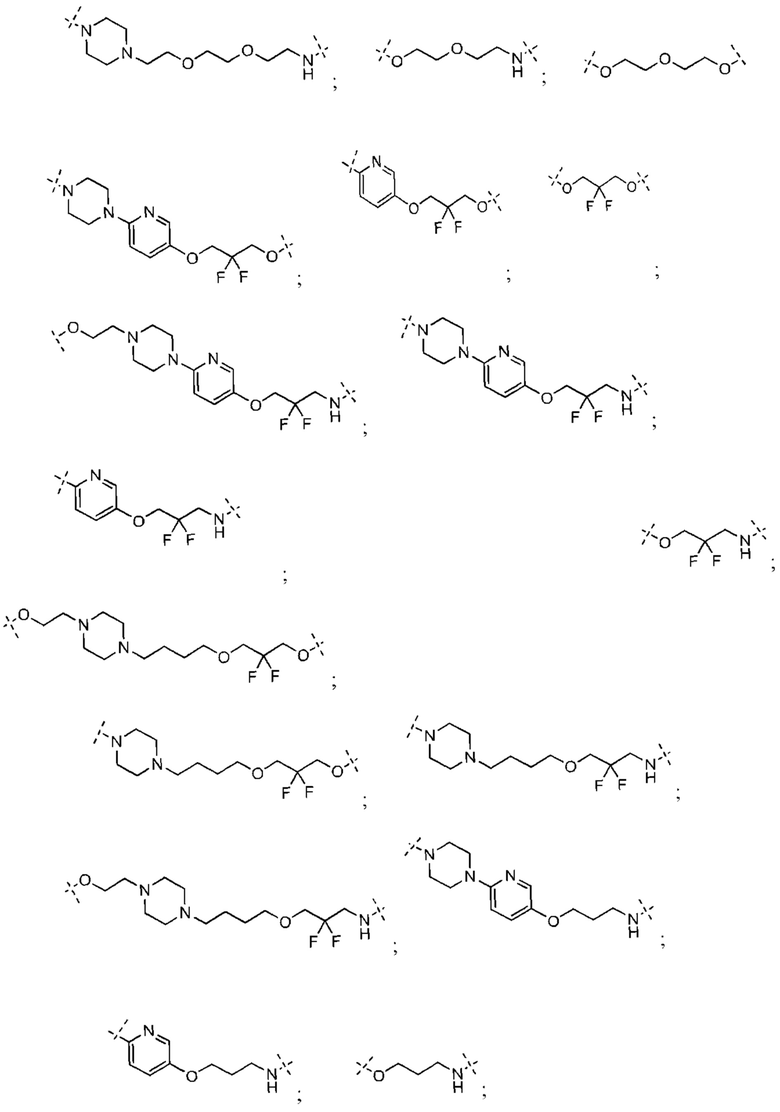











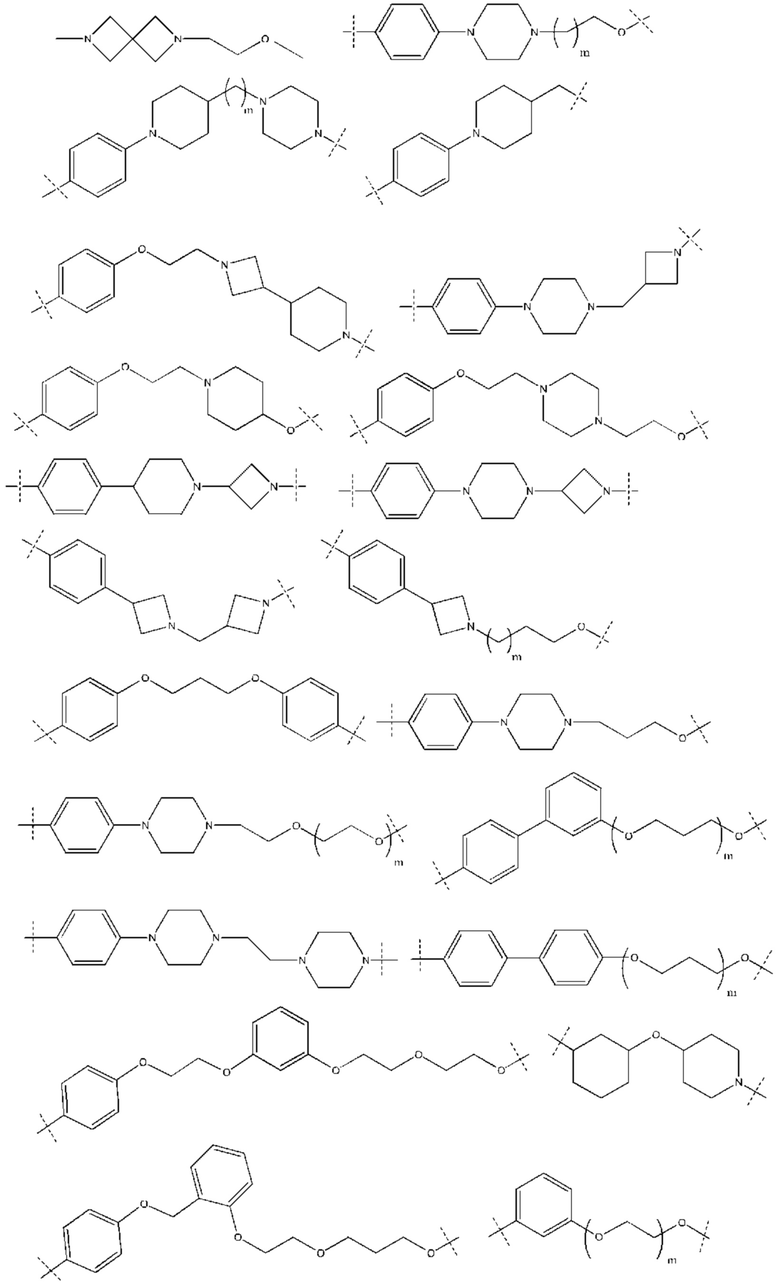






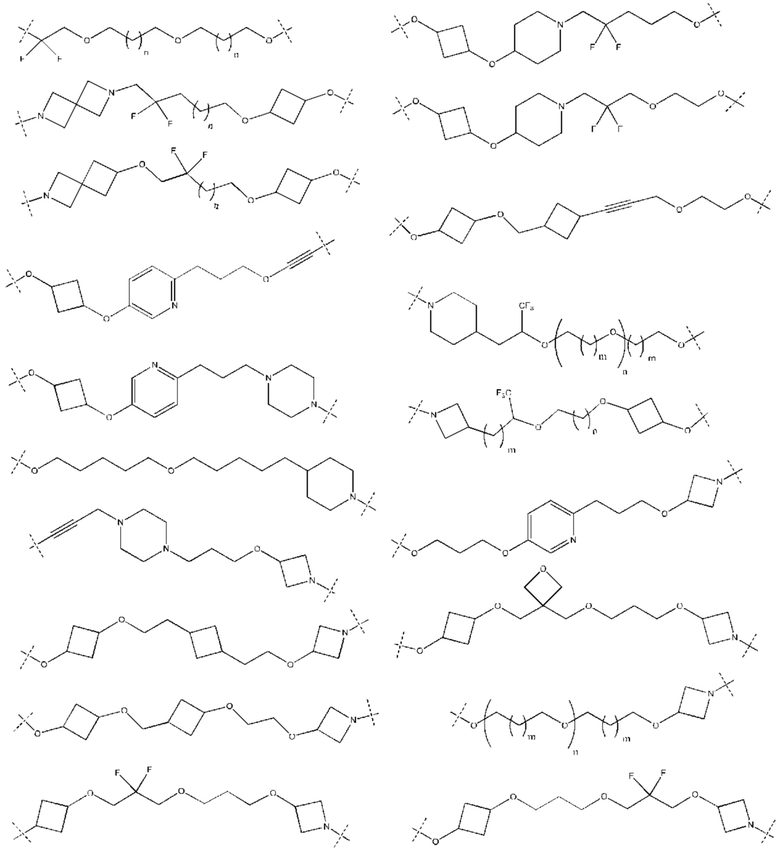
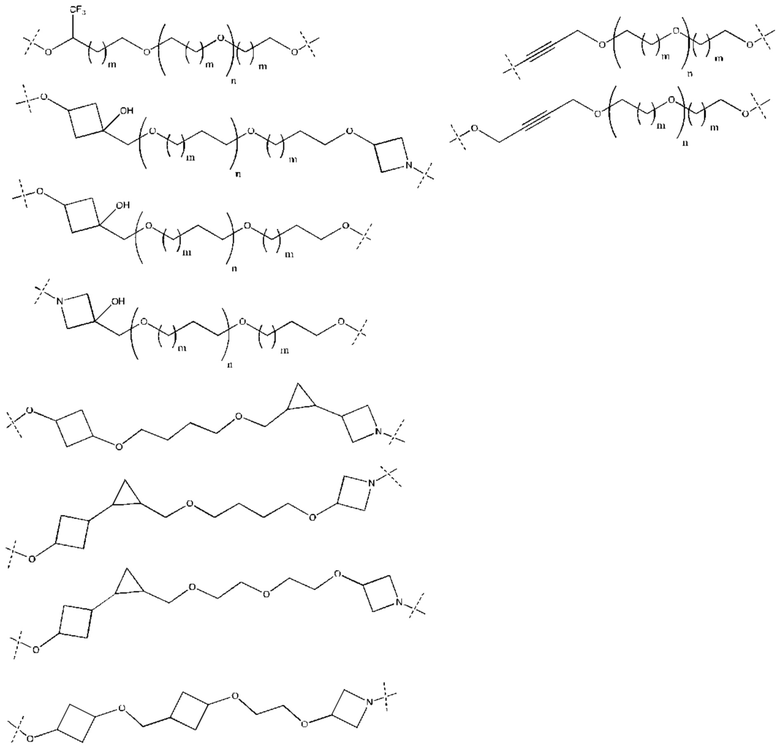


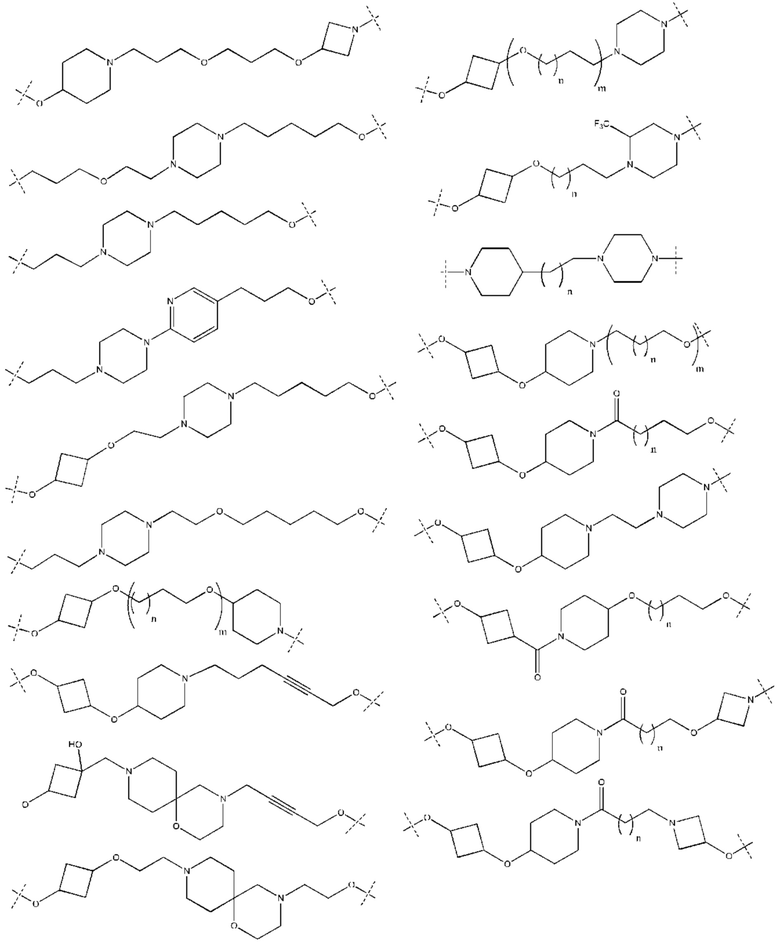
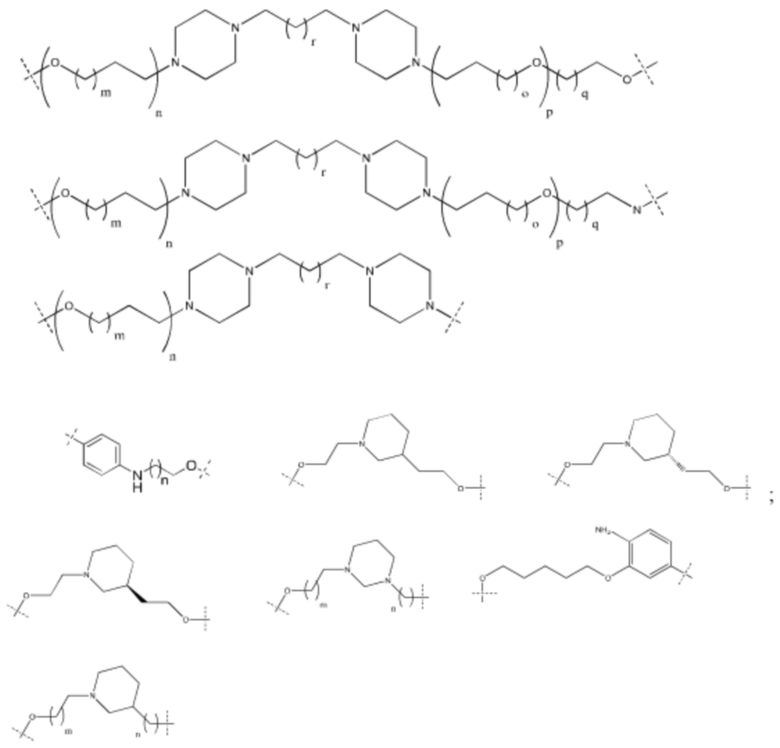


 где каждый m, n, о и р независимо равняется 0, 1, 2, 3, 4, 5, 6 или 7.
где каждый m, n, о и р независимо равняется 0, 1, 2, 3, 4, 5, 6 или 7.
[287] В любом аспекте или варианте осуществления, описанных в данном документе, L выбран из группы, состоящей из




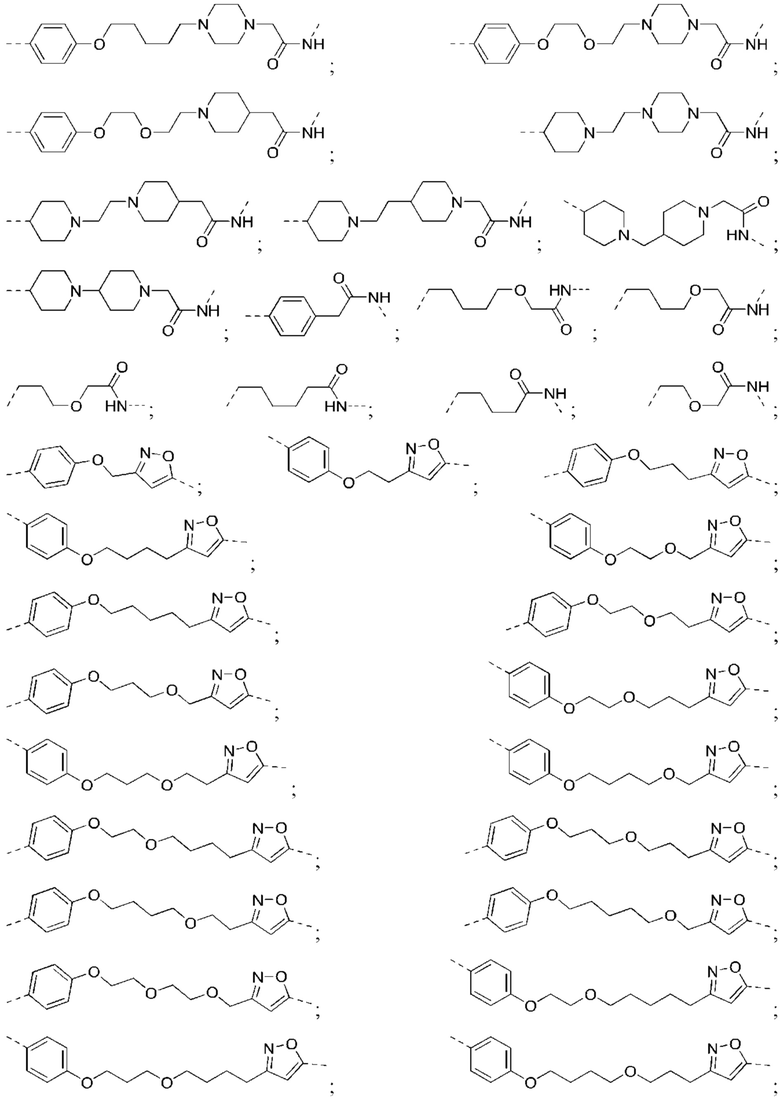





[288] В дополнительных вариантах осуществления линкер (L) предусматривает структуру, выбранную без ограничения из структур, показанных ниже, где пунктирная линия указывает на точку присоединения к фрагментам РТМ или ULM.

где
каждый из WL1 и WL2 независимо представляет собой 4-8-членное кольцо с 0-4 гетероатомами, необязательно замещенное RQ, при этом каждая RQ независимо представляет собой Н, галоген, ОН, CN, CF3, NH2, карбоксил, C1-С6алкил (линейный, разветвленный, необязательно замещенный), C1-С6алкокси (линейный, разветвленный, необязательно замещенный), или 2 группы RQ, взятые вместе с атомом, к которому они присоединены, образуют 4-8-членную кольцевую систему, содержащую 0-4 гетероатома;
каждый YL1 независимо представляет собой связь, C1-С6алкил (линейный, разветвленный, необязательно замещенный), и необязательно один или более атомов С заменены О; или C1-С6алкокси (линейный, разветвленный, необязательно замещенный);
n составляет 0-10; и
пунктирная линия указывает на точку присоединения к фрагментам РТМ или ULM.
[289] В дополнительных вариантах осуществления линкер (L) предусматривает структуру, выбранную без ограничения из структур, показанных ниже, где пунктирная линия указывает на точку присоединения к фрагментам РТМ или ULM.
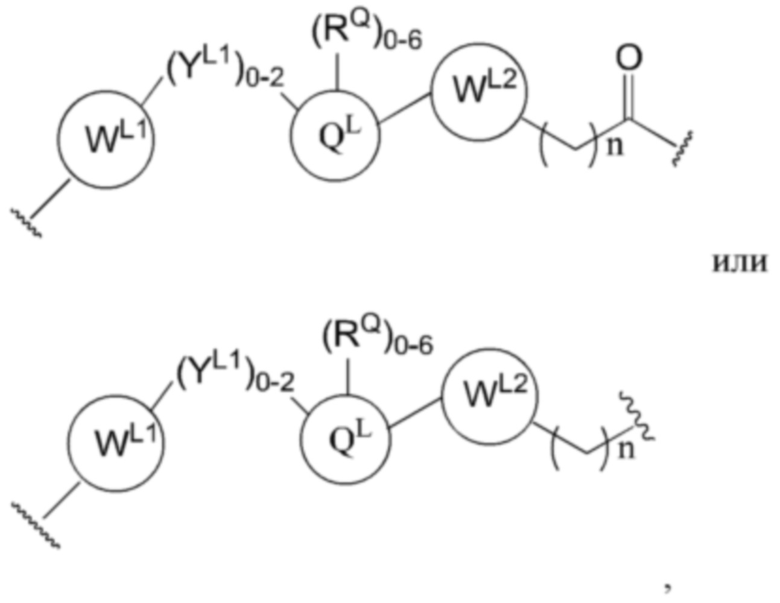
где
каждый из WL1 и WL2 независимо представляет собой арил, гетероарил, циклическую группу, гетероциклическую группу, C1-6алкил (линейный, разветвленный, необязательно замещенный), С1-С6алкокси (линейный, разветвленный, необязательно замещенный), бициклическую группу, биарил, бигетероарил или бигетероциклическую группу, при этом каждое необязательно замещено RQ, при этом каждая RQ независимо представляет собой Н, галоген, ОН, CN, CF3, NH2, карбоксил, гидроксил, нитро, С≡СН, С2-6алкенил, С2-6алкинил, C1-С6алкил (линейный, разветвленный, необязательно замещенный), C1-С6алкокси (линейный, разветвленный, необязательно замещенный), OC1-3алкил (необязательно замещенный 1 или более -F), ОН, NH2, NRY1RY2, CN, или 2 группы RQ, взятые вместе с атомом, к которому они присоединены, образуют 4-8-членную кольцевую систему, содержащую 0-4 гетероатома;
каждый YL1 независимо представляет собой связь, NRYL1, О, S, NRYL2, CRYL1RYL2, С=O, C=S, SO, SO2, C1-С6алкил (линейный, разветвленный, необязательно замещенный), и необязательно один или более атомов С заменены О; C1-С6алкокси (линейный, разветвленный, необязательно замещенный);
QL представляет собой 3-6-членное алициклическое или ароматическое кольцо с 0-4 гетероатомами, бигетероциклическое или бициклическое, необязательно соединенное мостиковой связью, необязательно замещенное 0-6 RQ, при этом каждая RQ независимо представляет собой Н, C1-6алкил (линейный, разветвленный, необязательно замещенный 1 или более атомами галогена, С1-6алкоксилом), или 2 группы RQ, взятые вместе с атомом, к которому они присоединены, образуют 3-8-членную кольцевую систему, содержащую 0-2 гетероатома);
каждый из RYL1, RYL2 независимо представляет собой Н, ОН, C1-6алкил (линейный, разветвленный, необязательно замещенный 1 или более атомами галогена, C1-6алкоксилом), или R1, R2 вместе с атомом, к которому они присоединены, образуют 3-8-членную кольцевую систему, содержащую 0-2 гетероатома);
n составляет 0-10; и
пунктирная линия указывает на точку присоединения к фрагментам РТМ или ULM.
[290] В дополнительных вариантах осуществления линкерная группа представляет собой необязательно замещенный (поли)этиленгликоль, содержащий от 1 до приблизительно 100 этиленгликолевых звеньев, от приблизительно 1 до приблизительно 50 этиленглико левых звеньев, от 1 до приблизительно 25 этиленглико левых звеньев, от приблизительно 1 до 10 этиленглико левых звеньев, от 1 до приблизительно 8 этиленгликолевых звеньев и от 1 до 6 этиленгликолевых звеньев, от 2 до 4 этиленгликолевых звеньев, или необязательно замещенные алкильные группы с вкраплениями необязательно замещенных атомов О, N, S, Р или Si. В определенных вариантах осуществления линкер замещен арильной, фенильной, бензильной, алкильной, алкиленовой или гетероциклической группой. В определенных вариантах осуществления линкер может являться асимметричным или симметричным.
[291] В любом из вариантов осуществления соединений, описанных в данном документе, линкерная группа может представлять собой любой подходящий фрагмент, описанный в данном документе. В одном варианте осуществления линкер представляет собой замещенную или незамещенную полиэтиленгликолевую группу с размером в диапазоне от приблизительно 1 до приблизительно 12 этиленгликолевых звеньев, от 1 до приблизительно 10 этиленгликолевых звеньев, приблизительно от 2 приблизительно до 6 этиленгликолевых звеньев, от приблизительно 2 до 5 этиленгликолевых звеньев, от приблизительно 2 до 4 этиленгликолевых звеньев.
[292] В другом варианте осуществления настоящее изобретение направлено на соединение, которое предусматривает группу РТМ, описанную выше, которая связывается с целевым белком (например, ER) или полипептидом, которые убиквитинированы убиквитинлигазой и непосредственно химически соединены с группой ULM или посредством линкерного фрагмента L, или альтернативно РТМ представляет собой группу ULM', которая также является фрагментом, связывающим Е3-убиквитинлигазу, который может быть идентичным или отличным от группы ULM, описанной выше, и непосредственно соединен с группой ULM непосредственно или посредством линкерного фрагмента; и при этом L представляет собой линкерный фрагмент, описанный выше, который может присутствовать или отсутствовать и который химически (ковалентно) связывает ULM с РТМ, или его фармацевтически приемлемую соль, энантиомер, стереоизомер, сольват или полиморф.
[293] В определенных вариантах осуществления линкерная группа L представляет собой группу, содержащую одно или более ковалентно связанных структурных звеньев, независимо выбранных из группы, состоящей из
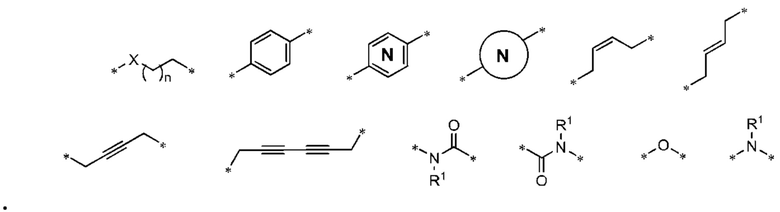
X выбран из группы, состоящей из О, N, S, S(O) и SO2; n представляет собой целое число от 1 до 5; RL1 представляет собой водород или алкил, 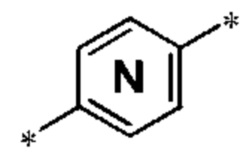 представляет собой моно- или бициклический арил или гетероарил, необязательно замещенные 1-3 заместителями, выбранными из алкила, галогена, галогеналкила, гидрокси, алкокси или пиано;
представляет собой моно- или бициклический арил или гетероарил, необязательно замещенные 1-3 заместителями, выбранными из алкила, галогена, галогеналкила, гидрокси, алкокси или пиано;  представляет собой моно- или бициклический циклоалкил или гетероциклоалкил, необязательно замещенные 1-3 заместителями, выбранными из алкила, галогена, галогеналкила, гидрокси, алкокси или циано; и фрагмент фенильного кольца может быть необязательно замещен 1, 2 или 3 заместителями, выбранными из группы, состоящей из алкила, галогена, галогеналкила, гидрокси, алкокси и циано. В одном варианте осуществления линкерная группа L содержит не более 10 ковалентно связанных структурных звеньев, описанных выше.
представляет собой моно- или бициклический циклоалкил или гетероциклоалкил, необязательно замещенные 1-3 заместителями, выбранными из алкила, галогена, галогеналкила, гидрокси, алкокси или циано; и фрагмент фенильного кольца может быть необязательно замещен 1, 2 или 3 заместителями, выбранными из группы, состоящей из алкила, галогена, галогеналкила, гидрокси, алкокси и циано. В одном варианте осуществления линкерная группа L содержит не более 10 ковалентно связанных структурных звеньев, описанных выше.
[294] Хотя группа ULM и группа РТМ могут быть ковалентно связаны с линкерной группой посредством любой группы, которая является подходящей и устойчивой относительно химической природы линкера, в предпочтительных аспектах настоящего изобретения линкер независимо ковалентно связан с группой ULM и группой РТМ предпочтительно посредством амидной, сложноэфирной, сложнотиоэфирной групп, кетогруппы, карбаматной группы (уретановой группы), атома углерода или эфирной группы, каждая группа из которых может быть включена где-либо на группе ULM и группе РТМ с обеспечением максимального связывания группы ULM с убиквитинлигазой и группы РТМ с целевым белком, подлежащим разрушению. (Следует отметить, что в определенных аспектах, если группа РТМ представляет собой группу ULM, целевой белок, подлежащий разрушению, может сам по себе представлять убиквитинлигазу). В определенных предпочтительных аспектах линкер может быть соединен с необязательно замещенной алкильной, алкиленовой, алкеновой или алкиновой группой, арильной группой или гетероциклической группой на группах ULM и/или РТМ.
Иллюстративные РТМ
[295] В предпочтительных аспектах настоящего изобретения группа РТМ представляет собой группу, которая связывается с целевыми белками. Мишени группы РТМ являются многочисленными по своей природе и выбраны из белков, которые экспрессируются в клетке так, что по меньшей мере часть последовательностей встречается в клетке и может связываться с группой РТМ. Термин «белок» включает олигопептиды и полипептидные последовательности достаточной длины для того, чтобы они могли связываться с группой РТМ в соответствии с настоящим изобретением. Любой белок в эукариотической системе или микробной системе, в том числе вирусе, бактерии или грибах, как описано далее в данном документе, являются мишенями убиквитинирования, опосредованного соединениями в соответствии с настоящим изобретением. Предпочтительно целевой белок представляет собой эукариотический белок.
[296] Группы РТМ в соответствии с настоящим изобретением включают, например, любой фрагмент, который специфически связывается с белком (связывается с целевым белком), и включают следующие неограничивающие примеры низкомолекулярных фрагментов, нацеливающихся на белок: ингибиторы Hsp90, ингибиторы киназы, ингибиторы HDM2 и MDM2, соединения, нацеливающиеся на бромодоменсодержащие белки человека BET, ингибиторы HDAC, ингибиторы лизинметилтрансферазы человека, ингибиторы ангиогенеза, соединения, воздействующие на ядерные гормональные рецепторы, иммуносупрессорные соединения и соединения, целенаправленно воздействующие на рецептор ароматических углеводородов (AHR), среди многочисленных других. В композициях, описанных ниже, проиллюстрированы некоторые из представителей низкомолекулярных фрагментов, связывающих целевой белок. Такие низкомолекулярные фрагменты, связывающие целевой белок, также включают фармацевтически приемлемые соли, энантиомеры, сольваты и полиморфы таких композиций, а также другие малые молекулы, которые могут нацеливаться на белок, представляющий интерес. Такие связывающие фрагменты соединены с фрагментом, связывающим убиквитинлигазу, предпочтительно с помощью линкера с целью размещения целевого белка (с которым связан фрагмент, нацеливающийся на белок) в непосредственной близости от убиквитинлигазы для убиквитинирования и разрушения.
[297] Любой белок, который может связываться с фрагментом, нацеливающимся на белок, или группой РТМ и может подвергаться действию убиквитинлигазы или разрушаться ею, является целевым белком в соответствии с настоящим изобретением. В целом, целевые белки могут включать, например, структурные белки, рецепторы, ферменты, белки поверхности клеток, белки, относящиеся к общему функционированию клетки, в том числе белки, вовлеченные в каталитическую активность, ароматазную активность, двигательную активность, хеликазную активность, метаболические процессы (анаболизм и катаболизм), антиоксидантную активность, протеолиз, биосинтез, белки с киназной активностью, оксидоредуктазной активностью, трансферазной активностью, гидролазной активностью, лиазной активностью, изомеразной активностью, лигазной активностью, активностью регуляторного фермента, активностью переносчика сигнала, активностью структурной молекулы, связывающей активностью (белок, липид, углевод), рецепторной активностью, вовлеченные в клеточную подвижность, мембранный синтез, клеточную коммуникацию, регуляцию биологических процессов, развитие, клеточную дифференциацию, ответ на стимул, ассоциированные с поведением клетки белки, ассоциированные с адгезией клеток белки, белки, вовлеченные в гибель клеток, белки, вовлеченные в транспорт (в том числе активность транспортера белков, ядерно-цитоплазматический транспорт, активность ионного транспортера, активность канала-транспортера, активность в отношении переноса, пермеазная активность, активность в отношении секреции, активность транспортера электронов, патогенез, активность регулятора шаперонов, активность в отношении связывания нуклеиновой кислоты, активность регулятора транскрипции, активность в отношении внеклеточной организации и биогенеза, активность регулятора трансляции). Белки, представляющие интерес, могут включать белки эукариотов и прокариотов, в том числе людей как мишени для терапии лекарственным средством, других животных, в том числе домашних животных, микроорганизмов для определения мишеней антибиотиков и других противомикробных средств и растений и даже вирусов, среди многочисленных других.
[298] Настоящее изобретение может применяться для лечения ряда болезненных состояний и/или состояний, в том числе любого болезненного состояния и/или состояния, при котором нарушена регуляция белков, и при котором пациент получит пользу от разрушения и/или ингибирования белков.
[299] В дополнительном аспекте в описании представлены терапевтические композиции, содержащие эффективное количество соединения, описанного в данном документе, или его солевой формы и фармацевтически приемлемый носитель, добавку или вспомогательное вещество и необязательно дополнительное биологически активное средство. Терапевтические композиции модулируют разрушение белка у пациента или субъекта, например, у животного, как, например, у человека, и могут применяться для лечения или облегчения болезненных состояний или состояний, модулирование которых обеспечивается посредством разрушения белка. В определенных вариантах осуществления терапевтические композиции, описанные в данном документе, можно применять для обеспечения разрушения белков, представляющих интерес, для лечения или облегчения заболевания, например рака. В определенных дополнительных вариантах осуществления заболевание представляет собой рак молочной железы. В определенных дополнительных вариантах осуществления заболевание представляет собой по меньшей мере одно из рака молочной железы, рака матки, рака яичников, рака предстательной железы, рака эндометрия, эндометриоза или их комбинации.
[300] В альтернативных аспектах настоящее изобретение относится к способу лечения болезненного состояния или облегчения симптомов заболевания или состояния у субъекта, нуждающегося в этом, путем разрушения белка или полипептида, за счет которых модулируется болезненное состояние или состояние, включающему введение указанному пациенту или субъекту эффективного количества, например терапевтически эффективного количества, по меньшей мере одного соединения, описанного в данном документе выше, необязательно в комбинации с фармацевтически приемлемым носителем, добавкой или вспомогательным веществом и необязательно дополнительным биологически активным средством, при этом композиция является эффективной в лечении или облегчении заболевания или нарушения или их симптома у субъекта. Способ в соответствии с настоящим изобретением можно применять для лечения большого количества болезненных состояний или состояний, в том числе рака, посредством введения эффективного количества по меньшей мере одного соединения, описанного в данном документе. Болезненное состояние или состояние может представлять собой заболевание, вызванное микробным организмом или другим экзогенным организмом, таким как вирус, бактерия, гриб, простейшие или другой микроорганизм, или может представлять собой болезненное состояние, которое вызвано сверхэкспрессией белка, что приводит к болезненному состоянию и/или состоянию.
[301] В другом аспекте в описании предусмотрены способы идентификации эффектов разрушения белков, представляющих интерес, в биологической системе с применением соединений в соответствии с настоящим изобретением.
[302] Термин «целевой белок» используется в данном документе для описания белка или полипептида, которые представляют собой мишень для связывания с соединением в соответствии с настоящим изобретением и разрушения посредством убиквитинлигазы. Такие низкомолекулярные фрагменты, связывающие целевой белок, также включают фармацевтически приемлемые соли, энантиомеры, сольваты и полиморфы таких композиций, а также другие малые молекулы, которые могут нацеливаться на белок, представляющий интерес. Данные связывающие фрагменты соединены с по меньшей мере одной группой ULM (например, VLM, CLM, ILM и/или MLM) с помощью по меньшей мере одной линкерной группы L.
[303] Целевые белки, которые могут быть связаны с фрагментом, нацеливающимся на белок, и разрушены с помощью лигазы, с которой связан фрагмент, связывающий убиквитинлигазу, включают любые белок или пептид, в том числе их фрагменты, их аналоги и/или их гомологи. Целевые белки включают белки и пептиды, обладающие любой биологической функцией или активностью, в том числе структурной, регуляторной, гормональной, ферментативной, генетической, иммунологической, сократительной, в отношении хранения, транспорта и передачи сигнала. Более конкретно, ряд мишеней для лекарственного средства для терапевтических средств для человека представляет собой белки-мишени, с которыми может связываться фрагмент, нацеливающийся на белок, и встраивать их в соединения в соответствии с настоящим изобретением. Они включают белки, которые можно применять для сохранения функции при многочисленных полигенных заболеваниях, в том числе, например, В7.1 и В7, TINFR1m, TNFR2, NADPH-оксидаза, BclIBax и другие партнеры в пути апоптоза, рецептор С5а, HMG-CoA-редуктаза, фосфодиэстераза типа PDE V, фосфодиэстераза типа 4 PDE IV, PDE I, PDEII, PDEIII, ингибитор скваленциклазы, CXCR1, CXCR2, синтаза оксида азота (NO), циклооксигеназа 1, циклооксигеназа 2, рецепторы 5НТ, дофаминовые рецепторы, G-белки, т.е. Gq, гистаминовые рецепторы, 5-липооксигеназа, триптаза, представляющая собой серинпротеазу, тимидилатсинтаза, пурин-нуклеозидфосфорилаза, GAPDH трипаносом, гликогенфосфорилаза, угольная ангидраза, хемокиновые рецепторы, JAW STAT, RXR и подобные, протеаза HIV 1, интеграза HIV 1, нейраминидаза вируса гриппа, обратная транскриптаза гепатита В, натриевый канал, белок множественной лекарственной устойчивости (MDR), Р-гликопротеин (и MRP), тирозинкиназы, CD23, CD124, тирозинкиназа р56 lck, CD4, CD5, рецептор IL-2, рецептор, IL-1 TNF-альфаR, ICAM1, каналы Cat+, VCAM, интегрин VLA-4, селектины, CD40/CD40L, невокинины и рецепторы, инозинмонофосфатдегидрогеназа, МАР-киназа р38, путь RaslRaflMEWERK, превращающий интерлейкин-1 фермент, каспаза, HCV, протеаза NS3, геликаза РНК HCV NS3 RNA, глицинамид-рибонуклеотид-формилтрансфераза, протеаза риновируса 3С, протеаза вируса простого герпеса-1 (HSV-I), протеаза цитомегаловируса (CMV), поли(ADP-рибоза)полимераза, циклинзависимые киназы, фактор роста эндотелия сосудов, окситоциновый рецептор, ингибитор микросомального транспортного белка, ингибитор транспорта желчных кислот, ингибиторы 5-альфа-редуктазы, ангиотензин-11, глициновый рецептор, рецептор обратного захвата норадреналина, эндотелиновые рецепторы, нейропептид Y и рецептор, эстрогеновые рецепторы, андрогеновые рецепторы, аденозиновые рецепторы, аденозинкиназа и АМР-дезаминаза, пуринергические рецепторы (P2Y1, P2Y2, P2Y4, P2Y6, Р2Х1-7), фарнезилтрансферазы, геранилгеранилтрансфераза, рецептор TrkA для NGF, бета-амилоид, тирозинкиназа Flk-IIKDR, витронектиновый рецептор, интегриновый рецептор, Her-21 neu, ингибитор теломеразы, питозольный фосфолипаза А2 и рецепторная тирозинкиназа. Дополнительные белки-мишени включают, например, экдизон 20-монооксидазу, ионный канал, представляющий собой лигандзависимый хлоридный канал GABA, ацетилхолинэстеразу, белок, представляющий собой потенциалочувствительный натриевый канал, кальций, высвобождающий канал из клетки, и хлоридные каналы. Еще одни дополнительные целевые белки включают ацетил-СоА-карбоксилазу, аденилосукцинатсинтетазу, протопорфириногеноксидазу и енолпирувилшикиматфосфатсинтазу.
[304] Данные различные белки-мишени можно применять в скринингах по идентификации фрагментов соединения, которые связываются с белком, и посредством встраивания фрагмента в соединения в соответствии с настоящим изобретением уровень активности белка может быть изменен для достижения конечного терапевтического результата.
[305] Термин «фрагмент, нацеливающийся на белок» или РТМ используется для описания малой молекулы, которая связывается с целевым белком или другим белком или полипептидом, представляющим интерес, и обеспечивает размещение/присутствие данного белка или полипептида в непосредственной близости от убиквитинлигазы таким образом, что может происходить разрушение белка или полипептида посредством убиквитинлигазы. Неограничивающие примеры низкомолекулярных фрагментов, связывающих целевой белок, включают ингибиторы Hsp90, ингибиторы киназы, ингибиторы MDM2, соединения, целенаправленно воздействующие на бромодоменсодержащие белки BET человека, ингибиторы HDAC, ингибиторы лизинметилтрансферазы человека, ингибиторы ангиогенеза, иммуносупрессорные соединения и соединения, целенаправленно воздействующие на рецептор ароматических углеводородов (AHR), среди многочисленных других. В композициях, описанных ниже, проиллюстрированы некоторые из представителей низкомолекулярных целевых белков.
[306] Иллюстративные фрагменты, нацеливающиеся на белок, в соответствии с настоящим изобретением включают, ингибиторы галогеналкандегалогеназы, ингибиторы Hsp90, ингибиторы киназы, ингибиторы MDM2, соединения, целенаправленно воздействующие на бромодоменсодержащие белки BET человека, ингибиторы HDAC, ингибиторы лизинметилтрансферазы человека, ингибиторы ангиогенеза, иммуносупрессорные соединения и соединения, целенаправленно воздействующие на рецептор ароматических углеводородов (AHR).
[307] В композициях, описанных в данном документе, проиллюстрированы некоторые из представителей данных типов низкомолекулярных фрагментов, связывающих целевой белок. Такие низкомолекулярные фрагменты, связывающие целевой белок, также включают фармацевтически приемлемые соли, энантиомеры, сольваты и полиморфы таких композиций, а также другие малые молекулы, которые могут нацеливаться на белок, представляющий интерес. Источники, цитируемые в данном документе ниже, включены в данный документ посредством ссылки во всей своей полноте.
[308] В другом аспекте настоящее изобретение предусматривает соединение или РТМ формулы (IPTM),

где
каждый ХРТМ независимо представляет собой СН, N;
 указывает на место присоединения по меньшей мере одного линкера, VLM, VLM', CLM, CLM', ILM, ILM', VLM, РТМ, РТМ' или их комбинации;
указывает на место присоединения по меньшей мере одного линкера, VLM, VLM', CLM, CLM', ILM, ILM', VLM, РТМ, РТМ' или их комбинации;
каждый RPTM1 независимо представляет собой ОН, галоген, O(CO)RPTM, где RPTM представляет собой алкильную или циклоалкильную группу с 1-6 атомами углерода или арильные группы, при этом замещение может предусматривать моно-, ди- или тризамещение;
каждый RPTM2 независимо представляет собой Н, галоген, CN, CF3, алкокси, при этом замещение может предусматривать моно- или дизамещение; и
каждый RPTM3 независимо представляет собой Н, галоген, при этом замещение может предусматривать моно- или дизамещение.
[309] В любом аспекте или варианте осуществления, описанных в данном документе, РТМ представлен формулой (IIPTM),

где
ХРТМ представляет собой СН, N;
 указывает на место присоединения по меньшей мере одного линкера, VLM, VLM', CLM, CLM', ILM, ILM', VLM, РТМ, РТМ' или их комбинации;
указывает на место присоединения по меньшей мере одного линкера, VLM, VLM', CLM, CLM', ILM, ILM', VLM, РТМ, РТМ' или их комбинации;
каждый RPTM1 независимо представляет собой ОН, галоген (например, F);
каждый RPTM2 независимо представляет собой Н, галоген (например, F), CF3, при этом замещение может предусматривать моно- или дизамещение; и
каждый RPTM3 независимо представляет собой галоген (например, F), при этом замещение может предусматривать моно- или дизамещение.
[310] В определенных вариантах осуществления в по меньшей мере одном из L
ХРТМ в формуле (IIPTM) представляет собой СН;
RPTM1 в формуле (IIPTM) представляет собой ОН;
RPTM2 в формуле (IIPTM) представляет собой Н;
каждый RPTM3 в формуле (IIPTM) независимо представляет собой Н или F;
или их комбинация.
Иллюстративные PROTAC, целенаправленно воздействующие на ER
[311] В настоящем изобретении определены соединения, способные подавлять функцию эстрогенового рецептора, в том числе соединения, которые разрушают эстрогеновый рецептор.
[312] Как описано выше, в любом аспекте или варианте осуществления, описанных в данном документе, настоящее изобретение предусматривает бифункциональные соединения PROTAC, содержащие по меньшей мере одну тетрагидронафталиновую группу, тетрагидроизохинолиновую группу или их комбинацию; линкер и по меньшей мере один из лиганда, связывающегося с VHL, лиганда, связывающегося с цереблоном, или их комбинации.
[313] В любом аспекте или варианте осуществления, описанных в данном документе, соединение выбрано из группы, состоящей из соединений 1-547 (показанных на таблицах 1 и 2) и их солей и полиморфов.
Терапевтические композиции
[314] Фармацевтические композиции, содержащие комбинации эффективного количества по меньшей мере одного бифункционального соединения, описанного в данном документе, и одно или более из соединений, описанных далее в данном документе, все в эффективных количествах, в комбинации с фармацевтически эффективным количеством носителя, добавки или вспомогательного вещества, представляют собой дополнительный аспект настоящего изобретения.
[315] В настоящее изобретение включены в применимых случаях композиции, содержащие фармацевтически приемлемые соли, в частности, соли присоединения кислоты или основания соединений, описанных в данном документе. Кислоты, которые применяют для получения фармацевтически приемлемых солей присоединения кислоты вышеуказанных основных соединений, пригодных в соответствии с данным аспектом, представляют собой кислоты, которые образуют нетоксичные соли присоединения кислоты, т.е. соли, содержащие фармакологически приемлемые анионы, такие как, среди ряда других, гидрохлоридные, гидробромидные, гидройодидные, нитратные, сульфатные, бисульфатные, фосфатные, кислые фосфатные, ацетатные, лактатные, цитратные, кислые цитратные, тартратные, битартратные, сукцинатные, малеатные, фумаратные, глюконатные, сахаратные, бензоатные, метансульфонатные, этансульфонатные, ензолсульфонатные, п-толуолсульфонатные и памоатные [т.е. 1,1'-метилен-бис-(2-гидрокси-3 нафтоат)] соли.
[316] Фармацевтически приемлемые соли присоединения основания также могут применяться для получения фармацевтически приемлемых форм солей соединений или производных в соответствии с настоящим изобретением. Химические основания, которые можно применять в качестве реагентов для получения фармацевтически приемлемых основных солей соединений по настоящему изобретению, которые имеют кислотную природу, представляют собой основания, которые образуют нетоксичные основные соли с такими соединениями. Такие нетоксичные основные соли включают, среди прочих, без ограничения соли, полученные из таких фармакологически приемлемых катионов, как катионы щелочных металлов (например, калия и натрия) и катионы щелочноземельных металлов (например, кальция, цинка и магния), аммониевые или водорастворимые соли присоединения амина, как, например, N-метилглюкаминовые (меглюминовые) и низшие алканоламмониевые, а также другие основные соли фармацевтически приемлемых органических аминов.
[317] Соединения, описанные в данном документе, в соответствии с настоящим изобретением можно вводить одной дозой или разделенными дозами пероральным, парентеральным или местным путями. Введение активного соединения может варьироваться от непрерывного (внутривенное вливание) до нескольких пероральных введений в сутки (например, Q.I.D.) и может включать среди прочих путей введения пероральное, местное, парентеральное, внутримышечное, внутривенное, подкожное, трансдермальное (которое может включать средство, усиливающее проникновение), буккальное, подъязычное и суппозиторное введение. Таблетки для перорального применения, покрытые кишечнорастворимой оболочкой, также можно применять для увеличения биодоступности соединений при пероральном пути введения. Наиболее эффективная лекарственная форма будет зависеть от фармакокинетических характеристик конкретного выбранного средства, а также тяжести заболевания у пациента. Также может использоваться введение соединений в соответствии с настоящим изобретением в виде спреев, туманов или аэрозолей для интраназального, интратрахеального или ингаляционного введения. Следовательно, настоящее изобретение также направлено на фармацевтические композиции, содержащие эффективное количество соединения, описанного в данном документе, необязательно в комбинации с фармацевтически приемлемым носителем, добавкой или вспомогательным веществом. Соединения в соответствии с настоящим изобретением можно вводить в формах с немедленным высвобождением, с высвобождением через определенные промежутки времени или с замедленным или контролируемым высвобождением. Формы с замедленным или контролируемым высвобождением предпочтительно вводят перорально, но также в суппозиторной и трансдермальной или других формах для местного применения. Внутримышечные инъекции в липосомной форме также можно применять для контроля или замедления высвобождения соединения в месте инъекции.
[318] Композиции, описанные в данном документе, можно составлять традиционным способом с применением одного или более фармацевтически приемлемых носителей, а также их можно вводить в виде составов с контролируемым высвобождением. Фармацевтически приемлемые носители, которые можно применять в данных фармацевтических композициях, включают без ограничения иониты, оксид алюминия, стеарат алюминия, лецитин, сывороточные белки, такие как сывороточный альбумин человека, буферные вещества, такие как фосфаты, глицин, сорбиновая кислота, сорбат калия, смеси неполных глицеридов насыщенных растительных жирных кислот, воду, соли или электролиты, такие как проламин сульфат, гидрофосфат динатрия, гидрофосфат калия, хлорид натрия, соли цинка, коллоидный диоксид кремния, трисиликат магния, поливинилпирролидон, вещества на основе целлюлозы, полиэтиленгликоль, натрий-карбоксиметилцеллюлозу, полиакрилаты, воски, блок-сополимеры полиэтилена и полиоксипропилена, полиэтиленгликоль и ланолин.
[319] Композиции, описанные в данном документе, можно вводить перорально, парентерально, с помощью ингаляционного спрея, местно, ректально, назально, буккально, вагинально или посредством имплантированного резервуара. Термин «парентеральный», используемый в данном документе, включает методики подкожной, внутривенной, внутримышечной, внутрисуставной, интрасиновиальной, интрастернальной, интратекальной, внутрипеченочной, внутриочаговой и внутричерепной инъекции или инфузии. Композиции предпочтительно вводят перорально, внутрибрюшинно или внутривенно.
[320] Стерильные инъекционные формы композиций, описанных в данном документе, могут представлять собой водную или маслянистую суспензию. Данные суспензии можно составлять в соответствии с методиками, известными из уровня техники, с применением подходящих диспергирующих или смачивающих средств и суспендирующих средств. Стерильный инъекционный препарат также может представлять собой стерильные инъекционные раствор или суспензию в нетоксичных разбавителе или растворителе, приемлемых для парентерального введения, например, в виде раствора в 1,3-бутандиоле. Приемлемыми средами-носителями и растворителями, которые можно применять, являются вода, раствор Рингера и изотонический раствор хлорида натрия. Кроме того, стерильные нелетучие масла традиционно применяют в качестве растворителя или суспендирующей среды. Для этой цели можно применять любое легкое нелетучее масло, в том числе синтетические моно- или диглицериды. Жирные кислоты, такие как олеиновая кислота, и их производные, представляющие собой глицериды, являются применимыми для получения инъекционных препаратов, также как и природные фармацевтически приемлемые масла, такие как оливковое масло или касторовое масло, особенно в их полиоксиэтилированных формах. Данные масляные растворы или суспензии также могут содержать разбавитель или диспергирующее средство, представляющее собой длинноцепочечный спирт, такой как указанный в фармакопеи Швейцарии или подобный спирт.
[321] Фармацевтические композиции, описанные в данном документе, можно вводить перорально в любой лекарственной форме, приемлемой для перорального введения, в том числе без ограничения в капсулах, таблетках, водных суспензиях или растворах. В случае таблеток для перорального применения общепринятые носители включают лактозу и кукурузный крахмал. Также, как правило, добавляют смазывающие средства, такие как стеарат магния. Для перорального введения в форме капсул применимые разбавители включают лактозу и высушенный кукурузный крахмал. Если для перорального применения требуются водные суспензии, то активный ингредиент объединяют с эмульгирующими и суспендирующими средствами. При необходимости также можно добавлять определенные подсластители, ароматизаторы или красящие вещества.
[322] В качестве альтернативы, фармацевтические композиции, описанные в данном документе, можно вводить в форме суппозиториев для ректального введения. Их можно получить посредством смешивания средства с подходящим не вызывающим раздражения вспомогательным веществом, которое является твердым при комнатной температуре, но жидким при температуре в прямой кишке, и, следовательно, будет плавиться в прямой кишке с высвобождением лекарственного средства. Такие материалы включают масло какао, пчелиный воск и полиэтиленгликоли.
[323] Фармацевтические композиции, описанные в данном документе, также можно вводить местно. Подходящие составы для местного применения легко получить для каждой из таких областей или органов. Местное применение по отношению к нижнему отделу кишечника можно осуществлять с помощью состава, представляющего собой ректальный суппозиторий (см. выше), или подходящего состава для спринцевания. Также можно применять приемлемые для местного применения трансдермальные пластыри.
[324] Для местных применений фармацевтические композиции можно составлять в форме подходящей мази, содержащей активный компонент, суспендированный или растворенный в одном или более носителях. Носители для местного введения соединений по настоящему изобретению включают без ограничения минеральное масло, вазелиновое масло, белый вазелин, соединение, представляющее собой пропиленгликоль, полиоксиэтилен, полиоксипропилен, эмульгированный воск и воду. В определенных предпочтительных аспектах настоящего изобретения соединения можно наносить в виде покрытия на стент, который хирургическим путем имплантируют пациенту, с целью предотвращения окклюзии в стенте у пациента или снижения вероятности ее возникновения.
[325] В качестве альтернативы, фармацевтические композиции можно составлять в форме подходящего лосьона или крема, содержащего активные компоненты, суспендированные или растворенные в одном или более фармацевтически приемлемых носителях. Подходящие носители включают без ограничения минеральное масло, сорбитанмоностеарат, полисорбат 60, воск в виде сложных цетиловых эфиров, цетеариловый спирт, 2-октилдодеканол, бензиловый спирт и воду.
[326] Для офтальмологического применения фармацевтические композиции можно составлять в виде тонкодисперсных суспензий в изотоническом стерильном солевом растворе с отрегулированным значением рН или предпочтительно в виде растворов в изотоническом стерильном солевом растворе с отрегулированным значением рН с консервантом, таким как хлорид бензалкония, или без него. В качестве альтернативы, для офтальмологических применений фармацевтические композиции можно составлять в форме мази, как, например, с вазелином.
[327] Фармацевтические композиции, описанные в данном документе, также можно вводить с помощью назального аэрозоля или посредством ингаляции. Такие композиции получают в соответствии с методиками, хорошо известными в области фармацевтического составления, и их можно получать в виде растворов в солевом растворе с применением бензилового спирта или других подходящих консервантов, стимуляторов абсорбции для увеличения биодоступности, фторуглеродов и/или других традиционных солюбилизирующих или диспергирующих средств.
[328] Количество соединения в фармацевтической композиции, описанной в данном документе, которое может быть объединено с материалами-носителями с получением единой лекарственной формы, будет изменяться в зависимости от организма и заболевания, подлежащих лечению, конкретного способа введения. Предпочтительно, композиции должны быть составлены таким образом, чтобы содержать от приблизительно 0,05 миллиграмм до приблизительно 750 миллиграмм или больше, более предпочтительно от приблизительно 1 миллиграмм до приблизительно 600 миллиграмм и еще более предпочтительно от приблизительно 10 миллиграмм до приблизительно 500 миллиграмм активного ингредиента в отдельности или в комбинации с по меньшей мере одним другим соединением в соответствии с настоящим изобретением.
[329] Также следует понимать, что конкретный режим дозирования и схема лечения для любого конкретного пациента будут зависеть от ряда факторов, в том числе от активности конкретного применяемого соединения, возраста, веса тела, общего состояния здоровья, пола, рациона, времени введения, скорости экскреции, комбинации лекарственных средств и оценки лечащего врача, а также тяжести конкретного заболевания или состояния, подлежащих лечению.
[330] Пациента или субъекта, нуждающихся в терапии с применением соединений в соответствии со способами, описанными в данном документе, можно лечить путем введения пациенту (субъекту) эффективного количества соединения в соответствии с настоящим изобретением, в том числе его фармацевтически приемлемых солей, сольватов или полиморфов, необязательно в фармацевтически приемлемом носителе или разбавителе, либо отдельно, либо в комбинации с другими известными терапевтическими средствами, определенными далее в данном документе.
[331] Данные соединения можно вводить любым подходящим путем, например, перорально, парентерально, внутривенно, внутрикожно, подкожно или местно, в том числе трансдермально, в форме жидкости, крема, геля или твердой форме или в форме аэрозоля.
[332] Активное соединение включают в фармацевтически приемлемый носитель или разбавитель в количестве, достаточном для доставки пациенту терапевтически эффективного количества для желаемого показания, не вызывая серьезных токсических эффектов у пациента, получающего лечение. Предпочтительная доза активного соединения для всех перечисленных в данном документе состояний находится в диапазоне от приблизительно 10 нг/кг до 300 мг/кг, предпочтительно от 0,1 до 100 мг/кг в сутки, в общем от 0,5 до приблизительно 25 мг на килограмм веса тела реципиента/пациента в сутки. Типичная доза для местного применения будет находиться в диапазоне от 0,01 до 5% вес/вес в подходящем носителе.
[333] Соединение удобно вводить в любой подходящей стандартной лекарственной форме, в том числе без ограничения лекарственной форме, содержащей менее 1 мг, от 1 мг до 3000 мг, предпочтительно от 5 до 500 мг активного ингредиента на единичную лекарственную форму. Доза для перорального введения, составляющая приблизительно 25-250 мг, зачастую является подходящей.
[334] Активный ингредиент предпочтительно вводят для достижения максимальных концентраций активного соединения в плазме крови, составляющих приблизительно 0,00001-30 мМ, предпочтительно приблизительно 0,1-30 мкМ. Этого можно достичь, например, посредством внутривенной инъекции раствора или состава активного ингредиента необязательно в солевом растворе или водной среде или введения активного ингредиента в виде болюса. Пероральное введение также является подходящим для достижения эффективных концентраций активного средства в плазме крови.
[335] Концентрация активного соединения в составе лекарственного средства будет зависеть от скоростей абсорбции, распределения, инактивации и экскреции лекарственного средства, а также от других факторов, известных специалистам в данной области техники. Следует отметить, что величины дозы также будут варьировать в зависимости от тяжести состояния, подлежащего облегчению. Также следует понимать, что для любого конкретного субъекта конкретные режимы дозирования должны корректироваться с течением времени в соответствии с индивидуальной потребностью и профессиональным суждением специалиста, осуществляющего или контролирующего введение композиций, и что диапазоны концентраций, изложенные в данном документе, являются исключительно иллюстративными и не предназначены для ограничения объема или применения на практике заявляемой композиции. Активный ингредиент можно вводить за один раз или можно разделить на несколько меньших доз, подлежащих введению с различными интервалами времени.
[336] Композиции для перорального применения обычно будут включать инертный разбавитель или съедобный носитель. Они могут быть заключены в желатиновые капсулы или спрессованы в таблетки. С целью перорального терапевтического введения активное соединение или его производное, представляющее собой пролекарство, можно объединять со вспомогательными веществами и применять в форме таблеток, пастилок или капсул. Фармацевтически совместимые связывающие вещества и/или вспомогательные материалы можно включать как часть композиции.
[337] Таблетки, пилюли, капсулы, пастилки и т.п. могут содержать любой из следующих ингредиентов или соединения подобного происхождения: связующее, такое как микрокристаллическая целлюлоза, трагакантовая камедь или желатин; вспомогательное вещество, такое как крахмал или лактоза, диспергирующее вещество, такое как альгиновая кислота, примогель или кукурузный крахмал; смазывающее вещество, такое как стеарат магния или Sterotes; вещество, способствующее скольжению, такое как коллоидный диоксид кремния; подсластитель, такой как сахароза или сахарин; или ароматизирующее вещество, такое как ароматизатор с запахом мяты перечной, метилсалицилат или ароматизатор с запахом апельсина. Если стандартная лекарственная форма представляет собой капсулу, то она может содержать в дополнение к материалу вышеуказанного типа жидкий носитель, такой как жирное масло. Кроме того, стандартные лекарственные формы могут содержать другие различные материалы, которые изменяют физическую форму лекарственной формы, например, покрытия из сахара, шеллака или кишечнорастворимых средств.
[338] Активное соединение или его фармацевтически приемлемую соль можно вводить в виде компонента настойки, суспензии, сиропа, облатки, жевательной резинки или т.п. Сироп может содержать в дополнение к активным соединениям сахарозу в качестве подсластителя и определенные консерванты, красители и красящие средства, а также вкусоароматические добавки.
[339] Активное соединение или его фармацевтически приемлемые соли также можно смешивать с другими активными материалами, которые не влияют отрицательно на необходимое действие, или с материалами, которые дополняют необходимое действие, такие как противораковые средства, среди прочих. В некоторых предпочтительных аспектах настоящего изобретения одно или более соединений в соответствии с настоящим изобретением совместно вводят с другим биологически активным средством, таким как противораковое средство или средство, способствующее заживлению ран, в том числе антибиотик, описанные далее в данном документе.
[340] Растворы или суспензии, используемые для парентерального, внутрикожного, подкожного или местного применения, могут включать следующие компоненты: стерильный разбавитель, такой как вода для инъекций, солевой раствор, нелетучие масла, полиэтиленгликоли, глицерин, пропиленгликоль или другие синтетические растворители; антибактериальные средства, такие как бензиловый спирт или метилпарабены; антиоксиданты, такие как аскорбиновая кислота или бисульфит натрия; хелатирующие вещества, такие как этилендиаминтетрауксусная кислота; буферы, такие как ацетаты, цитраты или фосфаты, и вещества для регулирования тоничности, такие как хлорид натрия или декстроза. Препарат для парентерального введения может содержаться в ампулах, одноразовых шприцах или многодозовых флаконах, изготовленных из стекла или пластика.
[341] При введении внутривенно предпочтительные носители представляют собой физиологический солевой раствор или фосфатно-солевой буферный раствор (PBS).
[342] В одном варианте осуществления активные соединения получают с носителями, которые будут защищать соединение от быстрого выведения из организма, как, например, состав с контролируемым высвобождением, в том числе имплантаты и микроинкапсулированные системы доставки. Можно применять биологически разлагаемые биосовместимые полимеры, такие как этиленвинилацетат, полиангидриды, полигликолевую кислоту, коллаген, сложные полиортоэфиры и полимолочную кислоту. Способы получения таких составов будут очевидны специалистам в данной области техники.
[343] Липосомные суспензии также могут представлять собой фармацевтически приемлемые носители. Их можно получить в соответствии со способами, известными специалистам в данной области техники, например, как описано в патенте США №4522811 (который включен в данный документ посредством ссылки во всей своей полноте). Например, липосомные составы можно получить путем растворения подходящего(-их) липида(-ов) (таких как стеароилфосфатидилэтаноламин, стеароилфосфатидилхолин, арахадоилфосфатидилхолин и холестерин) в неорганическом растворителе, который затем выпаривают, оставляя тонкую пленку высушенного липида на поверхности контейнера. Затем водный раствор активного соединения вносят в контейнер. Затем контейнер вращают вручную для отделения липидного материала от стенок контейнера и диспергирования липидных агрегатов, за счет чего образуется липосомная суспензия.
Терапевтические способы
[344] В дополнительном аспекте в описании представлены терапевтические композиции, содержащие эффективное количество соединения, описанного в данном документе, или его солевой формы и фармацевтически приемлемый носитель. Терапевтические композиции модулируют разрушение белка у пациента или субъекта, например, у животного, как, например, у человека, и могут применяться для лечения или облегчения болезненных состояний или состояний, модулирование которых обеспечивается посредством разрушения белка.
[345] Термины «лечить», «осуществлять лечение» и «лечение» и т.д., используемые в данном документе, относятся к любому действию, обеспечивающему пользу для пациента, которому могут вводить соединения по настоящему изобретению, в том числе лечение любого болезненного состояния или состояния, модулируемых за счет белка, с которым связываются соединения по настоящему изобретению. Болезненные состояния или состояния, в том числе рак и/или эндометриоз, которые можно лечить с применением соединений в соответствии с настоящим изобретением, изложены в данном документе выше.
[346] В описании представлены терапевтические композиции, описанные в данном документе, для обеспечения разрушения белков, представляющих интерес, для лечения или облегчения заболевания, например, рака. В определенных дополнительных вариантах осуществления заболевание представляет собой рак молочной железы, рак матки, рак яичников, рак эндометрия, эндометриоз, нейродегенеративное заболевание, воспалительное заболевание (например, красная волчанка), аутоиммунное заболевание (например, красная волчанка) или их комбинацию. В связи с этим, в другом аспекте в описании представлен способ обеспечения убиквитинирования/разрушения целевого белок в клетке. В определенных вариантах осуществления способ предусматривает введение бифункционального соединения, описанного в данном документе, содержащего, например, ULM и РТМ, предпочтительно соединенные посредством линкерного фрагмента, описанного далее в данном документе, где ULM связан с РТМ, и при этом ULM распознает белок убиквитинового пути (например, убиквитинлигазу, такую как Е3-убиквитинлигаза, в том числе цереблон, VHL, IAP и/или MDM2), и РТМ распознает целевой белок так, что при размещении целевого белка в непосредственной близости от убиквитинлигазы будет происходить разрушение целевого белка, что, таким образом приводит к разрушению целевого белка/подавлению его эффектов и контролю уровней белка. Контроль уровней белка, предоставляемый настоящим изобретением, обеспечивает лечение болезненного состояния или состояния, модулируемых за счет целевого белка путем снижения уровня данного белка в клетке, например клетке пациента. В определенных вариантах осуществления способ предусматривает введение эффективного количества соединения, описанного в данном документе, необязательно включающего фармацевтически приемлемые вспомогательное вещество, носитель, вспомогательное средство, другое биологически активное средство или их комбинацию.
[347] В дополнительных вариантах осуществления в описании представлены способы лечения или облегчения заболевания, нарушения или их симптома у субъекта или пациента, например, у животного, такого как человек, включающие введение субъекту, нуждающемуся в этом, композиции, содержащей эффективное количество, например терапевтически эффективное количество, соединения, описанного в данном документе, или его солевой формы и фармацевтически приемлемые вспомогательное вещество, носитель, вспомогательное средство, другое биологически активное средство или их комбинация, при этом композиция является эффективной для лечения или облегчения заболевания или нарушения или их симптома у субъекта.
[348] В другом аспекте в описании предусмотрены способы идентификации эффектов разрушения белков, представляющих интерес, в биологической системе с применением соединений в соответствии с настоящим изобретением.
[349] В другом варианте осуществления настоящее изобретение направлено на способ лечения пациента-человека, нуждающегося в модулировании болезненного состояния или состояния за счет белка, где разрушение данного белка будет оказывать терапевтический эффект у пациента, при этом способ предусматривает введение нуждающемуся пациенту эффективного количества соединения в соответствии с настоящим изобретением, необязательно в комбинации с другим биологически активным средством. Болезненное состояние или состояние могут представлять собой заболевание, вызванное микробным организмом или другим экзогенным организмом, таким как вирус, бактерия, гриб, простейшие или другой микроорганизм, или могут представлять собой болезненное состояние, которое вызвано сверхэкспрессией белка (например, ER), что приводит к болезненному состоянию и/или состоянию.
[350] Термин «болезненное состояние или состояние» используется для описания любого болезненного состояния или состояния, при котором происходит нарушение регуляции белка (т.е. количество ER, экспрессируемого у пациента, является повышенным), и при этом разрушение одного или более белков у пациента может обеспечивать благоприятную терапию или облегчение симптомов у пациента, нуждающегося в этом. В определенных случаях болезненное состояние или состояние можно излечить.
[351] Болезненные состояния или состояния, которые можно лечить с применением соединений в соответствии с настоящим изобретением включают, например, астму, аутоиммунные заболевания, такие как рассеянный склероз, различные виды рака, диабет, заболевание сердечно-сосудистой системы, гипертонию, воспалительное заболевание кишечника, эндометриоз, задержку в умственном развитии, расстройство настроения, ожирение, рефракционную аномалию, бесплодность, синдром Ангельмана, болезнь Канавана, целиакию, болезнь Шарко-Мари-Тута, муковисцидоз, мышечная дистрофия Дюшенна, гемохроматоз, гемофилию, синдром Клайнфелтера, нейрофиброматоз, фенилкетонурию, поликистозная болезнь почек, синдром Прадера-Вилли (PKD1) или 4 (PKD2), серповидноклеточное заболевание, болезнь Тея-Сакса, синдром Тернера.
[352] Термин «неоплазия» или «рак» применяют по всему описанию для описания патологического процесса, который приводит к образованию и росту ракового или злокачественного новообразования, т.е. аномальной ткани, которая растет посредством клеточной пролиферации, зачастую более быстро, чем нормальная ткань, и продолжает расти после прекращения стимула, который инициировал новый рост. Злокачественные новообразования демонстрируют частичное или полное отсутствие структурной организации и функциональной координации с нормальной ткани и большинство распространяется в окружающие ткани, метастазируют в несколько мест и вероятно вернутся вновь после попытки удаления и обусловят смерть пациент, если их недостаточно лечить. Применяемый в данном документе термин «неоплазия» применяют для описания всех раковых болезненных состояний и включает или охватывает патологический процесс, ассоциированный со злокачественными гематогенными, асцитическими и солидными опухолями. Иллюстративные виды рака, которые можно лечить с помощью соединений по настоящему изобретению либо в отдельности, либо в комбинации с по меньшей мере одним дополнительным противораковым средством, включают плоскоклеточную карциному, базальноклеточную карциному, аденокарциному, виды гепатоцеллюларной карциномы и виды почечноклеточной карциномы, рак мочевого пузыря, колоректальный рак, рак молочной железы, шейки матки, эндометрия, ободочной кишки, пищевода, головы, почки, печени, легкого, шеи, яичника, поджелудочной железы, предстательной железы и желудка; виды лейкоза; виды доброкачественной и злокачественной лимфомы, в частности лимфомы Беркитта и неходжкинской лимфомы; виды доброкачественной и злокачественной меланомы; миелопролиферативные заболевания; виды саркомы, в том числе саркома Юинга, гемангиосаркома, саркома Капоши, липосаркома, виды миосаркомы, периферическая нейроэпителиома, синовиальная саркома, виды глиомы, виды астроцитомы, виды олигодендроглиомы, виды эпендимомы, виды глиобастомы, виды нейробластомы, виды ганглионевромы, виды ганглиоглиомы, виды медуллобластомы, опухоли клеток шишковидного тела, виды менингиомы, виды менингеальной саркомы, виды нейрофибромы и виды шванномы; колоректальный рак, рак молочной железы, рак предстательной железы, рак шейки матки, рак матки, рак легкого, рак яичников, рак яичка, рак щитовидной железы, астроцитому, рак пищевода, рак поджелудочной железы, рак желудка, рак печени, рак толстой кишки, меланому; карциносаркому, болезнь Ходжкина, опухоль Вильмса и виды тератокарциномы. Дополнительные виды рака, которые можно лечить с применением соединений в соответствии с настоящим изобретением, включают, например, Т-клеточный острый лимфобластный лейкоз (T-ALL), Т-клеточную лимфобластную лимфому (T-LL), периферическую Т-клеточную лимфому, Т-клеточный лейкоз у взрослых, пре-В ALL, виды пре-В лимфомы, В-крупноклеточную лимфому, лимфому Беркитта, В-клеточный ALL, положительный по филадельфийской хромосоме ALL и положительный по филадельфийской хромосоме CML.
[353] Термин «биологически активное средство» используется для описания средства, отличного от соединения в соответствии с настоящим изобретением, которое применяют в комбинации с соединениями по настоящему изобретению в качестве средства с биологической активностью для содействия в осуществлении предполагаемой терапии, ингибирования и/или предупреждения/профилактики, для которых применяют соединения по настоящему изобретению. Предпочтительные биологически активные средства для применение в данном документе включают такие средства, которые обладают фармакологической активностью, подобную активности, для которой применяют или вводят соединения по настоящему изобретению, и включают, например, противораковые средства, противовирусные средства, особенно в том числе средства против HIV и средства против HCV, противомикробные средства, противогрибковые средства и т.д.
[354] Термин «дополнительное противораковое средство» применяют для описания противоракового средства, которое можно объединять с соединениями в соответствии с настоящим изобретением для лечения рака. Такие средства включают, например, эверолимус, трабектедин, абраксан, TLK 286, AV-299, DN-101, пазопаниб, GSK690693, RTA 744, ON 0910.Na, AZD 6244 (ARRY-142886), AMN-107, TKI-258, GSK461364, AZD 1152, энзастаурин, вандетаниб, ARQ-197, MK-O457, MLN8054, PHA-739358, R-763, AT-9263, ингибитор FLT-3, ингибитор VEGFR, ингибитор TK EGFR, ингибитор киназа Aurora, модулятор PIK-1, ингибитор Bcl-2, ингибитор HDAC, ингибитор c-MET, ингибитор PARP, ингибитор Cdk, ингибитор TK EGFR, ингибитор IGFR-TK, антитело к HGF, ингибитор киназы PI3, ингибитор АКТ, ингибитор mTORC1/2, ингибитор JAK/STAT, ингибитор контрольной точки 1 или 2, ингибитор киназа фокальных контактов, ингибитор киназы Мар-киназы (mek), антитело к ловушке VEGF, пеметрексед, эрлотиниб, дазатаниб, нилотиниб, декатаниб, панитумумаб, амрубицин, ореговомаб, Lep-etu, нолатрексед, azd2171, батабулин, офатумумаб, занолимумаб, эдотекарин, тетрандрин, рубитекан, тесмилифен, облимерсен, тицилимумаб, ипилимумаб, госсипол, Bio 111, 131-I-TM-601, ALT-110, BIO 140, CC 8490, циленгитид, гиматекан, IL13-PE38QQR, INO 1001, IPdR1 KRX-0402, лукантон, LY317615, нейрадиаб, витесан, Rta 744, Sdx 102, талампанель, атрасентан, Xr 311, ромидепсин, ADS-100380, сунитиниб, 5-фторурацил, вориностат, этопозид, гемцитабин, доксорубицин, липосомальный доксорубицин, 5'-дезокси-5-фторуридин, винкристин, темозоломид, ZK-304709, селициклиб; PD0325901, AZD-6244, капецитабин, L-глутаминовую кислоту, N-[4-[2-(2-амино-4,7-дигидро-4-оксо-1Н-пирроло[2,3-d]пиримидин-5-ил)этил]бензоил]-, динатриевую соль, гептагидрат, камптотецин, PEG-меченный иринотекан, тамоксифен, торемифена цитрат, анастразол, эксеместан, летрозол, DES (диэтилстилбестрол), эстрадиол, эстроген, сопряженный эстроген, бевацизумаб, IMC-1С11, CHIR-258); 3-[5-(метилсульфонилпиперадинметил)индолилхинолон, ваталаниб, AG-013736, AVE-0005, гозерелина ацетат, лейпролида ацетат, трипторелина памоат, медроксипрогестерона ацетат, гидроксипрогестерона капроат, мегестрола ацетат, ралоксифен, бикалутамид, флутамид, нилутамид, мегестрола ацетат, СР-724714; TAK-165, HKI-272, эрлотиниб, лапатаниб, канертиниб, антитело к ABX-EGF, эрбитукс, EKB-569, PKI-166, GW-572016, лонафарниб, BMS-214662, типифарниб; амифостин, NVP-LAQ824, субероиланилидгидроксамовую кислоту, вальпроевую кислоту, трихостатин A, FK-228, SU11248, сорафениб, KRN951, аминоглютетимид, арнсакрин, анагрелид, L-аспарагиназа, вакцина на основе бацилл Кальметта-Герена (BCG), адриамицин, блеомицин, бусерелин, бусульфан, карбоплатин, кармустин, хлорамбуцил, цисплатин, кладрибин, клодронат, ципротерон, цитарабин, дакарбазин, дактиномицин, даунорубицин, диэтилстилбестрол, эпирубицин, флударабин, флудрокортизон, флуоксиместерон, флутамид, гливек, гемцитабин, гидроксимочевина, идарубицин, ифосфамид, иматиниб, лейпролид, левамизол, ломустин, мехлоретамин, мелфалан, 6-меркаптопурин, месну, метотрексат, митомицин, митотан, митоксантрон, нилутамид, октреотид, оксалиплатин, памидронат, пентостатин, пликамицин, порфимер, прокарбазин, ралтитрексед, ритуксимаб, стрептозоцин, тенипозид, тестостерон, талидомид, тиогуанин, тиотепу, третиноин, виндезин, 13-цис-ретиноевую кислоту, фенилаланин горчица, урацил мустард, эстрамустин, алтретамин, флоксуридин, 5-деоксиуридин, цитозинарабинозид, 6-мекаптопурин, дезоксисоформицин, кальцитриол, вальрубицин, митрамицин, винбластин, винорелбин, топотекан, разоксин, маримастат, COL-3, неовастат, BMS-275291, скваламин, эндостатин, SU5416, SU6668, EMD121974, интерлейкин-12, IM862, ангиостатин, витаксин, дролоксифен, идоксифен, спиронолактон, финастерид, цимитидин, трастузумаб, денилейкин дифтитокс, гефитиниб, бортезимиб, паклитаксел, не содержащий кремофор паклитаксел, доцетаксел, эпитилон В, BMS- 247550, BMS-310705, дролоксифен, 4-гидрокситамоксифен, пипендоксифен, ERA-923, арзоксифен, фулвестрант, аколбифен, лазофоксифен, идоксифен, TSE-424, HMR- 3339, ZK186619, топотекан, PTK787/ZK 222584, VX-745, PD 184352, рапамицин, 40-О-(2-гидроксиэтил)рапамицин, темсиролимус, АР-23573, RAD001, АВТ-578, ВС-210, LY294002, LY292223, LY292696, LY293684, LY293646, вортманнин, ZM336372, L-779,450, PEG-филграстим, дарбэпоэтин, эритропоэтин, гранулоцитарный колониестимулирующий фактор, золендронат, преднизон, цетуксимаб, гранулоцитарно-макрофагальный колониестимулирующий фактор, гистрелин, пегилированный интерферон альфа-2а, интерферон альфа-2а, пегилированный интерферон альфа-2b, интерферон альфа-2b, азацитидин, PEG-L-аспарагиназа, леналидомид, гемтузумаб, гидрокортизон, интерлейкин-11, дексразоксан, алемтузумаб, полностью транс-ретиноевую кислоту, кетоконазол, интерлейкин-2, мегестрол, иммунноглобулин, азотистый иприт, метилпреднизолон, ибритугумомуб тиуксетан, андрогены, децитабин, гексаметилмеламин, бексаротен, тозитумомаб, триоксид мышьяка, кортизон, эдитронат, митотан, циклоспорин, липосомальный даунорубицин, аспарагиназа Edwina, стронций 89, касопитант, нетупитант, антагонист рецептора NK-1, палоносетрон, апрепитант, дифенгидрамин, гидроксизин, метоклопрамид, лоразепам, альпразолам, галоперидол, дроперидол, дронабинол, дексаметазон, метилпреднизолон, прохлорперазин, гранисетрон, ондансетрон, доласетрон, трописетрон, PEG-филграстим, эритропоэтин, эпоэтин альфа, дарбэпоэтин альфа и их смеси.
[355] Термин «средство против HIV» или «дополнительное средство против HIV» включает, например, нуклеозидные ингибиторы обратной транскриптазы (NRTI), другие отличные от нуклеозидных ингибиторов ингибиторы обратной транскриптазы (т.е. ингибиторы, которые являются иллюстративными для настоящего изобретения), ингибиторы протеазы, ингибиторы слияния, среди прочих, иллюстративные соединения, которые могут включать, например, 3ТС (ламивудин), AZT (зидовудин), (-)-FTC, ddI (диданозин), ddC (зальцитабин), абакавир (ABC), тенофовир (РМРА), D-D4FC (реверсет), D4T (ставудин), рацивир, L-FddC, L-FD4C, NVP (невирапин), DLV (делавирдин), EFV (эфавиренз), SQVM (саквинавира мезилат), RTV (ритонавир), IDV (индинавир), SQV (саквинавир), NFV (нелфинавир), APV (ампренавир), LPV (лопинавир), ингибиторы слияния, такие как Т20, среди прочих, фузеон и их смеси, в том числе соединения против HIV, находящиеся в настоящее время на клинических испытаниях или в разработке.
[356] Другие средства против HIV, которые можно применять с совместным введением с соединениями в соответствии с настоящим изобретением, включают, например, другие NNRTI (т.е. отличные от NNRTI в соответствии с настоящим изобретением) и могут быть выбраны из группы, состоящей из невирапина (BI-R6-587), делавирдина (U-90152S/T), эфавиренза (DMP-266), UC-781 (N-[4-хлор-3-(3-метил-2-бутенилокси)фенил]-2-метил-3-фуранкарботиамид), этравина (ТМС125), тровидина (Ly300046.HCl), MKC-442 (эмивирин, коактинон), HI-236, HI-240, HI-280, HI-281, рилпивирина (ТМС-278), MSC-127, HBY 097, DMP266, байкалина (TJN-151) ADAM-II (метил-3',3'-дихлор-4',4''-диметокси-5',5''-бис(метоксикарбонил)-6,6-дифенилгексеноат), метил-3-бром-5-(1-5-бром-4-метокси-3-(метоксикарбонил)фенил)гепт-1-енил)-2-метоксибензоата (аналог алкенилдиарилметана, аналог Adam), (5-хлор-3-(фенилсульфинил)-2'-индолекарбоксамид), ААР-ВНАР (U-104489 или PNU-104489), каправирина (AG-1549, S-1153), атевирдина (U-87201E), ауринтрикарбоновой кислоты (SD-095345), 1-[(6-ниано-2-индолил)карбонил]-4-[3-(изопропиламино)-2-пиридинил]пиперазина, 1-[5-[[N-(метил)метилсульфониламино]-2-индолилкарбонил-4-[3-(изопропиламино)-2-пиридинил]пиперазина, 1-[3-(этиламино)-2-[пиридинил]-4-[(5-гидрокси-2-индолил)карбонил]пиперазина, 1-[(6-формил-2-индолил)карбонил]-4-[3-(изопропиламино)-2-пиридинил]пиперазина, 1-[[5-(метилсульфонилокси)-2-индоил)карбонил]-4-[3-(изопропиламино)-2-пиридинил]пиперазина, U88204E, бис(2-нитрофенил)сульфона (NSC 633001), каланолида A (NSC675451), каланолида В, 6-бензил-5-метил-2-(циклогексилокси)пиримидин-4-она (DABO-546), DPC 961, E-EBU, E-EBU-dm, E-EPSeU, E-EPU, фоскарнета (фоскавир), НЕРТ (1-[(2-гидроксиэтокси)метил]-6-(фенилтио)тимин), НЕРТ-М (1-[(2-гидроксиэтокси)метил]-6-(3-метилфенил)тио)тимин), НЕРТ-S (1-[(2-гидроксиэтокси)метил]-6-(фенилтио)-2-тиотимин), инофиллума Р, L-737,126, мишеламин A (NSC650898), мишеламина В (NSC649324), мишеламина F, 6-(3,5-диметилбензил)-1-[(2-гидроксиэтокси)метил]-5-изопропилурацила, 6-(3,5-диметилбензил)-1-(этиоксиметил)-5-изопропилурацила, NPPS, E-BPTU (NSC 648400), олтипраза (4-метил-5-(пиразинил)-3Н-1,2-дитиол-3-тиона), N-{2-(2-хлор-6-фторфенэтил]-N'-(2-тиазолил)тиомочевины (Cl, F производное РЕТТ), N-{2-(2,6-дифторфенэтил]-N'-[2-(5-бромпиридил)]тиомочевины (производное РЕТТ), N-{2-(2,6-дифторфенэтил]-N'-[2-(5-метилпиридил)]тиочевины {пиридилпроизводное РЕТТ), N-[2-(3-фторфуранил)этил]-N'-[2-(5-хлорпиридил)]тиомочевины, N-[2-(2-фтор-6-этоксифенэтил)]-N'-[2-(5-бромпиридил)]тиомочевины, N-(2-фенэтил)-N'-(2-тиазолил)тиомочевины (LY-73497), L-697,639, L-697,593, L-697,661, 3-[2-(4,7-дифторбензоксазол-2-ил)этил}-5-этил-6-метил(пипридин-2(1Н)-тиона (производное 2-пиридинона), 3-[[(2-метокси-5,6-диметил-3-пиридил)метил]амин]-5-этил-6-метил(пипридин-2(1Н)-тиона, R82150, R82913, R87232, R88703, R89439 (ловирид), R90385, S-2720, сурамина натрий, TBZ (тиазолобензимидазол, NSC 625487), тиазолоизоиндол-5-она, (+)(R)-9b-(3,5-диметилфенил-2,3-дигидротиазоло[2,3-а]изоиндол-5(9bH)-она, тивирапина (R86183), UC-38 и UC-84, среди прочих.
[357] Термин «фармацевтически приемлемая соль» используется по всему описанию для описания в применимых случаях солевой формы одного или более из соединений, описанных в данном документе, которые присутствуют для увеличения растворимости соединения в желудочных соках желудочно-кишечного тракта пациента с целью способствовать растворению и биодоступности соединений. Фармацевтически приемлемые соли включают соли, полученные из фармацевтически приемлемых неорганических или органических оснований и кислот в соответствующих случаях. Подходящие соли включают соли, полученные из щелочных металлов, такие как калиевые и натриевые соли, щелочноземельных металлов, такие как кальциевые, магниевые и аммониевые соли, среди ряда других кислот и оснований, хорошо известных в области фармацевтики. Натриевые и калиевые соли являются особенно предпочтительными как соли нейтрализации фосфатов в соответствии с настоящим изобретением.
[358] Термин «фармацевтически приемлемое производное» используется по всему описанию для описания любой фармацевтически приемлемой формы пролекарства (такой как сложный эфир, амид, другая группа пролекарства), которая при введении пациенту предоставляет непосредственно или опосредованно соединение по настоящему изобретению или активный метаболит соединения по настоящему изобретению.
Общие подходы к синтезу
[359] Для осуществления на практике синтеза и оптимизации бифункциональных молекул, описанных в данном документе, можно найти решение в постадийном или модульном способе. Например, идентификация соединений, которые связываются с целевыми молекулы, может предусматривать операции скрининга с высокой или средней пропускной способностью, если подходящие лиганды не являются непосредственно доступными. Не редки случаи, когда исходные лиганды требуют циклов итерационного проектирования и оптимизации для улучшения субоптимальных аспектов, идентифицированных с помощью данных из подходящих in vitro и фармакологических и/или ADMET анализов. Часть операции оптимизации/SAR будет заключаться в тестировании положений лиганда, которые допускают замещение и которые могут быть подходящими местами для присоединения химических групп линкера, ранее указанного в данном документе. Если доступны кристаллографические или ЯМР данные о структуре, их можно применять для фокусирования на таком синтетическом усилии.
[360] Очень похожим образом можно идентифицировать и оптимизировать лиганды для Е3-лигазы, т.е. ULM/ILM/VLM/CLM/ILM.
[361] Имея в своем распоряжении РТМ и ULM (например, ILM, VLM, CLM и/или ILM) специалист в данной области техники может применять известные способы синтеза для их комбинации с линкерным фрагментом или без него. Линкерные фрагменты можно синтезировать в диапазоне составов, значений длины и эластичности и функционализированные так, что группы РТМ и ULM могут быть присоединены последовательно к дальним концам линкера. Таким образом, можно создать и профилировать библиотеку бифункциональных молекул в фармакологических исследованиях и ADMET/PK анализах in vitro и in vivo. Как и с группами РТМ и ULM, конечные бифункциональные молекулы можно подвергать циклам итерационного проектирования и оптимизации с целью определения молекул с необходимыми свойствами.
[362] В некоторых случаях могут быть необходимы стратегии введения защитной группы и/или взаимопревращения функциональных групп (FGI) для способствования получению необходимых веществ. Данные химические способы широко известный химику, специализирующемуся в области органического синтеза, и множество способов можно найти в руководствах, таких как "Greene's Protective Groups in Organic Synthesis" Peter G.M. Wuts и Theodora W. Greene (Wiley) и "Organic Synthesis: The Disconnection Approach" Stuart Warren and Paul Wyatt (Wiley).
Контроль уровня белка
[363] В данном описании также представлены способы контроля уровней белка в клетке. Они основаны на применении соединений, описанных в данном документе, которые, как известно, взаимодействуют с конкретным целевым белком так, что разрушение целевого белка in vivo приведет к контролю количества белка в биологической системе, предпочтительно с конкретной терапевтической пользой.
[364] Следующие примеры применяют для способствования описанию настоящего изобретения, но не должны рассматриваться как ограничивающие настоящее изобретение каким-либо образом.
Конкретные варианты осуществления настоящего изобретения
[365] Настоящее изобретение охватывает следующие конкретные варианты осуществления. Данные следующие варианты осуществления могут включать все признаки, перечисленные в предыдущем варианте осуществления, как указано. Если применимо, следующие варианты осуществления также могут включать признаки, перечисленные в любом предыдущем варианте осуществления включительно или в альтернативе (например, восьмой вариант осуществления может включать признаки, перечисленные в первом варианте осуществления, как перечислено, и/или признаки любого из второго по седьмой варианты осуществления).
[366] В определенных вариантах осуществления в описании представлены следующие иллюстративные молекулы PROTAC, целенаправленно воздействующие на ER (такие как соединения в таблицах 1 и 2, например, соединения 1-547), в том числе их соли, пролекарства, полиморфы, аналоги, производные и дейтерированные формы.
[367] Аспект настоящего изобретения предусматривает бифункциональное соединение, имеющее химическую структуру:

или его фармацевтически приемлемую соль, энантиомер, стереоизомер, сольват, полиморф или пролекарство,
где
ULM представляет собой низкомолекулярный фрагмент, связывающий Е3-убиквитинлигазу, который связывает Е3-убиквитинлигазу;
L представляет собой связь или химический линкерный фрагмент, соединяющий ULM и РТМ; и
РТМ представляет собой фрагмент, нацеливающийся на белок, представляющий собой эстрогеновый рецептор, представленный с помощью химической структуры:

где
каждый ХРТМ независимо представляет собой СН, N;
 указывает на место присоединения по меньшей мере одного из линкера, ULM, ULM', РТМ' или их комбинации;
указывает на место присоединения по меньшей мере одного из линкера, ULM, ULM', РТМ' или их комбинации;
каждый RPTM1 независимо представляет собой ОН, галоген, алкокси, метокси, этокси, O(CO)RPTM, при этом замещение может предусматривать моно-, ди- или тризамещение, и RPTM представляет собой алкильную или циклоалкильную группу с 1-6 атомами углерода или арильные группы;
каждый RPTM2 независимо представляет собой Н, галоген, CN, CF3, линейный или разветвленный алкил (например, линейный или разветвленный С1-С4алкил), алкокси, метокси, этокси, при этом замещение может предусматривать моно- или дизамещение;
каждый RPTM3 независимо представляет собой Н, галоген, при этом замещение может предусматривать моно- или дизамещение; и
RPTM4 представляет собой Н, алкил, метил, этил.
[368] В любом аспекте или варианте осуществления, описанных в данном документе, фрагмент, связывающий Е3-убиквитинлигазу, нацеливается на Е3-убиквитинлигазу, выбранную из группы, состоящей из белка Гиппеля-Линдау (VLM), цереблона (CLM), гомолога 2 double minute мыши (MLM) и IAP (ILM).
[369] В любом аспекте или варианте осуществления, описанных в данном документе, ULM представляет собой фрагмент, связывающийся с белком Гиппеля-Линдау (VHL) лигазного комплекса (VLM), с химической структурой, представленной с помощью:

где
каждый из X1, X2 независимо выбран из группы, состоящей из связи, О, NRY3, CRY3RY4 C=S, SO, и SO2;
каждый из RY3, RY4 независимо выбран из группы, состоящей из Н, линейного или разветвленного C1-6алкила, необязательно замещенного 1 или более атомами галогена, необязательно замещенного C1-6алкоксила (например, необязательно замещенного 0-3 группами RP);
RP представляет собой 0, 1, 2 или 3 группы, при этом каждая независимо выбрана из группы, состоящей из Н, галогена, -ОН, C1-3алкила, С=O;
W3 выбран из группы, состоящей из необязательно замещенного -Т-N(R1aR1b)X3, -T-N(R1aR1b), -Т-арила, необязательно замещенного -Т-гетероарила, необязательно замещенного -Т-гетероцикла, необязательно замещенного -NR1-T-арила, необязательно замещенного -NR1-Т-гетероарила или необязательно замещенного -NR1-Т-гетероцикла;
X3 представляет собой С=O, R1, R1a, R1b;
каждый из R1, R1a, R1b независимо выбран из группы, состоящей из Н, линейной или разветвленной C1-С6алкильной группы, необязательно замещенной 1 или более атомами галогена или группами -ОН, RY3C=O, RY3C=S, RY3SO, RY3SO2, N(RY3RY4)C=O, N(RY3RY4)C=S, N(RY3RY4)SO и N(RY3RY4)SO2;
T выбран из группы, состоящей из необязательно замещенного алкила, группы -(СН2)n-, где каждая из метиленовых групп необязательно замещена одним или двумя заместителями, выбранными из группы, состоящей из галогена, метила, линейной или разветвленной C1-С6алкильной группы, необязательно замещенной 1 или более атомами галогена или группами -ОН, или необязательно замещенной аминокислотной боковой цепи; и
n составляет 0-6,
W4 представляет собой  или
или 
каждый из R14a, R14b независимо выбран из группы, состоящей из Н, галогеналкила или необязательно замещенного алкила;
W5 выбран из группы, состоящей из фенила или 5-10-членного гетероарила,
R15 выбран из группы, состоящей из Н, галогена, CN, ОН, NO2, NR14aR14b, OR14a, CONR14aR14b, NR14aCOR14b, SO2NR14aR14b, NR14aSO2R14b, необязательно замещенного алкила, необязательно замещенного галогеналкила, необязательно замещенного галогеналкокси; арила, гетероарила, циклоалкила или циклогетероалкила;
и где пунктирная линия указывает на участок присоединения по меньшей мере одного РТМ, другого ULM (ULM') или химического линкерного фрагмента, связывающего по меньшей мере один РТМ, или ULM', или оба из них, к ULM.
[370] В любом аспекте или варианте осуществления, описанных в данном документе, ULM представляет собой фрагмент, связывающийся с белком Гиппеля-Линдау (VHL) лигазного комплекса (VLM), с химической структурой, представленной с помощью:

где
W3 выбран из группы, состоящей из необязательно замещенного арила, необязательно замещенного гетероарила или 
R9 и R10 независимо представляют собой водород, необязательно замещенный алкил, необязательно замещенный циклоалкил, необязательно замещенный гидроксиалкил, необязательно замещенный гетероарил или галогеналкил, или R9, R10 и атом углерода, к которому они присоединены, образуют необязательно замещенный циклоалкил;
R11 выбран из группы, состоящей из необязательно замещенной гетероциклической группы, необязательно замещенного алкокси, необязательно замещенного гетероарила, необязательно замещенного арила, 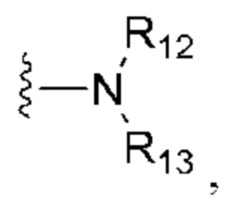

R12 выбран из группы, состоящей из Н или необязательно замещенного алкила;
R13 выбран из группы, состоящей из Н, необязательно замещенного алкила, необязательно замещенного алкилкарбонила, необязательно замещенного (циклоалкил)алкилкарбонила, необязательно замещенного аралкилкарбонила, необязательно замещенного арилкарбонила, необязательно замещенного (гетероциклил)карбонила или необязательно замещенного аралкила;
каждый из R14a, R14b независимо выбран из группы, состоящей из Н, галогеналкила или необязательно замещенного алкила;
W5 выбран из группы, состоящей из фенила или 5-10-членного гетероарила,
R15 выбран из группы, состоящей из Н, галогена, CN, ОН, NO2, N R14aR14b, OR14a, CONR14aR14b, NR14aCOR14b, SO2NR14aR14b, NR14a SO2R14b, необязательно замещенного алкила, необязательно замещенного галогеналкила, необязательно замещенного галогеналкокси; арила, гетероарила, циклоалкила или циклогетероалкила, при этом каждый необязательно замещен;
R16 независимо выбран из группы, состоящей из Н, галогена, необязательно замещенного алкила, необязательно замещенного галогеналкила, гидрокси или необязательно замещенного галогеналкокси;
ο равняется 0, 1, 2, 3 или 4;
R18 независимо выбран из группы, состоящей из галогена, необязательно замещенного алкокси, циано, необязательно замещенного алкила, галогеналкила, галогеналкокси или линкера; и
р равняется 0, 1, 2, 3 или 4, и где пунктирная линия указывает на участок присоединения по меньшей мере одного РТМ, другого ULM (ULM') или химического линкерного фрагмента, связывающего по меньшей мере один РТМ, или ULM', или оба из них, к ULM.
[371] В любом аспекте или варианте осуществления, описанных в данном документе, ULM предусматривает химическую структуру, выбранную из группы:
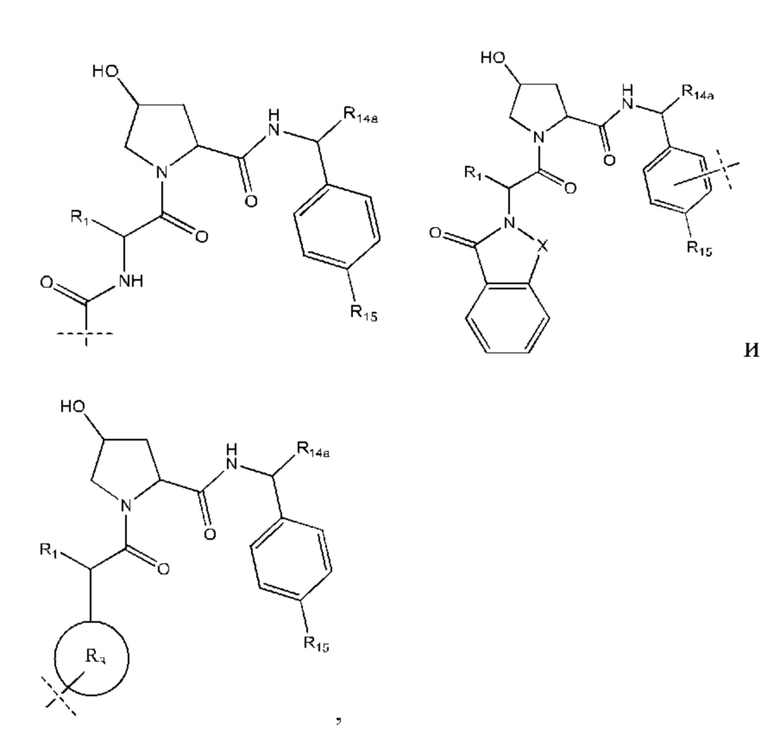
где
R1 представляет собой Н, этил, изопропил, трет-бутил, втор-бутил, циклопропил, циклобутил, циклопентил или циклогексил; необязательно замещенный алкил, необязательно замещенный гидроксиалкил, необязательно замещенный гетероарил или галогеналкил;
R14a представляет собой Н, галогеналкил, необязательно замещенный алкил, метил, фторметил, гидроксиметил, этил, изопропил или циклопропил;
R15 выбран из группы, состоящей из Н, галогена, CN, ОН, NO2, необязательно замещенного гетероарила, необязательно замещенного арила; необязательно замещенного алкила, необязательно замещенного галогеналкила, необязательно замещенного галогеналкокси, циклоалкила или циклогетероалкила;
X представляет собой С, СН2 или С=O;
R3 отсутствует или представляет собой необязательно замещенный 5- или 6-членный гетероарил; и
где пунктирная линия указывает на участок присоединения по меньшей мере одного РТМ, другого ULM (ULM') или химического линкерного фрагмента, связывающего по меньшей мере один РТМ, или ULM', или оба из них, к ULM.
[372] В любом аспекте или варианте осуществления, описанных в данном документе, ULM предусматривает группу в соответствии с химической структурой:

где
R1' в ULM-g представляет собой необязательно замещенную C1-С6алкильную группу, необязательно замещенную -(СН2)nOH, необязательно замещенную -(CH2)nSH, необязательно замещенную (СН2)n-O-(С1-С6)алкильную группу, необязательно замещенную (СН2)n-WCOCW-(С0-С6)алкильную группу, содержащую эпоксидный фрагмент WCOCW, где каждый W независимо представляет собой Н или C1-С3алкильную группу, необязательно замещенную -(СН2)nCOOH, необязательно замещенную -(СН2)nC(O)-(С1-С6алкил), необязательно замещенную -(CH2)nNHC(O)-R1, необязательно замещенную -(CH2)nC(O)-NR1R2, необязательно замещенную -(CH2)nOC(O)-NR1R2, -(CH2O)nH, необязательно замещенную -(CH2)nOC(O)-(C1-С6алкил), необязательно замещенную -(СН2)nC(O)-O-(С1-С6алкил), необязательно замещенную -(CH2O)nCOOH, необязательно замещенную -(ОСН2)nO-(С1-С6алкил), необязательно замещенную -(CH2O)nC(O)-(С1-С6алкил), необязательно замещенную -(OCH2)nNHC(O)-R1, необязательно замещенную -(CH2O)nC(O)-NR1R2, -(CH2CH2O)nH, необязательно замещенную -(CH2CH2O)nCOOH, необязательно замещенную -(ОСН2СН2)nO-(С1-С6алкил), необязательно замещенную -(CH2CH2O)nC(O)-(C1-С6алкил), необязательно замещенную -(OCH2CH2)nNHC(O)-R1, необязательно замещенную -(CH2CH2O)nC(O)-NR1R2, необязательно замещенную -SO2RS, необязательно замещенную S(O)RS, NO2, CN или галоген (F, Cl, Br, I, предпочтительно F или Cl);
каждый из R1 и R2 в ULM-g независимо представляет собой Н или C1-С6алкильную группу, которая может быть необязательно замещена одной или двумя гидроксильными группами или не более чем тремя галогене о держащими группами (предпочтительно фтором);
RS в ULM-g представляет собой C1-С6алкильную группу, необязательно замещенную арильную, гетероарильную или гетероциклическую группу или группу -(CH2)mNR1R2;
каждый из X и X' в ULM-g независимо представляет собой С=O, C=S, -S(O), S(O)2, (предпочтительно как X, так и X' представляют собой С=O);
R2' в ULM-g представляет собой необязательно замещенную -(СН2)n-(C=O)u(NR1)v(SO2)wалкильную группу, необязательно замещенную группу -(СН2)n-(C=O)u(NR1)v(SO2)wNR1NR2N, необязательно замещенный -(CH2)n-(C=O)u(NR1)v(SO2)w-арил, необязательно замещенный -(CH2)n-(C=O)u(NR1)v(SO2)w-гетероарил, необязательно замещенный -(CH2)n-(C=O)vNR1(SO2)w-гетероарил, необязательно замещенный -NR1-(CH2)n-C(O)u(NR1)v(SO2)w-алкил, необязательно замещенную -NR1-(CH2)n-C(O)u(NR1)v(SO2)w-NR1NR2N, необязательно замещенную -NR1-(CH2)n-C(O)u(NR1)v(SO2)w-NR1C(O)R1N, необязательно замещенный -NR1-(CH2)n-(C=O)u(NR1)v(SO2)w-арил, необязательно замещенный -NR1-(CH2)n-(C=O)u(NR1)v(SO2)w-гетероцикл или необязательно замещенный -NR1-(CH2)n-(C=O)vNR1(SO2)w-гетероцикл, необязательно замещенную -XR2'-алкильную группу; необязательно замещенную -XR2'-арильную группу; необязательно замещенную -XR2'-гетероарильную группу; необязательно замещенную -XR2'-гетероциклическую группу; необязательно замещенный;
R3' в ULM-g представляет собой необязательно замещенный алкил, необязательно замещенный -(CH2)n-(O)u(NR1)v(SO2)w-алкил, необязательно замещенный -(CH2)n-C(O)u(NR1)v(SO2)w-NR1NR2N, необязательно замещенный -(CH2)n-C(O)u(NR1)v(SO2)w-NR1C(O)R1N, необязательно замещенный -(CH2)n- C(O)u(NR1)v(SO2)w-C(O)NR1R2, необязательно замещенный -(CH2)n-C(O)u(NR1)v(SO2)w-арил, необязательно замещенный -(CH2)n-C(O)u(NR1)v(SO2)w-гетероарил, необязательно замещенный -(CH2)n-C(O)u(NR1)v(SO2)w-гетероцикл, необязательно замещенный -NR1-(CH2)n-C(O)u(NR1)v(SO2)w-арил, необязательно замещенный -NR1-(CH2)n-C(O)u(NR1)v(SO2)w-NR1NR2N, необязательно замещенный -NR1-(CH2)n-C(O)u(NR1)v(SO2)w-NR1C(O)R1N, необязательно замещенный -NR1-(CH2)n-C(O)u(NR1)v(SO2)w-арил, необязательно замещенный -NR1-(CH2)n-C(O)u(NR1)v(SO2)w-гетероарил, необязательно замещенный -NR1-(CH2)n-C(O)u(NR1)v(SO2)w-гетероцикл, необязательно замещенный -O-(CH2)n-(C=O)u(NR1)v(SO2)w-алкил, необязательно замещенный -O-(CH2)n-(C=O)u(NR1)v(SO2)w-NR1NR2N, необязательно замещенный -О-(CH2)n-(C=O)u(NR1)v(SO2)w-NR1C(O)R1N, необязательно замещенный -O-(СН2)n-(C=O)u(NR1)v(SO2)w-арил, необязательно замещенный -O-(CH2)n-(C=O)u(NR1)v(SO2)w-гетероарил или необязательно замещенный -O-(CH2)n-(C=O)u(NR1)v(SO2)w-гетероцикл; -(СН2)n-(N)n'-(СН2)n-(V)n'-алкильную группу, необязательно замещенную -(СН2)n-(N)n'-(СН2)n-(V)n'-арильную группу, необязательно замещенную -(CH2)n-(V)n'-(СН2)n-(N)n'-гетероарильную группу, необязательно замещенную -(CH2)n-(V)n'-(CH2)n-(V)n'-гетероциклическую группу, необязательно замещенную -(CH2)n-N(R1')(C=O)m'-(V)n'-алкильную группу, необязательно замещенную -(CH2)n-N(R1')(C=O)m'-(V)n'-арильную группу, необязательно замещенную -(CH2)n-N(R1')(C=O)m'-(V)n'-гетероарильную группу, необязательно замещенную -(CH2)n-N(Rr)(C=O)m'-(V)n'-гетероциклическую группу, необязательно замещенную -XR3'-алкильную группу; необязательно замещенную -XR3'-арильную группу; необязательно замещенную -XR3’-гетероарильную группу; необязательно замещенную -XR3'-гетероциклическую группу; необязательно замещенные;
каждый из R1N и R2N в ULM-g независимо представляет собой Н, C1-С6алкил, который необязательно замещен одной или двумя гидроксильными группами и не более чем тремя галогенсодержащими группами, или необязательно замещенную -(СН2)n-арильную, -(СН2)n-гетероарильную или -(СН2)n-гетероциклическую группу;
V в ULM-g представляет собой О, S или NR1;
R1 в ULM-g является таким же, как указано выше;
каждый из R1 и R1' в ULM-g независимо представляет собой Н или C1-С3алкильную группу;
каждый из XR2' и XR3' в ULM-g независимо представляет собой необязательно замещенную -(СН2)n-, -(CH2)n-CH(Xv)=CH(Xv)- (цис или транс), -(СН2)n-СН≡СН-, -(CH2CH2O)n- или С3-С6циклоалкильную группу, где Xv представляет собой Н, галоген или C1-С3алкильную группу, которая необязательно замещена;
каждый m в ULM-g независимо равняется 0, 1, 2, 3, 4, 5, 6;
каждый m' в ULM-g независимо равняется 0 или 1;
каждый n в ULM-g независимо равняется 0, 1, 2, 3, 4, 5, 6;
каждый n' в ULM-g независимо равняется 0 или 1;
каждый u в ULM-g независимо равняется 0 или 1;
каждый v в ULM-g независимо равняется 0 или 1;
каждый w в ULM-g независимо равняется 0 или 1; и
любой один или более из R1', R2', R3', X и X' в ULM-g необязательно модифицированы так, чтобы ковалентно связываться с группой РТМ посредством линкерной группы, если РТМ не представляет собой ULM', или если РТМ представляет собой ULM', то любой один или более из R1', R2', R3', X и X' в каждом из ULM и ULM' необязательно модифицированы так, чтобы ковалентно связываться друг с другом непосредственно или посредством линкерной группы, или ее фармацевтически приемлемую соль, стереоизомер, сольват или полиморф.
[373] В любом аспекте или варианте осуществления, описанных в данном документе, ULM представляет собой фрагмент, связывающийся с цереблоном Е3-лигазного комплекса (CLM), выбранный из группы, состоящей из талидомида, леналидомида, помалидомида, их аналогов, их изостеров или их производных.
[374] В любом аспекте или варианте осуществления, описанных в данном документе, CLM имеет химическую структуру, представленную:

где
W выбран из группы, состоящей из CH2, CHR, С=O, SO2, NH и N-алкила;
каждый X независимо выбран из группы, состоящей из О, S и Н2;
Y выбран из группы, состоящей из CH2, -C=CR', NH, N-алкила, N-арила, N-гетероарила, N-циклоалкила, N-гетероциклила, О и S;
Z выбран из группы, состоящей из О, S и H2;
G и G' независимо выбраны из группы, состоящей из Н, алкила (линейного, разветвленного, необязательно замещенного), ОН, R'OCOOR, R'OCONRR'', СН2-гетероциклила, необязательно замещенного R', и бензила, необязательно замещенного R';
Q1, Q2, Q3 и Q4 представляют собой атом углерода С, замещенный группой, независимо выбранной из R', N или N-оксида;
А независимо выбран из группы, состоящей из Н, алкила (линейного, разветвленного, необязательно замещенного), циклоалкила, Cl и F;
R предусматривает -CONR'R'', -OR', -NR'R'', -SR', -SO2R', -SO2NR'R'', -CR'R''-, -CR'NR'R''-, (-CR'O)nR'', -арил, -гетероарил, -алкил (линейный, разветвленный, необязательно замещенный), -циклоалкил, -гетероциклил, -P(O)(OR')R'', -P(O)R'R'', -OP(O)(OR')R'', -OP(O)R'R'', -Cl, -F, -Br, -I, -CF3, -CN, -NR'SO2NR'R'', -NR'CONR'R'', -CONR'COR'', -NR'C(=N-CN)NR'R'', -C(=N-CN)NR'R'', -NR'C(=N-CN)R'', -NR'C(=C-NO2)NR'R'', -SO2NR'COR'', -NO2, -CO2R', -C(C=N-OR')R'', -CR'=CR'R'', -CCR', -S(C=O)(C=N-R')R'', -SF5 и -OCF3;
R' и R'' независимо выбраны из группы, состоящей из связи, Н, алкила, циклоалкила, арила, гетероарила, гетероциклической группы, -C(=O)R, гетероциклила, каждый из которых необязательно замещен;
 представляет собой связь, которая может обеспечивать стереоспецифическую конфигурацию ((R) или (S)) или не обеспечивать стереоспецифическую конфигурацию; и
представляет собой связь, которая может обеспечивать стереоспецифическую конфигурацию ((R) или (S)) или не обеспечивать стереоспецифическую конфигурацию; и
Rn предусматривает функциональную группу или атом,
где n представляет собой целое число 1-10, и где
если n равняется 1, то Rn модифицирован так, чтобы ковалентно связываться с линкерной группой (L), и
если n равняется 2, 3 или 4, то один Rn модифицирован так, чтобы ковалентно связываться с линкерной группой (L), а любой другой Rn необязательно модифицирован так, чтобы ковалентно связываться с РТМ, CLM, вторым CLM, имеющим такую же химическую структуру, как CLM, CLM', вторым линкером или любым их множеством или комбинацией.
[375] В любом аспекте или варианте осуществления, описанных в данном документе, CLM имеет химическую структуру, представленную:
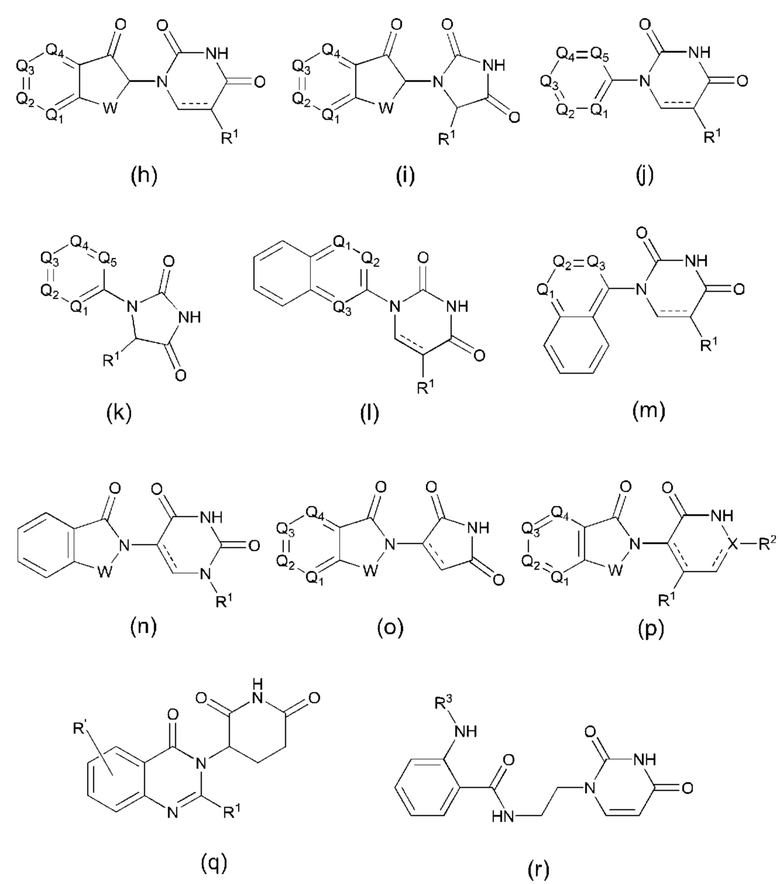
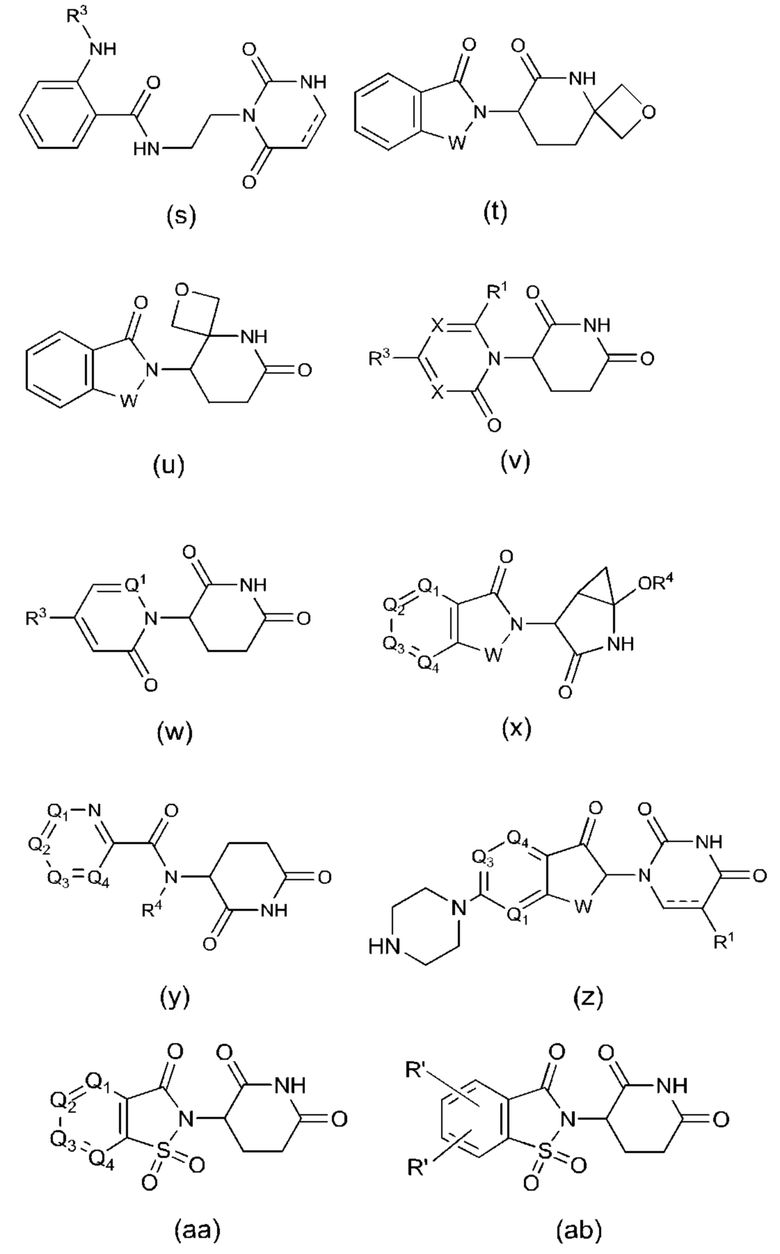
где
W в формулах (h) - (ab) независимо выбран из CH2, CHR, С=O, SO2, NH и N-алкила;
Q1, Q2, Q3, Q4, Q5 в формулах (h) - (ab) независимо представляют собой атом углерода С, замещенный группой, независимо выбранной из R', N или N-оксида;
R1 в формулах (h) - (ab) выбран из Н, CN, С1-С3-алкила;
R2 в формулах (h) - (ab) выбран из группы, состоящей из Н, CN, С1-С3-алкила, CHF2, CF3, СНО;
R3 в формулах (h) - (ab) выбран из Н, алкила, замещенного алкила, алкокси, замещенного алкокси;
R4 в формулах (h) - (ab) выбран из Н, алкила, замещенного алкила;
R5 в формулах (h) - (ab) представляет собой Н или низший алкил;
X в формулах (h) - (ab) представляет собой С, СН или N;
R' в формулах (h) - (ab) выбран из Н, галогена, алкила, замещенного алкила, алкокси, замещенного алкокси;
R в формулах (h) - (ab) представляет собой Н, ОН, низший алкил, низший алкокси, циано, галогенированный низший алкокси или галогенированный низший алкил;
 в формулах (h) - (ab) представляет собой одинарную или двойную связь; и
в формулах (h) - (ab) представляет собой одинарную или двойную связь; и
CLM ковалентно связан с РТМ, химической линкерной группой (L), ULM, CLM (или CLM') или их комбинацией.
[376] В любом аспекте или варианте осуществления, описанных в данном документе, ULM представляет собой фрагмент, связывающий (MDM2), (MLM) при этом химический фрагмент выбран из группы, состоящей из замещенных имидазолинов, замещенных спироиндолинонов, замещенных пирролидинов, замещенных пиперидинонов, замещенных морфолинонов, замещенных пирролопиримидинов, замещенных имидазолопиридинов, замещенного тиазолоимидазолина, замещенных пирролопирролидинонов и замещенных изохино линонов.
[377] В любом аспекте или варианте осуществления, описанных в данном документе, ULM представляет собой фрагмент, связывающийся с IAP Е3-убиквитинлигазного комплекса (ILM), содержащий аминокислоты аланин (А), валин (V), пролин (Р) и изолейцин (I) или их неприродные миметики.
[378] В любом аспекте или варианте осуществления, описанных в данном документе, ULM представляет собой фрагмент, связывающийся с IAP Е3-убиквитинлигазного комплекса (ILM), содержащий тетрапептидный фрагмент AVPI или его производное.
[379] В любом аспекте или варианте осуществления, описанных в данном документе, линкер (L) предусматривает химическое структурное звено, представленное формулой:

где
(AL)q представляет собой группу, которая соединена с по меньшей мере одним из ULM, РТМ или как с одним, так и с другим; и
q представляет собой целое число, которое больше или равно 1,
каждый AL независимо выбран из группы, состоящей из связи, CRL1RL2, О, S, SO, SO2, NRL3, SO2NRL3, SONRL3, CONRL3, NRL3CONRL4, NRL3SO2NRL4, CO, CRL1=CRL2, C≡C, SiRL1RL2, P(O)RL1, P(O)ORL1, NRL3C(=NCN)NRL4, NRL3C(=NCN), NRL3C(=CNO2)NRL4, С3-11циклоалкила, необязательно замещенного 0-6 группами RL1 и/или RL2, С3-11гетероциклила, необязательно замещенного 0-6 группами RL1 и/или RL2, арила, необязательно замещенного 0-6 группами RL1 и/или RL2, гетероарила, необязательно замещенного 0-6 группами RL1 и/или RL2, где каждая из RL1 или RL2 независимо необязательно соединена с другими группами с образованием циклоалкильного и/или гетероциклильного фрагмента, необязательно замещенного 0-4 группами RL5;
каждая из RL1, RL2, RL3, RL4 и RL5 независимо представляет собой Н, галоген, C1-8алкил, ОС1-8алкил, SC1-8алкил, NHC1-8алкил, N(С1-8алкил)2, С3-11циклоалкил, арил, гетероарил, С3-11гетероциклил, ОС1-8циклоалкил, SC1-8циклоалкил, NHC1-8циклоалкил, N(С1-8циклоалкил)2, N(С1-8циклоалкил)(С1-8алкил), ОН, NH2, SH, SO2C1-8алкил, Р(O)(ОС1-8алкил)(С1-8алкил), Р(O)(ОС1-8алкил)2, СС-С1-8алкил, ССН, CH=CH(C1-8алкил), С(С1-8алкил)=СН(С1-8алкил), С(С1-8алкил)=С(С1-8алкил)2, Si(OH)3, Si(C1-8алкил)2, Si(OH)(C1-8алкил)2, СОС1-8алкил, СО2Н, галоген, CN, CF3, CHF2, CH2F, NO2, SF5, SO2NHC1-8алкил, SO2N(C1-8алкил)2, SONHC1-8алкил, SON(C1-8алкил)2, CONHC1-8алкил, CON(C1-8алкил)2, N(C1-8алкил)CONH(C1-8алкил), N(C1-8алкил)CON(C1-8алкил)2, NHCONH(C1-8алкил), NHCON(C1-8алкил)2, NHCONH2, N(C1-8алкил)SO2NH(C1-8алкил), N(C1-8алкил)SO2N(C1-8алкил)2, NHSO2NH(C1-8алкил), NHSO2N(C1-8алкил)2, NHSO2NH2.
[380] В любом аспекте или варианте осуществления, описанных в данном документе, линкер (L) предусматривает группу, представленную общей структурой, выбранной из группы, состоящей из:
-N(R)-(CH2)m-O(CH2)n-O(CH2)o-O(CH2)p-O(CH2)q-O(CH2)r-OCH2-,
-O-(CH2)m-O(CH2)n-O(CH2)o-O(CH2)p-O(CH2)q-O(CH2)r-OCH2-,
-O-(CH2)m-O(CH2)n-O(CH2)o-O(CH2)p-O(CH2)q-O(CH2)r-O-;
-N(R)-(CH2)m-O(CH2)n-O(CH2)o-O(CH2)p-O(CH2)q-O(CH2)r-O-;
-(CH2)m-O(CH2)n-O(CH2)o-O(CH2)p-O(CH2)q-O(CH2)r-O-;
-(CH2)m-O(CH2)n-O(CH2)o-O(CH2)p-O(CH2)q-O(CH2)r-OCH2-;



 где m, n, о, р, q и r независимо равняются 0, 1, 2, 3, 4, 5, 6, при условии, что если число равняется нулю, то связь N-O или O-O отсутствует, R выбран из группы, состоящей из Н, метила и этила, и X выбран из группы, состоящей из Н и F;
где m, n, о, р, q и r независимо равняются 0, 1, 2, 3, 4, 5, 6, при условии, что если число равняется нулю, то связь N-O или O-O отсутствует, R выбран из группы, состоящей из Н, метила и этила, и X выбран из группы, состоящей из Н и F;
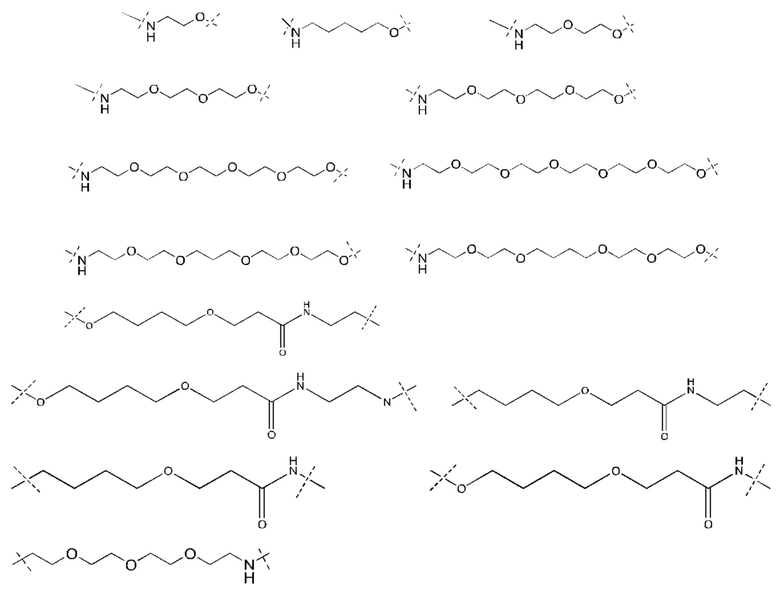







каждый n и m в линкере может независимо равняться 0, 1, 2, 3, 4, 5, 6.
[381] В любом аспекте или варианте осуществления, описанных в данном документе, линкер (L) выбран из группы, состоящей из:


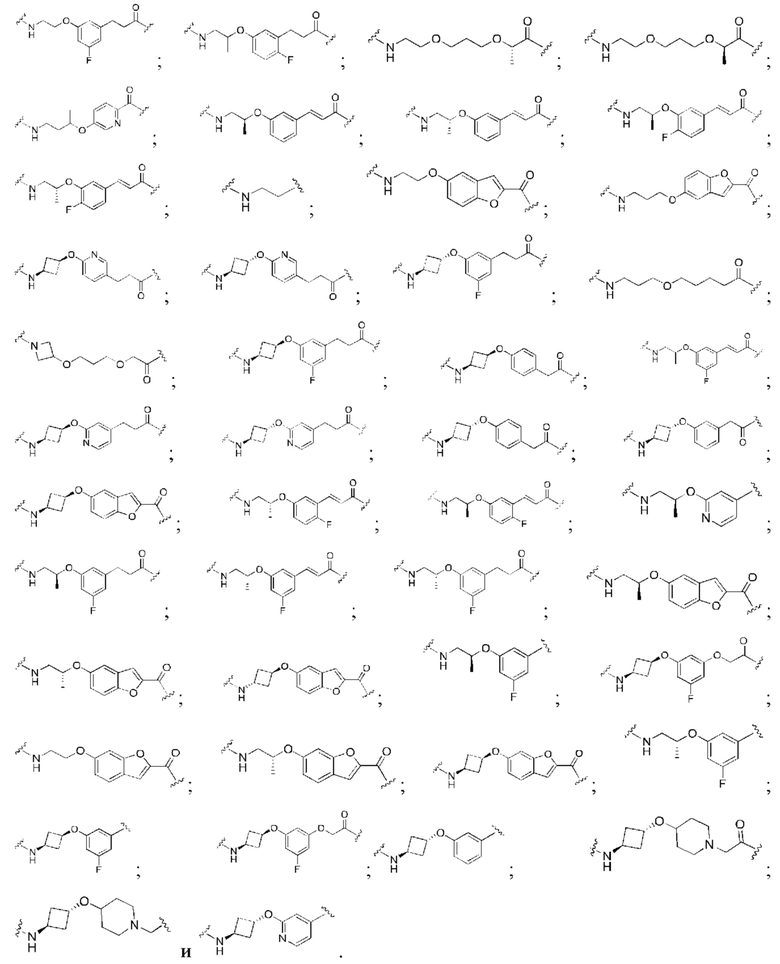
[382] В любом аспекте или варианте осуществления, описанных в данном документе, линкер (L) выбран из группы, состоящей из:

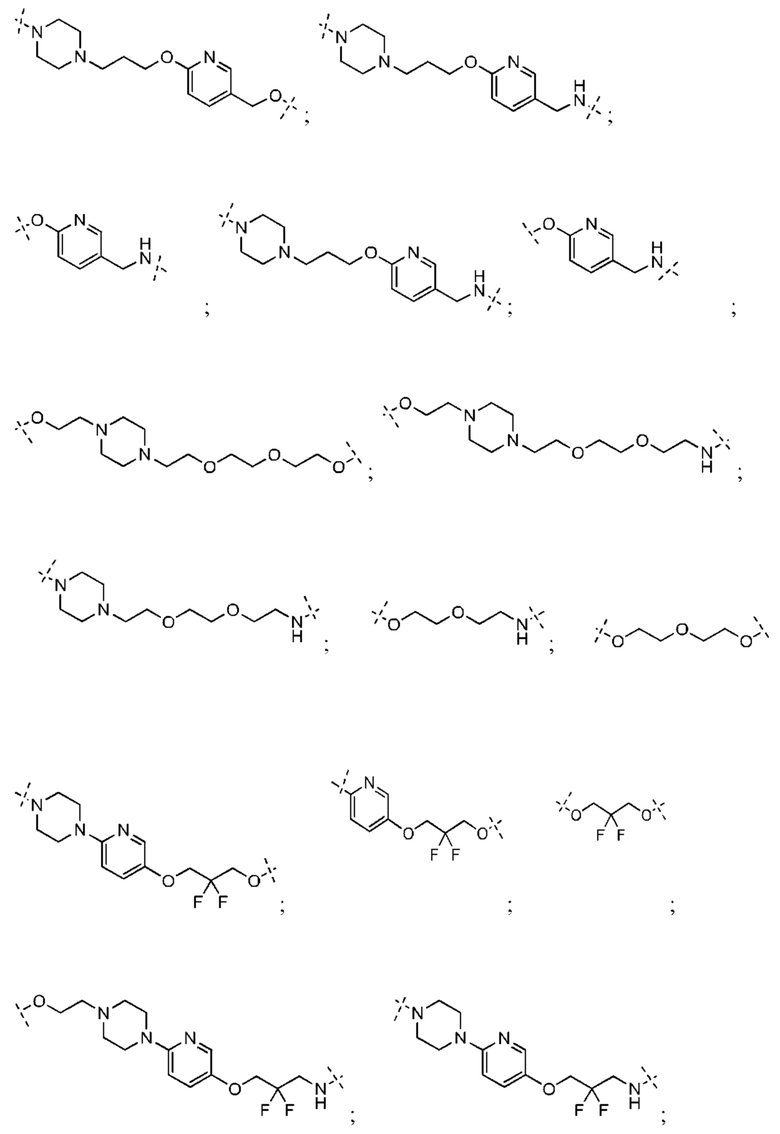















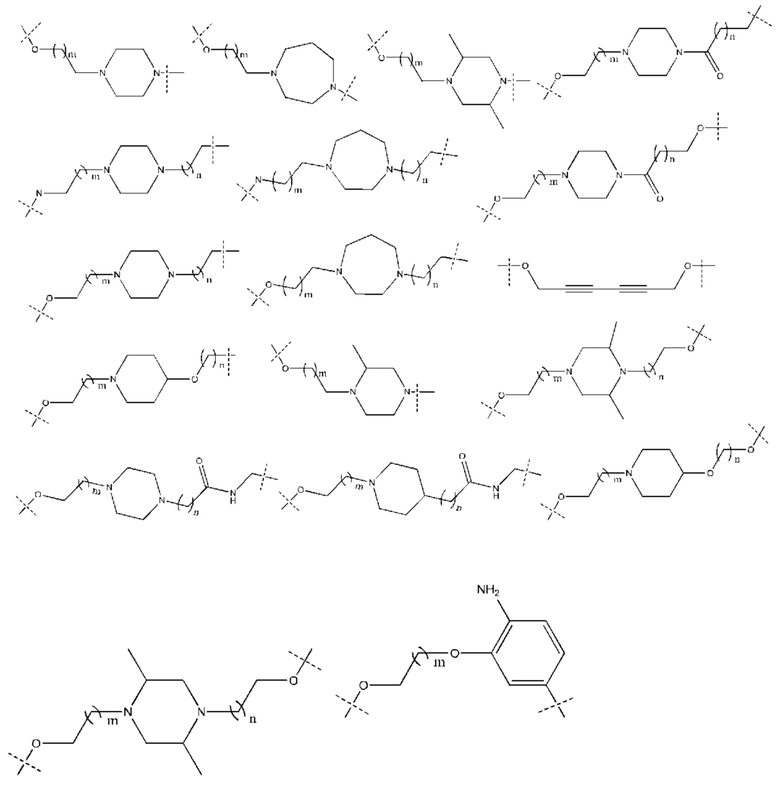











 где каждый m, n, о и р независимо равняется 0, 1, 2, 3, 4, 5, 6 или 7.
где каждый m, n, о и р независимо равняется 0, 1, 2, 3, 4, 5, 6 или 7.
[383] В любом аспекте или варианте осуществления, описанных в данном документе, L выбран из группы, состоящей из
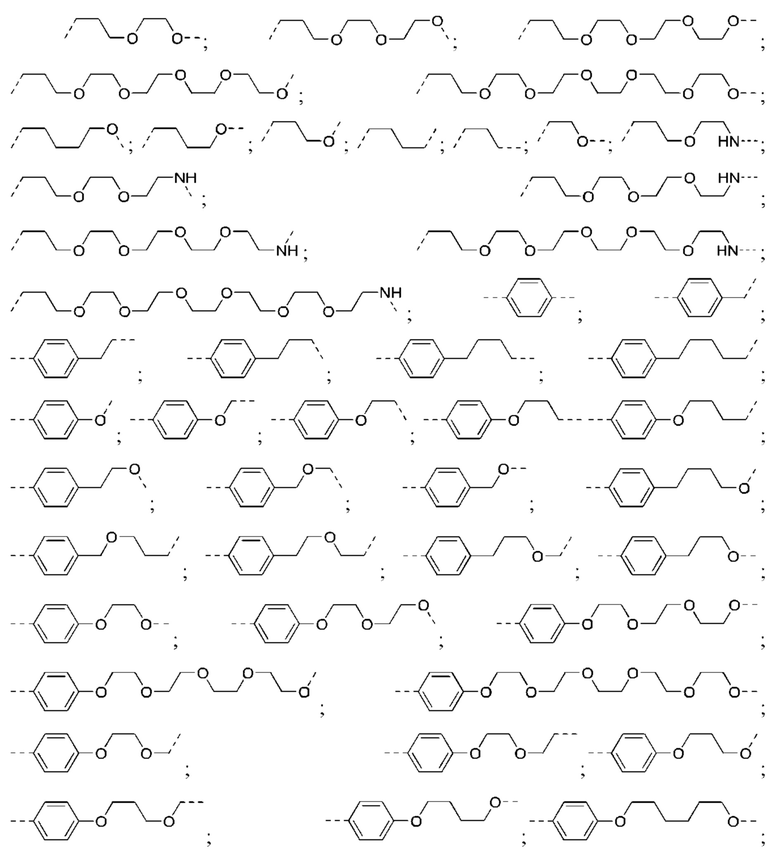




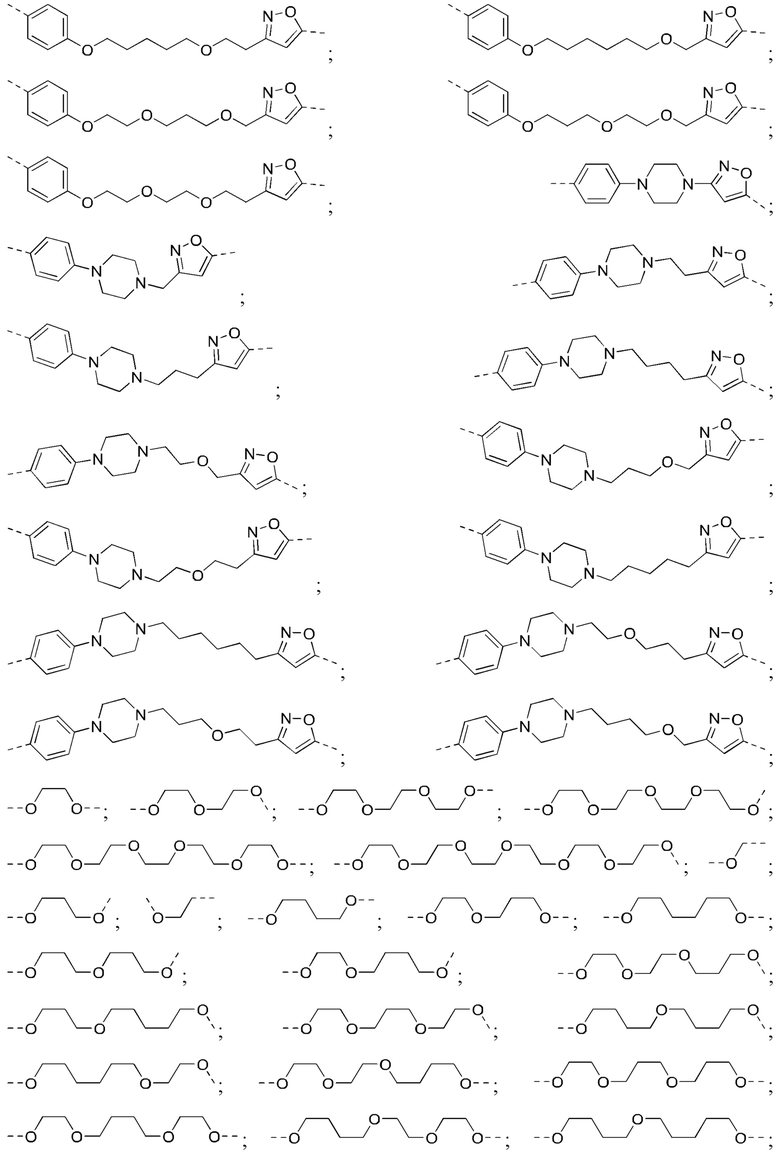


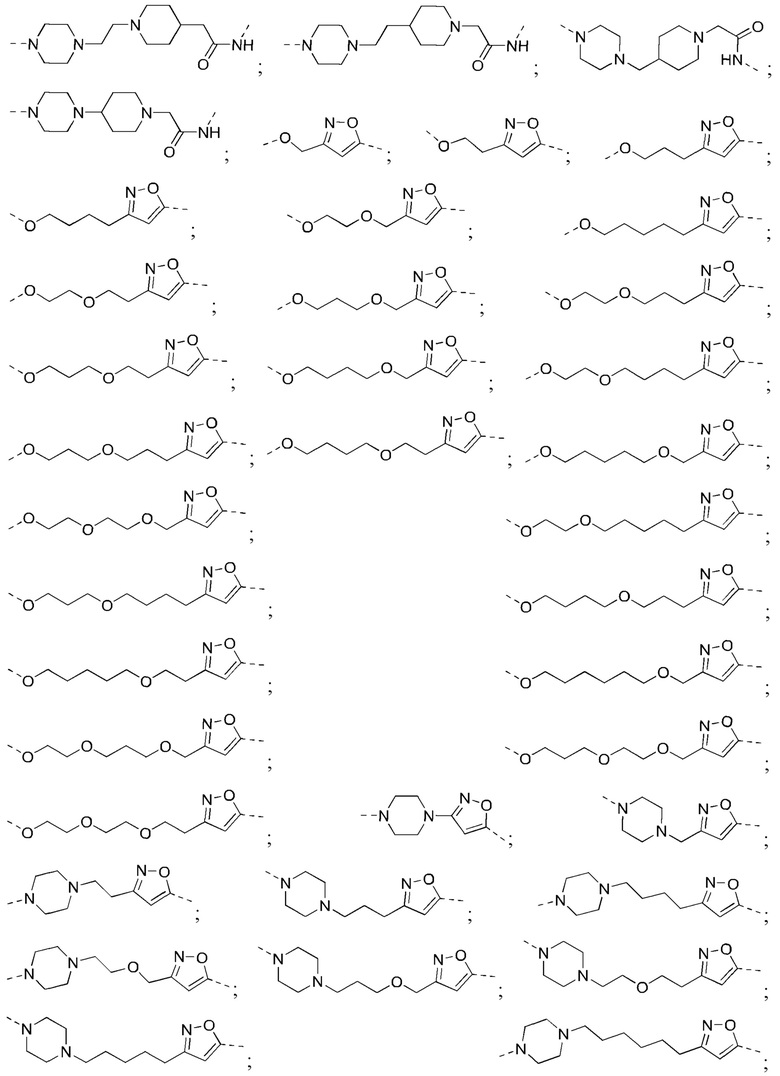
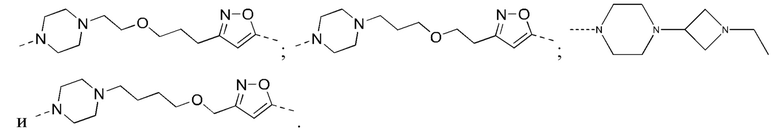
[384] В любом аспекте или варианте осуществления, описанных в данном документе, линкер (L) представляет собой полиэтиленоксигруппу, необязательно замещенную арилом или фенилом, содержащую от 1 до 10 этиленгликолевых звеньев.
[385] В любом аспекте или варианте осуществления, описанных в данном документе, линкер (L) предусматривает следующую химическую структуру:
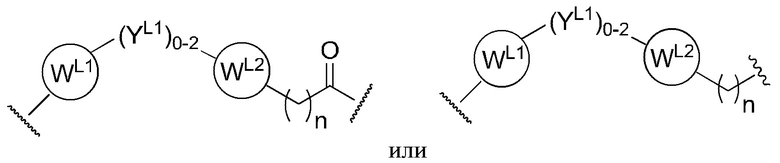
где
каждый из WL1 и WL2 независимо представляет собой 4-8-членное кольцо с 0-4 гетероатомами, необязательно замещенное RQ, при этом каждая RQ независимо представляет собой Н, галоген, ОН, CN, CF3, NH2, карбоксил, С1-С6алкил (линейный, разветвленный, необязательно замещенный), С1-С6алкокси (линейный, разветвленный, необязательно замещенный), или 2 группы RQ, взятые вместе с атомом, к которому они присоединены, образуют 4-8-членную кольцевую систему, содержащую 0-4 гетероатома;
каждый YL1 независимо представляет собой связь, С1-С6алкил (линейный, разветвленный, необязательно замещенный), и необязательно один или более атомов С заменены О; или С1-С6алкокси (линейный, разветвленный, необязательно замещенный);
n представляет собой целое число 0-10; и
 указывает на точку присоединения к фрагментам РТМ или ULM.
указывает на точку присоединения к фрагментам РТМ или ULM.
[386] В любом аспекте или варианте осуществления, описанных в данном документе, линкер (L) предусматривает следующую химическую структуру:
 или
или

где
каждый из WL1 и WL2 независимо представляет собой арил, гетероарил, циклическую группу, гетероциклическую группу, C1-6алкил (линейный, разветвленный, необязательно замещенный), С1-С6алкокси (линейный, разветвленный, необязательно замещенный), бициклическую группу, биарил, бигетероарил или бигетероциклическую группу, при этом каждое необязательно замещено RQ, при этом каждая RQ независимо представляет собой Н, галоген, ОН, CN, CF3, NH2, карбоксил, гидроксил, нитро, С=СН, С2-6алкенил, С2-6алкинил, C1- С6алкил (линейный, разветвленный, необязательно замещенный), C1-С6алкокси (линейный, разветвленный, необязательно замещенный), OC1-3алкил (необязательно замещенный 1 или более -F), ОН, NH2, NRY1RY2, CN, или 2 группы RQ, взятые вместе с атомом, к которому они присоединены, образуют 4-8-членную кольцевую систему, содержащую 0-4 гетероатома;
каждый YL1 независимо представляет собой связь, NRYL1, О, S, NRYL2, CRYL1RYL2, С=O, C=S, SO, SO2, C1-С6алкил (линейный, разветвленный, необязательно замещенный), и необязательно один или более атомов С заменены О; C1-С6алкокси (линейный, разветвленный, необязательно замещенный);
QL представляет собой 3-6-членное алициклическое или ароматическое кольцо с 0-4 гетероатомами, бигетероциклическое или бициклическое, необязательно соединенное мостиковой связью, необязательно замещенное 0-6 RQ, при этом каждая RQ независимо представляет собой Н, C1-6алкил (линейный, разветвленный, необязательно замещенный 1 или более атомами галогена, С1-6алкоксилом), или 2 группы RQ, взятые вместе с атомом, к которому они присоединены, образуют 3-8-членную кольцевую систему, содержащую 0-2 гетероатома);
каждый из RYL1, RYL2 независимо представляет собой Н, ОН, C1-6алкил (линейный, разветвленный, необязательно замещенный 1 или более атомами галогена, С1-6алкоксилом), или R1, R2 вместе с атомом, к которому они присоединены, образуют 3-8-членную кольцевую систему, содержащую 0-2 гетероатома);
n представляет собой целое число 0-10; и
 указывает на точку присоединения к фрагментам РТМ или ULM.
указывает на точку присоединения к фрагментам РТМ или ULM.
[387] В любом аспекте или варианте осуществления, описанных в данном документе, соединение содержит несколько ULM, несколько РТМ, несколько линкеров или любые их комбинации.
[388] В любом аспекте или варианте осуществления, описанных в данном документе, соединение выбрано из группы, состоящей из: Соединения 1-547 (т.е. соединение, выбранное из таблицы 1 или таблицы 2).
[389] Другой аспект настоящего изобретения предусматривает композицию, содержащую эффективное количество бифункционального соединения по настоящему изобретению и фармацевтически приемлемый носитель.
[390] В любом аспекте или варианте осуществления, описанных в данном документе, композиция дополнительно содержит по меньшей мере одно из дополнительного биологически активного средства или другого бифункционального соединения согласно любому из пп. 1-23.
[391] В любом аспекте или варианте осуществления, описанных в данном документе, дополнительное биологически активное средство представляет собой противораковое средство.
[392] Дополнительные аспект настоящего изобретения предусматривает композицию, содержащую фармацевтически приемлемый носитель и эффективное количество по меньшей мере одного соединения по настоящему изобретению, для лечения заболевания или нарушения у субъекта, при этом способ предусматривает введение композиции субъекту, нуждающемуся в этом, где соединение является эффективным в лечении или облегчении по меньшей мере одного симптома заболевания или нарушения.
[393] В любом аспекте или варианте осуществления, описанных в данном документе, заболевание или нарушение ассоциировано с накоплением и агрегацией эстрогенового рецептора.
[394] В любом аспекте или варианте осуществления, описанных в данном документе, заболевание или нарушение представляют собой рак или неоплазию, ассоциированные с накоплением и агрегацией эстрогенового рецептора.
[395] В любом аспекте или варианте осуществления, описанных в данном документе, заболевание или нарушение представляют собой рак молочной железы или рак матки.
[396] В любом аспекте или варианте осуществления, описанных в данном документе, заболевание или нарушение представляют собой эндометриоз.
Общие подходы к синтезу
[397] Для осуществления на практике синтеза и оптимизации бифункциональных молекул, описанных в данном документе, можно найти решение в постадийном или модульном способе. Например, идентификация соединений, которые связываются с целевыми молекулы, может предусматривать операции скрининга с высокой или средней пропускной способностью, если подходящие лиганды не являются непосредственно доступными. Не редки случаи, когда исходные лиганды требуют циклов итерационного проектирования и оптимизации для улучшения субоптимальных аспектов, идентифицированных с помощью данных из подходящих in vitro и фармакологических и/или ADMET анализов. Часть операции оптимизации/SAR будет заключаться в тестировании положений лиганда, которые допускают замещение и которые могут быть подходящими местами для присоединения химических групп линкера, ранее указанного в данном документе. Если доступны кристаллографические или ЯМР данные о структуре, их можно применять для фокусирования на таком синтетическом усилии.
[398] Очень похожим образом можно идентифицировать и оптимизировать лиганды для Е3-лигазы, т.е. ULM//VLM/CLM.
[399] Имея в своем распоряжении РТМ и ULM (например, VLM и/или CLM) специалист в данной области техники может применять известные способы синтеза для их комбинации с линкерным фрагментом или без него. Линкерные фрагменты можно синтезировать в диапазоне составов, значений длины и эластичности и функционализированные так, что группы РТМ и ULM могут быть присоединены последовательно к дальним концам линкера. Таким образом, можно создать и профилировать библиотеку бифункциональных молекул в фармакологических исследованиях и ADMET/PK анализах in vitro и in vivo. Как и с группами РТМ и ULM, конечные бифункциональные молекулы можно подвергать циклам итерационного проектирования и оптимизации с целью определения молекул с необходимыми свойствами.
[400] Соединения по настоящему изобретению [например, общих формул (I), (IPTM) и (IIPTM) и бифункциональные соединения, их содержащие] можно получить с помощью способов, известных в области органического синтеза, как представлено для конкретных иллюстративных соединениях или соединений, описанных в данной заявке. Во всех способах, хорошо понятно, что в случае необходимости можно применять защитные группы для чувствительных или реакционноспособных групп в соответствии с общими принципами химии. Защитными группами манипулируют в соответствии со стандартными способами органического синтеза (Т.W. Green and P.G.M. Wuts (1999) Protective Groups in Organic Synthesis, 3rd edition, John Wiley & Sons). Данные группы удаляют на подходящей стадии синтеза соединения с применением способов, которые легко понятны специалистам в данной области техники. Выбор способов, а также реакционных условий и порядок их проведения будет соответствовать получению соединений по настоящему изобретению, в том числе соединений формул (I), (IPTM) и (IIPTM) и бифункциональных соединений, их содержащих. Схемы, описанные ниже, иллюстрируют общие способы получения соединений со структурой, представленной с помощью формул (I), (IPTM) и (IIPTM).
[401] Соединения по настоящему изобретению можно синтезировать путем соединения фрагмента, связывающегося с ER, полученного в соответствии со схемой 1-1-схемой 1-40, с фрагментом, связывающимся с цереблоном, полученным в соответствии со схемой 2-1 - схемой 2-47. Подробный синтез иллюстративных соединений по настоящему изобретению дополнительно описан на схеме 3-1 - схеме 3-88.
[402] Сокращения
[403] ACN: ацетонитрил
[404] ADDP: 1,1'-(азодикарбонил)дипиперидин
[405] BAST: трифторид N,N-бис(2-метоксиэтил)аминосеры
[406] ВРО: бензоилпероксид
[407] Cbz: карбонилбензилокси
[408] DAST: трифторид диэтиламиносеры
[409] DBE: 1,2-дибромэтан
[410] DCE: 1,2-дихлорэтан
[411] DCM: дихлорметан
[412] DEAD: диэтилазодикарбоксилат
[413] DIAD: диизопропилазодикарбоксилат
[414] DIBAL: гидрид диизобутилалюминия
[415] DIE А или DIPEA: диизопропилэтиламин
[416] DMA: N,N-диметилацетамид
[417] DMF: N,N-диметилформамид
[418] DMP: перйодинан Десса-Мартина
[419] ЕА: этилацетат
[420] EDCI: 1-этил-3-(3-диметиламинопропил)карбодиимид
[421] HBTU: гексафторфосфат N,N,N'N'-тетраметил-O-(1H-бензотриазол-1-ил)урония
[422] HMDS: бис(триметилсилил)амин
[423] НМРА: гексаметилфосфорамид
[424] LDA: диизопропиламид лития
[425] МСРВА: мета-хлорпероксибензойная кислота
[426] MsCl: метансульфонилхлорид
[427] M.W: обработка с помощью микроволнового излучения
[428] NBS: N-бромсукцинимид
[429] NMP: N-метилпирролидон
[430] РСС: хлорхромат пиридиния
[431] Pd-118 или Pd(dtpf)Cl2: 1,1'-бис(ди-трет-бутилфосфино)ферроцендихлорпалладий
[432] Pd(dppf)Cl2: 1,1'-бис(дифенилфосфино)ферроцендихлорпалладий
[433] Pd(dba)2: бис(дибензилиденацетон)палладий
[434] Pd2(dba)3: трис(дибензилиденацетон)дипалладий
[435] PPTS: п-толуолсульфонат пиридиния
[436] PTSA: п-толуолсульфоновая кислота
[437] RuPhos-Pd-G3: метансульфонат [(2-дициклогексилфосфино-2',6'-диизопропокси-1,1'-бифенил)-2-(2'-амино-1,1'-бифенил)]палладия(II)
[438] RuPhos-Pd-G2: хлор[(2-дициклогексилфосфино-2',6'-диизопропокси-1,1'-бифенил)-2-(2'-амино-1,1'-бифенил)]палладий(II)
[439] SFC: сверхкритическая флюидная хроматография
[440] t-BuXPhos-Pd-G3: метансульфонат [(2-ди-трет-бутилфосфино-2',4',6'-триизопропил-1,1'-бифенил)-2-(2'-амино-1,1'-бифенил)]палладия(II)
[441] TEA: триметиламин
[442] TFA: трифторуксусная кислота
[443] TLC: тонкослойная хроматография
[444] ТМР: 2,2,6,6-тетраметилпиперидин
[445] TEMPO: 2,2,6,6-тетраметилпиперидин-N-оксид
[446] TosCl или TsCl: п-толуолсульфонилхлорид
[447] TsOH: п-толуолсульфоновая кислота
[448] XantPhos: 4,5-бис(дифенилфосфино)-9,9-диметилксантен
[449] XPhos: 2-дициклогексилфосфино-2'4'6'-триизопропилбифенил
[450] XPhos-Pd-G3: метансульфонат [(2-дициклогексилфосфино-2',4',6'-триизопропил-1,1'-бифенил)-2-(2'-амино-1,1'-бифенил)]палладия(II)
[451] 12354-85-7: бис(пентаметилциклопентадиенилродия дихлорид)
[452] На общих схемах синтеза 1-1 - 1-40 описаны пути, применяемые для получения иллюстративных лигандов ER и иллюстративных лигандов ER с частичными линкерными фрагментами, соединенными с ними.
[453] Общая схема синтеза 1-1 для получения промежуточного соединения
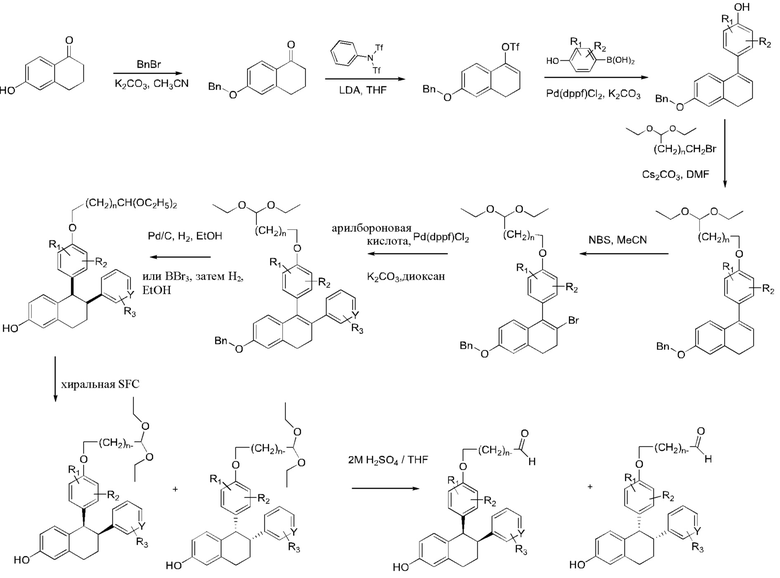
Если число n может равняться 0-4; Y может представлять собой СН, N; R1, R2 и R3 могут представлять собой Н, F, CF3. В случае удаления защитной бензильной группы с применением BBr3, с функциональной группы ацеталя также будет снята защита с обеспечением необходимого промежуточного соединения, представляющего собой альдегид.
[454] Общая схема синтеза 1-2 для получения промежуточного соединения

[455] Общая схема синтеза 1-3 для получения промежуточного соединения

где n=0, 1, 2, 3, 4; Y=СН, N; R=Н, F, CF3
[456] Общая схема синтеза 1-4 для получения промежуточного соединения
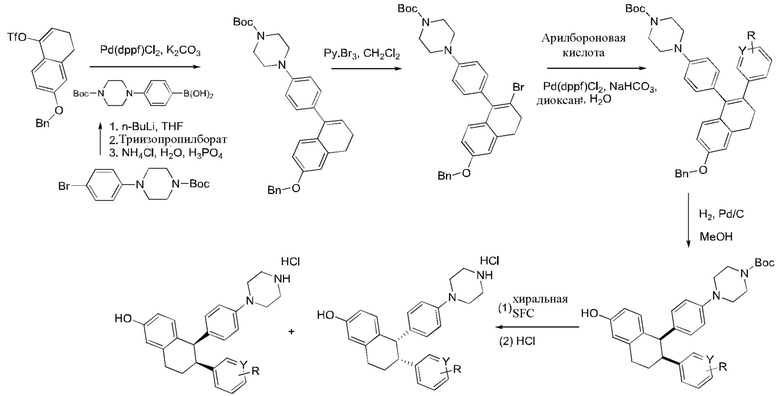
где Y=СН, N; R=H, F, CF3
[457] Общая схема синтеза 1-5 для получения промежуточного соединения

где Y=СН, N; R=Н, F, CF3
[458] Общая схема синтеза 1-6 для получения промежуточного соединения

[459] Общая схема синтеза 1-7 для получения промежуточного соединения

[460] Общая схема синтеза 1-8 для получения промежуточного соединения

где Y=СН, N; R=H, F, CF3
[461] Общая схема синтеза 1-9 для получения промежуточного соединения
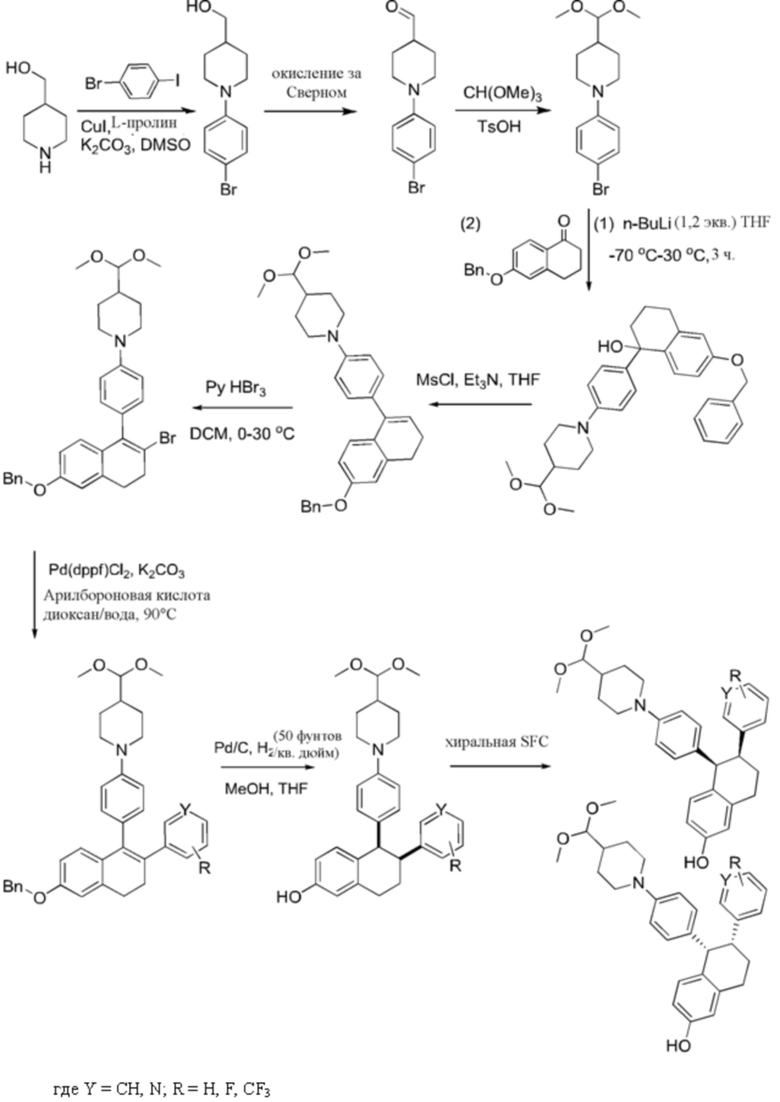
где Y=СН, N; R=H, F, CF3
[462] Общая схема синтеза 1-10 для получения промежуточного соединения

где Y=СН, N; R=H, F, CF3
[463] Общая схема синтеза 1-11 для получения промежуточного соединения
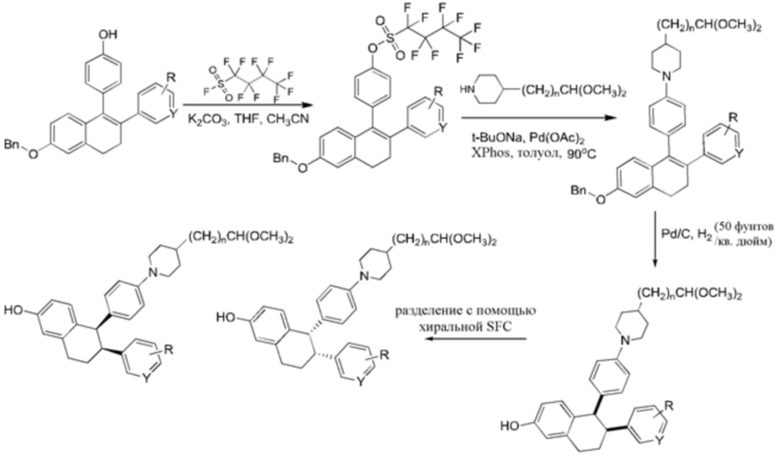
где n = 0, 1, 2, 3; Y = СН, N; R = Н, F, CF3
[464] Общая схема синтеза 1-12 для получения промежуточного соединения
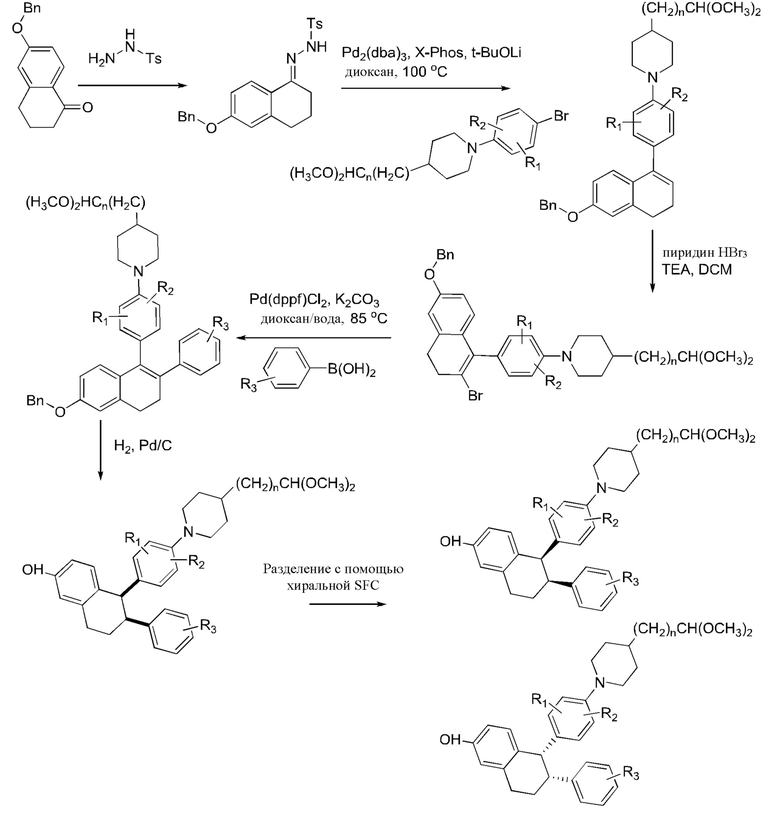
где n=0, 1, 2, 3; R1, R2 и R3=H, F, CF3
[465] Общая схема синтеза 1-13 для получения промежуточного соединения

X и Y = H, F; L = (CH2), где n = 0, 1, 2
[466] Общая схема синтеза 1-14 для получения промежуточного соединения

[467] Общая схема синтеза 1-15 для получения промежуточного соединения

[468] Общая схема синтеза 1-16 для получения промежуточного соединения

[469] Общая схема синтеза 1-17 для получения промежуточного соединения

[470] Общая схема синтеза 1-18 для получения промежуточного соединения

[471] Общая схема синтеза 1-19 для получения промежуточного соединения

[472] Общая схема синтеза 1-20 для получения промежуточного соединения

[473] Общая схема синтеза 1-21 для получения промежуточного соединения

[474] Общая схема синтеза 1-22 для получения промежуточного соединения

[475] Общая схема синтеза 1-23 для получения промежуточного соединения
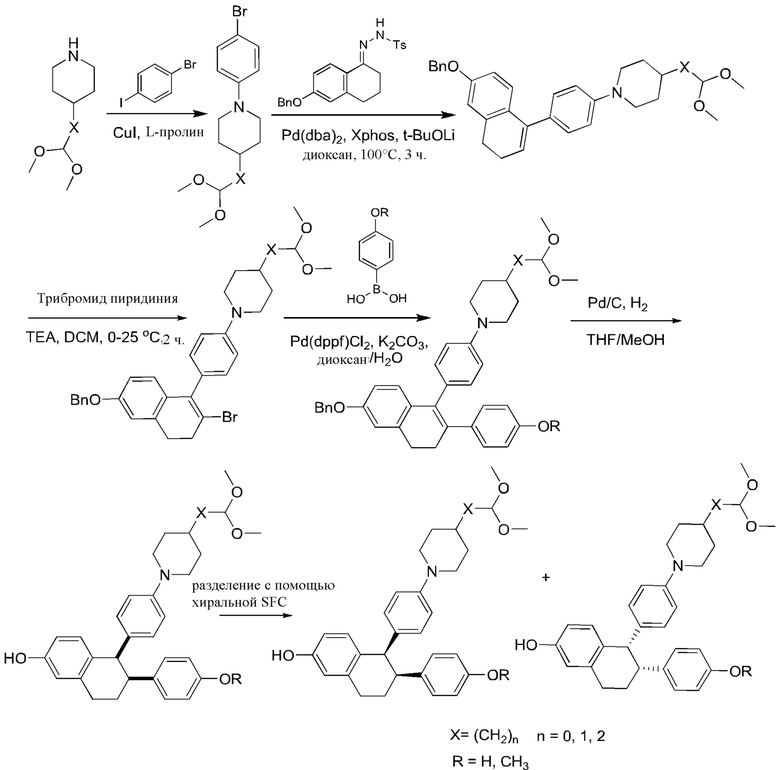
[476] Общая схема синтеза 1-24 для получения промежуточного соединения
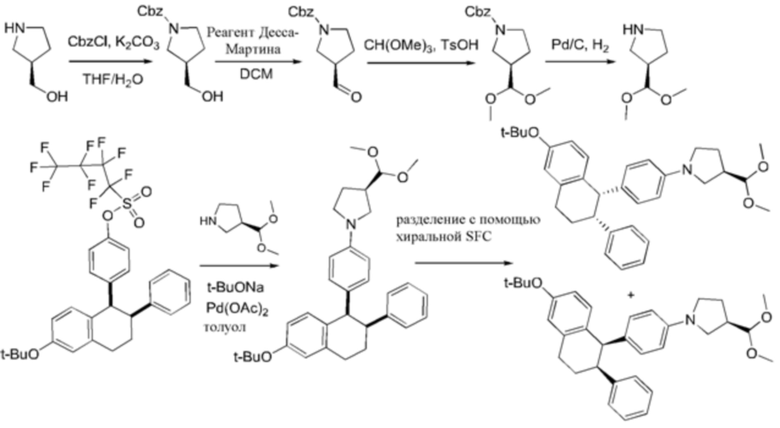
[477] Общая схема синтеза 1-25 для получения промежуточного соединения

[478] Общие схемы синтеза 1-26а и 1-26b для получения промежуточных соединений
Схема 1-26а

Схема 1-26b
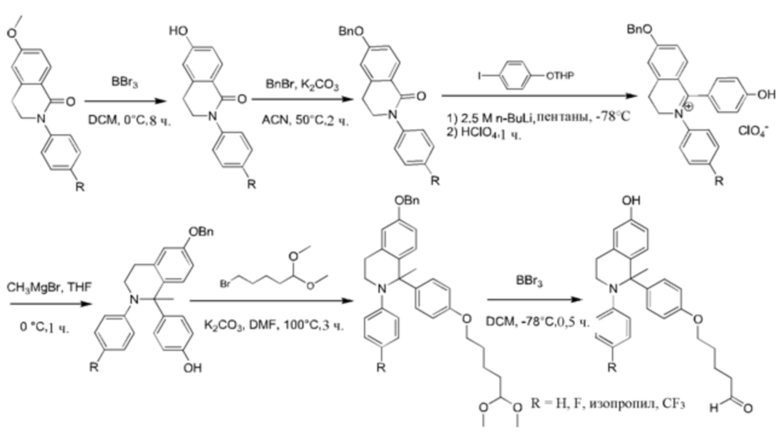
[479] Общие схемы синтеза 1-27 для получения промежуточных соединений

[480] Общая схема синтеза 1-28 для получения промежуточного соединения

[481] Общая схема синтеза 1-29 для получения промежуточного соединения

[482] Общая схема синтеза 1-30 для получения промежуточного соединения

[483] Общая схема синтеза 1-31 для получения промежуточного соединения

[484] Общая схема синтеза 1-32 для получения промежуточного соединения

[485] Общая схема синтеза 1-33 для получения промежуточного соединения

[486] Общая схема синтеза 1-34 для получения промежуточного соединения

[487] Общая схема синтеза 1-35 для получения промежуточного соединения

[488] Общая схема синтеза 1-36 для получения промежуточного соединения
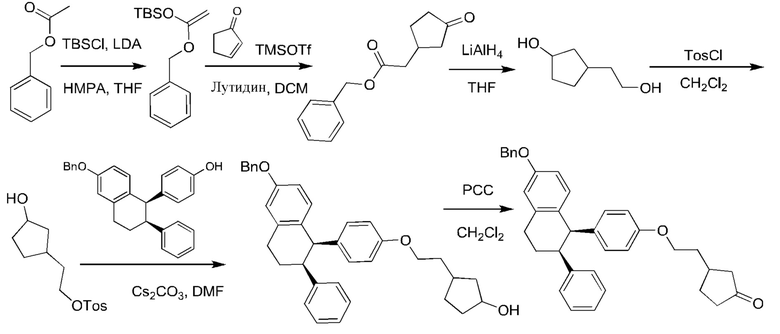
[489] Общие схемы синтеза 1-37а и 1-37b для получения промежуточных соединений
Схема 1-37а
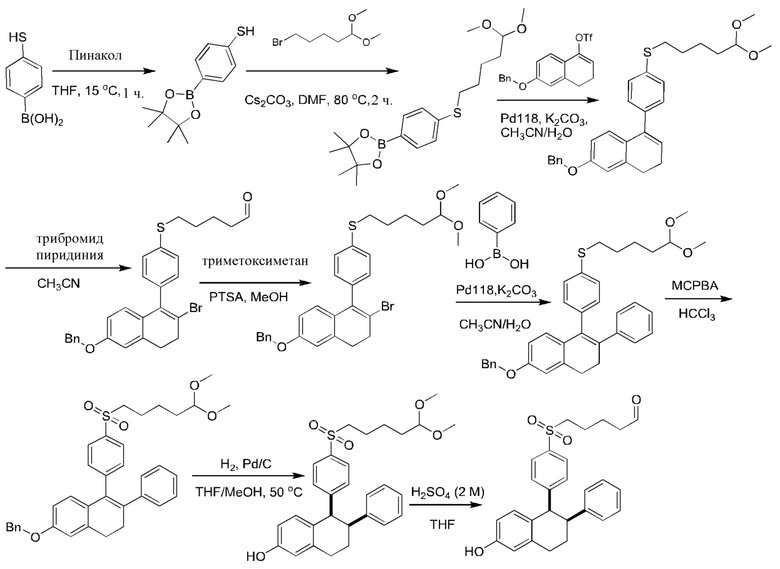
Схема 1-37b

[490] Общая схема синтеза 1-38 для получения промежуточного соединения

[491] Общая схема синтеза 1-39 для получения промежуточного соединения

[492] Общая схема синтеза 1-40 для получения промежуточного соединения

[493] На общих схемах синтеза 2-1 - 2-47 описаны пути, применяемые для получения иллюстративных фрагментов, связывающихся с цереблоном, и фрагментов, связывающихся с цереблоном, с частичными линкерными фрагментами, соединенными с ними.
[494] Общие схемы синтеза 2-1а - 2-1d для получения промежуточных соединений
Схема 2-1а

Схема 2-1b
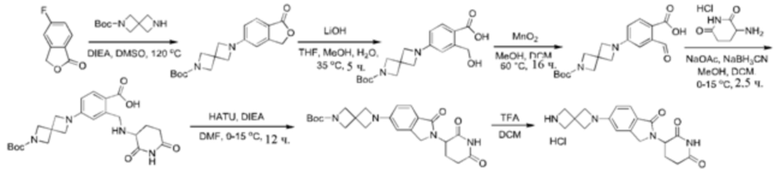
Схема 2-1c
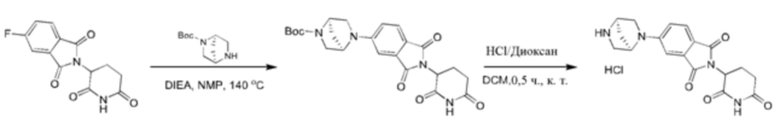
Схема 2-1d

[495] Общая схема синтеза 2-2 для получения промежуточного соединения

[496] Общая схема синтеза 2-3 для получения промежуточного соединения

[497] Общая схема синтеза 2-4 для получения промежуточного соединения

[498] Общая схема синтеза 2-5 для получения промежуточного соединения

[499] Общая схема синтеза 2-6 для получения промежуточного соединения

[500] Общая схема синтеза 2-7 для получения промежуточного соединения

[501] Общие схемы синтеза 2-8а и 2-8b для получения промежуточного соединения
Схема 2-8а
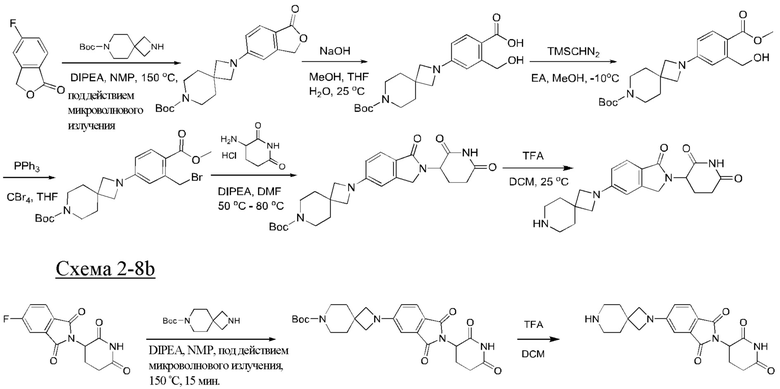
Схема 2-8b

[502] Общая схема синтеза 2-9 для получения промежуточного соединения

[503] Общая схема синтеза 2-10 для получения промежуточного соединения

[504] Общие схемы синтеза 2-11а - 2-11b для получения промежуточных соединений
Схема 2-11а
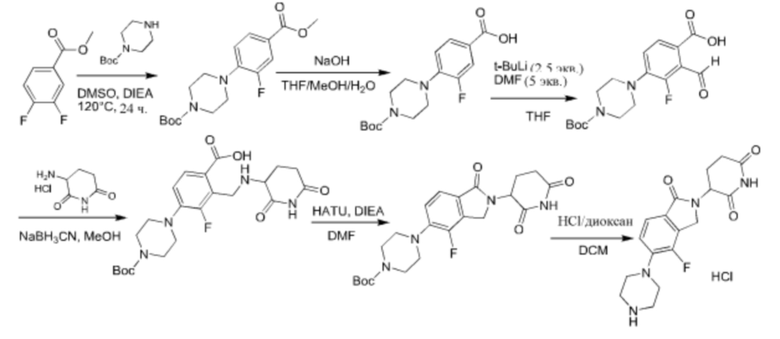
Схема 2-11b
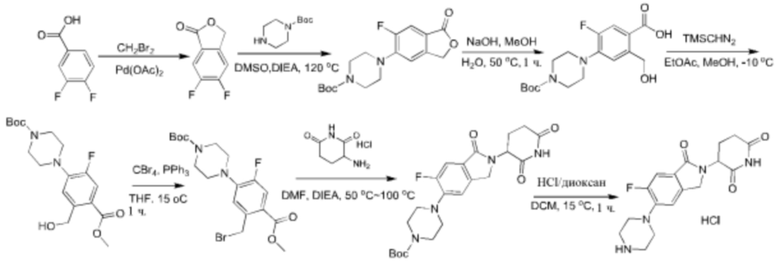
Схема 2-11c

[505] Общая схема синтеза 2-12 для получения промежуточного соединения

[506] Общая схема синтеза 2-13 для получения промежуточного соединения

[507] Общая схема синтеза 2-14 для получения промежуточного соединения

[508] Общая схема синтеза 2-15 для получения промежуточного соединения

[509] Общая схема синтеза 2-16 для получения промежуточного соединения

[510] Общая схема синтеза 2-17 для получения промежуточного соединения
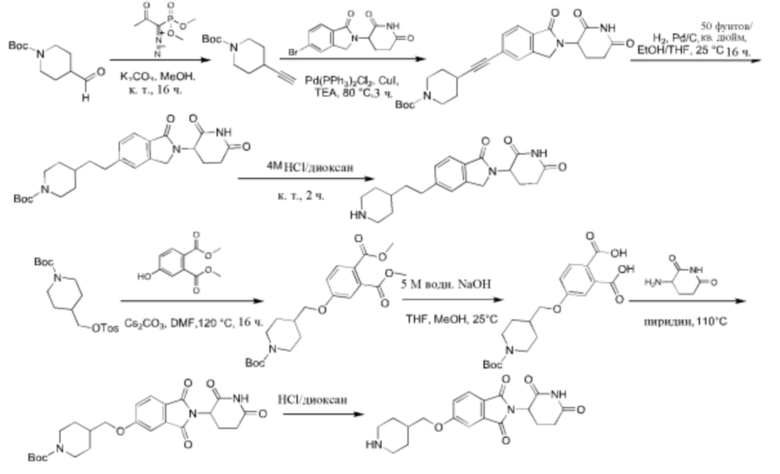
[511] Общие схемы синтезы 2-18а - 2-18b для получения промежуточного соединения
Схема 2-18а
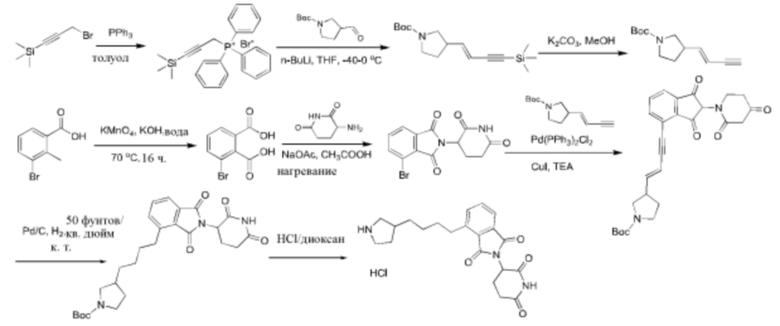
Схема 2-18b

[512] Общая схема синтеза 2-19 для получения промежуточного соединения

[513] Общие схемы синтеза 2-20а - 2-20b для получения промежуточных соединений
Схема 2-20а
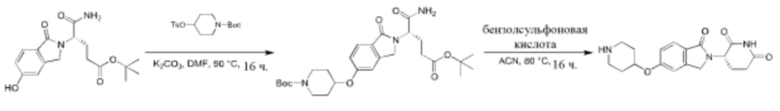
Схема 2-20b

[514] Общая схема синтеза 2-21 для получения промежуточного соединения
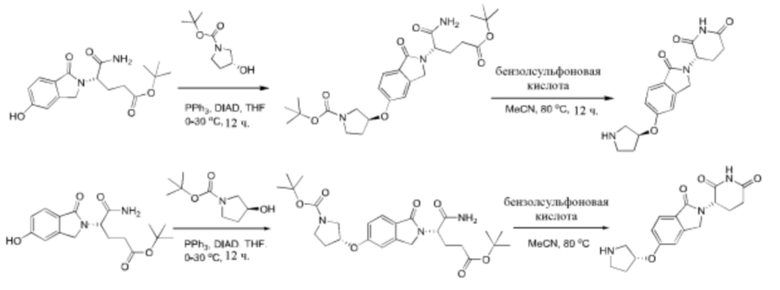
[515] Общая схема синтеза 2-22 для получения промежуточного соединения

[516] Общая схема синтеза 2-23 для получения промежуточного соединения

[517] Общая схема синтеза 2-24 для получения промежуточного соединения

[518] Общая схема синтеза 2-25 для получения промежуточного соединения

[519] Общая схема синтеза 2-26 для получения промежуточного соединения
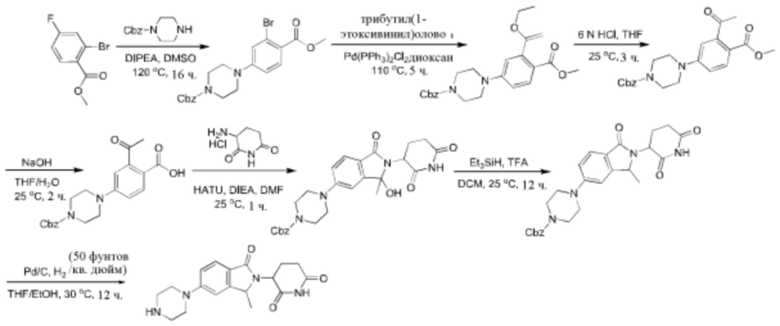
[520] Общая схема синтеза 2-27 для получения промежуточного соединения
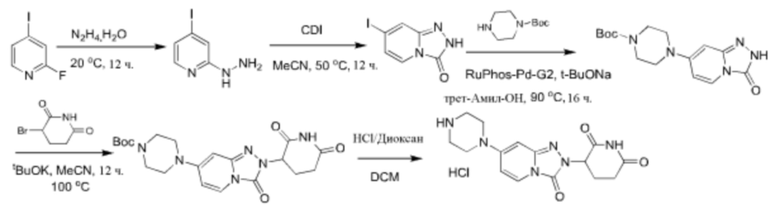
[521] Общая схема синтеза 2-28 для получения промежуточного соединения

[522] Общая схема синтеза 2-29 для получения промежуточного соединения

[523] Общая схема синтеза 2-30 для получения промежуточного соединения

[524] Общая схема синтеза 2-31 для получения промежуточного соединения

[525] Общая схема синтеза 2-32 для получения промежуточного соединения

[526] Общая схема синтеза 2-33 для получения промежуточного соединения

[527] Общая схема синтеза 2-34 для получения промежуточного соединения

[528] Общая схема синтеза 2-35 для получения промежуточного соединения

[529] Общая схема синтеза 2-36 для получения промежуточного соединения
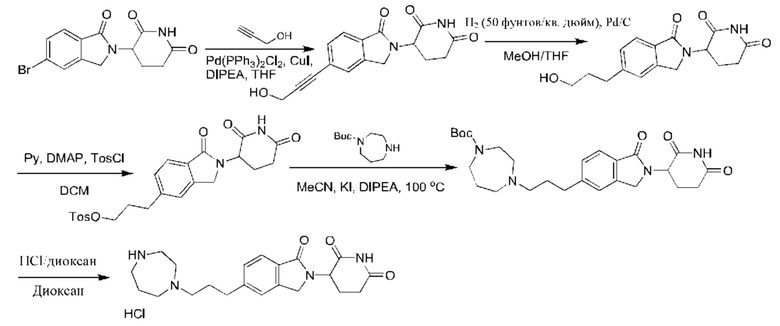
[530] Общая схема синтеза 2-37 для получения промежуточного соединения

[531] Общая схема синтеза 2-38 для получения промежуточного соединения

[532] Общая схема синтеза 2-39 для получения промежуточного соединения

[533] Общая схема синтеза 2-40 для получения промежуточного соединения

[534] Общие схемы синтеза 2-41а и 2-4 lb для получения промежуточных соединений
Схема 2-41а

Схема 2-41b

[535] Общая схема синтеза 2-42 для получения промежуточного соединения

[536] Общая схема синтеза 2-43 для получения промежуточного соединения

[537] Общая схема синтеза 2-44 для получения промежуточного соединения
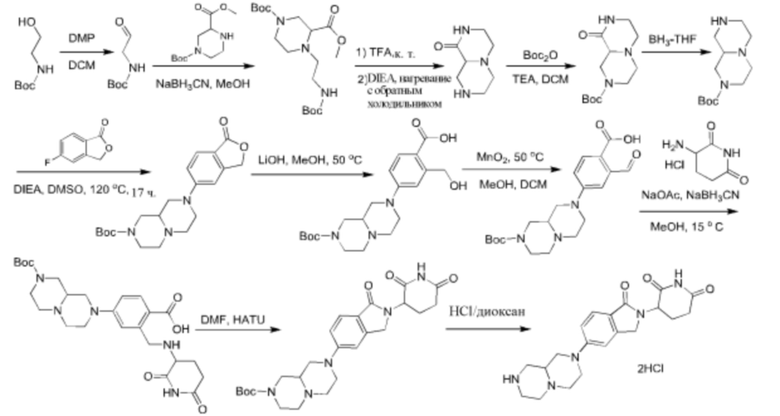
[538] Общие схемы синтеза 2-45а - 2-45с для получения промежуточных соединений
Схема 2-45а

Схема 2-45b

Схема 2-45с

[539] Общая схема синтеза 2-46 для получения промежуточного соединения

[540] Общая схема синтеза 2-47 для получения промежуточного соединения

[541] На общих схемах синтеза 3-1 - 3-88 описаны пути, применяемые для получения иллюстративных химерных соединений по настоящему изобретению.
[542] Общая схема синтеза 3-1
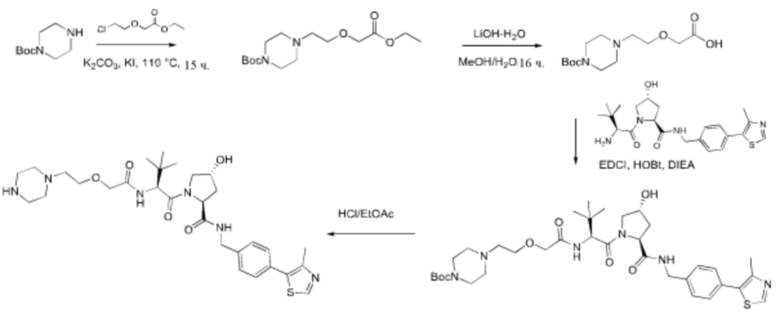
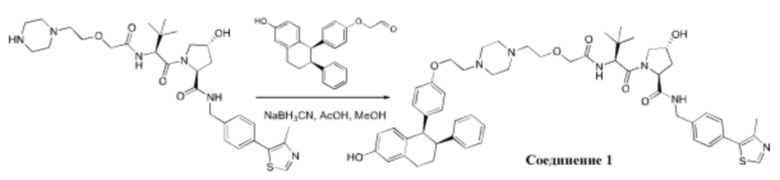

[543] В качестве альтернативы, соединение 1 и соединение 2 также можно получать с применением схемы синтеза 3-2.
[544] Общая схема синтеза 3-2
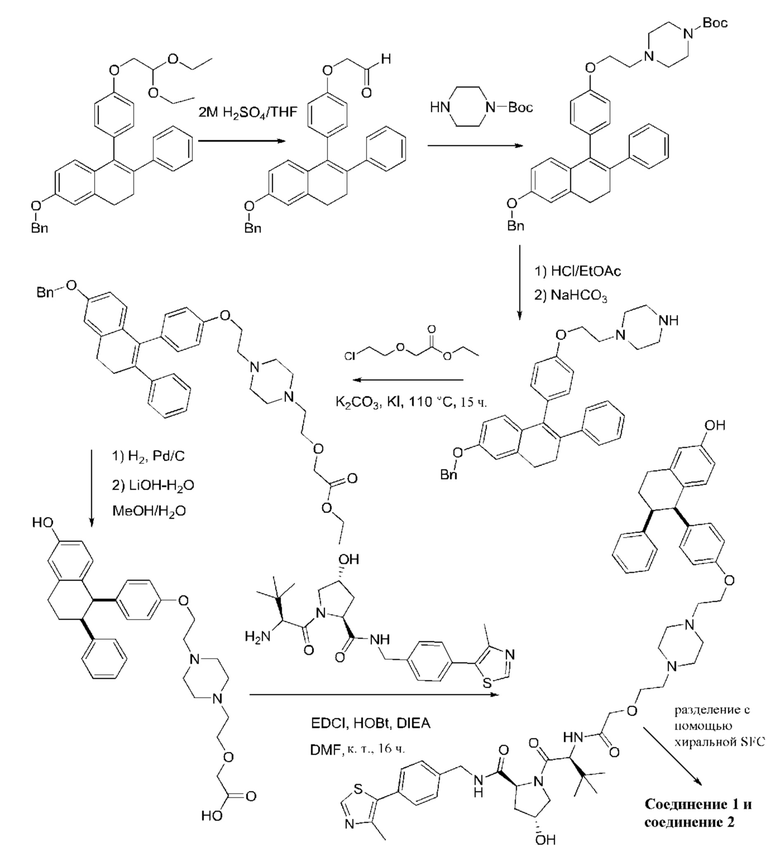
[545] Общая схема синтеза 3-3

[546] Где X на схеме 3-3 может представлять собой Н, F, C1-С6алкил (линейный, разветвленный, необязательно замещенный), ОСН3, CF3; и арильное кольцо может являться моно- или дизамещенным X.
[547] Общая схема синтеза 3-4

[548] Общая схема синтеза 3-5


[549] Общая схема синтеза 3-6

[550] Общая схема синтеза 3-7

[551] Общая схема синтеза 3-8

[552] Общая схема синтеза 3-9

[553] Общая схема синтеза 3-10

[554] Общая схема синтеза 3-11
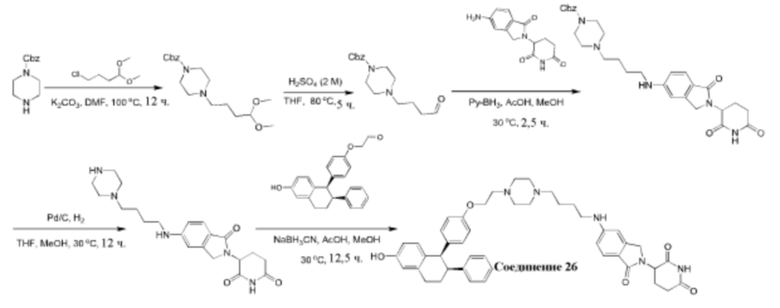
[555] Общая схема синтеза 3-12

[556] Общая схема синтеза 3-13


[557] Общая схема синтеза 3-14

[558] Общая схема синтеза 3-15
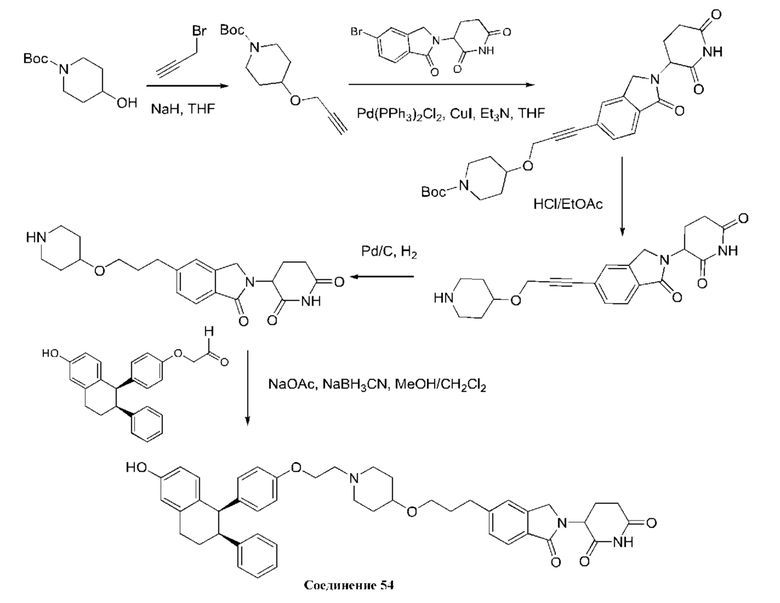
[559] Общая схема синтеза 3-16
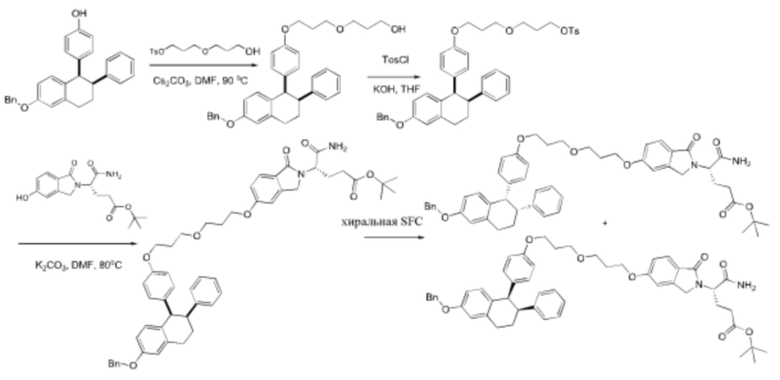
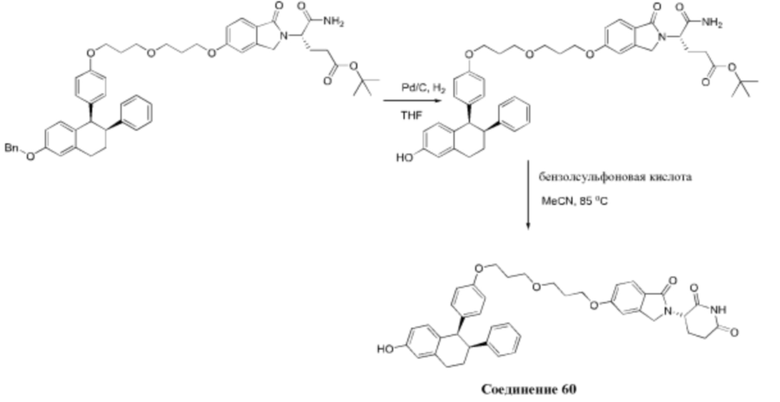
[560] Общая схема синтеза 3-17

[561] Общая схема синтеза 3-18

[562] Общая схема синтеза 3-19

[563] Общая схема синтеза 3-20

[564] Общая схема синтеза 3-21

[565] Общая схема синтеза 3-22

[566] Общая схема синтеза 3-23

[567] Общая схема синтеза 3-24 для получения заявленных соединений

[568] Общая схема синтеза 3-25

[569] Общая схема синтеза 3-26
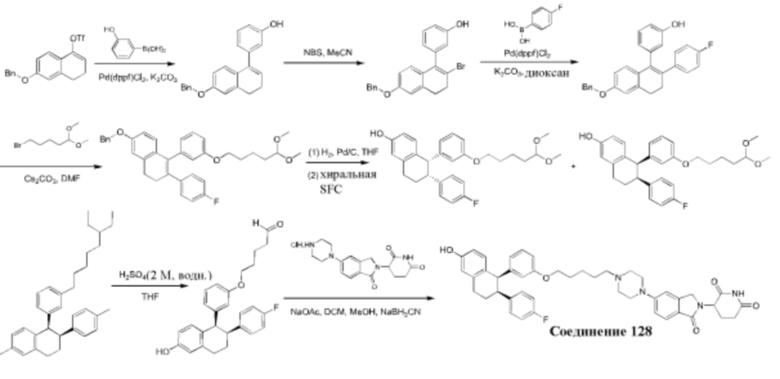
[570] Общая схема синтеза 3-27

[571] Общая схема синтеза 3-28

[572] Общая схема синтеза 3-29

[573] Общая схема синтеза 3-30

[574] Общая схема синтеза 3-31

[575] Общая схема синтеза 3-32

[576] Общая схема синтеза 3-33

[577] Общая схема синтеза 3-34

[578] Общая схема синтеза 3-35
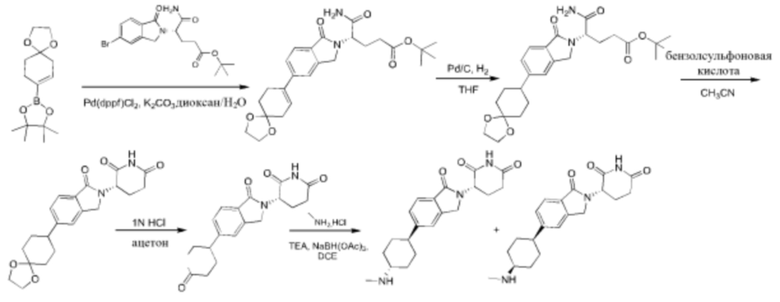

[579] Общая схема синтеза 3-36

[580] Общая схема синтеза 3-37


[581] Общая схема синтеза 3-38
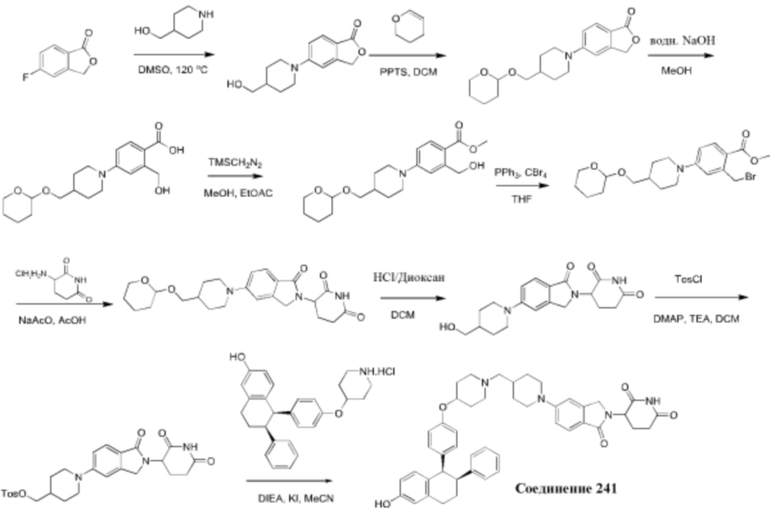
[582] Общая схема синтеза 3-39

[583] Общая схема синтеза 3-40

[584] Общая схема синтеза 3-41
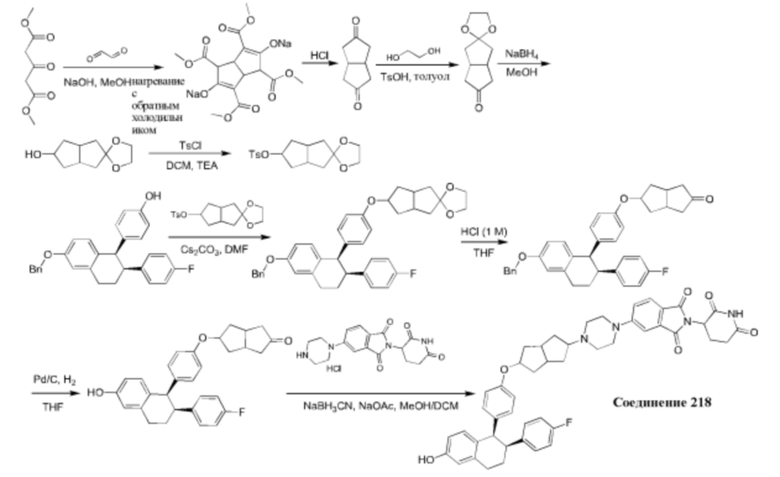
[585] Общая схема синтеза 3-42

[586] Общая схема синтеза 3-43

[587] Общая схема синтеза 3-44 для получения заявленных соединений

[588] Общая схема синтеза 3-45 для получения заявленных соединений

[589] Общая схема синтеза 3-46 для получения заявленных соединений

[590] Общая схема синтеза 3-47

[591] Общая схема синтеза 3-48

[592] Общая схема синтеза 3-49 для получения заявленных соединений

[593] Общая схема синтеза 3-50

[594] Общая схема синтеза 3-51
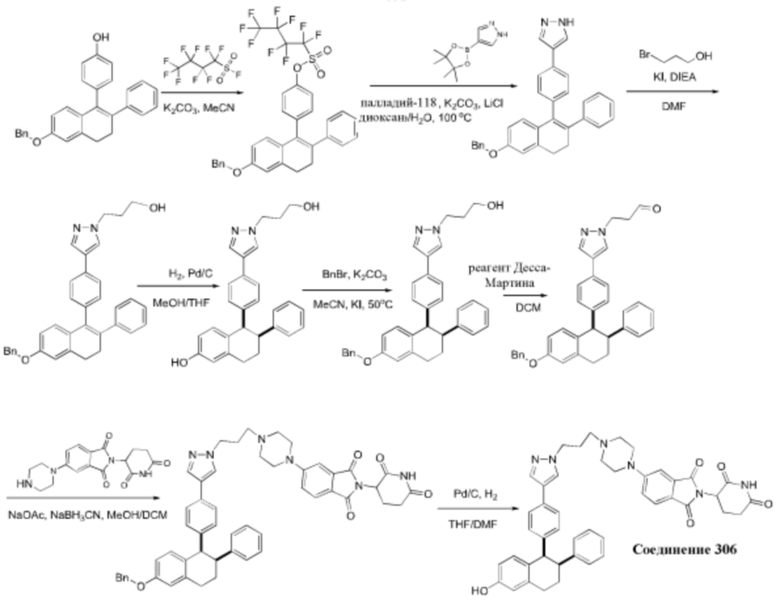
[595] Общая схема синтеза 3-52

[596] Общая схема синтеза 3-53

[597] Общая схема синтеза 3-54

[598] Общая схема синтеза 3-55
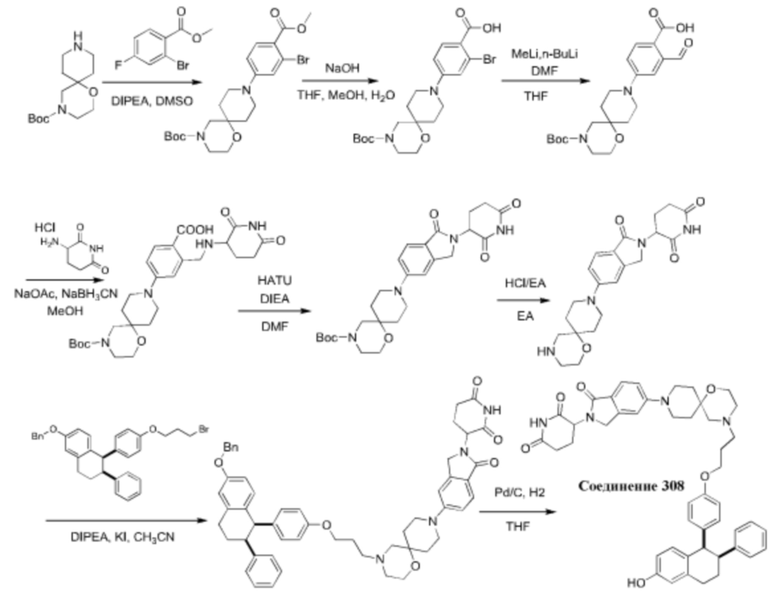
[599] Общая схема синтеза 3-57

[600] Общая схема синтеза 3-58
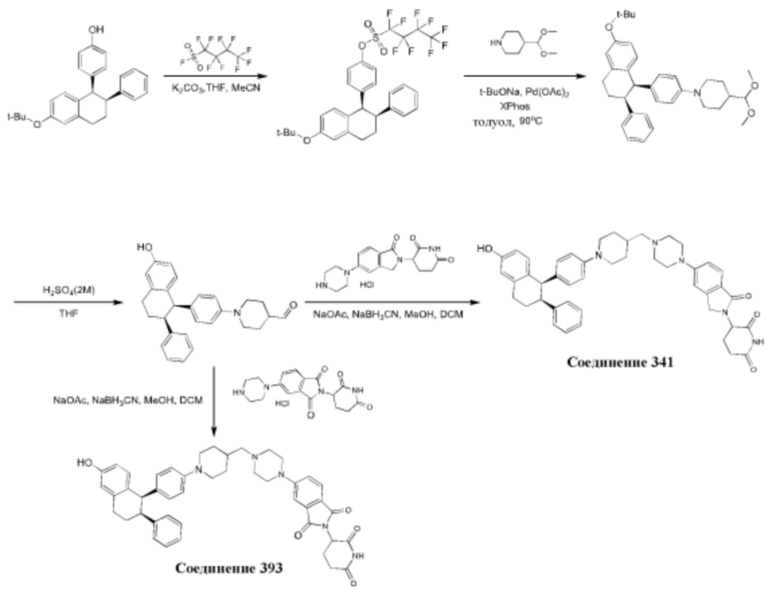
[601] Общая схема синтеза 3-59

[602] Общая схема синтеза 3-60

[603] Общая схема синтеза 3-61

[604] Общая схема синтеза 3-62

[605] Общая схема синтеза 3-63

[606] Общая схема синтеза 3-64

[607] Общая схема синтеза 3-65
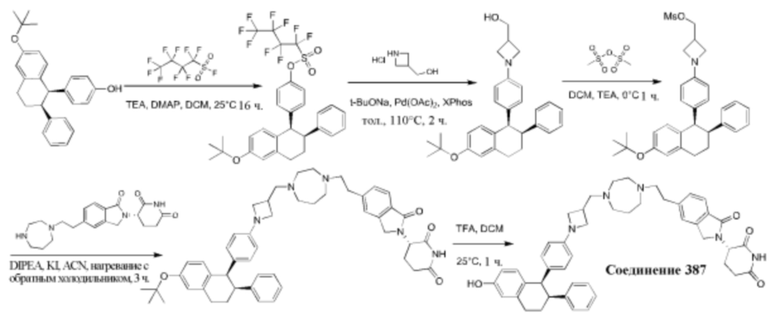
[608] Общая схема синтеза 3-66

[609] Общая схема синтеза 3-67

[610] Общая схема синтеза 3-68

[611] Общая схема синтеза 3-69

[612] Общая схема синтеза 3-70
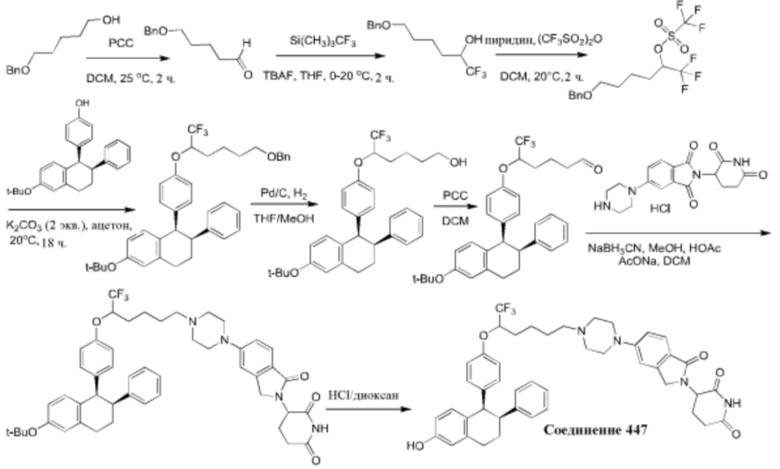
[613] Общая схема синтеза 3-71

[614] Общая схема синтеза 3-73

[615] Общая схема синтеза 3-74

[616] Общая схема синтеза 3-75
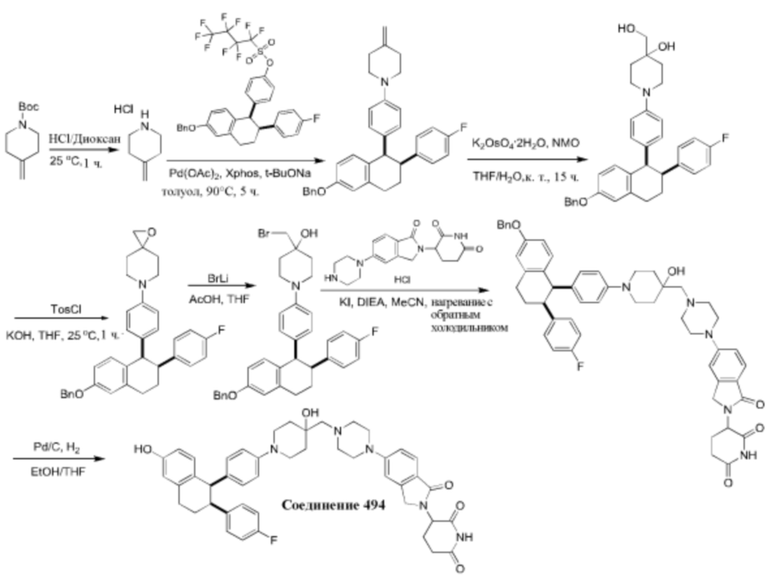
[617] Общая схема синтеза 3-76

[618] Общая схема синтеза 3-77

[619] Общая схема синтеза 3-78

[620] Общая схема синтеза 3-80

[621] Общая схема синтеза 3-81

[622] Общая схема синтеза 3-82


[623] Общая схема синтеза 3-83
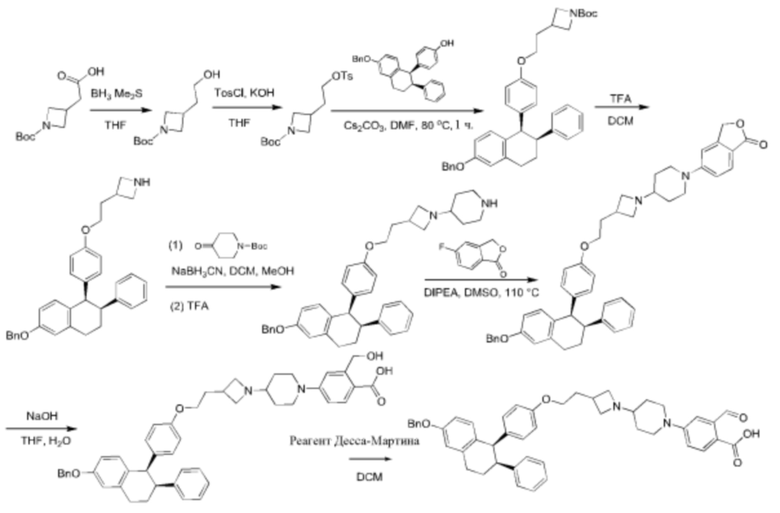

[624] Общая схема синтеза 3-84
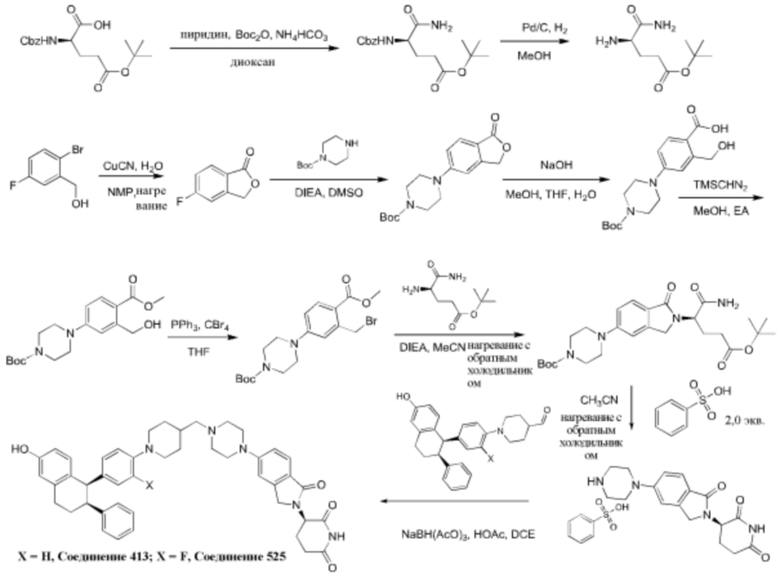
[625] Общая схема синтеза 3-85

[626] Общая схема синтеза 3-86

[627] Общая схема синтеза 3-87

[628] Общая схема синтеза 3-88

Примеры
[629] Характеристики всех синтезированных соединений определяли с помощью 1H-ЯМР и их чистоту анализировали с помощью LC/MS при длине волны 214 и 254 нм с УФ-детектированием. Чистота каждого соединения в таблице 1 и таблице 2 составляли более 90%. Обнаруженная молекулярную массу из LC/MS перечислена в таблице 1 (см. фигуру 5) и таблице 2 (см. фигуру 6) как [М+Н]+. Способы синтеза, применяемые для получения отдельных соединений, перечислены в таблице 1 и таблице 2. Некоторые молекулы в таблице 1 и таблице 2 получали в виде солевых форм, таких как гидрохлорид, ацетат, формиат или трифлат. Перечислены структуры только нейтральной формы каждого соединения. 1H-ЯМР иллюстративных соединений перечислены в таблице 3 (см. фигуру 7). Хотя химические названия, перечисленные в таблице 3, представлены для нейтральных форм иллюстративных соединений, соответствующие данные 1H-ЯМР предусматривают как нейтральные формы, так и солевые формы.
[630] Все синтезированные химерные молекулы оценивали в отношении связывания с мишенью в клетках T47D с применением коммерческого набора для анализа с применением репортерного гена ERE-люциферазы. В анализе включали 10% FBS и измерили, что уровень эстрогена, составлял 10 пМ. Связывание с мишенью выражали в виде IC50 в отношении супрессии индуцированного эстрогеном сигнала и результат перечислены в таблице 1 и таблице 2.
[631] Иллюстративные соединения по настоящему изобретению тестировали в отношении разрушения ERα в клетках MCF7 с применением анализа In-Cell Western™ (LI-COR®; Линкольн, Небраска). Активность в отношении разрушения перечислена в таблице 3 в виде DC50 и Dmax, где DC50 рассчитывали на основе аппроксимации кривой с применением модуля AC AS для кривой доза-ответ (McNeil & Со Inc.). Dmax рассчитывали на основе уравнения [(ERα самый высокий уровень - ERα самый низкий)/(ERα самый высокий уровень)].
[632] Иллюстративные соединения, которые демонстрировали активность в отношении разрушения, показанную в таблице 3, дополнительно тестировали в отношении разрушения ERα в клетках MCF7 с применением стандартной методики вестерн-блоттинга. На фигуре 2 и фигуре 3 проиллюстрированы результаты анализа иллюстративных соединений с помощью анализа посредством вестерн-блоттинга.
[633] Соединения, полученные в данной заявке, также анализировали в отношении их способности разрушать ERα в клетках MCF7 и T47D. На фигуре 4 показаны результаты разрушения для выбранных иллюстративных соединений.
[634] Анализ с применением ERE-люциферазы для оценивания связывания с мишенью для иллюстративных соединений. Клетки T47D-KBluc (АТСС № CRL_2865, T47D раковые клетки молочной железы человека, стабильно трансфицированные конструкцией эстрогенчувствительный элемент/промотор/ген-репортер люциферазы) высевали в 96-луночные белые непрозрачные планшеты в среде для роста RPMI, дополненной 10% фетальной бычьей сывороткой, и обеспечивали их адгезию в течение ночи в инкубаторе при 37°C с повышенной влажностью. На следующий день клетки обрабатывали PROTAC с применением 12-точечной кривой концентрации (максимальная конечная концентрация составляла 300 нМ с последующими концентрациями в 3 раза меньше, при этом самая низкая концентрация в анализе составляла 2 пМ). Каждый PROTAC тестировали независимо в двух экспериментах в 96-луночных планшетах. Через 24 часов среду удаляли и в лунки добавляли буфер для лизиса. После лизиса добавляли Bright-Glo™ субстрат для анализа с применением люциферазы (Promega, Мадисон, Висконсин) и измеряли активность люциферазы с применением планшет-ридера Cytation 3 (BioTek™, Винооски, Вермонт). Каждое соединение анализировали в двух повторностях и активность рассчитывали в виде IC50 с применением программного обеспечения GraphPad Prism (Сан Диего, Калифорния).
[635] Анализ разрушения эстрогенового рецептора-альфа (ERα) в клетках MCF-7 с применением способа вестерн-блоттинга Иллюстративные новые разрушители ERα оценивали в отношении их активности касательно разрушения ERα в клетках MCF-7 посредством вестерн-блоттинга. Анализ проводили в присутствии 10% фетальной бычьей сыворотки (FBS) или высокопроцентной человеческой или мышиной сыворотки.
[636] Анализ посредством вестерн-блоттинга, осуществляемый в отношении иллюстративных соединений по настоящему изобретению, проводили с помощью одного из двух следующих анализов, которые обеспечивали сравнимые результаты.
[637] Клетки MCF7 выращивали в DMEM/F12 с 10% фетальной бычьей сывороткой и высевали при плотности 24000 клеток на лунку в 100 мкл в 96-луночных прозрачных планшетах для культивирования тканей. На следующий день клетки обрабатывали PROTAC с применением 7-точечной кривой концентрации, при этом 100 нМ являлась максимальной концентрацией, и осуществляли последовательные разведения для получения других концентраций (30 нМ, 10 нМ, 3 нМ, 1 нМ и 0,3 нМ). При всех концентрация 0,01% DMSO является конечной концентрацией в лунке. На следующий день содержимое планшетов ас пир провал и, промывали с помощью 50 мкл холодного PBS. Клетки подвергали лизису с помощью 50 мкл/лунка буфера для лизиса клеток при 4°С (№по каталогу 9803; Cell Signaling Technology, Данверс, Массачусетс) (20 мМ Tris-HCL (рН 7,5), 150 мМ NaCl, 1 мМ Na2EDTA, 1 мМ EGTA, 1% Triton, 2,5 мМ пирофосфат натрия, 1 мМ В-глицерофосфат, 1 мМ ванадат натрия, 1 мкг/мл лейпептин). Лизаты осветляли при 16000 × g в течение 10 мину г и 2 мкг белка подвергали анализу SDS-PAGE и следующему иммуноблоттингу в соответствии со стандартными протоколами. Применяемые антитела представляли собой антитела к ERα (Cell Signaling Technologies. № по каталогу 8644) и тубулину (Sigma, № по каталогу Т9026; Сент-Луис, Миссури). Реагенты для детектирования представляли собой субстраты ECL Clarity для вестерн-блоттинга (Bio-Rad № по каталогу 170-5060; Геркулес, Калифорния).
[638] В качестве альтернативы, клетки MCF7 выращивали в DMEM/F12 с 10% фс тальмой бычьей сывороткой и высевал и при плотности 24000 клеток на лунку в 500 мкл в 24-луночных прозрачных планшетах для культивирования тканей. На следующий день клетки обрабатывали с помощью PROTAC с применением 5-точечной кривой концентрации (100 нМ, 33 нМ, 11 нМ, 3,7 нМ и 1,2 нМ) в присутствии 0.01% DM SO. Через 72 часа содержимое лунок аспирировали и промывали с помощью 500 мкл PBS. Клетки подвергали лизису с помощью 100 мкл/лунка буфера для лизиса клеток при 4°С (№ по каталогу 9803; Cell Signaling Technology, Данверс, Массачусетс) (20 мМ Tris-HCL (рН 7,5), 150 мМ NaCl, 1 мМ Na2EDTA, 1 мМ EGTA, 1% Triton, 2,5 мМ пирофосфат натрия. 1 м\1 В-глицерофосфат, 1 мМ ванадат натрия, 1 мкг/мл лейпептин). Лизаты осветляли при 16000 × g в течение 10 минут и 2 мкг белка подвергали анализу SDS-PAGE и следующему иммуноблоттингу в соответствии со стандартными протоколами. Применяемые антитела представляли собой антитела к ERα (Cell Signaling Technologies. №по каталогу 8644) и тубулину (Sigma, №по каталогу Т9026; Сент-Луис, Миссури). Реагенты для детектирования представляли собой еубе граты ECL Clarity для вестерн-блоттинга (Bio-Rad № по каталогу 170-5060; Геркулес, Калифорния)
[639] Анализ разрушения эстрогенового рецептора-альфа (ERα) в клетках T47D с применением способа вестерн-блоттинга Применяли тот же протокол, описанный выше в отношении клеток MCF7, за исключением того, что применяли клетки T47D вместо клеток MCF7.
[640] Анализ разрушения эстрогенового рецептора-альфа (ERα) с применением анализа In-Cell Western™ Разрушение ERg с помощью заявленных соединений определяли в клетках MCF7 с применением анализа In-Cell Western™. Вкратце, клетки MCF7 высевали в 96-луночных планшетах (2000 клеток на лунку в 100 мкл среды) и инкубировали при 37°С в атмосфере 5% СО2 в инкубаторе с повышенной влажностью в течение ночи. Сто (100) мкл среды, содержащей тестируемое соединение (при 2х концентрации), добавляли в подходящие лунки с обеспечением 11 серийно уменьшающихся концентраций (максимальная конечная концентрация 1 мкМ, затем в 3 раза меньше для следующих 10 концентраций); также добавляли для каждого соединения среду-носитель, представляющей собой контроль (DMSO). Для каждого эксперимента все соединения анализировали на планшетах в двух повторностях. Затем клетки инкубировали в течение 5 дней в вышеуказанной среде. Анализ завершали путем удаления среды, одного промывания с помощью ледяного PBS и добавления 50 мкл параформальдегида (PFA: 4% в PBS). Через 15 минут в PFA при комнатной температуре клетки подвергали пермеабилизации в Tris-фосфатно-солевом буферном растворе с Tween (0,1%) (TBST), дополненном Triton Х-100 (0,5%), в течение 15 минут. Затем клетки блокировали в BSA (TBST с BSA, 3%) в течение одного часа. Добавляли первичные антитела для обнаружения ERg (моноклональное антитело кролика, 1:1000, Cell Signaling Technology, №по каталогу 8644) и тубулина (моноклональное антитело мыши, 1:5000, Sigma № по каталогу Т6074) в TBST с BSA (3%). Клетки инкубировали в течение ночи при 4°С.Затем клетки дважды промывали с помощью TBST при комнатной температуре и затем инкубировали с флуоресцентно-мечеными вторичными антителами к Ig кролика и Ig мыши (IRDye®; LI-COR; Линкольн, Небраска) в блокирующем буферу LI-COR (№по каталогу 927-50000) в течение одного часа при комнатной температуре. После 3 промываний с помощью TBST буфер удаляли и планшеты считывали на инфракрасной системе визуализации Odyssey® (LI-COR®; Линкольн, Небраска) при 700 нм и 800 нм. С применением коммерческого программного обеспечения (ImageStudio™; LI-COR, Линкольн, Небраска) количественно определяли интенсивность окрашивания для ERα и тубулина в каждой лунке и экспортировали для анализа. Для каждой точки данных интенсивность для ERα нормализовали относительно интенсивности для тубулина, и для каждого соединения все нормализированные 3Начения интенсивности нормализовали относительно среды-носителя, представляющей собой контроль. 3Начения DC50 и Dmax определяли после 4-параметрической аппроксимации кривой IC50 с применением модуля ACAS для кривой доза-ответ (McNeil & Со Inc.).
[641] Данные касательно разрушения делили на категории следующим образом: диапазоны DC50 касательно разрушения: DC50 < 5 нМ (А); 5 нМ < DC50 < 50 нМ (В); DC50 > 50 нМ (С), и диапазоны Dmax касательно разрушения: Dmax > 75% (А); 50% < Dmax < 75 (В); Dmax < 50% (С). Активность в отношении разрушения иллюстративных соединений перечислена в таблице 3.
[642] Экспериментальные процедуры для синтеза PROTAC, целенаправленно воздействующих на ER
[643] Синтез (2S,4R)-4-гидрокси-1-[(2S)-2-(2-{2-[4-(2-{4-[(1R,2S)-6-гидрокси-2-фенил-1,2,3,4-тетрагидронафталин-1-ил]фенокси}этил)пиперазин-1-ил]этокси}ацетамидо)-3,3-диметилбутаноил]-N-{[4-(4-метил-1,3-тиазол-5-ил)фенил]метил}пирролидин-2-карбоксамила (иллюстративное соединение 1)
[644] Стадия 1. Получение трет-бутил-4-(2-(2-этокси-2-оксоэтокси)этил)пиперазин-1-карбоксилата

[645] К раствору трет-бутилпиперазин-1-карбоксилата (1,50 г, 8,05 ммоль, 1,00 экв.) в N,N-диметилформамиде (30 мл) добавляли карбонат цезия (2,89 г, 8,86 ммоль, 1,10 экв.), йодид калия (134 мг, 0,8 ммоль, 0,10 экв.) и этил-2-(2-хлорэтокси)ацетат (1,68 г, 10,06 ммоль, 1,25 экв.) при 25°С. Полученную смесь перемешивали при 110°С в течение 16 часов. С помощью LC/MS показывали исчезновение исходного вещества, и необходимое соединение образовалось. Смесь выливали в насыщенный солевой раствор (100 мл) и затем экстрагировали этилацетатом (50 мл × 5). Объединенные органические слои высушивали над безводным сульфатом натрия, фильтровали и концентрировали в вакууме. Остаток дополнительно очищали с помощью колоночной хроматографии на силикагеле (петролейный эфир : этилацетат = от 15:1 до 5:1) с получением трет-бутил-4-[2-(2-этокси-2-оксо-этокси)этил]пиперазин-1-карбоксилата (2,40 г, 2,91 ммоль, выход 36%, чистота 38%) в виде бесцветного масла. LC/MS (ESI) масса/заряд: 317,1 [М+1]+.
[646] Стадия 2. Получение 2-(2-(4-(трет-бутоксикарбонил)пиперазин-1-ил)этокси)уксусной кислоты
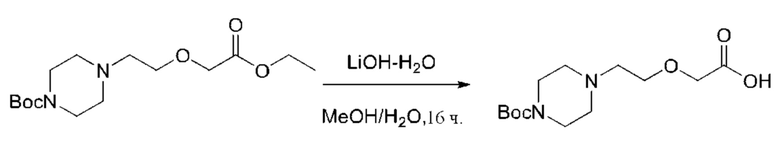
[647] К раствору трет-бутил-4-[2-(2-этокси-2-оксоэтокси)этил]пиперазин-1-карбоксилата (750 мг, 2,37 ммоль, 1,00 экв.) в метаноле (5 мл) и воде (5 мл) добавляли моногидрат гидроксида лития (497 мг, 11,85 ммоль, 5,00 экв.) при 25°С. Полученную смесь перемешивали при 25°С в течение 16 часов. С помощью LC/MS показывали, что исходное вещество исчезло, и необходимое соединение было обнаружено. Затем реакционную смесь регулировали до рН=(5~6) с помощью хлористоводородной кислоты (2 М, 0,5 мл) и концентрировали при пониженном давлении с удалением метанола. Остаток экстрагировали этилацетатом (3 мл × 2). Объединенные органические слои промывали насыщенным солевым раствором (3 мл × 2), высушивали над безводным сульфатом натрия, фильтровали и концентрировали в вакууме. Получали 2-[2-(4-трет-бутоксикарбонилпиперазин-1-ил)этокси]уксусную кислоту (350 мг, 1,21 ммоль, выход 51%) в виде бесцветного масла, которое непосредственно применяли для следующей стадии без дополнительной очистки. 1Н ЯМР (400 МГц, CDCl3) δ: 6,50 (br, 1H), 4,02 (s, 2Н), 3,78 (t, J=4,8 Гц, 2Н), 3,65-3,62 (m, 4Н), 3,47-3,38 (m, 2Н), 2,82-2,79 (m, 4Н), 1,46 (s, 9Н).
[648] Стадия 3. Получение трет-бутил-4-[2-({[(2S)-1-[(2S,4R)-4-гидрокси-2-({[4-(4-метил-1,3-тиазол-5-ил)фенил]метил}карбамоил)пирролидин-1-ил]-3,3-диметил-1-оксобутан-2-ил]карбамоил}метокси)этил]пиперазин-1-карбоксилата
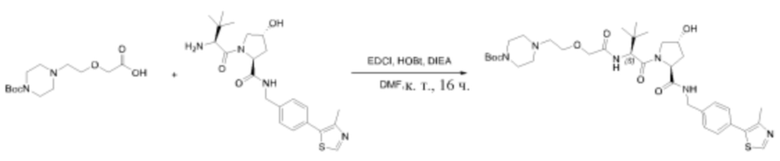
[649] К раствору 2-[2-(4-трет-бутоксикарбонилпиперазин-1-ил)этокси]уксусной кислоты (170 мг, 0,59 ммоль, 1,00 экв.) в N,N-диметилформамиде (6 мл) добавляли гидрохлорид 1-этил-3-(3-диметиламинопропил)карбодиимида (226 мг, 1,18 ммоль, 2,00 экв.), 1-гидроксибензотриазол (119 мг, 0,88 ммоль, 1,50 экв.), диизопропилэтиламин (228 мг, 1,77 ммоль, 3,00 экв.) и гидрохлорид (2S,4R)-1-[(2S)-2-амино-3,3-диметилбутаноил]-4-гидрокси-N-[[4-(4-метилтиазол-5-ил)фенил]метил]пирролидин-2-карбоксамида (275 мг, 0,59 ммоль, 1,00 экв.) при 25°С. Полученную смесь перемешивали при 25°С в течение 16 часов. С помощью LC/MS показывали исчезновение исходного вещества, и необходимое соединение было обнаружено. Смесь выливали в насыщенный солевой раствор (30 мл) и затем экстрагировали этилацетатом (15 мл × 5). Объединенные органические слои высушивали над безводным сульфатом натрия, фильтровали и концентрировали в вакууме. Остаток дополнительно очищали с помощью препаративной TLC (SiO2, дихлорметан : метанол = 10:1) с получением трет-бутил-4-[2-({[(2S)-1-[(2S,4R)-4-гидрокси-2-({[4-(4-метил-1,3-тиазол-5-ил)фенил]метил}карбамоил)пирролидин-1-ил]-3,3-диметил-1-оксобутан-2-ил]карбамоил}метокси)этил]пиперазин-1-карбоксилата (320 мг, 0,45 ммоль, выход 77%, чистота 99%) в виде бесцветного масла. LC/MS (ESI) масса/заряд: 701,2 [М+1]+; 1Н ЯМР (400 МГц, CDCl3) δ: 8,84 (s, 1H), 7,42-7,39 (m, 5Н), 4,54-4,51 (m, 4Н), 4,34 (m, 1H), 4,05-3,96 (m, 2Н), 3,76-3,70 (m, 2Н), 3,67-3,60 (m, 2Н), 3,41-3,35 (m, 4Н), 2,72-2,66 (m, 2Н), 2,57-2,55 (m, 4Н), 2,53 (s, 3Н), 2,27-2,19 (m, 1H), 2,13-2,05 (m, 1H), 1,38 (s, 9Н), 1,00 (s, 9Н).
[650] Стадия 4. Получение (2S,4R)-1-[(2S)-3,3-диметил-2-{2-[2-(пиперазин-1-ил)этокси]ацетамидо}бутаноил]-4-гидрокси-N-{[4-(4-метил-1,3-тиазол-5-ил)фенил]метил}пирролидин-2-карбоксамида

[651] К раствору трет-бутил-4-[2-({[(2S)-1-[(2S,4R)-4-гидрокси-2-({[4-(4-метил-1,3-тиазол-5-ил)фенил]метил}карбамоил)пирролидин-1-ил]-3,3-диметил-1-оксобутан-2-ил]карбамоил}метокси)этил]пиперазин- 1-карбоксилата (110 мг, 0,16 ммоль, 1,00 экв.) в этилацетате (3 мл) добавляли хлористоводородную кислоту/этилацетат (4,0 М, 3 мл) при 25°С. Полученную смесь перемешивали при 25°С в течение 0,5 часа. С помощью LC/MS показывали исчезновение исходного вещества, и необходимое соединение было обнаружено. Смесь концентрировали при пониженном давлении. Получали гидрохлорид (2S,4R)-1-[(2S)-3,3-диметил-2-[[2-(2-пиперазин-1-илэтокси)ацетил] амино]бутаноил]-4-гидрокси-N-[[4-(4-метилтиазол-5-ил)фенил]метил]пирролидин-2-карбоксамида (100 мг, 0,12 ммоль, выход 77%, чистота 77%) в виде желтого твердого вещества. LC/MS (ESI) масса/заряд: 601,2 [М+1]+; 1H ЯМР (400 МГц, МЕТАНОЛ-d4) δ: 7,56-7,50 (m, 5Н), 4,63-4,51 (m, 5Н), 4,45-4,38 (m, 1H), 4,24 (s, 2Н), 3,99-3,91 (m, 4Н), 3,84-3,78 (m, 2Н), 3,71-3,61 (m, 4Н), 3,56-3,50 (m, 2Н), 2,57 (m, 4Н), 2,32-2,24 (m, 1H), 2,15-2,04 (m, 1H), 1,07 (s, 9Н).
[652] Стадия 5. Получение 7-бензилокси-4-[4-(2,2-диэтоксиэтокси)фенил]-1,2-дигидронафталина
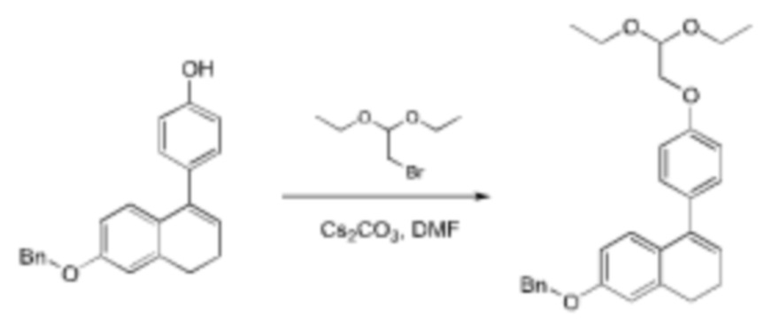
[653] К раствору 4-(6-бензилокси-3,4-дигидронафталин-1-ил)фенола (22 г, 66,99 ммоль, 1,00 же., полученного в соответствии с процедурами на стадии 1-3, описанными для иллюстративного соединения 62) в N,N-диметилформамиде (200 мл) добавляли карбонат цезия (43,65 г, 133,98 ммоль, 2,00 экв.) и 2-бром-1,1-диэтоксиэтан (26,4 г, 133,98 ммоль, 20 мл, 2,00 экв.). Реакционную смесь перемешивали при 100°С в течение 2 часов. С помощью TLC (петролейный эфир : этилацетат = 10:1) показывали, что большая часть исходного вещества была израсходована. К смеси добавляли этилацетат (600 мл) и воду (300 мл). Органическую фазу отделяли. Объединенную органическую фазу промывали солевым раствором (300 мл × 3), высушивали над сульфатом натрия, фильтровали и концентрировали в вакууме. Остаток очищали с помощью хроматографии на силикагеле (петролейный эфир : этилацетат = от 1:0 до 25:1) с получением 7-бензилокси-4-[4-(2,2-диэтоксиэтокси)фенил]-1,2-дигидронафталина (21 г, 47,24 ммоль, выход 70%) в виде желтого масла. 1H-ЯМР (400 МГц, CDCl3) δ 7,46-7,31 (m, 5Н), 7,29-7,24 (m, 2Н), 6,96-6,91 (m, 3Н), 6,86 (d, J=2,4 Гц, 1H), 6,71 (dd, J=8,4, 2,8 Гц, 1H), 5,92 (t, J=4,8 Гц, 1H), 5,07 (s, 2Н), 4,88 (t, J=5,2 Гц, 1H), 4,05 (d, J=5,2 Гц, 2Н), 2,83-3,76 (m, 2Н), 3,71-3,63 (m, 2Н), 2,82 (t, J=8,0 Гц, 2Н), 2,40-2,35 (m, 2Н), 1,28 (t, J=6,8 Гц, 6Н).
[654] Стадия 6. Получение 7-(бензилокси)-3-бром-4-(4-(2,2-диэтоксиэтокси)фенил)-1,2-дигидронафталина

[655] К раствору 7-бензилокси-4-[4-(2,2-диэтоксиэтокси)фенил]-1,2-дигидронафталина (20 г, 44,99 ммоль, 1,00 экв.) в ацетонитриле (480 мл) добавляли N-бромсукцинимид (8,41 г, 47,24 ммоль, 1,05 экв.). Реакционную смесь перемешивали при 20°С в течение 3 часов. С помощью TLC (петролейный эфир : этилацетат = 10:1) и LC/MS показывали, что необходимый продукт образовался. К смеси добавляли насыщенный раствор бикарбоната натрия (500 мл), полученную смесь экстрагировали этилацетатом (400 мл × 3). Объединенную органическую фазу промывали солевым раствором (80 мл), высушивали над сульфатом натрия, фильтровали и концентрировали в вакууме. Остаток очищали с помощью хроматографии на силикагеле (петролейный эфир : этилацетат = от 1:0 до 30:1) с получением 7-(бензилокси)-3-бром-4-(4-(2,2-диэтоксиэтокси)фенил)-1,2-дигидронафталина (12,4 г, 23,69 ммоль, выход 53%) в виде светло-желтого твердого вещества. LC/MS (ESI) масса/заряд: 545,2, 547,2 [М+23, М+25]+; 1H-ЯМР (400 МГц, CDCl3) δ 7,44-7,31 (m, 5Н), 7,16-7,13 (m, 2Н), 7,01-6,97 (m, 2Н), 6,80 (d, J=2,4 Гц, 1H), 6,63 (dd, J=8,4, 2,8 Гц, 1H), 6,59 (t, J=8,8 Гц, 1H), 5,04 (s, 2Н), 4,89 (t, J=5,2 Гц, 1H), 4,07 (d, J=5,2 Гц, 2Н), 3,83-3,77 (m, 2Н), 3,72-3,66 (m, 2Н), 3,02-2,93(m, 4Н), 1,28 (t, J=6,8 Гц, 6Н).
[656] Стадия 7. Получение 7-бензилокси-4-[4-(2,2-диэтоксиэтокси)фенил]-3-фенил-1,2-дигидронафталина

[657] К раствору 7-бензилокси-3-бром-4-[4-(2,2-диэтоксиэтокси)фенил]-1,2-дигидронафталина (12,4 г, 23,69 ммоль, 1,00 экв.), фенилбороновой кислоты (2,89 г, 23,69 ммоль, 1,00 экв.) в диоксане (100 мл) и воде (20 мл) добавляли карбонат калия (6,55 г, 47,38 ммоль, 2,00 экв.) и дихлорид (1,1'-бис(дифенилфосфино)ферроцен)палладия(II) (1,73 г, 2,37 ммоль, 0,10 экв.) в атмосфере азота. Реакционную смесь перемешивали при 100°С в течение 3 часов. С помощью LC/MS показывали, что большая часть исходного вещества была израсходована. К смеси добавляли воду (300 мл), полученную смесь экстрагировали этилацетатом (150 мл × 3). Объединенную органическую фазу промывали солевым раствором (200 мл × 2), высушивали над сульфатом натрия, фильтровали и концентрировали в вакууме. Остаток очищали с помощью хроматографии на силикагеле (петролейный эфир : этилацетат = от 1:0 до 30:1) с получением 7-бензилокси-4-[4-(2,2-диэтоксиэтокси)фенил]-3-фенил-1,2-дигидронафталина (10,4 г, 19,97 ммоль, выход 84%) в виде белого твердого вещества. LC/MS (ESI) масса/заряд: 521,3 [М+1]+; 1H ЯМР (400 МГц, CDCl3) δ 7,46-7,32 (m, 5Н), 7,14-6,95 (m, 7Н), 6,87 (d, J=2,4 Гц, 1H), 6,79 (d, J=8,8 Гц, 2Н), 6,72 (d, J=8,4 Гц, 1H), 6,67 (dd, J=8,4, 2,8 Гц, 1H), 5,08 (s, 2Н), 4,83 (t, J=5,2 Гц, 1H), 3,99 (d, J=5,2 Гц, 2Н), 3,82-3,74 (m, 2Н), 3,67-3,63 (m, 2Н), 2,97-2,93 (m, 2Н), 2,81-2,77 (m, 2Н), 1,26 (t, J=6,8 Гц, 6Н).
[658] Стадия 8. Получение 5,6-цис-5-(4-(2,2-диэтоксиэтокси)фенил)-6-фенил-5,6,7,8-тетрагидронафталин-2-ола

[659] К раствору 7-бензилокси-4-[4-(2,2-диэтоксиэтокси)фенил]-3-фенил-1,2-дигидронафталина (4 г, 7,68 ммоль, 1,00 экв.) в этиловом спирте (150 мл) и тетрагидрофуране (30 мл) добавляли палладий/уголь (400 мг, 10% Pd) в атмосфере азота. Реакционную смесь перемешивали при 20°С в атмосфере водорода (50 фунтов/кв. дюйм) в течение 24 часов. С помощью TLC (петролейный эфир : этилацетат = 3:1) и LC/MS обнаружили, что большая часть исходного вещества была израсходована. Смесь фильтровали и фильтрат концентрировали в вакууме с получением 5,6-цис-5-(4-(2,2-диэтоксиэтокси)фенил)-6-фенил-5,6,7,8-тетрагидронафталин-2-ола (3,3 г, 7,09 ммоль, выход 92%, чистота 93%) в виде желтого масла. LC/MS (ESI) масса/заряд: 455,3 [М+23]+; 1H-ЯМР (400 МГц, CDCl3) δ 7,19-7,12 (m, 3Н), 6,83-6,79 (m, 3Н), 6,71 (d, J=8,4 Гц, 1H), 6,59-6,53 (m, 3Н), 6,31 (d, J=8,4 Гц, 2Н), 4,81-4,77 (m, 2Н), 4,23 (d, J=4,8 Гц, 1H), 3,90 (dd, J=4,8, 1,6 Гц, 2Н), 3,78-3,71 (m, 2Н), 3,65-3,58 (m, 2Н), 3,38-3,33 (m, 1H), 3,10-2,96 (m, 2Н), 2,23-2,16 (m, 1H), 1,84-1,79 (m, 1H), 1,24 (t, J=6,8 Гц, 6Н).
[660] Стадия 9. Получение (1R,2S)-1-[4-(2,2-диэтоксиэтокси)фенил]-2-фенилтетралин-6-ола
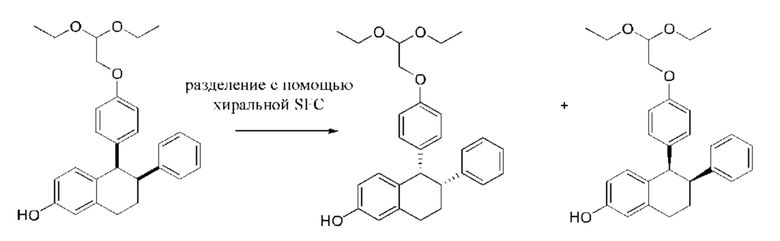
[661] 1,2-цис-1-[4-(2,2-Диэтоксиэтокси)фенил]-2-фенилтетралин-6-ол (6,6 г, 15,26 ммоль, 1,00 экв.) очищали с помощью SFC с применением хиральной колонки (колонка: AD, 250 мм × 30 мм, 10 мкм; подвижная фаза: 0,1% гидроксид аммония в метаноле; B%: 25%-25%, 3,5 мин.). Получали (1S,2R)-1-[4-(2,2-диэтоксиэтокси)фенил]-2-фенилтетралин-6-ол (2,5 г, 5,18 ммоль, выход 68%) в виде первой фракции и получали (1R,2S)-1-[4-(2,2-диэтоксиэтокси)фенил]-2-фенилтетралин-6-ол (2,5 г, 5,18 ммоль, выход 68%) в виде второй фракции. Обе фракции представляли собой светло-желтое масло.
[662] Стадия 10. Получение 2-[4-[(1R,2S)-6-гидрокси-2-фенилтетралин-1-ил]фенокси]ацетальдегида

[663] К раствору (1R,28)-1-[4-(2,2-диэтоксиэтокси)фенил]-2-фенилтетралин-6-ола (1,5 г, 3,47 ммоль, 1,00 экв.) в тетрагидрофуране (70 мл) добавляли раствор серной кислоты (2 М, 70 мл, 40,00 экв.). Реакционную смесь перемешивали при 70°С в течение 2 часов. С помощью TLC (петролейный эфир : этилацетат = 1:1) показывали, что большая часть исходного вещества была израсходована. К смеси добавляли воду (100 мл), полученную смесь экстрагировали этилацетатом (100 мл × 3). Объединенную органическую фазу промывали солевым раствором (100 мл × 2), высушивали над сульфатом натрия, фильтровали и концентрировали в вакууме с получением 2-[4-[(1R,2S)-6-гидрокси-2-фенилтетралин-1-ил]фенокси]ацетальдегида (1,17 г, 3,26 ммоль, выход 94%) в виде светло-желтого твердого вещества.
[664] Стадия 11. Получение (2S,4R)-4-гидрокси-1-[(2S)-2-(2-{2-[4-(2-{4-[(1R,2S)-6-гидрокси-2-фенил-1,2,3,4-тетрагидронафталин-1-ил]фенокси}этил)пиперазин-1-ил]этокси}ацетамидо)-3,3-диметилбутаноил]-N-{[4-(4-метил-1,3-тиазол-5-ил)фенил]метил}пирролидин-2-карбоксамида (иллюстративное соединение 1)

[665] К раствору гидрохлорида (2S,4R)-1-[(2S)-3,3-диметил-2-[[2-(2-пиперазин-1-илэтокси)ацетил]амино]бутаноил]-4-гидрокси-N-[[4-(4-метилтиазол-5-ил)фенил]метил]пирролидин-2-карбоксамида (45 мг, 0,07 ммоль, 1,00 экв.) в дихлорметане (3 мл) и метаноле (1,5 мл) добавляли ацетат натрия (12 мг, 0,14 ммоль, 2,00 экв.) при 25°С. Смесь перемешивали в течение получаса и затем добавляли 2-[4-[(1R,2S)-6-гидрокси-2-фенилтетралин-1-ил]фенокси]ацетальдегид (28 мг, 0,08 ммоль, 1,10 экв.) с последующим добавлением цианоборгидрида натрия (9 мг, 141 мкмоль, 2,00 экв.). Полученную смесь перемешивали при 25°С в течение 16 часов. С помощью LC/MS показывали практически полное исчезновение исходного вещества, и необходимое соединение было обнаружено. Смесь концентрировали в вакууме. Остаток добавляли в насыщенный солевой раствор (10 мл) и затем экстрагировали дихлорметаном (10 мл × 5). Объединенные органические слои высушивали над безводным сульфатом натрия, фильтровали и концентрировали в вакууме. Остаток дополнительно очищали с помощью препаративной TLC (SiO2, дихлорметан : метанол = 10:1) с получением (2S,4R)-4-гидрокси-1-[(2S)-2-[[2-[2-[4-[2-[4-[(1R,2S)-6-гидрокси-2-фенилтетралин-1-ил]фенокси]этил]пиперазин-1-ил]этокси]ацетил]амино]-3,3-диметил-бутаноил]-N-[[4-(4-метилтиазол-5-ил)фенил]метил]пирролидин-2-карбоксамида (8 мг, 0,009 ммоль, выход 12%, чистота 98%) в виде белого твердого вещества. LC/MS (ESI) масса/заряд: 943,1 [М+1]+; 1Н ЯМР (400 МГц, DMSO-d6) δ: 9,36-9,10 (br, 1H), 8,95 (s, 1H), 8,60 (t, J=5,6 Гц, 1H), 7,39 (m, 5Н), 7,16-7,12 (m, 3Н), 6,82 (d, J=7,2 Гц, 2Н), 6,64-6,61 (m, 2Н), 6,51-6,34 (m, 3Н), 6,26-6,24 (m, 2Н), 5,25-5,10 (m, 1H), 4,59-4,51 (m, 1H), 4,48-4,32 (m, 3Н), 4,29-4,15 (m, 2Н), 3,80-3,70 (m, 4Н), 3,63-3,55 (m, 3Н), 3,34-3,26 (m, 8Н), 3,05-2,84 (m, 2Н), 2,48-2,43 (m, 9Н), 2,11-2,01 (m, 2Н), 1,95-1,85 (m, 1H), 1,75-1,65 (m, 1H), 0,93 (s, 9Н).
[666] Синтез (2S,4R)-4-гидрокси-1-[(2S)-2-{2-[2-(4-{2-[4-(6-гидрокси-2-фенил-1,2,3,4-тетрагидроизохинолин-1-ил)фенокси]этил}пиперазин-1-ил)этокси]ацетамидо}-3,3-диметилбутаноил]-N-[(1S)-1-[4-(4-метил-1,3-тиазол-5-ил)фенил]этил]пирролидин- 2-карбоксамида (иллюстративное соединение 6)
[667] Стадия 1. Получение 2-(3-бензилоксифенил)уксусной кислоты

[668] К раствору 2-(3-гидроксифенил)уксусной кислоты (20 г, 131,45 ммоль, 1,00 экв.) в этаноле (300 мл) добавляли гидроксид калия (18,44 г, 328,62 ммоль, 2,50 экв.), йодид натрия (492 мг, 3,29 ммоль, 0,03 экв.) и бромметилбензол (23,61 г, 138,02 ммоль, 1,05 экв.). Полученную смесь перемешивали при 90°С в течение 16 часов. LCMS указывала на завершение реакции. Реакционную смесь концентрировали с удалением растворителя. Остаток разбавляли водой (100 мл) и нейтрализовали концентрированной хлористоводородной кислотой до рН=3, затем фильтровали и собирали твердое вещество. Необходимый продукт, 2-(3-бензилоксифенил)уксусную кислоту (16 г, 66,04 ммоль, выход 50%), получали в виде белого твердого вещества. 1Н-ЯМР (400 МГц, DMSO-d6) δ 7,47-7,35 (m, 5Н), 7,23 (t, J=7,8 Гц, 1H), 6,92-6,83 (m, 3Н), 5,08 (s, 2Н), 3,54 9S, 2Н).
[669] Стадия 2. Получение 4-аллилоксибензойной кислоты
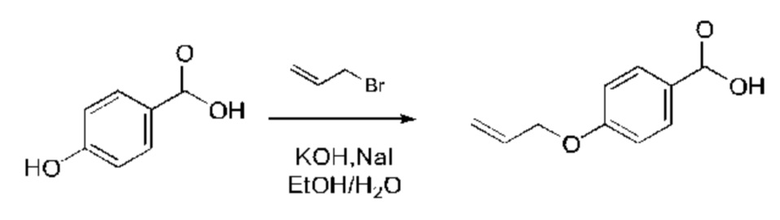
[670] 4-Гидроксибензойную кислоту (14 г, 101,36 ммоль, 1,00 экв.) растворяли в этаноле (200 мл), затем добавляли водный раствор (50 мл), содержащий гидроксид калия (14,22 г, 253,40 ммоль, 2,50 экв.) и йодид натрия (456 мг, 3,04 ммоль, 0,03 экв.), при 20°С и смесь перемешивали при 20°С в течение 2 часов. Затем добавляли по каплям 3-бромпроп-1-ен (12,88 г, 106,43 ммоль, 1,05 экв.). Полученную смесь перемешивали при 90°С в течение 16 часов. Необходимый продукт определяли с помощью LC/MS. Реакционную смесь концентрировали с удалением этанола, остаток нейтрализовали концентрированной хлористоводородной кислотой до рН около 3, и затем экстрагировали этилацетатом (300 мл × 2), объединенную органическую фазу промывали солевым раствором (100 мл), высушивали над сульфатом натрия и концентрировали. Остаток очищали с помощью колоночной хроматографии на силикагеле (дихлорметан : метанол = от 1:0 до 30:1). Получали необходимый продукт, 4-аллилоксибензойную кислоту (6 г, 33,67 ммоль, выход 33%), в виде белого твердого вещества. LC/MS (ESI) масса/заряд: 179,0 [М+1]+; 1H ЯМР (400 МГц, DMSO-d6) δ 12,65 (br, 1H), 7,89 (d, J=8,8 Гц, 2H), 7,03 (d, J=8,8 Гц, 2H), 6,10-6,00 (m, 1H), 5,43 (d, J=17,2, 1,2 Гц, 1H), 5,28 (dd, J=10,4, 1,2 Гц, 1H), 4,64 (d, J=5,2 Гц, 2H).
[671] Стадия 3. Получение 2-[3-(бензилокси)фенил]-N-фенилацетамида
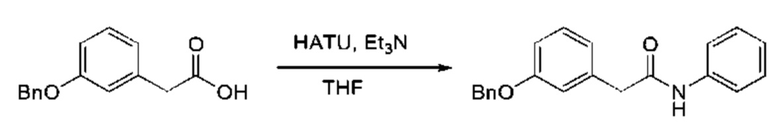
[672] К раствору 2-(3-бензилоксифенил)уксусной кислоты (16 г, 66,04 ммоль, 1,00 экв.) в тетрагидрофуране (200 мл) добавляли анилин (6,77 г, 72,64 ммоль, 6,64 мл, 1,10 экв.), HATU (30,13 г, 79,25 ммоль, 1,20 экв.) и триэтиламин (13,37 г, 132,08 ммоль, 18 мл, 2,00 экв.). Полученную смесь перемешивали при 20°С в течение 1 часа. TLC (петролейный эфир : этилацетат = 3:1) указывала на завершение реакции. Реакционную смесь концентрировали. Остаток растворяли в этилацетате (500 мл), промывали 1 н. хлористоводородной кислотой (100 мл), солевым раствором (200 мл), высушивали над сульфатом натрия и затем концентрировали. Остаток растирали со смесью петролейный эфир : этилацетат = 3:1 (200 мл) и затем фильтровали. Получали необходимый продукт, 2-(3-бензилоксифенил)-N-фенилацетамид (19,50 г, 59,47 ммоль, выход 90%, чистота 97%), в виде белого твердого вещества. LC/MS (ESI) масса/заряд: 318,0 [М+1]+.
[673] Стадия 4. Получение N-[2-(3-бензилоксифенил)этил]анилина

[674] К раствору 2-(3-бензилоксифенил)-N-фенилацетамида (12 г, 37,81 ммоль, 1,00 экв.) в тетрагидрофуране (200 мл) добавляли по каплям алюмогидрид лития (2,15 г, 56,72 ммоль, 1,50 экв.) при 0°С. Полученную смесь перемешивали при 0°С в течение дополнительных 2 часов. TLC (петролейный эфир : этилацетат = 3:1) указывала на завершение реакции. Затем добавляли 2 мл воды и 2 мл 15% водного раствора гидроксида натрия с гашением реакции, полученную смесь перемешивали в течение дополнительных 30 минут, затем фильтровали и осадок на фильтре дополнительно промывали этилацетатом (500 мл). Фильтрат концентрировали. Остаток очищали с помощью колоночной хроматографии на силикагеле (петролейный эфир : этилацетат = от 20:1 до 10:1). Получали необходимый продукт, N-[2-(3-бензилоксифенил)этил]анилин (6 г, 19,78 ммоль, выход 52%), в виде желтого масла. 1Н-ЯМР (400 МГц, CDCl3) δ 7,48-7,34 (m, 5Н),7,28-7,19 (m, 3Н), 6,90-6,88 (m, 3Н), 6,74 (t, J=7,2 Гц, 1H), 6,64 (dd, J=8,4, 0,8 Гц, 2Н), 5,09 (s, 2Н), 3,71 (br, 1H), 3,43 (t, J=7,2 Гц, 2Н), 2,92 (t, J=7,2 Гц, 2Н).
[675] Стадия 5. Получение 4-(аллилокси)-N-(3-(бензилокси)фенэтил)-N-фенилбензамида

[676] К раствору 4-аллилоксибензойной кислоты (4,58 г, 25,71 ммоль, 1,30 экв.) в дихлорметане (200 мл) добавляли оксалилдихлорид (5,02 г, 39,56 ммоль, 3,46 мл, 2,00 экв.). Полученную смесь перемешивали при 20°С в течение 2 часов. Затем смесь концентрировали с удалением растворителя. Остаток растворяли в толуоле (100 мл) и добавляли N-[2-(3-бензилоксифенил)этил]анилин (6 г, 19,78 ммоль, 1,00 экв.) и карбонат натрия (6,29 г, 59,34 ммоль, 3,00 экв.). Полученную смесь перемешивали при 100°С в течение 2 часов. TLC (петролейный эфир : этилацетат = 3:1) указывала на завершение реакции. Реакционную смесь фильтровали с удалением неорганического основания, фильтрат концентрировали. Остаток очищали с помощью колоночной хроматографии на силикагеле (петролейный эфир : этилацетат = от 30:1 до 10:1). Получали необходимый продукт, 4-(аллилокси)-N-(3-(бензилокси)фенэтил)-N-фенилбензамид (8,00 г, выход 87%), в виде желтого масла. LC/MS (ESI) масса/заряд: 464,1 [М+1]+; 1Н-ЯМР (400 МГц, CDCl3) δ 7,46-7,34 (m, 5Н), 7,28-7,15 (m, 6Н), 6,92-6,83 (m, 5Н), 6,71-6,67 (m, 2Н), 6,04-5,97 (m, 1H), 5,41-5,35 (m, 1H), 5,28 (dq, J=10,4, 1,6 Гц, 1H), 5,05 (s, 2Н), 4,48 (dt, J=5,2, 1,6 Гц, 2Н), 4,15-4,10 (m, 2Н), 3,03-2,99 (m, 2Н).
[677] Стадия 6. Получение 1-(4-аллилоксифенил)-6-бензилокси-2-фенил-3,4-дигидро-1H-изохинолина

[678] К раствору 4-аллилокси-N-[2-(3-бензилоксифенил)этил]-N-фенилбензамида (8 г, 17,26 ммоль, 1,00 экв.) в толуоле (80 мл) добавляли оксихлорид фосфора (52,93 г, 345,20 ммоль, 32,08 мл, 20,00 экв.). Раствор нагревали до 120°С в течение 16 часов. С помощью LC/MS показывали, что исходное вещество было израсходовано. К раствору добавляли борогидрид натрия (1,31 г, 34,52 ммоль, 2,00 экв.) при 20°С. Раствор перемешивали при 20°С в течение 2 часов. С помощью LC/MS показывали завершение реакции. Растворитель удаляли и остаток гасили водой (30 мл). Смесь экстрагировали этилацетатом (30 мл × 3). Органический слой высушивали над сульфатом натрия, фильтровали и концентрировали в вакууме с получением 1-(4-аллилоксифенил)-6-бензилокси-2-фенил-3,4-дигидро-1Н-изохинолина (5,5 г, 12,29 ммоль, выход 71%) в виде белого твердого вещества. LC/MS (ESI) масса/заряд: 448,1 [М+1]+.
[679] Стадия 7. Получение 4-(6-(бензилокси)-2-фенил-1,2,3,4-тетрагидроизохинолин-1-ил)фенола
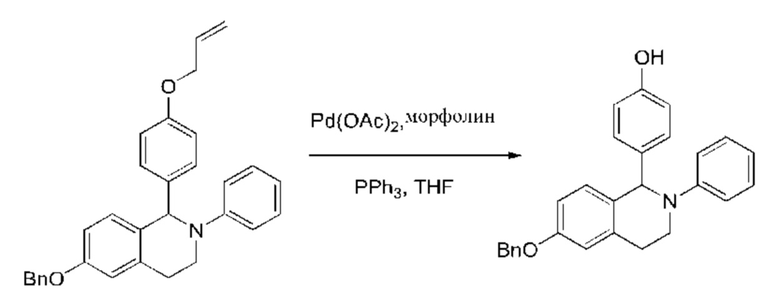
[680] К раствору 1-(4-аллилоксифенил)-6-бензилокси-2-фенил-3,4-дигидро-1Н-изохинолина (5,5 г, 12,29 ммоль, 1,00 экв.) в тетрагидрофуране (100 мл) добавляли трифенилфосфин (4,84 г, 18,43 ммоль, 1,50 экв.), морфолин (1,28 г, 14,75 ммоль, 1,30 мл, 1,20 экв.), ацетат палладия (276 мг, 1,23 ммоль, 0,10 экв.). Полученную смесь перемешивали при 20°С в течение 16 часов. LC/MS указывала на завершение реакции. Реакционную смесь фильтровали через слой целита и осадок промывали 100 мл этилацетата. Фильтрат концентрировали с удалением растворителя. Остаток дополнительно очищали с помощью полупрепаративной HPLC с обращенной фазой (колонка: Phenomenex Synergi Max-RP 250 × 50 мм, 10 мкм; подвижная фаза: вода с 0,1% TFA/ацетонитрил; В%: ацетонитрил 10%-65%). Собранную фракцию концентрировали с удалением большей части ацетонитрила. Полученную смесь экстрагировали этилацетатом (250 мл × 3). Объединенную органическую фазу промывали солевым раствором (400 мл), высушивали над сульфатом натрия, фильтровали и концентрировали в вакууме. Получали необходимый продукт, 4-(6-(бензилокси)-2-фенил-1,2,3,4-тетрагидроизохинолин-1-ил)фенол (3,9 г, выход 78%), в виде желтого твердого вещества. LC/MS (ESI) масса/заряд: 408,0 [М+1]+; 1H-ЯМР (400 МГц, CD3OD) δ 7,46-7,44 (m, 2Н), 7,40-7,36 (m, 2Н), 7,33-7,30 (m, 1H), 7,24 (t, J=8,0 Гц, 2Н), 7,06-6,92 (m, 5Н), 6,87-6,83 (m, 3Н), 6,66-6,63 (m, 2Н), 5,79 (s, 1H), 5,07 (s, 2Н), 3,72-3,50 (m, 2Н), 3,02 (br, 2Н).
[681] Стадия 8. Получение трет-бутил-4-[2-[4-(6-бензилокси-2-фенил-3,4-дигидро-1H-изохинолин-1-ил)фенокси]этил]пиперазин-1-карбоксилата

[682] К раствору 4-(6-бензилокси-2-фенил-3,4-дигидро-1H-изохинолин-1-ил)фенола (2,30 г, 5,64 ммоль, 1,00 экв.), трет-бутил-4-(2-хлорэтил)пиперазин-1-карбоксилата (1,68 г, 6,77 ммоль, 1,20 экв.) в N,N-диметилформамиде (20 мл) добавляли карбонат цезия (2,76 г, 8,46 ммоль, 1,50 экв.) и йодид калия (94 мг, 0,56 ммоль, 0,10 экв.) в атмосфере азота. Реакционную смесь перемешивали при 90°С в течение 16 часов. С помощью LC/MS показывали, что большая часть исходного вещества была израсходована. К смеси добавляли воду (150 мл), полученную смесь экстрагировали этилацетатом (50 мл × 3). Объединенную органическую фазу промывали солевым раствором (100 мл × 2), высушивали над сульфатом натрия, фильтровали и концентрировали в вакууме. Остаток очищали с помощью хроматографии на силикагеле (петролейный эфир/этилацетат = от 20/1 до 1/1) с получением трет-бутил-4-[2-[4-(6-бензилокси-2-фенил-3,4-дигидро-1H-изохинолин-1-ил) фенокси]этил]пиперазин-1-карбоксилата (2,5 г, 3,97 ммоль, выход 70%, чистота 98%) в виде желтого твердого вещества. LC/MS (ESI) масса/заряд: 620,3 [М+1]+; 1Н-ЯМР (400 МГц, DMSO-d6) δ 7,44-7,37 (m, 4H), 7,32-7,28 (m, 2H), 7,17-7,11 (m, 4H), 6,87-6,80 (m, 6H), 6,64 (t, J=7,2 Гц, 1H), 5,84 (s, 1H), 5,07 (s, 2H), 4,06-3,98 (m, 2H), 3,67-3,62 (m, 1H), 3,44-3,40 (m, 1H), 3,29-3,27 (m, 4H), 2,96-2,79 (m, 2H), 2,65 (t, J=5,6 Гц, 2H), 2,39 (t, J=4,8 Гц, 4H), 1,38 (s, 9H).
[683] Стадия 9. Получение 6-(бензилокси)-2-фенил-1-(4-(2-(пиперазин-1-ил)этокси)фенил)-1,2,3,4-тетрагидроизохинолина

[684] К раствору трет-бутил-4-[2-[4-(6-бензилокси-2-фенил-3,4-дигидро-1Н-изохинолин-1-ил)фенокси]этил]пиперазин-1-карбоксилата (1,00 г, 1,61 ммоль, 1,00 экв.) в дихлорметане (40 мл) добавляли трифторуксусную кислоту (10,00 мл) при 25°С. Смесь перемешивали при 25°С в течение 16 часов. С помощью TLC (дихлорметан : метанол = 10:1) показывали, что исходное вещество было полностью израсходовано. Реакционную смесь выливали в воду (100 мл) и затем нейтрализовали бикарбонатом натрия. Полученную смесь экстрагировали этилацетатом (150 мл × 3). Объединенную органическую фазу промывали солевым раствором (250 мл × 2), высушивали над безводным сульфатом натрия, фильтровали и концентрировали в вакууме с получением 6-бензилокси-2-фенил-1-[4-(2-пиперазин-1-илэтокси)фенил]-3,4-дигидро-1H-изохинолина (0,80 г, 1,54 ммоль, выход 95%) в виде желтого масла. LC/MS (ESI) масса/заряд: 520,3 [М+1]+.
[685] Стадия 10. Получение этил-2-(2-(4-(2-(4-(6-(бензилокси)-2-фенил-1,2,3,4-тетрагидроизохинолин-1-ил)фенокси)этил)пиперазин-1-ил)этокси)ацетата

[686] К раствору этил-2-(2-хлорэтокси)ацетата (0,24 г, 1,44 ммоль, 1,00 экв.) и 6-бензилокси-2-фенил-1-[4-(2-пиперазин-1-илэтокси)фенил]-3,4-дигидро-1H-изохинолина (0,75 г, 1,44 ммоль, 1,0 экв.) в N,N-диметилформамиде (10 мл) добавляли йодид натрия (0,22 г, 1,44 ммоль, 1,00 экв.) и карбонат цезия (0,94 г, 2,88 ммоль, 2,00 экв.) при 25°С. Смесь нагревали до 100°С и перемешивали при 100°С в течение 16 часов. С помощью LC/MS показывали, что реакция завершилась, и необходимый продукт образовался. Смесь выливали в воду (50 мл) и водную фазу экстрагировали этилацетатом (50 мл × 3). Объединенную органическую фазу промывали солевым раствором (100 мл × 2), высушивали над безводным сульфатом натрия, фильтровали и концентрировали в вакууме. Остаток очищали с помощью колоночной хроматографии на силикагеле (дихлорметан : метанол = 50:1) с получением этил-2-[2-[4-[2-[4-(6-бензилокси-2-фенил-3,4-дигидро-1Н-изохинолин-1-ил)фенокси]этил]пиперазин-1-ил]этокси]ацетата (0,58 г, 0,90 ммоль, выход 62%) в виде желтого масла. LC/MS (ESI) масса/заряд: 650,3 [М+1]+.
[687] Стадия 11. Получение 2-(2-(4-(2-(4-(6-гидрокси-2-фенил-1,2,3,4-тетрагидроизохинолин-1-ил)фенокси)этил)пиперазин-1-ил)этокси)уксусной кислоты

[688] К раствору этил-2-[2-[4-[2-[4-(6-бензилокси-2-фенил-3,4-дигидро-1Н-изохинолин-1-ил)фенокси]этил]пиперазин-1-ил]этокси]ацетата (0,40 г, 0,62 ммоль, 1,00 экв.) в диоксане (6 мл) добавляли концентрированную хлористоводородную кислоту (11,8 М, 8 мл). Смесь перемешивали при 100°С в течение 1 часа. С помощью LC/MS показывали, что исходное вещество было израсходовано, и необходимый продукт образовался. Смесь охлаждали до 25°С и рН регулировали до 5 насыщенным раствором бикарбоната натрия. Водную фазу экстрагировали этилацетатом (50 мл × 5). Объединенную органическую фазу высушивали с помощью безводного сульфата натрия, фильтровали и концентрировали в вакууме с получением 2-[2-[4-[2-[4-(6-гидрокси-2-фенил-3,4-дигидро-1H-изохинолин-1-ил)фенокси]этил]пиперазин-1-ил]этокси]уксусной кислоты (0,32 г, 0,42 ммоль, выход 68%, чистота 69%) в виде желтого масла. Неочищенный продукт непосредственно применяли для следующей стадии без дополнительной очистки. LC/MS (ESI) масса/заряд: 532,3 [М+1]+.
[689] Стадия 12. Получение (2S,4R)-4-гидрокси-1-((2S)-2-(2-(2-(4-(2-(4-(6-гидрокси-2-фенил-1,2,3,4-тетрагидроизохинолин-1-ил)фенокси)этил)пиперазин-1-ил)этокси)ацетамидо)-3,3-диметилбутаноил)-N-((S)-1-(4-(4-метилтиазол-5-ил)фенил)этил)пирролидин-2-карбоксамида (иллюстративное соединение 6)

[690] К раствору 2-[2-[4-[2-[4-(6-гидрокси-2-фенил-3,4-дигидро-1Н-изохинолин-1-ил)фенокси]этил]пиперазин-1-ил]этокси]уксусной кислоты (0,16 г, 0,30 ммоль, 1,00 же), 1-гидроксибензотриазола (0,05 г, 0,36 ммоль, 1,20 экв.) и гидрохлорида 1-(3-диметиламинопропил)-3-этилкарбодиимида (0,09 г, 0,45 ммоль, 1,50 экв.) в N,N-диметилформамиде (5 мл) добавляли N,N-диизопропилэтиламин (0,19 г, 1,50 ммоль, 0,26 мл, 5,00 экв). Смесь перемешивали при 25°С в течение получаса и затем добавляли (2S,4R)-1-[(2S)-2-амино-3,3-диметилбутаноил]-4-гидрокси-N-[(1S)-1-[4-(4-метилтиазол-5-ил)фенил]этил]пирролидин-2-карбоксамид (0,14 г, 0,30 ммоль, 1,00 же., соль HCl). Полученную смесь перемешивали при 25°С в течение 16 часов. С помощью LC/MS показывали завершение реакции. Смесь выливали в 100 мл насыщенного солевого раствора и затем экстрагировали этилацетатом (50 мл × 3). Объединенные органические слои высушивали над безводным сульфатом натрия, фильтровали и концентрировали в вакууме. Остаток дополнительно очищали с помощью полупрепаративной HPLC с обращенной фазой (колонка: Phenomenex Synergi С18 150 мм × 25 мм, 10 мкм; подвижная фаза: вода с 0,05% гидроксид аммония/ацетонитрил; В%: 28%-48%, 7,8 мин.). Собранную фракцию концентрировали с удалением большей части ацетонитрила и лиофилизировали с получением (2S,4R)-4-гидрокси-1-[(2S)-2-[[2-[2-[4-[2-[4-(6-гидрокси-2-фенил-3,4-дигидро-1H-изохинолин-1-ил)фенокси]этил]пиперазин-1-ил]этокси]ацетил]амино]-3,3-диметилбутаноил]-N-[(1S)-1-[4-(4-метилтиазол-5-ил)фенил]этил]пирролидин-2-карбоксамида (25,8 мг, 0,03 ммоль, выход 9%, чистота 98%) в виде серого твердого вещества. LC/MS (ESI) масса/заряд: 958,5 [М+1]+; 1Н-ЯМР (400 МГц, CD3OD) δ 8,88 (s, 1H), 7,46-7,40 (m, 4Н), 7,16 (t, J=8,0 Гц, 2Н), 7,09-7,04 (m, 3Н), 6,87 (d, J=8,0 Гц, 2Н), 6,79 (d, J=8,0 Гц, 2Н), 6,72-6,63 (m, 3Н), 5,72 (s, 1H), 5,03-4,96 (m, 1H), 4,69 (s, 1H), 4,58 (m, 1H), 4,45 (m, 1H), 4,10-3,97 (m, 4Н), 3,86-3,84 (m, 1H), 3,78-3,70 (m, 3Н), 3,63-3,58 (m, 1H), 3,45-3,39 (m, 1H), 2,91-2,79 (m, 4Н), 2,76-2,51 (m, 9Н), 2,49 (s, 3Н), 2,23-2,17 (m, 1H), 2,01-1,97 (m, 1H), 1,54 (d, J=7,2, 3Н), 1,05 (s, 9Н).
[691] Синтез 3-{5-[4-(5-{4-[(1R,2S)-6-гидрокси-2-фенил-1,2,3,4-тетрагидронафталин-1-ил]фенокси}пентил)пиперазин-1-ил]-1-оксо-2,3-дигидро-1Н-изоиндол-2-ил}пиперидин-2,6-диона (иллюстративное соединение 62)
[692] Стадия 1. Получение 6-бензилокситетралин-1-она

[693] К раствору 6-гидрокситетралин-1-она (100 г, 616,56 ммоль, 1,00 экв.) в ацетонитриле (1000 мл) добавляли карбонат калия (170,43 г, 1,23 моль, 2,00 экв.) и бензилбромид (126,54 г, 739,87 ммоль, 88 мл, 1,20 экв.). Реакционную смесь перемешивали при 50°С в течение 2 часов. С помощью TLC (петролейный эфир : этилацетат = 5:1) показывали, что большая часть исходного вещества была израсходована. К смеси добавляли воду (1000 мл), полученную смесь экстрагировали этилацетатом (600 мл × 3). Объединенную органическую фазу промывали солевым раствором (800 мл), высушивали над сульфатом натрия, фильтровали и концентрировали в вакууме. Остаток растирали с петролейным эфиром и этилацетатом (303 мл, петролейный эфир : этилацетат = 100:1, об. : об.). Смесь фильтровали и осадок на фильтре промывали петролейным эфиром (50 мл × 2), высушивали в вакууме с получением 6-бензилокситетралин-1-она (146 г, 578,65 ммоль, выход 94%) в виде коричневого твердого вещества. 1H-ЯМР (400 МГц, CDCl3) δ 8,02 (d, J=8,8 Гц, 1H), 7,45-7,34 (m, 5Н), 6,91 (dd, J=8,8, 2,4 Гц, 1H), 6,80 (d, J=2,4 Гц, 1H), 5,12 (s, 2H), 2,93 (t, J=6,0 Гц, 2H), 2,62 (t, J=6,4 Гц, 2H), 2,15-2,09 (m, 2H).
[694] Стадия 2. Получение (6-бензилокси-3,4-дигидронафталин-1-ил)трифторметансульфоната

[695] К раствору 6-бензилокситетралин-1-она (80 г, 317,07 ммоль, 1,00 экв.) в тетрагидрофуране (1000 мл) добавляли диизопропиламид лития (2 М, 237,8 мл, 1,50 экв.) при -70°С. Смесь перемешивали при -70°С в течение 1 часа, затем к смеси добавляли по каплям 1,1,1-трифтор-N-фенил-N-(трифторметилсульфонил)метансульфонамид (124,6 г, 348,78 ммоль, 1,10 экв.) в тетрагидрофуране (300 мл). Реакционную смесь перемешивали при 20°С в течение 1 часа. С помощью TLC (петролейный эфир : этилацетат = 10:1) показывали, что большая часть исходного вещества была израсходована. К смеси добавляли насыщенный раствор хлорида аммония (600 мл), органическую фазу отделяли. К смеси добавляли этилацетат (600 мл), полученную смесь промывали солевым раствором (600 мл × 2). Объединенную органическую фазу высушивали над сульфатом натрия, фильтровали и концентрировали в вакууме. Остаток очищали с помощью флэш-хроматографии на силикагеле (петролейный эфир : этилацетат = от 1:0 до 50:1) с получением (6-бензилокси-3,4-дигидронафталин-1-ил)трифторметансульфоната (88 г, 228,95 ммоль, выход 72%) в виде светло-желтого твердого вещества. 1Н ЯМР (400 МГц, CDCl3) δ 7,46-7,33 (m, 5Н), 7,27 (d, J=8,4 Гц, 1H), 6,87-6,83 (m, 2Н), 5,88 (t, J=4,8 Гц, 1H), 5,09 (s, 2Н), 2,85 (t, J=8,0 Гц, 2Н), 2,52-2,47 (m, 2Н).
[696] Стадия 3. Получение 4-(6-бензилокси-3,4-дигидронафталин-1-ил)фенола

[697] К раствору (6-бензилокси-3,4-дигидронафталин-1-ил)трифторметансульфоната (80 г, 208,13 ммоль, 1,00 экв.), (4-гидроксифенил)бороновой кислоты (34,45 г, 249,76 ммоль, 1,20 экв.) в диоксане (700 мл) и воде (120 мл) добавляли карбонат калия (57,53 г, 416,26 ммоль, 2,00 экв.) и дихлорид (1,1'-бис(дифенилфосфино)ферроцен)палладия(II) (15,23 г, 20,81 ммоль, 0,10 экв.) в атмосфере азота. Реакционную смесь перемешивали при 100°С в течение 3 часов. С помощью TLC (петролейный эфир : этилацетат = 5:1) показывали, что большая часть исходного вещества была израсходована. К смеси добавляли воду (600 мл), полученную смесь экстрагировали этилацетатом (600 мл × 3). Объединенную органическую фазу промывали солевым раствором (800 мл × 2), высушивали над сульфатом натрия, фильтровали и концентрировали в вакууме. Остаток очищали с помощью хроматографии на силикагеле (петролейный эфир : этилацетат = от 50:1 до 5:1) с получением 4-(6-бензилокси-3,4-дигидронафталин-1-ил)фенола (60 г, 182,70 ммоль, выход 88%) в виде красного твердого вещества. 1Н ЯМР (400 МГц, CDCl3) δ 7,47-7,36 (m, 6Н), 7,24-7,22 (m, 2Н), 6,97 (t, J=8,8 Гц, 1H), 6,88-6,24 (m, 3Н), 6,73 (dd, J=8,4, 2,8 Гц, 1H), 5,93 (t, J=4,8 Гц, 1H), 5,08 (s, 2Н), 2,83 (t, J=8,0 Гц, 2Н), 2,41-2,36 (m, 2Н).
[698] Стадия 4. Получение [4-(6-бензилокси-3,4-дигидронафталин-1-ил)фенил]ацетата

[699] К раствору 4-(6-бензилокси-3,4-дигидронафталин-1-ил)фенола (60 г, 182,70 ммоль, 1,00 экв.), триэтиламина (46,22 г, 456,76 ммоль, 63,3 мл, 2,50 экв.) в дихлорметане (400 мл) добавляли по каплям ацетилхлорид (21,51 г, 274,06 ммоль, 19,6 мл, 1,50 экв.) при 0°С.Реакционную смесь перемешивали при 20°С в течение 1 часа. С помощью TLC (петролейный эфир : этилацетат = 5:1) показали, что большая часть исходного вещества была израсходована. К смеси добавляли воду (300 мл), органическую фазу отделяли. Органическую фазу промывали солевым раствором (200 мл × 2), высушивали над сульфатом натрия, фильтровали и концентрировали в вакууме с получением [4-(6-бензилокси-3,4-дигидронафталин-1-ил)фенил]ацетата (66 г, неочищенный) в виде желтого твердого вещества. 1Н ЯМР (400 МГц, CDCl3) δ 7,46-7,32 (m, 7Н), 7,10 (d, J=8,4 Гц, 2Н), 6,96 (d, J=8,4 Гц, 1H), 6,87 (d, J=2,4 Гц, 1H), 6,73 (dd, J=2,4, 8,4 Гц, 1H), 5,97 (t, J=4,4 Гц, 1H), 5,08 (s, 2Н), 2,83 (t, J=8,0 Гц, 2Н), 2,42-2,37 (m, 2Н), 2,34 (s, 3Н).
[700] Стадия 5. Получение [4-(6-бензилокси-2-бром-3,4-дигидронафталин-1-ил)фенил]ацетата

[701] К раствору [4-(6-бензилокси-3,4-дигидронафталин-1-ил)фенил]ацетата (44 г, 118,78 ммоль, 1,00 экв.) в ацетонитриле (880 мл) тремя порциями добавляли N-бромсукцинимид (22,20 г, 124,72 ммоль, 1,05 экв.). Реакционную смесь перемешивали при 20°С в течение 2 часов. С помощью LC/MS показывали, что большая часть исходного вещества была израсходована. К смеси добавляли насыщенный раствор бикарбоната натрия (500 мл), полученную смесь экстрагировали этилацетатом (500 мл × 3). Объединенную органическую фазу промывали солевым раствором (800 мл × 2), высушивали над сульфатом натрия, фильтровали и концентрировали в вакууме. Остаток очищали с помощью хроматографии на силикагеле (петролейный эфир : этилацетат = от 100:1 до 40:1) с получением [4-(6-бензилокси-2-бром-3,4-дигидронафталин-1-ил)фенил]ацетата (33 г, 73,44 ммоль, выход 61,83%) в виде светло-желтого твердого вещества. LC/MS (ESI) масса/заряд: 449,0, 451,0 [М, М+2]+. 1Н ЯМР (400 МГц, CDCl3) δ 7,33-7,23 (m, 5Н), 7,15 (d, J=8,4 Гц, 2Н), 7,07 (d, J=8,4 Гц, 2Н), 6,71 (s, 1H), 6,55-6,48 (m, 2Н), 4,94 (s, 2Н), 2,93-2,83 (m, 4Н), 2,24 (s, 3Н).
[702] Стадия 6. Получение [4-(6-бензилокси-2-фенил-3,4-дигидронафталин-1-ил)фенил]ацетата
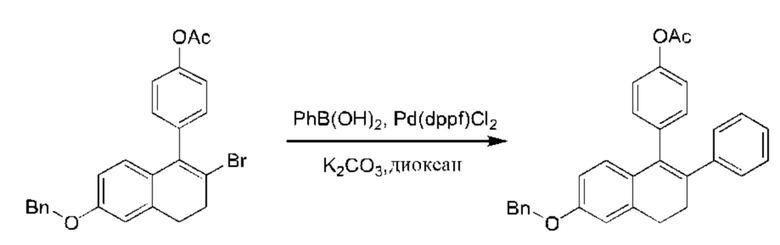
[703] К раствору [4-(6-бензилокси-2-бром-3,4-дигидронафталин-1-ил)фенил]ацетата (48 г, 106,82 ммоль, 1,00 экв.), фенилбороновой кислоты (13,68 г, 112,16 ммоль, 1,05 экв.) в диоксане (400 мл) и воде (60 мл) добавляли карбонат калия (29,53 г, 213,64 ммоль, 2,00 экв.) и дихлорид (1,1'-бис(дифенилфосфино)ферроцен)палладия(II) (7,82 г, 10,68 ммоль, 0,10 экв.) в атмосфере азота. Реакционную смесь перемешивали при 100°С в течение 3 часов. С помощью TLC (петролейный эфир : этилацетат = 5:1) и LC/MS показывали, что большая часть исходного вещества была израсходована. К смеси добавляли воду (400 мл), полученную смесь экстрагировали этилацетатом (300 мл × 3). Объединенную органическую фазу промывали солевым раствором (500 мл × 2), высушивали над сульфатом натрия, фильтровали и концентрировали в вакууме. Остаток очищали путем растирания с метанолом (200 мл). Осадок на фильтре очищали с помощью хроматографии на силикагеле (петролейный эфир : этилацетат = от 100:1 до 5:1) с получением [4-(6-бензилокси-2-фенил-3,4-дигидронафталин-1-ил)фенил]ацетата (43 г, 96,30 ммоль, выход 90%) в виде светло-желтого твердого вещества. LC/MS (ESI) масса/заряд: 447,2 [М+1]+. 1Н ЯМР (400 МГц, CDCl3) δ 7,47-7,32 (m, 5Н), 7,15-7,04 (m, 5Н), 7,03-6,96 (m, 4Н), 6,88 (d, J=2,4 Гц, 1H), 6,75 (d, J=8,4 Гц, 1H), 6,69 (dd, J=2,4, 8,4 Гц, 1H), 5,09 (s, 2Н), 2,99- 2,95 (m, 2Н), 2,83-2,79 (m, 2Н), 2,30 (s, 3Н).
[704] Стадия 7. Получение [4-[(1,2-цис)-6-гидрокси-2-фенилтетралин-1-ил]фенил]ацетата

[705] К раствору [4-(6-бензилокси-2-фенил-3,4-дигидронафталин-1-ил)фенил]ацетата (17 г, 38,07 ммоль, 1,00 экв.) в метаноле (350 мл) и тетрагидрофуране (70 мл) добавляли палладий/уголь (2 г, 10%) в атмосфере азота. Реакционную смесь перемешивали при 20°С в атмосфере водорода (50 фунтов/кв. дюйм) в течение 24 часов. С помощью TLC (петролейный эфир : этилацетат = 3:1) и LC/MS показывали, что большая часть исходного вещества была израсходована. Остаток очищали с помощью хроматографии на силикагеле (петролейный эфир : дихлорметан = от 10:1 до 0:1) с получением [4-[(1,2-цис)-6-гидрокси-2-фенилтетралин-1-ил]фенил]ацетата (9,5 г, 26,50 ммоль, выход 70%) в виде белого твердого вещества и также дополнительно 4,5 г неочищенного продукта. LC/MS (ESI) масса/заряд: 381,0 [М +23]+; 1Н ЯМР (400 МГц, CDCl3) δ 7,20-7,15 (m, 3Н), 6,83-6,80 (m, 3Н), 6,74-6,70 (m, 3Н), 6,58 (dd, J=2,4, 8,4 Гц, 1Н), 6,43-6,40 (m, 2Н), 4,94 (s, 1Н), 4,29 (d, J=5,2 Гц, 1Н), 3,52-3,37 (m, 1Н), 3,11-2,97 (m, 2Н), 2,25 (s, 3Н), 2,23-2,07 (m, 1Н), 1,86-1,81 (m, 1Н).
[706] Стадия 8. Получение [4-[(1,2-цис)-6-бензилокси-2-фенилтетралин-1-ил]фенил] ацетата
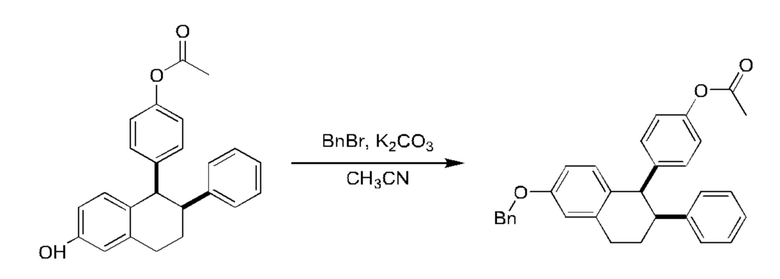
[707] К раствору [4-[(1,2-цис)-6-гидрокси-2-фенилтетралин-1-ил]фенил]ацетата (9,5 г, 26,50 ммоль, 1,00 экв.) в ацетонитриле (100 мл) добавляли карбонат калия (7,33 г, 53,01 ммоль, 2,00 экв.) и бензилбромид (6,8 г, 39,76 ммоль, 4,7 мл, 1,50 экв.). Реакционную смесь перемешивали при 50°С в течение 16 часов. С помощью TLC (петролейный эфир : дихлорметан = 2:1) показывали, что большая часть исходного вещества была израсходована. К смеси добавляли воду (200 мл), полученную смесь экстрагировали этилацетатом (100 мл × 3). Объединенную органическую фазу промывали солевым раствором (200 мл), высушивали над сульфатом натрия, фильтровали и концентрировали в вакууме. Остаток очищали с помощью хроматографии на силикагеле (петролейный эфир : дихлорметан = от 50:1 до 2:1) с получением [4-[(1,2-цис)-6-бензилокси-2-фенилтетралин-1-ил]фенил]ацетата (11 г, 24,52 ммоль, выход 92%) в виде белого твердого вещества. 1Н ЯМР (400 МГц, CDCl3) δ: 7,48-7,32 (m, 5Н), 7,20-7,13 (m, 3Н), 6,89-6,86 (m, 2Н), 6,84-6,75 (m, 3Н), 6,73-6,69 (m, 2Н), 6,42-6,40 (m, 2Н), 5,07 (s, 2Н), 4,30 (d, J=5,2 Гц, 1Н), 3,42-3,38 (m, 1Н), 3,14-3,01 (m, 2Н), 2,24 (s, 3Н), 2,22-2,13 (m, 1Н), 1,86-1,82 (m, 1Н).
[708] Стадия 9. Получение 4-[(1,2)-цис-(6-бензилокси-2-фенилтетралин-1-ил)]фенола

[709] К раствору, содержащему [4-(1,2)-цис-(6-бензилокси-2-фенилтетралин-1-ил)фенил]ацетат (11 г, 24,52 ммоль, 1,00 экв.) в тетрагидрофуране (30 мл), воде (15 мл) и метаноле (15 мл), добавляли гидроксид лития (5,15 г, 122,62 ммоль, 5,00 экв.). Реакционную смесь перемешивали при 20°С в течение 1 часа. С помощью TLC (петролейный эфир : этилацетат = 3:1) показывали, что большая часть исходного вещества была израсходована. К смеси добавляли хлористоводородную кислоту (2 М, 80 мл) и воду (50 мл) с регулированием до рН ~ 7, полученную смесь экстрагировали этилацетатом (100 мл × 3). Объединенную органическую фазу промывали солевым раствором (150 мл), высушивали над сульфатом натрия, фильтровали и концентрировали в вакууме. Остаток очищали с помощью хроматографии на силикагеле (петролейный эфир : дихлорметан = от 10:1 до 0:1) с получением 4-[(1,2)-цис-(6-бензилокси-2-фенилтетралин-1-ил)]фенола (9,2 г, 22,63 ммоль, выход 92%) в виде белого твердого вещества. 1H ЯМР (400 МГц, CDCl3) δ 7,48-7,33 (m, 5Н), 7,21-7,14 (m, 3Н), 6,90-6,76 (m, 5Н), 6,47 (d, J=5,2 Гц, 1Н), 6,30 (d, J=5,2 Гц, 1Н), 6,42-6,40 (m, 2Н), 5,07 (s, 2Н), 4,54 (s, 1Н), 4,30 (d, J=5,2 Гц, 1Н), 3,42-3,38 (m, 1Н), 3,14-3,01 (m, 2Н), 2,22-2,13 (m, 1Н), 1,86-1,82 (m, 1Н).
[710] Стадия 10. Получение (1,2)-цис-6-(бензилокси)-1-(4-((5-бромпентил)окси)фенил)-2-фенил-1,2,3,4-тетрагидронафталина

[711] К раствору 4-(6-бензилокси-2-фенилтетралин-1-ил)фенола (600 мг, 1,48 ммоль, 1,00 экв.) в ацетоне (10 мл) добавляли карбонат калия (612 мг, 4,43 ммоль, 3,00 экв.) и 1,5-дибромпентан (1 г, 4,43 ммоль, 0,6 мл, 3,00 экв.). Смесь перемешивали при 70°С в течение 12 часов. С помощью LC/MS показывали, что реакция завершилась, и необходимый продукт образовался. Реакционную смесь разбавляли водой (30 мл) и экстрагировали этилацетатом (20 мл × 2). Объединенную органическую фазу промывали солевым раствором (10 мл × 2), высушивали с помощью безводного сульфата натрия, фильтровали и концентрировали в вакууме. Остаток очищали с помощью колоночной хроматографии (петролейный эфир : этилацетат = от 1:0 до 20:1) с получением (1,2)-цис-6-бензилокси-1-[4-(5-бромпентокси)фенил]-2-фенилтетралина (620 мг, 1,12 ммоль, выход 75%) в виде бесцветного масла. LC/MS (ESI) масса/заряд: 555,2 [М+1]+; 1H ЯМР (400 МГц, DMSO-d6) δ 7,49-7,45 (m, 2Н), 7,44-7,39 (m, 2Н), 7,37-7,31 (m, 1Н), 7,21-7,14 (m, 3Н), 6,91-6,85 (m, 2Н), 6,82 (dd, J=2,0, 7,2 Гц, 2Н), 6,79-6,74 (m, 1Н), 6,56-6,50 (m, 2Н), 6,33 (d, J=8,4 Гц, 2Н), 5,08 (s, 2Н), 4,25 (d, J=5,2 Гц, 1Н), 3,85 (t, J=6,4 Гц, 2Н), 3,43 (t, J=6,4 Гц, 2Н), 3,40-3,33 (m, 1Н), 3,18-2,98 (m, 2Н), 2,28-2,13 (m, 1Н), 1,92 (q, J=7,2 Гц, 2Н), 1,87-1,80 (m, 1Н), 1,80-1,71 (m, 2Н), 1,64-1,56 (m, 2Н)
[712] Стадия 11. Получение (1R,2S)-6-гидрокси-1-(4-((5-бромпентил)окси)фенил)-2-фенил-1,2,3,4-тетрагидронафталина
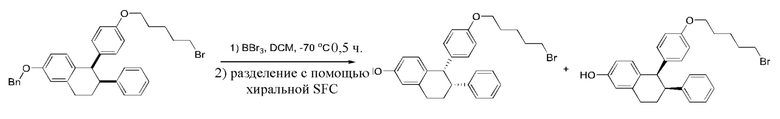
[713] К раствору (1,2)-цис-6-бензилокси-1-[4-(5-бромпентокси)фенил]-2-фенилтетралина (620 мг, 1,12 ммоль, 1,00 экв.) в дихлорметане (15 мл) добавляли трибромид бора (1,7 г, 6,72 ммоль, 0,65 мл, 6,00 экв.) при -70°С. Смесь перемешивали при -70°С в течение 1 часа. С помощью TLC (петролейный эфир : этилацетат = 3:1) показывали, что большая часть исходного вещества была израсходована, и образовалось новое пятно. Реакционную смесь гасили насыщенным раствором бикарбоната натрия (5 мл) при -70°С, и затем разбавляли водой (8 мл) и экстрагировали дихлорметаном (5 мл × 2). Объединенную органическую фазу промывали насыщенным солевым раствором (5 мл × 2), высушивали с помощью безводного сульфата натрия, фильтровали и концентрировали в вакууме. Остаток очищали с помощью препаративной TLC (петролейный эфир : этилацетат = 3:1) с получением необходимого соединения (240 мг, выход 46%, чистота 90%) в виде белого твердого вещества, которое дополнительно разделяли с помощью хиральной SFC (колонка: OJ 250 мм × 30 мм, 10 мкм; подвижная фаза: 0,1% гидроксид аммония в метаноле; В%: 40%-40%, 2,4 мин.) с получением первой фракции (1S,2R)-1-[4-(5-бромпентокси)фенил]-2-фенилтетралин-6-ола (100 мг, 0,21 ммоль, выход 38%) в виде белого твердого вещества и следующей фракции (1R,2S)-6-(бензилокси)-1-(4-((5-бромпентил)окси)фенил)-2-фенил-1,2,3,4-тетрагидронафталина (100 мг, 0,21 ммоль, выход 38%) в виде белого твердого вещества.
[714] Стадия 12. Получение трет-бутил-4-(1-оксо-3Н-изобензофуран-5-ил)пиперазин-1-карбоксилата
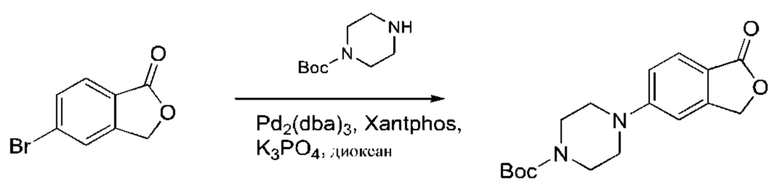
[715] К раствору 5-бром-3Н-изобензофуран-1-она (45 г, 211,24 ммоль, 1,00 экв.) и трет-бутилпиперазин-1-карбоксилата (39,34 г, 211,24 ммоль, 1,00 экв.) в диоксане (500 мл) добавляли трис(дибензилиденацетон)дипалладий(0) (19,34 г, 21,12 ммоль, 0,10 экв.), 4,5-бис(дифенилфосфино)-9,9-диметилксантен (12,22 г, 21,12 ммоль, 0,10 экв.) и фосфат калия (89,68 г, 422,48 ммоль, 2,00 экв.). Смесь нагревали до 100°С в течение 16 часов в защитной атмосфере азота. С помощью TLC (этилацетат : петролейный эфир = 1:2) показывали завершение реакции. Смесь фильтровали через слой целита и фильтрат концентрировали в вакууме. Остаток растирали в смеси этилацетат : петролейный эфир (500 мл, об./об. = 1:2) с получением трет-бутил-4-(1-оксо-3Н-изобензофуран-5-ил)пиперазин-1-карбоксилата (50 г, 122,5 ммоль, выход 58%, чистота 78%) в виде желтого твердого вещества. 1Н ЯМР (400 МГц, DMSO) δ 7,62 (d, J=8,8 Гц, 1Н), 7,10 (dd, J=8,8 Гц, 2 Гц, 1Н), 7,04 (s, 1Н), 5,25 (s, 2Н), 3,47-3,45 (m, 4Н), 3,45-3,38 (m, 4Н), 1,42 (s, 9Н).
[716] Стадия 13. Получение 4-(4-трет-бутоксикарбонилпиперазин-1-ил)-2-(гидроксилметил)бензойной кислоты

[717] К смеси трет-бутил-4-(1-оксо-3Н-изобензофуран-5-ил)пиперазин-1-карбоксилата (47,8 г, 150,14 ммоль, 1,00 экв.) в тетрагидрофуране (150 мл), метаноле (150 мл) и воде (150 мл) добавляли гидроксид натрия (24 г, 600 ммоль, 4,00 экв.). Смесь перемешивали при 25°С в течение 1 часа. С помощью TLC (этилацетат : петролейный эфир = 1:2) показывали завершение реакции. Раствор регулировали до рН = 4-5 с помощью водного раствора гидрохлорида (1 М) и экстрагировали этилацетатом (100 мл × 5). Органические слои концентрировали в вакууме. Неочищенный материал растирали в смеси этилацетат : петролейный эфир (450 мл, об.:об. = 1:2) с получением 4-(4-трет-бутоксикарбонилпиперазин-1-ил)-2-(гидроксиметил)бензойной кислоты (40 г, 118,91 ммоль, выход 79%) в виде желтого твердого вещества. 1Н ЯМР (400 МГц, DMSO) δ 12,36 (s, 1Н), 7,78 (d, J=8,8 Гц, 1Н), 7,22 (d, J=2 Гц, 1Н), 6,81 (dd, J=8,8, 1 Гц), 5,10 (s, 1Н), 4,80 (s, 2Н), 3,47-3,44 (m, 4Н), 3,29-3,27 (m, 4Н), 1,42 (s, 9Н).
[718] Стадия 14. Получение трет-бутил-4-[3-(гидроксиметил)-4-метоксикарбонилфенил]пиперазин-1-карбоксилата

[719] К раствору 4-(4-трет-бутоксикарбонилпиперазин-1-ил)-2-(гидроксиметил)бензойной кислоты (20 г, 59,46 ммоль, 1,00 экв.) в метаноле (100 мл) и этилацетате (100 мл) добавляли имино(триметилсилилметилен)аммоний (2 М, 89 мл, 3,00 экв.) при -10°С. Раствор перемешивали при -10°С в течение 0,25 часа. С помощью TLC (этилацетат : петролейный эфир = 1:2) показывали завершение реакции. Раствор гасили водой (300 мл) и экстрагировали этилацетатом (150 мл × 3). Органический слой высушивали над сульфатом натрия и фильтровали. Фильтрат концентрировали с получением трет-бутил-4-[3-(гидроксиметил)-4-метоксикарбонилфенил]пиперазин-1-карбоксилата (20,84 г, неочищенный), полученного в виде коричневого масла.
[720] Стадия 15. Получение трет-бутил-4-[3-(бромметил)-4-метоксикарбонилфенил]пиперазин-1-карбоксилата

[721] К раствору трет-бутил-4-[3-(гидроксиметил)-4-метоксикарбонилфенил]пиперазин-1-карбоксилата (20,84 г, 59,47 ммоль, 1,00 экв.) в тетрагидрофуране (200 мл) добавляли трифенилфосфин (23,4 г, 89,21 ммоль, 1,50 экв.) и пербромметан (29,58 г, 89,21 ммоль, 1,50 экв.). Раствор перемешивали при 25°С в течение 1 часа. С помощью TLC (этилацетат : петролейный эфир = 1:3) показывали завершение реакции. Раствор гасили водой (200 мл) и экстрагировали этилацетатом (100 мл × 2). Органический слой высушивали над сульфатом натрия и фильтровали. Фильтрат концентрировали в вакууме. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат : петролейный эфир = 1:50-1:8) с получением трет-бутил-4-[3-(бромметил)-4-метоксикарбонилфенил]пиперазин-1-карбоксилата (12 г, 29,03 ммоль, выход 49%) в виде бледно-желтого масла. 1Н ЯМР (300 МГц, CDCl3) δ 7,93 (s, J=9,0 Гц, 1Н), 6,88 (d, J=2,4 Гц, 1Н), 6,78 (dd, J=9,0, 2,4 Гц, 1Н), 4,97 (s, 2Н), 3,89 (s, 3Н), 3,64-3,57 (m, 4Н), 3,34-3,30 (m, 4Н), 1,42 (s, 9Н).
[722] Стадия 16. Получение трет-бутил-4-[2-(2,6-диоксо-3-пиперидил)-1-оксоизоиндолин-5-ил]пиперазин-1-карбоксилата

[723] К раствору трет-бутил-4-[3-(бромметил)-4-метоксикарбонилфенил]пиперазин-1-карбоксилата (12 г, 29,03 ммоль, 1,00 экв.) в ацетонитриле (300 мл) добавляли гидрохлорид 3-аминопиперидин-2,6-диона (7,17 г, 43,55 ммоль, 1,50 экв.) и N-этил-N-изопропилпропан-2-амин (11,26 г, 87,09 ммоль, 15 мл, 3,00 экв.). Раствор перемешивали при 80°С в течение 16 часов. С помощью LC/MS показывали завершение реакции. Реакционную смесь охлаждали до 20°С и фильтровали. Твердое вещество промывали ацетонитрилом (30 мл) с получением трет-бутил-4-[2-(2,6-диоксо-3-пиперидил)-1-оксоизоиндолин-5-ил]пиперазин-1-карбоксилата (6 г, 14 ммоль, выход 48%) в виде белого твердого вещества. 1Н ЯМР (400 МГц, DMSO) δ 10,91 (s, 1Н), 7,53 (d, J=8,4 Гц, 1Н), 7,06-7,04 (m, 2Н), 5,03 (dd, J=13,2, 5,2 Гц, 1Н), 4,35-4,19 (m, 2Н), 3,48-3,45 (m, 4Н), 3,27-3,26 (m, 4Н), 2,89-2,87 (m, 1Н), 2,60-2,56 (m, 1Н), 2,38-2,34 (m, 1Н), 1,98-1,96 (m, 1Н), 1,42 (s, 9Н).
[724] Стадия 17. Получение гидрохлорида 3-(1-оксо-5-пиперазин-1-илизоиндолин-2-ил)пиперидин-2,6-диона

[725] К смеси трет-бутил-4-[2-(2,6-диоксо-3-пиперидил)-1-оксоизоиндолин-5-ил]пиперазин-1-карбоксилата (6 г, 14 ммоль, 1,00 экв.) в диоксане (70 мл) добавляли смесь гидрохлорид/диоксан (4 М, 100 мл, 28,57 экв.). Смесь перемешивали при 25°С в течение 2 часов. С помощью LC/MS показывали завершение реакции. Смесь выливали в этилацетат (400 мл) и перемешивали в течение 30 минут. Суспензию фильтровали и твердое вещество собирали с получением гидрохлорида 3-(1-оксо-5-пиперазин-1-илизоиндолин-2-ил)пиперидин-2,6-диона (5 г, 13,71 ммоль, выход 98%) в виде белого твердого вещества. 1H-ЯМР (400 МГц, DMSO) δ: 10,95 (s, 1Н), 9,49 (s, 2Н), 7,57 (d, J=8,4 Гц, 1Н), 7,15-7,10 (m, 2Н), 5,05 (dd, J=13,2, 5,2 Гц, 1Н), 4,37-4,20 (m, 2Н), 3,55-3,53 (m, 4Н), 3,20-3,19 (m, 4Н), 2,90-2,86 (m, 1Н), 2,60-2,56 (m, 1Н), 2,38-2,34 (m, 1Н), 1,98-1,96 (m, 1Н).
[726] Стадия 18. Получение 3-{5-[4-(5-{4-[(1R,2S)-6-гидрокси-2-фенил-1,2,3,4-тетрагидронафталин-1-ил]фенокси}пентил)пиперазин-1-ил]-1-оксо-2,3-дигидро-1Н-изоиндол-2-ил}пиперидин-2,6-диона (иллюстративное соединение 62)

(1R,2S)-1-[4-(5-Бромпентокси)фенил]-2-фенилтетралин-6-ол (50 мг, 0,11 ммоль, 1,00 экв.), гидрохлорид 3-(1-оксо-5-пиперазин-1-илизоиндолин-2-ил)пиперидин-2,6-диона (47 мг, 0,13 ммоль, 1,20 экв.) и диизопропилэтиламин (70 мг, 0,53 ммоль, 0,1 мл, 5,00 экв.) помещали в пробирку для микроволновой обработки в N-метил-2-пирролидинон (3 мл). Герметично закрытую пробирку нагревали при 140°С в течение 2 часов с помощью микроволнового излучения. С помощью LC/MS показывали, что реакция завершилась, и необходимый продукт образовался. Реакционную смесь разбавляли водой (15 мл) и экстрагировали этилацетатом (5 мл × 2). Объединенную органическую фазу промывали насыщенным солевым раствором (5 мл × 2), высушивали с помощью безводного сульфата натрия, фильтровали и концентрировали в вакууме. Остаток очищали с помощью препаративной TLC (дихлорметан : метанол = 10:1) с получением 3-{5-[4-(5-{4-[(1R,2S)-6-гидрокси-2-фенил-1,2,3,4-тетрагидронафталин-1-ил]фенокси}пентил)пиперазин-1-ил]-1-оксо-2,3-дигидро-1Н-изоиндол-2-ил}пиперидин-2,6-диона (16,9 мг, 0,02 ммоль, выход 22%, чистота 99,9%) в виде белого твердого вещества. Данное твердое вещество преобразовывали в гидрохлоридную соль. LC/MS (ESI) масса/заряд: 713,3 [М+1]+; 1H-ЯМР (400 МГц, DMSO-d6) δ: 10,96 (s, 1Н), 10,69 (s, 1Н), 9,16 (s, 1Н), 7,58 (d, J=8,4 Гц, 1Н), 7,23-7,08 (m, 5Н), 6,83 (d, J=6,4 Гц, 2Н), 6,67-6,59 (m, 2Н), 6,57-6,45 (m, 3Н), 6,27 (d, J=8,8 Гц, 2Н), 5,06 (dd, J=5,2, 13,2 Гц, 1Н), 4,40-4,31 (m, 1Н), 4,28-4,14 (m, 2Н), 3,99 (d, J=13,2 Гц, 2Н), 3,83 (t, J=6,4 Гц, 2Н), 3,58-3,51 (m, 2Н), 3,34-3,21 (m, 3Н), 3,16-3,04 (m, 4Н), 3,03-2,84 (m, 3Н), 2,62-2,56 (m, 1Н), 2,44-2,35 (m, 1Н), 2,16-2,02 (m, 1Н), 2,01-1,92 (m, 1Н), 1,83-1,63 (m, 5Н), 1,46-1,35 (m, 2Н).
[727] Синтез 2-(2,6-диоксопиперидин-3-ил)-5-(4-(5-(4-((1R,2S)-6-гидрокси-2-фенил-1,2,3,4-тетрагидронафталин-1-ил)фенокси)пентил)пиперазин-1-ил)изоиндолин-1,3-диона (иллюстративное соединение 69)

(1R, 2S)-1-[4-(5-Бромпентокси)фенил]-2-фенилтетралин-6-ол (50 мг, 0,11 ммоль, 1,00 экв., полученный на стадии 11 получения иллюстративного соединения 62), 2-(2,6-диоксо-3-пиперидил)-5-пиперазин-1-илизоиндолин-1,3-дион (49 мг, 0,13 ммоль, 1,20 экв., гидрохлорид, полученный на стадии 3 получения иллюстративного соединения 393) и диизопропилэтиламин (70 мг, 0,53 ммоль, 0,1 мл, 5,00 экв.) помещали в пробирку для микроволновой обработки в 1-метил-2-пирролидинон (3 мл). Герметично закрытую пробирку нагревали при 140°С в течение 2 часов с помощью микроволнового излучения. С помощью LC-MS показывали завершение реакции, и необходимое значение MS можно было обнаружить. Реакционную смесь разбавляли водой (15 мл) и экстрагировали этилацетатом (5 мл × 2). Объединенную органическую фазу промывали насыщенным солевым раствором (5 мл × 2), высушивали с помощью безводного сульфата натрия, фильтровали и концентрировали в вакууме. Реакционную смесь фильтровали и очищали с помощью препаративной HPLC (колонка: Phenomenex Synergi С18 150×25 мм, 10 микрон; подвижная фаза: [вода (0,225% муравьиной кислоты)-ACN]; В%: 20%-50%, 10 мин.). Собранную фракцию концентрировали с удалением большей части ацетонитрила и добавляли хлористоводородную кислоту (1 М, 2 мл). Раствор лиофилизировали с получением 2-(2,6-диоксо-3-пиперидил)-5-[4-[5-[4-[(1R,2S)-6-гидрокси-2-фенилтетралин-1-ил]фенокси]пентил]пиперазин-1-ил]изоиндолин-1,3-диона (18,10 мг, 0,02 ммоль, выход 22%, чистота 98%, гидрохлорид) в виде желтого твердого вещества, представляющего собой соль хлористоводородной кислоты. LC-MS (ESI) масса/заряд: 727,3 [М+1]+. 1Н ЯМР (400 МГц, DMSO-d6) δ: 11,10 (s, 1Н), 10,14 (s, 1Н), 9,14 (s, 1Н), 7,76 (d, J=8,4 Гц, 1Н), 7,48 (s, 1Н), 7,35 (d, J=8,4 Гц, 1Н), 7,18-7,09 (m, 3Н), 6,83 (d, J=6,8 Гц, 2Н), 6,66-6,59 (m, 2Н), 6,53 (d, J=8,8 Гц, 2Н), 6,48 (dd, J=2,4, 8,4 Гц, 1Н), 6,27 (d, J=8,8 Гц, 2Н), 5,09 (dd, J=5,2, 13,2 Гц, 1Н), 4,27-4,15 (m, 3Н), 3,83 (t, J=6,4 Гц, 2Н), 3,61-3,50 (m, 2Н), 3,31-3,24 (m, 3Н), 3,17-3,05 (m, 4Н), 3,03-2,82 (m, 3Н), 2,63-2,57 (m, 2Н), 2,17-1,97 (m, 2Н), 1,80-1,63 (m, 5Н), 1,48-1,35 (m, 2Н).
[728] Синтез 3-[5-[4-[[1-[4-[(1R,2S)-6-гидрокси-2-фенилтетралин-1-ил]фенил]-4-пиперидил]метил]пиперазин-1-ил]-1-оксоизоиндолин-2-ил]пиперидин-2,6-диона (иллюстративное соединение 341)
[729] Стадия 1. Получение 6-трет-бутокситетралин-1-она

[730] К перемешиваемому раствору 6-гидрокситетралин-1-она (50 г, 308,29 ммоль, 1 экв.) в безводном дихлорметане (2000 мл) при 0°С добавляли трет-бутил-2,2,2-трихлорэтанимидат (67,36 г, 308,29 ммоль, 55 мл, 1 экв.) и пара-толуолсульфонат пиридиния (7,75 г, 30,83 ммоль, 0,1 экв.). Реакционную смесь перемешивали при 10°С в течение 3 часов. Добавляли дополнительную порцию трет-бутил-2,2,2-трихлорэтанимидата (67,36 г, 308,29 ммоль, 55 мл, 1 экв.) и пара-толуолсульфоната пиридиния (7,75 г, 30,83 ммоль, 0,1 экв.) и реакционную смесь перемешивали при 10°С в течение 15 часов. Данный процесс повторяли три раза. С помощью тонкослойной хроматографии (петролейный эфир : этилацетат = 3:1, Rf=0,8) показывали, что большая часть реагирующего вещества все еще оставалась, реакционную смесь перемешивали при 10°С в течение 72 часов. Реакционную смесь гасили путем добавления раствора гидрокарбоната натрия (1500 мл) при 15°С и затем экстрагировали дихлорметаном (300 мл × 3). Объединенные органические слои промывали солевым раствором (300 мл × 2), высушивали над безводным сульфатом натрия, фильтровали и концентрировали при пониженном давлении. Остаток очищали с помощью хроматографии на силикагеле (петролейный эфир : этилацетат = от 100:1 до 50:1) с получением 6-трет-бутокситетралин-1-она (21 г, 96,20 ммоль, выход 31%) в виде желтого масла. 1Н ЯМР (400 МГц, CDCl3) δ 7,97 (d, J=8,8 Гц, 1Н), 6,91 (dd, J=2,4, 8,8 Гц, 1Н), 6,82 (d, J=2,0 Гц, 1Н), 2,93-3,90 (t, J=6,0 Гц, 2Н), 2,63-2,60 (m, t, J=6,0 Гц, 2Н), 2,13 (m, 2Н), 1,43 (s, 9Н)
[731] Стадия 2. Получение (6-трет-бутокси-3,4-дигидронафталин-1-ила) трифторметансульфонат
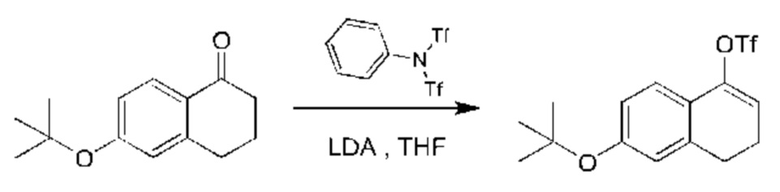
[732] К раствору 6-трет-бутокситетралин-1-она (40 г, 183,24 ммоль, 1 экв.) в тетрагидрофуране (500 мл) добавляли диизопропиламид лития (2 М, 137 мл, 1,5 экв.) при -70°С. Смесь перемешивали при -70°С в течение 1 часа, затем к смеси по каплям добавляли 1,1,1-трифтор-N-фенил-N-(трифторметилсульфонил)метансульфонамид (72,01 г, 201,56 ммоль, 1,1 экв.) в тетрагидрофуране (200 мл). Реакционную смесь перемешивали при 20°С в течение 2 часов. С помощью тонкослойной хроматографии (петролейный эфир : этилацетат = 5:1) показывали завершение реакции. К смеси добавляли насыщенный раствор хлорида аммония (300 мл), органическую фазу отделяли. К смеси добавляли этилацетат (500 мл × 3), полученную смесь промывали солевым раствором (1000 мл × 2). Объединенную органическую фазу высушивали над сульфатом натрия, фильтровали и концентрировали в вакууме. Остаток очищали с помощью хроматографии на силикагеле (петролейный эфир : этилацетат = от 1:0 до 50:1) с получением (6-трет-бутокси-3,4-дигидронафталин-1-ил)трифторметансульфоната (52 г, 144,64 ммоль, выход 78%, чистота 97%) в виде желтого масла. LC-MS (ESI) масса/заряд: 294,9 [М+1-56]+. 1H-ЯМР (400 МГц, CDCl3) δ: 7,30 (d, J=6,4 Гц, 1Н), 6,91 (d, J=8,4 Гц, 1Н), 6,84 (s, 1Н), 5,95 (s, 1Н), 2,93-2,78 (m, 2Н), 2,59-2,46 (m, 2Н), 1,42 (s, 9Н).
[733] Стадия 3. Получение 4-(6-трет-бутокси-3,4-дигидронафталин-1-ил)фенола
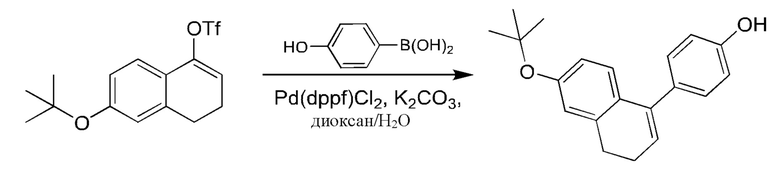
[734] К раствору (6-трет-бутокси-3,4-дигидронафталин-1-ил)трифторметансульфоната (52 г, 148,42 ммоль, 1 экв.), (4-гидроксифенил)бороновой кислоты (24,57 г, 178,11 ммоль, 1,2 экв.) в диоксане (800 мл) и воде (150 мл) добавляли карбонат калия (41,03 г, 296,84 ммоль, 2 экв.) и дихлорид (1,1'-бис(дифенилфосфино)ферроцен)палладия(II) (10,86 г, 14,84 ммоль, 0,1 экв.) в атмосфере азота. Реакционную смесь перемешивали при 100°С в течение 10 часов. С помощью тонкослойной хроматографии (петролейный эфир : этилацетат = 5:1) показывали завершение реакции. Остаток разбавляли водой (500 мл) и экстрагировали этилацетатом (500 мл × 2). Объединенные органические слои промывали солевым раствором (1000 мл × 2), высушивали с помощью безводного сульфата натрия, фильтровали и концентрировали в вакууме. Остаток очищали с помощью хроматографии на силикагеле (петролейный эфир: тетрагидрофуран = от 50:1 до 20:1) с получением 4-(6-трет-бутокси-3,4-дигидронафталин-1-ил)фенола (43 г, 131,46 ммоль, выход 88%, чистота 90%) в виде желтого масла. LCMS (ESI) масса/заряд: 239,1 [М+1-56]+; 1Н-ЯМР (400 МГц, CDCl3) δ 7,23 (d, J=7,6 Гц, 2Н), 6,91 (d, J=8,0 Гц, 1Н), 6,87-6,79 (m, 3Н), 6,73 (d, J=8,4 Гц, 1Н), 5,95 (s, 1Н), 4,83-4,75 (m, 1Н), 2,87-2,73 (m, 2Н), 2,44-2,31 (m, 2Н), 1,37 (s, 9Н)
[735] Стадия 4. Получение 4-(2-бром-6-трет-бутокси-3,4-дигидронафталин-1-ил)фенола

[736] К раствору 4-(6-трет-бутокси-3,4-дигидронафталин-1-ил)фенола (1 г, 3,06 ммоль, 1 экв.) в ацетонитриле (20 мл) тремя порциями добавляли N-бромсукцинимид (489 мг, 2,75 ммоль, 0,9 экв.). Реакционную смесь перемешивали при 20°С в течение 1,5 часа. С помощью LC-MS показывали завершение реакции. Остаток разбавляли водой (20 мл) и экстрагировали этилацетатом (20 мл × 2). Объединенные органические слои промывали солевым раствором (20 мл × 2), высушивали с помощью безводного сульфата натрия, фильтровали и концентрировали в вакууме. Остаток очищали с помощью хроматографии на силикагеле (петролейный эфир : этилацетат = от 1:0 до 20:1) с получением 4-(2-бром-6-трет-бутокси-3,4-дигидронафталин-1-ил)фенола (1 г, 2,46 ммоль, выход 80%, чистота 91%) в виде желтого масла. LC-MS (ESI) масса/заряд: 316,9 [М+1-56]+; 1Н-ЯМР (400 МГц, CDCl3) δ 7,12 (d, J=8,4 Гц, 2Н), 6,90 (d, J=8,0 Гц, 2Н), 6,77 (s, 1Н), 6,69-6,62 (m, 1Н), 6,60-6,53 (m, 1Н), 4,86 (s, 1Н), 2,96 (s, 4Н), 1,35 (s, 9Н).
[737] Стадия 5. Получение 4-(6-трет-бутокси-2-фенил-3,4-дигидронафталин-1-ил)фенола
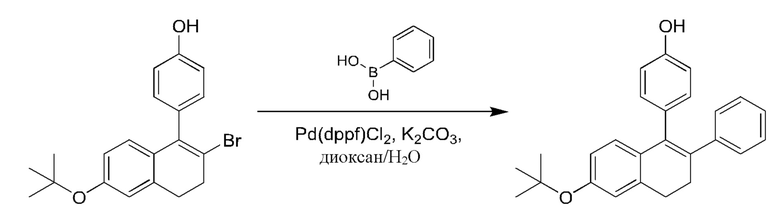
[738] К раствору 4-(2-бром-6-трет-бутокси-3,4-дигидронафталин-1-ил)фенола (1 г, 2,46 ммоль, 1 экв.), фенилбороновой кислоты (314 мг, 2,58 ммоль, 1,05 экв.) в диоксане (10 мл) и воде (2 мл) добавляли карбонат калия (678 мг, 4,91 ммоль, 2 экв.) и дихлорид (1,1'-бис(дифенилфосфино)ферроцен)палладия(II) (179 мг, 0,24 ммоль, 0,1 экв.) в атмосфере азота. Реакционную смесь перемешивали при 100°С в течение 12 часов. С помощью LC-MS показывали завершение реакции. Остаток разбавляли водой (20 мл) и экстрагировали этилацетатом (20 мл × 2). Объединенные органические слои промывали солевым раствором (20 мл × 3), высушивали с помощью безводного сульфата натрия, фильтровали и концентрировали в вакууме. Остаток очищали с помощью хроматографии на силикагеле (петролейный эфир : этилацетат = от 1:0 до 10:1) с получением 4-(6-трет-бутокси-2-фенил-3,4-дигидронафталин-1-ил)фенола (930 мг, 2,35 ммоль, выход 95%, чистота 93%) в виде оранжевого масла. LCMS(ESI) масса/заряд: 314,1 [М+1-56]+; 1H-ЯМР (400 МГц, CDCl3) δ 7,16-7,09 (m, 2Н), 7,08-6,99 (m, 3Н), 6,97-6,89 (m, 2Н), 6,86-6,82 (m, 1Н), 6,74-6,66 (m, 4Н), 4,70 (s, 1Н), 2,99-2,89 (m, 2Н), 2,84-2,75 (m, 2Н), 1,37 (s, 9Н)
[739] Стадия 6. Получение 4-(6-трет-бутокси-2-фенилтетралин-1-ил)фенола

[740] К раствору 4-(6-трет-бутокси-2-фенил-3,4-дигидронафталин-1-ил)фенола (930 мг, 2,35 ммоль, 1 экв.) в тетрагидрофуране (20 мл) и метаноле (4 мл) добавляли катализатор, представляющий собой палладий на активированном угле (100 мг, чистота 10%) в атмосфере азота. Суспензию дегазировали под вакуумом и три раза продували водородом. Смесь перемешивали в атмосфере водорода (50 фунтов/кв. дюйм) при 30°С в течение 36 часов. С помощью LC-MS показывали завершение реакции. Реакционную смесь фильтровали и раствор концентрировали. Полученный материал непосредственно применяли на следующей стадии без дополнительной очистки с получением цис-4-(6-трет-бутокси-2-фенилтетралин-1-ил)фенола (870 мг, 2,14 ммоль, выход 91%, чистота 91%) в виде белого твердого вещества. LC-MS (ESI) масса/заряд: 317,0 [М+1-56]+; 1Н-ЯМР (400 МГц, CDCl3) δ 7,22-7,12 (m, 3Н), 6,89-6,78 (m, 4Н), 6,74 (dd, J=2,0, 8,4 Гц, 1Н), 6,45 (d, J=8,4 Гц, 2Н), 6,27 (d, J=8,4 Гц, 2Н), 4,51 (s, 1Н), 4,25 (d, J=4,8 Гц, 1Н), 3,38 (dd, J=3,2, 12,8 Гц, 1Н), 3,08-2,99 (m, 2Н), 2,27-2,08 (m, 1Н), 1,87-1,76 (m, 1Н), 1,37 (s, 9Н)
[741] Стадия 7. Получение WX-ARV-HD-012-E1, 4-[(1S,2R)-6-трет-бутокси-2-фенилтетралин-1-ил] фенола

[742] 4-(6-трет-Бутокси-2-фенилтетралин-1-ил)фенол (870 мг, 2,13 ммоль, 1 экв.) подвергали сверхкритической флюидной хроматографии для хирального разделения (колонка: AD, 250 мм × 30 мм. 5 мкм; подвижная фаза: 0,1% гидроксид аммония в метаноле. 20%-20%. 4,2 мин. для каждого прогона) с получением 4-[(1S,2R)-6-трет-бутокси-2-фенилтетралин-1-ил]фенола (420 мг, 1,04 ммоль, выход 97%, чистота 92%) в виде первой фракции и 4-[(1R,2S)-6-трет-бутокси-2-фенилтетралин-1-ил] фенола (420 мг, 1,04 ммоль, выход 97%, чистота 92%) в виде второй фракции. Фракция 1: [α]D=+336,9 (С=0,50 г/100 мл в этилацетате, 25°С), LC-MS (ESI) масса/заряд: 395,1 [М+23]+; 1H ЯМР (400 МГц, DMSO-d6) δ 9,02 (s, 1Н), 7,20-7,07 (m, 3Н), 6,87-6,79 (m, 3Н), 6,79-6,72 (m, 1Н), 6,71-6,64 (m, 1Н), 6,36 (d, J=8,4 Гц, 2Н), 6,15 (d, J=8,4 Гц, 2Н), 4,19 (d, J=4,8 Гц, 1Н), 3,31-3,26 (m, 1Н), 3,09-2,89 (m, 2Н), 2,17-2,04 (m, 1Н), 1,79-1,65 (m, 1Н), 1,29 (s, 9Н). Фракция 2: [α]D=-334,1 (С=0,50 г/100 мл в этилацетате, 25°C), LC-MS (ESI) масса/заряд: 395,2 [М+23]+; 1Н-ЯМР (400 МГц, DMSO-d) δ: 9,02 (s, 1Н), 7,21-7,06 (m, 3Н), 6,88-6,78 (m, 3Н), 6,78-6,72 (m, 1Н), 6,71-6,64 (m, 1Н), 6,36 (d, J=8,4 Гц, 2Н), 6,15 (d, J=8,4 Гц, 2H), 4,19 (d, J=4,8 Гц, 1Н), 3,30-3,27 (m, 1Н), 3,08-2,90 (m, 2Н), 2,16-2,04 (m, 1Н), 1,79-1,65 (m, 1Н), 1,29 (s, 9Н).
[743] Стадия 8. Получение 4-(6-бензилокси-2-фенил-3,4-дигидронафталин-1-ил)фенил]1,1,2,2,3,3,4,4,4-нонафторбутан-1-сульфоната

[744] К раствору 4-[(1R,2S)-6-трет-бутокси-2-фенилтетралин-1-ил]фенола (1 г, 2,68 ммоль, 1 экв.) и 1,1,2,2,3,3,4,4,4-нонафторбутан-1-сульфонилфторида (811 мг, 2,68 ммоль, 1 экв.) в тетрагидрофуране (5 мл) и ацетонитриле (5 мл) добавляли карбонат калия (557 мг, 4,03 ммоль, 1,5 экв.). Реакционную смесь перемешивали при 25°С в течение 16 часов. TLC (петролейный эфир : этилацетат = 10:1) указала, что исходное вещество было полностью израсходовано, и образовалось одно новое пятно. Реакционную смесь концентрировали при пониженном давлении. Остаток очищали с помощью хроматографии на силикагеле (петролейный эфир : этилацетат = от 1:0 до 50:1). Получали необходимое соединение, [4-[(1R,2S)-6-трет-бутокси-2-фенилтетралин-1-ил]фенил]1,1,2,2,3,3,4,4,4-нонафторбутан-1-сульфонат (1,6 г, 2,44 ммоль, выход 91%), в виде бесцветного масла. 1H ЯМР (400 МГц, CDCl3) δ 7,21-7,11 (m, 3Н), 6,94-6,86 (m, 3Н), 6,84-6,73 (m, 4Н), 6,46 (d, J=8,8 Гц, 2Н), 4,33 (d, J=5,2 Гц, 1Н), 3,50-3,40 (m, 1Н), 3,16-2,95 (m, 2Н), 2,20-2,02 (m, 1Н), 1,91-1,79 (m, 1Н), 1,38 (s, 9Н)
[745] Стадия 9. Получение 1-[4-(6-бензилокси-2-фенил-3,4-дигидронафталин-1-ил)фенил]-4-(диметоксиметил)пиперидина

[746] Смесь [4-[(1R,2S)-6-трет-бутокси-2-фенилтетралин-1-ил]фенил]1,1,2,2,3,3,4,4,4-нонафторбутан-1-сульфоната (1,6 г, 2,44 ммоль, 1 экв.), 4-(диметоксиметил)пиперидина (584 мг, 3,67 ммоль, 1,5 экв.), трет-бутоксида натрия (705 мг, 7,33 ммоль, 3 экв.), ацетата палладия (82 мг, 0,37 ммоль, 0,15 экв.) и дициклогексилфосфино-2',4',6'-триизопропилбифенила (233 мг, 0,49 ммоль, 0,2 экв.) в толуоле (30 мл) дегазировали и три раза продували азотом и затем смесь перемешивали при 90°С в течение 16 часов в атмосфере азота. С помощью LC-MS показывали один основной пик с определенным необходимым значением MS. TLC (петролейный эфир : этилацетат = 10:1) указала, что исходное вещество было полностью израсходовано, и образовалось одно новое пятно. Смесь охлаждали, разбавляли этилацетатом (50 мл), фильтровали через подушку из целита, осадок на фильтре промывали этилацетатом (30 мл). Фильтрат концентрировали. Остаток очищали с помощью хроматографии на силикагеле (петролейный эфир : этилацетат = от 100:1 до 10:1). Получали необходимое соединение, 1-[4-[(1R,2S)-6-трет-бутокси-2-фенилтетралин-1-ил]фенил]-4-(диметоксиметил)пиперидин (1,1 г, 2,14 ммоль, выход 87%), в виде белого твердого вещества. LC-MS (ESI) масса/заряд: 514,3 [М+1]+; 1H ЯМР (400 МГц, CDCl3) δ 7,21-7,11 (m, 3Н), 6,88-6,78 (m, 4Н), 6,73 (dd, J=2,4, 8,0 Гц, 1Н), 6,57 (d, J=8,4 Гц, 2Н), 6,27 (d, J=8,8 Гц, 2Н), 4,23 (d, J=4,8 Гц, 1Н), 4,06 (d, J=7,2 Гц, 1Н), 3,63-3,52 (m, 2Н), 3,41-3,30 (m, 7Н), 3,13-2,96 (m, 2Н), 2,54 (d, J=2,0, 12,0 Гц, 2Н), 2,28-2,10 (m, 1Н), 1,85-1,63 (m, 4Н), 1,49-1,31 (m, 11Н).
[747] Стадия 10. Получение 1-[4-[(1R,2S)-6-гидрокси-2-фенилтетралин-1-ил]фенил]пиперидин-4-карбальдегида

[748] К раствору 1-[4-[(1R,2S)-6-трет-бутокси-2-фенилтетралин-1-ил]фенил]-4-(диметоксиметил)пиперидина (1,1 г, 2,14 ммоль, 1 экв.) в тетрагидрофуране (45 мл) добавляли серную кислоту (2 М, 43 мл, 40 экв.). Реакционную смесь перемешивали при 70°С в течение 1 часа. LC (петролейный эфир : этилацетат = 3:1) указала, что исходное вещество было полностью израсходовано, и образовалось одно новое пятно. Реакционную смесь гасили путем добавления насыщенного раствора бикарбоната натрия до рН=7~8 и экстрагировали этилацетатом (20 мл × 2). Объединенные органические слои промывали солевым раствором (20 мл), высушивали над сульфатом натрия, фильтровали и концентрировали при пониженном давлении. Остаток применяли на следующей стадии без дополнительной очистки. Получали необходимое соединение, 1-[4-[(1R,2S)-6-гидрокси-2-фенилтетралин-1-ил]фенил]пиперидин-4-карбальдегид (900 мг, 2,14 ммоль, выход 99%, чистота 97%), в виде светло-желтого твердого вещества. LCMS MS (ESI) масса/заряд: 412,1 [М+1]+
[749] Стадия 11. Получение 3-[5-[4-[[1-[4-[(1R,2S)-6-гидрокси-2-фенилтетралин-1-ил]фенил]-4-пиперидил]метил]пиперазин-1-ил]-1-оксоизоиндолин-2-ил]пиперидин-2,6-диона (иллюстративное соединение 341)

[750] К раствору гидрохлорида 3-(1-оксо-5-пиперазин-1-илизоиндолин-2-ил)пиперидин-2,6-диона (319 мг, 0,87 ммоль, полученный на стадии 17, описанной для иллюстративного соединения 62) в метаноле (4 мл) и дихлорметане (4 мл) добавляли ацетат натрия (120 мг, 1,46 ммоль, 2 экв.). Смесь перемешивали при 20°С в течение 0,5 ч., затем к смеси добавляли 1-[4-[(1R,2S)-6-гидрокси-2-фенилтетралин-1-ил]фенил]пиперидин-4-карбальдегид (300 мг, 0,73 ммоль, 1 экв.) и пианоборгидрид натрия (137 мг, 2,19 ммоль, 3 экв.). Смесь перемешивали при 20°С в течение 12 ч. С помощью LC-MS показывали, что исходное вещество было полностью израсходовано, и определили один основной пик с необходимым значением MW. Реакционную смесь концентрировали при пониженном давлении. Остаток очищали с помощью препаративной HPLC (колонка Phenomenex lima С18, 250×50 мм, 10 мкм; подвижная фаза: [вода (0,05% HCl)-ацетонитрил]; В%: ацетонитрил 10%-40% за 30 мин.). Получали необходимое соединение, 3-[5-[4-[[1-[4-[(1R,2S)-6-гидрокси-2фенилтетралин-1-ил]фенил]-4-пиперидил]метил]пиперазин-1-ил]-1-оксоизоиндолин-2-ил]пиперидин-2,6-дион (288,4 мг, 0,37 ммоль, выход 51%), в виде белого твердого вещества, представляющего собой гидрохлоридную соль. LC-MS (ESI) масса/заряд: 724,4 [М+1]+; 1Н ЯМР (400 МГц, DMSO-d6) δ 10,97 (s, 1Н), 10,83 (s, 0,9Н, HCl), 7,60 (d, J=8,5 Гц, 1Н), 7,40 (br s, 2Н), 7,22-7,11 (m, 5Н), 6,83 (d, J=6,0 Гц, 2H), 6,69-6,63 (m, 2Н), 6,58-6,47 (m, 3Н), 5,07 (dd, J=5,2, 13,2 Гц, 1Н), 4,41-4,30 (m, 2Н), 4,28-4,21 (m, 1Н), 4,00 (d, J=12,7 Гц, 2H), 3,61 (d, J=11,0 Гц, 2H), 3,54-3,36 (m, 6Н), 3,16 (br s, 4H), 3,06-2,84 (m, 3Н), 2,76-2,53 (m, 1Н), 2,43-2,33 (m, 1Н), 2,27 (br s, 1H), 2,16-2,04 (m, 3H), 2,02-1,69 (m, 5H).
[751] Синтез 3-[5-[4-[2-[1-[4-[(1R,2S)-6-гидрокси-2-фенилтетралин-1-ил]фенил]-4-пиперидил]этил]пиперазин-1-ил]-1-оксоизоиндолин-2-ил]пиперидин-2,6-диона (иллюстративное соединение 343)
[752] Стадия 1. Получение бензил-4-(2-гидроксиэтил)пиперидин-1-карбоксилата
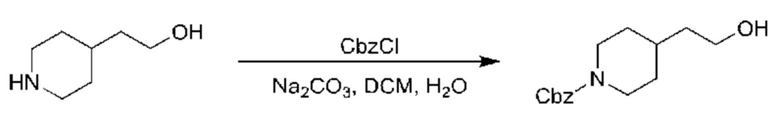
[753] К раствору 2-(4-пиперидил)этанола (5 г, 38,70 ммоль, 1 экв.) в дихлорметане (100 мл) добавляли карбонат натрия (18,5 г, 174,2 ммоль, 4,5 экв.) в воде (100 мл) при 0°С и добавляли по каплям бензилхлорформиат (7,3 г, 42,6 ммоль, 6 мл, 1,1 экв.). Смесь перемешивали при 20°С в течение 12 часов. Смесь разбавляли водой (100 мл), экстрагировали дихлорметаном (100 мл × 2). Объединенные органические слои промывали солевым раствором (100 мл × 2), высушивали над сульфатом натрия, фильтровали и концентрировали при пониженном давлении. Остаток очищали с помощью хроматографии на силикагеле (петролейный эфир/этилацетат = от 10:1 до 2:1). Получали бензил-4-(2-гидроксиэтил)пиперидин-1-карбоксилат (9,9 г, 37,40 ммоль, выход 48%) в виде бесцветного масла. 1Н ЯМР (400 МГц, CDCl3) δ 7,43-7,30 (m, 5Н), 5,14 (s, 2Н), 4,30-4,14 (m, 2Н), 3,73 (t, 2Н), 2,80 (s, 2Н), 1,72 (d, 2Н), 1,68-1,61 (m, 1Н), 1,54 (m, 2Н), 1,30-1,24 (m, 1Н), 1,17 (d, 2Н).
[754] Стадия 2. Получение 4-(2-оксоэтил)пиперидин-1-карбоксилата
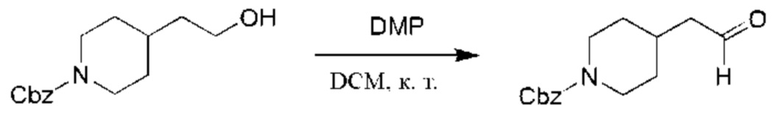
[755] К раствору бензил-4-(2-гидроксиэтил)пиперидин-1-карбоксилата (9 г, 34,20 ммоль, 1,0 экв.) в дихлорметане (150 мл) добавляли реагент Десса-Мартина (15,9 г, 37,6 ммоль, 11,6 мл, 1,1 экв.) при 0°С. Смесь перемешивали при 20°С в течение 3 часов. Реакционную смесь гасили путем добавления насыщенного раствора бикарбоната натрия (50 мл) при 15°С и фильтровали с удалением нерастворимого остатка, затем разбавляли дихлорметаном 100 мл. Органический слой промывали солевым раствором 60 мл (20 мл × 3), высушивали над сульфатом натрия, фильтровали и концентрировали при пониженном давлении. Остаток очищали с помощью хроматографии на силикагеле (петролейный эфир/этилацетат = от 1/0 до 5:1) с получением бензил-4-(2-оксоэтил)пиперидин-1-карбоксилата (7,3 г, 28,1 ммоль, выход 82%) в виде желтого масла. 1Н ЯМР (400 МГц, CDCl3) δ = 10,12-9,46 (m, 1Н), 7,60-7,07 (m, 5Н), 5,04 (s, 2Н), 4,36-3,89 (m, 2Н), 2,74 (s, 2Н), 2,40-2,24 (m, 2Н), 2,09-1,91 (m, 1Н), 1,63 (d, J=12,2 Гц, 2Н), 1,30-1,09 (m, 2Н).
[756] Стадия 3. Получение бензил-4-(2,2-диметоксиэтил)пиперидин-1-карбоксилата

[757] К раствору бензил-4-(2-оксоэтил)пиперидин-1-карбоксилата (8 г, 30,60 ммоль, 1 экв.) в метиловом спирте (80 мл) добавляли триметоксиметан (16,2 г, 153,1 ммоль, 16,8 мл, 5 экв.) и 4-метилбензолсульфоновую кислоту (291 мг, 1,5 ммоль, 0,05 экв.). Смесь перемешивали при 15°С в течение 1 часа. Реакционную смесь гасили путем добавления воды (50 мл) при 15°С и затем разбавляли 100 мл дихлорметана. Органический слой промывали солевым раствором (20 мл × 3), высушивали над сульфатом натрия, фильтровали и концентрировали при пониженном давлении с получением бензил-4-(2,2-диметоксиэтил)пиперидин-1-карбоксилата (9,3 г, 30,1 ммоль, выход 98%) в виде желтого масла. 1Н ЯМР (400 МГц, CDCl3) δ 7,37-7,11 (m, 5Н), 5,04 (s, 2Н), 4,39 (t, J=5,6 Гц, 1Н), 4,07 (s, 2Н), 3,31-3,12 (m, 6Н), 2,70 (s, 2Н), 1,70-1,56 (m, 2Н), 1,54-1,41 (m, 3Н), 1,19-0,99 (m, 2Н).
[758] Стадия 4. Получение 4-(2,2-диметоксиэтил)пиперидина

[759] Смесь бензил-4-(2,2-диметоксиэтил)пиперидин-1-карбоксилата (9,3 г, 30,10 ммоль, 1 экв.) и катализатора, представляющего собой палладий на активированном угле (1 г, 3 ммоль, чистота 10%, 0,1 экв.), в метилом спирте (130 мл) дегазировали и 3 раза продували водородом. Смесь перемешивали при 15°С в течение 15 часов в атмосфере водорода при 15 фунтов/кв. дюйм. Реакционную смесь фильтровали и концентрировали при пониженном давлении с получением 4-(2,2-диметоксиэтил)пиперидина (5 г, 28,9 ммоль, выход 96%) в виде желтого масла. 1Н ЯМР (400 МГц, CDCl3) δ 4,48 (t, J=5,6 Гц, 1Н), 3,39-3,26 (m, 6Н), 3,05 (d, J=12,0 Гц, 2Н), 2,60 (dt, J=2,5, 12,2 Гц, 2Н), 1,87 (s, 1Н), 1,69 (d, J=12,8 Гц, 2Н), 1,59-1,47 (m, 3Н), 1,27-1,00 (m, 2Н).
[760] Стадия 5. Получение 1,1-[4-(6-бензилокси-2-фенил-3,4-дигидронафталин-1-ил)фенил]-4-(2,2-диметоксиэтил)пиперидина
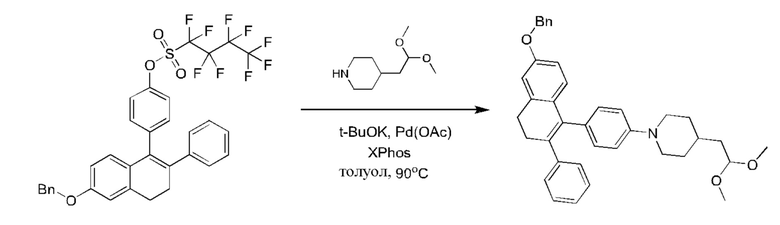
[761] Смесь [4-(6-бензилокси-2-фенил-3,4-дигидронафталин-1-ил)фенил]1,1,2,2,3,3,4,4,4-нонафторбутан-1-сульфоната (3 г, 4,37 ммоль, 1 экв., полученного с применением того же способа, как описано для иллюстративного соединения 341), 4-(2,2-диметоксиэтил)пиперидина (1,14 г, 6,6 ммоль, 1,5 экв.), ацетата палладия (147,15 мг, 0,66 ммоль, 0,15 экв.), трет-бутоксида натрия (1,3 г, 13,1 ммоль, 3 экв.) и дициклогексилфосфино-2',4',6'-триизопропилбифенила (624,9 мг, 1,3 ммоль, 0,3 экв.) в толуоле (50 мл) дегазировали и 3 раза продували азотом. Смесь перемешивали при 90°С в течение 16 часов в атмосфере азота. Реакционную смесь фильтровали и концентрировали при пониженном давлении. Остаток очищали с помощью хроматографии на силикагеле (петролейный эфир/этилацетат = от 1/0 до 15:1) с получением 1-[4-(6-бензилокси-2-фенил-3,4-дигидронафталин-1-ил)фенил]-4-(2,2-диметоксиэтил)пиперидина (2,2 г, 3,93 ммоль, выход 90%) в виде белого твердого вещества. 1Н ЯМР (400 МГц, CDCl3) δ=7,47-7,30 (m, 5Н), 7,15-7,07 (m, 2Н), 7,07-7,00 (m, 3Н), 6,92 (d, J=8,5 Гц, 2Н), 6,86 (d, J=2,3 Гц, 1Н), 6,79 (dd, J=5,6, 8,4 Гц, 3Н), 6,67 (dd, J=2,5, 8,5 Гц, 1Н), 5,07 (s, 2Н), 4,53 (t, J=5,5 Гц, 1Н), 3,64 (d, J=12,3 Гц, 2Н), 3,34 (s, 6Н), 3,02-2,87 (m, 2Н), 2,83-2,73 (m, 2Н), 2,67 (t, J=11,3 Гц, 2Н), 1,83 (d, J=12,5 Гц, 2Н), 1,57 (s, 3Н), 1,49-1,32 (m, 2Н).
[762] Стадия 6. Получение 1-[4-[4-(2,2-диметоксиэтил)-1-пиперидил]фенил]-2-фенилтетралин-6-ола
[763] С помощью гидрогенизации бензилового эфира из стадии 5 с применением той же процедуры, как описано для иллюстративного соединения 341, получали необходимый фенол. 1Н ЯМР (400 МГц, CDCl3) δ 7,19-7,12 (m, 3Н), 6,85-6,77 (m, 3Н), 6,70 (d, J=2,6 Гц, 1Н), 6,58 (d, J=8,7 Гц, 2Н), 6,53 (dd, J=2,7, 8,3 Гц, 1Н), 6,29 (d, J=8,6 Гц, 2Н), 4,51 (t, J=5,7 Гц, 1Н), 4,20 (d, J=4,9 Гц, 1Н), 3,58-3,46 (m, 2Н), 3,38-3,34 (m, 1Н), 3,33 (s, 6Н), 3,11-2,95 (m, 2Н), 2,58 (dt, J=2,3, 12,0 Гц, 2Н), 2,26-2,10 (m, 1Н), 1,89-1,73 (m, 3Н), 1,62-1,55 (m, 2Н), 1,54-1,46 (m, 1Н), 1,42-1,29 (m, 2Н).
[764] Стадия 7. Получение (1S,2R)-1-[4-[4-(2,2-диметоксиэтил)-1-пиперидил]фенил]-2-фенилтетралин-6-ола и и (1S,2R)-1-[4-[4-(2,2-диметоксиэтил)-1-пиперидил]фенил]-2-фенилтетралин-6-ола

1-[4-[4-(2,2-Диметоксиэтил)-1-пиперидил]фенил]-2-фенилтетралин-6-ол из стадии 6 (0,5 г, 1,1 ммоль, 1 экв.) подвергали разделению с помощью SFC с применением хиральной колонки (колонка: AD, 250 мм × 30 мм, 10 мкм; подвижная фаза: (0,1% гидроксид аммония в метиловом спирте, 40%-40%, каждый прогон 4,7 мин.) с получением первой фракции, представляющей собой (1S,2R)-1-[4-[4-(2,2-диметоксиэтил)-1-пиперидил]фенил]-2-фенилтетралин-6-ол (0,23 г, 0,49 ммоль, выход 92%, чистота 100%) в виде бесцветного масла, и вторая фракция обеспечила получение (1R,2S)-1-[4-[4-(2,2-диметоксиэтил)-1-пиперидил]фенил]-2-фенилтетралин-6-ола (0,23 г, 0,49 ммоль, выход 92%, чистота 100%) в виде бесцветного масла. LCMS (ESI) масса/заряд: 472,4 [М+1]+.
[765] Стадия 8. Получение 2-[1-[4-[(1R,2S)-6-гидрокси-2-фенилтетралин-1-ил]фенил]-4-пиперидил]ацетальдегида
[766] Данный альдегид получали с применением того же способа, как описано для иллюстративного соединения 341. 1Н ЯМР (400 МГц, CDCl3) δ=9,95-9,73 (m, 1Н), 7,18-7,13 (m, 3Н), 6,88-6,78 (m, 3Н), 6,71 (d, J=2,5 Гц, 1Н), 6,58 (dd, J=2,6, 8,2 Гц, 3Н), 6,30 (d, J=8,3 Гц, 2Н), 4,80-4,52 (m, 1Н), 4,21 (d, J=5,1 Гц, 1Н), 3,84-3,72 (m, 2Н), 3,53 (s, 2Н), 3,42-3,27 (m, 1Н), 3,05 (d, J=4,5 Гц, 1Н), 2,64 (s, 2Н), 2,41 (d, J=5,8 Гц, 2Н), 2,25-2,11 (m, 1Н), 2,08-1,92 (m, 1Н), 1,80 (d, J=12,9 Гц, 2Н), 1,01-0,66 (m, 1Н).
[767] Стадия 9. Получение 3-[5-[4-[2-[1-[4-[(1R,2S)-6-гидрокси-2-фенилтетралин-1-ил]фенил]-4-пиперидил]этил]пиперазин-1-ил]-1-оксоизоиндолин-2-ил]пиперидин-2,6-диона (иллюстративное соединение 343)

[768] К раствору гидрохлорида 3-(1-оксо-5-пиперазин-1-илизоиндолин-2-ил)пиперидин-2,6-диона (85 мг, 0,24 ммоль, 1 экв., полученного как описано для иллюстративного соединения 62) в дихлорметане (1 мл) и метиловом спирте (5 мл) одной порцией добавляли ацетат натрия (77 мг, 0,94 ммоль, 4 экв.) при 25°С. Смесь перемешивали при 25°С в течение 1 часа и добавляли 2-[1-[4-[(1R,2S)-6-гидрокси-2-фенилтетралин-1-ил]фенил]-4-пиперидил]ацетальдегид (100 мг, 0,24 ммоль, 1 экв.) и уксусную кислоту (525 мг, 8,74 ммоль, 37,2 экв), смесь перемешивали при 25°С в течение 1 часа. Затем одной порцией добавляли цианоборгидрид натрия (29 мг, 0,47 ммоль, 2 экв.), смесь перемешивали при 25°С в течение 1 часа. Реакционную смесь концентрировали при пониженном давлении. Остаток очищали с помощью препаративной HPLC (колонка: Phenomenex Synergi С18 150×25 мм, 10 мкм; подвижная фаза: [вода (0,05% хлористоводородной кислоты)-ацетонитрил]; В%: 15%-35%, 7,8 мин.) с получением 3-[5-[4-[2-[1-[4-[(1R,2S)-6-гидрокси-2фенилтетралин-1-ил]фенил]-4-пиперидил]этил]пиперазин-1-ил]-1-оксоизоиндолин-2-ил]пиперидин-2,6-диона (117,7 мг, выход 64%, чистота 99%) в виде грязно-белого твердого вещества, представляющего собой гидрохлоридную соль. LC-MS (ESI) масса/заряд: 738,3 [М+1]+; 1Н ЯМР (400 МГц, DMSO) δ 11,24 (s, 1Н), 10,95 (s, 1Н), 7,58 (d, J=8,5 Гц, 1Н), 7,48 (d, J=6,8 Гц, 2Н), 7,20-7,11 (m, 5Н), 6,83 (d, J=6,9 Гц, 2Н), 6,69-6,61 (m, 2Н), 6,53 (d, J=7,3 Гц, 3Н), 5,06 (dd, J=4,6, 13,2 Гц, 1Н), 4,42-4,18 (m, 3Н), 4,00 (d, J=12,8 Гц, 2Н), 3,58 (d, J=10,9 Гц, 2Н), 3,47-3,27 (m, 6Н), 3,23-3,03 (m, 4Н), 3,02-2,84 (m, 3Н), 2,71-2,52 (m, 1Н), 2,39 (d, J=13,7 Гц, 2Н), 2,10-1,71 (m, 10Н).
[769] Синтез 2-(2,6-диоксопиперидин-3-ил)-5-(4-((1-(4-((1R,2S)-6-гидрокси-2-фенил-1,2,3,4-тетрагидронафталин-1-ил)фенил)пиперидин-4-ил)метил)пиперазин-1-ил)изоиндолин-1,3-диона (иллюстративное соединение 393)
[770] Стадия 1. Получение 2-(2,6-диоксопиперидин-3-ил)-5-фторизоиндолин-1,3-диона

[771] К раствору 5-фторизобензофуран-1,3-диона (15 г, 90,30 ммоль, 1,00 экв.) в уксусной кислоте (200 мл) добавляли ацетат натрия (14,8 г, 180,60 ммоль, 2,00 экв.) и гидрохлорид 3-аминопиперидин-2,6-диона (14,9 г, 90,30 ммоль, 1,00 экв.). Смесь перемешивали при 120°С в течение 12 часов. Реакционную смесь концентрировали при пониженном давлении с удалением большей части уксусной кислоты. Остаток выливали в воду (200 мл) и перемешивали в течение 10 минут. Смесь фильтровали. Осадок на фильтре промывали водой (30 мл × 2) и высушивали с получением 2-(2,6-диоксо-3-пиперидил)-5-фторизоиндолин-1,3-диона (24 г, 86,89 ммоль, выход 96%) в виде грязно-белого твердого вещества. LC-MS (ESI) масса/заряд: 277,1 [М+1]+; 1Н-ЯМР (400 МГц, DMSO-d6) δ 11,13 (s, 1Н), 8,00 (dd, J=4,4, 8,4 Гц, 1Н), 7,84 (dd, J=2,4, 7,2 Гц, 1Н), 7,75-7,68 (m, 1Н), 5,16 (dd, J=5,2, 12,8 Гц, 1Н), 2,95-2,84 (m, 1Н), 2,66-2,52 (m, 2Н), 2,14-2,02 (m, 1Н).
[772] Стадия 2. Получение трет-бутил-4-(2-(2,6-диоксопиперидин-3-ил)-1,3-диоксоизоиндолин-5-ил)пиперазин-1-карбоксилата

[773] 2-(2,6-Диоксо-3-пиперидил)-5-фторизоиндолин-1,3-дион (1 г, 3,62 ммоль, 1,00 экв.), трет-бутил-пиперазин-1-карбоксилат (742 мг, 3,98 ммоль, 1,10 экв.) и диизопропилэтиламин (1,4 г, 10,86 ммоль, 1,9 мл, 3,00 экв.) помещали в пробирку для микроволновой обработки в 1-метил-2-пирролидинон (15 мл). Герметично закрытую пробирку нагревали при 140°С в течение 2 часов в условиях нагревания с помощью микроволнового излучения (4 партии параллельно). Реакционную смесь разбавляли водой (120 мл) и экстрагировали этилацетатом (50 мл × 2). Объединенную органическую фазу промывали насыщенным солевым раствором (30 мл × 2), высушивали с помощью безводного сульфата натрия, фильтровали и концентрировали в вакууме. Остаток очищали с помощью колоночной хроматографии (петролейный эфир : этилацетат = от 3:1 до 1:1) с получением трет-бутил-4-[2-(2,6-диоксо-3-пиперидил)-1,3-диоксоизоиндолин-5-ил]пиперазин-1-карбоксилата (4 г, 9,04 ммоль, выход 62%) в виде желтого твердого вещества. LC-MS (ESI) масса/заряд: 343,0 [М-100]+; 1H-ЯМР (400 МГц, CDCl3) δ 8,23 (s, 1Н), 7,71 (d, J=8,4 Гц, 1Н), 7,28 (d, J=2,4 Гц, 1Н), 7,06 (dd, J=2,4, 8,4 Гц, 1Н), 4,95 (dd, J=5,2, 12,4 Гц, 1Н), 3,66-3,57 (m, 4Н), 3,45-3,39 (m, 4Н), 2,94-2,85 (m, 1Н), 2,80-2,71 (m, 1Н), 2,17-2,09 (m, 1Н), 2,07-1,98 (m, 1Н), 1,49 (s, 9Н).
[774] Стадия 3. Получение 2-(2,6-диоксопиперидин-3-ил)-5-(пиперазин-1-ил)изоиндолин-1,3-диона
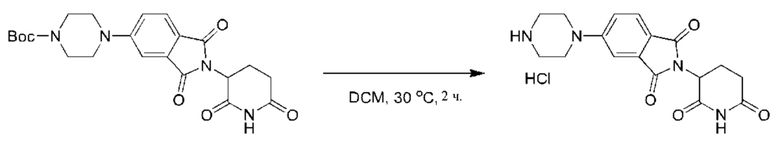
[775] К раствору трет-бутил-4-[2-(2,6-диоксо-3-пиперидил)-1,3-диоксоизоиндолин-5-ил]пиперазин-1-карбоксилата (4 г, 9,04 ммоль, 1,00 экв.) в дихлорметане (20 мл) добавляли смесь хлористоводородная кислота/диоксан (4 М, 22 мл, 10,00 экв.). Смесь перемешивали при 30°С в течение 2 часов. Реакционную смесь концентрировали при пониженном давлении с удалением дихлорметана, диоксана и хлористоводородной кислоты с получением 2-(2,6-диоксо-3-пиперидил)-5-пиперазин-1-ил-изоиндолин-1,3-диона (3,2 г, 8,45 ммоль, выход 93%, гидрохлорид) в виде желтого твердого вещества. LCMS (ESI) масса/заряд: 343,0 [М+1]+; 1Н ЯМР (400 МГц, DMSO-d6) δ 11,10 (s, 1Н), 9,56 (s, 2Н), 7,74 (d, J=8,4 Гц, 1Н), 7,45 (d, J=2,4 Гц, 1Н), 7,33 (dd, J=2,4, 8,4 Гц, 1Н), 5,09 (dd, J=5,2, 13,2 Гц, 1Н), 3,77-3,68 (m, 4Н), 3,25-3,15 (m, 4Н), 2,96-2,83 (m, 1Н), 2,63-2,53 (m, 2Н), 2,08-1,99 (m, 1Н).
[776] Стадия 4. Получение 2-(2,6-диоксопиперидин-3-ил)-5-(4-((1-(4-((1R,2S)-6-гидрокси-2-фенил-1,2,3,4-тетрагидронафталин-1-ил)фенил)пиперидин-4-ил)метил)пиперазин-1-ил)изоиндолин-1,3-диона (иллюстративное соединение 393)

[777] К смеси гидрохлорида 2-(2,6-диоксо-3-пиперидил)-5-пиперазин-1-илизоиндолин-1,3-диона (46 мг, 0,12 ммоль, 1 экв.) и ацетата натрия (15 мг, 0,18 ммоль, 1,5 экв.) в дихлорметане (2 мл) и метаноле (2 мл) добавляли уксусную кислоту (0,4 мл) при 25°С в атмосфере азота. Смесь перемешивали при 25°С в течение 15 минут, затем добавляли 1-(4-((1R,2S)-6-гидрокси-2-фенил-1,2,3,4-тетрагидронафталин-1-ил)фенил)пиперидин-4-карбальдегид (50 мг, 0,12 ммоль, 1 экв., полученный как описано для иллюстративного соединения 341) и смесь перемешивали в течение 0,5 часа. Полученную смесь охлаждали до 0°С, добавляли цианоборгидрид натрия (38 мг, 0,61 ммоль, 5 экв.) и смесь дополнительно перемешивали при 25°С в течение 1 часа. Реакционную смесь концентрировали при пониженном давлении. Остаток очищали с помощью препаративной HPLC с получением 2-(2,6-диоксопиперидин-3-ил)-5-(4-((1-(4-((1R,2S)-6-гидрокси-2-фенил-1,2,3,4-тетрагидронафталин-1-ил)фенил)пиперидин-4-ил)метил)пиперазин-1-ил)изоиндолин-1,3-диона (59,9 мг, 0,08 ммоль, выход 63%) в виде желтого твердого вещества, представляющего собой соль муравьиной кислоты. LC-MS (ESI) масса/заряд: 738,4 [М+1]+; 1Н ЯМР (400 МГц, DMSO-d6) δ 11,08 (s, 1Н), 9,13 (br s, 1Н), 8,19 (s, 1Н), 7,67 (d, J=8,5 Гц, 1Н), 7,33 (s, 1Н), 7,25 (br d, J=8,5 Гц, 1Н), 7,17-7,08 (m, 3Н), 6,83 (br d, J=6,8 Гц, 2H), 6,64 (d, J=8,3 Гц, 1H), 6,60 (d, J=2,3 Гц, 1H), 6,53 (d, J=8,8 Гц, 2H), 6,47 (dd, J=2,4, 8,2 Гц, 1H), 6,19 (d, J=8,7 Гц, 2H), 5,07 (dd, J=5,3, 12,9 Гц, 1H), 4,12 (d, J=4,5 Гц, 1H), 3,50-3,41 (m, 12H), 2,99-2,84 (m, 3H), 2,62-2,53 (m, 3H), 2,23-2,18 (m, 2H), 2,12-1,97 (m, 2H), 1,80-1,61 (m, 4H), 1,23-1,05 (m, 2H).
[778] Синтез 2-(2,6-диоксопиперидин-3-ил)-5-(4-(2-(1-(4-((1R,2S)-6-гидрокси-2-фенил-1,2,3,4-тетрагидронафталин-1-ил)фенил)пиперидин-4-ил)этил)пиперазин-1-ил)изоиндолин-1,3-диона (иллюстративное соединение 395)

К раствору гидрохлорида 2-(2,6-диоксо-3-пиперидил)-5-пиперазин-1-ил-изоиндолин-1,3-диона (107 мг, 0,3 ммоль, 1,2 экв., полученного как описано для иллюстративного соединения 393) в дихлорметане (3 мл) и метаноле (1 мл) добавляли ацетат натрия (38 мг, 0,5 ммоль, 2 экв.) при 25°С. После добавления смесь перемешивали при данной температуре в течение 30 мин. и затем добавляли 2-[1-[4-[(1R,2S)-6-гидрокси-2-фенилтетралин-1-ил]фенил]-4-пиперидил] ацетальдегид (100 мг, 0,3 ммоль, 1 экв., полученного как описано для иллюстративного соединения 343) при 25°С. Полученную смесь перемешивали при 25°С в течение 30 минут. Затем добавляли цианоборгидрид натрия (29 мг, 0,5 ммоль, 2 экв.). Полученную смесь перемешивали при 25°С в течение 1 часа. Реакционную смесь концентрировали при пониженном давлении с удалением растворителя. Остаток очищали с помощью препаративной HPLC (колонка: Phenomenex Synergi С18 150×25 мм, 10 мкм; подвижная фаза: [вода (0,225% муравьиной кислоты) и ацетонитрил]; В%: 16%-40% за 8 мин.) с получением 2-(2,6-диоксо-3-пиперидил)-5-[4-[2-[1-[4-[(1R,2S)-6-гидрокси-2-фенилтетралин-1-ил]фенил]-4-пиперидил]этил]пиперазин-1-ил]изоиндолин-1,3-диона (114,8 мг, 0,2 ммоль, выход 65%) в виде желтого твердого вещества, представляющего собой соль муравьиной кислоты. LC-MS (ESI) масса/заряд: 752,3 [М+1]+; 1Н-ЯМР (400 МГц, DMSO-d6) δ 11,08 (s, 1Н), 9,10 (s, 1Н), 8,15 (s, 1Н) 7,68-7,66 (d,1H), 7,31 (s, 1H), 7,25 (d, 1H), 7,20-7,10 (m, 3H), 6,82 (d, 2H), 6,65-6,58 (m, 2H), 6,52-6,40 (m, 3H), 6,19 (d, 2H), 5,08-5,04 (m, 1H), 4,12-4,11 (d, J=4 Гц, 1H), 3,50-3,41 (m 12H), 2,99-2,83 (m, 3H), 2,60-2,52 (m, 3H), 2,40-2,32 (m, 2H), 2,15-1,95 (m, 2H), 1,71 (m, 3H), 1,40 (m, 3H), 1,17 (m, 2H).
[779] Синтез (3S)-3-[5-[4-[[1-[4-[(1R,2S)-6-гидрокси-2-фенилтетралин-1-ил]фенил]-4-пиперидил]метил]пиперазин-1-ил]-1-оксоизоиндолин-2-ил]пиперидин-2,6-диона (иллюстративное соединение 411)
[780] Стадия 1. Получение трет-бутил-(4S)-5-амино-4-(бензилоксикарбониламино)-5-оксопентаноата

Смесь (2S)-2-(бензилоксикарбониламино)-5-трет-бутокси-5-оксопентановой кислоты (20 г, 59,28 ммоль, 1,00 экв.), ди-трет-бутилдикарбоната (94,85 ммоль, 21,79 мл, 1,60 экв.) и пиридина (9,38 г, 118,57 ммоль, 9,57 мл, 2,00 экв.) в 1,4-диоксане (200 мл) дегазировали при 0°С и 3 раза продували азотом, а затем смесь перемешивали при 0°С в течение 0,5 часа в атмосфере азота. Добавляли бикарбонат аммония (14,06 г, 177,85 ммоль, 14,65 мл, 3,00 экв.) при 0°С. Смесь перемешивали при 25°С в течение 16 часов. С помощью LC-MS показывали необходимую массу. Летучие вещества удаляли при пониженном давлении. Остаток разбавляли водой (300 мл) и экстрагировали этилацетатом (300 мл × 1). Объединенную органическую фазу промывали водн. хлористоводородной кислотой (0,5 М, 200 мл × 2), насыщенным раствором бикарбоната натрия (300 мл × 3) и солевым раствором (500 мл × 3), высушивали с помощью безводного сульфата натрия, фильтровали и концентрировали в вакууме с получением неочищенного продукта. Неочищенный продукт растирали (петролейный эфир : этилацетат = 10:1, 300 мл) с получением трет-бутил-(4S)-5-амино-4-(бензилоксикарбониламино)-5-оксопентаноата (19 г, 56,08 ммоль, выход 94%, чистота 99%) в виде белого твердого вещества. LC-MS (ESI) масса/заряд: 359,0 [М+23]+. 1Н-ЯМР (400 МГц, CDCl3) δ 7,39-7,29 (m, 5Н), 6,38 (s, 1Н), 5,74 (d, J=7,2 Гц, 1Н), 5,58 (s, 1Н), 5,11 (s, 2Н), 4,25 (d, J=5,6 Гц, 1Н), 2,55-2,41 (m, 1Н), 2,39-2,27 (m, 1Н), 2,18-2,04 (m, 1Н), 2,02-1,85 (m, 1Н), 1,45 (s, 9Н).
[781] Стадия 2. Получение трет-бутил-(4S)-4,5-диамино-5-оксопентаноата

[782] К раствору трет-бутил-(4S)-5-амино-4-(бензилоксикарбониламино)-5-оксопентаноата (19 г, 56,48 ммоль, 1,00 экв.) в метаноле (200 мл) добавляли палладий на угле (2 г, 10%) в атмосфере азота. Суспензию дегазировали и 3 раза продували водородом. Смесь перемешивали в атмосфере Н2 (50 фунтов/кв. дюйм) при 25°С в течение 16 часов. С помощью тонкослойной хроматографии (петролейный эфир : этилацетат = 1:2) показывали завершение реакции. Реакционную смесь фильтровали и фильтрат концентрировали. Получали соединение, трет-бутил-(4S)-4,5-диамино-5-оксопентаноат (11 г, 54,39 ммоль, выход 96%), в виде светло-зеленого масла. 1Н ЯМР (400 МГц, CDCl3) δ 7,03 (br s, 1Н), 5,55 (br s, 1Н), 3,44 (br s, 1H), 2,49-2,31 (m, 2H), 2,11 (dd, J=6,0, 12,8 Гц, 1H), 1,92-1,76 (m, 1H), 1,66 (s, 2H), 1,45 (s, 9H),
[783] Стадия 3. Получение трет-бутил-4-[2-[(1S)-4-трет-бутокси-1-карбамоил-4-оксобутил]-1-оксоизоиндолин-5-ил]пиперазин-1-карбоксилата

К раствору трет-бутил-4-[3-(бромметил)-4-метоксикарбонилфенил]пиперазин-1-карбоксилата (1,5 г, 3,63 ммоль, 1 экв., полученного на стадии 15 для иллюстративного соединения 62) в ацетонитриле (30 мл) добавляли трет-бутил-(4S)-4,5-диамино-5-оксопентаноат (1,10 г, 5,44 ммоль, 1,5 экв.) и диизопропилэтиламин (1,41 г, 10,89 ммоль, 1,90 мл, 3 экв.). Смесь перемешивали при 80°С в течение 12 часов. С помощью LC-MS показывали завершение реакции. Смесь разбавляли водой (30 мл) и экстрагировали этилацетатом (20 мл × 3). Объединенные органические слои промывали солевым раствором (30 мл × 2), высушивали с помощью безводного сульфата натрия, фильтровали и фильтрат концентрировали в вакууме. Остаток очищали с помощью препаративной HPLC с обращенной фазой (колонка: Phenomenex Synergi Max-RP 250×50 мм, 10 микрон; подвижная фаза: [вода (0,225% муравьиной кислоты)-ацетонитрил]; В%: 40% ацетонитрила -70% ацетонитрила за 30 мин.) с получением трет-бутил-4-[2-[(1S)-4-трет-бутокси-1-карбамоил-4-оксобутил]-1-оксоизоиндолин-5-ил]пиперазин-1-карбоксилата (1,6 г, 2,94 ммоль, выход 81,05%, чистота 92%) в виде грязно-белого твердого вещества. LC-MS (ESI) масса/заряд: 503,2 [М+1]+.
[784] Стадия 4. Получение (3S)-3-(1-оксо-5-пиперазин-1-илизоиндолин-2-ил)пиперидин-2,6-диона

К раствору трет-бутил-4-[2-[(1S)-4-трет-бутокси-1-карбамоил-4-оксобутил]-1-оксоизоиндолин-5-ил]пиперазин-1-карбоксилата (700 мг, 1,39 ммоль, 1 экв.) в ацетонитриле (15 мл) добавляли бензолсульфоновую кислоту (440 мг, 2,79 ммоль, 2 экв). Смесь перемешивали при 85°С в течение 12 часов. С помощью LC-MS показывали завершение реакции. Смесь концентрировали в вакууме. Остаток растирали с этилацетатом (30 мл × 3) с получением (3S)-3-(1-оксо-5-пиперазин-1-илизоиндолин-2-ил)пиперидин-2,6-диона (630 мг, неочищенный) в виде серого твердого вещества. LC-MS (ESI) масса/заряд: 329,1 [М+1]+; 100% ее из анализа посредством хиральной SFC.
[785] Стадия 5. Получение (3S)-3-[5-[4-[[1-[4-[(1R,2S)-6-гидрокси-2-фенилтетралин-1-ил]фенил]-4-пиперидил]метил]пиперазин-1-ил]-1-оксоизоиндолин-2-ил]пиперидин-2,6-диона (иллюстративное соединение 411)
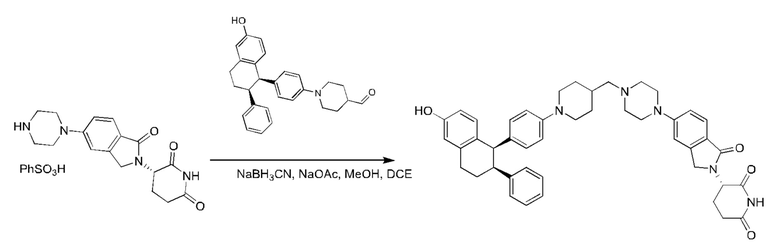
К смеси (3S)-3-(1-оксо-5-пиперазин-1-илизоиндолин-2-ил)пиперидин-2,6-диона (1,30 г, 3,47 ммоль, 1 экв., бензолсульфонат) в дихлорметане (8 мл) и метаноле (32 мл) одной порцией добавляли ацетат натрия (854 мг, 10,41 ммоль, 3 экв.) при 20°С. Смесь перемешивали при 20°С в течение 10 минут. Затем добавляли 1-[4-[(1R,2S)-6-гидрокси-2-фенилтетралин-1-ил]фенил]пиперидин-4-карбальдегид (1 г, 2,43 ммоль, 0,7 экв., полученный как описано для иллюстративного соединения 341). Смесь перемешивали при 20°С в течение 10 минут. После этого одной порцией добавляли уксусную кислоту (0,2 мл) и цианоборгидрид натрия (436 мг, 6,94 ммоль, 2 экв). Смесь перемешивали при 20°С в течение 40 минут. Смесь концентрировали в вакууме и добавляли 50 мл тетрагидрофурана и 20 мл воды. Смесь перемешивали в течение 20 минут. Добавляли насыщенный водный раствор бикарбоната натрия с регулированием рН до 8-9. Водную фазу экстрагировали этилацетатом и тетрагидрофураном (об.:об. = 2:1, 60 мл × 3). Объединенную органическую фазу промывали солевым раствором (60 мл × 1), высушивали с помощью безводного сульфата натрия, фильтровали и концентрировали в вакууме. Остаток очищали с помощью препаративной HPLC с обращенной фазой (колонка: Phenomenex luma С18 250×50 мм, 10 микрон; подвижная фаза: [вода (0,225% муравьиной кислоты) - ацетонитрил]; В%: 20%-50% за 30 мин.). Получали продукт, (3S)-3-[5-[4-[[1-[4-[(1R,2S)-6-гидрокси-2-фенилтетралин-1-ил]фенил]-4-пиперидил]метил]пиперазин-1-ил]-1-оксоизоиндолин-2-ил]пиперидин-2,6-дион (964 мг, 1,23 ммоль, выход 35%, чистота 98%, формиат), в виде белого твердого вещества, представляющего собой соль муравьиной кислоты после лиофилизации. Хиральную чистоту анализировали с помощью хиральной SFC (Chiralcel OJ-3 50×456 мм, 3 микрон; подвижная фаза: 50% этанол (0,05% DEA) в СО2; расход: 3 мл/мин., длина волны: 220 нм) и наблюдаемый tp = 2,89 мин. с de более 95%. [α]D=-267,5 (с=0,2 в DMF, 25°С). LC-MS (ESI) масса/заряд: 724,2 [М+1]+. 1Н ЯМР (400 МГц, DMSO-d6) δ 10,94 (s, 1Н), 8,16 (s, 1Н, формиат), 7,51 (d, J=8,8 Гц, 1Н), 7,21-6,98 (m, 5Н), 6,83 (d, J=6,4 Гц, 2H), 6,68-6,57 (m, 2Н), 6,56-6,44 (m, 3Н), 6,20 (d, J=8,8 Гц, 2H), 5,04 (dd, J=5,2, 13,2 Гц, 1Н), 4,32 (d, J=16,8 Гц, 1Н), 4,19 (d, J=17,2 Гц, 1Н), 4,12 (d, J=4,8 Гц, 1Н), 3,51 (br d, J=10,0 Гц, 4H), 3,27 (br s, 8H), 3,03-2,82 (m, 3Н), 2,63-2,54 (m, 1Н), 2,43-2,28 (m, 2H), 2,19 (d, J=6,8 Гц, 2H), 2,15-2,02 (m, 1Н), 2,01-1,89 (m, 1Н), 1,83-1,51 (m, 4H), 1,28-1,04 (m, 2H).
[786] Свободная несолевая форма, 1Н-ЯМР (400 МГц, DMSO-d6) δ 10,93 (s, 1Н), 9,09 (s, 1Н), 7,51 (d, J=8,8 Гц, 1Н), 7,18-7,09 (m, 3Н), 7,08-7,02 (m, 2Н), 6,83 (d, J=6,4 Гц, 2Н), 6,64 (d, J=8,4 Гц, 1Н), 6,60 (d, J=2,0 Гц, 1Н), 6,53 (d, J=8,8 Гц, 2Н), 6,48 (dd, J=2,4, 8,4 Гц, 1Н), 6,20 (d, J=8,8 Гц, 2Н), 5,04 (dd, J=5,2, 13,2 Гц, 1Н), 4,39-4,27 (m, 1Н), 4,24-4,15 (m, 1Н), 4,12 (d, J=4,8 Гц, 1Н), 3,51 (d, J=9,6 Гц, 2Н), 3,29-3,24 (m, 5Н), 3,03-2,83 (m, 3Н), 2,62-2,54 (m, 4Н), 2,52 (s, 3Н), 2,41-2,36 (m, 1Н), 2,19 (d, J=7,2 Гц, 2Н), 2,15-2,08 (m, 1Н), 2,00-1,89 (m, 1Н), 1,81-1,58 (m, 4Н), 1,22-1,06 (m, 2Н).
[787] Синтез (3R)-3-[5-[4-[[1-[4-[(1R,2S)-6-гидрокси-2-фенилтетралин-1-ил]фенил]-4-пиперидил]метил]пиперазин-1-ил]-1-оксоизоиндолин-2-ил]пиперидин-2,6-диона (иллюстративное соединение 413)
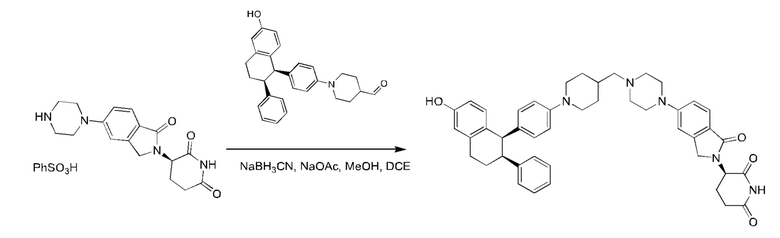
Данное соединение (соль муравьиной кислоты) получали с применением той же процедуры, описанной для получения соединения 411, за исключением того, что применяли (2R)-2-(бензилоксикарбониламино)-5-трет-бутокси-5-оксопентановую кислоту в получении (3R)-3-(1-оксо-5-пиперазин-1-илизоиндолин-2-ил)пиперидин-2,6-дион. Хиральную чистоту выделенной соли муравьиной кислоты анализировали с помощью хиральной SFC при тех же условиях, как и описанные для соединения 411, и наблюдали tp=2,12 мин. с de 100%. [α]D=-224,1 (с=0,1 в DMF, 25°С). LC-MS (ESI) масса/заряд: 724,3 [М+1]+; 1H ЯМР (400 МГц, DMSO-d6) δ 10,95 (s, 1Н), 9,11 (s, 1Н, фенол), 8,15 (s, 0,9Н, формиат), 7,53 (d, J=8,4 Гц, 1Н), 7,19-7,10 (m, 3Н), 7,09-7,01 (m, 2Н), 6,85 (d, J=7,2 Гц, 2Н), 6,69-6,59 (m, 2Н), 6,57-6,45 (m, 3Н), 6,21 (d, J=8,4 Гц, 2Н), 5,05 (dd, J=5,2, 13,2 Гц, 1Н), 4,33 (d, J=16,8 Гц, 1Н), 4,20 (d, J=16,8 Гц, 1Н), 4,14 (d, J=4,4 Гц, 1Н), 3,52 (br d, 4Н), 3,40-3,25 (br, 8Н), 3,05-2,83 (m, 3Н), 2,59 (m, 1Н), 2,47-2,30 (m, 2Н), 2,23 (d, J=6,8 Гц, 2H), 2,16-2,01 (m, 1Н), 2,00-1,91 (m, 1Н), 1,82-1,62 (m, 4Н), 1,25-1,11 (m, 2Н).
[788] Свободная несолевая форма, 1Н ЯМР (400 МГц, DMSO-d6) δ 10,93 (s, 1Н), 9,09 (s, 1Н), 7,51 (d, J=8,8 Гц, 1Н), 7,20-7,08 (m, 3Н), 7,08-7,02 (m, 2Н), 6,83 (d, J=6,4 Гц, 2Н), 6,64 (d, J=8,4 Гц, 1Н), 6,60 (d, J=2,4 Гц, 1Н), 6,53 (d, J=8,8 Гц, 2Н), 6,48 (dd, J=2,4, 8,4 Гц, 1Н), 6,20 (d, J=8,8 Гц, 2Н), 5,04 (dd, J=5,2, 13,2 Гц, 1Н), 4,32 (d, J=17,2 Гц, 1Н), 4,19 (d, J=17 Гц, 1Н), 4,12 (d, J=4,8 Гц, 1Н), 3,51 (br d, J=10,0 Гц, 2Н), 3,29-3,24 (m, 5Н), 3,03-2,83 (m, 3Н), 2,62-2,54 (m, 4Н), 2,52 (br s, 3Н), 2,41-2,36 (m, 1Н), 2,19 (d, J=7,2 Гц, 2H), 2,15-2,08 (m, 1Н), 2,00-1,89 (m, 1Н), 1,81-1,58 (m, 4Н), 1,22-1,06 (m, 2Н).
[789] Синтез 3-[5-[4-[[1-[2-фтор-4-[(1R,2S)-6-гидрокси-2-фенилтетралин-1-ил]фенил]-4-пиперидил]метил]пиперазин-1-ил]-1-оксоизоиндолин-2-ил]пиперидин-2,6-дионв (иллюстративное соединение 419)
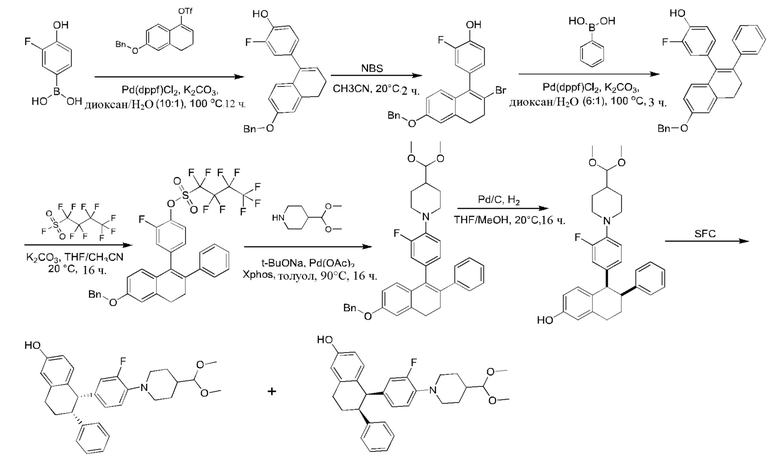

[790] С применением пути синтеза, описанного выше, за тех же условий, описанных для иллюстративного соединения 341 (за исключением того, что применяли 3-F-4-гидроксифенилбороновую кислоту вместо 4-гидроксифенилбороновой кислоты), получали 3-[5-[4-[[1-[2-фтор-4-[(1R,2S)-6-гидрокси-2-фенилтетралин-1-ил]фенил]-4-пиперидил]метил]пиперазин-1-ил]-1-оксоизоиндолин-2-ил]пиперидин-2,6-дион (76,0 мг, 0,09 ммоль, выход 50% в последней стадии) в виде белого твердого вещества, представляющего собой соль муравьиной кислоты. LC-MS (ESI) масса/заряд: 742,3 [М+1]+; 1H-ЯМР (400 МГц, DMSO-d6) δ 10,95 (s, 1Н), 8,18 (s, 0,9Н, формиат), 7,51 (d, J=8,8 Гц, 1Н), 7,20-7,12 (m, 3Н), 7,06-7,04 (m, 2Н), 6,86 (d, J=6,5 Гц, 2Н), 6,67-6,61 (m, 3Н), 6,49 (dd, J=2,4, 8,4 Гц, 1Н), 6,09 (dd, J=1,6, 8,0 Гц, 1Н), 5,96 (d, J=14,4 Гц, 1Н), 5,04 (dd, J=5,2, 13,2 Гц, 1Н), 4,32 (d, J=17,2 Гц, 1Н), 4,22-4,17 (m, 2Н), 3,34-3,11 (m, 13Н), 3,00-2,87 (m, 3Н), 2,60-2,54 (m, 1Н), 2,43-2,35 (m, 1Н), 2,20 (d, J=6,8 Гц, 2Н), 2,08-1,94 (m, 2Н), 1,77-1,55 (m, 4Н), 1,25-1,15 (m, 2Н).
[791] Синтез (3S)-3-[5-[4-[[1-[2-фтор-4-[(1R,2S)-6-гидрокси-2-фенилтетралин-1-ил]фенил]-4-пиперидил]метил]пиперазин-1-ил]-1-оксоизоиндолин-2-ил]пиперидин-2,6-диона (иллюстративное соединение 524)

К смеси (3S)-3-(1-оксо-5-пиперазин-1-илизоиндолин-2-ил)пиперидин-2,6-диона (1,24 г, 3,33 ммоль, 1 экв., бензолсульфонат) в дихлорметане (8 мл) и метаноле (32 мл) одной порцией добавляли ацетат натрия (818 мг, 9,98 ммоль, 3 экв.) при 20°С. Смесь перемешивали при 20°С в течение 10 мин. Добавляли 1-[2-фтор-4-[(1R,2S)-6-гидрокси-2-фенилтетралин-1-ил]фенил]пиперидин-4-карбальдегид (1 г, 2,33 ммоль, 0,7 экв). Смесь перемешивали при 20°С в течение 10 мин. Затем одной порцией добавляли уксусную кислоту (0,2 мл) и цианоборгидрид натрия (418 мг, 6,65 ммоль, 2 экв). Смесь перемешивали при 20°С в течение 40 мин. Смесь концентрировали в вакууме. Затем добавляли 50 мл тетрагидрофурана и 20 мл воды и смесь перемешивали в течение 20 мин. Добавляли насыщенный водный раствор бикарбоната натрия с регулированием рН до 8-9. Водную фазу экстрагировали этилацетатом и тетрагидрофураном (об.:об. = 2:1, 60 мл × 3). Объединенную органическую фазу промывали солевым раствором (60 мл × 1), высушивали с помощью безводного сульфата натрия, фильтровали и концентрировали в вакууме. Остаток очищали с помощью препаративной HPLC с обращенной фазой (колонка: Phenomenex lima С18 250×50 мм, 10 микрон; подвижная фаза: [вода (0,225% муравьиной кислоты) - ацетонитрил]; В%: 26%-56% за 30 мин.). Получали продукт, (3S)-3-[5-[4-[[1-[2-фтор-4-[(1R,2S)-6-гидрокси-2-фенилтетралин-1-ил]фенил]-4-пиперидил]метил]пиперазин-1-ил]-1-оксоизоиндолин-2-ил]пиперидин-2,6-дион (909 мг, 1,12 ммоль, выход 33%, чистота 96%, формиатная соль), в виде белого твердого вещества после лиофилизации. Хиральную чистоту анализировали с помощью хиральной SFC (Chiralcel OJ-3 50×4,6 мм, 3 мкм; подвижная фаза: 50% этанол (0,05% DEA) в СО2; расход: 3 мл/мин., длина волны: 220 нм) и наблюдаемый tp=2,89 мин. с диастереоизомерной чистотой (de) более 95%. [α]D=-256,8 (с=0,2 в DMF, 25°С).
[792] LC-MS (ESI) масса/заряд: 742,2 [М+1]+; 1Н ЯМР (400 МГц, DMSO-d6) δ 10,94 (s, 1Н), 8,15 (s, 0,7Н, формиат), 7,51 (d, J=8,8 Гц, 1Н), 7,24-7,10 (m, 3Н), 7,09-6,97 (m, 2Н), 6,86 (d, J=6,8 Гц, 2Н), 6,72-6,57 (m, 3Н), 6,50 (dd, J=2,4, 8,4 Гц, 1Н), 6,09 (d, J=8,4 Гц, 1Н), 6,01-5,90 (m, 1Н), 5,04 (dd, J=5,2, 13,2 Гц, 1Н), 4,32 (d, J=17 Гц, 1Н), 4,22-4,18 (m, 2Н), 3,35-3,23 (m, 9Н), 3,19 (d, J=8,4 Гц, 3Н), 3,09-2,78 (m, 3Н), 2,63-2,54 (m, 1Н), 2,42-2,28 (m, 2Н), 2,20 (d, J=6,8 Гц, 2Н), 2,14-2,00 (m, 1Н), 1,99-1,89 (m, 1Н), 1,84-1,52 (m, 4Н), 1,32-1,10 (m, 2Н).
[793] Свободная несолевая форма, 1Н ЯМР (400 МГц, DMSO-d6) δ 10,94 (s, 1Н), 9,15 (s, 1Н), 7,51 (d, J=8,4 Гц, 1Н), 7,23-7,10 (m, 3Н), 7,09-7,01 (m, 2Н), 6,86 (d, J=6,8 Гц, 2Н), 6,72-6,56 (m, 3Н), 6,50 (d, J=7,6 Гц, 1Н), 6,09 (d, J=8,0 Гц, 1Н), 5,97 (d, J=14,0 Гц, 1Н), 5,04 (dd, J=4,8, 13,2 Гц, 1Н), 4,38-4,27 (m, 1Н), 4,24-4,19 (m, 1Н), 4,18 (s, 1Н), 3,30-3,23 (m, 5Н), 3,23-3,15 (m, 2Н), 3,06-2,81 (m, 3Н), 2,65-2,54 (m, 4Н), 2,52-2,51 (m, 3Н), 2,42-2,34 (m, 1Н), 2,20 (d, J=7,2 Гц, 2Н), 2,13-2,01 (m, 1Н), 2,00-1,91 (m, 1Н), 1,84-1,70 (m, 3Н), 1,68-1,54 (m, 1Н), 1,24-1,11 (m, 2Н).
[794] Синтез (3R)-3-[5-[4-[[1-[2-фтор-4-[(1R,2S)-6-гидрокси-2-фенилтетралин-1-ил]фенил]-4-пиперидил]метил]пиперазин-1-ил]-1-оксоизоиндолин-2-ил]пиперидин-2,6-диона (иллюстративное соединение 525)
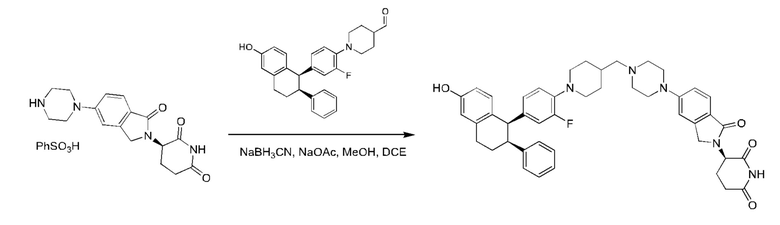
Данное соединение получали с применением той же процедуры, как описано для иллюстративного соединения 524, за исключением того, что применяли (3R)-3-(1-оксо-5-пиперазин-1-илизоиндолин-2-ил)пиперидин-2,6-дион. Очищенную соль муравьиной кислоты анализировали с помощью хиральной SFC при тех же условиях, как и соединение 524, tp=1,76 мин., de 100%). [α]D=-231,6 (с=0,1 в DMF, 25°С). LC-MS (ESI) масса/заряд: 742,3 [М+1]+; 1H ЯМР (400 МГц, DMSO-d6) δ 10,94 (s, 1Н), 9,16 (s, 1Н), 8,13 (s, 0,35Н, формиат), 7,53 (d, J=8,4 Гц, 1Н), 7,20-7,10 (m, 3Н), 7,08-7,00 (m, 2Н), 6,86 (d, J=6,8 Гц, 2Н), 6,68-6,60 (m, 3Н), 6,50 (m, 1Н), 6,09 (d, J=8,4 Гц, 1Н), 5,97 (d, J=14,4 Гц, 1Н), 5,04 (dd, J=5,2, 13,2 Гц, 1Н), 4,33 (d, J=17,2 Гц, 1Н), 4,22-4,15 (m, 2Н), 3,42-3,35 (m, 6Н), 3,20 (br d, J=8,4 Гц, 3Н), 3,01-2,81 (m, 4Н), 2,76-2,51 (m, 4Н), 2,42-2,25 (m, 3Н), 2,15-1,88 (m, 2Н), 1,80-1,51 (m, 4Н), 1,30-1,15 (m, 2Н).
[795] Свободная несолевая форма 1H ЯМР (400 МГц, DMSO-d6) δ: 10,93 (s, 1Н), 9,15 (s, 1Н), 7,51 (d, J=8,8 Гц, 1Н), 7,23-7,09 (m, 3Н), 7,08-7,01 (m, 2Н), 6,86 (d, J=6,4 Гц, 2H), 6,69-6,63 (m, 2H), 6,63-6,60 (m, 1Н), 6,50 (dd, J=2,4, 8,4 Гц, 1Н), 6,09 (d, J=8,4 Гц, 1Н), 5,97 (d, J=14,0 Гц, 1Н), 5,04 (dd, J=5,2, 13,2 Гц, 1Н), 4,37-4,27 (m, 1Н), 4,24-4,19 (m, 1Н), 4,18 (s, 1Н), 3,30-3,23 (m, 5H), 3,23-3,15 (m, 2H), 3,06-2,81 (m, 3Н), 2,65-2,54 (m, 4H), 2,52-2,51 (m, 3Н), 2,42-2,34 (m, 1Н), 2,20 (d, J=7,2 Гц, 2H), 2,13-2,01 (m, 1Н), 2,00-1,91 (m, 1Н), 1,84-1,70 (m, 3Н), 1,68-1,54 (m, 1Н), 1,24-1,11 (m, 2Н).
[796] Синтез 3-[5-[4-[[1-[3-фтор-4-[(1S,2S)-6-гидрокси-2-фенилтетралин-1-ил]фенил]-4-пиперидил]метил]пиперазин-1-ил]-1-оксоизоиндолин-2-ил]пиперидин-2,6-диона (иллюстративное соединение 496)
[797] Стадия 1. Получение [1-(4-бром-3-фторфенил)-4-пиперидил]метанола
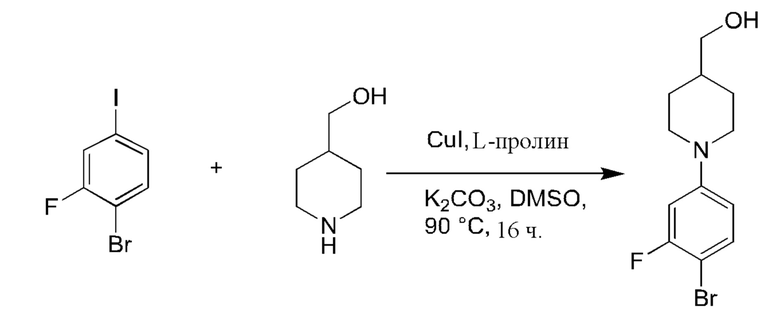
1-Бром-2-фтор-4-йодбензол (25 г, 83,09 ммоль, 1 экв.), 4-пиперидилметанол (10,53 г, 91,39 ммоль, 1,1 экв.), L-пролин (3,83 г, 33,23 ммоль, 0,4 экв.), йодид меди(I) (3,16 г, 16,62 ммоль, 0,2 экв.) и карбонат калия (22,97 г, 166,17 ммоль, 2 экв.) в DMSO (400 мл) дегазировали и затем нагревали до 90°С в течение 10 часов в атмосфере азота. Смесь разбавляли этилацетатом (500 мл), промывали насыщенным раствором хлорида аммония (150 мл), высушивали над безводным сульфатом натрия и фильтровали. Фильтрат концентрировали в вакууме. Остаток очищали с помощью хроматографии на силикагеле (петролейный эфир/этилацетат = от 10/1 до 2/1) с получением [1-(4-бром-3-фторфенил)-4-пиперидил]метанола (5,02 г, 17,42 ммоль, выход 21%) в виде желтого твердого вещества. 1Н ЯМР (400 МГц, МЕТАНОЛ-d4) δ 7,26-7,41 (m, 1 Н), 6,63-6,83 (m, 2 Н), 3,68-3,81 (m, 2 Н), 3,45 (d, J=6,40 Гц, 2 Н), 3,33 (s, 1 Н), 2,73 (br t, J=12,23 Гц, 2 Н), 1,84 (br d, J=12,92 Гц, 2 H), 1,64 (br d, J=3,26 Гц, 1 H), 1,33 (q, J=12,30 Гц, 2 Н).
[798] Стадия 2. Получение 1-(4-бром-3-фторфенил)пиперидин-4-карбальдегида

К смеси оксалилдихлорида (6,61 г, 52,06 ммоль, 4,6 мл, 3 экв.) в дихлорметане (50 мл) добавляли по каплям раствор DMSO (5,42 г, 69,41 ммоль, 5,4 мл, 4 экв.) в дихлорметане (50 мл) при -68°С. После завершения добавления смесь перемешивали при -68°С в течение 30 минут. Затем к реакционной смеси добавляли по каплям раствор [1-(4-бром-3-фторфенил)-4-пиперидил]метанола (5 г, 17,35 ммоль, 1 экв.) в дихлорметане (50 мл). После завершения добавления смесь перемешивали при -68°С в течение 1 часа. Затем добавляли по каплям триэтиламин (14,05 г, 138,81 ммоль, 19,3 мл, 8 экв.) при -68°С. Смесь перемешивали при 25°С в течение 16 часов. Реакционная смесь не содержала примесей в соответствии с TLC. Добавляли насыщенный раствор бикарбоната натрия (80 мл). Органическую фазу промывали солевым раствором (300 мл), высушивали с помощью безводного сульфата натрия, фильтровали и концентрировали в вакууме. Остаток очищали с помощью хроматографии на силикагеле (петролейный эфир/этилацетат = от 100/1 до 10/1) с получением 1-(4-бром-3-фторфенил)пиперидин-4-карбальдегида (4,98 г, неочищенный) в виде желтого масла.
[799] Стадия 3. Получение 1-(4-бром-3-фторфенил)-4-(диметоксиметил)пиперидина

К раствору 1-(4-бром-3-фторфенил)пиперидин-4-карбальдегида (4,9 г, 17,12 ммоль, 1 экв.) в триметоксиметане (38,72 г, 364,87 ммоль, 40 мл, 21,31 экв.) добавляли пара-толуолсульфоновую кислоту (147 мг, 0,85 ммоль, 0,05 экв.). Смесь перемешивали при 25°С в течение 16 часов. Реакционную смесь гасили раствором бикарбоната натрия и затем экстрагировали 200 мл этилацетата. Объединенные органические слои промывали 200 мл солевого раствора, высушивали над безводным сульфатом натрия, фильтровали и концентрировали при пониженном давлении. Остаток очищали с помощью хроматографии на силикагеле (петролейный эфир/этилацетат = от 1:0 до 30:1) с получением 1-(4-бром-3-фторфенил)-4-(диметоксиметил)пиперидина (4,6 г, 13,85 ммоль, выход 81%) в виде желтого масла. LC-MS (ESI) масса/заряд: 331,9 [М+1]+; 1Н ЯМР (400 МГц, CDCl3) δ 7,17-7,29 (m, 1 Н), 6,45-6,68 (m, 2 Н), 3,99 (d, J=7,03 Гц, 1 Н), 3,59 (br d, J=12,42 Гц, 2 H), 3,30 (s, 6 Н), 2,62 (td, J=12,39, 2,45 Гц, 2 H), 1,62-1,84 (m, 3 Н), 1,27-1,42 (m, 2 Н).
[800] Стадия 4. Получение 4-(диметоксиметил)-1-[3-фтор-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)фенил]пиперидина

К раствору 1-(4-бром-3-фторфенил)-4-(диметоксиметил)пиперидина (1 г, 3.01 ммоль, 1 экв.), 4,4,5,5-тетраметил-2-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1,3,2-диоксаборолана (1,22 г, 4,82 ммоль, 1,6 экв.), ацетата калия (590 мг, 6.02 ммоль, 2 экв.) и 2-ди-трет-бутилфосфино-2,4,6-триизопропилбифенила (287 мг, 0,60 ммоль, 0,2 экв.) в диоксане (10 мл) добавляли ацетат палладия(II) (81 мг, 0,36 ммоль, 0,12 экв.) в атмосфере азота. Смесь перемешивали при 100°С в атмосфере азота в течение 3 часов. Реакционную смесь концентрировали при пониженном давлении. Остаток очищали с помощью хроматографии на силикагеле (петролейный эфир/этилацетат = от 1:0 до 30:1) с получением 4-(диметоксиметил)-1-[3-фтор-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)фенил]пиперидина (800 мг, 2,11 ммоль, выход 70%) в виде серого твердого вещества.
[801] Стадия 5. Получение 1-[4-(6-бензилокси-3,4-дигидронафталин-1-ил)-3-фторфенил]-4-(диметоксиметил)пиперидина

К раствору 4-(диметоксиметил)-1-[3-фтор-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)фенил]пиперидина (700 мг, 1,85 ммоль, 1 экв.) и (6-бензилокси-3,4-дигидронафталин-1-ил)трифторметансульфоната (709 мг, 1,85 ммоль, 1 экв.) в диоксане (12 мл) и воде (2 мл) добавляли [1,1'-бис(дифенилфосфино)ферроцен]дихлорпалладий(II) (135 мг, 0,18 ммоль, 0,1 экв.) и карбонат калия (765 мг, 5,54 ммоль, 3 экв.) в атмосфере азота. Смесь перемешивали при 90°С в течение 3 часов. Реакционную смесь фильтровали и концентрировали при пониженном давлении. Остаток очищали с помощью хроматографии на силикагеле (петролейный эфир/этилацетат = от 1:0 до 30:1) с получением 1-[4-(6-бензилокси-3,4-дигидронафталин-1-ил)-3-фторфенил]-4-(диметоксиметил)пиперидина (850 мг, 1,74 ммоль, выход 94%) в виде желтого твердого вещества. LC-MS (ESI) масса/заряд: 488,1 [М+1]+; 1Н ЯМР (400 МГц, CDCl3) δ 7,28-7,45 (m, 5 Н), 7,11 (t, J=8,60 Гц, 1 Н), 6,77-6,84 (m, 2 Н), 6,69 (ddd, J=8,60, 6,46, 2,51 Гц, 2 Н), 6,63 (dd, J=13,36, 2,45 Гц, 1 Н), 5,93 (t, J=4,52 Гц, 1 Н), 5,04 (s, 2 Н), 4,05-4,15 (m, 1 Н), 3,74 (br d, J=12,55 Гц, 2 H), 3,36-3,40 (m, 6 Н), 2,83 (t, J=7,97 Гц, 2 H), 2,72 (td, J=12,33, 2,45 Гц, 2 H), 2,39 (td, J=7,91, 4,77 Гц, 2 H), 1,71-1,89 (m, 3 Н), 1,40-1,51 (m, 2 Н).
[802] Стадия 6. Получение 1-[4-(6-бензилокси-2-бром-3,4-дигидронафталин-1-ил)-3-фторфенил]-4-(диметоксиметил)пиперидина

К раствору 1-[4-(6-бензилокси-3,4-дигидронафталин-1-ил)-3-фторфенил]-4-(диметоксиметил)пиперидина (870 мг, 1,78 ммоль, 1 экв.) и триэтиламина (270 мг, 2,68 ммоль, 0,3 мл, 1,5 экв.) в дихлорметане (20 мл) добавляли трибромид пиридиния (570 мг, 1,78 ммоль, 1 экв.) при 0°С. Смесь перемешивали при 25°С в течение 0,5 часа. Реакционную смесь промывали водным раствором сульфита натрия (40 мл) и экстрагировали дихлорметаном (120 мл). Объединенные органические слои промывали солевым раствором (100 мл), высушивали над сульфатом натрия, фильтровали и концентрировали при пониженном давлении. Остаток очищали с помощью хроматографии на силикагеле (петролейный эфир/этилацетат = от 1:0 до 20:1) с получением 1-[4-(6-бензилокси-2-бром-3,4-дигидронафталин-1-ил)-3-фторфенил]-4-(диметоксиметил)пиперидина (680 мг, 1,20 ммоль, выход 67%) в виде желтого твердого вещества. LC-MS (ESI) масса/заряд: 568,0 [М+1]+.
[803] Стадия 7. Получение 1-[4-(6-бензилокси-2-фенил-3,4-дигидронафталин-1-ил)-3-фторфенил]-4-(диметоксиметил)пиперидина

К раствору 1-[4-(6-бензилокси-2-бром-3,4-дигидронафталин-1-ил)-3-фторфенил]-4-(диметоксиметил)пиперидина (680 мг, 1,20 ммоль, 1 экв.) и фенилбороновой кислоты (146 мг, 1,20 ммоль, 1 экв.) в диоксане (18 мл) и воде (3 мл) добавляли [1,1'-бис(дифенилфосфино)ферроцен]дихлорпалладий(II) (87 мг, 0,12 ммоль, 0,1 экв.) и карбонат калия (331 мг, 2,40 ммоль, 2 экв.). Смесь перемешивали при 100°С в течение 3 часов. Реакционную смесь фильтровали и концентрировали при пониженном давлении. Остаток очищали с помощью хроматографии на силикагеле (петролейный эфир/этилацетат = от 1:0 до 10:1) с получением 1-[4-(6-бензилокси-2-фенил-3,4-дигидронафталин-1-ил)-3-фторфенил]-4-(диметоксиметил)пиперидин (600 мг, 1,06 ммоль, выход 88%) в виде желтого масла. LC-MS (ESI) масса/заряд: 564,2 [М+1]+; 1Н ЯМР (400 МГц, CDCl3) δ 7,31-7,48 (m, 5 Н), 7,04-7,19 (m, 5 Н), 6,78-6,91 (m, 2 Н), 6,65-6,76 (m, 2 Н), 6,49-6,60 (m, 2 Н), 5,08 (s, 2 Н), 4,08-4,12 (m, 1 Н), 3,69 (br d, J=12,42 Гц, 2 H), 3,34-3,45 (m, 6 Н), 2,88-3,08 (m, 2 Н), 2,73-2,88 (m, 2 Н), 2,68 (td, J=12,33, 2,32 Гц, 2 H), 1,82-1,92 (m, 1 Н), 1,82-1,92 (m, 1 Н), 1,72-1,81 (m, 1 Н), 1,36-1,52 (m, 2 Н).
[804] Стадия 8. Получение 1-[4-[4-(диметоксиметил)-1-пиперидил]-2-фторфенил]-2-фенилтетралин-6-ола

К раствору 1-[4-(6-бензилокси-2-фенил-3,4-дигидронафталин-1-ил)-3-фторфенил]-4-(диметоксиметил)пиперидина (680 мг, 1,21 ммоль, 1 экв.) в метаноле (10 мл) и тетрагидрофуране (10 мл) добавляли катализатор, представляющий собой 10% палладий на активированном угле, в атмосфере азота. Смесь перемешивали при 25°С в течение 16 часов в атмосфере водорода (15 фунтов/кв. дюйм). Остаток очищали с помощью препаративной HPLC (колонка: Phenomenex Synergi С18 150×25 мм, 10 микрон, подвижная фаза: [вода (0,225% муравьиной кислоты)-ACN]; В%: 35%-65% за 10 мин.). Получали соединение, цис-1-[4-[4-(диметоксиметил)-1-пиперидил]-2-фторфенил]-2-фенилтетралин-6-ол (450 мг, 0,94 ммоль, выход 78%), в виде желтого твердого вещества. LC-MS (ESI) масса/заряд: 476,1 [М+1]+.
[805] Стадия 9. Получение (1S,2S)-1-[4-[4-(диметоксиметил)-1-пиперидил]-2-фторфенил]-2-фенилтетралин-6-ола

1-[4-[4-(Диметоксиметил)-1-пиперидил]-2-фторфенил]-2-фенилтетралин-6-ол (450 мг, 0,94 ммоль, 1 экв.) очищали с помощью SFC (колонка: AD, 250 мм × 30 мм, 10 микрон); подвижная фаза: [0,1% гидроксида аммония в МеОН]; В%: 50%-50% за 3,7 мин. для каждого прогона, всего 180 мин.). Получали соединение, (1S,2S)-1-[4-[4-(диметоксиметил)-1-пиперидил]-2-фторфенил]-2-фенилтетралин-6-ол (170 мг, 0,35 ммоль, выход 37%), в виде желтого масла.
[806] Стадия 10 и 11. Получение 3-[5-[4-[[1-[3-фтор-4-[(1S,2S)-6-гидрокси-2-фенилтетралин-1-ил]фенил]-4-пиперидил]метил]пиперазин-1-ил]-1-оксоизоиндолин-2-ил]пиперидин-2,6-диона (иллюстративное соединение 496)

С применением той же процедуры, описанной на стадии 10 и стадии 11 для иллюстративного соединения 341, соединение, 3-[5-[4-[[1-[3-фтор-4-[(1S,2S)-6-гидрокси-2-фенилтетралин-1-ил]фенил]-4-пиперидил]метил]пиперазин-1-ил]-1-оксоизоиндолин-2-ил]пиперидин-2,6-дион, получали в виде белого твердого вещества, представляющего собой соль муравьиной кислоты. LC-MS (ESI) масса/заряд: 742,2 [М+1]+; 1H ЯМР (400 МГц, DMS0-d6) δ 10,94 (s, 1Н, имид), 9,14 (br s, 1Н, фенол), 8,20 (s, 0,45Н, формиат), 7,52 (d, J=8,8 Гц, 1Н), 7,08-7,03 (m, 5 Н), 6,83 (m, 2Н), 6,62 (m, 2Н), 6,58-6,42 (m, 3Н), 6,26 (br d, J=13,68 Гц, 1 Н), 5,04 (dd, J=13,36, 5,08 Гц, 1Н), 4,45 (br d, J=5,02 Гц, 1Н), 4,33 (d, J=16,8 Гц, 1Н), 4,20 (d, J=16,8 Гц, 1Н), 3,63-3,50 (m, 2Н), 3,29-3,21 (m, 9Н), 3,03-2,84 (m, 3Н), 2,60 (br, 3Н), 2,40-2,35 (m, 1Н), 2,19 (br d, J=6,7 Гц, 3Н), 2,01-1,91 (m, 1Н), 1,79-1,64 (m, 4Н), 1,20-1,07 (m, 2Н).
| название | год | авторы | номер документа |
|---|---|---|---|
| МОДУЛЯТОРЫ ПРОТЕОЛИЗА ЭСТРОГЕНОВЫХ РЕЦЕПТОРОВ И СВЯЗАННЫЕ С НИМИ СПОСОБЫ ПРИМЕНЕНИЯ | 2018 |
|
RU2797808C2 |
| МОДУЛЯТОРЫ ПРОТЕОЛИЗА И СООТВЕТСТВУЮЩИЕ СПОСОБЫ ПРИМЕНЕНИЯ | 2019 |
|
RU2805511C2 |
| ПОЛИЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ И СПОСОБЫ ЦЕЛЕНАПРАВЛЕННОЙ ДЕГРАДАЦИИ ПОЛИПЕПТИДОВ БЫСТРО УСКОРЕННОЙ ФИБРОСАРКОМЫ | 2019 |
|
RU2830173C2 |
| PROTAC, ЦЕЛЕНАПРАВЛЕННО ВОЗДЕЙСТВУЮЩИЕ НА ТАУ-БЕЛОК, И СВЯЗАННЫЕ С НИМИ СПОСОБЫ ПРИМЕНЕНИЯ | 2017 |
|
RU2805523C2 |
| СОЕДИНЕНИЯ, ЦЕЛЕНАПРАВЛЕННО ВОЗДЕЙСТВУЮЩИЕ НА BRM, И СВЯЗАННЫЕ С НИМИ СПОСОБЫ ПРИМЕНЕНИЯ | 2019 |
|
RU2797832C2 |
| СОЕДИНЕНИЕ, НАЦЕЛЕННОЕ НА БЕЛОК И ЕГО ДЕГРАДАЦИЮ, И СПОСОБ ЕГО ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2021 |
|
RU2829459C1 |
| ЛИГАНДЫ ЦЕРЕБЛОНА И БИФУНКЦИОНАЛЬНЫЕ СОЕДИНЕНИЯ, СОДЕРЖАЩИЕ ИХ | 2018 |
|
RU2795146C2 |
| ПРОИЗВОДНЫЕ БОРОНОВОЙ КИСЛОТЫ И ИХ ТЕРАПЕВТИЧЕСКИЕ ПРИМЕНЕНИЯ | 2017 |
|
RU2773346C2 |
| СОЕДИНЕНИЯ ДЛЯ ЛЕЧЕНИЯ ОПОСРЕДОВАННЫХ КОМПЛЕМЕНТОМ НАРУШЕНИЙ | 2015 |
|
RU2703995C2 |
| ИНГИБИТОРЫ MEK И ИХ ТЕРАПЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ | 2021 |
|
RU2812929C1 |


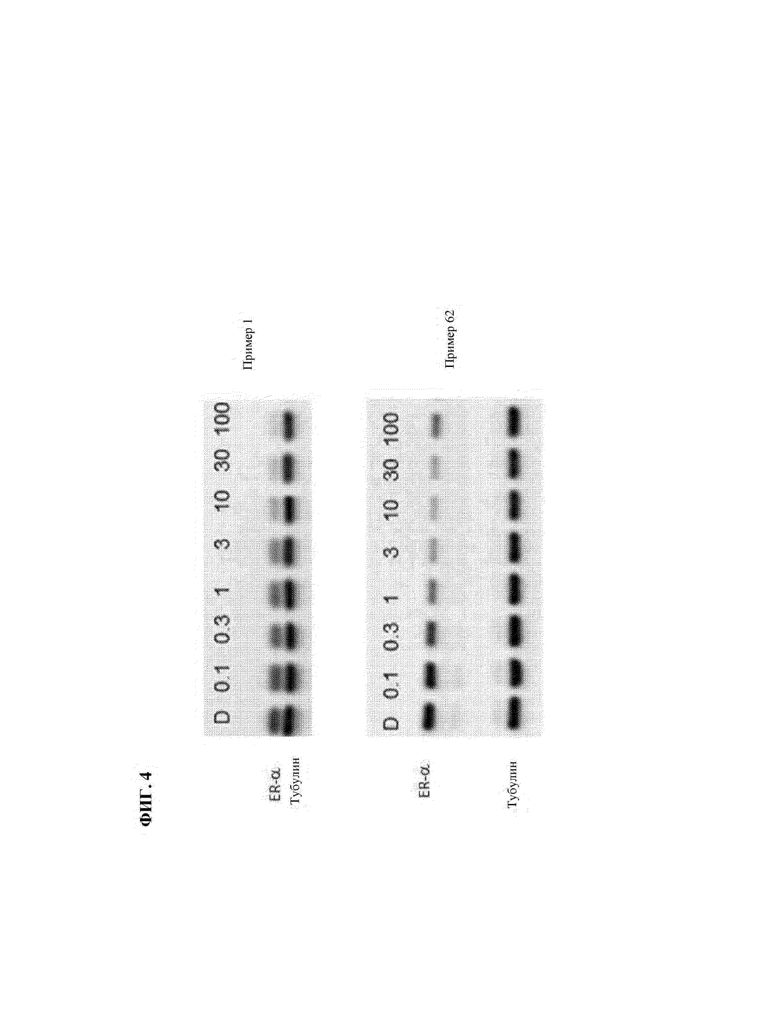













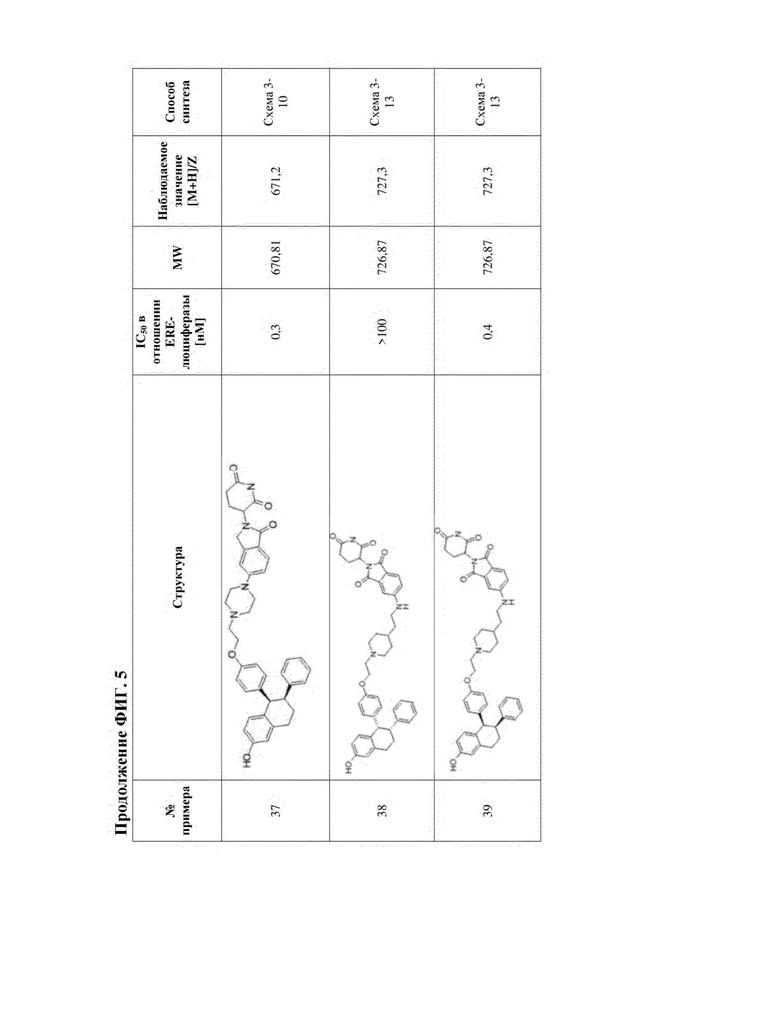
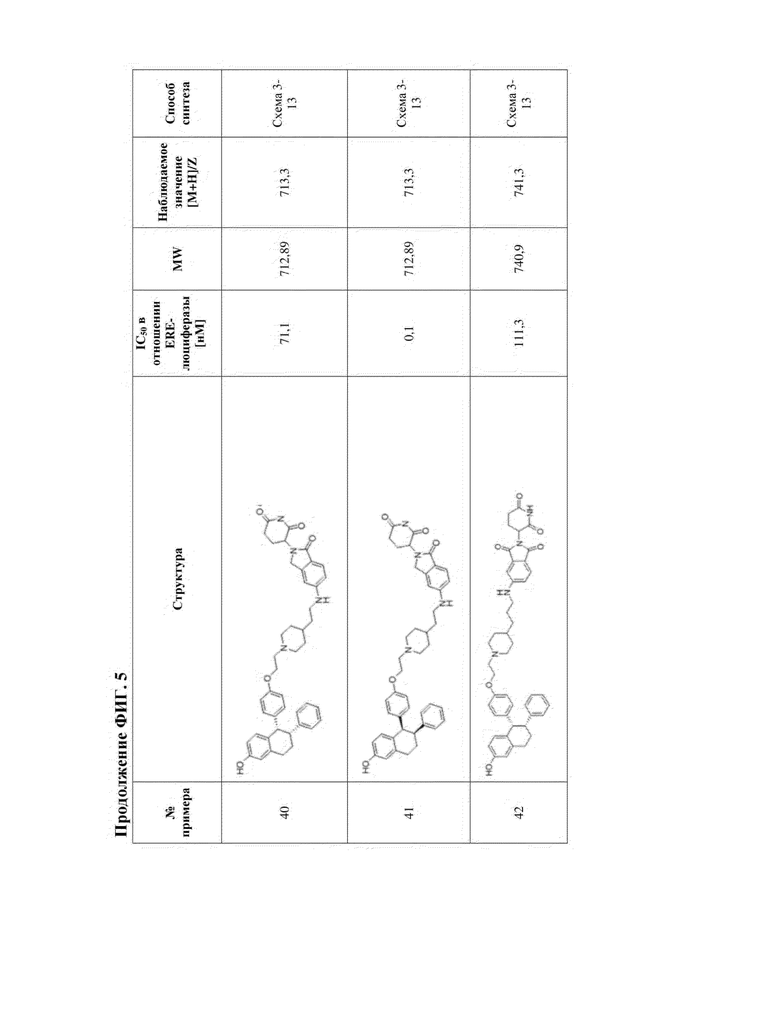
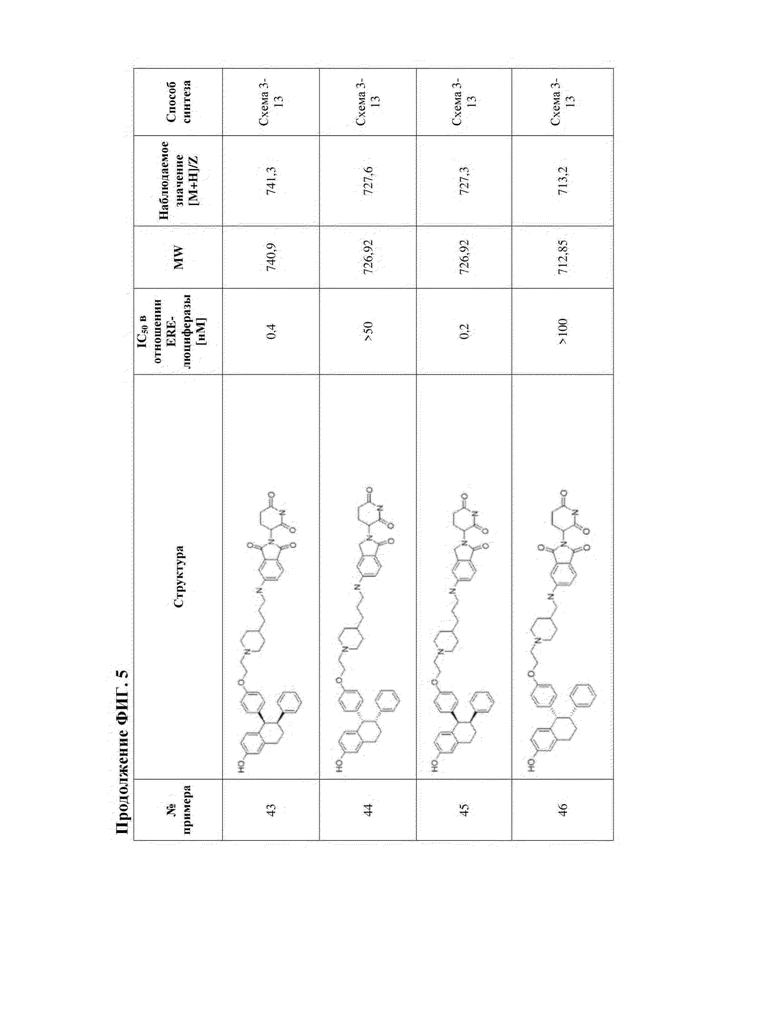




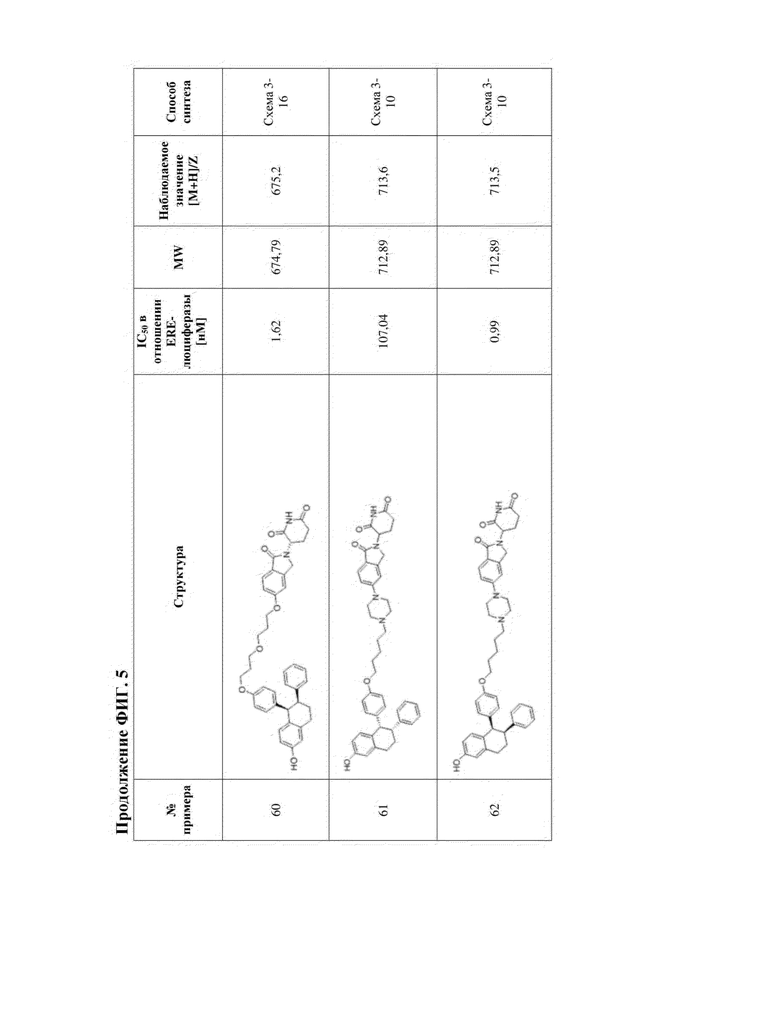











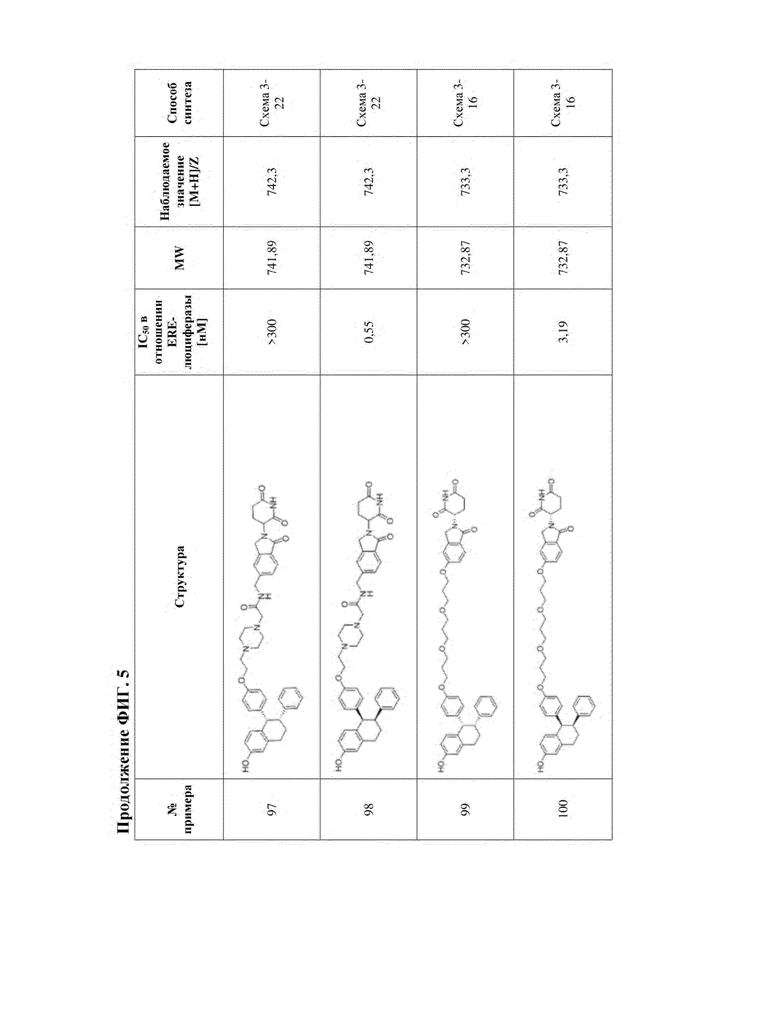


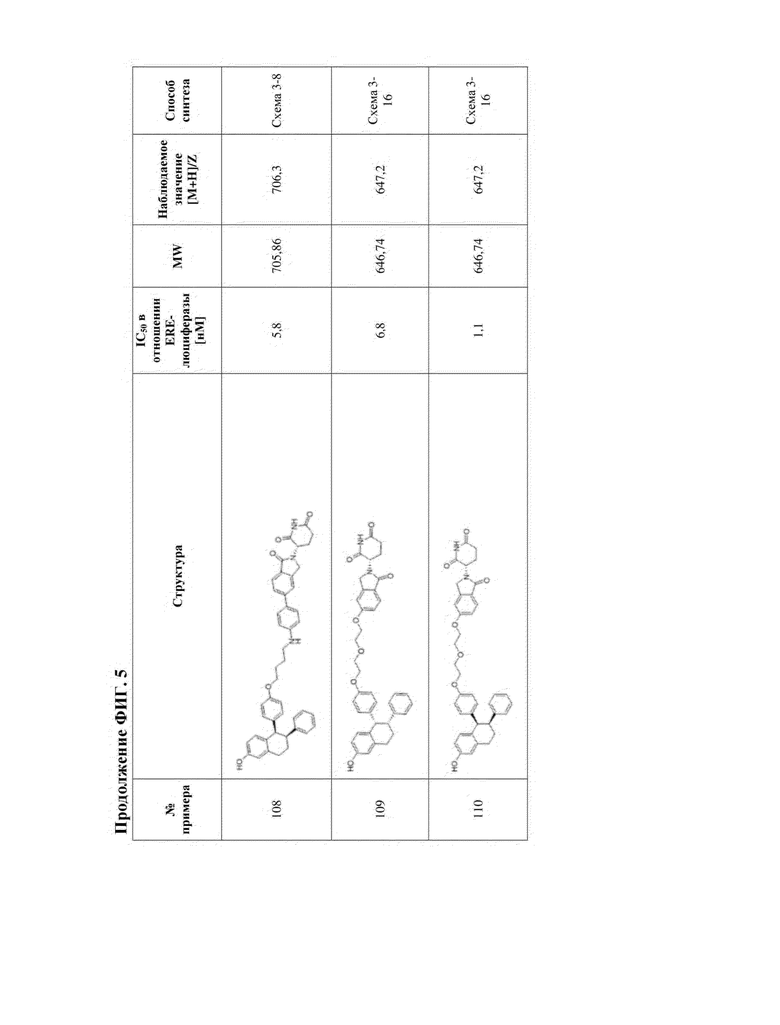





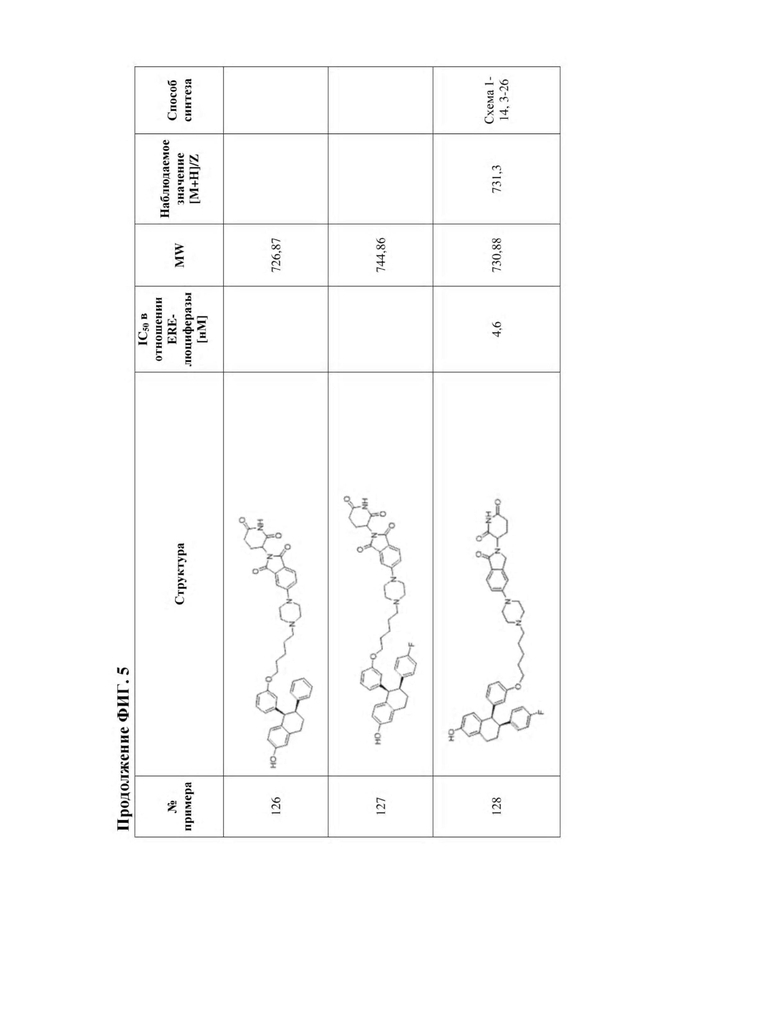



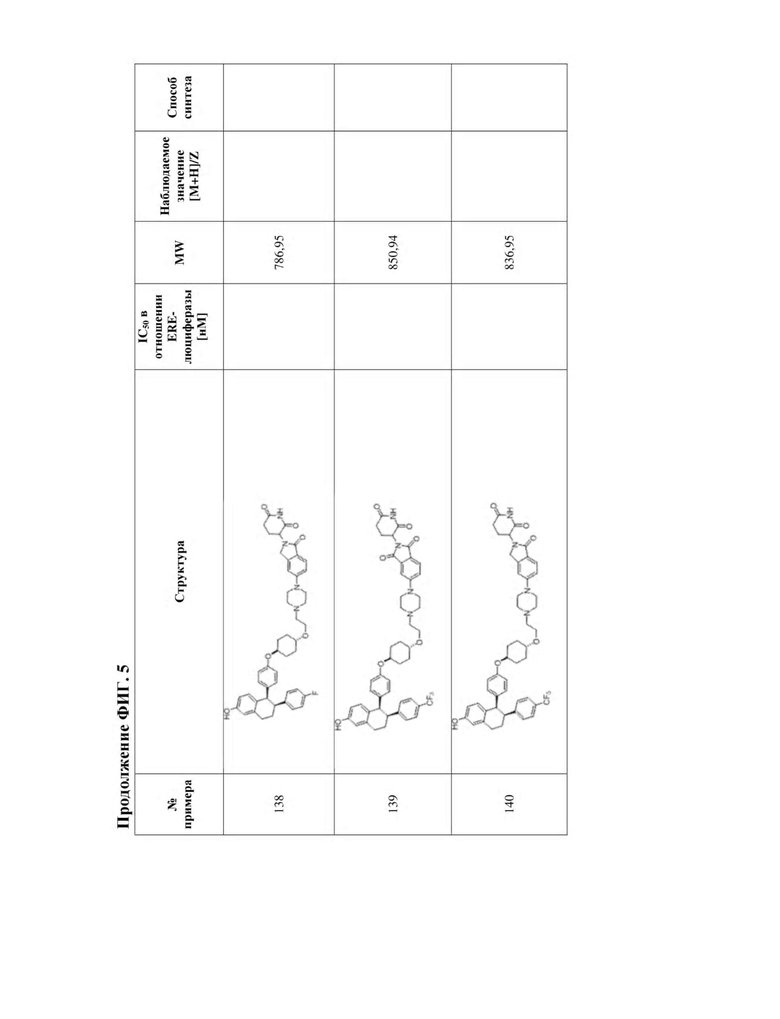



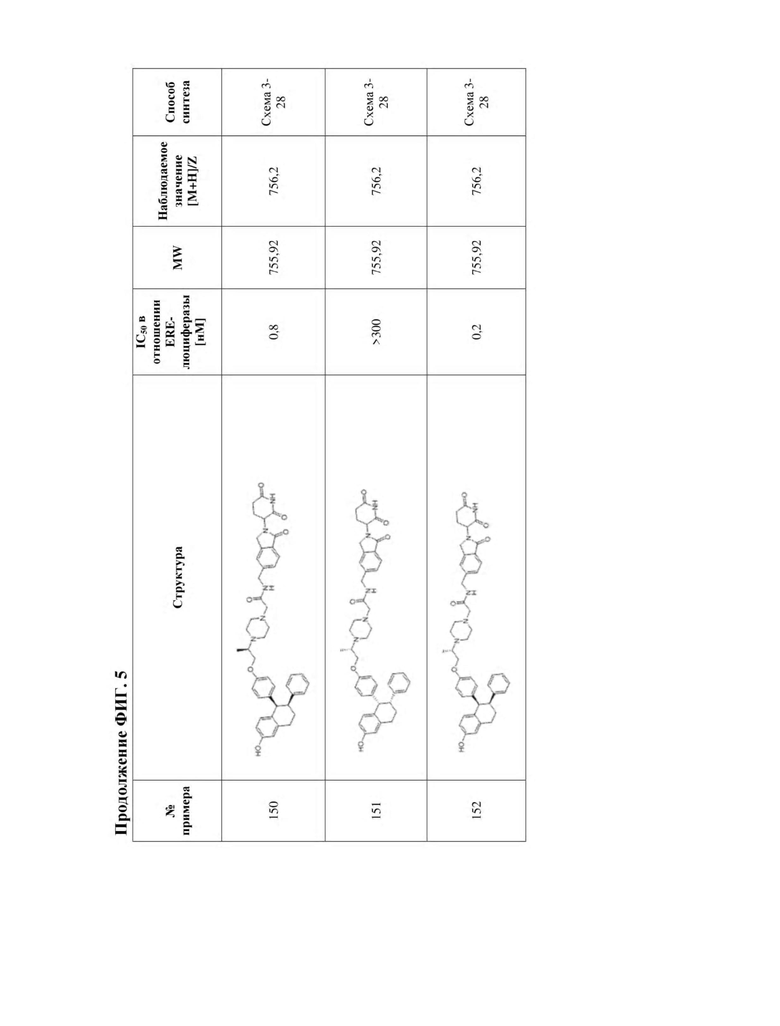

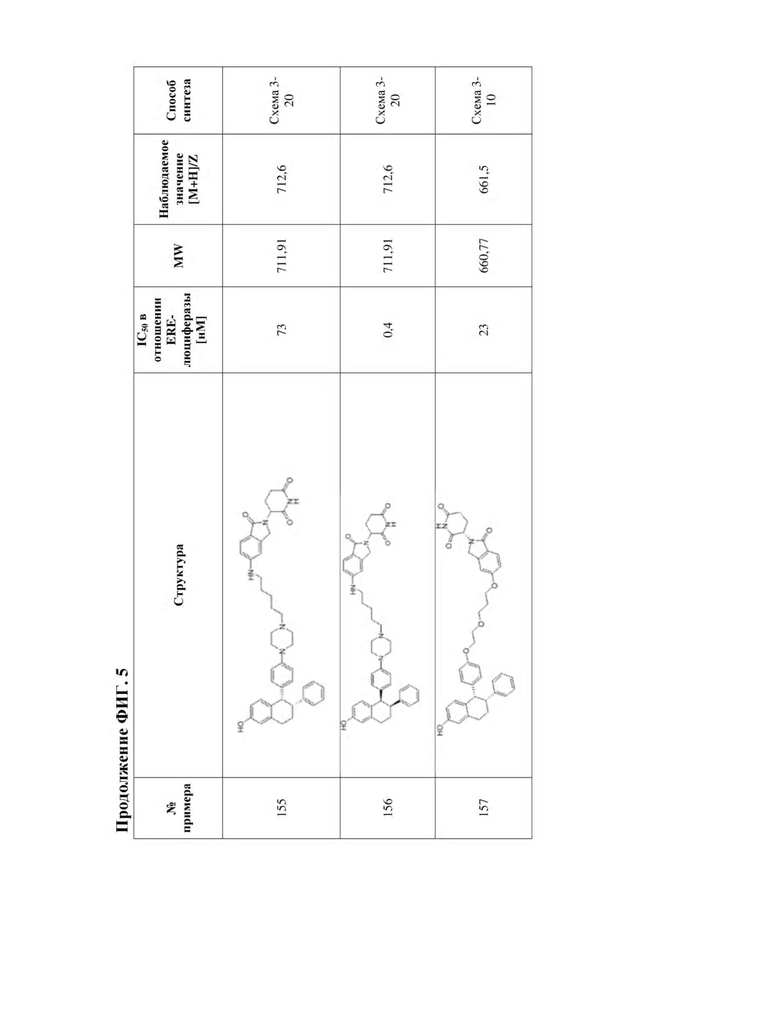




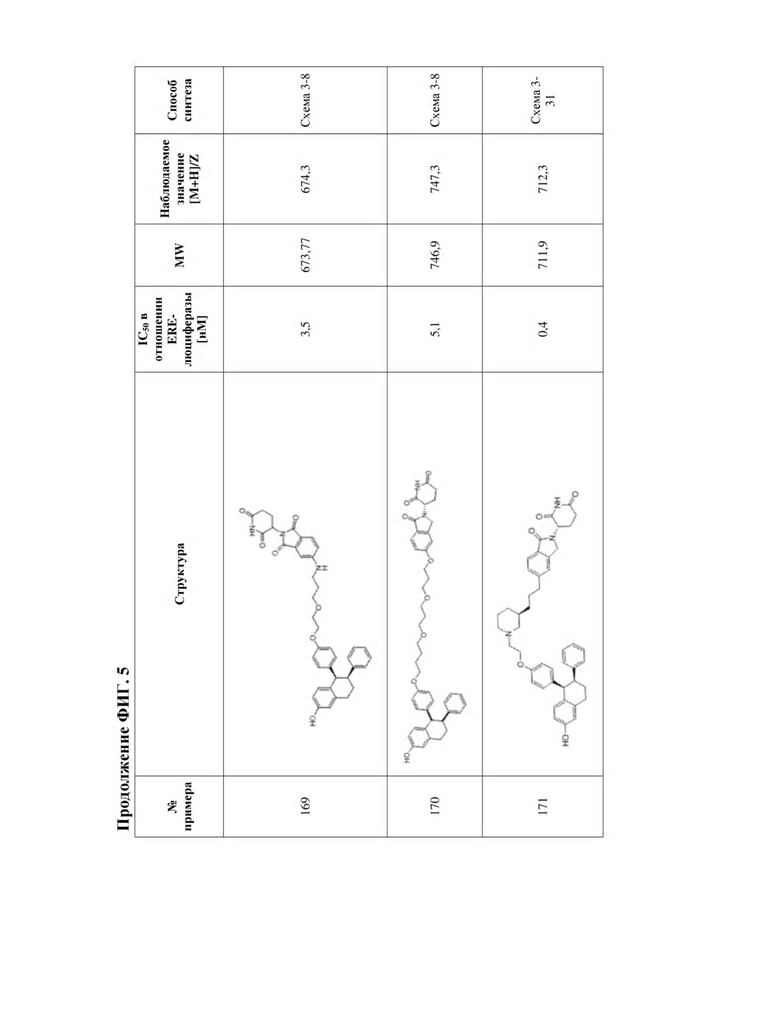


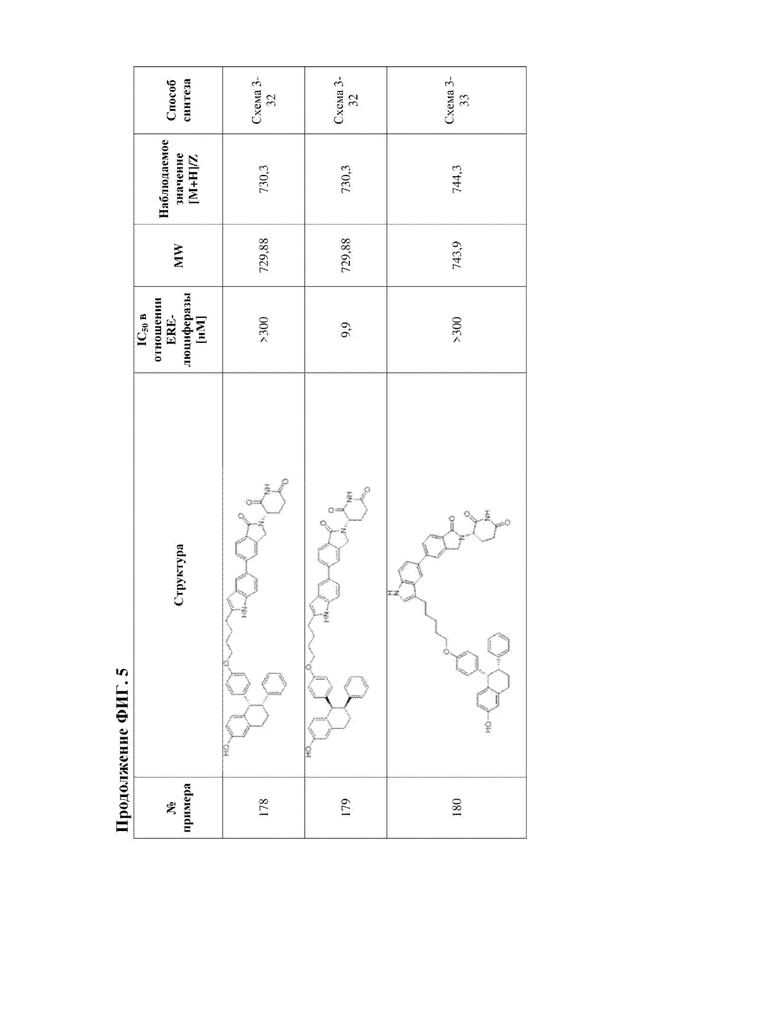









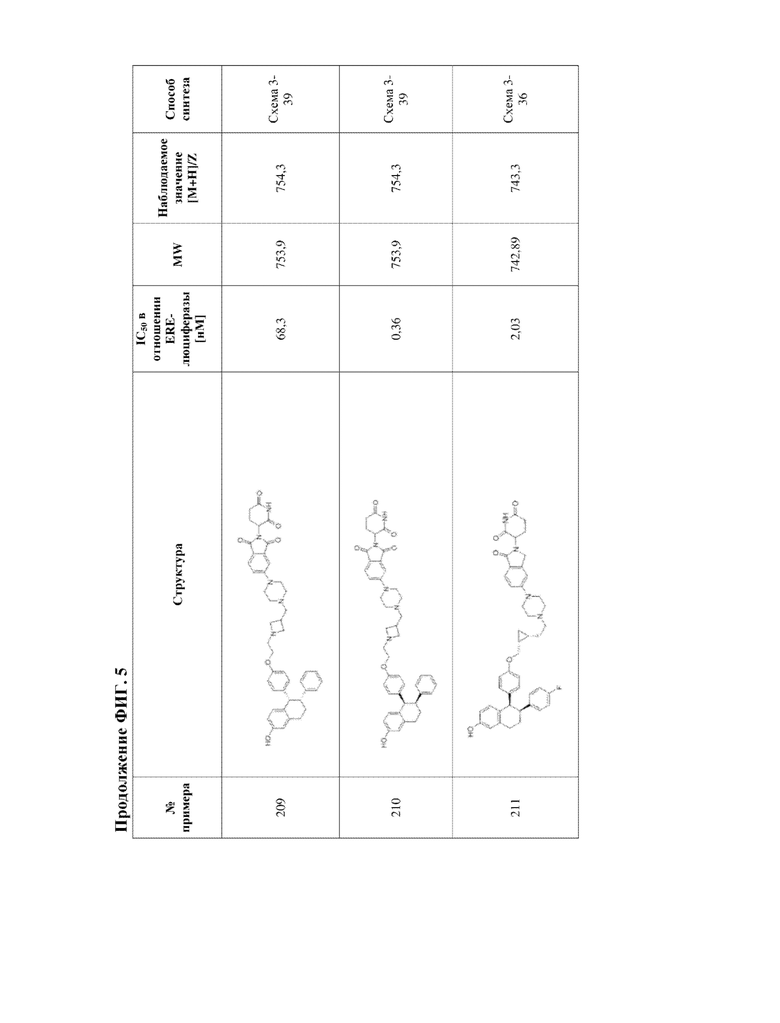

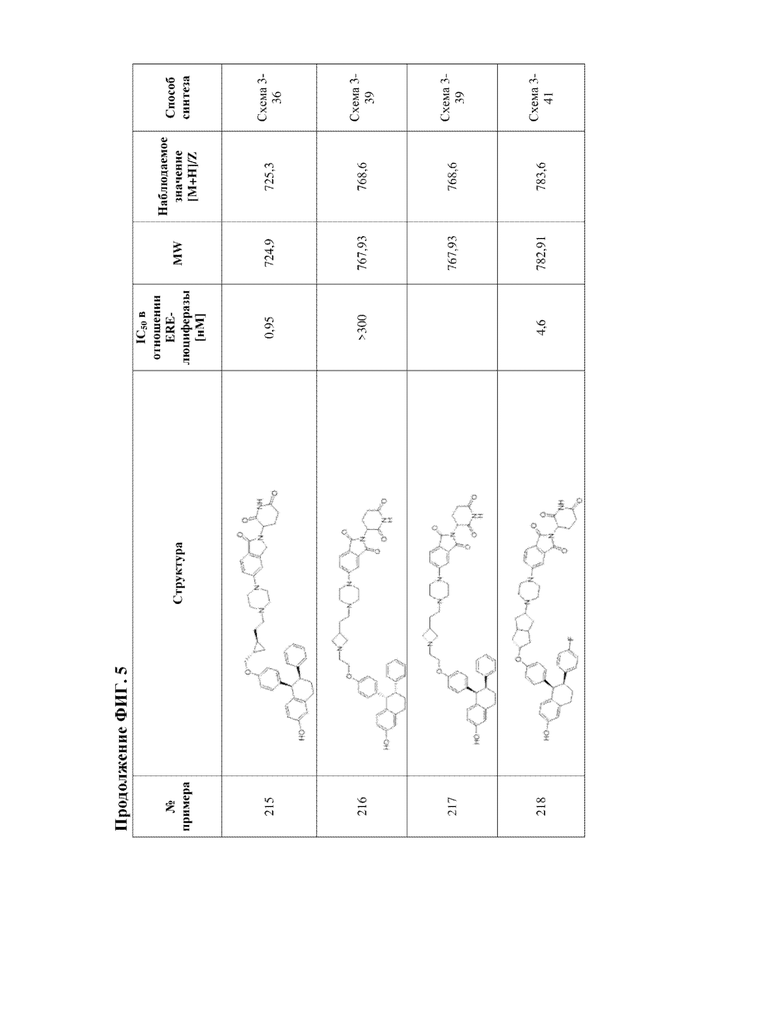

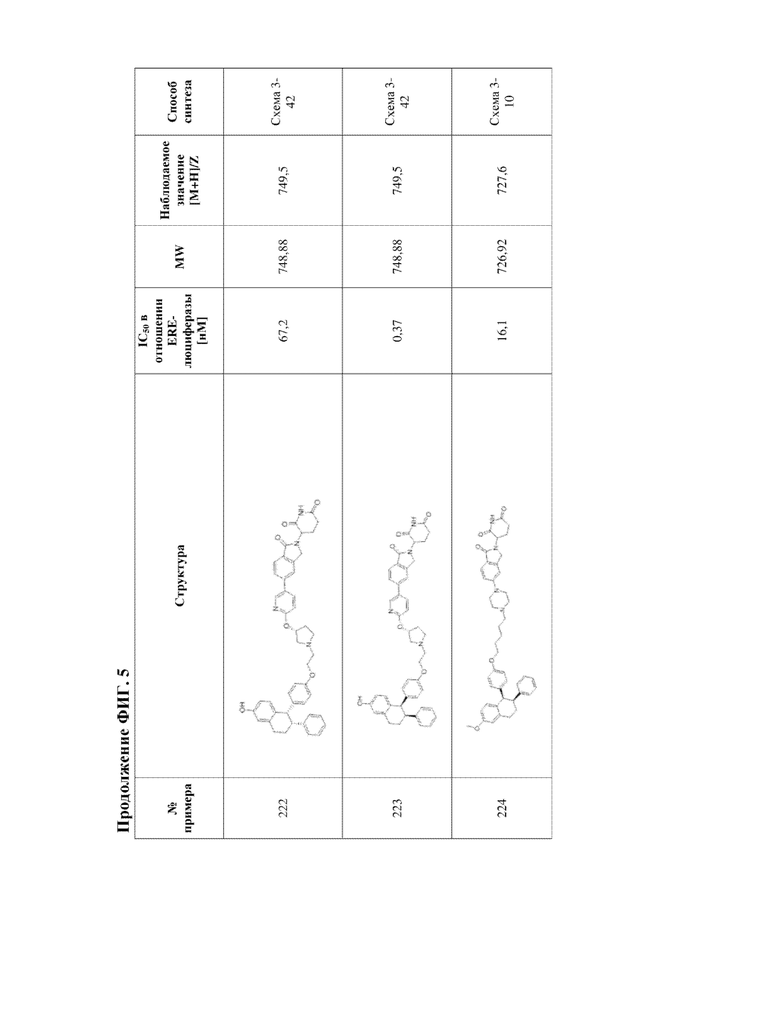

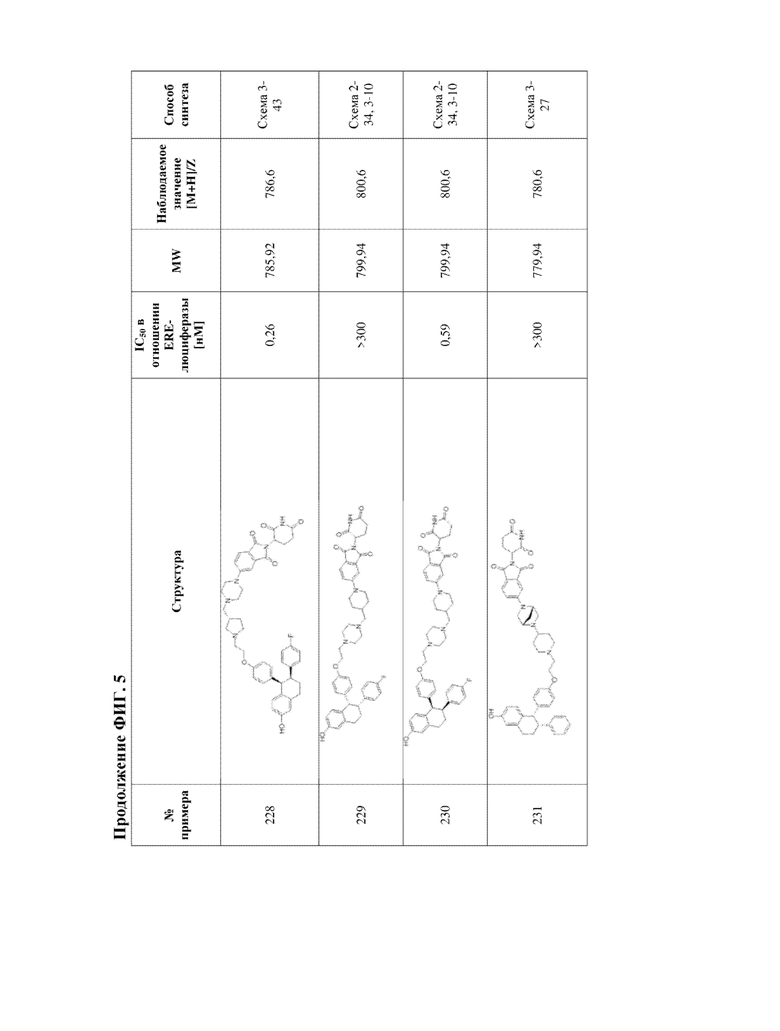
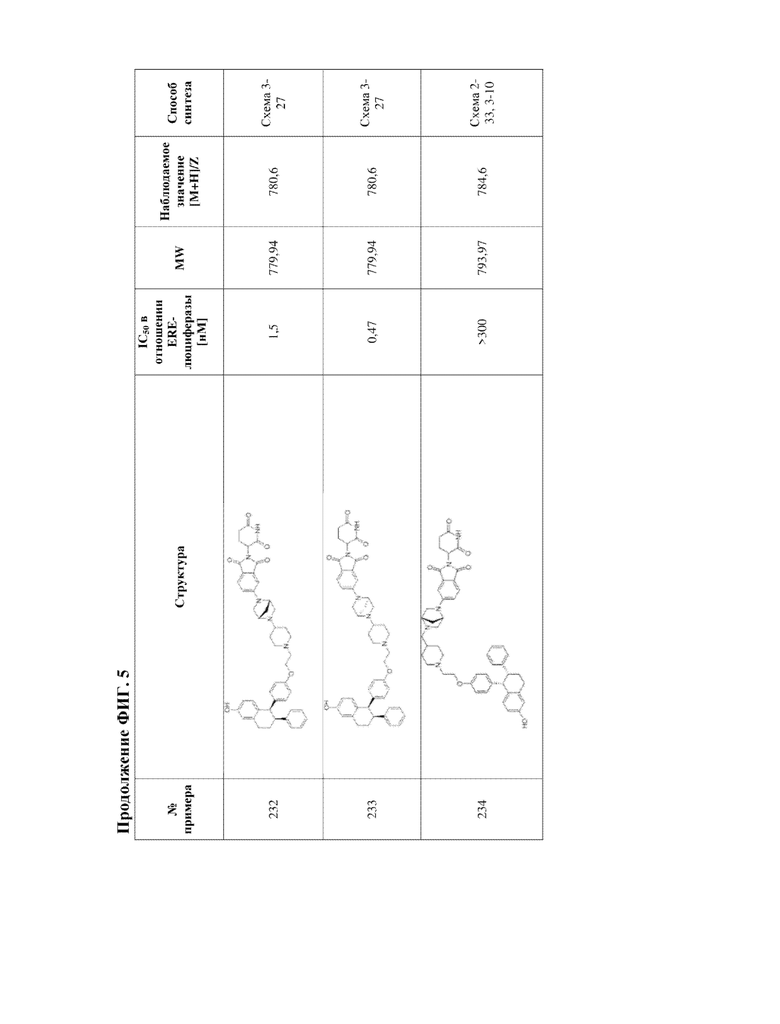


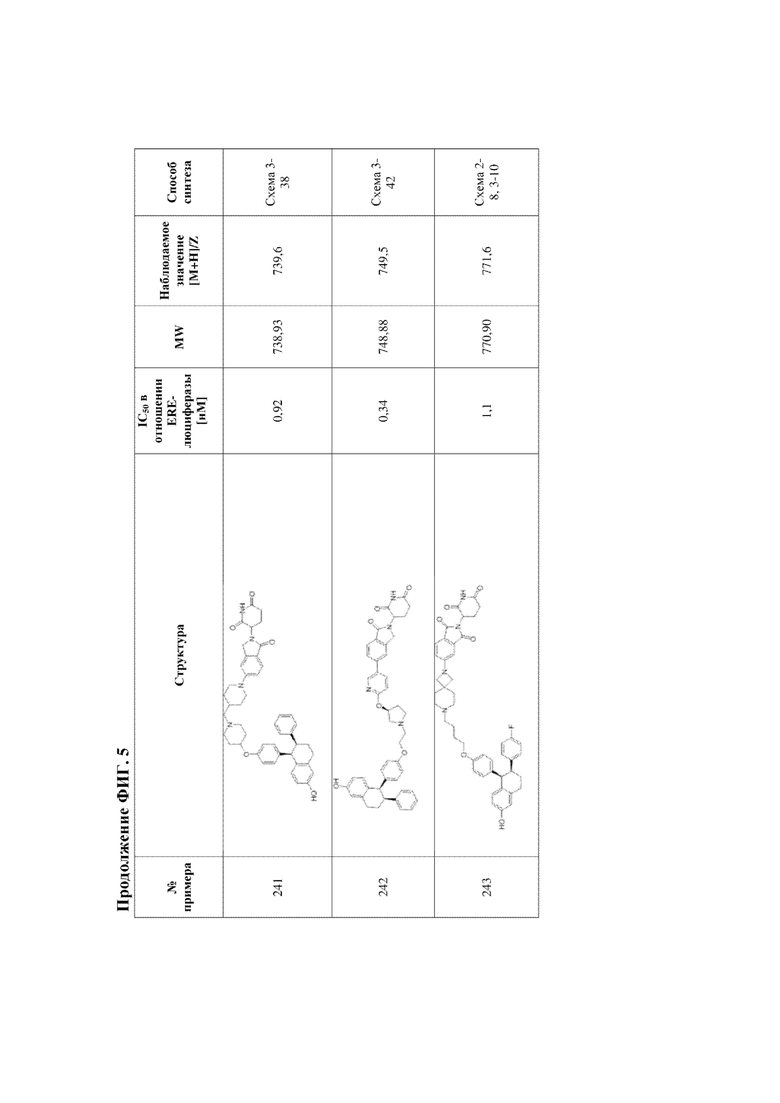
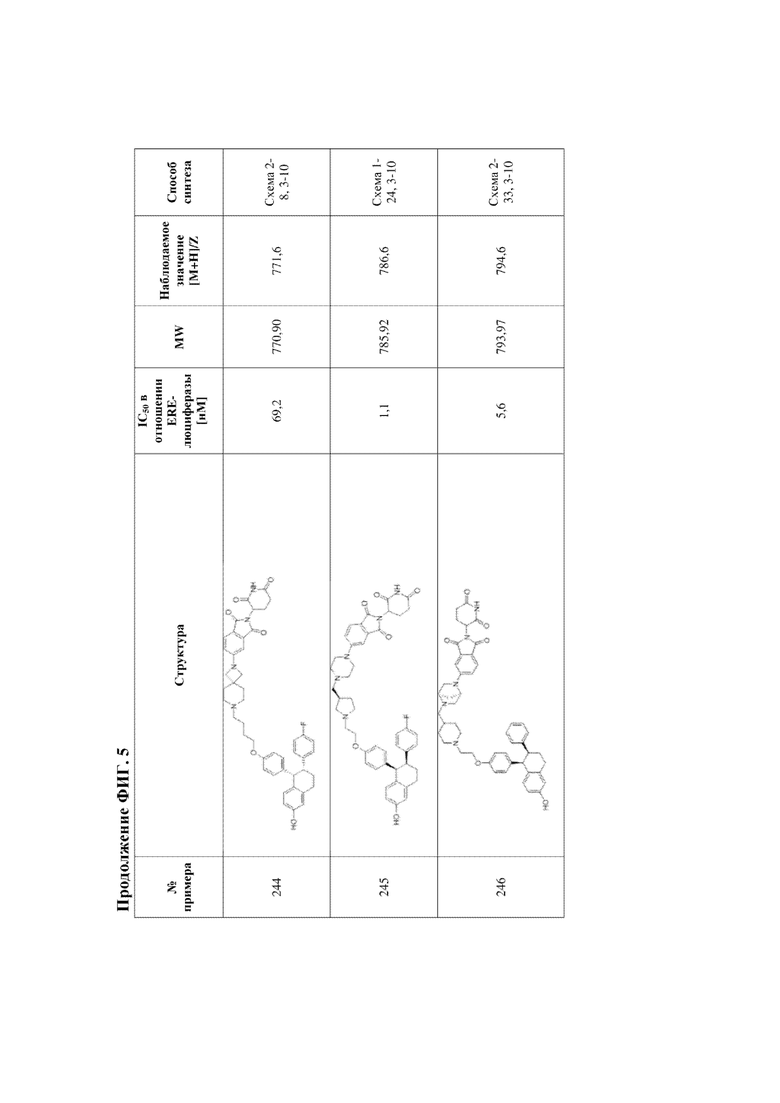





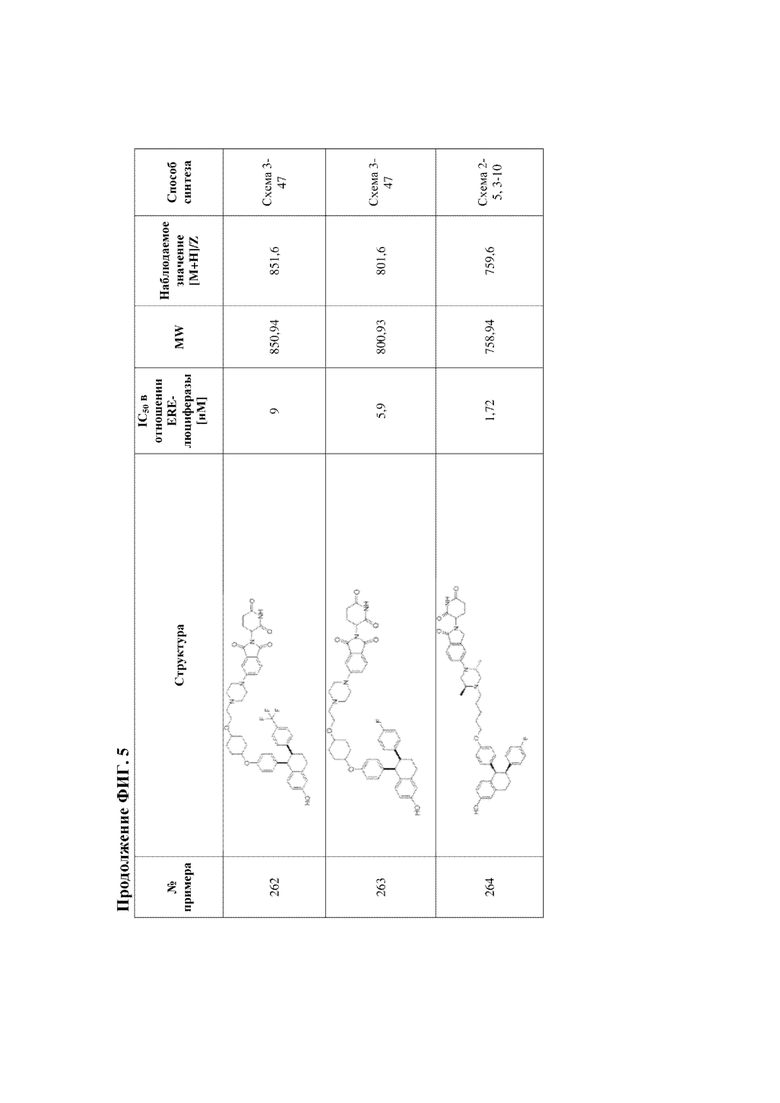
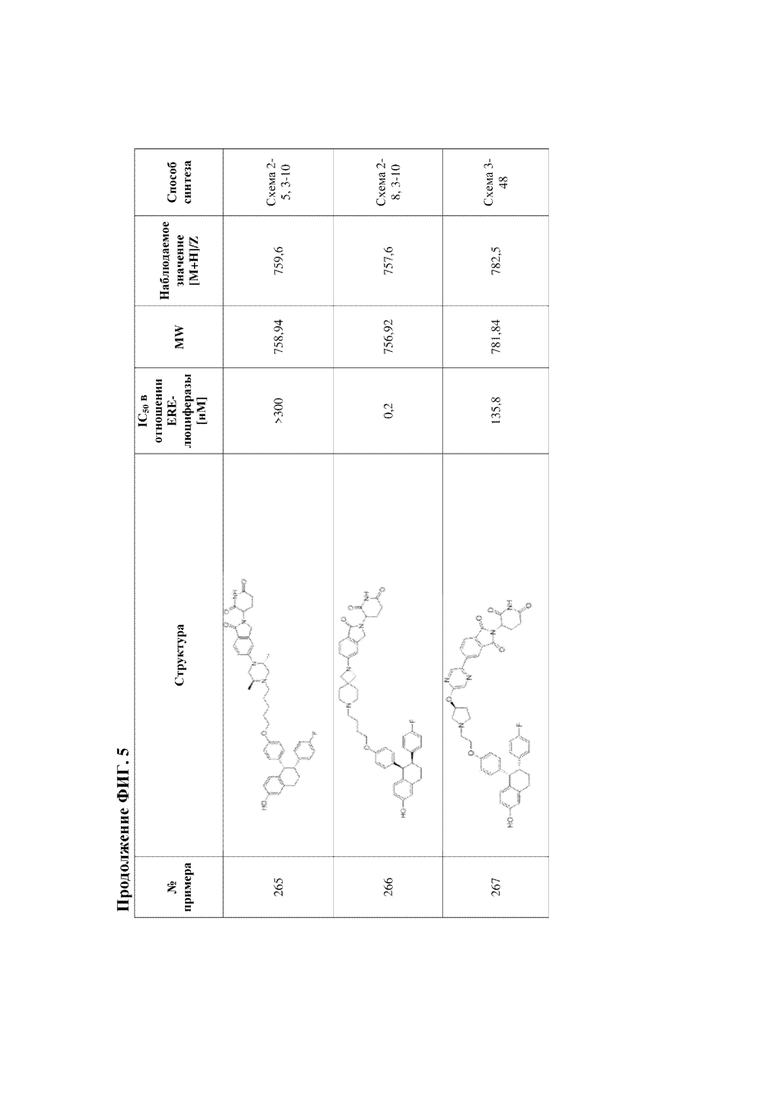
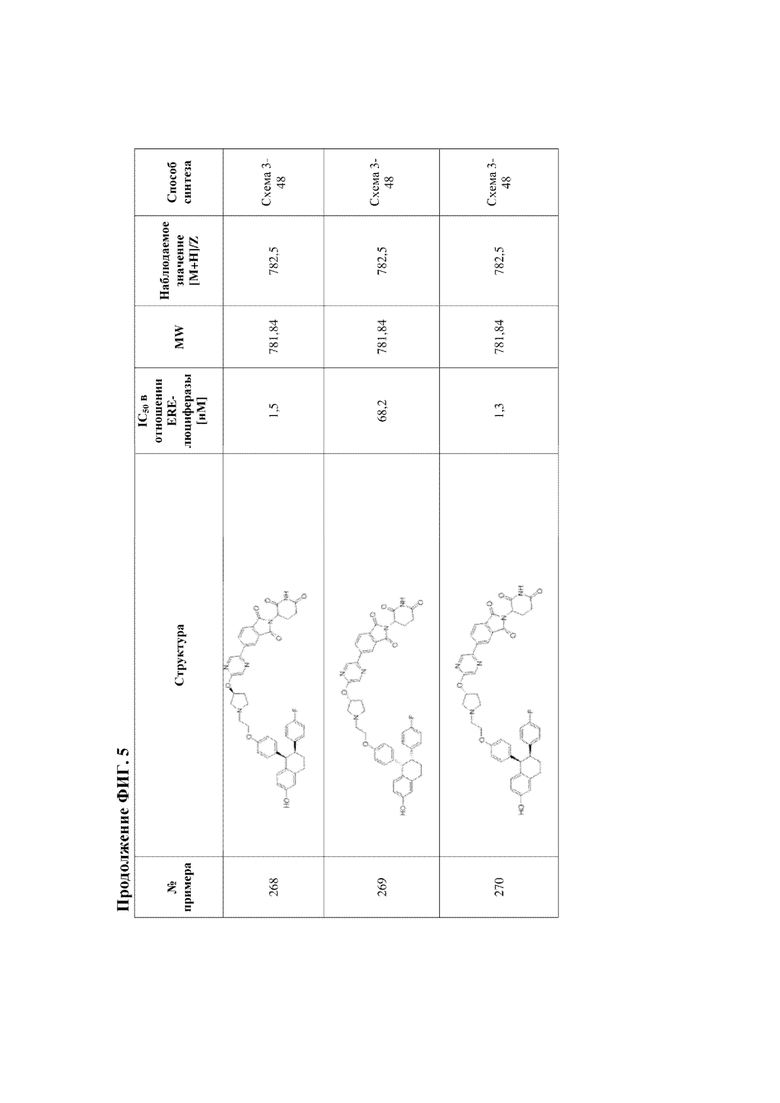





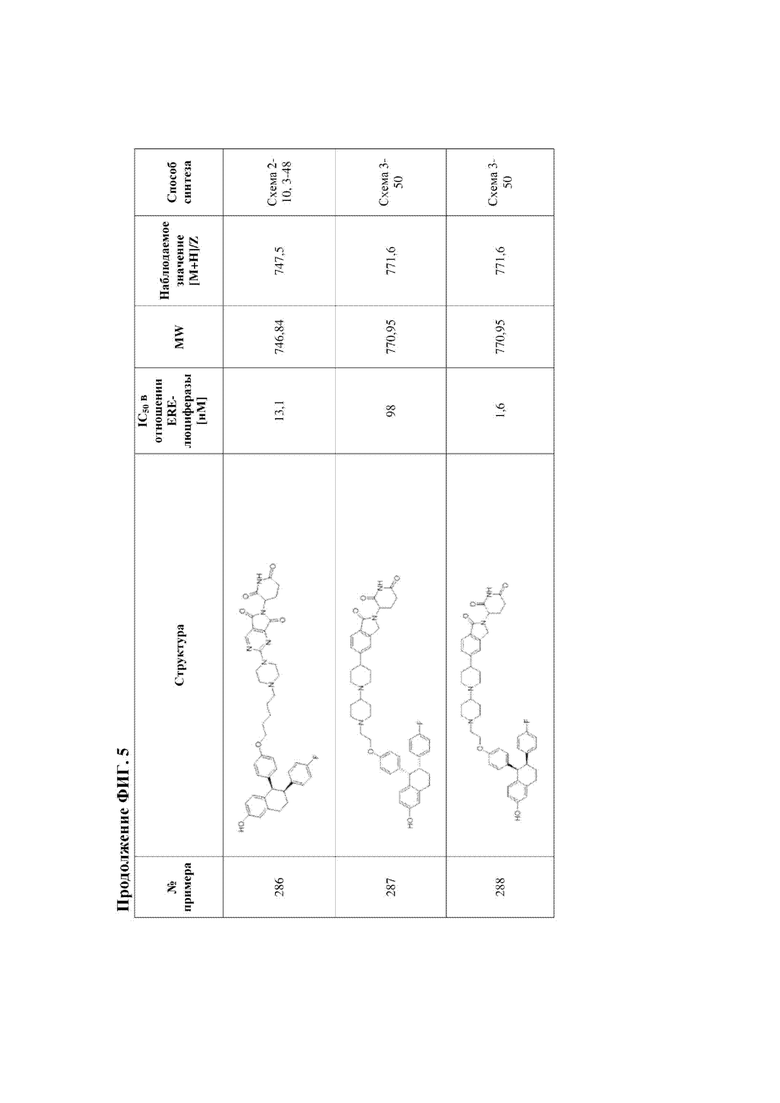
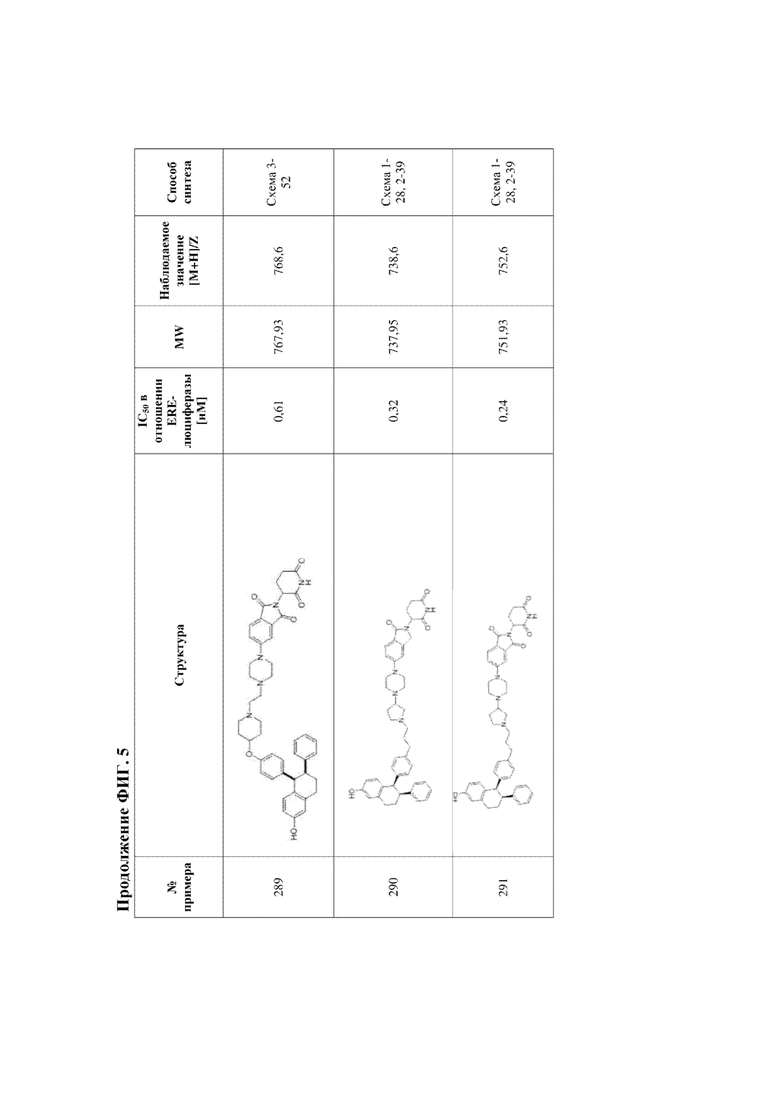







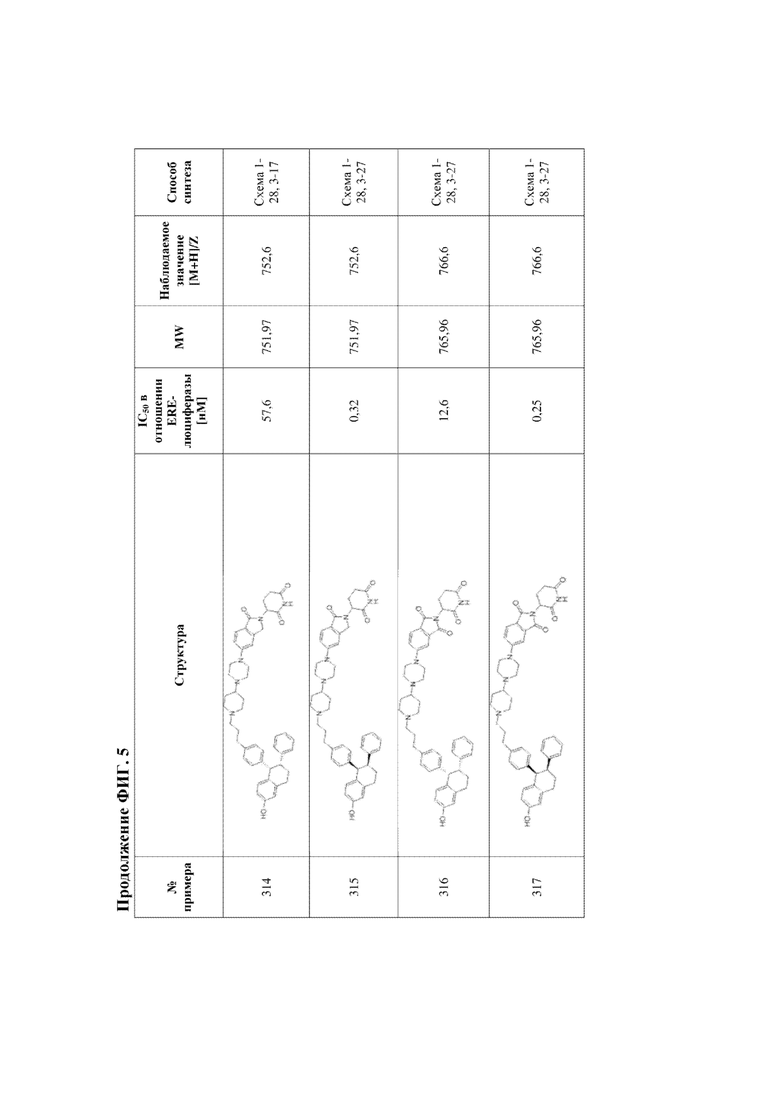
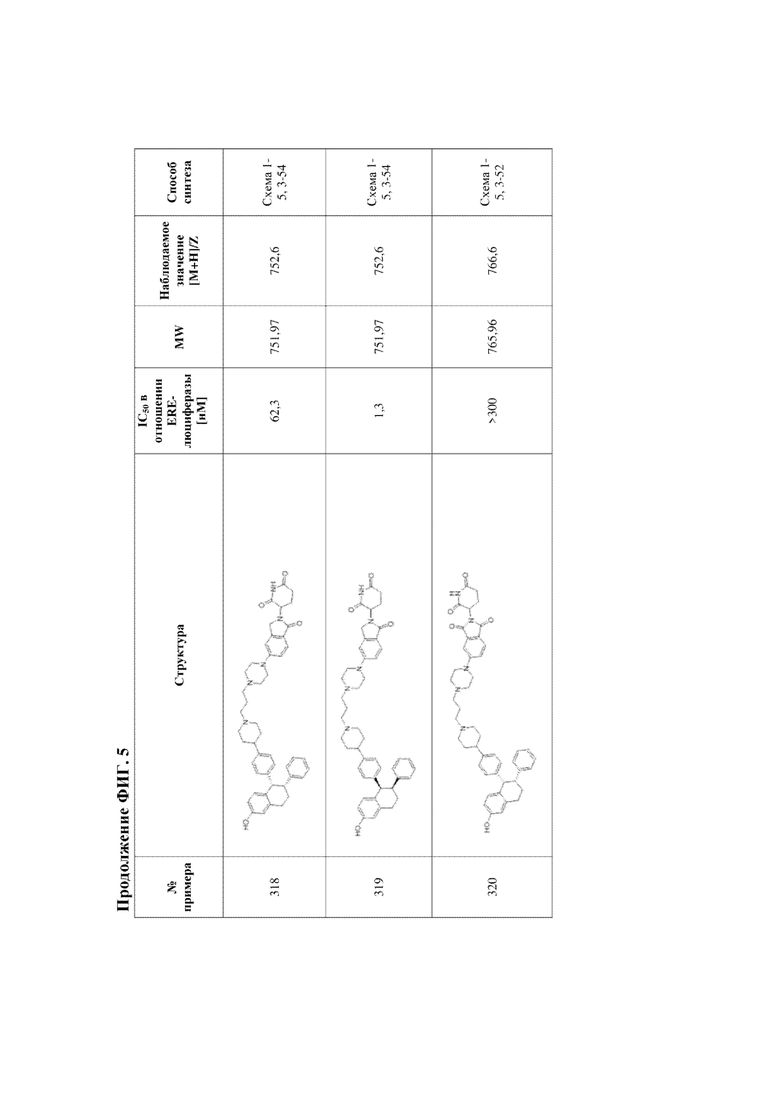



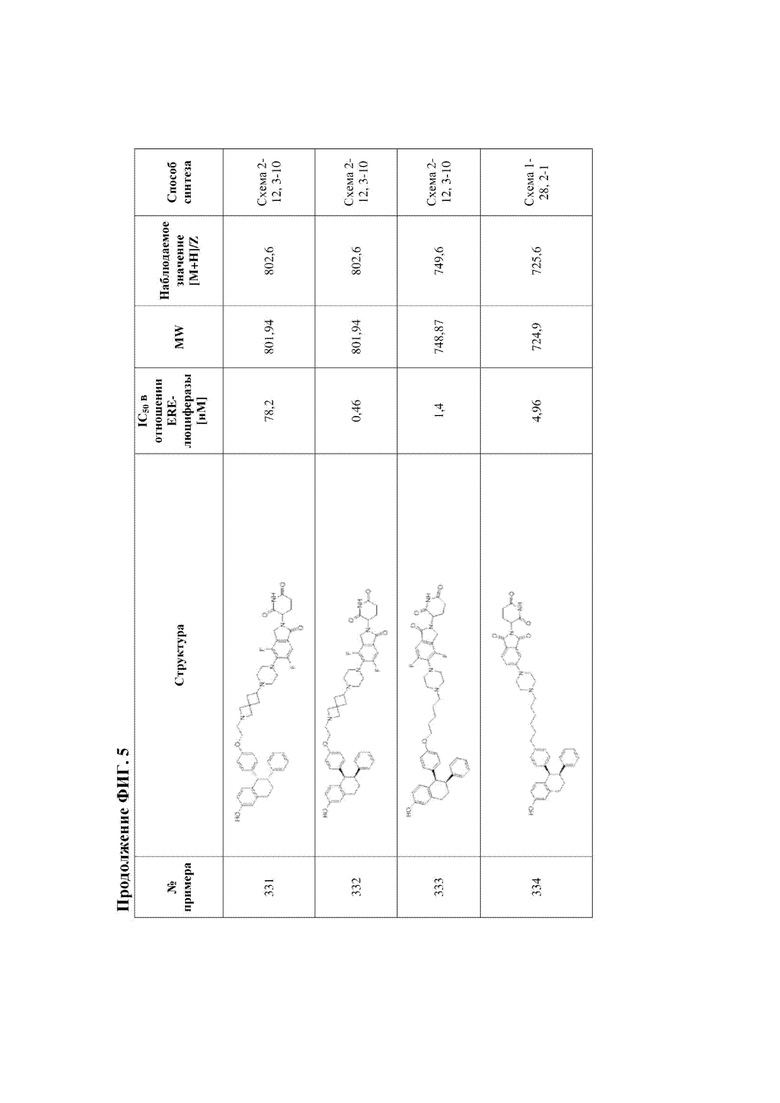

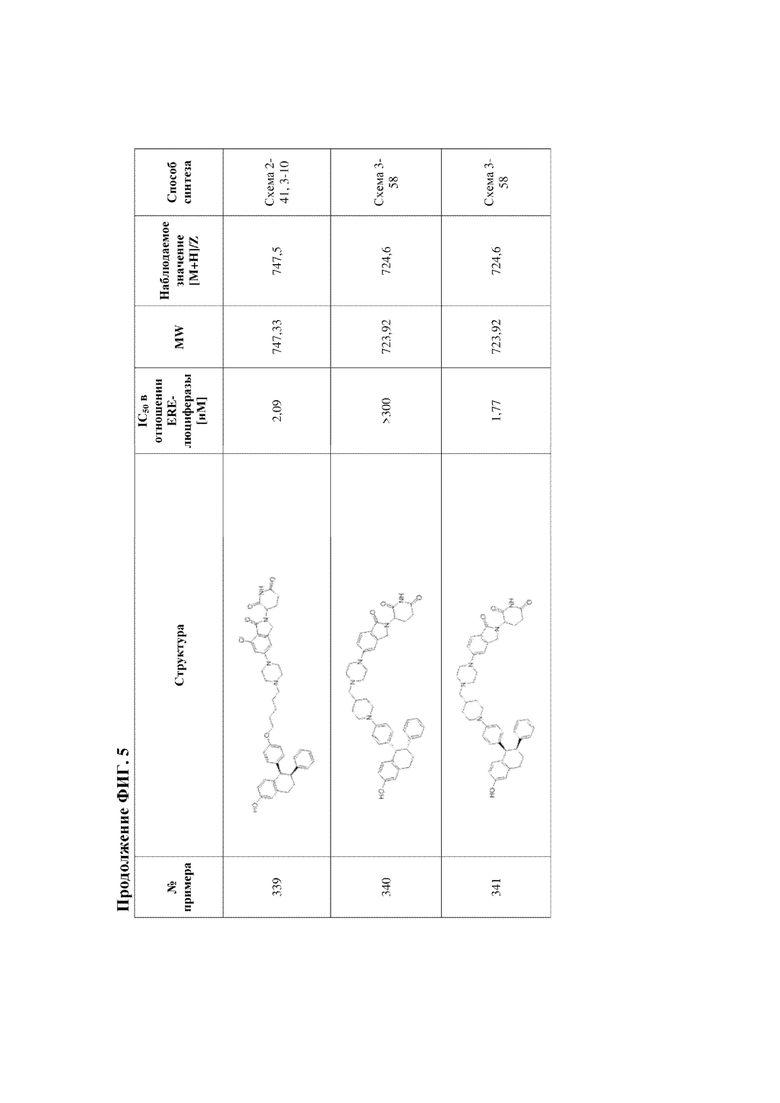
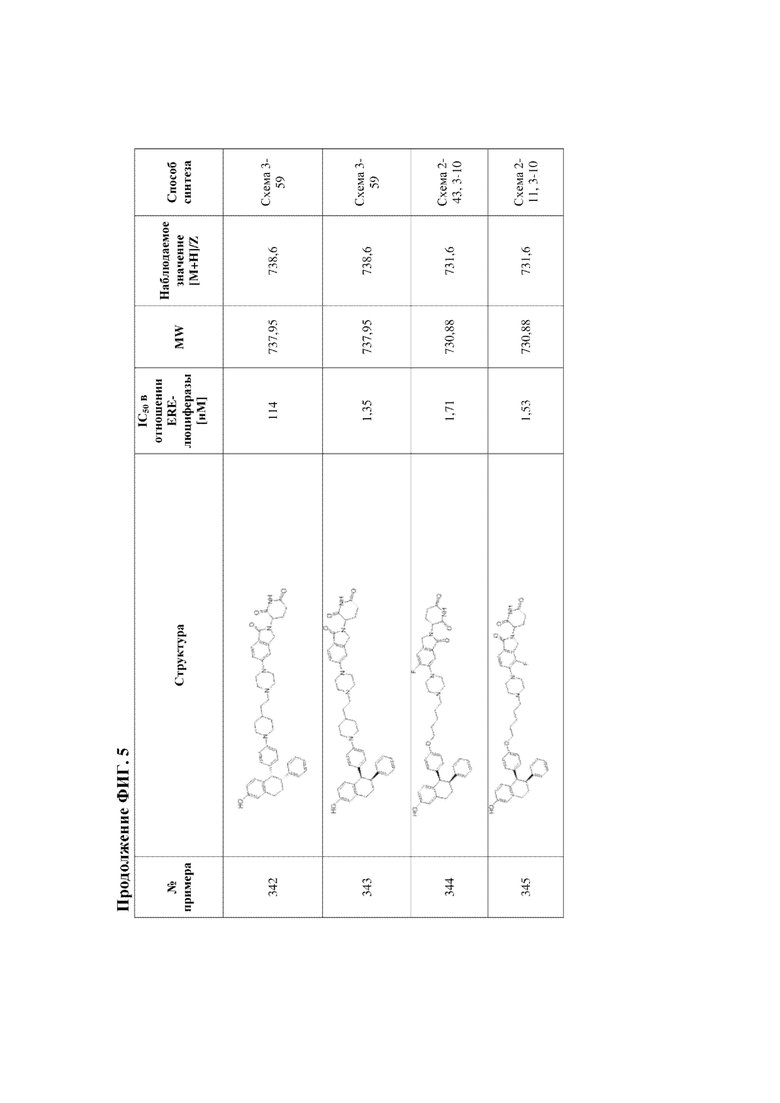

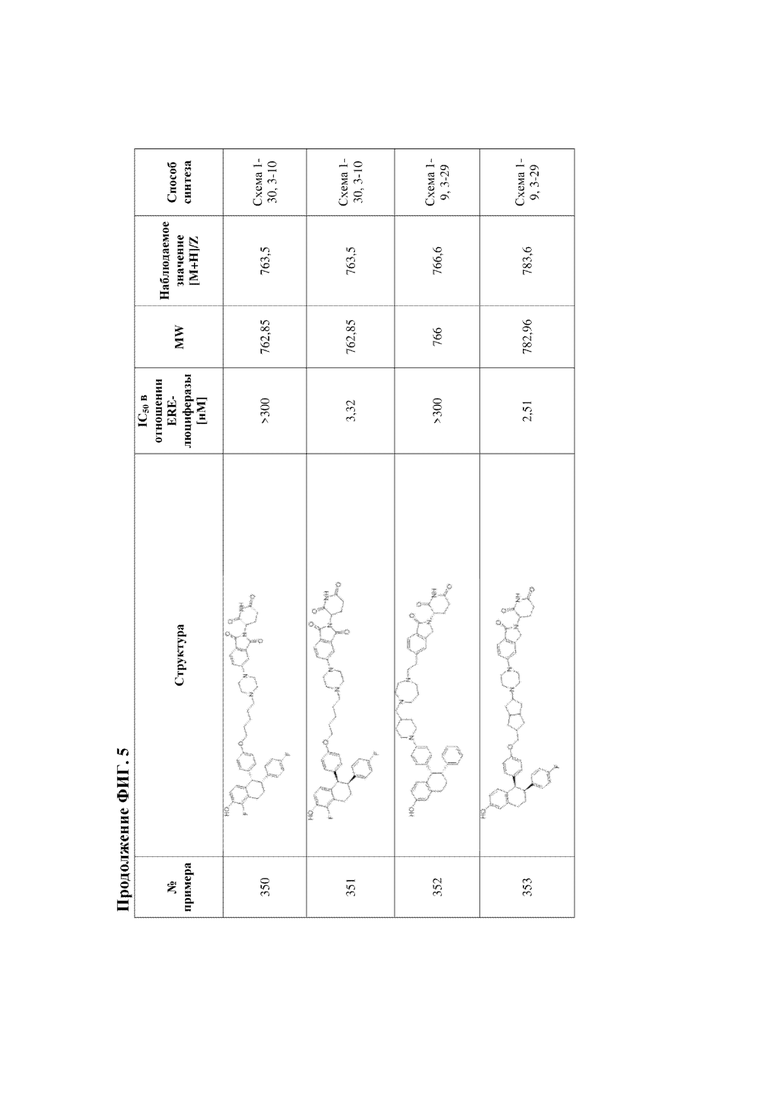
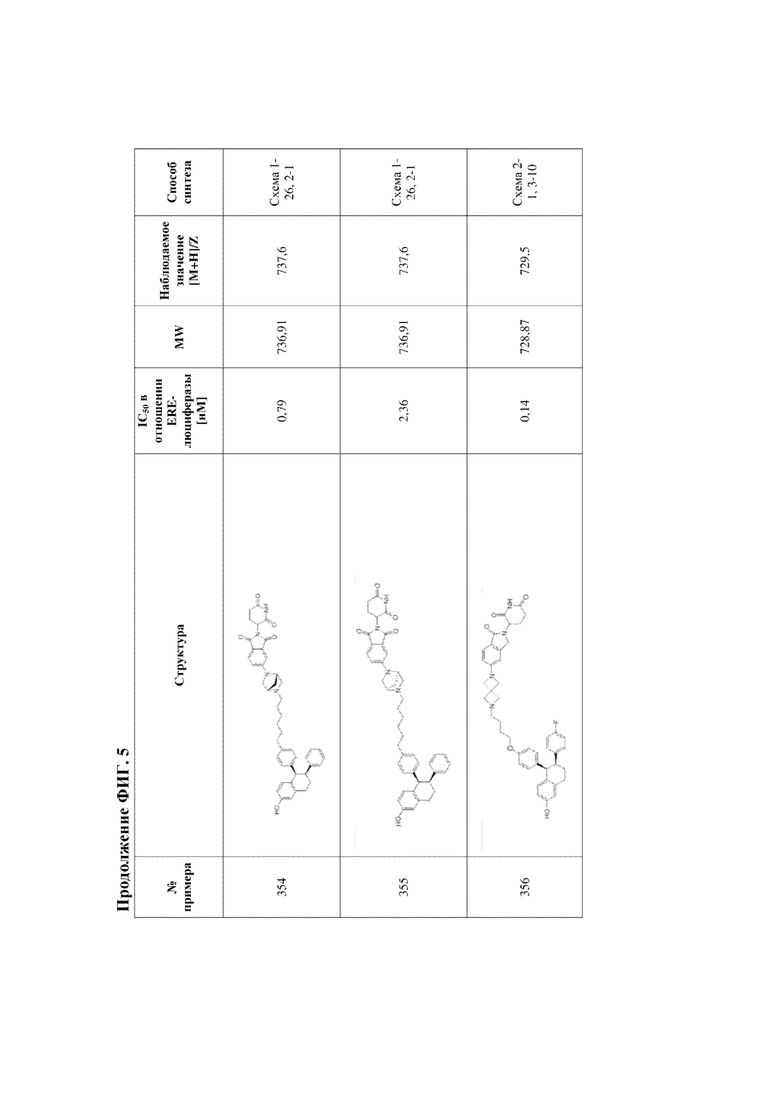
















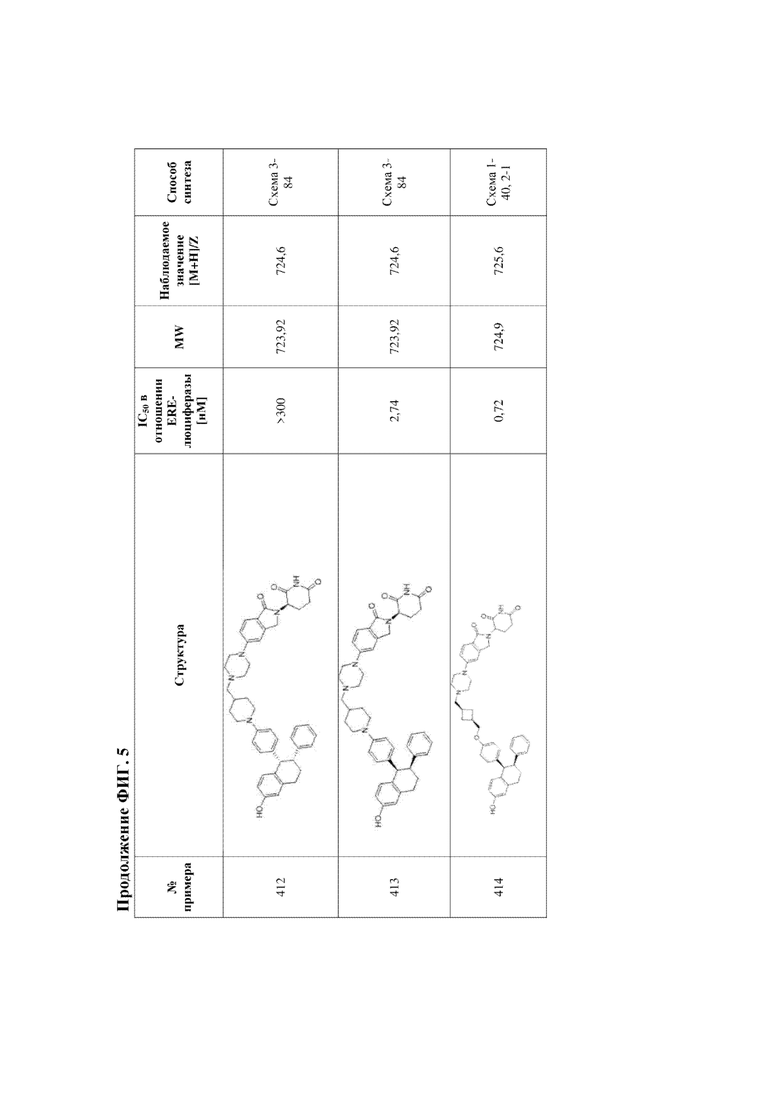
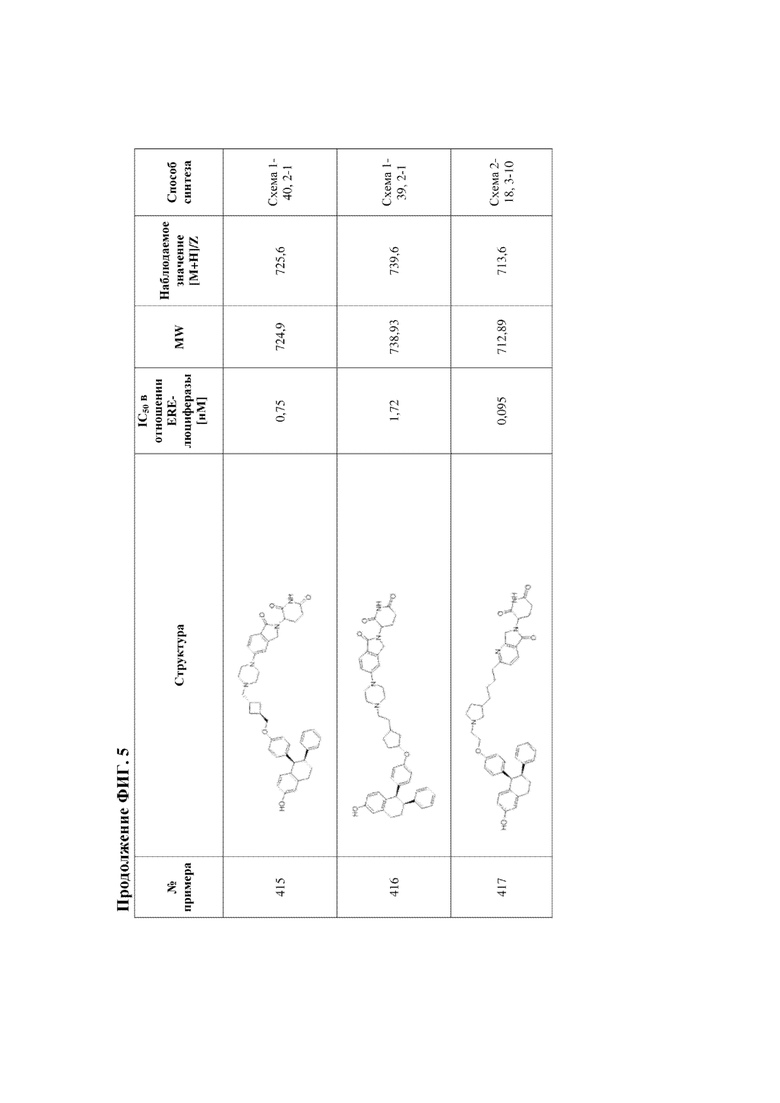

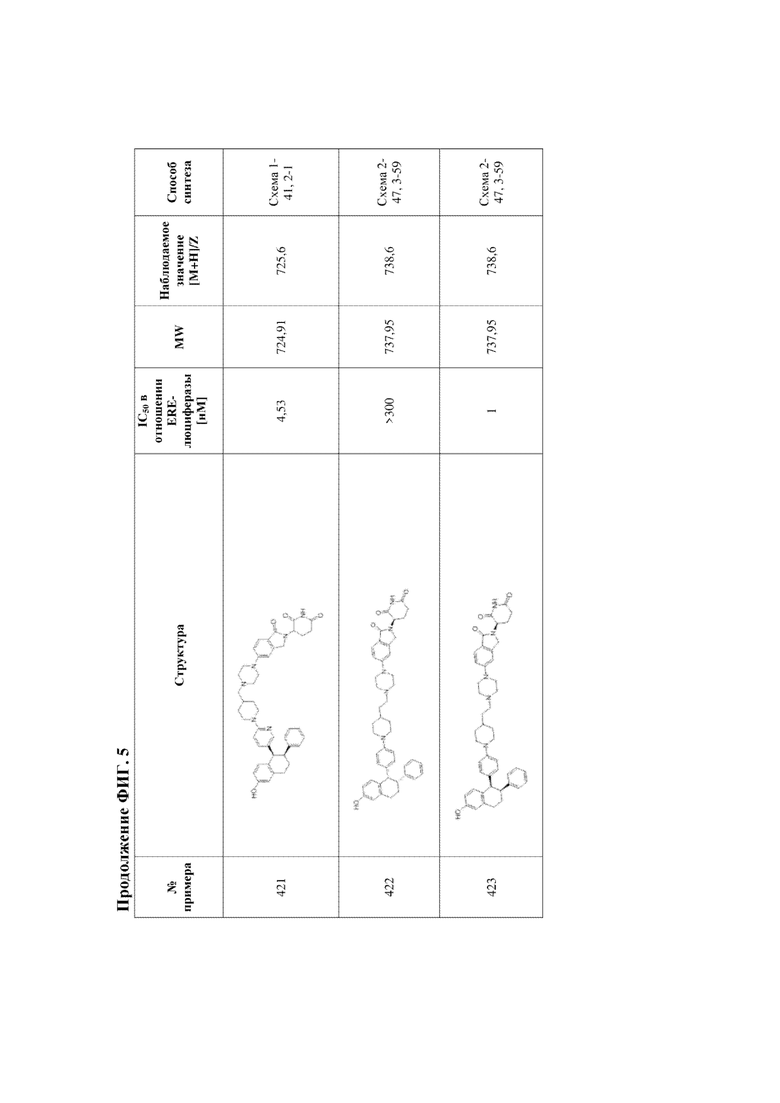


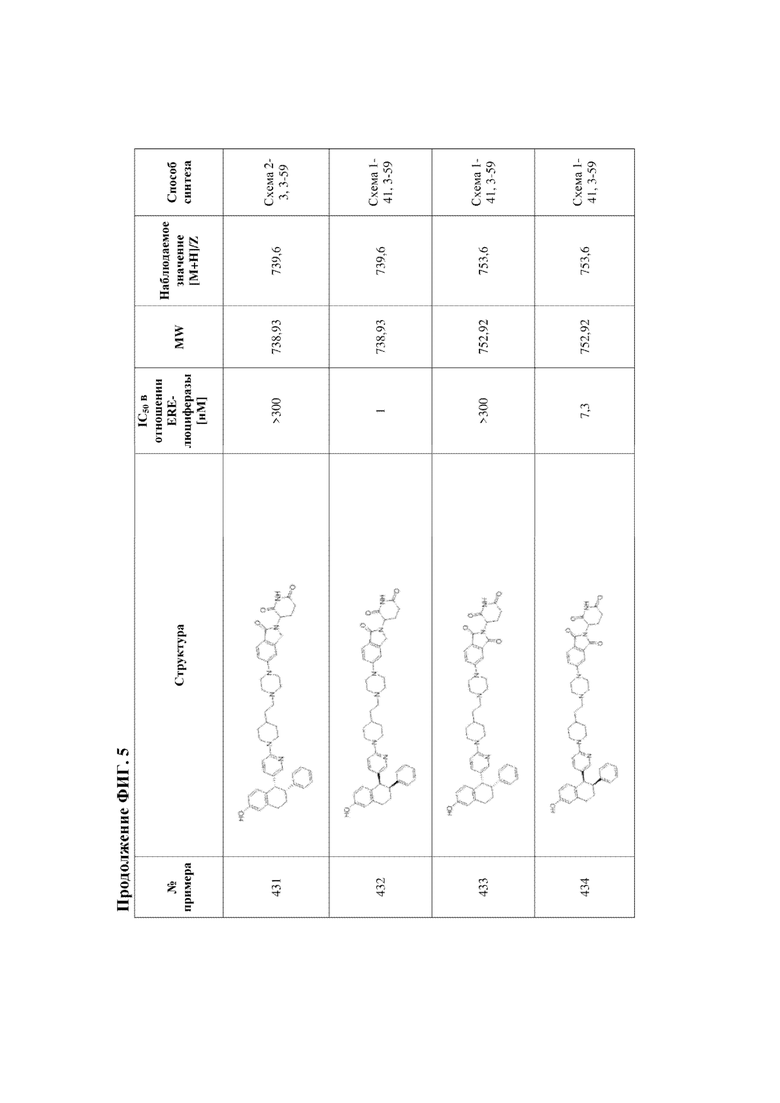
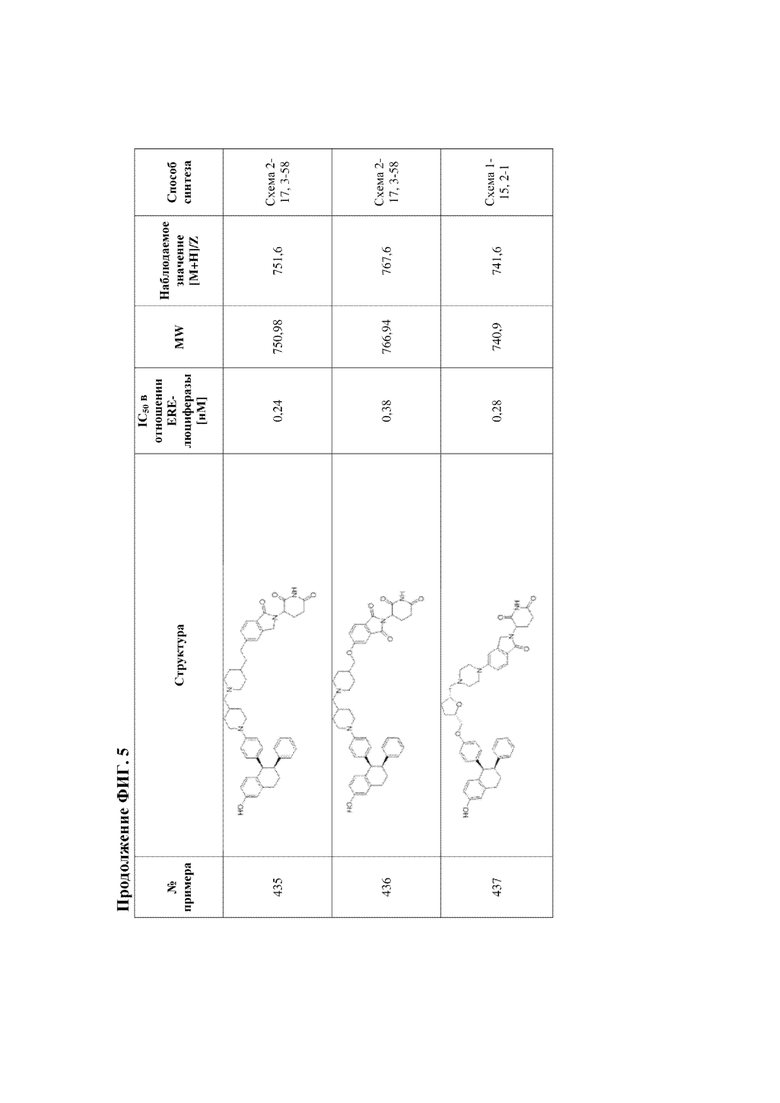
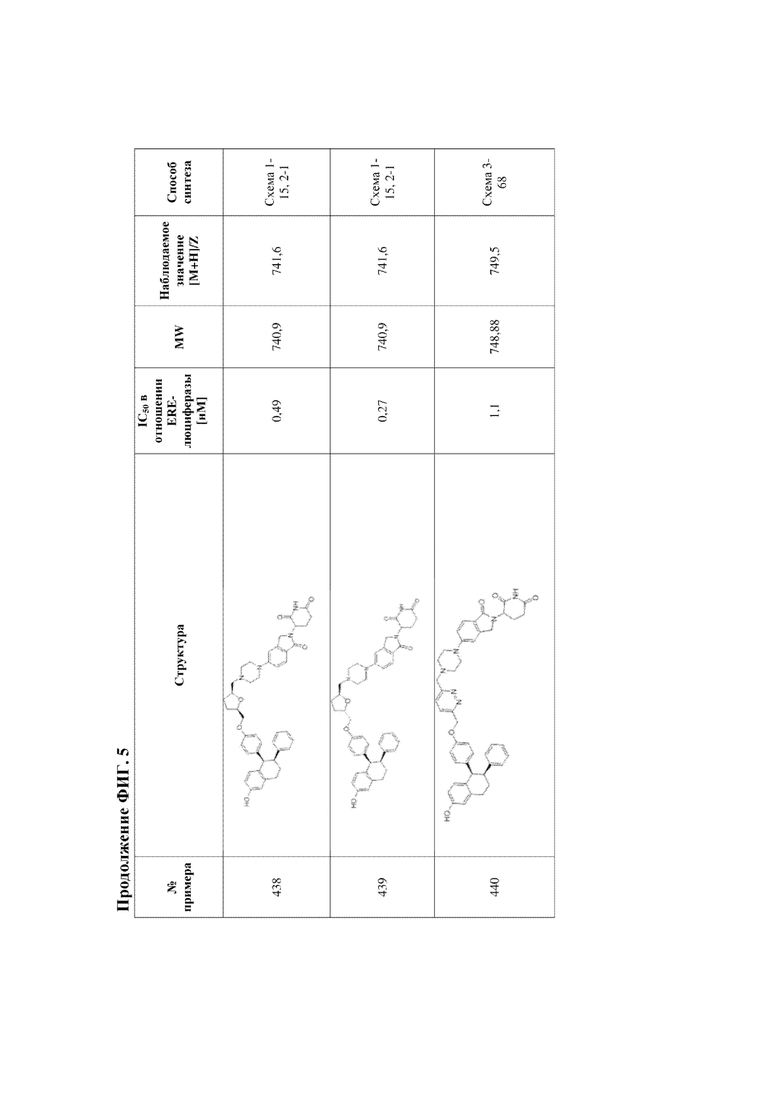





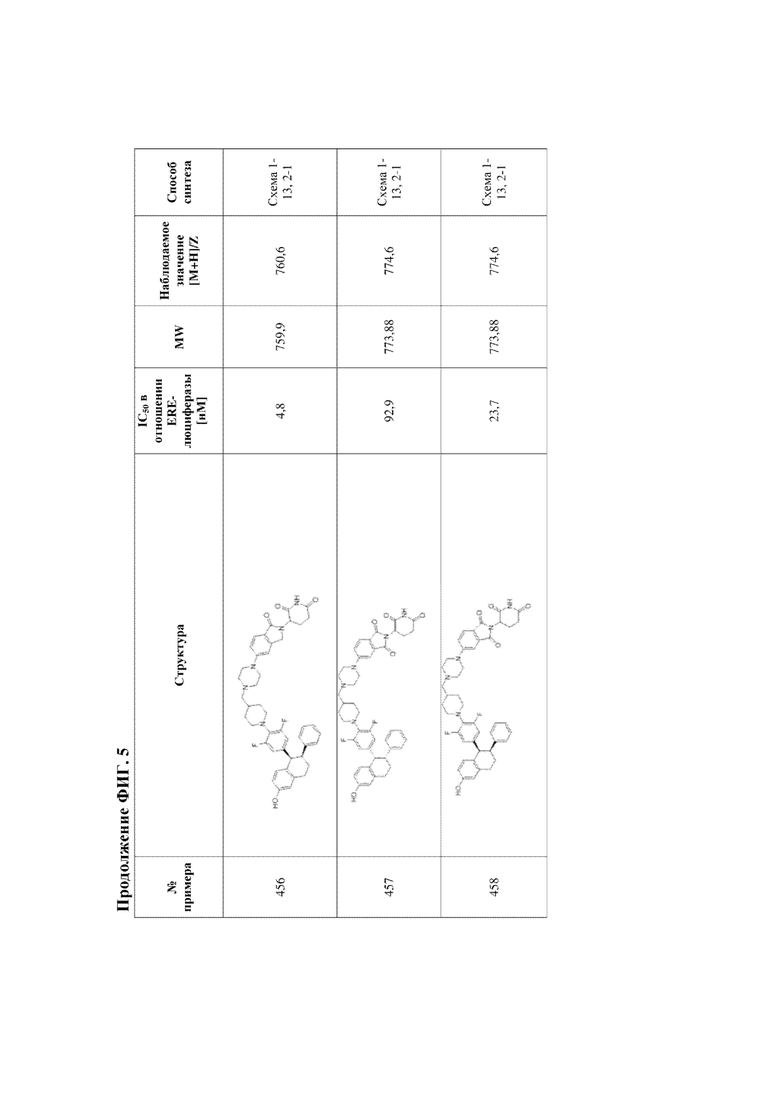




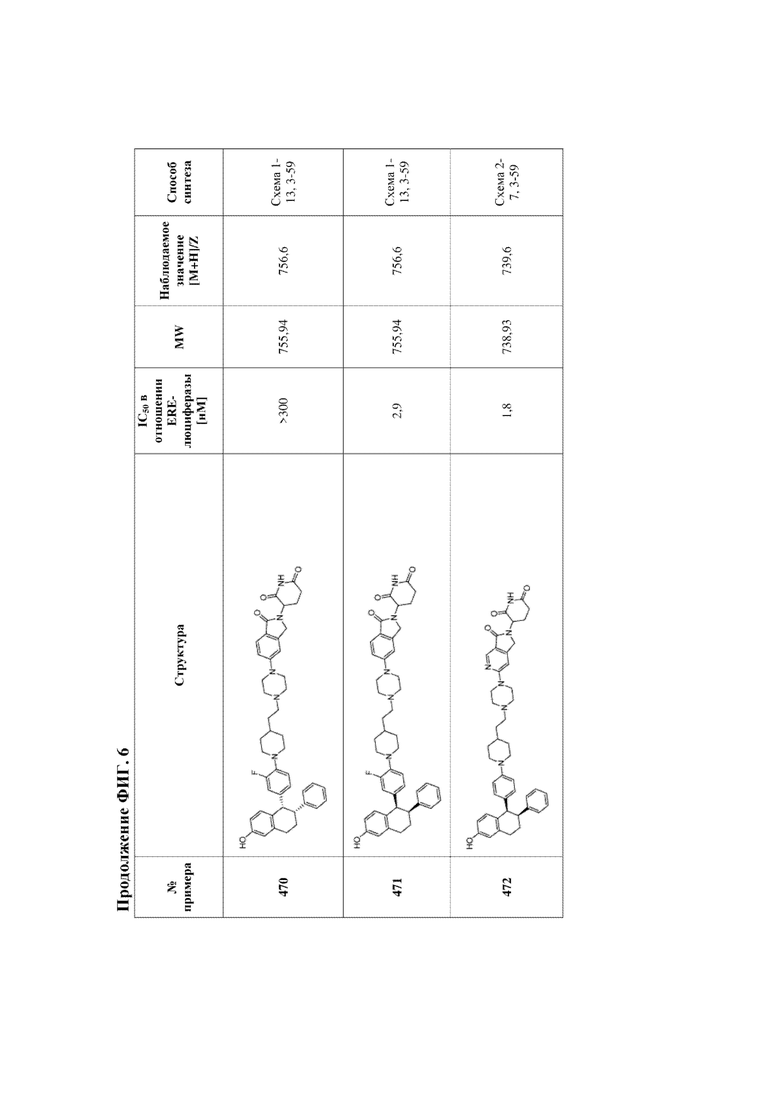


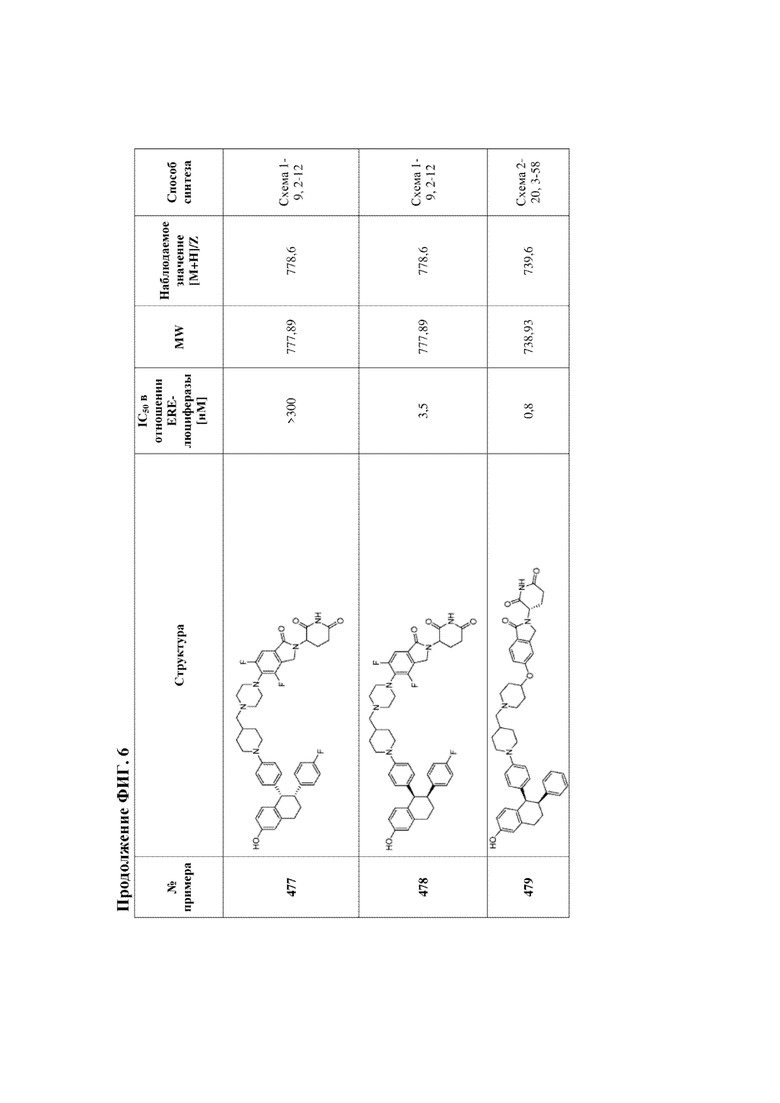

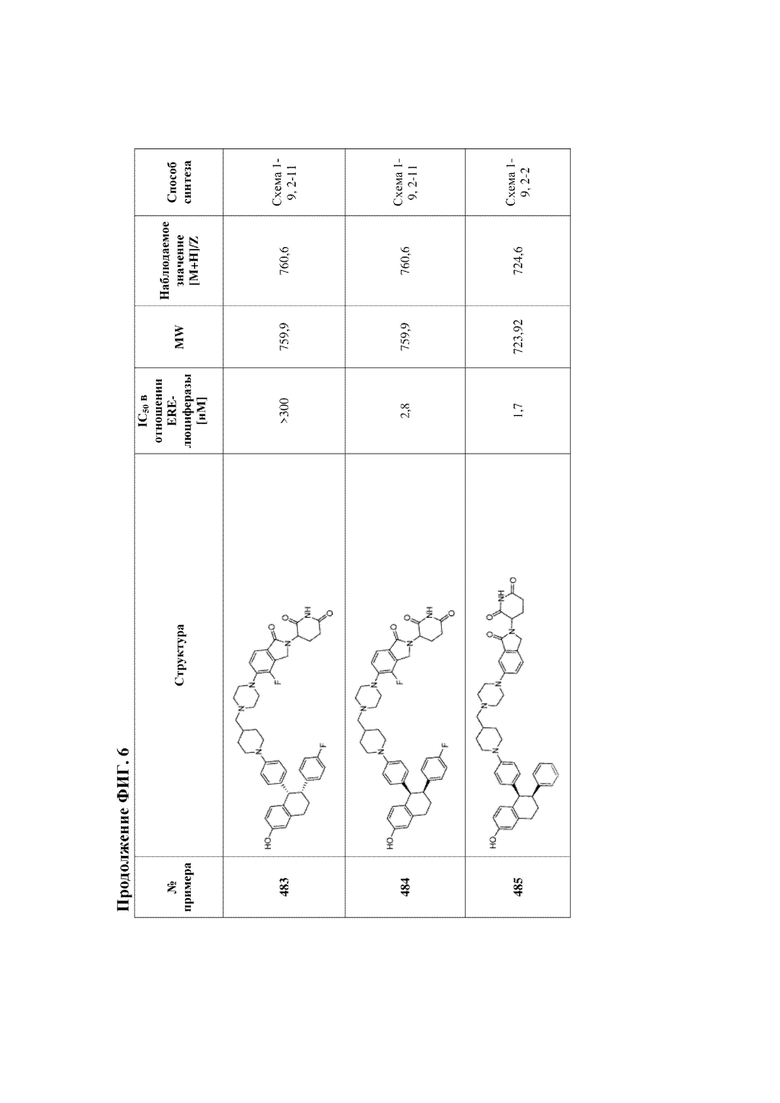



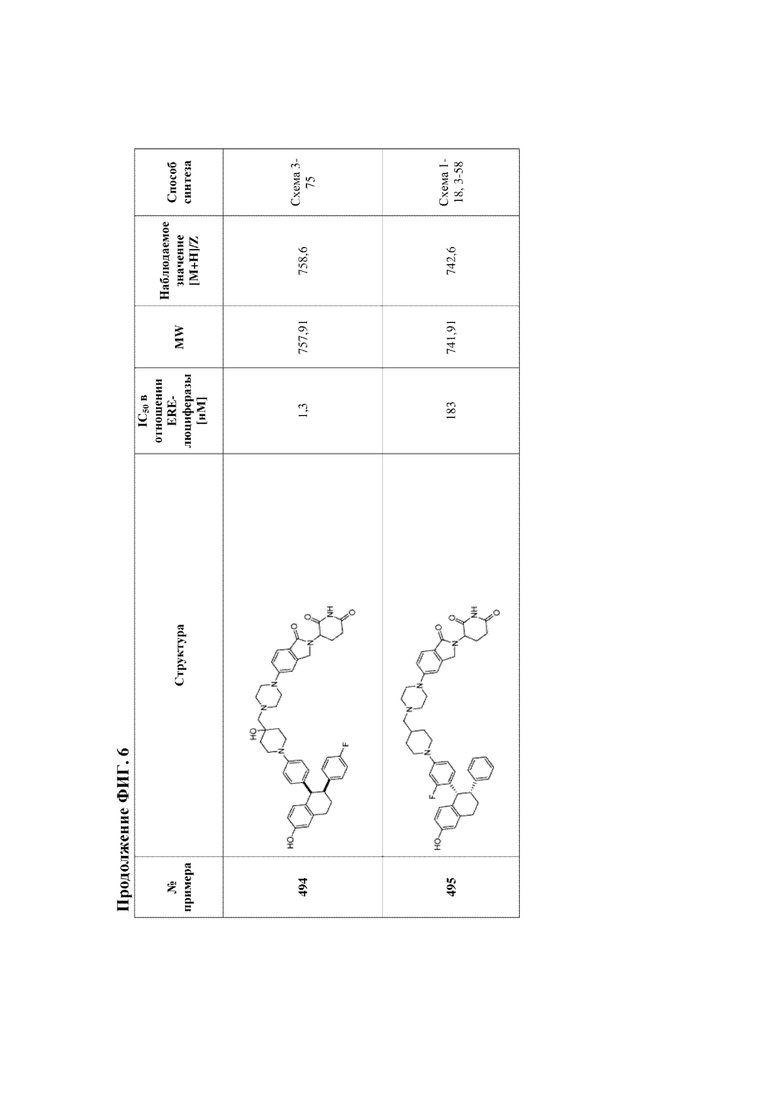





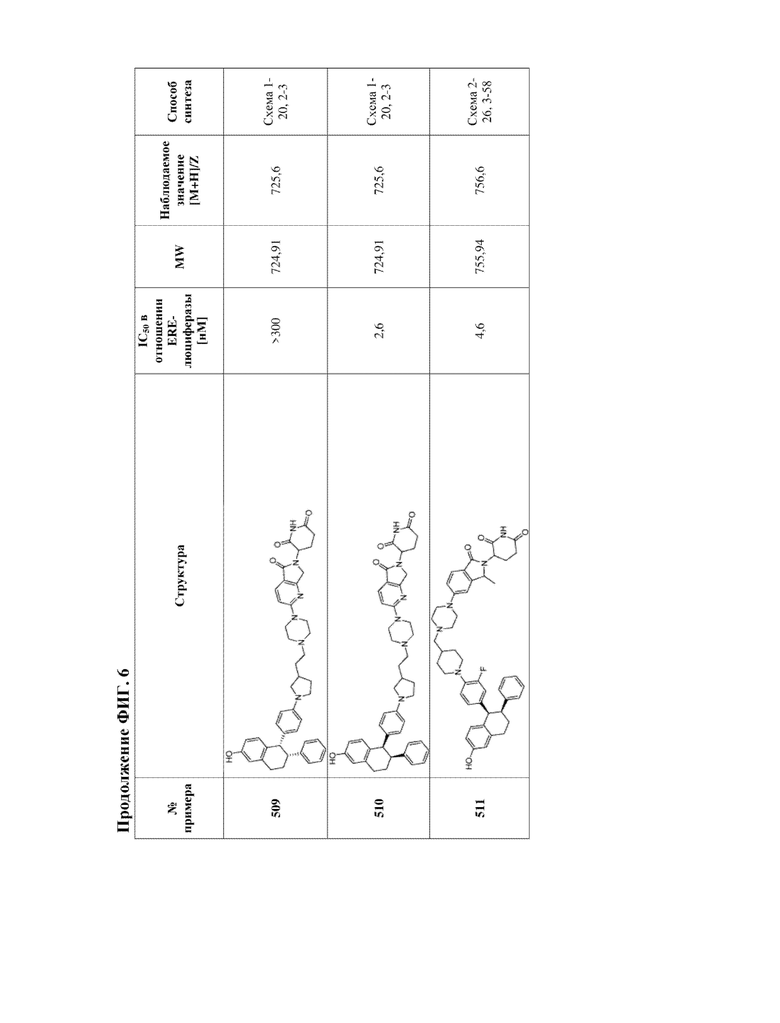















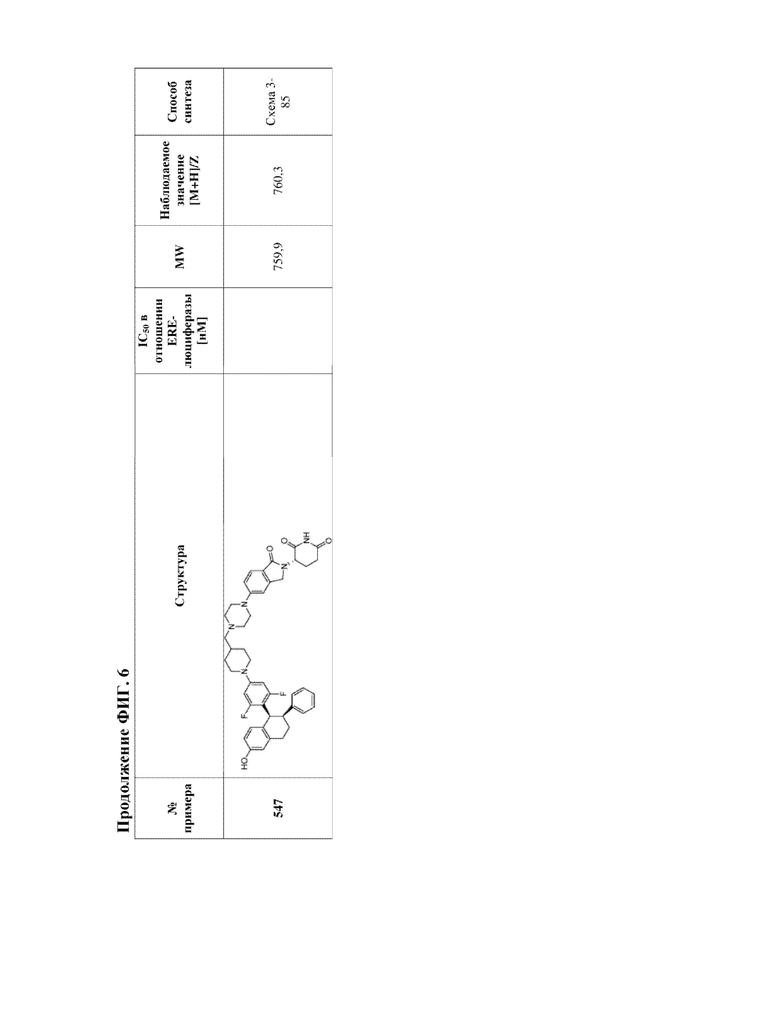



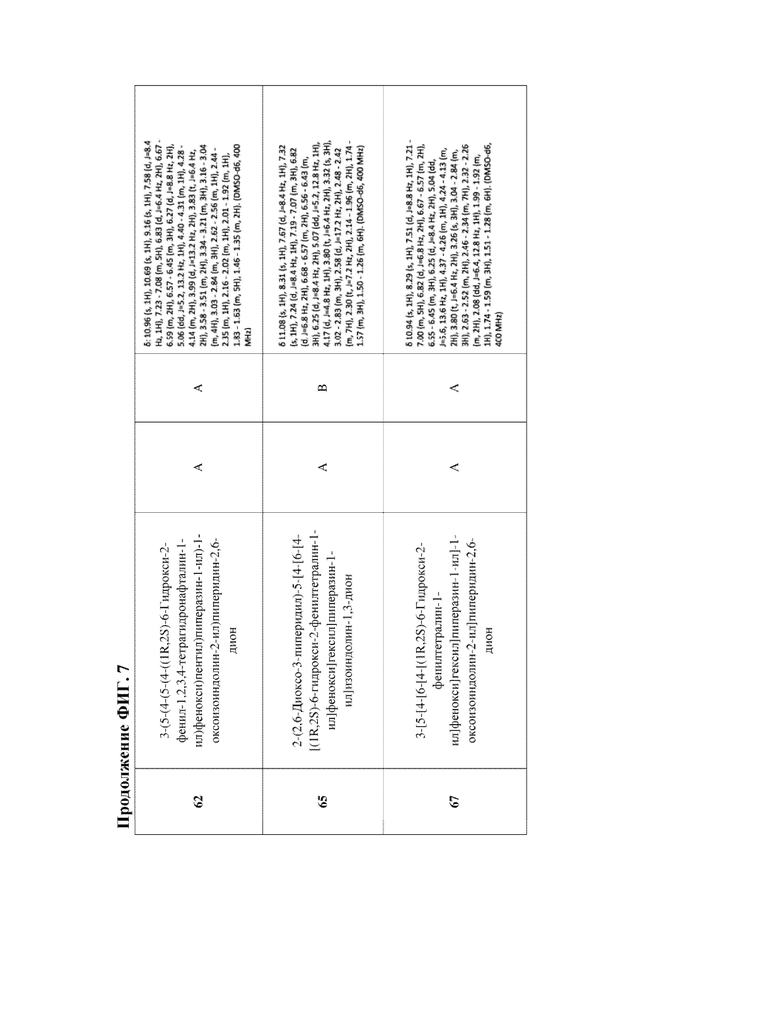

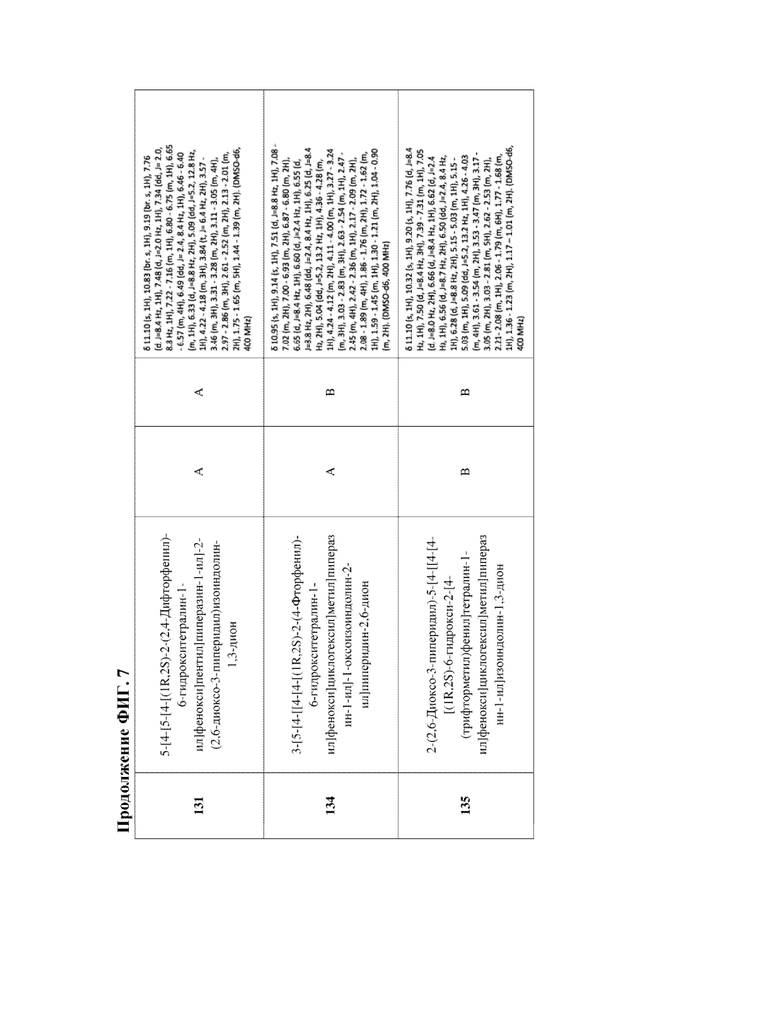



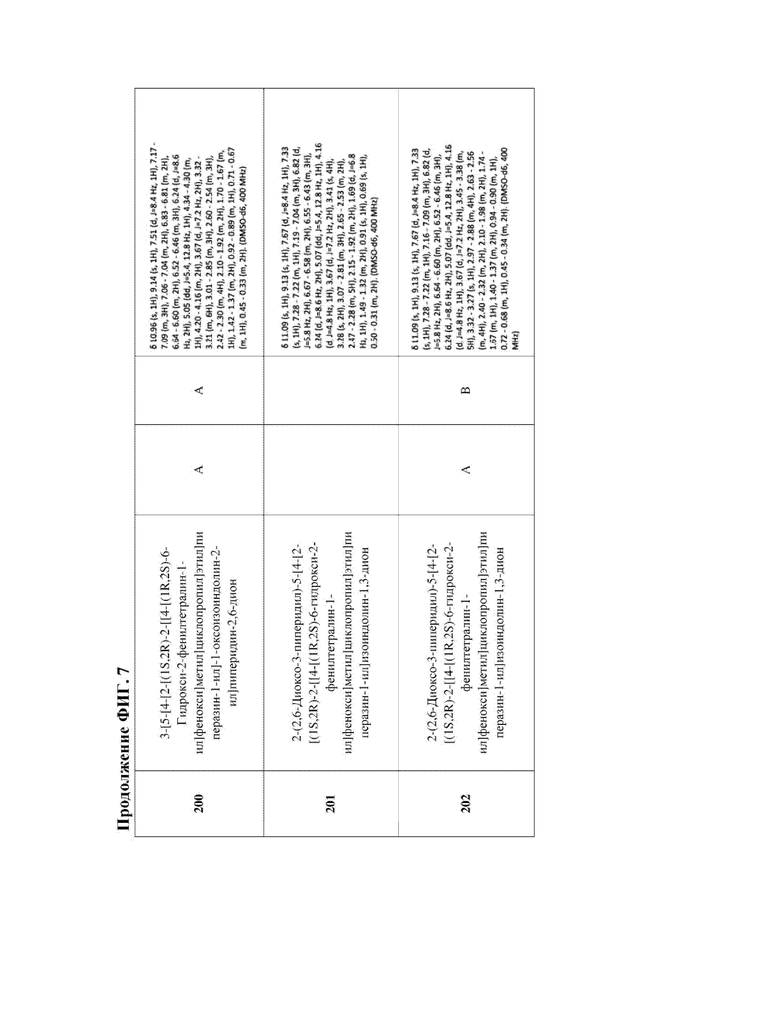




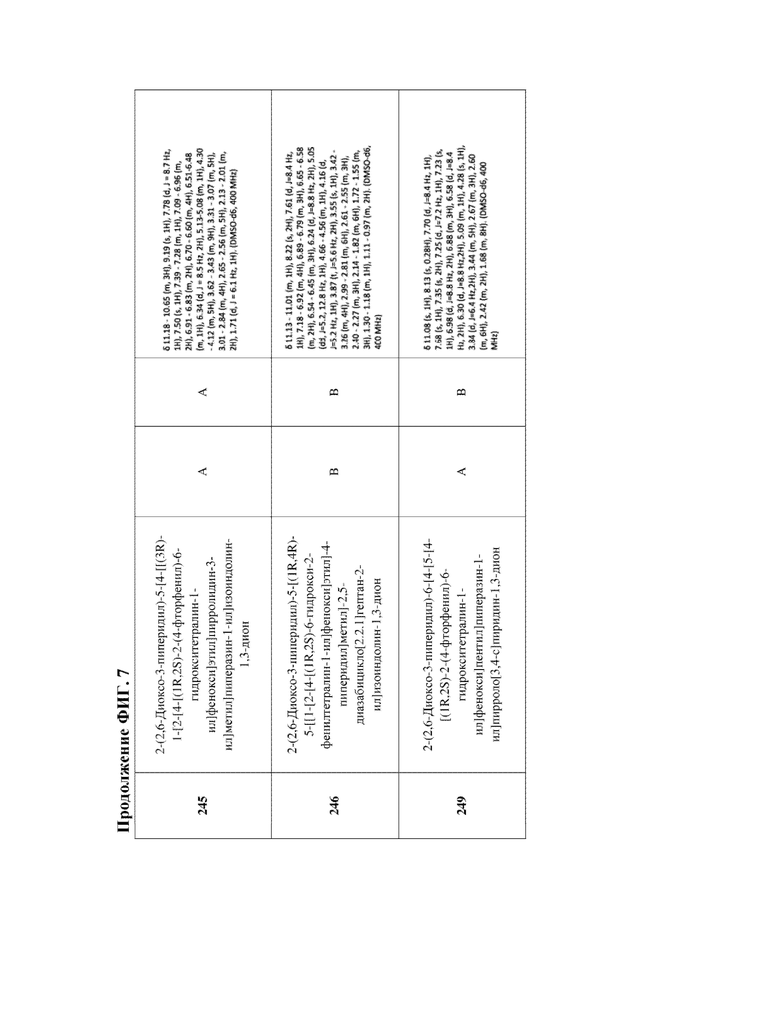











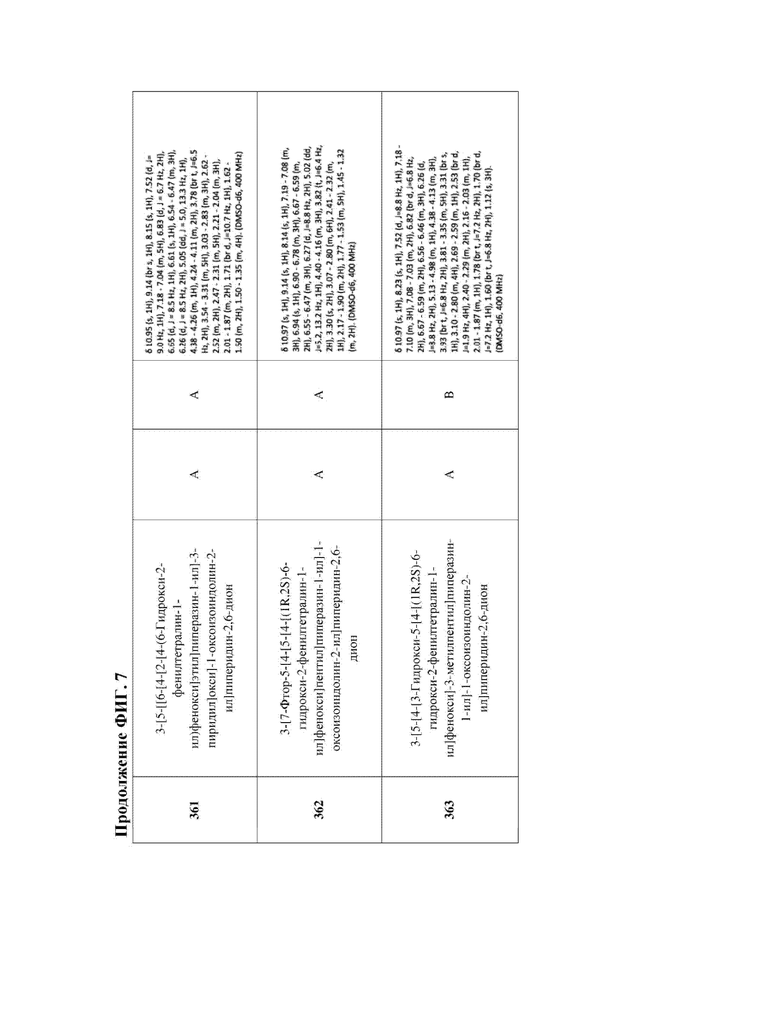








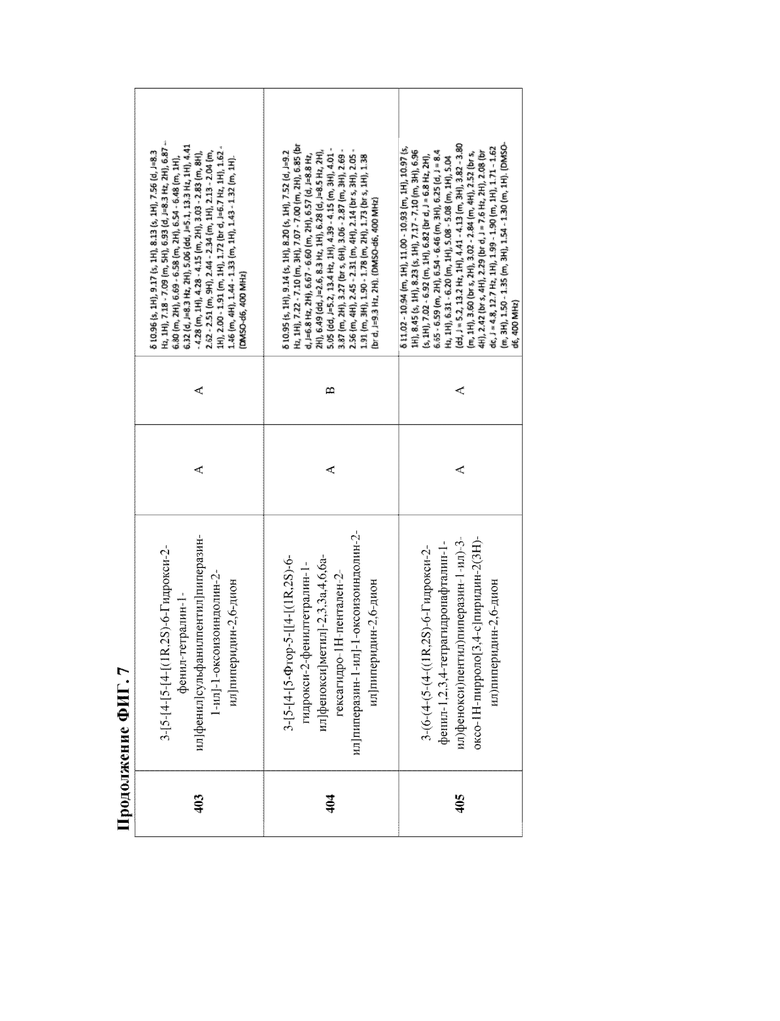
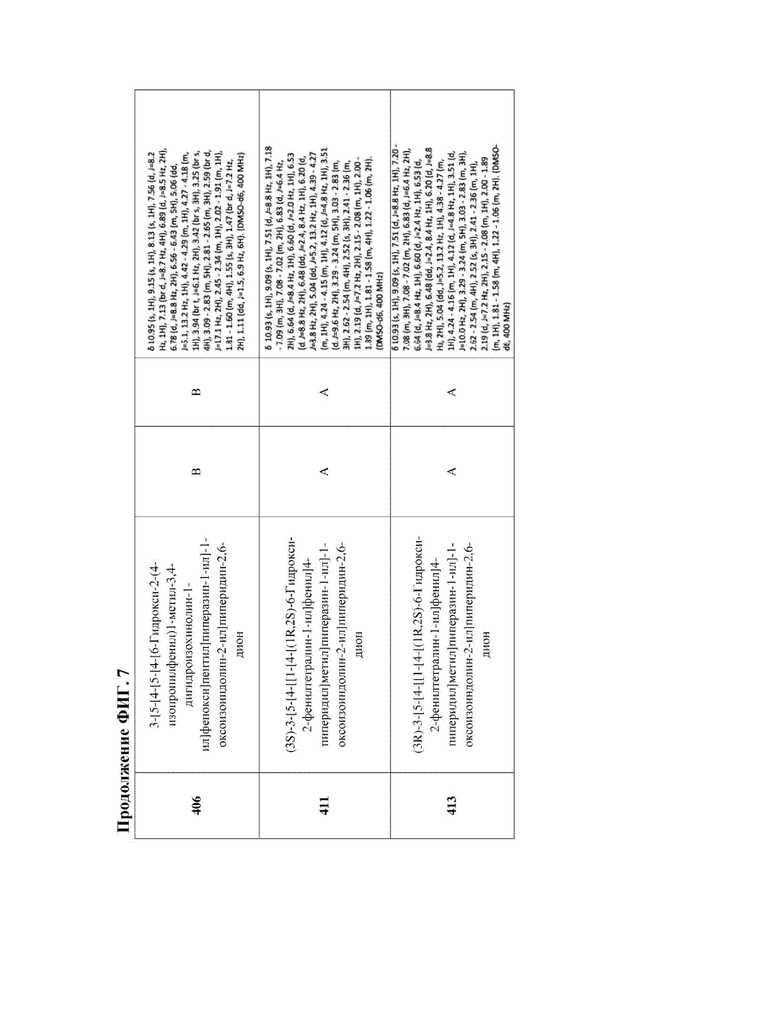




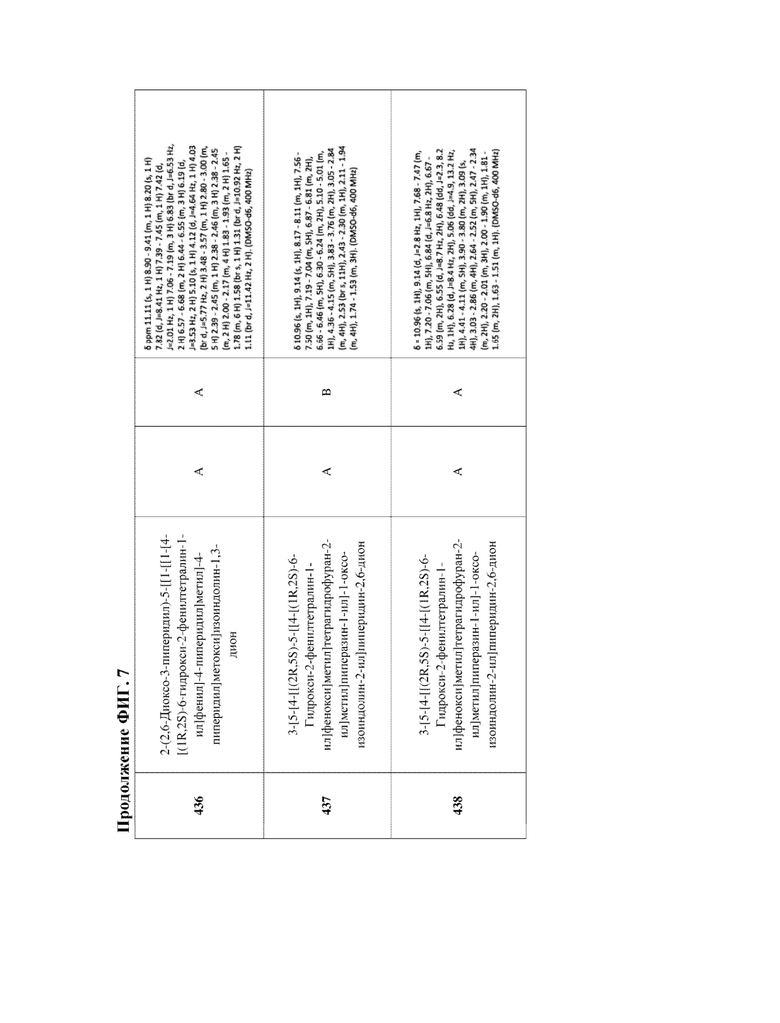




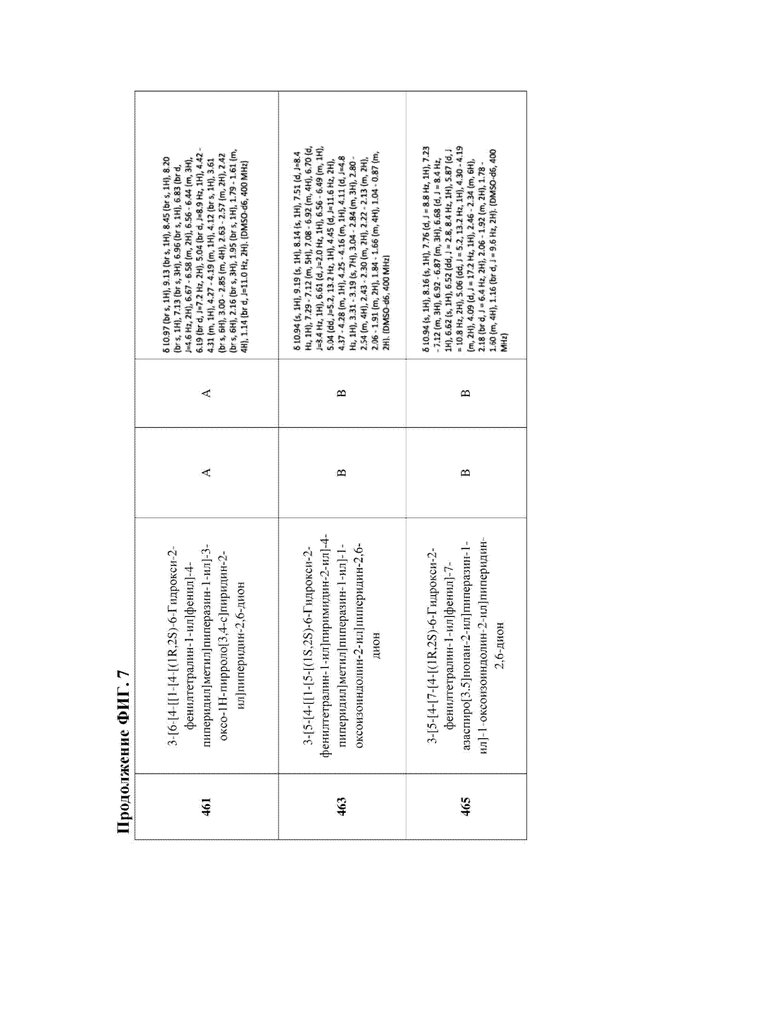


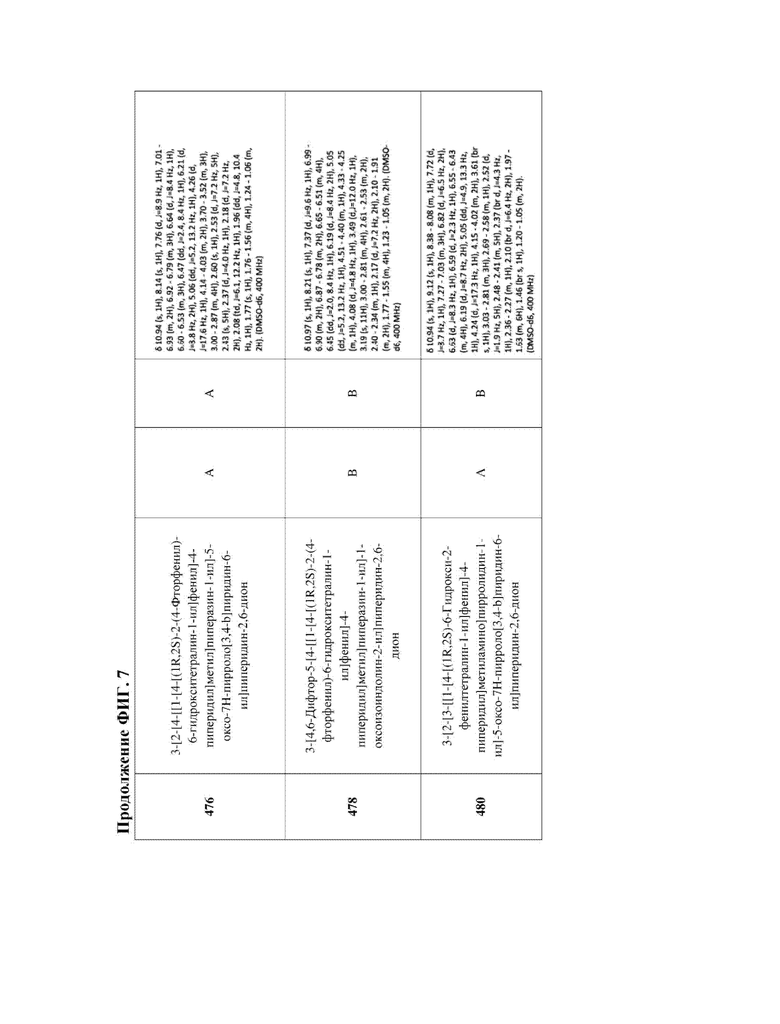
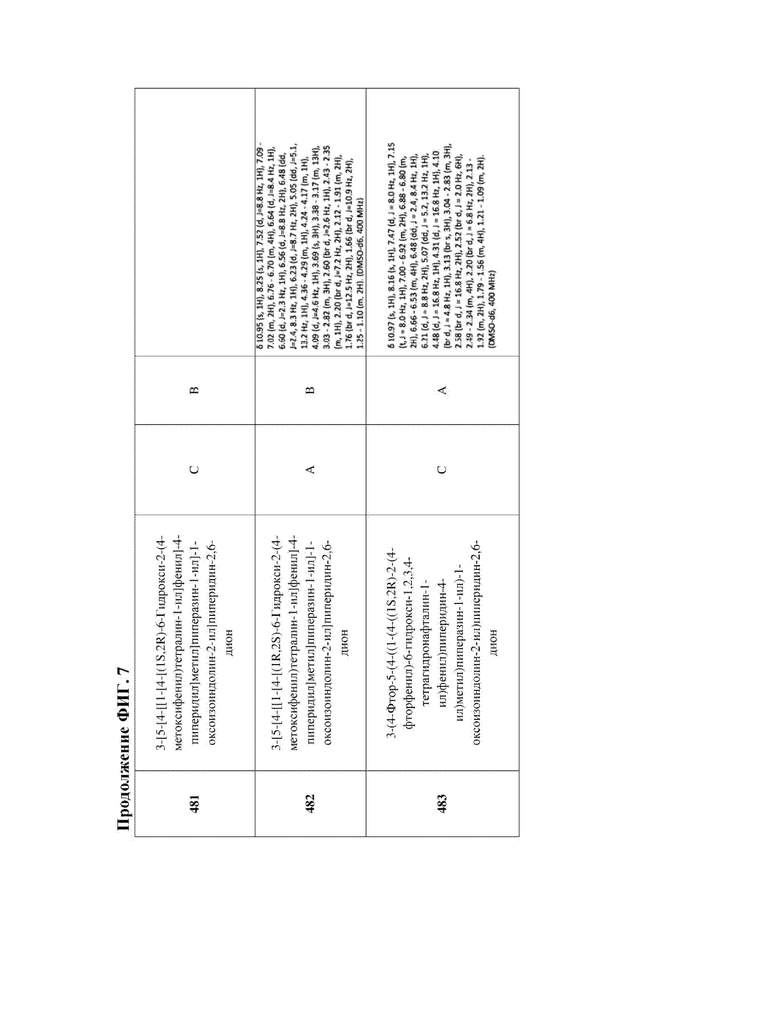










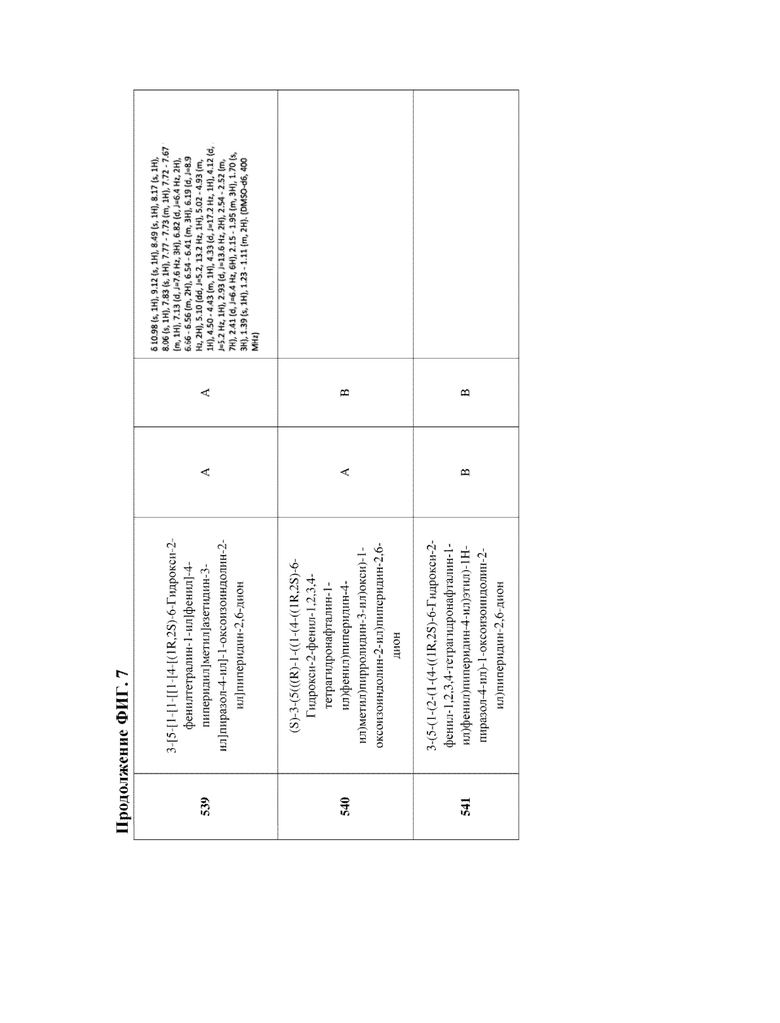

Настоящее изобретение относится к бифункциональным соединениям, которые находят применение в качестве модуляторов эстрогенового рецептора (целевой белок). В частности, настоящее изобретение относится к бифункциональным соединениям, имеющим химическую структуру ULM-L-PTM, которые содержат на одном конце лиганд, который связывается с Е3-убиквитинлигазой, и на другом конце фрагмент, который связывается с целевым белком так, что целевой белок размещен в непосредственной близости от убиквитинлигазы, с осуществлением разрушения и ингибирования целевого белка. В общей формуле ULM-L-PTM : ULM представляет собой химическую структуру (а), W выбран из группы, состоящей из CH2, CHR и C=O; каждый X представляет собой O; Z представляет собой O; G представляет собой H; Q1, Q2, Q3 и Q4 независимо представляют собой N или C, независимо замещенные R или H; A представляет собой H или линейный или разветвленный C1-6 алкил; n представляет собой 1, 2 или 3; каждый R независимо выбран из -OR’, -NR’R”, -CR’R”-, 6-членного арила, 5- или 6-членного гетероарила с одним или двумя гетероатомами, линейного или разветвленного C1-6 алкила, C3-7 циклоалкила, C3-7 гетероциклила с одним, двумя или тремя гетероатомами, где один R ковалентно связан с L; R' и R'' независимо представляют собой связь или H; и  представляет собой связь, которая может обеспечивать стереоспецифическую конфигурацию или не обеспечивать стереоспецифическую конфигурацию; и где каждый гетероатом ULM представляет собой азот; L представляет собой химическую линкерную группу, представленную формулой -(AL)q-, причем (AL)q соединена с ULM и PTM; q представляет собой 1, 2, 3 4, 5, 6, 7, 8, 9, 10, 11, 12 или 13; каждый AL независимо выбран из связи, CRL1RL2, O, S, SO, SO2, NRL3, CO, C≡C, C3-11циклоалкила, C3-11гетероциклила, имеющего 1 или 2 атома N или O и необязательно замещенного 1 группой RL1, и 5- или 6-членного гетероарила, имеющего 1, 2 или 4 атома N; и каждая из RL1, RL2, RL3, RL4 и RL5 независимо представляет собой H, галоген или C1-8алкил; PTM представляет собой структуру формулу (IРТМ), каждый XPTM независимо представляет собой CH или N;
представляет собой связь, которая может обеспечивать стереоспецифическую конфигурацию или не обеспечивать стереоспецифическую конфигурацию; и где каждый гетероатом ULM представляет собой азот; L представляет собой химическую линкерную группу, представленную формулой -(AL)q-, причем (AL)q соединена с ULM и PTM; q представляет собой 1, 2, 3 4, 5, 6, 7, 8, 9, 10, 11, 12 или 13; каждый AL независимо выбран из связи, CRL1RL2, O, S, SO, SO2, NRL3, CO, C≡C, C3-11циклоалкила, C3-11гетероциклила, имеющего 1 или 2 атома N или O и необязательно замещенного 1 группой RL1, и 5- или 6-членного гетероарила, имеющего 1, 2 или 4 атома N; и каждая из RL1, RL2, RL3, RL4 и RL5 независимо представляет собой H, галоген или C1-8алкил; PTM представляет собой структуру формулу (IРТМ), каждый XPTM независимо представляет собой CH или N;  указывает на место присоединения L; RPTM1 представляет собой 1, 2 или 3 замещения, каждое замещение независимо выбрано из OH, галогена и C1-6алкокси; RPTM2 представляет собой 1 или 2 замещения, каждое замещение независимо выбрано из H, галогена, CF3, линейного или разветвленного C1-6алкила, метокси; RPTM3 представляет собой 1 или 2 замещения, каждое замещение независимо представляет собой H или галоген; и RPTM4 представляет собой H или метил. 13 з.п. ф-лы, 7 ил., 544 пр.
указывает на место присоединения L; RPTM1 представляет собой 1, 2 или 3 замещения, каждое замещение независимо выбрано из OH, галогена и C1-6алкокси; RPTM2 представляет собой 1 или 2 замещения, каждое замещение независимо выбрано из H, галогена, CF3, линейного или разветвленного C1-6алкила, метокси; RPTM3 представляет собой 1 или 2 замещения, каждое замещение независимо представляет собой H или галоген; и RPTM4 представляет собой H или метил. 13 з.п. ф-лы, 7 ил., 544 пр.
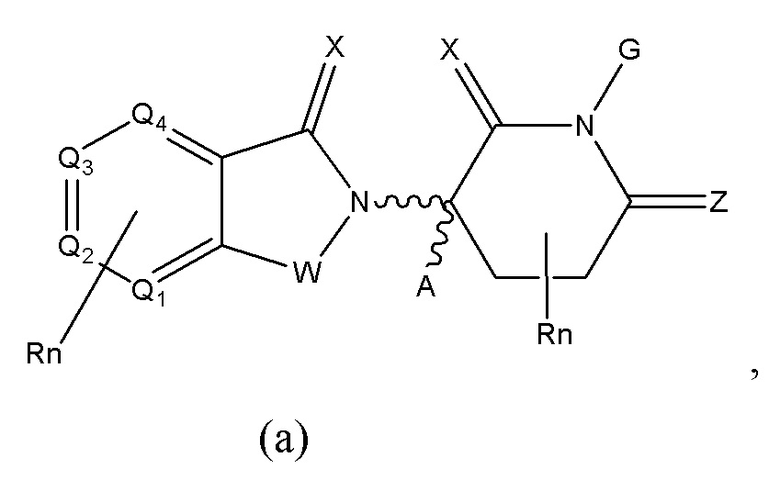
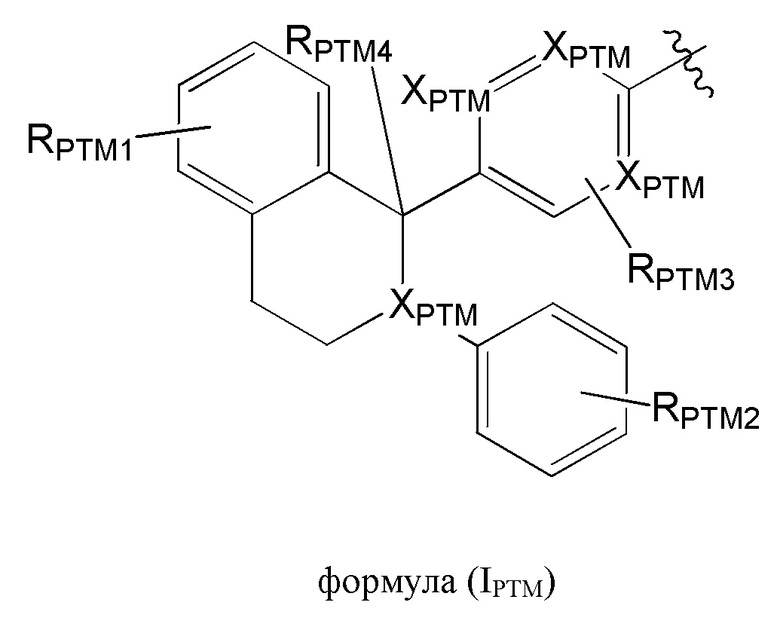
1. Бифункциональное соединение, имеющее химическую структуру:
ULM-L-PTM,
где
(a) ULM представляет собой химическую структуру, представленную:
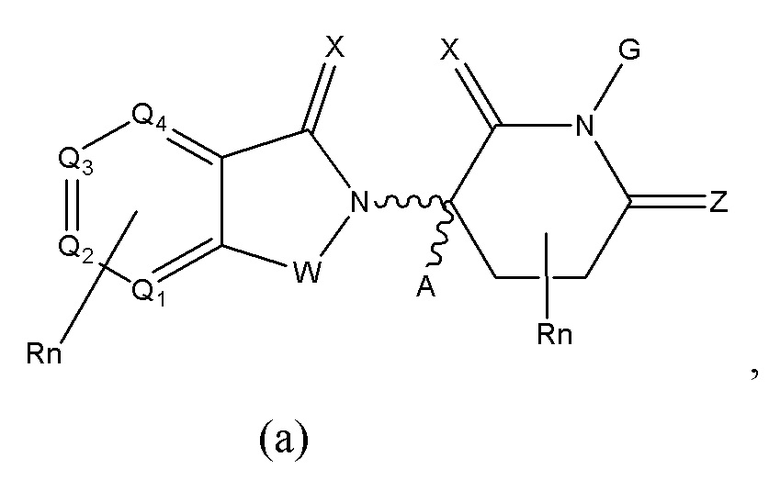
где:
W выбран из группы, состоящей из CH2, CHR и C=O;
каждый X представлят собой O;
Z представлят собой O;
G представлят собой H;
Q1, Q2, Q3 и Q4 независимо представляют собой N или C, независимо замещенные R или H;
A представляет собой H или линейный или разветвленный C1-6 алкил;
n представлят собой 1, 2 или 3;
каждый R независимо выбран из -OR', -NR’R'', -CR'R'-, 6-членного арила, 5- или 6-членного гетероарила с одним или двумя гетероатомами, линейного или разветвленного C1-6 алкила, C3-7 циклоалкила, C3-7 гетероциклила с одним, двумя или тремя гетероатомами, где один R ковалентно связан с L;
R' и R'' независимо представляют собой связь или H; и
 представляет собой связь, которая может обеспечивать стереоспецифическую конфигурацию или не обеспечивать стереоспецифическую конфигурацию; и
представляет собой связь, которая может обеспечивать стереоспецифическую конфигурацию или не обеспечивать стереоспецифическую конфигурацию; и
где каждый гетероатом ULM представляет собой азот;
(b) L представляет собой химическую линкерную группу, представленную формулой -(AL)q-, причем
(AL)q соединена с ULM и PTM;
q представляет собой 1, 2, 3 4, 5, 6, 7, 8, 9, 10, 11, 12 или 13;
каждый AL независимо выбран из связи, CRL1RL2, O, S, SO, SO2, NRL3, CO, C≡C, C3-11циклоалкила, C3-11гетероциклила, имеющего 1 или 2 атома N или O и необязательно замещенного 1 группой RL1, и 5- или 6-членного гетероарила, имеющего 1, 2 или 4 атома N; и
каждая из RL1, RL2, RL3, RL4 и RL5 независимо представляет собой H, галоген или C1-8алкил; и
(с) PTM представлен с помощью химической структуры:

где
каждый XPTM независимо представляет собой CH или N;
 указывает на место присоединения L;
указывает на место присоединения L;
RPTM1 представляет собой 1, 2 или 3 замещения, каждое замещение независимо выбрано из OH, галогена и C1-6алкокси;
RPTM2 представляет собой 1 или 2 замещения, каждое замещение независимо выбрано из H, галогена, CF3, линейного или разветвленного C1-6алкила, метокси;
RPTM3 представляет собой 1 или 2 замещения, каждое замещение независимо представляет собой H или галоген; и
RPTM4 представляет собой H или метил.
2. Бифункциональное соединение по п. 1, где PTM представлен с помощью химической структуры

3. Бифункциональное соединение по любому из пп. 1 или 2, где каждый AL независимо выбран из группы, состоящей из CRL1RL2, O, NRL3, CO, C≡C, C3-11циклоалкила, C3-11гетероциклила, необязательно замещенного 1 группой RL1 и 5- или 6-членного гетероарила, имеющего 1, 2 или 4 атома N; и
каждая из RL1, RL2, RL3, RL4 и RL5 независимо представляет собой H, галоген или C1-8алкил.
4. Бифункциональное соединение по одному любому из пп. 1-3, где L представлен структурой, выбранной из:

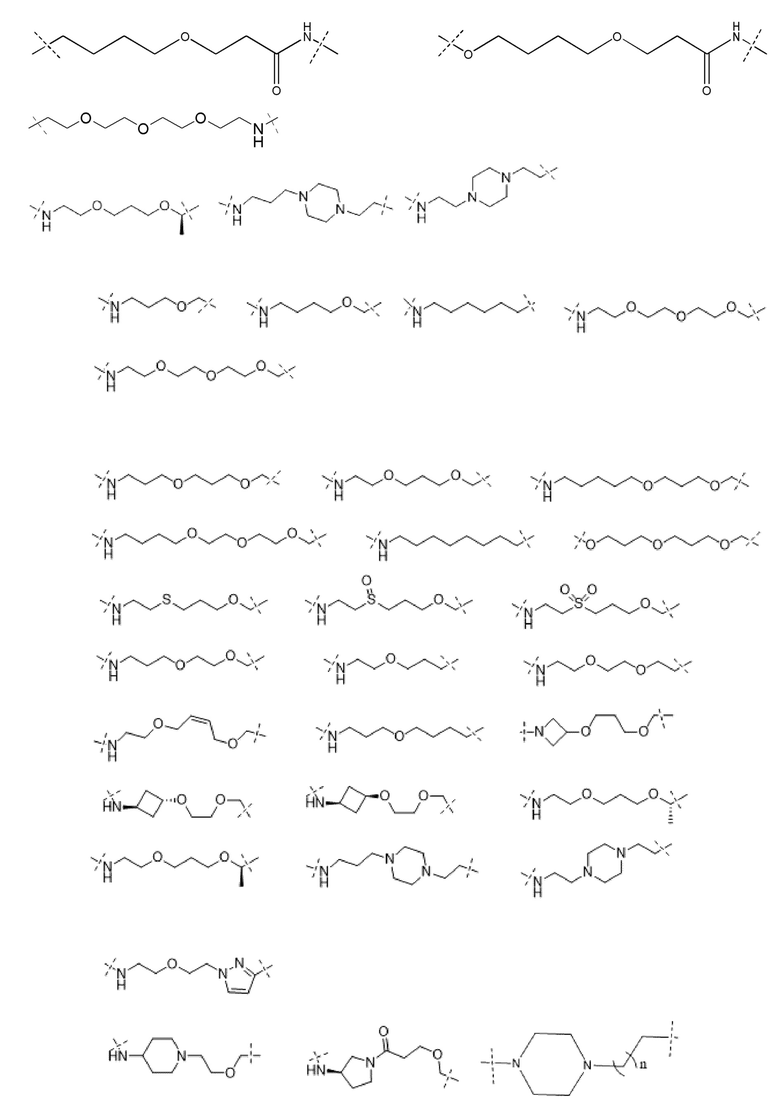






где:
каждый из m, n, o и r из L независимо равняется 0, 1, 2, или 3, при условии, что если число равняется нулю, то связь N-O или O-O отсутствует.
5. Бифункциональное соединение по одному любому из пп. 1-3, где L выбрана из:



6. Бифункциональное соединение по одному любому из пп. 1-3, где L выбрана из:
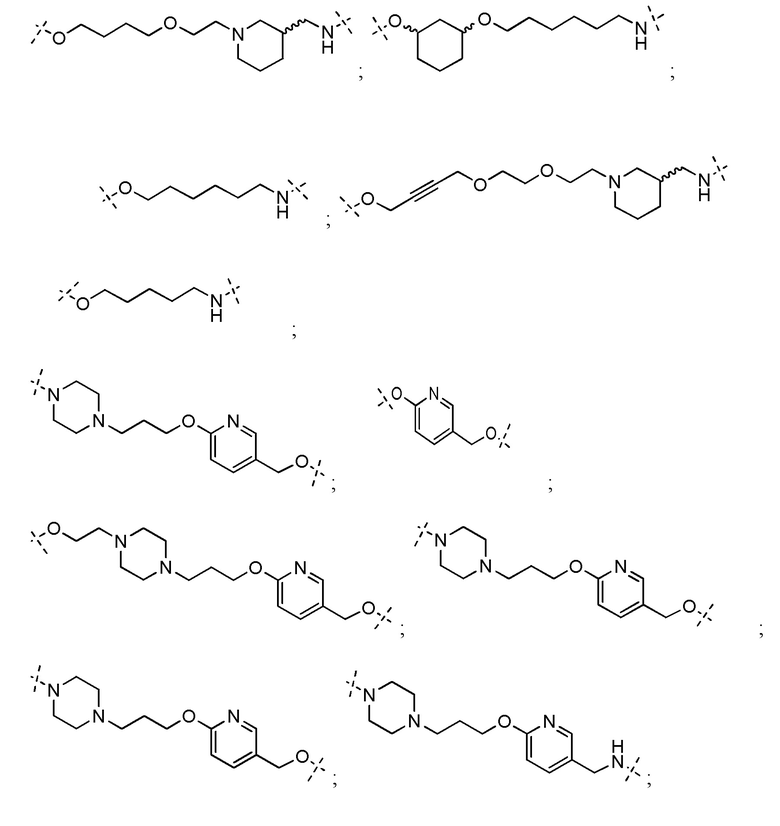

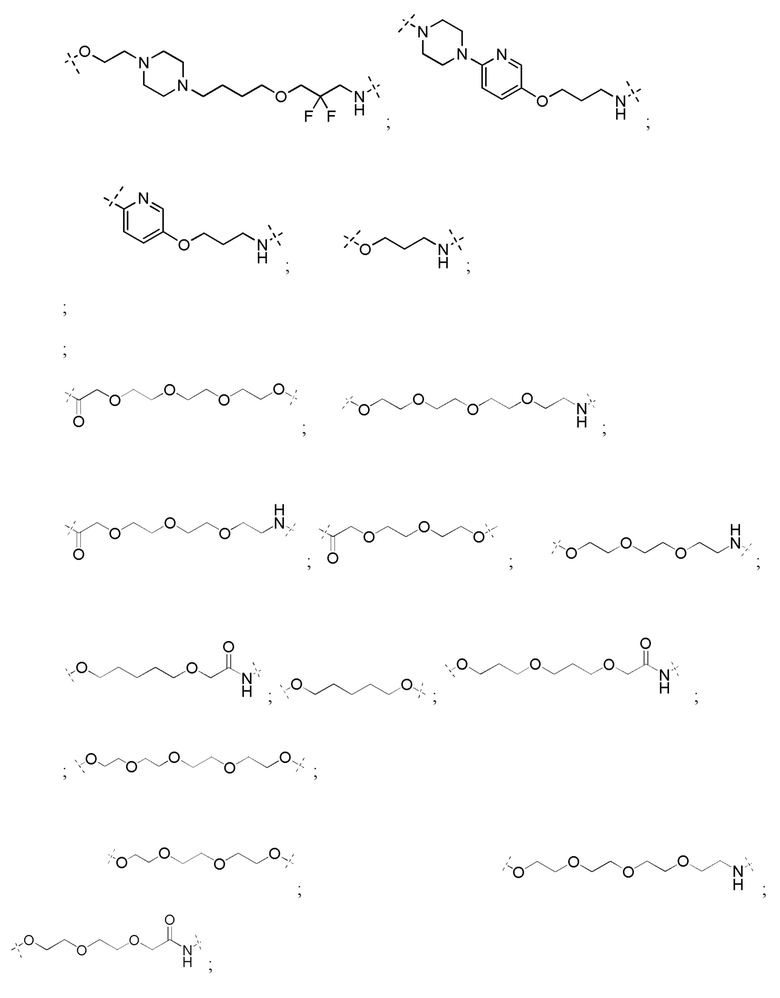
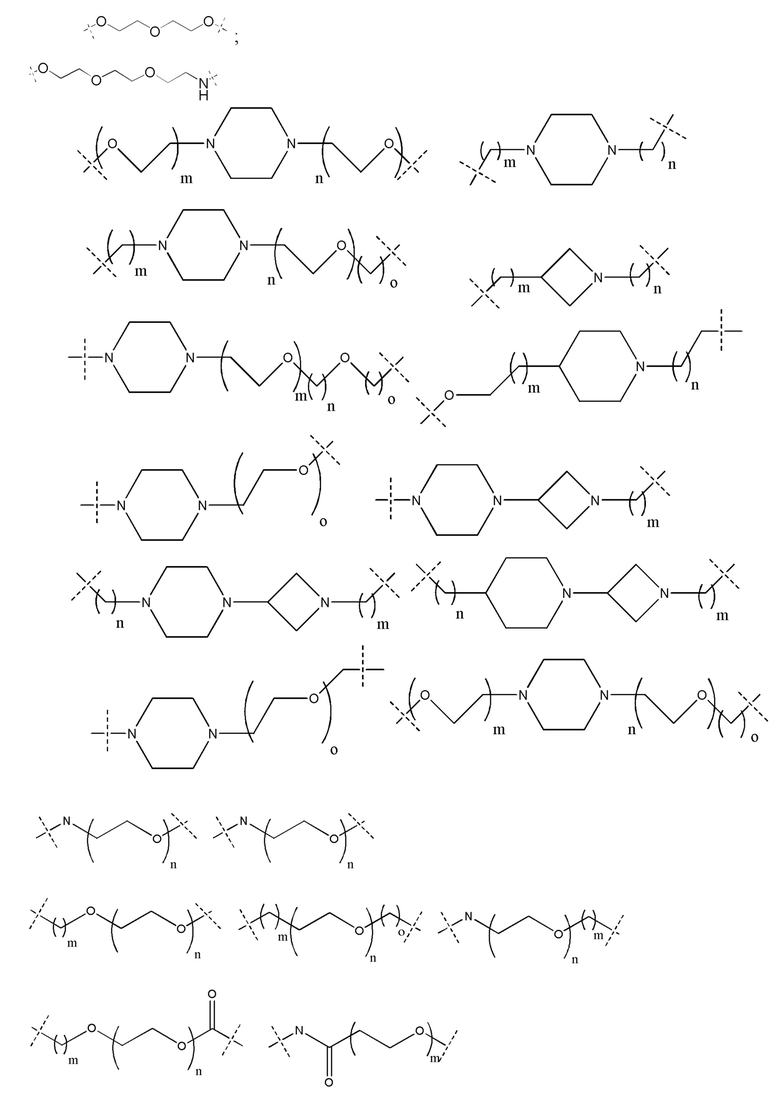





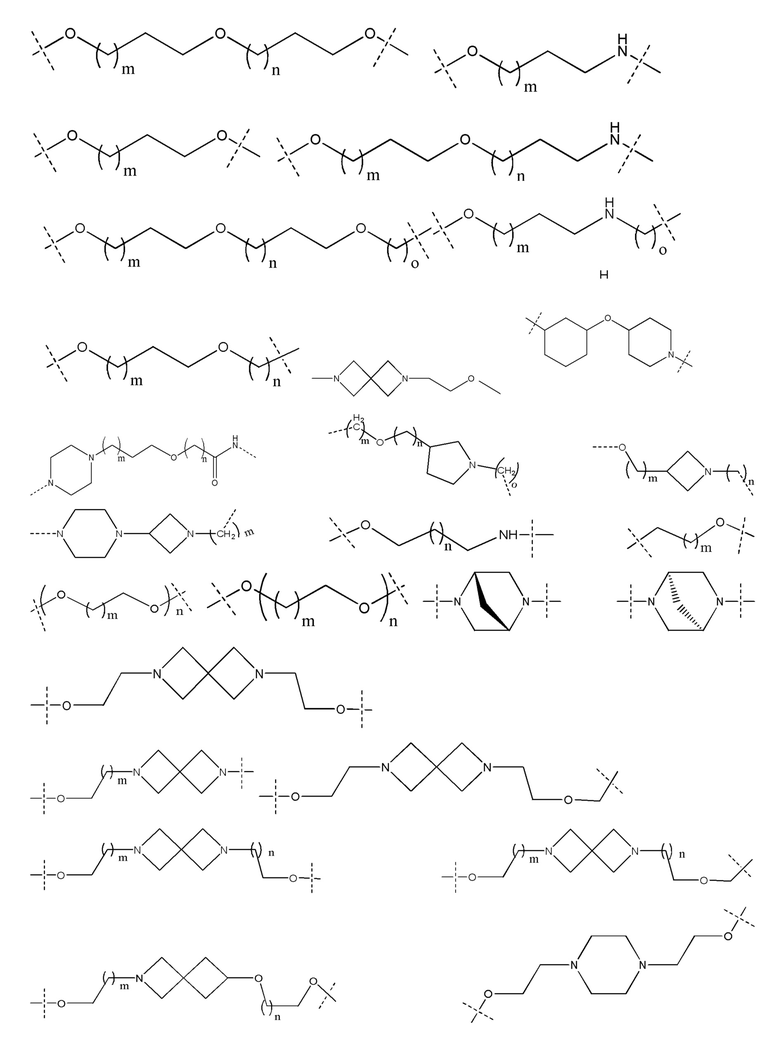






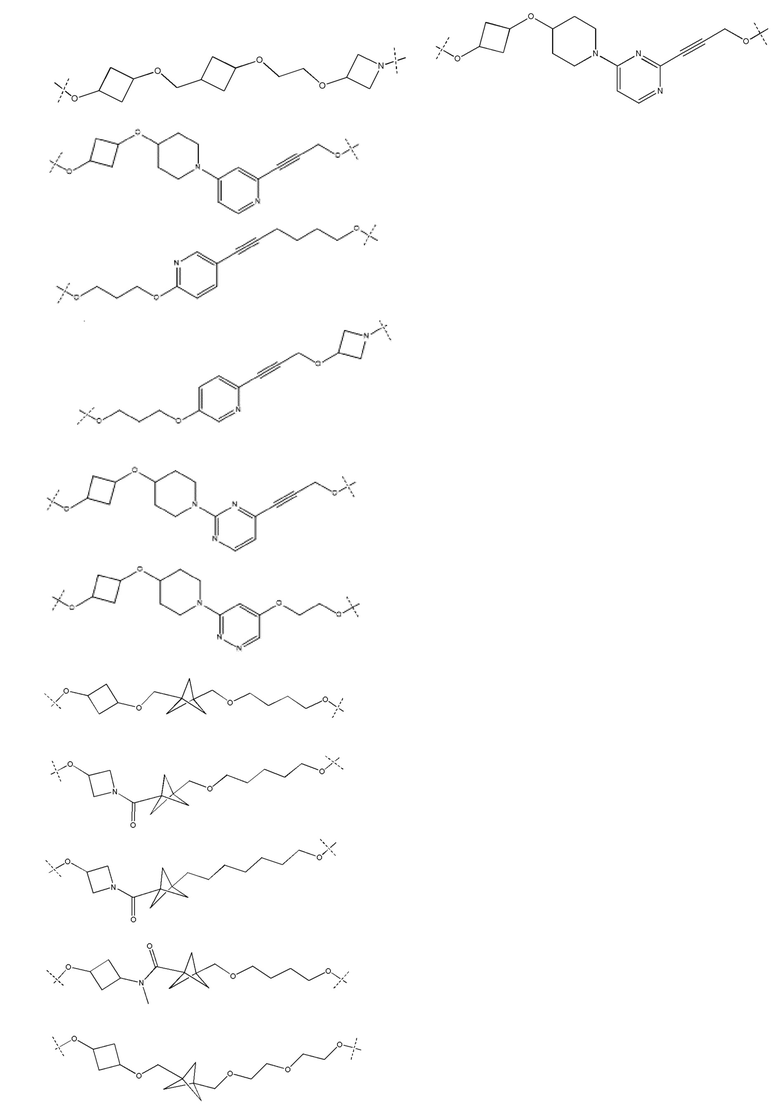



где каждый m или n независимо равняется 0, 1 или 2, и каждый o или p независимо равняется 0, 1, 2 или 3,
причем общее количество звеньев (AL) не превышает 13.
7. Бифункциональное соединение по одному любому из пп. 1-3, где химическая линкерная группа (L) выбрана из:




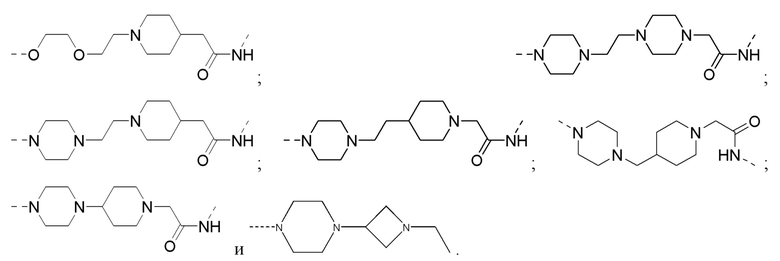
8. Бифункциональное соединение по одному любому из пп. 1-3, где L представляет собой полиэтиленоксигруппу, содержащую 1, 2, 3 или 4 этиленгликолевых звеньев.
9. Бифункциональное соединение по одному любому из пп. 1-3, где L имеет химическую структуру:
 или
или 
где
каждый из WL1 и WL2 независимо представляет собой 4-8-членный циклоалкил, 4-8-членный гетероциклил с 1-2 гетероатомами, выбранными из N и O, и необязательно замещенный 1 RQ, или 5-6-членный гетероарил, содержащий 1, 2 или 4 атома N, причем RQ выбран из H, галоген, или C1-С6алкила;
каждый YL1 независимо представляет собой связь или O;
n представляет собой 1, 2, 3, 4, 5, 6, 7 или 8; и
 указывает на точку присоединения к PTM или ULM.
указывает на точку присоединения к PTM или ULM.
10. Бифункциональное соединение по одному любому из пп. 1-3, где L имеет химическую структуру:
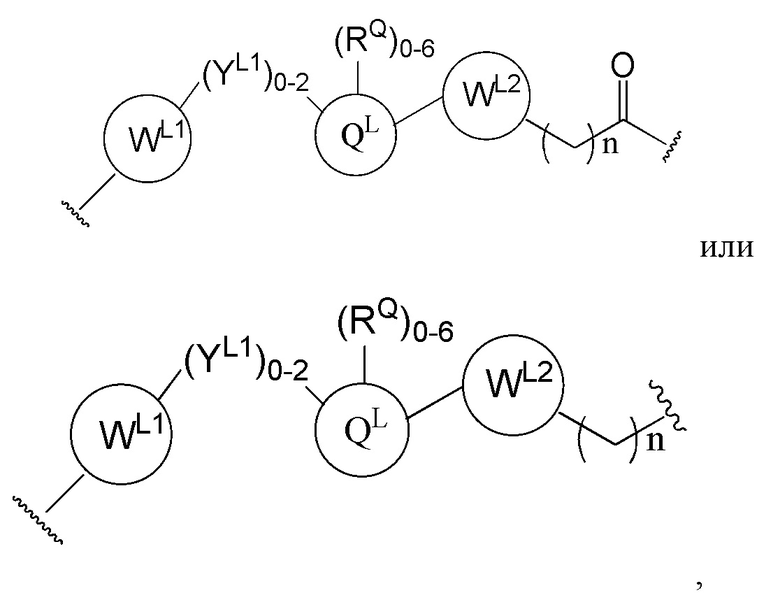
где
каждый из WL1 и WL2 независимо представляет 5- или 6-членный гетероарил, содержащий 1, 2 или 4 атома N, C3-7 циклическую группу, C3-7 гетероциклическую группу, содержащую 1 или 2 гетероатома, выбранных из N или O и необязательно монозамещенную галогеном или C1-8алкилом, C1-С6алкил, необязательно замещенный 1 или 2 галогенами или C1-8алкилом;
каждый YL1 независимо представляет собой связь, NRYL1, O, S, NRYL2, CRYL1RYL2, C=O, SO2, необязательно замещенный линейный или разветвленный C1-6алкокси, или необязательно замещенный линейный или разветвленный C1-С6алкил, и необязательно один или более атомов C заменены O;
QL представляет собой 3-6-членное алициклическое или 5-6-членное гетероароматическое кольцо с 1, 2 или 4 атома азота и каждая RQ представляет собой H;
каждый из RYL1, RYL2 независимо представляет собой H, галоген или C1-6алкил, необязательно замещенный 1 или 2атомами галогена, или C1-8алкилом;
n представляет собой целое число от 0, 1, 2, 3, 4, 5, 6 или 7; и
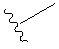 указывает на точку присоединения к фрагментам PTM или ULM.
указывает на точку присоединения к фрагментам PTM или ULM.
11. Бифункциональные соединения по п. 9 или 10, где L выбрана из:

12. Бифункциональное соединение по п. 1, где соединение выбрано из:




13. Бифункциональное соединение по п. 1, где соединение выбрано из группы, состоящей из:
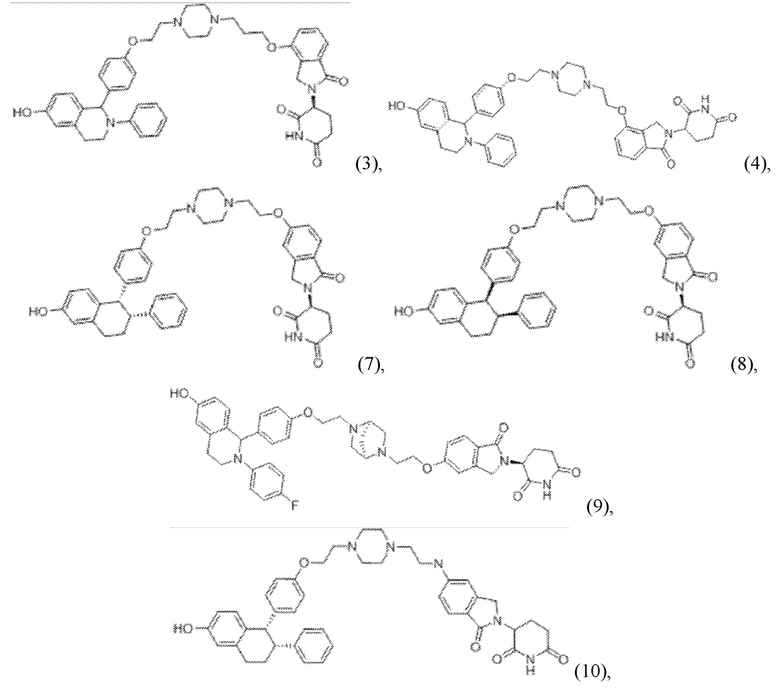



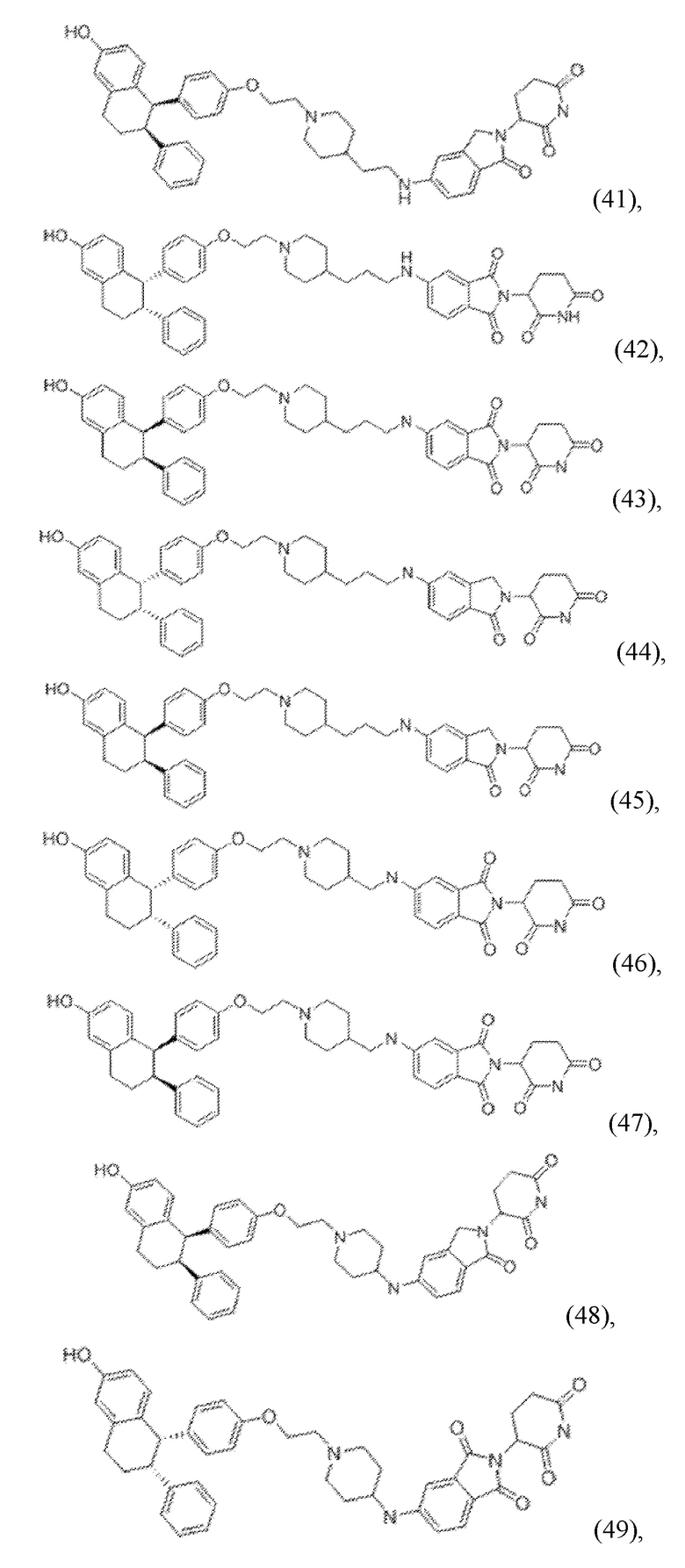

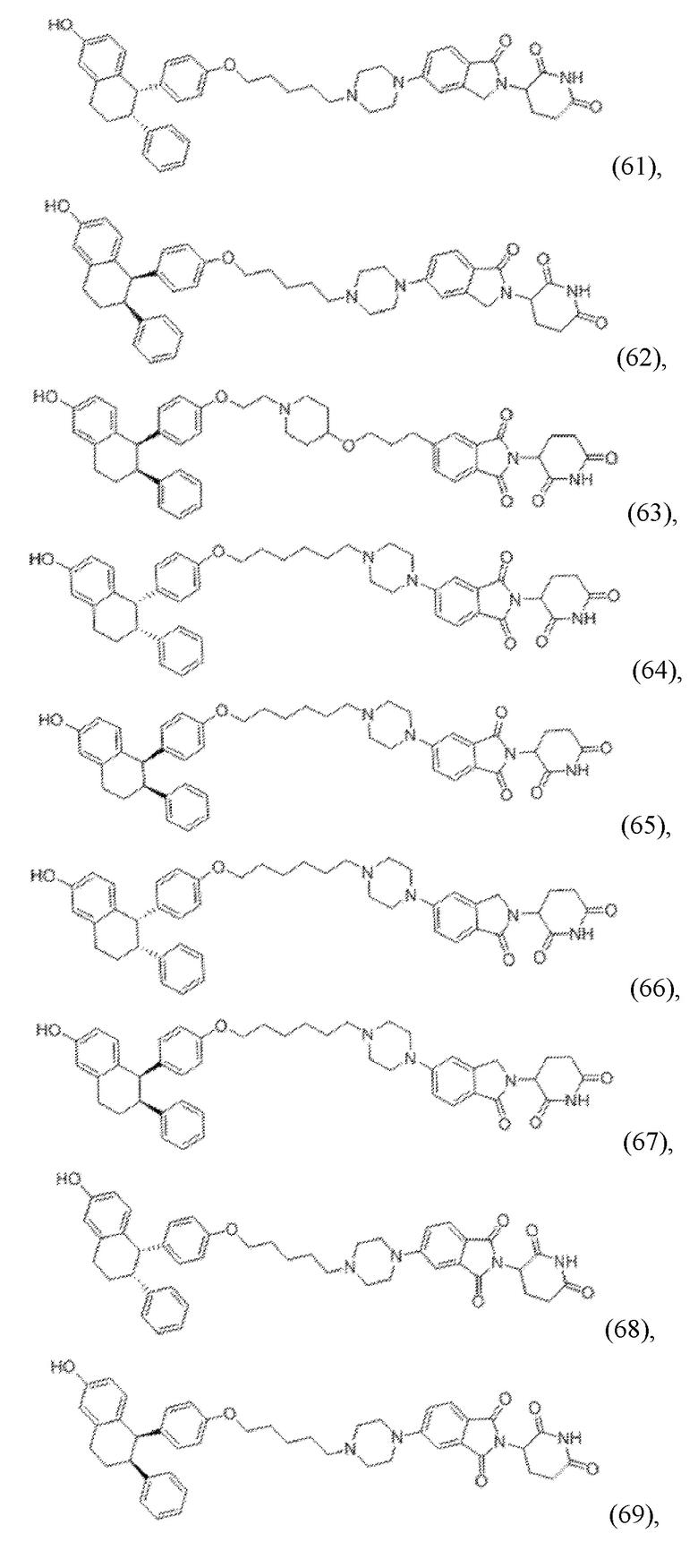


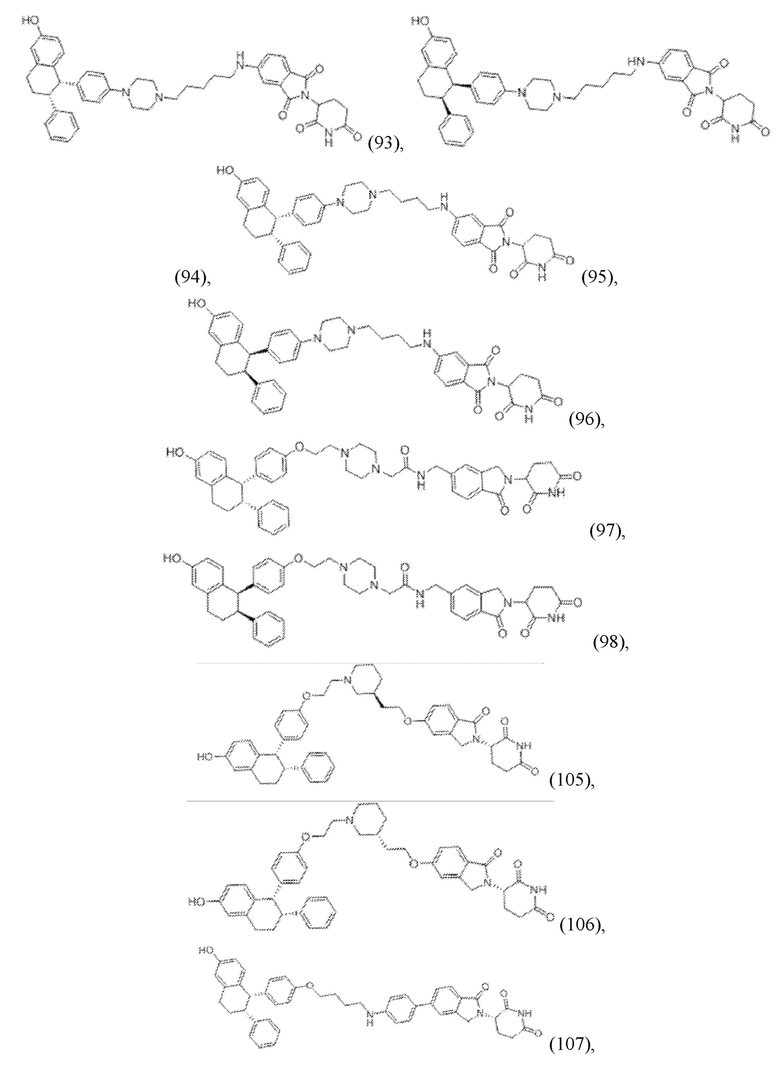

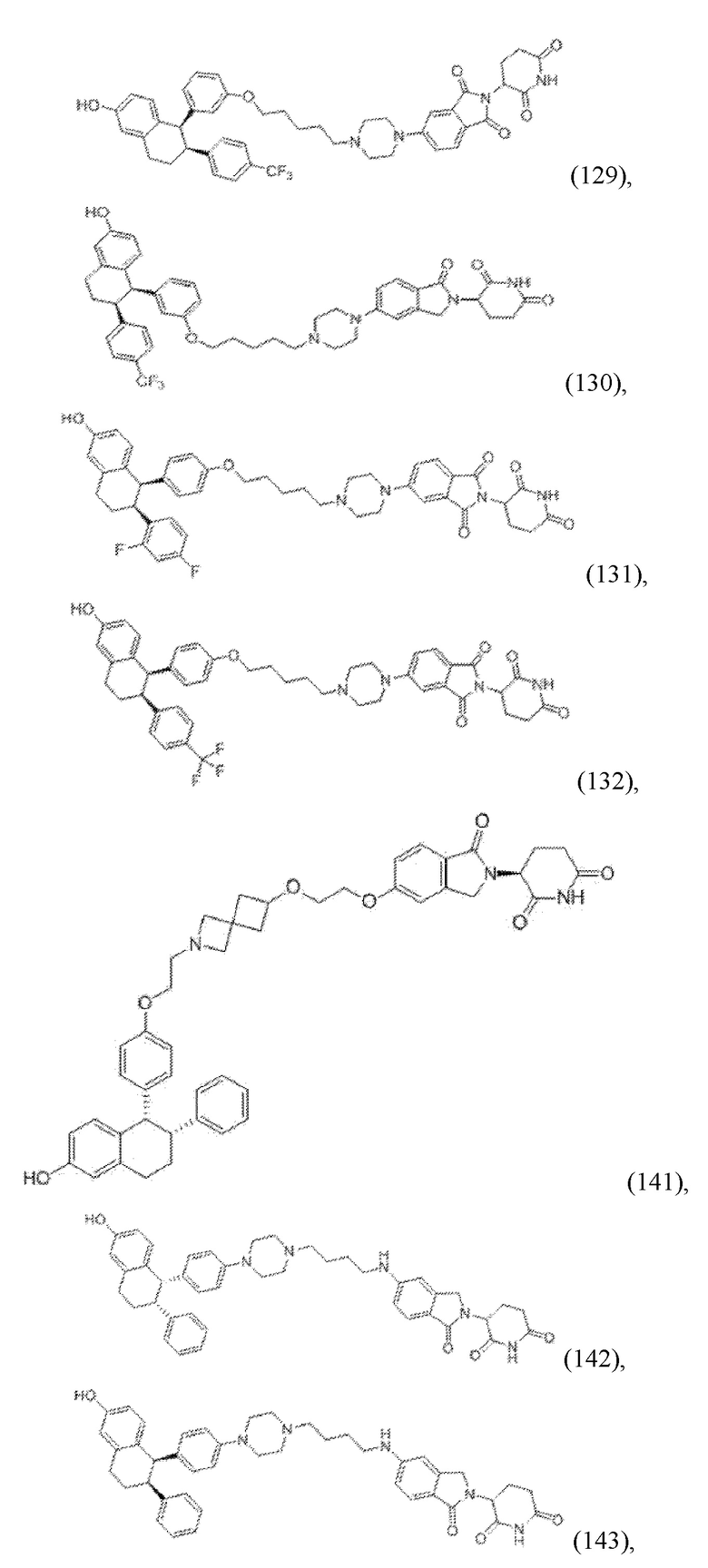












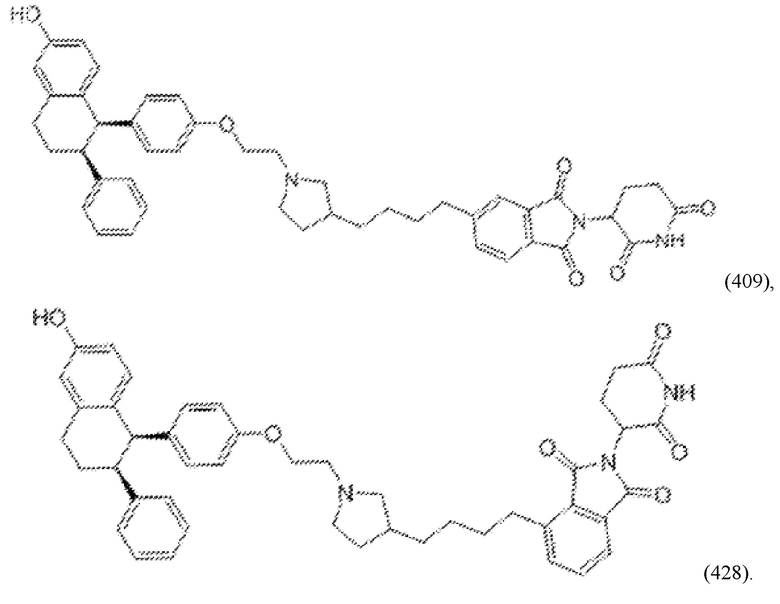
14. Бифункциональное соединение по п. 1, где соединение выбрано из группы, состоящей из:



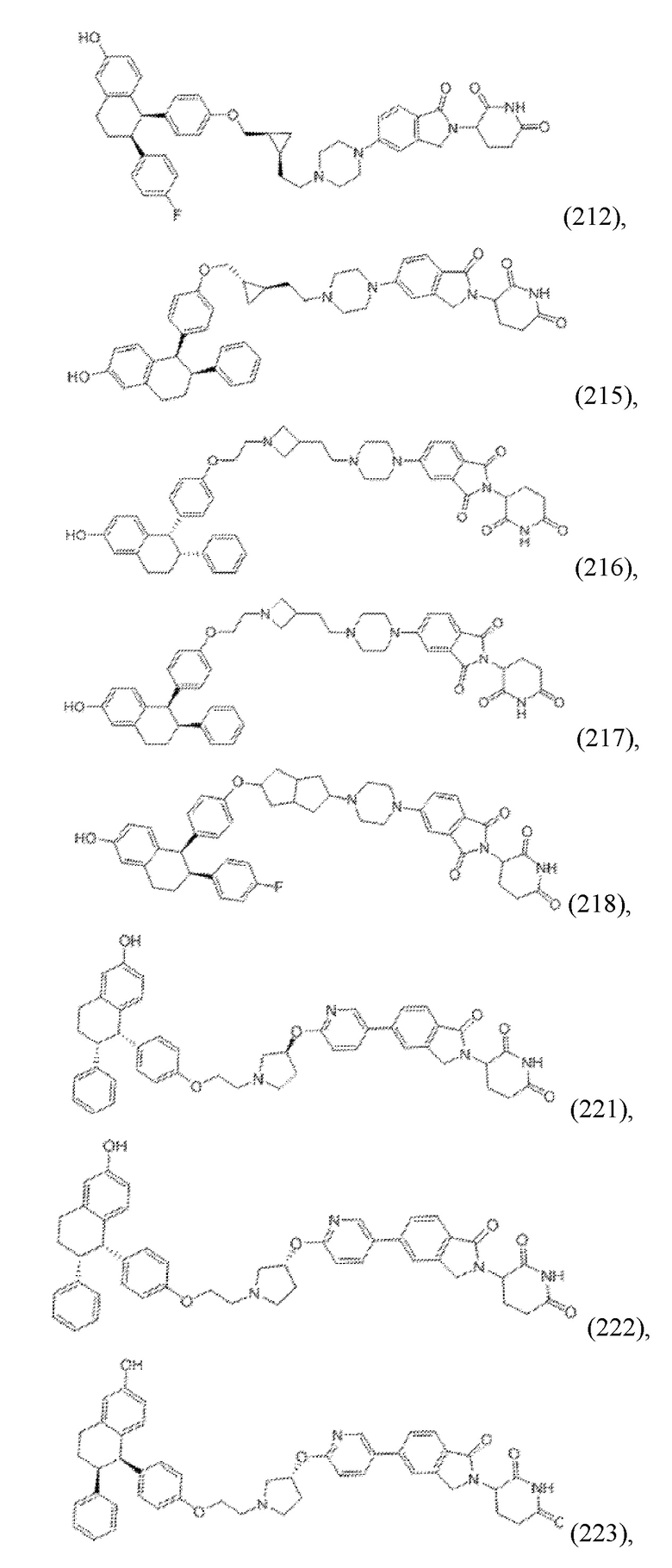






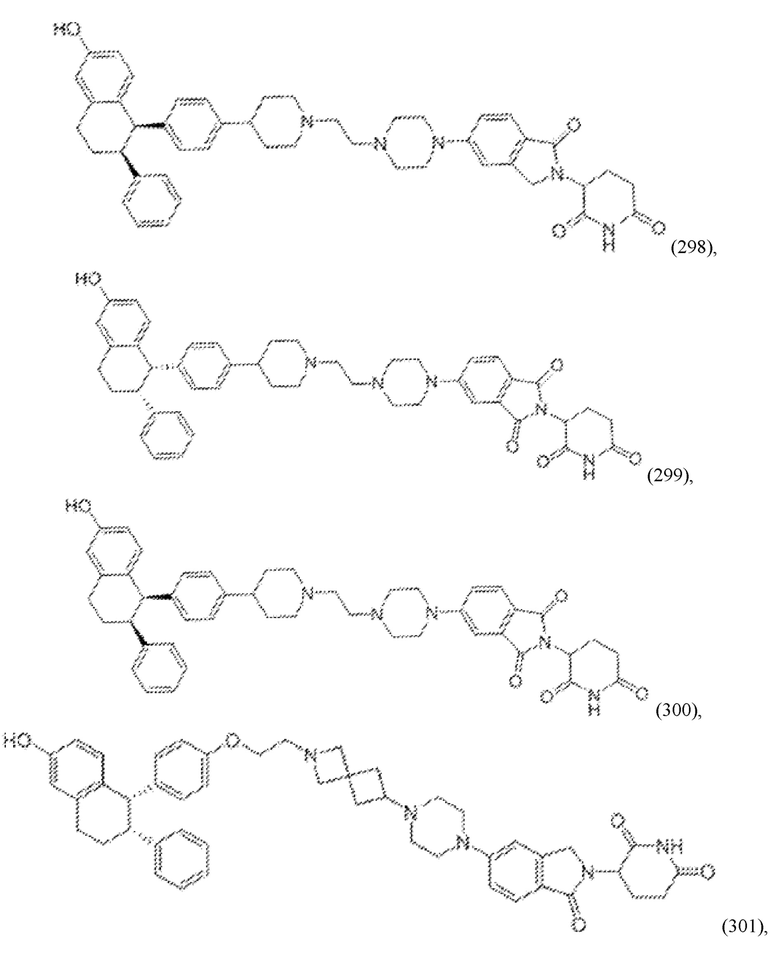
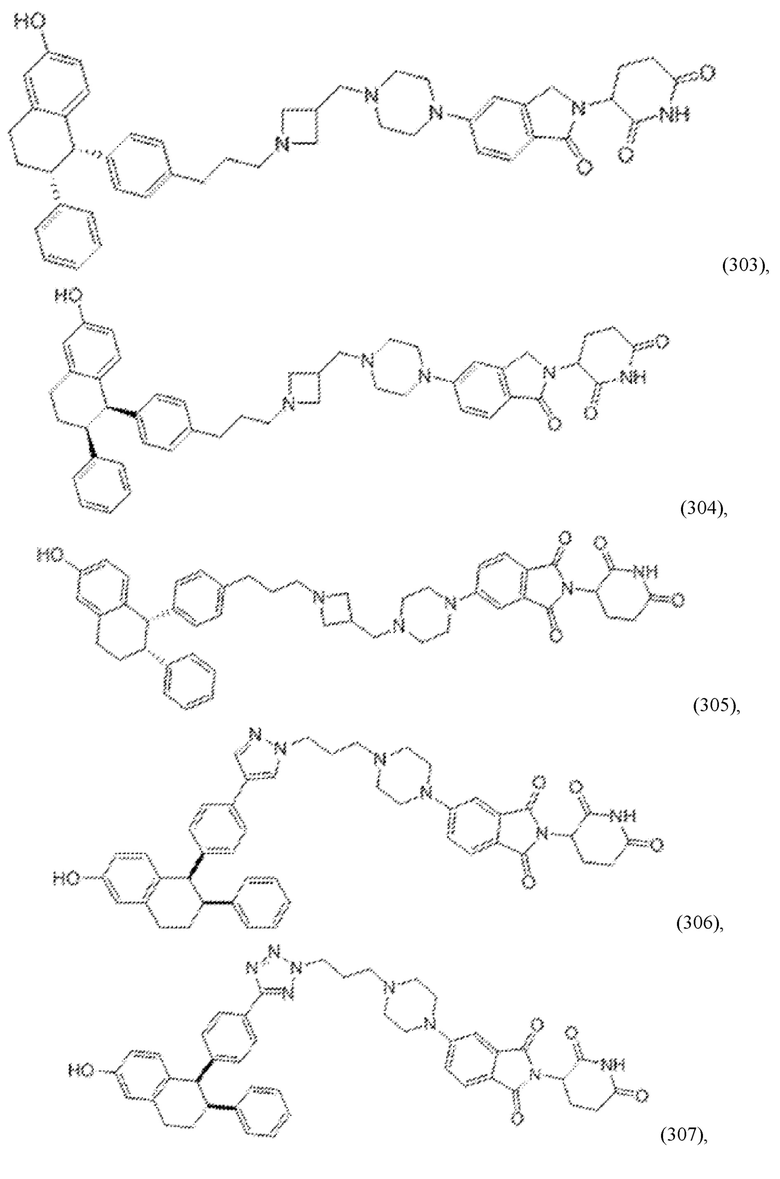

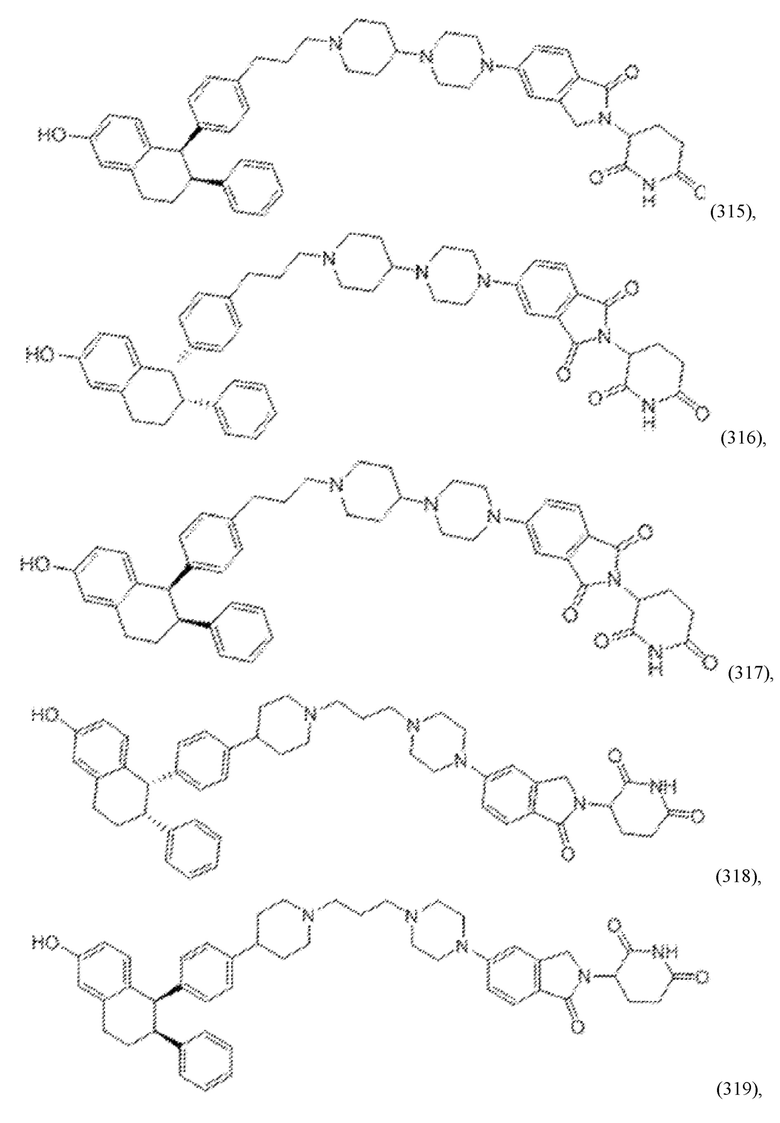


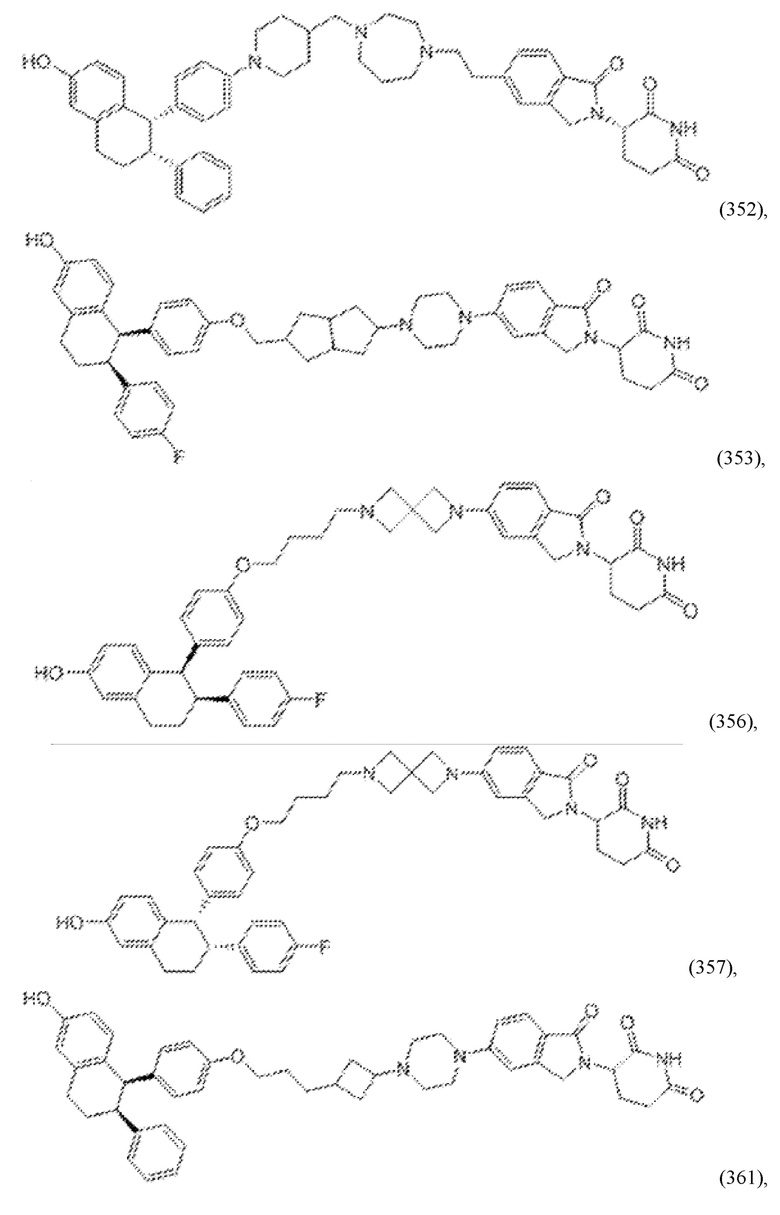






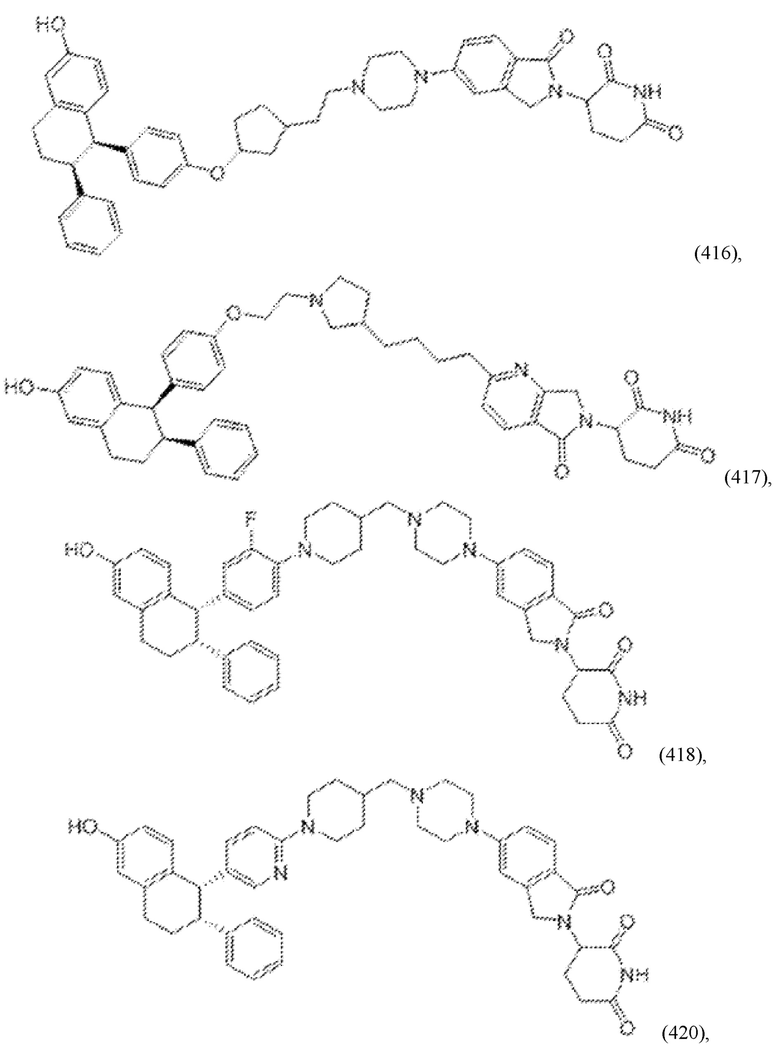
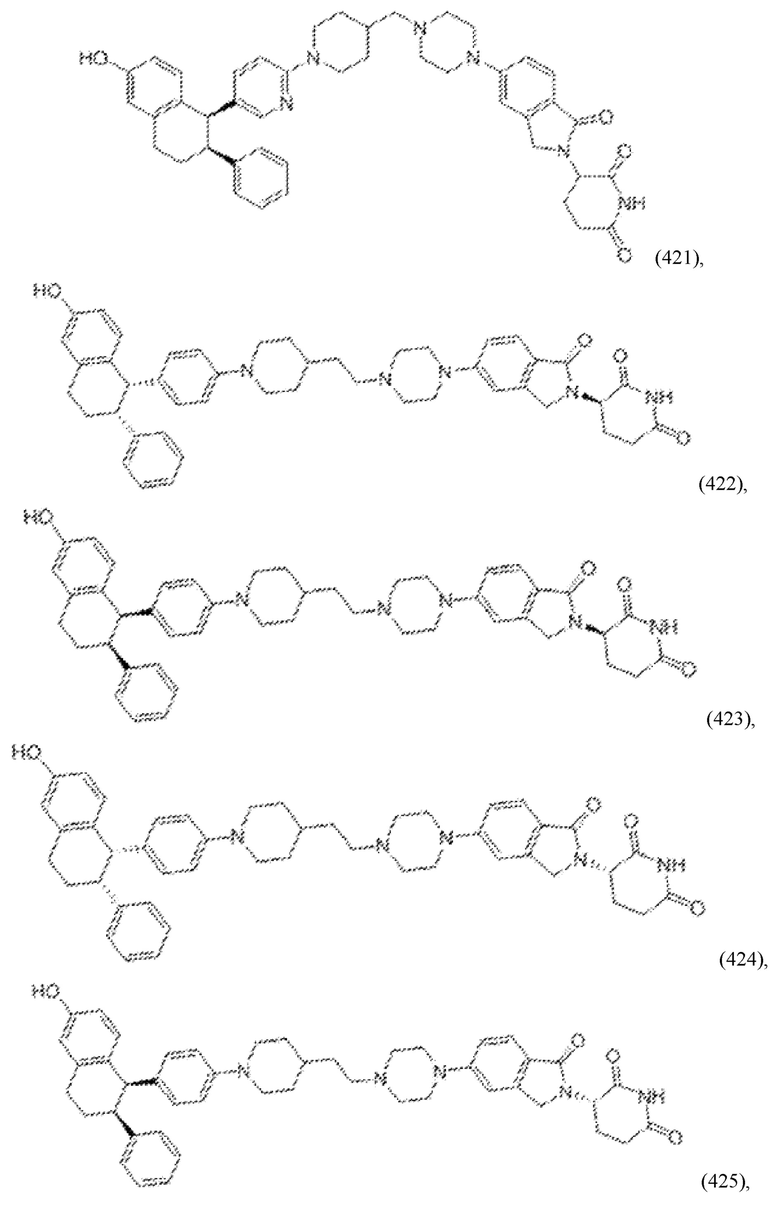



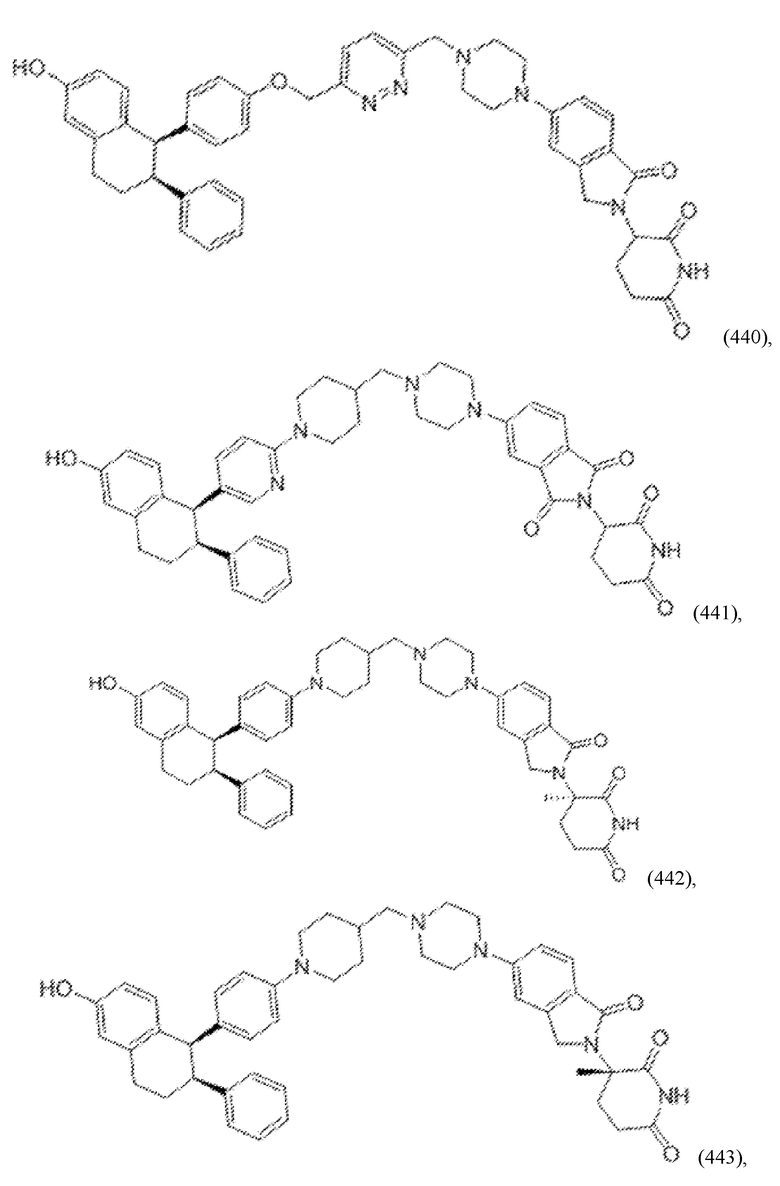









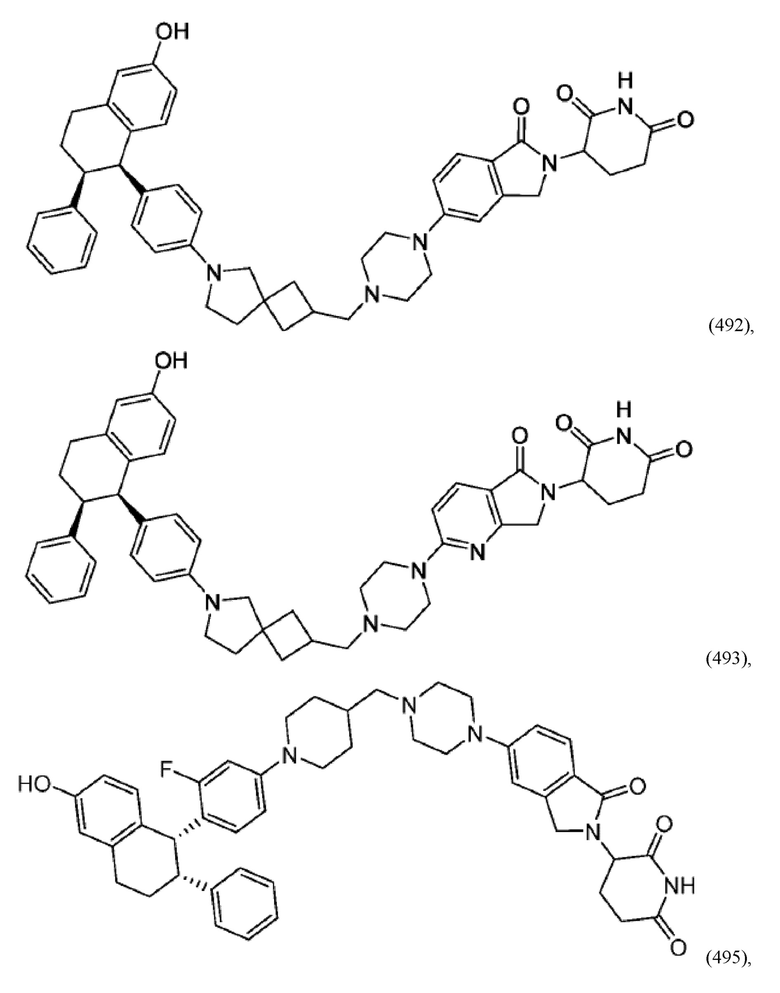





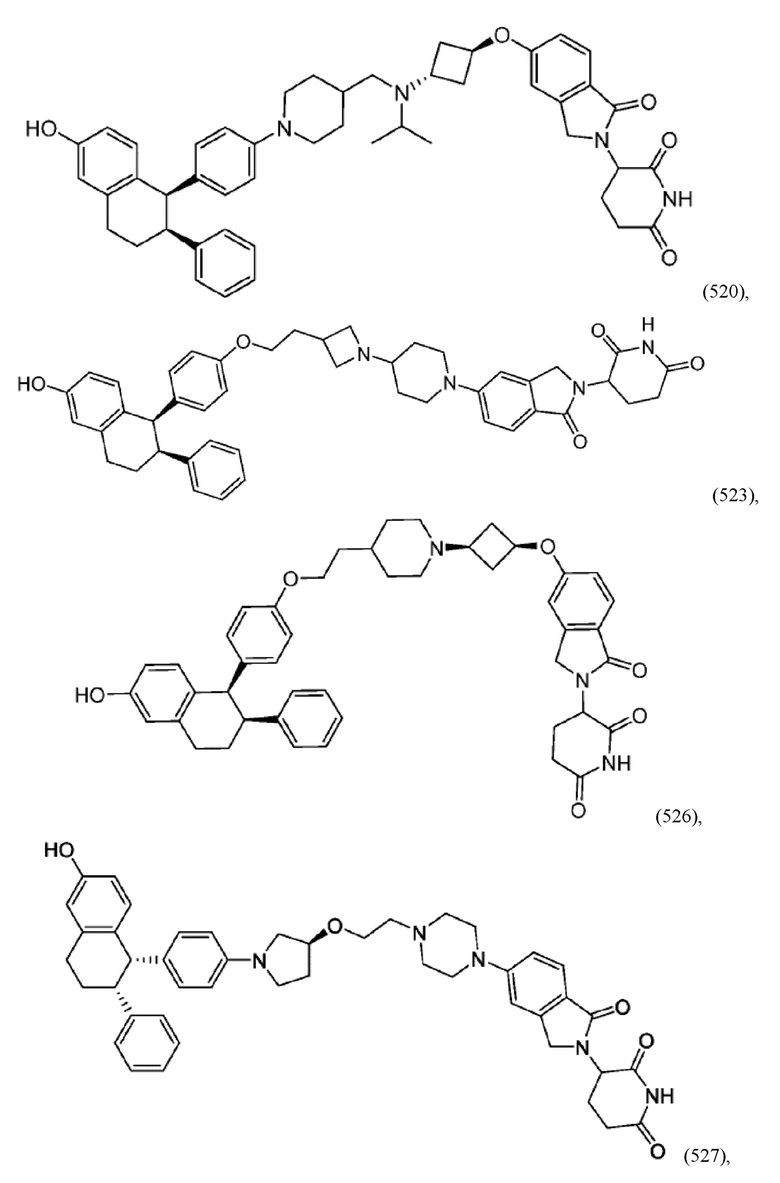

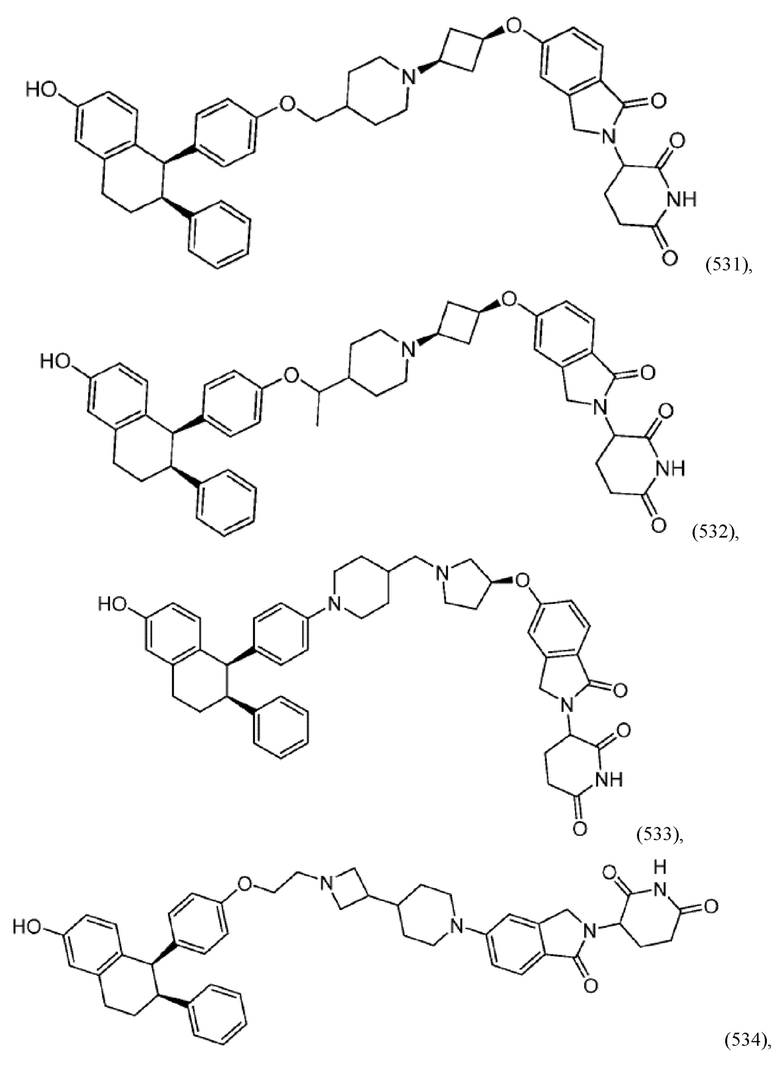




| US 20160045607 A1, 18.02.2016 | |||
| WO 2016097071 A1, 23.06.2016 | |||
| US 20160058872 A1, 03.03.2016 | |||
| Ashini L | |||
| Wijayaratne, Donald P | |||
| McDonnell "The Human Estrogen Receptor- Is a Ubiquitinated Protein WhoseStability Is Affected Differentially by Agonists, Antagonists, andSelective Estrogen Receptor Modulators", THE JOURNAL OF BIOLOGICAL CHEMISTRY, Vol |
Авторы
Даты
2023-06-01—Публикация
2017-12-01—Подача