ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
По настоящей заявке испрашивается приоритет по временной патентной заявке США № 62/785647, поданной 27 декабря 2018 года, включенной в настоящее описание в качестве ссылки в полном объеме.
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
Настоящая заявка содержит список последовательностей, поданный в электронном виде в формате ASCII и, таким образом, включенный в нее в качестве ссылки в полном объеме. Указанная копия ASCII создана 14 февраля 2020 года, названа 4690_0016i_SL.txt и имеет размер 8518 байт.
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к некоторым фармацевтическим молекулам и композициям и их применению для лечения злокачественного новообразования и, в частности, применению молекул малой интерферирующей РНК (миРНК), ингибирующих TGF-бета 1 и Cox-2, в отдельности или в комбинации с ингибиторами иммунных контрольных точек, для лечения злокачественного новообразования.
УРОВЕНЬ ТЕХНИКИ
В недавних работах ингибиторы иммунных контрольных точек определены как важные мишени для борьбы со злокачественными новообразованиями. Рецепторы, такие как PD-1 (на поверхности T-клеток) могут взаимодействовать с лигандами (например, PD-L1) на поверхности опухолевых клеток, и связывание между этими молекулами приводит к передаче сигнала в T-клетку о том, что опухоль не должна быть разрушена. Таким образом, этот механизм передачи сигнала тщательно исследовали для изучения и идентификации способов его блокирования и, таким образом, стимуляции распознавания опухолей иммунной системой, приводящей к усилению уничтожения опухолей.
Существует множество обнаруженных контрольных точек, включая CTLA4, Lag3, Tim3, PD-1 и PD-L1. Например, показано, что антитела против PD-1 или против PD-L1 блокируют взаимодействие между рецептором PD-1 и лигандом PD-L1, и это ингибирует сигнал "не ешь меня" от опухолевой клетки к T-клетке, что в ином случае предотвращает действие T-клетки по выполнению своего нормального ответа на опухоли и другие чужеродные клетки посредством высвобождения ферментов, уничтожающих клетки.
С началом использования этих антител (пембролизумаб, Keytruda и т.д.) в клинических условиях обнаружили, что лечение пациентов этими средствами может способствовать очень сильному иммунному ответу у приблизительно 30% пациентов, что приводило к долговременному излечению этих пациентов. Однако, неясно, почему этот ответ наблюдали только у 30% пациентов, подвергаемых лечению, и, таким образом, исследования фокусировали на других путях и механизмах передачи сигнала, которые могут играть роль в ингибировании иммунной реакции и способности T-клеток уничтожать опухолевые клетки.
РНК-интерференция (РНКи) является последовательность-специфическим процессом деградации РНК, обеспечивающим относительно простой и прямой путь нокдауна или сайленсинга, теоретически, любого гена, содержащего гомологичную последовательность. При природной РНКи двухцепочечная РНК (дцРНК) расщепляется белком РНКазой III/хеликазой, Dicer, на молекулы малой интерферирующей РНК (миРНК), дцРНК по 19-27 нуклеотидов (н.) с 2-нуклеотидными липкими 3'-концами. Затем миРНК встраивается в многокомпонентную рибонуклеазу, названную РНК-индуцированный сайленсинг-комплекс (RISC). Одна цепь миРНК остается ассоциированной с RISC для направления комплекса в сторону когнатной РНК, имеющей последовательность, комплементарную направляющей оц-миРНК в RISC. Эта миРНК-направляемая эндонуклеаза расщепляет РНК, что приводит к укорочению и инактивации РНК-мишени. Недавние исследования показали полезность химически синтезированной 21-27-нуклеотидной миРНК, демонстрирующей эффекты РНКи в клетках млекопитающих и демонстрирующей, что термодинамическая стабильность гибридизации миРНК (на концах или в середине) играет центральную роль в определении функции молекул. Более подробные характеристики RISC, молекул миРНК и РНКи описаны в научной литературе.
Полезность РНКи в отрицательной регуляции экспрессии генов в клетках млекопитающих успешно показана в лабораторных условиях с использованием химически синтезированной миРНК или эндогенно экспрессируемой миРНК. Эндогенная миРНК сначала экспрессируется в виде малой шпилечной РНК (shRNA) с помощью экспрессирующего вектора (плазмидного или вирусного вектор), а затем процессируется Dicer, становясь функциональной миРНК.
Чтобы миРНК имела активность и могла осуществлять сайленсинг генов-мишеней, ее можно доставлять в клетки, где должен происходить сайленсинг, посредством трансфекции этих клеток. Одним из способов доставки миРНК в эти клетки является использование наночастиц, которые могут нести миРНК и делать возможным захват миРНК через внешнюю мембрану клетки, получая доступ к цитоплазме. Высвобождение миРНК в цитоплазму позволяет этим остаткам взаимодействовать с комплексом RISC, где антисмысловая цепь отделяется от смысловой цепи, смысловая цепь подвергается деградации, и антисмысловая цепь используется комплексом RISC для отслеживания мРНК в клетке по последовательности с комплементарностью в отношении антисмысловой последовательности. Это делает возможной гибридизацию двух последовательностей, а затем происходит расщепление мРНК под действием фермента Dicer.
мРНК предоставляет матрицу, отвечающую за трансляцию последовательности мРНК в действующий белок, необходимый клетке. Расщепление мРНК снижает способность клетки продуцировать пептид или белок, кодируемый мРНК. Сайленсинг генов под действием миРНК может демонстрировать пролонгированный эффект и зависит от оборота и баланса между скоростью синтеза, количеством мРНК и скоростью деградации мРНК и/или самого белка. Показано, что миРНК имеет мощный эффект сайленсинга в отношении гена-мишени, и далее это может приводить к пролонгированному снижению (от дней до недель) белкового продукта.
Повышенные уровни TGF-бета 1 вносят вклад в ингибирование проникновения T-клеток в области вблизи опухолей [1-3].
Например, в опухолях из пациентов с раком толстого кишечника [1,2] или метастатическим уротелиальным раком, которых лечили антителом против PD-L1 (атезолизумабом), отсутствие ответа было ассоциировано с передачей сигнала трансформирующего фактора роста β (TGFβ) в фибробластах. Главным образом, это наблюдали в опухолях, демонстрирующих исключение CD8+ T-клеток из паренхимы опухоли и накопление этих T-клеток в богатой фибробластами и коллагеном периопухолевой строме, что является распространенным фенотипом среди пациентов с метастатическим уротелиальным раком. Совместное введение блокирующего TGFβ антитела с антителами против PD-L1 снижало передачу сигнала TGFβ в стромальных клетках, и это, в свою очередь, делает возможным проникновение T-клеток в центр опухолей, что провоцирует противоопухолевый иммунитет и регрессирование опухоли в этой модели [3].
Хотя исследования [1] и [2] сфокусированы на раке толстого кишечника и [3] демонстрируют эффекты в отношении уротелиального рака, не было предпринято попыток исследовать синергию между ингибированием TGFβ1 и PD-L1 в отношении иммунного ответа, когда обе мишени ингибировали одновременно. Авторы настоящего изобретения исследовали полипептидные наночастицы (PNP) для доставки миРНК, нацеленной на TGFβ1 и Cox-2, в печень для исследования того, будет ли этот эффект улучшать эффективность антител против PD-L1 при этом заболевании. Доставка в эндотелиальные клетки, а также нормальные гепатоциты позволяет предполагать возможность сайленсинга двух генов вблизи опухоли.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
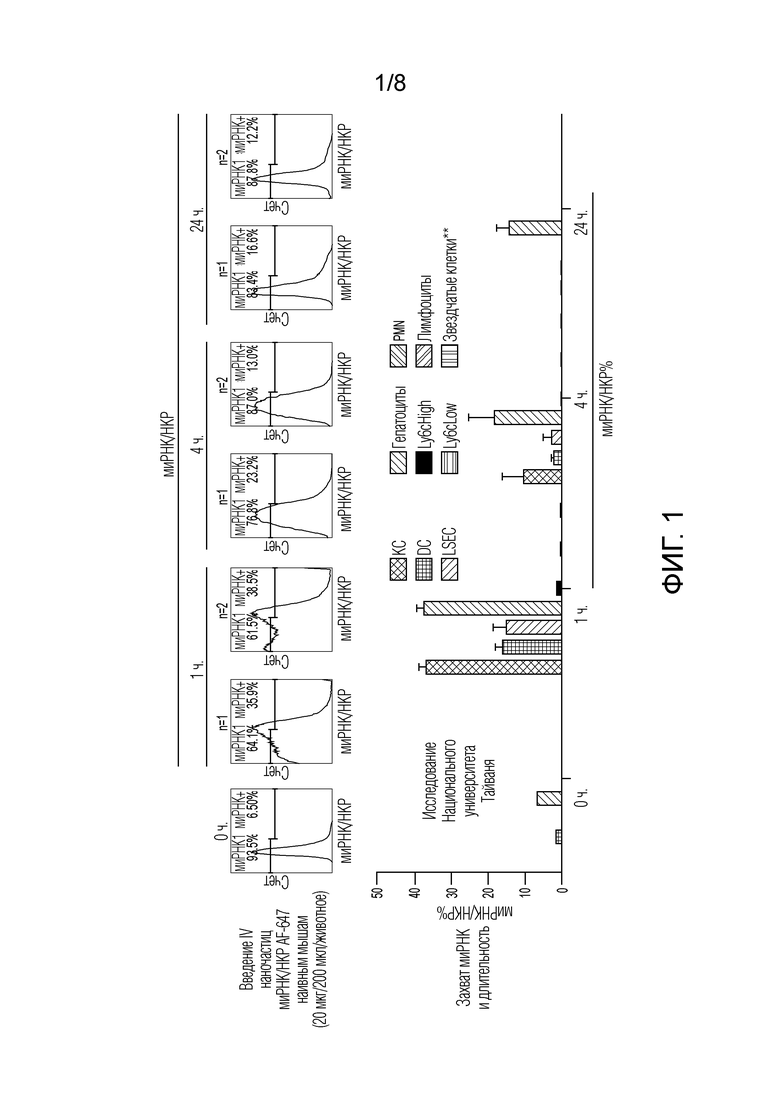
Фиг. 1. Локализация вводимых IV STP707 в клетках печени. Флуоресцентно меченую AF647 миРНК составляли с HKP для получения наночастицы. Наночастицы вводили мышам посредством IV инъекции (введение через хвостовую вену). В моменты времени, указанные на фигуре, животных умерщвляли, печень удаляли и иссекали и диссоциированные клетки подвергали проточной цитометрии с использованием меченых антител, что позволяло различать разные представленные типы клеток. Типы клеток приведены слева направо под каждым моментом времени: купферовские клетки (KC), дендритные клетки (DC), синусоидальные эндотелиальные клетки печени (LSEC), гепатоциты, Ly6cHigh клетки (воспалительные моноциты), Ly6cLow клетки, полиморфно-ядерные лейкоциты (PMN), лимфоциты и звездчатые клетки. На этой фигуре показано, что гепатоциты, купферовские клетки и клетки LSEC исходно захватывали STP707 через 1 ч. Популяция звездчатых клеток в печени составляла всего лишь 1,4% от популяции клеток. Хотя при проточной цитометрии наблюдали некоторые признаки захвата, сигнал был слишком низким, таким образом, авторы настоящего изобретения валидировали захват в первичных звездчатых клеток человека и демонстрировали исключительный захват и сайленсинг генов в этих клетках.
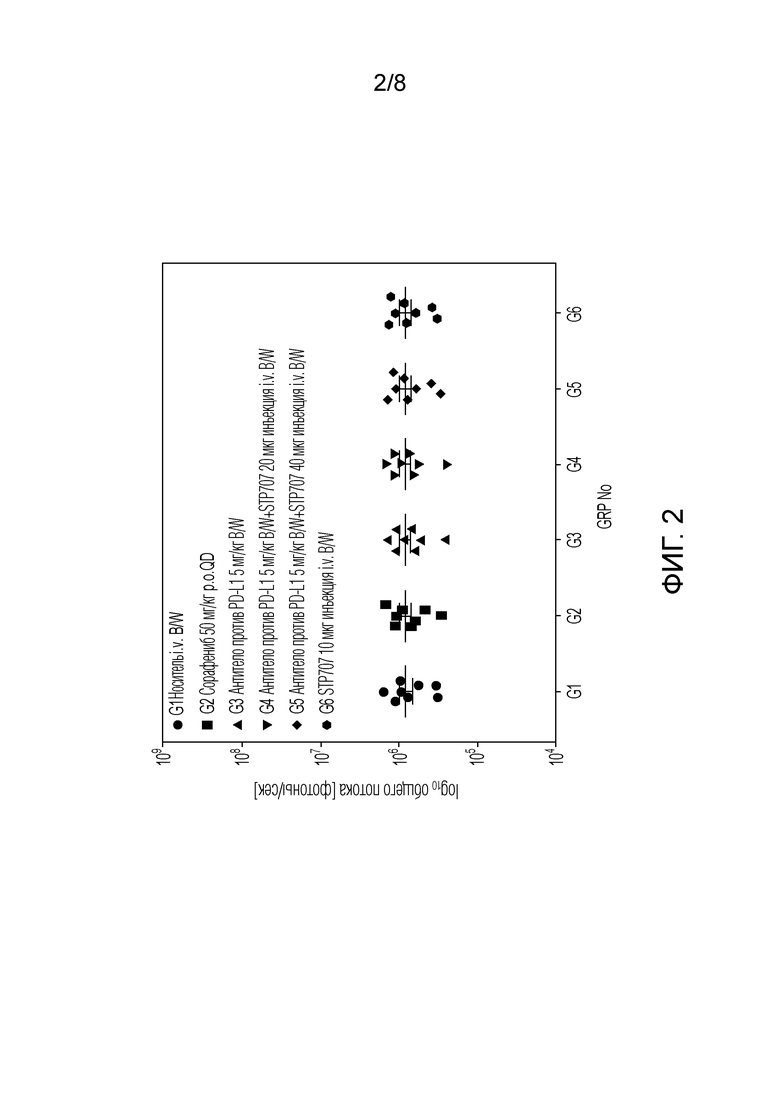
Фиг. 2. Используя субстрат люциферин, вводимый анестезированным животным, оценивали объем опухолей посредством измерения светового потока от каждого животного (измеряемого с использованием цифровой системы визуализации). Животных приписывали в когорту с учетом нормализации опухолей среди всех тестовых групп. На этой фигуре показаны исходные значения, получаемые при приписывании к группам, свидетельствующие об однородности размеров опухолей между когортами перед началом лечения.
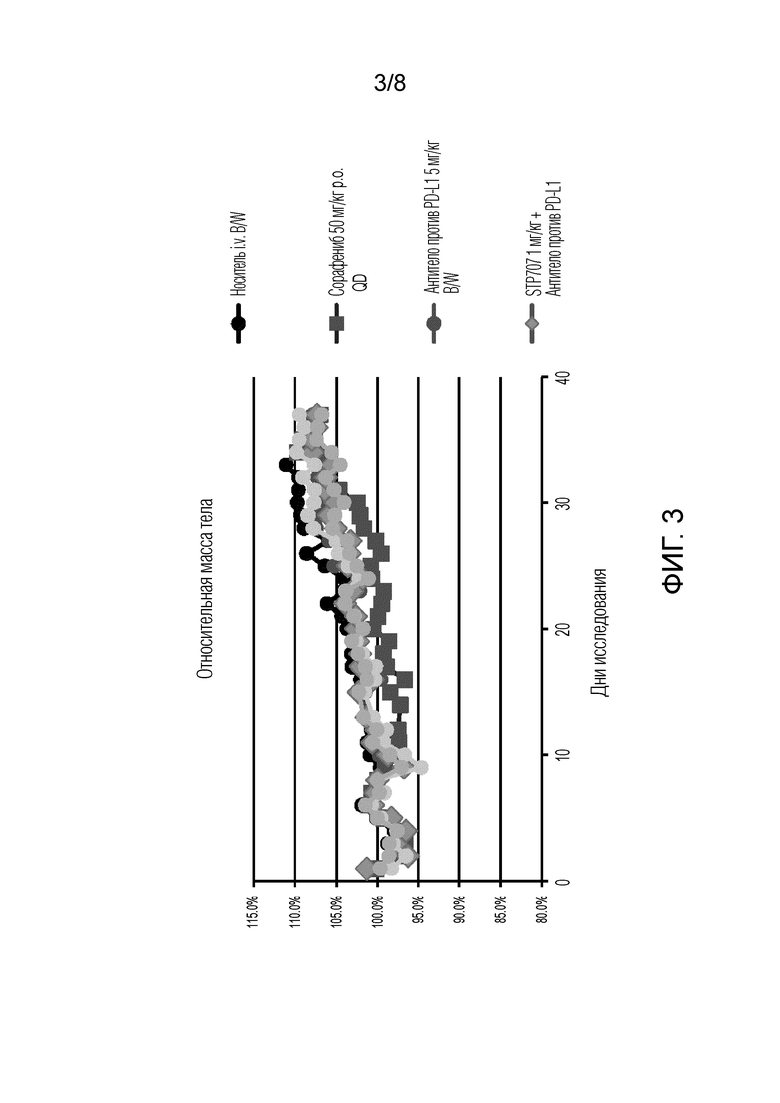
Фиг. 3. Массу тела животных подвергали мониторингу после каждого введения и усредняли массу тела среди всех животных в когорте. Строили график данных в виде % исходной массы тела до введения дозы.
Сорафениб в отдельности (красные квадраты) индуцировал небольшое изменение массы тела. Однако, все другие схемы лечения (STP707 в отдельности или+антитела против PD-L1) хорошо переносились, и не наблюдали значимой потери массы тела в группах лечения.
Фиг. 4. Измерения опухолеассоциированной биолюминесценции (TABL) осуществляли посредством введения субстрата люциферазы (люциферина) анестезированным животным, а затем визуализации света, генерируемого с помощью системы визуализации живых животных IVIS. Животным вводили средства на всем протяжении фазы введения (выделенная серым область) или в ином случае подвергали мониторингу без лечения в другие моменты времени.
Животные, которым вводили контроль (носитель), демонстрировали быстрый рост опухолей, что определяли по большему световому сигналу. При введении сорафениба и mAb против PD-L1 наблюдали статический эффект в отношении роста опухоли в фазу введения. STP707 в отдельности (40 мкг на инъекцию или ~2 мг/кг) или с mAb против PD-L1 проявляли значительное снижение опухолевых клеток после 5-6 доз. Опухоли не были видимыми в эти группах лечения.
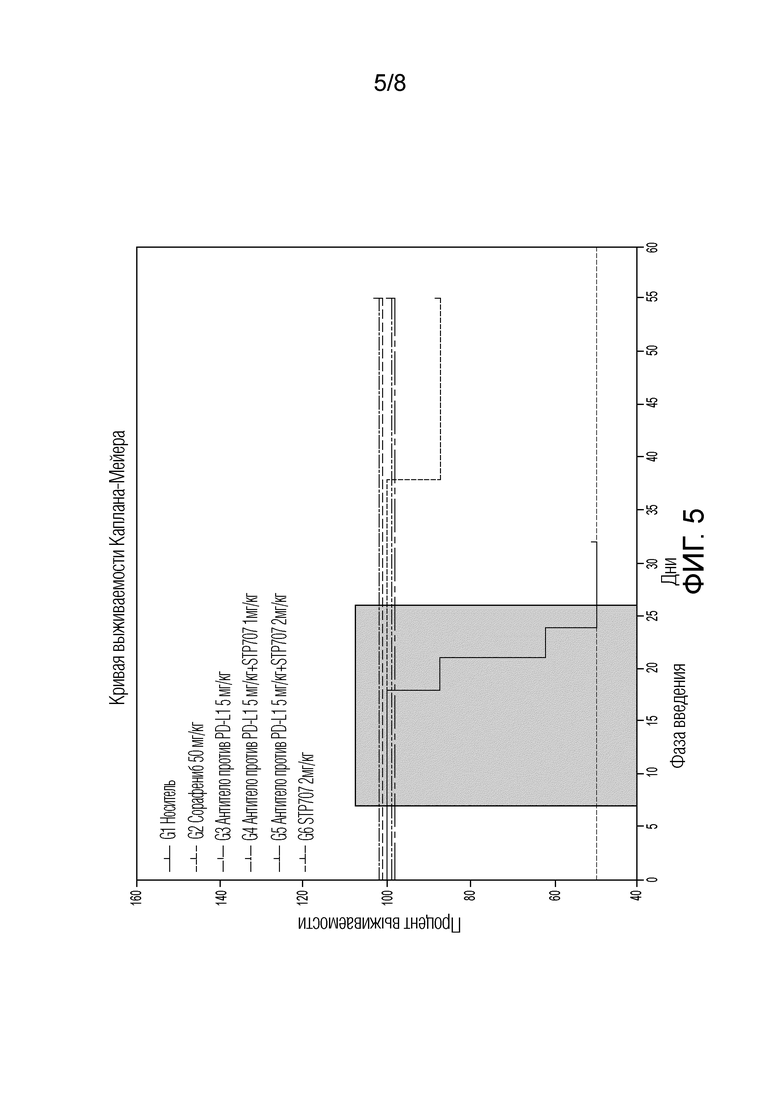
Фиг. 5. У контрольных животных (которым вводили носитель) наблюдали значительный эффект неконтролируемого роста опухоли в отношении жизнеспособности животных. 50% неподвергнутых лечению животных погибало, или их умерщвляли, в результате повышенной опухолевой нагрузки в течение фазы введения эксперимента. 1 животное умерщвляли через 37 дней в группе сорафениба. Ни одно животное не погибало в любой другой группе лечения.
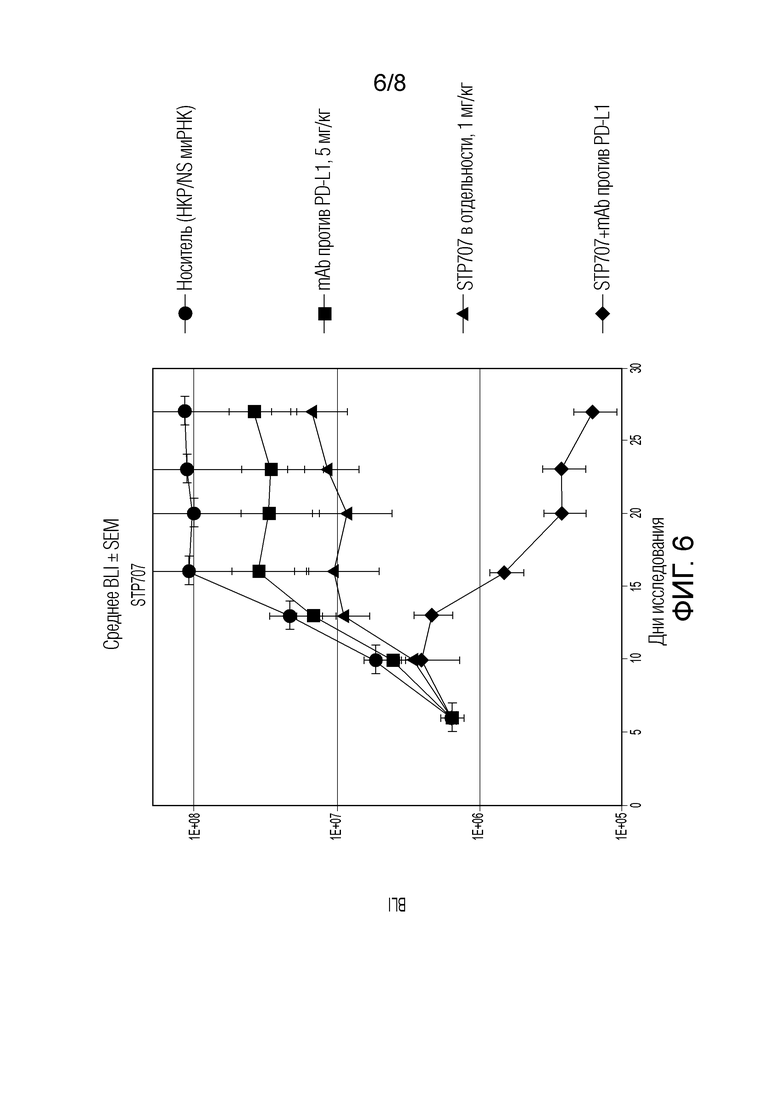
Фиг. 6. Данные свидетельствуют о том, что в контрольных образцах (PNP, нагруженных несайленсинговой (NS) миРНК) наблюдали значительное повышение роста опухолевых клеток, измеряемое посредством считывания потока вне животного с использованием системы визуализации IVIS. Антитело против PD-L1 демонстрировало слабый ингибиторный эффект в отношении роста опухоли. STP707 в отдельности (1 мг/кг) демонстрировали даже большее ингибирование роста опухоли, чем Ab против PD-L1, и в присутствии mAb против PD-L1, STP707 полностью уничтожали опухоль после 6 доз, что позволяет предполагать аддитивность эффекта в случае антитела.
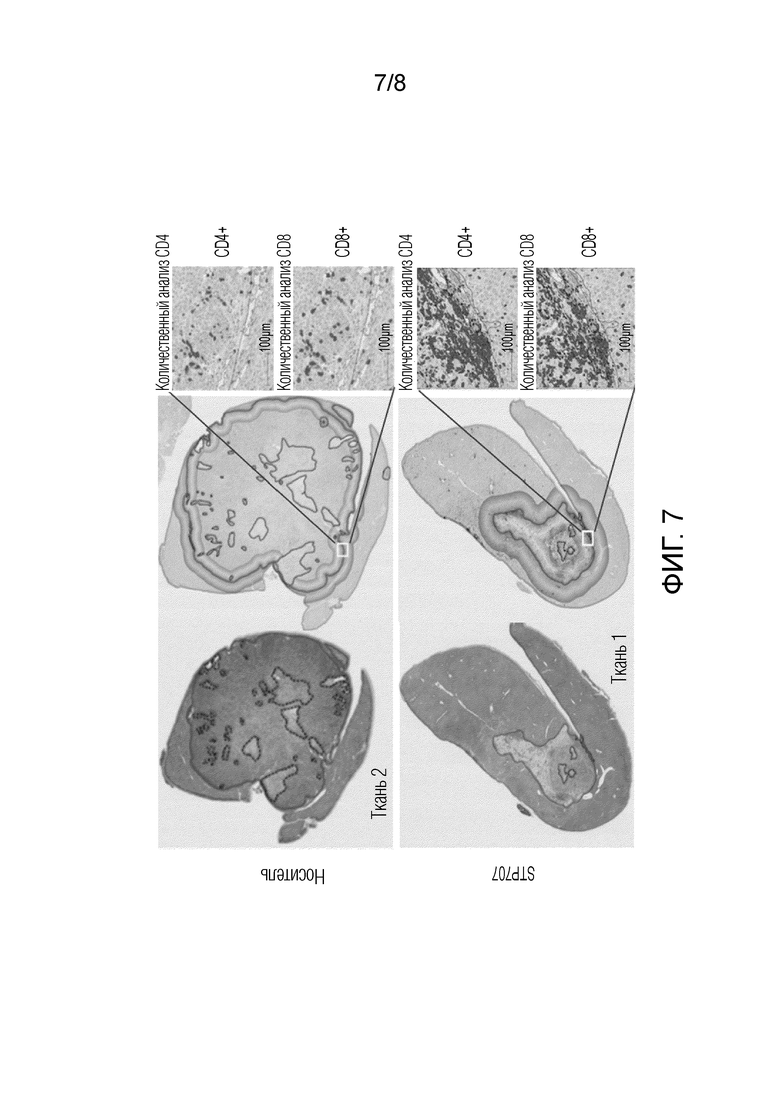
Фиг. 7. STP707 вводили в 3 дозах по 1 мг/кг животным с сингенной ортотопической опухолью HCC, а затем печень удаляли, получали срезы и окрашивали (гематоксилином и эозином) для демонстрации локализации и размера опухоли. Необходимо отметить значительное снижение размера опухоли при введении STP707 в течение этого короткого периода времени. В областях, показанных белыми рамками, CD4+ и CD8+ T-клетки количественно анализировали посредством окрашивания и подсчета окрашенных пятен. Эти области показаны в увеличенном масштабе справа от каждой фигуры, и можно четко видеть, что введение STP707 приводило к значительному повышению количества CD4+ и CD8+ T-клеток, присутствующих в зоне границы печени и опухоли, что позволяет предполагать, что введение STP707 делает возможным большее проникновение T-клеток в опухоль.
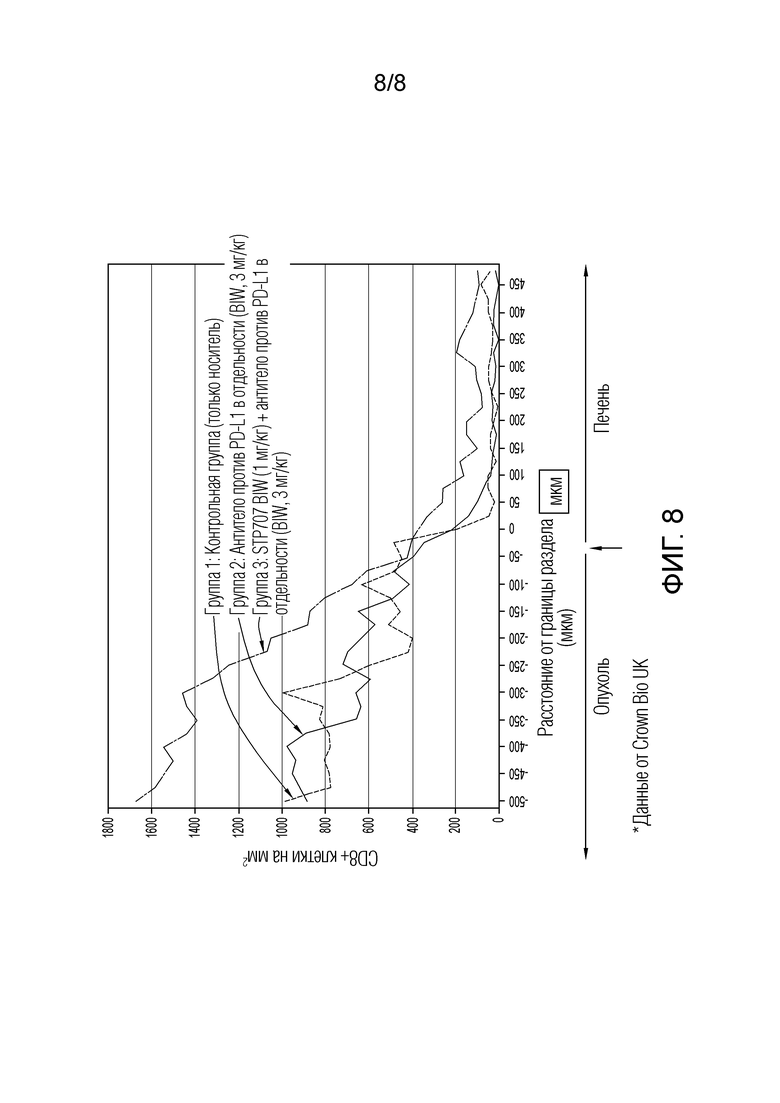
Фиг. 8. Используя изображения, схожие с показанными на фиг. 7, T-клетки количественно анализировали в различных сегментах, измеряя их на расстоянии от границы опухоли - внутрь, по направлению к опухоли, или вне, в направлении печени. В каждом сегменте (толщиной 50 мкм) T-клетки количественно анализировали и строили показанный график. Введение STP707 вместе с Ab против PD-L1 вызывало 2-кратное повышение CD8+ T-клеток при глубине 500 мкм в опухоли по сравнению с введением носителя в отдельности. Также показано повышение CD8+ T-клеток в печени вблизи опухоли, что позволяет предполагать возможное рекрутирование T-клеток, индуцированное уменьшением "стены" TGF-бета, окружающей опухоль.
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Изобретение относится к применению молекул малой интерферирующей РНК (миРНК), ингибирующих TGF-бета 1 и Cox-2 у индивидуума, в отдельности или в комбинации с ингибиторами иммунных контрольных точек для лечения злокачественного новообразования у индивидуума. В рамках изобретения термин "индивидуум" относится к любому млекопитающему, включая людей. Индивидуум может являться лабораторным животным, таким как грызун, хорек или не являющийся человеком примат. Предпочтительно, индивидуум является человеком.
В одном из вариантов осуществления изобретение относится к способу уничтожения злокачественных клеток у индивидуума посредством введения индивидууму терапевтически эффективного количества миРНК против TGF-бета 1. В одном из аспектов этого варианта осуществления миРНК против TGF-бета 1 вводят индивидууму внутривенно. В другом аспекте этого варианта осуществления миРНК против TGF-бета 1 вводят в опухоль индивидуума. В другом аспекте этого варианта осуществления миРНК против TGF-бета 1 вводят вблизи опухоли или системно в носителе, делающем возможной доставку в опухоль.
В другом варианте осуществления изобретение относится к способу лечения злокачественного новообразования у индивидуума посредством введения индивидууму терапевтически эффективного количества миРНК против TGF-бета 1. В одном из аспектов этого варианта осуществления миРНК против TGF-бета 1 вводят индивидууму внутривенно. В другом аспекте этого варианта осуществления миРНК против TGF-бета 1 вводят в опухоль индивидуума. В другом аспекте этого варианта осуществления, миРНК против TGF-бета 1 вводят вблизи опухоли или системно в носителе, делающем возможной доставку в опухоль.
Злокачественное новообразование (и злокачественные клетки) является любым злокачественным новообразованием, которым страдает индивидуум. Такие злокачественные новообразования включают рак печени, рак толстого кишечника, рак поджелудочной железы, рак легких и рак мочевого пузыря. Рак печени может являться первичным раком печени или злокачественным новообразованием, метастазирующим в печень из другой ткани. Первичный рак печени включает печеночноклеточную карциному и гепатобластому. Метастазирующие злокачественные новообразования включают рак толстого кишечника и рак поджелудочной железы.
Молекулы миРНК против TGF-бета 1 включают последовательности, указанные в таблице 1.
Таблица 1: Последовательности миРНК против TGF-бета 1
hmTF-25-1: смысловая 5'-r(GGAUCCACGAGCCCAAGGGCUACCA)-3' (SEQ ID NO: 1)
антисмысловая 5'-r(UGGUAGCCCUUGGGCUCGUGGAUCC)-3 (SEQ ID NO: 2)
hmTF-25-2: смысловая 5'-r(CCCAAGGGCUACCAUGCCAACUUCU)-3' (SEQ ID NO: 3)
антисмысловая 5'-r(AGAAGUUGGCAUGGUAGCCCUUGGG)-3' (SEQ ID NO: 4)
hmTF-25-3:смысловая 5'-r(GAGCCCAAGGGCUACCAUGCCAACU)-3' (SEQ ID NO: 5)
антисмысловая 5'-r(AGUUGGCAUGGUAGCCCUUGGGCUC)-3' (SEQ ID NO: 6)
hmTF25-4: смысловая, 5'-r(GAUCCACGAGCCCAAGGGCUACCAU)-3' (SEQ ID NO: 7)
антисмысловая, 5'-r(AUGGUAGCCCUUGGGCUCGUGGAUC)-3' (SEQ ID NO: 8)
hmTF25-5: смысловая, 5'-r(CACGAGCCCAAGGGCUACCAUGCCA)-3' (SEQ ID NO: 9)
антисмысловая, 5'-r(UGGCAUGGUAGCCCUUGGGCUCGUG)-3' (SEQ ID NO: 10)
hmTF25-6: смысловая, 5'-r(GAGGUCACCCGCGUGCUAAUGGUGG)-3' (SEQ ID NO: 11)
антисмысловая, 5'-r(CCACCAUUAGCACGCGGGUGACCUC)-3' (SEQ ID NO: 12)
hmTF25-7: смысловая, 5'-r(GUACAACAGCACCCGCGACCGGGUG)-3' (SEQ ID NO: 13)
антисмысловая, 5'-r(CACCCGGUCGCGGGUGCUGUUGUAC)-3' (SEQ ID NO: 14)
hmTF25-8: смысловая, 5'-r(GUGGAUCCACGAGCCCAAGGGCUAC)-3' (SEQ ID NO: 15)
антисмысловая, 5'-r(GUAGCCCUUGGGCUCGUGGAUCCAC)-3' (SEQ ID NO: 16)
В одном из аспектов миРНК против TGF-бета 1 содержит следующие последовательности: смысловую: 5'-cccaagggcuaccaugccaacuucu-3' (SEQ ID NO: 3); антисмысловую: 5'-agaaguuggcaugguagcccuuggg-3' (SEQ ID NO: 4).
МиРНК против TGF-бета 1 вводят индивидууму в фармацевтически приемлемом носителе. Такие носители включают разветвленные гистидин-лизиновые полимеры. В одном из вариантов осуществления таких полимеров полимер имеет формулу (R)K(R)-K(R)-(R)K(X), где R=KHHHKHHHKHHHKHHHK (SEQ ID NO: 17) или R=KHHHKHHHKHHHHKHHHK (SEQ ID NO: 18), X=C(O)NH2, K=лизин и H=гистидин. Такие полимеры образуют наночастицу с миРНК против TGF-бета 1. Наночастицу можно вводить индивидууму внутривенно или внутриопухолево.
В другом варианте осуществления изобретение относится к способ уничтожения злокачественных клеток у индивидуума посредством введения индивидууму терапевтически эффективного количества ингибитора иммунных контрольных точек с терапевтически эффективным количеством миРНК против TGF-бета 1. В одном из аспектов этого варианта осуществления введение ингибитора иммунных контрольных точек с миРНК против TGF-бета 1 повышает эффективность миРНК против TGF-бета 1.
В другом варианте осуществления изобретение относится к способу лечения злокачественного новообразования у индивидуума посредством введения индивидууму терапевтически эффективного количества ингибитора иммунных контрольных точек с терапевтически эффективным количеством миРНК против TGF-бета 1. В одном из аспектов этого варианта осуществления введение ингибитора иммунных контрольных точек с миРНК против TGF-бета 1 повышает эффективность миРНК против TGF-бета 1.
Как указано выше, ингибитор иммунных контрольных точек и миРНК против TGF-бета 1 вводят индивидууму внутривенно, в опухоль индивидуума, вблизи опухоли или системно в носителе, делающем возможной доставку в опухоль.
В одном из аспектов этого варианта осуществления ингибитор иммунных контрольных точек является моноклональным антителом, блокирующим взаимодействие между рецепторами, такими как PD-1, PD-L1, CTLA4, Lag3 и Tim3, и лигандами этих рецепторов на клетках млекопитающих, таких как клетки человека. В конкретном аспекте моноклональное антитело является моноклональным антителом против PD-1 или PD-L1. Примеры моноклональных антител включают атезолизумаб, дурвалумаб, ниволумаб, пембролизумаб и ипилимумаб.
В другом аспекте этого варианта осуществления ингибитор иммунных контрольных точек является низкомолекулярным соединением, блокирующим взаимодействие между рецепторами, такими как PD-1, PD-L1, CTLA4, Lag3 и Tim3, и лигандами этих рецепторов на клетках млекопитающих, таких как клетки человека. В конкретном аспекте низкомолекулярное соединение блокирует связывание между PD-1 и PD-L1. BMS202 и схожие лиганды являются примерами таких низкомолекулярных соединений.
В дополнительном варианте осуществления изобретение относится к способу уничтожения злокачественных клеток у индивидуума посредством введения индивидууму терапевтически эффективного количества миРНК против Cox-2 с терапевтически эффективным количеством миРНК против TGF-бета 1. В одном из аспектов этого варианта осуществления комбинацию вводят индивидууму внутривенно. В другом аспекте этого варианта осуществления комбинацию вводят в опухоль индивидуума. В другом аспекте этого варианта осуществления комбинацию вводят вблизи опухоли или системно в носителе, делающем возможной доставку в опухоль.
В еще одном дополнительном варианте осуществления изобретение относится к способу лечения злокачественного новообразования у индивидуума посредством введения индивидууму терапевтически эффективного количества миРНК против Cox-2 с терапевтически эффективным количеством миРНК против TGF-бета 1. В одном из аспектов этого варианта осуществления комбинацию вводят индивидууму внутривенно. В другом аспекте этого варианта осуществления комбинацию вводят в опухоль индивидуума. В другом аспекте этого варианта осуществления комбинацию вводят вблизи опухоли или системно в носителе, делающем возможной доставку в опухоль.
Молекулы миРНК против Cox-2 включают последовательности, указанные в таблице 2.
Таблица 2: Последовательности миРНК против Cox-2
hmCX-25-1: смысловая 5'-r(GGUCUGGUGCCUGGUCUGAUGAUGU)-3' (SEQ ID NO: 19)
антисмысловая 5'-r(ACAUCAUCAGACCAGGCACCAGACC)-3' (SEQ ID NO: 20)
hmCX-25-2: смысловая 5'-r(GAGCACCAUUCUCCUUGAAAGGACU)-3' (SEQ ID NO: 21)
антисмысловая 5'-r(AGUCCUUUCAAGGAGAAUGGUGCUC)-3' (SEQ ID NO: 22)
hmCX-25-3: смысловая 5'-r(CCUCAAUUCAGUCUCUCAUCUGCAA)-3' (SEQ ID NO: 23)
антисмысловая 5'-r(UUGCAGAUGAGAGACUGAAUUGAGG)-3' (SEQ ID NO: 24)
hmCX25-4: смысловая, 5'-r(GAUGUUUGCAUUCUUUGCCCAGCAC)-3' (SEQ ID NO: 25)
антисмысловая, 5'-r(GUGCUGGGCAAAGAAUGCAAACAUC)-3' (SEQ ID NO: 26)
hmCX25-5: смысловая, 5'-r(GUCUUUGGUCUGGUGCCUGGUCUGA)-3' (SEQ ID NO: 27)
антисмысловая, 5'-r(UCAGACCAGGCACCAGACCAAAGAC)-3' (SEQ ID NO: 29)
hmCX25-6: смысловая, 5'-r(GUGCCUGGUCUGAUGAUGUAUGCCA)-3' (SEQ ID NO: 29)
антисмысловая, 5'-r(UGGCAUACAUCAUCAGACCAGGCAC)-3' (SEQ ID NO: 30)
hmCX25-7: смысловая, 5'-r(CACCAUUCUCCUUGAAAGGACUUAU)-3' (SEQ ID NO: 31)
антисмысловая, 5'-r(AUAAGUCCUUUCAAGGAGAAUGGUG)-3' (SEQ ID NO: 32)
hmCX25-8: смысловая, 5'-r(CAAUUCAGUCUCUCAUCUGCAAUAA)-3' (SEQ ID NO: 33)
антисмысловая, 5'-r(UUAUUGCAGAUGAGAGACUGAAUUG)-3' (SEQ ID NO: 34)
В одном из аспектов миРНК против Cox-2 содержит следующие последовательности: смысловую: 5'-ggucuggugccuggucugaugaugu-3' (SEQ ID NO: 19); антисмысловую: 5'-acaucaucagaccaggcaccagacc-3' (SEQ ID NO: 20).
МиРНК против TGF-бета 1 и миРНК против Cox-2 вводят в фармацевтически приемлемом носителе. Такие носители включают разветвленные гистидин-лизиновые полимеры. В одном из вариантов осуществления таких полимеров полимер имеет формулу (R)K(R)-K(R)-(R)K(X), где R=KHHHKHHHKHHHKHHHK (SEQ ID NO: 17) или R=KHHHKHHHKHHHHKHHHK (SEQ ID NO: 18), X=C(O)NH2, K=лизин, H=гистидин и N=аспарагин. Такие полимеры образуют наночастицу с миРНК против TGF-бета 1 и миРНК против Cox-2. Наночастицу можно вводить индивидууму внутривенно или внутриопухолево.
Как указано выше в отношении миРНК против TGF-бета 1, злокачественное новообразование (и злокачественные клетки), на которое нацелена комбинация миРНК против TGF-бета 1 и миРНК против Cox-2, может являться любым злокачественным новообразованием, которым страдает индивидуум. Такие злокачественные новообразования включают рак печени, рак толстого кишечника, рак поджелудочной железы, рак легких и рак мочевого пузыря. Рак печени может являться первичным раком печени или злокачественным новообразованием, метастазирующим в печень из другой ткани. Первичный рак печени включает печеночноклеточную карциному и гепатобластому. Метастазирующие злокачественные новообразования включают рак толстого кишечника и рак поджелудочной железы.
В дополнительном варианте осуществления изобретение относится к способу уничтожения злокачественных клеток у индивидуума посредством введения индивидууму терапевтически эффективного количества ингибитора иммунных контрольных точек с терапевтически эффективным количеством миРНК против TGF-бета 1 и терапевтически эффективным количеством миРНК против Cox-2. Злокачественные клетки и злокачественные новообразования, на которые нацелен способ, являются любым злокачественным новообразованием, которым страдает индивидуум, включая описанные выше. В одном из аспектов этого варианта осуществления введение ингибитора иммунных контрольных точек с миРНК против TGF-бета 1 и миРНК против Cox-2 повышает эффективность любой миРНК в отдельности.
В еще одном дополнительном варианте осуществления изобретение относится к способу лечения злокачественного новообразования у индивидуума посредством введения индивидууму терапевтически эффективного количества ингибитора иммунных контрольных точек с терапевтически эффективным количеством миРНК против TGF-бета 1 и терапевтически эффективным количеством миРНК против Cox-2. Злокачественные клетки и злокачественные новообразования, на которые нацелен способ, являются любым злокачественным новообразованием, которым страдает индивидуум, включая описанные выше. В одном из аспектов этого варианта осуществления введение ингибитора иммунных контрольных точек с миРНК против TGF-бета 1 и миРНК против Cox-2 повышает эффективность любой из миРНК в отдельности.
Как указано выше, ингибитор иммунных контрольных точек, миРНК против TGF-бета 1 и миРНК против Cox-2 вводят внутривенно индивидууму, в опухоль индивидуума, вблизи опухоли или системно в носителе, делающем возможной доставку в опухоль.
Ингибитор иммунных контрольных точек, вводимый с комбинацией молекул миРНК, является моноклональным антителом или низкомолекулярным соединением, как описано выше. Его можно вводить до, после или одновременно с комбинацией молекул миРНК.
Изобретение относится к некоторым фармацевтическим композициям. В одном из вариантов осуществления композиция содержит миРНК против TGF-бета 1, как представлено в настоящем описании, в фармацевтически приемлемом носителе, как представлено в настоящем описании.
В другом варианте осуществления эту фармацевтическую композицию используют в комбинации с ингибитором иммунных контрольных точек, как представлено в настоящем описании. Таким образом, этот вариант осуществления изобретения относится к комбинации терапевтических лекарственных средств, содержащей ингибитор иммунных контрольных точек и фармацевтическую композицию, содержащую миРНК против TGF-бета 1 в фармацевтически приемлемом носителе, как представлено в настоящем описании.
В другом варианте осуществления изобретение относится к комбинации терапевтических лекарственных средств, содержащей ингибитор иммунных контрольных точек и фармацевтическую композицию, содержащую миРНК против TGF-бета 1, миРНК против Cox-2 и фармацевтически приемлемый носитель, как представлено в настоящем описании.
Комбинацию терапевтических лекарственных средств, представленную в настоящем описании, также можно использовать для повышения противоопухолевой эффективности ингибитора иммунных контрольных точек у индивидуума со злокачественным новообразованием. Терапевтически эффективное количество фармацевтической композиции, содержащей миРНК против TGF-бета 1 и миРНК против Cox-2, вводят индивидууму вместе с терапевтически эффективным количеством ингибитора контрольных точек. МиРНК против TGF-бета 1 снижает воспалительный ответ индивидуума на злокачественное новообразование и позволяет T-клеткам и другим иммунным клеткам лучше проникать в опухоль. Она также приводит к более сильному иммунному ответу на злокачественное новообразование у индивидуума, чем иммунный ответ, вызываемый ингибитором контрольных точек в отдельности. Этот ответ включает более высокую активацию T-клеток и их способность проникать в злокачественное новообразование. МиРНК против Cox-2 снижает воспалительный ответ индивидуума на злокачественное новообразование и/или снижает образование истощенных T-клеток или регуляторных T-клеток вокруг злокачественного новообразования.
Комбинацию терапевтических лекарственных средств, представленную в настоящем описании, также можно использовать для антигенного примирования T-клеток для распознавания и уничтожения злокачественных клеток у индивидуума и стимуляции T-клеточного иммунитета против злокачественного новообразования у индивидуума. Индивидууму вводят терапевтически эффективное количество комбинации. Злокачественные новообразования являются злокачественными новообразованиями, представленными в настоящем описании.
В одном конкретном варианте осуществления изобретение относится к способу лечения рака печени у индивидуума посредством введения индивидууму терапевтически эффективного количества фармацевтической композиции по изобретению или комбинации терапевтических лекарственных средств по изобретению. В одном из аспектов этого варианта осуществления рак печени является первичным раком печени. В конкретном аспекте первичный рак печени является печеночноклеточной карциномой или гепатобластомой. В другом аспекте этого варианта осуществления рак печени является злокачественным новообразованием, метастазирующим в печень из другой ткани организма индивидуума. Такие метастазирующие злокачественные новообразования включают рак толстого кишечника и рак поджелудочной железы. В одном из аспектов этого варианта осуществления индивидуум является человеком.
В другом конкретном варианте осуществления изобретение относится к способу уничтожения клеток печеночноклеточной карциномы у человека, включающему введение человеку терапевтически эффективного количества фармацевтической композиции, содержащей миРНК против TGF-бета 1 и миРНК против Cox-2 в фармацевтически приемлемом носителе, содержащем разветвленный гистидин-лизиновый полимер, образующий наночастицу с миРНК против TGF-бета 1 и миРНК против Cox-2, где миРНК против TGF-бета 1 содержит последовательности: смысловую: 5'-cccaagggcuaccaugccaacuucu-3' (SEQ ID NO: 3); антисмысловую: 5'-agaaguuggcaugguagcccuuggg-3' (SEQ ID NO: 4), и миРНК против Cox-2 содержит последовательности: смысловую: 5'-ggucuggugccuggucugaugaugu-3' (SEQ ID NO: 19); антисмысловую: 5'-acaucaucagaccaggcaccagacc-3' (SEQ ID NO: 20).
В другом конкретном варианте осуществления изобретение относится к способу уничтожения клеток печеночноклеточной карциномы у человека, включающему введение человеку терапевтически эффективного количества ингибитора иммунных контрольных точек и фармацевтической композиции, содержащей миРНК против TGF-бета 1 и миРНК против Cox-2 в фармацевтически приемлемом носителе, содержащем разветвленный гистидин-лизиновый полимер, образующий наночастицу с миРНК против TGF-бета 1 и миРНК против Cox-2, где миРНК против TGF-бета 1 содержит последовательности: смысловую: 5'-cccaagggcuaccaugccaacuucu-3' (SEQ ID NO: 3); антисмысловую: 5'-agaaguuggcaugguagcccuuggg-3' (SEQ ID NO: 5), и миРНК против Cox-2 содержит последовательности: смысловую: 5'-ggucuggugccuggucugaugaugu-3' (SEQ ID NO: 19); антисмысловую: 5'-acaucaucagaccaggcaccagacc-3' (SEQ ID NO: 20) и где ингибитор контрольных точек содержит моноклональное антитело, которое может связываться и блокировать взаимодействия между PD-1 и PD-L1. Такие моноклональные антитела включают атезолизумаб, дурвалумаб, ниволумаб, пембролизумаб и ипилимумаб.
В дополнительном конкретном варианте осуществления изобретение относится к комбинации терапевтических лекарственных средств, содержащей ингибитор иммунных контрольных точек и фармацевтическую композицию, содержащую миРНК против TGF-бета 1 и миРНК против Cox-2 в фармацевтически приемлемом носителе, где ингибитор контрольных точек содержит моноклональное антитело, выбранное из группы, состоящей из атезолизумаба, дурвалумаба, ниволумаба, пембролизумаба и ипилимумаба, миРНК против TGF-бета 1 содержит последовательности: смысловую: 5'-cccaagggcuaccaugccaacuucu-3' (SEQ ID NO: 3); антисмысловую: 5'-agaaguuggcaugguagcccuuggg-3' (SEQ ID NO: 4), миРНК против Cox-2 содержит последовательности: смысловую: 5'-ggucuggugccuggucugaugaugu-3' (SEQ ID NO: 19); антисмысловую: 5'-acaucaucagaccaggcaccagacc-3' (SEQ ID NO: 20), и фармацевтически приемлемый носитель содержит разветвленный гистидин-лизиновый полимер, образующий наночастицу с миРНК против TGF-бета 1 и миРНК против Cox-2. В одном из аспектов этого варианта осуществления разветвленный гистидин-лизиновый полимер имеет формулу (R)K(R)-K(R)-(R)K(X), где R=KHHHKHHHKHHHKHHHK (SEQ ID NO: 17) или KHHHKHHHKHHHHKHHHK (SEQ ID NO: 18), X=C(O)NH2, K=лизин, H=гистидин и N=аспарагин.
Определения
Рак печени является любым первичным злокачественным новообразованием в печени, т.е. возникающим в печени; или любым вторичным злокачественным новообразованием в печени, т.е. злокачественным новообразованием, метастазирующим в печень из другой ткани в организме млекопитающего. Примером первичного рака печени является печеночноклеточная карцинома. Примером вторичного рака печени является рак толстого кишечника.
Злокачественное новообразование является любой злокачественной опухолью.
Злокачественная опухоль представляет собой массу неопластических клеток.
Лечение представляет собой уничтожение некоторых или всех из злокачественных клеток, уменьшение размера злокачественного новообразования, ингибирование роста злокачественного новообразования или снижение скорости роста злокачественного новообразования у индивидуума.
МиРНК против TGF-бета 1 является молекулой миРНК, снижающей или предотвращающей экспрессию гена в клетке млекопитающего, кодирующего синтез белка TGF-бета 1.
МиРНК против Cox-2 является молекулой миРНК, снижающей или предотвращающей экспрессию гена в клетке млекопитающего, кодирующего синтез белка Cox-2.
Молекула миРНК является олигонуклеотидом-дуплексом, являющимся коротким, двухцепочечным полинуклеотидом, противодействующим экспрессии гена в клетке после встраивания молекулы в клетку. Например, она нацелена и связывается с комплементарной нуклеотидной последовательностью в одноцепочечной молекуле РНК-мишени. Молекулы миРНК химически синтезируют или иначе конструируют способами, известными специалистам в этой области. Такие способы описаны в патентах США №№ 5898031, 6107094, 6506559, 7056704 и европейских патентах №№ 1214945 и 1230375, включенных в настоящее описание в качестве ссылки в полном объеме. Как известно в этой области, если молекулу миРНК идентифицируют по конкретной нуклеотидной последовательности, термин "последовательность" относится к смысловой цепи молекулы-дуплекса. Один или более рибонуклеотидов, составляющих молекулу, можно химически модифицировать способами, известными в этой области. В дополнение к модификации на уровне одного или более из отдельных нуклеотидов, можно модифицировать остов олигонуклеотида. Дополнительные модификации включают использование низкомолекулярных соединений (например, молекул сахара), аминокислот, пептидов, холестерина и других крупных молекул для конъюгации на молекуле миРНК.
Разветвленный гистидин-лизиновый полимер является пептидом, состоящим из аминокислот гистидина и лизина. При синтезе множества аминокислот из общего лизинового кора пептид состоит из 4 плеч или ветвлений цепи. Такие полимеры описаны в патентах США № 7070807 B2, опубликованном 4 июля 2006 года, № 7163695 B2, опубликованном 6 января 2007 года, и № 7772201 B2, опубликованном 10 августа 2010 года, включенных в настоящее описание в качестве ссылки в полном объеме.
Ингибитор иммунных контрольных точек является лекарственным средством, блокирующим некоторые белки, продуцируемые некоторыми типами клеток иммунной системы, такими как T-клетки, и некоторыми злокачественными клетками. Эти белки контрольных точек помогают контролировать иммунные ответы и могут удерживать T-клетки от уничтожения злокачественных клеток. Если эти белки контрольных точек блокируют, это "отпускает тормоз" иммунной системы, и T-клетки могут лучше уничтожать злокачественные клетки. Примеры белков контрольных точек, обнаруживаемых на T-клетках или злокачественных клетках, включают PD-1/PD-L1 и CTLA-4/B7-1/B7-2.
Выражение "вблизи злокачественного новообразования" означает "в ткани или клетках, близких или окружающих опухоль или серию опухолевых клеток".
Выражение "повышение противоопухолевой эффективности" означает обеспечение большего снижения скорости роста опухолевых клеток, больший эффект уничтожения опухолевых клеток и/или снижения опухолевой массы и, в конечном итоге, достижения лучшего терапевтического эффекта посредством пролонгирования жизни индивидуума с опухолью. Такие эффекты могут опосредоваться прямым действием на сами опухолевые клетки, или повышением активности T-клеток, или механизмом, посредством которого T-клетки получают лучший доступ к опухолевым клеткам и/или активируются, стимулируя более сильную иммунную реакцию против опухоли с повышением способности распознавать опухолевые клетки даже после начального лечения или без нее.
В следующих примерах проиллюстрированы некоторые аспекты по изобретению, но не следует их истолковывать как ограничивающие объем настоящего изобретения.
ПРИМЕРЫ
Результаты экспериментов
STP707 состоит из 2 миРНК (нацеленных на гены TGF-бета 1 и Cox-2), защищенных полипептидной наночастицей для доставки, состоящей из разветвленного полипептида HKP (гистидин-лизинового полимера). STP707 описаны в патенте США № 9642873 B2, опубликованном 9 мая 2017 года, и заменяющем патенте США № RE46873 E, опубликованном 29 мая 2018 года, описания которых включены в настоящее описание в качестве ссылки в полном объеме.
Используя наночастицу разветвленного полипептида, состоящую из аминокислот гистидина и лизина (HKP), авторы настоящего изобретения показали, что инъекция IV позволяет наночастицам захватываться клетками в печени с более высокой эффективностью. Используя проточную цитометрию для измерения захвата флуоресцентно меченой миРНК из наночастиц, авторы настоящего изобретения демонстрировали доставку в конкретные типы клеток в печени, включая звездчатые клетки, клетки LSEC и гепатоциты, а также купферовские клетки (фиг. 1). Таким образом, это позволяет авторам настоящего изобретения предполагать, что можно достигать очень хорошей эффективности доставки миРНК в эти клетки печени и, таким образом, осуществлять сайленсинг интересующих мишеней в этих клетках.
Авторы настоящего изобретения исследовали STP707 в качестве монотерапии и в комбинации с моноклональным антителом (mAb) против PD-L1 (клоном моноклонального Ab против PD-L1 10F.9G2 от BioXcell, West Lebanon, NH 03784) в ортотопической модели печеночноклеточной карциномы на мышах с использованием биолюминесцентного варианта линии клеток Hepa 1-6 для мониторинга опухолевой нагрузки с течением времени.
Авторы настоящего изобретения использовали ортотопическую модель имплантата, где клетки рака печени HCC (клетки Hepa 1-6) хирургически имплантировали в орган, из которого их получали (печень). Линию клеток рака печени мыши модифицировали так, чтобы она экспрессировала люциферазу (Hepa 1-6-Lux). Затем, после введения субстрата животным степень роста опухолей в печени этих животных можно подвергать мониторингу с использованием системы детекции люминесценции. Это позволяет измерять рост опухоли неинвазивным образом, не вредя животным. Авторы настоящего изобретения осуществляли мониторинг опухолей этим способом. Авторы настоящего изобретения исследовали скорость роста в отсутствие какого-либо лечения (контрольная группа), с использованием золотого стандарта лечения печеночноклеточной карциномы у людей (сорафениб - ингибитор киназ; 50 мг/кг, вводимый QD) и валидированного антитела мыши против PD-L1, как показано, ингибирующего рост опухоли у животных с ортотопическими опухолями Hepa 1-6 (вводимого BIW в дозе 5 мг/кг).
Авторы настоящего изобретения также сравнивали эффект миРНК, как показано, ингибирующей TGF-бета и Cox-2 (STP707), доставляемой с использованием пептидных наночастиц HKP (вводимой IV BIW в дозе 40 мкг или 20 мкг на инъекцию). Авторы настоящего изобретения дополнительно анализировали эффект STP707 при введении с антителом против PD-L1.
Авторы настоящего изобретения исследовали STP707 на эффективность при лечении HCC с использованием сингенной, ортотопической модели печеночноклеточной карциномы на мышах с помощью биолюминесцентного варианта линии клеток Hepa 1-6 для мониторинга опухолевой нагрузки с течением времени.
Эксперименты осуществляли с использованием линии мышей C57BL/6J из Charles River Labs.
Носитель (HKP+несайленсинговая миРНК; контроль) или STP707 вводили внутривенно (iv).
8 животных случайным образом приписывали к каждой группе лечения. Группы лечения являлись следующими:
1. Только носитель
2. Сорафениб (50 мг/кг) p.o., QD
3. Антитело против PD-L1 (5 мг/кг), i.p., BIW
4. Антитело против PD-L1 (5 мг/кг), i.p., BIW+20 мкг STP707/инъекция IV BIW
5. Антитело против PD-L1 (5 мг/кг), i.p., BIW+40 мкг STP707/инъекция IV BIW
6. 40 мкг STP707/инъекция IV BIW в отдельности
Животных рандомизировали в начале эксперимента по массе тела. Рандомизация обеспечивала очень схожее распределение масс среди выбранных животных в каждой группа, как показано на фиг. 2.
Массу тела животных измеряли ежедневно в течение фазы введения исследования эффективности. Строили график средних масс тела каждой группы (фигура 3). Сорафениб в отдельности индуцировал небольшое изменение массы тела. Однако, все другие схемы лечения (STP707 в отдельности или+против PD-L1) хорошо переносились, и не наблюдали значимой потери массы тела в группах лечения.
Рост опухоли подвергали мониторингу посредством биолюминесцентной визуализации и количественного анализа опухолеассоциированной биолюминесценции (TABL). Строили график TABL по дням исследования, показанный на фигуре 4.
После завершения запланированной фазы введения разрастание опухоли подвергали мониторингу в группах 2-6. Не наблюдали вторичного роста опухоли перед последним днем исследования (днем 50), что позволяет предполагать, что лечение было очень эффективным в ингибировании роста опухоли и предотвращении вторичного роста, что позволяет предполагать выраженный эффект в отношении жизнеспособности опухоли.
Эффект способов комбинированного лечения дополнительно подтвержден в анализе выживаемости (с использованием суррогатных конечных точек человека) всех мышей в исследовании (фигура 5). Конечную точку для прекращения исследования для человека определяли как достижение опухолями максимального разрешенного размера или демонстрация опухолями нежелательных клинических признаков. Все схемы лечения приводили к статистически значимо улучшенной выживаемости, о чем свидетельствует логарифмический ранговый критерий (Мантеля-Кокса) (p=0,0001) и критерий Гехана-Бреслоу-Вилкоксона (p=0,0002). Не наблюдали значимых различий выживаемости среди групп лечения.
Для валидации полученных результатов авторы настоящего изобретения повторяли исследование с использованием более низкой дозы STP707 (1 мг/кг) (фиг. 6).
Полученные данные подтверждают наблюдение о том, что STP707 проявляет монотерапевтическое действие против опухоли - снижение роста относительно контрольной (неподвергнутой лечению) когорты. В группе STP707 наблюдали лучшую эффективность, чем в группе антитела (PD-L1) в отдельности.
В этом исследовании STP707 проявляли монотерапевтическую активность, превышающую активность антитела против PD-L1 в отдельности. Однако комбинирование STP707 с антителом уменьшало опухоль до недетектируемых уровней после 4 доз.
Т.к. не наблюдали опухолей в любой из групп лечения с использованием STP707, авторы настоящего изобретения повторяли исследование, но с использованием только 3 доз STP707 1 мг/кг. После третьей дозы животных умерщвляли, печень удаляли, получали срезы и окрашивали их на CD4+ и CD8+ T-клетки посредством иммуногистохимии.
Даже в этих исследованиях сниженных доз авторы настоящего изобретения наблюдали значительное различие между необработанными (контрольными) образцами и обработанными STP707 образцами в терминах общего размера опухоли. У неподвергнутых лечению животных опухоль почти полностью соответствовала размеру печени, в то время как в образцах из групп с STP707 опухоли значительно уменьшались (фиг. 7).
Кроме того, окрашивание IHC на CD4+ и CD8+ T-клетки демонстрировало значительное повышение этих T-клеток, проникающих в опухоль в образцах из групп, которым вводили STP707 (фиг. 7 и фиг. 8).
Анализ изображений осуществляли для количественного анализа CD4+ и CD8+ T-клеток на границе между опухолью и печенью, показанной цветными линиями на образцах опухолей. Эти линии чертили на расстоянии 50 мкм от границы опухоли - в направлении опухоли или вовне, от опухоли, но в сторону печени. С помощью анализа изображений подсчитывали все CD8+ T-клетки в каждом 50-мкм сегменте, и строили график данных, показанный на фигуре 8.
Введение STP707 вместе с Ab против PD-L1 демонстрировало 2-кратное повышение CD8+ T-клеток на расстоянии 500 мкм в опухоли. Оно также демонстрировало повышение CD8+ T-клеток в печени опухоли, что позволяет предполагать возможное рекрутирование T-клеток, индуцированное уменьшением "стены" TGF-бета, окружающей опухоль.
Выводы
Основной целью этого исследования являлось определение переносимости и эффективности STP707 (полипептидных наночастиц HKP, содержащих миРНК против TGF-бета 1 и Cox-2) в качестве монотерапии и в комбинации с антителом против PD-L1 в ортотопической модели печеночноклеточной карциномы на мышах с использованием биолюминесцентного варианта линии клеток Hepa 1-6.
Все схемы лечения хорошо переносились в тестируемых дозах и составах; не наблюдали нежелательных клинических признаков или потери массы тела в любой из групп лечения.
Все схемы лечения приводили к статистически значимому снижению роста опухоли по сравнению с контролем. Однако, монотерапия STP707 (2 мг/кг) приводила к снижению роста опухоли, которое также наблюдали при комбинировании с Ab против PD-L1. Снижение дозы STP707 до 1 мг/кг приводило к более низкому эффекту STP707 в отдельности, но в этом случае становится более очевидной его аддитивность с Ab против PD-L1.
По-видимому, комбинация антитела против PD-L1 5 мг/кг и STP705 (20 мкг на инъекцию (1 мг/кг)) являлась более эффективной, чем монотерапия STP705, являющаяся более эффективной, чем антитело против PD-L1 5 мг/кг.
Другие результаты свидетельствовали о том, что STP707 усиливали действие антитела против PD-L1, что приводило к значительному снижению жизнеспособности опухоли без возвращения опухолевых клеток даже после прекращения введения на 2+ недели. То, что авторы настоящего изобретения продемонстрировали доставку в печень с использованием этого состава, вводимого IV, позволяет авторам настоящего изобретения предполагать, что можно лечить опухоли, находящиеся в печени, с использованием этой схемы лечения. Это будет включать любые опухоли, от природы возникающие в печени (гепатобластома или печеночноклеточная карцинома (HCC)) или опухоли, метастазирующие в печень (например, рак толстого кишечника).
Кроме того, в предыдущих исследованиях авторы настоящего изобретения показали возможность снижения экспрессия этих 2 генов-мишеней, если продукт вводят посредством инъекции (например, внутрикожно). Это позволяет авторам настоящего изобретения предполагать возможность достижения той же терапевтической пользы от стимуляции иммунного ответа в опухолях, когда продукт вводят посредством инъекции вблизи опухоли. Это можно использовать для рака кожи (например, немеланомного рака кожи или меланомных опухолей кожи) или в опухолях в других органах, где материал можно инъецировать вблизи очага опухоли для стимуляции того же эффекта.
ССЫЛКИ
[1] Liu et al., Cancer Cell Int (2015) 15:106-112 "Cyclooxygenase-2 promotes tumor growth and suppresses tumor immunity"
[2] Zelenay et al., Cell (2015) 162: 1257-1270 "Cyclooxygenase-Dependent Tumor Growth through Evasion of Immunity"
[3] Mariathasan et al., Nature (2018) 554; 544-548 "TGFβ attenuates tumour response to PD-L1blockade by contributing to exclusion of T cells"
Все публикации, указанные в настоящем описании, включая выданные патенты и опубликованные патентные заявки, и все записи в базах данных, указанные с адресами URL или регистрационными номерами, включены в настоящее описание в качестве ссылок в полном объеме.
Хотя настоящее изобретение описано в отношении некоторых вариантов осуществления, и многие подробности приведены в иллюстративных целях, специалистам в этой области очевидно, что возможны дополнительные варианты осуществления изобретения, и что некоторые подробности, представленные в настоящем описании, могут варьироваться без отклонения от основных принципов изобретения.
--->
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> SIPHKOMICS, INC.
<120> САЙЛЕНСИНГ TGF-БЕТА 1 И COX-2 С ИСПОЛЬЗОВАНИЕМ МИРНК, ДОСТАВЛЯЕМОЙ В
ПОЛИПЕПТИДНОЙ НАНОЧАСТИЦЕ, В ОТДЕЛЬНОСТИ И В КОМБИНАЦИИ С ИНГИБИТОРАМИ
ИММУННЫХ КОНТРОЛЬНЫХ ТОЧЕК ДЛЯ ЛЕЧЕНИЯ ЗЛОКАЧЕСТВЕННОГО НОВООБРАЗОВАНИЯ
<130> 4690.0016I
<140> PCT/US2019/068499
<141> 2019-12-24
<150> 62/785,647
<151> 2018-12-27
<160> 34
<170> PatentIn version 3.5
<210> 1
<211> 25
<212> РНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический олигонуклеотид
<400> 1
ggauccacga gcccaagggc uacca 25
<210> 2
<211> 25
<212> РНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический олигонуклеотид
<400> 2
ugguagcccu ugggcucgug gaucc 25
<210> 3
<211> 25
<212> РНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический олигонуклеотид
<400> 3
cccaagggcu accaugccaa cuucu 25
<210> 4
<211> 25
<212> РНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический олигонуклеотид
<400> 4
agaaguuggc augguagccc uuggg 25
<210> 5
<211> 25
<212> РНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический олигонуклеотид
<400> 5
gagcccaagg gcuaccaugc caacu 25
<210> 6
<211> 25
<212> РНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический олигонуклеотид
<400> 6
aguuggcaug guagcccuug ggcuc 25
<210> 7
<211> 25
<212> РНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический олигонуклеотид
<400> 7
gauccacgag cccaagggcu accau 25
<210> 8
<211> 25
<212> РНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический олигонуклеотид
<400> 8
augguagccc uugggcucgu ggauc 25
<210> 9
<211> 25
<212> РНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический олигонуклеотид
<400> 9
cacgagccca agggcuacca ugcca 25
<210> 10
<211> 25
<212> РНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический олигонуклеотид
<400> 10
uggcauggua gcccuugggc ucgug 25
<210> 11
<211> 25
<212> РНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический олигонуклеотид
<400> 11
gaggucaccc gcgugcuaau ggugg 25
<210> 12
<211> 25
<212> РНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический олигонуклеотид
<400> 12
ccaccauuag cacgcgggug accuc 25
<210> 13
<211> 25
<212> РНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический олигонуклеотид
<400> 13
guacaacagc acccgcgacc gggug 25
<210> 14
<211> 25
<212> РНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический олигонуклеотид
<400> 14
cacccggucg cgggugcugu uguac 25
<210> 15
<211> 25
<212> РНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический олигонуклеотид
<400> 15
guggauccac gagcccaagg gcuac 25
<210> 16
<211> 25
<212> РНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический олигонуклеотид
<400> 16
guagcccuug ggcucgugga uccac 25
<210> 17
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический пептид
<400> 17
Lys His His His Lys His His His Lys His His His Lys His His His
1 5 10 15
Lys
<210> 18
<211> 18
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический пептид
<400> 18
Lys His His His Lys His His His Lys His His His His Lys His His
1 5 10 15
His Lys
<210> 19
<211> 25
<212> РНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический олигонуклеотид
<400> 19
ggucuggugc cuggucugau gaugu 25
<210> 20
<211> 25
<212> РНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический олигонуклеотид
<400> 20
acaucaucag accaggcacc agacc 25
<210> 21
<211> 25
<212> РНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический олигонуклеотид
<400> 21
gagcaccauu cuccuugaaa ggacu 25
<210> 22
<211> 25
<212> РНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический олигонуклеотид
<400> 22
aguccuuuca aggagaaugg ugcuc 25
<210> 23
<211> 25
<212> РНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический олигонуклеотид
<400> 23
ccucaauuca gucucucauc ugcaa 25
<210> 24
<211> 25
<212> РНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический олигонуклеотид
<400> 24
uugcagauga gagacugaau ugagg 25
<210> 25
<211> 25
<212> РНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический олигонуклеотид
<400> 25
gauguuugca uucuuugccc agcac 25
<210> 26
<211> 25
<212> РНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический олигонуклеотид
<400> 26
gugcugggca aagaaugcaa acauc 25
<210> 27
<211> 25
<212> РНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический олигонуклеотид
<400> 27
gucuuugguc uggugccugg ucuga 25
<210> 28
<211> 25
<212> РНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический олигонуклеотид
<400> 28
ucagaccagg caccagacca aagac 25
<210> 29
<211> 25
<212> РНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический олигонуклеотид
<400> 29
gugccugguc ugaugaugua ugcca 25
<210> 30
<211> 25
<212> РНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический олигонуклеотид
<400> 30
uggcauacau caucagacca ggcac 25
<210> 31
<211> 25
<212> РНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический олигонуклеотид
<400> 31
caccauucuc cuugaaagga cuuau 25
<210> 32
<211> 25
<212> РНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический олигонуклеотид
<400> 32
auaaguccuu ucaaggagaa uggug 25
<210> 33
<211> 25
<212> РНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический олигонуклеотид
<400> 33
caauucaguc ucucaucugc aauaa 25
<210> 34
<211> 25
<212> РНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический олигонуклеотид
<400> 34
uuauugcaga ugagagacug aauug 25
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБЫ ТЕРАПИИ НА ОСНОВЕ CAR Т-КЛЕТОК С ПОВЫШЕННОЙ ЭФФЕКТИВНОСТЬЮ | 2016 |
|
RU2788131C2 |
| ИММУНОТЕРАПИЯ РАКА | 2014 |
|
RU2744194C2 |
| КОМПОЗИЦИИ И СПОСОБЫ ЛЕЧЕНИЯ ИНФЕКЦИЙ И ОПУХОЛЕЙ | 2007 |
|
RU2540490C2 |
| ИНГИБИТОРЫ ПУТИ IL-4/IL-13 ДЛЯ ПОВЫШЕННОЙ ЭФФЕКТИВНОСТИ ПРИ ЛЕЧЕНИИ ЗЛОКАЧЕСТВЕННЫХ НОВООБРАЗОВАНИЙ | 2020 |
|
RU2836467C2 |
| СПОСОБЫ ЛЕЧЕНИЯ КОЛОРЕКТАЛЬНОГО РАКА | 2014 |
|
RU2674147C2 |
| ТЕРАПЕВТИЧЕСКИЕ КОМПОЗИЦИИ И СПОСОБЫ ПРОТИВ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ С МОЛЕКУЛАМИ РНКИ, НАПРАВЛЕННЫМИ ПРОТИВ HSP47 | 2015 |
|
RU2756253C2 |
| ЛЕЧЕНИЕ ЗАБОЛЕВАНИЙ, СВЯЗАННЫХ С ГЕНОМ РАЗВИТИЯ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ, ПУТЕМ ИНГИБИРОВАНИЯ ПРИРОДНОГО АНТИСМЫСЛОВОГО ТРАНСКРИПТА К ГЕНУ РАЗВИТИЯ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ | 2011 |
|
RU2612161C2 |
| КОМПОЗИЦИИ И СПОСОБЫ ЛЕЧЕНИЯ ИНФЕКЦИЙ И ОПУХОЛЕЙ | 2007 |
|
RU2478400C2 |
| СПОСОБЫ ЛЕЧЕНИЯ РАКА С ИСПОЛЬЗОВАНИЕМ АНТАГОНИСТОВ, СВЯЗЫВАЮЩИХ С ОСЬЮ PD-1, И ИНГИБИТОРОВ TIGIT | 2014 |
|
RU2825390C2 |
| АНТИТЕЛА ПРОТИВ 4-1BB ЧЕЛОВЕКА И ИХ ПРИМЕНЕНИЕ | 2018 |
|
RU2725811C1 |

Изобретение относится к области медицины и фармацевтики, а именно к способу уничтожения злокачественных клеток у индивидуума, включающему введение индивидууму терапевтически эффективного количества комбинации миРНК против TGF-бета 1 и миРНК против Cox-2, где комбинацию вводят вместе с ингибитором иммунных контрольных точек для лечения злокачественного новообразования. Технический результат заключается в лечении злокачественного новообразования с применением молекул миРНК, ингибирующих TGF-бета 1 и Cox-2, в комбинации с ингибитором иммунных контрольных точек. 27 з.п. ф-лы, 8 ил., 2 табл., 1 пр.
1. Способ уничтожения злокачественных клеток у индивидуума, включающий введение индивидууму терапевтически эффективного количества комбинации миРНК против TGF-бета 1 и миРНК против Cox-2, где комбинацию вводят вместе с ингибитором иммунных контрольных точек для лечения злокачественного новообразования.
2. Способ по п. 1, где комбинацию вводят внутривенно индивидууму.
3. Способ по п. 1, где злокачественные клетки составляют злокачественную опухоль и комбинацию вводят в опухоль или вблизи опухоли.
4. Способ по любому из пп. 1-3, где злокачественное новообразование включает рак печени.
5. Способ по п. 4, где рак печени включает первичный рак печени.
6. Способ по п. 5, где первичный рак печени включает печеночноклеточную карциному или гепатобластому.
7. Способ по п. 4, где злокачественное новообразование метастазировало в печень из другой ткани организма индивидуума.
8. Способ по п. 7, где метастазирующее злокачественное новообразование включает рак толстого кишечника.
9. Способ по любому из пп. 1-8, где миРНК против TGF-бета 1 выбирают из группы, состоящей из SEQ ID NO: 1-16.
10. Способ по любому из пп. 1-9, где миРНК против TGF-бета 1 содержит последовательности: смысловую: 5’-cccaagggcuaccaugccaacuucu-3’ (SEQ ID NO: 3); антисмысловую: 5’-agaaguuggcaugguagcccuuggg-3’ (SEQ ID NO: 4).
11. Способ по любому из пп. 1-10, где комбинацию вводят в фармацевтически приемлемом носителе.
12. Способ по п. 11, где фармацевтически приемлемый носитель содержит разветвленный гистидин-лизиновый полимер.
13. Способ по п. 12, где разветвленный гистидин-лизиновый полимер образует наночастицу с комбинацией.
14. Способ по п. 12 или 13, где разветвленный гистидин-лизиновый полимер имеет формулу (R)K(R)-K(R)-(R)K(X), где R=KHHHKHHHKHHHKHHHK (SEQ ID NO: 17) или R=KHHHKHHHKHHHHKHHHK (SEQ ID NO: 18), X=C(O)NH2, K=лизин, H=гистидин.
15. Способ по п. 13 или 14, где наночастицу вводят индивидууму внутривенно.
16. Способ по любому из пп. 1-12, где миРНК против Cox-2 выбирают из группы, состоящей из SEQ ID NO: 19-24.
17. Способ по п. 16, где миРНК против Cox-2 содержит последовательности: смысловую: 5’-ggucuggugccuggucugaugaugu-3’ (SEQ ID NO: 19); антисмысловую: 5’-acaucaucagaccaggcaccagacc-3’ (SEQ ID NO: 20).
18. Способ по п. 17, где разветвленный гистидин-лизиновый полимер образует наночастицу с комбинацией.
19. Способ по п. 17 или 18, где разветвленный гистидин-лизиновый полимер имеет формулу (R)K(R)-K(R)-(R)K(X), где R=KHHHKHHHKHHHKHHHK (SEQ ID NO: 17) или R=KHHHKHHHKHHHHKHHHK (SEQ ID NO: 18), X=C(O)NH2, K=лизин, H=гистидин.
20. Способ по п. 18 или 19, где наночастицу вводят индивидууму внутривенно.
21. Способ по любому из пп. 1-20, где ингибитор иммунных контрольных точек включает моноклональное антитело.
22. Способ по п. 21, где моноклональное антитело блокирует взаимодействие между рецепторами на клетке индивидуума, выбранными из группы, состоящей из PD-1, PD-L1, CTLA4, Lag3 и Tim3, и лигандами этих рецепторов.
23. Способ по п. 21, где моноклональное антитело представляет собой моноклональное антитело к PD1 или PDL1.
24. Способ по п. 21, где моноклональное антитело выбирают из группы, состоящей из атезолизумаба, дурвалумаба, ниволумаба, пембролизумаба и ипилимумаба.
25. Способ по любому из пп. 1-24, где ингибитор иммунных контрольных точек включает низкомолекулярное соединение.
26. Способ по п. 25, где низкомолекулярное соединение блокирует взаимодействие между рецепторами на клетке индивидуума, выбранными из группы, состоящей из PD-1, PD-L1, CTLA4, Lag3 и Tim3, и лигандами этих рецепторов.
27. Способ по п. 25, где низкомолекулярное соединение блокирует связывание между PD1 и PDL1.
28. Способ по п. 25, где низкомолекулярное соединение представляет собой BMS202.
| WO 2018175323 A1, 27.09.2018 | |||
| WO 2004009769 A2, 29.01.2004 | |||
| WO 2018064611 A1, 05.04.2018 | |||
| FUTAMI K | |||
| et al | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Станок для изготовления деревянных ниточных катушек из цилиндрических, снабженных осевым отверстием, заготовок | 1923 |
|
SU2008A1 |
| - Vol | |||
| Прибор, замыкающий сигнальную цепь при повышении температуры | 1918 |
|
SU99A1 |
| - No | |||
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| - P | |||
| Цинковальный котел | 1920 |
|
SU1227A1 |
| DENG H | |||
| et al | |||
| The application of nanotechnology in immune checkpoint blockade for cancer treatment // | |||
Авторы
Даты
2023-06-06—Публикация
2019-12-24—Подача