Изобретение относится к области генной инженерии и биотехнологии, а именно к направляющим РНК, которые могут быть использованы в системах CRISPR-Cas12 в составе рибонуклеопротеиновых комплексов для выявления (обнаружения, детекции) РНК вируса гепатита С генотипов 1b и 3а, а также к способам получения препаратов рибонуклеопротеинового комплекса CRISPR-Cas и к самим препаратам.
Изобретение позволяет in vitro выявлять единичные копии РНК вируса гепатита С генотипов 1b и 3а.
Направляющие РНК, описанные в настоящей заявке, могут быть использованы для детекции РНК вируса гепатита С генотипов 1b и 3а после проведения специфической амплификации фрагмента генома вируса гепатита С генотипов 1b и 3а. Амплификация при этом может быть проведена различными способами, среди которых полимеразная цепная реакция (PCR); петлевая изотермическая амплификация (LAMP); геликаза-зависимая амплификация (HDA); рекомбиназа-опосредованная амплификация (RPA); амплификация со смещением цепи (SDA); амплификация, основанная на последовательности нуклеиновых кислот (NASBA); опосредованная транскрипцией амплификация (ТМА); амплификация, опосредованная никирующим ферментом (NEAR); круговая амплификация (RCA) и многие другие виды амплификации.
Направляющие РНК, описанные в настоящей заявке, могут быть использованы для разработки высокочувствительных и высокотехнологичных диагностических систем нового поколения на основе CRISPR технологий для совершенствования методов диагностики инфекционных заболеваний.
Для решения эпидемиологических задач по расшифровке вспышек инфекционных болезней, выявления и идентификации возбудителя, а также детекции специфических бактериальных и вирусных генов необходимы разработка и внедрение в практику работы надзорных и мониторинговых служб современных технологий молекулярной эпидемиологии. Одной из таких технологий является использование элементов генетического редактирования системы CRISPR-Cas. Данная технология развивается достаточно эффективно в отношении создания средств лечения некоторых болезней, несмотря на ряд трудностей, связанных с возникновением непредвиденных мутаций. При углубленных исследованиях в области применения CRISPR-Cas системы, было выяснено, что она может быть использована для тонких диагностических процедур при выявлении возбудителя/ей инфекции у человека, а также их генотипирования.
В 2018 г. было показано, что один из ферментов CRISPR системы - Cas12 после распознавания своей целевой ДНК-мишени начинает неспецифически гидролизовать одноцепочечную ДНК. Такое свойство Cas12 можно использовать в качестве индикатора присутствия определенной мишени, например, генома вируса или бактерии. Исследователи использовали это открытие для создания технологической платформы обнаружения нуклеиновых кислот, известной как DETECTR (DNA Endonuclease Targeted CRISPR Trans Reporter - ДНК-нацеленная эндонуклеаза CRISPR трансрепортер). Предложенная платформа объединяет нуклеазу Cas12a, ее направляющую РНК, специфичную к нуклеиновой кислоте, и флуоресцентную репортерную молекулу. Впервые технология DETECTR была использована для выявления и генотипирования вируса папилломы человека. DETECTR в течение 1 ч позволила дифференцировать HPV16 и HPV18 в неочищенных экстрактах ДНК из культивируемых клеток человека и клинических образцов. При этом DETECTR корректно (сопоставимо с результатами ПЦР-анализа) идентифицировала HPV16 в 25 и HPV18 - в 23 из 25 клинических образцов [J.S. Chen, E. Ma, L.B. Harrington et al., CRISPR-Cas12a target binding unleashes indiscriminate single-stranded DNase activity, Science 360(6387) (2018) 436-9, doi: 10.1126/science.aar6245].
He менее важным приложением системы CRISPR-Cas является идентификация патогенов и детекция специфических бактериальных генов с помощью платформы SHERLOCK (specific high-sensitivity enzymatic reporter unlocking - ферментативная специфическая высокочувствительная разблокировка репортера). Предложенная платформа объединяет нуклеазу Cas13a, ее направляющую РНК, специфичную к нуклеиновой кислоте, и флуоресцентную репортерную молекулу. Комплекс Cas13a связывает и расщепляет предварительно амплифицированную нуклеиновую кислоту-мишень с высокой специфичностью. С помощью SHERLOCK удалось корректно дифференцировать близкородственные штаммы вируса Зика и Денге [J.S. Gootenberg, О.О. Abudayyeh, J.W. Lee et al., Nucleic acid detection with CRISPR-Cas13a/C2c2, Science 356(6336) (2017) 438-42, doi: 10.1126/science.aam9321].
SHERLOCK была усовершенствована (SHERLOCKv2) и позволила выявлять в одном анализе до 4 мишеней. Мультиплексирование было достигнуто путем объединения нескольких нуклеаз Cas13 и нуклеазы Cas12 со специфичными флуоресцентными репортерными комплексами, которые обеспечивали детекцию сигнала на разных длинах волн. Количественное обнаружение было достигнуто путем оптимизации концентраций олигонуклеотидов, используемых на этапе предварительной амплификации, чтобы входной сигнал и интенсивность сигнала тесно коррелировали в широком диапазоне концентраций образца. Повышенная чувствительность была достигнута путем добавления Csm6 для увеличения интенсивности расщепления флуоресцентного репортера. Стоит отметить, что SHERLOCKv2 является портативным анализом за счет того, что обнаружение показаний флуоресценции в предложенной технологии заменено на визуальную детекцию на тест-полосках [J.S. Gootenberg, О.О. Abudayyeh, M.J. Kellner et al., Multiplexed and portable nucleic acid detection platform with Cas13, Cas12a, and Csm6, Science 360(6387) (2018) 439-44, doi: 10.1126/science.aaq0179].
На основе SHERLOCK была разработана технология HUDSON (heating unextracted diagnostic samples to obliterate nucleases - нагревание неэкстрагированных диагностических образцов для уничтожения нуклеаз), которая устраняет необходимость в экстракции нуклеиновых кислот и позволяет обнаруживать патогены непосредственно в биологических образцах пациента (образец крови, сыворотки или плазмы крови, клеток крови, слюны, мокроты, лимфоидных тканей, тканей кроветворных органов и других биологических материалов). В HUDSON нагревание и химическое восстановление инактивируют нуклеазы, присутствующие в высоких концентрациях в биологических образцах пациента, после чего вирусные частицы лизируются, высвобождая нуклеиновые кислоты в раствор. HUDSON позволяет в течение 2 ч с высокой чувствительностью обнаружить вирус Денге в образцах цельной крови, сыворотки и слюны пациентов. Кроме того, HUDSON позволяет дифференцировать четыре серотипами вируса Денге и выявлять 6 наиболее распространенных мутаций обратной транскриптазы ВИЧ [С. Myhrvold, С.А. Freije, J.S. Gootenberg et al., Field-deployable viral diagnostics using CRISPR-Cas13, Science 360(6387) (2018) 444-8, doi: 10.1126/science.aas8836].
В связи с этим крайне актуальной является задача разработки новых эффективных методик выявления нуклеиновых кислот возбудителей инфекционных заболеваний, основанных на генетических технологиях, таких как CRISPR-Cas.
Из уровня техники известны научные статьи, описывающие обнаружение 5×109 копий РНК вируса гепатита С с помощью CRISPR-Cas12a без стадии предварительной амплификации [Nguyen, L.Т., Smith, В.М., & Jain, Р.K. (2020). Enhancement of trans-cleavage activity of Cas12a with engineered crRNA enables amplified nucleic acid detection. Nature communications, 11(1), 4906. https://doi.org/10.1038/s41467-020-18615-1]. Также известны решения, описывающие выявление 7,55×105 копий РНК вируса гепатита С с применением CRISPR-Cas12a и предварительной амплификации методом петлевой изотермической амплификации [Kham-Kjing, N., Ngo-Giang-Huong, N., Tragoolpua, K., Khamduang, W., & Hongjaisee, S. (2022). Highly Specific and Rapid Detection of Hepatitis С Virus Using RT-LAMP-Coupled CRISPR-Cas12 Assay. Diagnostics (Basel, Switzerland), 12(7), 1524. https://doi.org/10.3390/diagnostics12071524].
Кроме того, известны научные статьи, в которых описана разработка и получение направляющих РНК CRISPR-Cas13 для терапии инфекций, вызванных вирусом гепатита С [Ashraf, M.U., Salman, H.M., Khalid, M.F., Khan, M., Anwar, S., Afzal, S., Idrees, M., & Chaudhary, S.U. (2021). CRISPR-Cas13a mediated targeting of hepatitis С virus internal-ribosomal entry site (IRES) as an effective antiviral strategy. Biomedicine & pharmacotherapy=Biomedecine & pharmacotherapie, 136, 111239. https://doi.org/10.1016/j.biopha.2021.111239].
Из уровня техники известны: мультиплексная диагностика на основе эффекторной системы CRISPR [Заявка на патент на изобретение RU 2020124203, дата подачи 20.12.2018]; РНК-проводник St10 для использования в высокоспецифической системе нуклеаз Streptococcus thermophilus CRISPR/Cas9 (StCas9) и применение указанного РНК-проводника и белка StCas9 для подавления экспрессии вируса гепатита В в клетке-хозяине и для элиминации вирусной ДНК из клетки-хозяина [патент RU 2694396, дата приоритета 14.12.2018, дата регистрации 12.07.2019]; новые ферменты CRISPR и системы [патент RU 2771826, дата приоритета по заявке 2018101732 от 17.06.2016, опубликовано 12.05.2022]. Из перечисленных выше материалов ни один нельзя отнести к ближайшим аналогам настоящего изобретения в виду того, что направляющие РНК, описанные в настоящей заявке, предназначены для разработки высокочувствительных и высокотехнологичных диагностических систем нового поколения на основе CRISPR технологий для совершенствования методов диагностики инфекционных заболеваний.
Ближайшими аналогами заявляемого решения являются изобретения по патентам RU 2782700 (дата приоритета 27.12.2021), RU 2782951 (дата приоритета 27.12.2021), заявка на патент №2021139116 (дата подачи 27.12.2021), направленные на получение направляющих РНК, предназначенных для разработки высокочувствительных и высокотехнологичных диагностических систем нового поколения для выявления ДНК вируса гепатита В на основе CRISPR технологий. Однако, для расширения спектра подобных диагностических систем и совершенствования методов диагностики инфекционных заболеваний и эпидемиологического надзора необходимо разрабатывать новые методы для выявления нуклеиновых кислот вирусов, вызывающих инфекционные заболевания человека.
Исходя из вышеизложенного, возникает техническая проблема, заключающаяся в необходимости разработки и получения направляющих РНК для выявления единичных копий РНК вируса гепатита С генотипов 1b и 3а, in vitro.
Предложенная технология перспективна для разнообразных применений, включая количественное определение ДНК/РНК, быструю мультиплексную детекцию экспрессии, другие виды чувствительной детекции, например, выявление загрязнения образцов нуклеиновыми кислотами. Технология основанная на CRISPR-Cas является многофункциональной, устойчивой к ошибкам технологией детекции ДНК, пригодной для быстрой постановки диагнозов, включая инфекционные заболевания, и генотипирования инфекционных агентов и выявление генов антибиотикоустойчивости и генов, кодирующих экзотоксины, бактериальных патогенов.
Применение предложенной технологии делает возможным создание диагностических систем нового поколения, которые будут обладать следующими свойствами:
• высокая чувствительность;
• возможность проведения диагностики у постели больного;
• возможность проведения диагностики в полевых условиях без применения специализированного высокотехнологичного оборудования;
• скорость и простота анализа;
• сниженная стоимость анализа;
• отсутствие необходимости оснащения диагностической лаборатории дорогостоящим оборудованием;
• отсутствие необходимости проведения выделения нуклеиновых кислот возбудителя.
Изобретение относится к новым средствам - направляющим РНК, которые могут быть использованы в системах CRISPR-Cas12 для ультрачувствительного выявления, идентификации, обнаружения или детекции РНК вируса гепатита С генотипов 1b и 3а в биологических образцах.
Технической задачей предложенного изобретения является разработка новых средств - направляющих РНК, которые могут быть использованы в системах CRISPR-Cas12 с белками Cas12, например, LbCpf1 из Lachnospiraceae, для ультрачувствительного выявления РНК вируса гепатита С генотипов 1b и 3а.
При осуществлении настоящего изобретения, согласно приведенной в формуле изобретения совокупности существенных признаков, достигается неожиданный технический результат - возможность ультрачувствительного выявления РНК вируса гепатита С генотипов 1b и 3а до единичных копий в одной реакции. Изобретение обеспечивает повышение эффективности выявления РНК вируса гепатита С генотипов 1b и 3а до 5 раз. Также предложенное изобретение позволяет увеличить выход продукта реакции, получив желаемую концентрацию финального препарата направляющей РНК, и обеспечивает формирование корректной конформации шпильки, содержащейся в направляющей РНК.
Технический результат достигается за счет:
• разработки молекул направляющих РНК, которые могут быть использованы в системах CRISPR-Cas12 для ультра чувствительного выявления РНК вируса гепатита С генотипов 1b и 3а, где указанные направляющие РНК выбраны из последовательностей SEQ ID NO: 1-5, способны связываться с целевыми высоко консервативными участками генома вируса гепатита С генотипов 1b и 3а, содержат РНК-шпильку, которая распознается РНК-направляемой ДНК-эндонуклеазой LbCpf1 из Lachnospiraceae, с обеспечением выявления единичных копий РНК вируса гепатита С генотипов 1b и 3а.
• применения РНК-направляемой ДНК-эндонуклеаз LbCpf1 из Lachnospiraceae, полученной согласно способу, разработанному авторами ранее (Патент RU №2707542, дата приоритетат 28.03.2019), для создания рибонуклеопротеиновых комплексов (РПК) системы CRISPR-Cas, пригодных для детекции РНК вируса гепатита С генотипов 1b и 3а в ультра низких концентрациях (единичные копии).
• разработки набора специфических олигонуклеотидов, выбранных из SEQ ID NO: 6-11, для предварительной амплификации фрагмента генома вируса гепатита С генотипов 1b и 3а.
• оптимизации условий проведения предварительной амплификации фрагмента генома вируса гепатита С генотипов 1b и 3а.
• определения условий проведения ультрачувствительной детекции РНК вируса гепатита С генотипов 1b и 3а и установления последовательности стадий метода.
Направляющие РНК согласно настоящему изобретению соответствуют высоко консервативным фрагментам генома вируса гепатита С генотипов 1b и 3а. Наиболее предпочтительны направляющие РНК, распознающиеся РНК-направляемой ДНК-эндонуклеазой LbCpf1 из Lachnospiraceae, характеризующиеся, имеющие или содержащие нуклеотидную последовательность, выбранную из:
• SEQ ID NO: 1;
• SEQ ID NO: 2;
• SEQ ID NO: 3;
• SEQ ID NO: 4;
• SEQ ID NO: 5;
• или идентичной любой из них по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99%,
• или комплементарной любой из них,
• или гибридизующейся с любой из них в строгих условиях.
Специфические олигонуклеотиды для проведения предварительной амплификации фрагмента генома вируса гепатита С генотипов 1b и 3а согласно настоящему изобретению соответствуют высоко консервативному участку генома вируса гепатита С генотипов 1b и 3а. Наиболее предпочтительны олигонуклеотиды, характеризующиеся, имеющие или содержащие нуклеотидную последовательность, выбранную из:
• SEQ ID NO: 6;
• SEQ ID NO: 7;
• SEQ ID NO: 8;
• SEQ ID NO: 9;
• SEQ ID NO: 10;
• SEQ ID NO: 11;
• или идентичной любой из них по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99%,
• или комплементарной любой из них,
• или гибридизующейся с любой из них в строгих условиях.
Согласно предложенному изобретению получают рибонуклеопротеиновые комплексы (РПК), состоящие из по меньшей мере одной направляющей РНК и РНК-направляемой ДНК-нуклеазы системы CRISPR-Cas LbCpf1 из Lachnospiraceae, пригодные для использования для выявления РНК вируса гепатита С генотипов 1b и 3а в ультранизких концентрациях (единичные копии).
Препараты РПК представляют собой растворы, содержащие направляющую РНК, выбранную из SEQ ID NO: 1-5, объединенную с белком системы CRISPR-Cas (LbCpf1 из Lachnospiraceae) или лиофильно высушенные РПК.
Полученные направляющие РНК могут быть использованы в составе набора для обнаружения РНК вируса гепатита С генотипов 1b и 3а с инструкцией по применению.
Набор может дополнительно включать компоненты для проведения предварительной амплификации высококонсервативного фрагмента генома вируса гепатита С генотипов 1b и 3а, в том числе один или несколько специфических олигонуклеотидов, выбранных из SEQ ID NO: 6-11. При этом по меньшей мере одна направляющая РНК в составе набора может находиться в комплексе с белком системы CRISPR-Cas (LbCpf1 из Lachnospiraceae) в одном контейнере или отдельно в разных контейнерах.
Способ получения препарата рибонуклеопротеинового комплекса CRISPR-Cas предусматривает:
(i) синтез направляющей РНК с SEQ ID NO: 1-5,
(ii) объединение Cas-белка семейства CRISPR-Cas LbCpf1 из Lachnospiraceae, в комплекс с по меньшей мере одной направляющей РНК, полученной на стадии (i), и при необходимости
(iii) лиофильную сушку рибонуклеопротеинового комплекса CRISPR-Cas, полученного на стадии (ii),
с получением, таким образом, препарата рибонуклеопротеинового комплекса CRISPR-Cas.
В предложенном способе синтез направляющих РНК может быть проведен методом in vitro транскрипции с последующим переосаждением продуктов реакции in vitro транскрипции из реакционной смеси добавлением хлорида натрия до конечной концентрации 400 mM и равного объема изопропилового спирта.
Также предложенный способ предусматривает непосредственно перед объединением с Cas-белком прогрев направляющей РНК при 90°С в течение 5 минут и позволяют медленно остыть до комнатной температуры, что обеспечивает формирование корректной конформации шпильки, содержащейся в направляющей РНК.
Предложен препарат рибонуклеопротеинового комплекса CRISPR-Cas для выявления РНК вируса гепатита С генотипов 1b и 3а, который может быть получен раскрытым в настоящей заявке способом. Препарат содержит Cas-белок семейства CRISPR-Cas LbCpf1 из Lachnospiraceae в комплексе с по меньшей мере одной направляющей РНК с SEQ ID NO: 1-5.
Препарат может быть представлен как в жидкой форме - раствора указанного рибонуклеопротеинового комплекса CRISPR-Cas, так и в виде лиофилизата лиофильно высушенного порошка указанного рибонуклеопротеинового комплекса CRISPR-Cas.
Предложенная технология позволяет определить единичные копии РНК вируса гепатита С генотипов 1b и 3а в биологических образцах пациента, выбранных из жидкости и/или ткани, предположительно содержащих вирус гепатита С генотипов 1b и 3а. Биологическим образцом может быть образец крови, сыворотки или плазмы крови, клеток крови, слюны, мокроты, лимфоидных тканей, тканей кроветворных органов и других биологических материалов от пациента, которые могут быть использованы для анализа на наличие РНК вируса гепатита С генотипов 1b и 3а.
Краткое описание чертежей
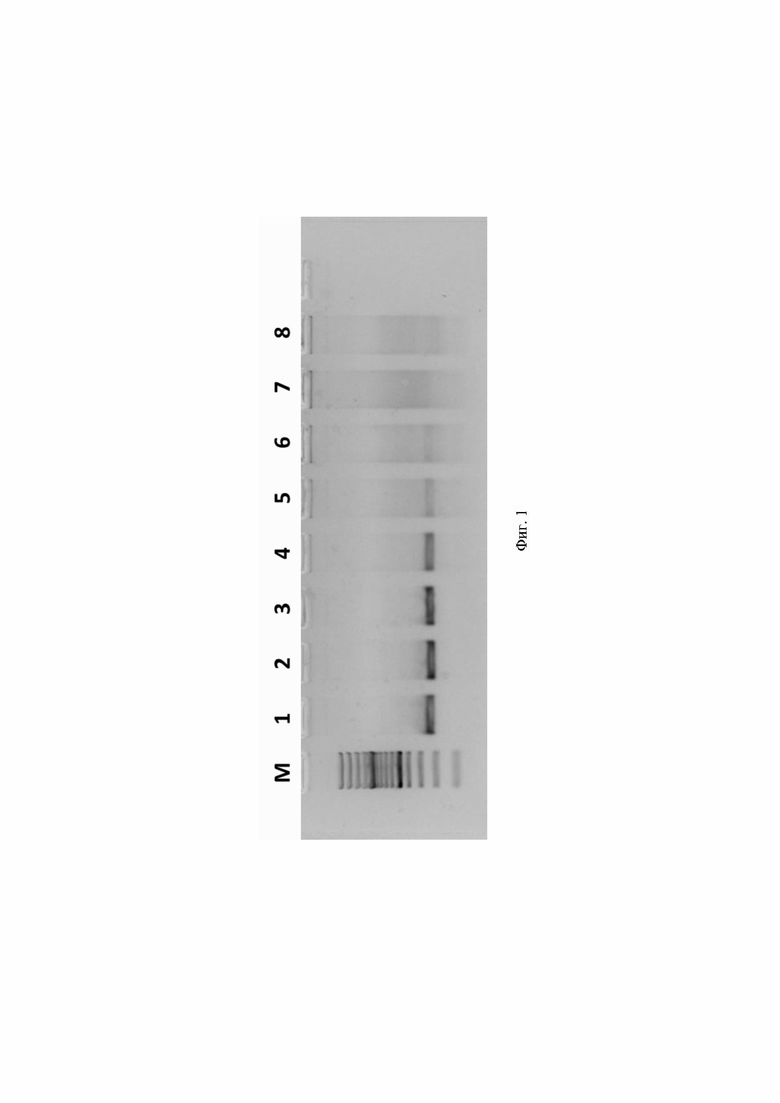
Фиг. 1. Визуализация амплифицированного фрагмента HCV 1b генома вируса гепатита С (размером 226 п.о.) после предварительной амплификации с использованием олигонуклеотидов 555_for_1 score 12 и 555_1_rev score 10 при помощи электрофореза в агарозном геле, где цифрами 1-8 обозначены:
1 - Продукт, полученный в ходе амплификации 2,3×106 копий модельной матрицы pGEM-T-HCV 1b;
2 - Продукт, полученный в ходе амплификации 2,3×105 копий модельной матрицы pGEM-T-HCV 1b;
3 - Продукт, полученный в ходе амплификации 2,3×104 копий модельной матрицы pGEM-T-HCV 1b;
4 - Продукт, полученный в ходе амплификации 2300 копий модельной матрицы pGEM-T-HCV 1b;
5 - Продукт, полученный в ходе амплификации 230 копий модельной матрицы pGEM-T-HCV 1b;
6 - Продукт, полученный в ходе амплификации 23 копии модельной матрицы pGEM-T-HCV 1b;
7 - Продукт, полученный в ходе амплификации 2,3 копии модельной матрицы pGEM-T-HCV 1b;
8 - отрицательный контроль, не содержащий модельной матрицы pGEM-T-HCV 1b;
М - стандарты молекулярных масс: снизу вверх 100, 200, 300, 400, 500, 600, 700, 800, 900, 1000, 1200, 1500, 2000, 3000 пар нуклеотидов (GeneRuler 100 bp Plus, Thermo Fisher Scientific, США).
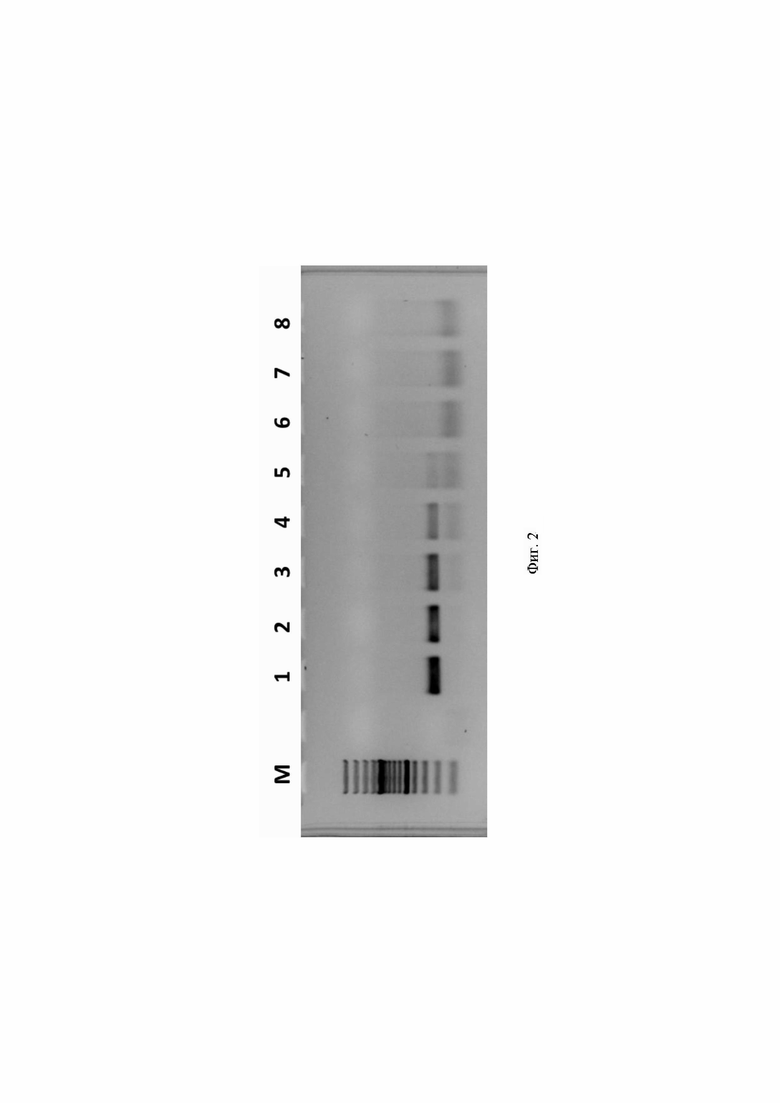
Фиг. 2. Визуализация амплифицированного фрагмента HCV 3а_1 генома вируса гепатита С (размером 210 п.о.) после предварительной амплификации с использованием олигонуклеотидов HCV3a for2 и HCV3a rev2 при помощи электрофореза в агарозном геле, где цифрами 1-8 обозначены:
1 - Продукт, полученный в ходе амплификации 2,3×106 копий модельной матрицы pGEM-T-HCV 3a_1;
2 - Продукт, полученный в ходе амплификации 2,3×105 копий модельной матрицы pGEM-T-HCV 3a_1;
3 Продукт, полученный в ходе амплификации 2,3×104 копий модельной матрицы pGEM-T-HCV 3a_1;
4 - Продукт, полученный в ходе амплификации 2300 копий модельной матрицы pGEM-T-HCV 3a_1;
5 - Продукт, полученный в ходе амплификации 230 копий модельной матрицы pGEM-T-HCV 3a_1;
6 - Продукт, полученный в ходе амплификации 23 копии модельной матрицы pGEM-T-HCV 3a_1;
7 - Продукт, полученный в ходе амплификации 2,3 копии модельной матрицы pGEM-T-HCV 3a_1;
8 - отрицательный контроль, не содержащий модельной матрицы pGEM-T-HCV 3а_1;
M - стандарты молекулярных масс: снизу вверх 100, 200, 300, 400, 500, 600, 700, 800, 900, 1000, 1200, 1500, 2000, 3000 пар нуклеотидов (GeneRuler 100 bp Plus, Thermo Fisher Scientific, США).
Фиг. 3. Визуализация амплифицированного фрагмента HCV 3а_2 генома вируса гепатита С (размером 405 п.о.) после предварительной амплификации с использованием олигонуклеотидов HCV3a for3 и HCV3a rev3 при помощи электрофореза в агарозном геле, где цифрами 1-8 обозначены:
1 - Продукт, полученный в ходе амплификации 2,3×106 копий модельной матрицы pGEM-T-HCV 3а_2;
2 - Продукт, полученный в ходе амплификации 2,3×105 копий модельной матрицы pGEM-T-HCV 3а_2;
3 - Продукт, полученный в ходе амплификации 2,3×104 копий модельной матрицы pGEM-T-HCV 3а_2;
4 - Продукт, полученный в ходе амплификации 2300 копий модельной матрицы pGEM-T-HCV 3а_2;
5 - Продукт, полученный в ходе амплификации 230 копий модельной матрицы pGEM-T-HCV 3а_2;
6 - Продукт, полученный в ходе амплификации 23 копии модельной матрицы pGEM-T-HCV 3а_2;
7 - Продукт, полученный в ходе амплификации 2,3 копии модельной матрицы pGEM-T-HCV 3а_2;
8 - отрицательный контроль, не содержащий модельной матрицы pGEM-T-HCV 3а_2;
M - стандарты молекулярных масс: снизу вверх 100, 200, 300, 400, 500, 600, 700, 800, 900, 1000, 1200, 1500, 2000, 3000 пар нуклеотидов (GeneRuler 100 bp Plus, Thermo Fisher Scientific, США).
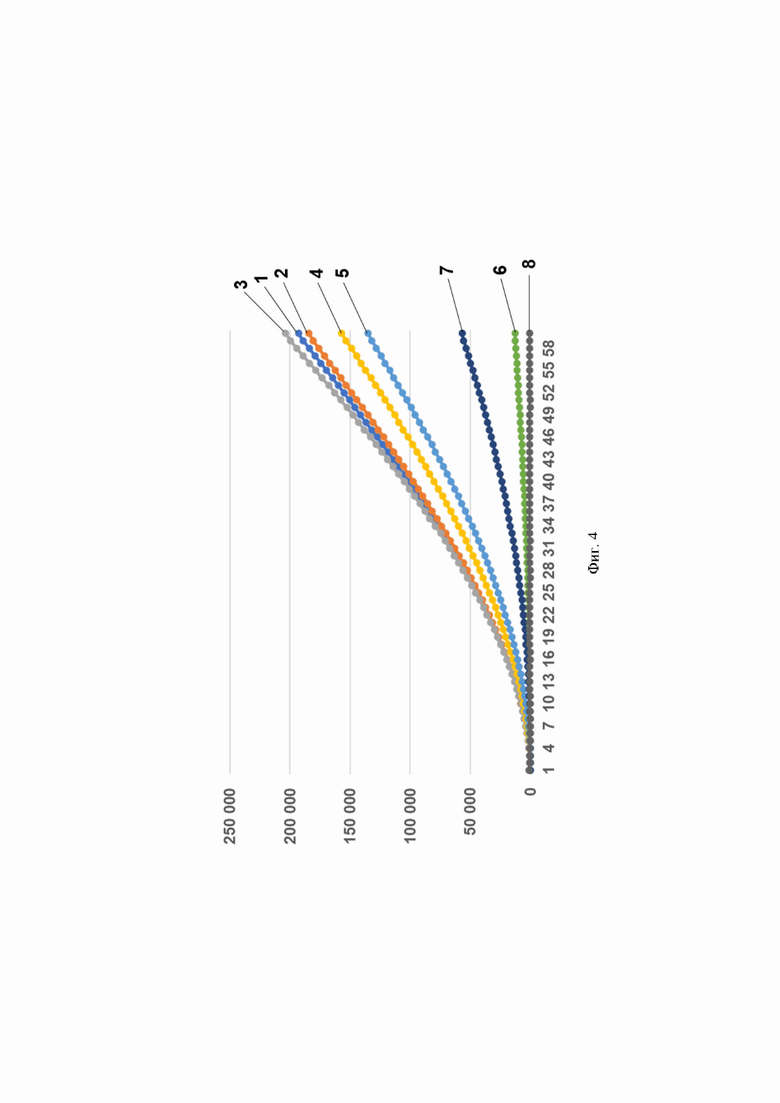
Фиг. 4. Профиль флуоресценции в реальном времени для предварительно амплифицированной мишени HCV 1b генома вируса гепатита С, обработанной рибонуклеопортеиновым комплексом, содержащим направляющую РНК crRNA HCV 1b №147 и белок LbCpf1, на котором посредством графика визуализировано выявление модельной матрицы pGEM-T-HCV 1b с помощью рибонуклеопротеиновых комплексов LbCpf1 из Lachnospiraceae, содержащих направляющую РНК crRNA HCV 1b №147, где:
- по вертикали указаны значения нормализированного флуоресцентного сигнала, создаваемого красителем;
- по горизонтали указано время флуоресценции, в минутах;
- на кривых 1-8 показано количество копий нуклеиновой кислоты на реакцию, а именно:
1 - 2300000 копий/реакция;
2 - 230000 копий/реакция;
3 - 23000 копий/реакция;
4 - 2300 копий/реакция;
5 - 230 копий/реакция;
6 - 23 копий/реакция;
7 - 2,3 копий/реакция;
8 - mQ (отрицательный контроль).
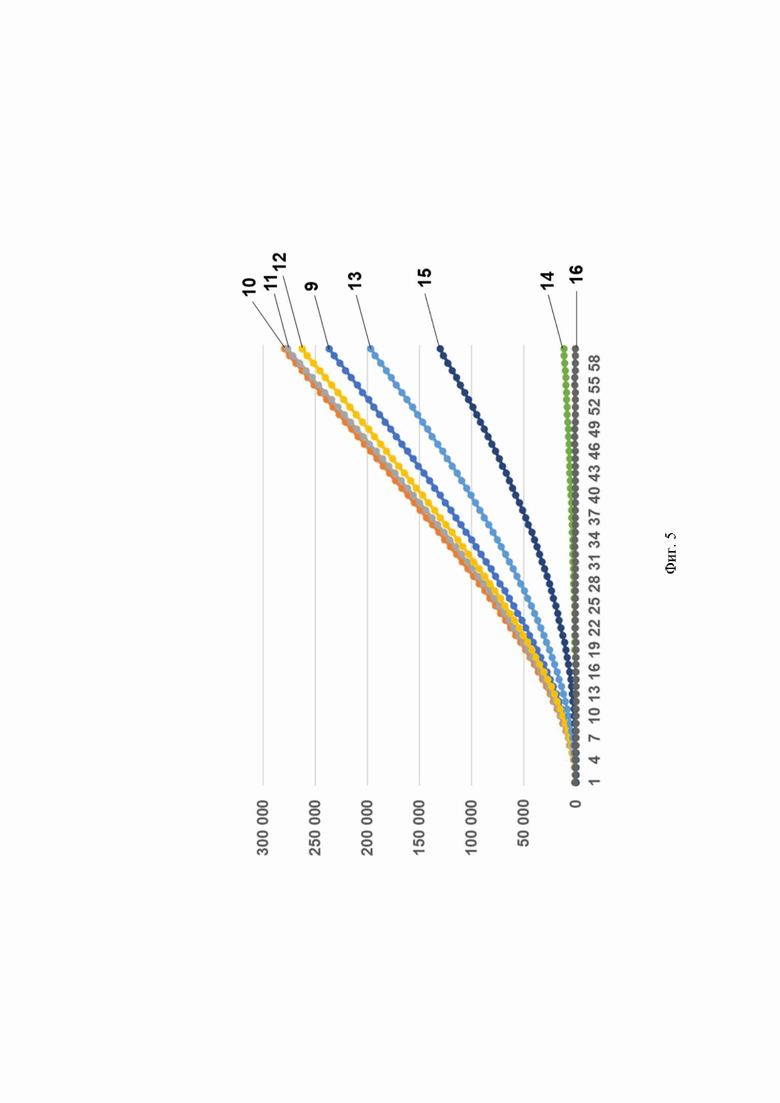
Фиг. 5. Профиль флуоресценции в реальном времени для предварительно амплифицированной мишени HCV 1b генома вируса гепатита С, обработанной рибонуклеопортеиновым комплексом, содержащим направляющую РНК crRNA HCV 1b №179 и белок LbCpf1, на котором посредством графика визуализировано выявление модельной матрицы pGEM-T-HCV 1b с помощью рибонуклеопротеиновых комплексов LbCpf1 из Lachnospiraceae, содержащих направляющую РНК crRNA HCV 1b №179, где:
- по вертикали указаны значения нормализированного флуоресцентного сигнала, создаваемого красителем;
- по горизонтали указано время флуоресценции, в минутах;
- на кривых 9-16 показано количество копий нуклеиновой кислоты на реакцию, а именно:
9 - 2300000 копий/реакция;
10 - 230000 копий/реакция;
11 - 23000 копий/реакция;
12 - 2300 копий/реакция;
13 - 230 копий/реакция;
14 - 23 копий/реакция;
15 - 2,3 копий/реакция;
16 - mQ (отрицательный контроль).
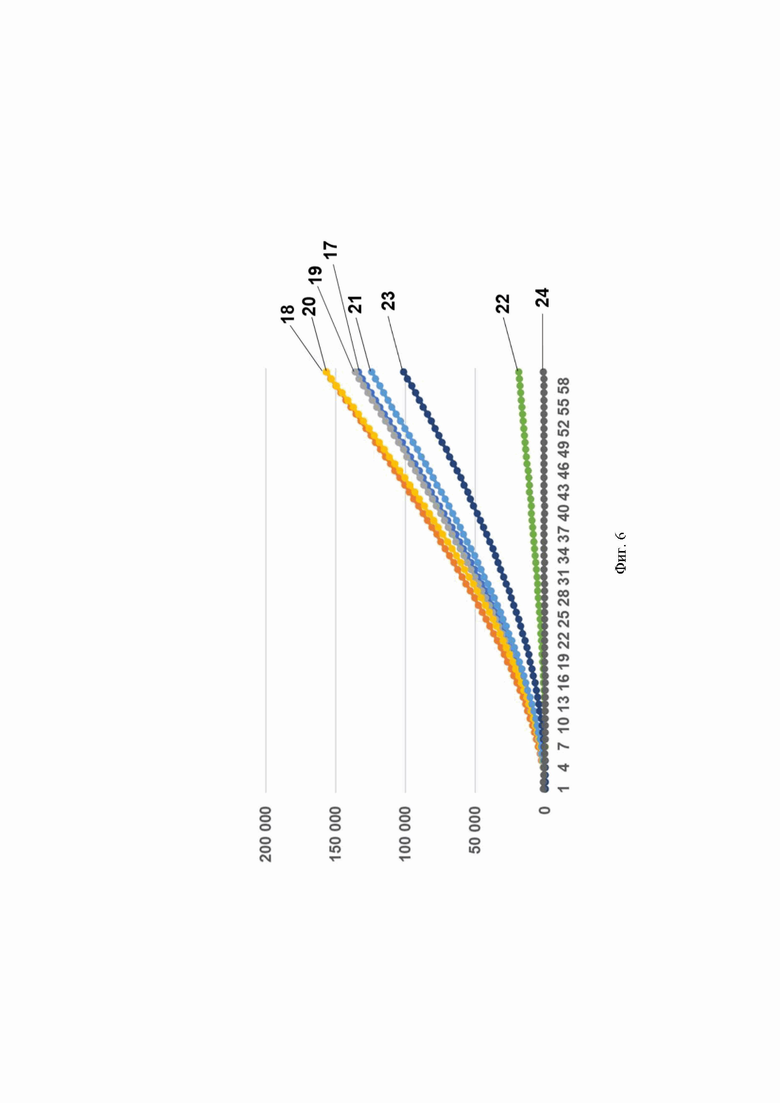
Фиг. 6. Профиль флуоресценции в реальном времени для предварительно амплифицированной мишени HCV 1b генома вируса гепатита С, обработанной рибонуклеопортеиновым комплексом, содержащим направляющую РНК crRNA HCV 1b №184 и белок LbCpf1, на котором посредством графика визуализировано выявление модельной матрицы pGEM-T-HCV 1b с помощью рибонуклеопротеиновых комплексов LbCpf1 из Lachnospiraceae, содержащих направляющую РНК crRNA HCV 1b №184, где:
- по вертикали указаны значения нормализированного флуоресцентного сигнала, создаваемого красителем;
- по горизонтали указано время флуоресценции, в минутах;
- на кривых 17-24 показано количество копий нуклеиновой кислоты на реакцию, а именно:
17 - 2300000 копий/реакция;
18 - 230000 копий/реакция;
19 - 23000 копий/реакция;
20 - 2300 копий/реакция;
21 - 230 копий/реакция;
22 - 23 копий/реакция;
23 - 2,3 копий/реакция;
24 - mQ (отрицательный контроль).
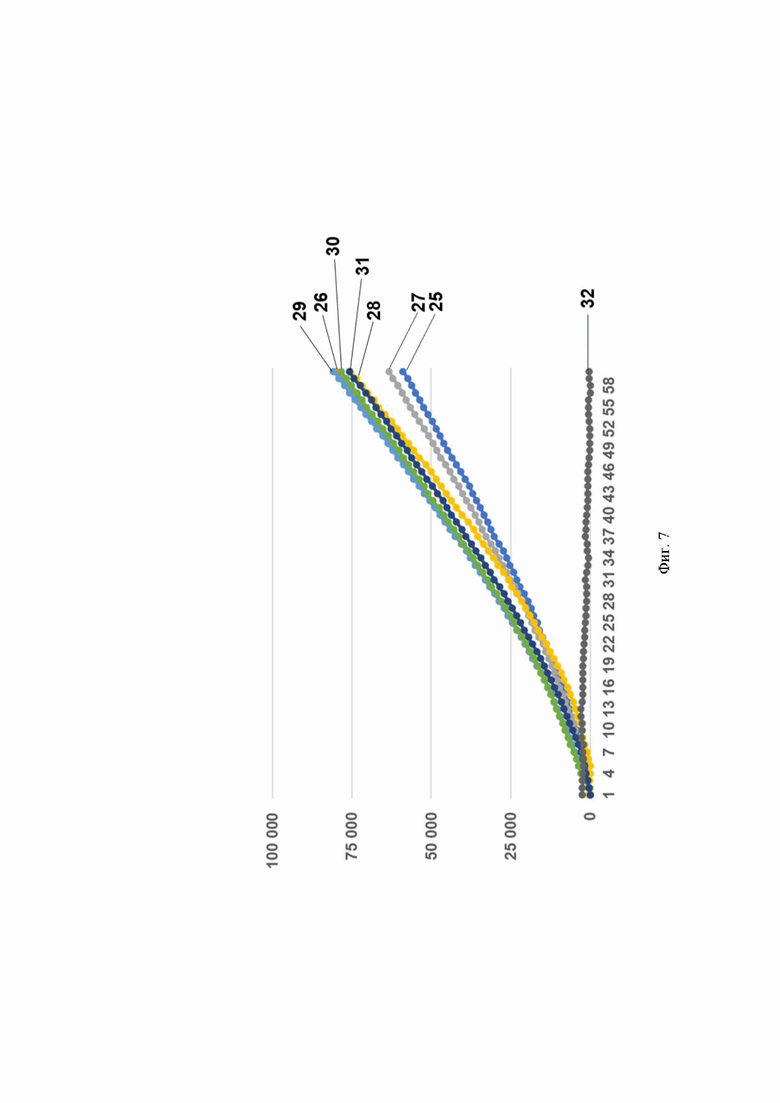
Фиг. 7. Профиль флуоресценции в реальном времени для предварительно амплифицированной мишени HCV 3а_1 генома вируса гепатита С, обработанной рибонуклеопортеиновым комплексом, содержащим направляющую РНК crRNA HCV 3а №3223 и белок LbCpf1, на котором посредством графика визуализировано выявление модельной матрицы pGEM-T-HCV 3а_1 с помощью рибонуклеопротеиновых комплексов LbCpf1 из Lachnospiraceae, содержащих направляющую РНК crRNA HCV 3а №3223, где:
- по вертикали указаны значения нормализированного флуоресцентного сигнала, создаваемого красителем;
- по горизонтали указано время флуоресценции, в минутах;
- на кривых 25-32 показано количество копий нуклеиновой кислоты на реакцию, а именно:
25 - 2300000 копий/реакция;
26 - 230000 копий/реакция;
27 - 23000 копий/реакция;
28 - 2300 копий/реакция;
29 - 230 копий/реакция;
30 - 23 копий/реакция;
31 - 2,3 копий/реакция;
32 - mQ (отрицательный контроль).
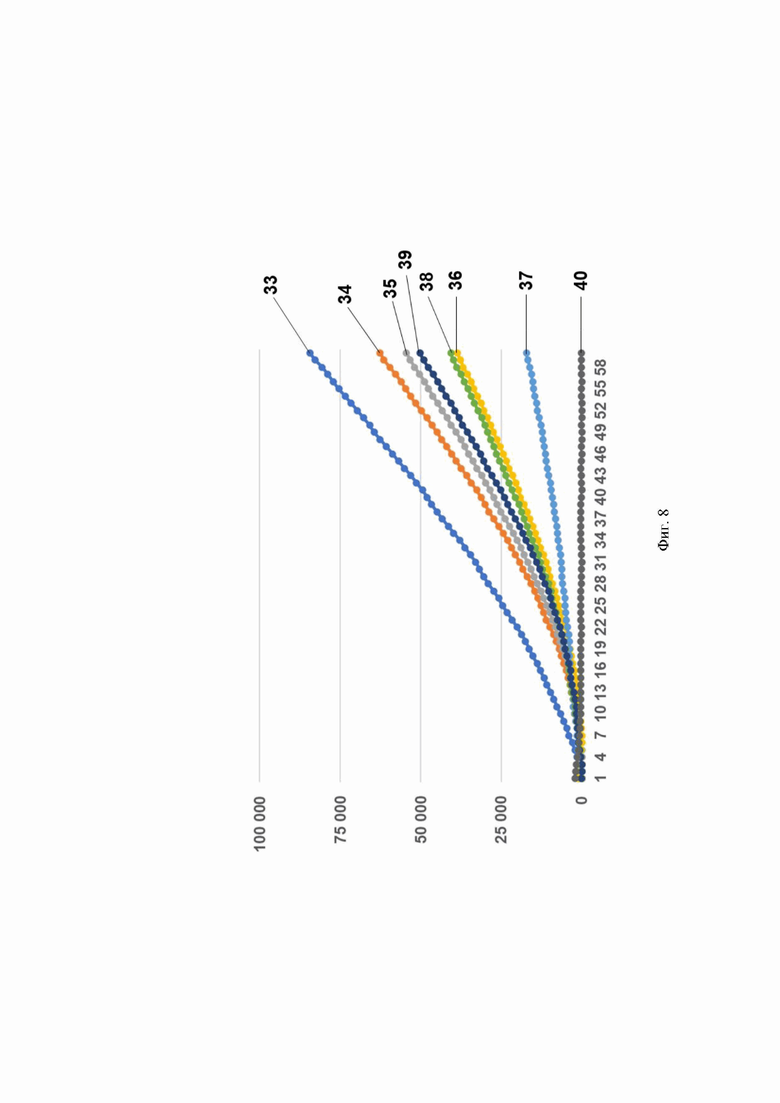
Фиг. 8. Профиль флуоресценции в реальном времени для предварительно амплифицированной мишени HCV 3а_2 генома вируса гепатита С, обработанной рибонуклеопортеиновым комплексом, содержащим направляющую РНК crRNA HCV 3а №4683 и белок LbCpf1, на котором посредством графика визуализировано выявление модельной матрицы pGEM-T-HCV 3а_2 с помощью рибонуклеопротеиновых комплексов LbCpf1 из Lachnospiraceae, содержащих направляющую РНК crRNA HCV 3а №4683, где:
- по вертикали указаны значения нормализированного флуоресцентного сигнала, создаваемого красителем;
- по горизонтали указано время флуоресценции, в минутах;
- на кривых 33-40 показано количество копий нуклеиновой кислоты на реакцию, а именно:
33 - 2300000 копий/реакция;
34 - 230000 копий/реакция;
35 - 23000 копий/реакция;
36 - 2300 копий/реакция;
37 - 230 копий/реакция; 38 - 23 копий/реакция;
39 - 2,3 копий/реакция;
40 - mQ (отрицательный контроль).
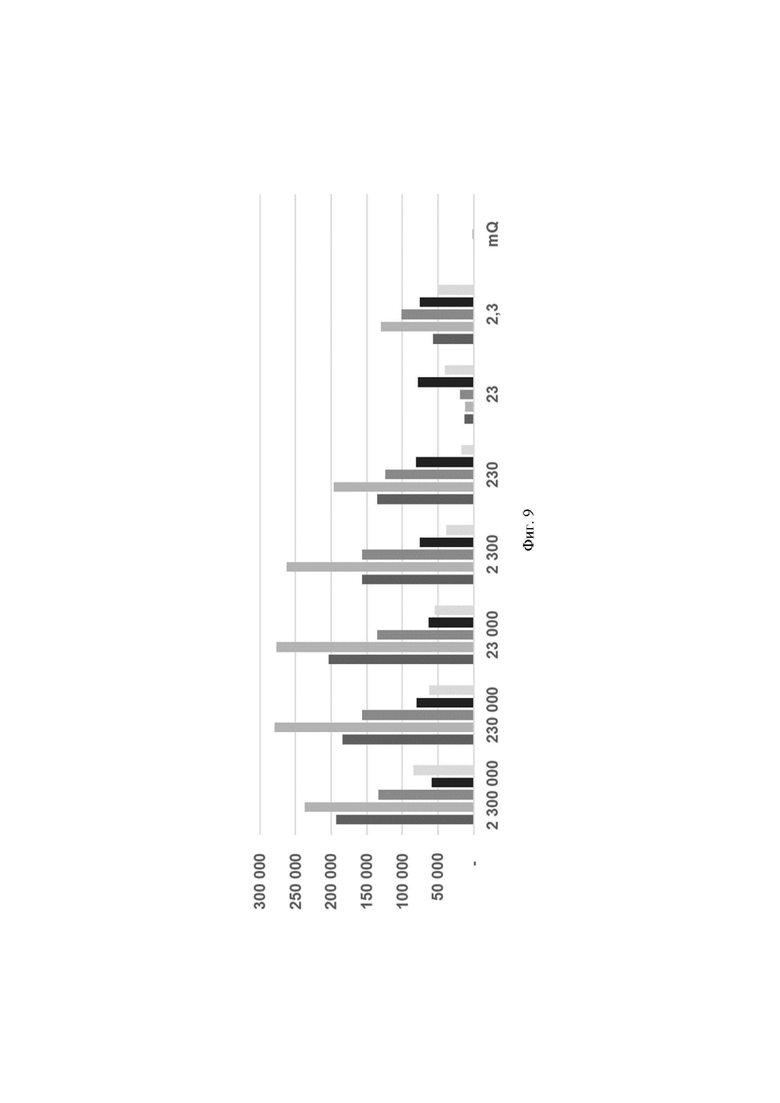
Фиг. 9. Значения флуоресценции в конечной точке (60 цикл анализа, 60 минут) для предварительно амплифицированных мишеней HCV 1b, HCV 3а_1 и HCV 3а_2 генома вируса гепатита С, обработанных рибонуклеопортеиновыми комплексами, содержащим направляющие РНК crRNA HCV 1b №147, crRNA HCV 1b №179, crRNA HCV 1b №184, crRNA HCV 3a №3223 и crRNA HCV 3a №4683, где посредством графика визуализировано выявление модельной матрицы вируса гепатита С с помощью рибонуклеопротеиновых комплексов LbCpf1 из Lachnospiraceae, при этом:
- по вертикали указаны значения нормализированного флуоресцентного сигнала, создаваемого красителем;
- по горизонтали указано количество копий модельной матрицы в реакции;
- столбцом  визуализирована эффективность выявления единичных копий модельной матрицы вируса гепатита С с использованием crRNA HCV 1b №147;
визуализирована эффективность выявления единичных копий модельной матрицы вируса гепатита С с использованием crRNA HCV 1b №147;
- столбцом визуализирована эффективность выявления единичных копий модельной матрицы вируса гепатита С с использованием crRNA HCV 1b №179;
- столбцом  визуализирована эффективность выявления единичных копий модельной матрицы вируса гепатита С с использованием crRNA HCV 1b №184;
визуализирована эффективность выявления единичных копий модельной матрицы вируса гепатита С с использованием crRNA HCV 1b №184;
- столбцом  визуализирована эффективность выявления единичных копий модельной матрицы вируса гепатита С с использованием crRNA HCV 3а №3223;
визуализирована эффективность выявления единичных копий модельной матрицы вируса гепатита С с использованием crRNA HCV 3а №3223;
- столбцом визуализирована эффективность выявления единичных копий модельной матрицы вируса гепатита С с использованием crRNA HCV 3а №4683.
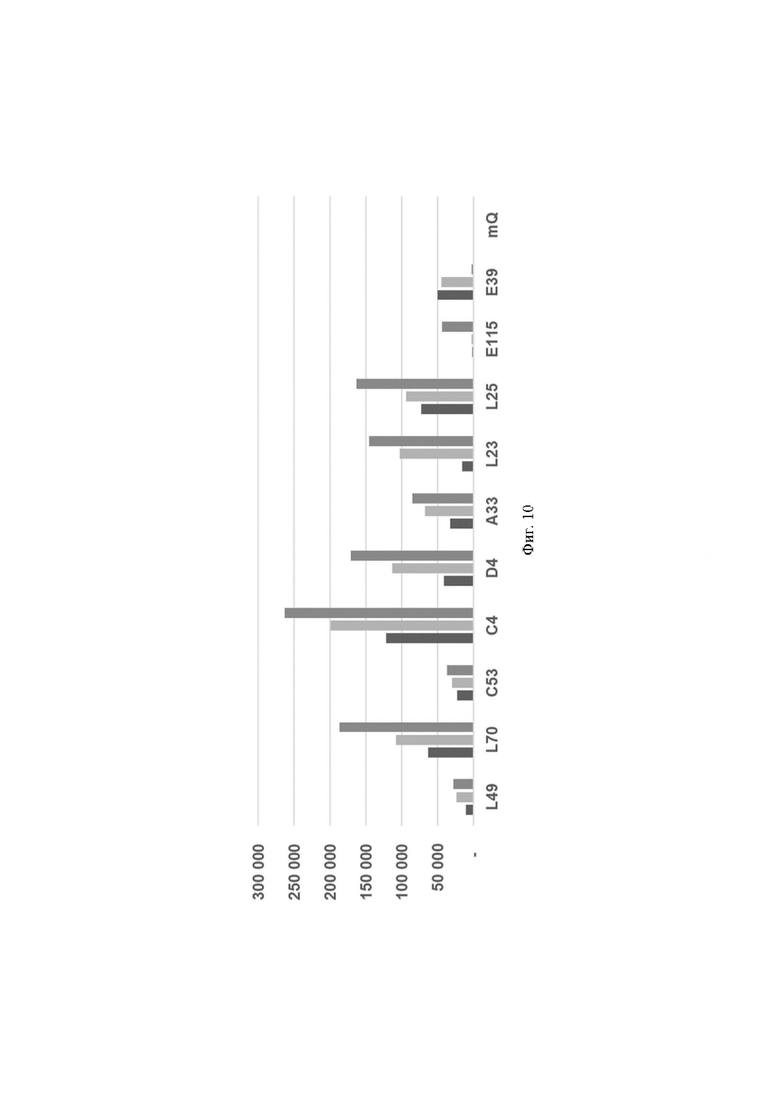
Фиг. 10. Значения флуоресценции в конечной точке (60 цикл анализа, 60 минут) для предварительно амплифицированной с клинических образцов мишени HCV 1b генома вируса гепатита С, обработанных рибонуклеопортеиновыми комплексами, содержащим направляющие РНК crRNA HCV 1b №147, crRNA HCV 1b №179 и crRNA HCV 1b №184, где посредством графика визуализировано выявление РНК вируса гепатита С с помощью рибонуклеопротеиновых комплексов LbCpf1 из Lachnospiraceae на ограниченной панели клинических образцов, при этом:
- по вертикали указаны значения нормализированного флуоресцентного сигнала, создаваемого красителем;
- по горизонтали указаны идентификаторы образца;
- столбцом  показана эффективность выявления РНК вируса гепатита С, содержащегося в составе препаратов, выделенных из клинических образцов, с использованием crRNA HCV 1b №147;
показана эффективность выявления РНК вируса гепатита С, содержащегося в составе препаратов, выделенных из клинических образцов, с использованием crRNA HCV 1b №147;
- столбцом показана эффективность выявления РНК вируса гепатита С, содержащегося в составе препаратов, выделенных из клинических образцов, с использованием crRNA HCV 1b №179;
- столбцом  показана эффективность выявления РНК вируса гепатита С, содержащегося в составе препаратов, выделенных из клинических образцов, с использованием crRNA HCV 1b №184.
показана эффективность выявления РНК вируса гепатита С, содержащегося в составе препаратов, выделенных из клинических образцов, с использованием crRNA HCV 1b №184.
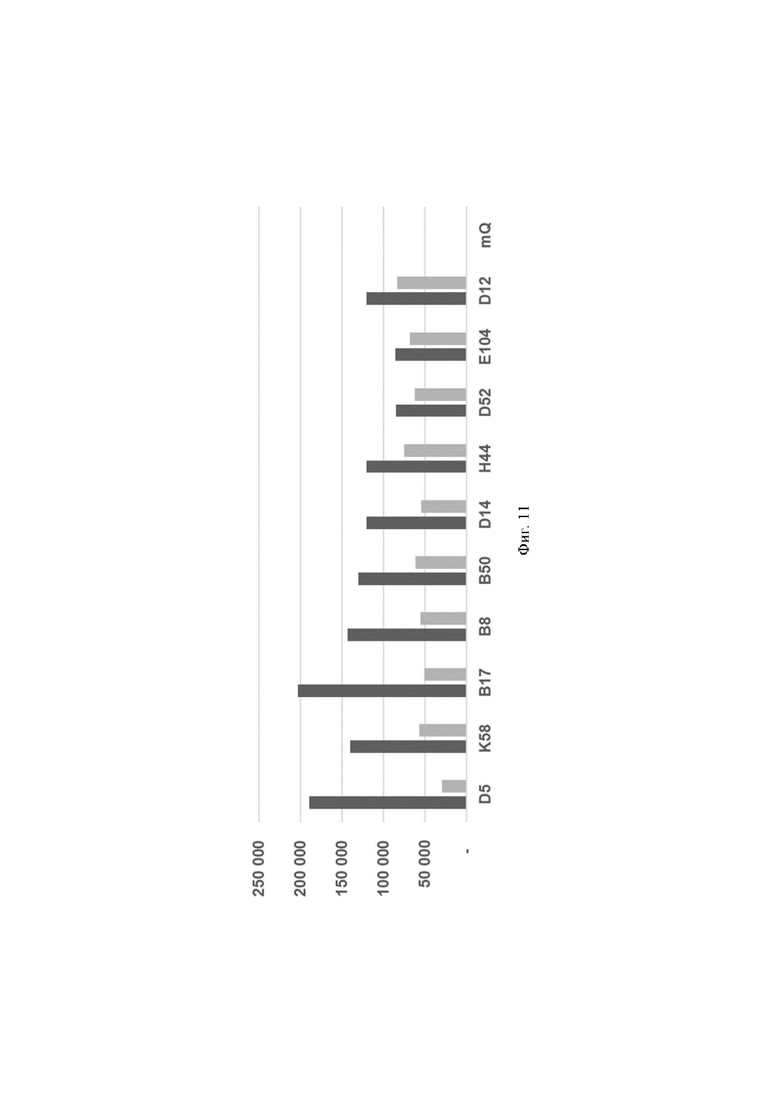
Фиг. 11. Значения флуоресценции в конечной точке (60 цикл анализа, 60 минут) для предварительно амплифицированных с клинических образцов мишеней HCV 3а_1 и HCV 3а_2 генома вируса гепатита С, обработанных рибонуклеопортеиновыми комплексами, содержащим направляющие РНК crRNA HCV 3а №3223 и crRNA HCV 3а №4683, где посредством графика визуализировано выявление РНК вируса гепатита С с помощью рибонуклеопротеиновых комплексов LbCpf1 из Lachnospiraceae на ограниченной панели клинических образцов, при этом:
- по вертикали указаны значения нормализированного флуоресцентного сигнала, создаваемого красителем;
- по горизонтали указаны идентификаторы образца;
- столбцом  показана эффективность выявления РНК вируса гепатита С, содержащегося в составе препаратов, выделенных из клинических образцов, с использованием crRNA HCV 3а №3223;
показана эффективность выявления РНК вируса гепатита С, содержащегося в составе препаратов, выделенных из клинических образцов, с использованием crRNA HCV 3а №3223;
- столбцом показана эффективность выявления РНК вируса гепатита С, содержащегося в составе препаратов, выделенных из клинических образцов, с использованием crRNA HCV 3а №4683.
Примеры осуществления изобретения
ПРИМЕР 1: ПОДБОР ПОСЛЕДОВАТЕЛЬНОСТЕЙ-МИШЕНЕЙ В ГЕНОМЕ ВИРУСА ГЕПАТИТА С ГЕНОТИПОВ 1В И 3А ДЛЯ СОЗДАНИЯ НАПРАВЛЯЮЩИХ РНК
Для подбора последовательностей-мишеней в геноме вируса гепатита С генотипов 1b и 3а для создания направляющих РНК были использованы современные алгоритмы in silico анализа нуклеотидных последовательностей и программы, находящиеся в открытом доступе, включая Benchling (https://www.benchling.com/molecular-biology/). Был составлен перечень участков в геноме вируса гепатита С генотипов 1b и 3а с теоретически рассчитанной вероятностью их расщепления в высоко консервативных участках (Таблица 1). Направляющие РНК, специфически узнающие высоко консервативные участки генома вируса гепатита С генотипов 1b и 3а, представлены уникальными последовательностями SEQ ID NO: 1-5.


ПРИМЕР 2: ПОДГОТОВКА МАТЕРИАЛА ДЛЯ ОБНАРУЖЕНИЯ РНК ВИРУСА ГЕПАТИТА С ГЕНОТИПОВ 1В И 3А МЕТОДОМ ПРЕДВАРИТЕЛЬНОЙ АМПЛИФИКАЦИИ
Подготовку материала для обнаружения РНК вируса гепатита С генотипов 1b и 3а проводили методом предварительной амплификации. В качестве модельных матриц, содержащих фрагменты генома вируса гепатита С генотипов 1b и 3а биологического образца, использовали плазмидные ДНК:
1) pGEM-T-HCV 1b, содержащую в своем составе фрагмент генома вируса гепатита С генотипа 1b (размером 226 п.о.), и
2) pGEM-T-HCV 3а_1, содержащую в своем составе фрагмент генома вируса гепатита С генотипов 3а (размером 210 п.о.), и
3) pGEM-T-HCV 3а_2, содержащую в своем составе фрагмент генома вируса гепатита С генотипов 3а (размером 405 п.о.).
Предварительную амплификацию участков, соответствующих фрагментам генома вируса гепатита С, проводили с использованием специфических олигонуклеотидов с SEQ ID NO: 6 и SEQ ID NO: 7 для получения фрагмента HCV 1b, SEQ ID NO: 8 и SEQ ID NO: 9 для получения фрагмента HCV 3а_1 и SEQ ID NO: 10 и SEQ ID NO: 11 для получения фрагмента HCV 3а_2, приведенных в Таблице 2.
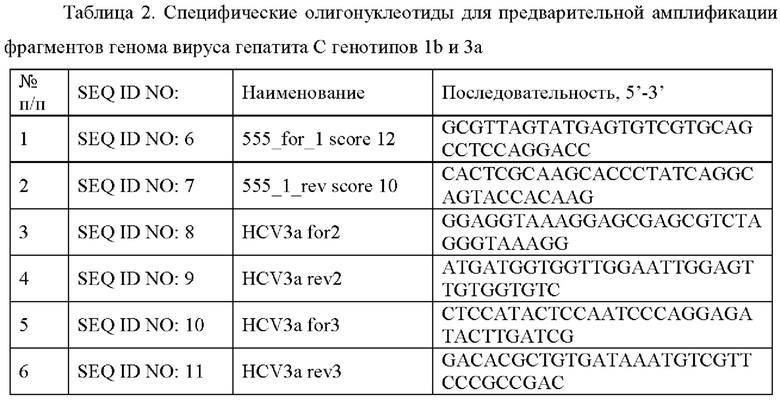
Продукты, кодирующие фрагменты HCV 1b, HCV 3а_1 и HCV 3а_2 генома вируса гепатита С, получали в реакции изотермической амплификации с использованием специфических олигонуклеотидов 555_for_1 score 12 и 555_1_rev score 10, HCV3a for2 и HCV3a rev2, HCV3a for3 и HCV3a rev3 соответственно (ГенТерра, Россия). Размер амплифицированного фрагмента HCV 1b составлял 226 пар нуклеотидов, HCV 3а_1 - 210 пар нуклеотидов, HCV 3а_2 - 405 пар нуклеотидов (Таблица 3).
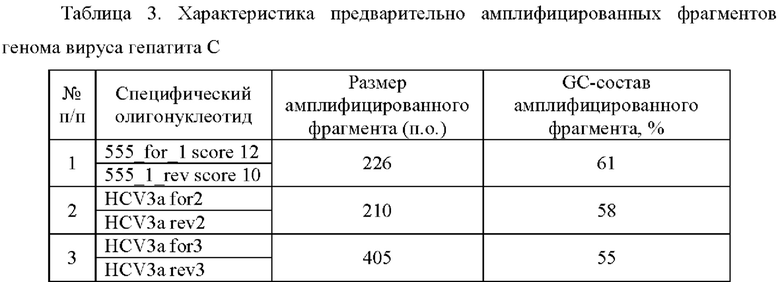
Амплификации для получения фрагментов генома вируса гепатита С проводилась при температуре 37°С в течение 60 минут.
В ходе подготовки материала для обнаружения РНК вируса гепатита С методом предварительной амплификации проводили титрование модельных матриц pGEM-T-HCV 1b, pGEM-T-HCV 3а_1 и pGEM-T-HCV 3а_2 путем приготовления серийных разведений (Таблица 4).

Для оценки эффективности предварительной амплификации полученные фрагменты генома вируса гепатита С генотипов 1b и 3а визуализировали при помощи электрофореза в агарозном геле (фиг. 1-3).
Подготовленный описанным способом материал использовали для экспериментов по выявлению РНК вируса гепатита С генотипов 1b и 3а с помощью рибонуклеопротеиновых комплексов LbCpf1 из Lachnospiraceae, содержащих направляющие РНК crRNA HCV 1b №147, crRNA HCV 1b №179, crRNA HCV 1b №184, crRNA HCV 3a №3223 и crRNA HCV 3a №4683, без предварительной очистки.
ПРИМЕР 3: ПОЛУЧЕНИЕ НАПРАВЛЯЮЩИХ РНК И СОЗДАНИЕ РИБОНУКЛЕОПРОТЕИНОВЫХ КОМПЛЕКСОВ ДЛЯ ОБНАРУЖЕНИЯ РНК ВИРУСА ГЕПАТИТА С ГЕНОТИПОВ 1В И 3А
Для получения направляющих РНК для обнаружения РНК вируса гепатита С генотипов 1b и 3а был разработан набор специфических олигонуклеотидов, приведенных в Таблице 5. Получение направляющих РНК проводили в несколько этапов:
1. получение ПЦР-продукта с использованием набора специфических олигонуклеотидов (Таблица 5), кодирующего направляющую РНК, способную связываться с целевым высоко консервативным участком генома вируса гепатита С генотипов 1b и 3а, содержащую РНК-шпильку, которая распознается РНК-направляемой ДНК-эндонуклеазой LbCpf1 из Lachnospiraceae;
2. очистка ПЦР-продукта, кодирующего направляющую РНК, специфичную к фрагменту генома вируса гепатита С генотипов 1b и 3а;
3. синтез направляющей РНК, специфичной к фрагменту генома вируса гепатита С генотипов 1b и 3а;
4. очистка направляющей РНК, специфичной к фрагменту генома вируса гепатита С генотипов 1b и 3а.
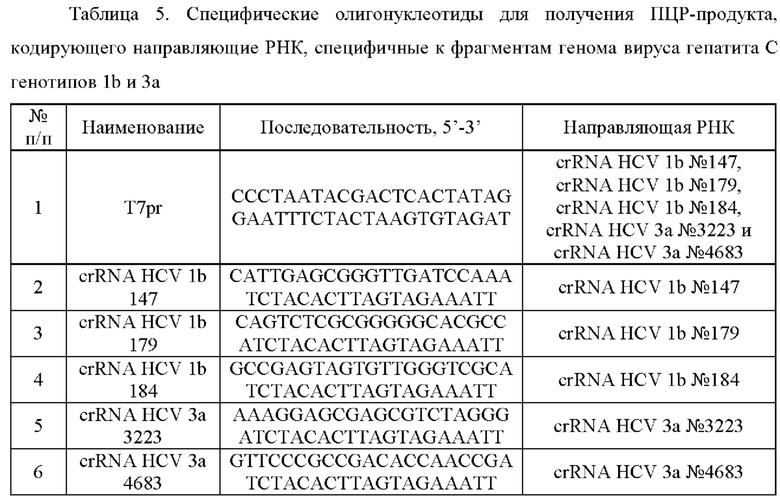
ПЦР-продукт, кодирующий направляющую РНК crRNA HCV 1b №147, получали в реакции амплификации с использованием ПЦР-смеси-2 blue (ФБУН ЦНИИ Эпидемиологии Роспотребнадзора, Россия) и специфических олигонуклеотидов T7pr и crRNA HCV 1b 147 (ГенТерра, Россия). Размер амплифицированного фрагмента, кодирующего crRNA HCV 1b №147, составлял 62 пары нуклеотидов.
ПЦР-продукт, кодирующий направляющую РНК crRNA HCV 1b №179, получали в реакции амплификации с использованием ПЦР-смеси-2 blue (ФБУН ЦНИИ Эпидемиологии Роспотребнадзора, Россия) и специфических олигонуклеотидов T7pr и crRNA HCV 1b 179 (ГенТерра, Россия). Размер амплифицированного фрагмента, кодирующего crRNA HCV 1b №179, составлял 62 пары нуклеотидов.
ПЦР-продукт, кодирующий направляющую РНК crRNA HCV 1b №184, получали в реакции амплификации с использованием ПЦР-смеси-2 blue (ФБУН ЦНИИ Эпидемиологии Роспотребнадзора, Россия) и специфических олигонуклеотидов T7pr и crRNA HCV 1b 184 (ГенТерра, Россия). Размер амплифицированного фрагмента, кодирующего crRNA HCV 1b №184, составлял 62 пары нуклеотидов.
ПЦР-продукт, кодирующий направляющую РНК crRNA HCV 3а №3223, получали в реакции амплификации с использованием ПЦР-смеси-2 blue (ФБУН ЦНИИ Эпидемиологии Роспотребнадзора, Россия) и специфических олигонуклеотидов T7pr и crRNA HCV 3а 3223 (ГенТерра, Россия). Размер амплифицированного фрагмента, кодирующего crRNA HCV 3а №3223, составлял 62 пары нуклеотидов.
ПЦР-продукт, кодирующий направляющую РНК crRNA HCV 3а №4683, получали в реакции амплификации с использованием ПЦР-смеси-2 blue (ФБУН ЦНИИ Эпидемиологии Роспотребнадзора, Россия) и специфических олигонуклеотидов T7pr и crRNA HCV 3а 4683 (ГенТерра, Россия). Размер амплифицированного фрагмента, кодирующего crRNA HCV 3а №4683, составлял 62 пары нуклеотидов.
Температурный профиль амплификации для получения ПЦР-продуктов, кодирующих направляющие РНК:
1. денатурация: 95°С в течение 3 минут;
2. 35 циклов амплификации:
95°С - 15 сек,
55°С - 45 сек,
72°С - 30 сек;
3. финальная элонгация: 72°С в течение 5 минут.
ПЦР-продукты, кодирующие направляющие РНК, специфичные к фрагментам генома вируса гепатита С генотипов 1b и 3а, визуализировали при помощи электрофореза в агарозном геле.
Очистку ПЦР-продуктов, кодирующих направляющие РНК, специфичные к фрагментам генома вируса гепатита С генотипов 1b и 3а, проводили с использованием коммерчески доступного набора ISOLATE II PCR and Gel Kit (BioLine, США) согласно инструкции производителя. Очищенные ПЦР-продукты, кодирующие направляющие РНК, специфичные к фрагментам генома вируса гепатита С генотипов 1b и 3а, использовали в качестве матрицы для синтеза направляющих РНК.
Синтез направляющих РНК, специфичных к фрагментам генома вируса гепатита С генотипов 1b и 3а, осуществляли методом in vitro транскрипции с использованием коммерчески доступных наборов реагентов (HiScribe™ Т7 High Yield RNA Synthesis Kit, NEB, США) согласно инструкции производителя. Продукты реакции in vitro транскрипции переосаждали из реакционной смеси добавлением хлорида натрия до конечной концентрации 400 mM и равного объема изопропилового спирта. Такие модификации протокола производителя, внесенные авторами, позволяют увеличить выход продукта реакции и получить желаемую концентрацию финального препарата направляющей РНК.
Создание готового рибонуклеопротеинового комплекса, содержащего белок семейства CRISPR-Cas LbCpf1 из Lachnospiraceae, и направляющую РНК авторы проводили по стандартному протоколу с некоторыми модификациями [С. Anders, M. Jinek, In vitro enzymology of Cas9, Methods Enzymol. 546 (2014) 1-20, https://doi.org/10.1016/B978-0-12-801185-0.00001-51.
Непосредственно перед объединением с Cas-белком препарат направляющей РНК (в количестве 250 нг) прогревали при 90°С в течение 5 минут и позволяли медленно остыть до комнатной температуры (инкубация при комнатной температуре не менее 10 минут). Такое прогревание необходимо для формирования корректной конформации шпильки, содержащейся в направляющей РНК. Многие производители коммерческих препаратов Cas-белков пропускают данный этап при подготовке рибонуклеопротеинового комплекса.
Для формирования готового рибонуклеопротеинового комплекса 250 нг Cas-белка LbCpf1 из Lachnospiraceae и подготовленную направляющую РНК смешивали и инкубировали 15 минут при комнатной температуре. Полученный таким способом рибонуклеопротеиновый комплекс готов для выявления РНК вируса гепатита С генотипов 1b и 3а.
ПРИМЕР 4: ОБНАРУЖЕНИЕ ЕДИНИЧНЫХ КОПИЙ РНК ВИРУСА ГЕПАТИТА С ГЕНОТИПОВ 1В И 3А С ПОМОЩЬЮ РИБОНУКЛЕОПРОТЕИНОВЫХ КОМПЛЕКСОВ CRISPR/CAS НА ПРИМЕРЕ МОДЕЛЬНОЙ МАТРИЦЫ
Предварительно амплифицированный материал, полученный способом, описанным в Примере 2, использовали в качестве матрицы для обнаружения РНК вируса гепатита С генотипов 1b и 3а с помощью рибонуклеопротеиновых комплексов CRISPR-Cas, полученных способом, описанным в Примере 3.
Для обнаружения РНК вируса гепатита С генотипов 1b и 3а с помощью рибонуклеопротеиновых комплексов CRISPR-Cas готовили реакционную смесь, содержащую следующие компоненты:
• 10× буфер (100 mM TrisHCl рН 8,0, 1 M NaCl);
• 50 mM MgCl2 (конечная концентрация в реакционной смеси 10 mM);
• 250 нг рибонуклеопротеинового комплекса (LbCpf1 из Lachnospiraceae и направляющие РНК crRNA HCV 1b №147, crRNA HCV 1b №179, crRNA HCV 1b №184, crRNA HCV 3a №3223 и crRNA HCV 3a №4683);
• 10 pmol флуоресцентный зонд (6FAM-TTATT-BHQ1);
• Мишень (предварительно амплифицированные фрагменты генома вируса гепатита С генотипов 1b и 3а);
• вода mQ.
Реакционные смеси, содержащие все необходимые компоненты, помещали в амплификатор QuantStudio 5 (Thermo Fisher Scientific, США) и задавали следующие параметры реакции:
30-60 циклов:
37°С-35 сек,
37°С - 25 сек, съемка флуоресценции.
В первую очередь были проведены эксперименты по обнаружению единичных копий РНК вируса гепатита С генотипов 1b и 3а с помощью рибонуклеопротеиновых комплексов CRISPR-Cas, сформированных на основе LbCpf1 из Lachnospiraceae, с использованием в качестве мишени модельных матриц - плазмидной ДНК pGEM-T-HCV 1b, содержащую в своем составе фрагмент генома вируса гепатита С генотипа 1b размером 226 п.о., плазмидной ДНК pGEM-T-HCV 3а_1, содержащую в своем составе фрагмент генома вируса гепатита С генотипов 3а размером 210 п.о., и плазмидной ДНК pGEM-T-HCV 3а 2, содержащую в своем составе фрагмент генома вируса гепатита С генотипов 3а размером 405 п.о.
Было показано, что рибонуклеопротеиновые комплексы CRISPR-Cas обладают способностью выявлять единичные копии РНК вируса гепатита С генотипов 1b и 3а. Типичные результаты анализа приведены на примерах профилей флуоресценции в реальном времени для предварительно амплифицированных мишеней HCV 1b, HCV 3а_1 и HCV 3а_2 вируса гепатита С генотипов 1b и 3а, обработанных рибонуклеопортеиновыми комплексами, содержащими направляющие РНК crRNA HCV 1b №147, crRNA HCV 1b №179, crRNA HCV 1b №184, crRNA HCV 3a №3223 и crRNA HCV 3a №4683 и белок LbCpf1, на Фиг. 4, Фиг. 5, Фиг. 6, Фиг. 7 и Фиг. 8, соответственно. Отметим, что в среднем уже на 13-ом цикле анализа (13 минут) значение сигнала, полученного в ходе детекции единичных копий (2,3 копий/реакция) РНК вируса гепатита С генотипов 1b и 3а, превышало значение «шума» (неспецифической флуоресценции контрольного образца, не содержащего мишени) минимум в пять раз, а к 18-ому циклу (18 минут анализа) в 10 и более раз.
В ходе работ была оценена эффективность выявления единичных копий РНК вируса гепатита С генотипов 1b и 3а, содержащегося в составе модельных матриц, с использованием различных направляющих РНК. Было показано, что рибонуклеопротеиновые комплексы CRISPR-Cas, сформированные на основе LbCpf1 из Lachnospiraceae и направляющих РНК, выявляют единичные копии РНК вируса гепатита С генотипов 1b и 3а с различной эффективностью, и их можно расположить в следующем порядке по уменьшению активности: crRNAHCV 1b №179 > crRNAHCV 1b №184 > crRNA HCV 3a №3223 > crRNA HCV 1b №147 > crRNA HCV 3a №4683 (Фиг. 9).
ПРИМЕР 5: ОБНАРУЖЕНИЕ РНК ВИРУСА ГЕПАТИТА С ГЕНОТИПОВ 1В И 3А С ПОМОЩЬЮ РИБОНУКЛЕОПРОТЕИНОВЫХ КОМПЛЕКСОВ CRISPR/CAS НА ОГРАНИЧЕННОЙ ПАНЕЛИ КЛИНИЧЕСКИХ ОБРАЗЦОВ
Разработанные направляющие РНК были апробированы на ограниченной панели клинических образцов (20 шт.), содержащих вируса гепатита С генотипов 1b и 3а (ранее подтверждено генотипированием).
Для обнаружения единичных копий РНК вируса гепатита С генотипов 1b и 3а с помощью рибонуклеопротеиновых комплексов CRISPR-Cas была проведена предварительная амплификация фрагментов генома вируса гепатита С. Для проведения предварительной амплификации из клинических образцов 20 пациентов с помощью коммерчески доступного набора «РИБО-преп» (ФБУН ЦНИИ Эпидемиологии Роспотребнадзора, Россия) согласно инструкции производителя были выделены препараты РНК.
Синтез кДНК фрагментов генома вируса гепатита С проводили методом обратной транскрипции с использованием специфических олигонуклеотидов 555_for_1 score 12 с SEQ ID NO: 6, HCV3a rev2 с SEQ ID NO: 9 и HCV3a rev3 с SEQ ID NO: 11 (Таблица 2) и обратной транскриптазы Superscript™ II (Thermo Fisher Scientific, США) при температуре 42°C. Продукты, кодирующие фрагменты генома вируса гепатита С, получали в реакции изотермической амплификации с использованием специфических олигонуклеотидов 555_for_1 score 12 и 555_1_rev score 10, HCV3a for2 и HCV3a rev2, HCV3a for3 и HCV3a rev3 соответственно (ГенТерра, Россия). Полученные продукты визуализировали при помощи электрофореза в агарозном геле.
Полученный таким способом материал использовали в качестве матрицы для обнаружения единичных копий РНК вируса гепатита С генотипов 1b и 3а с помощью рибонуклеопротеиновых комплексов CRISPR-Cas, полученных способом, описанным в Примере 3.
Обнаружение единичных копий РНК вируса гепатита С генотипов 1b и 3а с помощью рибонуклеопротеиновых комплексов CRISPR-Cas проводили способом, описанным в Примере 4.
В ходе проведенного анализа было показано, что рибонуклеопротеиновые комплексы CRISPR-Cas обладают способностью выявлять вирус гепатита С генотипов 1b и 3а в препаратах РНК, выделенных из клинических образцов. При этом в среднем уже на 13 цикле (13 минут) анализа значение сигнала превышало значение «шума» (неспецифической флуоресценции контрольного образца, не содержащего мишени) более чем в 5 раз, а к 18 циклу (18 минут) анализа - более чем в 10 раз (Таблица 6).
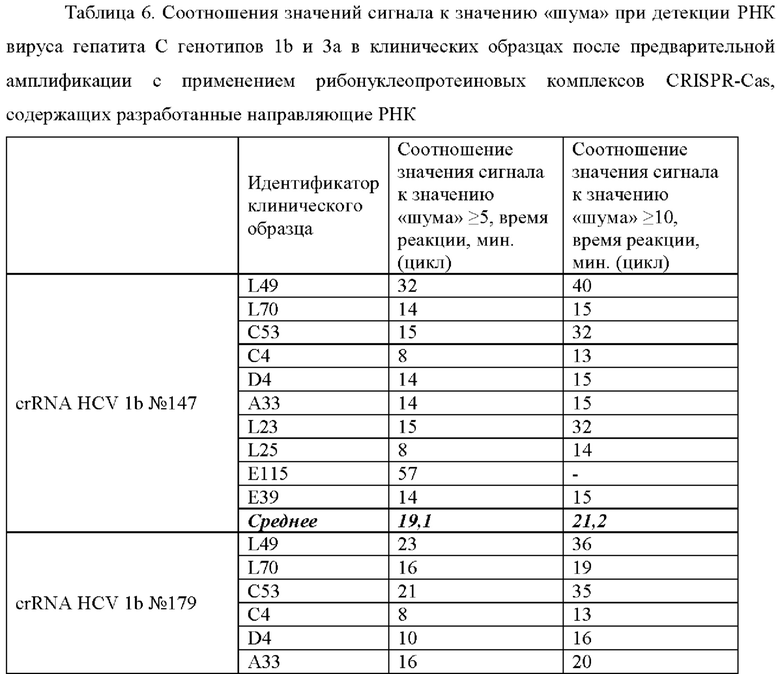
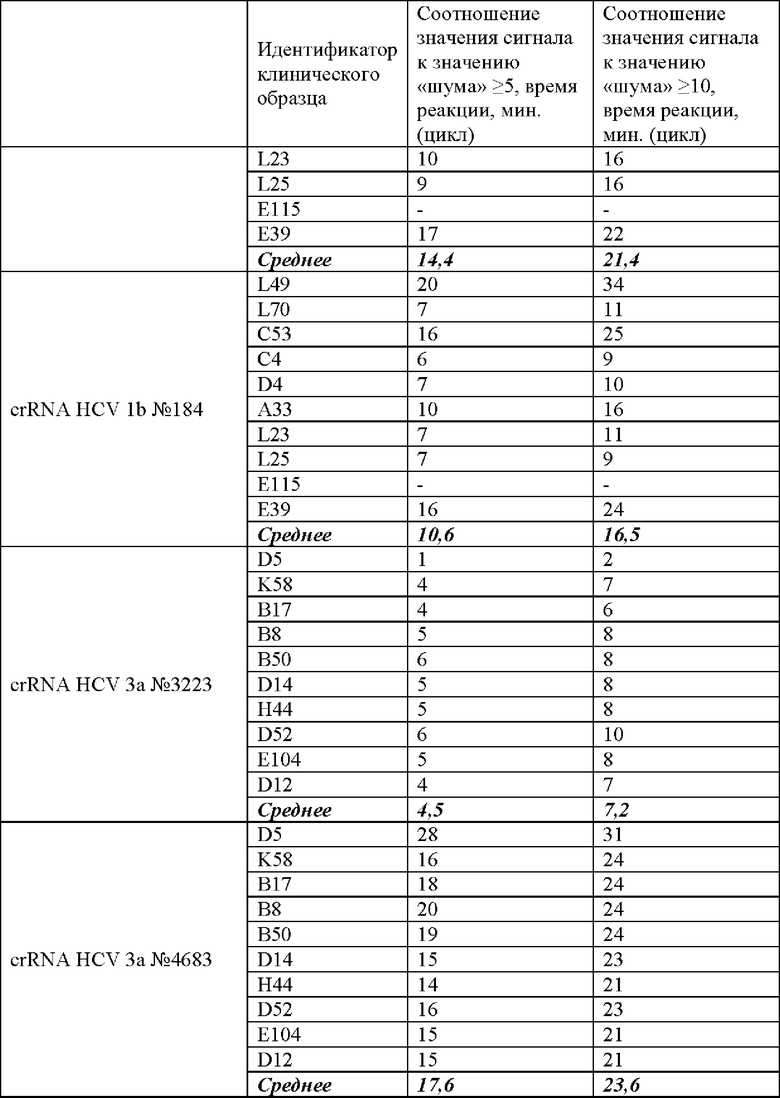
Типичные результаты анализа приведены на примерах значений флуоресценции в конечной точке (60 цикл анализа, 60 минут) для предварительно амплифицированных мишеней HCV 1b, HCV 3а_1 и HCV 3а_2 вируса гепатита С генотипов 1b и 3а (20 независимых клинических образцов), обработанных рибонуклеопортеиновыми комплексами, содержащими направляющие РНК crRNA HCV 1b №147, crRNA HCV 1b №179, crRNA HCV 1b №184, crRNA HCV 3a №3223 и crRNA HCV 3a №4683 и белок LbCpf1, на Фиг. 10 и Фиг. 11.
Эффективность выявления вируса гепатита С генотипов 1b и 3а, содержащегося в составе препаратов РНК, выделенных из клинических образцов, с использованием различных направляющих РНК в составе рибонуклеопротеиновых комплексов CRISPR-Cas, сформированных на основе LbCpf1 из Lachnospiraceae, оцененная по соотношению значений сигнала к значению «шума» при детекции, можно представить в следующем порядке по убыванию: crRNA HCV 3а №3223 > crRNA HCV 1b №184 > crRNA HCV 1b №179 > crRNA HCV 3a №4683 > crRNA HCV 1b №147 (Таблица 6).
Таким образом, разработанные направляющие РНК позволяют ультрачувствительно выявлять единичные копии РНК вируса гепатита С генотипов 1b и 3а, и способны обнаруживать его препаратах РНК, выделенных из клинических образцов, после предварительной амплификации в составе рибонуклеопротеиновых комплексов CRISPR-Cas.
--->
<?xml version="1.0" encoding="UTF-8"?>
<!DOCTYPE ST26SequenceListing PUBLIC "-//WIPO//DTD Sequence Listing
1.2//EN" "ST26SequenceListing_V1_2.dtd">
<ST26SequenceListing dtdVersion="V1_2" fileName="Способ получения
препарата рибонуклеопротеинового комплекса CRISPR-Cas и препарат для
выявления РНК вируса гепатита С генотипов 1b и 3a в ультранизких
концентрациях" softwareName="WIPO Sequence" softwareVersion="1.0.0"
productionDate="2022-11-28">
<ApplicationIdentification>
<IPOfficeCode>RU</IPOfficeCode>
<ApplicationNumberText>nn</ApplicationNumberText>
<FilingDate>2022-11-28</FilingDate>
</ApplicationIdentification>
<ApplicantName languageCode="ru">ФБУН ЦНИИ Эпидемиологии
Роспотребнадзора</ApplicantName>
<ApplicantNameLatin>FBUN CRIE</ApplicantNameLatin>
<InventionTitle languageCode="ru">Способ получения препарата
рибонуклеопротеинового комплекса CRISPR-Cas и препарат для выявления
РНК вируса гепатита С генотипов 1b и 3a в ультранизких
концентрациях</InventionTitle>
<SequenceTotalQuantity>11</SequenceTotalQuantity>
<SequenceData sequenceIDNumber="1">
<INSDSeq>
<INSDSeq_length>40</INSDSeq_length>
<INSDSeq_moltype>RNA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..40</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>other RNA</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier>
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>HCV </INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>aatttctactaagtgtagatttggatcaacccgctcaatg</INSDSeq
_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="2">
<INSDSeq>
<INSDSeq_length>40</INSDSeq_length>
<INSDSeq_moltype>RNA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..40</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>other RNA</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier>
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>HCV</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>aatttctactaagtgtagatggcgtgcccccgcgagactg</INSDSeq
_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="3">
<INSDSeq>
<INSDSeq_length>40</INSDSeq_length>
<INSDSeq_moltype>RNA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..40</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>other RNA</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier>
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>HCV</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>aatttctactaagtgtagatgcgacccaacactactcggc</INSDSeq
_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="4">
<INSDSeq>
<INSDSeq_length>40</INSDSeq_length>
<INSDSeq_moltype>RNA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..40</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>other RNA</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier>
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>HCV</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>aatttctactaagtgtagatccctagacgctcgctccttt</INSDSeq
_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="5">
<INSDSeq>
<INSDSeq_length>40</INSDSeq_length>
<INSDSeq_moltype>RNA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..40</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>other RNA</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier>
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>HCV</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>aatttctactaagtgtagatcggttggtgtcggcgggaac</INSDSeq
_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="6">
<INSDSeq>
<INSDSeq_length>34</INSDSeq_length>
<INSDSeq_moltype>DNA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..34</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>other DNA</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier>
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>HCV</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>gcgttagtatgagtgtcgtgcagcctccaggacc</INSDSeq_seque
nce>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="7">
<INSDSeq>
<INSDSeq_length>34</INSDSeq_length>
<INSDSeq_moltype>DNA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..34</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>other DNA</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier>
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>HCV</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>cactcgcaagcaccctatcaggcagtaccacaag</INSDSeq_seque
nce>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="8">
<INSDSeq>
<INSDSeq_length>32</INSDSeq_length>
<INSDSeq_moltype>DNA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..32</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>other DNA</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier>
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>HCV</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>ggaggtaaaggagcgagcgtctagggtaaagg</INSDSeq_sequenc
e>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="9">
<INSDSeq>
<INSDSeq_length>32</INSDSeq_length>
<INSDSeq_moltype>DNA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..32</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>other DNA</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier>
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>HCV</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>atgatggtggttggaattggagttgtggtgtc</INSDSeq_sequenc
e>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="10">
<INSDSeq>
<INSDSeq_length>33</INSDSeq_length>
<INSDSeq_moltype>DNA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..33</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>other DNA</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier>
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>HCV</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>ctccatactccaatcccaggagatacttgatcg</INSDSeq_sequen
ce>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="11">
<INSDSeq>
<INSDSeq_length>32</INSDSeq_length>
<INSDSeq_moltype>DNA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..32</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>other DNA</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier>
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>HCV</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>gacacgctgtgataaatgtcgttcccgccgac</INSDSeq_sequenc
e>
</INSDSeq>
</SequenceData>
</ST26SequenceListing>
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| Система CRISPR-Cas12 для выявления РНК вируса гепатита С генотипов 1b и 3a в ультранизких концентрациях | 2022 |
|
RU2800421C1 |
| Способ обнаружения РНК вируса гепатита С генотипов 1b и 3a в ультранизких концентрациях и специфические олигонуклеотиды для использования в способе | 2022 |
|
RU2800420C1 |
| Способ получения препарата рибонуклеопротеинового комплекса CRISPR-Cas12 и препарат для выявления ДНК вируса гепатита B в ультранизких концентрациях | 2021 |
|
RU2792891C1 |
| Система CRISPR-Cas12 для выявления ДНК вируса гепатита B в ультранизких концентрациях | 2021 |
|
RU2782700C1 |
| Способ обнаружения ДНК вируса гепатита B в ультранизких концентрациях и специфические олигонуклеотиды для использования в способе | 2021 |
|
RU2782951C1 |
| Способ получения препарата рибонуклеопротеинового комплекса CRISPR/Cas12 и препарат для выявления РНК вируса SARS-CoV-2 в ультранизких концентрациях | 2021 |
|
RU2764015C1 |
| Способ получения препарата рибонуклеопротеинового комплекса CRISPR-Cas и препарат для выявления гена антибиотикоустойчивости bla-TEM-1B в ультранизких концентрациях | 2023 |
|
RU2820307C1 |
| Способ получения препарата рибонуклеопротеинового комплекса CRISPR-Cas и препарат для выявления гена антибиотикоустойчивости bla-NDM-1 в ультранизких концентрациях | 2024 |
|
RU2839484C1 |
| Система CRISPR-Cas12 для выявления гена антибиотикоустойчивости bla-TEM-1B в ультранизких концентрациях | 2023 |
|
RU2829103C1 |
| Способ обнаружения РНК вируса SARS-CoV-2 в ультранизких концентрациях и специфические олигонуклеотиды для использования в способе | 2021 |
|
RU2764021C1 |

Группа изобретений относится к области генной инженерии и биотехнологии, а именно к получению рибонуклеопротеиновых комплексов системы CRISPR-Cas. Предложены способ получения препарата рибонуклеопротеинового комплекса CRISPR-Cas и препарат рибонуклеопротеинового комплекса CRISPR-Cas. Проводят синтез направляющей РНК с SEQ ID NO: 1-5. Объединяют Cas-белок семейства CRISPR-Cas LbCpf1 из Lachnospiraceae в комплекс с по меньшей мере одной полученной направляющей РНК. Изобретения обеспечивают выявление единичных копий РНК вируса гепатита С генотипов 1b и 3a. 2 н. и 4 з.п. ф-лы, 11 ил., 6 табл., 5 пр.
1. Способ получения препарата рибонуклеопротеинового комплекса CRISPR-Cas, отличающийся тем, что содержит стадии:
(i) синтеза направляющей РНК с SEQ ID NO: 1-5;
(ii) объединения Cas-белка семейства CRISPR-Cas LbCpf1 из Lachnospiraceae в комплекс с по меньшей мере одной направляющей РНК, полученной на стадии (i); и при необходимости
(iii) лиофильной сушки рибонуклеопротеинового комплекса CRISPR-Cas, полученного на стадии (ii), с получением, таким образом, препарата рибонуклеопротеинового комплекса CRISPR-Cas.
2. Способ по п.1, где синтез направляющих РНК осуществляют методом in vitro транскрипции с последующим переосаждением продуктов реакции in vitro транскрипции из реакционной смеси добавлением хлорида натрия до конечной концентрации 400 мM и равного объема изопропилового спирта.
3. Способ по любому из пп.1, 2, где непосредственно перед объединением с Cas-белком направляющую РНК прогревают при 90°С в течение 5 минут и позволяют медленно остыть до комнатной температуры, что обеспечивает формирование корректной конформации шпильки, содержащейся в направляющей РНК.
4. Препарат рибонуклеопротеинового комплекса CRISPR-Cas для выявления РНК вируса гепатита С генотипов 1b и 3a, полученный способом по любому из пп.1-3, содержащий Cas-белок семейства CRISPR-Cas LbCpf1 из Lachnospiraceae в комплексе с по меньшей мере одной направляющей РНК с SEQ ID NO: 1-5.
5. Препарат по п.4, где препарат представляет собой раствор указанного рибонуклеопротеинового комплекса CRISPR-Cas.
6. Препарат по п.4, где указанный препарат лиофилизирован.
Авторы
Даты
2023-07-05—Публикация
2022-11-29—Подача