[0001] Настоящее изобретение в целом относится к способу, аналитическому устройству и набору для мультиплексных биохимических анализов, позволяющим сделать результаты тестирования, полученные в различных лабораториях, сравнимыми. В частности, настоящее изобретение относится к многократному применению различных контрольных образцов, что в совокупности позволяет как гармонизировать результаты тестирования, так и выполнить диагностику оборудования для тестирования.
[0002] Биохимические измерения широко применяются для диагностики, мониторинга и лечения заболеваний. Хотя большинство биохимических анализов выдают одинарные выходные данные, то есть измеряют присутствие или концентрацию одного определенного биомаркера, расширяется применение мультиплексных анализов. В мультиплексном анализе определяют присутствие или концентрацию множества биомаркеров по существу одновременно (например, в тот же день или одну неделю) в одной или более аликвот одного образца. Каждый биомаркер можно анализировать с применением одного и того же устройства, или может потребоваться несколько устройств для анализа всего набора биомаркеров. Полученные данные затем объединяют для формирования выходных данных или выхода (например, единой оценки риска или некоторого паттерна, указывающего на характеристики образца). Мультиплексные анализы повышают эффективность, но усложняют процедуру калибровки.
[0003] В частном типе биохимического анализа, иммуноанализе, используют антитела для специфического определения присутствия или концентрации белка или другого антигена. Иммуноанализы могут быть конкурентными или неконкурентными, твердофазными или жидкофазными, и могут потребовать или не потребовать этапа разделения. Для целей обнаружения в иммуноанализах может применяться меченый антиген или меченое антитело и один или более участков, где происходят поддающиеся обнаружению реакции.
[0004] Специалисту хорошо известно, что иногда выходные данные биохимического анализа могут иметь произвольный характер. В качестве выходных данных может применяться концентрация биомаркера. Однако также возможно определить количество биохимического вещества в единицах эффективности, как это делается для белкового препарата Фактор IX (производства компании Baxter). Люди с дефицитом этого белка страдают гемофилией B, нарушением свертывания крови. Фактор IX количественно выражают в произвольных единицах эффективности фермента, так что определенное количество этого лекарственного препарата обеспечивает определенную ферментативную активность независимо от фактической концентрации фактора IX. В рамках этого биохимического анализа есть несколько систем форматов и стандартов выходных данных. Как правило, у этих выходных данных варьируют единицы измерения и различается линейность отклика. Эта вариабельность затрудняет оценку любых выходных биохимических данных. В случаях, когда необходимо объединить несколько результатов анализов, ситуация становится еще более сложной, и если разные лаборатории проводят один и тот же анализ с применением разных типов аналитических приборов, неизбежная вариабельность между различными лабораториями, различными приборами и различными типами приборов увеличивает общую вариабельность.
[0005] Медицинское сообщество признало, что необходима гармонизация, и были внедрены процедуры для контроля и стандартизации качества результатов конкретного биохимического анализа конкретной лаборатории. Многие клинические/аналитические лаборатории проводят поверку анализа на трех уровнях. Согласно первому уровню, в каждый анализ обычно встроены один или более калибровочных образцов, чтобы получить известные данные для интерполяции результатов для неизвестных образцов. Если калибровочная кривая не соответствует заранее определенным стандартам, результаты анализа считаются ненадежными. Согласно второму уровню, существуют образцы положительного контроля местного производства с известными свойствами, независимые от калибровочных образцов. Если калибровочная кривая не может воспроизвести известные свойства образцов положительного контроля, результаты анализа считаются ненадежными. Третий уровень, часто называемый "квалификационная проверка", включает использование внешней доверенной стороны для предоставления контрольных образцов, и если калибровочная кривая не способна воспроизвести известные свойства внешних контрольных образцов, результаты анализа считаются ненадежными.
[0006] Одним из примеров контроля третьего уровня является Коллегия американских патологов (College of American Pathologists, CAP), организация, миссией которой является содействие и продвижение передового опыта в практике патологии и лабораторной медицины во всем мире (www.cap.org). CAP имеет программу аккредитации, которая предоставляет клиническим лабораториям доступ к внешним контрольным образцам, с целью гарантировать, что указанная лаборатория действительно проводит клинические лабораторные исследования надлежащим образом. Например, CAP требует, чтобы все лаборатории, которые проводят измерения общего сывороточного IgE, демонстрировали удовлетворительные результаты в одном из нескольких замаскированных внешних межлабораторных инспекций для проверки квалификации. Такие инспекции для проверки квалификации проводятся несколько раз в год. В исключительных случаях у "провальных" клинических лабораторий в США, не прошедших несколько последовательных инспекций, лицензия может быть отозвана.
[0008] Один пример описан в отчете “Proficiency Survey-Based Evaluation of Clinical Total and Allergen-Specific IgE Assay Performance”, Robert G Hamilton, опубликованного в Arch Pathol Lab Med. 2010; 134: 975–982, которая включена в настоящий документ в качестве ссылки. Программа, описанная в этой публикации, относится как к определению общего IgE, так и к определению аллергенспецифического IgE приблизительно в 200 сертифицированных клинических лабораториях с применением оборудования от нескольких поставщиков. Один и тот же набор образцов был предоставлен всем участвующим лабораториям и проанализирован централизованно, как описано в этом документе. Было отмечено, что для общего IgE большинство анализов обеспечивают хорошую эффективность, хотя одна технология давала систематически более низкие результаты концентрации при высоких уровнях IgE (рис. 1 в “Proficiency Survey-Based Evaluation of Clinical Total and Allergen-Specific IgE Assay Performance”). Для аллергенспецифического IgE различия в результатах концентрации между различными лабораториями и технологиями были намного больше. Так, для кошачьего аллергена, одна технология давала среднюю концентрацию IgE в отобранном образце, превышающую 14 кЕд/л, тогда как две другие технологии давали среднюю концентрацию IgE в том же отобранном образце приблизительно 4 кЕд/л (рис. 2 в “Proficiency Survey-Based Evaluation of Clinical Total and Allergen-Specific IgE Assay Performance”). Это означает, что сертифицированные клинические лаборатории могут для одного и того же образца давать значения концентрации аллерген-специфического IgE, различающиеся более чем в три раза. Обычным расхождением между технологиями, согласно тому же раскрытию, является 50% разница между самым высоким и самым низким зафиксированным значением концентрации (усредненным по нескольким клинически сертифицированным пользователям каждой технологии) для одного и того же образца. Важно отметить, что такая разница между самым высоким и самым низким зафиксированными значениями концентрации считается приемлемой в свете доступного международного стандарта Всемирной организации здравоохранения (ВОЗ), как видно из раскрытия “3rd International Standard for serum IgE. Report of the international collaborative study to evaluate the candidate preparation”, Susan J Thorpe с соавторами, причем данное раскрытие обозначено как WHO/BS/2013.2220. Международный стандарт обычно предоставляется с целью стандартизации результатов различных лабораторий.
[0008] Потенциальным следствием такой приемлемой вариабельности между лабораториями для анализов IgE является наличие обширных методических материалов, таких как “Serological IgE Analyses in the Diagnostic Algorithm for Allergic Disease.”, Hamilton and Oppenheimer, опубликованные в J Allergy Clin Immunol Pract. Nov-Dec; 3(6):833-40. doi: 10.1016/j.jaip.2015.08.016. Методические материалы такого типа подготавливают пользователя к интерпретации данных, которые могут отличаться в зависимости от места получения, вместо функциональной гармонизации результатов анализов между различными лабораториями.
[0009] Другой пример области, в которой используется квалификационная проверка, раскрыт в работе “Standardization of Measurements for Cholesterol, Triglycerides, and Major Lipoproteins”, Warnick с соавторами, опубликованной в Lab Medicine (август 2008 г., том 39, номер 8; DOI: 10.1309/6UL9RHJH1JFFU4PY). В этой публикации обсуждается стандартизация и квалификационная проверка анализа холестерина и подобных молекул. Это раскрытие показывает, что квалификационная проверка для анализа общего холестерин давала очень хорошие результаты, участвующие лаборатории соответствовали критериям приемлемости в 97% проведенных тестов. Вместе с тем определение отдельных классов холестерина, таких как холестерин липопротеинов низкой плотности (ЛПНП) и липопротеинов высокой плотности (ЛПВП), было более вариабельным, и только 84-90% тестов соответствовали критериям приемлемости. Это означает, что по меньшей мере 1 из 10 образцов пациентов подвергается риску быть проанализированным в анализе, выходящим за пределы признанных критериев приемлемости эффективности для определения холестерина.
[0010] Подобные наблюдения были сделаны для диагностики и/или оценки риска рака простаты. В отчете “Between-method differences in prostate-specific antigen assays affect prostate cancer risk prediction by nomograms”, C Stephan с соавторами, Clin. Chem. 2011 Jul;57(7):995-1004. doi: 10.1373/clinchem.2010.151472, который включен в настоящее описание в качестве ссылки, определение риска рака простаты было оценено с использованием номограмм с применением значений PSA (ПСА), полученных с различных платформ. Это наблюдение особенно актуально, для случая, когда для получения значений биомаркеров в одном и том же мультиплексном анализе используются различные инструментальные платформы.
[0011] Настоящее изобретение применимо для мультиплексных анализов независимо от количества аналитических устройств, используемых для получения данных. Пример мультиплексного анализа, в котором все данные получены с помощью одного аналитического устройства, раскрыт в отчете “Validation of a multiplex chip-based assay for the detection of autoantibodies against citrullinated peptides.”, Hansson с соавторами, опубликованном в Arthritis Res Ther. 2012 Oct 1;14(5):R201, который включен в настоящий документ посредством ссылки. Пример мультиплексного анализа, в котором данные получены с помощью различных аналитических устройств, раскрыт в заявке на патент WO 2014079865, которая включена в настоящий документ в качестве ссылки.
[0012] Вышеописанные характеристики анализов одного аналита (т.е. анализов, которые определяют количественно концентрацию одного компонента, например концентрацию PSA в сыворотке) являются трудными для интерпретации, но контролируемыми. При объединении нескольких аналитов в мультиплексный тест аналогичные сложности будут возникать для каждого аналита, присутствующего в мультиплексной панели, что приведет к значительным проблемам как при проведении мультиплексных анализов, так и при интерпретации данных мультиплексных анализов. Настоящее изобретение направлено на решение таких проблем, чтобы улучшить эффективность мультиплексных анализов.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0013] Согласно одному аспекту настоящее изобретение в соответствии с различными вариантами реализации улучшает контроль третьего уровня для мультиплексных анализов за счет многократного применения внешних контрольных образцов, также называемых стандартами гармонизации, и за счет включения этих стандартов гармонизации в интерпретацию анализа.
[0014] Согласно одному варианту реализации настоящего изобретения предложен способ гармонизации результатов тестирования биологических образцов в мультиплексных биохимических анализах, при котором присутствие и/или концентрация каждого из набора множества биомаркеров определяют по существу одновременно в одном и том же образце. Данный способ включает количественное определение присутствия и/или концентрации по меньшей мере двух различных биомаркеров в биологическом образце и в образце стандарта гармонизации, независимо в каждом образце, с помощью определенного устройства для мультиплексного биохимического анализа, реализованного в аналитическом приборе определенного типа; получение результатов тестирования образцов в компьютерный модуль принятия решений для гармонизации результатов тестирования этого биологического образца; и преобразование результатов тестирования биологического образца с применением компьютерного модуля принятия решений. Преобразование результатов тестирования биологического образца включает преобразование, по меньшей мере, результатов тестирования образца стандарта гармонизации в обобщенные единицы (generalized units, GE). Наконец, преобразованные результаты образца стандарта гармонизации используют для приведения результатов биологического образца к обобщенным единицам (GE).
[0015] Применение обобщенных единиц (GE) устраняет систематическую ошибку, улучшает сопоставимость результатов между лабораториями и технологическими платформами и позволяет централизованно интерпретировать результаты.
[0016] Согласно другому варианту реализации настоящего изобретения предложено определенное устройство для мультиплексного биохимического анализа, адаптированное для реализации в аналитическом приборе определенного типа и определения присутствия или концентрации по меньшей мере двух разных биомаркеров в биологическом образце и в образце стандарта гармонизации, независимо в каждом образце, которые могут быть количественно определены с помощью этого аналитического прибора.
[0017] Согласно одному варианту реализации устройство для биохимического анализа включает 10 или более независимых и одновременных анализов, причем стандарт гармонизации содержит по меньшей мере 90% биомаркеров, которые являются частью анализа. Согласно альтернативным вариантам реализации, может быть предпочтительным постоянно изменять свойства стандарта гармонизации, чтобы регулярно тестировать несколько аспектов мультиплексного анализа.
[0018] Согласно одному варианту реализации устройство для биохимического анализа содержит твердую фазу с иммобилизованными на ней по меньшей мере двумя различными категориями лигандов, при этом каждая категория лигандов может быть иммобилизована на одном компоненте или на нескольких компонентах, которые вместе составляют устройство, и :
- первая категория лигандов специфически связывается с биомаркером рака предстательной железы (РПЖ) и включает множество различных лигандов, специфически связывающихся с каждым из множества различных биомаркеров РПЖ, предпочтительно по меньшей мере с одним из PSA, iPSA, tPSA, fPSA, и hK2, и необязательно MSMB и/или MIC-1; и
- вторая категория лигандов специфически связывается с однонуклеотидным полиморфизмом, связанным с раком простаты (SNPpc), и включает множество различных лигандов, специфически связывающихся с каждым из множества различных SNPpc, таких как по меньшей мере один из rs11672691, rs11704416, rs3863641, rs12130132, rs4245739, rs3771570, rs7611694, rs1894292, rs6869841, rs2018334, rs16896742, rs2273669, rs1933488, rs11135910, rs3850699, rs11568818, rs1270884, rs8008270, rs4643253, rs684232, rs11650494, rs7241993, rs6062509, rs1041449, rs2405942, rs12621278, rs9364554, rs10486567, rs6465657, rs2928679, rs6983561, rs16901979, rs16902094, rs12418451, rs4430796, rs11649743, rs2735839, rs9623117 и rs138213197.
[0019] Согласно одному варианту реализации на твердой фазе дополнительно иммобилизована третья категория лигандов, которая специфически связывается с SNP-ассоциированным биомаркером (SNPbm), и включает один или множество различных лигандов, специфически связывающихся с одним или каждым из множества различных SNPbm, таких как по меньшей мере один из rs1227732, rs3213764, rs1354774, rs2736098, rs401681, rs10788160, rs11067228, rs1363120, rs888663 и rs1054564.
[0020] Согласно другому варианту реализации настоящего изобретения предложен набор, содержащий устройство для биохимического анализа в соответствии с описанными выше различными вариантами реализации.
[0021] Согласно другому варианту реализации настоящего изобретения предложена система для гармонизации результатов тестирования биологических образцов в мультиплексных биохимических анализах, причем эта система включает определенное устройство для мультиплексного биохимического анализа, реализованное в аналитическом приборе определенного типа, адаптированное как для количественной оценки присутствия или концентрации по меньшей мере двух разных биомаркеров в биологическом образце, так и по меньшей мере двух разных биомаркеров в образце стандарта гармонизации, независимо в каждом образце, компьютерный модуль принятия решений, содержащий средство для получения результатов тестирования образца в компьютерный модуль принятия решений для гармонизации результатов тестирования биологического образца; и средство для преобразования результатов тестирования биологического образца с применением компьютерного модуля принятия решений. Средство преобразования результатов тестирования биологического образца приспособлено для преобразования результатов тестирования образца стандарта гармонизации в обобщенные единицы и для приведения результатов биологического образца к обобщенным единицам.
[0022] Согласно второму аспекту изобретения предложен компьютерный программный продукт, содержащий инструкции для инициирования выполнения компьютером инструкций для выполнения этапов способа, предоставленных модулем принятия решений.
[0023] В одном варианте реализации в систему включен компьютерный модуль принятия решений.
[0024] В одном варианте реализации все компоненты компьютерного модуля принятия решений обеспечивает компьютерный программный продукт, интегрированный в единое устройство, которым может быть сервер, персональный компьютер, аналитический прибор или любое другое устройство со способностью к обработке данных.
[0025] Согласно одному аспекту стандарты гармонизации могут быть привязаны к производственным стандартам.
[0026] Согласно одному аспекту может быть предусмотрена обязанность поставщика новой партии стандартов гармонизации выполнять гармонизацию, как описано выше, перед доставкой заказчику.
[0027] Преимущество различных вариантов реализации настоящего изобретения состоит в том, что они облегчают сравнение результатов тестирования, полученных в разных лабораториях.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0028] Далее варианты реализации настоящего изобретения будут описаны со ссылкой на чертежи, из которых:
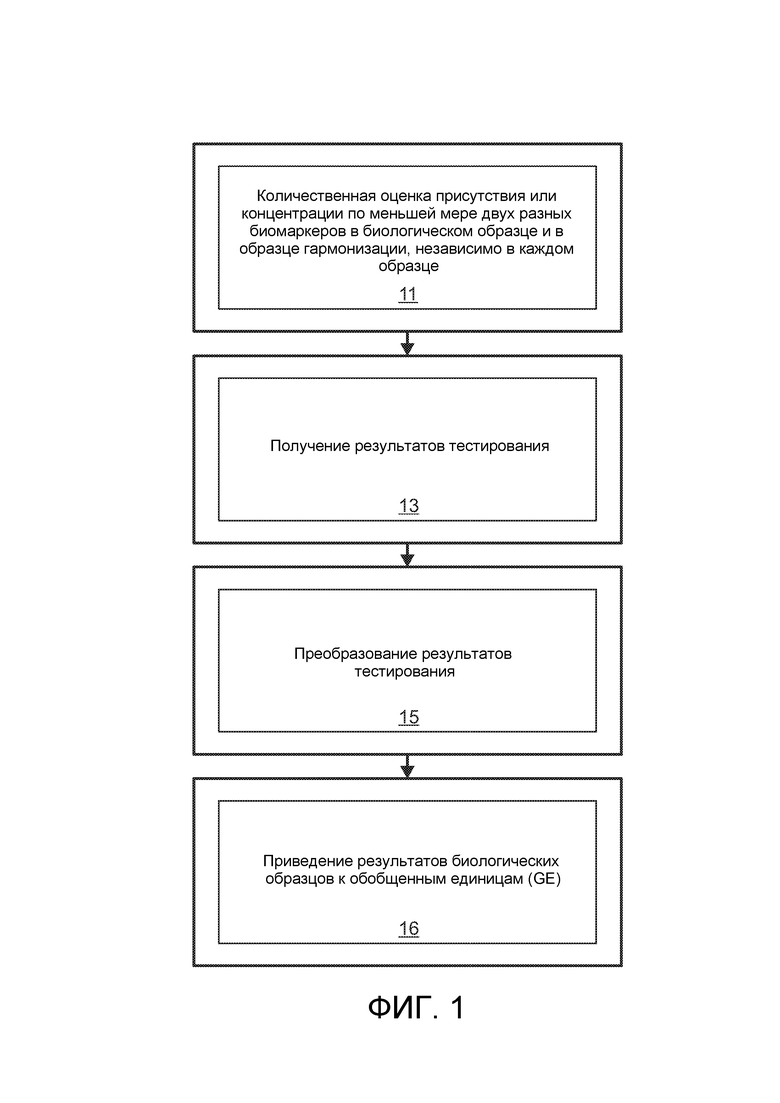
[0029] На фиг. 1 показана блок-схема способа согласно одному варианту реализации изобретения.
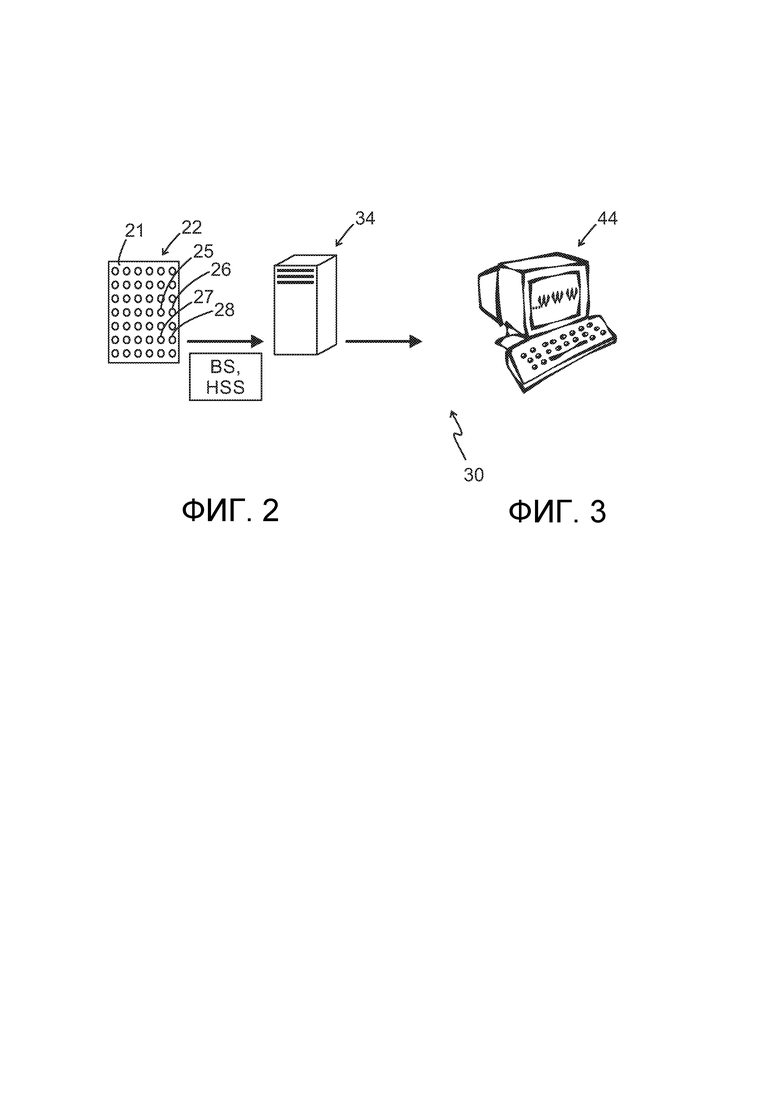
[0030] На фиг. 2 показано определенное устройство для мультиплексного биохимического анализа согласно одному варианту реализации изобретения.
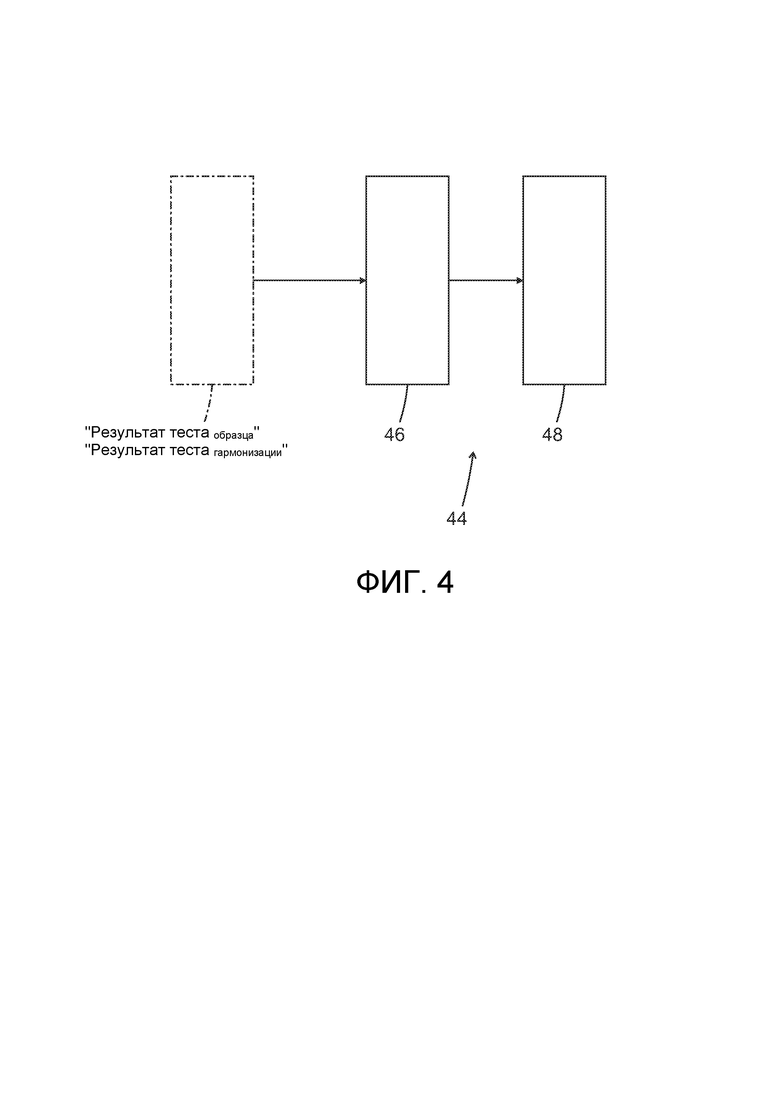
[0031] На фиг. 3 показана блок-схема системы согласно одному варианту реализации изобретения.
[0032] На фиг. 4 показана блок-схема компьютерного модуля принятия решений.
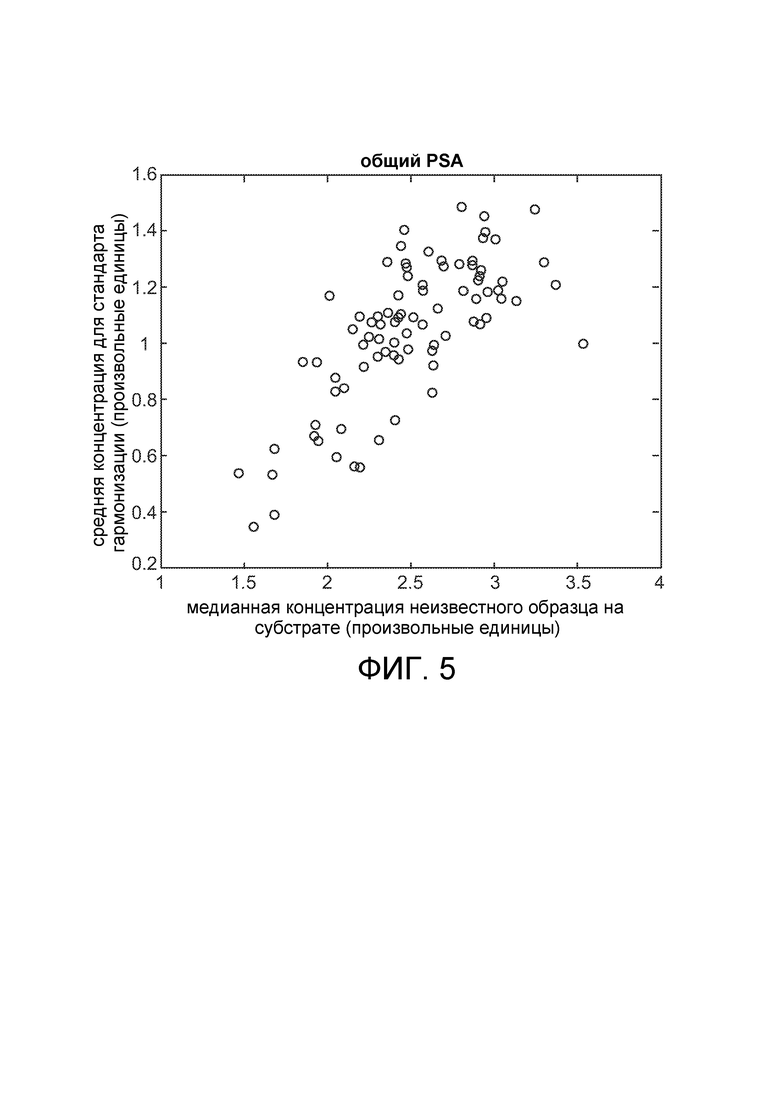
[0033] На фиг. 5 показано среднее значение общего PSA для стандартов гармонизации (в произвольных единицах) по оси ординат и медианное значение общего PSA для неизвестного образца (т.е. образца пациента) на том же субстрате по оси абсцисс (в тех же произвольных единицах).
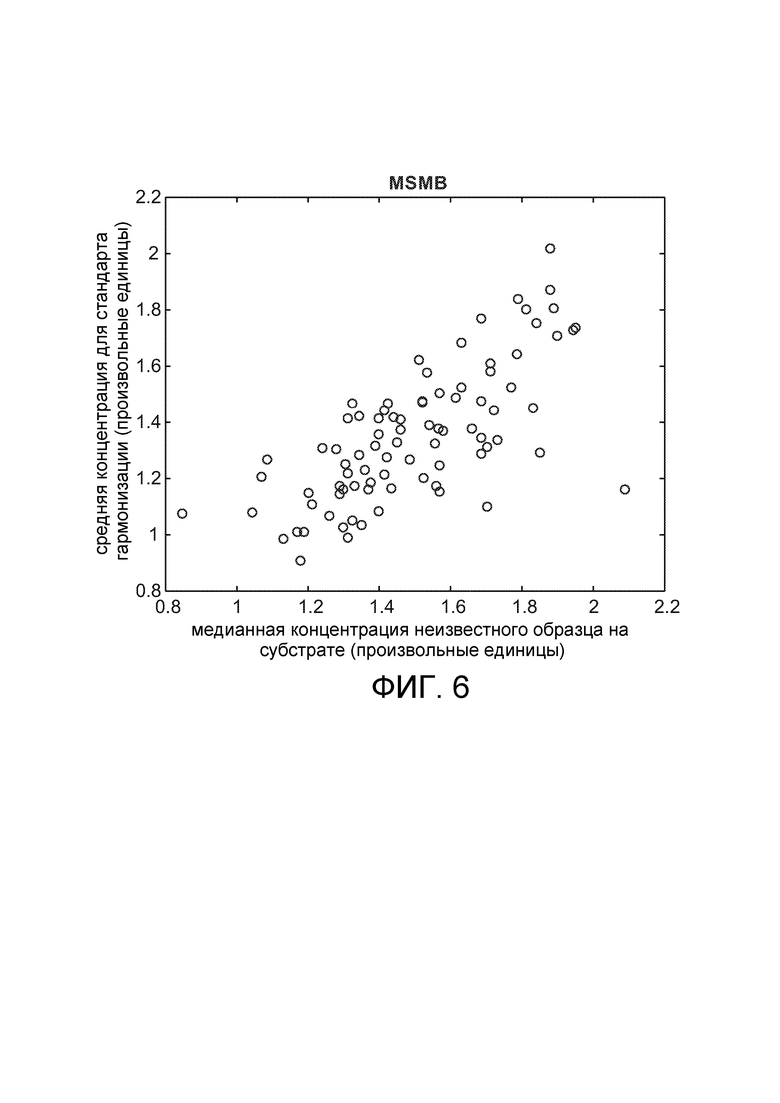
[0034] На фиг. 6 показано среднее значение MSMB для стандартов гармонизации (в произвольных единицах) по оси ординат и медианное значение MSMB (микросеминопротеин-бета) для неизвестного образца (т.е. образца пациента) на том же субстрате по оси абсцисс (в тех же произвольных единицах).
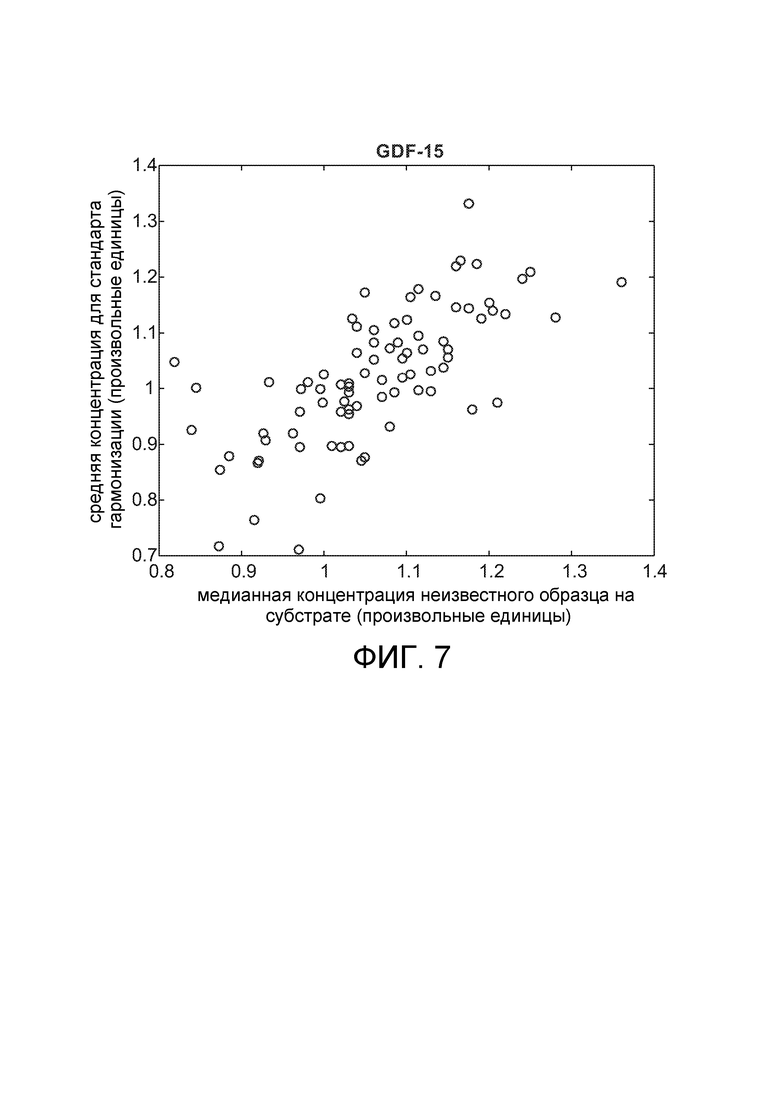
[0035] На фиг. 7 показано среднее значение GDF-15 (фактор роста и дифференцировки - 15) для стандартов гармонизации (в произвольных единицах) по оси ординат и медианное значение GDF-15 для неизвестного образца (т.е. образца пациента) на том же субстрате по оси абсцисс (в тех же произвольных единицах).
ПОДРОБНОЕ ОПИСАНИЕ ВАРИАНТОВ РЕАЛИЗАЦИИ
[0036] Для целей этого раскрытия и для ясности даны следующие определения:
[0037] Термин "диагностический анализ" относится к обнаружению (детектированию) присутствия или характеризации патологического состояния. Его можно употреблять взаимозаменяемо с терминами "диагностический способ" или "диагностический тест". Диагностические тесты могут различаться по чувствительности и специфичности.
[0038] Термин "прогностический анализ" относится к оценке риска развития патологического состояния. Его можно употреблять наравне с терминами "прогностический способ" или "прогностический тест". Прогностические тесты, при прогнозировании конкретного события, аналогичны диагностическим тестам и могут в таких случаях различаться по своей чувствительности и специфичности. Одним из таких примеров является прогностический анализ, прогнозирующий необходимость активной терапии.
[0039] Термин "аналитическое устройство" относится к физическому устройству для проведения анализа, которое может содержать или более компонентов, вместе составляющих это устройство.
[0040] Одним из показателей полезности диагностического инструмента является "площадь под характеристической кривой рабочих характеристик приемника (ROC-кривой)", которая широко известна как статистика ROC-AUC. Этот широко распространенный показатель учитывает как чувствительность, так и специфичность инструмента. Как правило, ROC-AUC находится в диапазоне от 0,5 до 1,0, где значение 0,5 указывает на то, что инструмент не имеет диагностической ценности, а значение 1,0 указывает на то, что инструмент имеет 100% чувствительность и 100% специфичность.
[0041] Термин "чувствительность" относится к доле всех субъектов, нуждающихся в активном лечении, которые верно идентифицированы как таковые (что равно количеству истинноположительных результатов, деленному на сумму количества истинноположительных и ложноотрицательных результатов).
[0042] Термин "специфичность" относится к доле всех субъектов, не нуждающихся в активном лечении (т.е. для которых достаточно динамического наблюдения), которые верно идентифицированы в таковом качестве (что равно количеству истинноотрицательных результатов, деленному на сумму количества истинноотрицательных и ложноотрицательных результатов).
[0043] Термин "аналит" относится к целевому биохимическому веществу/биомаркеру, который подлежит обнаружению и/или количественному определению в анализе. Примеры аналитов: белки, олигонуклеотиды или химические соединения.
[0044] Термин "распознающий элемент" относится к объекту, способному взаимодействовать с конкретным аналитом. Одним неограничивающим примером распознающего элемента является антитело, которое специфически связывает определенный аналит. Другим неограничивающим примером распознающего элемента является аптамер, который специфически связывает определенный аналит.
[0045] Термин "биомаркер" означает белок, часть белка, пептид, полипептид, олигонуклеотид (ДНК или РНК), химическое соединение, метаболиты, катаболиты или циркулирующие клетки (такие как циркулирующие опухолевые клетки в качестве одного неограничивающего примера), который можно использовать в качестве биологического маркера, например в диагностических целях. В анализе биомаркер обычно является аналитом.
[0046] Термин "стандарт гармонизации" относится к образцу, свойства которого известны производителю, но обычно неизвестны пользователю. Стандарт гармонизации обеспечивает охват не менее 50% отдельных анализов или биомаркеров, которые анализируются в мультиплексном анализе.
[0047] Термин "мультиплексный биохимический анализ" относится к анализу, который объединяет по меньшей мере два разных значения биомаркера (например, концентрацию биомаркера в биологическом образце или обнаруживаемое присутствие биомаркера в биологическом образце, в качестве двух неограничивающих примеров) с целью оценки состояния донора биологического образца (например, оценки риска ракового заболевания, в качестве неограничивающего примера). Значения биомаркеров могут быть получены с применением нескольких компонентов анализа, каждый из которых дает по меньшей мере одно значение биомаркера и вместе составляет мультиплексный анализ, или могут быть получены с применением только одного устройства для анализа, дающего все желаемые значения биомаркеров, или любой другой их комбинации, которая в совокупности дает все желаемые значения биомаркеров. Мультиплексный биохимический анализ в контексте настоящего раскрытия дает все желаемые значения биомаркеров в течение периода времени, который близок к самому продолжительному времени хранения данного биологического образца. В случае образца крови, который перерабатывается в плазму или сыворотку, типичное самое продолжительное время хранения в холодильнике составляет для анализов белковых биомаркеров приблизительно 2-4 недели, потому что при более длительном хранении разложение самого образца может повлиять на точность определяемых значений биомаркеров. В частных вариантах реализации мультиплексный биохимический анализ объединяет значения по меньшей мере десяти различных биомаркеров, значения по меньшей мере двадцати различных биомаркеров, значения по меньшей мере тридцати различных биомаркеров, значения по меньшей мере сорока различных биомаркеров или значения по меньшей мере пятидесяти различных биомаркеров.
[0048] База данных однонуклеотидных полиморфизмов (dbSNP) представляет собой архив генетических вариаций внутри и между различными видами, разработанный и размещенный на своих ресурсах Национальным центром биотехнологической информации (NCBI) в сотрудничестве с Национальным исследовательским институтом генома человека (NHGRI), которые оба расположены в США. Хотя название этой базы данных подразумевает коллекцию только одного класса полиморфизмов (то есть однонуклеотидных полиморфизмов (SNP)), на самом деле она содержит целый ряд молекулярных вариаций. Каждая уникальная представленная запись SNP получает идентификационный номер SNP ("rs#"; "refSNP-кластер"). В настоящей заявке SNP в основном идентифицируются с помощью номеров rs#.
[0049] Далее мы обращаемся к фиг. 1, которая показывает блок-схему способа согласно одному варианту реализации раскрытия.
[0050] На первом этапе а) присутствие или концентрацию по меньшей мере двух разных биомаркеров в биологическом образце BS и в образце стандарта гармонизации HSS, независимо в каждом образце BS, HSS определяют количественно 11 с помощью определенного устройства для мультиплексного биохимического анализа, реализованного в аналитическом приборе определенного типа, оба из которых более подробно описаны ниже со ссылкой на фиг. 2 и 3.
[0051] Затем на втором этапе b) результаты тестирования "Результат теста образца", "Результат теста гармонизации" образцов BS, HSS принимают 13 в компьютерный вычислительный модуль 44 для преобразования 15 на этапе c) результатов тестирования "Результат теста образца", полученных для образца BS, и гармонизации результатов тестирования "Результат теста образца" биологического образца BS.
[0052] Преобразование 15 результатов тестирования "Результат теста образца" биологического образца BS включает в себя преобразование, по меньшей мере, результатов тестирования "Результат теста гармонизации" образца стандарта гармонизации HSS в обобщенные единицы (GE). Наконец, результаты тестирования "Результат теста образца" биологического образца BS приводят к обобщенным единицам (GE).
[0053] Согласно одному варианту реализации этапы от а) до с) повторяют по меньшей мере дважды в течение определенного периода времени.
[0054] Согласно одному варианту реализации этапы с а) по с) повторяют с другим биологическим образцом и с применением результатов "Результат теста гармонизации" по меньшей мере двух стандартов гармонизации HSS, количественно определенных в различные моменты времени, в качестве входных данных для преобразования 15 в обобщенные единицы (GE).
[0055] Согласно одному варианту реализации этапы с а) по с) повторяют с другим биологическим образцом BS и с другим стандартом гармонизации HSS, и с применением результатов "Результат теста гармонизации" по меньшей мере двух стандартов гармонизации HSS, количественно определенных в различные моменты времени, в качестве входных данных для преобразования 15 в обобщенные единицы (GE).
[0056] Описан неограничивающий пример. Анализируют биологический образец для измерения биомаркеров от 1 до n в образце, при этом измеренные количества биомаркеров в образце обозначены SM1 - SMn, где n может быть целым числом от 2 до 10, 20, 30, 40, 50 или более. Исследуют образец гармонизации с биомаркерами от 1 до n (или больше или меньше биомаркеров) в тех же условиях (т.е. в той же лаборатории, с тем же оборудованием и оператором), при этом измеренные количества биомаркеров обозначены как HM1 - HMn. Используя компьютерный модуль принятия решений, измеренные количества биомаркеров в образце гармонизации преобразуют в обобщенные единицы путем сравнения с известными обобщенными единицами KGE1 - KGEn для биомаркеров образца гармонизации и создания функции/алгоритма на основании различий между всеми измеренными биомаркерами гармонизации HM1 - HMn и известными обобщенными единицами KGE1 - KGEn. Эту функция/алгоритм затем используют для преобразования SM1 - SMn в обобщенные единицы для биомаркеров образца, SGE1 - SGEn, которые затем могут использоваться для диагностической оценки.
[0057] Гармонизацию используют для корректировки различий между технологиями, различий между лабораториями и различий между одноразовыми устройствами для анализа. Если и HM1, и HM2 для конкретной лаборатории имеют ожидаемые значения (указанная производителем истинная концентрация маркеров в каждом стандарте гармонизации), то будет применяться только поправка на различия между технологиями. Например, известно, что определенные платформы определения PSA (простатоспецифический антиген) имеют систематические различия с занижением на 5-10%. Поэтому, если HM1 и HM2 измеряют на таком устройстве, ожидается, что измеренные HM1 и HM2 будут на 10% ниже, чем известные обобщенные единицы, и, следовательно, для всех образцов потребуется корректировка путем умножения на 1,1 для соответствия профилю измерения данных, используемого для создания алгоритма. Далее, если HM1,… HMn спорадически отклоняются от ожидаемых значений, проблема может быть в одноразовых устройствах для анализа, то есть, при применении некоторых одноразовых устройств концентрация значительно завышается или занижается. Если все HM1, HM2,… HMn последовательно отличаются от ожидаемых значений, можно предположить, что также данные образца последовательно отличаются тем же образом, и значения HM1, HM2,… HMn могут определять преобразование данных образца. Например, если HM1 = 0,5 * ожидаемое значение KGE1 и HM2 = 0,5 * ожидаемое значение KGE2, то все данные образцов умножают на 2 для получения значений в обобщенных единицах. Таким образом, в упрощенном виде (значение образца в обобщенных единицах) = (измеренное значение образца)/СРЕДНЕЕ (HM1/KGE1; HM2/KGE2;… HMn/KGEn). Следовательно, если HM1 = 2 * KGE1 и то же самое верно для всех других значений HMn/KGEn, то среднее = 2 и измеренные значения образцов следует разделены на 2 для корректировки на неожиданно высокие значения HM1, HM2,… HMn. Очевидно, что в мультиплексной системе описанный этап преобразования является достаточно сложным.
[0058] KGE1 - KGEn и HM1 - HMn, которые имеют небольшие различия (меньше заданного минимума), могут указывать на присутствие шума в системе измерения, и компьютерный модуль принятия решений может быть запрограммирован так, чтобы не применять поправки для различий меньше заданного минимума (отражающего совокупный шум), т. е. система имеет ограничение шума. С другой стороны, для KGE1 - KGEn и HM1 - HMn с большими различиями компьютерный модуль принятия решений может быть запрограммирован так, чтобы предупреждать пользователя, когда наблюдаются большие различия (например, превышающие заранее определенный максимум), и может быть сделано одно из нескольких предупреждений. Например, стохастические/случайные и/или большие вариации соотношений HM/KGE могут указывать на небрежность операторов, низкое и/или меняющееся качество одноразовых устройств и т. д., в то время как систематические и последовательные отклонения могут указывать на то, что в рассматриваемой лаборатории что-то систематически делается отлично от других, и может потребоваться обновление значений KGE для этой конкретной лаборатории. Отношения HM/KGE также могут иметь сезонные колебания, например, результаты анализа зимой отличаются от показателей анализа летом, в качестве неограничивающего примера.
[0059] Согласно одному варианту реализации этапы с а) по с) повторяют с другим биологическим образцом (BS) или другим стандартом гармонизации (HSS), и с применением результатов "Результат теста гармонизации" по меньшей мере двух стандартов гармонизации (HSS), определенных количественно в разные моменты времени, в качестве выходных данных для преобразования (15) в обобщенные единицы (GE).[0060] Далее обратимся к фиг. 2.
[0061] На фиг. 2 показан вариант реализации определенного устройства 22 для мультиплексного биохимического анализа, выполненного с возможностью реализации в аналитическом приборе 34 определенного типа и имеющего присутствие или концентрацию по меньшей мере двух разных биомаркеров 25, 26 в биологическом образце BS и двух разных биомаркеров 27, 28 в образце стандарта гармонизации HSS. Одним неограничивающим примером устройства 22 для мультиплексного биохимического анализа является микрочип. Микрочип 22 обычно содержит твердую подложку 21, на которой расположено множество распознающих элементов 25, 26, 27, 28, каждый из которых способен специфически взаимодействовать с различными определенными аналитами и иммобилизовать их. Обычно в качестве распознающих элементов используют антитела. После связывания аналитов со их соответствующими элементами распознавания твердую подложку промывают и вводят реагент для обнаружения в контакт с твердой подложкой. Реагент для обнаружения обычно представляет собой меченую молекулу, связывающуюся с одним или более аналитом, благодаря чему присутствие аналита обнаруживается посредством этой метки. При проведении анализа с помощью микрочипа типичный рабочий процесс включает контактирование твердой подложки с биологическим образцом с последующей инкубацией в течение 10-60 минут. После этого твердую подложку 21 промывают жидкостью, не содержащей никаких целевых аналитов. Добавляют меченый реагент для обнаружения (например, реагент, меченный флуоресцентной молекулой) и инкубируют в течение 10-60 минут. После окончательной промывки твердой подложки 21 микрочип 22 можно сканировать с помощью флуоресцентного сканера, чтобы выявить, какие пятна на микрочипе 22 продемонстрировали присутствие аналита.
[0062] Затем аналиты подвергают количественному определению в аналитическом приборе 34 в соответствии с этапом а), описанным выше со ссылкой на фиг. 1.
[0063] Согласно одному варианту реализации устройство для биохимического анализа содержит один или более твердофазных компонентов 21, на которых иммобилизованы по меньшей мере две разные категории лигандов, из которых:
- первая категория лигандов специфически связывается с биомаркером РПЖ и включает множество различных лигандов, специфически связывающихся с каждым из множества различных биомаркеров РПЖ, предпочтительно по меньшей мере с одним из PSA, iPSA, tPSA, fPSA и hK2, и, необязательно, MSMB и/или MIC-1; и
- вторая категория лигандов специфически связывается с SNPpc и включает множество различных лигандов, специфически связывающихся с каждым из множества различных SNPpc, например, по меньшей мере, с одним из rs11672691, rs11704416, rs3863641, rs12130132, rs4245739, rs3771570, rs7611694, rs1894292, rs6869841, rs2018334, rs16896742, rs2273669, rs1933488, rs11135910, rs3850699, rs11568818, rs1270884, rs8008270, rs4643253, rs684232, rs11650494, rs7241993, rs6062509, rs1041449, rs2405942, rs12621278, rs9364554, rs10486567, rs6465657, rs2928679, rs6983561, rs16901979, rs16902094, rs12418451, rs4430796, rs11649743, rs2735839, rs9623117 и rs138213197.
[0064] Согласно одному варианту реализации на твердой фазе 21 дополнительно иммобилизована третья категория лигандов, которые специфически связываются с SNPbm, и включает один или множество различных лигандов, специфически связывающихся с одним или каждым из множества различных SNPbm, например, по меньшей мере, с одним из rs1227732, rs3213764, rs1354774, rs2736098, rs401681, rs10788160, rs11067228, rs1363120, rs888663 и rs1054564.
[0065] Далее мы ссылаемся на фиг. 3, которая показывает систему 30 для гармонизации результатов тестирования биологических образцов в мультиплексных устройствах 22 для биохимического анализа, таких как микрочипы, и реализации способа, описанного выше в отношении варианта реализации, описанного и показанного на фиг. 1.
[0066] Система 30 содержит определенное мультиплексное устройство 22 для биохимического анализа, реализованное в аналитическом приборе определенного типа 34. Устройство 22 для биохимического анализа и аналитический прибор 34 оба,. как правило совместно, адаптированы для выполнения этапа a), т.е. для количественного определения 11 присутствия или концентрация по меньшей мере двух различных биомаркеров в биологическом образце и образце стандарта гармонизации, независимо в каждом образце. Система 30 дополнительно содержит компьютерный модуль принятия решений 44, содержащий компонент 46 для получения 13 результатов тестирования образцов в компьютерный модуль принятия решений 44; и компонент 48 для преобразования 15 результатов тестирования, полученных для биологического образца. Эти компоненты 46, 48 схематично показаны на фиг. 4. Компонент 48 для преобразования 15 результатов тестирования биологического образца выполнен с возможностью преобразования результатов тестирования образца стандарта гармонизации в обобщенные единицы (GE) и для приведения неизвестных результатов биологического образца к обобщенным единицам (GE).
[0067] Согласно аспекту раскрытия, компоненты 46 и 48, которые определяют модуль принятия решений 44 в этом примере, могут быть реализованы с помощью специального программного обеспечения (или встроенного программного обеспечения), выполняемого на одном или более обобщенных или специализированных компьютерных. устройствах. Такое вычислительное устройство может включать в себя один или более процессоров, например ЦП ("Центральный процессор"), ЦСП ("Цифровой сигнальный процессор"), ASIC ("Специализированная интегральная схема, Application-Specific Integrated Circuit"), дискретные аналоговые и/или цифровые компоненты или какое-либо другое программируемое логическое устройство, такое как FPGA ("Программируемая пользователем интегральная матрица"). В этом контексте следует понимать, что каждый "компонент" модуля принятия решений 44 относится к концептуальному эквиваленту этапа способа; не всегда существует однозначное соответствие между компонентами и отдельными частями аппаратных средств или программных процедур. Одна часть аппаратных средств иногда состоит из разных компонентов. Например, процессор может служить одним компонентом при выполнении одной инструкции, но служить другим компонентом при выполнении другой инструкции. Кроме того, в некоторых случаях один компонент может быть реализован одной инструкцией, а в некоторых других случаях - множеством инструкций. Вычислительное устройство может дополнительно включать в себя системную память и системную шину, которая соединяет различные компоненты системы, включая системную память, с процессором. Системная шина может быть любого из нескольких типов шинных структур, включая шину памяти или контроллер памяти, периферийную шину и локальную шину, использующую любую из множества шинных архитектур. Системная память может включать в себя компьютерные накопители в форме энергозависимой и/или энергонезависимой памяти, такой как постоянное запоминающее устройство (ROM), оперативное запоминающее устройство (RAM) и флэш-память. Специализированное программное обеспечение может храниться в системной памяти или на других съемных/несъемных энергозависимых/энергонезависимых компьютерных накопителях, которые включены в вычислительное устройство или доступны для него, например, магнитные носители, оптические носители, карты флэш-памяти, цифровая лента, твердотельное ОЗУ, твердотельное ПЗУ и т. д. Вычислительное устройство может включать в себя один или более интерфейсов связи, таких как последовательный интерфейс, параллельный интерфейс, интерфейс USB, беспроводной интерфейс, сетевой адаптер и т.д. К вычислительному устройству могут быть подключены одно или более устройств ввода-вывода через интерфейс связи, включая, например, клавиатуру, мышь, сенсорный экран, дисплей, принтер, дисковод и т.д. Специализированное программное обеспечение может быть введено в вычислительное устройство на любом подходящем машиночитаемом носителе, включая носитель информации, постоянное запоминающее устройство, или электрический несущий сигнал.
[0068] В одном варианте реализации способа измерение присутствия или отсутствия SNP (принадлежащего к любой категории SNP) включает измерение количества аллелей указанного SNP. В одном варианте реализации один или два аллеля соответствуют присутствию указанного SNP, а ноль аллелей соответствует отсутствию указанного SNP у указанного индивидуума; причем ноль аллелей соответствует гомозиготному отрицательному результату для указанного SNP, один аллель соответствует гетерозиготному положительному результату и два аллеля соответствуют гомозиготному положительному результату. Подходящие категории SNP включают, но не ограничиваются ими, SNP, относящиеся к заболеванию, с которым связан данный диагностический или прогностический анализ, SNP, относящиеся к факторам риска заболевания, с которым связан данный диагностический или прогностический анализ. Неограничивающими примерами факторов риска являются уровни белковых биомаркеров и ожирение.
[0069] В одном варианте реализации описанный выше этап а) способа включает применение одного или более аналитических устройств, включая, без ограничения, устройство для анализа ИФА, устройство для анализа на микрочипах, устройство для анализа иммунопреципитации, устройство для анализа иммунофлуоресценции, устройство для радиоиммуноанализа. или устройство масс-спектрометрии, использующее матричную лазерную десорбцию/ионизацию (MALDI) для измерения присутствия или концентрации биомаркера РПЖ.
[0070] В одном варианте реализации, который может быть объединен с вышеупомянутым вариантом реализации, описанный выше способ включает применение устройства масс-спектрометрии с применением матричной лазерной десорбции/ионизации (MALDI) для измерения присутствия или отсутствия SNP.
[0071] В одном варианте реализации описанный выше аналитический прибор включает одно или более аналитических устройств, включая, без ограничения, устройство для анализа ИФА, устройство для анализа на микрочипах, устройство анализа иммунопреципитации, устройство анализа иммунофлуоресценции, устройство радиоиммуноанализа. или устройство масс-спектрометрии, использующее матричную лазерную десорбцию/ионизацию (MALDI) для измерения присутствия или концентрации биомаркера РПЖ. В одном варианте реализации, который может быть объединен с вышеупомянутым вариантом реализации, вышеописанное устройство для анализа содержит устройство масс-спектрометрии с применением матричной лазерной десорбции/ионизации (MALDI) для измерения присутствия или отсутствия SNP.
[0072] Согласно дополнительному аспекту изобретения предложен набор для тестирования для выполнения этапа а) измерения присутствия или концентрации по меньшей мере двух биомаркеров и, необязательно, измерения присутствия или отсутствия по меньшей мере одного SNP из описанного выше способа для указания на присутствие или отсутствия определенного заболевания или патологического состояния у индивидуума, содержащий соответствующее аналитическое устройство, как описано выше, и применение по меньшей мере одного образца стандарта гармонизации HSS, чтобы сделать возможным преобразование измеренных значений в обобщенные единицы (GE), и, наконец, оценка вероятности присутствия у индивидуума указанного заболевания или патологического состояния.
[0073] Одним из возможных приложений настоящего способа является диагностический анализ для определения присутствия или отсутствия рака простаты, в котором подходящие биомаркеры включают, но не ограничиваются ими, PSA, iPSA, tPSA, fPSA и hK2 и, необязательно, MSMB. и/или MIC-1; и в котором подходящие SNP включают, но не ограничивается ими, rs582598, rs439378, rs2207790, rs1046011, rs10458360, rs7525167, rs10489871, rs7529518, rs4245739, rs4512641, rs10178804, rs11900952, rs1873555, rs10191478, rs6755901, rs6545962, rs721048, rs2710647, rs12612891, rs2028900, rs1009, rs12233245, rs6760417, rs10496470, rs10199796, rs12475433, rs16860513, rs12151618, rs3765065, rs13017302, rs12988652, rs871688, rs749264, rs3771570, rs4346531, rs6770955, rs12637074, rs2660753, rs13319878, rs6437715, rs2162185, rs1515542, rs2270785, rs9830294, rs1439024, rs6762443, rs888507, rs6794467, rs12490248, rs1477886, rs4833103, rs3796547, rs17779822, rs2366711, rs16849146, rs1894292, rs12640320, rs3805284, rs12500426, rs4699312, rs17021918, rs7679673, rs2047408, rs2647262, rs12506850, rs7658048, rs2078277, rs12505546, rs13113975, rs4246742, rs2736098, rs401681, rs11134144, rs10060513, rs40485, rs2087724, rs1482679, rs16901841, rs1295683, rs2070874, rs7752029, rs2018334, rs9358913, rs1140809, rs409558, rs3096702, rs9267911, rs2025645, rs9359428, rs6569371, rs2813522, rs1933488, rs712242, rs6934898, rs9456490, rs651164, rs3120137, rs9364554, rs9457937, rs10486562, rs10807843, rs7801918, rs6962297, rs2465796, rs6957416, rs7777631, rs2272316, rs6961773, rs2132276, rs13265330, rs16887736, rs2911756, rs2272668, rs2339654, rs1380862, rs9297746, rs12543663, rs10086908, rs16901922, rs1016343, rs17832285, rs16901979, rs4871779, rs10107982, rs16902094, rs620861, rs17467139, rs6983267, rs9297756, rs10094059, rs7818556, rs1992833, rs986472, rs12552397, rs4273907, rs4237185, rs753032, rs11253002, rs2386841, rs10795841, rs10508422, rs7075945, rs10508678, rs539357, rs10826398, rs3818714, rs7090755, rs10993994, rs4382847, rs1891158, rs10887926, rs10788160, rs6579002, rs10832514, rs7358335, rs1944047, rs3019779, rs10896437, rs12793759, rs7106762, rs7102758, rs2449600, rs585197, rs2509867, rs11568818, rs7125415, rs11601037, rs11222496, rs4570588, rs6489721, rs3213764, rs17395631, rs4423250, rs11168936, rs10875943, rs3759129, rs902774, rs1827611, rs4760442, rs11610799, rs6539333, rs11067228, rs7485441, rs6489794, rs4119478, rs17070292, rs2293710, rs17256058, rs1950198, rs2331780, rs7141529, rs12880777, rs17123359, rs785437, rs524908, rs12903579, rs7178085, rs7164364, rs896615, rs11634741, rs9972541, rs12594014, rs11631109, rs1558902, rs8044335, rs2738571, rs885479, rs385894, rs684232, rs4925094, rs17138478, rs11649743, rs2107131, rs7213769, rs12946864, rs306801, rs138213197, rs1863610, rs17224342, rs9911515, rs12947919, rs966304, rs17744022, rs7234917, rs1943821, rs2227270, rs1363120, rs888663, rs122773222, rs1054564, rs4806120, rs11672691, rs758643, rs3745233, rs6509345, rs2659051, rs2735839, rs1354774, rs2691274, rs6090461, rs2297434, rs6062509, rs2315654, rs2823118, rs2838053, rs398146, rs16988279, rs2269640, rs4822763, rs132774, rs747745, rs5978944, rs6530238, rs5934705, rs5935063, rs4830488, rs17318620, rs5945619, rs5945637, rs11091768, rs2473057, rs5918762, rs4844228, rs6625760 и rs17324573.
[0074] Настоящее изобретение в соответствии с различными вариантами реализации, описанными выше, обеспечивает гармонизацию результатов анализа, полученных в разных лабораториях, где использовались потенциально разные инструментальные платформы. Гармонизация достигается путем преобразования значений анализа в обобщенные единицы, которые являются сопоставимыми между разными инструментальными платформами. Существенным для работы способа является применение набора для гармонизации, который разработан таким образом, чтобы свойства по существу всех целевых аналитов в мультиплексном устройстве для биохимического анализа проверялись с помощью одного или более стандартов гармонизации. Чтобы проконтролировать любые отклонения от ожидаемых характеристик, каждый результат, полученный в одном анализе, преобразуют в обобщенные единицы (GE), в которых учитываются несколько аспектов, включая, но не ограничиваясь ими, систематическое отклонение в эффективности анализа, количественно определяемое с помощью контрольного образца гармонизации в данном анализе, любой систематический дрейф в данной лаборатории или оборудовании, количественно выраженный с применением текущего результата стандарта гармонизации в сочетании с несколькими предыдущими результатами стандарта гармонизации, а также характеристики типа прибора, используемого для получения результатов анализа.
[0075] Основной принцип изобретения согласно одному аспекту можно описать следующим образом. Предлагаемый способ гармонизации, раскрытый и заявленный в соответствии с различными вариантами реализации, направлен на гармонизацию выходных данных анализа из разных лабораторий, которые потенциально используют различные типы аналитического оборудования (инструментальные платформы). Для достижения гармонизации каждый набор неизвестных образцов (обычно образцов пациентов) дополняется стандартом гармонизации. Поскольку известно, что разные лаборатории и технологии могут систематически отличаться образом, меняющимся со временем, результаты стандарта гармонизации используют для приведения результатов всех неизвестных образцов к обобщенным единицам. Применение обобщенных единиц устраняет совокупность систематических ошибок и улучшает сопоставимость результатов между лабораториями и технологическими платформами и позволяет централизованно интерпретировать результаты. Таким образом, все диагностические, прогностические или другие клинические решения принимаются с применением обобщенных единиц так, чтобы достичь одинаковой эффективности диагностического/прогностического способа независимо от лаборатории или типа прибора.
[0076] Способ гармонизации требует, чтобы и лаборатория, и само оборудование были аттестованы, с целью выявить взаимосвязь между инфраструктурой/оборудованием и обобщенными единицами (GE).
[0077] Аналитический прибор аттестуют способом, который показывает, как нужно преобразовать выходные данные от этого типа прибора, чтобы он соответствовал обобщенным единицам измерения.
[0078] Лаборатория, которая использует ранее аттестованный аналитический прибор для проведения поддающегося универсализации анализа, также должна быть аттестована, чтобы показать, как нужно преобразовать влияние указанной лабораторной инфраструктуры и стандартных операционных процедур на выходные данные анализа, чтобы он соответствовал обобщенным единицам.
[0079] Аналитический прибор того типа, который ранее уже был аттестован, обычно не требует аттестации, если такой прибор приобретает другая лаборатория. Каждая новая установка (любого) прибора в лаборатории обычно требует повторной аттестации лаборатории для гармонизации выходных данных от указанного вновь установленного прибора.
[0080] После того, как аналитический прибор и лаборатория аттестованы для получения выходных данных анализа в обобщенных единицах, лаборатория использует аналитический прибор для определенных анализов, причем каждый анализ обычно включает один или более стандартов гармонизации. Стандарт гармонизации призван служить как независимым контролем (контроль третьего уровня) для большинства отдельных анализов в мультиплексной системе, так и опорной точкой для обобщения результата анализа. По завершении анализа выходные данные анализа (предпочтительно выходные данные в виде необработанных данных) обычно передают в центральное (цифровое) устройство, где фактические результаты анализа преобразуются в обобщенные единицы. Факторы, которые влияют на это преобразование, включают (но не ограничиваются ими) результаты стандарта гармонизации из настоящего анализа, результаты стандарта гармонизации из других лабораторий, в которых использовалась такая же партия стандартов гармонизации, характеристики прибора, характеристики лаборатории, партию реагентов, используемых для проведения и калибровки анализа, а также временную эволюцию результатов стандартов гармонизации в настоящей лаборатории.
[0081] Стандарт гармонизации не обязательно нужно всегда составлять одним и тем же образом. На самом деле предпочтительно постоянно изменять свойства стандарта гармонизации, чтобы регулярно тестировать несколько аспектов мультиплексного анализа. Например, если анализ измеряет концентрацию четырех биомаркеров в крови, было бы разумно иметь два разных стандарта гармонизации: один, в котором два биомаркера присутствуют в высокой концентрации, а два других - в низкой концентрации, и второй стандарт гармонизации с противоположным профилем концентраций. Посредством систематической и регулярной (обычно ежедневно или еженедельно) замены в каждом анализе одного стандарта гармонизации на другой не только будет количественно определена функция анализа в каждом анализе посредством теста измерения известного профиля высокой-высокой-низкой-низкой (или наоборот) концентрации, но после выполнения анализа обоих стандартов гармонизации будет проверен динамический диапазон анализа, поскольку в короткие сроки будут протестированы одна известная низкая концентрация и одна известная высокая концентрация для каждого из включенных биомаркеров.
[0082] Стандарты гармонизации могут дополнительно быть специально адаптированы для исследования частных аспектов мультиплексного анализа. Например, если в новой партии реагентов подозревается нецелевая перекрестная реактивность, набор стандартов гармонизации может быть разработан так, чтобы исследовать, присутствовала ли предполагаемая проблема или нет. Аналогичным образом, одна и та же партия стандартов гармонизации может быть распределена по нескольким различным лабораториям, что позволяет сравнивать и корректировать небольшие систематические отклонения между лабораториями, а также определять, испытывает ли какая-либо конкретная лаборатория проблемы с конкретным анализом.
[0083] Многокомпонентные устройства для биохимического анализа непрактичны для калибровки и контроля по одному. Поэтому обычные контрольные образцы и внешние стандарты непросто внедрять и оценивать. С применением стандарта гармонизации становится доступным мультиплексный контроль, который дополняет любые другие попытки контроля анализа. В тех случаях, когда профиль результатов известного стандарта гармонизации остается конфиденциальным, он также служит в качестве контроля безопасности или аутентичности. Зафиксированный профиль результатов для определенного и однозначно идентифицированного стандарта гармонизации, который значительно отличается от известного и ожидаемого профиля результатов, указывает на то, что либо в процессе обработки стандарта гармонизации произошли технические ошибки, либо стандарт гармонизации, используемый лабораторией, является контрафактным. Контрафактные реагенты могут снизить точность анализа и, следовательно, представляют серьезный риск для пациента.
[0084] Устройства для многокомпонентного биохимического анализа трудно произвести таким образом, чтобы все биомаркеры анализировались с одинаковой точностью и одинаковым динамическим диапазоном, независимо от производственной партии. При предположении, что для одного анализа выход продукции составляет 95% (т.е. 19 из 20 попыток производства успешны), для устройства для многокомпонентного биохимического анализа, содержащего 10 отдельных анализов, расположенных на одной твердой подложке, выход продукции будет составлять (0,95 ^ 10). * 100% = 59,8%. Насколько мы понимаем, этот факт является узким местом в разработке многокомпонентных анализов, в которые включены белковые молекулы, поскольку белки являются чувствительными и их трудно использовать в производстве, что автоматически приводит к низкому выходу продукции для многокомпонентных анализов. Настоящее изобретение позволяет допустить более низкую эффективность многокомпонентного анализа как такового, поскольку для корректировки отклонений, обнаруженных на твердой подложке при оценке неизвестных образцов, используют стандарт гармонизации. В качестве неограничивающего примера предположим, что внедрение обобщенных единиц посредством процедуры гармонизации позволяет снизить требования к эффективности для каждого отдельного анализа, таким образом, делая допустимой более низкую эффективность анализа и корректируя выходные данные посредством применения стандарта гармонизации. В случаях, когда исходный выход продукции составляет 95%, а внедрение процедуры гармонизации увеличивает выход до 98%, общий выход продукции многокомпонентного анализа, включающего 10 отдельных анализов, расположенных на одной твердой подложке, будет составлять (0,98 ^ 10) * 100% = 81,7%. Это означает, что небольшое увеличение выхода продукции для отдельных анализов может оказывать большое влияние на общий выход продукции для многокомпонентных анализов. Применение стандарта гармонизации является внешним способом увеличения выхода продукции и не требует внесения каких-либо изменений в существующие способы производства.
[0085] В случаях, когда анализ проводят на твердой подложке, содержащей множество независимых пятен, где на каждом пятне прикреплен распознающий элемент, такой как антитело, факторы гармонизации также могут быть включены в твердую подложку для анализа. Например, можно прикрепить один и тот же распознающий элемент к нескольким пятнам, причем одно подмножество пятен имеет известную более низкую плотность указанного распознающего элемента, а другие имеют более известную высокую плотность указанного распознающего элемента. Тогда при анализе с применением стандарта гармонизации можно оценить вариацию производительности пятен (путем сравнения результатов для нескольких пятен с одинаковой плотностью) и линейность производительности пятен (путем сравнения результатов для нескольких пятен с разной плотностью). Вариация линейности производительности пятен может вызвать вариацию динамического диапазона анализа. Посредством мониторинга линейности производительности пятен in situ с помощью стандарта гармонизации, становится возможным корректировать результаты для компенсации измененных характеристик анализа, таких как динамический диапазон.
[0086] Кроме того, в стандарт гармонизации и соответствующий многокомпонентный анализ можно включить совершенно постороннюю молекулу. Например, если тест разработан для применения у людей, стандарт гармонизации может быть дополнен белком мыши, а твердая подложка может быть разработана так, чтобы она включала анализы как для изначально намеченных биомаркеров человека, так и для добавленного белка мыши. Такой искусственный анализ, встроенный в многокомпонентный анализ и стандарт гармонизации, полезен, поскольку он служит функциональным контролем и стабильной точкой на протяжении всего анализа и оценки. Такая стабильная точка полезна для оценки внешнего повреждения компонентов, например при транспортировке реагентов или твердых подложек при повышенных температурах, которые могут снизить или даже свести к нулю эффективность анализа, что может представлять серьезный риск для пациента.
[0087] Несмотря на то, что это изобретение в первую очередь применимо к анализу, оценивающему концентрацию нескольких биомаркеров, некоторые варианты реализации применимы также к качественным анализам, таким как анализ генотипирования. В качестве неограничивающего примера стандарт гармонизации, применяемый в анализе генотипирования, в котором измеряют множество однонуклеотидных полиморфизмов (SNP), может служить в качестве контроля подлинности: благодаря известному профилю генотипирования стандарта гармонизации измеренный генотип можно сопоставить с известным генотипом, чтобы подтвердить функциональность анализа и подлинность анализа. В ситуации генотипирования можно дополнительно внедрить посторонние молекулы или разработать анализы для посторонних SNP, чтобы они служили функциональным контролем, подобно тому, как уже обсуждалось.
[0088] Чтобы проиллюстрировать, насколько важным может быть уменьшение систематической ошибки, были рассмотрены результаты большого популяционного исследования скрининга рака простаты. В этом исследовании несколько белковых биомаркеров, несколько SNP и несколько других относящихся к информации факторов (таких как возраст и семейный анамнез рака простаты и т. д.), были объединены в один балл риска, который оказался высоко функциональным для цели обнаружения рака простаты, как раскрыто в работе “Prostate cancer screening in men aged 50-69 years (STHLM3): a prospective population-based diagnostic study”, H Grönberg с соавторами, опубликованной в Lancet Oncology (November 9, 2015 http://dx.doi.org/10.1016/S1470-2045(15)00361-7), которая включена в настоящий документ в качестве ссылки. Белковые биомаркеры, использованные в этом исследовании, были измерены с использованием мультиплексной платформы, основанной на технологии ImmunoCAP ISAC (Thermo Fisher Scientific). В кратком изложении, было измерено приблизительно 70 образцов пациентов, 12 калибровочных образцов и 12 контрольных образцов с использованием одного и того же одноразового тестового устройства. При анализе чувствительности каждому одноразовому устройству был присвоен мультипликативный коэффициент, который применялся ко всем образцам и всем белковым биомаркерам на нем. Мультипликативным коэффициентам позволяли варьироваться в пределах определенного диапазона, и коэффициенты были выбраны так, чтобы повысить диагностическую эффективность с точки зрения ROC-AUC. Когда мультипликативным коэффициентам давали варьировать от 0,96 до 1,04, то есть когда каждое одноразовое устройство подвергалось систематической провокации величиной максимум 4%, эффективность диагностического анализа не улучшалась каким-либо значительным образом. Когда мультипликативным коэффициентам позволяли варьировать от 0,86 до 1,16, то есть когда каждое одноразовое устройство подвергалось систематической провокации величиной максимум 16%, эффективность диагностического анализа можно было явно улучшить с 0,74 до приблизительно 0,78. Такое увеличение эффективности превышает вклад любого из отдельных биомаркеров, за исключением общего PSA. Вывод из этого анализа чувствительности состоит в том, что способ, раскрытый Грёнбергом (Grönberg) и соавторами, требует высокого уровня контроля, так чтобы систематические ошибки и сдвиги в эффективности анализа составляли менее 16%.
[0089] Параллельно с исследованием, проведенным Грёнбергом и соавторами, была оценена эффективность анализа общего PSA на приборе Roche Cobas в обычной клинической лаборатории в Стокгольме. Данные контрольных образцов приблизительно за 2 года показали, что при смене партии калибровочных реагентов уровень общего PSA в контрольном образце может сдвигаться на 3-6%. Такой сдвиг сам по себе не окажет большого влияния на эффективность способа скрининга, раскрытого Гренбергом, но может стать проблемой в сочетании с другими потенциальными источниками систематической ошибки.
[0090] Еще одним мероприятием, проведенным параллельно с исследованием, выполненным Грёнбергом и соавторами, было сравнение общего PSA и свободного PSA, полученных от двух независимых поставщиков приборов, анализатора Roche Cobas и анализатора BRAHMS Kryptor (Thermo Fisher Scientific) в 282 образцах крови. Несмотря на то, что обе эти платформы одобрены для применения в обычных клинических лабораториях, наблюдалась систематическая разница в зафиксированных значениях: общий PSA из анализа, выполненного на Kryptor, был на 5% выше, чем из анализа, выполненного на Cobas, а свободный PSA из анализа, выполненного на Kryptor, был на 16% больше, чем из анализа, выполненного на Cobas.
[0091] В своей совокупности это иллюстрирует, что для мультиплексного анализа, раскрытого Грёнбергом, будет необходим строгий контроль систематической ошибки, и показывает, что существует потребность в настоящем изобретении, чтобы сделать способ Грёнберга широко применимым. Это согласуется с выводами в отчете “Between-method differences in prostate-specific antigen assays affect prostate cancer risk prediction by nomograms.” C Stephan и соавторы, опубликованном в Clin Chem. 2011 Jul;57(7):995-1004. doi: 10.1373/clinchem.2010.151472, как обсуждается в другом месте в настоящем раскрытии.
[0092] С более широкой точки зрения, мультиплексные анализы столкнутся с множеством проблем, прежде чем они смогут стать стабильно функциональными в диагностических или прогностических ситуациях. Функция мультиплексирования обеспечивает отличающуюся характеристику данных по сравнению с моноплексными анализами, что, в свою очередь, требует другого мышления при применении мультиплексных данных. Результаты, полученные из мультиплексных данных, могут предпочтительно рассматриваться как профиль (паттерн, отпечатки пальцев). Профиль состоит из нескольких точек данных, которые могут иметь как относительные, так и абсолютные связи между собой. При сравнении паттернов можно утверждать о сходстве, даже если часть точек данных отличается друг от друга. Это означает, что применение паттерна, содержащего несколько точек данных, будет по своей природе устойчивым к индивидуальным вариациям измеряемых объектов и позволяет мультиплексному анализу допускать больший шум, чем то, что обычно приемлемо для моноплексного анализа. Свойство избыточности мультиплексирования обсуждалось в контексте диагностики рака простаты в WO 2014079865, которая включена в настоящий документ в качестве ссылки. Еще одна общая проблема для анализов - систематические отклонения. Систематические различия существуют между инструментальными платформами, иногда между одноразовыми изделиями, используемыми в анализе, а также могут быть вызваны изменениями в преаналитических процедурах перед выполнением анализа. Систематические ошибки усложняют получение результата, потому что они связаны с проблемой пороговой величины; на каком именно уровне (величине или сходстве) результат должен быть отмечен как "положительный". В случае, когда мультиплексный анализ используется для диагностических целей, и когда по какой-то причине половина точек данных в анализе сдвинута вверх на 20%, результаты, которые ранее были сходны с заранее определенным профилем, могут больше не быть таковыми, что приводит к неточному результату анализа. Настоящее изобретение направлено на решение проблемы систематической ошибки путем внедрения стандарта гармонизации и преобразования мультиплексных данных в обобщенные единицы на основании результата стандарта гармонизации. Взятые в совокупности, применение профилей с учетом свойства избыточности, раскрытого в WO 2014079865, и реализация процедуры стандарта гармонизации настоящего изобретения, приводит к повышению надежности мультиплексных анализов.
ПРИМЕР 1
[0093] В этом примере использовалась подмножество данных, полученных в рамках исследования STHLM3. STHLM3 описано в работе “Prostate cancer screening in men aged 50–69 years (STHLM3): a prospective population-based diagnostic study” Грёнберга и соавторов, опубликованной в Lancet Oncology (Volume 16, No. 16, p1667–1676, December 2015), включенной в настоящий документ посредством ссылки. Подмножество данных, использованных в этом примере, включало данные белковых биомаркеров от 4335 индивидуумов (3585 с индексом Глисона ниже 7, 617 с индексом Глисона 7, 133 с индексом Глисона 8 или выше), в частности, концентрацию в крови общего PSA, свободного PSA, интактного свободного PSA, hK2, GDF-15 и MSMB. Определение концентрации в крови было проведено с применением формата микрочипа, где различные антитела были прикреплены к субстрату, образец пациента контактировал с субстратом с последующим контактированием набора молекул конъюгатов с субстратом, причем указанный набор конъюгатов содержал молекулы, специфически связывающиеся с различными белками, захваченными из образца пациента на субстрат. Молекулы конъюгата были помечены флуоресцентным красителем, чтобы их можно было определить количественно.
[0094] Каждый субстрат содержал 96 независимых и идентичных лунок, то есть можно было обрабатывать одновременно 96 независимых образцов. Данные для текущего примера были получены с использованием 12 лунок для целей калибровки, 9 лунок - для аналитических контролей (три контроля, каждый из которых анализировался в трех независимых лунках) и трех лунок для стандарта гармонизации (один стандарт исследовали в трех независимых лунках). Остальные 72 лунки были использованы для образцов пациентов. Таким образом, для получения данных для текущего примера потребовалось приблизительно 100 субстратов, а образцы пациентов были случайным образом распределены по субстратам.
[0095] При сравнении среднего значения для стандарта гармонизации со медианным значением 72 неизвестных образцов в каждом субстрате, три из шести белковых биомаркеров показали корреляцию. На фиг. 5 показано среднее значение общего PSA для стандартов гармонизации (в произвольных единицах) по оси ординат и медианное значение общего PSA неизвестных образцов (то есть образцов пациентов) на том же субстрате по оси абсцисс (в тех же произвольных единицах). В случаях, когда стандарт гармонизации дает значение ниже среднего, медиана неизвестных образцов была последовательно ниже среднего. Результаты для MSMB и GDF-15 были аналогичными, как показано на фиг. 6 и фиг. 7.
[0096] При сравнении 13 субстратов (453 пациента, из них 69 с индексом Глисона 7 и 12 с индексом Глисона 8 или выше), которые имели самые низкие значения общего PSA для стандарта гармонизации, с остальным набором данных были получены медианные концентрации биомаркеров для общего PSA и MSMB, представленные в таблице A. Медианные значения PSA для пациентов, проанализированных на 13 выбранных субстратах, были, независимо от агрессивности рака, последовательно ниже, чем медианное значение для пациентов с доброкачественными нераковыми опухолями в остальном наборе данных. Кроме того, значения MSMB для выбранных 13 субстратов были последовательно выше, независимо от агрессивности рака, по сравнению с остальным набором данных. Поскольку общий PSA положительно коррелирован с риском рака простаты (т.е. более высокое значение указывает на более высокий риск), а МСМБ отрицательно коррелирован (т.е. более низкое значение указывает на повышенный риск рака), 13 выбранных субстратов имели отклоняющиеся значения как для общего PSA, так и для МСМБ, причем одновременно отклоняющиеся таким образом, что маскировали риск, снижая точность.
[0097] Таблица A
[0098] Систематическое отклонение 13 выбранных субстратов можно скорректировать путем преобразования значений концентрации, полученных в результате анализа, с применением значений, полученных для образцов стандартов гармонизации на каждом субстрате. Поскольку определение концентрации любого образца ассоциировано с ошибкой, каждый субстрат был преобразован в обобщенные единицы с помощью следующего консервативного преобразования:
Корректирующий коэффициент = 2/(1 + (ожидаемое значение стандарта гармонизации - измеренное значение стандарта гармонизации)/(ожидаемое значение стандарта гармонизации)).
[0099] Это преобразование исправляет только половину отклонения, указанного стандартом гармонизации, и оно было выбрано для уменьшения распространения потенциальной ошибки измерения на образце гармонизации на обобщенные единицы. При сравнении общей эффективности с точки зрения различения между агрессивным раком (определяемого как индекс Глисона 7 или выше) и другими, применение обобщенных единиц не улучшило общую диагностическую эффективность с популяционной точки зрения. Это означает, что (а) подавляющее большинство полученных данных являются доброкачественными как есть и (b) обобщенные единицы можно применять безопасно с популяционной точки зрения. В крайних случаях, например, для 13 рассмотренных выше субстратов, обобщенные единицы будут важны, и улучшат точность для участвующих пациентов. Следовательно, с индивидуальной точки зрения, обобщенные единицы потенциально способны корректировать результаты анализа и давать адекватные оценки риска. В целом, это предполагает, что настоящее изобретение имеет очень большое значение для индивидуумов, анализы которых проводятся на субстрате, где образцы гармонизации указывают на систематическое отклонение, и имеет умеренное значение для большинства индивидуумов, анализы которых проводятся на субстрате, где образцы гармонизации показывают нормальные уровни.
[00100] Хотя изобретение было описано применительно к его предпочтительному варианту реализации который представляет собой наилучший способ исполнения, известный в настоящее время изобретателям, следует понимать, что без выхода за пределы объёма изобретения, изложенного в прилагаемой формуле изобретения, могут быть внесены различные изменения и модификации, которые будут очевидны для специалиста в этой области.
Предложенная группа изобретений относится к медицине, а именно к стандартизации. Предложен способ гармонизации результатов тестирования биологического образца в мультиплексном биохимическом анализе, где гармонизация результатов тестирования включает одновременное определение присутствия и/или концентрации нескольких биомаркеров в биологическом образце и приведение результатов тестирования от указанного биологического образца к виду, сопоставимому с результатами тестирования, полученными в других лабораториях. Предложено применение устройства для мультиплексного биохимического анализа и система для гармонизации результатов тестирования биологического образца в мультиплексном биохимическом анализе в соответствии с заявленным способом. Предложенная группа изобретений обеспечивает улучшение контроля третьего уровня для мультиплексных анализов за счет гармонизации результатов тестирования. 3 н. и 6 з.п. ф-лы, 7 ил., 1 табл., 1 пр.
1. Способ гармонизации результатов тестирования биологического образца в мультиплексном биохимическом анализе, где гармонизация результатов тестирования включает одновременное определение присутствия и/или концентрации нескольких биомаркеров в биологическом образце и приведение результатов тестирования от указанного биологического образца к виду, сопоставимому с результатами тестирования, полученными в других лабораториях, причем указанный способ включает этапы а) - с),
- а) количественное определение концентрации по меньшей мере двух различных биомаркеров в каждом из биологического образца и стандартного образца, посредством устройства для мультиплексного биохимического анализа, реализованного в аналитическом приборе,
причем стандартный образец имеет свойства, известные производителю стандартного образца, но не известные пользователю;
- b) получение результатов тестирования, т.е. результата тестирования биологического образца и результата тестирования стандартного образца, из разных мест тестирования в компьютерный модуль принятия решений; и
- с) преобразование результатов тестирования, полученных в биологическом образце, характеризующееся тем, что преобразование результатов тестирования биологического образца включает преобразование результатов тестирования стандартного образца в обобщенные единицы, GE, и приведение результатов биологического образца к указанным обобщенным единицам, GE, путем применения корректирующего коэффициента, где корректирующий коэффициент равен 2 / (1+(ожидаемое значение стандартного образца - измеренное значение стандартного образца)/(ожидаемое значение стандартного образца)).
2. Способ по п. 1, характеризующийся тем, что этапы от а) до с) повторяют по меньшей мере дважды.
3. Способ по п. 2, характеризующийся тем, что этапы от а) до с) повторяют с другим биологическим образцом и с применением результатов тестирования для по меньшей мере двух стандартных образцов - HSS, количественно определенных в разные моменты времени, в качестве входных данных в преобразовании в обобщенные единицы GE.
4. Способ по п. 2, характеризующийся тем, что этапы от а) до с) повторяют с другим биологическим образцом BS и другим стандартным образцом HSS, и с применением результатов тестирования для по меньшей мере двух стандартных образцов - HSS, количественно определенных в разные моменты времени, в качестве входных данных в преобразовании в обобщенные единицы GE.
5. Способ по п. 2, характеризующийся тем, что этапы от а) до с) повторяют с другим биологическим образцом BS или другим стандартным образцом HSS, и с применением результатов тестирования для по меньшей мере двух стандартных образцов HSS, количественно определенных в разные моменты времени, в качестве входных данных в преобразовании в обобщенные единицы GE.
6. Применение устройства для мультиплексного биохимического анализа в способе по п. 1, где устройство выполнено с возможностью реализации в аналитическом приборе и определения присутствия или концентрации по меньшей мере двух различных биомаркеров в биологическом образце - BS и в стандартном образце - HSS, независимо в каждом образце BS и HSS, которые могут быть количественно определены с помощью этого аналитического прибора, характеризующееся тем, что это устройство для биохимического анализа выполнено с возможностью обрабатывать независимые и одновременные анализы, причем стандартный образец HSS содержит по меньшей мере 90% биомаркеров которые являются частью анализа.
7. Применение по п. 6, где устройство содержит твердую фазу с иммобилизованными на ней по меньшей мере двумя различными категориями лигандов, причем:
- первая категория лигандов специфически связывается с биомаркером РПЖ - рака предстательной железы и включает множество различных лигандов, специфически связывающихся с каждым из множества различных биомаркеров РПЖ, предпочтительно по меньшей мере с одним из PSA, iPSA, tPSA, fPSA и hK2, и необязательно MSMB и/или MIC-1; и
- вторая категория лигандов специфически связывается с однонуклеотидным полиморфизмом, связанным с раком простаты - SNPpc, и включает по меньшей мере один из rs11672691, rs11704416, rs3863641, rs12130132, rs4245739, rs3771570, rs7611694, rs1894292, rs6869841, rs2018334, rs16896742, rs2273669, rs1933488, rs11135910, rs3850699, rs11568818, rs1270884, rs8008270, rs4643253, rs684232, rs11650494, rs7241993, rs6062509, rs1041449, rs2405942, rs12621278, rs9364554, rs10486567, rs6465657, rs2928679, rs6983561, rs16901979, rs16902094, rs12418451, rs4430796, rs11649743, rs2735839, rs9623117 и rs138213197.
8. Применение по п. 7, в котором на твердой фазе дополнительно иммобилизована третья категория лигандов, которая специфически связывается с SNP-ассоциированным биомаркером - SNPbm и включает один или множество различных лигандов, специфически связывающихся с одним или каждым из множества различных SNPbm, таких как по меньшей мере один из rs1227732, rs3213764, rs1354774, rs2736098, rs401681, rs10788160, rs11067228, rs1363120, rs888663 и rs1054564.
9. Система для гармонизации результатов тестирования биологического образца в мультиплексном биохимическом анализе в соответствии со способом по п. 1, причем система включает:
- устройство для мультиплексного биохимического анализа, реализованное в аналитическом приборе, причем оба из устройства для анализа и аналитического прибора адаптированы для количественной оценки концентрации по меньшей мере двух различных биомаркеров в каждом из биологического образца - BS и стандартного образца - HSS, независимо в каждом образце BS и HSS, компьютерный модуль принятия решений, содержащий:
- компонент для получения результатов тестирования, т.е. Тест BS и Тест HSS, образцов BS и HSS из разных мест тестирования в компьютерный модуль принятия решений; и
- компонент для преобразования результатов тестирования, т.е. Тест BS, полученных для биологического образца BS, характеризующийся тем, что компонент для преобразования результатов тестирования для биологического образца BS выполнен с возможностью преобразования результатов тестирования Тест HSS стандартного образца HSS в обобщенные единицы, GE, и выполнен с возможностью приведения результатов тестирования биологического образца к обобщенным единицам, GE, путем применения корректирующего коэффициента, где корректирующий коэффициент равен 2 / (1+(ожидаемое значение стандартного образца - измеренное значение стандартного образца)/(ожидаемое значение стандартного образца)).
| WO 2014079865 A1, 30.05.2014 | |||
| ПЕТРОВ А.И | |||
| Исследование и практическая реализация программно-аппаратных средств проведения полимеразной цепной реакции с наблюдением в реальном времени | |||
| Дисс | |||
| канд | |||
| тех | |||
| наук | |||
| Санкт-Петербург, 2016, 112 c. | |||
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| Bio-Rad Laboratories, 31 Dec 2011, 260 с | |||
| (Ссылка помещена на сайт в | |||
Авторы
Даты
2024-04-17—Публикация
2019-01-22—Подача