Изобретение относится к медицине, а именно к хирургии и может быть применено в качестве способа стимуляции регенерации и профилактики несостоятельности кишечных анастомозов с использованием аутогенных факторов роста.
Существует способ, направленный на улучшение условий заживления кишечного анастомоза и герметизацию кишечных швов с использованием медицинского клея «Сульфакрилат». Однако данный способ имеет следующие недостатки: отсутствие в составе клея биологически активных веществ определяет отсутствие эффекта стимуляции регенерации кишечного анастомоза; плохая адгезия клея к тканям зоны кишечного анастомоза; в процессе полимеризации клея в области кишечных швов возможно формирование зоны асептического коагуляционного некроза, что может препятствовать регенерации кишечного шва и увеличивать риск его несостоятельности [Регистрационное удостоверение №ФС 01031444/2587-06 от 07 февраля 2006 года, Марченко В.Т. Клинические и морфологические аспекты применения нового клея «Сульфакрилат» в хирургии органов грудной и брюшной полости. Дис. док. мед. наук. - Новосибирск. - 2004. - 212 с.].
Известен способ интраоперационной профилактики несостоятельности анастомозов полых органов желудочно-кишечного тракта и улучшения условий их регенерации путем интраоперационного введения в стенки полых органов субсерозно, отступя от линии швов на 1,0 см, 25%-ного раствора 5-оксиметилурацила в количестве 0,5 мл на 1 см2 [Пат. 2304972 Российская Федерация, МПК A61K 31/7072. Способ интраоперационной профилактики несостоятельности анастомозов полых органов в хирургии желудочно-кишечного тракта / В.В. Плечев [и др.]; заявитель и патентообладатель ГОУ ВПО БГМУ РОСЗДРАВА – № 2005141843/14; заявл. 27.12. 2005; опубл. 27.08.2007, Бюл. № 24]. Данный способ обеспечивает увеличение скорости восстановления регионарного кровотока зоны анастомоза, позволяет формировать межкишечный анастомоз в условиях нарушения микроциркуляции кишечной стенки. Однако при инъекционном введении отступя от линии шва на 1 см происходит дополнительное субсерозное повреждение стенки кишечника, а также применение 5-оксиметилурацила не обеспечивает достаточной стимуляции регенерации кишечного анастомоза при его малой доступности и стоимости.
Наиболее близким к заявляемому способу является метод погружения краев энтеротомной раны в плазму обогащенную тромбоцитами (PRP-Platelet Rich Plasma) и выдерживания их в течение 5 минут до образования студенистого сгустка, с последующим наложением кишечного анастомоза [Fresno L, Fondevila D, Bambo O, Chacaltana A, García F, Andaluz A. Effects of platelet-rich plasma on intestinal wound healing in pigs. Vet J. 2010 Sep;185(3):322-7. doi: 10.1016/j.tvjl.2009.06.009. Epub 2009 Jul 17. PMID: 19616459; Giusto G, Vercelli C, Iussich S, Tursi M, Perona G, Gandini M. Comparison of the effects of platelet-rich or growth factor-rich plasma on intestinal anastomosis healing in pigs. BMC Vet Res. 2017 Jun 19;13(1):188. doi: 10.1186/s12917-017-1102-8. PMID: 28629420; PMCID: PMC5477282]. Однако данный способ имеет ряд недостатков связанных с нанесением геля на поверхность анастомоза: в зоне анастомоза отмечается усиление процесса спайкообразования; отмечаются большие технические трудности наложения анастомоза, связанных с предупреждением удаления с поверхности краев анастомоза сформировавшегося студенистого сгустка из обогащенной тромбоцитами плазмы; погружение кровоточащих и загрязненных кишечным содержимым краев кишечника в обогащенную тромбоцитами плазму отрицательно влияет на эффективность и концентрацию ее исходного состава.
Цель: разработка нового способа стимуляции регенерации и профилактики несостоятельности кишечных анастомозов с использованием интраоперационного инъекционного введения аутогенных факторов роста в составе обогащенной тромбоцитами плазмы.
Указанная цель достигается тем, что перед наложением дигестивного анастомоза в мышечный слой его дистального и проксимального краев, инъекционным способом вводятся аутогенные факторы роста, содержащиеся в предварительно подготовленной из собственной крови пациента, обогащенной тромбоцитами аутоплазмы.
Технический результат при использовании изобретения - стимуляция регенерации и профилактика несостоятельности кишечных анастомозов за счет ускорения неоангеогенеза, увеличения скорости локального кровотока и миграции клеточных элементов.
Способ осуществляется следующим образом.
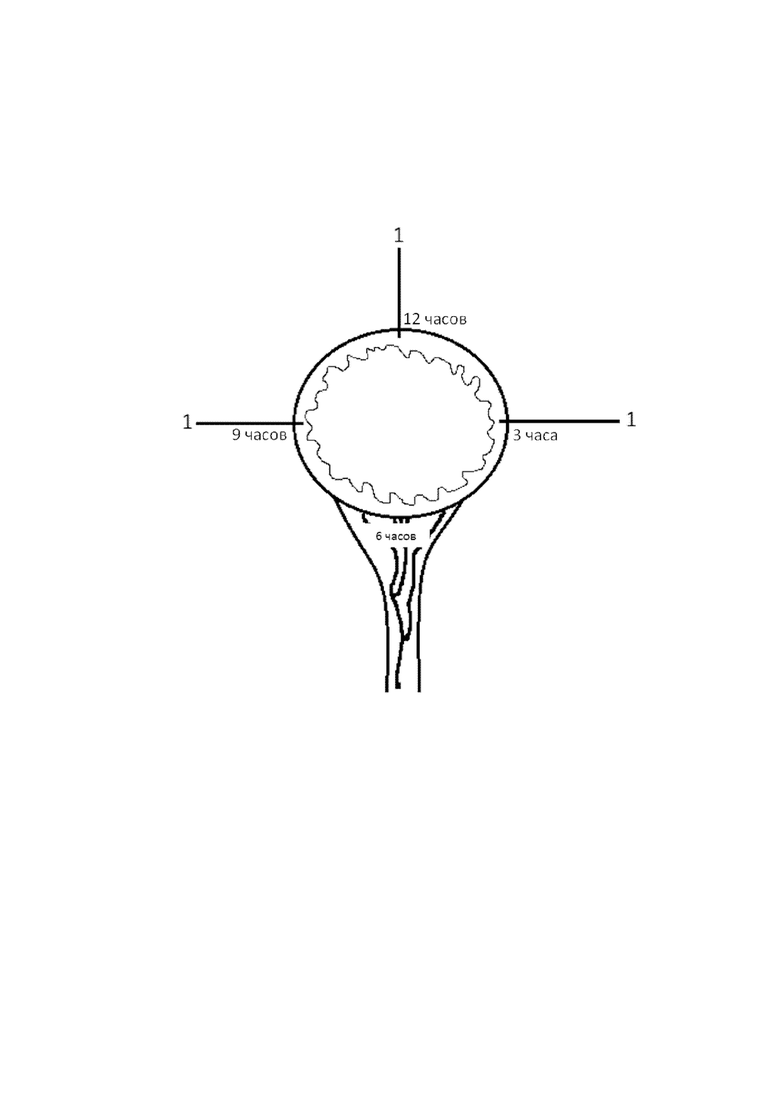
После выполнения лапаротомии, резекции кишечника или энтеротомии, оперативный прием завершается наложением кишечного анастомоза определенного способа (конец - в конец, бок - в бок, конец - в бок) и рядности (однорядный, двухрядный). При формировании кишечного анастомоза применяется классическая техника его выполнения. Однако перед наложением кишечных швов, в мышечный слой стенки дистального и проксимального краев анастомоза, с использованием инъекционной иглы размером 32G и инсулинового шприца (1 мл), вводится обогащенная тромбоцитами аутоплазма, содержащая аутогенные факторы роста (Фиг.). При этом введение обогащенной тромбоцитами аутоплазмы, содержащей аутогенные факторы роста, проводится со стороны раневого края кишки, исключая травматизацию серозной и слизистой оболочки, путем введения иглы на глубину 5 мм. от края. В раневые края дистального и проксимального участка кишки, формирующих кишечный анастомоз, осуществляется по 3 инъекции с введением 0,5 мл обогащенной тромбоцитами аутоплазмы, в проекции 3, 9 и 12 часов условного циферблата, принимая за 6 часов брыжеечную часть раневого края кишки. После введения в раневые края дистального и проксимального участка кишки обогащенной тромбоцитами аутоплазмы, содержащей аутогенные факторы роста, осуществляется наложение кишечных швов с окончательным формированием кишечного анастомоза. Обогащенная тромбоцитами аутоплазма, содержащая аутогенные факторы роста, подготавливается интраоперационно, непосредственно перед ее введением в раневые края дистального и проксимального участка кишки формируемого анастомоза. При этом выполнялся забор венозной крови пациента в объеме 6-9 мл. После заполнения кровью стандартной пробирки, используемой для приготовления обогащенной тромбоцитами аутоплазмы, выполняется ее центрифугирование в режиме 3500 оборотов в минуту в течение 5 минут. Из центрифугированной в пробирке венозной крови осуществляют точный забор выделившегося слоя плазмы, в 6 шприцев по 0,5 мл плазмы в каждый (по 3 шприца на раневой край дистального и проксимального участка кишки формируемого анастомоза).
Краткое описание чертежа.
Цифрой «1» указаны места инъекций обогащенной тромбоцитами аутоплазмы в раневые края дистального и проксимального участка кишки, в проекции 3, 9 и 12 часов условного циферблата, принимая за 6 часов брыжеечную часть раневого края кишки.
Пример 1. Эксперимент выполнен на 30 половозрелых лабораторных кроликах-самцах породы «Советская шиншилла» (весом 2,0 ± 0,5 кг). Под внутривенным наркозом препаратом «Золетил 100» (0,5 мг/кг) выполнялась энтеротомия с последующим наложением тонкокишечного анастомоза «конец в конец» (контрольный анастомоз) на расстоянии 15 см от илеоцекального угла, затем отступив на 30 см от наложенного анастомоза, выполнялась энтеротомия с последующей инъекций обогащенной тромбоцитами аутоплазмы в мышечный слой (по вышеописанной методике) и наложением кишечного анастомоза (все анастомозы выполнялись однорядным узловым швом атравматическим материалом «VICRYL 4-0»). Сравнительная оценка состояния зоны кишечного анастомоза проводилась на 3, 7, 14 сутки. Выполнялась морфологическая (макро- и микроскопическая) оценка состояния области кишечного анастомоза, оценка состояния микроциркуляции методом лазерной допплеровской флоуметрии (ЛДФ) с использованием двуканального лазерного анализатора. При выполнении ЛДФ определялись: величина среднего потока перфузии крови – «М» в интервале времени регистрации в перфузионных единицах (пф. ед.), среднее колебание перфузии относительно значения М (σ – «Флакс»), вычисляемое по формуле для среднеквадратичного отклонения (пф. ед.), коэффициент вариации - Kv (Kv=σ/М·100%).
Сравнительная оценка показателей состояния локального кровотока представлены в таблице 1.
Таблица 1 – Показатели состояния локального кровотока.
Примечание: * - (р<0,001), ** - (р<0,01), *** - (р<0,05), достоверность оценивалась с помощью U-критерия Манна-Уитни.
Выполненное макроскопическое исследование показало, отсутствие достоверного различия с контрольным анастомозом при оценке уровня адгезиогенеза, при этом в опытной группе отмечалось меньшее число осложнений и достоверные макроскопические признаки сформированности анастомоза. Микроскопическое (гистологическое) исследование выявило в опытной группе по сравнению с контрольной ускорение динамики репарации, усиление ангеогенеза, снижение воспалительной инфильтрации и ускорение признаков завершения организации соединительной ткани. При выполнении ЛДФ в опытной группе определялось достоверное увеличение величины среднего потока перфузии крови и скорости локального кровотока.
Как следует из приведенных результатов эксперимента, применение нового способа стимуляции регенерации с использованием аутогенных факторов роста, по сравнению с контрольным анастомозом показывает функциональное улучшение микроциркуляции, снижение ишемии ткани, отсутствие признаков усиления адгезиогенеза, ускорение неоангеогенеза и процесса репарации в зоне дигестивного анастомоза, демонстрируя потенциал применения данного способа для снижения частоты возможных осложнений, связанных с его несостоятельностью.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЛЕЧЕНИЯ РЕЦИДИВНЫХ СТРИКТУР БУЛЬБОЗНОГО ОТДЕЛА УРЕТРЫ У МУЖЧИН | 2019 |
|
RU2710217C1 |
| СПОСОБ ФОРМИРОВАНИЯ ПИЩЕВОДНО-ТОНКОКИШЕЧНОГО АНАСТОМОЗА ПРИ ХИРУРГИЧЕСКОМ ЛЕЧЕНИИ КАРДИОЭЗОФАГЕАЛЬНОГО РАКА | 2008 |
|
RU2391055C2 |
| СПОСОБ ФОРМИРОВАНИЯ АРЕФЛЮКСНОГО ПИЩЕВОДНО-КИШЕЧНОГО АНАСТОМОЗА ПОСЛЕ ГАСТРЭКТОМИИ | 2006 |
|
RU2327426C1 |
| Способ формирования однорядного кишечного анастомоза с использованием прецизионного шва | 2022 |
|
RU2786698C1 |
| СПОСОБ ПРОФИЛАКТИКИ НЕСОСТОЯТЕЛЬНОСТИ МЕЖКИШЕЧНЫХ АНАСТОМОЗОВ | 2007 |
|
RU2326703C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ РАКА ПРОКСИМАЛЬНОГО ОТДЕЛА ЖЕЛУДКА | 2000 |
|
RU2175854C2 |
| СПОСОБ ПРОФИЛАКТИКИ НЕСОСТОЯТЕЛЬНОСТИ АППАРАТНОГО КОЛОРЕКТАЛЬНОГО АНАСТОМОЗА | 2014 |
|
RU2567917C1 |
| СПОСОБ ПОСЛЕОПЕРАЦИОННОЙ ПРОФИЛАКТИКИ НЕСОСТОЯТЕЛЬНОСТИ ТОЛСТО-ТОЛСТОКИШЕЧНОГО АНАСТОМОЗА | 2013 |
|
RU2523822C1 |
| СПОСОБ ФОРМИРОВАНИЯ ТЕРМИНОЛАТЕРАЛЬНОГО ПАНКРЕАТОЕЮНОАНАСТОМОЗА ПРИ ПАНКРЕАТОДУОДЕНАЛЬНОЙ РЕЗЕКЦИИ | 2006 |
|
RU2293530C1 |
| СПОСОБ ДИСТАЛЬНОЙ РЕЗЕКЦИИ ЖЕЛУДКА | 2006 |
|
RU2290879C1 |
Изобретение относится к медицине, а именно к абдоминальной хирургии. Перед наложением кишечных швов в раневые края дистального и проксимального участка кишки формируемого анастомоза выполняют по 3 инъекции 0,5 мл обогащенной тромбоцитами аутоплазмы, содержащую аутогенные факторы роста. Инъекции выполняют в мышечный слой на глубину 0,5 см на 3, 9 и 12 часах условного циферблата, принимая за 6 часов брыжеечную часть раневого края кишки. Способ обеспечивает стимуляцию регенерации кишечного анастомоза за счет ускорения неоангеогенеза, увеличения скорости локального кровотока и миграции клеточных элементов, тем самым снижает риск возникновения послеоперационных осложнений, в том числе несостоятельности анастомоза. 1 табл., 1 пр.
Способ стимуляции регенерации кишечных анастомозов с использованием аутогенных факторов роста, отличающийся тем, что перед наложением кишечных швов в раневые края дистального и проксимального участка кишки формируемого анастомоза выполняют по 3 инъекции 0,5 мл обогащенной тромбоцитами аутоплазмы, содержащую аутогенные факторы роста, в мышечный слой со стороны раневого края кишки, исключая травматизацию серозной и слизистой оболочки кишки, на глубину 0,5 см на 3, 9 и 12 часах условного циферблата, принимая за 6 часов брыжеечную часть раневого края кишки, с последующим наложением кишечных швов и завершением формирования кишечного анастомоза.
| DZHUMABEKOV B.N | |||
| et al | |||
| Platelet-rich autoplazma effect on intestinal anastomosis regeneration in rabbits, Lib Oncol | |||
| Станок для придания концам круглых радиаторных трубок шестигранного сечения | 1924 |
|
SU2019A1 |
| Способ моделирования болезни Гиршпрунга в эксперименте | 2016 |
|
RU2634033C1 |
| СПОСОБ ПРОФИЛАКТИКИ НЕСОСТОЯТЕЛЬНОСТИ АНАСТОМОЗОВ ПОЛЫХ ОРГАНОВ ЖЕЛУДОЧНО-КИШЕЧНОГО ТРАКТА У БОЛЬНЫХ С МОРБИДНЫМ ОЖИРЕНИЕМ И МЕТАБОЛИЧЕСКИМ СИНДРОМОМ С ИСПОЛЬЗОВАНИЕМ ПРЕПАРАТА ЭНТЕРОСАН | 2007 |
|
RU2349329C1 |
| Искрогасительная катушка для трамвайного контроллера | 1927 |
|
SU15637A1 |
| АГАЕВ Э.К | |||
| Несостоятельность швов кишечных анастомозов у больных после экстренной и неотложной резекции кишки | |||
| Хирургия | |||
| Журнал им | |||
Авторы
Даты
2023-08-01—Публикация
2022-05-26—Подача